Лечение бруксизма у взрослых, цены в ЦПС Доктор Левин в Москве
Бруксизм — непроизвольное скрежетание зубами из-за мышечного спазма, чаще проявляется во сне. Постоянное травмирование зубов и мягких тканей вокруг них приводит к патологической стираемости эмали, болезням десен, расшатыванию и потере зубов, проблемам с челюстным суставом, а на этом фоне — к общему ухудшению состояния здоровья. Лечение патологии в нашем Центре комплексное, включает устранение причины, только потом — последствий.
Причины бруксизма
Возникновение болезни объясняется сочетанными нарушениями различных систем в организме — пищеварительной, нервной, эндокринной.
Выделяют основные группы причин бруксизма:
Стоматологические
У пациентов выявляются:
- Частичная утрата зубов с дефектами зубного ряда
- Воспаление десен и шаткость зубов, пародонтит
- Аномалии прикуса
- Некачественно установленные брекет-системы и зубные протезы
- Боли и ограничение подвижности в височно-нижнечелюстном суставе (ВНЧС)
Во всех этих случаях происходит нарушение контакта зубов верхней и нижней челюстей, жевательная нагрузка распределяется неравномерно, мышцы лица перенапрягаются и спазмируются.
Остеопатические
Традиционно считается, что кости черепа у человека подвижны только при рождении и в раннем детском возрасте. Сторонники остеопатии считают, что у взрослых они тоже находятся в движении и совершают от 8 до 12 сжатий и расширений в минуту. Такие циклы остеопаты называют «дыханием жизни» или кранио-сакральным ритмом. Он может нарушаться и блокировать черепные швы при родовых травмах, осложненных родах, неправильном прикусе.
Бруксизм — это неудачные попытки нервной и мышечной систем снять блок и вернуть «дыхание жизни». Остеопаты считают неправильной установку протезов, соединяющих левую и правую половины черепа, — они тоже провоцируют спазматическое сокращение лицевых мышц.
Психологические
Симптомы болезни впервые появляются после резкой смены эмоционального состояния — стресса или трудной жизненной ситуации.
Склонность к депрессиям, тревожности четко коррелирует с наличием ночного скрежета: у ¾ пациентов отделений неврозов обнаруживают дисфункции жевательных мышц.
Тип личности, темперамент человека тоже влияют на появление болезни: у холериков при повышенной раздражительности и агрессивной настроенности патология лицевой мускулатуры не является редкостью.
Неврогенные
Бруксизм тесно связан с патологией нервной системы. Ему часто сопутствуют ночные апноэ, храп, кошмарные сновидения, сомнамбулизм. Выявляются и хронические заболевания — паркинсонизм, эпилепсия, энурез, деменция. При тщательном обследовании обнаруживают нарушение передачи импульсов по нервным волокнам.
Эффективное лечение таких состояний приводит к заметному ослаблению симптомов бруксизма.
Патологические проявления развиваются также при неправильном образе жизни (нарушении ритма сна и бодрствования, влиянии вредных производственных факторов), наличии вредных привычек (никотиновой, алкогольной зависимости и наркомании), при заболеваниях внутренних органов, хронических расстройствах питания.
Осложнения
Частые приступы бруксизма с постоянным травмированием твердых и мягких тканей полости рта становятся причиной преждевременного изнашивания зубов, воспалительных заболеваний мягких тканей, дисфункции височно-нижнечелюстного сустава.
Повышенная стираемость зубов
В естественных условиях происходят возрастные изменения зубной эмали — она постепенно стирается на жевательных и режущих поверхностях. Зубы адаптируются к нагрузкам и продолжают функционировать. Патологическая стираемость при бруксизме затрагивает не только эмаль, но и дентин, а в дальнейшем обнажает пульпу. Коронка зуба полностью разрушается.
Закономерно появляются проблемы:
На фоне снижения прикуса происходит формирование старческих черт лица с нарушенными пропорциями — уменьшенными размерами нижней челюсти, асимметрией лица.
Нарушение функции ВНЧС
Проявляется частичной или полной невозможностью жевания и способности внятно разговаривать.
Настораживающие признаки: болезненность жевательных мышц, напряжение и повышенный тонус, быстрая утомляемость мышечного аппарата во время еды.
При отсутствии лечения болезнь прогрессирует:
Повторяющиеся эпизоды бруксизма ведут к трудностям в ортопедическом и ортодонтическом лечении — установленные протезы быстро разрушаются, поэтому большинство методов восстановления зубного ряда таким пациентам недоступно. До принятия решения о протезировании необходимо выявить и устранить провоцирующий фактор.
Бруксизм — патология сложная, но не приговор
Заболевание имеет множество причин и следствий, но грамотный подход к диагностике и лечению позволяет избавиться от нее и избежать опасных последствий.
Левин Дмитрий Валерьевич
Главный врач и основатель ЦПС «Доктор Левин»
К какому врачу обращаться?
Изначально для установления диагноза и выбора тактики лечения необходима консультация гнатолога или же стоматолога-ортопеда или ортодонта с гнатологической подготовкой. Гнатология — наука о взаимодействии всех составляющих зубочелюстного аппарата. Изучает и лечит заболевания, связанные с нарушением работы челюстей, жевательных мышц, связок, суставов.
Изучает и лечит заболевания, связанные с нарушением работы челюстей, жевательных мышц, связок, суставов.
Гнатолог находит причины бруксизма, планирует стоматологическое лечение. В случае необходимости врач направляет пациента к узкому специалисту. Это может быть:
- Невролог — выявляет аномальную активность мозга, наличие скрытых эпилептических очагов и других органических поражений мозга.
- Психиатр — замечает нарушения психоэмоционального состояния и корректирует проявления депрессии.
Смежные специалисты назначают препараты с седативным и миорелаксирующим действием, антидепрессанты и поливитамины.
Диагностика
Диагностика бруксизма сложная и многоуровневая, предусматривает:
Как избавиться от бруксизма
Лечение этой патологии комплексное, направлено на устранение выявленной причины и последствий в такой последовательности:
- Защита зубов
В зуботехнической лаборатории изготавливается специальная мягкая каппа от бруксизма, которая надевается на ночь и препятствует стиранию зубов.
- Устранение причины
Проводятся стоматологические мероприятия для снижения гипертонуса мышц, параллельно назначают антидепрессанты, успокоительные, витамины. - Лечение последствий
При слабо выраженной стертости зубов укрепляют эмаль. В остальных случаях проводят восстановление фотополимерными пломбами или протезирование.
Методы лечения в ЦПС «Доктор Левин»
Ночные каппы от бруксизма
На первом этапе лечения бруксизма применяются специальные ночные каппы — релаксационные шины на зубы из низкоаллергенного пластика. Их устанавливают на одну или обе челюсти.
Основная роль каппы — дать уцелеть зубам от стирания и смещения ночью, когда человек скрежещет зубами непроизвольно и не контролирует себя.
В случае возникновения приступа каппа:·
- разгружает лицевые мышцы, расслабляет их;
- предохраняет зубы от дальнейшего разрушения.
Ночная каппа не влияет на причину болезни и ее последствия не устраняет.
Пришлифовка зубов
Метод используют на втором этапе лечения, если причиной болезни признано неправильное соотношение жевательных поверхностей верхних и нижних зубов. В этом случае находят контактирующие зубы и частично стачивают с них твердые ткани.
Основная цель процедуры — создать равномерный контакт по всему зубному ряду.
После пришлифовки:
- снимается чрезмерная нагрузка на челюсть;
- по всем участкам она распределяется равномерно;
- устраняются острые края зубов, которые травмировали язык и слизистую оболочку;
- пациент избавляется от мелких травм и повреждений в ротовой полости.
TENS-терапия
Следующий этап лечения — TENS-терапия, аппаратная электростимуляция жевательных мышц. Она нужна, чтобы расслабить мышцы и вернуть правильное положение нижней челюсти и височно-нижнечелюстному суставу. Процедуру проводят перед ортопедическим или ортодонтическим лечением.
Низкочастотные микротоки усиливают поступление в мышцы кислорода и питательных веществ, ускоряют отток застойной венозной крови.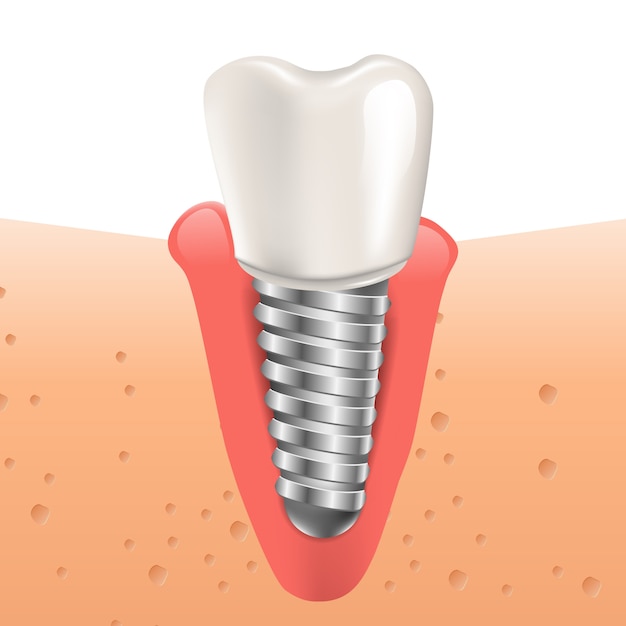
В результате:
- снимается мышечный спазм, восстанавливается эластичность мышечных волокон;
- устраняются дисфункция ВНЧС и повышенный тонус жевательных мышц;
- челюсти идеально смыкаются и не вызывают болезненных ощущений.
Сплинт-терапия
Сплинт-терапия может использоваться как альтернатива TENS-стимуляции или параллельно с ней. Это метод расслабления мышц и восстановления нормальной функции ВНЧС с помощью индивидуальной силиконовой шины (от англ. splint — шина, накладка). Ее устанавливают на челюсть и носят круглосуточно в среднем 2-6 месяцев. Пациент периодически посещает врача для коррекции положения накладки.
Облегчение наступает уже в первые дни:
- приходят в нормальный тонус жевательные мышцы;
- растягиваются укороченные связки;
- челюсть и головка сустава возвращаются в физиологическое положение;
- быстро уменьшаются головные боли и мышечные спазмы;
- снижается дискомфорт в шейной области.
Ботулинотерапия
Нейропротеины (ботулотоксины) блокируют передачу нервных импульсов по мышцам. Препарат вводят точечно в виде инъекций в определенные зоны лица на этапе устранения причин бруксизма. Такой метод необходим для снятия тонуса напряженных лицевых мышц и налаживания работы ВНЧС.
После одной процедуры:
- жевательные мышцы расслабляются и становятся частично неподвижными;
- исчезают боли и перенапряжение;
- крепко сжать челюсти не удается даже при неосознанных попытках.
Эффект длительный — до нескольких месяцев.
Коррекция прикуса
После улучшения состояния, снижения мышечного тонуса переходят к этапу исправления прикуса с помощью брекет-систем и элайнеров.
- Брекет-системы — ортодонтические устройства с замочками на зубах, соединенные жесткой дугой. Перед установкой ей задают правильное положение по форме будущего зубного ряда. В это положение она стремится вернуться будучи уже на зубах, давит на них.
 Ортодонт периодически корректирует силу давления, а зубы постепенно перемещаются и выравниваются.
Ортодонт периодически корректирует силу давления, а зубы постепенно перемещаются и выравниваются. - Элайнеры — прозрачные съемные каппы, изготовленные по компьютерной технологии для постоянного давления на зубной ряд. Обеспечивают перемещение зубов по заранее составленному 3D-плану.
Обе системы носят от года и более.
Восстановление зубов
Когда причины нарушений устранены, переходят к заключительному этапу — восстановительному:
- Разрушенные и стертые зубы реставрируют с помощью пломб и вкладок, тонких керамических накладок — виниров и одиночных протезов-коронок. Все они предохраняют зубы от дальнейшего изнашивания.
- На месте отсутствующих зубных единиц устанавливают импланты или изготавливают мостовидные протезы.
Процедуры имплантации и протезирования возможны только при устранении первопричин болезни. Иначе никакая ортопедическая конструкция не выдержит и неизбежно разрушится.
Эффективность мероприятий
Эффективность лечения зависит от своевременного начала терапии.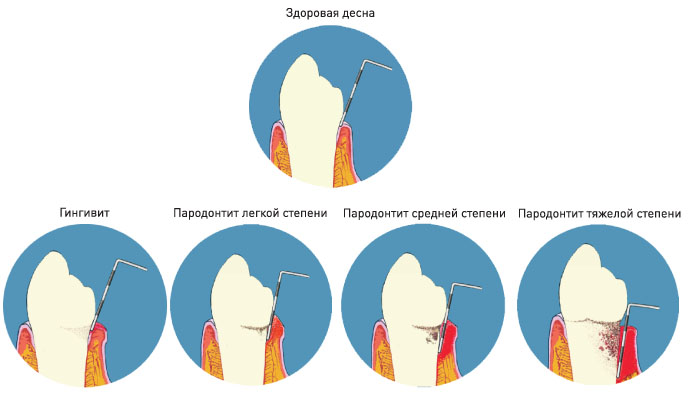
- На начальных стадиях заболевания для выздоровления хватает пришлифовывания зубов, приема медикаментозных средств и нескольких TENS-сеансов.
- При длительном течении заболевания, когда зубы разрушены и появляются многочисленные осложнения, потребуются все составляющие комплекса, в т.ч. дорогостоящее протезирование всех зубов.
Признаки и симптомы, требующие обращения к врачу
Внимательный пациент замечает симптомы, при которых следует незамедлительно прийти в клинику:
Визит в клинику нельзя откладывать надолго: посещение врача должно быть своевременным, чтобы не допустить тяжелых последствий, проблем с тугоподвижностью челюстного сустава и нестабильностью шейного отдела позвоночника, соответственно длительного и финансово затратного лечения.
Частые вопросы пациентов
Можно ли ставить импланты при бруксизме?
Можно, ведь восстановление утраченных зубов — это обязательный этап лечения. Единственное условие — предварительно провести углубленную диагностику и устранить мышечный спазм. При указании на бруксизм даже после восстановления тонуса мышц принимаются дополнительные меры, чтобы увеличить прочность конструкций на имплантатах.
При указании на бруксизм даже после восстановления тонуса мышц принимаются дополнительные меры, чтобы увеличить прочность конструкций на имплантатах.
Левин Дмитрий Валерьевич Челюстно-лицевой хирург, главный врач Центра
Что делать для профилактики, чтобы избежать развития бруксизма?
Если человек или его близкие заметили хотя бы единичные симптомы бруксизма, нужно пройти диагностику. Врач озвучит план, как всесторонне подойти к проблеме и устранить ее.
Со специалистом стоит согласовать и меры самопомощи: перед сном проводить легкий массаж подбородка и висков, делать упражнения на расслабление мышц.
Закрепит эффект и здоровый образ жизни — полноценный ночной сон, умеренные физические нагрузки на свежем воздухе, ограниченное количество кофе и чая, травяные ванны.
Левин Дмитрий Валерьевич
Автор статьи. Челюстно-лицевой хирург, главный врач Центра
Опубликовано: 09.06.2022
Обновлено: 13.06.2022
лечение без удаления, симптомы и причины, фото
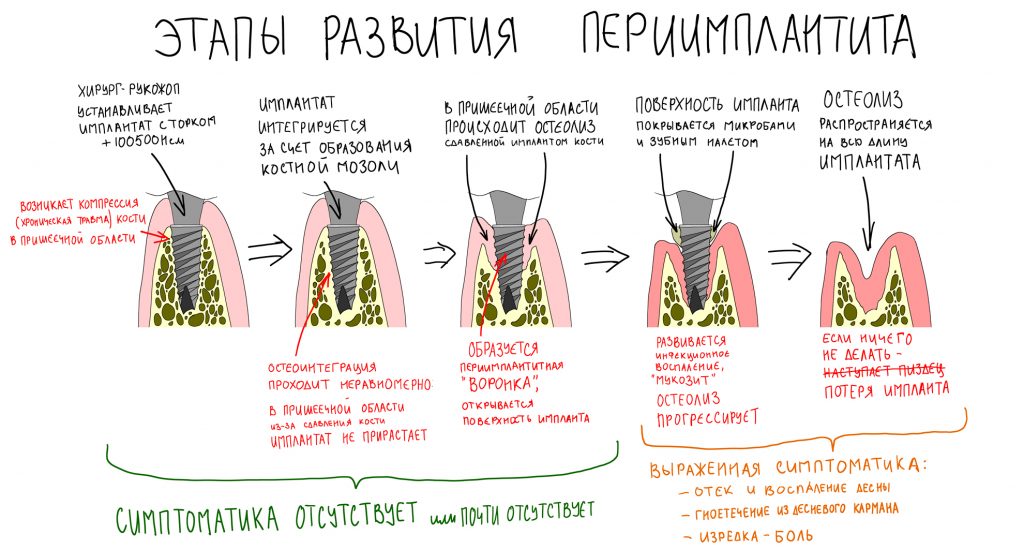
Периимплантит развивается не сразу после установки имплантов. В начале может быть незаметным, со временем приводит к разрушению кости. Как заметить это заболевание, почему это возникает, если после имплантации прошло много времени?
Хирург-имплантолог Ахтанин Александр Александрович рассказал о симптомах, причинах появления и методах лечения периимплантита после имплантации.
Переимплантит – определение
Как определить?
Стадии развития
Причины
Классификация
Диагностика
Методы лечения
Осложнения
Что это такое?
Периимплантит – это воспаление слизистой и соединительной ткани, которое приводит к разрушению кости вокруг импланта. Возникает из-за патогенных бактерий, которые развиваются в биоплёнке над титановым стержнем.
Возникает из-за патогенных бактерий, которые развиваются в биоплёнке над титановым стержнем.
Мнение эксперта
В 2017 году проходило собрание Европейской федерации пародонтологии (EFP) и Американской академии пародонтологии (AAP). В результате был опубликован доклад, в котором врачи точно сформулировали определение периимплантита.
“Патологическое состояние, возникающее в тканях вокруг дентального импланта из-за зубного налета. Основные признаки – воспаление слизистой и резорбция кости. В норме после имплантации отсутствует покраснение десны, кровотечение при зондировании, отек и нагноение.”
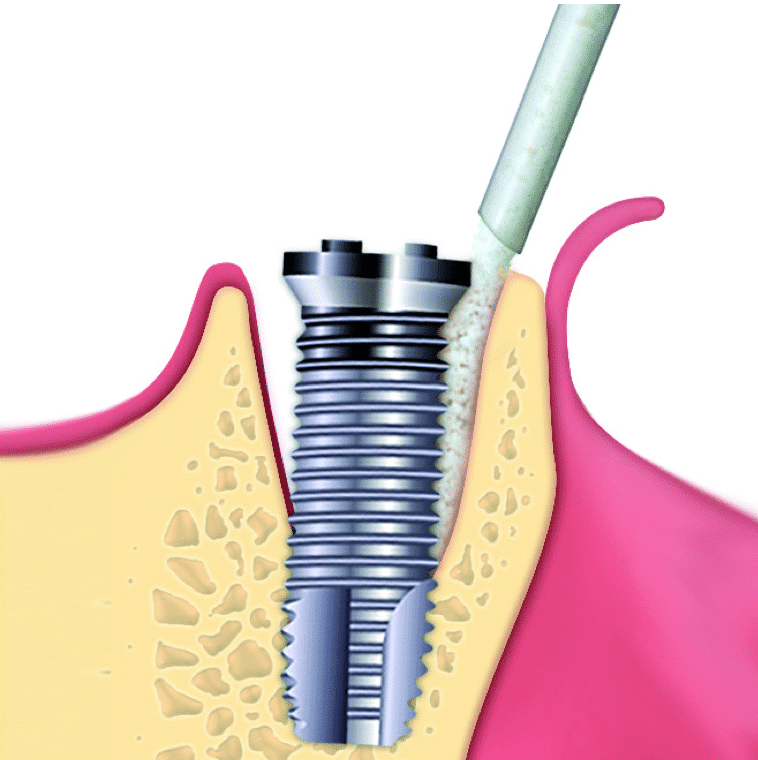
Перед появлением периимплантита чаще всего развивается мукозит. Это воспаление десны, при котором слизистая припухает и меняет цвет (краснеет или синеет). Десневой край начинает отходить от коронки, постепенно оголяется шейка импланта.
Вылечить это заболевание можно, если пройти профессиональную чистку полости рта и удалить все патогенные бактерии.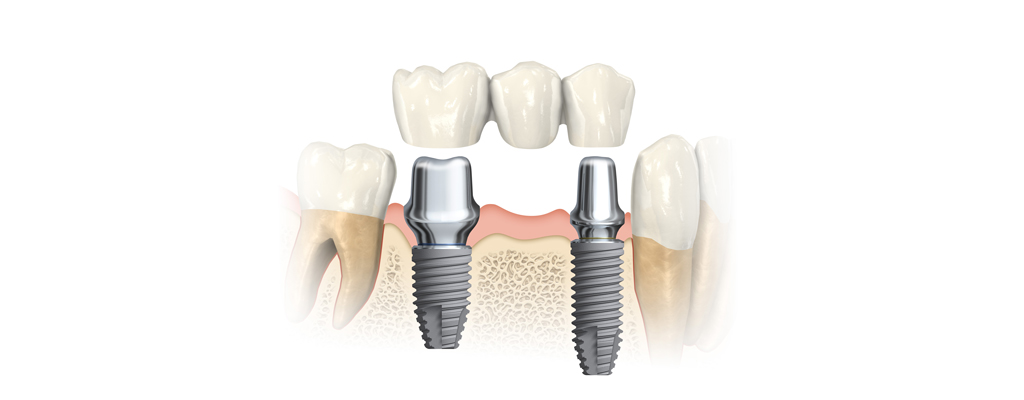 Также врач может назначить курс антибиотиков. Так можно предотвратить развитие периимплантита, воспаление никак не затронет кость.
Также врач может назначить курс антибиотиков. Так можно предотвратить развитие периимплантита, воспаление никак не затронет кость.
Симптомы
Для периимплантита характерен комплекс симптомов. Нужно рассматривать их вместе, чтобы увидеть целую картину:
- Покраснение десны. Кровь приливает к воспаленному участку, из-за этого десна меняет цвет.
- Образование десневого кармана. Край слизистой отходит от коронки, образуется пустота. Основная причина – уменьшение объема челюстной кости. В этом кармане накапливаются патогенные бактерии, омертвевшие частицы, остатки еды, которые провоцируют воспаление.
- Опускание края десны. Из-за воспаления разрушается слизистая и костная ткань вокруг импланта. Десневой край опускается, так как его больше ничего не фиксирует, оголяется шейка искусственного корня. Особенно заметно, если титановый стержень в фронтальном отделе.
- Кровотечение при зондировании (проверка глубины десневого кармана). Кровь выделяется из тонкого слоя соединительной ткани при разрушении слизистой.
- Выделение гноя. Происходит из-за накопления патогенных бактерий в десневом кармане.
- Подвижность импланта. Один из основных признаков отторжения титанового стержня. Связана с разрушением кости, которая его поддерживает.
- Боль при жевании. Из-за давления имплант задевает воспаленную десну вокруг. Это вызывает острую боль.
Как развивается периимплантит?
- В течение первых 3-6 месяцев после имплантации, титановый стержень приживается к костной ткани. Вокруг импланта образуется вторичная (ламеллярная) кость.
Небольшие изменения в строении костной ткани – это норма (встречается в 50% случаев). Они никак не влияют на внешний вид десны и имплантов, не доставляют неудобств, видны только на рентгене.
Мнение эксперта
Если в течение полугода после операции, имплантат начинает расшатываться, это может говорить о его неприживлении. Значит воспаление началось еще до того, как вокруг титанового стержня сформировалась вторичная кость.
Значит воспаление началось еще до того, как вокруг титанового стержня сформировалась вторичная кость.
- Без должной гигиены на поверхности искусственных коронок накапливается налет (биопленка) из патогенных бактерий и остатков еды.
- Эти микроорганизмы провоцируют развитие мукозита. Заболевание поражает соединительную ткань вокруг очага заражения. Его можно вылечить без последствий. Для этого нужно удалить налет и после этого тщательно следить за гигиеной полости рта, чтобы воспаление не развилось повторно.
- Если не обращать внимания на мукозит, заболевание начинает прогрессировать. Патогенные бактерии и инфекция поражают не только поверхность слизистой, но и вторичную кость вокруг титанового стержня.
Если пациент следит за гигиеной полости рта, инфекция не появится сама по себе. Но если воспаление уже началось из-за скопления патогенных бактерий, вокруг импланта оно будет развиваться быстрее, чем вокруг естественных зубов. Связано это с двумя причинами:
- Коллагеновый связочный аппарат удерживает зубы.
 Волокна этого аппарата расположены горизонтально вокруг естественных зубов. Но после имплантации они становятся вертикальными, то есть проходят параллельно с титановым стержнем. Из-за этого инфекция не останавливается, а продолжает продвигаться вдоль связочного аппарата к вершине импланта.
Волокна этого аппарата расположены горизонтально вокруг естественных зубов. Но после имплантации они становятся вертикальными, то есть проходят параллельно с титановым стержнем. Из-за этого инфекция не останавливается, а продолжает продвигаться вдоль связочного аппарата к вершине импланта. - Слой соединительной ткани. Между корнями зуба и альвеолярной костью есть тонкая прослойка соединительной ткани. Она защищает кость от проникновения инфекции. Но титановый стержень устанавливают сразу в альвеолярную кость, поэтому при периимплантите ее поражает инфекция.
Причины периимплантита
Основной фактор развития воспаления – это плохая гигиена. Но есть ситуации, которые увеличивают риск появления инфекции:
Общие заболевания:
- Пародонтит. Систематические исследования показали, что пациенты, у которых до имплантации был пародонтит, гораздо чаще сталкиваются с развитием мукозита и периимплантита (вероятность на 36,5% выше, чем у пациентов, которые не страдали от болезней десен).
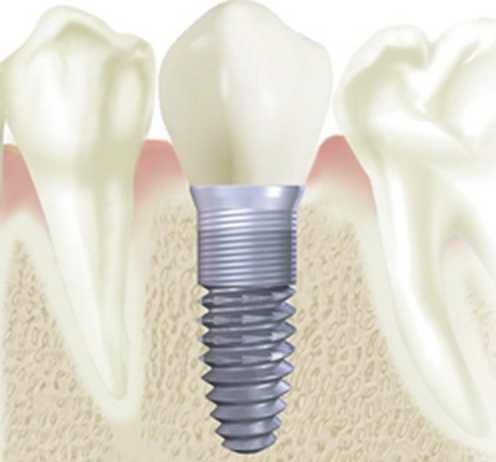
- Сахарный диабет. Плохо контролируемый уровень сахара в крови способствует благоприятной среде для развития патогенных бактерий в полости рта. При этом диабет никак не влияет на риск отторжения имплантов, если уровень сахара хорошо контролируется.
Вредные привычки:
- Алкоголь. Исследование, которое проводили в течение трех лет, показало, что при ежедневном употреблении больше 10 грамм алкоголя, риск развития периимплантита увеличивается. Спирт обжигает слизистую, ослабляет иммунитет, из-за этого инфекция распространяется быстрее.
- Курение. Никотин сужает сосуды, питание тканей уменьшается, заживление проходит медленнее. При развитии воспаления, десна не успевает заживать и инфекция проникает к кости.
 По статистике периимплантит у курильщиков развивается в 27% случаев, в то время как у некурящих в 6%. Всего было проведено более 71 исследование, которое подтверждает, что курение провоцирует периимплантит.
По статистике периимплантит у курильщиков развивается в 27% случаев, в то время как у некурящих в 6%. Всего было проведено более 71 исследование, которое подтверждает, что курение провоцирует периимплантит.
Наследственность. Генетические признаки иногда могут влиять на восприимчивость организма к инфекциям. Из-за этого вероятность развития воспаления увеличивается.
Прием препаратов. Бисфосфонаты – это группа лекарств, которые угнетают костный метаболизм. Их назначают, чтобы предотвратить разрушение костной ткани. Но при этом вокруг импланта не формируется ламеллярная кость. Фиксация титанового стержня непрочная, инфекция легко может проникнуть к его вершине.
Факторы, связанные с имплантом
В современной стоматологии чаще используют гладкие титановые стержни. Если конструкция шероховатая, в бороздках скапливаются патогенные бактерии. Из-за этого вероятность развития инфекции и разрушения кости увеличивается.
Но даже если стоматолог использует гладкие конструкции, есть и другие причины развития периимплантита:
- Излишек цемента.
 Если в основании коронки слишком много стоматологического материала, площадь бактериального налета увеличивается.
Если в основании коронки слишком много стоматологического материала, площадь бактериального налета увеличивается. - Перегрузка. Если врач установил имплант под неправильным углом или неверно рассчитал соотношение искусственного корня и коронки, давление на титановый стержень распределяется неравномерно. Может вызвать смещение оси и разрушение кости вокруг.
- Несовпадение штифта и супраструктуры. Если фиксация коронки на абатмент неплотная, в пустотах скапливаются остатки еды и микробы.
Классификация периимплантита
По стандартной системе у заболевания есть три степени тяжести:
- Начальная. Десневой край отслаивается, появляется карман глубиной до 4 мм. Этот показатель называется – глубина зондирования (probing depth или PD). Может выделяться гной и кровь при зондировании. Потеря костной ткани – менее 25% по длине титанового стержня.
- Умеренная. Глубина кармана увеличивается до 6 мм, симптомы становятся более заметными.
 Разрушение кости – до 50%.
Разрушение кости – до 50%. - Запущенная. PD – до 8 мм. Кровотечение и нагноения увеличивается, резорбция кости больше 50% длины импланта.
Если заболевание в стадии ремиссии, симптомы становятся менее заметными. Но при этом PD продолжает увеличиваться.
Диагностика
Основная цель стоматолога – заметить развитие заболевания на первом этапе. Чем раньше врач диагностирует периимплантит, тем больше шансов вылечить его без последствий.
- Осмотр
- Зондирование
- Компьютерная томография
- Периапикальный рентген
Специалист оценивает состояние полости рта: наличие отека, покраснения, свищевого хода или выделения гноя из десневой борозды, количество налета на коронках. Спрашивает, когда появились первые симптомы, замечал ли пациент кровотечение во время чистки зубов.
С помощью стоматологических инструментов врач осторожно отодвигает десневой край и измеряет глубину кармана. Отмечает, есть ли кровотечение: если слой слизистой внутри кармана сильно поврежден, кровь будет выделяться даже при легком прикосновении.
В отличие от рентгена, на КТ видно объемное изображение челюсти. Так врач может определить затронула ли инфекция костную ткань. Если кость начала разрушаться, определяет степень резорбции. Благодаря этому можно точно составить план лечения.
Метод позволяет сделать снимок одного зуба и увидеть состояние тканей вокруг искусственного корня. Так врач видит объем ламеллярной кости и патологические процессы, которые проходят в тканях пародонта, например, абсцессы (нагноение).
Этапы лечения
Если врач назначает терапию на начальной стадии, есть возможность восстановить область вокруг титанового стержня без хирургического вмешательства, устранить инфекцию и сохранить имплант. Поэтому важно записаться в клинику сразу после появления первых симптомов заболевания.
Местная санация
Чтобы бактерии не развивались в полости рта и не проникали в воспаленные ткани, нужно очистить от налета все зубы и слизистую. Врач использует ультразвуковую чистку и кюретки с мягким покрытием (специальные инструменты для соскабливания налета). Цель – устранить бактериальную пленку, остатки еды, гной.
Врач использует ультразвуковую чистку и кюретки с мягким покрытием (специальные инструменты для соскабливания налета). Цель – устранить бактериальную пленку, остатки еды, гной.
Мнение эксперта
Результаты исследования Karringet al. показали, что одного очищения от бактериального налета недостаточно для полного лечения периимплантита. Общая площадь бактерий уменьшается, но инфекция продолжает развиваться и поражать кость. Такой вид лечения может помочь только на ранних стадиях мукозита.
Обеззараживание поверхности имплантов
Важно не повредить поверхность конструкции, лучше всего для деликатной очистки подходят:
- Ультразвук. Врач использует специальный инструмент с пластиковым наконечником, чтобы не повредить поверхность импланта. При процедуре оборудование работает в щадящем режиме.
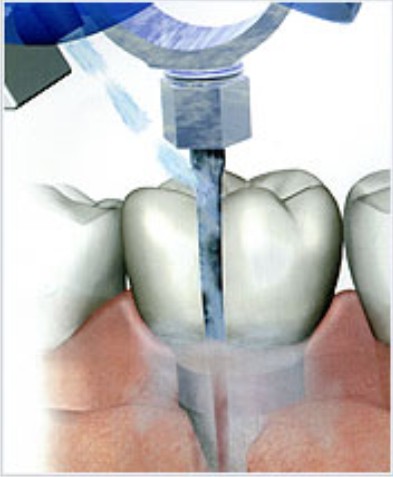
- AirFlow. Очищение с помощью струи воды с абразивными микрочастицами, которая подается под давлением.
 Позволяет устранить бактерии и налет в труднодоступных местах.
Позволяет устранить бактерии и налет в труднодоступных местах.
После механического очищения врач использует антисептические растворы, в составе которых перекись водорода или хлоргексидин. После обработки накладывает марлевую повязку, которая пропитана физиологическим раствором.
Медикаментозное лечение
Пациент проходит микробиологический анализ полости рта. В зависимости от степени развития инфекции и от видов бактерий врач назначает лекарства.
- При локализованном воспалении. Назначают антибиотики от периимплантита: Тетрациклин или Миноциклин курсом до 10 дней.
- При разросшейся инфекции. Для лечения врачи назначают разные антибиотики: Орнидазол 500 мг в течение 10 дней; Метронидазол 250 мг в течение 10 дней; комбинация Метронидазола (500 мг) и Амоксициллина (375 мг) в течение 10 дней.
Применение антибиотиков помогает только при неглубоком периимплантите. Прием препаратов осуществлять строго по дозировке от врача.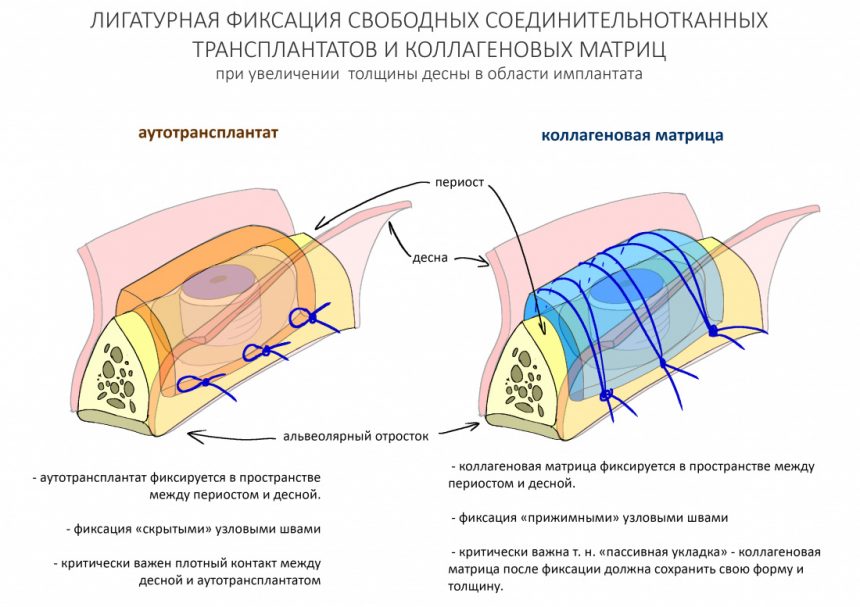 Не занимайтесь самолечением!
Не занимайтесь самолечением!
Хирургический метод
Пластика мягких тканей
В норме десна прочно прикреплена к надкостнице рядом с зубами и имплантом. Но при периимплантите, десневой край начинает отходить, опускаться. Тогда врач проводит пластику:
- Врач берет трансплантат (собственную донорскую ткань) с неба или с бугра верхней челюсти пациента. В этих зонах ткань богата коллагеновыми волокнами.
- В месте, куда перенесут трансплантат врач создает мягкотканный карман или тоннель с помощью скальпеля.
- С трансплантата удаляют слой покрывного эпителия, затем его подсаживают в карман или тоннель.
- Трансплантат фиксируют. После операции врач назначает антисептики и обезболивающие.
Такой способ подходит даже если объем кости вокруг импланта уменьшился на 30%-50%. Титановый стержень будет прочно зафиксирован и прослужит еще очень долго и без костной пластики. Такой способ менее травматичный.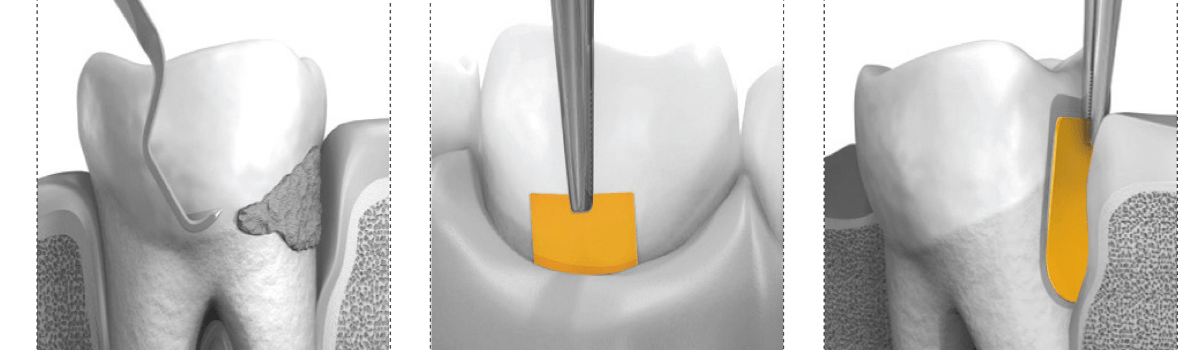
Костная пластика
Если пластики десны недостаточно, имплант остается подвижным, задача врача – увеличить костный объем вокруг него. Способ наращивания кости выбирают после компьютерной томографии.
Операция проходит в несколько этапов:
- Стоматолог разрезает десну специальным инструментом и отодвигает пародонтальный лоскут.
- Удаляет грануляционную ткань. Это твердые образования, которые появляются после травм, воспаления слизистой. Для удаления используют кюретки или эрбиевый лазер.
- Очищает имплант и обрабатывает пародонтальный карман антисептиком, чтобы устранить патогенные бактерии внутри десны.
- Врач проводит направленную тканевую регенерацию. Для этого закладывает аутокость или костную стружку (если резорбция незначительная). После закрывает костнозамещающий материал барьерной мембраной (пленка, которая фиксирует костный трансплантат, защищает его от повреждений).
- Закрывает десневой лоскут и накладывает шов.
 Если дефект кости был неглубоким, имплант можно сразу же нагрузить протезом. При одностеночном или двухстеночном дефекте (значительная потеря объема кости), закладывается больше костнозамещающего материала. Поэтому перед установкой протеза, должно пройти время.
Если дефект кости был неглубоким, имплант можно сразу же нагрузить протезом. При одностеночном или двухстеночном дефекте (значительная потеря объема кости), закладывается больше костнозамещающего материала. Поэтому перед установкой протеза, должно пройти время. - После операции врач назначает антибиотики, обезболивающие и антисептики (хлоргексидин), чтобы предотвратить развитие осложнений.
Какие материалы применяют при направленной костной регенерации?
- Аутокость. Костная ткань пациента, которую получают во время операции. Этот материал обладает биосовместимостью и потенциалом роста (больше вероятность появления новой ламеллярной кости вокруг импланта).
- Ксенокость. Материал, который получают из костной ткани животных. Основа для роста собственной кости пациента.
- Костная стружка. Небольшое количество собственной кости, которую закладывают при легкой резорбции.
- Остеоиндукторы.
 Морфогенетические протеины кости появляются при сильном повреждении. При лечении периимплантита используют этот материал, так как он стимулирует образование новой кости.
Морфогенетические протеины кости появляются при сильном повреждении. При лечении периимплантита используют этот материал, так как он стимулирует образование новой кости.
Удаление импланта
Крайний случай, если кость продолжает разрушаться уже после лечения. Тогда титановый стержень можно заменить на другой и провести имплантацию одновременно с костной пластикой. Такой вариант подходит, если атрофия кости незначительная. В противном случае установку нового импланта нужно отложить до тех пор, пока костный объем не восстановится.
Но такие случаи встречаются крайне редко. При положительном настрое пациента имплант можно сохранить практически во всех случаях. Исключение: значительная потеря кости и сильное не проходящее воспаление.
Если имплант удалили из-за периимплантита, клиника установит новый бесплатно. Гарантия на лечение прописана в договоре.
Какие могут быть осложнения?
- Перелом титанового стержня
Во время периимплантита фиксация импланта ослабевает, он начинает двигаться.
 Из-за смещения оси титанового стержня, давление на него распределяется неравномерно. Это приводит к появлению микротрещин и перелому.
Из-за смещения оси титанового стержня, давление на него распределяется неравномерно. Это приводит к появлению микротрещин и перелому.
- Атрофия кости Воспаление в слизистой приводит к разрушению костной ткани. Вокруг импланта образуются мягкие гранулемы, которые не фиксируют титановый стержень. Со временем они разрастаются, это может привести к критическому разрушению челюстной кости и потере естественных зубов.
- Отторжение импланта Из-за отсутствия надежной фиксации имплант становится подвижным. При жевании титановый стержень смещается и вызывает острую боль. Единственный выход – удалить конструкцию.
Профилактика
Чтобы периимплантит не развился повторно, нужно правильно соблюдать гигиену полости рта:
- Регулярно посещать стоматолога. Раз в полгода нужно проходить профессиональную чистку зубов и проверять глубину зубодесневого кармана.
- Ежедневно чистить зубы. Лучше использовать мягкие зубные щетки и зубную пасту без абразивных частиц.
 Так на протезе не появятся микротрещины, в которых скапливаются патогенные бактерии.
Так на протезе не появятся микротрещины, в которых скапливаются патогенные бактерии. - Использовать ирригатор. Устройство, которое очищает зубы с помощью струи воды под давлением. Так можно удалить налет даже из труднодоступных участков.
- Полоскать полость рта антисептиками. Такой способ помогает избавиться не только от остатков еды, но и от микробов на поверхности протеза.
|
Эксперт, автор статьи: Ахтанин Александр Павлович Стоматолог-ортопед, имплантолог Опыт имплантации 35 лет Материал обновлен: 11 октября 2021 г. |
Другой полезный материал
Альтернатива базальной имплантации
Лучшие швейцарские импланты
Имплантация и неправильный прикус: с чего начать?
Компьютерное 3D моделирование имплантации зубов
Адрес клиники:
Москва, ул. Маршала Рыбалко д.2 к.3
+7(495)120-30-65Режим работы:
Маршала Рыбалко д.2 к.3
+7(495)120-30-65Режим работы:
Peri-implantitis Update: Индикаторы риска, диагностика и лечение
1. Amornvit P, Rokaya D, Bajracharya S, Keawcharoen K, Supavanich W. Лечение обструктивного апноэ во сне с помощью имплантата, удерживающего устройство для продвижения нижней челюсти. Мир Джей Дент. 2014;5(03):184–189. [Google Scholar]
2. Moraschini V, Poubel L A, Ferreira V F, Barboza E dosS. Оценка выживаемости и показателей успешности зубных имплантатов, о которых сообщалось в лонгитюдных исследованиях с периодом наблюдения не менее 10 лет: систематический обзор. Int J Oral Maxillofac Surg. 2015;44(03):377–388. [PubMed] [Академия Google]
3. Lee C T, Huang Y W, Zhu L, Weltman R. Распространенность периимплантита и периимплантного мукозита: систематический обзор и метаанализ. Джей Дент. 2017; 62:1–12. [PubMed] [Google Scholar]
4. Berglundh T, Armitage G, Araujo M G et al. Периимплантатные заболевания и состояния: согласованный отчет рабочей группы 4 Всемирного семинара 2017 г. по классификации периодонтальных и периимплантатных заболеваний и состояний. Дж. Клин Пародонтол. 2018;45 20:S286–S291. [PubMed] [Академия Google]
Berglundh T, Armitage G, Araujo M G et al. Периимплантатные заболевания и состояния: согласованный отчет рабочей группы 4 Всемирного семинара 2017 г. по классификации периодонтальных и периимплантатных заболеваний и состояний. Дж. Клин Пародонтол. 2018;45 20:S286–S291. [PubMed] [Академия Google]
5. Наджиб С., Зафар М.С., Хуршид З., Зохаиб С., Алмас К. Роль питания в здоровье пародонта: обновленная информация. Питательные вещества. 2016;8(09):530. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Ниази Ф., Насим М., Хуршид З., Зафар М.С., Алмас К. Роль жевательной палочки Salvadora persica (мисвак): натуральная зубная щетка для целостного здоровья полости рта. Евр Джей Дент. 2016;10(02):301–308. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Matsuda S, Movila A, Suzuki M et al. Новый метод забора жидкости из десневой борозды у мышиной модели пародонтита. Дж Иммунол Методы. 2016; 438:21–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Каркуак О.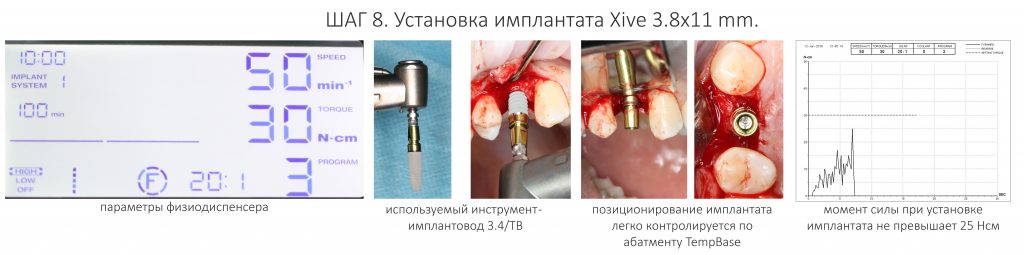 , Берглунд Т. Состав поражений периимплантита и периодонтита человека. Джей Дент Рез. 2014;93(11):1083–1088. [Статья бесплатно PMC] [PubMed] [Google Scholar]
, Берглунд Т. Состав поражений периимплантита и периодонтита человека. Джей Дент Рез. 2014;93(11):1083–1088. [Статья бесплатно PMC] [PubMed] [Google Scholar]
9. Zhang L, Li X, Yan H, Huang L. Металлопротеиназа матрикса слюны (MMP)-8 как биомаркер периодонтита: систематический обзор, соответствующий PRISMA, и метаданные. -анализ. Медицина (Балтимор) 2018;97(03):e9642. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Папи П., Ди Карло С., Розелла Д., Де Анджелис Ф., Капогреко М., Помпа Г. Периимплантит и антитела к внеклеточному матриксу: исследование случай-контроль. Евр Джей Дент. 2017;11(03):340–344. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Телес Р., Телес Ф., Фриас-Лопес Дж., Пастер Б., Хаффаджи А. Уроки, извлеченные и невыученные в микробиологии пародонта. Пародонтол 2000. 2013;62(01):95–162. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Hasturk H, Kantarci A. Активация и разрешение воспаления пародонта и его системное воздействие.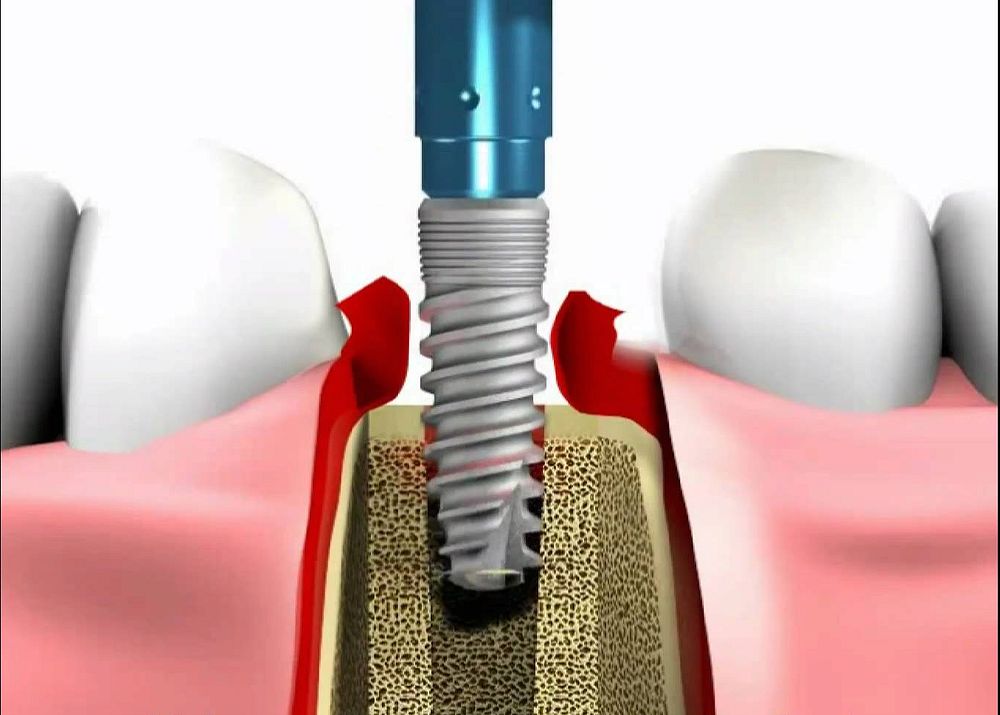 Пародонтол 2000. 2015;69(01):255–273. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Пародонтол 2000. 2015;69(01):255–273. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Renvert S, Polyzois I. Индикаторы риска периимплантатного мукозита: систематический обзор литературы. Дж. Клин Пародонтол. 2015;42 16:S172–S186. [PubMed] [Академия Google]
14. Staubli N, Walter C, Schmidt JC, Weiger R, Zitzmann N U. Избыток цемента и риск периимплантатного заболевания – систематический обзор. Clin Oral Implants Res. 2017;28(10):1278–1290. [PubMed] [Google Scholar]
15. Катафучи М., Вайнштейн Б.Ф., Леру Б.Г., Чен Ю.В., Доберт Д.М. Контур реставрации является индикатором риска периимплантита: рентгенографический анализ поперечного сечения. Дж. Клин Пародонтол. 2018;45(02):225–232. [PubMed] [Google Scholar]
16. Jepsen S, Berglundh T, Genco R et al. Первичная профилактика периимплантита: лечение периимплантного мукозита. Дж. Клин Пародонтол. 2015;42 16:S152–S157. [PubMed] [Академия Google]
17. Schwarz F, Derks J, Monje A, Wang HL. Периимплантит. Дж. Клин Пародонтол. 2018;45 20:S246–S266. [PubMed] [Google Scholar]
Дж. Клин Пародонтол. 2018;45 20:S246–S266. [PubMed] [Google Scholar]
18. Периимплантатный мукозит и периимплантит: современное понимание их диагнозов и клинических проявлений. J Пародонтол. 2013;84(04):436–443. [PubMed] [Google Scholar]
19. Sasada Y, Cochran D L. Соединения имплантат-абатмент: обзор биологических последствий и последствий периимплантита. Оральные челюстно-лицевые имплантаты Int J. 2017;32(06):1296–1307. [PubMed] [Google Scholar]
20. Schwarz F, Alcoforado G, Nelson K et al. Влияние соединения имплантата с абатментом, положения обработанного воротника/микрозазора и переключения платформы на изменения уровня костного гребня. Консенсусный отчет Camlog Foundation. Clin Oral Implants Res. 2014;25(11):1301–1303. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Monje A, Insua A, Wang H-L. Понимание периимплантита как связанного с бляшками и локализованного заболевания: о местных предрасполагающих факторах. Дж. Клин Мед. 2019;8(02):279. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Krennmair G, Seemann R, Piehslinger E. Зубные имплантаты у пациентов с ревматоидным артритом: клинические результаты и периимплантационные данные. Дж. Клин Пародонтол. 2010;37(10):928–936. [PubMed] [Google Scholar]
Krennmair G, Seemann R, Piehslinger E. Зубные имплантаты у пациентов с ревматоидным артритом: клинические результаты и периимплантационные данные. Дж. Клин Пародонтол. 2010;37(10):928–936. [PubMed] [Google Scholar]
23. Korsch M, Obst U, Walther W. Цемент-ассоциированный периимплантит: ретроспективное клиническое обсервационное исследование фиксированных реставраций с опорой на имплантаты с использованием метакрилатного цемента. Clin Oral Implants Res. 2014;25(07):797–802. [PubMed] [Google Scholar]
24. Yi Y, Koo K T, Schwarz F. Ben Amara H, Heo SJ. Ассоциация протезных особенностей и периимплантита: перекрестное исследование. Дж. Клин Пародонтол. 2020;47(03):392–403. [PubMed] [Google Scholar]
25. Goiato MC, Shibayama R, Gennari Filho H et al. Распределение напряжения в протезах с опорой на имплантаты с использованием различных систем соединения и длины консоли: цифровая фотоупругость. J Med Eng Technol. 2016;40(02):35–42. [PubMed] [Академия Google]
26. Amornvit P, Rokaya D, Keawcharoen K, Thongpulsawasdi N. Распределение напряжения в протезе пальца с фиксацией на имплантатах: исследование методом конечных элементов. J Clin Diagn Res. 2013;7(12):2851–2854. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Amornvit P, Rokaya D, Keawcharoen K, Thongpulsawasdi N. Распределение напряжения в протезе пальца с фиксацией на имплантатах: исследование методом конечных элементов. J Clin Diagn Res. 2013;7(12):2851–2854. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Чанг М., Хронопулос В., Маттеос Н. Влияние чрезмерной окклюзионной нагрузки на успешно остеоинтегрированные зубные имплантаты: обзор литературы. Джей Инвестиг Клин Дент. 2013;4(03):142–150. [PubMed] [Google Scholar]
28. Шеридан Р.А., Декер А.М., Плонка А.Б., Ван Х.Л. Роль окклюзии в имплантационной терапии: всесторонний обновленный обзор. Имплант Дент. 2016;25(06):829–838. [PubMed] [Google Scholar]
29. Ренверт С., Перссон Г.Р., Пирих Ф.К., Камарго П.М. Здоровье периимплантата, мукозит вокруг имплантата и периимплантит: определение случая и диагностические соображения. Дж. Клин Пародонтол. 2018;45 20:S278–S285. [PubMed] [Google Scholar]
30. Коста Ф. О., Такенака-Мартинес С., Кота Л. О., Феррейра С. Д., Силва Г. Л., Коста Дж. Э. Заболевания вокруг имплантатов у субъектов с профилактическим обслуживанием и без него: 5-летнее наблюдение. вверх. Дж. Клин Пародонтол. 2012;39(02):173–181. [PubMed] [Академия Google]
Д., Силва Г. Л., Коста Дж. Э. Заболевания вокруг имплантатов у субъектов с профилактическим обслуживанием и без него: 5-летнее наблюдение. вверх. Дж. Клин Пародонтол. 2012;39(02):173–181. [PubMed] [Академия Google]
31. Monje A, Aranda L, Diaz K T et al. Влияние поддерживающей терапии на профилактику периимплантатных заболеваний: систематический обзор и метаанализ. Джей Дент Рез. 2016;95(04):372–379. [PubMed] [Google Scholar]
32. Фарсай П.С. Поддерживающая терапия (КПТ) потенциально может улучшить выживаемость имплантатов (sr), периимплантит и периимплантативный мукозит. J Evid Основанная Dent Pract. 2020;20(01):101414. [PubMed] [Google Scholar]
33. Ephros H, Kim S, DeFalco R. Периимплантит: оценка и лечение. Дент Клин Норт Ам. 2020;64(02):305–313. [PubMed] [Академия Google]
34. Toma S, Brecx MC, Lasserre J F. Клиническая оценка трех хирургических методов лечения периимплантита: рандомизированное контролируемое клиническое исследование. Дж. Клин Мед. 2019;8(07):E966. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Вальдеррама П., Уилсон Т. Г., мл. Детоксикация поверхностей имплантатов, пораженных периимплантатным заболеванием: обзор хирургических методов. Инт Дж. Дент. 2013;2013:740680. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Zafar M S. Сравнение влияния ручной и ультразвуковой обработки на механические свойства поверхности корня. Евр Джей Дент. 2016;10(04):517–521. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Persson GR, Samuelsson E, Lindahl C, Renvert S. Механическое нехирургическое лечение периимплантита: одностороннее слепое рандомизированное продольное клиническое исследование. II. Микробиологические результаты. Дж. Клин Пародонтол. 2010;37(06):563–573. [PubMed] [Google Scholar]
38. Pedrazzi V, Escobar EC, Cortelli J R et al. Использование противомикробного ополаскивателя для полости рта в качестве дополнительного метода борьбы с периимплантной биопленкой. Браз Орал Рез. 2014; 28 (Spec No): S1806–8. 32420140002003E16. [PubMed] [Академия Google]
32420140002003E16. [PubMed] [Академия Google]
39. Hallström H, Persson GR, Lindgren S, Renvert S. Санация периимплантита открытым лоскутом с добавлением системных антибиотиков или без них: рандомизированное клиническое исследование. Дж. Клин Пародонтол. 2017;44(12):1285–1293. [PubMed] [Google Scholar]
40. Rudolf JL, Moser C, Sculean A, Eick S. Антибиопленочная активность хлоргексидина диглюконата in vitro на мембранах на основе полилактида и коллагена. Здоровье полости рта BMC. 2019;19(01):291. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Менезес К. М., Фернандес-Коста А. Н., Сильва-Нето Р. Д., Кальдерон П. С., Гургель Б. С. Эффективность 0,12% хлоргексидина глюконата для нехирургического лечения периимплантатного мукозита. J Пародонтол. 2016;87(11):1305–1313. [PubMed] [Google Scholar]
42. Liu J X, Werner J, Kirsch T, Zuckerman JD, Virk M S. Оценка цитотоксичности хлоргексидина глюконата на фибробластах, миобластах и остеобластах человека. J Bone Jt Infect. 2018;3(04):165–172. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2018;3(04):165–172. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. van Winkelhoff A J. Антибиотики в лечении периимплантита Eur J Oral Implantology 20125 (Suppl) S43–S50. [PubMed] [Google Scholar]
44. Cha J K, Lee J S, Kim C S. Хирургическая терапия периимплантита местным миноциклином: 6-месячное рандомизированное контролируемое клиническое исследование. Джей Дент Рез. 2019;98(03):288–295. [PubMed] [Google Scholar]
45. Heo S, Kim HJ, Joo JY, Lee J, Kim SJ, Choi J. Упрощенное нехирургическое лечение периимплантита с использованием хлоргексидина и гидрохлорида миноциклина. J Пародонтальные имплантаты Sci. 2018;48(05):326–333. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Рокая Д., Шриманипонг В., Сапкота Дж., Цинь Дж., Сиралартмукул К., Сиривонгрунгсон В. Полимерные материалы и пленки в стоматологии: обзор. J Adv Res. 2018;14:25–34. [PMC free article] [PubMed] [Google Scholar]
47. Carcuac O, Derks J, Abrahamsson I, Wennström JL, Petzold M, Berglundh T. Хирургическое лечение периимплантита: 3-летние результаты рандомизированного контролируемого клинического исследования. пробный. Дж. Клин Пародонтол. 2017;44(12):1294–1303. [PubMed] [Google Scholar]
Хирургическое лечение периимплантита: 3-летние результаты рандомизированного контролируемого клинического исследования. пробный. Дж. Клин Пародонтол. 2017;44(12):1294–1303. [PubMed] [Google Scholar]
48. Carcuac O, Derks J, Charalampakis G, Abrahamsson I, Wennström J, Berglundh T. Дополнительная системная и местная противомикробная терапия при хирургическом лечении периимплантита: рандомизированное контролируемое клиническое исследование. Джей Дент Рез. 2016;95(01):50–57. [PubMed] [Google Scholar]
49. Garcia de Carvalho G, Sanchez-Puetate JC, Casalle N, Marcantonio E, Jr, Leal Zandim-Barcelos D. Антимикробная фотодинамическая терапия, связанная с регенерацией кости при лечении периимплантита: случай отчет. Фотодиагност Фотодин Тер. 2020;30:101705. [PubMed] [Google Scholar]
50. Skallevold H E, Rokaya D, Khurshid Z, Zafar M S. Применение биоактивного стекла в стоматологии. Int J Mol Sci. 2019;20(23):E5960. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Махтей Э. Э. Альтернативные методы лечения периимплантита. Adv Med. 2014;2014:487903. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Махтей Э. Э. Альтернативные методы лечения периимплантита. Adv Med. 2014;2014:487903. [Статья бесплатно PMC] [PubMed] [Google Scholar]
52. Нтроука В.И., Слот Д.Е., Луропулу А., Ван дер Вейден Ф. Влияние химиотерапевтических агентов на загрязненные поверхности титана: систематический обзор. Clin Oral Implants Res. 2011;22(07):681–690. [PubMed] [Google Scholar]
53. Gosau M, Hahnel S, Schwarz F, Gerlach T, Reichert TE, Bürgers R. Влияние шести различных методов дезинфекции периимплантита на биопленку ротовой полости человека in vivo. Clin Oral Implants Res. 2010;21(08):866–872. [PubMed] [Академия Google]
54. Guimarães L F, Fidalgo T K, Menezes GC, Primo L G, Costa e Silva-Filho F. Влияние лимонной кислоты на культивируемые остеобластические клетки человека. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010;110(05):665–669. [PubMed] [Google Scholar]
55. Wohlfahrt J C, Lyngstadaas S P, Rønold H J et al. Пористые гранулы титана в хирургическом лечении периимплантатных костных дефектов: рандомизированное клиническое исследование. Оральные челюстно-лицевые имплантаты Int J. 2012;27(02):401–410. [PubMed] [Академия Google]
Оральные челюстно-лицевые имплантаты Int J. 2012;27(02):401–410. [PubMed] [Академия Google]
56. Kotsakis G A, Lan C, Barbosa J et al. Антимикробные агенты, используемые при лечении периимплантита, изменяют физико-химию и цитосовместимость титановых поверхностей. J Пародонтол. 2016;87(07):809–819. [PubMed] [Google Scholar]
57. Бюргерс Р., Витеси С., Ханель С., Госау М. Влияние различных местных антисептиков периимплантита на Staphylococcus epidermidis, Candida albicans и Streptococcus sanguinis. Arch Oral Biol. 2012;57(07):940–947. [PubMed] [Академия Google]
58. Мослеми Н., Шахназ А., Бахадор А., Тораби С., Джаббари С., Оскуэй З. А. Влияние послеоперационного амоксициллина на раннюю бактериальную колонизацию борозды вокруг имплантата: рандомизированное контролируемое клиническое исследование. J Dent (Тегеран) 2016;13(05):309–317. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Alshehri F A. Роль лазеров в лечении периимплантатных заболеваний: обзор. Саудовская Дент Дж. 2016; 28 (03): 103–108. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Саудовская Дент Дж. 2016; 28 (03): 103–108. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Наджиб С., Хуршид З., Зафар М.С., Аджлал С. Применение усиления света за счет стимулированного излучения (лазеров) для восстановительной стоматологии. Медицинская практика. 2016;25(03):201–211. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Ашнагар С., Новзари Х., Нохбатольфогахай Х., Ягуб Заде Б., Чинифоруш Н., Чухачи Заде Н. Лазерное лечение периимплантита: обзор литературы. J Lasers Med Sci. 2014;5(04):153–162. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Lin G-H, Suárez López Del Amo F, Wang H-L. Лазерная терапия для лечения периимплантного мукозита и периимплантита: обзор лучших доказательств Американской академии пародонтологии. J Пародонтол. 2018;89(07):766–782. [PubMed] [Академия Google]
63. Мехтиев И., Гюльсен У., Сентюрк М. Ф., Саян Н. Б. Рентгенологическая оценка увеличения верхнечелюстной пазухи с усилением низкоинтенсивной лазерной терапией с одновременной установкой зубных имплантатов. Энн Максиллофак Хирург. 2019;9(01):48–52. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Энн Максиллофак Хирург. 2019;9(01):48–52. [Статья бесплатно PMC] [PubMed] [Google Scholar]
64. Смео К., Нашер Р., Гуткнехт Н. Антибактериальный эффект лазера Er:YAG при лечении периимплантита и их влияние на поверхности имплантатов: обзор литературы. Лазерная дентальная наука. 2018;2(04):201–211. [Академия Google]
65. Clem D, Gunsolley J C. Лечение периимплантита с использованием лазера Er:YAG и костной пластики. проспективная последовательная оценка серии случаев: 1 год после терапии. Int J Пародонтология Restorative Dent. 2019;39(04):479–489. [PubMed] [Google Scholar]
66. Yoshino T, Yamamoto A, Ono Y. Инновационная технология регенерации для лечения периимплантита с помощью лазера Er:YAG на основе микробиологического диагноза: серия случаев. Int J Пародонтология Restorative Dent. 2015;35(01):67–73. [PubMed] [Академия Google]
67. Джагадиш Пай Б., Шридхар А., Камат В., Джайсвал Н., Малаги С., Радхика Б. Дополнительное использование диодных лазеров при лечении периимплантита: серия случаев. Имплантат Джей Дент. 2014; 4:91–97. [Google Scholar]
Имплантат Джей Дент. 2014; 4:91–97. [Google Scholar]
68. Mailoa J, Lin G H, Chan H L, MacEachern M, Wang H L. Клинические результаты использования лазеров для детоксикации поверхности периимплантита: систематический обзор и метаанализ. J Пародонтол. 2014;85(09):1194–1202. [PubMed] [Google Scholar]
69. Kotsakis G A, Konstantinidis I, Karoussis I K, Ma X, Chu H. Систематический обзор и метаанализ действия различных длин волн лазера при лечении периимплантита. J Пародонтол. 2014;85(09): 1203–1213. [PubMed] [Google Scholar]
70. Чан Х-Ю, Пак С-Ю, Ким Дж-А, Ким Ю-К, Ли Х-Дж. Ранняя радиографическая диагностика периимплантита улучшает результаты лечения периимплантита: 5-летнее ретроспективное исследование после нехирургического лечения. J Пародонтальные имплантаты Sci. 2015;45(03):82–93. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Jepsen K, Jepsen S, Laine M L et al. Реконструкция костных дефектов вокруг имплантата: многоцентровое рандомизированное исследование. Джей Дент Рез. 2016;95(01):58–66. [PubMed] [Google Scholar]
Джей Дент Рез. 2016;95(01):58–66. [PubMed] [Google Scholar]
72. Мацубара В.Х., Леонг Б.В., Леонг М.Дж.Л., Лоуренс З., Беккер Т., Куаранта А. Очищающий потенциал различных аэроабразивных порошков и их влияние на шероховатость поверхности имплантата. Clin Implant Dent Relat Res. 2020;22(01):96–104. [PubMed] [Google Scholar]
73. Tastepe C S, Liu Y, Visscher C M, Wismeijer D. Очистка и модификация внутриротовых загрязненных титановых дисков абразивной обработкой порошком фосфата кальция. Clin Oral Implants Res. 2013;24(11):1238–1246. [PubMed] [Академия Google]
74. Schwarz F, Becker K, Renvert S. Эффективность воздушной полировки для нехирургического лечения периимплантатных заболеваний: систематический обзор. Дж. Клин Пародонтол. 2015;42(10):951–959. [PubMed] [Google Scholar]
75. Tastepe C S, van Waas R, Liu Y, Wismeijer D. Абразивная обработка воздушным порошком как метод очистки поверхности имплантата: обзор литературы. Оральные челюстно-лицевые имплантаты Int J. 2012;27(06):1461–1473. [PubMed] [Google Scholar]
2012;27(06):1461–1473. [PubMed] [Google Scholar]
76. Englezos E, Cosyn J, Koole S. Jacquet W, De Bruyn H. Резективное лечение периимплантита: клинические и рентгенологические результаты через 2 года. Int J Пародонтология Restorative Dent. 2018;38(05):729–735. [PubMed] [Google Scholar]
77. Aljateeli M, Fu J H, Wang HL. Борьба с потерей костной массы вокруг имплантата: современное понимание. Clin Implant Dent Relat Res. 2012;14 01:e109–e118. [PubMed] [Google Scholar]
78. Ramel C F, Lüssi A, Özcan M, Jung R E, Hämmerle CH, Thoma DS. Шероховатость поверхности зубных имплантатов и время лечения с использованием шести различных процедур имплантации. Clin Oral Implants Res. 2016;27(07):776–781. [PubMed] [Google Scholar]
79. Chan H L, Oh WS, Ong H S et al. Влияние имплантопластики на прочность комплекса имплантат-абатмент. Оральные челюстно-лицевые имплантаты Int J. 2013;28(06):1530–1535. [PubMed] [Академия Google]
80. Daugela P, Cicciù M, Saulacic N. Хирургическое регенеративное лечение периимплантита: метаанализ последних результатов в систематическом обзоре литературы. J Oral Maxillofac Res. 2016;7(03):e15. [PMC free article] [PubMed] [Google Scholar]
Хирургическое регенеративное лечение периимплантита: метаанализ последних результатов в систематическом обзоре литературы. J Oral Maxillofac Res. 2016;7(03):e15. [PMC free article] [PubMed] [Google Scholar]
81. Wiltfang J, Zernial O, Behrens E, Schlegel A, Warnke PH, Becker S T. Регенеративное лечение периимплантитных костных дефектов с помощью комбинации аутологичной кости и деминерализованный ксеногенный костный трансплантат: серия из 36 дефектов. Clin Implant Dent Relat Res. 2012;14(03):421–427. [PubMed] [Академия Google]
82. Зафар М.С., Хуршид З., Алмас К. Прогресс и проблемы инженерии тканей полости рта. Tissue Eng Regen Med. 2015;12(06):387–397. [Google Scholar]
83. Шейх З., Наджиб С., Хуршид З., Верма В., Рашид Х., Глогауэр М. Биоразлагаемые материалы для восстановления костей и тканевой инженерии. Материалы (Базель) 2015;8(09):5744–5794. [Бесплатная статья PMC] [PubMed] [Google Scholar]
84. McGuire M K, Tavelli L, Feinberg S E et al. Технологии регенеративной медицины на основе живых клеток для аугментации мягких тканей пародонта. J Пародонтол. 2020;91(02):155–164. [PubMed] [Google Scholar]
J Пародонтол. 2020;91(02):155–164. [PubMed] [Google Scholar]
85. Дарби И. Б., Моррис К. Х. Систематический обзор использования факторов роста в регенерации пародонта человека. J Пародонтол. 2013;84(04):465–476. [PubMed] [Google Scholar]
86. Trinh H A, Dam V V, Le B, Pittayapat P, Thunyakitpisal P. Непрямая аугментация синуса с добавлением биоматериала и без него: рандомизированное контролируемое клиническое исследование. Имплант Дент. 2019;28(06):571–577. [PubMed] [Google Scholar]
87. Sheikh Z, Hamdan N, Ikeda Y, Grynpas M, Ganss B, Glogauer M. Натуральные трансплантационные ткани и синтетические биоматериалы для реконструктивных применений пародонта и альвеолярной кости: обзор. Биоматер Рез. 2017;21:9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Декер А.М., Шеридан Р., Лин Г.Х., Суттибуняпан П., Кэрролл В., Ван Х.Л. Система прогнозирования периимплантатных заболеваний. Имплант Дент. 2015;24(04):416–421. [PubMed] [Google Scholar]
89. Ханиф А., Куреши С., Шейх З., Рашид Х. Осложнения в имплантологии. Евр Джей Дент. 2017;11(01):135–140. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Ханиф А., Куреши С., Шейх З., Рашид Х. Осложнения в имплантологии. Евр Джей Дент. 2017;11(01):135–140. [Статья бесплатно PMC] [PubMed] [Google Scholar]
90. Eroglu C N, Ertugrul A S, Eskitascioglu M, Eskitascioglu G. Изменения поверхности кости и протравленных кислотой и пескоструйных имплантатов после имплантации и удаления. Евр Джей Дент. 2016;10(01):77–81. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Лечение периимплантита – PMC
Dent Res J (Исфахан). 2012 сентябрь-октябрь; 9(5): 516–521.
doi: 10.4103/1735-3327.104867
1 и 1
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
и потеря костной массы вокруг остеоинтегрированного имплантата в процессе его функционирования. Этиология инфекции имплантата обусловлена состоянием ткани, окружающей имплантат, конструкцией имплантата, степенью шероховатости, внешней морфологией и чрезмерной механической нагрузкой. Микроорганизмами, наиболее часто вызывающими отторжение имплантата, являются спирохеты и подвижные формы грамотрицательных анаэробов, если их происхождение не является результатом простой механической перегрузки. Диагноз ставится на основании изменения цвета десны, кровоточивости и зондирования периимплантатных карманов, нагноения, рентгенографии и постепенной потери высоты кости вокруг зуба. Лечение будет различаться в зависимости от того, является ли это случаем периимплантного мукозита или периимплантита. Лечение инфекции имплантата должно быть сосредоточено на контроле инфекции, детоксикации поверхности имплантата и регенерации альвеолярной кости. В этой обзорной статье рассматриваются различные варианты лечения периимплантита. В статье также дано краткое описание этиопатогенеза, особенностей клиники и диагностики периимплантита.
Микроорганизмами, наиболее часто вызывающими отторжение имплантата, являются спирохеты и подвижные формы грамотрицательных анаэробов, если их происхождение не является результатом простой механической перегрузки. Диагноз ставится на основании изменения цвета десны, кровоточивости и зондирования периимплантатных карманов, нагноения, рентгенографии и постепенной потери высоты кости вокруг зуба. Лечение будет различаться в зависимости от того, является ли это случаем периимплантного мукозита или периимплантита. Лечение инфекции имплантата должно быть сосредоточено на контроле инфекции, детоксикации поверхности имплантата и регенерации альвеолярной кости. В этой обзорной статье рассматриваются различные варианты лечения периимплантита. В статье также дано краткое описание этиопатогенеза, особенностей клиники и диагностики периимплантита.
Ключевые слова: Зубной имплантат, периимплантит, периимплантационный мукозит
Название периимплантатное заболевание относится к патологическим воспалительным изменениям, происходящим в тканях, окружающих несущий имплантат. [1] В рамках концепции периимплантатного заболевания описываются два состояния: периимплантатный мукозит и периимплантит. Перимплантатный мукозит определяется как обратимая воспалительная реакция в мягких тканях, окружающих имплантат.[2] Периимплантит — это воспалительная реакция с потерей опорной кости в тканях, окружающих имплантат.[3] Сообщалось, что общая частота периимплантита составляет от 5% до 8% для выбранных систем имплантатов.[4] Все большее число исследований предполагает, что анаэробные бактерии зубного налета могут оказывать неблагоприятное воздействие на здоровье тканей вокруг имплантата, что приводит к периимплантиту.[5] Периимплантис также может быть напрямую связан с неадекватным распределением жевательного давления на ткани, окружающие имплантат, что приводит к расшатыванию искусственных опор, инфицированию окружающих тканей и, как следствие, воспалительным процессам.[6] Отказ зубного имплантата часто связан с нарушением остеоинтеграции. Зубной имплантат считается несостоятельным, если он утрачен, подвижен или имеет потерю костной ткани вокруг имплантата более 1,0 мм в первый год и более 0,2 мм через год.
[1] В рамках концепции периимплантатного заболевания описываются два состояния: периимплантатный мукозит и периимплантит. Перимплантатный мукозит определяется как обратимая воспалительная реакция в мягких тканях, окружающих имплантат.[2] Периимплантит — это воспалительная реакция с потерей опорной кости в тканях, окружающих имплантат.[3] Сообщалось, что общая частота периимплантита составляет от 5% до 8% для выбранных систем имплантатов.[4] Все большее число исследований предполагает, что анаэробные бактерии зубного налета могут оказывать неблагоприятное воздействие на здоровье тканей вокруг имплантата, что приводит к периимплантиту.[5] Периимплантис также может быть напрямую связан с неадекватным распределением жевательного давления на ткани, окружающие имплантат, что приводит к расшатыванию искусственных опор, инфицированию окружающих тканей и, как следствие, воспалительным процессам.[6] Отказ зубного имплантата часто связан с нарушением остеоинтеграции. Зубной имплантат считается несостоятельным, если он утрачен, подвижен или имеет потерю костной ткани вокруг имплантата более 1,0 мм в первый год и более 0,2 мм через год. Периимплантит может привести к потере костной ткани вокруг имплантата и, в конечном итоге, к потере имплантата. Оптимальным результатом лечения периимплантита является регенерация утраченного имплантата, поддерживающего твердые и мягкие ткани.[7]
Периимплантит может привести к потере костной ткани вокруг имплантата и, в конечном итоге, к потере имплантата. Оптимальным результатом лечения периимплантита является регенерация утраченного имплантата, поддерживающего твердые и мягкие ткани.[7]
Бактериальные инфекции играют наиболее важную роль в отказе зубных имплантатов. Обнаружено, что бактериальная флора, связанная с пародонтитом и периимплантитом, одинакова.[8] К микроорганизмам, наиболее часто вызывающим отторжение имплантата, относятся грамотрицательные анаэробы, такие как Prevotella intermedia, Porphyromonas gingivalis, Aggregatibacter actinomycetemcomitans, Bacterioides forsythus, Treponema denticola, Prevotella nigrescens, Peptostreptococcus micros 9.0207 и Fusobacterium nucleatum . [8,9] Здоровая ткань вокруг имплантата играет важную роль в качестве биологического барьера для некоторых агентов, вызывающих заболевание вокруг имплантата, и если она разрушается, бактериальное загрязнение распространяется непосредственно на кости, что приводит к ее быстрому разрушению. Чрезмерное механическое напряжение, плохая конструкция имплантата и коррозия, которая может возникнуть при соединении конструкции из неблагородного металла с титановым имплантатом, являются важными факторами в возникновении и развитии периимплантита. Другие этиологические факторы включают сахарный диабет, остеопороз, курение, длительное лечение кортикостероидами, облучение и химиотерапию.
Чрезмерное механическое напряжение, плохая конструкция имплантата и коррозия, которая может возникнуть при соединении конструкции из неблагородного металла с титановым имплантатом, являются важными факторами в возникновении и развитии периимплантита. Другие этиологические факторы включают сахарный диабет, остеопороз, курение, длительное лечение кортикостероидами, облучение и химиотерапию.
Следующие признаки и симптомы типичны для периимплантитных поражений: рентгенологические признаки вертикальной деструкции альвеолярного гребня. Дефект обычно блюдцеобразной формы с остеоинтеграцией апикальной части фиксатора; вертикальная деструкция кости, связанная с формированием периимплантного кармана; кровотечение и нагноение при зондировании; возможный отек тканей вокруг имплантата и гиперплазия. Боль является необычным признаком, который, если он присутствует, обычно связан с острой инфекцией. Диагноз периимплантита требует тщательной дифференциации от периимплантатного мукозита, первичных неудач в достижении тканевой интеграции и проблем без воспалительного компонента. Диагностические параметры, используемые для оценки периимплантита, включают клинические показатели, зондирование периимплантата с использованием жесткого пластикового зонда, кровотечение при зондировании (ВОР), нагноение, подвижность, рентгенографию периимплантата и микробиологию.
Диагностические параметры, используемые для оценки периимплантита, включают клинические показатели, зондирование периимплантата с использованием жесткого пластикового зонда, кровотечение при зондировании (ВОР), нагноение, подвижность, рентгенографию периимплантата и микробиологию.
В свете вышеупомянутых данных и с учетом постоянно растущего числа имплантатов, устанавливаемых в повседневной клинической практике, разумно ожидать увеличения распространенности периимплантита, что подчеркивает необходимость предсказуемой терапии. Периимлантит и его причины до сих пор плохо изучены.[1] Процесс принятия решения о поддерживающей терапии и лечении периимплантита должен быть рациональным и основанным на фактических данных подходом.[10]
Микрофлора полости рта, по-видимому, является определяющим фактором успеха или неудачи имплантации зубов. Как только поверхность имплантата попадает в ротовую полость, она немедленно покрывается белковым слоем — пленкой слюны — и заселяется микроорганизмами ротовой полости, образуя микробную биопленку.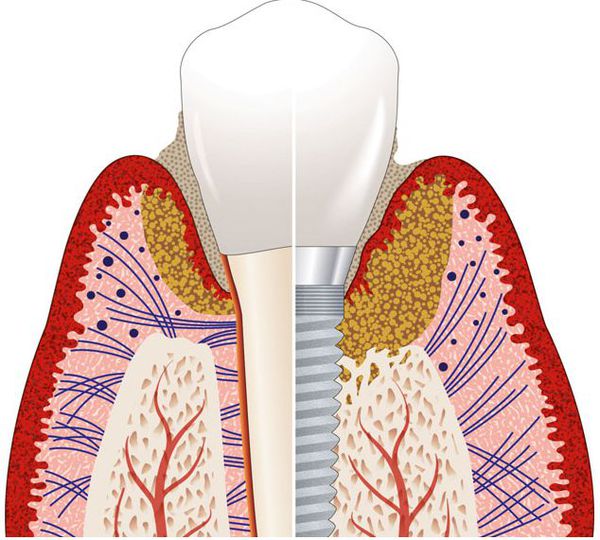 основывается либо на имеющихся доказательствах лечения периодонтита, либо на клинических эмпирических значениях, но не на конкретных научных данных. Поверхностные санации являются основным элементом лечения пародонтита и периимплантита. Однако винтовая конструкция имплантатов в сочетании с различными модификациями поверхности титана может способствовать накоплению зубного налета, что приводит к образованию бактериальной биопленки. Механическая обработка таких поверхностей может иметь ограниченный эффект и, конечно же, не может привести к полному удалению всех прилипших микроорганизмов. Поэтому для улучшения нехирургических вариантов лечения периимплантатного мукозита и периимплантита была предложена дополнительная периимплантационная терапия, такая как антибиотики, антисептики, ультразвуковое и лазерное лечение. Регенеративные процедуры с использованием заменителя костного трансплантата в сочетании с мембраной были предложены для лечения костных дефектов в запущенных случаях периимплантита.
основывается либо на имеющихся доказательствах лечения периодонтита, либо на клинических эмпирических значениях, но не на конкретных научных данных. Поверхностные санации являются основным элементом лечения пародонтита и периимплантита. Однако винтовая конструкция имплантатов в сочетании с различными модификациями поверхности титана может способствовать накоплению зубного налета, что приводит к образованию бактериальной биопленки. Механическая обработка таких поверхностей может иметь ограниченный эффект и, конечно же, не может привести к полному удалению всех прилипших микроорганизмов. Поэтому для улучшения нехирургических вариантов лечения периимплантатного мукозита и периимплантита была предложена дополнительная периимплантационная терапия, такая как антибиотики, антисептики, ультразвуковое и лазерное лечение. Регенеративные процедуры с использованием заменителя костного трансплантата в сочетании с мембраной были предложены для лечения костных дефектов в запущенных случаях периимплантита.
Местная санация
Имплантат следует очищать более мягкими инструментами, чем титан, такими как полировка резиновой чашечкой с пастой, зубной нитью, межзубными щетками или пластиковыми инструментами для удаления зубного камня. Было показано, что они не делают поверхность имплантата шероховатой, в отличие от металлических и ультразвуковых скейлеров.[11] Хотя повреждение поверхности имплантата можно практически предотвратить, используя либо ультразвуковой скейлер с неметаллическим наконечником, либо кюретки из смолы/углеродного волокна, наличие резьбы на имплантате и/или шероховатость поверхности имплантата могут затруднить доступ для очистки [12].
Исследование, проведенное Karring et al. .[13] продемонстрировало, что одной только обработки подслизистой оболочки, осуществляемой с использованием либо ультразвукового устройства, либо кюреток из углеродного волокна, недостаточно для обеззараживания поверхностей имплантатов с периимплантатными карманами. ≥ 5 мм и открытая резьба имплантата.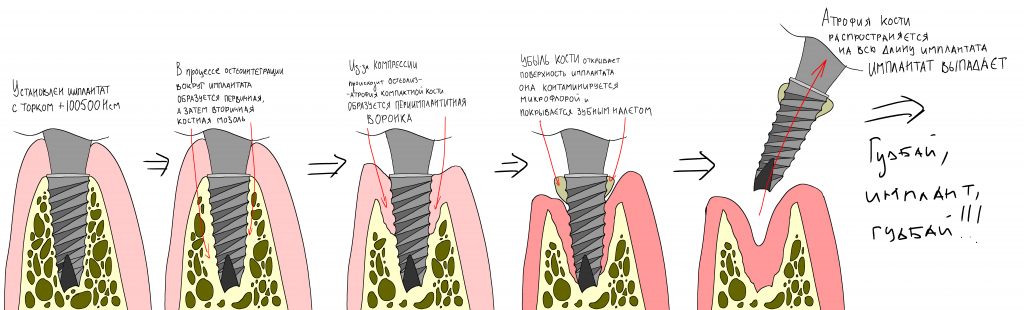 Таким образом, кажется разумным предположить, что механическая или ультразвуковая санация сама по себе не может быть адекватным методом для разрешения периимплантита.
Таким образом, кажется разумным предположить, что механическая или ультразвуковая санация сама по себе не может быть адекватным методом для разрешения периимплантита.
Обеззараживание поверхности имплантата
Четыре метода обеззараживания поверхности имплантата сравнивались на модели обезьяны: (1) метод абразивного порошка с последующим нанесением лимонной кислоты, (2) метод абразивного порошка с воздухом, (3) марля, смоченная физиологическим раствором, с последующим нанесением лимонной кислоты, и (4) марля, смоченная попеременно 0,1% хлоргексидином и физиологическим раствором.[14] Клинические параметры, рентгенография (включая количественную цифровую субтракционную рентгенографию), гистология и стереология не выявили существенных различий между любым из использованных методов. Выводы из исследование in vitro , сочетающее фотосенсибилизацию раствором толудинового синего и мягкое лазерное облучение, показало, что удаление бактерий с различных поверхностей титана без модификации поверхности имплантата возможно [15].
Фотодинамическая терапия — это неинвазивный метод, который можно использовать для уменьшения количества микроорганизмов при периимплантите.[16] В качестве местного антисептика можно использовать 2% хлоргексидин или 3% перекись водорода. Обеззараживание пораженных имплантатов с титановыми поверхностями, обработанными плазменным напылением или пескоструйной обработкой/кислотным травлением, может быть наиболее легко и эффективно достигнуто путем применения марли, смоченной попеременно хлоргексидином и физиологическим раствором.[12]
Нехирургическое лечение поражений периимплантита с использованием легированного эрбием: иттриевого, алюминиевого и гранатового (Er:YAG) лазера показало снижение количества F. nucleatum через 1 месяц после терапии.[17] Согласно Schwarz et al. [18], Er:YAG-лазер и комбинация механической обработки/хлоргексидина одинаково эффективны через 6 месяцев после терапии в значительном улучшении глубины кармана для зондирования вокруг имплантата и уровня клинического прикрепления, но использование Er:YAG-лазер обеспечивает значительно большее снижение кровотечения при зондировании по сравнению с дополнительным применением хлоргексидина. Однако в последующем исследовании Шварца et al ., [19] эффективность лазера Er:YAG, по-видимому, ограничивалась 6-месячным периодом, особенно при запущенных поражениях периимплантита. Далее было высказано предположение, что одного курса лечения Er:YAG-лазером может быть недостаточно для достижения стабильной терапии периимплантита и что дополнительные терапевтические меры, такие как дополнительное использование Er:YAG-лазера и/или последующая костная могут потребоваться регенеративные процедуры.
Однако в последующем исследовании Шварца et al ., [19] эффективность лазера Er:YAG, по-видимому, ограничивалась 6-месячным периодом, особенно при запущенных поражениях периимплантита. Далее было высказано предположение, что одного курса лечения Er:YAG-лазером может быть недостаточно для достижения стабильной терапии периимплантита и что дополнительные терапевтические меры, такие как дополнительное использование Er:YAG-лазера и/или последующая костная могут потребоваться регенеративные процедуры.
Противоинфекционная терапия
Конкретная микробная информация о наличии предполагаемых патогенов необходима для принятия значимого решения относительно системной или местной антибактериальной терапии. Хотя состав поддесневого микробного компонента важен для выбора препарата, характер перорального распределения потенциальных патогенов также важен для принятия решения о том, следует ли вводить антимикробный агент местно или системно. Для выполнения этой задачи клиницисту необходимо посмотреть на состояние пародонта оставшихся зубов.
Исследование Schwarz et al. .[18] продемонстрировало, что лечение периимплантатной инфекции путем механической обработки пластиковыми кюретками в сочетании с терапией антисептиком (0,2% хлоргексидина) может привести к статистически значимому уменьшению кровотечения при зондировании, пери — зондирование глубины кармана имплантата и уровень клинического прикрепления через 6 месяцев по сравнению с исходным уровнем. Исследование, проведенное Renvert и соавт. [20], показало, что добавление антисептической терапии к механической обработке не дает дополнительных преимуществ при неглубоких периимплантатных поражениях, когда средняя глубина кармана для зондирования была <4 мм. Таким образом, представляется, что добавление антисептической терапии к механической обработке не дает дополнительных преимуществ при неглубоких периимплантатных поражениях со средней глубиной зондирования кармана <4 мм, но, по-видимому, обеспечивает дополнительные клинические улучшения при глубоких периимплантатных поражениях со средней глубиной зондирования кармана. >5 мм.
>5 мм.
Пациенты, страдающие локальными периимплантными проблемами при отсутствии других инфекций, могут быть кандидатами на лечение с помощью устройств для местной доставки лекарств. Местное применение антибиотиков путем введения тетрациклиновых нитей на 10 дней [5] может обеспечить устойчивую высокую дозу противомикробного препарата именно в пораженный участок в течение нескольких дней. Использование минокклиновых микросфер в качестве дополнения к механической терапии полезно при лечении периимплантатных поражений, но лечение может потребоваться повторить [21]. Исследование Ренверта et al. . [20] продемонстрировали, что дополнительные преимущества, получаемые от добавления антибиотика миноциклина к механической обработке раны, как правило, больше, хотя и в ограниченной степени, чем те, которые достигаются при комбинированном использовании антисептика (хлоргексидин) и механической обработки. санация. Улучшение глубины зондирования вокруг имплантата, достигнутое при дополнительном применении миноциклина, может сохраняться в течение краткосрочного периода в 12 месяцев. В исследовании Renvert et al. [20] выявленная потеря кости составила не более трех витков резьбы имплантата.
В исследовании Renvert et al. [20] выявленная потеря кости составила не более трех витков резьбы имплантата.
Если проблема носит генерализованный характер, собирают конкретную микробиологическую информацию и системно назначают антибиотики. Lang и соавт. [5] предлагают следующие схемы антибиотикотерапии: системный орнидазол 500 мг два раза в день в течение 10 дней или метронидазол 250 мг три раза в день в течение 10 дней или комбинация метронидазола 500 мг и амоксициллина 375 мг один раз в день в течение 10 дней. Если периимплантит связан с персистирующим заболеванием пародонта, необходимо лечить оба состояния. В этом случае можно рассмотреть дополнительное применение системных антибиотиков. В настоящее время нет доступных клинических испытаний по системному введению антибиотиков для терапии периимплантита.
При условии соблюдения механических и антисептических протоколов до назначения антибиотикотерапии представляется, что неглубокие инфекции вокруг имплантатов можно успешно контролировать с помощью антибиотиков.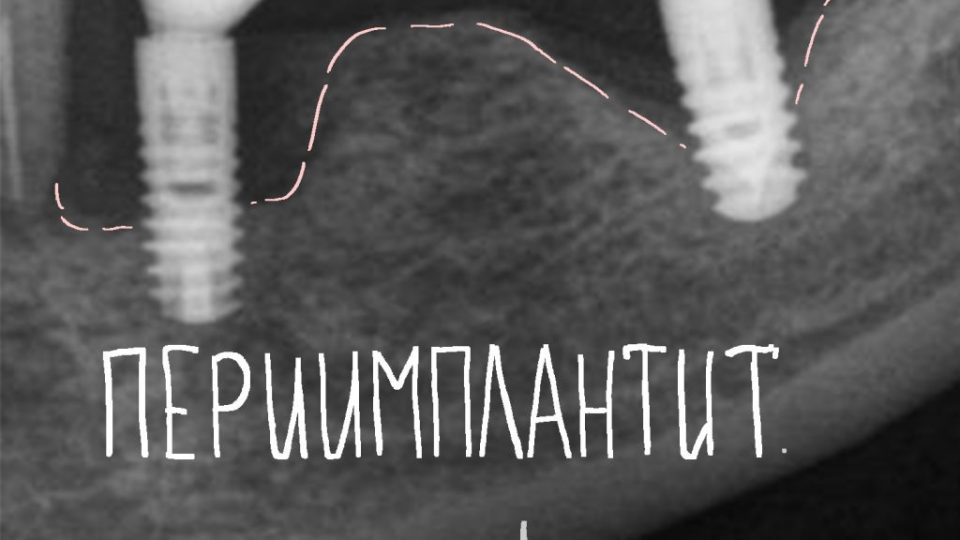 [1] Но все еще остается открытым вопрос, можно ли адекватно лечить более глубокие периимплантатные поражения нехирургическим путем, комбинируя местный антибиотик и механическую обработку.
[1] Но все еще остается открытым вопрос, можно ли адекватно лечить более глубокие периимплантатные поражения нехирургическим путем, комбинируя местный антибиотик и механическую обработку.
Хирургическая техника
Хирургическая резекция обычно ограничивается имплантатами, установленными в неэстетичных местах.[22] Хирургический лоскут помогает в комплексной хирургической обработке и обеззараживании пораженного имплантата. Проведенное хирургическое лечение с использованием: (1) аутокостных трансплантатов, покрытых мембранами, (2) только аутокостных трансплантатов, (3) только мембран и (4) процедуры лоскута контрольного доступа показало, что дефекты, обработанные покрытыми мембранами аутогенными трансплантатами кость продемонстрировала значительно большее количество костной регенерации и реостеоинтеграции, чем у тех, кто лечился с помощью других трех процедур. [12] Однако обнажение мембран является частым осложнением после таких процедур. Воздействие пористых мембран из вспененного ПТФЭ может привести к проникновению бактерий и вызвать инфекцию. [23]
[23]
На сегодняшний день нет доступных рандомизированных контролируемых клинических испытаний по использованию операции лоскута доступа (санация открытым лоскутом) только для лечения периимплантита. Рандомизированное сравнительное клиническое исследование, проведенное Romeo и соавт. [24, 25], показало, что резекционные хирургические процедуры в сочетании с имплантопластикой могут оказывать положительное влияние на показатели выживаемости имплантатов с шероховатой поверхностью, пораженных периимплантитом, а также на периимплантит. клинические параметры имплантата, такие как глубина зондирования кармана, нагноение и кровотечение из борозды. Исследование Шварца et al. . [26] продемонстрировали, что как нанокристаллический гидроксиапатит, так и направленная костная регенерация обеспечивают клинически значимое улучшение клинических параметров после 6 месяцев заживления без погружения. Двухлетние результаты Schwarz et al. . [27] того же клинического исследования еще раз продемонстрировали, что оба метода лечения были эффективны в обеспечении клинически значимого уменьшения глубины зондирования кармана и увеличения уровня клинического прикрепления, но применение комбинация природного костного минерала и коллагеновой мембраны, по-видимому, коррелирует с более значительными улучшениями этих клинических параметров и, следовательно, связана с более предсказуемым и улучшенным результатом заживления.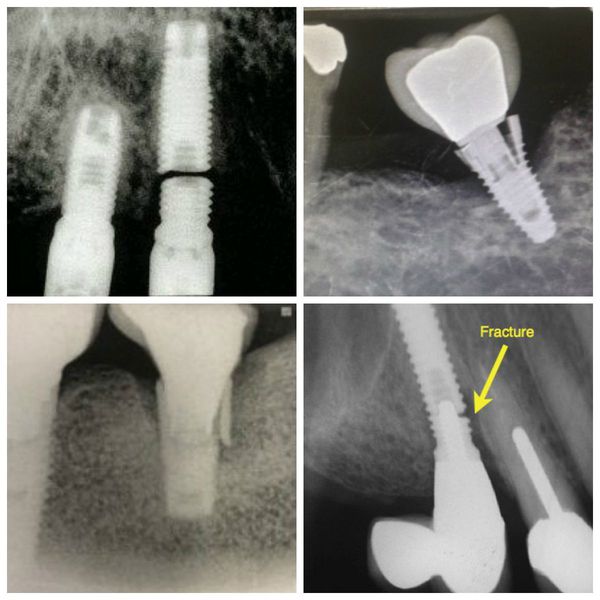 К сожалению, относительно небольшой размер выборки исследования (22 пациента) не позволил провести надежное статистическое сравнение эффективности двух терапевтических процедур. В целом необходимо накапливать больше данных о различных регенеративных методиках лечения периимплантитов.
К сожалению, относительно небольшой размер выборки исследования (22 пациента) не позволил провести надежное статистическое сравнение эффективности двух терапевтических процедур. В целом необходимо накапливать больше данных о различных регенеративных методиках лечения периимплантитов.
Эксплантация
Если имеется прогрессирующая потеря костной массы и невозможно сохранить имплантат, его необходимо удалить. Если было принято решение об удалении имплантата, доступны трепаны для эксплантации, подходящие для соответствующей системы имплантатов. Следует отметить, что эти трепаны имеют внешний диаметр до 1,5 мм больше, чем диаметр удаляемого имплантата. Таким образом, эксплантация может быть связана со значительным удалением кости, включая кортикальный слой щечной или язычной кости, и повреждением соседних естественных зубов, где межкорневое пространство ограничено. Альтернативный подход заключается в том, чтобы допустить прогрессирующую потерю костной массы из-за периимплантита, что приводит к достаточной потере костной ткани, чтобы можно было удалить имплантат с помощью щипцов для извлечения.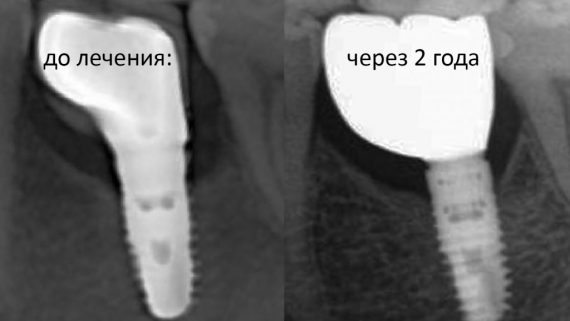 Имплантаты могут быть удалены щипцами, когда остаточная костная опора составляет менее 3–4 мм.
Имплантаты могут быть удалены щипцами, когда остаточная костная опора составляет менее 3–4 мм.
В связи с тем, что частота поздних отторжений имплантатов относительно низка, количество лонгитюдных исследований, оценивающих различные протоколы лечения периимплантита, ограничено. Более того, этические соображения часто не позволяют включать в такие испытания надлежащий плацебо-контроль. Протокол лечения будет отличаться в зависимости от того, является ли это периимплантным мукозитом или периимплантитом. Если нет потери костной массы, т. е. в случае мукозита, бактериальный налет и конкременты следует удалить, а химический контроль налета достигается с помощью местного применения 0,12% хлоргексидина каждые 8–12 ч в течение 15 дней; пациент должен дать инструкции по гигиене полости рта. Конструкция протеза также должна быть проверена и при необходимости изменена, чтобы исправить дефекты конструкции, препятствующие надлежащей гигиене, а также скорректировать вовлеченные факторы биомеханического стресса. После того, как этот начальный этап завершен, необходимо запланировать периодические проверки, постепенно сокращая интервалы между посещениями технического обслуживания.[28]
После того, как этот начальный этап завершен, необходимо запланировать периодические проверки, постепенно сокращая интервалы между посещениями технического обслуживания.[28]
Если диагностирован периимплантит, лечение будет зависеть от количества утраченной кости и эстетического воздействия рассматриваемого имплантата. Если потеря костной массы находится на начальной стадии, лечение будет таким же, как и при периимплантном мукозите, с добавлением обеззараживания ортопедических абатментов и антибиотиков. Если потеря костной ткани прогрессирует или сохраняется, несмотря на первоначальное лечение, необходимо хирургическим путем очистить мягкие ткани вокруг имплантата, пораженные хронической инфекцией, обеззаразить поверхность микроимплантата и, наконец, применить методы костной регенерации, направленные на восстановление утраченной кости.
До сих пор не было установлено ни одной методологии в качестве золотого стандарта лечения периимплантита. Таким образом, терапия периимплантита включает (а) нехирургическую фазу, включающую санацию механическими средствами, ультразвуковыми или лазерными устройствами, отдельно или в сочетании с антисептиками и/или антибиотиками, и (б) хирургическую фазу с использованием либо резективной или регенеративные методы.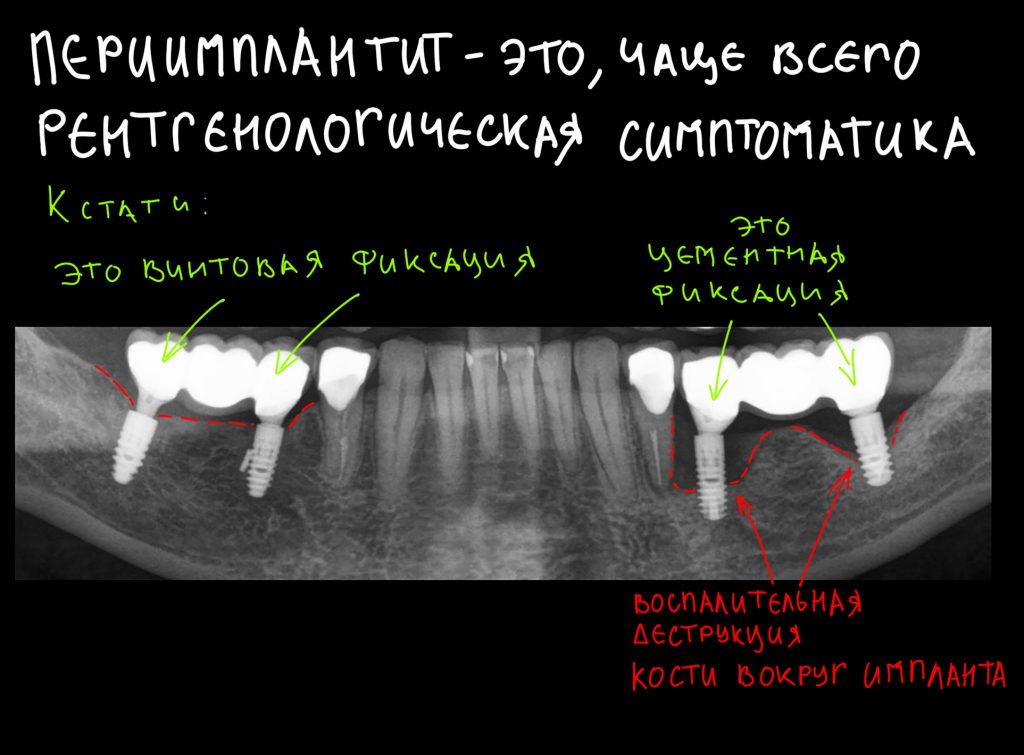
Имеющиеся рандомизированные контролируемые и/или сравнительные клинические испытания по лечению периимплантита ограничены по количеству и имеют короткие периоды наблюдения и небольшие размеры выборки, что свидетельствует о высоком риске систематической ошибки. До сих пор сомнительно, какие терапевтические стратегии являются наиболее эффективными для лечения периимплантитных поражений в зависимости от их морфологии, протяженности и тяжести. Однако это не означает, что применяемые в настоящее время методы лечения могут не давать положительных результатов в клинической практике.
Несмотря на недостаточный уровень существующих доказательств, некоторые данные, как правило, указывают на следующее. Одной обработки подслизистой оболочки может быть недостаточно для удаления бактериальной нагрузки с поверхностей имплантатов с периимплантными карманами ≥5 мм [13]. Использование лазера Er:YAG может улучшить клинические параметры вокруг имплантата в течение 6 месяцев, но остается неясным, могут ли эти эффекты сохраняться с течением времени. [19] Комбинация миноциклина и механической обработки, по-видимому, обеспечивает улучшение результатов лечения, хотя и в ограниченной степени, по сравнению с комбинацией хлоргексидина и механической обработки, по крайней мере, в течение краткосрочного периода в 12 месяцев.[20] Направленная костная регенерация или применение костного заменителя (нанокристаллического гидроксиапатита) могут быть эффективными при лечении периимплантитных поражений.[26]
[19] Комбинация миноциклина и механической обработки, по-видимому, обеспечивает улучшение результатов лечения, хотя и в ограниченной степени, по сравнению с комбинацией хлоргексидина и механической обработки, по крайней мере, в течение краткосрочного периода в 12 месяцев.[20] Направленная костная регенерация или применение костного заменителя (нанокристаллического гидроксиапатита) могут быть эффективными при лечении периимплантитных поражений.[26]
Только долгосрочные клинические рандомизированные контролируемые испытания могут дать окончательный ответ на вопрос о наилучшем способе решения проблем с имплантантами.
Долгосрочный успех имплантата зависит от регулярной программы обслуживания. Во время поддерживающей фазы ткань вокруг имплантата должна быть оценена на наличие воспаления. Рентгенограммы дадут состояние кости вокруг имплантатов. Эти программы помогают в долгосрочном успехе имплантата.
Прогноз пораженного имплантата будет зависеть от раннего выявления и лечения периимплантатного мукозита и периимплантита.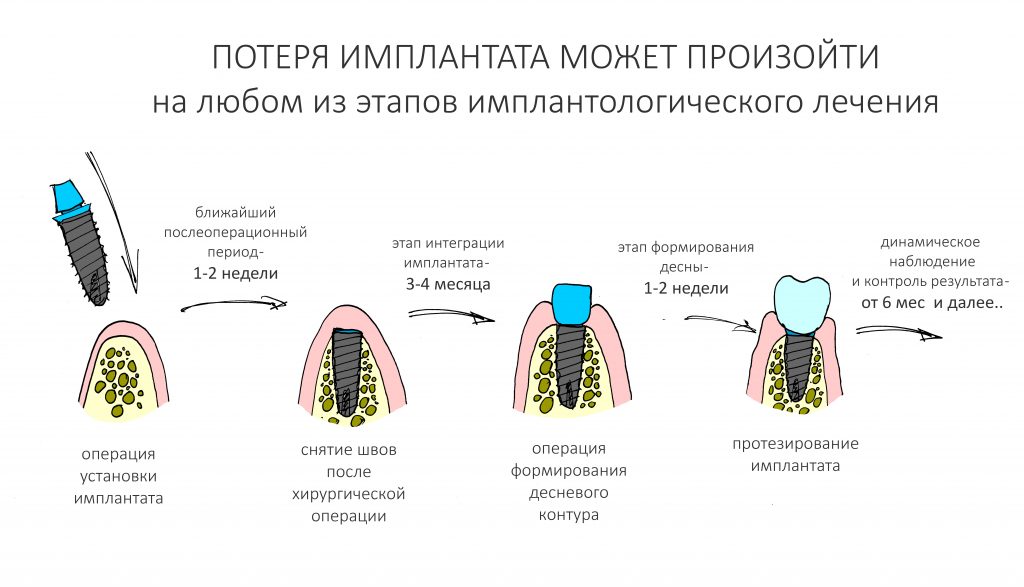 Несмотря на то, что исследования, посвященные различным методам лечения периимплантита, несопоставимы, общая картина некоторого клинического улучшения возникает при использовании противоинфекционной терапии с точки зрения разрешения воспаления и заживления костей. Это наблюдение в сочетании с нашими знаниями о неоспоримой роли пародонтальных патогенов в этиологии периимплантита указывает на то, что какая-то форма противоинфекционной терапии должна сочетаться с любой другой стратегией решения этой проблемы.
Несмотря на то, что исследования, посвященные различным методам лечения периимплантита, несопоставимы, общая картина некоторого клинического улучшения возникает при использовании противоинфекционной терапии с точки зрения разрешения воспаления и заживления костей. Это наблюдение в сочетании с нашими знаниями о неоспоримой роли пародонтальных патогенов в этиологии периимплантита указывает на то, что какая-то форма противоинфекционной терапии должна сочетаться с любой другой стратегией решения этой проблемы.
Источник поддержки: Нет.
Конфликт интересов: Не заявлено.
1. Момбелли А., Ланг Н.П. Диагностика и лечение периимплантита. Пародонтология 2000. 1998;17:63–76. [PubMed] [Google Scholar]
2. Йованович С. Лечение периимплантатного разрушения вокруг функционирующих остеоинтегрированных зубных имплантатов. J Пародонтол. 1993;64:1176–83. [PubMed] [Google Scholar]
3. Альбректссон Т., Исидор Ф. Согласованный отчет о заседании IV.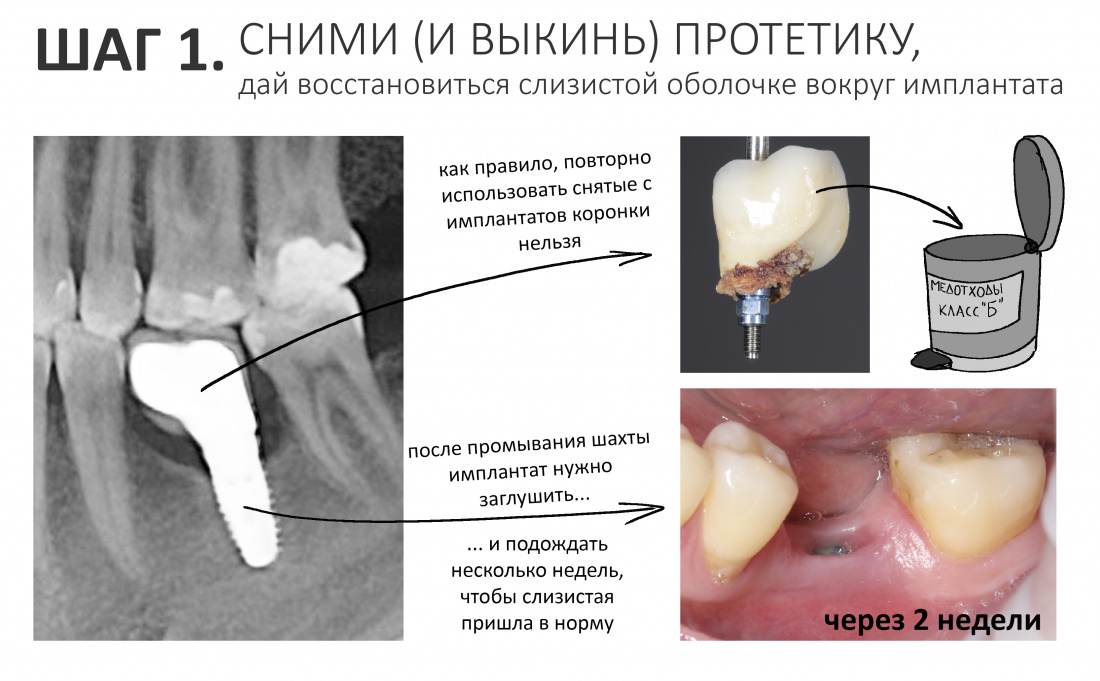 В: Ланг Н.П., Карринг Т., редакторы. Материалы первого европейского семинара по пародонтологии. Лондон: квинтэссенция; 1994. стр. 365–9. [Google Scholar]
В: Ланг Н.П., Карринг Т., редакторы. Материалы первого европейского семинара по пародонтологии. Лондон: квинтэссенция; 1994. стр. 365–9. [Google Scholar]
4. Берглунд Т., Перссон Л., Клинге Б. Систематический обзор частоты биологических и технических осложнений в имплантации зубов, о котором сообщалось в проспективных лонгитюдных исследованиях продолжительностью не менее 5 лет. Дж. Клин Пародонтол. 2002; 29 (Приложение 3): 197–212. [PubMed] [Google Scholar]
5. Ланг Н.П., Уилсон Т.Г., Корбет Э.Ф. Биологические осложнения при имплантации зубов: их профилактика, диагностика и лечение. Clin Oral Implants Res. 2000; 11 (Приложение 1): 146–55. [PubMed] [Академия Google]
6. Георгиев Т. Способ лечения периимплантитов. Journal of IMAB – Annual Proceeding (Scientific Papers) 2009 book 2. [Google Scholar]
7. Смайлер Д., Солтан М. Дерево решений по костной пластике: систематическая методология создания новой кости. Имплант Дент. 2006; 15:122–8. [PubMed] [Google Scholar]
8.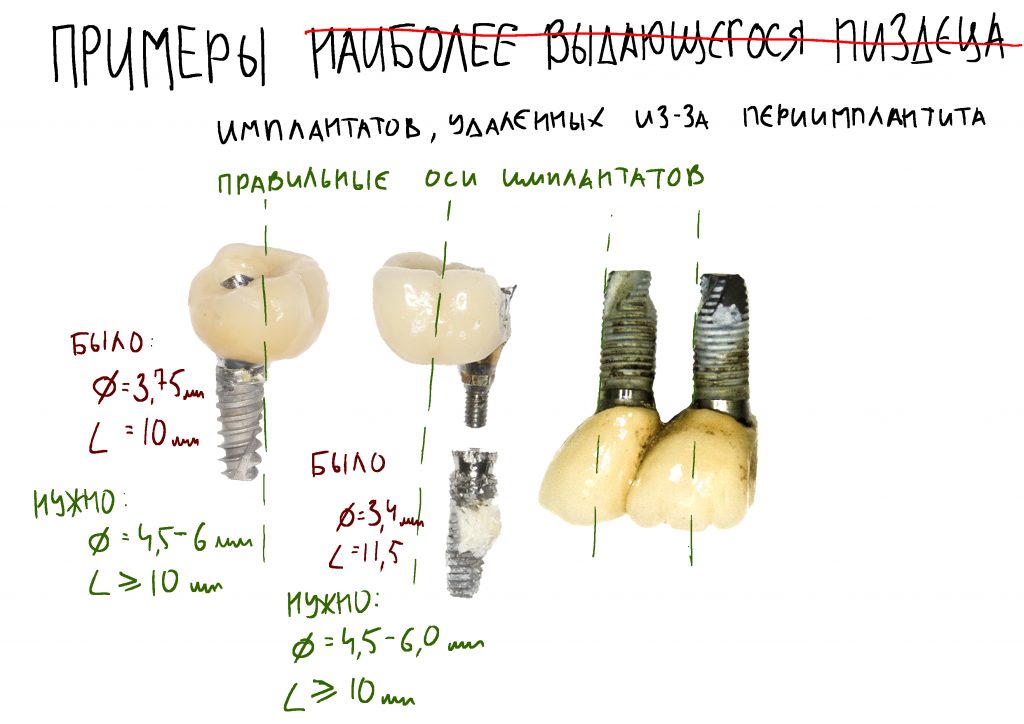 Heydenrijk K, Meijer JA, Van der Reijden WA, Raghoebar GM, Vissink A, Stegenga B. Микробиота вокруг корневых внутрикостных имплантатов: обзор литературы. Оральные челюстно-лицевые имплантаты Int J. 2002;17:829–38. [PubMed] [Google Scholar]
Heydenrijk K, Meijer JA, Van der Reijden WA, Raghoebar GM, Vissink A, Stegenga B. Микробиота вокруг корневых внутрикостных имплантатов: обзор литературы. Оральные челюстно-лицевые имплантаты Int J. 2002;17:829–38. [PubMed] [Google Scholar]
9. Shibli JA, Compagnoni MM, Moreira RF, Marcantonio E. Микробиологический и рентгенографический анализ индуцированного лигатурой периимплантита с различными поверхностями зубных имплантатов. Оральные челюстно-лицевые имплантаты Int J. 2003; 18: 383–90. [PubMed] [Google Scholar]
10. Абрахамссон И., Берглунд Т., Веннстрем Дж., Линде Дж. Характеристики твердых и мягких тканей периимплантата при различных системах имплантатов. Сравнительное исследование на собаке. Clin Oral Implants Res. 1996;7:212–9. [PubMed] [Google Scholar]
11. Матарассо С., Куаремба Г., Кораджио Ф., Вайя Э., Кафьеро С., Ланг Н.П. Уход за имплантатами: исследование in vitro , посвященное модификациям поверхности титановых имплантатов после применения различных профилактических процедур. Clin Oral Implants Res. 1996; 7: 64–72. [PubMed] [Google Scholar]
Clin Oral Implants Res. 1996; 7: 64–72. [PubMed] [Google Scholar]
12. Schou S, Berglundh T, Lang NP. Хирургическое лечение периимплантита. Оральные челюстно-лицевые имплантаты Int J. 2004; 19 (прил.): 140–9. [PubMed] [Академия Google]
13. Карринг Э.С., Ставропулос А., Эллегаард Б., Карринг Т. Лечение периимплантита системой «Векторс». Пилотное исследование. Clin Oral Implants Res. 2005; 16: 288–93. [PubMed] [Google Scholar]
14. Schou S, Holmstrup P, Jorgensen T, Skovgaard LT, Stoltze K, Hjorting-Hansen E, et al. Подготовка поверхности имплантата при хирургическом лечении экспериментального периимплантита с использованием аутогенного костного трансплантата и мембраны из вспененного политетрафторэтилена у яванских макаков. Clin Oral Implants Res. 2003; 14: 412–22. [PubMed] [Академия Google]
15. Хаас Р., Дёртбудак О., Менсдорф-Пуйи Н., Майлат Г. Уничтожение бактерий на различных поверхностях имплантатов с помощью фотосенсибилизации и мягкого лазера. Исследование in vitro .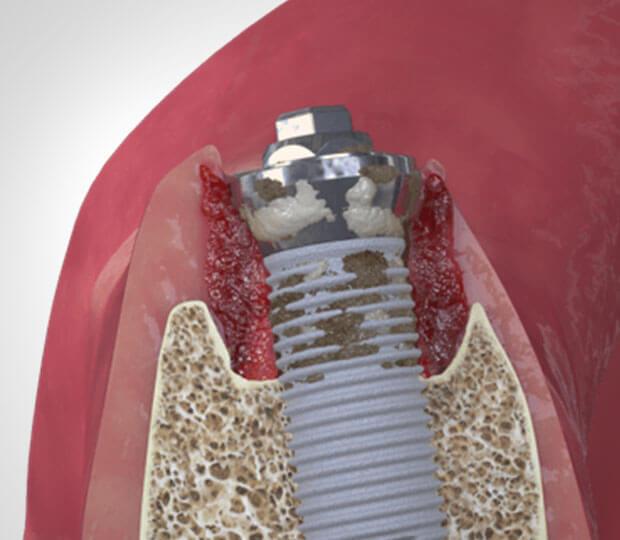 Clin Oral Implants Res. 1997; 8: 249–54. [PubMed] [Google Scholar]
Clin Oral Implants Res. 1997; 8: 249–54. [PubMed] [Google Scholar]
16. Ricardo RA, Ney SA, Marco AG, Jonathan F, Carlos A, Aécio MY, et al. Сравнительное исследование между эффектами фотодинамической терапии и традиционной терапии на уменьшение количества микробов при индуцированном лигатурой периимплантите у собак. J Пародонтол. 2005; 76: 1275–81. [PubMed] [Академия Google]
17. Rutger GP, Ann-Marie RJ, Christel L, Stefan R. Микробиологические результаты после нехирургического легирования эрбием: иттриевого, алюминиевого и гранатового лазера или воздушно-абразивного лечения периимплантита: рандомизированное клиническое исследование. J Пародонтол. 2011;82:1267–78. [PubMed] [Google Scholar]
18. Schwarz F, Sculean A, Bieling K, Ferrari D, Rothamel D, Becker J. Двухлетние клинические результаты после лечения поражений периимплантита с использованием нанокристаллического гидроксиапатита или природного костного минерала в в сочетании с коллагеновой оболочкой. Дж. Клин Пародонтол. 2008;35:80–7. [PubMed] [Академия Google]
2008;35:80–7. [PubMed] [Академия Google]
19. Schwarz F, Bieling K, Bonsmann M, Latz T, Becker J. Нехирургическое лечение умеренных и запущенных периимплантитных поражений: контролируемое клиническое исследование. Клин Орал Инвест. 2006; 10: 279–88. [PubMed] [Google Scholar]
20. Renvert S, Lessem J, Dahlen G, Renvert H, Lindahl C. Механическая и повторная противомикробная терапия с использованием местной системы доставки лекарств при лечении периимплантита: рандомизированное клиническое исследование. J Пародонтол. 2008; 79: 836–44. [PubMed] [Академия Google]
21. Renvert S, Lessem J, Dahlén G, Lindahl C, Svensson M. Микросферы миноциклина для местного применения по сравнению с гелем хлоргексидина для местного применения в качестве дополнения к механической обработке зарождающихся периимплантатных инфекций: рандомизированное клиническое исследование. Дж. Клин Пародонтол. 2006; 33: 362–9. [PubMed] [Google Scholar]
22. Чен С., Дарби И. Зубные имплантаты: техническое обслуживание, уход и лечение инфекций вокруг имплантатов. Ост Дент Дж. 2003; 48: 212–20. [PubMed] [Google Scholar]
Ост Дент Дж. 2003; 48: 212–20. [PubMed] [Google Scholar]
23. Nowzari H, Slots J. Микробиологические и клинические исследования политетрафторэтиленовых мембран для направленной костной регенерации вокруг имплантатов. Оральные челюстно-лицевые имплантаты Int J. 1995;10:67–73. [PubMed] [Google Scholar]
24. Romeo E, Ghisolfi M, Murgolo N, Chiapasco M, Lops D, Vogel G. Терапия периимплантита с помощью резективной хирургии. 3-летнее клиническое испытание оральных имплантатов грубой винтовой формы. Часть I: Клинический результат. Clin Oral Implants Res. 2005; 16:9–18. [PubMed] [Google Scholar]
25. Romeo E, Lops D, Chiapasco M, Ghisolfi M, Vogel G. Терапия периимплантита резекционной хирургией. 3-летнее клиническое испытание оральных имплантатов грубой винтовой формы. Часть II: Рентгенографический результат. Clin Oral Implants Res. 2007;18:179–87. [PubMed] [Google Scholar]
26. Schwarz F, Bieling K, Latz T, Nuesry E, Becker J. Заживление внутрикостных периимплантитных дефектов после применения нанокристаллического гидроксиапатита (Ostimt) или ксенотрансплантата бычьего происхождения (Bio -Osst) в сочетании с коллагеновой мембраной (Bio-Gidet).