Наращивание костной ткани в стоматологии перед имплантацией
Наращивание костной ткани при имплантации — это вспомогательная процедура в стоматологическом процессе. Она расширяет возможности и добавляет объем челюсти. Сейчас используются современные опоры, которые изготавливаются из сверхпрочных медицинских составов. Поэтому методика наращивания костной ткани при имплантации применяется в клиниках реже. Ее выбирают при плохом состоянии места, после удаления зуба, которое было травмировано операцией или опухолью. Процедура помогает решить проблему с нехваткой поверхности для экспресс-имплантации в один этап.
Аугментация — это хирургическая операция, которая направлена на формирование искусственной полости в костном покрове. Производится введение специального материала или подсадка. Все методики распределяются по способу наращивания объемов.
Важно! Рассасывание кости происходит через три месяца после удаления зуба.
Объем теряется в различных направлениях. От этого зависит разновидность импланта, который будет использоваться при вживлении.
От этого зависит разновидность импланта, который будет использоваться при вживлении.
Стоматология активно развивается в вопросах хирургических вмешательств, внедряя новые методики. Именно поэтому способов замещения и добавления поверхности множество, но многие из них не теряют своей актуальности. Выделим наиболее распространенные варианты аугментации:
- Применение барьерных мембран — это профилактика, которая исключает импланты с наращиванием ткани, так как клетки эпителия не срастаются. После удаления зуба стоматолог закладывает остеопластический материал и перекрывает его.
- Расщепление кости используется в том случае, если нужно расширить альвеолярный гребень, для этого она делится на две части. Срок заживления биологической мембраны составляет до полугода.
- Аутотрансплантация — метод используется при наличии травм или в послеоперационный период. Заключается в пересадке части тазовой кости пациента в его же челюсть. Также применяется часть подбородка или нижней челюсти.

- Синус-лифтинг верхней челюсти — это щадящий способ операционного вмешательства.
- Гранульная остеопластика выполняется с применением искусственных материалов, восстанавливает высоту кости. Для этого стоматолог вскрывает десну и заполняет лунку гранулами, которые затем перекрываются биомембраной, могут быть установлены дополнительно импланты с наращиванием ткани. После этого стоматолог ушивает десну, срок заживления составляет шесть месяцев.
Выбор в пользу определенного способа основывается на предварительных анализах и комплексном изучении особенностей десны пациента.
Зачем наращивать костную ткань
При наличии дефекта в ложе оно не принимается имплантом. Если данная особенность располагается в вертикальной и горизонтальной плоскости, тогда стоматолог использует имплант с наращиванием ткани или подбирает индивидуальный метод исправления дефекта.
При хирургическом удалении зуба возможны повреждения различного характера, которые приводят к физиологической перенастройке организма. Формирование узкого гребня провоцирует применение дополнительных технологий в стоматологическом процессе.
Формирование узкого гребня провоцирует применение дополнительных технологий в стоматологическом процессе.
Восстановить объем кости можно только хирургическим путем. Она требует длительного периода восстановления, а также может вызвать ощущение дискомфорта. Последствия должны строго контролироваться специалистом. Операция длится более одного часа.
Рекомендации специалиста
Важно! Наша клиника не делает аугментацию, материал представлен в ознакомительных целях.
Перед работой стоматолог обязан провести полную санацию полости рта. Нередко может понадобиться костная пластика. Главное — помнить, что перед хирургическим вмешательством требуется пройти все необходимые обследования. Они определят возможность использования данного способа наращивания.
После процедуры стоматолог выдает пациенту рекомендации по уходу за полостью рта. Их нужно соблюдать ровно в том объеме, который требуется для полной реабилитации пациента.
Современные технологии позволяют добавить эпителий без хирургического вмешательства.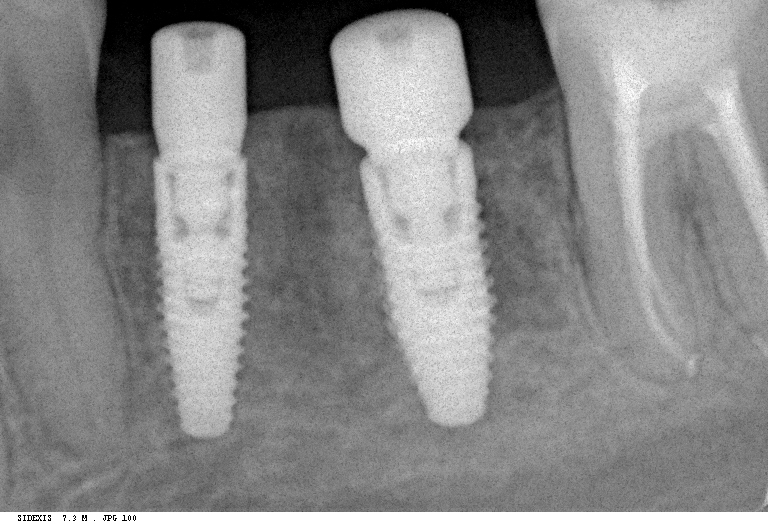 Это намного безопаснее и не требует абсолютно здорового организма.
Это намного безопаснее и не требует абсолютно здорового организма.
←Вернуться к списку статей
Синус лифтинг — наращивание костной ткани для имплантации зубов
Синус-лифтинг – это хирургическая процедура, заключающаяся в поднятии дна гайморовой пазухи. В стоматологии данная манипуляция проводиться в основном перед постановкой дентальных имплантатов.
При постановке имплантатов, чаще всего возникает проблема отсутствия необходимого объема костной ткани. Другими словами не хватает кости, в которую необходимо установить дентальный имплантат. Это вполне решаемая задача, благодаря так называемой костной пластике. С помощью собственной или искусственно выращенной кости, наращивается недостающий объем. На нижней челюсти все просто, а с верхней челюстью возникают затруднения, так как она имеет две воздушные полости, называемые гайморовыми пазухами или синусами. Очень часто встречается то, что дно гайморовой пазухи обращенной к корням зубов верхней челюсти, очень тонкое.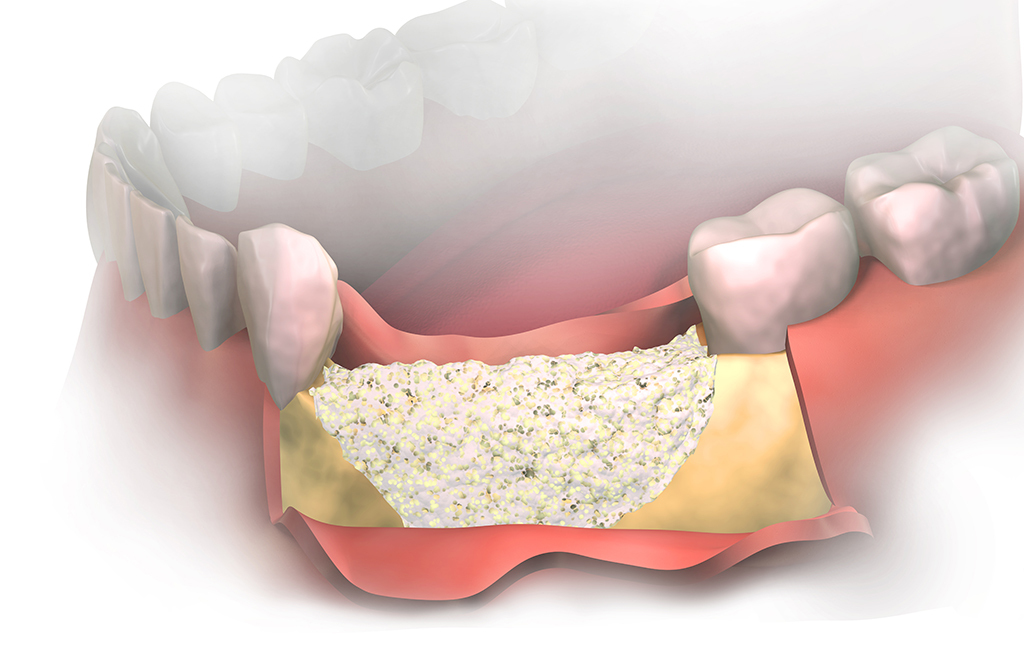 Из-за чего поставить зубной имплантат не представляется возможным. Именно поэтому придумали такую операцию, как поднятие дна гайморовой пазухи или другими словами синус-лифтинг.
Из-за чего поставить зубной имплантат не представляется возможным. Именно поэтому придумали такую операцию, как поднятие дна гайморовой пазухи или другими словами синус-лифтинг.
Синус-лифтинг – это операция, во время которой проводится искусственное увеличение массива костной ткани дна верхнечелюстной пазухи при недостаточном ее количестве, препятствующей проведению имплантации в области боковых зубов верхней челюсти. Анатомия верхнечелюстной пазухи меняется ровно настолько, насколько кости не хватает для установки импланта.
Цель операции – введение в область дна гайморовой пазухи костного вещества, которое в течение 8 – 12 месяцев преобразуется в собственную костную ткань.
Процедура синус-лифтинга очень проста и легко переносится пациентом, ускоряется процесс восстановления костной ткани в области дефекта.
Различают открытый и закрытый синус-лифтинг.
При закрытом сину-слифтинге костное вещество вводится через окно имплантата.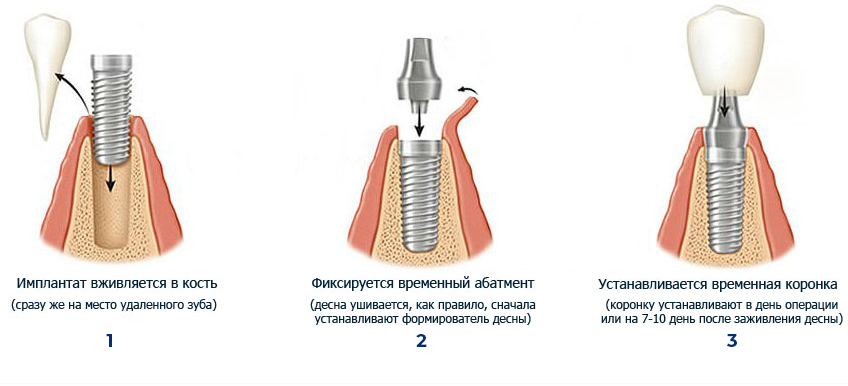
При открытом синус-лифтинге – через боковой доступ через преддверие полости рта.
Так как синус-лифтингэто достаточно серьезное оперативное вмешательство, помимо стандартных послеоперационных ограничений, существует ряд рекомендаций, которые в обязательном порядке необходимо выполнять на протяжении 3-4 недель. А именно, после синус-лифтигна нельзя сморкаться, чихать, пить напитки через трубочку, летать на самолете и нырять под воду. Рекомендуется кашлять и чихать, открывая рот и при этом прикрываться носовым платком. Так же, назначаются антибиотики широкого спектра, кератопластики локально, для быстрого заживления операционной раны и сосудосуживающие препараты, которые необходимо закапывать в полость носа.
Выполнение всех рекомендаций позволит свести к минимуму все возможные осложнения, в виде гайморита, смещения костного материала и повторного инфицирования.
youtube.com/v/DucFgDd05dY?version=3&hl=ru_RU&rel=0″ type=»application/x-shockwave-flash»/>
Наращивание кости для установки имплантатов: последние достижения
1. Альхаммади М.С., Аль-Машраки А.А., Алнами Р.Х. и соавт. Точность и воспроизводимость измерений лица на цифровых фотографиях и фотографиях, полученных с помощью конусно-лучевой компьютерной томографии (КЛКТ). Диагностика . 2021;11(5):с. 757. doi: 10.3390/diagnostics11050757. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2. Рокая Д., Суттагул К., Сапкота Б., Махарджан С. К. Гендерное сравнение соотношения передних зубов верхней челюсти и размеров лица. Журнал международных стоматологических медицинских исследований . 2018;11(1):465–469. [Google Scholar]
3. Рокая Д., Бхаттараи Б., Суттагул К., Кафле Д., Хумагайн М. Подбородочно-губные борозды: эстетическая классификация. Журнал Института медицинских наук им. Датта Меге Университета . 2018;13(1):16–19. doi: 10.4103/jdmimsu.jdmimsu_80_17. [CrossRef] [Google Scholar]
doi: 10.4103/jdmimsu.jdmimsu_80_17. [CrossRef] [Google Scholar]
4. Humagain M., Rokaya D., Srii R., Dixit S., Kafle D. Гендерное сравнение эстетики зенита десны. Медицинский журнал Университета Катманду (KUMJ) . 2016;14(54):148–152. [PubMed] [Google Scholar]
5. Papathanasiou E., Finkelman M., Hanley J., Parashis A.O. Распространенность, этиология и лечение периимплантатного мукозита и периимплантита: опрос пародонтологов в США. Журнал пародонтологии . 2016;87(5):493–501. doi: 10.1902/jop.2015.150476. [PubMed] [CrossRef] [Google Scholar]
6. Годовой отчет за 2013 г., открывая новую страницу, Straumann, 2013 г., http://www.straumann.com/content/dam/internet/straumanncom/Resources/investor-relations /annual-report/2013/STMN-2013-Annual-Report.pdf.
7. Рокая Д., Шриманипонг В., Виситрасамеевон В., Хумагайн М., Туньякитписал П. Обновление периимплантита: индикаторы риска, диагностика и лечение. Европейский журнал дерматологии . 2020;14(4):672–682. doi: 10.1055/s-0040-1715779. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020;14(4):672–682. doi: 10.1055/s-0040-1715779. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Kurtz S.M., Devine J.N. Биоматериалы PEEK в травматологических, ортопедических и спинальных имплантатах.
9. Аморнвит П., Рокая Д., Байрачарья С., Кеавчароен К., Супаванич В. Лечение обструктивного апноэ во сне с помощью имплантата, удерживающего устройство для продвижения нижней челюсти. Всемирный стоматологический журнал . 2014;5(3):184–189. doi: 10.5005/jp-journals-10015-1285. [CrossRef] [Google Scholar]
10. Trinh H. A., Dam V. V., Le B., Pittayapat P., Thunyakitpisal P. Непрямая аугментация синуса с добавлением биоматериала и без него: рандомизированное контролируемое клиническое исследование. Имплантационная стоматология . 2019;28(6):571–577. doi: 10.1097/ID.0000000000000941.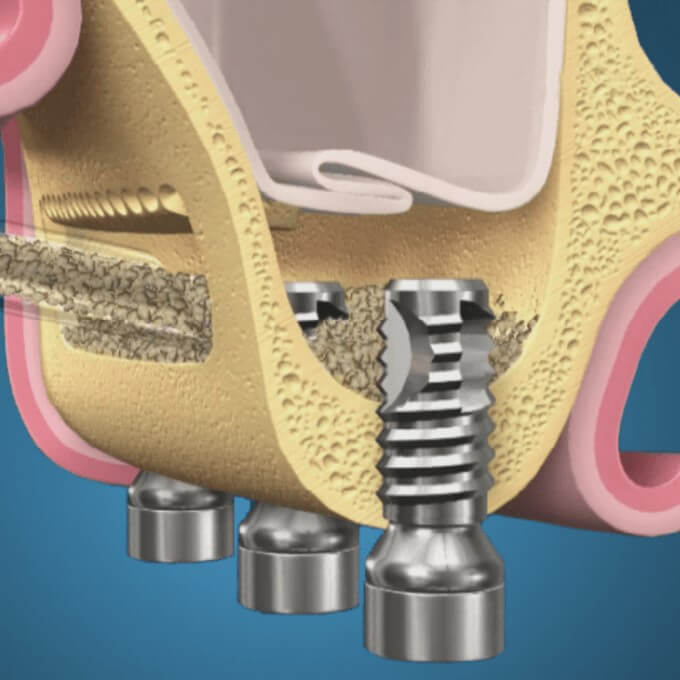 [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
11. Lee J.D., Jung S., Wang C.-W., Lee S.J. Интегрированный цифровой и традиционный рабочий процесс лечения в управляемой полной реабилитации ротовых имплантатов: отчет о клиническом случае. Стоматологический журнал . 2019;7(4):с. 100. doi: 10.3390/dj7040100. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Поли П. П., Муктадар А. К., Соуза Ф. А., Майорана К., Беретта М. Компьютерная установка имплантата в сочетании с компьютерной регенерацией кости в лечении атрофированных частично беззубых альвеолярных гребней: исследование, подтверждающее концепцию. Журнал стоматологических наук . 2021;16(1):333–341. doi: 10.1016/j.jds.2020.02.010. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Веннерберг А., Альбректссон Т. О поверхностях имплантатов: обзор современных знаний и мнений. Международный журнал челюстно-лицевых имплантатов . 2010;25(1):63–74. [PubMed] [Google Scholar]
14.
15. Шриманипонг В. Различная топография поверхности дентального имплантата. Стоматологический журнал Чулалонгкорнского университета . 2001; 24:51–56. [Google Scholar]
16. Jazayeri H.E., Tahriri M., Razavi M., et al. Текущий обзор материалов и стратегий для потенциального использования в регенерации тканей челюстно-лицевой области. Материаловедение и инженерия: C . 2017; 70 (часть 1): 913–929. doi: 10.1016/j.msec.2016.08.055. [PubMed] [CrossRef] [Google Scholar]
17. García-Gareta E., Coathup M.J., Blunn G.W. Остеоиндукция материалов для костной пластики для восстановления и регенерации кости. Кость . 2015; 81: 112–121. [PubMed] [Google Scholar]
18. Sayed M.E., Mugri M.H., Almasri M.A., et al. Роль стволовых клеток в усилении остеоинтеграции зубных имплантатов: систематический обзор. Покрытия . 2021;11 doi: 10.3390/покрытия11091035. [CrossRef] [Google Scholar]
Sayed M.E., Mugri M.H., Almasri M.A., et al. Роль стволовых клеток в усилении остеоинтеграции зубных имплантатов: систематический обзор. Покрытия . 2021;11 doi: 10.3390/покрытия11091035. [CrossRef] [Google Scholar]
19. Bhandi S., Alkahtani A., Reda R., et al. Секреция паратгормона и экспрессия рецепторов определяют возрастную степень остеогенной дифференцировки стволовых клеток пульпы зуба. Журнал персонализированной медицины . 2021; 11(5) doi: 10.3390/jpm11050349. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Tappa K., Jammalamadaka U. Новые биоматериалы, используемые в методах медицинской 3D-печати. Журнал функциональных биоматериалов . 2018;9(1) doi: 10.3390/jfb
17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Дерахшанфар С., Мбелек Р., Сюй К., Чжан С., Чжун В., Син М. 3D-биопечать для биомедицинских устройств и тканевой инженерии : обзор последних тенденций и достижений.  2018;3(2):144–156. doi: 10.1016/j.bioactmat.2017.11.008. [PubMed] [CrossRef] [Google Scholar]
2018;3(2):144–156. doi: 10.1016/j.bioactmat.2017.11.008. [PubMed] [CrossRef] [Google Scholar]
22. Деев Р. В., Дробышев А. Ю., Бозо И. Ю., Исаев А. А. Обычные и активированные костные трансплантаты: прикладная классификация и основные признаки. Международная организация биомедицинских исследований . 2015;2015:19. doi: 10.1155/2015/365050.365050 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Chiapasco M., Casentini P., Zaniboni M. Процедуры увеличения кости в имплантологии. Международный журнал челюстно-лицевых имплантатов . 2009; 24: 237–259. [PubMed] [Google Scholar]
24. Kim Y.J., Saiki C.E.T., Silva K., et al. Формирование кости в трансплантатах с биооссом и аутогенной костью в разных пропорциях в своде черепа кролика. Международный стоматологический журнал . 2020;2020:6. doi: 10.1155/2020/2494128.2494128 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Кумар П., Винита Б., Фатима Г. Костные трансплантаты в стоматологии. Журнал фармации и смежных биологических наук . 2013;5:С125–С127. doi: 10.4103/0975-7406.113312. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Костные трансплантаты в стоматологии. Журнал фармации и смежных биологических наук . 2013;5:С125–С127. doi: 10.4103/0975-7406.113312. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
26. Moussa N., Fan Y., Dym H. Материалы для костной пластики челюстно-лицевой области. Стоматологические клиники Северной Америки . 2021;65(1):167–195. doi: 10.1016/j.cden.2020.09.012. [PubMed] [CrossRef] [Google Scholar]
27. Laurencin C., Khan Y., El-Amin S.F. Заменители костных трансплантатов. Экспертиза медицинских изделий . 2006;3(1):49–57. doi: 10.1586/17434440.3.1.49. [PubMed] [CrossRef] [Google Scholar]
28. Мусса Н. Т., Дым Х. Материалы для костной пластики челюстно-лицевой области. Стоматологические клиники Северной Америки . 2020;64(2):473–490. doi: 10.1016/j.cden.2019.12.011. [PubMed] [CrossRef] [Академия Google]
29. Carmagnola D., Abati S., Celestino S., Chiapasco M., Bosshardt D., Lang N.P. Оральные имплантаты, помещенные в костные дефекты, обработанные биооссом, остим-пастой или периогласом: экспериментальное исследование на кролике голени. Клинические исследования оральных имплантатов . 2008;19(12):1246–1253. doi: 10.1111/j.1600-0501.2008.01584.x. [PubMed] [CrossRef] [Google Scholar]
Клинические исследования оральных имплантатов . 2008;19(12):1246–1253. doi: 10.1111/j.1600-0501.2008.01584.x. [PubMed] [CrossRef] [Google Scholar]
30. Browaeys H., Bouvry P., De Bruyn H. Обзор литературы по биоматериалам в процедурах увеличения синуса. Клиническая имплантология и связанные с ней исследования . 2007;9(3):166–177. doi: 10.1111/j.1708-8208.2007.00050.x. [PubMed] [CrossRef] [Google Scholar]
31. Чавда С., Левин Л. Исследования увеличения вертикального и горизонтального альвеолярного гребня на людях, сравнивающие различные типы материалов для костных трансплантатов: систематический обзор. Журнал оральной имплантологии . 2018;44(1):74–84. doi: 10.1563/aaid-joi-d-17-00053. [PubMed] [CrossRef] [Google Scholar]
32. Maiorana C., Poli P.P., Mascellaro A., Ferrario S., Beretta M. Зубные имплантаты, установленные в резорбированные альвеолярные гребни, реконструированные с помощью аутогенных накладных трансплантатов из гребня подвздошной кости: а 26- Среднее последующее ретроспективное исследование за год.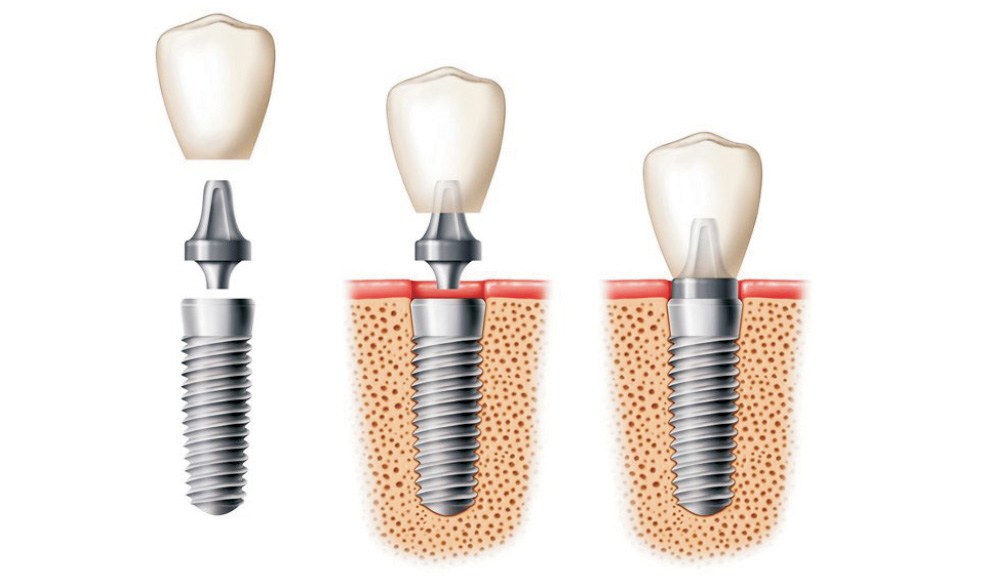 Журнал черепно-челюстно-лицевой хирургии . 2019;47(5):805–814. doi: 10.1016/j.jcms.2019.02.002. [PubMed] [CrossRef] [Google Scholar]
Журнал черепно-челюстно-лицевой хирургии . 2019;47(5):805–814. doi: 10.1016/j.jcms.2019.02.002. [PubMed] [CrossRef] [Google Scholar]
33. Агалу Т. Л., Мой П. К. Какие методы наращивания твердых тканей наиболее успешны для обеспечения костной поддержки при установке имплантатов? Международный журнал челюстно-лицевых имплантатов . 2007; 22:49–70. [PubMed] [Google Scholar]
34. Йылмаз М., Вайвада Х., Мендерес А., Демирдовер С., Кизилкая А. Сравнение васкуляризированного малоберцового лоскута и лоскута гребня подвздошной кости для реконструкции нижней челюсти. Журнал черепно-лицевой хирургии . 2008;19(1):227–234. doi: 10.1097/scs.0b013e31815c942c. [PubMed] [CrossRef] [Google Scholar]
35. Ferri J., Piot B., Ruhin B., Mercier J. Преимущества и недостатки свободного лоскута малоберцовой кости при реконструкции нижней челюсти. Журнал челюстно-лицевой хирургии . 1997;55(5):440–448. [PubMed] [Google Scholar]
36. Fasano D. , Montanari F.M., Cocchi R., Marchetti C. Малоберцовая кость со свободным лоскутом для реконструкции составных дефектов нижней челюсти. Acta Otorhinolaryngologica Italica . 1996;16(1):25–29. [PubMed] [Google Scholar]
, Montanari F.M., Cocchi R., Marchetti C. Малоберцовая кость со свободным лоскутом для реконструкции составных дефектов нижней челюсти. Acta Otorhinolaryngologica Italica . 1996;16(1):25–29. [PubMed] [Google Scholar]
37. Lonie S., Herle P., Paddle A., Pradhan N., Birch T., Shayan R. Реконструкция нижней челюсти: метаанализ подвздошных и малоберцовых лоскутов. ANZ Журнал хирургии . 2016;86(5):337–342. doi: 10.1111/ans.13274. [PubMed] [CrossRef] [Google Scholar]
38. Патель С.Ю., Ким Д.Д., Гали Г.Е. Челюстно-лицевая реконструкция с использованием васкуляризированных лоскутов малоберцовой кости и внутрикостных имплантатов. Клиники челюстно-лицевой хирургии Северной Америки . 2019;31(2):259–284. doi: 10.1016/j.coms.2018.12.005. [PubMed] [CrossRef] [Google Scholar]
39. Джексон Р. С., Прайс Д. Л., Арсе К., Мур Э. Дж. Оценка клинических результатов остеоинтегрированной дентальной имплантации свободных лоскутов малоберцовой кости для реконструкции нижней челюсти. Пластическая хирургия лица JAMA . 2016;18(3):201–206. doi: 10.1001/jamafacial.2015.2271. [PubMed] [CrossRef] [Google Scholar]
Пластическая хирургия лица JAMA . 2016;18(3):201–206. doi: 10.1001/jamafacial.2015.2271. [PubMed] [CrossRef] [Google Scholar]
40. Wei F.-C., Santamaria E., Chang Y.-M., Chen H.-C. Реконструкция нижней челюсти свободным кожно-костным лоскутом малоберцовой кости с одновременной установкой остеоинтегрированных дентальных имплантатов. Журнал черепно-лицевой хирургии . 1997;8(6):512–521. doi: 10.1097/00001665-199711000-00018. [PubMed] [CrossRef] [Google Scholar]
41. Барбер Б. Р., Дзигелевски П. Т., Чука Р., О’Коннелл Д., Харрис Дж. Р., Сейкали Х. Свободный малоберцовый лоскут с вдавленным в кость костью: долгосрочный успех зубного имплантата и осложнений по сравнению с традиционной трансплантацией малоберцовой ткани. Голова и шея . 2016; 38: E1783–E1787. doi: 10.1002/hed.24315. [PubMed] [CrossRef] [Академия Google]
42. Дзегилевски П.Т., Млынарек А.М., Харрис Дж.Р. и др. Свободный малоберцовый лоскут с укорочением кости: новый метод увеличения плотности кости для имплантации зубов при костной реконструкции. Голова и шея . 2014;36(11):1648–1653. doi: 10.1002/hed.23510. [PubMed] [CrossRef] [Google Scholar]
Голова и шея . 2014;36(11):1648–1653. doi: 10.1002/hed.23510. [PubMed] [CrossRef] [Google Scholar]
43. Димитриу Р., Джонс Э., МакГонагл Д., Джанноудис П.В. Регенерация кости: современные концепции и направления будущего. Медицина БМС . 2011;9(1):с. 66. дои: 10.1186/1741-7015-9-66. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
44. Yildirim M., Spiekermann H., Handt S., Edelhoff D. Увеличение верхнечелюстной пазухи с помощью ксенотрансплантата bio-oss и аутогенной внутриротовой кости для качественного улучшения места имплантации: гистологическое и гистоморфометрическое клиническое исследование у людей. Международный журнал челюстно-лицевых имплантатов . 2001;16(1):23–33. [PubMed] [Google Scholar]
45. Cordaro L., Bosshardt D.D., Palattella P., Rao W., Serino G., Chiapasco M. Трансплантация верхнечелюстной пазухи с помощью керамики bio-ossor straumannbone: результаты гистоморфометрии из рандомизированного контролируемого мультицентра клиническое испытание. Клинические исследования оральных имплантатов . 2008;19(8):796–803. doi: 10.1111/j.1600-0501.2008.01565.x. [PubMed] [CrossRef] [Google Scholar]
Клинические исследования оральных имплантатов . 2008;19(8):796–803. doi: 10.1111/j.1600-0501.2008.01565.x. [PubMed] [CrossRef] [Google Scholar]
46. Meijndert L., Raghoebar G.M., Schüpbach P., Meijer H.J.A., Vissink A. Качество кости в месте имплантации после реконструкции локального дефекта переднего гребня верхней челюсти с подбородком кости или депротеинизированной губчатой бычьей кости. Международный журнал челюстно-лицевой хирургии . 2005;34(8):877–884. doi: 10.1016/j.ijom.2005.04.017. [PubMed] [CrossRef] [Академия Google]
47. Thuaksuban N., Nuntanaranont T., Pripatnanont P. Сравнение аутогенного костного трансплантата в сочетании с депротеинизированной бычьей костью и аутогенного костного трансплантата для лечения альвеолярной щели. Международный журнал челюстно-лицевой хирургии . 2010;39(12):1175–1180. doi: 10.1016/j.ijom.2010.07.008. [PubMed] [CrossRef] [Google Scholar]
48. Камаджаджа Д.Б., Абидин З.З., Диана Р. и др.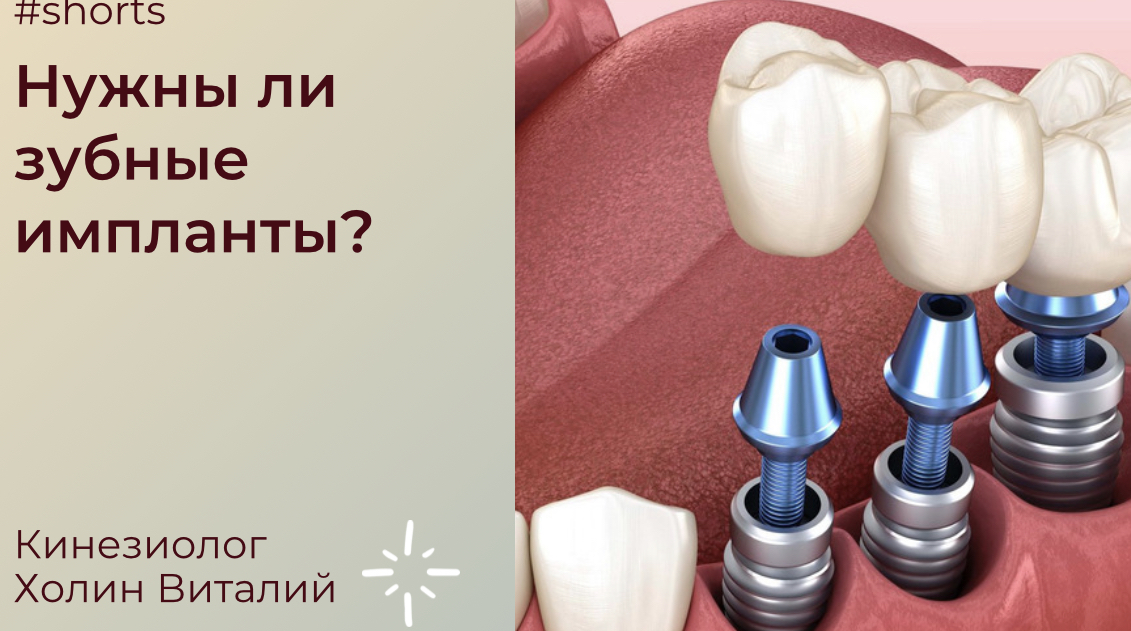 Анализ in vivo остеогенной активности и способности к регенерации кости деминерализованного лиофилизированного ксенотрансплантата бычьей кости: потенциального кандидата в качестве наполнителя альвеолярной кости. Международный стоматологический журнал . 2021;2021:10. doi: 10.1155/2021/1724374.1724374 [Статья PMC free] [PubMed] [CrossRef] [Google Scholar]
Анализ in vivo остеогенной активности и способности к регенерации кости деминерализованного лиофилизированного ксенотрансплантата бычьей кости: потенциального кандидата в качестве наполнителя альвеолярной кости. Международный стоматологический журнал . 2021;2021:10. doi: 10.1155/2021/1724374.1724374 [Статья PMC free] [PubMed] [CrossRef] [Google Scholar]
49. Medikeri R., Meharwade V., Sinha K. Влияние рекомбинантного костного морфогенетического белка-2 по сравнению с другими биоматериалами в лечении внутрикостных дефектов у больных пародонтитом: систематический обзор. Журнал Индийского общества пародонтологии . 2019;23(4):311–315. doi: 10.4103/jisp.jisp_748_18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Шейх З., Джавид М., Хамдан Н., Хашми Р. Регенерация кости с использованием костных морфогенетических белков и различных носителей биоматериалов. Материалы . 2015;8(4):1778–1816. дои: 10.3390/ma8041778. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Ху К., Олсен Б. Р. Роль сосудистого эндотелиального фактора роста в восстановлении и регенерации кости. Кость . 2016;91:30–38. doi: 10.1016/j.bone.2016.06.013. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ху К., Олсен Б. Р. Роль сосудистого эндотелиального фактора роста в восстановлении и регенерации кости. Кость . 2016;91:30–38. doi: 10.1016/j.bone.2016.06.013. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Hu K., Olsen B.R. VEGF, полученный из остеобластов, регулирует дифференцировку остеобластов и формирование кости во время восстановления кости. Журнал клинических исследований . 2016;126(2):509–526. doi: 10.1172/jci82585. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Zhang W., Zhu C., Wu Y., et al. VEGF и BMP-2 способствуют регенерации кости, способствуя самонаведению и дифференцировке стволовых клеток костного мозга. Европейские элементы и материалы . 2014; 27:1–11. [PubMed] [Академия Google]
54. Holloway J.L., Ma H., Rai R., Burdick J.A. Модулирование плотности сшивания и деградации гидрогеля для контроля доставки костного морфогенетического белка и формирования кости in vivo. Журнал контролируемого выпуска .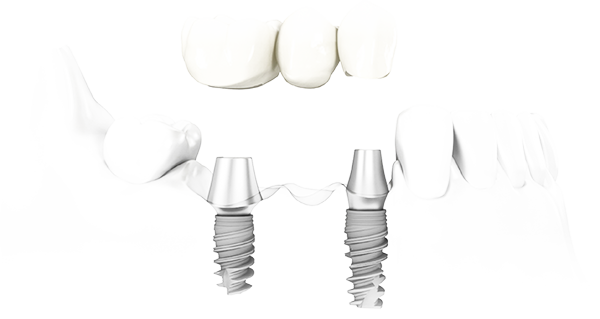 2014; 191:63–70. doi: 10.1016/j.jconrel.2014.05.053. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2014; 191:63–70. doi: 10.1016/j.jconrel.2014.05.053. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
55. Yun Y.-R., Jang J. H., Jeon E., et al. Введение факторов роста для регенерации кости. Регенеративная медицина . 2012;7(3):369–385. doi: 10.2217/rme.12.1. [PubMed] [CrossRef] [Google Scholar]
56. Chang P.-C., Dovban A.S., Lim L.P., Chong L.Y., Kuo M.Y., Wang C.-H. Двойная доставка PDGF и симвастатина для ускорения регенерации пародонта in vivo. Биоматериалы . 2013;34(38):9990–9997. doi: 10.1016/j.biomaterials.2013.09.030. [PubMed] [CrossRef] [Google Scholar]
57. Kasten P., Beyen I., Bormann D., Luginbühl R., Plöger F., Richter W. Влияние двух точечных мутаций в GDF-5 на эктопическую кость формирование в β — каркас из трикальцийфосфата. Биоматериалы . 2010;31(14):3878–3884. doi: 10.1016/j.biomaterials.2010.01.109. [PubMed] [CrossRef] [Google Scholar]
58. Kleinschmidt K., Ploeger F., Nickel J. , Glockenmeier J., Kunz P., Richter W. Улучшенная реконструкция архитектуры длинных костей с помощью мутанта фактора роста, сочетающего положительные особенности ГДФ-5 и БМП-2. Биоматериалы . 2013;34(24):5926–5936. doi: 10.1016/j.biomaterials.2013.04.029. [PubMed] [CrossRef] [Академия Google]
, Glockenmeier J., Kunz P., Richter W. Улучшенная реконструкция архитектуры длинных костей с помощью мутанта фактора роста, сочетающего положительные особенности ГДФ-5 и БМП-2. Биоматериалы . 2013;34(24):5926–5936. doi: 10.1016/j.biomaterials.2013.04.029. [PubMed] [CrossRef] [Академия Google]
59. Wegman F., Bijenhof A., Schuijff L., Oner F.C., Dhert W.J., Alblas J. Остеогенная дифференцировка в результате генной терапии на основе плазмидной ДНК BMP-2 in vitro и in vivo. Европейские элементы и материалы . 2011;21:230–242. [PubMed] [Google Scholar]
60. Evans C. H. Доставка генов в кости. Расширенные обзоры доставки лекарств . 2012;64(12):1331–1340. doi: 10.1016/j.addr.2012.03.013. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
61. Каплан А. И. Мезенхимальные стволовые клетки и генная терапия. Клиническая ортопедия и родственные исследования . 2000;379:S67–S70. doi: 10.1097/00003086-200010001-00010. [PubMed] [CrossRef] [Google Scholar]
62. Chow L.K., Cheung L.K. Полезность стереомоделей в челюстно-лицевой хирургии. Журнал челюстно-лицевой хирургии . 2007;65(11):2260–2268. doi: 10.1016/j.joms.2006.11.041. [PubMed] [CrossRef] [Google Scholar]
Chow L.K., Cheung L.K. Полезность стереомоделей в челюстно-лицевой хирургии. Журнал челюстно-лицевой хирургии . 2007;65(11):2260–2268. doi: 10.1016/j.joms.2006.11.041. [PubMed] [CrossRef] [Google Scholar]
63. Фам А. М., Рафии А. А., Мецгер М. С., Джамали А., Стронг Б. Э. Компьютерное моделирование и интраоперационная навигация в челюстно-лицевой хирургии. Отоларингология-Хирургия головы и шеи . 2007;137(4):624–631. doi: 10.1016/j.otohns.2007.06.719. [PubMed] [CrossRef] [Google Scholar]
64. Буту М., Родино С., Пентеа М., Адина Н., Петраче П., Бутнариу М. ИК-спектроскопия муки из костей европейского зайца. Дайджест журнала Nanomater Biostructures . 2014;9(4):1317–1322. [Google Scholar]
65. Бутнариу М., Негреа П., Лупа Л. и др. Очистка от загрязнителей редкоземельными элементами сорбционным процессом с использованием органических природных сорбентов. Международный журнал экологических исследований и общественного здравоохранения . 2015;12(9):11278–11287. doi: 10.3390/ijerph220911278. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2015;12(9):11278–11287. doi: 10.3390/ijerph220911278. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
66. Reda R., Zanza A., Cicconetti A., et al. Ультразвуковая визуализация в стоматологии: обзор литературы. Журнал обработки изображений . 2021;7(11):с. 238. doi: 10.3390/jimaging7110238. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Schlee M., Rothamel D. Аугментация гребня с использованием индивидуальных аллогенных костных блоков. Имплантационная стоматология . 2013;22(3):212–218. doi: 10.1097/id.0b013e3182885fa1. [PubMed] [CrossRef] [Google Scholar]
68. Касап Н., Ластер З., Лавив А. и др. Рекомбинантный человеческий костный морфогенетический белок-2, заключенный в неперфорированную титановую оболочку над высокопрофильными зубными имплантатами в большеберцовой кости кролика: пилотное исследование увеличения кости. Международный журнал челюстно-лицевых имплантатов . 2013;28(6):e349–e356. doi: 10.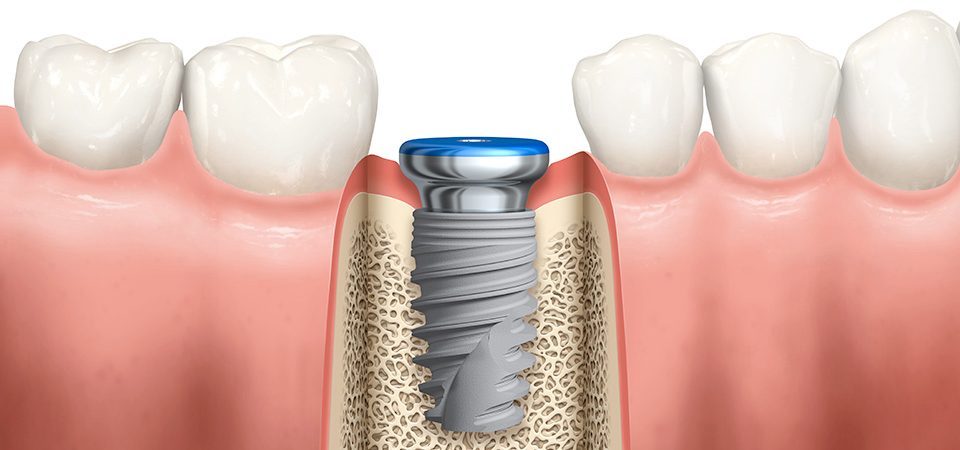 11607/jomi.te15. [PubMed] [CrossRef] [Академия Google]
11607/jomi.te15. [PubMed] [CrossRef] [Академия Google]
Имплантаты — костная пластика для зубных имплантатов
Услуги > Имплантаты > Зубные имплантаты
Зубные имплантаты становятся общепринятым методом замены отсутствующих зубов. Во многих случаях они могут быть предпочтительнее альтернативы мостовидному протезу или частичному протезу. Однако установка зубных имплантатов требует тщательной оценки и рассмотрения, особенно в отношении кости, в которую устанавливается имплантат.
Зачем беспокоиться о костях?Зубной имплантат представляет собой металлический штифт, вставляемый в челюстную кость и используемый в качестве фиксатора, поверх которого устанавливается коронка (зуб). При установке имплантата необходимо обеспечить его полную стабильность ( остеоинтеграция ) в кости, чтобы он был достаточно прочным, чтобы поддерживать зуб на нем. Необходимо уделять большое внимание тому, чтобы вокруг имплантата было достаточно кости, поскольку это обеспечивает прочность и стабильность зубного имплантата. Таким образом, основной задачей при установке зубного имплантата является обеспечение достаточного объема кости вокруг него по высоте, ширине и глубине. |
| Сколько кости необходимо вокруг зубного имплантата? Как правило, вокруг зубного имплантата требуется костная ткань толщиной не менее 1 мм. Когда имплантат находится рядом с зубом или другим имплантатом, требуется больше места. Если кости недостаточно, чтобы полностью покрыть имплантат, потребуется костный трансплантат. |
При оценке высоты кости просто должно быть достаточно кости, чтобы имплантат был полностью погружен. Однако важно следить за тем, чтобы имплантат не проникал так глубоко, чтобы задевать другие анатомические структуры (например, нерв в нижней челюсти или пазуху в верхней челюсти). При установке имплантатов на верхнюю челюсть может не хватить места по вертикали, и для восстановления кости может потребоваться синус-лифтинг .
Типы костных трансплантатов
Костный трансплантат представляет собой добавление кости или костноподобного материала с целью увеличения объема кости в челюсти. Как правило, кость размещается и заживает до того, как можно будет установить имплантат. Период заживления может варьироваться в зависимости от типа используемой кости.
Существует много типов костных трансплантатов, но все они относятся к одной из нескольких категорий:
Аутотрансплантат – кость, взятая из собственного тела пациента.
Allograft – bone from a genetically similar organism
Xenograft – bone from a genetically dissimilar organism
Synthetic – a synthetic biocompatible material
The type of bone graft that будет выбрано будет зависеть от ситуации и от количества требуемой кости.
Сроки установки костных трансплантатов
В зависимости от ситуации костные трансплантаты могут быть размещены одновременно с имплантатом или до него.


