Герпетический стоматит — симптомы, причины, течение заболевания.
Герпетический стоматит – инфекционное заболевание, вызванное вирусом герпеса. Оно составляет 80 % всех видов стоматитов и возникает в основном у детей до 3 лет, очень редко – у подростков и взрослых.
Симптомы
Клиническую картину сопровождает ярко выраженная симптоматика:
Острая форма герпетического стоматита сопровождается сильной болью и жжением в местах локализации язв, которые образуются на месте лопнувших волдырей и напоминают афты (язвочки с экссудатом, окруженные покрасневшим ободком на слизистой). Поэтому герпетический стоматит называют ещё афтозным.
Причины возникновения герпетического стоматита
Источник заболевания – вирус герпеса. Он попадает в организм человека при контакте с зараженным, бытовым путем (через предметы быта) или вертикальным (от матери к ребенку в период беременности или родов). Далее вирус разносится с кровотоком по всему организму и встраивается в геном нейронов. С этого момента он сопровождает человека до конца жизни и проявляется на фоне сниженного иммунитета.
Далее вирус разносится с кровотоком по всему организму и встраивается в геном нейронов. С этого момента он сопровождает человека до конца жизни и проявляется на фоне сниженного иммунитета.
Однако существуют факторы риска заболевания:
-
травмы слизистой рта;
-
плохая гигиена полости рта;
-
заболевания десен;
-
стрессы;
-
неполноценное питание.
Течение заболевания
Инкубационный период герпетического стоматита – до 26 дней, но чаще его признаки появляются уже на 5-7-й день. Срок инкубации не отражается на тяжести заболевания.
Симптомы появляются мгновенно: слизистая рта отекает, краснеет, покрывается язвами, повышается температура тела, слюноотделение не контролируется, увеличиваются лимфоузлы под челюстью, ухудшается общее состояние.
Так протекает острая форма герпетического стоматита. При своевременном лечении выздоровление наступает через одну-три недели, этот срок зависит от статуса иммунитета организма.
Невылеченная острая форма переходит в хроническую, когда оставшиеся очаги инфекции повторяются так часто, что язвы не успевают заживать и поражают обширную поверхность слизистой рта. Патологию может сопровождать кровоточивость десен, подвижность и выпадение зубов, ларингит.
Герпетический стоматит может протекать в легкой, средней и тяжелой форме.
Симптомы легкой формы:
-
отечность и болезненность слизистой рта;
-
-
небольшое повышение температуры.
Симптомы средней формы:
-
язвы покрывают всю слизистую рта, затрудняя прием пищи;
-
движение языка вызывает боль и сильный дискомфорт;
-
слюноотделение не контролируется;
-
температура тела повышается до 39 градусов;
-
появляется сильная головная боль;
-
тонус организма снижается.

Симптомы тяжелой формы:
Необходимость обращения к врачу
Если игнорировать симптомы герпетического стоматита и не обращаться к врачу, инфекция проникнет в кровь и разнесется по всему организму. А в период исчезновения видимых признаков болезни нередко возникают осложнения.
Не занимайтесь самолечением: оно будет неполноценным или ошибочным; адекватную терапию может назначить только врач.
Лечение герпесного (герпетического/вирусного) стоматита в Одинцово
Герпесный (герпетический) стоматит проявляется на пике падения иммунитета, а также после контактов с уже болеющими людьми. Его возбудитель – простой вирус герпеса: тип HSV-1 у детей, HSV-1 и HSV-2 у взрослых. Наиболее часто диагноз «герпесный стоматит» ставят малышам в возрасте 9-28 месяцев и подросткам. Взрослые болеют редко, но в более тяжелой форме.
Причины и симптомы герпетического стоматита
Причины появление герпесного стоматита зависят от возраста пациента. У совсем маленьких детей заболеванию способствует исчезновение антител, полученных от матери. Собственные антитела у малыша еще не появились, что делает ребенка особенно уязвимым к вирусу. У детей старше 3-х лет, подростков и взрослых развитие вирусного стоматита провоцирует:
У совсем маленьких детей заболеванию способствует исчезновение антител, полученных от матери. Собственные антитела у малыша еще не появились, что делает ребенка особенно уязвимым к вирусу. У детей старше 3-х лет, подростков и взрослых развитие вирусного стоматита провоцирует:
- контакт с больным взрослым или ребенком;
- снижение общего или местного иммунитета;
- травмы слизистой полости рта;
- сильный стресс и нервное напряжение;
- использование чужих средств гигиены;
- хронические ЛОР-болезни;
- заболевания эндокринной системы, ЖКТ;
- гормональные сбои.
Видимая стадия стоматита – герпетические пузырьки на слизистой десен, щек, языка. Ей предшествует общее недомогание: повышение температуры, снижение аппетита, головная боль, ухудшение настроения, зуд и покалывание в месте будущих пузырьков.
Осмотр пациента показывает:
- многочисленные пузырьки от 1 мм – на слизистой и в горле;
- язвочки от вскрывшихся образований – с зубчатыми границами;
- слившиеся изъявления – при запущенной болезни.
Выявление и лечение герпетического стоматита
Пузырьковая сыпь явственно указывает на природу недуга, но эрозивные участки схожи у разных видов стоматитов. Это основная причина необходимости лабораторных исследований – определении вируса на соскобе со слизистой.
Для лечения герпесного (вирусного) стоматита стоматолог разрабатывает алгоритм под конкретного пациента, в который включены обязательные препараты:
- противовирусные;
- жаропонижающие;
- антисептические;
- обезболивающие;
-
заживляющие.
Также врач рекомендует соблюдение постельного режима, обильное питье для исключения интоксикации, соблюдение правил личной гигиены. Одновременно с лечением стоматолог назначает терапию для восстановления микрофлоры полости рта – физиопроцедуры, витамины.
Важно не только вылечить заболевание, но и исключит рецидивы в дальнейшем. Частые случаи герпетического стоматита провоцируют развитие хронической формы с обострениями при простуде и ОРВИ.
Общие вопросы о герпетическом гингивостоматите
Опубликовано 10 марта 2022 г. доктором Ист Уорник DDS
По мере того, как наши дети растут, мы сталкиваемся со всевозможными заболеваниями, травмами и инфекциями, о существовании которых мы никогда не знали, некоторые из них имеют сложные названия, такие как герпетический гингивостоматит. , инфекция полости рта, которая встречается в основном у маленьких детей и связана с вирусом простого герпеса.
Однако, несмотря на свое длинное название, герпетический гингивостоматит не является сложным заболеванием, но с ним должны быть знакомы родители маленьких детей.
Что это?
Герпетический гингивостоматит (ГГ) представляет собой заразную инфекцию полости рта, которая обычно отмечается при первом контакте ребенка с вирусом простого герпеса. Риск заражения (HG) может быть увеличен из-за плохой гигиены полости рта, например, недостаточной или эффективной чистки зубов. HG — очень неприятная инфекция, особенно для малышей, так как она вызывает появление волдырей, как правило, на языке, губах, деснах, щеках и нёбе. После того, как волдыри лопнут, могут образоваться столь же болезненные язвы. У детей также может быть высокая температура, которая обычно возникает до появления волдырей.
Как это повлияет на моего ребенка?
Герпетический гингивостоматит причиняет боль малышам и может привести в бешенство родителей. Одним из основных побочных эффектов инфекции является то, что детям очень неудобно есть и пить. Поэтому пострадавшие становятся очень раздражительными, потому что они голодны, а также могут обезвоживаться из-за нехватки жидкости. Вы также можете заметить отек вокруг рта и чрезмерное слюнотечение.
Вы также можете заметить отек вокруг рта и чрезмерное слюнотечение.
Как лечить?
Не существует лекарства от герпетического гингивостоматита или волшебного зелья, чтобы избавиться от него. В большинстве случаев родители могут предпринять шаги для устранения симптомов инфекции и, возможно, немного ускорить выздоровление. Ребенку могут быть назначены противовирусные препараты, такие как ацикловир, который хорошо зарекомендовал себя в лечении вирусов, связанных с простым герпесом. Для облегчения боли могут быть предложены полоскания рта и анальгетики, чтобы дети могли оставаться должным образом обезвоженными, пока они поражены инфекцией.
Если ребенок может есть и пить, лучше избегать горячей, острой или соленой пищи и напитков, поскольку они усугубляют состояние. Хотя это может быть болезненно, чистка зубов должна продолжаться, чтобы избавиться от бактерий во рту, ускорить выздоровление и предотвратить повторное заражение.
Могу ли я заразиться герпетическим гингивостоматитом?
Герпетический гингивостоматит заразен, и дети легко передают его друг другу, если они склонны делиться друг с другом едой, напитками и посудой.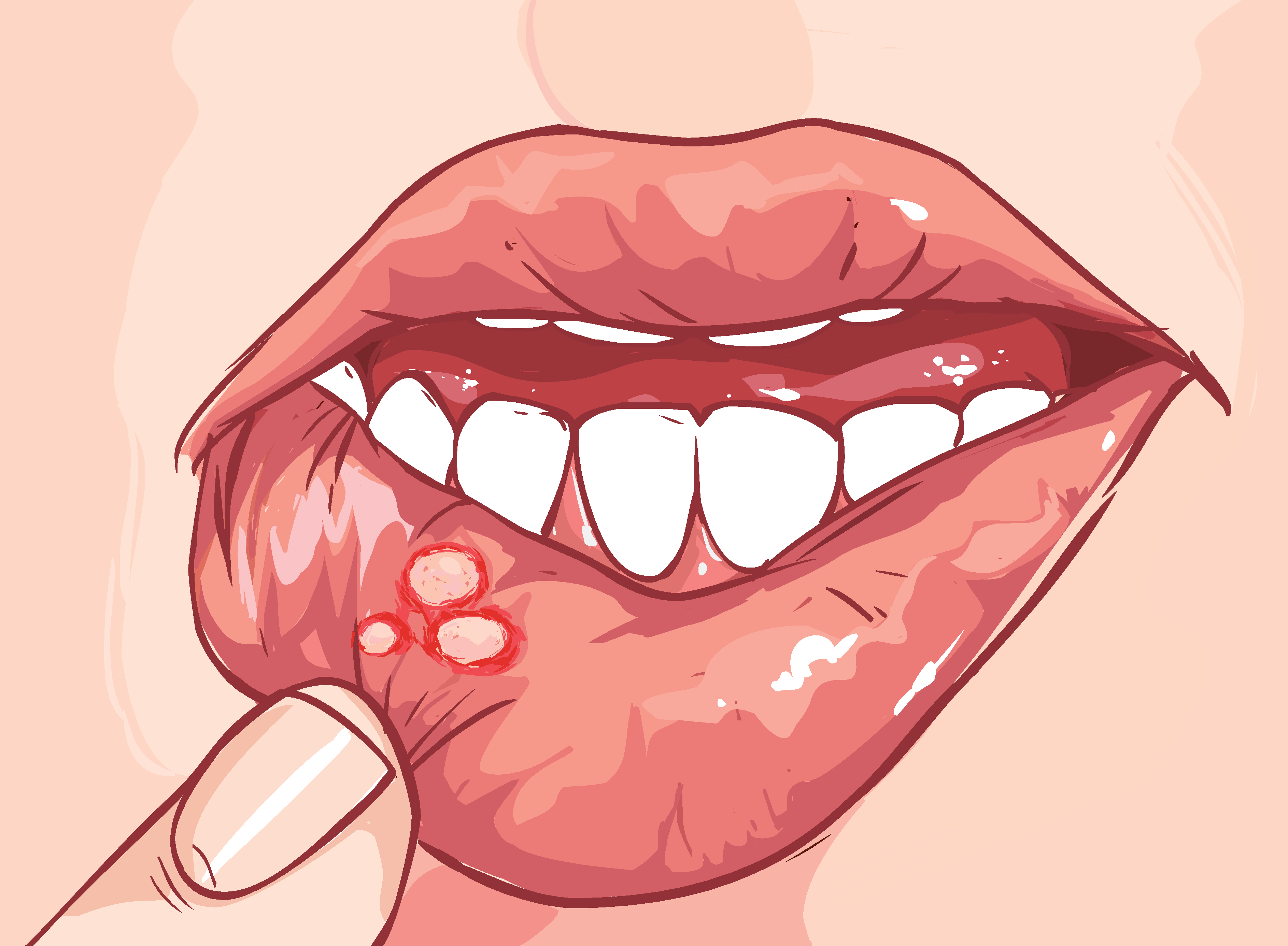 Поцелуи также могут способствовать распространению инфекции. Поскольку маленькие дети часто тянут игрушки в рот, совместное использование этих игрушек также должно быть запрещено во время любой вспышки.
Поцелуи также могут способствовать распространению инфекции. Поскольку маленькие дети часто тянут игрушки в рот, совместное использование этих игрушек также должно быть запрещено во время любой вспышки.
В большинстве случаев герпетический гингивостоматит проходит примерно через 2 недели, но, к сожалению, как только у ребенка развивается эта инфекция, он также становится более склонным к развитию рецидивирующих язв и язв во рту. На самом деле, исследования Американской академии педиатрии показывают, что около 40% детей, перенесших HG, будут страдать от язв и болячек в течение жизни, в том числе во взрослом возрасте.
Лучший способ избежать развития этой инфекции — внимательно следить за здоровьем зубов вашего маленького ребенка. Помогите им регулярно чистить зубы, пока они не смогут делать это без присмотра, и водите их к стоматологу для регулярных осмотров и чистки. Если ваш старший ребенок носит ретейнер, убедитесь, что он
регулярно чистится, как и любой стоматологический прибор, который регулярно вводится и вынимается из полости рта.
Если у вас есть другие вопросы о герпетическом гингивостоматите, позвоните нам по телефону (907) 562-1003, чтобы назначить встречу с одним из наших сертифицированных детских стоматологов.
Поиск
Советы по уходу за полостью рта
- Почему изо рта моего ребенка так неприятно пахнет?
- Почему у моего ребенка кровоточат десны при чистке зубов?
- Что вызывает кариес?
- Герпетический гингивостоматит
- Герметики для здоровых зубов вашего ребенка
Развитие стоматита, вызванного вирусом простого герпеса, во время лечения цидофовиром | Клинические инфекционные заболевания
Журнальная статья
Кристофер С. Дворжак,
Кристофер С. Дворжак
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Мортон Дж. Коуэн,
Коуэн,
Мортон Дж. Коуэн
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Биляна Хорн,
Биляна Хорн
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Пегги С. Вайнтруб
Пегги С. Вайнтруб
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Клинические инфекционные заболевания , том 49, выпуск 8, 15 октября 2009 г., страницы e92–e95, https://doi.org/10.1086/605678
Опубликовано:
15 октября 2009 г. 3
3 История статьиПолучен:
09 апреля 2009 г.
Принято:
04 июня 2009 г.
Принято:
17 сентября 2009
Опубликовано:
15 октября 2009 г.
Фильтр поиска панели навигации Клинические инфекционные заболеванияЭтот выпускIDSA JournalsInfectious DiseasesBooksJournalsOxford Academic Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Клинические инфекционные заболеванияЭтот выпускIDSA JournalsInfectious DiseasesBooksJournalsOxford Academic Термин поиска на микросайте
Advanced Search
Abstract
Мы сообщаем о 3 детях, у которых после трансплантации гемопоэтических стволовых клеток развился стоматит, вызванный вирусом простого герпеса (ВПГ), при еженедельном приеме цидофовира в качестве профилактического лечения цитомегаловирусной инфекции. Все пациенты хорошо ответили на лечение ацикловиром или ганцикловиром. Несмотря на чувствительность ВПГ к цидофовиру in vitro, лечение этим препаратом один раз в неделю может быть недостаточной профилактикой у детей.
Все пациенты хорошо ответили на лечение ацикловиром или ганцикловиром. Несмотря на чувствительность ВПГ к цидофовиру in vitro, лечение этим препаратом один раз в неделю может быть недостаточной профилактикой у детей.
Использование цидофовира, противовирусного агента, аналога нуклеотида, увеличивается у детей, перенесших трансплантацию гемопоэтических стволовых клеток (ТГСК) для лечения инфекций, вызванных цитомегаловирусом (ЦМВ) [1], аденовирусом [2–7] и вирусом ВК [8, 9]. Существуют две разные стратегии дозирования: 5 мг/кг один раз в неделю [1–3, 7, 8, 10, 11] и 1 мг/кг 3 раза в неделю [4–6, 9]. Цидофовир также может быть использован для лечения инфекции, вызванной устойчивым к ацикловиру вирусом простого герпеса типа 1 (ВПГ-1) [8, 10, 11]. Однако в настоящее время мы сообщаем о 3 детях, у которых развился стоматит, вызванный ВПГ-1, при еженедельном приеме цидофовира для лечения реактивации ЦМВ-инфекции.
Пациент 1. 11-летнему HSV-1-серопозитивному мальчику была проведена трансплантация 8/8 HLA-совместимого аллогенного костного мозга от неродственного донора для лечения острого лимфобластного лейкоза в третьей полной ремиссии. Его режим кондиционирования состоял из 1350 сГр общего облучения тела, циклофосфамида и лошадиного антитимоцитарного глобулина. Перед трансплантацией и пациент, и его донор были отмечены как серопозитивные по ЦМВ. Через месяц после трансплантации у него развилась виремия ЦМВ (1500 копий/мл), которую превентивно лечили ганцикловиром (5 мг/кг два раза в день в течение 3 недель, затем один раз в день в течение 12 недель). Через четыре месяца после трансплантации у него развилась острая, а затем прогрессирующая обширная хроническая болезнь кожи «трансплантат против хозяина» (РТПХ). Его хроническую РТПХ лечили преднизоном перорально (1 мг/кг, чередуя с 0,65 мг/кг через день), мофетилом микофенолата (15 мг/кг перорально два раза в день; последний уровень микофеноловой кислоты 1,7 мкг/мл) и топические кортикостероиды. На фоне иммуносупрессии для лечения хронической РТПХ он получал профилактически перорально ацикловир (400 мг/м 2 два раза в день).
Его режим кондиционирования состоял из 1350 сГр общего облучения тела, циклофосфамида и лошадиного антитимоцитарного глобулина. Перед трансплантацией и пациент, и его донор были отмечены как серопозитивные по ЦМВ. Через месяц после трансплантации у него развилась виремия ЦМВ (1500 копий/мл), которую превентивно лечили ганцикловиром (5 мг/кг два раза в день в течение 3 недель, затем один раз в день в течение 12 недель). Через четыре месяца после трансплантации у него развилась острая, а затем прогрессирующая обширная хроническая болезнь кожи «трансплантат против хозяина» (РТПХ). Его хроническую РТПХ лечили преднизоном перорально (1 мг/кг, чередуя с 0,65 мг/кг через день), мофетилом микофенолата (15 мг/кг перорально два раза в день; последний уровень микофеноловой кислоты 1,7 мкг/мл) и топические кортикостероиды. На фоне иммуносупрессии для лечения хронической РТПХ он получал профилактически перорально ацикловир (400 мг/м 2 два раза в день).
Через двенадцать с половиной месяцев после ТГСК полимеразная цепная реакция (ПЦР) выявила нагрузку ЦМВ 1240 копий/мл. Поскольку у пациента в анамнезе была умеренная панцитопения, вторичная по отношению либо к РТПХ, либо к лекарствам, и во избежание дополнительной миелосупрессии, связанной с терапией ганцикловиром, был начат цидофовир (5 мг/кг один раз в неделю, вводимый с пробенецидом), а профилактический прием ацикловира был прекращен (рис. 1А). ). Четырнадцать дней спустя (13 месяцев после ТГСК) у него появились 3-дневные язвы во рту. В культуре одного из поражений полости рта вырос ВПГ-1. Пероральный ацикловир (400 мг/м 2 три раза в день) был возобновлен, и поражения полости рта исчезли в течение 3 дней. Он получал одновременно ацикловир и цидофовир в течение 3 недель без повышения уровня креатинина в сыворотке. К этому времени он стал отрицательным на ЦМВ с помощью ПЦР, поэтому цидофовир был прекращен, а доза ацикловира была снижена до двух раз в день. На момент написания прошло 26 месяцев после ТГСК, и его хроническая РТПХ медленно улучшалась.
Поскольку у пациента в анамнезе была умеренная панцитопения, вторичная по отношению либо к РТПХ, либо к лекарствам, и во избежание дополнительной миелосупрессии, связанной с терапией ганцикловиром, был начат цидофовир (5 мг/кг один раз в неделю, вводимый с пробенецидом), а профилактический прием ацикловира был прекращен (рис. 1А). ). Четырнадцать дней спустя (13 месяцев после ТГСК) у него появились 3-дневные язвы во рту. В культуре одного из поражений полости рта вырос ВПГ-1. Пероральный ацикловир (400 мг/м 2 три раза в день) был возобновлен, и поражения полости рта исчезли в течение 3 дней. Он получал одновременно ацикловир и цидофовир в течение 3 недель без повышения уровня креатинина в сыворотке. К этому времени он стал отрицательным на ЦМВ с помощью ПЦР, поэтому цидофовир был прекращен, а доза ацикловира была снижена до двух раз в день. На момент написания прошло 26 месяцев после ТГСК, и его хроническая РТПХ медленно улучшалась.
Рисунок 1
Открыть в новой вкладкеСкачать слайд
Сроки применения противовирусных препаратов у 3 детей, реципиентов трансплантации гемопоэтических стволовых клеток, в связи с реактивацией цитомегаловирусной (ЦМВ) инфекции и развитием стоматита. Обратите внимание на разницу в шкале между панелями A (месяцы) и B (недели). ACV, ацикловир; CDV, цидофовир; ФОС, фоскарнет; ГЦВ, ганцикловир; ПЦР, полимеразная цепная реакция.
Обратите внимание на разницу в шкале между панелями A (месяцы) и B (недели). ACV, ацикловир; CDV, цидофовир; ФОС, фоскарнет; ГЦВ, ганцикловир; ПЦР, полимеразная цепная реакция.
Пациент 2. 7-летнему HSV-1-серопозитивному мальчику была проведена трансплантация 7/8 HLA-совместимого аллогенного костного мозга от неродственного донора для лечения гиподиплоидного острого лимфобластного лейкоза во второй полной ремиссии. Его режим кондиционирования был идентичен таковому у пациента 1. Его профилактика острой РТПХ состояла из циклоспорина и метотрексата. У него 2 раза был тяжелый ВПГ-стоматит после консолидирующей химиотерапии, по поводу которой он дважды получил 7-дневный курс ацикловира (10 мг/кг/доза 3 раза в день). Перед трансплантацией и пациент, и его донор были отмечены как серопозитивные по ЦМВ. На 5-е сутки после ТГСК методом ПЦР выявлена ЦМВ-нагрузка 200 копий/мл. Повторная ПЦР показала 400 копий/мл на 7-й день и 1200 копий/мл на 10-й день. апластическую фазу после ТГСК, цидофовир (5 мг/кг один раз в неделю, вводимый с пробенецидом) был начат на 12-й день, а профилактический прием ацикловира был прекращен. Количество его копий CMV продолжало расти, достигнув пика в 23,9.00 копий/мл на 17-й день.
Количество его копий CMV продолжало расти, достигнув пика в 23,9.00 копий/мл на 17-й день.
Через девятнадцать дней после ТГСК у него появились поражения на губах. В культуре одного из поражений полости рта вырос ВПГ-1. Минимальная ингибирующая концентрация (МИК) для ацикловира составила 1,6 мкг/мл (чувствительный), а МИК для фоскарнета — 50 мкг/мл (чувствительный) (Focus Technologies). К 22 дню у него были признаки приживления нейтрофилов, поэтому прием цидофовира был прекращен и начато введение ганцикловира (5 мг/кг внутривенно два раза в день) (рис. 1В). Поражения в ротовой полости быстро разрешились, и к 46 дню ПЦР перестала обнаруживать как ЦМВ, так и HHV-6. В течение этого времени пациенту требовалась терапия гранулоцитарным колониестимулирующим фактором два раза в неделю для поддержания абсолютного числа нейтрофилов >1×. 10 9 кл/л. Терапия ганцикловиром была снижена до одного раза в день в течение дополнительных 4 недель, а профилактическая терапия ацикловиром была возобновлена. На момент написания статьи прошло 9 месяцев после ТГСК, и пациент чувствовал себя хорошо.
На момент написания статьи прошло 9 месяцев после ТГСК, и пациент чувствовал себя хорошо.
Пациент 3. 3-летнему HSV-1-серопозитивному мальчику была проведена трансплантация 5/8 HLA-совместимых гаплосовместимых Т-клеточно-обедненных стволовых клеток периферической крови от его матери для лечения ювенильного миеломоноцитарного лейкоза. Его режим кондиционирования состоял из 1200 сГр общего облучения тела, флударабина, тиотепы и кроличьего лошадиного антитимоцитарного глобулина. Перед трансплантацией и пациент, и его донор были отмечены как серопозитивные по ЦМВ. Его рутинная противовирусная профилактика после трансплантации состояла из внутривенного введения фоскарнета (60 мг/кг два раза в день) с 1 по 21 день с последующим пероральным приемом ацикловира (500 мг/м 9 ).0202 2 три раза в день). На 27-й день после трансплантации ПЦР выявила ЦМВ-нагрузку 600 копий/мл. Повторная ПЦР показала 1000 копий CMV/мл на 35-й день. Ацикловир был прекращен на 29-й день, и он начал лечение ганцикловиром внутривенно (5 мг/кг два раза в день) в течение 4 дней; однако это было остановлено из-за снижения абсолютного количества нейтрофилов. Лечение цидофовиром (5 мг/кг один раз в неделю с пробенецидом) начали на 33-й день (рис. 1В).
Лечение цидофовиром (5 мг/кг один раз в неделю с пробенецидом) начали на 33-й день (рис. 1В).
Через 48 дней после ТГСК у него появились 4-дневные язвы во рту. В культуре одного из поражений полости рта вырос ВПГ-1. Пероральный ацикловир (500 мг/м 2 три раза в день) был возобновлен, и поражения полости рта быстро разрешились. Он получал одновременно ацикловир и цидофовир в течение 6 недель, с исчезновением виремии ЦМВ и без повышения уровня креатинина в сыворотке. На момент написания прошло 6 месяцев после ТГСК, и он получал дополнительную химиотерапию и иммунотерапию для лечения прогрессирования ювенильного миеломоноцитарного лейкоза.
Обсуждение. Из-за отсутствия значительной миелосупрессии цидофовир является привлекательным средством против ЦМВ для использования у детей, реципиентов ТГСК, которые не переносят ганцикловир. Кроме того, это единственный известный агент с активностью in vitro против аденовирусных инфекций. Из-за in vitro чувствительности ВПГ к цидофовиру, а также перекрывающейся нефротоксичности, клиницисты, начинающие терапию цидофовиром, могут отказаться от профилактики ацикловиром, ожидая, что цидофовир также будет служить для предотвращения реактивации инфекции ВПГ. Тем не менее, мы наблюдали 3 детей, у которых развился стоматит, подтвержденный культуральным подтверждением ВПГ-1, после прекращения профилактического приема ацикловира и во время приема цидофовира один раз в неделю.
Тем не менее, мы наблюдали 3 детей, у которых развился стоматит, подтвержденный культуральным подтверждением ВПГ-1, после прекращения профилактического приема ацикловира и во время приема цидофовира один раз в неделю.
Одним из возможных объяснений этого вывода может быть то, что у всех 3 пациентов были устойчивые к цидофовиру штаммы ВПГ; однако это кажется маловероятным, поскольку на момент развития стоматита они получали терапию цидофовиром всего 7–12 дней. Все 3 пациента ранее получали ацикловир и/или ганцикловир. Механизмом резистентности к этим агентам обычно являются мутации вирусной тимидинкиназы, тогда как резистентность ВПГ к цидофовиру, по-видимому, опосредована мутациями вирусной ДНК-полимеразы, поэтому перекрестная резистентность встречается редко [12, 13]. Однако пациент 3 получал в течение 21 дня фоскарнет, резистентность к которому опосредована мутациями в ДНК-полимеразе, что делает его потенциальным механизмом развития инфекции ВПГ-1 у этого пациента во время приема цидофовира. К сожалению, тестирование чувствительности к цидофовиру образцов ВПГ-1, полученных от наших пациентов, не проводилось, поскольку изоляты больше не были доступны. Wyles и коллеги [13] сообщили о 3 взрослых, у которых после химиотерапии или ТГСК развилась резистентная к цидофовиру ВПГ-инфекция. 50% ингибирующая концентрация цидофовира была повышена у всех 3 пациентов, а резистентность к ацикловиру (как in vitro, так и in vivo) также была отмечена у 2 пациентов [13]. Подобно всем трем нашим пациентам, третий пациент хорошо ответил на ацикловир [13].
К сожалению, тестирование чувствительности к цидофовиру образцов ВПГ-1, полученных от наших пациентов, не проводилось, поскольку изоляты больше не были доступны. Wyles и коллеги [13] сообщили о 3 взрослых, у которых после химиотерапии или ТГСК развилась резистентная к цидофовиру ВПГ-инфекция. 50% ингибирующая концентрация цидофовира была повышена у всех 3 пациентов, а резистентность к ацикловиру (как in vitro, так и in vivo) также была отмечена у 2 пациентов [13]. Подобно всем трем нашим пациентам, третий пациент хорошо ответил на ацикловир [13].
С другой стороны, возможно, что фармакокинетика терапии цидофовиром один раз в неделю у детей недостаточна для предотвращения реактивации ВПГ-инфекции. Насколько нам известно, исследования фармакокинетики цидофовира у детей не проводились, и используемые в настоящее время режимы дозирования основаны на исследованиях взрослых. Следует отметить, что в одной группе наблюдался случай бессимптомной инфекции ВПГ через 2 недели после начала курса цидофовира (1 мг/кг 3 раза в неделю) для лечения аденовирусной инфекции. В отличие от наших 3 пациентов, этот пациент не лечился, и у него никогда не появлялись признаки заболевания ВПГ [5]. Однако другая группа сообщила, что у 2 из 16 пациентов, получавших цидофовир 3 раза в неделю, развился ВПГ-стоматит [6]. Напротив, Legrand et al [7] сообщили, что у 1 из 7 пациентов, получавших лечение цидофовиром один раз в неделю, развились оральные некротические поражения HSV. Тем не менее, другие группы, использующие цидофовир один раз в неделю у детей, не прокомментировали проблемы с реактивацией инфекции ВПГ [1-3], хотя одна группа специально сообщила о возобновлении профилактического приема ацикловира через 4 дня после инфузий цидофовира [3]. Это может отражать разницу в подавлении ВПГ между режимами дозирования один раз в неделю и три раза в неделю. Интересно, что трое детей, инфицированных ацикловир- и/или фоскарнет-резистентным ВПГ-1, успешно лечились цидофовиром один раз в неделю [8, 10, 11]. Поэтому точный механизм развития ВПГ-1 стоматита у наших пациентов на фоне приема цидофовира неясен.
В отличие от наших 3 пациентов, этот пациент не лечился, и у него никогда не появлялись признаки заболевания ВПГ [5]. Однако другая группа сообщила, что у 2 из 16 пациентов, получавших цидофовир 3 раза в неделю, развился ВПГ-стоматит [6]. Напротив, Legrand et al [7] сообщили, что у 1 из 7 пациентов, получавших лечение цидофовиром один раз в неделю, развились оральные некротические поражения HSV. Тем не менее, другие группы, использующие цидофовир один раз в неделю у детей, не прокомментировали проблемы с реактивацией инфекции ВПГ [1-3], хотя одна группа специально сообщила о возобновлении профилактического приема ацикловира через 4 дня после инфузий цидофовира [3]. Это может отражать разницу в подавлении ВПГ между режимами дозирования один раз в неделю и три раза в неделю. Интересно, что трое детей, инфицированных ацикловир- и/или фоскарнет-резистентным ВПГ-1, успешно лечились цидофовиром один раз в неделю [8, 10, 11]. Поэтому точный механизм развития ВПГ-1 стоматита у наших пациентов на фоне приема цидофовира неясен. Будущие педиатрические испытания цидофовира, как мы надеемся, прояснят его фармакокинетику у детей и определят оптимальную стратегию дозирования. Следует проводить тщательный мониторинг прорывной инфекции ВПГ-1.
Будущие педиатрические испытания цидофовира, как мы надеемся, прояснят его фармакокинетику у детей и определят оптимальную стратегию дозирования. Следует проводить тщательный мониторинг прорывной инфекции ВПГ-1.
В заключение, клиницисты, использующие цидофовир, должны знать, что режим дозирования один раз в неделю может быть недостаточным для предотвращения реактивации инфекции HSV-1 у педиатрических пациентов. Несмотря на потенциально перекрывающуюся нефротоксичность, следует рассмотреть возможность продолжения профилактического приема ацикловира; по крайней мере, клиницисты должны тщательно следить за симптомами и при необходимости оперативно вмешиваться.
Благодарности
Потенциальный конфликт интересов. Все авторы: конфликтов нет.
Каталожные номера
1
Cesaro
S
,
,
Manzardo
C
, и др.
Цидофовир для реактивации цитомегаловируса у детей после трансплантации гемопоэтических стволовых клеток
34
(стр.
129
—
32
)
2
Юсуф
U
,
,
, и др.
Цидофовир для лечения аденовирусной инфекции у детей с трансплантацией гемопоэтических стволовых клеток
81
(стр.
1398
—
404
)
3 2
Muller
053 ,
Левин
М
,
, и др.
Клиническая и in vitro оценка цидофовира для лечения аденовирусной инфекции у детей, получающих трансплантацию гемопоэтических стволовых клеток
41
(стр.
1812
—
6
)
4
Hoffman
J
,
.0003
,
,
Капур
N
.
Аденовирусные инфекции и проспективное исследование цидофовира при трансплантации гемопоэтических стволовых клеток у детей
7
(стр.
388
—
94
)
5
Anderson
E
,
Guzman -Cottril0003
J
,
Клецель
M
, и др.
Дети, инфицированные аденовирусом высокого риска, реципиенты аллогенных гемопоэтических клеток-предшественников и превентивная терапия цидофовиром
12
(стр.
219
—
27
)
6 3
Нагафудзи
030053 ,
,
Henzan
H
, и др.
Цидофовир для лечения аденовирусного геморрагического цистита у реципиентов трансплантата гемопоэтических стволовых клеток
34
(стр.
909
—
14
)
7
LEGRAND
F
,
Berrebi
0002 D
,
Хоухоу
N
, и др.
Ранняя диагностика аденовирусной инфекции и лечение цидофовиром после трансплантации костного мозга у детей
,
Трансплантация костного мозга
27
(стр.
621
—
6
)
8
Andrei
G
,
Fiten
G
,
0003
P
,
Губо
P
, и др.
Двойная инфекция полиомавирусом BK и устойчивым к ацикловиру вирусом простого герпеса, успешно пролеченная цидофовиром у реципиента трансплантата костного мозга
9
(стр.
126
—
31
)
9
Фарачи
M
,
Кузуббо
D
,
Ланино
E
, и др.
Низкая доза цидофовира без пробенецида для лечения геморрагического цистита, вызванного вирусом BK, после трансплантации гемопоэтических стволовых клеток
28
(стр.
55
—
7
)
10
Bryant
P
,
Sasadeusz
J
,
Carapetis
J
,
Waters
K
,
Curtis
N
.
Успешное лечение фоскарнерезистентного стоматита простого герпеса внутривенным введением цидофовира у ребенка
20
(стр.
1083
—
6
)
11
,
Schneider
P
,
Young
P
, at.
Лечение цидофовиром инфекции вируса простого герпеса, устойчивого к ацикловиру и фоскарнету, у ребенка после неродственной трансплантации костного мозга
,
Трансплантация костного мозга
26
(стр.
903
—
5
)
12
Морфин
F
,
Thouvenot
D
.
Резистентность вируса простого герпеса к противовирусным препаратам
26
(стр.
29
—
37
)
13
Wyles
0002 D,
Patel
A
,
Madinger
N
,
Bessesen
,
.


 Dvorak, Morton J. Cowan, Biljana Horn, Peggy S. Weintrub, Развитие стоматита, вызванного вирусом простого герпеса, во время лечения цидофовиром, Клинические инфекционные заболевания , том 49, выпуск 8, 15 октября 2009 г., страницы e92–e95, https://doi.org/10.1086/605678
Dvorak, Morton J. Cowan, Biljana Horn, Peggy S. Weintrub, Развитие стоматита, вызванного вирусом простого герпеса, во время лечения цидофовиром, Клинические инфекционные заболевания , том 49, выпуск 8, 15 октября 2009 г., страницы e92–e95, https://doi.org/10.1086/605678