Гранулема на корне зуба, что это такое, удаление гранулемы, причины, как вылечить воспаление
Содержание:
Что такое гранулема
Причины гранулемы
Разновидности гранулем
Лечение гранулемы у взрослых
Лечение грунулемы у детей
Гранулема на корне зуба — широко распространенное заболевание, поражающее полость рта как у взрослого поколения, так и у детей. Гранулему зуба практически невозможно вылечить на запущенной стадии, поэтому единственно возможным выходом остается удаление зуба. Чтобы избежать негативных последствий, важно своевременно обнаружить заболевание и обратиться к профессиональному стоматологу, который оценит серьезность проблемы и подскажет, какие меры предпринять для скорейшего выздоровления.
Что такое гранулема зуба
Понять, что такое гранулема зуба, несложно по ее внешним признакам. Гранулема зуба напоминает плотный узелок примерно в 5-8 мм в диаметре. При этом ближайшая зона окружения гранулемы подвергается воспалительным процессам. Нередко зубную гранулему называют опухолью или кистой. Такое осложнение наиболее часто появляется при наличии других заболеваний стоматологического характера.
Нередко зубную гранулему называют опухолью или кистой. Такое осложнение наиболее часто появляется при наличии других заболеваний стоматологического характера.
Игнорирование заболевания приводит к его дальнейшему развитию: грануляционные ткани быстро разрастаются, инфекция распространяется и стимулирует разрушение здоровых зубных тканей.
Причины возникновения гранулемы
Причиной проявления зубной гранулемы может быть ряд стоматологических заболеваний. Чаще всего к гранулеме приводит неизлеченный пульпит, который сопровождается инфекционным воспалением нервов в зубном корне. Нередко гранулема становится следствием кариеса или периодонтита, но возможно появление воспаления и вследствие инфицирования зуба при антисептическом удалении пульпы или лечении зубных каналов.
Капсула гранулемы может появиться и прорастать в полости рта и при многих других нарушениях функционирования иммунной системы. Изначально нарушения вызывают возникновение в пульпе микробов, что позже создает воспаление и полностью ее разрушает. По мере размножения микробов во рту костные ткани инфицируются, что в итоге приводит к формированию капсулы из соединительных тканей, в которых происходит борьба с такими микробами. Эта капсула и является гранулемой.
По мере размножения микробов во рту костные ткани инфицируются, что в итоге приводит к формированию капсулы из соединительных тканей, в которых происходит борьба с такими микробами. Эта капсула и является гранулемой.
Разрастание гранулемы возможно при стрессовых потрясениях, перенесенном простудном заболевании, при переохлаждении вследствие резкой перемены климата и даже при переутомлении от физических нагрузок.
Разновидности гранулем
Некоторое время гранулема на зубе может развиваться без проявления каких-либо симптомов. Определить тип новообразования, как правило, получается лишь при проявлении рентгенологического снимка. Различают следующие виды гранулем:
- сложная гранулема — при таком новообразовании на снимке заметны тяжи в виде белых нитей. Это свидетельствует о запущенной стадии болезни, что привело к образованию фиброзных волокон в капсуле гранулемы;
- составная гранулема — новообразование, часто встречающееся у детей. При таком заболевании внутри капсулы расположен зачаток зуба.
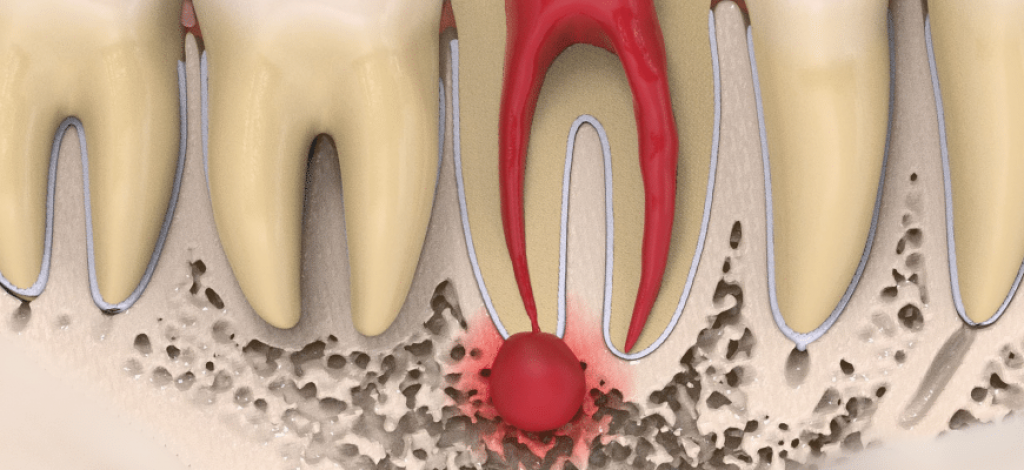 Инфицирование зачатка приводит к тому, что постоянный зуб не сможет прорастать в зубной дуге, если не произвести своевременное лечение.
Инфицирование зачатка приводит к тому, что постоянный зуб не сможет прорастать в зубной дуге, если не произвести своевременное лечение.
Лечение гранулемы у взрослых
Воспаление гранулемы сопровождается разной технологией лечения для взрослых и детей. Первая стадия лечения для взрослых — выполнение радиовизиографии или рентгенографии. С уточнением диагноза стоматолог выбирает, как вылечить гранулему. Здоровье ротовой полости восстанавливают терапевтическим методом либо при помощи хирургического вмешательства — выбор способа зависит от размера гранулемы, от здоровья зубных тканей и наличия серьезных осложнений.
При хирургическом вмешательстве происходит удаление зуба, что сопровождается резекцией верхней части корня и гемисекцией зуба. В самых сложных случаях нередко возникает потребность во вскрытии десны, чтобы в течение нескольких дней с помощью дренажа устранить гной из ротовой полости. Процесс сопровождается приемом антибиотиков и обезболивающих препаратов. По окончании процедуры, если зуб удаляется не полностью, а частично, на него устанавливается коронка.
По окончании процедуры, если зуб удаляется не полностью, а частично, на него устанавливается коронка.
Консервативное лечение зубной гранулемы всегда сопровождается пломбированием корневого канала. Воспаление полости рта устраняется антибиотиками, травами лечебного характера и сульфаниламидными средствами. В момент пломбирования происходит очистка канала зуба с удалением из гранулемы накопившегося гноя. По окончанию процедуры в зуб закладывается лекарство, а через пару дней канал вторично обрабатывается антибактерицидными средствами.
Лечение гранулемы у детей
Удаление гранулемы у детей должно быть более щадящим. При проявлении симптомов не решайте самостоятельно, как правильно удалить гранулему. Запрещается применять горячие компрессы — они только замедляют выздоровление, приводя к распространению гноя. Наши квалифицированные врачи помогут оперативно справиться с гранулемой без негативных последствий для здоровья Вашего ребенка.
Смотреть цены
Запись на прием к врачу-стоматологу
Еще статьи по тематике Хирургия
Удаление или лечение зубов
Ваши вопросы
Здравствуйте! Один стоматолог сказал, что мне лучше удалить зубы мудрости, но они вроде здоровые. Скажите, нужно ли удалять зубы мудрости?
Скажите, нужно ли удалять зубы мудрости?
Что лучше поставить, коронки или виниры?
Добрый день! Мне требуется удаление одного зуба, верхней пятерки. Слышала, что одновременно с этим сразу можно провести имплантацию. Можно ли удалить зуб и сразу поставить имплантант в вашей клинике?
Врачи-стоматологи
главный врач, стоматолог
Запись на прием
врач-стоматолог
Запись на прием
Задать вопрос доктору
Телефон
Эл.почта
Вопрос
Способы лечения гранулемы при перфорации канала зуба
Лечение зуба – это сложный комплекс различных действий, очередность которых во многом зависит от индивидуального состояния пациента. Современная стоматология достигла той стадии развития, когда для устранения одной проблемы существует множество способов, и лечащий врач самостоятельно подбирает не только медикаменты, но и способы воздействия на пораженную область. Однако в некоторых случаях неправильные действия стоматолога могут привести к тому, что потребуется проводить дополнительные лечебные процедуры, поэтому так важно выбрать хорошего врача. В нашей клинике лечение гранулемы при перфорации канала зуба осуществляется такими методами, чтобы применяемые лекарственные средства не привели к ухудшению общего состояния.
В нашей клинике лечение гранулемы при перфорации канала зуба осуществляется такими методами, чтобы применяемые лекарственные средства не привели к ухудшению общего состояния.
Что такое гранулема и в чем опасность образования
Гранулемой называют небольшое образование в верхней части зубного корня, которое состоит из воспаленных тканей. Новообразование имеет вид небольшого узелка, и разглядеть его невооруженным глазом практически невозможно, но постепенно небольшой очаг воспаления перерастает в кисту, которая заполняется клетками мертвой ткани и вызывает интенсивное воспаление здоровых тканей зуба. По этой причине лечение гранулемы при перфорации канала зуба нельзя откладывать, и следует заняться решением этой проблемы как можно скорее.
Существует несколько причин появление гранулемы – одни естественные и вызваны плохим состоянием зубных тканей, другие могут быть напрямую связаны с неправильными действиями стоматолога. Например, плохая очистка канала зуба ведет к появлению инфекции в этой области. Результатом может стать развитие гранулемы, поэтому доверять даже простые лечебные процедуры можно только опытным стоматологам с большим опытом работы. Гранулема также может возникнуть при перфорации канала зуба, так как образуется отверстие в тканях зуба, через которые свободно могут проникать различные микробы и инфекции. Лечение гранулемы при перфорации канала зуба нельзя откладывать надолго, так как через образовавшееся отверстие внутрь зуба попадают кусочки пищи и создают очаг воспаления.
Результатом может стать развитие гранулемы, поэтому доверять даже простые лечебные процедуры можно только опытным стоматологам с большим опытом работы. Гранулема также может возникнуть при перфорации канала зуба, так как образуется отверстие в тканях зуба, через которые свободно могут проникать различные микробы и инфекции. Лечение гранулемы при перфорации канала зуба нельзя откладывать надолго, так как через образовавшееся отверстие внутрь зуба попадают кусочки пищи и создают очаг воспаления.
Консервативное лечение гранулемы
Существует несколько методик лечения, которые равны по эффективности, но применяются в зависимости от индивидуального состояния пациента. Например, на ранних этапах развития новообразования эффективнее всего применять медикаментозное или консервативное лечение гранулемы. Комплекс лечебных процедур заключается в приеме различных лекарственных средств от болеутоляющих до антибиотиков, список лекарств подбирается после согласования с врачом.
При таком лечении главная цель заключается в снятии воспаления и купировании болевого синдрома. Если все медикаменты подобраны правильно, то гранулема рассосется через несколько недель. Как уже упоминалось ранее, лечение гранулемы медикаментозным методом применимо только на ранних стадиях появления заболевания. Если была нарушена целостность канала зуба, медикаментозный курс дополняется процедурами очистки очага воспаления.
Если все медикаменты подобраны правильно, то гранулема рассосется через несколько недель. Как уже упоминалось ранее, лечение гранулемы медикаментозным методом применимо только на ранних стадиях появления заболевания. Если была нарушена целостность канала зуба, медикаментозный курс дополняется процедурами очистки очага воспаления.
Лечение гранулемы при перфорации канала зуба в обязательном порядке включает работу над областью зубного корня. Чистка канала – довольно болезненная процедура, поэтому ее проводят только после обезболивания всей области. Чистка осуществляется механическими способами, поэтому для работы обычно используется бормашина и различные стоматологические инструменты. После того, как канал зуба полностью очищен от любых микроорганизмов и воспалений, в область гранулемы вводится специальный препарат для рассасывания новообразования. Как видите, данная процедура требует детального изучения состояния пациента и профессионального подхода к лечению. Если вам назначили лечение гранулемы при перфорации канала зуба в Подольске, важно уделить внимание выбору стоматологической клиники. Отличные результаты демонстрируют врачи стоматологии «Аликсма», которые не только обладают нужным опытом для работы со сложными образованиями, но и используют инновационные методы лечения.
Отличные результаты демонстрируют врачи стоматологии «Аликсма», которые не только обладают нужным опытом для работы со сложными образованиями, но и используют инновационные методы лечения.
Хирургические методики
В ситуации, когда новообразование достигло больших размеров, воздействовать на него медикаментами не имеет смысла. Гораздо эффективнее удалить его хирургическим путем, но подобная методика обычно подразумевает удаление всего зуба или значительной его части. Как правило, к такому способу прибегают в тех случаях, когда диаметр гранулемы превышает один сантиметр или на одном зубе располагается сразу несколько образований.
В зависимости от состояния зуба и стадии развития заболевания лечение гранулемы при перфорации канала зуба хирургическим способом может предполагать удаление омертвевших тканей при помощи жгута или части зуба вместе с гранулемой. В первом случае разрезается десна, и через полученное отверстие к очагу воспаления подводится жгут, через который удаляется гной. Такая методика отличается длительностью, так как удаление гноя может занять несколько часов. После полной очистки корня стоматолог закрывает место обработки пломбой.
Такая методика отличается длительностью, так как удаление гноя может занять несколько часов. После полной очистки корня стоматолог закрывает место обработки пломбой.
Большие новообразования проще удалить вместе с частью костной ткани или избавиться от больного зуба полностью. Решение принимает лечащий врач после внимательного изучения всех анализов, так как целью хорошего стоматолога является сохранение зуба или хотя бы его части.
Если вы хотите пройти лечение гранулемы при перфорации канала зуба недорого и при этом получить качественный сервис и профессиональное отношение, обращайтесь в клинику «Аликсма». Наш стоматологический центр собрал штат квалифицированных специалистов, которые постоянно работают над улучшением своих навыков и применяют не только традиционные методы лечения, но и современные подходы. В нашей клинике вы можете пройти лечение гранулемы при перфорации канала зуба по лучшим ценам и избавиться от такой проблемы навсегда.
P.S. Если Вам нужно произвести лечение зубов в Подольске, то одним из наиболее важных моментов будет диагностика зубов, ведь только отталкиваясь от нее можно максимально точно определить проблему и устранить ее. Чтобы провести данную процедуру, мы рекомендуем Вам обратиться к нам, позвонив по телефону или написав в форму обратной связи! Вежливые менеджеры обязательно ответят на Ваши вопросы и проконсультируют. Мы сделаем Вам красивую улыбку, полную белоснежных зубов. Обращайтесь! До связи!
Чтобы провести данную процедуру, мы рекомендуем Вам обратиться к нам, позвонив по телефону или написав в форму обратной связи! Вежливые менеджеры обязательно ответят на Ваши вопросы и проконсультируют. Мы сделаем Вам красивую улыбку, полную белоснежных зубов. Обращайтесь! До связи!
Нехирургическое лечение большого периапикального поражения с использованием аспирации в сочетании с тройной антибиотиковой пастой и гидроксидом кальция
Иран Endod J. 2010 Autumn; 5(4): 179–182.
Опубликовано в Интернете 15 ноября 2010 г.
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
Известно, что стойкие микроорганизмы в корневом канале вызывают неэффективность эндодонтического лечения. Чрезмерно растянутая гуттаперча также может действовать как раздражитель перирадикулярных тканей, что приводит к обширным периапикальным поражениям. Извлечение чрезмерно растянутой гуттаперчи нехирургическим путем может оказаться сложной задачей.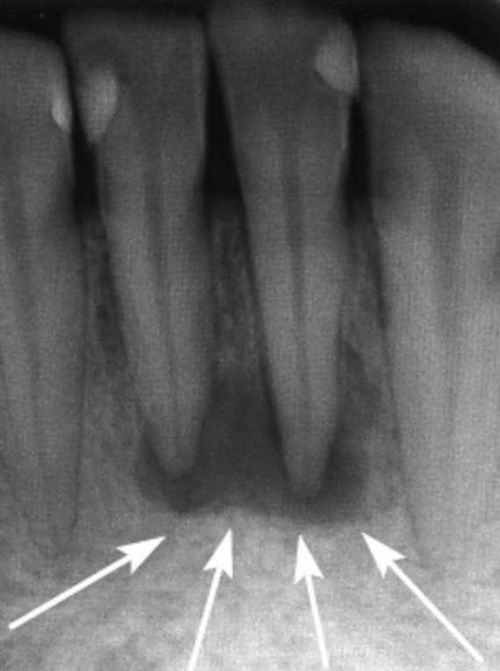 Этот случай описывает нехирургическое лечение большого периапикального поражения, связанного с чрезмерно растянутой гуттаперчей. Была предпринята попытка извлечения гуттаперчи, но слишком растянутую часть удалить не удалось. Аспирацию гнойного экссудата проводили через корневой канал с применением тройной антибиотической пасты. Через 2 недели пасту с антибиотиком заменили гидроксидом кальция для усиления костной регенерации. Периапикальное поражение показало значительное периапикальное заживление через 15 месяцев. Результаты этого случая демонстрируют, что аспирация в сочетании с тройной пастой с антибиотиком и гидроксидом кальция может быть использована для лечения больших периапикальных поражений, связанных с чрезмерно растянутой гуттаперчей.
Этот случай описывает нехирургическое лечение большого периапикального поражения, связанного с чрезмерно растянутой гуттаперчей. Была предпринята попытка извлечения гуттаперчи, но слишком растянутую часть удалить не удалось. Аспирацию гнойного экссудата проводили через корневой канал с применением тройной антибиотической пасты. Через 2 недели пасту с антибиотиком заменили гидроксидом кальция для усиления костной регенерации. Периапикальное поражение показало значительное периапикальное заживление через 15 месяцев. Результаты этого случая демонстрируют, что аспирация в сочетании с тройной пастой с антибиотиком и гидроксидом кальция может быть использована для лечения больших периапикальных поражений, связанных с чрезмерно растянутой гуттаперчей.
Ключевые слова: Периапикальные заболевания, препараты для лечения корневых каналов, антибиотики, гидроксид кальция, повторное лечение
Основной причиной неэффективности лечения корневых каналов являются стойкие микроорганизмы, которые остаются после лечения или повторного загрязнения системы каналов из-за неадекватной герметизации ( 1). Гуттаперча, наиболее часто используемый материал для пломбирования корней, также может действовать как раздражитель перирадикулярных тканей, если она выходит за пределы апикального отверстия (2,3). С такими зубами могут быть связаны большие периапикальные поражения. Имеются клинические данные, свидетельствующие о том, что по мере увеличения размеров периапикального поражения увеличивается частота корешковых кист. Однако было показано, что поражения диаметром ≥20 мм представляют собой гранулемы (4).
Гуттаперча, наиболее часто используемый материал для пломбирования корней, также может действовать как раздражитель перирадикулярных тканей, если она выходит за пределы апикального отверстия (2,3). С такими зубами могут быть связаны большие периапикальные поражения. Имеются клинические данные, свидетельствующие о том, что по мере увеличения размеров периапикального поражения увеличивается частота корешковых кист. Однако было показано, что поражения диаметром ≥20 мм представляют собой гранулемы (4).
Варианты лечения крупных периапикальных поражений варьируются от нехирургического лечения корневых каналов и апикальной хирургии до экстракции (5). Тем не менее, растущий интерес к повторному эндодонтическому лечению связан с увеличением потребности пациентов в сохранении зубов (1). Принятие хирургического подхода требует рассмотрения нескольких ключевых факторов, таких как близость поражения к соседним жизненно важным зубам, посягательство на анатомические структуры, сотрудничество с пациентом и продолжительность лечения (4,5).
Для лечения периапикальных поражений использовались различные нехирургические методы (5-11). Когда для зуба с чрезмерно растянутой гуттаперчей используется нехирургический метод повторного лечения, извлечение чрезмерно растянутой гуттаперчи может оказаться сложной задачей.
В следующем клиническом случае сообщается о лечении большого периапикального поражения, связанного с чрезмерно растянутой гуттаперчей, с использованием аспирации в сочетании с тройной пастой с антибиотиком и гидроксидом кальция, поскольку хирургический подход не мог быть принят из-за отказа пациента.
43-летний пациент был направлен в отделение консервативной стоматологии и эндодонтии больницы стоматологического колледжа Гоа с болью и припухлостью неба в левой передней области верхней челюсти. Пациент сообщил о травме передних зубов около 2 лет назад, которую лечил стоматолог общей практики.
Через год после операции у пациента развилась небная опухоль; пациент принимал самостоятельно антибиотики и анальгетики в течение этого периода в один год, однако опухоль неоднократно рецидивировала.
Внутриротовой осмотр выявил плотную небную припухлость, простирающуюся от зубов № 9 до 11. Зубы № 8 и 10 были изменены в цвете и не реагировали на тест на чувствительность пульпы. Соседние зубы реагировали в пределах нормы.
На периапикальной рентгенограмме выявлено большое периапикальное просветление (~1,7×1,4 см в диаметре), по-видимому, затрагивающее верхушки зубов № 9 и 10 (). Зуб № 10 показал рентгеноконтрастный материал, который выступал из пространства корневого канала и за пределы рентгенологически апекса примерно на 2,5 мм. Также была отмечена неадекватная адаптация гуттаперчи на апексе, что, вероятно, еще больше усугубило плохое апикальное прилегание. В зубе №8 рентгеноконтрастный материал распространялся только до средней трети пространства корневого канала. Рентгенопрозрачное выпячивание в средней трети корневого канала свидетельствовало о внутреннем резорбтивном дефекте.
Открыть в отдельном окне
A) Периапикальная рентгенограмма, показывающая большую периапикальную рентгенопрозрачность, по-видимому, затрагивающую верхушки зубов № 9 и 10. Зуб № 10 показывает рентгеноконтрастный материал, выходящий за пределы рентгенологической верхушки приблизительно на 2,5 мм. B) Периапикальная рентгенограмма, показывающая гуттаперчу за верхушкой корня, которую невозможно извлечь, и нет. 40-ручный К-файл, выходящий за пределы апикального отверстия. C) Периапикальная рентгенограмма через 5 месяцев, показывающая благоприятное периапикальное заживление. Ослабленная коронковая структура зуба была удалена. D) Периапикальная рентгенограмма через 1 год 3 месяца, показывающая значительное периапикальное заживление, несмотря на чрезмерно растянутую гуттаперчу
Зуб № 10 показывает рентгеноконтрастный материал, выходящий за пределы рентгенологической верхушки приблизительно на 2,5 мм. B) Периапикальная рентгенограмма, показывающая гуттаперчу за верхушкой корня, которую невозможно извлечь, и нет. 40-ручный К-файл, выходящий за пределы апикального отверстия. C) Периапикальная рентгенограмма через 5 месяцев, показывающая благоприятное периапикальное заживление. Ослабленная коронковая структура зуба была удалена. D) Периапикальная рентгенограмма через 1 год 3 месяца, показывающая значительное периапикальное заживление, несмотря на чрезмерно растянутую гуттаперчу
Для лечения периапикального поражения был предложен хирургический доступ, но пациент от него отказался. Следовательно, было принято решение применить нехирургический метод повторного лечения зуба № 10. Также было принято решение о одновременном ретинировании зуба №8, учитывая некачественную обтурацию и возможность внутренней резорбции.
После удаления небной реставрации с зуба №10 в устье корневого канала был виден обтурационный материал из гуттаперчи. Также была отмечена ослабленная коронковая структура зуба, что требует установки штифта после эндодонтического лечения. Затем была предпринята попытка удаления гуттаперчи. Между гуттаперчей и стенкой канала создавали пространство с помощью ручных К-файлов (Dentsply Maillefer, Ballaigues, Швейцария), а гуттаперчу извлекали из корневого канала с помощью ручных Н-файлов (Dentsply Maillefer, Ballaigues, Швейцария). Растворитель для этой цели не использовался. Однако извлечь гуттаперчу за верхушку корня не удалось. Ручной К-файл №40 свободно прошел за апикальное отверстие (). Пальцем надавливали на небную припухлость, которая выделяла гнойный экссудат из канала. Зуб был обработан до размера ISO 50 с использованием ручных К-файлов с 3% гипохлоритом натрия (Vensons India, Бангалор, Индия) для ирригации между инструментами. Гнойный экссудат аспирировали, как описано Fernandes и Ataide, путем введения иглы 25 размера, прикрепленной к шприцу объемом 5 мл, за апикальное отверстие (11). Пальцевое давление оказывалось на припухлость, в то время как канал был высушен бумажными штифтами (Dentsply Maillefer, Ballaigues, Швейцария) и впоследствии временным.
Также была отмечена ослабленная коронковая структура зуба, что требует установки штифта после эндодонтического лечения. Затем была предпринята попытка удаления гуттаперчи. Между гуттаперчей и стенкой канала создавали пространство с помощью ручных К-файлов (Dentsply Maillefer, Ballaigues, Швейцария), а гуттаперчу извлекали из корневого канала с помощью ручных Н-файлов (Dentsply Maillefer, Ballaigues, Швейцария). Растворитель для этой цели не использовался. Однако извлечь гуттаперчу за верхушку корня не удалось. Ручной К-файл №40 свободно прошел за апикальное отверстие (). Пальцем надавливали на небную припухлость, которая выделяла гнойный экссудат из канала. Зуб был обработан до размера ISO 50 с использованием ручных К-файлов с 3% гипохлоритом натрия (Vensons India, Бангалор, Индия) для ирригации между инструментами. Гнойный экссудат аспирировали, как описано Fernandes и Ataide, путем введения иглы 25 размера, прикрепленной к шприцу объемом 5 мл, за апикальное отверстие (11). Пальцевое давление оказывалось на припухлость, в то время как канал был высушен бумажными штифтами (Dentsply Maillefer, Ballaigues, Швейцария) и впоследствии временным. К концу приема припухлость неба уменьшилась в размерах. Однако на следующем приеме через неделю после операции пациент пожаловался на боль и подобный отек неба; временная реставрация также утрачена, из канала гнойное отделяемое. Затем было решено использовать тройную антибиотическую пасту из ципрофлоксацина 500 мг (Ciplox 500 мг, Cipla Ltd, Сикким, Индия), метронидазола 400 мг (Aristogyl, Aristo Pharmaceuticals Pvt Ltd, Индия) и миноциклина 100 мг (Ranbaxy Laboratories Ltd, Солан, Индия). Аллергии на применяемые антибиотики у пациента не было. Кремообразная паста, описанная Takushige 9.0037 и др. Было приготовлено (12). После аспирации гнойного экссудата и высушивания канала пасту использовали как внутриканальное лекарственное средство. Повторное лечение зуба № 8 также было начато и завершено на следующих посещениях. Через 2 недели пациент был бессимптомным и не было никаких признаков отека. Тройную антибиотическую пасту промывали из канала 3% раствором гипохлорита натрия. Гнойного отделяемого из канала не было.
К концу приема припухлость неба уменьшилась в размерах. Однако на следующем приеме через неделю после операции пациент пожаловался на боль и подобный отек неба; временная реставрация также утрачена, из канала гнойное отделяемое. Затем было решено использовать тройную антибиотическую пасту из ципрофлоксацина 500 мг (Ciplox 500 мг, Cipla Ltd, Сикким, Индия), метронидазола 400 мг (Aristogyl, Aristo Pharmaceuticals Pvt Ltd, Индия) и миноциклина 100 мг (Ranbaxy Laboratories Ltd, Солан, Индия). Аллергии на применяемые антибиотики у пациента не было. Кремообразная паста, описанная Takushige 9.0037 и др. Было приготовлено (12). После аспирации гнойного экссудата и высушивания канала пасту использовали как внутриканальное лекарственное средство. Повторное лечение зуба № 8 также было начато и завершено на следующих посещениях. Через 2 недели пациент был бессимптомным и не было никаких признаков отека. Тройную антибиотическую пасту промывали из канала 3% раствором гипохлорита натрия. Гнойного отделяемого из канала не было. Канал был высушен, и паста гидроксида кальция (RC Cal, Prime Dental, Индия) использовалась в качестве внутриканального лекарственного средства, позволяющего некоторую экструзию в периапикальной области. Затем гидроксид кальция заменяли каждый месяц. Через 5 месяцев наблюдалось благоприятное периапикальное заживление (). Ослабленная коронковая структура зуба была удалена, а корневой канал обтурирован, после чего была установлена штифтовая конструкция и восстановлена культя. Рентгенограмма, сделанная через 15 месяцев, показала значительное периапикальное заживление (1). Пациент был бессимптомным и был назначен на повторный контрольный прием.
Канал был высушен, и паста гидроксида кальция (RC Cal, Prime Dental, Индия) использовалась в качестве внутриканального лекарственного средства, позволяющего некоторую экструзию в периапикальной области. Затем гидроксид кальция заменяли каждый месяц. Через 5 месяцев наблюдалось благоприятное периапикальное заживление (). Ослабленная коронковая структура зуба была удалена, а корневой канал обтурирован, после чего была установлена штифтовая конструкция и восстановлена культя. Рентгенограмма, сделанная через 15 месяцев, показала значительное периапикальное заживление (1). Пациент был бессимптомным и был назначен на повторный контрольный прием.
Дренирование важно при консервативном лечении больших периапикальных поражений. При прямом и немедленном дренировании локализованных опухолей, абсцессов или кист симптомы уменьшаются, и может возникнуть фиброплазия и миграция клеток (13,14). Fernandes и Ataide сообщили об использовании простой аспирации через корневой канал при лечении большого периапикального поражения (11). Аспирация неизвестного костного образования является относительно безобидной хирургической процедурой, которая может предоставить информацию о наличии гноя, кистозной жидкости или кровотечения. Гнойный характер экссудата в данном случае мог бы объяснить неадекватность одной только техники аспирации. Об этом факте также сообщал ранее Hoen и др. , который описал технику аспирации и ирригации с использованием щечно-небного доступа (7). Они заявили, что этот метод можно использовать только при поражениях, которые, по-видимому, представляют собой неинфицированные периапикальные кисты. Этот вывод был основан на типе удаленной жидкости и отсутствии микробного присутствия как в культуре, так и в образцах, окрашенных по Граму.
Аспирация неизвестного костного образования является относительно безобидной хирургической процедурой, которая может предоставить информацию о наличии гноя, кистозной жидкости или кровотечения. Гнойный характер экссудата в данном случае мог бы объяснить неадекватность одной только техники аспирации. Об этом факте также сообщал ранее Hoen и др. , который описал технику аспирации и ирригации с использованием щечно-небного доступа (7). Они заявили, что этот метод можно использовать только при поражениях, которые, по-видимому, представляют собой неинфицированные периапикальные кисты. Этот вывод был основан на типе удаленной жидкости и отсутствии микробного присутствия как в культуре, так и в образцах, окрашенных по Граму.
Доказано, что паста с тройным антибиотиком эффективно устраняет бактерии из инфицированных тканей зубов (12,15,16). Метронидазол обладает широким бактерицидным спектром в отношении анаэробов. Ципрофлоксацин и миноциклин эффективны против бактерий, устойчивых к метронидазолу (16). Несмотря на небольшое количество применяемого препарата, перед их применением необходимо исключить чувствительность пациентов к химическим веществам или антибиотикам (17). Недостатком пасты с тройным антибиотиком является изменение цвета зубов, вызванное миноциклином. Цефаклор и фосфомицин предложены в качестве альтернативы миноциклину с точки зрения их антибиотической эффективности, но необходимы дальнейшие клинические исследования, чтобы продемонстрировать их эффективность в корневом канале (18). В данном клиническом случае паста с антибиотиком использовалась в связи с гнойным характером экссудата в течение 2 недель. Затем его заменили гидроксидом кальция для усиления костной регенерации костной полости. Многие исследователи утверждают, что прямой контакт между гидроксидом кальция и периапикальными тканями благотворно влияет на остеоиндуктивные свойства материала (19).,20). Сообщалось о высокой степени успеха при использовании гидроксида кальция за пределами апекса в случаях больших периапикальных поражений (21).
Несмотря на небольшое количество применяемого препарата, перед их применением необходимо исключить чувствительность пациентов к химическим веществам или антибиотикам (17). Недостатком пасты с тройным антибиотиком является изменение цвета зубов, вызванное миноциклином. Цефаклор и фосфомицин предложены в качестве альтернативы миноциклину с точки зрения их антибиотической эффективности, но необходимы дальнейшие клинические исследования, чтобы продемонстрировать их эффективность в корневом канале (18). В данном клиническом случае паста с антибиотиком использовалась в связи с гнойным характером экссудата в течение 2 недель. Затем его заменили гидроксидом кальция для усиления костной регенерации костной полости. Многие исследователи утверждают, что прямой контакт между гидроксидом кальция и периапикальными тканями благотворно влияет на остеоиндуктивные свойства материала (19).,20). Сообщалось о высокой степени успеха при использовании гидроксида кальция за пределами апекса в случаях больших периапикальных поражений (21). Следовательно, гидроксид кальция был преднамеренно экструдирован за пределы апикального отверстия, что привело к благоприятной костной регенерации, несмотря на чрезмерно растянутую гуттаперчу.
Следовательно, гидроксид кальция был преднамеренно экструдирован за пределы апикального отверстия, что привело к благоприятной костной регенерации, несмотря на чрезмерно растянутую гуттаперчу.
Сотрудничество с пациентом является важным фактором при использовании хирургического подхода при лечении периапикальных поражений. Использование аспирации вместе с пастой с тройным антибиотиком и гидроксидом кальция может помочь в лечении нехирургических случаев.
Неудачное эндодонтическое лечение может быть хорошим кандидатом на консервативное лечение. Тщательная очистка и формирование канала наряду с дезинфекцией являются ключевыми факторами в начале периапикального заживления. Различные методы лечения, такие как использование пасты с тройным антибиотиком и гидроксида кальция, могут улучшить и ускорить процесс заживления.
1. Schirrmeister JF, Liebenow AL, Braun G, Wittmer A, Hellwig E, Al-Ahmad A. Обнаружение и уничтожение микроорганизмов в запломбированных корнях зубов, связанных с перирадикулярными поражениями: исследование in vivo. Дж Эндод. 2007; 33: 536–40. [PubMed] [Академия Google]
Дж Эндод. 2007; 33: 536–40. [PubMed] [Академия Google]
2. Райзинг Д.В., Голдман М., Брайтон С.М. Гистологическая оценка 3 экспериментальных материалов для пломбирования корневых каналов. Дж Эндод. 1975; 1: 172–7. [PubMed] [Google Scholar]
3. Pascon EA, Spångberg LS. Цитотоксичность материалов для пломбирования корневых каналов in vitro: 1. Гуттаперча. Дж Эндод. 1990; 16: 429–33. [PubMed] [Google Scholar]
4. Морс Д.Р., Бхамбхани С.М. Дилемма стоматолога: нехирургическое эндодонтическое лечение или периапикальная хирургия зубов с выраженным поражением пульпы и сопутствующим периапикальным рентгенопрозрачным поражением. Oral Surg Oral Med Oral Pathol. 1990;70:333–40. [PubMed] [Google Scholar]
5. Лушин Р.Дж., Веллер Р.Н., Беллицци Р., Кулильд Дж.К. 2-дневная декомпрессия: история болезни первого моляра верхней челюсти. Дж Эндод. 1991; 17:85–87. [PubMed] [Google Scholar]
6. Шах Н. Нехирургическое лечение периапикальных поражений: проспективное исследование. Oral Surg Oral Med Oral Pathol. 1988; 66: 365–71. [PubMed] [Google Scholar]
Oral Surg Oral Med Oral Pathol. 1988; 66: 365–71. [PubMed] [Google Scholar]
7. Hoen MM, LaBounty GL, Strittmatter EJ. Консервативное лечение персистирующих перирадикулярных образований с использованием аспирации и ирригации. Дж Эндод. 1990;16:182–186. [PubMed] [Google Scholar]
8. Чалишкан М.К. Прогноз больших кистоподобных периапикальных поражений после нехирургического лечения корневых каналов: клинический обзор. Int Endod J. 2004; 37: 408–16. [PubMed] [Google Scholar]
9. Er K, Kuştarci A, Ozan U, Taşdemir T. Нехирургическое эндодонтическое лечение инвагинального dens invaginatus в нижнечелюстном премоляре с большим перирадикулярным поражением: клинический случай. Дж Эндод. 2007; 33: 322–4. [PubMed] [Google Scholar]
10. Мецгер З., Хубер Р., Славеску Д., Драгомиреску Д., Тобис И., Беттер Х. Кинетика заживления периапикальных поражений, усиленная процедурой апексума: клиническое исследование. Дж Эндод. 2009 г.;35:153–9. [PubMed] [Google Scholar]
11. Fernandes M, De Ataide I. Нехирургическое лечение большого периапикального поражения с использованием простой техники аспирации: клинический случай. Int Endod J. 2010; 43: 536–42. [PubMed] [Google Scholar]
Fernandes M, De Ataide I. Нехирургическое лечение большого периапикального поражения с использованием простой техники аспирации: клинический случай. Int Endod J. 2010; 43: 536–42. [PubMed] [Google Scholar]
12. Takushige T, Cruz EV, Asgor Moral A, Hoshino E. Эндодонтическое лечение молочных зубов с использованием комбинации антибактериальных препаратов. Int Endod J. 2004; 37: 132–8. [PubMed] [Google Scholar]
13. Gutmann JL, Fava LR. Перирадикулярное заживление и апикальное закрытие нежизнеспособного зуба при наличии бактериального загрязнения. Инт Эндод Дж. 1992;25:307–11. [PubMed] [Google Scholar]
14. Gutmann JL, Dumsha TC, Lovdahl PE. Решение проблем при лечении болезненных зубов. В: Gutmann JL, Dumsha TC, Lovdahl PE, Hovland EC, редакторы. Решение проблем в эндодонтии. 4-е издание. Сент-Луис: Мосби; 2006. С. 281–309. [Google Scholar]
15. Hoshino E, Kurihara-Ando N, Sato I, Uematsu H, Sato M, Kota K, Iwaku M. Антибактериальная чувствительность in vitro бактерий, взятых из инфицированного дентина корня, к смеси ципрофлоксацина, метронидазола и миноциклин. Инт Эндод Дж. 1996;29:125–30. [PubMed] [Google Scholar]
Инт Эндод Дж. 1996;29:125–30. [PubMed] [Google Scholar]
16. Sato I, Ando-Kurihara N, Kota K, Iwaku M, Hoshino E. Стерилизация инфицированного дентина корневого канала путем местного применения смеси ципрофлоксацина, метронидазола и миноциклина in situ. Int Endod J. 1996; 29: 118–24. [PubMed] [Google Scholar]
17. Озан Ю, Куршат Э. Эндодонтическое лечение большого кистоподобного перирадикулярного поражения с использованием комбинации антибиотиков: клинический случай. Дж Эндод. 2005; 31: 898–900. [PubMed] [Академия Google]
18. Kim JH, Kim Y, Shin SJ, Park JW, Jung IY. Изменение цвета несформированного постоянного резца, связанное с тройной терапией антибиотиками: клинический случай. Дж Эндод. 2010;36:1086–91. [PubMed] [Google Scholar]
19. Ghose LJ, Baghdady VS, Hikmat BYM. Апексификация несформированных верхушек депульпированных постоянных передних зубов гидроксидом кальция. Дж Эндод. 1987; 13: 285–90. [PubMed] [Google Scholar]
20. Ротштейн И., Фридман С. , Кац Дж. Апикальное закрытие корней зрелых моляров с использованием гидроксида кальция. Oral Surg Oral Med Oral Pathol. 1990;70:656–60. [PubMed] [Google Scholar]
, Кац Дж. Апикальное закрытие корней зрелых моляров с использованием гидроксида кальция. Oral Surg Oral Med Oral Pathol. 1990;70:656–60. [PubMed] [Google Scholar]
21. Чалишкан М.К., Тюркюн М. Периапикальное восстановление и апикальное закрытие депульпированного зуба с использованием гидроксида кальция. Oral Surg Oral Med Oral Pathol. 1997; 84: 683–687. [PubMed] [Google Scholar]
Хроническая гранулематозная болезнь и другие нарушения фагоцитарной клетки
Хроническая гранулематозная болезнь (ХГБ) — это генетическое (наследственное) заболевание, при котором клетки организма, поедающие определенных захватчиков (также называемые фагоцитами), не производят водород перекись и другие химические вещества, необходимые для уничтожения определенных бактерий и плесени. В результате этого дефекта у пациентов с ХГБ больше инфекций, а также у них слишком много иммунных клеток, образующих «узлы», называемые гранулемами, отсюда и название болезни. Еще одна проблема при ХГБ заключается в том, что у пациентов может развиться чрезмерное воспаление даже при отсутствии инфекции, и это воспаление может вызвать диарею, проблемы с мочевым пузырем и почками.
Дополнительные ресурсы и вспомогательные материалы
Определение хронической гранулематозной болезни
Фагоциты (от греческого phagein, «поедать») представляют собой лейкоциты, которые могут окружать и поглощать микроорганизмы в крошечных компартментах клетки. Эти отсеки, называемые фагосомами, заполнены химическими веществами, которые помогают убивать бактерии и грибки. Эти химические вещества включают перекись водорода и отбеливатель, которые производятся в этих отсеках и достигают там высоких уровней. Различают два основных типа фагоцитов: нейтрофилы и моноциты. Они выползают из кровеносных сосудов и направляются прямо туда, где есть инфекция. Когда они попадают в место заражения, они ищут бактерии или грибки и проглатывают их в фагосомы. Затем нормальный фагоцит закачивает в компартмент перекись водорода, отбеливатель и другие токсины, чтобы убить заражающий организм.
Фагоциты CGD в норме направляются к очагам инфекции, где они поглощают заражающие микробы. Однако они не могут производить перекись водорода и отбеливатель, как это делают нормальные клетки, потому что им не хватает ключевых белков, которые помогают производить отбеливатель. Очень примечательно, что фагоциты больных ХГБ могут защищать от большинства инфекций, но не от всех. Больные ХГБ имеют нормальный иммунитет к большинству вирусов и некоторым бактериям и грибкам, поэтому они не инфицированы постоянно. Они могут пройти от нескольких месяцев до нескольких лет без инфекций, а затем у них будет тяжелая форма. Пациенты с ХГБ вырабатывают нормальные антитела, поэтому, в отличие от пациентов с проблемами лимфоцитов, пациенты с ХГБ не особенно восприимчивы к вирусам.
Однако они не могут производить перекись водорода и отбеливатель, как это делают нормальные клетки, потому что им не хватает ключевых белков, которые помогают производить отбеливатель. Очень примечательно, что фагоциты больных ХГБ могут защищать от большинства инфекций, но не от всех. Больные ХГБ имеют нормальный иммунитет к большинству вирусов и некоторым бактериям и грибкам, поэтому они не инфицированы постоянно. Они могут пройти от нескольких месяцев до нескольких лет без инфекций, а затем у них будет тяжелая форма. Пациенты с ХГБ вырабатывают нормальные антитела, поэтому, в отличие от пациентов с проблемами лимфоцитов, пациенты с ХГБ не особенно восприимчивы к вирусам.
Таким образом, фагоциты CGD не могут вырабатывать перекись водорода и отбеливать, что приводит к инфекциям, вызванным лишь несколькими бактериями и грибками, включая Staphylococcus aureus , Burkholderia cepacia complex , Serratia marcescens , Asperillus Nocardia и . Большая часть остальной части их иммунной системы в норме.
Большая часть остальной части их иммунной системы в норме.
Клиническая картина хронической гранулематозной болезни
Дети с ХГБ обычно здоровы при рождении. Наиболее распространенной инфекцией ХГБ в младенчестве является кожная или костная инфекция, вызванная бактериями 9.0037 Serratia marcescens , и любой младенец с инфекцией этим конкретным микроорганизмом должен быть проверен на ХГБ. Фактически, любой младенец или ребенок со значительной инфекцией любым из ранее перечисленных организмов должен быть проверен на ХГБ.
Инфекции при ХГБ могут поражать любой орган или ткань, но обычными местами инфекции являются кожа, легкие, лимфатические узлы, печень и кости. Инфекции могут разрываться и дренироваться с замедленным заживлением и остаточным рубцеванием. Инфекция лимфатических узлов (под мышкой, в паху, на шее) является распространенной проблемой при ХГБ, часто требующей дренирования или хирургического вмешательства вместе с антибиотиками.
Пневмония является распространенной проблемой при ХГБ. Пневмония, вызванная грибком Aspergillus , может протекать очень медленно, сначала вызывая только утомляемость и только позже вызывая кашель или боль в груди. Грибковые пневмонии часто не вызывают лихорадки. Напротив, бактериальные инфекции ( Staphylococcus aureus , Burkholderia cepacia complex , Serratia marcescens , Nocardia ) обычно очень быстро проявляются лихорадкой и кашлем. В частности, Nocardia вызывает высокую температуру и абсцессы легких, которые могут разрушить части легкого. Важно выявить инфекцию и возбудителя на ранней стадии и полностью вылечить инфекцию, обычно в течение длительного периода времени, поэтому крайне важно своевременно обратиться за медицинской помощью. Рентген грудной клетки и компьютерная томография (КТ) грудной клетки очень полезны. Однако, если наблюдается пневмония, очень важно точно выяснить, какой микроб ее вызывает, для чего может потребоваться биопсия, обычно выполняемая с помощью иглы или бронхоскопа, а не хирургического вмешательства.
Пневмония, вызванная грибком Aspergillus , может протекать очень медленно, сначала вызывая только утомляемость и только позже вызывая кашель или боль в груди. Грибковые пневмонии часто не вызывают лихорадки. Напротив, бактериальные инфекции ( Staphylococcus aureus , Burkholderia cepacia complex , Serratia marcescens , Nocardia ) обычно очень быстро проявляются лихорадкой и кашлем. В частности, Nocardia вызывает высокую температуру и абсцессы легких, которые могут разрушить части легкого. Важно выявить инфекцию и возбудителя на ранней стадии и полностью вылечить инфекцию, обычно в течение длительного периода времени, поэтому крайне важно своевременно обратиться за медицинской помощью. Рентген грудной клетки и компьютерная томография (КТ) грудной клетки очень полезны. Однако, если наблюдается пневмония, очень важно точно выяснить, какой микроб ее вызывает, для чего может потребоваться биопсия, обычно выполняемая с помощью иглы или бронхоскопа, а не хирургического вмешательства. Лечение может занять много недель.
Лечение может занять много недель.
Абсцессы печени встречаются примерно у трети пациентов с ХГБ. Абсцесс может проявляться лихорадкой и усталостью, но также может вызывать легкую боль в правой верхней части живота. Для диагностики требуется какое-то сканирование (магнитно-резонансная томография или МРТ, КТ, УЗИ), а пункционная биопсия необходима для определения конкретной причины инфекции. Staphylococcus aureus вызывает большинство абсцессов печени у пациентов с ХГБ. Часто абсцессы печени трудно дренировать, и может потребоваться хирургическое вмешательство. Иногда абсцессы можно лечить антибиотиками и стероидами, которые уменьшают воспаление и улучшают действие антибиотиков.
Костная инфекция (остеомиелит) может поражать руки и ноги, но также может поражать позвоночник, особенно если грибковая инфекция в легких распространяется на позвоночник.
Появляются новые антибиотики и противогрибковые препараты, многие из которых очень активны при приеме внутрь.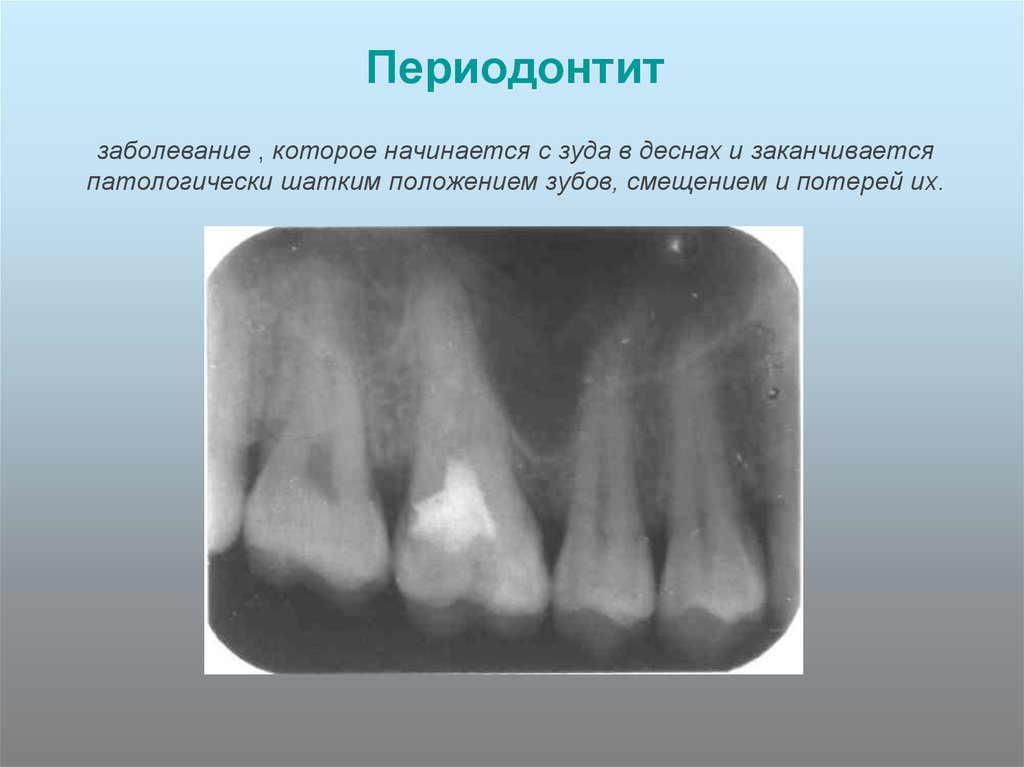 Показатели излечения от инфекций у пациентов с ХГБ очень высоки и значительно улучшаются благодаря ранней диагностике и терапии.
Показатели излечения от инфекций у пациентов с ХГБ очень высоки и значительно улучшаются благодаря ранней диагностике и терапии.
Одним из самых сложных аспектов ХГБ являются проблемы с кишечником. Примерно у 40-50% пациентов с ХГБ развивается воспаление в кишечнике, не являющееся явно следствием специфической инфекции. Это воспаление может быть ошибочно диагностировано как болезнь Крона, и оно очень похоже на нее. Он также отвечает на большинство тех же методов лечения (антибиотики, стероиды, другие препараты, подавляющие иммунитет). Однако инъекционные препараты, блокирующие воспалительную молекулу фактора некроза опухоли альфа (TNFα), которые очень эффективны при болезни Крона, приводят к тяжелым инфекциям у пациентов с ХГБ, и их следует избегать. Аналогичные проблемы могут возникать в мочевом пузыре или мочеточниках, вызывая проблемы с мочеиспусканием.
Диагностика хронической гранулематозной болезни
Существует пять различных генетических видов ХГБ. Наиболее распространенная форма называется Х-сцепленной, потому что она находится на Х-хромосоме (70% случаев в США) и поражает почти только мальчиков. Однако остальные четыре типа расположены на других хромосомах и имеют аутосомно-рецессивное наследование. Эти формы одинаково поражают мальчиков и девочек, поэтому около 15% случаев приходится на девочек. При Х-сцепленной форме заболевают мальчики, в то время как девочки являются относительно бессимптомными носителями. (См. главу «Наследование»).
Однако остальные четыре типа расположены на других хромосомах и имеют аутосомно-рецессивное наследование. Эти формы одинаково поражают мальчиков и девочек, поэтому около 15% случаев приходится на девочек. При Х-сцепленной форме заболевают мальчики, в то время как девочки являются относительно бессимптомными носителями. (См. главу «Наследование»).
Тяжесть ХГБ можно частично определить по конкретной мутации в гене. Обычно инфекции начинаются в детстве, что приводит к установлению диагноза. Однако у некоторых пациентов с ХГБ инфекция может отсутствовать до позднего подросткового или взрослого возраста. Педиатры и терапевты не могут игнорировать возможность ХГБ у взрослых с пневмонией с характерным для ХГБ возбудителем. Таким образом, любой пациент любого возраста с инфекцией типа ХГБ ( Staphylococcus aureus , Burkholderia cepacia complex , Serratia marcescens , Nocardia и Aspergillus ) должны быть протестированы на ХГД, если нет веской причины не делать этого.
Самый точный тест на ХГБ измеряет перекись водорода в фагоцитах с использованием химического вещества под названием дигидрородамин. Тест называется восстановлением дигидрородамина или DHR. Существуют и другие типы тестов, которые до сих пор используются для диагностики ХГБ, например, слайд-тест нитросинего тетразолия (NBT). Тест NBT по-прежнему ценен, но более подвержен неправильным показаниям.
После постановки диагноза ХГБ полезно подтвердить генетический подтип ХГБ для генетического консультирования, а также потому, что некоторые типы ХГБ нуждаются в трансплантации костного мозга больше, чем другие.
Лечение хронической гранулематозной болезни
Ранняя диагностика инфекции и быстрое агрессивное применение соответствующих антибиотиков — лучший способ лечения инфекций ХГБ. Начальная терапия антибиотиками, направленная на обычных подозреваемых, имеет смысл в ожидании результатов посевов, но важно попытаться идентифицировать конкретную инфекцию, а не просто гадать все время. При серьезных инфекциях ХГБ могут потребоваться внутривенные антибиотики. Переливание фагоцитов иногда используется, когда инфекция особенно опасна для жизни.
При серьезных инфекциях ХГБ могут потребоваться внутривенные антибиотики. Переливание фагоцитов иногда используется, когда инфекция особенно опасна для жизни.
Все пациенты с ХГБ должны получать антибиотикопрофилактику (профилактику), обычно триметоприм/сульфаметоксазол ( котримоксазол , бактрим или септра ) и итраконазол. Они уменьшают инфекции почти на 70%. Поскольку инфекции, важные для ХГБ, находятся в окружающей среде и обычно не переносятся в нашем организме, эффект профилактики заключается в том, чтобы построить стену вокруг пациента: ее все еще можно перепрыгнуть, но профилактика затрудняет проникновение инфекций. , Это также означает, что организмы, которые являются проблемой, обычно не воспринимают антибиотики, поэтому у них не развивается резистентность.
Ежедневные дозы перорального противогрибкового препарата итраконазол уменьшают грибковые инфекции при ХГБ. Максимальная профилактика инфекций при ХГБ включает лечение пероральными дозами котримоксазола два раза в день и итраконазола один раз в день плюс инъекции гамма-интерферона три раза в неделю.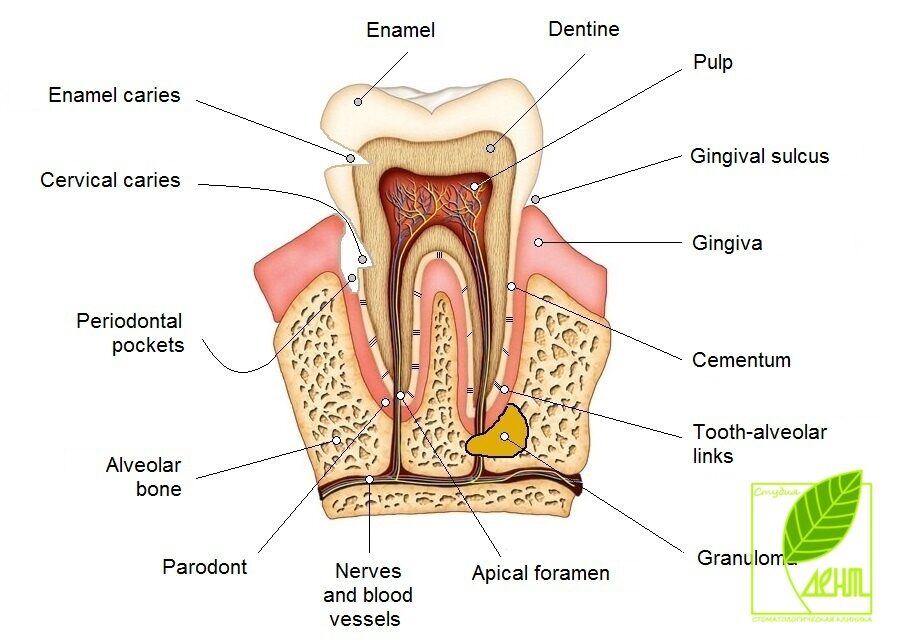 При таком профилактическом лечении средняя частота тяжелых инфекций при ХГБ составляет менее одного раза в четыре года. Конечно, на эту частоту будут влиять и индивидуальные факторы.
При таком профилактическом лечении средняя частота тяжелых инфекций при ХГБ составляет менее одного раза в четыре года. Конечно, на эту частоту будут влиять и индивидуальные факторы.
Гамма-интерферон обычно вырабатывается организмом, но его также можно вводить в виде инъекций для повышения иммунитета. Пациенты с ХГБ, получающие гамма-интерферон (под кожу три раза в неделю), имеют на 70% меньше инфекций, а если инфекции все же возникают, они могут быть менее серьезными. Гамма-интерферон не является лекарством от ХГБ. Это может вызвать лихорадку, усталость и депрессию. Может помочь прием ацетаминофена (тайленола) перед инъекцией. Некоторые пациенты предпочитают не принимать гамма-интерферон, потому что им не нравятся инъекции, из-за стоимости или из-за побочных эффектов. Даже дозы ниже стандартной рекомендации могут обеспечить некоторую защиту от инфекции. Побочные эффекты обычно связаны с дозой и могут быть уменьшены за счет снижения дозы или частоты приема.
Трансплантация гемопоэтических стволовых клеток может быть излечивающим методом лечения ХГБ, но она сложна и еще не широко доступна.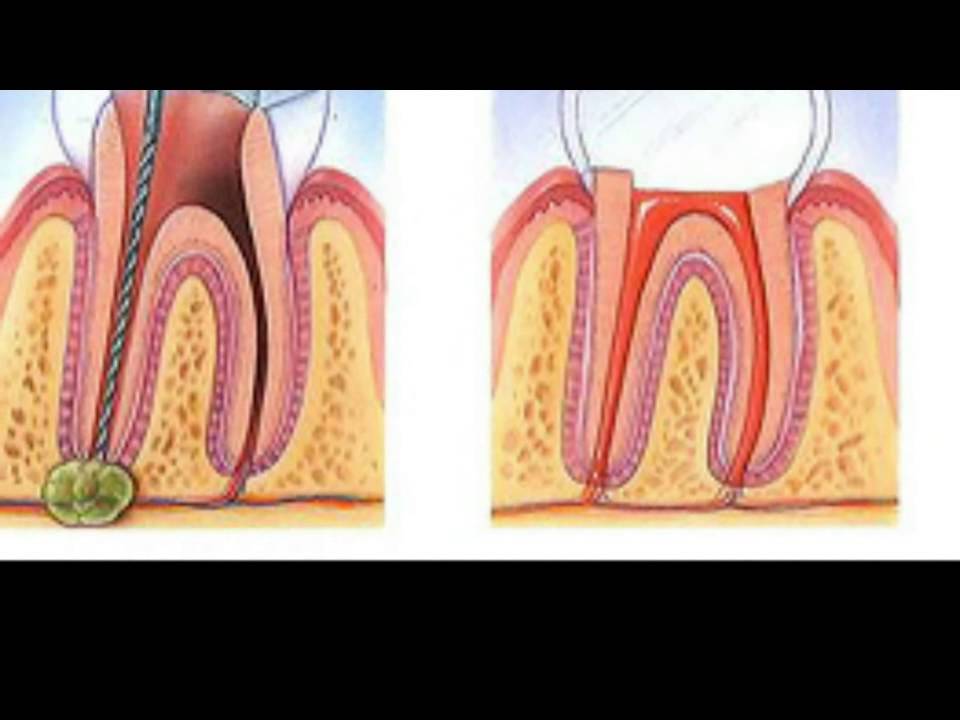 У пациентов может не быть полностью совместимого нормального брата или сестры, или они могут чувствовать себя достаточно хорошо при нормальном лечении, поэтому они не хотят трансплантацию. Тем не менее, у некоторых пациентов с ХГБ есть хорошие варианты трансплантации, и они могут захотеть изучить это. При правильном доноре и здоровом пациенте трансплантация костного мозга может быть очень эффективной. Генная терапия пока не является средством лечения ХГБ. Однако некоторые лаборатории работают над этой новой терапией, и генная терапия может стать вариантом в будущем.
У пациентов может не быть полностью совместимого нормального брата или сестры, или они могут чувствовать себя достаточно хорошо при нормальном лечении, поэтому они не хотят трансплантацию. Тем не менее, у некоторых пациентов с ХГБ есть хорошие варианты трансплантации, и они могут захотеть изучить это. При правильном доноре и здоровом пациенте трансплантация костного мозга может быть очень эффективной. Генная терапия пока не является средством лечения ХГБ. Однако некоторые лаборатории работают над этой новой терапией, и генная терапия может стать вариантом в будущем.
Многие врачи советуют плавать только в хорошо хлорированных бассейнах. В частности, солоноватая вода может подвергать пациентов воздействию организмов, которые особенно опасны при ХГБ ( Francisella philomiragia , Chromobacterium violaceum ). Аспергиллы присутствуют во многих образцах марихуаны, поэтому пациентам с ХГБ следует избегать их употребления.
Основной риск для пациентов с ХГБ связан с обращением с садовой мульчей (измельченной заплесневелой корой деревьев) или почвой для горшков. Этот тип воздействия может вызвать тяжелую опасную для жизни пневмонию из-за вдыхания грибка Aspergillus, который любит жить в разлагающихся растительных остатках. Пациенты с ХГБ должны оставаться в помещении во время мульчирования в соседних дворах. Когда мульча плотно прилегает к земле и не разбрасывается и не сгребается, она представляет гораздо меньшую опасность для пациентов с ХГБ. Пациентам следует избегать переворачивания навозных или компостных куч, пересадки комнатных растений, уборки подвалов или гаражей, удаления ковров, проведения сноса, копания в грязи, пыльных условиях, стрижки травы, сгребания листьев, сеновалов и сараев. Пациенты должны обращаться к своим врачам даже по поводу незначительных инфекций.
Этот тип воздействия может вызвать тяжелую опасную для жизни пневмонию из-за вдыхания грибка Aspergillus, который любит жить в разлагающихся растительных остатках. Пациенты с ХГБ должны оставаться в помещении во время мульчирования в соседних дворах. Когда мульча плотно прилегает к земле и не разбрасывается и не сгребается, она представляет гораздо меньшую опасность для пациентов с ХГБ. Пациентам следует избегать переворачивания навозных или компостных куч, пересадки комнатных растений, уборки подвалов или гаражей, удаления ковров, проведения сноса, копания в грязи, пыльных условиях, стрижки травы, сгребания листьев, сеновалов и сараев. Пациенты должны обращаться к своим врачам даже по поводу незначительных инфекций.
Ожидания для пациентов с хронической гранулематозной болезнью
Качество жизни и продолжительность жизни пациентов с ХГБ значительно улучшились за последние 50 лет. Подавляющее большинство детей с ХГБ могут рассчитывать на то, что они доживут до зрелого возраста, и многие взрослые пациенты с ХГБ работают, вступают в брак и рожают детей. Однако пациенты с ХГБ остаются в группе значительного риска инфицирования на протяжении всей жизни. Они должны принимать профилактические меры, сохранять осторожность и получать раннюю диагностику и лечение возможных инфекций. Пациентам с ХГБ может потребоваться госпитализация для определения очагов и причин инфекций. При серьезных инфекциях могут потребоваться внутривенные антибиотики. Профилактические антибиотики и лечение гамма-интерфероном увеличивают периоды здоровой жизни. Подавляющее большинство пациентов достигают зрелого возраста, когда серьезные инфекции, как правило, возникают реже.
Однако пациенты с ХГБ остаются в группе значительного риска инфицирования на протяжении всей жизни. Они должны принимать профилактические меры, сохранять осторожность и получать раннюю диагностику и лечение возможных инфекций. Пациентам с ХГБ может потребоваться госпитализация для определения очагов и причин инфекций. При серьезных инфекциях могут потребоваться внутривенные антибиотики. Профилактические антибиотики и лечение гамма-интерфероном увеличивают периоды здоровой жизни. Подавляющее большинство пациентов достигают зрелого возраста, когда серьезные инфекции, как правило, возникают реже.
Другие нарушения фагоцитарной функции
Основными фагоцитирующими лейкоцитами являются полиморфноядерные гранулоциты (PMN, также известные как нейтрофилы). Чтобы быть эффективным, нейтрофил должен переместиться к месту инфекции, проглотить организм и затем убить организм. (См. главу « Иммунная система и первичные иммунодефициты ».)
Нейтропении
более 2000 клеток/мкл). В зависимости от тяжести и продолжительности нейтропения может привести к серьезной и фатальной инфекции или перемежающейся инфекции кожи, слизистых оболочек, костей, лимфатических узлов, печени, селезенки или кровотока (сепсис).
В зависимости от тяжести и продолжительности нейтропения может привести к серьезной и фатальной инфекции или перемежающейся инфекции кожи, слизистых оболочек, костей, лимфатических узлов, печени, селезенки или кровотока (сепсис).
Нейтропения может возникать при рождении и сохраняться на протяжении всей жизни. Одна форма, называемая тяжелой врожденной нейтропенией (синдром Костмана), является аутосомно-рецессивным заболеванием. Это расстройство связано с аномалией гена HAX1 . Эти дети нуждаются в лечении гранулоцитарным колониестимулирующим фактором (Г-КСФ) и могут быть кандидатами на трансплантацию костного мозга.
Другой формой нейтропении является циклическая нейтропения, которая представляет собой аутосомно-доминантное заболевание, при котором нейтропения возникает каждые две-четыре недели и длится около недели. Это связано с дефектом гена, называемым ЭЛА2 .
Третья форма, доброкачественная хроническая нейтропения, имеет низкую, но не опасную для жизни нейтропению и часто протекает бессимптомно. Последней формой является иммунная нейтропения, обычно присутствующая при рождении, но иногда проявляющаяся позже. В этом состоянии есть антитела к нейтрофилам, которые вызывают их разрушение. Лечение всех этих заболеваний может включать антибиотики для лечения инфекций, профилактические антибиотики, внутривенное введение иммуноглобулина, инъекции G-CSF или трансплантацию костного мозга.
Последней формой является иммунная нейтропения, обычно присутствующая при рождении, но иногда проявляющаяся позже. В этом состоянии есть антитела к нейтрофилам, которые вызывают их разрушение. Лечение всех этих заболеваний может включать антибиотики для лечения инфекций, профилактические антибиотики, внутривенное введение иммуноглобулина, инъекции G-CSF или трансплантацию костного мозга.
Некоторые первичные иммунодефициты могут сопровождаться нейтропенией. Эти иммунодефициты включают Х-сцепленный синдром гипер-IgM (дефицит лиганда CD40), общий вариабельный иммунодефицит (CVID), Х-сцепленную агаммаглобулинемию (XLA), синдром WHIM, синдром Вискотта-Олдрича и дефицит GATA2. Некоторые из этих пациентов приобретают аутоиммунные антитела к собственным нейтрофилам. Это антитело вызывает аутоиммунную нейтропению из-за ускоренного разрушения нейтрофилов. Все эти болезни более подробно обсуждаются в других главах настоящего Справочника.
Дефекты, убивающие фагоциты
Некоторые редкие дефекты фагоцитов связаны с неспособностью убивать микроорганизмы, как у пациентов с ХГБ. Их следует заподозрить у пациентов с подозрением на ХГБ, но тесты на это заболевание в норме. К ним относятся дефекты ферментов или недостаточность глюкозо-6-фосфатдегидрогеназы, миелопероксидазы, глутатионредуктазы и глутатионсинтетазы.
Их следует заподозрить у пациентов с подозрением на ХГБ, но тесты на это заболевание в норме. К ним относятся дефекты ферментов или недостаточность глюкозо-6-фосфатдегидрогеназы, миелопероксидазы, глутатионредуктазы и глутатионсинтетазы.
Дефицит адгезии лейкоцитов
Для проникновения нейтрофилов в ткани и удаления захватчиков они должны иметь возможность покинуть кровеносные сосуды и проникнуть в ткани. Этот процесс сложен, и существует несколько специфических дефектов, нарушающих его. Дефицит адгезии лейкоцитов типа I (LAD1) является результатом мутаций в гене CD18. LAD1, безусловно, является наиболее распространенной причиной недостаточности адгезии лейкоцитов, и ее обычно устраняют трансплантацией костного мозга. Однако более легкие формы LAD1 иногда можно лечить только антибиотиками. Дефицит адгезии лейкоцитов типа II (LAD2) возникает из-за мутаций в ферменте, который прикрепляет фукозу (разновидность сахара) к белкам. Этих пациентов можно лечить, употребляя большое количество фукозы. Дефицит адгезии лейкоцитов III типа (LAD3) вызывается мутациями в гене 9.0037 ФЕРМТ3 .
Дефицит адгезии лейкоцитов III типа (LAD3) вызывается мутациями в гене 9.0037 ФЕРМТ3 .
Дефицит специфических гранул
Дефицит специфических гранул встречается крайне редко и связан с дефектами киллинга и уменьшением количества гранул в нейтрофилах. Пациенты подвержены риску бактериальных и грибковых инфекций.
Болезнь накопления гликогена типа Ib
Болезнь накопления гликогена типа Ib представляет собой заболевание с нейтропенией, плохим уничтожением гранулоцитов, большой печенью и низким уровнем сахара в крови. Это связано с дефектом фермента переносчика глюкозо-6-фосфата 1 с накоплением гликогена в печени.
Дефицит β-актина
Дефицит β-актина связан с нарушением движения гранулоцитов (хемотаксис) и рецидивирующей инфекцией. β-актин является структурным белком, обеспечивающим движение клеток. Некоторые пациенты с хемотаксическими нарушениями имеют тяжелый пародонтит и раннюю потерю зубов. Три из этих синдромов называются синдромом Папийона-Лефебра, препубертатным пародонтитом и ювенильным пародонтитом.
Chediak Higashi
Синдром Чедиака-Хигаси (CHS) — редкое аутосомно-рецессивное заболевание, возникающее в результате дефекта полимеризации микротрубочек. CHS — это заболевание, вызывающее нарушение уничтожения бактерий из-за нарушения образования фаголизосом. В фагосомах нарушена дегрануляция лизосом, поэтому фагоцитированные бактерии не разрушаются ферментами лизосом. Характерны гигантские гранулы внутри нейтрофилов. Кроме того, нарушается секреция литических секреторных гранул цитотоксическими Т-клетками. Люди с CHS имеют частичный альбинизм (светлая кожа и серебристые волосы) и имеют проблемы с чувствительностью к солнцу и светобоязнью. Другие признаки и симптомы значительно различаются, но распространены частые инфекции и невропатия. Инфекции поражают слизистые оболочки, кожу и дыхательные пути. Больные дети восприимчивы к инфекции грамположительными и грамотрицательными бактериями и грибами, с Staphylococcus aureus выделяется. Большинство детей с CHS в конечном итоге достигают стадии, известной как ускоренная фаза, также известная как лимфомоподобный синдром.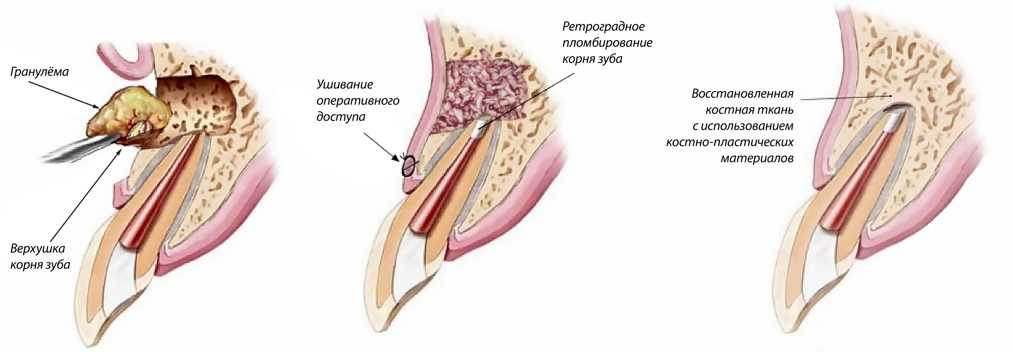 Эта тяжелая фаза заболевания может быть вызвана вирусной инфекцией, обычно вирусом Эпштейна-Барра (ВЭБ). В ускоренной фазе дефектные лейкоциты бесконтрольно делятся и проникают во многие органы тела. Ускоренная фаза связана с лихорадкой, эпизодами аномального кровотечения, распространенными инфекциями и недостаточностью органов. Эти медицинские проблемы обычно опасны для жизни в детстве. Специфического лечения СГС не существует. Трансплантация костного мозга, по-видимому, была успешной у нескольких пациентов. Инфекции лечат антибиотиками, а абсцессы при необходимости дренируют хирургическим путем.
Эта тяжелая фаза заболевания может быть вызвана вирусной инфекцией, обычно вирусом Эпштейна-Барра (ВЭБ). В ускоренной фазе дефектные лейкоциты бесконтрольно делятся и проникают во многие органы тела. Ускоренная фаза связана с лихорадкой, эпизодами аномального кровотечения, распространенными инфекциями и недостаточностью органов. Эти медицинские проблемы обычно опасны для жизни в детстве. Специфического лечения СГС не существует. Трансплантация костного мозга, по-видимому, была успешной у нескольких пациентов. Инфекции лечат антибиотиками, а абсцессы при необходимости дренируют хирургическим путем.
Синдром Гришелли
Синдром Гришелли (СГ) является редким аутосомно-рецессивным заболеванием, которое приводит к разбавлению пигмента кожи и волос, наличию больших скоплений пигмента в волосяных стержнях и накоплению меланосом в меланоцитах. Существует три различных формы СГ, каждая из которых вызвана различным генным дефектом, и только СГ типа 2 (вызванный мутацией в гене RAB27A) является первичным иммунодефицитом. Griscelli описал детей с расстройством, напоминающим CHS. Характерны частичный альбинизм, частые гнойные инфекции и острые эпизоды лихорадки, нейтропении и тромбоцитопении. Несмотря на достаточное количество Т- и В-лимфоцитов, пациенты страдали гипогаммаглобулинемией, дефицитом продукции антител и неспособны к отсроченной гиперчувствительности кожи и отторжению кожного трансплантата. Отличия от CHS заключались в морфологической нормальности полиморфноядерных лейкоцитов; гигантские гранулы ХС не обнаружены. Морфологические характеристики гипопигментации также отличают заболевание от CHS, а также от других пигментных аномалий человека. Другим отличием была нормальная активность специфической протеазы лейкоцитов, которая очень низка при CHS. СГ с частичным альбинизмом и нарушением иммунитета (теперь называемый СГ типа 2) представляет собой серьезное иммунодефицитное заболевание, при котором у многих пациентов развивается гемофагоцитарный синдром, потенциально приводящий к смерти в отсутствие трансплантации костного мозга.
Griscelli описал детей с расстройством, напоминающим CHS. Характерны частичный альбинизм, частые гнойные инфекции и острые эпизоды лихорадки, нейтропении и тромбоцитопении. Несмотря на достаточное количество Т- и В-лимфоцитов, пациенты страдали гипогаммаглобулинемией, дефицитом продукции антител и неспособны к отсроченной гиперчувствительности кожи и отторжению кожного трансплантата. Отличия от CHS заключались в морфологической нормальности полиморфноядерных лейкоцитов; гигантские гранулы ХС не обнаружены. Морфологические характеристики гипопигментации также отличают заболевание от CHS, а также от других пигментных аномалий человека. Другим отличием была нормальная активность специфической протеазы лейкоцитов, которая очень низка при CHS. СГ с частичным альбинизмом и нарушением иммунитета (теперь называемый СГ типа 2) представляет собой серьезное иммунодефицитное заболевание, при котором у многих пациентов развивается гемофагоцитарный синдром, потенциально приводящий к смерти в отсутствие трансплантации костного мозга.
