Лечение гнойных ран с применением раневых покрытий на пенной основе с технологией Гидрофайбер
Наличие в структуре больных хирургических стационаров большого числа пациентов с гнойными заболеваниями мягких тканей позволяет отнести данную проблему в разряд важнейших в современной хирургии. По данным различных авторов, доля пациентов хирургического профиля с гнойной патологией составляет от 15 до 40%. До 30% в структуре смертности после хирургических вмешательств составляют гнойные осложнения [1, 2].
Значительные материальные затраты на лечение этой категории пациентов переводят проблему из разряда медицинских в разряд социально-экономических. Быстрое развитие устойчивости патогенной микрофлоры к антибактериальным препаратам и смена возбудителя раневой инфекции в процессе лечения, в том числе инфицирование госпитальной флорой, выводит на первый план необходимость тщательного выбора способа местного лечения инфицированных ран [3, 4]. В настоящее время существует множество данных о большом количестве методов позволяющих улучшить результаты лечения гнойных ран и снизить риск гнойных послеоперационных осложнений [3—7].
Большая роль в решении данного вопроса отводится современным перевязочным средствам и раневым покрытиям, которые обладают широким спектром воздействия на рану. Они не только обеспечивают механическую защиту раны, но и подавляют патогенную микрофлору, обладают противовоспалительным, обезболивающим эффектом, обеспечивают адекватный отток экссудата, тем самым снижая бактериальную обсемененность, создают оптимальную среду для быстрого очищения и стимулируют процессы заживления в ране. Абсолютно понятно, что традиционные перевязочные материалы не удовлетворяют данным требованиям [8]. Несомненно, важным фактором в процессе лечения также является удобство применения раневого покрытия как для врача, так и для пациента. Раневое покрытие должно быть эстетически приятным и в минимальной степени ограничивать повседневную активность, сохраняя привычное качество жизни пациента, что особенно важно для людей молодого и трудоспособного возраста.
Цель исследования — оценка эффективности современных подходов к лечению гнойных ран с применением раневых покрытий на пенной основе с технологией Гидрофайбер в сравнении с традиционным методом ведения ран.
Материал и методы
Провели анализ результатов лечения 34 пациентов с гнойными ранами различной этиологии, которые находились на лечении в клинике госпитальной хирургии ГБОУ ВПО «Самарский государственный медицинский университет» с августа по декабрь 2017 г. Пациенты были разделены на две группы: контрольную и основную. В основной группе местное лечение ран проводилось с применением раневого покрытия на пенной основе с технологией Гидрофайбер. Повязка, созданная по данной технологии, при контакте с экссудатом принимает гелеобразную консистенцию, абсорбирует и удерживает непосредственно внутри волокон значительное количество раневого экссудата и бактерии. В контрольной группе местное лечение ран проводилось с помощью традиционной методики с применением марлевых мазевых повязок.
Значимость различий количественных данных оценивали с использованием t-критерия Стьюдента, при оценке различия долей использовали критерий χ2. Критическое значение уровня значимости принималось равным 5% (р≤0,05).
Критическое значение уровня значимости принималось равным 5% (р≤0,05).
Критериями включения в исследование являлись: возраст пациентов от 16 до 65 лет; наличие гнойной раны мягких тканей, в том числе после оперативного лечения — вскрытия гнойных очагов
Критериями исключения служили: гнойные осложнения оперативных вмешательств; возраст до 16 лет, и более 65 лет; септические состояния; иммунодефицитные состояния (в том числе ВИЧ инфекция).
В зависимости от локализации и распространенности гнойного процесса пациенты основной и контрольной групп распределены следующим образом (табл. 1).
Таблица 1. Распределение пациентов по локализации и виду гнойного очага (n=34)
Из табл. 1 видно, что преобладают пациенты с абсцессами мягких тканей (44% от общего числа пациентов).
В основную группу вошли 17 пациентов: 10 (58,8%) женщин и 7 (41,2%) мужчин, средний возраст 31,1 года. Пациенты в возрасте от 16 до 35 лет составили 76,5% (n=13), от 36 до 60 лет — 23,5% (n=4).
В контрольную групу вошли 17 больных: 11 (64,7%) женщин и 6 (35,3%) мужчин, средний возраст 30,2 года. Пациенты в возрасте от 16 до 35 лет составили 82,4% (n
Таким образом, статистически значимых различий в группах по полу (χ2=0,73) и возрасту (χ2=1,06) не выявлено (p≥0,05).
Средний уровень лейкоцитов крови при поступлении в основной группе 12,1±0,8 тыс. в 1 мм3, в контрольной группе 12,4±0,7 тыс. в 1 мм3. Статистически значимой разницы в этих показателях не обнаружено (t=1,17, df =32, р≥0,05).
У всех пациентов на первом этапе проводилось адекватное хирургическое пособие, заключающееся во вскрытии и дренировании гнойного очага, хирургической обработке раны, удалении некротических тканей, промывании раны раствором антисептика. Оперативное вмешательство в основной группе заканчивалось наложением современного раневого покрытия на пенной основе с применением технологии Гидрофайбер, а в контрольной группе — традиционной марлевой повязки с мазью на основе полиэтиленгликоля (левомеколь).
Смена повязки проводилась в срок от 2 до 5 сут по мере накопления отделяемого в повязке в основной группе и ежедневно — в контрольной.
Эффективность лечения оценивалась: по наличию клинических симптомов (температурная реакция организма, наличие отека и гиперемии вокруг раны, динамика очищения ран от гноя и фибрина), по динамике лабораторных показателей (количество лейкоцитов крови), по результатам микробиологического мониторинга (видовой и количественный состав флоры, чувствительность к антибактериальным препаратам).
Результаты и обсуждение
Температура тела и общее самочувствие нормализовались в основной группе на 2-е сутки (1,8±0,2), а в группе сравнения на 3—4-е сутки (2,9±0,4) (t=10,6, р<0,05).
Отсутствие отека мягких тканей и гиперемии кожного покрова вокруг раны отмечалось в основной группе в среднем к 4,2±1,8 суток, в контрольной к 5,4±2,6 суток (

На 3-е сутки средний уровень лейкоцитов крови в основной группе составил 7,2±0,4 тыс. в 1 мм3, в контрольной группе — 8,1±0,3 тыс. в 1 мм3 (t=8,18, р<0,05).
Таким образом, выявлены достоверные статистические различия в скорости стихания воспалительных явлений в основной и контрольной группах. Эти данные свидетельствуют о более выраженной динамике нормализации температурной реакции, снижения местной воспалительной реакции и уровня лейкоцитоза у пациентов основной группы.
Стерильный посев из раны на 5-е сутки в основной группе отмечен у 41,1% пациентов, в контрольной группе — только у 5,9%. В основной группе снижение бактериальной контаминации на 50% отмечено у 58,9% пациентов, а в основной — у 47,1%. Стерильный посев из раны в основной группе у 88,2% отмечен только на 10-е сутки. Также в основной группе отмечено более быстрое очищение раны от гноя и фибрина и появление грануляционной ткани (табл. 2).
Таблица 2. Показания эффективности лечения в основной и контрольной группах
Показания эффективности лечения в основной и контрольной группах
Достоверные статистические различия между группами выявлены: по динамике очищения раны (χ2=14,7, p<0,05), по динамике деконтаминации раны (χ2=14,4, p<0,05), по снижению контаминации на 50% к 5-м суткам (χ
В большинстве случаев видовой состав флоры как в группе исследования, так и в группе сравнения был представлен монокультурой S. aureus.
В 11,8% случаях видовой состав флоры был представлен ассоциацией из 2 микроорганизмов (S. aureus в сочетании с S. Epidtrmidis, S. aureus в сочетании с E. coli) (табл. 3).
Таблица 3. Микрофлора, высеянная из гнойной полости у больных основной и контрольной групп при первичном микробиологическом исследовании
У 3 (17,6%) пациентов из контрольной группы на 5-е сутки произошла смена видового состава возбудителя. Во всех случаях в посеве обнаруживалась E. coli, что потребовало коррекции антибактериальной терапии. В основной группе вторичного инфицирования ран не отмечалось, что можно связать с меньшим количеством перевязок и более выраженным антибактериальным эффектом раневого покрытия.
Во всех случаях в посеве обнаруживалась E. coli, что потребовало коррекции антибактериальной терапии. В основной группе вторичного инфицирования ран не отмечалось, что можно связать с меньшим количеством перевязок и более выраженным антибактериальным эффектом раневого покрытия.
Во всех случаях применения раневых покрытий пациенты основной группы отмечали удобство в использовании повязок, особенно возможность принимать душ, не боясь отклеивания повязки и попадания воды на рану, эстетичный внешний вид.
Клинические примеры
1. Пациентка Т., 47 лет, госпитализирована в хирургическое отделение с диагнозом: инфицированная рана голени. В анамнезе бытовая травма. В течение недели лечилась у хирурга поликлиники. Проводились перевязки, пероральный прием антибиотиков. Динамика отрицательная. При осмотре, в средней трети голени рана 4×2 см, глубиной до 2 см, с гнойным отделяемым.
Рис. 1. 1-е сутки, вид раны. Посев: S. Aureus 104.
Проводилась антибактериальная терапия (рис. 2). Раневое покрытие снято на 5-е сутки. Взят посев на флору. Отека и гиперемии нет. Раневой дефект уменьшился в размерах, покрыт грануляционной тканью (рис. 3). Нормализовалась температура тела и показатели общего анализа крови. Пациентка выписана на амбулаторное долечивание.
Рис. 2. Вид раны с наложенной повязкой.
Рис. 3. Вид раны на 5-е сутки. Посев стерилен.
2. Больная Т., 18 лет. Диагноз: постинъекционный абсцесс ягодичной области. При оперативном лечении эвакуировано около 20 мл густого гноя (рис. 4, 5, 6).
Рис. 4. Вид раны после вскрытия и дренирования гнойной полости. Посев из раны: Staphylococcusaureus 104.
Рис. 5. Наложена повязка.
Рис. 6. Вид раны на 5-е сутки. Посев из раны. Роста микрофлоры не выявлено. Рана с явлениями грануляции. Отека и гиперемии вокруг раны нет. Гнойного отделяемого нет. Рана уменьшилась в размерах.
Рана с явлениями грануляции. Отека и гиперемии вокруг раны нет. Гнойного отделяемого нет. Рана уменьшилась в размерах.
Применение современных раневых покрытий на пенной основе с технологии Гидрофайбер позволяет улучшить результаты лечения пациентов с гнойными ранами различной этиологии. По нашим данным, при использовании повязок с технологией Гидрофайбер статистически достоверно отмечается более быстрое купирование воспалительного процесса в ране и окружающих тканях, достоверно уменьшаются сроки очищения и микробной деконтаминации в гнойном очаге.
Возможность увеличения времени между перевязками при применении современных раневых покрытий с технологией Гидрофайбер, а также их антибактериальный эффект способствуют снижению риска вторичного инфицирования раны госпитальными штаммами микроорганизмов.
Применение современных раневых покрытий на пенной основе с технологией Гидрофайбер позволяет снизить сроки госпитализации, что сокращает затраты на стационарное лечение данной группы пациентов.
Пациенты основной группы отмечали удобство и приятный внешний вид повязок и возможность полноценного проведения гигиенических процедур в сравнении с пациентами контрольной группы, у которых применялся стандартный перевязочный материал, возможность полноценного проведения гигиенических процедур.
Авторы заявляют об отсутствии конфликта интересов.
Лечение гнойно-воспалительных процессов | MAJOR CLINIC
Вскрытие фурункула
Фурункул — поражение волосяного фолликула стафилококковой или стрептококковой природы. Может быть самостоятельным заболеванием и осложнением стафилодермии. Часто развивается у людей с ослабленным иммунитетом. Заболевание обладает выраженной стадийностью:
- стадия инфильтрации — поражённый фолликул краснеет и несколько приподнимается над кожей;
- гнойный фурункул образуется на третьи-четвертые сутки, когда достигает диаметра 1-3 см, а внутри формируется гнойно-некротический стержень;
- стадия заживления наступает после вскрытия фурункула.

Фурункул в стадии нагноения очень болезненный, возможно появление общей реакции в виде гипертермии, слабости, недомогания. Быстро помочь помогает хирургическое вскрытие нагноившегося фурункула с обеспечением оттока содержимого, применением местных антибактериальных средств.
Вскрытие карбункула
Карбункулом называется группа рядом расположенных фурункулов. Заболевание сопровождается высокой температурой и слабостью. Время созревания составляет 10-14 дней и всё это время он доставляет больному ужасные мучения. После вскрытия остаётся глубокая рана, которая у детей и ослабленных пациентов может достигать мышечного слоя.
Карбункул требует качественной хирургической помощи. Его вскрывают и тщательно дренируют. Назначают антисептические, антибактериальные и другие средства.
Вскрытие абсцесса
Абсцесс (в переводе с латинского «нарыв») — гнойное расплавление тканей с образованием полости. Может развиться в любых органах и тканях: подкожно-жировой клетчатке, мышцах, внутренних органах, костях. От других гнойно-воспалительных заболеваний он отличается наличием пиогенной мембраны, ограничивающей абсцедирующую полость.
От других гнойно-воспалительных заболеваний он отличается наличием пиогенной мембраны, ограничивающей абсцедирующую полость.
Симптомы абсцесса:
- местные — покраснение, боль, припухлость;
- общие — гипертермия, слабость, головная боль, тошнота, отсутствие аппетита.
Отдельные виды патологии
Абсцесс ягодицы развивается в результате неправильно проведенной внутримышечной инъекции (обычно непрофессионалами в домашних условиях). Вскрытие гнойной полости абсцесса — единственный метод эффективной помощи пациенту.
Абсцессом может закончиться бартолинит — воспаление бартолиновой железы, расположенной в преддверии влагалища. При этом женщина испытывает такие боли, что не может сделать даже шаг. Экстренное вскрытие абсцесса бартолиновой железы быстро улучшает самочувствие, способствует полному выздоровлению.
Ещё Гиппократ говорил: «Увидел гной — вскрой!» В наше время дренирование абсцесса — необходимое условие для избавления от этого патологического состояния.
Лечение абсцесса терапевтическими методами невозможно. Если воспаление находится на стадии инфильтрации — можно попытаться остановить процесс назначением адекватной антибактериальной терапии. Если же появился гнойный мешок — абсцесс необходимо вскрыть. В противном случае высока вероятность развития системного поражения крови — сепсиса. А это уже смертельно опасное заболевание.
Лечение панариция на руке
Панариций — воспаление тканей дистальных (конечных) фаланг пальцев. Чаще поражает пальцы рук. Причиной заболевания становится проникновение инфекции под кожу вследствие мелких травм, порезов, царапин, уколов. Панариций на пальце причиняет боль и значительное неудобство. Справиться с ним эффективно помогает только оперативное вмешательство со вскрытием и дренированием гнойной полости.
Паронихий
Гнойное поражение затрагивающее околоногтевые ткани называется паронихием. Паронихий (или паронихия) возникают в ответ на травму ногтевого ложа. Причиной чаще всего становится неудачный маникюр, мелкие травмы и порезы. Кандидозная паронихия развивается при грибковом поражении тканей у ногтя. Это происходит в том случае, когда руки человека постоянно контактируют с водой. В группе риска повара и кондитеры, работники сельского хозяйства. Лечение паронихия должно начинаться как можно раньше, так как заболевание легко переходит в хроническую форму и избавиться от него становится тяжело.
Кандидозная паронихия развивается при грибковом поражении тканей у ногтя. Это происходит в том случае, когда руки человека постоянно контактируют с водой. В группе риска повара и кондитеры, работники сельского хозяйства. Лечение паронихия должно начинаться как можно раньше, так как заболевание легко переходит в хроническую форму и избавиться от него становится тяжело.
Лечение гидраденита
Гидраденит — воспаление потовых апокриновых желез в подмышечной области, у ануса, в паху и некоторых других местах. В народе заболевание называют «сучье вымя» за характерный конусообразный вид. Патология сопровождается выраженным болевым синдромом и склонна к рецидивированию. Поэтому при первых признаках болезни следует немедленно обратиться к хирургу и пройти полноценный курс лечения.
Обращайтесь в клинику MAJOR CLINIC
В нашей клинике используют современное оборудование и инструментарий, позволяющий аккуратно провести все необходимые манипуляции и обеспечить быстрое заживление ран. Применяются самые прогрессивные методики лечения гнойно-воспалительных заболеваний. Даются рекомендации по профилактике возникновения подобной патологии в будущем. Записаться на прием легко по телефону и на сайте.
Применяются самые прогрессивные методики лечения гнойно-воспалительных заболеваний. Даются рекомендации по профилактике возникновения подобной патологии в будущем. Записаться на прием легко по телефону и на сайте.
Хирургическое лечение гнойных ран при синдроме диабетической стопы – Республиканская клиническая больница МЗ РТ (РКБ РТ)
17.07.2017
Гнойные раны у диабетиков являются частым следствием синдрома диабетической стопы и представляют большую сложность в лечении, поскольку при наличии данного хронического заболевания невозможно лечить саму рану, не учитывая диагноза. Лечение таких пациентов, число которых растет с каждым годом, является одним из приоритетных направлений отделения гнойной хирургии ГАУЗ «РКБ МЗ РТ». Благодаря стратегии, основанной на комплексном мультидисциплинарном подходе, значительной части пациентов с осложнениями синдрома диабетической стопы удается избежать высокой ампутации либо сохранить конечность. Об опыте применения тактики комплексного лечения данной патологии у больных сахарным диабетом рассказал специалист отделения, врач-хирург высшей категории Ахунзянов Айрат Алмазович.
Об опыте применения тактики комплексного лечения данной патологии у больных сахарным диабетом рассказал специалист отделения, врач-хирург высшей категории Ахунзянов Айрат Алмазович.
— Что включает в себя комплексный подход к лечению осложнений у пациентов с синдромом диабетической стопы?
— Мультидисциплинарный подход к лечению таких пациентов в отделении гнойной хирургии РКБ сочетает хирургическое, эндокринологическое, ангиохирургическое, физиотерапевтическое и медикаментозное лечение. Так, при поступлении пациента в стационар проводится вскрытие и санирование гнойных ран, рентгеновское исследование стопы на предмет костной патологии и разрушения суставов, а также анализ крови для выявления воспалительных изменений; ведется ежедневная обработка раны; назначается антибиотикотерапия с целью купирования инфекции.
Важная составляющая комплексного лечения коррекция самого сахарного диабета. Поэтому пациенту четырехкратно в течение суток производится контроль уровня сахара в крови, под наблюдением эндокринолога проводится коррекция лечения диабета с учетом его рекомендаций. В обязательном порядке проводится ультразвуковая диагностика сосудов, а также, по показаниям, дистальная ангиография, причем нередко с одномоментной эндоваскулярной дилатацией. Пациенту также назначается лекарственная терапия, по выписке даются подробные рекомендации по лечению на дому и правильному бразу жизни.
В обязательном порядке проводится ультразвуковая диагностика сосудов, а также, по показаниям, дистальная ангиография, причем нередко с одномоментной эндоваскулярной дилатацией. Пациенту также назначается лекарственная терапия, по выписке даются подробные рекомендации по лечению на дому и правильному бразу жизни.
— Какие средства используются сегодня для местного лечения гнойных ран?
— Сегодня методы местного лечения вышли далеко за рамки привычных мазевых и водных повязок. Современный перевязочный материал дает огромные возможности, являясь, по сути, частью терапии. Так, серебросодержащие повязки с антибактериальными свойствами из полиамидной сетки, покрытой элементарным серебром, позволяют сохранять кожные трансплантаты при аутодермопластике; специальное серебряное покрытие предохраняет рану от инфицирования, и при перевязке не повреждается кожный лоскут. Повязки в форме подушечки, центральная составная часть которой содержит суперабсорбирующий полимер, увлажняющие рану и поглощающие при этом раневое отделяемое в течение 24 часов, хорошо зарекомендовали себя не только при диабетической стопе, но и при лечении пролежней, трофических язв. За счет этого ускоряется и облегчается процесс очистки раны, пациент лучше переносит перевязку, не испытывает болевых ощущений в ране. Специальные губчатые повязки, разработанные для лечения трофических язв и пролежней, способствуют сохранению микроклимата в ране, росту краевой эпителизации, ускоряют заживление (внутри них находится дренажный материал, также способный поглощать раневое отделяемое). При варикозной болезни, обширных некротических ранах применяются абсорбирующие альгинатные повязки для очистки глубоких ран, обладающие высокой сорбционной способностью благодаря волокнам альгината кальция. Такая повязка может оставаться на ране от суток до нескольких дней, обеспечивая ускоренное заживление раны. Современные достижения в области перевязочных материалов во многом облегчают работу хирургов, ускоряют получение позитивных результатов лечения, и мы рады, что в распоряжении наших хирургов имеются эти средства. Что касается препаратов для обработки ран, мы традиционно используем йодинол и хлоргексидин.
За счет этого ускоряется и облегчается процесс очистки раны, пациент лучше переносит перевязку, не испытывает болевых ощущений в ране. Специальные губчатые повязки, разработанные для лечения трофических язв и пролежней, способствуют сохранению микроклимата в ране, росту краевой эпителизации, ускоряют заживление (внутри них находится дренажный материал, также способный поглощать раневое отделяемое). При варикозной болезни, обширных некротических ранах применяются абсорбирующие альгинатные повязки для очистки глубоких ран, обладающие высокой сорбционной способностью благодаря волокнам альгината кальция. Такая повязка может оставаться на ране от суток до нескольких дней, обеспечивая ускоренное заживление раны. Современные достижения в области перевязочных материалов во многом облегчают работу хирургов, ускоряют получение позитивных результатов лечения, и мы рады, что в распоряжении наших хирургов имеются эти средства. Что касается препаратов для обработки ран, мы традиционно используем йодинол и хлоргексидин. По нашим многолетним наблюдениям, это самые оптимальные и безопасные препараты для местного лечения ран в случае гнойных поражений при диабетической стопе. Среди массы антисептических средств можно выделить бесспиртовой кожный антисептик «Октенисепт», который, воздействуя на разнообразную микрофлору, в том числе внутрибольничную, позволяет ликвидировать воспалительные процессы.
По нашим многолетним наблюдениям, это самые оптимальные и безопасные препараты для местного лечения ран в случае гнойных поражений при диабетической стопе. Среди массы антисептических средств можно выделить бесспиртовой кожный антисептик «Октенисепт», который, воздействуя на разнообразную микрофлору, в том числе внутрибольничную, позволяет ликвидировать воспалительные процессы.
— Какое место занимает в лечении больных физиотерапия?
— Вот уже практически пять лет мы используем метод вакуумной терапии. Каждая палата в отделении оборудована консолями Drager, также имеется аппарат Vivano фирмы Hartmann. Внедрив вакуумное лечение в повседневную работу отделения, мы стали получать хорошие результаты даже, казалось бы, в безвыходных ситуациях. Механизм действия вакуумной терапии сводится к тому, что происходит прерывистая вакуумная аспирация раневого отделяемого, что способствует росту грануляции и ускоряет сроки очищения ран. Конечная цель терапии – сохранение пациенту опорной конечности, и на фоне вакуумного лечения нам это стало удаваться чаще. Использование данной методики показало свою эффективность и при лечении длительно незаживающих пролежней, инфицированных послеоперационных ран и других. В ряде случаев лечение осуществляется совместно со специалистами Республиканского центра лазерной хирургии РКБ, который возглавляет профессор Д.М. Красильников. Для ускорения раневого процесса производится облучение раны инфракрасным лазером непосредственно во время перевязок. Это существенно ускоряет заживление раны.
Использование данной методики показало свою эффективность и при лечении длительно незаживающих пролежней, инфицированных послеоперационных ран и других. В ряде случаев лечение осуществляется совместно со специалистами Республиканского центра лазерной хирургии РКБ, который возглавляет профессор Д.М. Красильников. Для ускорения раневого процесса производится облучение раны инфракрасным лазером непосредственно во время перевязок. Это существенно ускоряет заживление раны.
— Каковы показания к проведению оперативных вмешательств: ампутации костных структур, сосудистой хирургии?
— Хирургическое лечение гнойных ран при диабетической стопе, как правило, требует вскрытия гной ных очагов. Если в зоне гнойного воспаления оказываются нежизнеспособные костные ткани (пальцы, суставы) или сухожилия, эти участки подлежат удалению. Также если у пациента развились гнойные осложнения, которые уже вышли за пределы стопы, например, гнойные затеки на голень, в подколенную область, и высока вероятность развития сепсиса, мы взвешиваем риски, оцениваем возможность развития генерализованной инфекции и потери самого пациента, принимая решение об органоуносящей операции. В целом при отсутствии грубых сосудистых нарушений в конечности прогноз обычно довольно благоприятный. Куда сложнее, если имеются выраженные ишемические изменения: облитерирующий атеросклероз или диабетическая микро- и макроангиопатия, при которой страдают как капилляры, так и берцовые артерии. В этом случае ввиду плохого кровоснабжения раневой процесс значительно замедляется, что нередко приводит к вторичному некрозу раны. Поэтому одной из составляющих комплексного лечения является сосудистая диагностика, определяющая показания к проведению реконструктивных сосудистых операций, в том числе баллонной ангиопластике, которые выполняются в отделении рентгенохирургических методов диагностики и лечения РКБ. Это необходимо для улучшения сосудистого кровотока, который обеспечивает ускорение раневых процессов: если есть сосудистые нарушения, то без проведения соответствующей коррекции местное хирургическое лечение не всегда может привести к положительному результату.
В целом при отсутствии грубых сосудистых нарушений в конечности прогноз обычно довольно благоприятный. Куда сложнее, если имеются выраженные ишемические изменения: облитерирующий атеросклероз или диабетическая микро- и макроангиопатия, при которой страдают как капилляры, так и берцовые артерии. В этом случае ввиду плохого кровоснабжения раневой процесс значительно замедляется, что нередко приводит к вторичному некрозу раны. Поэтому одной из составляющих комплексного лечения является сосудистая диагностика, определяющая показания к проведению реконструктивных сосудистых операций, в том числе баллонной ангиопластике, которые выполняются в отделении рентгенохирургических методов диагностики и лечения РКБ. Это необходимо для улучшения сосудистого кровотока, который обеспечивает ускорение раневых процессов: если есть сосудистые нарушения, то без проведения соответствующей коррекции местное хирургическое лечение не всегда может привести к положительному результату.
— Какие рекомендации получает пациент при выписке из стационара?
— Хирургическое лечение в стационаре занимает, как правило, не более месяца. Затем пациент продолжает лечение в амбулаторных условиях. Мы наблюдаем всех наших пациентов даже после выписки: даем рекомендации на следующие несколько недель, и если у больного наступает ухудшение состояния или возникают вопросы, он может обратиться к своему лечащему врачу за консультацией или за направлением на повторную госпитализацию.
Затем пациент продолжает лечение в амбулаторных условиях. Мы наблюдаем всех наших пациентов даже после выписки: даем рекомендации на следующие несколько недель, и если у больного наступает ухудшение состояния или возникают вопросы, он может обратиться к своему лечащему врачу за консультацией или за направлением на повторную госпитализацию.
Рекомендации включают контроль гликемии, регулярное наблюдение у хирурга или в кабинете диабетической стопы, соблюдение щадящего режима для поврежденной стопы, включая ношение ортопедической обуви со специальными стельками, избегание любых травмирующих кожу стопы манипуляций.
В ряде случаев с этой целью мы накладываем повязки Total contact cast – полимерный гипс, который позволяет регулировать нагрузку на стопу при диабетической артропатии и избежать разрушения стопы и голеностопного сустава в процессе амбулаторного лечения.
Как правило, в его ношении человек нуждается достаточно длительное время: каст служит до полугода, а затем заменяется на новый. Отказ от его ношения чреват разрушением голеностопного сустава и осложнениями в виде гнойного артрита и флегмоны. Практика знает случаи, когда пациенты, закончив стационарное лечение, несмотря на показания,отказывались от этой манипуляции, а через некоторое время возвращались в больницу вновь – уже на ампутацию.
Отказ от его ношения чреват разрушением голеностопного сустава и осложнениями в виде гнойного артрита и флегмоны. Практика знает случаи, когда пациенты, закончив стационарное лечение, несмотря на показания,отказывались от этой манипуляции, а через некоторое время возвращались в больницу вновь – уже на ампутацию.
Что касается медикаментозного лечения, то пациенты, перенесшие баллонную ангиопластику при ишемическом типе диабетической стопы, в течение полугода принимают препараты, улучшающие кровоток. Другая группа препаратов направлена на лечение диабетической полинейропатии, это препараты альфа-липоевой кислоты. Их прием рекомендован при нейропатической форме синдрома диабетической стопы. При смешанном варианте лечения пациенту рекомендуется профилактическими курсами принимать поочередно препараты и первой, и второй группы.
— Каков прогноз при синдроме диабетической стопы и ее осложнениях?
— Все зависит от того, насколько пациент, прошедший курс стационарного лечения, следит за своим состоянием, степенью компенсированности сахарного диабета: в случае неконтролируемой гипергликемии процесс разрушения организма происходит очень быстро. Другим компонентом успешности лечения является сосудистая функция. При выраженных проявлениях артериальной недостаточности нижних конечностей в ряде случаев высока вероятность развития гангрены. Все эти факторы риска находят свое отражение в рекомендациях по лечению и правильному образу жизни для пациента.
Другим компонентом успешности лечения является сосудистая функция. При выраженных проявлениях артериальной недостаточности нижних конечностей в ряде случаев высока вероятность развития гангрены. Все эти факторы риска находят свое отражение в рекомендациях по лечению и правильному образу жизни для пациента.
Медицинский журнал «Дело Жизни»
№4 (12) 2016
Елена Рычкова
ДЖ-4(12)2016_Ахунзянов
Лечение гнойных ран в Москве в Открытой клинике
Вскрытие и лечение гнойных ран в «Открытой Клинике»
Гнойные раны могут представлять угрозу для жизни человека, поэтому «Открытая Клиника» оказывает срочное лечение в таких случаях с возможным вскрытием и устранением очага воспаления. Методы терапии врач определяет исходя из стадии раневого процесса. В начальной фазе квалифицированные хирурги проводят очищение раны и ее детоксикацию. Не исключена и хирургическая обработка при лечении гнойных ран с последующей стимуляцией регенерации тканей на втором этапе терапии.
Наш медицинский центр имеет богатую диагностическую и лечебную базу, это позволяет нам оказывать комплексную медицинскую помощь при наличии у пациента гнойных ран. Они активно впитывают токсины, что может привести к интоксикации всего организма. В «Открытой Клинике» вы оперативно получите необходимое врачебное содействие по доступной цене. Определить патологический процесс в ране после пореза или выдавливания прыща нетрудно, характерными признаками являются:
- отечность тканей;
- цвет раны зеленовато-желтоватый с темными краями;
- окружная гиперемия;
- выраженный болевой синдром;
- в ране виден гной и отмершие клетки.
При значительном поражении мягких тканей довольно быстро наступает интоксикация как реакция на всасываемые через рану токсины и продукты распада. Лечением гнойных ран на ногах занимается врач-хирург. Оно не обязательно включает в себя хирургическое вмешательство, иногда можно обойтись местным лечением, особенно на начальном этапе развития патологии.
При обширном поражении наблюдается высокая температура, озноб, повышенная потливость, потеря аппетита. Если не оказать комплексное лечение гнойных ран пациенту в таком состоянии, велика вероятность развития осложнений: воспаление лимфатических сосудов, вен, абсцесса, флегмоны. Терапия в хирургическом отделении «Открытой Клиники» включает в себя:
- промывание, дренирование раны;
- стимуляцию регенерации кожи;
- антибиотикотерапию;
- лечебные перевязки;
- иммунотерапию.
Какие именно процедуры нужно провести пациенту, определяет хирург после первичного осмотра в любом из наших отделений. Для этого нужно приехать в Москву, если вы не проживаете в столице. Мы предоставляем стационар, процедуры по восстановлению и реабилитации. Получить дополнительную консультацию и необходимое лечение вы можете в любой день недели, ведь мы работаем без перерывов и выходных.
Лечение гнойных ран Текст научной статьи по специальности «Клиническая медицина»
doi: 10. 18484/2305-0047.2015.6.680 А.А. ТРЕТЬЯКОВ, С.В. ПЕТРОВ, А.Н. НЕВЕРОВ, А.Ф. ЩЕТИНИН
18484/2305-0047.2015.6.680 А.А. ТРЕТЬЯКОВ, С.В. ПЕТРОВ, А.Н. НЕВЕРОВ, А.Ф. ЩЕТИНИН
ЛЕЧЕНИЕ ГНОЙНЫХ РАН
ГБОУ ВПО «Оренбургский государственный медицинский университет»,
Российская Федерация
Количество пациентов с острыми гнойными заболеваниями мягких тканей не уменьшается, и имеет тенденцию к росту, составляя до 35-40% от всего количества хирургических пациентов. Успех хирургического лечения острых гнойных заболеваний мягких тканей во многом зависит от радикальности оперативного пособия, выполняемого при адекватном обезболивании. Важным фактором, способствующим успешному заживлению раны, является создание условий для ее адекватного дренирования в послеоперационном периоде. Использование антибактериальных средств является частью комплексного лечения пациентов с острой гнойной хирургической инфекцией. Разработка методов современного активного лечения связана с пересмотром основных положений классического инцизионно-дренажного способа и изменением сути самой операции. Они предусматривают более радикальное целенаправленное оперативное вмешательство в зоне гнойного очага с обеспечением эффективного адекватного дренажа и совершенно иное, более активное лечение гнойной раны в фазу воспаления и в фазу регенерации. При применении любой дренажной системы необходимо соблюдать особенные условия. Необходимость раннего и быстрейшего закрытия гнойной раны привела к поиску и созданию условий для наложения швов и кожной пластики. Перспективным путем преодоления антибиотикорезистентности стало применение пробиотиков. Еще одним новым направлением в решении проблемы лечения гнойно-воспалительных процессов различной локализации является включение в комплексное лечение нейропептидов, в частности гипоталамического нанопептида — окситоцина.
Разработка методов современного активного лечения связана с пересмотром основных положений классического инцизионно-дренажного способа и изменением сути самой операции. Они предусматривают более радикальное целенаправленное оперативное вмешательство в зоне гнойного очага с обеспечением эффективного адекватного дренажа и совершенно иное, более активное лечение гнойной раны в фазу воспаления и в фазу регенерации. При применении любой дренажной системы необходимо соблюдать особенные условия. Необходимость раннего и быстрейшего закрытия гнойной раны привела к поиску и созданию условий для наложения швов и кожной пластики. Перспективным путем преодоления антибиотикорезистентности стало применение пробиотиков. Еще одним новым направлением в решении проблемы лечения гнойно-воспалительных процессов различной локализации является включение в комплексное лечение нейропептидов, в частности гипоталамического нанопептида — окситоцина.
Ключевые слова: гнойные раны, хирургическое лечение, тактика лечения, дренаж, антибиотикорези-стентность, пробиотики, нейропептиды
The number of patients with acute purulent diseases of the soft tissues hasn’t reduced and tends to rise, accounting for 35-40% of all surgical patients. The success of the surgical treatment of acute purulent diseases of soft tissues depends on radical surgical aids, performed with adequate anesthesia. Drainage of wound fluid is an factor important to successful wound healing in the incisional period. The use of antibiotics is included in a comprehensive treatment of patients with acute purulent surgical infection. The development of current methods of active treatment is related to the revision of the main points of the classical incision-drainage method and changing the very nature of the operation itself. They envisage a targeted radical surgery in the site of supportive focus to provide the effective and adequate drainage so as completely different, more aggressive therapy of purulent wounds in the inflammatory and regeneration phases. Any drainage system requires some special conditions. The necessity for early and rapid closing of purulent wound led to the search and creation of conditions for sutures and skin plasty. A new perspective way to overcome antibiotic resistance is considered to use probiotics.
The success of the surgical treatment of acute purulent diseases of soft tissues depends on radical surgical aids, performed with adequate anesthesia. Drainage of wound fluid is an factor important to successful wound healing in the incisional period. The use of antibiotics is included in a comprehensive treatment of patients with acute purulent surgical infection. The development of current methods of active treatment is related to the revision of the main points of the classical incision-drainage method and changing the very nature of the operation itself. They envisage a targeted radical surgery in the site of supportive focus to provide the effective and adequate drainage so as completely different, more aggressive therapy of purulent wounds in the inflammatory and regeneration phases. Any drainage system requires some special conditions. The necessity for early and rapid closing of purulent wound led to the search and creation of conditions for sutures and skin plasty. A new perspective way to overcome antibiotic resistance is considered to use probiotics. Another new direction in solving the issue of the treatment of chronic inflammatory processes of different localization is the inclusion of neuropeptides such as hypothalamic nanopeptid (oxytocin) in a comprehensive treatment.
Another new direction in solving the issue of the treatment of chronic inflammatory processes of different localization is the inclusion of neuropeptides such as hypothalamic nanopeptid (oxytocin) in a comprehensive treatment.
Keywords: purulent wounds, surgical treatment, treatment tactics, drainage, resistance to antibiotics, probiotics, neuropeptides
Novosti Khirurgii. 2015 Nov-Dec; Vol 23 (6): 680-687 Treatment of Purulent Wounds
A.A. Tretyakov, S.V. Petrov, A.N. Neverov, A.F. Shchetinin
Введение
Частота гнойных раневых осложнений на протяжении последних 50 лет практически не изменялась [1, 2, 3]. Следует отметить и тот факт, что около 42% летальных исходов хирургических вмешательств связаны с гнойно-воспалительными осложнениями [4, 5]. Количество пациентов с острыми гнойными заболеваниями мягких тканей не уменьшается и имеет тенденцию к росту, составляя до 35-40% от всего количества хирургических пациентов [1, 6]. Учащение гнойных раневых осложнений
Количество пациентов с острыми гнойными заболеваниями мягких тканей не уменьшается и имеет тенденцию к росту, составляя до 35-40% от всего количества хирургических пациентов [1, 6]. Учащение гнойных раневых осложнений
и гнойных заболеваний требует больших затрат на лечение. Таким образом, лечебное и социальное значение проблемы лечения ран требует изучения, разработки и совершенствования.
Поиски методов лечения гнойных ран и борьбы с раневой инфекцией имеют длительную историю. Отдельные ее вехи отмечались впечатляющими достижениями, когда многие проблемы гнойной хирургии считались решенными и хирурги, казалось, получили наконец многообещающие антибактериальные средства. Такие надежды не раз возлагались на антибиотики, протеолитические ферменты, на методы
физического воздействия — лазер, ультразвук, гипербарическую оксигенацию [4, 7, 8, 9].
Однако в дальнейшем все эти методы наряду с положительными результатами проявили недостатки биологического, технического и экономического ряда. Они не обладали универсальным воздействием на раневой процесс, и проблема лечения гнойной инфекции (первичной гнойной раны) сохраняет свою актуальность, нуждаясь в последующих разработках [10, 11, 12].
До настоящего времени достаточно широко распространен так называемый инцизионно-дренажный способ. Он предусматривает вскрытие гнойного очага и открытое ведение раны в послеоперационном периоде. Следует отметить некоторые недостатки, существенно снижающие эффективность подобного лечения. Частая смена марлевых дренажей в течение суток практически невозможна. Кроме того, при их удалении повреждается грануляционная ткань, высок риск госпитального инфицирования раны и, наконец, значительно увеличивается продолжительность лечения. Это обусловлено тем, что при инцизионно-дренажном способе затягивается главным образом фаза воспаления и раневой процесс пролонгируется, а в борьбе с инфекцией организм остается практически «в одиночестве» [1, 13].
В данной ситуации хирург вынужденно оказывается в положении пассивного наблюдателя, когда заживление раны происходит без активного его влияния на развитие раневого процесса, а очищение раны обеспечивается лишь природными возможностями. Повышается степень риска возникновения осложнений в процессе лечения в виде затеков и генерализации инфекции [14, 15, 16]. Однако инцизионно-дренаж-ный способ является классическим, в целом он определяет тактику в лечении острых гнойных заболеваний мягких тканей и гнойных ран.
Как о варианте пособия, связанного с обработкой гнойного очага, можно сказать о пункционном способе лечения ран, когда пункцией эвакуируют гной, а полость промывают антисептиком. Такой закрытый метод, по мнению ряда авторов, достаточно эффективен при отграниченных гнойниках в мягких тканях [16]. Тем не менее, пункционный способ во многих случаях не приводит к полному выздоровлению, т. к. в тканях остаются некротические участки, которые служат прекрасной средой для размножения микроорганизмов, затягивая тем самым воспалительный процесс и приводя его к хроническому течению [17, 18, 19].
к. в тканях остаются некротические участки, которые служат прекрасной средой для размножения микроорганизмов, затягивая тем самым воспалительный процесс и приводя его к хроническому течению [17, 18, 19].
Создание и разработка методов современного активного лечения связаны с пересмотром
основных положений классического инцизи-онно-дренажного способа и изменением сути самой операции. Они предусматривают более радикальное целенаправленное оперативное вмешательство в зоне гнойного очага с обеспечением эффективного адекватного дренажа и совершенно иное, более активное лечение гнойной раны в фазу воспаления и в фазу регенерации [20].
Хирургическая обработка гнойного очага
Успех хирургического лечения острых гнойных заболеваний мягких тканей во многом зависит от радикальности оперативного пособия, выполняемого при адекватном обезболивании [20, 21]. Цель операции, носящей название «хирургическая обработка гнойного очага» в отличие от еще распространенного, к сожалению, «вскрытия гнойника» достаточно лаконично сформулировал А.Н. Беркутов (1973) [22]: «…путем иссечения поврежденных тканей добиться того, чтобы стенками раны стали живые ткани, способные активно противодействовать развитию микробов, подавлять их жизнедеятельность с помощью фагоцитов и защитных гуморальных факторов».
До начала операции необходимы информация о распространенности воспалительного процесса, локализации эпицентра гнойника и знание путей генерализации инфекции в данной области. Используются термографическая индикация очага воспаления, ультразвуковое исследование. Радикальность манипуляций зависит от выполнения некрэктомии, иссечению подлежат девитализированные ткани.
В настоящее время существует большое число критериев оценки жизнеспособности тканей. Это термография раневой зоны, прижизненное окрашивание тканей, компостер-биопсия тканей, радиоизотопный метод, активность креатининкиназы, ультразвуковое сканирование, электрическое сопротивление (импеданс) ткани, люминесцентная флюоро-скопия [1, 8, 11, 12].
Обработка гнойного очага должна осуществляться хирургической бригадой в условиях операционной с обеспечением адекватного обезболивания. Далее, если виды собственно оперативного вмешательства (в данном случае ликвидация гнойного очага) при всех активных методах относительно одинаковы, то в послеоперационном периоде должны быть сохранены все принципы лечения гнойной раны с использованием различных средств воздействия на раневой процесс (лазер, ультразвук и др.). Именно в этом заключаются суть и название
того или иного способа активного хирургического лечения острой гнойной инфекции [2, 17, 20, 21, 23].
Тактика и выбор сроков операции
Мнение хирургов о необходимости операции при гнойно-некротических заболеваниях едино. Сама суть вмешательства претерпела эволюционное развитие от дренирующего разреза до хирургической обработки гнойного очага. Вопрос же о своевременности ее проведения не находит единой согласованной тактики, а имеющиеся в литературе сведения об этом крайне противоречивы [20, 21, 24].
Вопрос же о своевременности ее проведения не находит единой согласованной тактики, а имеющиеся в литературе сведения об этом крайне противоречивы [20, 21, 24].
Существует доктрина, выделяющая раннюю, отсроченную и позднюю операции при обработке раны, но она более соответствует тактике при массовом поступлении пациентов с ранами и более подходит к военно-полевым условиям, когда первая помощь завершается эвакуацией. В мирное же время возникает необходимость в иных подходах.
При гнойно-воспалительных заболеваниях по срочности выполнения хирургической обработки гнойного очага В. К. Гостищев (1996) [24] выделяет экстренные, срочные и плановые операции. Экстренная операция проводится по жизненным показаниям, когда малейшая ее отсрочка угрожает жизни больного. Срочная — по абсолютным показаниям, когда длительная отсрочка может привести к развитию различных осложнений (хронический остеомиелит, длительно незаживающие раны и т. д.). Проведение плановых операций осуществляется по относительным показаниям, например? по поводу трофической язвы, при эпителиально-копчиковом свище и т.п. Таким образом, с помощью предлагаемой классификации унифицируется лечебная тактика независимо от локализации острого гнойного воспалительного процесса и вида заболевания.
д.). Проведение плановых операций осуществляется по относительным показаниям, например? по поводу трофической язвы, при эпителиально-копчиковом свище и т.п. Таким образом, с помощью предлагаемой классификации унифицируется лечебная тактика независимо от локализации острого гнойного воспалительного процесса и вида заболевания.
Некоторые авторы [2, 11, 20, 25] считают, что в большинстве случаев пациенты с острыми гнойными заболеваниями мягких тканей в день поступления в экстренном порядке и тем более ночью оперироваться не должны. Оперативное вмешательство необходимо отложить на 12-16 ч, используя время для минимального обследования пациента. По их мнению, операция хирургической обработки гнойного очага обширна по объему и достаточно травматична, требует применения современных медикаментозных средств, высокого технического обеспечения и адекватного обезболивания. Отсрочка оперативного вмешательства у пациентов с сахарным диабетом на 1-1,5 сут. не оказывает негативного
не оказывает негативного
влияния на исход заболевания, наоборот, она позволяет объективно оценить состояние и провести соответствующую коррекцию уровня глюкозы и исследовать микрофлору очага воспаления с целью проведения рациональной антибиотикотерапии в послеоперационном периоде.
Именно отсроченная операция позволяет провести нужное диагностическое обследование и коррекцию жизненных функций организма. Это не отражается на состоянии пациентов, которые до госпитализации болеют в течение нескольких дней и недель. Кроме того, хирургическая обработка гнойного очага в дневное время всегда выполняется под контролем опытного врача. Немаловажно и то, что оперативное вмешательство и последующее лечение больного до выписки проводятся одним врачом.
При отсроченной операции всегда возможно использование необходимого технического обеспечения (лазер, ультразвук, вакуум-терапия, криовоздействие, плазменная обработка, метод пульсирующей струи антисептика) для создания максимальной радикальности операции [26, 27, 28, 29, 30, 31].
Исключение составляют пациенты с анаэробной инфекцией, которым хирургическую обработку гнойного очага приходится выполнять по экстренным показаниям. Операцию при анаэробной инфекции необходимо проводить как можно раньше, при первом же подозрении, не дожидаясь результатов микробиологического исследования. Это обусловлено тем, что быстрое распространение инфекционного процесса резко ухудшает состояние пациента и неизбежно увеличивает объем самого оперативного вмешательства [20, 32].
Наиболее сложным представляется вопрос о сроках выполнения операции у тех пациентов, которые поступают в общехирургическое отделение во время дежурств, т.е. в отсутствие квалифицированного хирурга и должного технического обеспечения радикальности операции, включая и топографо-анатомическую диагностику локализации и распространенности гнойного процесса. Дежурный врач, пренебрегая отсутствием условий, как правило, не утруждает себя выбором оптимального решения и удовлетворяется лишь обычным рассечением тканей над местом воспаления с тампонированием гнойной раны. К сожалению, наряду с минимальной пользой и паллиативностью такого вмешательства возникает неизбежный риск инфицирования агрессивной флорой последующих оперируемых по поводу полостной или другой острой хирургической патологии [2]. По данным С.М. Курбангалеева [17], по этой
К сожалению, наряду с минимальной пользой и паллиативностью такого вмешательства возникает неизбежный риск инфицирования агрессивной флорой последующих оперируемых по поводу полостной или другой острой хирургической патологии [2]. По данным С.М. Курбангалеева [17], по этой
причине более 95% пациентов, поступающих в специализированное отделение хирургической инфекции, нуждаются в повторных операциях. Учитывая довольно частое возникновение осложнений в виде затеков, прорывов в соседние клетчаточные пространства, а также генерализацию инфекции, современной операцией следует считать радикальную хирургическую обработку гнойного очага, произведенную в полном объеме.
Вторичная хирургическая обработка раны
Часто приходится сталкиваться с проблемой лечения пациентов, первично обратившихся по поводу гнойной раны. Хирурги, как правило, склонны лечить эти раны традиционным способом путем ежедневных перевязок. Однако для предотвращения возможных осложнений (флегмона, глубокий абсцесс, лимфаденит, признаки генерализации инфекции) и для сокращения сроков лечения целесообразнее производить вторичную хирургическую обработку раны с адекватной ревизией и дренированием очага [1, 2, 16, 23].
Однако для предотвращения возможных осложнений (флегмона, глубокий абсцесс, лимфаденит, признаки генерализации инфекции) и для сокращения сроков лечения целесообразнее производить вторичную хирургическую обработку раны с адекватной ревизией и дренированием очага [1, 2, 16, 23].
Дренирование раны
Важным фактором, способствующим успешному заживлению раны, является создание условий для ее адекватного дренирования в послеоперационном периоде. При открытой курации гнойной раны в качестве дренажа применяют перчаточную резину, марлевые турун-ды, салфетки, трубки с расчетом на пассивный отток отделяемого из раневой полости.
В начале XX века Р. Мориссон (1916) использовал шов на гнойную рану после ее хирургической обработки с обязательным промыванием антисептиками зашитой раневой полости. В дальнейшем возможность применения шва в лечении гнойной раны была подтверждена многими исследователями. Видоизменялась лишь защита тканей паравульнарной зоны от микробной инвазии путем массивной антибактериальной терапии при рациональном подборе [21, 33, 34].
Видоизменялась лишь защита тканей паравульнарной зоны от микробной инвазии путем массивной антибактериальной терапии при рациональном подборе [21, 33, 34].
Другим средством защиты обработанной и зашитой гнойной раны, получившим название проточного ферментативного некролиза, является ферментотерапия с использованием протеаз для промывания раневой полости [35, 36, 37].
Что касается задержки в ране детрита, то известно, что заживление гранулирующей раны прежде всего зависит от жизнеспособности тканей и в меньшей степени от наличия микробов в
раневой зоне. Поэтому даже полное лекарственное подавление микрофлоры не предотвращает повторного нагноения раны. Следует помнить, что при применении любой дренажной системы необходимо соблюдать два условия:
1. Использование трубок из полихлорвинила или другого материала эффективно лишь при их постоянном промывании какой-либо жидкостью с сохранением проходимости дренажа. В противном случае трубки закупориваются сгустками крови, некротическими массами и подсыхающим гноем.
В противном случае трубки закупориваются сгустками крови, некротическими массами и подсыхающим гноем.
2. Обязательным элементом аспирационно-го функционирования такой системы является непременная ее герметизация как физическое условие принудительного выведения экссудата.
Для эффективного удаления раневого экссудата Н.Н. Каншин [21] применил двухпро-светную трубку, через малый канал которой вводится промывной антисептик, а через большой удаляется содержимое из полости. Автор использовал изоляцию раны с помощью швов и воздействовал на ткани через трубку. Он склонен считать данный способ вариантом управляемой абактериальной среды, при котором, как полагает автор, предупреждается реинфициро-вание раны и улучшаются результаты лечения (косметичность, функциональность исхода, сокращение сроков пребывания в стационаре). При дальнейшем изучении гидродинамики промывных систем и течения раневого процесса в условиях принудительной аспирации были выявлены существенные их недостатки, а именно: антибактериальные препараты контактируют в основном со стенками трубки и банки сборника и удивительно мало взаимодействуют с тканями раневой зоны и микрофлорой [12, 21, 33, 34]. Это в значительной степени нивелируется при так называемом фракционном промывании полости раны с помощью автоматических программных устройств [21, 35].
Это в значительной степени нивелируется при так называемом фракционном промывании полости раны с помощью автоматических программных устройств [21, 35].
Таким образом, повысить эффективность очищения раны при использовании различных дренажных систем можно путем варьирования характеристики антисептика, антибиотика и даже протеолитического фермента.
Мы всецело разделяем точку зрения В.К. Гостищева [24], утверждающего, что громоздкость приспособлений и большие объемы стерильных растворов ограничивают приме -нение этих методов в широкой хирургической практике.
Хирургическое закрытие раны
Необходимость раннего и быстрейшего закрытия гнойной раны привела к поиску и соз-
данию условий для наложения швов и кожной пластики. Различают: 1) первичный шов — шов после завершения первичной хирургической обработки раны; 2) вторичный ситуационный шов — шов после вторичной хирургической обработки раны независимо от сроков ее выполнения.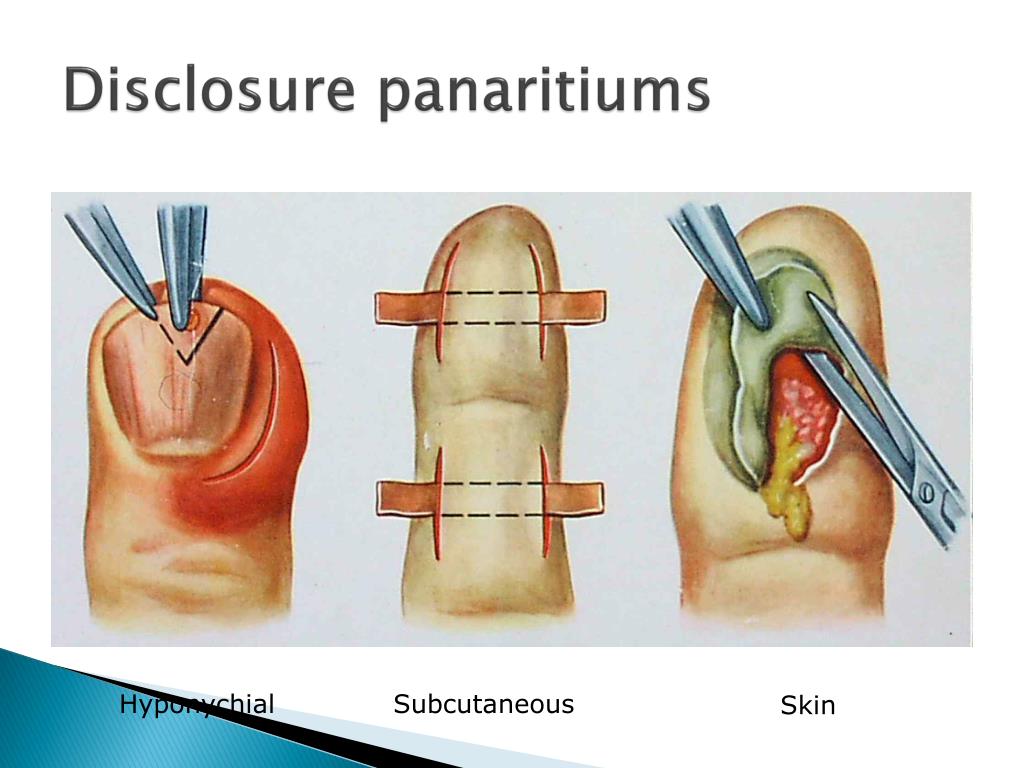
Для реализации одного из основных принципов активного хирургического лечения гнойных ран, а именно возможно раннего закрытия раневой поверхности с помощью швов, необходимы следующие условия: очищение раны от девитализированных тканей; отсутствие выраженных воспалительных изменений в тканях паравульнарной зоны; возможность хорошего (без натяжения) сопоставления краев раны.
Другой способ раннего закрытия раневой поверхности — кожная пластика.
Эффективность кожной пластики во многом зависит от адекватной подготовки раневой поверхности. Прежде чем выполнять эту операцию, необходимо добиться полного очищения раны. Кроме того, обязательным условием является незначительная (ниже критического уровня) микробная обсемененность раны — 10 микробных тел на 1 см2 [38, 39].
Адекватная подготовка раны к аутодер-мопластике достигается вакуум-обработкой поверхности, а также с помощью протеолити-ческих ферментов [27, 30]. Хорошие результаты при кожной пластике получены также при ведении раны в послеоперационном периоде в условиях управляемой абактериальной среды [21, 40, 41].
Хорошие результаты при кожной пластике получены также при ведении раны в послеоперационном периоде в условиях управляемой абактериальной среды [21, 40, 41].
Необходимо подчеркнуть чрезвычайно важный аспект, связанный не только с обязательной подготовкой раневой поверхности, требующей покрова, но и с выбором времени производства пластики. Следует помнить, что в основании грануляционной ткани после двух-, трехнедельной культивации образуется соединительнотканный каркас, который позднее становится анатомическим препятствием для полноценного кровоснабжения кожных трансплантатов. По этой причине последние обречены на гибель, и потому так важно не упустить время проведения кожной пластики, которую желательно выполнить в течение 3-й недели лечения.
Особенности антибиотикотерапии
Использование антибактериальных средств является частью комплексного лечения пациентов с острой гнойной хирургической инфекцией. В настоящее время установлено, что, к сожалению, у 30% пациентов при применении
В настоящее время установлено, что, к сожалению, у 30% пациентов при применении
антибиотиков возникают побочные реакции и осложнения — от аллергии до анафилактического шока с летальным исходом, отмечено токсическое действие антибиотиков на различные органы и системы [5, 42].
Нерациональное применение антибиотиков приводит к появлению резистентности у микроорганизмов к используемым лекарственным препаратам, опасной формой которой является антибиотикозависимость.
Антибиотикотерапия изменила течение раневого процесса, возникли определенные трудности в диагнозе его фазовости и прогнозировании исхода; кроме того, участились хронические формы течения и рецидивы воспаления [5, 43, 44].
Некоторые исследователи считают перспективным эндолимфатическое использование антибиотиков, поскольку при этом они получали ощутимый терапевтический эффект [45].
Существенным прогрессом в хирургическом лечении гнойных ран с применением антибио-тикотерапии является создание мазей на водорастворимой основе, благодаря которым стало возможным местное применение антибиотиков и других лекарственных средств в первую фазу раневого процесса, т.е. в тот период заболевания, когда это максимально необходимо. В состав этих мазей входит физиологически неактивный водорастворимый продукт, обладающий дегидратирующим эффектом не только по отношению к тканям, но, главное, к микробной клетке, вызывая ее обезвоживание и гибель.
Использование пробиотиков и окситоцина
Перспективным путем преодоления анти-биотикорезистентности стало применение про-биотиков. В последние годы выполнено большое количество исследований, доказывающих эффективность использования препаратов из нормальной флоры человека — сенной палочки для лечения многих видов хирургической патологии. Лечебно-профилактическое действие препаратов из бацилл, в одних случаях может достигаться преимущественно за счет антагонистических свойств бацилл в других — за счет продукции ими ферментов, в третьих — за счет активации защитных реакций. Но, как правило, участие в процессе одновременно принимают несколько факторов [46, 47].
Лечебно-профилактическое действие препаратов из бацилл, в одних случаях может достигаться преимущественно за счет антагонистических свойств бацилл в других — за счет продукции ими ферментов, в третьих — за счет активации защитных реакций. Но, как правило, участие в процессе одновременно принимают несколько факторов [46, 47].
Еще одним новым направлением в решении проблемы лечения гнойно-воспалительных процессов различной локализации является включение в комплексное лечение нейропептидов, в частности, гипоталамического нанопептида — окситоцина. Методы хирургического лечения
ран переживают этап «вторжения нейропепти-дов мозга» в традиционные представления об управлении процессами пролиферации, роста и цитодифференцировки различных тканей [48]. Исследование показывает, что в критических, аварийных ситуациях, как известно, сопровождающихся значительной активизацией гипоталамо-гипофизарной нейросекреторной системы (ГГНС), а также при повреждениях различных тканей млекопитающих гипотала-мические нанопептиды (окситоцин, вазопрес-син) осуществляют существенное адаптогенное влияние и имеют немаловажное значение в развитии долговременной (структурной) адаптации клеток и тканей. К тому же указанные гуморальные факторы выступают как стимуляторы репаративных процессов.
К тому же указанные гуморальные факторы выступают как стимуляторы репаративных процессов.
На основании комплексных многочисленных исследований был сделан вывод о том, что окситоцин вполне обоснованно может рассматриваться как межсистемный регулятор элементарных процессов репаративных гистогенезов (в частности, процессов пролиферации, роста, до-дифференцировки, адекватных межклеточных и межтканевых корреляций, функционально значимых цитодифференцировок) [49].
Применение окситоцина в комплексном лечении гнойных процессов при сахарном диабете, особенно при местном его применении, в значительной мере усиливает процессы васкулогенеза, пролиферации эндотелиоцитов, гистиоцитов и моноцитарных макрофагов, что в свою очередь приводит к эффективному очищению раны и формированию полноценной грануляционной соединительной ткани, создающей адекватные условия для репарации эпителиальных структур раневой поверхности, в том числе по принципу «первичного натяжения», улучшению репаративных процессов в костной ткани. Антимикробный эффект исследуемых гормонов проявлялся в условиях in vitro в основном в отношении грамположительных микроорганизмов и в значительно меньшей степени — грамотрицательных бактерий.
Антимикробный эффект исследуемых гормонов проявлялся в условиях in vitro в основном в отношении грамположительных микроорганизмов и в значительно меньшей степени — грамотрицательных бактерий.
Заключение
Проблема лечения гнойно-воспалительных заболеваний мягких тканей далека от окончательного решения. Основными направлениями изучения данной патологии на сегодняшний момент, видимо, следует считать:
1. Оптимизацию хирургического доступа.
2. Применение современных методов физического, медикаментозного воздействия на раневой процесс.
3. Рациональную антибиотикотерапию.
4. Изучение возможности создания оптимальных условий взаимодействия макро- и микроорганизмов при гнойно-воспалительном процессе.
5. Внедрение перспективных методов преодоления антибиотикорезистентности на основании применения пробиотиков и гипо-таламических нанопептидов.
ЛИТЕРАТУРА
1. Корейба К. А. Хирургические инфекционные поражения кожи и мягких тканей. Лечение длительно незаживающих ран : моногр. / К. А. Корейба,
A. Р. Газиев. — Казань : Отечество, 2011. — 253 с.
2. Кочоров О. Т. Современное состояние вопроса хирургического лечения ран и раневой инфекции / О. Т. Кочоров, Ш. М. Чынгышпаев, Р. А. Турсунов // Вестн. Авиценны. — 2011. — № 1. — С. 22-25.
3. Бесчастнов В. В. Новый способ активного лечения гнойных ран мягких тканей / В. В. Бесчастнов,
B. Н. Марамохин // Изв. высших учебных заведений. Поволж. регион. Мед. науки. — 2010. — № 3. —
Н. Марамохин // Изв. высших учебных заведений. Поволж. регион. Мед. науки. — 2010. — № 3. —
C. 59-67.
4. Блатун Л. А. Местное медикаментозное лечение ран. Проблемы и новые возможности их решения / Л. А. Блатун // Consilium medicum. Хирургия. -2007. — № 1. — С. 51-59.
5. Яковлев С. В. Госпитальные инфекции, вызванные грамотрицательными микроорганизмами: клиническое значение и современные возможности терапии / С. В. Яковлев // Инфекции и антимикроб. терапия. — 2007. — № 6. — С. 133-36.
6. Are we getting necrotizing soft tissue infections right? A 10 — year review / D. Proud [et al.] // ANZ J Surg.-2014 Jun. — Vol. 84, N 6. — P. 468-72 doi: 10.1111/ ans.12412.
7. Моторина И. Г. Современные представления о физиотерапевтических способах лечения хронических ран / И. Г. Моторина, Л. К. Куликов, Т. И. Мелешко // Сиб. мед. журн. — 2012. — Т. 114, № 7. — С. 8-11.
Г. Моторина, Л. К. Куликов, Т. И. Мелешко // Сиб. мед. журн. — 2012. — Т. 114, № 7. — С. 8-11.
8. Блатун Л. А. Местное медикаментозное лечение ран / Л. А. Блатун // Хирургия. Журн. им. Н. И. Пирогова. — 2011. — № 4. — С. 51-59.
9. Современные взгляды на патогенез и лечение гнойных ран / О. Э. Луцевич [и др.] // Хирургия. Журн. им. Н. И. Пирогова. — 2011. — № 5. -С. 72-77.
10. The sanford guide to antimicrobial therapy / ed. O. Gilbert, M. Sande. — 3-rd ed. — Antimicrob Therapy Inc, 2003.
11. Привольнев В. В. Основные принципы местного лечения ран и раневой инфекции / В. В. При-вольнев, Е. В. Каракулина // Клин. микробиол. и антимикроб. химиотер. — 2011. — Т. 13, № 3. -С. 214-22.
12. Хирургическое лечение ран: современные подходы / Ю. М. Бейзеров [и др.] // Хирургия. Восточ. Европа. — 2012. — № 3. — С. 286-87.
М. Бейзеров [и др.] // Хирургия. Восточ. Европа. — 2012. — № 3. — С. 286-87.
13. Are we really seeing the total costs of surgical site infections? A Spanish study / J. L. Alfonso [et al.] //
Wound Repair Regen. — 2007 Jul-Aug. — Vol. 15, N 4. — P. 474-81.
14. Абаев Ю. К. Справочник хирурга. Раны и раневая инфекция / Ю. К. Абаев. — Феникс, 2005. — 427 с.
15. Лечение пациентов с гнойными ранами путем применения аспирационно-проточно-промывного дренажа новой конструкции / Н. С. Казарян [и др.] // Вестн. Рос. акад. мед. наук. — 2013. — № 12. -С. 64-68.
16. Зак В. И. Местное лечение постинъекционных абсцессов комбинацией окситоцина и антибиотиков / В. И. Зак, П. П. Курлаев // Хирургия. Журн. им. Н. И. Пирогова. — 1985. — № 5. — С. 112-15.
— С. 112-15.
17. Курбангалеев С. М. Гнойная инфекция в хирургии / С. М. Курбангалеев. — М. : Медицина, 1985. — 272 с.
18. Лечение ран с помощью аппликационно-инъ-екционного введения гидролизата коллагена /
A. А. Андреев [и др.] // Глоб. науч. потенциал. -2013. — № 6. — С. 5-8.
19. Сорбционно-дренажное устройство в лечении гнойных ран и абсцессов мягких тканей / С. М. Смотрин [и др.] // Хирургия. Восточ. Европа. -2012. — № 3. — С. 308-309.
20. Кузин М. И. Раны и раневая инфекция / М. И. Кузин, Б. М. Костюченок, И. И. Колкер. -М. : Медицина, 1991. — 687 с.
21. Каншин Н. Н. Принципы закрытого аспираци-онно-промывного лечения загрязненных и нагноившихся ран / Н. Н. Каншин // Хирургия. — 1989. -№ 6. — С. 112-15.
Н. Каншин // Хирургия. — 1989. -№ 6. — С. 112-15.
22. Беркутов А. Н. Учебник военно-полевой хирургии / А. Н. Беркутов. — 2-е изд., доп. и испр. — Л., 1973. — 569 с.
23. Халилов М. А. Вопросы оптимизации местного лечения гнойных ран / М. А. Халилов // Человек и его здоровье. — 2009. — № 3. — С. 31-37.
24. Гостищев В. К. Оперативная гнойная хирургия /
B. К. Гостищев. — М. : Медицина, 1996. — 416 с.
25. Yao K. Post-operative wound management / K. Yao, L. Bae, W. P. Yew // Aust Fam Physician. -2013 Dec. — Vol. 42, N 12. — P. 867-70.
26. Загиров У. З. Озоно-магнитофорез в лечении гнойной раны / У. З. Загиров, У. М. Исаев, М. А. Салихов // Вестн. новых мед. технологий. -2007. — Т. 14, № 3. — С. 207-208.
— Т. 14, № 3. — С. 207-208.
27. Ларичев А. Б. Вакуум-терапия в комплексном лечении гнойных ран / А. Б. Ларичев, А. В. Антонюк, B. C. Кузьмин // Хирургия. Журн. им. Н. И. Пирогова. — 2008. — № 6. — С. 22-26.
28. Глухов А. А. Экспериментальное обоснование применения программируемой магнитотерапии в лечении ран мягких тканей / А. А. Глухов, О. С. Скоры-нин // Вестн. эксперим. и клин. хирургии. — 2009. -Т. 2, № 4. — С. 305-15.
29. Глухов А. А. Оптимизация лечения ран мягких тканей с применением поляризованного облучения и гидропрессивных технологий / А. А. Глухов, А. В. Лоб-цов, Н. Т. Алексеева // Систем. анализ и управление в биомед. системах. — 2010. — Т. 9, № 1. — С. 253-56.
30. Вакуум-терапия в лечении ран и раневой инфекции / В. Н. Оболенский [и др.] // Рус. мед. журнал. — 2010. — Т. 18, № 17. — С. 1064-72.
— Т. 18, № 17. — С. 1064-72.
31. Крайневысокочастотная и лазерная терапия в лечении больных с гнойными ранами мягких тканей / В. А. Дербенев [и др.] // Лазер. медицина. — 2010. — Т. 14, № 3. — С. 8-11.
32. Кулешов С. Е. Анаэробная клостридиальная и неклостридиальная инфекция в хирургии / С. Е. Кулешов. — М. : Медицина, 1993.
33. Blueman D. The use of larval therapy to reduce the bacterial load in chronic wounds / D. Blueman, C. Bous-field // J Wound Care. — 2012 May. — Vol. 21, N 5. -P. 244-53.
34. Полуоткрытый способ лечения гнойных ран мягких тканей / С. Г. Измайлов [и др.] // Соврем. технологии в медицине. — 2010. — № 1. — С. 56-59.
35. Полимерный сорбент регенкур в лечении гнойных ран / В. К. Гостищев [и др.] // Хирургия. Журн. им. Н. И. Пирогова. — 1993. — № 11. — С. 3-6.
Журн. им. Н. И. Пирогова. — 1993. — № 11. — С. 3-6.
36. Использование биологических свойств перфтора-на при местном лечении гнойных ран / Е. М. Мохов [и др.] // Рос. мед. журн. — 2011. — № 3. — С. 10-13.
37. Мохов Е. М. Применение озонированного пер-фторана при лечении гнойных ран / Е. М. Мохов, С. И. Воробьев, А. Р. Армасов // Вестн. эксперим. и клин. хирургии. — 2012. — Т. V, № 2. — С. 324-30.
38. Магомедов А. Р. К вопросу о лечении гнойных ран / А. Р. Магомедов // Вестн. Оренбург. гос. унта. — 2011. — № 16. — С. 308-309.
39. Новое в лечении гнойных ран / Ф. Е. Шин [и др.] // Моск. хирург. журн. — 2011. — № 5. — С. 51-54.
40. Surgical wound infection as a performance indicator: agreement of common definitions of wound infection in 4773 patients / A. P. Wilson [et al.] // BMJ. — 2004 Sep 25. — Vol. 329, N 7468. — P. 720.
P. Wilson [et al.] // BMJ. — 2004 Sep 25. — Vol. 329, N 7468. — P. 720.
41. Lipsky B. A. Medical treatment of diabetic foot infections / B. A. Lipsky // Clin Infect Dis. — 2004 Aug 1. — Vol. 39. — Suppl. 2. — P. S104-14.
42. Козлов Р. С. Нозокомиальные инфекции: эпидемиология, патогенез, профилактика, контроль / Р. С. Козлов // Клин. микробиол. антимикроб. химиотерапия. — 2000. — Т. 2, № 1. — С. 16-30.
43. Определение чувствительности микроорганизмов к антибактеральным препаратам : метод. рекомендации / С. В. Сидоренко [и др.] // Клин. микробиол. антимикроб. химиотерапия. — 2004. — Т. 6, № 4. -С. 306-59.
44. Verd6 Soriano J, Nolasco Bonmati A. ALEA study. Treatment of chronic wounds infected by the application of silver dressings nanocrystalline combined with dressings hydrocellular / J. Verd6 Soriano, A. Nolasco Bonmati // Rev Enferm. — 2010 Oct. — Vol. 33, N 10. -P. 6-14. [Article in Spanish]
Verd6 Soriano, A. Nolasco Bonmati // Rev Enferm. — 2010 Oct. — Vol. 33, N 10. -P. 6-14. [Article in Spanish]
45. Shi E. Maggot debridement therapy: a systematic review / E. Shi, D. Shofler // Br J Community Nurs. -2014 Dec. — Suppl. Wound Care. — P. S6-13. doi: 10.12968/bjcn.2014.19.Sup12.S6.
46. Слепых Н. И. Профилактика и лечение послеоперационных раневых инфекций пробио-тиком споробактерином : пособие для врачей / Н. И. Слепых, А. А. Стадников, А. А. Третьяков. -Оренбург, 2001. — 39 с.
47. Никитенко В. И. Роль транслокации в патогенезе хирургической инфекции / В. И. Никитенко,
В. В. Захаров, А. В. Бородин // Хирургия. Журн. им. Н.И. Пирогова. — 2001. — № 2. — С. 63-65.
48. Усиление антимикробного действия антибиотиков в комбинации с окситоцином / О. В. Бухарин [и др.] // Антибиотики. — 1984. — № 5. — С. 365-69.
49. Гавриленко В. Г. Морфологическая характеристика раневого процесса у больных с диабетическими гнойно-некротическими поражениями стоп при воздействии окситоцином / В. Г. Гавриленко, В. К. Есипов, К. Г. Сивожелезов // Морфология. -2003. — Т. 124, № 5. — С. 24-28.
Адрес для корреспонденции
460000, Российская Федерация,
г. Оренбург, ул. Советская, д. 6,
ГБОУ ВПО «Оренбургский государственный
медицинский университет»,
кафедра хирургии ИПО,
тел. раб.: +7 3532 34-92-71,
тел. моб. +7 922 625-2531,
моб. +7 922 625-2531,
e-mail: [email protected],
Петров Сергей Валентинович
Сведения об авторах
Третьяков А.А., д.м.н., профессор, заведующий кафедрой хирургии ИПО ГБОУ ВПО «Оренбургский государственный медицинский университет». Петров С.В., к.м.н., ассистент кафедры хирургии ИПО ГБОУ ВПО «Оренбургский государственный медицинский университет».
Неверов А.Н., к.м.н., доцент кафедры хирургии ИПО ГБОУ ВПО «Оренбургский государственный медицинский университет».
Щетинин А.Ф., к.м.н., доцент кафедры хирургии ИПО ГБОУ ВПО «Оренбургский государственный медицинский университет».
Поступила 3.06.2015 г.
Гнойный гайморит, симптомы и лечение гнойного гайморита
С полостью носа сообщается несколько придаточных пазух.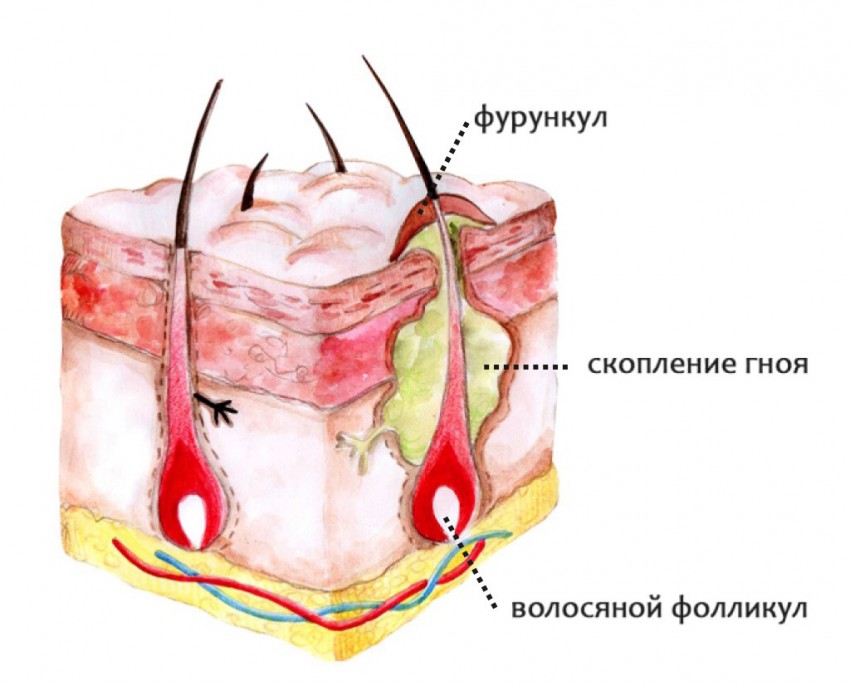 Парная гайморова пазуха расположена в толще верхней челюсти и выстлана тонкой слизистой оболочкой. Причиной ее воспаления становится распространение инфекции из полости носа.
Парная гайморова пазуха расположена в толще верхней челюсти и выстлана тонкой слизистой оболочкой. Причиной ее воспаления становится распространение инфекции из полости носа.
Гнойный гайморит сопровождается нарушением оттока образующегося воспалительного экссудата из-за сопутствующего отека слизистой оболочки. При этом возникают благоприятные условия для размножения патогенных микроорганизмов. Продукты их распада, пострадавший эпителий слизистой и погибшие иммунные клетки образуют гной.
По течению гнойный гайморит может быть острым и хроническим. Во втором случае заболевание длится более 4 недель, протекает с чередованием ремиссий и обострений. Обострения характеризуются усилением симптомов гнойного гайморита.
Симптомы гнойного гайморита
Присоединение бактериальной микрофлоры отмечается на 4 -5 день заболевания. Появляются такие симптомы гнойного гайморита:
- проявления общей интоксикации – слабость, потливость, озноб;
- развитие лихорадки с повышением температуры тела до 38° и выше;
- интенсивная головная боль, сильная болезненность в области верхней челюсти, особенно выраженная по утрам и при наклоне головы вперед, часто только с одной стороны;
- отечность мягких тканей лица и век;
- заложенность носа и ушей, снижение обоняния, умеренные гнойные выделения из носа, кашель, зубная боль.

При несвоевременном лечении гнойного гайморита возможно развитие внутричерепных осложнений, например, менингита.
Предположить развитие гнойного процесса в верхнечелюстной пазухе можно в том случае, если эти признаки появились через несколько дней после возникновения первых симптомов респираторного заболевания. Кроме того, нагноение содержимого пазухи может вызвать повторное ухудшение самочувствия больного через некоторое время после выздоровления от ОРЗ.
Причины
Гнойный гайморит возникает как осложнение катарального при нарушении эвакуации содержимого из пазухи. Это приводит к задержке секрета желез, формированию отрицательного давления в пазухе и снижению содержания в ней кислорода. Такая среда благоприятна для размножения болезнетворных микроорганизмов.
Предрасполагают к развитию острого гнойного гайморита аллергический или вирусный риниты, вызывающие отек и нарушение функции мерцательного эпителия.
Переходу болезни в хроническую форму способствуют:
- муковисцидоз и другие причины дискинезии реснитчатого эпителия;
- хроническое воспаление аллергической природы;
- иммунодефицитные состояния;
- гипертрофический ринит, деформация носовой перегородки, полипы носа и другие анатомические препятствия для нормального потока воздуха;
- кариес зубов, хронический отит, тонзиллит.
Самый частый возбудитель заболевания – золотистый стафилококк. В случае хронического течения нередко обнаруживается синегнойная палочка и другие грам-отрицательные бактерии. У трети больных имеется смешанный состав микрофлоры. Нередко гнойный гайморит вызывают микроорганизмы, живущие в полости носа в нормальных условиях и попадающие в гайморову пазуху при чихании, кашле, насморке. Чтобы полностью вылечить гнойный гайморит, рекомендуется определить вид возбудителя болезни.
Диагностика гнойного гайморита
При хронической форме болезни назначается диагностическая пункция. Она выполняется через нижний носовой ход и дает возможность определить количество и характер содержимого. После бактериологического исследования пунктата во многих случаях удается определить возбудителя болезни. Это дает возможность выбора наиболее эффективных антибиотиков для лечения гнойного гайморита.
Методы диагностики:
- передняя риноскопия после обработки слизистой сосудосуживающими средствами;
- эндоскопия полости носа с помощью гибкого оптического прибора малого диаметра;
- УЗИ верхнечелюстных пазух для оценки толщины их стенок и наличия экссудата;
- рентгенография придаточных пазух для определения патологических изменений слизистой, оценки пневматизации (наличия воздуха) и количества гнойного содержимого в пазухе;
- компьютерная томография – наиболее информативный способ диагностики хронического гайморита, который позволяет определить распространенность и характер поражения.
Лечение гнойного гайморита в острой форме обычно не требует проведения такого комплекса исследований. Диагностика осуществляется на основании клинических данных.
Лечение гнойного гайморита
Терапия острой формы болезни обычно проводится с использованием медикаментов. Назначаются антибиотики, преимущество отдается средствам из группы макролидов. Они безопасны и действуют на большинство возбудителей синуситов.
Назначаются противовоспалительные препараты, муколитические средства, деконгестанты для улучшения оттока гнойного содержимого из пазухи.
Лечение гнойного гайморита без прокола дополняется промываниями носовой полости растворами антисептиков (фурацилин, хлоргексидин и другие).
Показания к пункции (проколу) гайморовой пазухи ограничены. Это обусловлено высоким риском осложнений и достаточной эффективностью антибактериальной терапии. Тем не менее, метод используется в тяжелых случаях заболевания, особенно при вероятности внутричерепных осложнений. Пазуху пунктируют с помощью специальной иглы, удаляют гнойное содержимое, промывают полость. В некоторых случаях после этого в пазуху вводится тонкая трубка – дренаж.
Положительные эффекты дренирования пазухи:
- обеспечение постоянного оттока гнойного экссудата;
- дополнительное поступление воздуха в полость пазухи, что угнетающе действует на болезнетворные микроорганизмы;
- устранение отрицательного давления в пазухе, что улучшает отток содержимого;
- возможность регулярного промывания полости растворами лекарственных средств.
Дренирование верхнечелюстной пазухи можно провести и без прокола с помощью специального катетера ЯМИК.
После ликвидации гнойного воспаления назначают физиопроцедуры (УВЧ, УФО, электрофорез) для улучшения кровоснабжения пазухи и ускорения эвакуации остаточного содержимого.
Лечение гнойного гайморита при хроническом течении процесса требует значительных затрат времени. Обострения лечатся по тем же принципам, что и острое воспаление верхнечелюстной пазухи. Важно удаление очагов хронического воспаления в полости рта и носоглотке, лечение кариеса. Назначаются иммуностимулирующие средства.
В период ремиссии используется физиотерапия, санаторное лечение.
В тяжелых случаях заболевания выполняется хирургическое вмешательство – гайморотомия. Операция включает вскрытие пазухи и тщательное очищение ее стенок. Помимо традиционной методики, применяется эндоскопическая техника гайморотомии. Такая операция сопровождается минимальным повреждением тканей, коротким восстановительным периодом и отсутствием тяжелых осложнений.
Профилактика
Для профилактики гнойного гайморита рекомендуется:
- вовремя лечить ОРЗ, не допуская осложнений в виде синусита;
- проводить терапию хронического тонзиллита, кариеса зубов и других очагов инфекции;
- исправлять деформацию носовой перегородки, удалять полипы;
- повышать неспецифическую резистентность организма путем витаминизированного питания, закаливания, физической активности и отказа от вредных привычек.
Всех пациентов с острым и хроническим гайморитом мы приглашаем на лечение в платное отделение нашего медицинского центра. Здесь проводится тщательная диагностика и лечение по современным стандартам, с учетом индивидуальных особенностей каждого больного. В нашем центре работают ЛОР-врачи с большим опытом и высоким уровнем квалификации, что позволяет им лечить гайморит с хорошими результатами.
Лечение гнойных ран
Лечение гнойных ран состоит из местного и общего лечения. Характер лечения, кроме того, определяется фазой раневого процесса.
Местное лечение
Задачи лечения в фазе воспаления
В первой фазе раневого процесса (фаза воспаления) перед хирургом стоят следующие основные задачи:
• борьба с микроорганизмами в ране;
• обеспечение адекватного дренирования экссудата;
• содействие скорейшему очищению раны от некротических тканей;
• снижение проявлений воспалительной реакции.
При местном лечении гнойной раны используют методы механической, физической, химической, биологической и смешанной антисептики.
При нагноении послеоперационной раны обычно бывает достаточно снять швы и широко развести её края. При выраженном воспалении и обширном некрозе в гнойной ране необходимо выполнение вторичной хирургической обработки (ВХО) раны.
Вторичная хирургическая обработка раны
Показанием к ВХО раны является наличие гнойной раны при отсутствии адекватного оттока из неё (задержка гноя) или образовании обширных зон некроза и гнойных затёков. Противопоказанием служит только крайне тяжёлое состояние больного, при этом ограничиваются вскрытием и дренированием гнойного очага.
Задачи, стоящие перед хирургом, выполняющим ВХО раны:
• вскрытие гнойного очага и затёков;
• иссечение нежизнеспособных тканей;
• осуществление адекватного дренирования раны.
Перед началом ВХО следует определить видимые границы воспаления, локализацию гнойного расплавления, наиболее короткий доступ к нему с учётом расположения раны, а также возможные пути распространения инфекции (по ходу сосудисто-нервных пучков, мышечно-фасциальных влагалищ). Кроме пальпаторного исследования, применяют различные виды инструментальной диагностики: ультразвуковой, термографический, рентгеновский (при остеомиелите) методы, КТ.
Как и первичная хирургическая обработка, ВХО является самостоятельным оперативным вмешательством. Её выполняют в операционной бригадой хирургов с использованием обезболивания. Только адекватная анестезия позволяет решить все задачи ВХО. После вскрытия гнойного очага проводят тщательную инструментальную и пальцевую ревизию по ходу самой раны и возможного нахождения затёков, которые в последующем также вскрывают через основную рану или контрапертуру и дренируют. Выполнив ревизию и определив объём некроза, производят эвакуацию гноя и иссечение нежизнеспособных тканей (некрэктомия). При этом нельзя забывать, что вблизи или в самой ране могут находиться крупные сосуды и нервы, которые необходимо сохранить. Перед окончанием операции полость раны обильно промывают антисептическими растворами (пероксид водорода, борная кислота и др.), рыхло тампонируют марлевыми тампонами с антисептиками и дренируют. Наиболее выгодным способом лечения при обширных гнойных ранах является проточно-промывное дренирование. В случае локализации повреждения на конечности необходима иммобилизация. Чаще используют гипсовую лонгету.
В табл. 4-2 представлены основные отличия ПХО и ВХО раны.
Лечение гнойной раны после операции
После выполнения ВХО или простого раскрытия (вскрытия) раны на каждой перевязке врач осматривает рану и оценивает её состояние, отмечая динамику процесса. Края обрабатывают спиртом и йодсодержащим раствором. Полость раны очищают марлевым шариком или салфеткой от гноя и свободно лежащих секвестров, острым путём иссекают некротические ткани. Затем следует промывание антисептиками (3% раствор перекиси водорода, 3% раствор борной кислоты, нитрофурал и др.), дренирование (по показаниям) и рыхлое тампонирование с использованием различных антисептических средств.
Таблица 4-2. Отличия первичной и вторичной хирургической обработки раны
Основные мероприятия по лечению гнойной раны в фазе воспаления связаны с необходимостью осуществления оттока экссудата и борьбы с инфекцией. Поэтому применяют гигроскопические повязки, возможно использование гипертонического раствора (10% раствор хлорида натрия). Основными антисептическими средствами являются 3% раствор борной кислоты, 0,02% водный раствор хлоргексидина, 1% раствор гидроксиметилхиноксилиндиоксида, нитрофурал (раствор 1:5000).
В первой фазе заживления, когда имеется обильная экссудация, нельзя применять мазевые препараты, так как они создают препятствие оттоку отделяемого, в котором находится большое количество бактерий, продуктов протеолиза, некротических тканей. Лишь на 2-3-и сутки возможно применение водорастворимых мазей на полиэтиленоксидной основе. В их состав введены различные антимикробные препараты: хлорамфеникол, гидроксиметилхиноксилиндиоксид, метронидазол + хлорамфеникол, нитрофурал, диэтиламинопентилнитрофурил винилхинолин карбоксамид, мафенид (10% мазь мафенида). Кроме того, в состав мазей входят такие препараты, как тримекаин, с целью обезболивающего эффекта и метилурацил, обладающий анаболической и антикатаболической активностью, с целью стимуляции процессов клеточной регенерации.
Определённое значение в лечении гнойных ран имеет «химическая некрэктомия» с помощью протеолитических ферментов, оказывающих некролитическое и противовоспалительное действия. Для этого используют трипсин, химотрипсин. Препараты засыпают в рану в сухом виде или вводят в растворе антисептиков. Для активного удаления гнойного экссудата непосредственно в рану укладывают сорбенты, наиболее распространённым из них является лигнин гидролизный.
С целью повышения эффективности ВХО и дальнейшего лечения гнойных ран в современных условиях применяют разнообразные физические методы воздействия. Широко используют ультразвуковую кавитацию ран, вакуумную обработку гнойной полости, обработку пульсирующей струёй, различные способы применения лазера. Все эти методы преследуют цель ускорения очищения от некротических тканей и губительного воздействия на микробные клетки.
Лечение в фазе регенерации
В фазе регенерации, когда рана очистилась от нежизнеспособных тканей и стихло воспаление, приступают к следующему этапу лечения, основными задачами которого являются стимуляция репаративных процессов и подавление инфекции.
Во второй фазе заживления процесс образования грануляционной ткани играет ведущую роль. В этом периоде при отсутствии осложнений экссудация резко сокращается и необходимость в гигроскопичной повязке, применении гипертонических растворов и дренировании отпадает. Грануляции очень нежные и ранимые, поэтому становится необходимым применение препаратов на мазевой основе, препятствующей механической травматизации. Наиболее эффективны мази, содержащие стимулирующие вещества (5% и 10% метилурациловая мазь). Однако, несмотря на то, что грануляционная ткань выполняет и защитную функцию, полностью исключить возможность повторного развития инфекционного процесса нельзя. Поэтому во время перевязок раны продолжают промывать растворами антисептиков, используют мази, эмульсии и линименты, включающие антибиотики (хлорамфениколовая, тетрациклиновая, гентамициновая мази и др.). Широкое применение находят многокомпонентные мази, содержащие противовоспалительные, антисептические, стимулирующие регенерацию и улучшающие региональное кровообращение вещества (гидрокортизон + окситетрациклин, бальзамический линимент по А.В. Вишневскому).
Для ускорения заживления ран используют методику наложения вторичных швов (ранних и поздних), а также стягивание краёв раны лейкопластырем.
Лечение ран в фазе образования и реорганизации рубца
В третьей фазе заживления основными задачами становятся ускорение эпителизации раны и защита её от излишней травматизации. С этой целью используют повязки с индифферентными и стимулирующими мазями, а также физиотерапевтические процедуры.
Физиотерапия
Физиотерапевтические процедуры занимает значительное место в лечении гнойных ран. В первой фазе для купирования острых явлений воспаления, уменьшения отёка, болевого синдрома, ускорения отторжения некротизированных тканей используют электрическое поле УВЧ и УФО в эритемной дозе, которое также стимулирует фагоцитарную активность лейкоцитов и оказывает антимикробное действие. Для местного введения антибиотиков, ферментов, противовоспалительных и обезболивающих препаратов используют электро- и фонофорез. Следует помнить, что при недостаточном оттоке гнойного содержимого физиотерапевтические процедуры приводят к усугублению гнойно-воспалительного процесса.
Во второй и третьей фазах раневого процесса с целью активизации репаративных процессов и эпителизации применяют УФО и лазерное облучение расфокусированным лучом. Сосудорасширяющим и стимулирующим действиями обладает магнитное поле: при воздействии пульсирующим магнитным полем уменьшается размер рубца.
В течение всего периода раневого процесса возможно применение гипербарической оксигенации, улучшающей насыщение тканей кислородом.
Лечение в абактериальной среде
При обширных раневых дефектах и ожогах с успехом применяют лечение в управляемой абактериальной среде. Существуют изоляторы общего и местного типов, изоляция всего пациента необходима при лечении больных с пониженной устойчивостью к инфекции: после онкологических операций, сопровождающихся массивной химиотерапией или лучевым лечением; при трансплантации органов, сопряжённой с постоянным приёмом иммунодепрессантов, сдерживающих реакцию отторжения; различных заболеваниях крови, вызывающих нарушение и угнетение лимфопоэза.
Лечение в абактериальной среде проводят без наложения повязки, что способствует высушиванию раны, которое неблагоприятно воздействует на микроорганизмы. В изоляторе поддерживают следующие параметры: температура 26-32°С, избыточное давление 10-15 мм рт. ст, относительная влажность 50-65%. Параметры могут изменяться в зависимости от характера течения раневого процесса.
Лечение специальными повязками
В современной практике местного лечения как чистых, так и гнойных ран всё чаще применяют методику с использованием готовых повязок отечественного и зарубежного производства, содержащих многокомпонентные наполнители. В состав повязок для применения в I фазе входят препараты, способные поглощать раневой экссудат, адсорбировать бактериальные клетки и токсины, способствовать лизису некротических масс. В повязках для II и III фаз содержатся наполнители, обеспечивающие защиту грануляций и «молодого» рубца, стимуляцию репаративных процессов. Данную методику применяют и для временного закрытия обширных раневых поверхностей с целью сокращения потерь белка, электролитов, жидкости. Наиболее распространёнными повязками в настоящее время являются Васкопран, Альгипор, Сорбалгон, Суспурдерм, Гидроколл и др.
Общее лечение
Общее лечение раневой инфекции имеет несколько направлений:
• антибактериальная терапия;
• дезинтоксикация;
• иммунокорригирующая терапия;
• противовоспалительная терапия;
• симптоматическая терапия.
Антибактериальная терапия
Антибактериальная терапия является одним из компонентов комплексной терапии гнойных заболеваний и, в частности, гнойных ран. Применяют её в основном в I, а также во II и III фазах раневого процесса.
При отсутствии у больного признаков интоксикации, небольших размерах раны, сохранении целостности костных структур, магистральных сосудов и отсутствии сопутствующих заболеваний обычно достаточно только местного лечения. В иной ситуации антибактериальную терапию следует начать как можно раньше.
Одним из основных принципов терапии является применение препарата, к которому чувствительна микрофлора раны. Но с момента забора материала до получения результатов исследования порой проходят не одни сутки. Тогда желательно введение антибиотика, к которому обычно наиболее чувствительна предполагаемая инфекция. В таком случае может помочь определение характерных особенностей гноя, присущих какому-либо микроорганизму.
Стафилококки чаще всего образуют густой гной желтоватого оттенка, стрептококки — жидкий гной жёлто-зелёного цвета или типа сукровицы, кишечная палочка — гной коричневого цвета с характерным запахом, синегнойная палочка даёт соответствующее окрашивание повязок и сладковатый запах (сходными признаками обладает гной, образованный протеем, но обычно не имеет зелёного цвета). Нельзя забывать, что в гнойной ране чаще встречается смешанная инфекция, поэтому предпочтительнее на начальных этапах назначение антибактериальных препаратов широкого спектра действия. После определения чувствительности можно сменить антибиотик.
В антибактериальную терапию входят также строго направленные против определённых бактерий или их групп препараты. Находят своё применение различные бактериофаги — стрептококковый, стафилококковый, протейный, синегнойный, колифаг, а также комплексные фаги, например пиофаг, состоящий из нескольких видов бактериофагов. С целью пассивной иммунизации вводят антистафилококковый γ-глобулин, различные виды плазм [гипериммунную антистафилококковую, антиэширихиозную, антисинегнойную и антилипополисахаридную (против грамотрицательных микроорганизмов].
Дезинтоксикация
Большой объём некроза и развивающаяся инфекция обусловливают насыщение организма токсинами. У больного с гнойной раной в I фазе раневого процесса проявляются все признаки интоксикации (озноб, лихорадка, потливость, слабость, головная боль, отсутствие аппетита), на- растают воспалительные изменения в анализах крови и мочи. Всё это служит показанием к проведению дезинтоксикационной терапии, которая включает следующие методы (по нарастанию их сложности и эффективности):
• инфузия солевых растворов;
• метод форсированного диуреза;
• применение дезинтоксикационных кровезамещающих растворов;
• экстракорпоральные способы детоксикации.
Выбор способа зависит прежде всего от выраженности интоксикации и тяжести состояния пациента.
В фазе регенерации и образования рубца необходимости в проведении дезинтоксикационной терапии обычно нет.
Иммунокорригирующая терапия
При возникновении в ране гнойного процесса, развитии интоксикации часто возникает снижение сопротивляемости организма с падением уровня выработки антител, фагоцитарной активности, дефицитом субпопуляций лимфоидных клеток и замедлением их дифференцировки. К этому приводит и длительное применение мощных антибактериальных препаратов. Данные изменения способствуют дальнейшему развитию инфекции, увеличению зоны вторичного некроза и прогрессирующему ухудшению состояния больного.
С целью коррекции этого временного дефицита применяют иммуномодуляторы. Наиболее широко используют интерфероны, левамизол, препараты вилочковой железы. Тем не менее, при длительном введении и больших дозах эти препараты подавляют выработку собственных иммунных клеток. В последнее время всё большее внимание уделяют созданным методом генной инженерии цитокинам, в частности интерлейкинам, имеющим широкие показания к применению при иммунодефицитных состояниях. Созданы и используются в лечении человеческие рекомбинантные интерлейкин-1 и интерлейкин-2.
Активную иммунизацию анатоксинами и вакцинами используют с профилактической целью, дабы подготовить больного к борьбе с инфекцией собственными силами. Обычно применяют стафилококковый анатоксин, поливалентную синегнойную вакцину и др.
Противовоспалительная терапия
Противовоспалительная терапия не является ведущим способом лечения ран, применяется достаточно редко и сводится к введению глюкокортикоидов и нестероидных противовоспалительных средств. Кроме обезболивающего действия, эти препараты способствуют уменьшению проявления воспаления, снижению отёка, повышению перфузии и оксигенации окружающих рану тканей, улучшению их метаболизма. Это приводит к ускорению образования линии демаркации и скорейшему очищению от некроза.
Симптоматическая терапия
В фазе воспаления за счёт отёка тканей развивается болевой синдром. Поэтому при необходимости вводят анальгетики (обычно ненаркотические). При лихорадке применяют жаропонижающие средства. При значимой кровопотере проводят переливание компонентов крови и кровезамещающих растворов.
При обширных раневых дефектах с потерей через их поверхность жидкости, белков и электролитов в инфузионную замещающую терапию включают белковые гидролизаты, нативную плазму, смеси аминокислот и полиионные растворы. В общеукрепляющую терапию входят витамины различных групп (С, В, Е, А) и стимуляторы регенерации (метилурацил, оротовая кислота, анаболические гормоны). У больных с выраженными нарушениями деятельности различных органов и систем вследствие травмы или осложнений гнойной раны необходима их коррекция.
Одновременно проводят лечение сопутствующих заболеваний, ухудшающих общее состояние больного и заживление раны (коррекция сахарного диабета, нормализация кровообращения и т.д.).
Раны с обильным или гнойным дренажом
Рана с обильным или гнойным дренажом — это локализованный дефект или выемка кожи или подлежащих мягких тканей, которая дает большое количество серозных , кровяных , серозно-кровяных или гнойных выделений . Гнойный дренаж из раны густой желтого, зеленого или коричневого цвета с резким, сильным, зловонным, фекальным или затхлым запахом. Гнойный дренаж — признак нездоровой раны и требует лечения.
Симптомы гнойного дренажа
Для большинства ран небольшое количество жидкого экссудата бледного цвета является нормальным. Поскольку все раны загрязнены, с некротической тканью или без нее, они будут иметь запах. Бактерии разных видов имеют разный запах, цвет и консистенцию, а мертвые ткани в ране вносят дополнительные бактерии в пораженный участок. Увеличение количества или консистенции экссудата вместе с изменением цвета указывает на повод для беспокойства, а также на изменение запаха.
Рисунок 1: Зачеркание раневого экссудата
Рисунок 2: Лечение экссудата, язва ноги с сильным дренированием
Рисунок 3: Удаление раневой повязки неэффективно для управления экссудатом
Этиология
Экссудат или дренаж раны — это результат расширения кровеносных сосудов на ранней воспалительной стадии заживления, возможно, вызванный присутствием определенных бактерий. Пытаясь залечить рану, организм создает и поддерживает оптимальную влажную среду в ране.Экссудат — это производная сыворотки с высоким содержанием белка и различными добавками, способствующими заживлению; Экссудат состоит из мертвых клеток и разжиженных некротических остатков, активных лейкоцитов, факторов роста и естественных ферментов, которые стимулируют автолиз и заживление, по крайней мере, когда они присутствуют в острой ране.
Факторы риска
Во всех ранах должна наблюдаться некоторая форма экссудации, но из некоторых может выделяться больше, чем из других, из-за любого числа факторов, включая расположение раны, давление, гидростатическое давление, температуру, инфекцию, размер раны, использованные повязки и тип раны.Пациенты с диабетом, невропатией или сосудистыми заболеваниями подвергаются более высокому риску хронических ран и повышенного дренирования ран.
Осложнения
Состав экссудата из хронических ран отличается от состава экссудата из острых ран и может способствовать дальнейшему воспалению и препятствовать росту и заживлению.
Диагностические исследования
Оценка объема и внешнего вида экссудата может многое рассказать врачу о ходе заживления раны. Эта оценка раны может включать в себя отслеживание количества смен повязок, необходимых в день, и визуальный осмотр снятой повязки.Некоторую клиническую преемственность можно поддерживать с помощью инструмента оценки, такого как континуум экссудата.
Лечение ран тяжелым или гнойным дренажом
При лечении необходимо соблюдать баланс между сдерживанием сильного дренажа и предотвращением мацерации и поддержанием влажной среды раны. Ответы должны варьироваться в зависимости от потребностей пациента, типа и местоположения раны и от того, на какой стадии процесса заживления находится рана. Существует множество доступных повязок, позволяющих правильно сочетать повязку и потребности раны.При ранах с венозной недостаточностью компрессия и возвышение могут быть полезны для улучшения кровообращения и подавления экссудата. У некоторых обильных дренажей может быть основная причина, которую можно лечить, например, инфекция. Некоторые более глубокие или туннельные раны с экссудатом могут подходить для лечения ран с отрицательным давлением.
Список литературы
Краснер Д. Уход за хроническими ранами 5. HMP Communications; 2012.
Морган Н. Типы раневого экссудата. Консультант по уходу за раной. 2012; Июнь.
Белый R, Раскрой KF.Современное управление экссудатом: обзор методов лечения ран. Всемирные раны. 2006.
White R. Управление экссудатом. Время ухода. 2001. 97 (9): 11.
.Источник изображения: Medetec (www.medetec.co.uk). Используется с разрешения.
Гной: виды, причины, лечение, профилактика
Гной — это густое жидкое вещество, которое образуется в результате воспалительной реакции организма на инфекцию. Он состоит из скоплений дегенерирующих лейкоцитов, мертвых или живых бактерий (или других микроорганизмов) и остатков тканей.Гной обычно непрозрачного бело-желтого цвета, но может иметь коричневый или даже зеленый оттенок. Обычно он не имеет запаха, хотя некоторые виды бактерий выделяют гной с неприятным запахом.
Медицинский термин для обозначения гноя — гнойный экссудат. Его также иногда называют гнойным дренажом, а жидкость иногда называют ликвором.
Небольшое количество гноя, например от прыщей, обычно не является поводом для беспокойства, но гной на месте раны, хирургического разреза или глубокого внутреннего расположения может потребовать медицинского вмешательства.Лечение гнойных инфекций может включать прием антибиотиков, дренажные процедуры или хирургическое удаление инфицированных тканей.
Гной — это густое белое вещество, которое обычно является признаком инфекции. Медицинский термин для обозначения гноя — гнойный экссудат. Его также иногда называют гнойным дренажом; жидкость иногда называют ликером пури.
Функция
Гной — это признак того, что ваше тело начало бороться с инфекцией, посылая в эту область клетки, борющиеся с инфекцией.
Гной часто является частью абсцесса, скоплением гноя в полости, образовавшейся в результате разрушения инфицированных тканей. Абсцессы могут возникать непосредственно под кожей или в любом месте тела и обычно являются результатом проникновения бактерий, таких как Streptococcus или Staphylococcus aureus , в ткани, например через небольшое отверстие в коже.
Грибок или паразиты также могут привести к абсцессам. Как только бактерии или другие микроорганизмы начинают размножаться, они выделяют токсины, разрушающие клетки.Это вызывает иммунный ответ, при котором лейкоциты (белые кровяные тельца) направляются к месту, чтобы убить и поглотить бактерии и разрушить мертвые ткани. Во время этого процесса белые кровяные тельца также разрушаются и умирают, образуя гной.
Типы
Гной может быть виден на поверхности кожи или образовываться внутри как осложнение инфекции или травмы.
Кожная инфекция
Типы кожных заболеваний, характеризующиеся гноем на поверхности кожи или непосредственно под ней, включают:
- Угри: Поры, забитые маслом и мусором, образуют на поверхности кожи прыщики или пустулы, содержащие гной.
- Фолликулит: Маленькие прыщики на инфицированных волосяных фолликулах
- Фурункулы или фурункулы: Болезненные узелковые образования на инфицированных волосяных фолликулах, которые обычно вызываются Staphylococcus aureus
- Карбункулы, соединенные Группа A
- Поверхностная инфекция области хирургического вмешательства (SSI): SSI находится только на уровне кожи, где вдоль разреза может образовываться гной, который при прикосновении может стать красным и болезненным.
- Травматические раны: Гной и желтая корка на месте раны, вызванные травмой или физической травмой, могут сопровождаться болью или опухолью.
Внутренняя инфекция
Гнойные абсцессы могут образовываться внутри, например, во рту или рядом с внутренними органами. Это может быть результатом хирургического осложнения, травмы или невылеченной бактериальной или грибковой инфекции. Существует множество типов внутренних абсцессов и состояний, которые могут привести к гною, в том числе:
- Абсцессный зуб : Зубная инфекция в корне зуба или рядом с ним
- Глубокий SSI: Инфекция может возникать внутри мышц и других тканей или может образовываться в органе или зоне операции
- Перитонзиллярный абсцесс : Пятна гноя в задней части глотки или за миндалинами могут формироваться как симптом ангины или ангины
- Эмпиема : скопление гноя в плевральной полости между легкими и грудной клеткой стенка, которая может быть осложнением бактериальной пневмонии или операции на легких
- Абсцесс головного мозга : Редкий гнойный отек мозга, который может быть вызван бактериальной или грибковой инфекцией
- Септический артрит : серьезная инфекция суставов которые могут образоваться после того, как бактерии попадают с кровотоком в сустав
Причины
Проколы, царапины, царапины или другие отверстия на коже могут позволить бактериям, живущим на коже, проникнуть в организм и вызвать инфекцию.Сюда входят хирургические разрезы. Также могут быть глубокие внутренние инфекции с гноем, возникающие после операций, травм или болезней.
Существуют определенные факторы и основные состояния, которые могут подвергнуть вас риску инфекций и гнойных осложнений:
- Плохая гигиена, например, не мыть руки перед прикосновением к ране
- Диабет
- Пожилой возраст
- Курение
- Тяжелое ожирение
- Нарушение иммунной системы, ВИЧ-инфекция или рак
- Лекарства, снижающие активность иммунной системы, такие как кортикостероиды или иммунодепрессанты
- Паралич или ограниченная подвижность
- Низкая температура тела
- Длительные операции и госпитализация
- Экстренные процедуры
У людей с ослабленной иммунной системой гной может никогда не образовываться в инфицированной области, но большинство обнаружит, что инфекция приводит к выделениям из этой области, а также к возможности покраснения, боли или болезненности, отека и лихорадки.
Лечение
Большинство ИОХВ и кожных ран лечат пероральными антибиотиками или мазями. Антибиотики важны, потому что они помогают организму быстрее заживать и могут предотвратить обострение инфекции.
Лаура Портер / ВеривеллВаш врач может собрать дренаж из раны и отправить его в лабораторию, чтобы определить, какой тип бактерий вызывает инфекцию. Этот процесс, называемый тестом на культуру и чувствительность , может использоваться для определения того, к какому антибиотику чувствительны бактерии и который может наиболее эффективно уничтожить бактерии.
В случае послеоперационного гноя ваш врач может порекомендовать специальную программу ухода за надрезом и, возможно, захочет увидеть ваш разрез, чтобы убедиться, что нет основной проблемы.
В некоторых случаях для устранения инфекции может потребоваться процедура дренирования абсцесса для удаления гноя или хирургическая обработка раны (удаление мертвой ткани).
В случае сепсиса, опасного и опасного для жизни состояния, при котором инфекция попадает в кровоток и может распространяться по всему телу, потребуется госпитализация.
Профилактика
Есть простые вещи, которые вы можете сделать, чтобы снизить риск развития гнойной инфекции:
- Осторожно промойте порезы и другие раны водой с мылом.
- Следуйте инструкциям врача после операции или госпитализации при травмах.
- Мойте руки регулярно и тщательно.
- Не выдавливайте гной из прыщей или нарывов. Вместо этого аккуратно прикладывайте теплый компресс несколько раз в день.
- Не делитесь полотенцами или бритвой
- Соблюдайте здоровую сбалансированную диету
- Будьте бдительны в отношении контроля уровня сахара в крови, если у вас диабет
- Бросьте курить
Агрессивная очистка инфицированной кожи может принести больше вреда, чем пользы, потому что раздраженная рана легче инфицируется, а также будет более нежной или даже болезненной.То же самое касается таких поражений, как прыщи или нарывы. Относитесь к любому состоянию кожи так же бережно, как к спине ребенка.
Подготовка к операции
По данным Центров по контролю и профилактике заболеваний, от 1% до 3% людей, перенесших операции, заболевают инфекцией. Есть шаги, которые вы можете предпринять до и после любой процедуры, чтобы снизить риск SSI.
Перед операцией-
В ночь перед операцией вымойте все тело с мылом в ванне или душе.
-
Не бриться рядом с местом проведения операции, так как это может вызвать раздражение кожи и повысить предрасположенность к инфекции. (Ваш врач может использовать электрическую машинку для стрижки волос непосредственно перед операцией, чтобы удалить волосы в этой области.)
-
Семья или друзья должны всегда мыть руки перед посещением и не трогать рану, если только они не ухаживают за вашей раной
-
Следуйте инструкциям по уходу за раной во время и после выписки из больницы
-
Всегда мойте руки до и после ухода за раной
-
Большинство хирургических инфекций происходит в течение месяца.В течение этого времени ежедневно проверяйте разрез на наличие признаков инфекции.
-
Не трите разрез, не смазывайте его мазью с антибиотиком и не очищайте спиртом или перекисью, если это не рекомендовано вашим врачом.
Следите за тем, чтобы разрез оставался сухим и закройте его чистой повязкой. Вы можете оставить его непокрытым, но если дренаж протекает с участка, это может испачкать одежду и создать больше беспорядка, чем необходимо. В общем, делайте то, что рекомендовано в ваших инструкциях по уходу за разрезом после операции, если вам не сказано иное.
Когда звонить врачу
Всегда обращайтесь к врачу, если вы видите гной, особенно после физической травмы или операции, или если у вас есть покраснение или боль в ране, поскольку все это признаки инфекции.
Хирургический разрез с гноем нельзя игнорировать, но многие виды дренажа — это нормально. Прозрачная жидкость или жидкость с оттенком крови, которая в значительной степени прозрачная, считается нормой, если из раны не выходит большое количество.
Если у вас мутный или бело-желтый дренаж, его следует немедленно осмотреть врач.Это не означает, что крошечное пятнышко белого дренажа должно привести к вызову 911 в 2 часа ночи, но нельзя игнорировать гной в течение нескольких дней. Игнорирование инфекции может привести к серьезным проблемам, более длительному выздоровлению и большему количеству рубцов. Вызов вашего врача или хирурга должен быть приоритетом.
Если у вас есть рана или хирургический разрез и вы испытываете какие-либо симптомы гриппа, даже без гноя, обратитесь за неотложной медицинской помощью. Нелеченные инфекции могут подвергнуть вас риску серьезных или даже опасных для жизни состояний, таких как сепсис, и их нельзя игнорировать.
Предупреждающие знаки
Обратитесь за неотложной медицинской помощью, если у вас есть какие-либо из следующих симптомов ИОХВ или сепсиса:
- Покраснение и боль в области раны или операции
- Мутный дренаж из раны или разреза
- Лихорадка
- Путаница или дезориентация
- Одышка
- Высокая частота пульса
- Дрожь
- Сильная боль или дискомфорт или
- Липкая или потная кожа
Слово Verywell
Одна из самых важных вещей, которые вы можете сделать, чтобы избежать заражения гноем, — это часто мыть руки.Это очень важно до и после ухода за неровностями кожи, разрезами или ранами. Если предотвратить инфекцию уже слишком поздно, следуйте указаниям врача, чтобы ускорить заживление и свести к минимуму повреждение тканей и осложнения.
Если у вас есть рана, выделите время, чтобы правильно ее очистить, регулярно проверяйте рану на наличие каких-либо признаков инфекции и при необходимости защищайте ее.
Инфекции кожи и мягких тканей
Резюме
Инфекции кожи и мягких тканей (SSTI) — это группа гетерогенных состояний, поражающих эпидермис, дерму, подкожную ткань или поверхностную фасцию.Неосложненные инфекции чаще всего вызываются грамположительными патогенами (Streptococcus, Staphylococcus), которые проникают в кожу после незначительных травм (например, царапин, укусов насекомых). Осложненные инфекции имеют более высокую тенденцию быть полимикробными. SSTI в основном проявляются болезненными, теплыми, эритематозными кожными поражениями, а также могут привести к скоплению гнойной жидкости и / или некрозу пораженной ткани. Системные симптомы, такие как лихорадка, обычно являются признаком более тяжелых инфекций. Факторы риска развития SSTI (или более тяжелых форм SSTI) включают сахарный диабет, иммунодефицит и хронический отек.Диагностика в основном клиническая, но некоторым пациентам может потребоваться визуализация или лабораторные исследования. Гнойные инфекции, такие как абсцессы, в первую очередь лечат с помощью разреза и дренажа, в то время как негнойные инфекции (например, рожа, целлюлит) требуют лечения антибиотиками. Некротические инфекции мягких тканей (NSTI) имеют высокий уровень смертности; они требуют неотложной хирургической помощи и требуют немедленной обработки раны.
Обзор
Поражение тканей SSTI (от поверхностного к глубокому): импетиго (поверхностный эпидермис), рожа (поверхностная дерма и лимфатические сосуды), целлюлит (глубокая дерма и подкожная клетчатка), некротический фасциит (поверхностная фасция)
Кардинальные признаки воспаления
Факторы риска инфекций кожи и мягких тканей
[1]- Местные факторы
- Системные факторы
- Повышенное воздействие патогенов
- Нозокомиальные патогены (например,g., длительная госпитализация, операция)
- Воздействие воды (например, морская вода, горячие ванны)
- Долгосрочные внутрисосудистые устройства [2]
- Травма (например, открытые раны, открытые переломы)
Осложнения
- Местное распространение инфекции
- Системное вовлечение с лихорадкой и возможным сепсисом (подробные сведения о лечении тяжелых инфекций см. В разделе «Сепсис»)
- Распространение инфекции на отдаленные участки (см. «Стафилококковые инфекции»)
Гнойные инфекции кожи и мягких тканей
- Определения
- Клинические особенности
- Дифференциальный диагноз
Фурункулы на лице могут привести к серьезным осложнениям (например, к тяжелым осложнениям).г., периорбитальный целлюлит, тромбоз кавернозного синуса).
Абсцесс кожи
[3] [4]- Определение: скопление бело-желтого гноя, содержащее белки, лейкоциты (особенно нейтрофилы), бактерии и клеточный мусор, расположенное в дерме и подкожной клетчатке.
- Клинические особенности
- Дифференциальный диагноз: воспаленная эпидермоидная киста, карбункул.
-
Подтипы и варианты
- Рецидивирующий абсцесс кожи: новый абсцесс на месте перенесенной инфекции
- Сложный кожный абсцесс: кожный абсцесс, требующий специального лечения из-за его расположения (например,g., перианальный, периректальный), вовлеченные патогены (например, полимикробные, устойчивые патогены) или характеристики пациента (например, иммунодефицит) [4]
- Абсцесс мошонки: подкожное скопление гноя в области мошонки, обычно в результате воспаления волосяных фолликулов
При абсцессе мошонки и эпидидимите классические признаки воспаления являются заметными и помогают подтвердить диагноз.
Этиология
[3]Диагностика
[1] [3]Диагноз обычно клинический.Пациентам с системными симптомами могут быть показаны лабораторные исследования, посев и визуализация для оценки степени тяжести и индивидуального лечения.
- Лабораторные исследования
-
Изображение [8]
-
УЗИ мягких тканей
- Показания включают:
- Системные признаки инфекции (т. Е. Умеренное или тяжелое заболевание)
- Подтверждение диагноза до разреза и дренирования абсцесса
- Оценка размера, степени и глубины абсцесса [9] [10]
- Предполагаемый посторонний предмет в месте заражения (например,г., кончик иглы, заноза)
- Подозрение на сложный абсцесс кожи
- Возможные результаты [11]
- Показания включают:
- КТ / МРТ с внутривенным контрастом или без него: обычно требуется только для сложных кожных абсцессов (например, перианального абсцесса) и оценки осложнений (например, остеомиелита)
-
УЗИ мягких тканей
- Микробиология
- Дополнительная оценка: рассмотрите возможность дополнительной оценки основных состояний у пациентов с рецидивирующим абсцессом и / или сложным абсцессом кожи.
Лечение гнойных SSTI
Разрез и дренирование; являются основой лечения гнойных ИППП и обычно достаточны для легких инфекций. Пациентам с системными признаками инфекций требуется эмпирическая антибактериальная терапия; и, в тяжелых случаях, госпитализация для внутривенной терапии. Если они выполнены, микробиологические исследования могут быть использованы для корректировки режимов антибиотикотерапии.
Интервенционная терапия
[3] [4]- Разрез и дренаж (I&D)
-
Хирургический дренаж
- Обычно выполняется в операционной
- Показания включают:
Антибактериальная терапия
[3] [4]Легкие гнойные инфекции кожи обычно не требуют системного лечения антибиотиками после дренирования.
Поддерживающие меры
- Теплые компрессы (при фолликулитах, фурункулах и карбункулах)
- Покой и обезболивание по мере необходимости
- Держите пораженный участок чистым и сухим. [11]
- Рассмотрите возможность деколонизации MRSA при рецидивирующих абсцессах. [13]
- Рассмотрите возможность стационарного лечения пациентов с системными симптомами.
- См. «Сепсис» для получения дополнительной информации о ведении тяжелых инфекций.
Контрольный список неотложной помощи при гнойных инфекциях средней и тяжелой степени
Негнойные инфекции кожи и мягких тканей
Определения
[3] [4]Клинические особенности
[3] [4]- Местные признаки: эритема, отек, тепло, болезненность
- Специфично для рожи: приподнятое, резко очерченное поражение.
- Специфично для целлюлита: плохо выраженное поражение с уплотнением
- Кожный лимфатический отек (исторически называемый «апельсиновый апельсин»)
- Обычные места: нижние конечности, лицо
- Возможные дополнительные признаки
- Системные симптомы (при умеренных / тяжелых инфекциях): лихорадка, озноб, спутанность сознания , тошнота, головная боль, боль в мышцах и суставах
Патофизиология
[3] [4]- Попадание обычно происходит через незначительное повреждение кожи; Следовательно, рожа может распространяться по поверхностным лимфатическим сосудам.
- Может также быть вторичным по отношению к системной инфекции.
Как при рожистом воспалении, так и при целлюлите наиболее частой точкой проникновения патогена является небольшое поражение кожи (например, межпальцевой дерматит стопы).
Этиология
[3] [4]ГАЗ является наиболее частой причиной негнойных инфекций кожи и мягких тканей (например, рожи, целлюлита).
Диагностика
[3] [8]Диагноз обычно клинический.Пациентам с системными симптомами могут быть показаны лабораторные исследования, посев и визуализация для оценки степени тяжести и индивидуального лечения.
Лечение негнойных SSTI
[1] [3] [14]Эмпирическая терапия антибиотиками, активными против стрептококков и S. aureus, является основой лечения негнойных SSTI. Пациентам с системными симптомами часто требуется госпитализация и парентеральная антибактериальная терапия. Лечение также должно включать контроль любых предрасполагающих факторов (например,г., отеки, грибковые инфекции).
Антибактериальная терапия
Антибиотики должны быть нацелены против грамположительных патогенов и обеспечивать широкий спектр действия в тяжелых случаях. [4]
Поддерживающая терапия
- Подъем пораженных конечностей
- Отдых и лечение острой боли по мере необходимости
- См. «Сепсис» для получения более подробной информации о лечении тяжелых инфекций.
Контрольный список неотложной помощи при негнойных SSTI
Подтипы и варианты
Осложнения
[3] [4]- Рецидивирующие инфекции
- Абсцесс
- Инфекция более глубоких тканей: целлюлит, некротический фасциит, остеомиелит
- Тромбофлебит, лимфедема
- Системные осложнения (напр.г., сепсис, эндокардит, синдром стрептококкового токсического шока, постстрептококковый гломерулонефрит, острый ревматизм)
- При целлюлите глазницы: слепота, тромбоз кавернозного синуса, внутричерепной абсцесс
Некротические инфекции мягких тканей
Определения
[3] [4]Этиология
[3] [4]Единственный способ окончательно установить возбудителя — это получение глубокой тканевой культуры ( я.э., при хирургическом обследовании). Сами по себе клинические признаки недостаточно надежны, чтобы различать патогены.
Клинические признаки
[3] [4]- Системные симптомы: лихорадка, озноб, изменение психического статуса
- Кожные изменения
Некротический фасциит сначала распространяется вдоль фасции, а затем распространяется на поверхностные кожные ткани. Следовательно, местные результаты могут быть ничем не примечательными, и пациенты испытывают непропорционально высокий уровень боли.
Тревожные признаки, указывающие на некротизирующую инфекцию глубоких тканей, включают наличие крепитации, буллезных поражений, некроза кожи и признаков системной токсичности (особенно измененного психического статуса).
Диагностика
[3]Окончательный диагноз обычно ставится во время визуализации тканей во время операции. Если есть опасения по поводу некротизирующих ИСМТ, пациента следует немедленно направить в хирургическое отделение.
Визуализация и лабораторные исследования не должны откладывать операцию.
- Лабораторные исследования
- Микробиология
-
Визуализация: обычно не показано и не следует откладывать лечение [4] [8]
- КТ / МРТ с внутривенным контрастированием или без него [4]
- Рентгеновский снимок [4]
- Ультразвук: может определить скопление жидкости и диффузное утолщение глубоких тканей [4]
Посев на поверхностные раны может неточно отражать патогены, обнаруженные в глубоких тканях, и не должен использоваться для руководства.
Управление
[3] [4]- Если клинические признаки указывают на наличие ИМП, немедленно начните хирургическое лечение и лечение.
- Пациентам часто требуется гемодинамическая и респираторная поддержка и обычно требуется госпитализация в отделение интенсивной терапии; (см. «Сепсис» для получения дополнительных рекомендаций по ведению тяжелых инфекций).
Некротические инфекции мягких тканей требуют неотложной хирургической помощи.
Хирургическое обследование и обработка раны
- Процедура [4]
- Обширное обследование с хирургической обработкой раны (удаление некротизированной ткани)
- Получите образцы глубоких тканей для окрашивания по Граму, посева и гистопатологии.
- Ткань с неуверенной перфузией может быть оставлена для повторной оценки при втором вмешательстве.
- Повторное обследование каждые 12–36 часов до исчезновения признаков некротической ткани
- Дополнительные данные
- Фасция выглядит опухшей
- Тускло-серая фасция; участки некроза могут быть видны
- Возможен коричневый экссудат (без гноя)
- Простое рассечение плоскостей тканей тупым инструментом или пальцем в перчатке
Хирургическое исследование обеспечивает диагностическое подтверждение и позволяет провести хирургическое лечение.Его не следует откладывать при подозрении на NSTI!
Антибактериальная терапия
[3] [4]Поддерживающая терапия
[3] [4]Контрольный список неотложной помощи при некротизирующем эффекте SSTI
Осложнения
Дифференциальный диагноз
Антибактериальная терапия для кожи и мягких тканей инфекции
Степень тяжести SSTI
[3]| Степень серьезности SSTI [3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Степень | Характеристики | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Легкая SSTI | Средняя SSTI 70 | Средняя
Некротические инфекции всегда считаются тяжелыми!
Дифференциальный диагнозГангренозная эктима
Эризипелоид
Прочие
Перечисленные здесь дифференциальные диагнозы не являются исчерпывающими. Инфекции кожи и мягких тканей1. Hersh AL, и другие. Национальные тенденции в амбулаторных посещениях и назначении антибиотиков при инфекциях кожи и мягких тканей. Arch Intern Med . 2008; 168 (14): 1585–1591 …. 2. Паллин Д. Д., и другие.Увеличение числа посещений отделений неотложной помощи в США по поводу инфекций кожи и мягких тканей, а также изменение выбора антибиотиков во время появления метициллин-резистентного Staphylococcus aureus, связанного с населением. Энн Эмерг Мед . 2008. 51 (3): 291–298. 3. Эрон Л.Дж., и другие. Лечение инфекций кожи и мягких тканей. J Antimicrob Chemother . 2003; 52 (приложение 1): i3 – i17. 4. May AK. Инфекции кожи и мягких тканей. Surg Clin North Am . 2009. 89 (2): 403–420. 5. Стивенс Д.Л., и другие. Практические рекомендации по диагностике и лечению инфекций кожи и мягких тканей. Clin Infect Dis . 2014; 59 (2): e10 – e52. 6. Джонс МЭ, и другие. Эпидемиология и чувствительность к антибиотикам бактерий, вызывающих инфекции кожи и мягких тканей в США и Европе. Int J Антимикробные агенты . 2003. 22 (4): 406–419. 7. Стивенс Д.Л., и другие. Практические рекомендации по диагностике и лечению инфекций кожи и мягких тканей [опубликованные исправления появляются в Clin Infect Dis. 2005; 41 (12): 1830 и Clin Infect Dis. 2006; 42 (8): 1219]. Clin Infect Dis . 2005. 41 (10): 1373–1406. 8. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Неосложненные и сложные инфекции кожи и кожных структур — разработка противомикробных препаратов для лечения. http://www.fda.gov/ohrms/dockets/98fr/2566dft.pdf. По состоянию на 24 мая 2014 г. 9. Ki V, и другие. Бактериальные инфекции кожи и мягких тканей у взрослых: обзор их эпидемиологии, патогенеза, диагностики, лечения и места оказания помощи. Может ли заразить Dis Med Microbiol . 2008. 19 (2): 173–184. 10. Gabillot-Carré M, и другие. Острые бактериальные инфекции кожи и целлюлит. Curr Opin Infect Dis . 2007. 20 (2): 118–123. 11. Ковальски Т.Дж., и другие.Эпидемиология, лечение и профилактика внебольничных метициллин-устойчивых инфекций Staphylococcus aureus. Mayo Clin Proc . 2005. 80 (9): 1201–1207. 12. Май Л, и другие. Сообщается о заболеваемости инфекциями кожи и мягких тканей среди военнослужащих США. Travel Med Infect Dis . 2011; 9 (4): 213–220. 13. Decker CF. Инфекции кожи и мягких тканей у спортсмена. Dis Mon .2010. 56 (7): 414–421. 14. Suaya JA, и другие. Инфекции кожи и мягких тканей и связанные с ними осложнения у застрахованных на коммерческой основе пациентов в возрасте 0–64 лет с диабетом и без него в США. PLoS One . 2013; 8 (4): e60057. 15. Хабиф ТП. Клиническая дерматология: Цветное руководство по диагностике и терапии. 5-е изд. Нью-Йорк, штат Нью-Йорк: Мосби; 2010: 335–381. 16. Дженг А, и другие. Роль бета-гемолитических стрептококков в возникновении диффузного некультивируемого целлюлита. Медицина (Балтимор) . 2010. 89 (4): 217–226. 17. Moet GJ, и другие. Современные причины инфекций кожи и мягких тканей в Северной Америке, Латинской Америке и Европе: отчет программы SENTRY Antimicrobial Surveillance Programme (1998–2004 гг.). Диагностика Microbiol Infect Dis . 2007. 57 (1): 7–13. 18. Стенка ГД, и другие. Объективные критерии могут помочь отличить некротический фасциит от ненекротической инфекции мягких тканей. Am J Surg . 2000. 179 (1): 17–21. 19. Вонг CH, и другие. Шкала LRINEC (лабораторный индикатор риска некротического фасциита): инструмент для отличия некротического фасциита от других инфекций мягких тканей. Crit Care Med . 2004. 32 (7): 1535–1541. 20. Миллс А.М., и другие. Необходимы ли посевы крови у взрослых с целлюлитом? Энн Эмерг Мед . 2005. 45 (5): 548–549. 21. Perl B, и другие. Экономическая эффективность посевов крови для взрослых пациентов с целлюлитом. Clin Infect Dis . 1999. 29 (6): 1483–1488. 22. Барон Э.Дж., и другие. Руководство по использованию микробиологической лаборатории для диагностики инфекционных заболеваний. Clin Infect Dis . 2013; 57 (4): e22 – e121. 23. Abrahamian FM, и другие. Использование обычных посевов из раны для оценки кожных абсцессов на наличие метициллин-резистентного стафилококка, связанного с сообществом. Энн Эмерг Мед . 2007. 50 (1): 66–67. 24. Шмид М.Р., и другие. Дифференциация некротического фасциита и целлюлита с помощью МРТ. AJR Am J Roentgenol . 1998. 170 (3): 615–620. 25. Мальгем Дж., и другие. Некротический фасциит: вклад и ограничения диагностической визуализации. Костный сустав позвоночника . 2013. 80 (2): 146–154. 26. Марин Дж. Р., и другие.Экстренное ультразвуковое исследование инфекций кожи и мягких тканей в педиатрическом отделении. Acad Emerg Med . 2013. 20 (6): 545–553. 27. Micromedex 2.0. http://www.micromedexsolutions.com (требуется подписка). По состоянию на 25 мая 2014 г. 28. Williams DJ, и другие. Сравнительная эффективность стратегий лечения антибиотиками при инфекциях кожи и мягких тканей у детей. Педиатрия . 2011; 128 (3): e479 – e487. 29. Duong M, и другие. Рандомизированное контролируемое испытание антибиотиков при лечении внебольничных кожных абсцессов у педиатрических пациентов. Энн Эмерг Мед . 2010. 55 (5): 401–407. 30. Ханкин А, и другие. Нужны ли антибиотики после разреза и дренирования кожного абсцесса? Энн Эмерг Мед . 2007. 50 (1): 49–51. 31. Райт Т.Н., и другие. Минимально инвазивное дренирование подкожных абсцессов снижает стоимость больницы и продолжительность пребывания в больнице. South Med J . 2013. 106 (12): 689–692. 32. Лю Ц., и другие. Руководство по клинической практике Американского общества инфекционистов по лечению метициллин-резистентных инфекций Staphylococcus aureus у взрослых и детей [опубликованные поправки опубликованы в Clin Infect Dis. 2011; 53 (3): 319]. Clin Infect Dis . 2011; 52 (3): e18 – e55. 33. Хепберн MJ, и другие. Сравнение краткосрочного (5 дней) и стандартного (10 дней) лечения неосложненного целлюлита. Arch Intern Med . 2004. 164 (15): 1669–1674. 34. Чен А.Е., и другие. Рандомизированное контролируемое исследование цефалексина по сравнению с клиндамицином при неосложненных кожных инфекциях у детей. Педиатрия . 2011; 127 (3): e573 – e580. 35. Гурусамы К.С., и другие. Антибактериальная терапия для лечения метициллин-резистентных инфекций Staphylococcus aureus (MRSA) в хирургических ранах. Кокрановская база данных Syst Rev .2013; (8): CD009726. 36. Корвин П., и другие. Рандомизированное контролируемое исследование внутривенного лечения целлюлита антибиотиками в домашних условиях по сравнению с больничными. BMJ . 2005. 330 (7483): 129–135. 37. Эллис Р., и другие. Укусы собак и кошек [опубликованное исправление опубликовано в Am Fam Physician. 2015; 91 (10): 676]. Врач Фам . 2014. 90 (4): 239–243. 38. Томас К., и другие.Профилактические антибиотики для профилактики целлюлита (рожи) ног: результаты исследования PATCH II Сети клинических исследований дерматологии Великобритании. Br J Dermatol . 2012. 166 (1): 169–178. Тампонада сердца при гнойном перикардите, вызванном Cutibacterium acnesГнойный перикардит является потенциально смертельным заболеванием с высокой смертностью при отсутствии лечения. Cutibacterium acnes (ранее Propionibacterium acnes ) — анаэробные бактерии, которые повсеместно встречаются во флоре кожи и обычно считаются загрязнителями культур; однако у него есть патогенный потенциал.Мы представляем случай гнойного перикардита, вызванного C. acnes , который привел к тампонаде сердца. Первоначальная стабилизация и диагноз были выполнены с помощью перикардиоцентеза; После этого пациенту сделали перикардиальное окно. Из-за тяжелой аллергии на пенициллин он успешно прошел 14-дневный курс ванкомицина. Насколько нам известно, это только третий опубликованный случай гнойного перикардита с тампонадой сердца, вызванной C. acnes , и первый случай, получавший 14-дневный курс ванкомицина. 1. ВведениеГнойный перикардит — это редкая разновидность бактериального перикардита, который характеризуется макроскопическим или микроскопическим гнойным поражением перикарда и чаще всего развивается в результате прямого непрерывного распространения внутригрудной инфекции (такой как пневмония или медиастинит) или внутрисердечного источника и реже через гематогенное распространение. До Второй мировой войны гнойный перикардит был довольно распространенным заболеванием, его заболеваемость составляла 1 из 254 человек. Однако в эпоху современных противомикробных препаратов заболеваемость снизилась до 1 на 18 000 человек.Аналогичным образом изменился и спектр возбудителей, вызывающих заболевание, от подавляющего большинства грамположительных организмов к включению грамотрицательных и анаэробных организмов. Несмотря на снижение заболеваемости и улучшение противомикробных препаратов, гнойный перикардит остается важной причиной заболеваемости и смертности, поскольку при отсутствии лечения он быстро прогрессирует и приводит к смертельному исходу [1, 2]. Сообщается, что некоторые известные осложнения гнойного перикардита включают тампонаду сердца, констриктивный перикардит, псевдоаневризму левого желудочка и образование микотической аневризмы аорты, среди прочего [1–3].Тяжесть этих осложнений делает крайне важным высокий индекс подозрений, позволяющий оперативно диагностировать и лечить. 2. Описание клинического случая71-летний мужчина поступил в кардиологическую клинику с 3-недельной историей ухудшения одышки, ночной потливости и субъективной лихорадки. Следует отметить, что за неделю до этого он прошел ишемическое обследование, которое было значимым для недавно выявленного плеврального выпота слева, умеренного перикардиального выпота и легкого утолщения перикарда на КТ грудной клетки (рис. 1). Первоначальный медицинский осмотр был значимым для частоты сердечных сокращений 107 ударов в минуту и относительной гипотензии 98/61 мм рт. Кроме того, тоны сердца были отдаленными, но вздутие яремных вен отсутствовало. Позже выяснилось, что у него есть потенциальная актуальность: у него были прыщи на лице. На электрокардиограмме выявлена синусовая тахикардия. Была проведена трансторакальная эхокардиограмма (ТТЭ), которая показала, что выпот увеличился более чем на один сантиметр по сравнению с последней эхокардиограммой девятью днями ранее и теперь был большим и окружным с ранним диастолическим коллапсом правого желудочка, имеющим отношение к физиологии тампонады (Рисунки 2 и 3).Тем не менее, он также отметил неплеторическую нижнюю полую вену (НПВ) и отсутствие преувеличенной вариабельности респираторного притока. Неотложный перикардиоцентез был выполнен с удалением 370 мл негазированной серозно-кровянистой жидкости с немедленным улучшением гемодинамики и симптомов. Окраска по Граму перикардиальной жидкости показала микроскопический гнойный характер со смешанными воспалительными клетками. Была начата эмпирическая антибиотикотерапия широкого спектра действия ванкомицином. Как 72-часовые аэробные культуры, так и анаэробные культуры, выдержанные в течение шести дней, были отрицательными.Полные лабораторные данные до и после перикардиоцентеза можно найти в таблице ниже (Таблица 1).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
