причины, классификация ХРАС, симптомы и лечение
21 мая 2021
Хронический рецидивирующий афтозный стоматит (ХРАС) — это заболевание, которое проявляется регулярными (рецидивирующими) высыпаниями одиночных афт. Отличается длительным течением, заболевание может беспокоить на протяжении многих лет.1
МКБ — афтозный стоматит:
- К12.0. Рецидивирующие афты полости рта
- К12.00. Рецидивирующие (малые афты)
- К12.08. Другие уточненные рецидивирующие афты полости рта
- К 12.09. Рецидивирующие афты полости рта неуточненные
Как часто встречается афтозный стоматит?
Афтозный стоматит является часто встречающимся заболеванием, которым, по разным данным, страдают от 5 до 40% детей и взрослых разного возраста. Данные разнятся в зависимости от популяции.2-5
Причины афтозного стоматита
Точная причина данного заболевания остается неочевидной. Предполагают, что ХРАС имеет аллергическую природу, в качестве аллергенов могут выступать продукты питания, лекарства, зубные пасты, пыль и глисты. 6,7 Также причиной заболевания может быть аутоиммунная реакция организма.8 Прослеживается наследственная предрасположенность к данному заболеванию.
6,7 Также причиной заболевания может быть аутоиммунная реакция организма.8 Прослеживается наследственная предрасположенность к данному заболеванию.
Предрасполагающие факторы:
- заболевания органов пищеварения (гастрит, язвенная болезнь желудка, холецистит, болезнь Крона)
- дисбактериоз
- стресс
- дефицит железа, витаминов B1, B2, B6, B12, С
- хронические тонзиллиты, отиты и риниты
Классификация ХРАС:
ПРИЧИНЫ | КОММЕНТАРИЙ | ||
| причины: | Клинически выделяют несколько форм ХРАС: | комментарий: | 1) фибринозная форма: размер афт 2 — 3 мм, заживают за 6 — 8 дней |
| причины: | ХРАС как симптом заболевания: | комментарий: | 1) болезнь Бехчета |
| причины: | По степени тяжести ХРАС делят на: | комментарий: | 1) легкую форму: 1 — 2 афты, раз в 2 года |
Симптомы афтозного стоматита
- образование резко болезненных афт
- жжение слизистой оболочки
- дискомфорт при приеме пищи и разговоре
- постоянные рецидивы, чаще летом и осенью
Афта при ХРАС окружена красным ободком и покрыта налетом, ее контуры ровные, что отличает ее от травматической эрозии.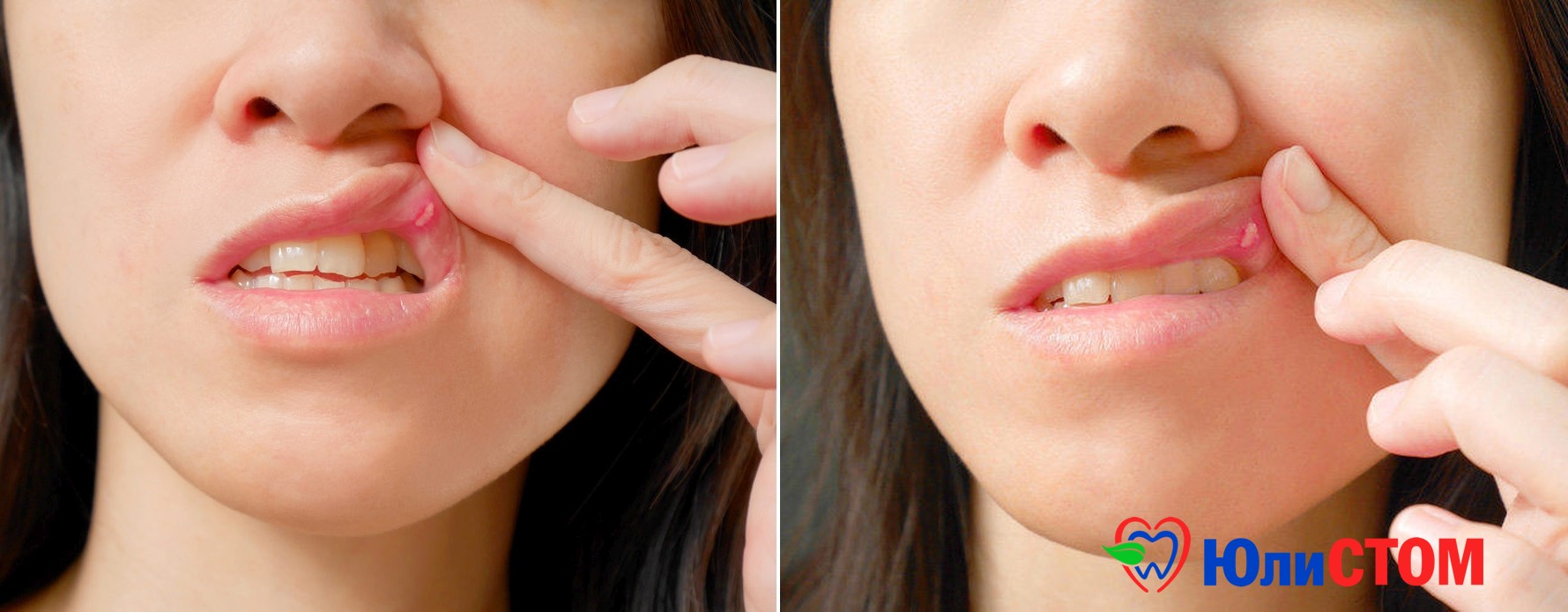
ХРАС как симптом болезни
Болезнь Бехчета — заболевание неизвестной этиологии, характеризуется поражением сосудов, появлением афт в ротовой полости и на половых органах, поражением глаз, суставов, желудочно-кишечного тракта, центральной нервной системы и других органов. Имеет хроническое течение, в отсутствии лечения может привести к инвалидности.9
Симптомы:
ХРАС
ХРАС — самый ранний симптом болезни, афты могут иметь любой размер, рецидивируют не реже 3 раз в год, чаще расположены на слизистой щек, губ, десен, языка
Поражение глаз
Увеит (воспаление оболочки глаза), ухудшается зрение, появляется «туман» перед глазами, покраснение глаз (редко), слезотечение
Язвы гениталий
Похожи на язвы в полости рта, но являются более глубокими и болезненными
Покраснение кожи
На коже наблюдается узловатая эритема (красные болезненные подкожные узлы), сыпь
Прочее
- поражение сосудов: тромбоз, аневризмы
- поражение нервной системы: кома, менингит, спутанность сознания
- поражение суставов: артрит
Болезнь Райтера – системное инфекционное заболевание, характеризующееся поражением слизистой оболочки полости рта, мочеполовой системы, глаз и суставов. Пусковым механизмом инфекции обычно являются хламидии и гонококки, но причиной может быть также генетическая предрасположенность. Заболевание имеет тяжелое течение, в случае осложнений приводит к инвалидности (слепоте, деформирующему артриту) и даже смерти.
Пусковым механизмом инфекции обычно являются хламидии и гонококки, но причиной может быть также генетическая предрасположенность. Заболевание имеет тяжелое течение, в случае осложнений приводит к инвалидности (слепоте, деформирующему артриту) и даже смерти.
Важно помнить, что ХРАС может быть симптомом более серьезного системного заболевания.
Профилактика ХРАС
Профилактика должна быть направлена на контроль состояния здоровья в целом, терапию хронических заболеваний и регулярные осмотры по поводу ХРАС. Для своевременного выявления рецидивов необходимо каждые 3 — 4 месяца посещать стоматолога. Стоит избегать использования зубных паст и средств гигиены с красителями или выявленными аллергенами. Прием антибиотиков должен проводиться только под контролем врача. Рекомендуется избегать сильных психоэмоциональных нагрузок. Важно заниматься укрепление иммунитета.
В этом могут помочь пастилки Тантум® Прополис.
Тантум
® ПрополисТантум® Прополис обладает иммуностимулирующим, противовирусным и противогрибковым действием и способствует заживлению при стоматите. Витамин С, входящий в состав пастилок, отвечает за регенерацию клеток и участвует в синтезе коллагена. Пастилки Тантум® Прополис являются эффективным средством для профилактики стоматита.12
Витамин С, входящий в состав пастилок, отвечает за регенерацию клеток и участвует в синтезе коллагена. Пастилки Тантум® Прополис являются эффективным средством для профилактики стоматита.12
Узнать больше
Лечение афтозного стоматита
Лечение зависит от тяжести и причины заболевания и включает:
- Местное лечение
- Общее лечение
Местное лечение:
Местное лечение должно быть направлено на уменьшение боли и уничтожение микробов. Для этого могут применяться препараты-антисептики с обезболивающим эффектом, например, на основе Бензидамина, содержащегося в Тантум® Верде.
Тантум® Верде обладает комплексным действием: оказывает противовоспалительное действие16, быстро уменьшает боль17, обладает антисептическим эффектом против большого спектра микроорганизмов и препятствует дальнейшему инфицированию18. Бензидамин в составе Тантум® Верде проникает в слизистую и накапливается в воспаленных тканях в эффективной концентрации.11-13
Бензидамин в составе Тантум® Верде проникает в слизистую и накапливается в воспаленных тканях в эффективной концентрации.11-13
При стоматите рекомендуется применять Тантум® Верде в виде раствора или спрея.
Спрей Тантум® Верде
подробнее
Раствор Тантум® Верде
подробнее
Таблетки Тантум® Верде
подробнее
При ХРАС важно проводить регулярную санацию полости рта, своевременно лечить кариес и его осложнения, проводить регулярную профессиональную гигиену полости рта. Кроме того, для снятия налета с афт могут применяться протеолитические ферменты, а для ускорения заживления — эпителизирующие препараты.
Общее лечение:
1) Обезболивающие препараты
2) Устранение очагов хронической инфекции
3) Десенсибилизирующая терапия: противоаллергические препараты
4) Иммуномодуляторы и витаминотерапия
5) Щадящая диета с исключением аллергенов, острой пищи и глютена
6) Применение средств для нормализации микрофлоры кишечника
7) Физиотерапия
8) Гормональная терапия в тяжёлых случаях
Успех лечения во многом зависит от выявления сопутствующего заболевания и аллергенов.
Общее лечение назначается после консультации с терапевтом, аллергологом и гастроэнтерологом. При болезни Бехчена лечение проводится совместно с врачом-ревматологом.
Лечение стоматита десен у взрослых от 1 155р в стоматологии на Динамо
Стоматит — достаточно распространённое воспалительное заболевание, поражающее слизистую оболочку рта. Оно встречается примерно у каждого пятого человека, независимо от возрастной группы.
Исключение вторичного инфицирования
Гипоаллергенные анестетики
Комплексная профилактика
ЛЕЧЕНИЕ ДЕСЕН
Цены на лечение стоматита
Поддерживающее пародонтологическое лечение
5400
р.
Аппликация лечебной повязки
1190
р.
ЛЕЧЕНИЕ ДЕСЕН
Каковы же причины возникновения или появления такого воспаления?
Чаще всего, стоматит возникает у человека не под влиянием какого-либо единственного фактора, а из-за целого ряда причин. К примеру, это может быть попадание в ротовую полость грибковой инфекции на фоне царапины или травмы десны. В качестве возможных факторов можно указать следующие:
К примеру, это может быть попадание в ротовую полость грибковой инфекции на фоне царапины или травмы десны. В качестве возможных факторов можно указать следующие:
- Повреждение слизистой оболочки (ожог, царапина, прокус щеки)
- попадание в ротовую полость грибков, бактерий
- стоматологические причины – зубной камень и зубной налёт, воспаление дёсен, кариес, негерметичные коронки, непрофессиональное протезирование
- недостаточная гигиена рта
- приём антибиотиков, угнетающих нормальную микрофлору рта
- расстройства органов пищеварения
- отравление тяжёлыми металлами
- воздействие ионизирующего излучения
- аллергия
- аутоиммунные реакции
ЛЕЧЕНИЕ ДЕСЕН
Как же понять — стоматит это или нет?
Возникает боль во рту, чувство жжения, зуда, покраснение, в дальнейшем появляется отёк, могут быть пузырьковые высыпания, эрозии, овальные или круглые язвочки, которые могут кровоточить и в дальнейшем покрываются плёнкой.
Место локализации язв — внутренняя сторона щёк и губ, языка, дёсны, область нёба, слизистая под языком и область миндалин.
ЛЕЧЕНИЕ ДЕСЕН
Стадии развития болезни
I стадия стоматита
Сопровождается появлением болезненной реакции во рту. Затем появляются покраснения и эрозии, которые покрываются плёнкой. Это так называемые афты. Появление афт вызывают резкую боль при разговоре и при приёме пищи.
II стадия стоматита
Спустя 1-2 дня после I стадии на языке появляется белый налёт. Часто в уголках рта возникает ангулит (трещинки или «заеды»). Возникают затруднения при открытии полости рта, проглатывании слюны, жевании.
III стадия стоматита
Образуются язвы и ранки. В дальнейшем ранки увеличиваются в размерах и в глубину, зачастую образуя одну язву большого размера.
Этой стадии развития болезни сопутствуют головная боль, слабость, общее ухудшение самочувствия, возможно повышение температуры, воспаление лимфатических узлов.
При появлении первых симптомов стоматита следует как можно быстрее обратиться к дипломированному специалисту. Это позволит подтвердить заболевание и начать лечение на ранней стадии. Невылеченный стоматит может дать дополнительные осложнения, к примеру, присоединение к нему вторичной инфекции, появление кровоточивости дёсен, выпадение зубов и прочие.
ЛЕЧЕНИЕ ДЕСЕН
Познакомьтесь с нашими врачами и запишитесь на консультацию
Наши врачи проходят обучение за рубежом:
В 2017 году успешно пройден магистерский курс по имплантации зубов в Будапеште. Также врачи сами являются руководителями стоматологических мастер-классов, семинаров, форумов, симпозиумов на территории России и СНГ.
ЛЕЧЕНИЕ ДЕСЕН
Диагностика стоматита
Каких-то специальных однозначных медицинских тестов, например посевов, на стоматит не бывает. Диагностика производится врачом визуально, путём осмотра поражений слизистой оболочки ротовой полости пациента. Врач, определяя характерные признаки, устанавливает конкретный вид стоматита. Также врач определяет план дополнительных медицинских исследований, таких как диагностика ПЦР, мазки на дисбактериоз и т.д. После обследования определяется тактика лечения.
Врач, определяя характерные признаки, устанавливает конкретный вид стоматита. Также врач определяет план дополнительных медицинских исследований, таких как диагностика ПЦР, мазки на дисбактериоз и т.д. После обследования определяется тактика лечения.
ЛЕЧЕНИЕ ДЕСЕН
Этапы лечения стоматита
- Назначение обезболивающих препаратов.
- Назначение местных анестезирующих средств (при сильных болях).
- Лечение стоматита с применением противовоспалительных, антисептических средств.
- Заживляющая терапия.
При своевременном обращении к врачу и вовремя начатом лечении, стоматит проходит достаточно быстро: через 5 –10 дней.
Для санации — очищения слизистой можно использовать полоскания на основе таких средств как отвар календулы, эвкалипта, люголь, малавит, ротокан, хлоргексидин, фурацилин и т.п.
В процессе лечения следует соблюдать диету с ограничением острой, горячей, холодной, кислой и грубой пищи.
При аллергическом стоматите применяются антигистаминные препараты, например, кларитин, тавегил, супрастин, лоратадин, цетиризин также бывает полезен прием иммуностимуляторов (имудон, рибомунил, бронхомунал, имунорикс, бронховаксон и др.).
При язвенном или афтозном стоматите местное лечение сочетается с общим лечением пациента.
При герпетическом стоматите назначается противовирусная терапия.
При кандидозном стоматите назначается специфическое лечение. Используется местная терапия противогрибковыми средствами. Местно, для обработки полости рта используется раствор кандид, раствор пимафуцина. Общее лечение включает пимафуцин, флюконазол, нистатин, дифлюкан и пр.).
ЛЕЧЕНИЕ ДЕСЕН
В процессе лечения используются следующие медикаментозные препараты
Анестетики
Призваны сократить болевые ощущения в полости рта (холисал, метрогил дента, калгель, камистад и др.)
Антибактериальные и противомикробные препараты
Направлены на предотвращение вторичного заражения стоматических язв бактериями и микробами (метрогил дента, октинисепт, холисал, тетроборат натрия, лизобакт, ларипронт, ингалипт, граммидин, фарингасепт и др. ).
).
Противовирусные препараты
Эффективны при лечении стоматита, имеющего вирусное происхождение (анаферон, эргоферон, ацикловир, умифеновир, свечи: виферон, генферон, кипферон и др.).
Заживляющие препараты
Призваны ускорить заживление образующихся на последней стадии болезни язв (сок алоэ, солкосерил, актовегин, элькар и пр.).
Помните, что приём препаратов должен идти по назначению врача, самолечение недопустимо.
Острый герпетический стоматит у детей (лекция)
Проблема заболеваний слизистой оболочки полости рта является одной из важнейших в стоматологии. Особое место в этой проблеме занимает острый герпетический стоматит, прежде всего потому, что на этот стоматит приходится более 80% среди всех заболеваний слизистой оболочки полости рта у детей. Кроме того, острый герпетический стоматит занимает одно из ведущих мест в детской инфекционной патологии, встречаясь чаще скарлатины, кори, эпидемического паротита, и лишь немного уступает ветряной оспе.
Совокупностью методов вирусологического, серологического и иммунофлюоресцентного исследования доказано, что острый герпетический стоматит является одной из клинических форм проявления первичной герпетической инфекции.
Распространение заболевания в 71% в возрасте от 1 года до 3 лет объясняется тем, что в этом возрасте у детей исчезают антитела, полученные от матери интерплацентарно, а также отсутствием зрелых систем специфического иммунитета и ведущей роли неспецифической защиты. Среди детей старшего возраста заболеваемость значительно ниже вследствие приобретенного иммунитета после перенесенной герпетической инфекции в ее разнообразных клинических проявлениях.
 д.).
д.).Большое значение в патогенезе заболевания придается лимфоузлам и элементам ретикулоэндотелиальной системы, что вполне согласуется с патогенезом последовательного развития клинических признаков стоматита. Появлению элементов поражения на слизистой оболочке рта предшествуют лимфадениты разной степени выраженности. Наиболее часто лимфаденит наблюдается при тяжелом и среднетяжелом течении стоматита. Как правило, они двусторонние, подчелюстные. Однако при среднетяжелой и тяжелой форме болезни возможны также и одновременные вовлечения в процесс шейных лимфатических узлов. Лимфаденит при остром герпетическом стоматите предшествует высыпаниям элементов поражения в полости рта, сопутствует всему течению болезни и остается на 7–10 дней после полной эпителизации элементов.
 Исследования неспецифической иммунологической реактивности установили нарушение защитных барьеров организма, которые отражали форму тяжести болезни и периоды ее развития. Среднетяжелая и тяжелая формы стоматита приводили к резкому угнетению естественного иммунитета, который восстанавливался через 7–14 дней после клинического выздоровления ребенка.
Исследования неспецифической иммунологической реактивности установили нарушение защитных барьеров организма, которые отражали форму тяжести болезни и периоды ее развития. Среднетяжелая и тяжелая формы стоматита приводили к резкому угнетению естественного иммунитета, который восстанавливался через 7–14 дней после клинического выздоровления ребенка.Острый герпетический стоматит, как и многие другие детские инфекционные заболевания, протекает в легкой, среднетяжелой и тяжелой формах. Развитие болезни проходит пять периодов: инкубационный, продромальный, период развития болезни, угасания и клинического выздоровления.
Тяжесть острого герпетического стоматита оценивается по выраженности и характеру симптома токсикоза и симптома поражения слизистой оболочки полости рта.
Легкая форма острого герпетического стоматита характеризуется внешним отсутствием симптомов интоксикации организма, продромальный период клинически отсутствует. Болезнь начинается как бы внезапно повышением температуры до 37–37,5°С.
 Общее состояние ребенка вполне удовлетворительное. У ребенка иногда обнаруживаются незначительные явления катара слизистой оболочки носа, дыхательных путей. В полости рта явления гиперемии, небольшого отека, главным образом в области десневого края (катаральный гингивит).
Общее состояние ребенка вполне удовлетворительное. У ребенка иногда обнаруживаются незначительные явления катара слизистой оболочки носа, дыхательных путей. В полости рта явления гиперемии, небольшого отека, главным образом в области десневого края (катаральный гингивит). В большинстве случаев на фоне усилившейся гиперемии в полости рта появляются одиночные или сгруппированные элементы поражения, количество которых обычно не превышает 6. Высыпания одноразовые. Длительность периода развития болезни 1–2 дня.
У детей, страдающих этой формой заболевания, как правило, отсутствуют изменения в крови, иногда только к концу болезни появляется незначительный лимфоцитоз (у детей 1–3 лет количество лимфоцитов и в норме составляет до 50%).
 Герпетические комплементсвязывающие антитела в период реконвалесценции определяются нечасто. При этой форме болезни хорошо выражены защитные механизмы слюны: рН 7,4±0,04, что соответствует оптимальному состоянию. В периоде разгара болезни в слюне появляется противовирусный фактор интерферон от 8 до 12 ед/мл. Снижение лизоцима в слюне не выражено.
Герпетические комплементсвязывающие антитела в период реконвалесценции определяются нечасто. При этой форме болезни хорошо выражены защитные механизмы слюны: рН 7,4±0,04, что соответствует оптимальному состоянию. В периоде разгара болезни в слюне появляется противовирусный фактор интерферон от 8 до 12 ед/мл. Снижение лизоцима в слюне не выражено.Среднетяжелая форма острого герпетического стоматита характеризуется достаточно четко выраженными симптомами токсикоза и поражения слизистой оболочки рта во все периоды болезни. Уже в продромальном периоде ухудшается самочувствие ребенка, появляются слабость, капризы, ухудшение аппетита, может быть катаральная ангина или симптомы острого респираторного заболевания. Подчелюстные лимфатические узлы увеличиваются, становятся болезненными. Температура поднимается до 37–37,5°С.
По мере нарастания болезни в период развития заболевания (фаза катарального воспаления) температура достигает 38–39°С, появляются головная боль, тошнота, бледность кожных покровов.
 На пике подъема температуры, усиленной гиперемии и выраженной отечности слизистой высыпают элементы поражения как в полости рта, так и нередко на коже лица приротовой области. В полости рта обычно от 10 до 20–25 элементов поражения. В этот период усиливается саливация, слюна становится вязкая, тягучая. Отмечаются ярко выраженный гингивит и кровоточивость десен.
На пике подъема температуры, усиленной гиперемии и выраженной отечности слизистой высыпают элементы поражения как в полости рта, так и нередко на коже лица приротовой области. В полости рта обычно от 10 до 20–25 элементов поражения. В этот период усиливается саливация, слюна становится вязкая, тягучая. Отмечаются ярко выраженный гингивит и кровоточивость десен.В крови отмечается СОЭ до 20 мм/ч, чаще лейкопения, иногда незначительный лейкоцитоз. Палочкоядерные лейкоциты и моноциты в пределах высших границ нормы, лимфоцитоз и плазмоцитоз. Нарастание титра герпетических комплементсвязывающих антител обнаруживается более часто, чем после перенесения легкой формы стоматита.

Продолжительность периода угасания болезни зависит от сопротивляемости организма ребенка, наличия в полости рта кариозных и разрушенных зубов, нерациональной терапии. Последние факторы способствуют слиянию элементов поражения, их последующему изъязвлению, появлению язвенного гингивита. Эпителизация элементов поражения затягивается до 4–5 дней. Дольше всего сохраняется гингивит, резкая кровоточивость и лимфаденит.
При среднетяжелом течении заболевания рН слюны становится более кислой, достигая во время высыпаний 6,96±0,07. Количество интерферона меньше, чем у детей с легким течением заболевания, однако не превышает 8 ед/мл и обнаруживается не у всех детей. Содержание лизоцима в слюне снижается больше, чем при легкой форме течения стоматита. Температура видимо неизмененной слизистой рта находится в соответствии с температурой тела ребенка, в то время как температура элементов поражения в стадии дегенерации на 1,0–1,2° ниже температуры неизмененной слизистой. С началом регенерации и в период эпителизации температура элементов поражения повышается до 1,8° и держится более высокой до полной эпителизации пораженной слизистой.

Тяжелая форма острого герпетического стоматита встречается значительно реже, чем среднетяжелая и легкая. В продромальный период у ребенка имеют место все признаки начинающегося острого инфекционного заболевания: апатия, адинамия, головная боль, кожно–мышечная гиперстезия и артралгия и др. Нередко наблюдаются симптомы поражения сердечно–сосудистой системы: бради– и тахикардия, приглушение тонов сердца, артериальная гипотония. У некоторых детей отмечаются носовые кровотечения, тошнота, рвота, отчетливо выраженный лимфаденит не только подчелюстных, но и шейных лимфоузлов.
В период развития болезни температура поднимается до 39–40°С. У ребенка появляется скорбное выражение губ, страдальческие запавшие глаза. Может быть нерезко выраженный насморк, покашливание, несколько отечны и гиперемированы конъюнктивы глаз. Губы сухие, яркие, запекшиеся. В полости рта слизистая отечна, ярко гиперемирована, резко выраженный гингивит.
Через 1–2 суток в полости рта начинают появляться элементы поражения – до 20–25.
 Часто высыпания в виде типичных герпетических пузырьков появляются на коже приротовой области, коже век и конъюнктиве глаз, мочке ушей, на пальцах рук (по типу панариция). Высыпания в полости рта рецидивируют, и поэтому в разгар болезни у тяжелобольного ребенка их насчитывают около 100. Элементы сливаются, образуя обширные участки некроза слизистой. Поражаются не только губы, щеки, язык, мягкое и твердое небо, но и десневой край. Катаральный гингивит переходит в язвенно–некротический. Резкий гнилостный запах изо рта, обильное слюнотечение с примесью крови. Усугубляются воспалительные явления на слизистой носа, дыхательных путей, глаз. В секрете из носа и гортани обнаруживаются также прожилки крови, а иногда отмечаются носовые кровотечения. В таком состоянии дети нуждаются в активном лечении у педиатра и стоматолога, в связи с чем целесообразной является госпитализация ребенка в изолятор педиатрической или инфекционной больницы.
Часто высыпания в виде типичных герпетических пузырьков появляются на коже приротовой области, коже век и конъюнктиве глаз, мочке ушей, на пальцах рук (по типу панариция). Высыпания в полости рта рецидивируют, и поэтому в разгар болезни у тяжелобольного ребенка их насчитывают около 100. Элементы сливаются, образуя обширные участки некроза слизистой. Поражаются не только губы, щеки, язык, мягкое и твердое небо, но и десневой край. Катаральный гингивит переходит в язвенно–некротический. Резкий гнилостный запах изо рта, обильное слюнотечение с примесью крови. Усугубляются воспалительные явления на слизистой носа, дыхательных путей, глаз. В секрете из носа и гортани обнаруживаются также прожилки крови, а иногда отмечаются носовые кровотечения. В таком состоянии дети нуждаются в активном лечении у педиатра и стоматолога, в связи с чем целесообразной является госпитализация ребенка в изолятор педиатрической или инфекционной больницы. У последних очень редко наблюдается токсическая зернистость. Герпетические комплементсвязывающие антитела в период реконвалесценции определяются, как правило, всегда.
У последних очень редко наблюдается токсическая зернистость. Герпетические комплементсвязывающие антитела в период реконвалесценции определяются, как правило, всегда.В слюне – кислая среда (рН 6,55±0,2), которая затем может сменяться более выраженной щелочностью (8,1–8,4). Интерферон обычно отсутствует, содержание лизоцима резко снижено.
Диагноз острого герпетического стоматита ставится на основании клинической картины заболевания. Использование вирусологических и серологических методов диагностики особенно в практическом здравоохранении затруднено. Это связано прежде всего с трудностью названных специальных методов исследования. Кроме того, с помощью этих методов можно получить результаты в лучшем случае к концу заболевания или спустя некоторое время после выздоровления. Такая ретроспективная диагностика не может удовлетворить врача–клинициста.
Следует подчеркнуть, что в последние годы находит все большее применение метод иммунофлюоресценции. Высокий процент совпадений (79,0±0,6%) диагноза острого герпетического стоматита по данным иммунофлюоресценции с результатами вирусологических и серологических исследований делают этот метод ведущим в диагностике заболевания.

Тактика врача при лечении больных острым герпетическим стоматитом должна определяться формой тяжести заболевания и периодом его развития.
В связи с особенностями течения острого герпетического стоматита рациональное питание и правильная организация кормления больного занимают немаловажное место в комплексе лечебных мероприятий. Пища должна быть полноценной, т.е. содержать все необходимые питательные вещества, а также витамины. Поэтому необходимо включать в диету свежие овощи, фрукты, ягоды, соки. Перед кормлением необходимо обезболить слизистую оболочку полости рта 2–5% раствором анестезиновой эмульсии.
Ребенка кормят преимущественно жидкой или полужидкой пищей, не раздражающей воспаленную слизистую оболочку. Большое внимание необходимо уделять введению достаточного количества жидкости. Это особенно важно при интоксикации. В процессе еды следует давать натуральный желудочный сок или его заменители, так как при болях во рту рефлекторно падает ферментативная активность желез желудка.

Местная терапия при остром герпетическом стоматите ставит перед собой следующие задачи:
а) снять или ослабить болезненные симптомы в полости рта;
б) предупредить повторные высыпания элементов поражения (реинфекция) и способствовать их эпителизации.
С первых дней периода развития заболевания острого герпетического стоматита, учитывая этиологию заболевания в местном лечении, серьезное внимание должно уделяться противовирусной терапии. С этой целью рекомендуется применять 0,25% оксолиновую, 0,5% теброфеновую мази, зовиракс, растворы интерферона и неоферона.
Названные лекарственные препараты рекомендуется применять многократно (3–4 раза в день) не только при посещении врача–стоматолога, но и дома. Следует иметь в виду, что противовирусными средствами рекомендуется воздействовать и на пораженные участки слизистой, и на области без наличия элементов поражения, так как они в большей степени обладают профилактическим эффектом, чем лечебным.
В период угасания болезни противовирусные средства можно отменить.

Ведущее значение в этот период болезни следует придавать кератопластическим средствам. Это прежде всего масляные растворы А и В, облепиховое масло, каратолин, масло шиповника, мази с метилурацилом, кислородный коктейль. Этими средствами обрабатывают элементы поражения 2–3 раза в день для ускорения эпителизации афт.
Не менее важно в этот период болезни уделять внимание явлениям кровоточивости десневого края (катаральный гингивит). «Зубы утонули в деснах» – наиболее частая жалоба родителей ребенка. Иногда гингивит катаральный переходит в язвенно–некротический. В последние годы для лечения кровоточивости десен широко применяется гель для десен «Метрогил–Дента». «Метрогил–Дента» одобрен Фармакологическим Государственным Комитетом Минздрава России от 10.12.98 г. Препарат обладает приятным освежающим мятным вкусом и наносится на область десен 2 раза в день. После нанесения геля в течение 15 минут нельзя полоскать рот и принимать пищу. Комбинация метронидазола (золотого стандарта анаэробицида) и хлоргексидина (признанного антисептика) эффективно подавляет аэробные и анаэробные микроорганизмы, вызывающие заболевания ротовой полости.
 Таким образом, включение в комплекс лечебных мероприятий у детей, больных острым герпетическим стоматитом, препарата «Метрогил–Дента» гель позволяет значительно уменьшить сроки выздоровления ребенка.
Таким образом, включение в комплекс лечебных мероприятий у детей, больных острым герпетическим стоматитом, препарата «Метрогил–Дента» гель позволяет значительно уменьшить сроки выздоровления ребенка.В заключение следует отметить, что острый герпетический стоматит, протекая в любой форме, является острым инфекционным заболеванием и требует во всех случаях внимания со стороны педиатра и стоматолога: чтобы обеспечить комплексное лечение, исключить контакт больного ребенка со здоровыми детьми, провести меры профилактики этого заболевания в детских коллективах.
Литература
1. Глинских Н.П. Герпесвирусы человека. В кн. Неизвестная эпидемия, герпес. Смоленск, 1997 г., с.8.
2. Елизарова В.М., Дроботько Л.Н., Страхова С.Ю. Клинико–иммунологическое обоснование применения имудона в терапии острого герпетического стоматита. МОРАГ 2000, Москва 7–10.02.2000г. с.151.
3. Елизарова В.М., Дроботько Л.Н., Страхова С.Ю. Применение имудона при лечении заболеваний слизистой оболочки полости рта. В кн. VII Российский национальный конгресс “Человек и лекарство”, М., 10–14 апреля 1999 г., с.254.
В кн. VII Российский национальный конгресс “Человек и лекарство”, М., 10–14 апреля 1999 г., с.254.
4. Елизарова В.М., Дроботько Л.Н., Страхова С.Ю. Имудон в детской стоматологии. Русский медицинский журнал, 2000 г., № 2, с.949.
5. Ершов Ф.И., Чижов Н.П. Лечение вирусных инфекций. Клиническая фармакология и терапия. 1995 г., № 4, с.75–78.
6. Семенова Т.Б., Губанова Е.И. Современные представления о клинике, особенностях, эпидемиологии и лечении простого герпеса. Лечащий врач, 1999 г., № 2–3, с.10–16.
7. Brown D. European Study of the epidemiology and seroprevalence of HSV–2. Serological assays for Herpes simplex virus infecttions: new developments. European Congress on STDs, 1996, р.19.
8. Overall I.C. Herpes simplex virus infection of the fetus and newborn. Pediatr. Ann. 1994, vol.73, № 2, р.194–198.
Сравнительная оценка низкоинтенсивной лазерной терапии и местного применения триамцинолона ацетонида 0,1% у пациентов с рецидивирующим афтозным стоматитом процесс.
 В этом исследовании изучались триамцинолон и низкоинтенсивная лазерная терапия рецидивирующих афтозных язв, в которых оценивалась их клиническая эффективность.
В этом исследовании изучались триамцинолон и низкоинтенсивная лазерная терапия рецидивирующих афтозных язв, в которых оценивалась их клиническая эффективность. Методология
Среди 60 субъектов 54 субъекта соответствовали критериям включения в возрастном диапазоне от 16 до 46 лет. Субъекты были случайным образом разделены на две группы: контрольная группа, которая получала местное применение 0,1% триамцинолона ацетонида четыре раза в день, и тестовая группа, которая подвергалась однократному применению низкоинтенсивной лазерной терапии через три дня. Оценки проводились в 1-й, 3-й, 5-й и 10-й дни. В качестве исходных данных использовались данные, полученные по качеству жизни, связанному со здоровьем полости рта (КЖ-ОРЗ) с использованием опросника КЖ-КЖ. Клинические параметры, такие как оценка боли, оценивались с использованием визуальной аналоговой шкалы, размер язвы с использованием зонда UNC-15, а эритема и оценка заживления оценивались с использованием шкалы эритемы и заживления.
Результат
По данным OHR-QoL статистически значимой разницы в качестве жизни испытуемых и контрольной группы не выявлено. Мы обнаружили, что боль и размер язвы значительно уменьшились (p=0,007) с первого по третий день (p=0,000), а затем снова значительно уменьшились (p=0,000) на 3-10 дни (p=0,000). На 3-й и 5-й дни в испытуемой группе наблюдалось значительное уменьшение боли и эритемы (р=0,13), а также улучшение заживления язв по сравнению с контрольной группой. На 3-й и 5-й дни размеры язв уменьшались одинаково в контрольной и опытной группах. На 10-й день у пациентов обеих групп уменьшились дискомфорт, эритема и размер язвы, а также улучшилось заживление язвы.
Заключение
Уменьшение боли и эритемы и улучшение заживления язвы были значительно выше у субъектов в тестовой группе по сравнению с контрольной группой на 3-й день. Уменьшение размера язвы было сравнимо с контрольной группой на 3-й и 5-й дни.
Введение
Рецидивирующий афтозный стоматит (РАС), иногда называемый язвенной болезнью, представляет собой инфекцию слизистых оболочек полости рта, вызванную воспалительным процессом [1]. ]. Одним из наиболее частых проявлений в младенчестве и подростковом возрасте является развитие болезненных, крошечных, круглых или овальных язв с четкими границами, эритематозными ореолами и желтым или сероватым дном [2]. Считается, что Т-лимфоциты играют решающую роль в развитии этого вида иммунологической дисфункции. Указываются многие этиологические факторы, такие как генетика, иммунология, повышенная чувствительность к пищевым продуктам и лекарствам, гормональные изменения, травма, гематологический дефицит (сывороточное железо, фолиевая кислота и витамин B12), экологический и психологический стресс и вирусные инфекции [3].
]. Одним из наиболее частых проявлений в младенчестве и подростковом возрасте является развитие болезненных, крошечных, круглых или овальных язв с четкими границами, эритематозными ореолами и желтым или сероватым дном [2]. Считается, что Т-лимфоциты играют решающую роль в развитии этого вида иммунологической дисфункции. Указываются многие этиологические факторы, такие как генетика, иммунология, повышенная чувствительность к пищевым продуктам и лекарствам, гормональные изменения, травма, гематологический дефицит (сывороточное железо, фолиевая кислота и витамин B12), экологический и психологический стресс и вирусные инфекции [3].
РАС делится на три отдельные категории: малые, большие и герпетиформные. Большинство мелких язв имеют диаметр менее 1 сантиметра, сохраняются в течение 7-14 дней и полностью заживают, не оставляя шрамов. Крупные язвы диаметром более сантиметра обычно заживают в течение 20–30 дней, часто остаются рубцы. Очаги многочисленны, сгруппированы до 3 миллиметров в диаметре и обычно заживают в течение 15 дней [4].
Лечение направлено на облегчение симптомов дискомфорта пациента. Терапевтические агенты, такие как топические стероиды, пероральный тетрациклин (тетрациклин для полоскания рта), прижигание нитратом серебра (низкоинтенсивная лазерная терапия [НИЛИ]) и криотерапия, использовались для облегчения боли у пациентов [4].
Этиология и причины возникновения РАС до сих пор остаются загадкой. На склонность к формированию РАС влияет широкий спектр переменных, включая генетическую предрасположенность, психологический стресс и тревогу, иммунологические нарушения, местную травму, микробные агенты и гематиновую недостаточность [2]. У 40% пациентов в семейном анамнезе был СПА, что явно указывает на генетическую предрасположенность к афтозным язвам. Инъекции анестезии, стоматологические процедуры и травмы зубной щеткой — все это было связано с появлением афтозного стоматита в прошлом. Дефицит витамина B12 и фолиевой кислоты может еще больше увеличить риск развития САС. Например, согласно исследованиям, болезнь Крона и язвенный колит связаны с афтами.
К сожалению, лечения РАС не существует. Симптоматическое облегчение является основной целью лечения, которое направлено на уменьшение дискомфорта, уменьшение размера и количества язв и сокращение периода заживления. Пациенты могут выбирать из множества лекарств для лечения своих заболеваний, включая антисептические и противовоспалительные препараты, антибиотики и кортикостероиды. Местно применяются кортикостероиды, такие как гемисукцинат гидрокортизона, ацетат триамцинолона и дипропионат беклометазона. Обладает противовоспалительным и особым ингибирующим действием на Т-лимфоцитоэпителиальные клетки [5]. Кортикостероиды, такие как ацетат триамцинолона, можно наносить на кожу или в рот для лечения САС.
За последние несколько лет лазеры добились значительных успехов в медицинском секторе. С другой стороны, лазеры уже давно используются в стоматологии. НИЛИ – это терапия источником света, которая обеспечивает монохроматический и когерентный свет одной длины волны.
Действует путем фотобиологической или биохимической стимуляции клеток. Изменяет деятельность клеток и тканей. Он увеличивает выработку АТФ (аденозинтрифосфата) и снижает потребность клеток в кислороде, стимулируя митохондрии. Уровни серотонина и эндорфина повышаются, уровни простагландина Е2 и интерлейкина-1 бета падают, и в результате боль уменьшается [6]. Активатор плазминогена, который отвечает за расщепление коллагена и, следовательно, способствует пролиферации, ингибируется, чтобы уменьшить воспалительную реакцию. Артериолы расширяются в результате свойств препарата улучшать микроциркуляцию. В результате увеличения количества фибробластов, которые пролиферируют и созревают в миофибробласты, а также количества секретируемого фактора роста фибробластов, сокращается время заживления. НИЛИ уменьшает отек, облегчает боль и способствует регенерации тканей [7].
Изменяет деятельность клеток и тканей. Он увеличивает выработку АТФ (аденозинтрифосфата) и снижает потребность клеток в кислороде, стимулируя митохондрии. Уровни серотонина и эндорфина повышаются, уровни простагландина Е2 и интерлейкина-1 бета падают, и в результате боль уменьшается [6]. Активатор плазминогена, который отвечает за расщепление коллагена и, следовательно, способствует пролиферации, ингибируется, чтобы уменьшить воспалительную реакцию. Артериолы расширяются в результате свойств препарата улучшать микроциркуляцию. В результате увеличения количества фибробластов, которые пролиферируют и созревают в миофибробласты, а также количества секретируемого фактора роста фибробластов, сокращается время заживления. НИЛИ уменьшает отек, облегчает боль и способствует регенерации тканей [7].
Когда речь идет о лечении людей с легкой формой САС, это исследование было направлено на оценку эффектов НИЛИ и триамцинолона ацетонида (ТА) (0,1%).
Материалы и методы
В исследовании приняли участие 60 пациентов амбулаторного отделения (ОПД) с рецидивирующей афтозной язвой, а также студенты и сотрудники NHDCRI. В рамках исследования, которое длилось с декабря 2016 года по апрель 2018 года, Институциональный наблюдательный совет New Horizon Dental College принял исследование (номер сертификата IRB: NHDC/PG/23/11/16). Каждому пациенту было предоставлено подробное объяснение операции и связанных с ней рисков, и было получено их информированное согласие. Пациентов выбирали случайным образом из списка тех, кто ранее проходил тестирование, и из 60 начавших терапию 54 завершили ее. Они были разделены на две группы, как показано ниже:
В рамках исследования, которое длилось с декабря 2016 года по апрель 2018 года, Институциональный наблюдательный совет New Horizon Dental College принял исследование (номер сертификата IRB: NHDC/PG/23/11/16). Каждому пациенту было предоставлено подробное объяснение операции и связанных с ней рисков, и было получено их информированное согласие. Пациентов выбирали случайным образом из списка тех, кто ранее проходил тестирование, и из 60 начавших терапию 54 завершили ее. Они были разделены на две группы, как показано ниже:
Группа 1 — контрольные субъекты, включая 26 субъектов, получавших 0,1% ТА для местного применения.
Группа 2. Испытуемые, включающие 28 субъектов, подвергающихся применению НИЛИ в кресле.
Критерии включения
Включены пациенты с достоверным анамнезом незначительного РАС (размером менее 10 мм), обратившиеся в OPD в течение дня после появления язвы. Были включены пациенты, попадающие в возрастную группу 15-50 лет, без дискриминации по полу пациентов. Также были включены пациенты, которые в настоящее время проходят или ранее лечились от САС.
Также были включены пациенты, которые в настоящее время проходят или ранее лечились от САС.
Критерии исключения
Критериями исключения были беременность и период лактации, пациенты с искусственными кардиостимуляторами, так как длительный контакт с электромагнитным излучением и лазером может повлиять на работу кардиостимулятора, пациенты со злокачественными заболеваниями, любые системные заболевания в анамнезе, такие как ВИЧ и диабет mellitus или любое состояние, которое может предрасполагать к образованию язв в полости рта, а также пациенты с язвами, вызванными местными или системными лекарствами, и язвы, которые в настоящее время лечатся любыми местными лекарствами или кортикостероидами.
Процедура
Субъекты, включенные в исследование, прошли скрининг для исключения язв, вызванных любыми другими причинами или вторичных по отношению к системным заболеваниям. При первом посещении всех пациентов просили заполнить анкету, которая включала демографические данные, такие как возраст и пол, а также конкретные вопросы, касающиеся заболевания, такие как предъявляемые жалобы, первый эпизод язвы, частота и количество язв. OHR-QoL14 (общее качество жизни, связанное со здоровьем, оцениваемое OHIP-14) Вопросы на английском/хинди, заданные респондентам, включали, как часто они сталкивались с САС, чтобы повлиять на качество их жизни в последний месяц. Ответы по шкале Лайкерта классифицировались следующим образом: 4 (часто), 3 (часто), 2 (иногда), 1 (редко) и 0 (никогда). Суммируя ответы на 14 вопросов, для получения окончательной оценки использовалась шкала с более высокими баллами, указывающими на худшее качество жизни OHR [8,9].].
OHR-QoL14 (общее качество жизни, связанное со здоровьем, оцениваемое OHIP-14) Вопросы на английском/хинди, заданные респондентам, включали, как часто они сталкивались с САС, чтобы повлиять на качество их жизни в последний месяц. Ответы по шкале Лайкерта классифицировались следующим образом: 4 (часто), 3 (часто), 2 (иногда), 1 (редко) и 0 (никогда). Суммируя ответы на 14 вопросов, для получения окончательной оценки использовалась шкала с более высокими баллами, указывающими на худшее качество жизни OHR [8,9].].
С 1-го по 5-й день участники были проинструктированы воздерживаться от употребления любых местных или системных препаратов или предметов, даже если они ранее использовали такие методы лечения.
Подбрасыванием монеты субъекты были случайным образом распределены в контрольную и испытуемую группы при наличии симптомов и вновь образовавшихся язв во рту РАС.
Субъекты группы 1 получали местно ТА 0,1%. Первичную аппликацию проводил клиницист в кресле, и пациент был проинформирован о применении, дозировке и частоте. Небольшое количество геля наносили на язву четыре раза в день и оставляли на язве на полчаса перед едой или питьем. Мы использовали один и тот же измерительный аппликатор для каждого пациента. Пациентов просили наносить гель ежедневно с 1 по 5 день. Последующий период для испытуемых составлял 10 дней. Карты комплаентности велись пациентами.
Небольшое количество геля наносили на язву четыре раза в день и оставляли на язве на полчаса перед едой или питьем. Мы использовали один и тот же измерительный аппликатор для каждого пациента. Пациентов просили наносить гель ежедневно с 1 по 5 день. Последующий период для испытуемых составлял 10 дней. Карты комплаентности велись пациентами.
В группе 2 для доставки LLLT участникам использовался диодный лазер с соблюдением всех соответствующих мер предосторожности при использовании лазера. Использовался лазер с длиной волны 810 нм, дифракцией 6,3 Дж/см и лазером расфокусированного режима, начиная с 10 мм от поражения и постепенно приближаясь к поражению в пределах 2 мм в течение примерно 30 секунд для начального прохода. Чтобы оценить, насколько сильную боль испытывает пациент, исследователи позволили ему или ей сделать глоток воды. Были использованы два дополнительных 30-секундных прохода, поскольку пациент не сообщил о каком-либо значимом уменьшении дискомфорта во время первых двух раундов. Между каждым проходом давался 20-секундный период охлаждения, а общее время лазерного воздействия составляло менее 2 минут. НИЛТ вводили на исходном уровне, в 1-й, 3-й и 5-й дни. За субъектами наблюдали в течение 10 дней.
Между каждым проходом давался 20-секундный период охлаждения, а общее время лазерного воздействия составляло менее 2 минут. НИЛТ вводили на исходном уровне, в 1-й, 3-й и 5-й дни. За субъектами наблюдали в течение 10 дней.
Язвы оценивались по следующим критериям: боль [1] — чтобы оценить интенсивность боли, участники использовали 10-балльную визуальную аналоговую шкалу, где 0 — отсутствие боли, 1–5 — умеренный дискомфорт и 6-10 представляют сильный дискомфорт; размер язвы [1] — Измерение размера поражения проводилось при каждом посещении с использованием калиброванного зонда UNC-15; шкала эритемы [10] — наличие, уменьшение и отсутствие эритемы оценивали с использованием критериев, определенных в таблице 9.0065 1 ; и шкала заживления [8] — Улучшение заживления язвы оценивали с использованием критериев, определенных в Таблице 2 .
| Оценка | Критерии |
| 0 | Нет эритемы |
| 1 | Светло-красный/розовый |
| 2 | Красный, но не темный |
| 3 | Очень красный/темный цвет |
Стол 1: индекс оценки эритемы
| Оценка | Критерии |
| 0 | Нет улучшения: EI <30 |
| 1 | Умеренное улучшение: 70%>EI≥30% |
| 2 | Заметное улучшение: 100%>EI≥70% |
| 3 | Исцеление: EI=100% |
Стол 2: индекс заживления
EI: индекс эритемы
Оценка проводилась в дни 1, 3, 5 и 10.
Статистический анализ
Электронная таблица Excel использовалась для создания и табулирования данных, а Статистический пакет для социальных наук (SPSS) версии 21 (IBM Corp, Армонк, Нью-Йорк) использовался для статистического анализа. Были использованы парные t-тесты и тесты одностороннего дисперсионного анализа (ANOVA), которые использовались для сравнения результатов по группам и отдельным посещениям, в то время как тесты Уилкоксона, тесты Манна-Уитни и тесты хи-квадрат использовались для изучения заживления эритемы. и язвы. В этом исследовании мы считали значимостью p-значение менее 0,05.
Результаты
В Биласпуре, Чхаттисгарх, с декабря 2016 г. по апрель 2018 г. исследователи из отдела оральной медицины и радиологии NHDCRI обследовали пациентов. В исследовании приняли участие 22 мужчины и 48 женщин. Было еще две группы участников: контрольная группа получала местное лечение ТА 0,1%, а тестовая группа получала НИЛИ, всего 60 человек.
«В контрольной группе было 8 мужчин и 18 женщин, в опытной — 11 мужчин и 17 женщин. Средний возраст составил 28,13 года в контрольной группе и 25,67 года в контрольной группе для обеих групп участников исследования. Возрастной диапазон для обеих групп составлял от 17 до 46 лет. Средний возраст респондентов из контрольной и тестовой групп существенно не различался».
Средний возраст составил 28,13 года в контрольной группе и 25,67 года в контрольной группе для обеих групп участников исследования. Возрастной диапазон для обеих групп составлял от 17 до 46 лет. Средний возраст респондентов из контрольной и тестовой групп существенно не различался».
Качество жизни
Что касается качества жизни, у контрольных субъектов средняя разница составила 18,7931 ± 6,6352 по сравнению с испытуемыми, у которых средняя разница составила 20,7742 ± 7,4953. Было обнаружено, что это статистически не значимо (p = 0,284) (Таблица 3 ).
| Группа | Н | Средняя разница | Стандартное отклонение | F-значение | р-значение | Значение |
| Управление | 29 | 18.7931 | 6.63529 | 1,169 | 0,284 | NS |
| Тест | 31 | 20,7742 | 7. 49537 49537 |
Стол 3: Качество жизни в контрольной и тестовой группах.
NS: незначительно
Используя отдельные вопросы из общей выборки, было обнаружено, что 81,7% испытывают трудности с произнесением каких-либо слов, за ними следуют 90%, которые считали, что их чувство вкуса ухудшилось, 98,3%, которые испытывали ужасную боль во рту, и 95%, которым было трудно пережевывать любую пищу. В общей сложности 68,3% участников сообщили о том, что чувствуют себя неловко, а 63,3% сообщили о напряжении из-за проблем с зубами или ртом; диета была неудовлетворительной для 83,3 % и 90 % были вынуждены прерывать прием пищи из-за проблем с зубами или полостью рта; 78,3 % сообщили о трудностях с расслаблением, 71,7 % смущались, а 70 % были раздражительны по отношению к другим людям (Таблица 9).0065 4 ).
| Серийный номер | Вопросы о качестве жизни | Частота | Процент |
| 1 | Были ли у вас проблемы с произношением слов из-за проблем с зубами или ртом? | 49 | 81,7 |
| 2 | Чувствовали ли вы, что ваше чувство вкуса ухудшилось из-за проблем с зубами или полостью рта? | 54 | 90 |
| 3 | Были ли у вас болезненные боли во рту? | 59 | 98,3 |
| 4 | Вам было неудобно есть какую-либо пищу из-за проблем с зубами или ртом? | 57 | 95 |
| 5 | Вы стеснялись своих зубов или рта? | 41 | 68,3 |
| 6 | Вы чувствовали напряжение из-за проблем с зубами или ртом? | 38 | 63,3 |
| 7 | Ваша диета была неудовлетворительной из-за проблем с зубами или полостью рта? | 50 | 83,3 |
| 8 | Приходилось ли Вам прерывать прием пищи из-за проблем с зубами или полостью рта? | 54 | 90 |
| 9 | Вам трудно расслабиться из-за проблем с зубами или полостью рта? | 47 | 78,3 |
| 10 | Вы были немного смущены из-за проблем с зубами или ртом? | 43 | 71,7 |
| 11 | Вы были немного раздражительны с другими людьми из-за проблем с зубами или ртом? | 42 | 70 |
| 12 | Испытывали ли Вы трудности при выполнении своей обычной работы из-за проблем с зубами или полостью рта? | 36 | 60 |
| 13 | Чувствовали ли вы, что жизнь в целом стала менее удовлетворительной из-за проблем с зубами или ртом? | 38 | 63,3 |
| 14 | Вы были полностью неспособны функционировать из-за проблем с зубами или ртом? | 29 | 48,3 |
Стол 4: Анкета о качестве жизни
Боль
Статистически значимой разницы в уровне боли между группами не было (p=0,104). Через три дня в испытуемой группе наблюдалось статистически значимое уменьшение боли; однако эта разница была незначительной (p=0,798). Достоверной разницы между опытной и контрольной группами на пятый день (р=0,853) в снижении оценки боли не наблюдалось. На 10-й день в тестовой группе наблюдалось несколько большее снижение оценки боли (0,0714 ± 0,26227), чем в контрольной группе (0,0769 ± 0,27175), но оно было статистически незначимым (p = 0,940) (таблица 5 ).
Через три дня в испытуемой группе наблюдалось статистически значимое уменьшение боли; однако эта разница была незначительной (p=0,798). Достоверной разницы между опытной и контрольной группами на пятый день (р=0,853) в снижении оценки боли не наблюдалось. На 10-й день в тестовой группе наблюдалось несколько большее снижение оценки боли (0,0714 ± 0,26227), чем в контрольной группе (0,0769 ± 0,27175), но оно было статистически незначимым (p = 0,940) (таблица 5 ).
| Параметр | Управление | Тест | F-значение | р-значение | ||||
| Среднее (ВАШ) | Стандартное отклонение | Среднее (ВАШ) | Стандартное отклонение | |||||
| Оценка боли 1 день | 4,5000 | 1.79444 | 5. 3214 3214 |
1,84699 | 2,74 | 0,104 | ||
| Оценка боли 3 дня | 2,9231 | 1,64738 | 3.0714 | 2,47848 | 0,066 | 0,798 | ||
| Оценка боли 5 дней | 0,8077 | 1.02056 | 0,7500 | 1.23603 | 0,035 | 0,853 | ||
| Оценка боли 10 дней | 0,0769 | 0,27175 | 0,0714 | 0,26227 | 0,006 | 0,940 | ||
Стол 5: изменение оценки боли от первого визита до четвертого визита в группе.
ВАШ: визуальная аналоговая шкала
Размер язвы
Размер язвы статистически не различался между испытуемой и контрольной группами (p=0,316) во всей выборке. Что касается уменьшения размера язвы, на 3-й день не было статистически значимой разницы между двумя группами (p=0,651). Ни в тестовой, ни в контрольной группах (p = 0,967) не было выявлено значимой разницы в уменьшении размера язвы на 5-й день. На 10-й день тестовая группа и контрольная группа показали статистически значимую разницу в уменьшении размера язвы (Таблица 6 ).
Ни в тестовой, ни в контрольной группах (p = 0,967) не было выявлено значимой разницы в уменьшении размера язвы на 5-й день. На 10-й день тестовая группа и контрольная группа показали статистически значимую разницу в уменьшении размера язвы (Таблица 6 ).
| Параметр | Управление | Тест | F-значение | р-значение | ||
| Среднее (размер язвы) | Стандартное отклонение | Среднее (размер язвы) | Стандартное отклонение | |||
| Размер язвы 1 день | 2,8077 | 1.41476 | 3,1786 | 1.27812 | 1,024 | 0,316 |
| Размер язвы 3 дня | 2.1154 | 1.27521 | 2,2857 | 1.46204 | 0,207 | 0,651 |
| Размер язвы 5 дней | 0,8462 | 0,92487 | 0,8571 | 1. 00791 00791 |
0,002 | 0,967 |
| Размер язвы 10 дней | 0,0000 | 0,00000 | 0,0000 | 0,00000 | ||
Стол 6: Изменение размера язвы с первого визита до четвертого визита в группе.
Показатель эритемы
В первый день у всех испытуемых была та или иная форма эритемы. Умеренная эритема наблюдалась у 42,3% (N=11) контрольных субъектов по сравнению с 39,3% (N=11) испытуемых. Выраженная эритема наблюдалась у 50% (N=13) контрольных субъектов по сравнению с 53,6% (N=15) испытуемых. Темная эритема наблюдалась у 7,7% (N=2) контрольных субъектов по сравнению с 7,1% (N=2) испытуемых. Статистической разницы между обеими группами не было (p=0,88). На 3-й день эритема не наблюдалась у 3,8% (N=1) контрольных субъектов по сравнению с 28,6% (N=8) испытуемых. Умеренная эритема наблюдалась у 690,2% (N=18) контрольных субъектов по сравнению с 46,4% (N=13) испытуемых. Выраженная эритема наблюдалась у 26,9% (N=7) контрольных субъектов по сравнению с 25% (N=7) испытуемых. Статистически значимая разница (p=0,13) существовала между обеими группами, поскольку в испытуемой группе наблюдался более высокий процент субъектов без эритемы (28,6%). На 5-й день у всех субъектов наблюдалось уменьшение эритемы, у 50 % (N=13) субъектов в контрольной группе эритема отсутствовала по сравнению с 60,7% (N=17) испытуемых. Умеренная эритема наблюдалась у 50% (N=13) контрольных субъектов по сравнению с 390,3% (N=11) испытуемых. Статистически значимая разница (p=0,43) существовала между обеими группами, поскольку в тестовой группе наблюдался более высокий процент субъектов с уменьшением эритемы по сравнению с контрольной группой. На 10-й день у более высокого процента контрольных субъектов не было эритемы, 96,2% (N = 25), по сравнению с 92,9% (N = 26) испытуемых. Умеренная эритема наблюдалась у 3,8% (N=1) контрольных субъектов по сравнению с 7,1% (N=2) испытуемых. Однако между обеими группами не было статистических различий (p = 0,6) (таблица 9).
Выраженная эритема наблюдалась у 26,9% (N=7) контрольных субъектов по сравнению с 25% (N=7) испытуемых. Статистически значимая разница (p=0,13) существовала между обеими группами, поскольку в испытуемой группе наблюдался более высокий процент субъектов без эритемы (28,6%). На 5-й день у всех субъектов наблюдалось уменьшение эритемы, у 50 % (N=13) субъектов в контрольной группе эритема отсутствовала по сравнению с 60,7% (N=17) испытуемых. Умеренная эритема наблюдалась у 50% (N=13) контрольных субъектов по сравнению с 390,3% (N=11) испытуемых. Статистически значимая разница (p=0,43) существовала между обеими группами, поскольку в тестовой группе наблюдался более высокий процент субъектов с уменьшением эритемы по сравнению с контрольной группой. На 10-й день у более высокого процента контрольных субъектов не было эритемы, 96,2% (N = 25), по сравнению с 92,9% (N = 26) испытуемых. Умеренная эритема наблюдалась у 3,8% (N=1) контрольных субъектов по сравнению с 7,1% (N=2) испытуемых. Однако между обеими группами не было статистических различий (p = 0,6) (таблица 9). 0065 7 , 8 ).
0065 7 , 8 ).
| Параметр | Нет эритемы | Легкая эритема | Эритема, но не темная эритема | Темная эритема | р-значение | Значение | ||||
| Управление | Тест | Управление | Тест | Управление | Тест | Управление | Тест | |||
| День 1 | 42,3% | 39,3% | 50,0% | 53,6% | 7,7% | 7,1% | 0,966 | НР | ||
| День 3 | 3,8% | 28,6% | 69,2% | 46,4% | 26,9% | 25,0% | 0,045 | С | ||
| День 5 | 50,0% | 60,7% | 50,0% | 39,3% | 0,429 | НР | ||||
| День 10 | 96,2% | 92,9% | 3,8% | 7,1% | 0,597 | НР | ||||
Стол 7: Сравнение оценки эритемы с первого визита до четвертого визита в группе.

NS: не имеет значения; S: значимый
| Параметр | Управление | Тест | Т-значение | р-значение | ||
| Среднее (эритема) | Стандартное отклонение | Среднее (эритема) | Стандартное отклонение | |||
| Эритема 1 день | 1,65 | 0,63 | 1,68 | 0,61 | -0,146 | 0,88 |
| Эритема 3 дня | 1,23 | 0,5 | 0,96 | 0,74 | 1,519 | 0,13 |
| Эритема 5 дней | 0,5 | 0,5 | 0,39 | 0,5 | 0,781 | 0,43 |
| Эритема 10 дней | 0,04 | 0,19 | 0,07 | 0,26 | -0,52 | 0,6 |
Стол 8: Изменение оценки эритемы с первого визита до четвертого визита в группе.

Оценка заживления язвы
На 3-й день все испытуемые продемонстрировали некоторое улучшение. У 14,3% (N=4) испытуемых улучшений не наблюдалось, а умеренное улучшение наблюдалось у 73,1% (N=19) контрольных субъектов по сравнению с 25% (N=7) испытуемых. Заметное улучшение было замечено в 26,9% (N=7) контрольных субъектов по сравнению с 53,6% (N=15) испытуемых и только 7,1% (N=2) испытуемых показали полное заживление. Статистически значимая разница (p = 0,15) существовала между обеими группами, поскольку у большего процента испытуемых наблюдалось выздоровление. На 5-й день умеренное улучшение наблюдалось у 15,4% (N=4) контрольных субъектов по сравнению с испытуемыми. Заметное улучшение наблюдалось у 46,2% (N=12) контрольных субъектов по сравнению с 57,1% (N=16) испытуемых. Полное заживление наблюдалось у 38,5% (N=10) контрольных субъектов по сравнению с 42,9%% (N=12) испытуемых. Между обеими группами существовала статистическая разница (p = 0,24), поскольку в тестовой группе наблюдался более высокий процент субъектов с улучшением заживления язвы по сравнению с контрольной группой. На 10-й день заметное улучшение наблюдалось у 3,8% (N=1) контрольных субъектов по сравнению с 7,1% (N=2) испытуемых. Полное заживление наблюдалось у более высокого процента контрольных субъектов, 96,2% (N = 25), по сравнению с 92,9% (N = 26) испытуемых. Значение p = 0,6 показало, что статистической разницы между двумя группами не было (таблица 9).0065 9 , 10 ).
На 10-й день заметное улучшение наблюдалось у 3,8% (N=1) контрольных субъектов по сравнению с 7,1% (N=2) испытуемых. Полное заживление наблюдалось у более высокого процента контрольных субъектов, 96,2% (N = 25), по сравнению с 92,9% (N = 26) испытуемых. Значение p = 0,6 показало, что статистической разницы между двумя группами не было (таблица 9).0065 9 , 10 ).
| Параметр | Без улучшения | Умеренное улучшение | Заметное улучшение | Исцеление | р-значение | Значение | ||||
| Управление | Тест | Управление | Тест | Управление | Тест | Управление | Тест | |||
| День 1 | 100,0% | 100,0% | ||||||||
| День 3 | 0,0% | 14,3% | 73,1% | 25,0% | 26,9% | 53,6% | 0,0% | 7,1% | 0,002 | С |
| День 5 | 15,4% | 0,0% | 46,2% | 57,1% | 38,5% | 42,9% | 0,096 | НР | ||
| День 10 | 3,8% | 7,1% | 96,2% | 92,9% | 0,597 | НР | ||||
Стол 9: Сравнение оценки заживления с первого визита до четвертого визита в группе.

NS: не имеет значения; S: значимый
| Параметр | Управление | Тест | Т-значение | p-значение | ||
| Среднее (заживление) | Стандартное отклонение | Среднее (заживление) | Стандартное отклонение | |||
| Исцеление 3 дня | 1,27 | 0,45 | 1,54 | 0,83 | -1,43 | 0,15 |
| Лечение 5 дней | 2,23 | 0,7 | 2,43 | 0,5 | -1,18 | 0,24 |
| Лечение 10 дней | 2,96 | 0,19 | 2,93 | 0,26 | 0,52 | 0,6 |
Стол 10: Изменение оценки заживления со второго визита к четвертому визиту в группе.

Наиболее частый вид рецидивирующей афтозной язвы, поражающий 5-66% людей. Это чаще встречается у людей в возрасте от 10 до 40 лет, и чаще страдают женщины и люди с более высоким социально-экономическим статусом. На неороговевающей слизистой оболочке рта изъязвления могут вызвать проблемы с приемом пищи, речью и глотанием. Где-то от 2 до 48 часов до образования язвы поражения начинаются с продромального жжения. На ранних стадиях появляется небольшая область эритемы. Белые папулы появляются быстро и увеличиваются в размерах в течение следующих 48-72 часов, прежде чем превратиться в язву [5].
Обсуждение
В настоящем исследовании афтозные язвы чаще наблюдались у женщин по сравнению с мужчинами (женщины = 69,2%, мужчины = 30,8%) в контрольной группе и (женщины = 60,7%, мужчины = 39,3%) в тестовая группа. Аналогичные результаты были получены Лалабоновой и Даскаловым [11] (мужчины = 17,2%, женщины = 82,8%), а Aggarwal H et al. [12] показали преобладание мужчин (мужчины = 18, женщины = 12). Средний возраст участников настоящего исследования составил 28,13 ± 7,62 года, 25,67 ± 5,27 года в контрольной и тестовой группах соответственно, что согласуется с данными Salman H et al. [5] (11-45 лет). Лалабонова и Даскалов [11] показали более высокий средний возраст 43,01 ± 1,25 года в своем исследовании, аналогичном настоящему исследованию.
Средний возраст участников настоящего исследования составил 28,13 ± 7,62 года, 25,67 ± 5,27 года в контрольной и тестовой группах соответственно, что согласуется с данными Salman H et al. [5] (11-45 лет). Лалабонова и Даскалов [11] показали более высокий средний возраст 43,01 ± 1,25 года в своем исследовании, аналогичном настоящему исследованию.
Большинство испытуемых, участвовавших в настоящем исследовании, были студентами. Студенты демонстрируют более высокий уровень стресса во время экзаменов, и многие взрослые также страдают, когда испытывают стресс в течение многих дней [13]. Также было высказано предположение, что недостаточность сна и питания из-за образа жизни часто приводит к дефициту основных витаминов и минералов, вызывая язвы во рту [14].
Стресс считается наиболее распространенным фактором, часто предрасполагающим к афтозной язве. Доступна психометрическая оценка с помощью различных инструментов: стресс, тревога и депрессия оцениваются с помощью опросника общего состояния здоровья (GHQ) и госпитальной тревожно-депрессивной депрессии (HAD), а качество жизни — с помощью OHR-QoL и профиля воздействия на здоровье полости рта (OHIP). В настоящем исследовании анкета OHR-QoL использовалась с должным разрешением на использование инструментов. Только 81,7% испытывали трудности с произнесением любых слов, 90 % считали, что их вкусовые ощущения ухудшились, 98,3 % испытывали дискомфорт во рту, а 95 % сталкивались с трудностями при приеме пищи, когда их спрашивали об их качестве жизни. Диета была неудовлетворительной у 83,3% пациентов, прием пищи прерывался из-за проблем с зубами или полостью рта у 90%, 71,7% чувствовали себя немного смущенными, а 70% были немного раздражительными по отношению к другим. 60% сообщили о трудностях при выполнении своей обычной работы, а 63,3% считают, что жизнь в целом менее удовлетворительна. Раджан Б. и соавт. [14] показали, что 51,98% страдали болью и функциональными нарушениями, тогда как 57% имели социальные и эмоциональные проблемы. Шестьдесят восемь процентов участников Gallo Cde B et al. [15] сообщили об эмоциональном стрессе.
В настоящем исследовании анкета OHR-QoL использовалась с должным разрешением на использование инструментов. Только 81,7% испытывали трудности с произнесением любых слов, 90 % считали, что их вкусовые ощущения ухудшились, 98,3 % испытывали дискомфорт во рту, а 95 % сталкивались с трудностями при приеме пищи, когда их спрашивали об их качестве жизни. Диета была неудовлетворительной у 83,3% пациентов, прием пищи прерывался из-за проблем с зубами или полостью рта у 90%, 71,7% чувствовали себя немного смущенными, а 70% были немного раздражительными по отношению к другим. 60% сообщили о трудностях при выполнении своей обычной работы, а 63,3% считают, что жизнь в целом менее удовлетворительна. Раджан Б. и соавт. [14] показали, что 51,98% страдали болью и функциональными нарушениями, тогда как 57% имели социальные и эмоциональные проблемы. Шестьдесят восемь процентов участников Gallo Cde B et al. [15] сообщили об эмоциональном стрессе.
Варианты лечения афтозных язв варьируются от местных стероидов, антибиотиков, местных анестезирующих гелей и прижигания нитратом серебра до НИЛТ и криотерапии, а также дополнительных методов лечения, таких как прижигание нитратом серебра [16]. Уменьшение боли, меньшие по размеру язвы, меньшее количество обострений эритемы, более быстрое заживление и более низкая частота рецидивов — все это основные цели терапии.
Уменьшение боли, меньшие по размеру язвы, меньшее количество обострений эритемы, более быстрое заживление и более низкая частота рецидивов — все это основные цели терапии.
Низкоинтенсивная лазерная терапия
Только 42,3% лиц, протестированных в текущем исследовании, продемонстрировали значительное снижение оценки боли (p=0,000) после проведения НИЛИ в расфокусированном режиме (длина волны 810 нм, 80 секунд на процедуру, 6,3 Дж). /см) на 3-й день. На 5-й день у 85,9% (р=0,000) лиц отмечалось уменьшение боли, а на 10-й день — у 98,6% испытуемых (р=0,000). К 5-му дню лечения общая оценка боли у пациента значительно снизилась (р=0,000), что привело к полному уменьшению боли. Например, Khademi и Am Shirani [17], de Souza et al. [18], а также Гали и Абдулхамед [19] обнаружили аналогичные результаты с использованием диодного лазера (670 нм, 50 МВт, 1,9 см в течение 1 минуты) и сообщили, что у 75% пациентов наблюдалось уменьшение боли после лечения, а полная регрессия произошла в среднем в течение четырех дней у 40%.
Механизм уменьшения боли НИЛТ объясняется повышенной выработкой АТФ в митохондриях нейронов. Чтобы уменьшить порог возникновения потенциала действия, количество синтезируемой АТФ уменьшается. Снижение болевых раздражителей может быть вызвано увеличением выработки фермента, известного как АТФ, которое может быть вызвано использованием НИЛТ [12].
На 1-3-й (р=0,000), 5-й (р=0,000) и 10-й (р=0,000) дни размер язвы в испытуемой группе значительно уменьшился. У 28% субъектов на 3-й день было отмечено уменьшение размера язвы, которое еще больше увеличилось до 73,19% субъектов к 5-му дню, а на 10-й день у 100% субъектов язвы отсутствовали. Аггарвал Х. и соавт. [12], Бабу и др. [7] и Jijin et al. [20] (810 нм) также обнаружили, что LLLT эффективно уменьшает размер язвы у 83,2% субъектов к третьему дню, что аналогично настоящему исследованию.
Раненую ткань можно лечить лазерами из-за их способности способствовать закрытию раны путем стимуляции продукции основного фактора роста фибробластов и дифференцировки фибробластов в миофибробласты [21].
Воспаление может проявляться в виде эритемы, формирующейся вокруг афтозной язвы. Уменьшение эритемы свидетельствует о том, что процесс заживления идет по плану. На 1-3-й (р=0,000), 5-й (р=0,000) и 10-й (р=0,001) день в опытной группе наблюдалось существенное уменьшение эритемы язв. Кроме того, у всех субъектов были обнаружены поражения, окруженные эритематозным ореолом, при первом посещении, но после применения НИЛИ наблюдалось значительное уменьшение эритемы у 28,6% субъектов на 3-й день, у 60,7% субъектов на 5-й день и у 92,9% субъектов к 10 дню. Salman H et al. [5] показали аналогичные результаты, что и настоящее исследование. Наличие эритемы вокруг язвы уменьшилось с 95,2% при первом посещении до 25% после двух доз лазерного облучения.
Было показано, что оптически активированные супрессорные Т-лимфоциты способны блокировать выработку антител В-лимфоцитами, что впоследствии приводило к уменьшению воспаления [18].
Эпителизация является признаком заживления. В настоящем исследовании в тестовой группе наблюдалось значительное улучшение заживления язв, оцененное с 3 по 5 день (p = 0,000) и на 10 день (p = 0,000). После применения НИЛТ оценивали заживление язв, и к 3-му дню наблюдалось значительное улучшение у 7,1% субъектов. Далее, к 5-му дню, 42,9% испытуемых и 92,9 % испытуемых к 10 дню показали улучшение заживления очага поражения. Lalabonova H et al., Bladowski et al., De Souza T et al. показали аналогичные результаты по сравнению с настоящим исследованием. Через 4-5 дней НИЛИ у 75,6% пациентов наблюдалась полная эпителизация. Лазеры используют точные длины волн света, от красного до ближнего инфракрасного, чтобы стимулировать и улучшать восстановление тканей.
В настоящем исследовании в тестовой группе наблюдалось значительное улучшение заживления язв, оцененное с 3 по 5 день (p = 0,000) и на 10 день (p = 0,000). После применения НИЛТ оценивали заживление язв, и к 3-му дню наблюдалось значительное улучшение у 7,1% субъектов. Далее, к 5-му дню, 42,9% испытуемых и 92,9 % испытуемых к 10 дню показали улучшение заживления очага поражения. Lalabonova H et al., Bladowski et al., De Souza T et al. показали аналогичные результаты по сравнению с настоящим исследованием. Через 4-5 дней НИЛИ у 75,6% пациентов наблюдалась полная эпителизация. Лазеры используют точные длины волн света, от красного до ближнего инфракрасного, чтобы стимулировать и улучшать восстановление тканей.
Увеличение местного кровотока в тканях и расширение капилляров являются двумя побочными эффектами НИЛИ. Фотохимическое, фотофизическое и фотобиологическое воздействие НИЛТ на ткани не связано с нагревом; скорее, они являются результатом правильной дозы фотонной энергии от LLLT. Активируются тучные клетки, вырабатывается АТФ и стимулируются лимфоциты. Эти провоспалительные цитокины и лейкоциты проникают в ткани при активации тучных клеток. НИЛИ может играть важную роль в ускорении заживления ран в полости рта [7].
Активируются тучные клетки, вырабатывается АТФ и стимулируются лимфоциты. Эти провоспалительные цитокины и лейкоциты проникают в ткани при активации тучных клеток. НИЛИ может играть важную роль в ускорении заживления ран в полости рта [7].
ТА 0,1% гель
В настоящем исследовании контрольная группа (ТА 0,1%) показала постепенное снижение оценки боли с 35,2% (р=0,000) до 82,3% (р=0,000) в течение пяти дней, в то время как 98,4 % субъектов показали уменьшение боли на 10-й день (p = 0,007). Унур М. и соавт. [22], Дешмукх и Багевади [23], Корай и др. [24] и Miles DA et al. [25] обнаружили аналогичное снижение оценки боли в течение семи дней. При использовании ТА в первые три дня терапии 20% пациентов сообщили об уменьшении боли [26].
Отмечалось постепенное уменьшение размеров язв у 24,7% субъектов с 1-го по 3-й день (р=0,000) и у 70% субъектов (р=0,000) к 5-му дню, при этом полное заживление язвы наблюдалось у 100% (р=0,000) к 10 дню в контрольной группе. Мехдипур М. и соавт. [27], Дешмукх и Багевади [23], а также Офлуоглу и соавт. [28] пришли к выводу, что размер язвы можно успешно контролировать с помощью ТА в течение пяти дней, что аналогично нашему исследованию.
и соавт. [27], Дешмукх и Багевади [23], а также Офлуоглу и соавт. [28] пришли к выводу, что размер язвы можно успешно контролировать с помощью ТА в течение пяти дней, что аналогично нашему исследованию.
Отек язв значительно уменьшился в контрольной группе между 1-м и 3-м днем (р=0,001), 5-м днем (р=0,000) и 10-м днем (р=0,000). У всех субъектов при первом посещении были обнаружены поражения, окруженные эритематозным ореолом, но после нанесения геля ТА наблюдалось значительное уменьшение эритемы у 3,8% субъектов к 3-му дню, у 50% субъектов к 5-му дню и у 96,2% испытуемых к 10 дню. Salman H et al. [5] предложили ТА в качестве альтернативного лечения РАС. Наличие эритемы вокруг язвы уменьшилось с 61,5% до 7,7% при третьем визите испытуемых.
Вазоконстрикция является основным механизмом действия ТА (Кеналога), который может иметь немедленный или атипичный эффект за счет снижения уровней катехоламинов, простагландинов или рецепторов в определенных клеточных участках. Из-за уменьшенного и увеличенного прикрепления лейкоцитов к тонкому эндотелию успокаивающие эффекты ТА (Кеналога) также могут быть связаны с сопротивлением потоку полиморфных атомарных лейкоцитов через тонкие перегородки тела. Это лекарство также снижает активность лимфоцитов и макрофагов, оказывая успокаивающее действие за счет снижения активности молекул лимфокинов. Пористость клеточных мембран уменьшается, токсины или лизосомальные белки поступают медленнее, а другие химические арбитры затруднены или неправильно доставлены на протяжении огненного цикла. Каждый из этих арбитров регулярно вносит свой вклад, так что пористость сосудов и последующие изменения, такие как отек, движение лейкоцитов и образование фибрина, могут увеличиваться [29].].
Это лекарство также снижает активность лимфоцитов и макрофагов, оказывая успокаивающее действие за счет снижения активности молекул лимфокинов. Пористость клеточных мембран уменьшается, токсины или лизосомальные белки поступают медленнее, а другие химические арбитры затруднены или неправильно доставлены на протяжении огненного цикла. Каждый из этих арбитров регулярно вносит свой вклад, так что пористость сосудов и последующие изменения, такие как отек, движение лейкоцитов и образование фибрина, могут увеличиваться [29].].
После применения геля ТА в контрольной группе наблюдалось значительное улучшение заживления язв, оцененное с 3-го по 5-й день (р=0,000) и на 10-й день (р=0,000). При первом посещении 26,9% субъектов в контрольной группе продемонстрировали заметное улучшение к 3-му дню. Это увеличилось до 38,5% субъектов к 5-му дню и 96,2% субъектов к 10-му дню. Наблюдалось заживление поражения; однако результаты были незначительными (p = 0,096 и p = 0,597). Унур М. и соавт. обнаружили, что 64% пациентов продемонстрировали значительное улучшение к 7-му дню, в то время как заживление язвы было заметно к 5-му дню в текущем исследовании. M. Unur и коллеги показали, что язва заживала быстрее после терапии дексаметазоном, чем после ТА. Аналогичный результат был получен Gowharyaqub et al. [30], когда было проведено сравнение местного применения доксициклина гиклата и однократного применения ТА.
M. Unur и коллеги показали, что язва заживала быстрее после терапии дексаметазоном, чем после ТА. Аналогичный результат был получен Gowharyaqub et al. [30], когда было проведено сравнение местного применения доксициклина гиклата и однократного применения ТА.
Глюкокортикоиды, такие как триамцинолон, обладают противовоспалительными и антипролиферативными свойствами при нанесении на кожу. Связываясь с определенными участками ответа дезоксирибонуклеиновой кислоты (ДНК) в ядре и рекрутируя белки-коактиваторы, димеры могут усиливать транскрипцию генов, но они также могут противодействовать функциям других факторов транскрипции [5].
Сравнение контрольной и испытуемой групп
В настоящем исследовании мы сравнили испытуемую и контрольную группы для оценки боли, размера язв, эритемы и заживления язв. Мы обнаружили, что к 3-му дню несколько более высокий процент субъектов, 42,3%, показал уменьшение боли в испытуемой группе по сравнению с 35,2% (p = 0,79).8) в контрольной группе, а к 5-м суткам этот показатель увеличился до 85% в основной группе и 82,3% в контрольной группе (р=0,853) с полным регрессом в обеих группах к 10-м суткам (р=0,940). Таким образом, НИЛИ продемонстрировала несколько лучшее снижение уровня боли к 3-му дню по сравнению с топическими стероидами. де Соуза и др. показали такие же результаты, как и в настоящем исследовании. Мир М. и соавт. обнаружили, что лазерная ручка и триамцинолон в мази орабаза имеют сходные результаты в снижении уровня боли при РАН, что было аналогично настоящему исследованию, наблюдаемому на 10-й день.
Таким образом, НИЛИ продемонстрировала несколько лучшее снижение уровня боли к 3-му дню по сравнению с топическими стероидами. де Соуза и др. показали такие же результаты, как и в настоящем исследовании. Мир М. и соавт. обнаружили, что лазерная ручка и триамцинолон в мази орабаза имеют сходные результаты в снижении уровня боли при РАН, что было аналогично настоящему исследованию, наблюдаемому на 10-й день.
В настоящем исследовании, когда оценивали размер язвы, несколько большее количество, 28%, субъектов продемонстрировало уменьшение к 3-му дню в тестовой группе по сравнению с 24,7% субъектов (p = 0,651) в экспериментальной группе. контрольная группа. На 5-й день наблюдалось дальнейшее уменьшение размера язвы у 73,1% в опытной группе и 70% в контрольной группе (p = 0,967), а к 10-му дню язва полностью зажила. Произошло значительное изменение размера язв в обеих группах. Таким образом, лазер показывает заживление, сравнимое с местным применением ТА. Салман Х. и др. [5] показали аналогичные результаты по сравнению с настоящим исследованием.
Мы обнаружили статистически значимую разницу (p=0,13) к 3-му дню, когда у 28,6% испытуемых не было эритемы по сравнению только с 3,8% контрольных субъектов, а к 5-му дню мы обнаружили статистически значимую разницу (p=0,43). ) между двумя группами, при этом у 60,7% субъектов в испытуемой группе не было эритемы по сравнению с 50% субъектов в контрольной группе. Салман Х. и др. [5] обнаружили сравнимые результаты с текущим исследованием при изучении эритемы, хотя они не обнаружили значительной корреляции между тестовой и контрольной группами. В то время как Лалабонова и соавт. наблюдали, что эритема полностью купировалась у лиц, получавших НИЛИ, после первого сеанса, она не изменилась ни у одного из пациентов, получавших лечение стероидами, что было несопоставимо с текущим исследованием.
В настоящем исследовании, когда было проведено сравнение между испытуемой группой и контрольной группой по заживлению язв, мы обнаружили, что значительно более высокий процент испытуемых (p = 0,15) к 3-му дню, 7,1%, сообщили об исцелении, в то время как никто контрольных субъектов показали заживление язвы. Аналогичным образом, на 5-й день значительно более высокий процент субъектов (р=0,24) в опытной группе, 42,9%, показал заживление язв по сравнению с 38,5% в контрольной группе. Соуза ТОФД и др. [18] получили аналогичные результаты, что и в настоящем исследовании. Напротив, Salman H et al. [5] не обнаружили существенной разницы в группах лазера и стероидов.
Аналогичным образом, на 5-й день значительно более высокий процент субъектов (р=0,24) в опытной группе, 42,9%, показал заживление язв по сравнению с 38,5% в контрольной группе. Соуза ТОФД и др. [18] получили аналогичные результаты, что и в настоящем исследовании. Напротив, Salman H et al. [5] не обнаружили существенной разницы в группах лазера и стероидов.
Ограничения исследования включают использование ограниченного размера выборки испытуемых, и в результатах может быть систематическая ошибка из-за анализа боли по визуальной шкале, когда восприятие боли пациентом может различаться в зависимости от болевого порога пациента. . В будущих исследованиях может быть проведено долгосрочное наблюдение за пациентами.
Выводы
НИЛИ в качестве терапии нового поколения для лечения различных заболеваний полости рта в последние годы стали использовать. Эта терапия представляет собой неинвазивный способ для клиницистов контролировать многие поражения, связанные с болью и жжением в полости рта. Таким образом, можно сделать вывод, что для достижения значительного уменьшения размера язв, лучшего заживления, уменьшения эритемы и меньшей частоты рецидивов можно использовать НИЛИ. Традиционные методы лечения также могут быть использованы, но, поскольку они немного лучше справляются с болью, использование лазеров может принести значительное облегчение субъектам и, следовательно, может быть хорошей альтернативой.
Таким образом, можно сделать вывод, что для достижения значительного уменьшения размера язв, лучшего заживления, уменьшения эритемы и меньшей частоты рецидивов можно использовать НИЛИ. Традиционные методы лечения также могут быть использованы, но, поскольку они немного лучше справляются с болью, использование лазеров может принести значительное облегчение субъектам и, следовательно, может быть хорошей альтернативой.
Рецидивирующие язвы полости рта: современные и будущие терапевтические подходы
Марко Mascitti 1* и Андреа Сантарелли 1
- 1 Политехнический университет Марке, кафедра клинических и стоматологических наук, Италия
Язвы в полости рта являются распространенной жалобой, заключающейся в очаговых дефектах слизистой оболочки полости рта. Клинически язвы в полости рта можно классифицировать на: острые язвы, если они длятся менее 2 недель; хронические язвы, если они продолжаются 2 недели и дольше; и рецидивирующие язвы полости рта (РОУ), характеризующиеся повторяющимися эпизодами с прерывистым заживлением. ROU включает широкую и гетерогенную группу состояний, имеющих общие клинические признаки периодических поражений полости рта (рис. 1).
Основными причинами ROU являются типичные рецидивирующие поражения, такие как рецидивирующий афтозный стоматит (РАС), болезнь Бехчета (ББ) и рецидивирующий герпесный стоматит. Есть также несколько клинических состояний, при которых пациенты могут сообщать о ROU, но только если эти состояния проходят через периоды ремиссии, такие как травма, побочные реакции на лекарства и дефицит питания. Целью данного устного сообщения является изучение терапевтических протоколов РАС и БАР, поскольку есть только два заболевания, по которым проводится значительное количество клинических исследований.
РАС — распространенное заболевание полости рта, характеризующееся неглубокими, округлыми, болезненными язвами с воспалительными ореолами, которые рецидивируют с интервалом в несколько дней или до 3 месяцев.
Клинически язвы в полости рта можно классифицировать на: острые язвы, если они длятся менее 2 недель; хронические язвы, если они продолжаются 2 недели и дольше; и рецидивирующие язвы полости рта (РОУ), характеризующиеся повторяющимися эпизодами с прерывистым заживлением. ROU включает широкую и гетерогенную группу состояний, имеющих общие клинические признаки периодических поражений полости рта (рис. 1).
Основными причинами ROU являются типичные рецидивирующие поражения, такие как рецидивирующий афтозный стоматит (РАС), болезнь Бехчета (ББ) и рецидивирующий герпесный стоматит. Есть также несколько клинических состояний, при которых пациенты могут сообщать о ROU, но только если эти состояния проходят через периоды ремиссии, такие как травма, побочные реакции на лекарства и дефицит питания. Целью данного устного сообщения является изучение терапевтических протоколов РАС и БАР, поскольку есть только два заболевания, по которым проводится значительное количество клинических исследований.
РАС — распространенное заболевание полости рта, характеризующееся неглубокими, округлыми, болезненными язвами с воспалительными ореолами, которые рецидивируют с интервалом в несколько дней или до 3 месяцев. РАС традиционно классифицируют по клиническим признакам на малые афты (MiRAS), большие афты (MjRAS) и герпетиформные изъязвления (HeRAS). MiRAS — самая распространенная форма (80%), характеризуется округлой формой, небольшими (10 мм) и сохраняется в течение длительного периода, оставляя рубцы. HeRAS — менее распространенная форма (5-10%), состоящая из небольших и множественных язв, напоминающих язвы вируса простого герпеса. Действительно, первое использование термина афты в отношении заболеваний полости рта приписывается Гиппократу, хотя вполне вероятно, что он использовал его при описании поражения молочницей. Лишь в 1888 г. немецкий врач фон Микулич-Радецкий описал МиРАС как нозологическую единицу (Mikulicz aphthae). Что касается двух других морфологических форм РАС, а также ББ, клинические описания были опубликованы несколькими авторами в 20 веке (рис. 2).
ББ — редкое мультисистемное рецидивирующее воспалительное заболевание, входящее в группу системных васкулитов. Чаще встречается в Турции и Восточной Азии; таким образом, он также известен как «болезнь Шелкового пути».
РАС традиционно классифицируют по клиническим признакам на малые афты (MiRAS), большие афты (MjRAS) и герпетиформные изъязвления (HeRAS). MiRAS — самая распространенная форма (80%), характеризуется округлой формой, небольшими (10 мм) и сохраняется в течение длительного периода, оставляя рубцы. HeRAS — менее распространенная форма (5-10%), состоящая из небольших и множественных язв, напоминающих язвы вируса простого герпеса. Действительно, первое использование термина афты в отношении заболеваний полости рта приписывается Гиппократу, хотя вполне вероятно, что он использовал его при описании поражения молочницей. Лишь в 1888 г. немецкий врач фон Микулич-Радецкий описал МиРАС как нозологическую единицу (Mikulicz aphthae). Что касается двух других морфологических форм РАС, а также ББ, клинические описания были опубликованы несколькими авторами в 20 веке (рис. 2).
ББ — редкое мультисистемное рецидивирующее воспалительное заболевание, входящее в группу системных васкулитов. Чаще встречается в Турции и Восточной Азии; таким образом, он также известен как «болезнь Шелкового пути». Классическая клиническая триада ББ состоит из: язвы в полости рта, язвы на гениталиях и глазных проявлений. Две разные исследовательские группы (International Study Group for BD, 1990; International Criteria for BD, 2006) предложили критерии диагностики заболевания. Для этой презентации важно подчеркнуть, что ROU присутствуют почти у всех пациентов с BD и клинически сходны с RAS. Учитывая транзиторный характер этих поражений, основными терапевтическими задачами являются: купирование боли, снижение частоты рецидивов и увеличение скорости заживления ран с отсутствием/минимальными побочными эффектами.
За последние десятилетия было протестировано более 60 различных фармацевтических продуктов. Среди них местные кортикостероиды могут ускорить заживление язв и уменьшить боль. Реакция пациента варьируется в зависимости от активности активного ингредиента. Основным побочным эффектом является повышенный риск развития кандидоза полости рта. Среди нестероидных препаратов амлексанокс представляет собой местную противовоспалительную молекулу, используемую для лечения РАС.
Классическая клиническая триада ББ состоит из: язвы в полости рта, язвы на гениталиях и глазных проявлений. Две разные исследовательские группы (International Study Group for BD, 1990; International Criteria for BD, 2006) предложили критерии диагностики заболевания. Для этой презентации важно подчеркнуть, что ROU присутствуют почти у всех пациентов с BD и клинически сходны с RAS. Учитывая транзиторный характер этих поражений, основными терапевтическими задачами являются: купирование боли, снижение частоты рецидивов и увеличение скорости заживления ран с отсутствием/минимальными побочными эффектами.
За последние десятилетия было протестировано более 60 различных фармацевтических продуктов. Среди них местные кортикостероиды могут ускорить заживление язв и уменьшить боль. Реакция пациента варьируется в зависимости от активности активного ингредиента. Основным побочным эффектом является повышенный риск развития кандидоза полости рта. Среди нестероидных препаратов амлексанокс представляет собой местную противовоспалительную молекулу, используемую для лечения РАС. В нескольких исследованиях сообщалось об эффективности в уменьшении боли и размера поражения, и это наиболее эффективно, если применять его в «продромальной» фазе. Системные кортикостероиды и иммуномодулирующие препараты, такие как левамизол и талидомид, использовались у пациентов с тяжелой и неэффективной ROU для уменьшения частоты, продолжительности и тяжести поражений слизистой оболочки. Однако серьезные побочные эффекты ограничивают их использование. Антимикробные агенты, которые были протестированы у пациентов с РАН, включают антибиотики и антисептики (например, хлоргексидин). Местное применение субантимикробных доз тетрациклинов (например, миноциклин, доксициклин), по-видимому, обладает антиколлагеназной активностью и иммуномодулирующим эффектом, демонстрируя потенциальные преимущества при РАС. Хлоргексидин 0,2% ополаскиватель для полости рта является одним из наиболее часто назначаемых средств у пациентов с жалобами на ROU. Среди препаратов с «барьерным эффектом» известны сукральфат и ребамипид, успешно применяемые при лечении язвенной болезни.
В нескольких исследованиях сообщалось об эффективности в уменьшении боли и размера поражения, и это наиболее эффективно, если применять его в «продромальной» фазе. Системные кортикостероиды и иммуномодулирующие препараты, такие как левамизол и талидомид, использовались у пациентов с тяжелой и неэффективной ROU для уменьшения частоты, продолжительности и тяжести поражений слизистой оболочки. Однако серьезные побочные эффекты ограничивают их использование. Антимикробные агенты, которые были протестированы у пациентов с РАН, включают антибиотики и антисептики (например, хлоргексидин). Местное применение субантимикробных доз тетрациклинов (например, миноциклин, доксициклин), по-видимому, обладает антиколлагеназной активностью и иммуномодулирующим эффектом, демонстрируя потенциальные преимущества при РАС. Хлоргексидин 0,2% ополаскиватель для полости рта является одним из наиболее часто назначаемых средств у пациентов с жалобами на ROU. Среди препаратов с «барьерным эффектом» известны сукральфат и ребамипид, успешно применяемые при лечении язвенной болезни. По этой причине эти препараты создают защитный барьер на поверхности язв в полости рта. Лазерная терапия низкого уровня (LLLT) — это световая терапия низкой интенсивности, которая применяется для лечения САС из-за ее потенциальных полезных эффектов, включая облегчение боли и заживление ран. В настоящее время сообщается о нескольких клинических испытаниях различных типов лазеров (например, Nd:YAG, Er:YAG, InGaAlP, GaAlAs и т. д.) при использовании для лечения РАС, что свидетельствует о терапевтической полезности НИЛТ. Определенные подгруппы пациентов с РАС имеют дефицит витаминов, что указывает на роль этих молекул в патогенезе язв в полости рта. Ежедневный прием витамина B12, по-видимому, эффективен для пациентов с САС, независимо от уровня витамина B12 в сыворотке крови. Напротив, ежедневный прием поливитаминов у пациентов с РАС не приводил к снижению числа или продолжительности эпизодов язвенной болезни полости рта. Недавние исследования предполагают потенциальную терапевтическую роль ежедневного приема омега-3 в лечении САС.
По этой причине эти препараты создают защитный барьер на поверхности язв в полости рта. Лазерная терапия низкого уровня (LLLT) — это световая терапия низкой интенсивности, которая применяется для лечения САС из-за ее потенциальных полезных эффектов, включая облегчение боли и заживление ран. В настоящее время сообщается о нескольких клинических испытаниях различных типов лазеров (например, Nd:YAG, Er:YAG, InGaAlP, GaAlAs и т. д.) при использовании для лечения РАС, что свидетельствует о терапевтической полезности НИЛТ. Определенные подгруппы пациентов с РАС имеют дефицит витаминов, что указывает на роль этих молекул в патогенезе язв в полости рта. Ежедневный прием витамина B12, по-видимому, эффективен для пациентов с САС, независимо от уровня витамина B12 в сыворотке крови. Напротив, ежедневный прием поливитаминов у пациентов с РАС не приводил к снижению числа или продолжительности эпизодов язвенной болезни полости рта. Недавние исследования предполагают потенциальную терапевтическую роль ежедневного приема омега-3 в лечении САС. Натуральная фитотерапия широко использовалась в качестве терапии РАС во многих странах на протяжении веков. Сегодня фитотерапия становится все более популярной и общепризнанной во всем мире, и было проведено несколько исследований у пациентов с РАС. Тем не менее, результаты все еще слишком неопределенны, чтобы делать твердые выводы об эффективности растительных продуктов для лечения ROU. Среди других терапевтических стратегий было предложено использование каппы для предотвращения развития РАС и использование аппликаций озона на язвы в полости рта.
Были предложены различные местные и системные методы лечения, такие как ополаскиватели для рта, гели, пасты и лазеры, но лишь немногие исследования продемонстрировали эффективность в лечении ROU. По этой причине было проведено несколько систематических обзоров с целью определения клинической эффективности и безопасности местных и системных вмешательств при лечении язв полости рта при РАС и БАР.
В 2012 году Броклхерст и соавт. провели Кокрановский обзор для определения клинической эффективности системных вмешательств при САС (Brocklehurst et al.
Натуральная фитотерапия широко использовалась в качестве терапии РАС во многих странах на протяжении веков. Сегодня фитотерапия становится все более популярной и общепризнанной во всем мире, и было проведено несколько исследований у пациентов с РАС. Тем не менее, результаты все еще слишком неопределенны, чтобы делать твердые выводы об эффективности растительных продуктов для лечения ROU. Среди других терапевтических стратегий было предложено использование каппы для предотвращения развития РАС и использование аппликаций озона на язвы в полости рта.
Были предложены различные местные и системные методы лечения, такие как ополаскиватели для рта, гели, пасты и лазеры, но лишь немногие исследования продемонстрировали эффективность в лечении ROU. По этой причине было проведено несколько систематических обзоров с целью определения клинической эффективности и безопасности местных и системных вмешательств при лечении язв полости рта при РАС и БАР.
В 2012 году Броклхерст и соавт. провели Кокрановский обзор для определения клинической эффективности системных вмешательств при САС (Brocklehurst et al. , 2012). Всего было включено 25 испытаний (22 плацебо-контролируемых и 8 непосредственных сравнительных испытаний), а исследуемые препараты были сгруппированы в группы «иммуномодулирующие/противовоспалительные» и «неопределенные». Результаты показали высокий риск систематической ошибки в большинстве исследований, в основном из-за плохой методологической строгости, и ни одно системное лечение не доказало свою эффективность при РАС. В 2014 году Тейлор и соавт. провели Кокрановский обзор для определения клинической эффективности и безопасности местного и системного лечения ROU, связанного с БАР (Taylor et al., 2014). Всего было включено 15 испытаний, сгруппированных в две категории: местное и системное лечение. Результаты показали высокий риск систематической ошибки в большинстве исследований, а качество доказательств варьировалось от умеренного до очень низкого. По этим причинам не было достаточных доказательств для поддержки или опровержения использования любого включенного лечения. В 2016 году Хан и соавт.
, 2012). Всего было включено 25 испытаний (22 плацебо-контролируемых и 8 непосредственных сравнительных испытаний), а исследуемые препараты были сгруппированы в группы «иммуномодулирующие/противовоспалительные» и «неопределенные». Результаты показали высокий риск систематической ошибки в большинстве исследований, в основном из-за плохой методологической строгости, и ни одно системное лечение не доказало свою эффективность при РАС. В 2014 году Тейлор и соавт. провели Кокрановский обзор для определения клинической эффективности и безопасности местного и системного лечения ROU, связанного с БАР (Taylor et al., 2014). Всего было включено 15 испытаний, сгруппированных в две категории: местное и системное лечение. Результаты показали высокий риск систематической ошибки в большинстве исследований, а качество доказательств варьировалось от умеренного до очень низкого. По этим причинам не было достаточных доказательств для поддержки или опровержения использования любого включенного лечения. В 2016 году Хан и соавт. провели систематический обзор для оценки клинической эффективности и безопасности НИЛИ у пациентов с СПА (Han et al., 2016). Всего было включено 10 испытаний, в которых проводилось сравнение между НИЛТ и плацебо или традиционной лекарственной терапией. Результаты показали, что, хотя НИЛИ кажется многообещающим эффективным методом лечения СПА, сложность выбора протоколов лечения (например, длины волны, плотности мощности, структуры импульса, времени лечения и т. д.) привела к недостаточности доказательств в поддержку или опровержение этого нового метода. лечение. Наконец, в 2016 г. Li et al. провели систематический обзор для оценки эффективности и безопасности местного лечения натуральными растительными лекарственными средствами у пациентов с СПА (Li et al., 2016). Всего было включено 13 испытаний, в которых использовались 12 различных видов фитотерапии (8 традиционных китайских и 4 иранских продукта) в различных фармацевтических формах (полоскания, порошки, таблетки и т. д.). Методологическое качество исследований было очень низким из-за отсутствия хорошо спланированных рандомизированных клинических испытаний.
провели систематический обзор для оценки клинической эффективности и безопасности НИЛИ у пациентов с СПА (Han et al., 2016). Всего было включено 10 испытаний, в которых проводилось сравнение между НИЛТ и плацебо или традиционной лекарственной терапией. Результаты показали, что, хотя НИЛИ кажется многообещающим эффективным методом лечения СПА, сложность выбора протоколов лечения (например, длины волны, плотности мощности, структуры импульса, времени лечения и т. д.) привела к недостаточности доказательств в поддержку или опровержение этого нового метода. лечение. Наконец, в 2016 г. Li et al. провели систематический обзор для оценки эффективности и безопасности местного лечения натуральными растительными лекарственными средствами у пациентов с СПА (Li et al., 2016). Всего было включено 13 испытаний, в которых использовались 12 различных видов фитотерапии (8 традиционных китайских и 4 иранских продукта) в различных фармацевтических формах (полоскания, порошки, таблетки и т. д.). Методологическое качество исследований было очень низким из-за отсутствия хорошо спланированных рандомизированных клинических испытаний. Кроме того, гетерогенность исследований была большой из-за нескольких типов лечения, дозировки, формулы, метода применения и продолжительности эксперимента. По этим причинам нет никаких доказательств эффективности местных растительных лекарственных средств при РАС.
В заключение, окончательный протокол лечения РАС остается неубедительным, и не существует терапии для предотвращения рецидива язв в полости рта (рис. 3). Местная терапия показана пациентам с множественными эпизодами САС и/или симптомами, влияющими на качество жизни. Паста амлексанокс или стероидные препараты для местного применения являются первой линией лечения САС. Другими местными агентами могут быть хлоргексидин и антимикробная жидкость для полоскания рта. Системная терапия в настоящее время обсуждается и должна быть зарезервирована только для тяжелой и неэффективной ROU. Что касается будущих перспектив лечения ROU, настоятельно необходимы хорошо спланированные и высококачественные рандомизированные клинические испытания.
Кроме того, гетерогенность исследований была большой из-за нескольких типов лечения, дозировки, формулы, метода применения и продолжительности эксперимента. По этим причинам нет никаких доказательств эффективности местных растительных лекарственных средств при РАС.
В заключение, окончательный протокол лечения РАС остается неубедительным, и не существует терапии для предотвращения рецидива язв в полости рта (рис. 3). Местная терапия показана пациентам с множественными эпизодами САС и/или симптомами, влияющими на качество жизни. Паста амлексанокс или стероидные препараты для местного применения являются первой линией лечения САС. Другими местными агентами могут быть хлоргексидин и антимикробная жидкость для полоскания рта. Системная терапия в настоящее время обсуждается и должна быть зарезервирована только для тяжелой и неэффективной ROU. Что касается будущих перспектив лечения ROU, настоятельно необходимы хорошо спланированные и высококачественные рандомизированные клинические испытания. Кроме того, необходимо более глубоко изучить новые патофизиологические аспекты ROU, такие как роль микробиоты или генетической предрасположенности, с помощью технологий высокопроизводительного секвенирования. Использование биологических препаратов, таких как агенты против TNF-альфа, нуждается в дальнейшем изучении в рандомизированных клинических исследованиях у пациентов с неэффективной ROU. Наконец, необходимо разработать новый фармацевтический состав с целью оптимизации местной доставки лекарств на слизистую оболочку полости рта.
Кроме того, необходимо более глубоко изучить новые патофизиологические аспекты ROU, такие как роль микробиоты или генетической предрасположенности, с помощью технологий высокопроизводительного секвенирования. Использование биологических препаратов, таких как агенты против TNF-альфа, нуждается в дальнейшем изучении в рандомизированных клинических исследованиях у пациентов с неэффективной ROU. Наконец, необходимо разработать новый фармацевтический состав с целью оптимизации местной доставки лекарств на слизистую оболочку полости рта.
1. Броклхерст П., Тикл М., Гленни А.М., Льюис М.А., Пембертон М.Н., Тейлор Дж., Уолш Т., Райли П. и Йейтс Дж.М. (2012). Системные вмешательства при рецидивирующем афтозном стоматите (язвах во рту). Системная версия Кокрановской базы данных, CD005411.
2. Тейлор Дж., Гленни А.М., Уолш Т., Броклхерст П., Райли П., Городкин Р. и Пембертон М. Н. (2014). Вмешательства для лечения язв в полости рта при болезни Бехчета. Системная версия Кокрановской базы данных, CD011018.
3. Хань М., Фанг Х., Ли К.Л., Цао Ю., Ся Р. и Чжан З.Х. (2016). Эффективность лазерной терапии при лечении рецидивирующего афтозного стоматита: систематический обзор. Scientifica (Каир) 2016, 30.
4. Ли, К.Л., Хуанг, Х.Л., Ван, В.К., и Хуа, Х. (2016). Эффективность и безопасность местного лечения травяными препаратами при рецидивирующем афтозном стоматите: системный обзор. Drug Des Devel Ther 10, 107–115.
Н. (2014). Вмешательства для лечения язв в полости рта при болезни Бехчета. Системная версия Кокрановской базы данных, CD011018.
3. Хань М., Фанг Х., Ли К.Л., Цао Ю., Ся Р. и Чжан З.Х. (2016). Эффективность лазерной терапии при лечении рецидивирующего афтозного стоматита: систематический обзор. Scientifica (Каир) 2016, 30.
4. Ли, К.Л., Хуанг, Х.Л., Ван, В.К., и Хуа, Х. (2016). Эффективность и безопасность местного лечения травяными препаратами при рецидивирующем афтозном стоматите: системный обзор. Drug Des Devel Ther 10, 107–115.
Ключевые слова: Рецидивирующие язвы в полости рта, Рецидивирующий афтозный стоматит (РАС), болезнь Бехчета (ББ), Местное лечение, системное лечение
Конференция:
5-й Национальный и 1-й Международный симпозиум Итальянского общества патологии и медицины полости рта, Анкона, Италия, 19–20 октября 2018 г.
Тип презентации: устное выступление
Тема: Заболевания полости рта
Цитата: Маскитти М и Сантарелли А (2019). Рецидивирующие язвы полости рта: современные и будущие терапевтические подходы. Фронт. Физиол. Тезисы конференции: 5-й национальный и 1-й международный симпозиум Итальянского общества патологии полости рта и медицины. doi: 10.3389/conf.fphys.2019.27.00093
Авторские права:
Тезисы в этом сборнике не подвергались рецензированию или проверкам Frontiers и не одобрены Frontiers.
Они доступны через издательскую платформу Frontiers в качестве услуги для организаторов и докладчиков конференций.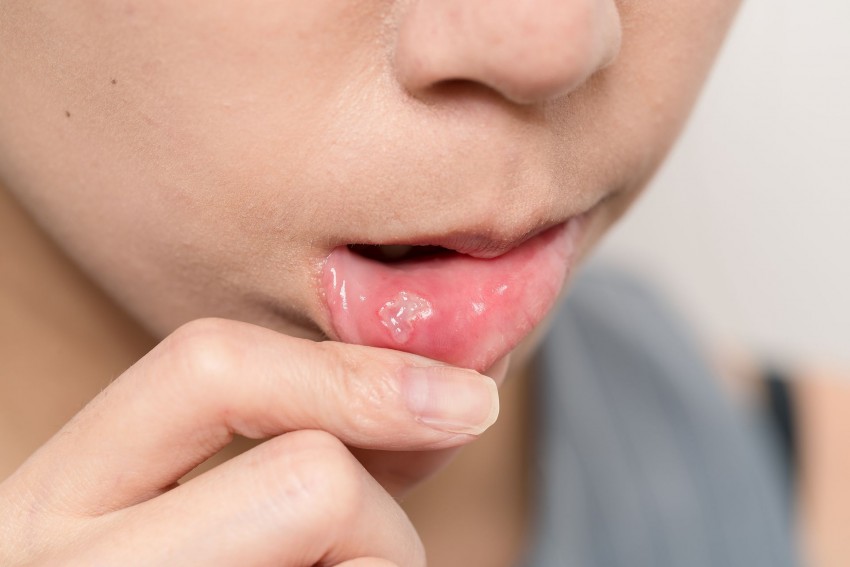
Авторские права на отдельные рефераты принадлежат автору каждого реферата или его/ее работодателю, если не указано иное.
Каждый реферат, а также коллекция рефератов публикуются под лицензией Creative Commons CC-BY 4.0 (с указанием авторства) (https://creativecommons.org/licenses/by/4.0/) и, таким образом, могут воспроизводиться, переводиться, адаптироваться. и быть предметом производных работ при условии указания авторов и Frontiers.
Условия и положения Frontiers см. на странице https://www.frontiersin.org/legal/terms-and-conditions.
Полученный: 27 ноября 2018 г .; Опубликовано в Интернете: 09 декабря 2019 г.
*
Переписка:
Доктор Марко Маскитти, Политехнический университет Марке, кафедра клинических и стоматологических наук, Анкона, Италия, marcomascitti86@hotmail. it
it
Лечение орального мукозита с применением ингибиторов mTOR: современное состояние знаний
J Oral Med Oral Surg 2019;25:11
Образовательная статья
Лечение орального мукозита с применением ингибиторов mTOR: современное состояние знаний
14 Anne Calvo ,2 * , Juliette Rochefort 1 ,2 ,3 , Marie José Javelot 1 , Vianney Descroix 1 ,2 and Géraldine Lescaille 1 ,2 ,3
1
Отделение челюстно-лицевой хирургии, Питье Сальпетриер
2
Факультет одонтологии, Париж Дидро
3
Центр иммунологии и инфекционных заболеваний (CIMI-Париж)
* Переписка: [email protected]
Получено:
28
Май
2018
Принято:
28
Август
2018
Реферат
Введение: Мукозит является хорошо известным побочным эффектом классических противоопухолевых методов лечения (химиотерапия и лучевая терапия). Благодаря значительным достижениям в персонализации лечения путем разработки таргетного лечения были описаны различные специфические внутриротовые поражения. Назначение: ингибиторы mTOR представляют собой таргетные противораковые препараты, используемые для лечения различных типов рака. Они могут вызывать внутриротовые язвы, которые могут быть серьезными, что может привести к снижению дозы или полному прекращению противоопухолевого лечения. Лечение этих инвалидизирующих и болезненных поражений является важной частью обеспечения эффективности лечения рака. Цель этой статьи — оценить современные знания о различных методах лечения, используемых в настоящее время, особенно о профилактических методах лечения. Заключение: Эффективное лечение поражений является основной частью лечения пациентов, получающих лечение ингибиторами mTOR, и должно проводиться специалистами по полости рта.
Благодаря значительным достижениям в персонализации лечения путем разработки таргетного лечения были описаны различные специфические внутриротовые поражения. Назначение: ингибиторы mTOR представляют собой таргетные противораковые препараты, используемые для лечения различных типов рака. Они могут вызывать внутриротовые язвы, которые могут быть серьезными, что может привести к снижению дозы или полному прекращению противоопухолевого лечения. Лечение этих инвалидизирующих и болезненных поражений является важной частью обеспечения эффективности лечения рака. Цель этой статьи — оценить современные знания о различных методах лечения, используемых в настоящее время, особенно о профилактических методах лечения. Заключение: Эффективное лечение поражений является основной частью лечения пациентов, получающих лечение ингибиторами mTOR, и должно проводиться специалистами по полости рта.
Ключевые слова: ингибитор mTOR / стоматит / целенаправленное противораковое лечение
© Авторы, 2019 г.
/by/4.0), что разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Введение
Известно, что лечение рака имеет много неблагоприятных побочных эффектов, особенно в полости рта [1]. Развитие лучевой терапии в конце девятнадцатого века для лечения рака верхних дыхательных путей (UADT) привело к появлению мукозита в 1930-х годах. Точно так же химиотерапевтическое лечение, начавшееся в 1940-х годах с использованием азотистого иприта и антифолатов, быстро ассоциировалось с этим осложнением. Таким образом, хорошо известно, что лучевая терапия головы и шеи и большинство традиционных цитотоксических химиотерапевтических средств могут привести к поражению слизистой оболочки желудочно-кишечного тракта и слизистой оболочки полости рта. Эти поражения являются результатом сложных биологических событий, биологическая прогрессия которых была описана Сонисом в виде пяти различных стадий. 1293 и др. в 2004 г. [2]. Первая стадия – инициация, которая непосредственно вызвана химиотерапией. В результате лечения образуются свободные радикалы, а реакция окисления вызывает разрушение клеток, тканей и сосудов. Второй этап – активация сигнала. На этом этапе свободные радикалы вызывают повреждение ДНК, что приводит к увеличению гибели клеток. Кроме того, активируются другие клеточные сигнальные пути, что приводит к выработке провоспалительных цитокинов, таких как TNF-α, IL-1 и IL-6. Затем, во время фазы передачи сигналов и амплификации, воспалительные реакции возникают циклически, вызывая каскад биологических событий, которые приводят к биологическому изменению тканей. Далее следует фаза изъязвления, во время которой воспалительные циклы могут быть очень тяжелыми и вызывать сильную боль. Язвы глубокие и широкие, обычно покрыты псевдомембраной, состоящей из мертвых фибринозных клеток. Наконец, в большинстве случаев фаза заживления наступает спонтанно в течение 2–3 недель. Результатом является возобновление эпителиальной пролиферации и дифференцировки.
1293 и др. в 2004 г. [2]. Первая стадия – инициация, которая непосредственно вызвана химиотерапией. В результате лечения образуются свободные радикалы, а реакция окисления вызывает разрушение клеток, тканей и сосудов. Второй этап – активация сигнала. На этом этапе свободные радикалы вызывают повреждение ДНК, что приводит к увеличению гибели клеток. Кроме того, активируются другие клеточные сигнальные пути, что приводит к выработке провоспалительных цитокинов, таких как TNF-α, IL-1 и IL-6. Затем, во время фазы передачи сигналов и амплификации, воспалительные реакции возникают циклически, вызывая каскад биологических событий, которые приводят к биологическому изменению тканей. Далее следует фаза изъязвления, во время которой воспалительные циклы могут быть очень тяжелыми и вызывать сильную боль. Язвы глубокие и широкие, обычно покрыты псевдомембраной, состоящей из мертвых фибринозных клеток. Наконец, в большинстве случаев фаза заживления наступает спонтанно в течение 2–3 недель. Результатом является возобновление эпителиальной пролиферации и дифференцировки. Клинически ткань выглядит здоровой, но остается значительно измененной.
Клинически ткань выглядит здоровой, но остается значительно измененной.
За последние 20 лет появились новые методы лечения в эпоху персонализированного лечения. Фактически, чтобы повысить эффективность лечения раковых клеток при одновременном снижении их токсичности, были разработаны методы лечения, специально нацеленные на определенные молекулярные пути в каждом раке: моноклональные антитела (суффикс -mab) и киназы-ингибиторы белков (суффикс -nib). Последние подразделяются на ингибиторы тирозинкиназы и ингибиторы серин-треонинкиназы (STKI), к которым относятся ингибиторы mTOR (суффикс -imus).
Хотя многие ингибиторы протеинкиназы могут быть связаны с поражением полости рта, ингибиторы mTOR являются наиболее опасными, особенно при тяжелых формах, требующих снижения дозы или прекращения лечения рака. Эти поражения отличаются от классических случаев мукозита.
Ингибиторы mTOR и применение в онкологии
Мишень рапамицина у млекопитающих, также известная как mTOR, была обнаружена в рапамицине, выделенном из Streptomyces hygroscopicus на острове Пасхи, и впервые была использована из-за его противогрибковых свойств. Одно из показаний к применению рапамицина, также называемого сиролимусом (Rapamune®), связано с его иммунодепрессивными свойствами, и в 2001 году ему было выдано разрешение на продажу при трансплантации почек для предотвращения отторжения трансплантата. В настоящее время он заменяет циклоспорин, если он противопоказан, а также используется из-за его антипролиферативных свойств на сосудистых стентах [3].
Одно из показаний к применению рапамицина, также называемого сиролимусом (Rapamune®), связано с его иммунодепрессивными свойствами, и в 2001 году ему было выдано разрешение на продажу при трансплантации почек для предотвращения отторжения трансплантата. В настоящее время он заменяет циклоспорин, если он противопоказан, а также используется из-за его антипролиферативных свойств на сосудистых стентах [3].
Тем не менее, в результате определения роли этой серин-треониновой внутриклеточной протеинкиназы, особенно в развитии и пролиферации клеток, появились другие указания на наличие ингибиторов mTOR. Его сигнальный путь на самом деле является частью пути PI3K/AKT/mTOR, который может быть затронут многими способами выше или ниже этой молекулы при различных типах рака.
Учитывая иммуносупрессивные эффекты, наблюдаемые при применении рапамицина, были разработаны другие аналоги с целью блокирования пути mTOR для наблюдения за противоопухолевыми эффектами за счет блокирования клеточного цикла, а также за счет снижения скорости экспрессии фактора роста эндотелия сосудов, что потенцирует процесс опухолевый ангиогенез.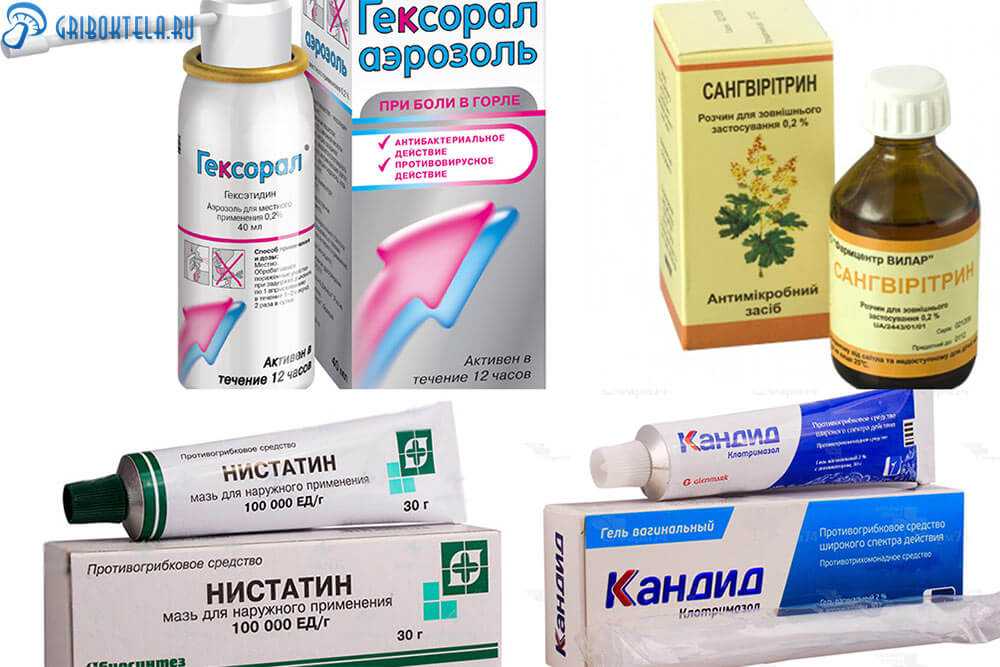 Ингибиторы mTOR, применяемые в онкологии, представляют собой селективные ингибиторы, вводимые перорально: темсиролимус (Торисел®) и эверолимус (Афинитор®). Ридафоролимус также используется в Соединенных Штатах, но не продается во Франции.
Ингибиторы mTOR, применяемые в онкологии, представляют собой селективные ингибиторы, вводимые перорально: темсиролимус (Торисел®) и эверолимус (Афинитор®). Ридафоролимус также используется в Соединенных Штатах, но не продается во Франции.
Темсиролимус показан при почечно-клеточном раке и мантийно-клеточной лимфоме, в то время как эверолимус, представляющий собой ингибирующую молекулу mTOR, наиболее назначаемую во Франции, имеет несколько показаний:
-
Рак почки на поздней стадии после неэффективности антиангиогенного лечения, такого как антиангиогенный сунитиниб (Сутент®) и сорафениб (Неваксар®)
-
Нейроэндокринные опухоли поджелудочной железы, не поддающиеся резекции, локально агрессивные или метастатические
-
HER2/neu-отрицательный и гормон-рецептор-положительный рак молочной железы у женщин в постменопаузе. В последнем случае эверолимус назначают после неэффективности лечения нестероидными ингибиторами ароматазы (летрозол (Фемара®) или анастрозол (Аримидекс®)) и сочетают с лечением экземестаном (Аромазин®).
Эпидемиология мукозита, вызванного ингибиторами mTOR
Мукозит является одним из наиболее распространенных и ограниченных видов токсичности, вызываемых ингибиторами mTOR. Обзор литературы, выполненный Мартиньшем и др. [4], который включает 44 исследования с участием более 2800 пациентов, получавших первичную терапию темсиролимусом или эверолимусом, показывает, что мукозит является наиболее частым побочным эффектом, которым страдают 73,4% пациентов, причем более 30% этих тяжелых случаев (20,7% степени 3 и 10). % класс 4). Эти поражения сохраняются в среднем через 10 дней после начала лечения, а тяжесть мукозита коррелирует с дозой [4]. Наконец, было замечено, что пациенты, получающие эверолимус в максимальной дозе (10 мг) в сочетании с экземестаном для лечения метастатического рака молочной железы, более склонны к развитию мукозита [5].
Клиническая картина мукозита, вызванного ингибиторами mTOR
Поражения полости рта, возникающие при лечении ингибитором mTOR, называемые mIAS (стоматит, ассоциированный с ингибитором mTOR), отличаются от мукозита, вызванного химиотерапией или лучевой терапией [6]. Они похожи на обычные одиночные или множественные поражения, которые часто представляют собой афтоидные поражения круглой или овальной формы с определенными характеристиками (рис. 1): [7]
Они похожи на обычные одиночные или множественные поражения, которые часто представляют собой афтоидные поражения круглой или овальной формы с определенными характеристиками (рис. 1): [7]
-
Обычно <1 см в диаметре
-
Очень инвалидизирующие даже при меньшем размере по сравнению с поражениями, вызванными другими методами лечения рака
-
Преимущественное поражение слизистых оболочек с небольшим ороговением или без него (слизистая оболочка щек, губ, языка и дна полости рта)
-
Поражает только ротовую полость, но не пищеварительный тракт [7–10]
Для определения тяжести этих язв в онкологии традиционно используют несколько международных шкал с использованием классификаций ВОЗ и Национального института рака NCI-CTCAE 3.0 и 4.0. Они основаны на функциональном воздействии, более или менее связанном с тяжестью и степенью клинических поражений (рис. 2).
|
Рисунок 1
Индуцированный эверолимусом мукозит с локализацией на латеральной поверхности языка. |
|
Рис. 2
NCI-CTCAE 3.0 и классификация ВОЗ для мукозита. |
Патофизиологические механизмы мукозита, вызванного ингибиторами mTOR
Однако мукозит является известным побочным эффектом лечения рака, вызванным токсичностью для тканей, механизмы, лежащие в основе осложнений со стороны слизистой оболочки полости рта при использовании ингибитора mTOR, не понятны, хотя было предложено несколько гипотез в качестве прямые или непрямые механизмы.
Принимая во внимание клинический афтоидный аспект, было предложено сходство между мИАС и рецидивирующим афтозным стоматитом (РАС). Петерсон и др. в 2016 г. [11] (рис. 3) предположили, что патофизиологические механизмы этих поражений могут быть сходными из-за хорошего терапевтического ответа на стероиды в обоих случаях. В случаях RAS эта команда также наблюдала, что иммунная инфильтрация поражений сочетала снижение регуляторных Т-клеток и сильную инфильтрацию цитотоксических Т-лимфоцитов, которые также можно было обнаружить при mIAS. Для других микробиота полости рта может вызывать поражения РАС и играть аналогичную роль в возникновении мИАС [12]. Однако исследование, опубликованное в 2017 г. [13], с использованием in vitro Органотипическая модель мИАС предполагает отсутствие связи между микробиотой полости рта и какой-либо индуцированной токсичностью этих противоопухолевых препаратов. Далее было показано, что сама молекула вызывает морфологические и цитологические изменения в слизистой оболочке полости рта. Наблюдались повышенный апоптоз и снижение клеточной пролиферации, а также высвобождение провоспалительных цитокинов, полученных из кератиноцитов в отсутствие бактерий [13].
Для других микробиота полости рта может вызывать поражения РАС и играть аналогичную роль в возникновении мИАС [12]. Однако исследование, опубликованное в 2017 г. [13], с использованием in vitro Органотипическая модель мИАС предполагает отсутствие связи между микробиотой полости рта и какой-либо индуцированной токсичностью этих противоопухолевых препаратов. Далее было показано, что сама молекула вызывает морфологические и цитологические изменения в слизистой оболочке полости рта. Наблюдались повышенный апоптоз и снижение клеточной пролиферации, а также высвобождение провоспалительных цитокинов, полученных из кератиноцитов в отсутствие бактерий [13].
|
Рис. 3
Сравнение клинических характеристик рецидивирующего афтоидного стоматита и стоматита, вызванного ингибитором рапамицина у млекопитающих. |
Лечение мукозита
Лечение мукозита в основном поддерживающее, что описано в публикациях MASCC (Многонациональной ассоциации поддерживающей терапии при раке). Таким образом, стандартное лечение мукозита основано на установлении подходящего режима гигиены полости рта и использовании 1,4% раствора бикарбоната натрия для полоскания рта, обычно используемого в сочетании с местными анестетиками, анальгетиками и противоязвенными препаратами. Существует также противогрибковая «волшебная жидкость для полоскания рта», в которой бикарбонат сочетается с антисептическим средством для полоскания рта, которое было признано неэффективным и поэтому в настоящее время не рекомендуется. Это лечение должно быть адаптировано в зависимости от тяжести мукозита и может потребовать снижения дозы или временного перерыва в лечении рака, а также, при необходимости, использования системных методов лечения.
Таким образом, стандартное лечение мукозита основано на установлении подходящего режима гигиены полости рта и использовании 1,4% раствора бикарбоната натрия для полоскания рта, обычно используемого в сочетании с местными анестетиками, анальгетиками и противоязвенными препаратами. Существует также противогрибковая «волшебная жидкость для полоскания рта», в которой бикарбонат сочетается с антисептическим средством для полоскания рта, которое было признано неэффективным и поэтому в настоящее время не рекомендуется. Это лечение должно быть адаптировано в зависимости от тяжести мукозита и может потребовать снижения дозы или временного перерыва в лечении рака, а также, при необходимости, использования системных методов лечения.
Учитывая клинические различия между мИАС и классическим мукозитом, необходимо специальное лечение. Несмотря на то, что клинических испытаний с высоким уровнем доказательности все еще мало, несколько групп экспертов предложили лечение поражений полости рта, вызванных ингибиторами mTOR [14–16]. Мы решили детализировать в этой статье конкретные аспекты этого управления.
Мы решили детализировать в этой статье конкретные аспекты этого управления.
Снижение дозы или прекращение лечения ингибитором mTOR
Таблица корректировки дозы предоставляется фармацевтической компанией в случае возникновения побочных эффектов. В случае поражений полости рта корректировка проводится на основе функциональных последствий (рис. 4). Причины изменения схем лечения изучались в нескольких когортных исследованиях. По Мартинсу и др. . снижение дозы потребовалось у 19,2% пациентов, получавших ингибиторы mTOR. Основными причинами такого снижения дозы были тромбоцитопения (37,2%) и мукозит (27,3%) [5]. В исследовании BOLERO-2 24% пациентов, получавших эверолимус в комбинации с экземестаном, нуждались в снижении дозы или прерывании лечения из-за мукозита любой степени тяжести.
|
Рис. 4
Коррекция дозы ингибиторов mTOR. |
Управление наркотиками
Противовоспалительные препараты
Одноцентровый ретроспективный анализ показывает, что у 87% пациентов, получавших ингибиторы mTOR (эверолимус или ридафоролимус), наблюдалось улучшение симптомов после местного или системного лечения кортикостероидами [11,18].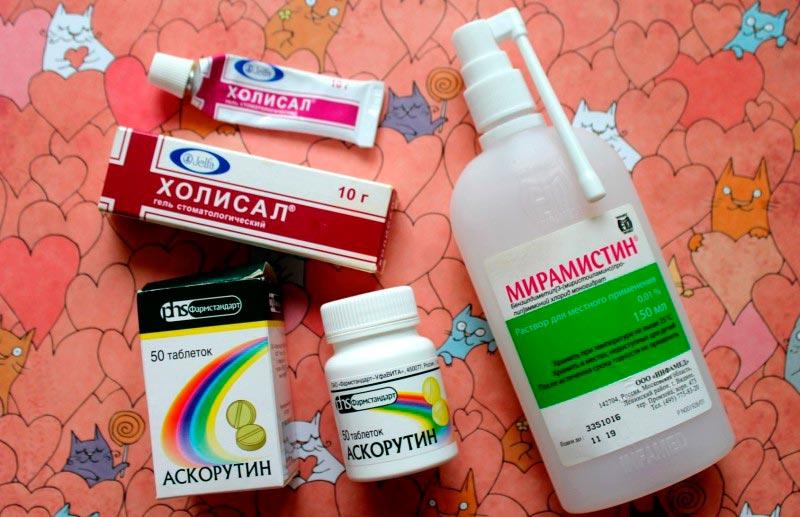 В другом недавнем исследовании (исследование SWISH), включавшем 86 пациентов в рамках многоцентрового одногруппового исследования фазы 2, показано, что профилактическое местное применение кортикостероидов приводит к очень значительному снижению частоты развития мукозита 2 степени как части лечения экземестаном и everolimus (частота 2,4% против 33% в исследовании BOLERO-2) [19]. После информирования пациентов о гигиене полости рта протокол начинали с полоскания рта раствором 10 мл дексаметазона в концентрации 0,5 мг/5 мл, начиная с первой дозы эверолимуса, из расчета четыре полоскания рта в день в течение минимум 8 недель, затем на усмотрение практикующего. Раствор выдерживали во рту 2 мин без приема пищи и жидкости в течение 1 ч. Помимо влияния на снижение местной токсичности, жидкости для полоскания рта с дексаметазоном хорошо переносились пациентами, и только у двух пациентов развилась грибковая инфекция. Другим преимуществом является то, что лечение рака может быть продолжено у пациентов без каких-либо модификаций дозы.
В другом недавнем исследовании (исследование SWISH), включавшем 86 пациентов в рамках многоцентрового одногруппового исследования фазы 2, показано, что профилактическое местное применение кортикостероидов приводит к очень значительному снижению частоты развития мукозита 2 степени как части лечения экземестаном и everolimus (частота 2,4% против 33% в исследовании BOLERO-2) [19]. После информирования пациентов о гигиене полости рта протокол начинали с полоскания рта раствором 10 мл дексаметазона в концентрации 0,5 мг/5 мл, начиная с первой дозы эверолимуса, из расчета четыре полоскания рта в день в течение минимум 8 недель, затем на усмотрение практикующего. Раствор выдерживали во рту 2 мин без приема пищи и жидкости в течение 1 ч. Помимо влияния на снижение местной токсичности, жидкости для полоскания рта с дексаметазоном хорошо переносились пациентами, и только у двух пациентов развилась грибковая инфекция. Другим преимуществом является то, что лечение рака может быть продолжено у пациентов без каких-либо модификаций дозы.
Во Франции продукты, доступные для местного применения стероидных противовоспалительных препаратов, в основном представляют собой преднизолон (Solupred®) в дозе 60 мг в половине стакана воды для использования в качестве жидкости для полоскания рта три раза в день и клобетазол 0,05% гель (Dermoval ® гель). Дексаметазон выпускается во флаконах по 20 мг/5 мл или 4 мг/1 мл для полоскания рта и метилпреднизолон 1 г (Solumedrol® 1 г) в виде порошка и растворяется в растворе для инъекций с помощью шприца. Профилактическое и лечебное назначение хлоргексидинового антисептика для полоскания рта не показало эффективности при этом состоянии [17]; следовательно, противовоспалительные препараты кажутся более перспективным подходом.
Другое поглощение: возможности низкочастотного лазера
Термин «лазер» является аббревиатурой для усиления света за счет стимулированного излучения. Существуют различные типы лазеров в зависимости от желаемого эффекта, времени воздействия и плотности мощности. Клеточные эффекты зависят от длины волны, дозы энергии, режима излучения и продолжительности воздействия луча на ткани. В многочисленных публикациях было показано, что маломощный лазер (НИЛИ для низкоинтенсивной лазерной терапии) эффективен при лечении мукозита в диапазоне длин волн 633–685 или 780–830 нм и мощности от 10 до 150 мВт, с энергия 2–3 Дж/см 9№ 1189 2 на обрабатываемую поверхность. Эти эффекты наблюдались особенно у молодых пациентов в рамках лечения гемопоэтическими стволовыми клетками при гематологических злокачественных новообразованиях или у пациентов, получавших лучевую терапию/химиотерапию при раке UADT [20]. Экспериментально было высказано предположение, что НИЛИ может снижать экспрессию воспалительных цитокинов, включая фактор некроза опухоли α (TNF α) и интерлейкин 1 (IL 1) [21]. Некоторые также предлагают использовать НИЛИ отдельно или в сочетании с кортикоидными ополаскивателями для лечения мИАС. Однако на сегодняшний день нет клинических испытаний, подтверждающих его использование по этому показанию.
Клеточные эффекты зависят от длины волны, дозы энергии, режима излучения и продолжительности воздействия луча на ткани. В многочисленных публикациях было показано, что маломощный лазер (НИЛИ для низкоинтенсивной лазерной терапии) эффективен при лечении мукозита в диапазоне длин волн 633–685 или 780–830 нм и мощности от 10 до 150 мВт, с энергия 2–3 Дж/см 9№ 1189 2 на обрабатываемую поверхность. Эти эффекты наблюдались особенно у молодых пациентов в рамках лечения гемопоэтическими стволовыми клетками при гематологических злокачественных новообразованиях или у пациентов, получавших лучевую терапию/химиотерапию при раке UADT [20]. Экспериментально было высказано предположение, что НИЛИ может снижать экспрессию воспалительных цитокинов, включая фактор некроза опухоли α (TNF α) и интерлейкин 1 (IL 1) [21]. Некоторые также предлагают использовать НИЛИ отдельно или в сочетании с кортикоидными ополаскивателями для лечения мИАС. Однако на сегодняшний день нет клинических испытаний, подтверждающих его использование по этому показанию. Поэтому можно предложить рекомендации и свести их в сводную таблицу [10] на основе модифицированного NCI-CTCAE 4.0. Алгоритм (рис. 5).
Поэтому можно предложить рекомендации и свести их в сводную таблицу [10] на основе модифицированного NCI-CTCAE 4.0. Алгоритм (рис. 5).
|
Рис. 5
Предлагаемые стратегии профилактики или лечения стоматита, связанного с ингибитором mTOR [10]. |
Заключение
Курс лечения ингибиторами mTOR может потребоваться прекратить при появлении тяжелого мукозита. Таким образом, лечение этих проявлений представляет собой серьезную проблему в общем лечении пациентов. Недавние исследования подтверждают хороший ответ афтоидных язв на лечение кортикостероидами, а профилактические полоскания рта дексаметазоном, по-видимому, обеспечивают адекватный ответ на эту проблему, позволяя чистое снижение частоты этих поражений. Следовательно, требуется стандартизированный процесс лечения, учитывающий профилактический мукозит, вызванный ингибиторами mTOR. Это предполагает тесное сотрудничество между специалистами по полости рта и онкологами, что позволяет создать курс лечения, при котором пациента после стоматологического осмотра и стоматологической реабилитации обучают правилам гигиены, информируют об этих поражениях и лечат их. Рис. 6).
Рис. 6).
|
Рис. 6
Процедура лечения пациентов, получающих лечение ингибиторами mTOR. |
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении этой статьи.
Каталожные номера
- Sibaud V, Vigarios E. Toxicités orales des thérapies ciblées anticancéreuses. Med Buccale Chir Buccale 2015; 21: 149–155. [Перекрестная ссылка] [Google ученый]
-
Sonis ST, Elting LS, Keefe D, Peterson DE, Schubert M, Hauer-Jensen M, et al. Перспективы повреждения слизистой оболочки, вызванного терапией рака: патогенез, измерение, эпидемиология и последствия для пациентов.
 Рак 2004; 100 (9 Дополнение): 1995–2025.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
Рак 2004; 100 (9 Дополнение): 1995–2025.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
- Степковски С.М., Тиан Л., Наполи К.Л., Гобриал Р., Ван М.Е., Чжоу Т.К. и др. Синергические механизмы, с помощью которых сиролимус и циклоспорин ингибируют отторжение аллотрансплантата сердца и почки крысы. Clin Exp Immunol 1997; 108:63–68. [Google ученый]
-
Мартинс Ф.
 , де Оливейра М.А., Ван К., Сонис С., Галлотини М., Джордж С. и др. Обзор пероральной токсичности, связанной с терапией ингибитором mTOR у онкологических больных. Oral Oncol 2013; 49: 293–298.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
, де Оливейра М.А., Ван К., Сонис С., Галлотини М., Джордж С. и др. Обзор пероральной токсичности, связанной с терапией ингибитором mTOR у онкологических больных. Oral Oncol 2013; 49: 293–298.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Руго Х.С., Причард К.И., Гнант М., Ногучи С., Пиккарт М., Хортобаги Г. и соавт. Частота и динамика нежелательных явлений, связанных с эверолимусом, у женщин в постменопаузе с распространенным раком молочной железы, положительным по гормональным рецепторам: выводы из BOLERO-2.
 Энн Онкол 2014; 25: 808–815.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
Энн Онкол 2014; 25: 808–815.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
- Agbo-Godeau SN, Scotte F. Gestion des effets secondaires des thérapies ciblées dans le Cancer du Rein: вторичные стоматологические эффекты (муциты, носовое кровотечение). Bull Cancer 2011; 98: 117–126. [Google ученый]
-
Vigarios E, Epstein JB, Sibaud V.
 Изменения слизистой оболочки полости рта, вызванные противоопухолевой таргетной терапией и ингибиторами иммунных контрольных точек. Support Care Cancer 2017; 25 (5): 1713–1739.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
Изменения слизистой оболочки полости рта, вызванные противоопухолевой таргетной терапией и ингибиторами иммунных контрольных точек. Support Care Cancer 2017; 25 (5): 1713–1739.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Сонис С., Трейстер Н., Чавла С., Деметри Г., Халуска Ф. Предварительная характеристика поражений полости рта, связанных с ингибиторами мишени рапамицина у млекопитающих у больных раком. Рак 2010; 116 (1): 210–215.
 [В паблике]
[Google ученый]
[В паблике]
[Google ученый]
- Бурс-Доэтс К.Б., Эпштейн Дж.Б., Рабер-Дурлахер Дж.Е., Оуверкерк Дж., Логан Р.М., Бракенхофф Дж.А. и др. Пероральные нежелательные явления, связанные с тирозинкиназой и ингибиторами рапамицина у млекопитающих при почечно-клеточной карциноме: структурированный обзор литературы. Онколог 2012;17 (1):135–144. [Перекрестная ссылка] [В паблике] [Google ученый]
-
Мартинс Ф.
 , де Оливейра М.А., Ван К., Сонис С., Галлоттини М., Джордж С., Трейстер Н. Обзор пероральной токсичности, связанной с терапией ингибитором mTOR у онкологических больных. Oral Oncol 2013; 49 (4): 293–298.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
, де Оливейра М.А., Ван К., Сонис С., Галлоттини М., Джордж С., Трейстер Н. Обзор пероральной токсичности, связанной с терапией ингибитором mTOR у онкологических больных. Oral Oncol 2013; 49 (4): 293–298.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Peterson DE, O’Shaughnessy JA, Rugo HS, Elad S, Schubert MM, Viet CT, et al. Повреждение слизистой оболочки полости рта, вызванное мишенью ингибиторов рапамицина у млекопитающих: новые перспективы патобиологии и влияние на клиническую практику.
 Cancer Med 2016; 5 (8): 1897–1907.
[Google ученый]
Cancer Med 2016; 5 (8): 1897–1907.
[Google ученый]
- Bankvall M, Sjoberg F, Gale G, Wold A, Jontell M, Ostman S. Микробиота полости рта у пациентов с рецидивирующим афтозным стоматитом. J Oral Microbiol 2014;6:25739. [Перекрестная ссылка] [В паблике] [Google ученый]
-
Сонис С.
 , Андреотта П.В., Линг Г. О патогенезе стоматита, связанного с ингибитором mTOR (mIAS) — исследования с использованием органотипической модели слизистой оболочки полости рта. Oral Dis 2017; 23 (3): 347–352.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
, Андреотта П.В., Линг Г. О патогенезе стоматита, связанного с ингибитором mTOR (mIAS) — исследования с использованием органотипической модели слизистой оболочки полости рта. Oral Dis 2017; 23 (3): 347–352.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Divers J, O’Shaughnessy J. Стоматит, связанный с использованием ингибиторов mTOR: последствия для пациентов с инвазивным раком молочной железы. Клин Дж. Онкол Нурс 2015; 19: 468–474.
 [Перекрестная ссылка]
[В паблике]
[Google ученый]
[Перекрестная ссылка]
[В паблике]
[Google ученый]
- Порта С., Останто С., Раво А., Климент М.А., Вайшампаян У., Уайт Д.А. и др. Лечение нежелательных явлений, связанных с применением эверолимуса у пациентов с распространенным почечно-клеточным раком. Eur J Рак 2011; 47: 1287–1298. [Перекрестная ссылка] [В паблике] [Google ученый]
-
Пилотт А.
 П., Хохос М.Б., Полсон К.М., Хуфтален Т.М., Трейстер М. Лечение стоматита у пациентов, получавших лечение ингибиторами рапамицина у млекопитающих. Clin J Oncol Nurs 2011;15:E83–E89.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
П., Хохос М.Б., Полсон К.М., Хуфтален Т.М., Трейстер М. Лечение стоматита у пациентов, получавших лечение ингибиторами рапамицина у млекопитающих. Clin J Oncol Nurs 2011;15:E83–E89.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Cardona A, Balouch A, Abdul MM, Sedghizadeh PP, Enciso R. Эффективность хлоргексидина для профилактики и лечения орального мукозита у онкологических больных: систематический обзор с метаанализами.
 J Oral Pathol Med 2017; 46 (9): 680–688.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
J Oral Pathol Med 2017; 46 (9): 680–688.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
- де Оливейра М.А., Мартинс К., Ван С., Сонис С., Деметри С., Джордж С. и др. Клиническая картина и лечение стоматита, связанного с ингибитором mTOR. Oral Oncol 2011;47:998–1003. [Перекрестная ссылка] [В паблике] [Google ученый]
-
Руго Х.
 С., Сеневиратне Л., Бек Дж.Т., Гласпи Дж.А., Пегуэро Дж.А., Плуард Т.Дж. и др. Профилактика стоматита, связанного с эверолимусом, у женщин с гормональным рецептор-положительным, HER2-отрицательным метастатическим раком молочной железы с помощью жидкости для полоскания рта дексаметазоном (SWISH): одногрупповое исследование фазы 2. Ланцет Онкол 2017;18(5):654–662.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
С., Сеневиратне Л., Бек Дж.Т., Гласпи Дж.А., Пегуэро Дж.А., Плуард Т.Дж. и др. Профилактика стоматита, связанного с эверолимусом, у женщин с гормональным рецептор-положительным, HER2-отрицательным метастатическим раком молочной железы с помощью жидкости для полоскания рта дексаметазоном (SWISH): одногрупповое исследование фазы 2. Ланцет Онкол 2017;18(5):654–662.
[Перекрестная ссылка]
[В паблике]
[Google ученый]
-
Lescaille G, Lang P, Ernenwein D, Javelot MJ, Descroix V.
 Intérêt de la photothérapie au Laser pour le traitement des mucites de la cavité buccale. Презентация d’un cas et revue de la littérature. Med Buccale Chir Buccale 2010; 16: 171–176.
[Перекрестная ссылка]
[Google ученый]
Intérêt de la photothérapie au Laser pour le traitement des mucites de la cavité buccale. Презентация d’un cas et revue de la littérature. Med Buccale Chir Buccale 2010; 16: 171–176.
[Перекрестная ссылка]
[Google ученый]
- Bensadoun RJ, Franquin JC, Ciais G, Darcourt V, Schubert MM, Viot M, et al. Низкоэнергетический гелий-неоновый лазер в профилактике радиационно-индуцированного мукозита. Многоцентровое рандомизированное исследование III фазы у больных раком головы и шеи. Support Care Cancer 1999;7(4):244–252. [Перекрестная ссылка] [В паблике] [Google ученый]
Все фигурки
|
Рисунок 1
Индуцированный эверолимусом мукозит с локализацией на латеральной поверхности языка. |
|
| В тексте | |
|
Рис. 2
NCI-CTCAE 3.0 и классификация ВОЗ для мукозита. |
|
| В тексте | |
|
Рис. 3
Сравнение клинических характеристик рецидивирующего афтоидного стоматита и стоматита, вызванного ингибитором рапамицина у млекопитающих. |
|
| В тексте | |
|
Рис. 4
Коррекция дозы ингибиторов mTOR. |
|
| В тексте | |
|
Рис. 5
Предлагаемые стратегии профилактики или лечения стоматита, связанного с ингибитором mTOR [10]. |
|
| В тексте | |
|
Рис. 6
Процедура лечения пациентов, получающих лечение ингибиторами mTOR. |

