Острый фиброзный пульпит, хронический фиброзный пульпит, лечение фиброзного пульпита.
Фиброзный пульпит является одной из разновидностей хронического пульпита. Его характерная особенность заключается в чрезмерном разрастании волокон соединительной ткани в полости зуба, что в итоге приводит к нарушениям кровоснабжения пульпы и её отмиранию.
Обращение за профессиональной помощью при хроническом фиброзном пульпите вовремя — залог восстановления внешнего вида и функциональных характеристик зуба. В то же время запущенное заболевание может привести к отмиранию пульпы и распространению воспалительного процесса на периодонт.
Стоит отметить, что хронический фибриозный пульпит может развиться в результате отсутствия лечения острого пульпита, а может быть и первичным процессом без острой стадии. Он может появиться и развиваться как на молочных, так и на постоянных зубах. Лечение фиброзного пульпита предусматривает хирургическое вмешательство.
Постановка временной пломбы — 550
Резекции верхушки корня (фронтальная группа) — 7000
Резекции верхушки корня (жевательная группа) — 9500
Механическая и медикаментозная обработка каналов при периодонтите (1 канал) — 1300
Закрытие перфораций (МТА) — 6 500
Этиология фиброзного пульпита
Причина развития хронической формы заболевания заключается во вскрытии коронковой зубной полости при остром фиброзном пульпите. Она сопровождается оттоком экссудата и некоторым облегчением для больного, поскольку боли, которые возникали при его накоплении, стихнут. Такой пульпит называют вторичным. Что касается первичного, то он является самостоятельной формой этого патологического состояния и развивается в закрытой полости зуба. Причины — нарушение техники проведения лечения кариеса запущенной формы (а именно — некорректное проведение обработки зубной полости, наложение лечебной прокладки или механическое повреждение зуба при вскрытии пульповой камеры).
Она сопровождается оттоком экссудата и некоторым облегчением для больного, поскольку боли, которые возникали при его накоплении, стихнут. Такой пульпит называют вторичным. Что касается первичного, то он является самостоятельной формой этого патологического состояния и развивается в закрытой полости зуба. Причины — нарушение техники проведения лечения кариеса запущенной формы (а именно — некорректное проведение обработки зубной полости, наложение лечебной прокладки или механическое повреждение зуба при вскрытии пульповой камеры).
Формы фиброзного пульпита
Выделяют две формы фиброзного пульпита: острую и хроническую. Чаще всего вторая возникает вследствие первой; помимо этого, возможны и обострения хронического фиброзного пульпита.
Хроническую форму можно назвать компенсацией, при которой происходит фиброзная трансформация нерва зуба с минимальным количеством экссудата. Процесс характеризуется разрастанием волокон соединительной ткани в зубном канале и уменьшением чувствительности зубного нерва. Он возникает в результате реактивности организма, который пытается подстроиться под происходящие процессы изменениями структуры пульпы. Последняя при этом не распадается.
Он возникает в результате реактивности организма, который пытается подстроиться под происходящие процессы изменениями структуры пульпы. Последняя при этом не распадается.
Воспалительные процессы пульпы в этот период исключают острые боли. Чаще всего этому способствует деструкция зуба под воздействием кариозных процессов, которая создаёт отток жидкости через отверстие. Несмотря на то, что болевая симптоматика при хронической форме несильная, зуб требует немедленного лечения. Пройдёт совсем немного времени — и часть пульпы погибнет, начнётся её некротизация, а гнойные воспалительные процессы перекинутся на ткани вокруг зубного корня. Результат? Охватывание надкостницы, развитие флюса и (нередко) удаление зуба.
Клинические проявления
Нередко эта разновидность пульпита протекает практически бессимптомно, из-за чего пациент не сразу обращается к стоматологу. Но для большинства случаев характерно следующее:
- тяжесть в больном зубе;
- болевые реакции в ответ на воздействие раздражителей;
- тянущая боль, которая усиливается при воздействии раздражителей и долго не проходит;
- неприятный запах изо рта из-за ухудшения гигиены;
- наличие глубокой кариозной полости с размягчённым дентином внутри.

При обострении хронической формы наблюдается спонтанное возникновение боли, её усиление ночью и распространение на всю челюсть.
Важно понимать, что нередко фиброзный пульпит выявляет стоматолог при проведении осмотра. Так происходит в том случае, когда кариозные полости «спрятаны»: к примеру, расположены под десной. В таких местах они недоступны раздражителям, поэтому пациент не ощущает сильных болей, которые заставили бы его обратиться за профессиональной помощью. Необходимо учитывать ещё один момент: если кариозная полость объединена с полостью зуба, больной не ощущает такого специфического симптома, как тяжесть в зубе. Более того: он не ощущает дискомфорта вообще, поэтому и за лечение не обращается. И это очень плохо, поскольку отсутствие лечения приведёт к деструкции зубных тканей, поражению надкостницы и развитию флюса, лечение которого нередко предусматривает удаление зуба.
Диагностика
Фиброзный пульпит нужно дифференцировать от следующих заболеваний:
- глубокий кариес;
- острый очаговый пульпит;
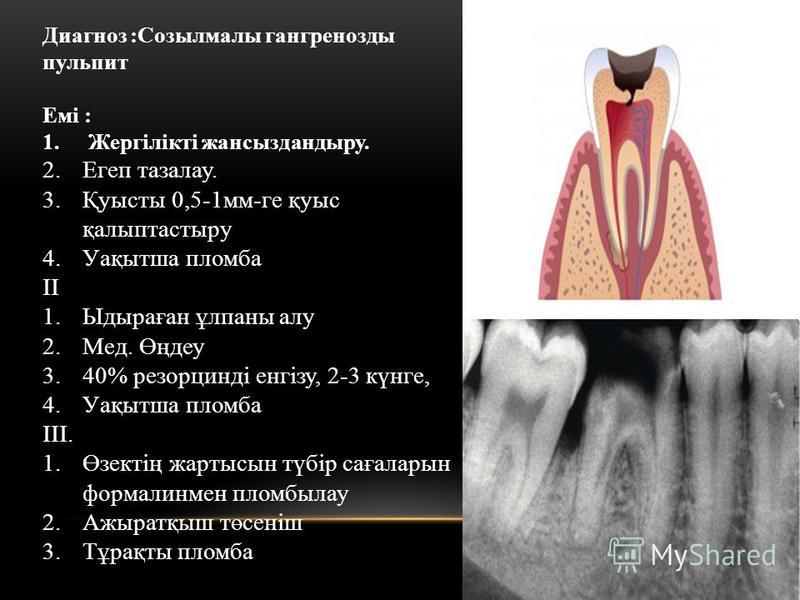
- хронический гангренозный пульпит.

Необходимо понимать, что правильно поставить диагноз может только квалифицированный опытный стоматолог после проведения осмотра и ряда диагностических исследований. Вот лишь некоторые признаки, которые позволяют отличить одно заболевание от другого:
| Симптом | Кариес | Очаговый пульпит | Гангренозный пульпит | Фиброзный пульпит |
|---|---|---|---|---|
| Боль | Недлительные боли при воздействии раздражителей разной природы | Ярко выраженные боли, которые длятся долго даже после устранения раздражителя | Длительная болевая симптоматика ноющего характера от раздражителей разной природы | Боли ноющего характера, которые слабо выражены, умеренные боли при воздействии раздражителей |
| Вид дефекта | Кариозная полость с фрагментами пищи и размягчённым дентином внутри | Большая и глубокая кариозная полость с большим количеством отмершего дентина | Большая и глубокая кариозная полость с большим количеством отмершего дентина | Большая кариозная полость, заполненная разрушенным дентином. |
Для того чтобы правильно поставить диагноз, врач-стоматолог проводит визуальный осмотр ротовой полости, назначает рентгенографию и электроодонтодиагностику. Осмотр позволяет выявить следующее:
- сильную болезненность при зондировании полости зуба;
- кровоточивость пульпы;
- сильную болезненность при перкуссии зуба;
- реакцию на термопробу.
Рентгенографическое исследование позволяет выявить наличие сообщения между кариозной и зубной полостями, а иногда — и расширение периодонтальной щели.
Наши врачи
Муратова Светлана Ивановна
Врач — гигиенист стоматологический
Стаж 12 лет
Записаться на прием
Сёмочкина Ирина Николаевна
Врач стоматолог-терапевт
Стаж 25 лет
Записаться на прием
Губанова Татьяна Васильевна
Врач стоматолог-ортопед
Стаж 33 года
Записаться на прием
Федосеев Михаил Иванович
Врач стоматолог-ортопед
Стаж 29 лет
Записаться на прием
Муратов Вадим Марсельевич
Врач — ортодонт
Стаж 14 лет
Записаться на прием
Могинов Данис Раисович
Врач стоматолог — ортопед
Стаж 19 лет
Записаться на прием
Елизарова Наталия Олеговна
Врач стоматолог-терапевт, заведующая отделением стоматологии
Стаж 42 года
Записаться на прием
Палащенко Татьяна Всеволодовна
Врач стоматолог-терапевт
Стаж 45 лет
Записаться на прием
Авлюкова Алтын Лиджи-Горяевна
Врач-стоматолог детский, врач-стоматолог
Стаж 16 лет
Записаться на прием
Киселева Елена Николаевна
Врач стоматолог-терапевт, врач высшей категории
Стаж 39 лет
Записаться на прием
Большова Оксана Игоревна
Врач стоматолог-ортодонт
Записаться на прием
Антюхин Евгений Борисович
Врач стоматолог-хирург
Стаж 18 лет
Записаться на прием
Туаев Сергей Казбекович
Врач стоматолог-имплантолог
Стаж 33 года
Записаться на прием
Максимец Вера Афанасьевна
Врач стоматолог-терапевт
Стаж 41 год
Записаться на прием
Кузовкова Марина Анатольевна
Врач стоматолог-терапевт, врач первой категории
Стаж 28 лет
Записаться на прием
Юнин Сергей Анатольевич
Врач стоматолог-ортопед, кандидат медицинских наук, врач высшей категории
Стаж 39 лет
Записаться на прием
Отзывы о наших врачах
Огромное спасибо стоматологу Елизаровой Наталье Олеговне за лечение! На первом приеме проведено обследование, сделаны снимки и назначено лечение! Профессионально! Очень деликатно! Замечательная клиника!
Читать весь отзыв
Абранина Людмила
25. 06.2022
06.2022
Проходила лечение в данной клинике, осталась более, чем довольна. Персонал вежлив и обходителен с каждым клиентом. Врач ( Авлюкова Алтан Лиджи-Гириевна) ответила на все возникающие вопросы, сам приём прошёл достаточно быстро и качественно! Однозначно буду пользоваться услугами данной клиники в …
Читать весь отзыв
Минаева Виктория Викторовна
19.06.2022
Лечение фиброзного пульпита
Как уже упоминалось, лечение хронического фиброзного пульпита проводится хирургическими методами. Оно направлено на устранение очага воспаления, предотвращение распространения заболевания и восстановление внешнего вида и функциональности зуба.
Одним из методов лечения хронического фиброзного пульпита является витальная экстирпация, которую проводят под местной анестезией. Процедура состоит из нескольких этапов:
- удаление тканей кариозной полости;
- проведение обработки при помощи антисептических препаратов;
- удаление пульпы сначала из коронковой, а затем — из корневой части зуба;
- пломбирование корневых каналов;
- пломбирование зуба.

Все эти манипуляции требуют одного приёма у стоматолога и считаются щадящими и физиологичными. Но если у пациента наблюдаются аллергические реакции на местные анестетики или непроходимость корневых каналов, требуется девитальная экстирпация. Она проводится в два захода, в первый из которых проводятся вскрытие пульпы и наложение на неё специальной пасты с последующей установкой временной пломбы. Мероприятия второго проводятся через 1–10 дней и заключаются в удалении отмершей пульпы, пломбировании каналов и зуба. Опытные стоматологи клиники ЦЭЛТ лечат фиброзный пульпит, добиваясь отличных результатов.
Часто задаваемые вопросы
Бывают ли осложнения после лечения фиброзного пульпита? И если да, то какие?
Как и после лечения любого другого заболевания, осложнения после лечения фиброзного пульпита бывают. Как правило, они возникают вследствие непрофессиональных действий врача и заключаются в следующем:
- Некачественное пломбирование зубных каналов, при которых в незапломбированных пустотах развиваются воспалительные процессы;
- Травмирование тканей периодонта при проведении обработки канала или извлечении нерва.
 Пациент будет испытывать болевую симптоматику, усиливающуюся при нажатии на зуб;
Пациент будет испытывать болевую симптоматику, усиливающуюся при нажатии на зуб; - Выведение материала для пломбирования за пределы зубного корня и его проникновение в гайморову пазуху при лечении верхней челюсти или в нижнечелюстной канал. В первом случае развивается гайморит, который сопровождается сильными болями, во втором — происходит воспаление периферических нервов.
Есть ли рекомендации, которые облегчат и ускорят восстановление после лечения пульпита?
Такие рекомендации существуют, стоматолог даст их Вам после завершения лечения. Они заключаются в следующем:
- запрет на приём пищи и полоскание рта в течение первых нескольких часов после стоматологических процедур;
- правильная и регулярная гигиена ротовой полости;
- аккуратное пережёвывание пищи и отказ от жёсткой пищи.
Каковы прогнозы на лечение фиброзного пульпита?
При своевременном обращении за профессиональной стоматологической помощью прогноз благоприятный. Пациент избавится от болей и ощущения дискомфорта в зубе. Эстетичность и функциональность зуба будут восстановлены. При несвоевременном обращении, когда процессы зашли слишком далеко и пульпит привёл к некрозу пульпу, — прогноз неблагоприятный, возможно развитие периодонтита.
Пациент избавится от болей и ощущения дискомфорта в зубе. Эстетичность и функциональность зуба будут восстановлены. При несвоевременном обращении, когда процессы зашли слишком далеко и пульпит привёл к некрозу пульпу, — прогноз неблагоприятный, возможно развитие периодонтита.
На вопросы отвечает:
Максимец Вера Афанасьевна
Врач стоматолог-терапевт
Стаж 41 год
Задать вопрос врачу
6. Патогенез хронического воспаления пульпы.
Независимо от этиологического фактора воспалительный процесс в пульпе, как и в других органах и тканях, имеет три компонента:
-альтерацию — первичное повреждение и изменение тканей,
-экссудацию — нарушение кровообращения, особенно в микроцир-куляторном русле,
-пролиферацию — размножение клеточных элементов.
Однако воспалительная реакция пульпы имеет свои особенности, связанные с анатомогистологическим ее строением. Так, в коронковой пульпе больше выражены явления экссудации, а в корневой — пролиферативные процессы. Указанные различия зависят от особеностей строения соединительной ткани коронковой и корневой части пульпы и, возможно, особенностей капиллярного кровообращения коронковой пульпы.
Указанные различия зависят от особеностей строения соединительной ткани коронковой и корневой части пульпы и, возможно, особенностей капиллярного кровообращения коронковой пульпы.
Хронический пульпит может возникнуть самостоятельно, минуя острую форму. Это зависит от вирулентности инфекционного начала, компенсаторно-приспособительных механизмов пульпы, общего иммунного статуса и др.
Наиболее доброкачественным исходом острой воспалительной Реакции пульпы является хронический фиброзный пульпит. Для него характерны активные процессы склероза, в результате Которых пульпа подвергается фиброзу, гиалинозу. Частично эта форма воспаления возникает, когда экссудат получает отток. Количество клеточных элементов в такой ткани падает.
Хронический гипертрофический пульпит характеризуется образованием богатой сосудами капиллярного типа грануляционной ткани, замещающей тканевые структуры пульпы. Продуктивное воспаление со временем может привести к развитию в пульпе склеротического процесса. Если доминирующим остается образование грануляционной ткани, то развивается пролиферативная гипертрофическая форма хронического пульпита, иногда с образованием выступающего из полости зуба полипа.
Если доминирующим остается образование грануляционной ткани, то развивается пролиферативная гипертрофическая форма хронического пульпита, иногда с образованием выступающего из полости зуба полипа.
Хронический гангренозный пульпит может развиваться из острого гнойного пульпита при наличии ряда факторов: снижении общей реактивности организма, истощении защитно-приспособи- тельных механизмов пульпы зуба и преобладании в микрофлоре анаэробных микроорганизмов.
7. Патологическая анатомия острых форм пульпита.
Гиперемия пульпы: воспалительная гиперемия пульпы представляет собой ограниченный участок с резко расширенной капиллярной сетью, инъекцией сосудов, переполнением их кровью. Наблюдаются краевое стояние лейкоцитов, эмиграция с диапедезом отдельных лейкоцитов
Ограниченный пульпит: определяется расширение сосудов, последние переполнены кровью. Целостность стенок сосудов чаще сохранена. Лишь в отдельных участках иногда выявляются мелкие надрывы и кровоизлияние в ткань пульпы, которая пропитана серозным экссудатом. Местами в ней есть отдельные скопления лейкоцитов. С повышением проницаемости сосудистой стенки увеличивается воспалительный инфильтрат. Слой одонтобластов остается морфологически неизмененным
Местами в ней есть отдельные скопления лейкоцитов. С повышением проницаемости сосудистой стенки увеличивается воспалительный инфильтрат. Слой одонтобластов остается морфологически неизмененным
Диффузный пульпит: пропитывания (отека) ткани пульпы серозным экссудатом, расширения кровеносных сосудов и переполнения их эритроцитами наблюдаются как в коронковой, так и в корневой пульпе. Отмечается краевое стояние лейкоцитов, их эмиграция, вследствие чего вокруг сосудов возникает инфильтрат (участки скопления лейкоцитов). Местами сосуды повреждены, видны их разрывы с выходом элементов крови.
Острый гнойный пульпит: значительное скопление экссудата, на некоторых участках наблюдается накопление лейкоцитов и образование абсцессов. Сосуды резко расширены на всем протяжении, стаз в капиллярах. В центральной части органического поражения пульпы образуется гнойник с поясом коллатерального воспаления вокруг него в виде переполненных кровью капилляров и эмиграции лейкоцитов. В динамике наблюдения прослеживается прогрессирование процесса, наступает картина диффузного гнойного воспаления ткани пульпы. Развитие процесса сопровождается расплавлением ткани в участках образования множественных мелких абсцессов, в центре которых находится скопление микроорганизмов. Слой одонтобластов в области абсцесса дистрофически изменен или полностью расплавлен.
Развитие процесса сопровождается расплавлением ткани в участках образования множественных мелких абсцессов, в центре которых находится скопление микроорганизмов. Слой одонтобластов в области абсцесса дистрофически изменен или полностью расплавлен.
Травматический пульпит:
Обычно патологоанатомические отклонения не наступают, лишь при остром течении кариеса наблюдаются признаки реактивных изменений, которые проявляются расширением сосудов и переполнением их кровью в прилежащих к перфорационному отверстию участках пульпы.
8. Патологическая анатомия хронических форм пульпита.
Хронический гипертрофический пульпит — характеризуется образованием богатой сосудами капиллярного типа грануляционной ткани, замещающей тканевые структуры пульпы;
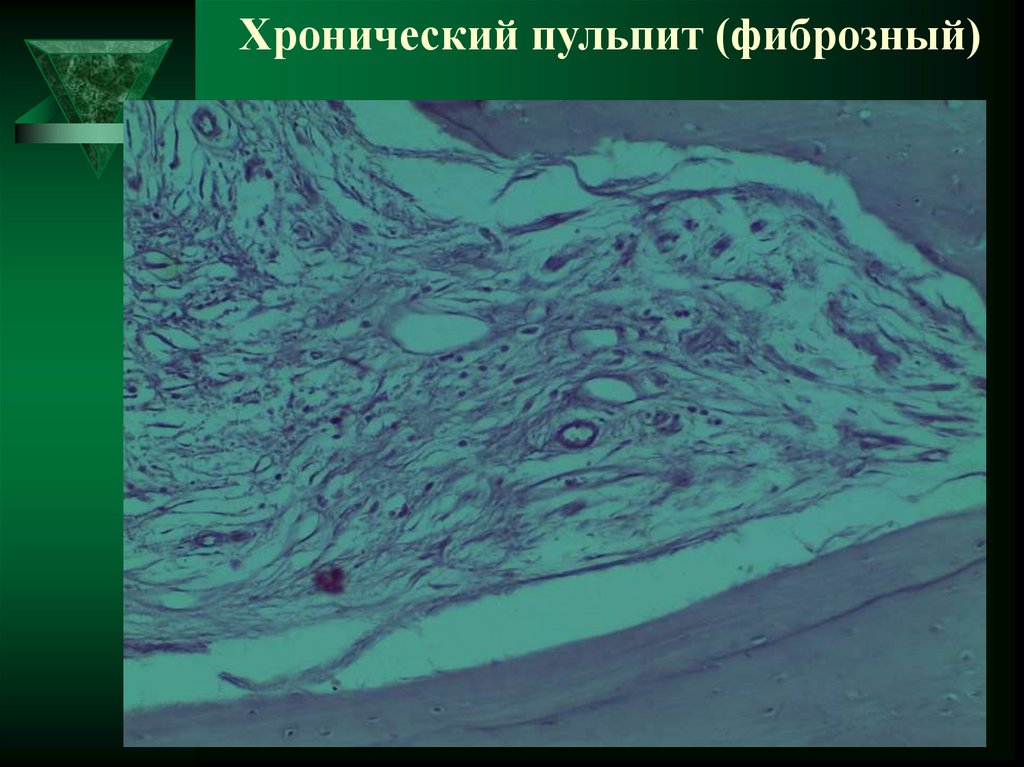
Хронический фиброзный пульпит — пульпа состоит из соединительнотканных волоконец, тонкостенных капилляров, среди которых находится большое количество клеточных элементов (фибробласты, гистиоциты, лейкоциты, эпителиоидные клетки). При длительном течении происходит созревание грануляционной ткани, поверхность ее покрывается эпителием, образуется полип пульпы;
При длительном течении происходит созревание грануляционной ткани, поверхность ее покрывается эпителием, образуется полип пульпы;
Хронический гангренозный пульпит — скопление бесструктурных масс с зернистым их распадом, в которых можно наблюдать массу бактерий, кристаллы жирных кислот, кровяной пигмент. На границе гангренозного распада и сохранившейся пульпы возникает демаркационный вал с признаками серозного воспаления и разрастанием молодой грануляционной ткани.
9. Клиника, дифференциальная диагностика острого очагового пульпита.
Жалобы от всех видов раздражителей, чаще от холодного. Не проходит после устранения причины. Самопроизвольные боли вечером. Иррадиация боли отсутствует. Пациент указывает конкретный зуб. Объективно: глубокая кариозная полость. Дно и стенки плотные. Зондирование болезненно в одной точке. Полость зуба не вскрыта (исключительно при препарировании вскрывает воспалительный очаг врач). Холодовые тесты положительны. Перкуссия безболезненна. ЭОД 18-20 МкА. Дифференциальная диагностика с глубоким кариесом, острым диффузным пульпитом, хроническим фиброзным пульпитом, паппилитом.
Дифференциальная диагностика с глубоким кариесом, острым диффузным пульпитом, хроническим фиброзным пульпитом, паппилитом.
Диагностика заболевания:
-лучевая диагностика (ОПТГ, прицельная рентгенография, МРТ),
-сбор клинического анализа (системное заболевание),
-стоматологический анамнез (характер боли, продолжительность…)
-обследование и тестирование (ЭОД, холодовые тесты, оценка состояния слизистой…)
Лечение хронического пульпита, лечение в стоматологии Москвы, стоимость лечения пульпита зубов, профилактика и симптомы, характерные признаки и причины возникновения, стоматологическая клиника
Сохраняем прежние цены! Забронировать цену
Москва, ул. Большая Спасская, 10к1
Комсомольская Сухаревская Проспект Мира
+7 (495) 125-25-20
Время работы: понедельник — суббота с 10:00 до 21:00
- Клиника
-
- Услуги
- Имплантация
- Ортодонт
- Цены
- Врачи
- % АКЦИЯ %
- Наши работы
- Видео
- Контакты
- org/» typeof=»BreadcrumbList»>
- •
- FAQ (Часто задаваемые вопросы)
- •
- Болезни зубов
По данным статистики, каждый пятый пациент стоматолога страдает пульпитом – воспалением пульпы (пучка кровеносных сосудов и нервных окончаний, который заполняет канал и расположенную в коронковой части зуба пульпарную камеру).
Осложнения этого заболевания очень серьёзны: при отсутствии надлежащего лечения может возникнуть периодонтит. Положение осложняется тем, что хроническая форма болезни имеет гораздо менее выраженные симптомы, чем острая, а часто протекает вообще бессимптомно. Только диагностика помогает выявить заболевание на начальных стадиях.
В московской стоматологической клинике «ДентаЛюкс-М» применяются новейшие методы диагностики и лечения всех форм хронического пульпита.
КЛАССИФИКАЦИЯ И СИМПТОМЫ ЗАБОЛЕВАНИЯ
При хроническом пульпите боли гораздо слабее, чем при остром, а могут и вообще отсутствовать. Если они всё же есть, то носят ноющий характер. Выделяют несколько разновидностей этого заболевания:
- Хронический фиброзный пульпит – наиболее часто встречающаяся форма. Поражённый зуб реагирует на термические, химические и механические раздражители (особенно на холодную пищу). Причём при контакте с раздражителем боль появляется не сразу, а если раздражитель убрать, она длится ещё некоторое время;
- Хронический гипертрофический пульпит не сопровождается постоянной болью, зато обладает наиболее заметными симптомами. Чаще всего такая форма заболевания поражает моляры, на жевательной поверхности которых имеются глубокие кариозные полости, сообщающиеся с пульпарной камерой. В результате инфицирования пульпы кариозная полость заполняется полипом (разросшейся грануляционной тканью). Боли пациент не ощущает до тех пор, пока полип не соприкоснётся с твёрдой или горячей пищей: в этом случае он начинает не только болеть, но и кровоточить;
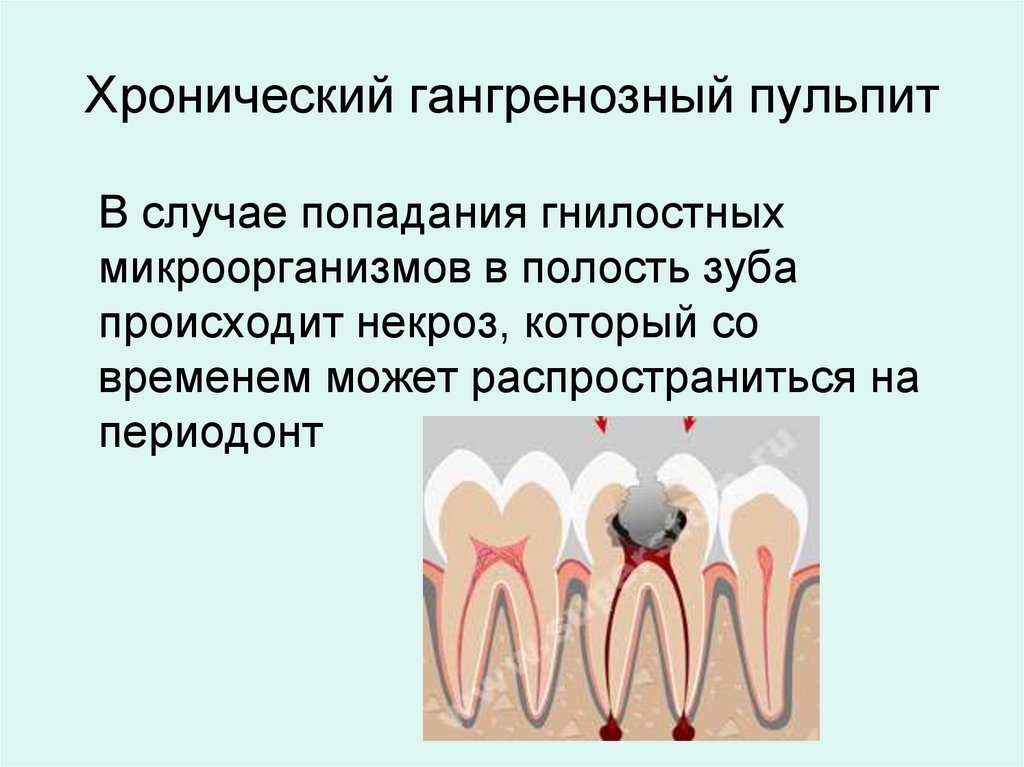
- Хронический гангренозный пульпит в первую очередь характеризуется неприятным запахом изо рта.
 Эту форму заболевания также называют язвенно-некротической, потому что она вызывает омертвение и разложение пульпы поражённого зуба. Боль и кровоточивость могут возникнуть при соприкосновении с горячей пищей.
Эту форму заболевания также называют язвенно-некротической, потому что она вызывает омертвение и разложение пульпы поражённого зуба. Боль и кровоточивость могут возникнуть при соприкосновении с горячей пищей.
СИМПТОМЫ ОБОСТРЕНИЯ ХРОНИЧЕСКОГО ПУЛЬПИТА
Обострение хронического пульпита, когда боль усиливается, можно принять за острую форму болезни. Обостряются чаще всего две формы заболевания: фиброзная и гангренозная. Обострение хронического пульпита может наступить из-за переохлаждения, инфекционного заболевания, снижающего иммунитет, контакта поражённого зуба с горячей, холодной, твёрдой пищей.
Характерный признак обострения – периодические сильные пульсирующие боли, которые начинаются внезапно. Но даже в короткие периоды, когда резких болей нет, часто возникают болевые ощущения, свойственные конкретной форме болезни, причём такое состояние может быть спровоцировано обычным контактом поражённого зуба с пищей.
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ ХРОНИЧЕСКОГО ПУЛЬПИТА
Существует несколько причин возникновения данного заболевания:
- К воспалению пульпы чаще всего приводит кариес.
 Если кариозная полость глубока, то перегородка между её дном и пульпарной камерой постепенно становится всё тоньше, и болезнетворные микроорганизмы получают доступ к пульпе;
Если кариозная полость глубока, то перегородка между её дном и пульпарной камерой постепенно становится всё тоньше, и болезнетворные микроорганизмы получают доступ к пульпе; - Механическое повреждение зуба;
- Истирание коронковой части зуба;
- Если иммунитет ослаблен инфекционным заболеванием, воспаление может развиться снизу, сперва поразив каналы, а затем уже – пульпарную камеру. Такой вид пульпита называют ретроградным.
ДИАГНОСТИКА ХРОНИЧЕСКОГО ПУЛЬПИТА
Для того, чтобы правильно поставить диагноз, стоматолог:
- Задаёт пациенту вопросы о характере и длительности болей;
- Осматривает полость рта. При этом могут проводиться зондирование, перкуссия (постукивание по зубу), накусывание на зуб;
- Делает рентген.
При различных формах пульпита возможны следующие результаты осмотра:
- При фиброзной форме – перкуссия и накусывание на зуб безболезненны. При вскрытии рога пульпы она болит и кровоточит;
- При гипертрофической форме виден полип, в результате зондирования он начинает кровоточить;
- При гангренозной форме зондирование может быть безболезненным, но на рентгеновском снимке видны изменения в верхушечной области корня.

Фото, на которых показаны последствия различных форм хронического пульпита, размещены на нашем сайте.
Очень важно отличать хронический пульпит от других заболеваний, имеющих схожие симптомы:
- При глубоком кариесе боль, вызванная раздражителем, проходит сразу по окончании контакта, а при воспалении пульпы пациент испытывает её ещё в течение 10 – 15 минут.
- Боли при обострении хронического пульпита и невралгии тройничного нерва весьма схожи. Разница состоит в том, что при невралгии ночью они ослабевают, при воспалении пульпы – усиливаются.
- При обострении хронического периодонтита любое прикосновение к зубу (перкуссия, накусывание) очень болезненно, при воспалении пульпы болевые ощущения отсутствуют.
МЕТОДЫ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПУЛЬПИТА
Лечение хронического пульпита можно проводить двумя способами:
- Консервативным – такое лечение возможно только на самых ранних стадиях заболевания. При использовании данного метода стоматологу удаётся сохранить большую часть пульпы.
 Из-за того, что большинство пациентов обращается к врачу на поздних стадиях, этот консервативный способ применяется очень редко;
Из-за того, что большинство пациентов обращается к врачу на поздних стадиях, этот консервативный способ применяется очень редко; - Хирургическим, при котором производится удаление пульпы. Такое лечение состоит из нескольких этапов. Методика хирургического лечения зависит от формы заболевания.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ХРОНИЧЕСКОГО ПУЛЬПИТА
В зависимости от формы заболевания выбирают алгоритм хирургического лечения:
- При фиброзной форме пациенту под местной анестезией тщательно очищают кариозную полость и удаляют перегородку между кариозной полостью и пульпарной камерой. Затем производят резекцию коронкового участка пульпы. Из предварительно расширенных каналов корня удаляют оставшуюся часть воспалённой пульпы. После обработки зуба противовоспалительными средствами устанавливают временную пломбу, которую затем меняют на постоянную;
- Методика лечения гипертрофического хронического пульпита похожа на методику лечения фиброзного. Большое внимание уделяется чистке и пломбированию каналов.
 Поскольку предстоит удаление значительной части или даже всей пульпы из зуба, иногда такую операцию проводят не под местным, а под общим наркозом;
Поскольку предстоит удаление значительной части или даже всей пульпы из зуба, иногда такую операцию проводят не под местным, а под общим наркозом; - Сложнее всего лечить гангренозную форму заболевания. После обезболивания из коронковой части зуба и каналов корня полностью удаляется пульпа. Чтобы нерв не кровоточил, его прижигают с помощью электрокоагуляции. Затем просушивают полость, накладывают антисептическую повязку и пломбируют каналы.
СТОИМОСТЬ ЛЕЧЕНИЯ ПУЛЬПИТА В МОСКВЕ
Цена лечения зависит от сложности (и степени запущенности) заболевания, а также от того, какой зуб поражён: однокорневой, двух- или трёхкорневой. Для своевременной диагностики хронического пульпита нужно посещать стоматолога не реже двух раз в год. Если у вас разболелся зуб, помните: обезболивающие средства лишь на время купируют боль, но не лечат. В этом случае, если вы хотите сберечь зубы, визит к стоматологу просто необходим.
В московской клинике «ДентаЛюкс-М» лечением хронического пульпита занимаются опытные специалисты, использующие современную технику и новейшие разработки в области стоматологии.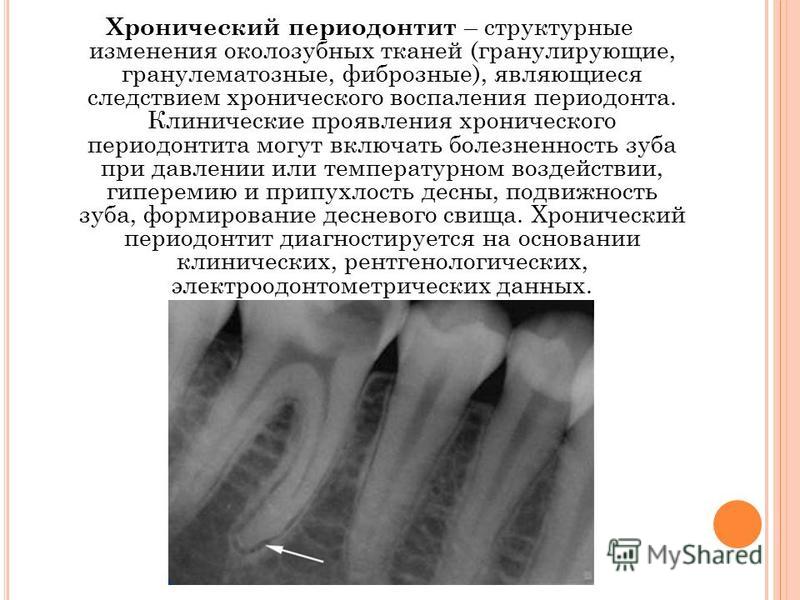 Стоимость лечения доступна самому широкому кругу потребителей. Если вы хотите, чтобы лечение хронического пульпита обошлось вам недорого, запишитесь на приём в стоматологическую клинику «ДентаЛюкс-М».
Стоимость лечения доступна самому широкому кругу потребителей. Если вы хотите, чтобы лечение хронического пульпита обошлось вам недорого, запишитесь на приём в стоматологическую клинику «ДентаЛюкс-М».
Услуги стоматологии
О нашей клинике на других площадках
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Введите ваше имя*
Дата посещения клинники ЯнварьФевральМартАпрельМайИюньИюльАвгустСентябрьОктябрьНоябрьДекабрь20192018201720162015
Ваша оценка ОтличноХорошоНормальноПлохоОчень плохо
Введите ваш отзыв*
Написать в WhatsAppЭтиология и патогенез пульпита.
 Классификация. Патологическая анатомия пульпита. Клиника. Диагностика
Классификация. Патологическая анатомия пульпита. Клиника. Диагностика Слайд 1
Описание слайда:
Этиология и патогенез пульпита. Классификация. Патологическая анатомия пульпита. Клиника. Диагностика, дифференциальная диагностика острых, хронических и обострившихся форм пульпита. Травматический, ретроградный, конкрементозный пульпит
Слайд 2
Описание слайда:
Причины возникновения пульпита Инфекция Механическая травма пульпы Химическая травма пульпы Образование дентиклей Предрасполагающие факторы: Снижение сопротивляемости пульпы зуба и в целом организма Сенсибилизация пульпы микроорганизмами и их токсинами
Слайд 3
Описание слайда:
Слайд 4
Описание слайда:
Патогенез воспаления пульпы Повреждение клеток пульпы и межклеточного вещества, волокон сосудов Нарушение проницаемости сосудов и стаз Пульпа полнокровна, отечна, накапливается серозная жидкость Через 6-8 часов серозный характер воспаления переходит в гнойный В коронковой пульпе из сосудов интенсивно мигрируют лейкоциты Наступает гипоксия Нарушаются обменные процессы в пульпе Усиливается анаэробный гликолиз Фагоцитарная активность клеток вследствие ацидоза угнетается, наблюдается распад пульпы
Слайд 5
Описание слайда:
Классификация пульпита Е.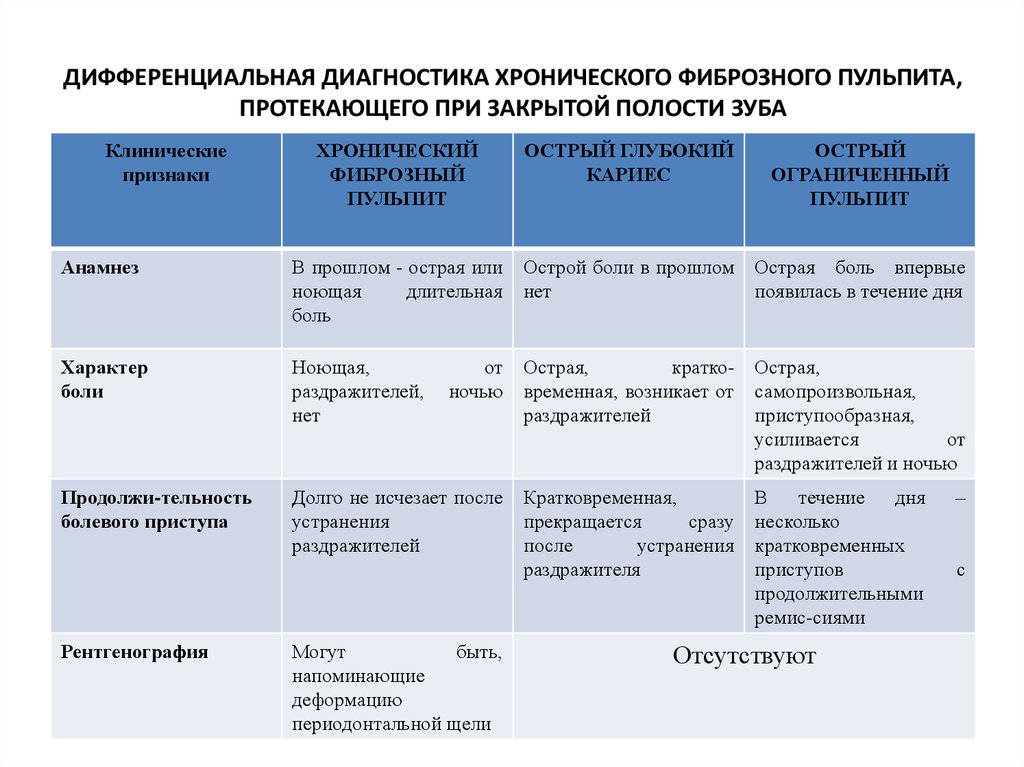 М.Гофунга (1927)
ОСТРЫЙ пульпит:
частичный
общий
общий гнойный
ХРОНИЧЕСКИЙ пульпит:
простой
гипертрофический
гангренозный
М.Гофунга (1927)
ОСТРЫЙ пульпит:
частичный
общий
общий гнойный
ХРОНИЧЕСКИЙ пульпит:
простой
гипертрофический
гангренозный
Слайд 6
Описание слайда:
Классификация пульпита Е.Е.Платонова (1968) ОСТРЫЙ пульпит: очаговый диффузный ХРОНИЧЕСКИЙ пульпит: фиброзный гипертрофический гангренозный ОБОСТРЕНИЕ ХРОНИЧЕСКОГО пульпита
Слайд 7
Описание слайда:
Иванов В.С. (1984) ОСТРЫЙ ПУЛЬПИТ Серозно-гнойный очаговый Гнойный диффузный ХРОНИЧЕСКИЙ ПУЛЬПИТ Простой (фиброзный) Пролиферативный Гангренозный ОБОСТРЕНИЕ ХРОНИЧЕСКОГО ПУЛЬПИТА
Слайд 8
Описание слайда:
Классификация пульпита кафедры терапевтической стоматологии ОСТРЫЙ пульпит – частичный, общий, общий гнойный ХРОНИЧЕСКИЙ пульпит – простой, гипертрофический, гангренозный ОБОСТРЕНИЕ ХРОНИЧЕСКОГО ПУЛЬПИТА ТРАВМАТИЧЕСКИЙ пульпит РЕТРОГРАДНЫЙ пульпит КОНКРЕМЕНТОЗНЫЙ пульпит
Слайд 9
Описание слайда:
Гистологическое строение пульпо-дентинного комплекса D — дентин, PD — предентин, OB — одонтобласты, CF (cell free zone) — бесклеточная зона, CR (cell rich zone) — зона богатая клетками
Слайд 10
Описание слайда:
Участок пульпы с лимфоидной инфильтрацией и полнокровием кровеносных сосудов Ораска гемотоксилин-эозин
Слайд 11
Описание слайда:
Хроническое воспаление пульпы: Нейтрофильная инфильтрация, полнокровие кровеносных сосудов, разрастание соединительной ткани
Слайд 12
Описание слайда:
Для острых форм пульпита характерны симптомы: «Самопроизвольная» боль, возникающая без воздействия внешних раздражителей Действие температурных, механических, химических раздражителей вызывает приступ длительной болевой реакции Усиление боли ночью Приступообразный характер боли с безболезненным промежутком
Слайд 13
Описание слайда:
острый частичный пульпит
Жалобы на боль от всех видов раздражителей и самопроизвольную, частота приступов боли от нескольких секунд до нескольких минут. В ночное время боль более интенсивная
При осмотре внешних изменений нет
Кариозная полость не сообщается с полостью зуба
Зондирование болезненно у рога пульпы, перкуссия безболезненна
Электровозбудимость пульпы снижена, но могут выявляться и нормальные показатели
В ночное время боль более интенсивная
При осмотре внешних изменений нет
Кариозная полость не сообщается с полостью зуба
Зондирование болезненно у рога пульпы, перкуссия безболезненна
Электровозбудимость пульпы снижена, но могут выявляться и нормальные показатели
Слайд 14
Описание слайда:
Дифференциальная диагностика: глубокий кариес острым общий пульпит хронический простой пульпит
Слайд 15
Описание слайда:
Острый общий пульпит Длительные болевые приступы с небольшими безболезненными промежутками Иногда боль не исчезает, а лишь стихает Характерна упорная ночная боль с иррадиацией в висок, скуловую область в зависимости от расположения больного зуба
Слайд 16
Описание слайда:
Клиника и диагностика Кариозная полость Перкуссия может быть слабо болезненна Зондирование резко болезненно по всему дну Электровозбудимость зуба снижается от 30-40 до 50-60 мкА
Слайд 17
Описание слайда:
Острый общий пульпит дифференцируют от острого частичного пульпита обострившегося хронического пульпита острого верхушечного периодонтита невралгии тройничного нерва гайморита альвеолита
Слайд 18
Описание слайда:
острый гнойный пульпит Рвущая, пульсирующая, почти непрерывная боль Интенсивность снижается от холодной воды Боль иррадиирует по ходу ветвей тройничного нерва При осмотре кариозная полость с невскрытой полостью зуба Перкуссия болезненна Электровозбудимость 50-60 мкА
Слайд 19
Описание слайда:
Общая симптоматика хронических форм пульпита Продолжительность (в течение нескольких лет) заболевания Слабо выраженные субъективные признаки Сильно разрушенные зубы Для всех форм хронического пульпита характерно наличие длительной боли от раздражителей Отсутствие рентгенологических изменений в периодонте
Слайд 20
Описание слайда:
хронический простой пульпит Приступообразная боль от всех видов раздражителей Зондирование дна обнаруживает болезненный вскрытый рог пульпы Электровозбудимость пульпы снижена до50-60 мкА
Слайд 21
Описание слайда:
Дифференциальная диагностика Глубокий кариес Острый частичный пульпит Хронический гангренозный пульпит
Слайд 22
Описание слайда:
хронический гангренозный пульпит Жалобы на ноющую боль от различного рода раздражителей, не прекращаю-щаяся после удаления раздражителя Иногда боль при перемене температуры воздуха При осмотре – глубокая кариозная полость с широко открытой полостью зуба Глубокое зондирование болезненно Электровозбудимость снижена до 80 мкА
Слайд 23
Описание слайда:
Дифференциальная диагностика Хронический простой пульпит Хронический верхушечный периодонтит
Слайд 24
Описание слайда:
Хронический гипертрофический пульпит Жалобы на ноющую боль в зубе от всех видов раздражителей Боль сохраняется после устранения раздражителя Разрастание пульпы легко кровоточит («дикое мясо»)
Слайд 25
Описание слайда:
Дифференциальная диагностика При локализации кариозной полости по 2 классу с разрастаниями десневого сосочка Разрастанием периодонта из бифуркации
Слайд 26
Описание слайда:
Обострение хронического пульпита Клиническая картина схожа с симптомами острых форм пульпита: Самопроизвольная, приступообразная, иррадиирующая боль Кариозная полость с всрытой пульповой камерой Электровозбудимость пульпы ниже 60 мкА
Слайд 27
Описание слайда:
Травматический пульпит
Слайд 28
Описание слайда:
Травматический пульпит верхнего центрального резца Пульповая камера вскрыта и оказалась в линии перелома
Слайд 29
Описание слайда:
Конкрементозный пульпит возникает на фоне отложения конкрементов в пульпе зуба Больные не могут указать причинный зуб В отличие от невралгии тройничного нерва приступ боли не возникает молниеносно, а развивается исподволь, постепенно Боль нарастает по интенсивности и длительности Через несколько дней (реже), недель или (чаще) месяцев достигает кульминации
Слайд 30
Описание слайда:
Обызвествленные структуры (кальцификаты) пульпы зуба: Диффузные — петрификация (конкрементоз) Локальные: а) дентикли- свободные пристеночные замурованные (интерстициальные) истинные (высокоорганизованные) ложные (низкоорганизованные) б) петрификаты Облитерация полости зуба и корневых каналов
Слайд 31
Описание слайда:
Возможные этиологические факторы возникновения кальцификатов пульпы: Наследственные нарушения формирования зубных Заболевания зубов и окружающих зуб тканей – Химические и физические раздражающие факторы — жевательные перегрузки (травматическая окклюзия) Травматические факторы Общие метаболические нарушения — системная терапия глюкокортикостероидами, гипервитаминоз D, тиреотоксикоз Возрастные изменения
Слайд 32
Описание слайда:
Патогенетические механизмы образования кальцификатов пульпы Постоянное дентинообразование, связанное с возрастом, или в ответ на воздействие раздражителя Выпадение кристаллов из пересыщенного раствора по аналогии с процессами патологического минерало-образования в организме Минерализация, возникающая на локально измененной органической матрице в результате воспалительных или дистрофических процессов в пульпе Трансформация малодифференцированных клеток в одонтобласты Солевая дистрофия ткани пульпы при общих обменных нарушениях в организме Возрастные дистрофические изменения ткани пульпы
Слайд 33
Описание слайда:
Диагностика На рентгенограмме на фоне полости зуба или корневого канала дентикли определяются в виде округлых, удлиненных или неправильной формы затенений, иногда их несколько Петрификаты, за исключением крупных, вследствие их меньшей обызвествленности и плотности практически не распознаются на рентгенограммах
Слайд 34
Описание слайда:
Ретроградный пульпит – воспаление происходит при отсутствии кариозной полости в зубе Причина возникновения – пародонтальный карман, ослабление реактивности организма, септическое состояние, острый лейкоз
Слайд 35
Описание слайда:
Вопросы обратной связи Как называется воспаление пульпы? Какие острые формы различают по классификации Гофунга Какие хронические формы пульпита различают по классификации Платонова? В каком году Гофунг предложил классификацию пульпита? Как называется пульпит, этиологическим фактором которого являются дентикли пульпы? Причина ретроградного пульпита
Пульпит | это.
 .. Что такое Пульпит?
.. Что такое Пульпит? Не следует путать с Бульбит
Пульпит — воспаление сосудисто-нервного пучка зуба (пульпы).
|
Содержание
|
Этиология
Наиболее часто пульпит является следствием неправильных действий врача (препарирование зуба под ортопедические конструкции, некачественные пломбы, оперативные вмешательства на пародонте, воздействие химических веществ), а также является осложнением кариеса, также описаны случаи ремитроградного пульпита (то есть инфицирование через апикальное отверстие).
Классификация
Острый пульпит
- гиперемия пульпы
- серозный ограниченный
- серозный диффузный
- гнойный
- травматический
Хронический пульпит
- фиброзный
- гангренозный
- гипертрофический (пролиферативный)
Обострение хронического пульпита
Конкрементозный пульпит
Пульпит осложнённый фокальным периодонтитом
Патогенез
Пульпиты подразделяются на острые и хронические. Под острым пульпитом понимают состояние, когда инфекция проникла в пульпу при закрытой пульпарной камере (через тонкую стенку разрушенного кариесом зуба). Острый пульпит вначале носит очаговый характер и протекает как серозное воспаление (серозный пульпит), затем появляется гнойный экссудат (гнойный пульпит). При этом появляются очень сильные боли вследствие накопления гнойного экссудата в закрытой пульпарной камере.
Хронические пульпиты чаще всего являются исходом острого.
Хронические пульпиты подразделяются на фиброзные, гипертрофические и гангренозные. Основная форма хронического пульпита это фиброзный пульпит, при котором происходит разрастание волокнистой соединительной ткани. При гипертрофическом пульпите происходит гипертрофическое разрастание пульпарной ткани через открытую кариозную полость. При гангренозном пульпите в коронковой пульпе обнаруживается распад ткани. В корневой пульпе обнаруживается грануляционная ткань.
Клиника
Острый пульпит
Острый очаговый и диффузный пульпит
Основные признаки острого пульпита это очень сильные, иррадиирующие (распространяющиеся) по ветвям тройничного нерва (при остром очаговом пульпите иррадиации нет, пациент четко может указать болезненный зуб) боли, которые усиливаются ночью. Боли носят периодический характер. Причинный зуб очень чувствителен к термическим раздражителям, причем боль усиливается и продолжается после удаления раздражителя (в отличие от кариеса). Перкуссия (постукивание) зуба нечувствительна или малочувствительна (в отличие от периодонтита).
Хронический пульпит
Хронический фиброзный пульпит
Это наиболее часто встречающиеся форма пульпита, которая является исходом острого пульпита.
Жалобы на боли от температурных и химических раздражителей, которые не проходят сразу после устранения причины, но чаще пациент жалоб не предъявляет, самопроизвольные боли отсутствует, и возникают лишь при обострении хронического процесса. При осмотре глубокая кариозная полость, полость зуба вскрыта в одной точке, зондирование резко болезненно. Если больной зуб находится под пломбой, то после удаления пломбы обнаруживается болезненное сообщение с полостью зуба. Перкуссия зуба безболезненная, но иногда сравнительная перкуссия помогает определить больной зуб.
Переходная складка без изменении. ЭОД-35мкА. Хронический фиброзный пульпит необходимо дифференцировать с глубоким кариесом, острым очаговым пульпитом и хроническим гангренозным пульпитом.
Хронический гипертрофический (пролиферативный) пульпит
При гипертрофическом пульпите в кариозной полости обнаруживается гипертрофированный фиброзный полип.
Хронический гангренозный пульпит
Гангренозный пульпит может протекать со значительными болевыми ощущениями, при этом зуб чувствителен к горячему, а холод успокаивает боль.
Обострение хронического пульпита
Лечение
Серозные пульпиты считаются обратимыми при надлежащем лечении (Ca-содержащие лечебные прокладки под пломбы, антибиотиковые повязки и пр.), которое направлено на ощелачивание полости зуба, с последующим образованием вторичного дентина. Показаниями к этому(биологическому) методу лечения являются молодой возраст (до 30 лет), отсутствие хронических заболеваний и достаточная кариес-резистентность (устойчивость тканей зуба к кариозному процессу). Возможно также частичное удаление пульпы (ампутация пульпы), однако, в настоящее время используется редко, в основном в молочных зубах и в зубах с несформированной верхушкой (до двух лет после прорезывания зуба).
При лечении острых гнойных и хронических пульпитов производится механическая и медикаментозная обработка системы корневых каналов (депульпирование — «удаление нерва») и пломбировка (герметичная обтурация) канала. Удаление нерва может проводиться как в одно посещение, так и в два. После анестезии создается сообщение с нервом, и на него накладывают девитализирующую пасту (в народе именуемую «мышьяк»; в действительности же, он уже практически не используется, будучи замененным новым средством — пастой на основе параформальдегида и анестетика; его можно оставлять на неделю, при этом, токсичность его гораздо ниже). Либо же под анестезией удаляется нерв, в канале оставляют лечебное вещество (для антисептики и снятия воспаления) через 3 дня зуб можно пломбировать. За время лечения необходимо сделать как минимум 2 снимка: первый — до начала лечения, для оценки длины и структуры каналов, второй — после, для оценки качества пломбирования каналов. Депульпированный зуб впоследствии нуждается в армировании (фиксация штифта из стекловолокна, титана, серебра, пр.) и/или покрытии коронкой, по показаниям.
Удаление нерва может проводиться как в одно посещение, так и в два. После анестезии создается сообщение с нервом, и на него накладывают девитализирующую пасту (в народе именуемую «мышьяк»; в действительности же, он уже практически не используется, будучи замененным новым средством — пастой на основе параформальдегида и анестетика; его можно оставлять на неделю, при этом, токсичность его гораздо ниже). Либо же под анестезией удаляется нерв, в канале оставляют лечебное вещество (для антисептики и снятия воспаления) через 3 дня зуб можно пломбировать. За время лечения необходимо сделать как минимум 2 снимка: первый — до начала лечения, для оценки длины и структуры каналов, второй — после, для оценки качества пломбирования каналов. Депульпированный зуб впоследствии нуждается в армировании (фиксация штифта из стекловолокна, титана, серебра, пр.) и/или покрытии коронкой, по показаниям.
Этапы витальной экстирпации
- Обезболивание
- Полное препарирование кариозной полости
- Вскрытие полости зуба
- Раскрытие полости зуба
- Ампутация коронковой пульпы
- Расширение устьев корневых каналов
- Экстирпация корневой пульпы
- Остановка кровотечения
- Диатермокоагуляция
- Определение рабочей длины корневого канала
- Механическая и медикаментозная обработка корневого канала
- Высушивание корневого канала
- Пломбирование корневого канала
- Наложение изолирующей прокладки
- Пломбирование зуба
Осложнения
Хронический пульпит без надлежащего лечения, при неадекватной обработке системы корневых каналов, при негерметичной обтурации канала или негерметичности восстановления зуба (пломбы, вкладки, накладки, коронки) может перейти в периодонтит.
Литература
- Терапевтическая стоматология, Е. В. Боровский и соов., Москва., 1998;
- Стоматология, Н. Н. Бажанов, «Медицина», Москва, 1990
Этиология и патогенез пульпита и апикального периодонтита
Глава 3. Этиология и патогенез пульпита и апикального периодонтита
Ашраф Ф. Фуад и Асма А. Хан
3.1 Введение 0 Этиологические факторы 0 патологические процессы, участвующие в развитии пульпита и апикального периодонтита. Источники микробного раздражения пульпы зуба разнообразны и могут исходить из коронарного (наиболее распространенного), латерального или апикального путей. Микробное раздражение пульпы зуба оказывает глубокое воздействие на эту ткань, часто вызывая тяжелые симптомы, но часто приводя к бессимптомной дегенерации ткани. Точно так же апикальный периодонтит может протекать бессимптомно, может быть связан с тяжелыми симптомами и может быть связан с распространяющимися, иногда опасными для жизни инфекциями. Точные причины вариации симптомов среди случаев с кажущимися сходными патологическими изменениями и отсутствия корреляции между симптомами и гистологическим видом пульпы зуба до конца не изучены. Хотя многие нейропептиды и другие медиаторы воспаления, которые связаны с болью, обнаруживаются в больших концентрациях при болезненном пульпите и апикальном периодонтите, неясно, почему в некоторых случаях они увеличиваются. Часто пульпа некротизируется без заметной связи с симптомами.
Точные причины вариации симптомов среди случаев с кажущимися сходными патологическими изменениями и отсутствия корреляции между симптомами и гистологическим видом пульпы зуба до конца не изучены. Хотя многие нейропептиды и другие медиаторы воспаления, которые связаны с болью, обнаруживаются в больших концентрациях при болезненном пульпите и апикальном периодонтите, неясно, почему в некоторых случаях они увеличиваются. Часто пульпа некротизируется без заметной связи с симптомами.
Заболевания пульпы и периапикальных тканей возникают в результате воспаления соответствующих тканей, что в конечном итоге приводит к дегенерации и некрозу пульпы, резорбции периапикальной кости, развитию воспалительного периапикального поражения, возможно кистозному образованию и, возможно, тяжелым инфекциям и/или или остеомиелит. В некоторых ситуациях может возникать резорбция корня различного типа, как непосредственно связанная с травматическим повреждением или ортодонтическим лечением, так и коварно по известным или неизвестным причинам.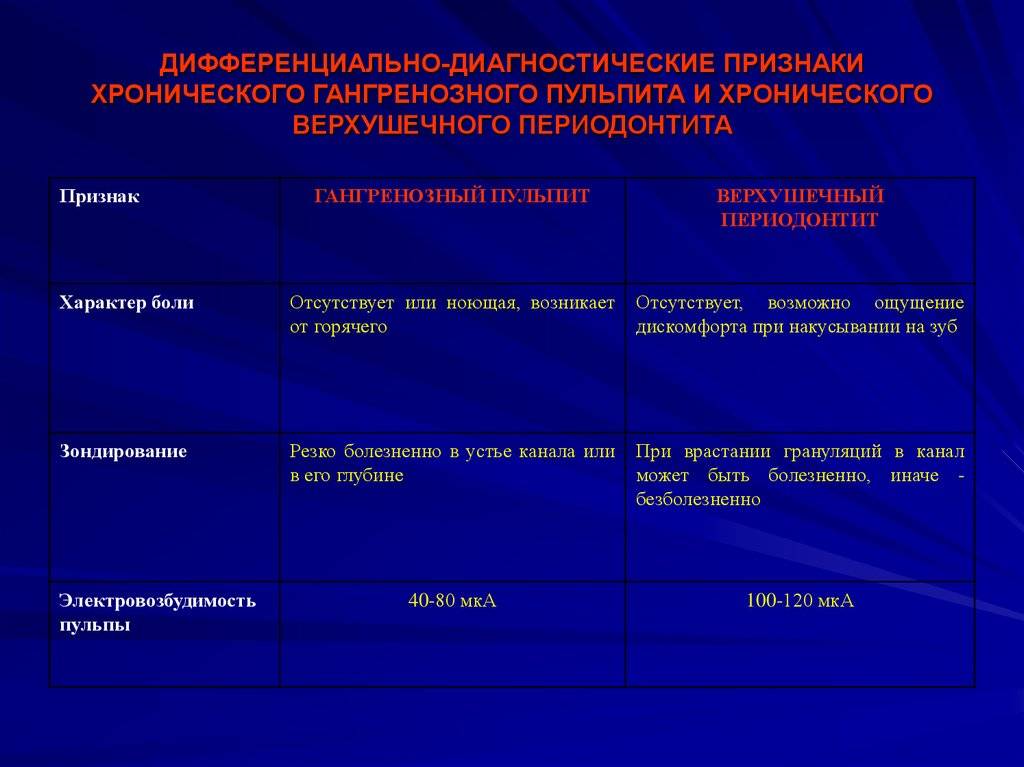 Принято считать, что резорбция корня имеет тот же патогенез, что и резорбция кости, после разрушения цемента, который защищает поверхность корня или предентин внутри. Все эти патологические состояния являются вариантами воспалительных реакций и опосредованы широким спектром цитокинов, хемокинов, нейропептидов, протеаз и других молекул, связанных с воспалением. Развитие неопластических изменений в пульпе не известно даже в ответ на метастатическое поражение костей челюсти. В этих случаях периапикальная кость может резорбироваться, но пульпа обычно сохраняет свою жизнеспособность. Этот факт важен для клинической дифференциации заболевания пульпы от других заболеваний, которые могут имитировать эндодонтический патоз, но не возникают из пульпы зуба. Интересно, почему пульпа кажется невосприимчивой к развитию новообразований, которые, если бы они присутствовали, привели бы к случаям спонтанного некроза пульпы или опухолевого заболевания пульпы.
Принято считать, что резорбция корня имеет тот же патогенез, что и резорбция кости, после разрушения цемента, который защищает поверхность корня или предентин внутри. Все эти патологические состояния являются вариантами воспалительных реакций и опосредованы широким спектром цитокинов, хемокинов, нейропептидов, протеаз и других молекул, связанных с воспалением. Развитие неопластических изменений в пульпе не известно даже в ответ на метастатическое поражение костей челюсти. В этих случаях периапикальная кость может резорбироваться, но пульпа обычно сохраняет свою жизнеспособность. Этот факт важен для клинической дифференциации заболевания пульпы от других заболеваний, которые могут имитировать эндодонтический патоз, но не возникают из пульпы зуба. Интересно, почему пульпа кажется невосприимчивой к развитию новообразований, которые, если бы они присутствовали, привели бы к случаям спонтанного некроза пульпы или опухолевого заболевания пульпы.
Исследования на животных показали, что после контакта пульпы с бактериями полости рта некроз пульпы и развитие апикального периодонтита происходят быстро и обычно происходят в течение нескольких недель на различных моделях млекопитающих. Бактериальная популяция в полости пульпы продолжает развиваться после некроза в зависимости от факторов окружающей среды, состава и питания. Важно отметить, что патогенез заболевания и ответ на лечение могут зависеть от продолжительности микробного раздражения. Длительное микробное раздражение при первичных инфекциях или после неполного лечения влияет на пространственное распределение микробных биопленок и их потенциальное распространение в сложную среду корневого канала, дентинные канальцы и, возможно, периапикальную область. Эффективность эндодонтической дезинфекции в этих местах снижается, и, следовательно, ответ на лечение может быть медленнее и менее стойким, чем в случае удаления зуба.
Бактериальная популяция в полости пульпы продолжает развиваться после некроза в зависимости от факторов окружающей среды, состава и питания. Важно отметить, что патогенез заболевания и ответ на лечение могут зависеть от продолжительности микробного раздражения. Длительное микробное раздражение при первичных инфекциях или после неполного лечения влияет на пространственное распределение микробных биопленок и их потенциальное распространение в сложную среду корневого канала, дентинные канальцы и, возможно, периапикальную область. Эффективность эндодонтической дезинфекции в этих местах снижается, и, следовательно, ответ на лечение может быть медленнее и менее стойким, чем в случае удаления зуба.
3.2 Этиология пульпита и апикального периодонтита
Микробные инфекции из кариозных поражений являются наиболее распространенной этиологией пульпита и апикального периодонтита. В норме коронки прорезавшихся зубов покрыты биопленками, состоящими из симбиотических микробных сообществ. В среде, богатой сахаром, определенные таксоны бактерий из этих сообществ выделяют кислоты, которые деминерализуют дентин, что приводит к образованию кариозных поражений. В то время как Streptococcus mutans долгое время считался единственным возбудителем кариеса, недавние исследования показывают, что кариес вызывается сложной микробиотой [39]., 128, 149]. Кариозные поражения, ограниченные эмалью, вызывают незначительные изменения в пульпе, такие как накопление клеток, экспрессирующих антиген МНС класса II. Как только кариесная биопленка разрушает эмаль и достигает дентина, она вызывает дальнейшие воспалительные изменения в пульпе [90, 91, 177, 232-234].
В среде, богатой сахаром, определенные таксоны бактерий из этих сообществ выделяют кислоты, которые деминерализуют дентин, что приводит к образованию кариозных поражений. В то время как Streptococcus mutans долгое время считался единственным возбудителем кариеса, недавние исследования показывают, что кариес вызывается сложной микробиотой [39]., 128, 149]. Кариозные поражения, ограниченные эмалью, вызывают незначительные изменения в пульпе, такие как накопление клеток, экспрессирующих антиген МНС класса II. Как только кариесная биопленка разрушает эмаль и достигает дентина, она вызывает дальнейшие воспалительные изменения в пульпе [90, 91, 177, 232-234].
Пульпа также может подвергаться прямому воздействию микроорганизмов и их побочных продуктов иными путями, чем кариозные поражения, например, в случаях травматических повреждений, приводящих к сложным переломам зубов, или в ситуациях ятрогенного обнажения пульпы. Роль заболеваний пародонта в возникновении воспаления и некроза пульпы остается спорной [81, 152]. Некоторые исследования предполагают, что заболевание пародонта вызывает приток воспалительных клеток и кальцификацию пульпы [115, 184]. Однако тотальный некроз пульпы отмечался только в тех зубах, где все основные апикальные отверстия были инфицированы бактериальным налетом. В доклиническом исследовании, в котором экспериментально вызывался маргинальный периодонтит, сообщалось о легких патологических изменениях пульпы в 57% зубов с пародонтитом [13]. Некроз пульпы отмечен только в одном зубе из 9.2 зуба в опытной группе. Другие исследования показывают, что заболевания пародонта не вызывают изменений в пульпе [137].
Некоторые исследования предполагают, что заболевание пародонта вызывает приток воспалительных клеток и кальцификацию пульпы [115, 184]. Однако тотальный некроз пульпы отмечался только в тех зубах, где все основные апикальные отверстия были инфицированы бактериальным налетом. В доклиническом исследовании, в котором экспериментально вызывался маргинальный периодонтит, сообщалось о легких патологических изменениях пульпы в 57% зубов с пародонтитом [13]. Некроз пульпы отмечен только в одном зубе из 9.2 зуба в опытной группе. Другие исследования показывают, что заболевания пародонта не вызывают изменений в пульпе [137].
В одном из основополагающих исследований роли бактериальной инфекции в заболеваниях пульпы и периапикальной области сравнивались результаты воздействия на пульпу стерильных и здоровых крыс [98]. У гнотобиотических крыс пульпа оставалась жизнеспособной, а апикальные ткани оставались нормальными в течение периода исследования. В этой группе крыс формирование полных дентинных мостиков отмечено к 28 дню после обнажения пульпы.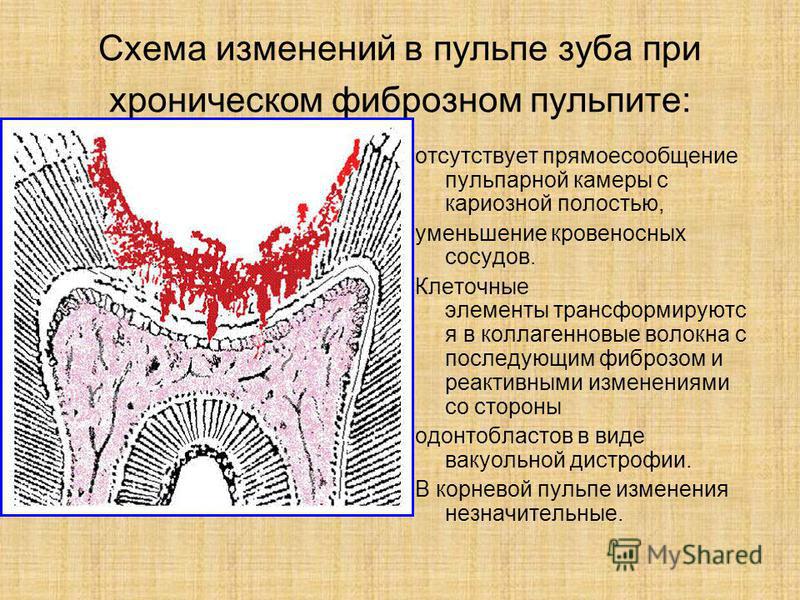 Напротив, у нормальных крыс в начале периода исследования развился некроз пульпы, за которым последовало развитие периапикальных абсцессов и гранулем. Еще одно основополагающее исследование инфекций системы корневых каналов включало изучение связи между различными таксонами. В этом исследовании на приматах системы корневых каналов зубов были инфицированы различными комбинациями видов бактерий. Это было первое исследование, показавшее, что таксоны образуют многовидовые сообщества в периапикальных тканях, которые при объединении вызывают более сильные воспалительные реакции [50]. Эти данные о том, что заболевания пульпы и периапикальных тканей вызываются полимикробными инфекциями, формирующими биопленки, подтверждаются несколькими другими исследованиями [12, 50, 165, 208].
Напротив, у нормальных крыс в начале периода исследования развился некроз пульпы, за которым последовало развитие периапикальных абсцессов и гранулем. Еще одно основополагающее исследование инфекций системы корневых каналов включало изучение связи между различными таксонами. В этом исследовании на приматах системы корневых каналов зубов были инфицированы различными комбинациями видов бактерий. Это было первое исследование, показавшее, что таксоны образуют многовидовые сообщества в периапикальных тканях, которые при объединении вызывают более сильные воспалительные реакции [50]. Эти данные о том, что заболевания пульпы и периапикальных тканей вызываются полимикробными инфекциями, формирующими биопленки, подтверждаются несколькими другими исследованиями [12, 50, 165, 208].
Развитие сложных молекулярных инструментов еще больше улучшило наше понимание полимикробной природы пульповых и периапикальных инфекций [59]. Например, в клиническом обсервационном исследовании изучались образцы, взятые из самого глубокого слоя кариозных поражений дентина, связанных с обнажением пульпы зубов с симптоматическим необратимым пульпитом (N=10) [170]. В половине случаев запущенного кариеса преобладали лактобациллы. В остальных наиболее доминирующими родами были Pseudoramibacter, Olsenella, Streptococcus и Stenotrophomonas. Напротив, в других исследованиях сообщается, что Prevotella является доминирующим родом при глубоком кариесе дентина [29]., 106, 133, 182]. Эти различия могут быть связаны с методологическими проблемами или могут быть связаны с географическими различиями в составе микробиоты полости рта [11].
В половине случаев запущенного кариеса преобладали лактобациллы. В остальных наиболее доминирующими родами были Pseudoramibacter, Olsenella, Streptococcus и Stenotrophomonas. Напротив, в других исследованиях сообщается, что Prevotella является доминирующим родом при глубоком кариесе дентина [29]., 106, 133, 182]. Эти различия могут быть связаны с методологическими проблемами или могут быть связаны с географическими различиями в составе микробиоты полости рта [11].
Интеграция наборов данных из культуральных и молекулярных исследований показывает, что более 460 уникальных бактериальных таксонов, принадлежащих к 100 родам и девяти типам, были идентифицированы при эндодонтических инфекциях. Преобладающие типы включают Firmicutes, Bacteroidetes, Actinobacteria и Proteobacteria [191]. Эти исследования также показывают, что микробное разнообразие при эндодонтических инфекциях не ограничивается бактериями; вместо этого он также включает грибы, археи [219, 220] и вирусы [28, 47, 82, 120, 158].
В то время как микробная инфекция является преобладающей этиологией воспаления пульпы, такие процедуры, как препарирование полости и реставрация, также могут неблагоприятно влиять на пульпу. Эмаль и дентин являются одними из самых твердых тканей в организме, и тепло, выделяющееся во время препарирования полости, потенциально может вызвать воспаление пульпы [116, 183, 197]. Большинство современных реставрационных материалов не оказывают неблагоприятного воздействия на пульпу до тех пор, пока ткань не подвергается непосредственному воздействию. Однако микроподтекания вокруг реставраций могут вызвать воспаление пульпы [73].
3.3 Воспаление в сравнении с инфекцией пульпы и периапикальных тканей
3.3.1 Бактериальное раздражение и инвазия пульпы зуба
или врожденные дефекты коронки приводят к воспалению пульпы. Даже ранний ямочный и фиссурный кариес связан с воспалением, которое соответствует распространению пораженных дентинных канальцев на пульпу [20].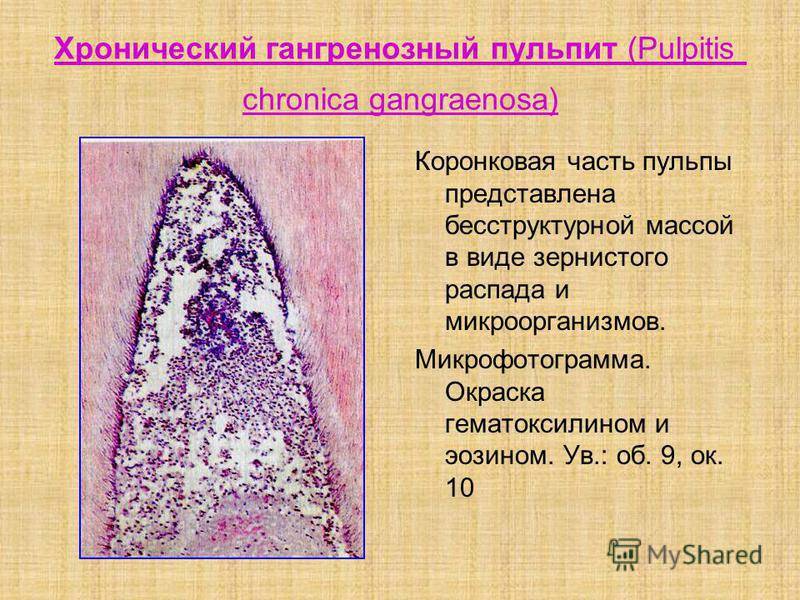 Аналогично, открытая поверхность корня, не покрытая цементом, позволяет бактериям проникать на внешнюю поверхность дентинных канальцев и приводит к легкому воспалению в соответствующей области пульпы [114]. В этих случаях бактерии могут физически не присутствовать в пульпе, но секретировать ферменты, токсины или молекулы клеточной стенки, которые перемещаются по канальцам и вызывают раздражение пульпы. По мере приближения бактериального раздражения к пульпе воспаление усиливается в зоне, ближайшей к раздражителям, и в конечном итоге распространяется на отдаленные участки пульпы. Степень воспаления пульпы коррелирует с количеством бактериальных раздражителей и их близостью к пульпе [140, 165]. В конце концов, бактериальная инфекция достигает пульпы и распространяется по витальной пульпе, что приводит к дегенерации пульпы и инициированию периапикального воспаления. Такой же процесс воспаления с последующей потенциальной инфекцией в конечном итоге происходит и в периапикальных отростках, особенно после полного некроза пульпы.
Аналогично, открытая поверхность корня, не покрытая цементом, позволяет бактериям проникать на внешнюю поверхность дентинных канальцев и приводит к легкому воспалению в соответствующей области пульпы [114]. В этих случаях бактерии могут физически не присутствовать в пульпе, но секретировать ферменты, токсины или молекулы клеточной стенки, которые перемещаются по канальцам и вызывают раздражение пульпы. По мере приближения бактериального раздражения к пульпе воспаление усиливается в зоне, ближайшей к раздражителям, и в конечном итоге распространяется на отдаленные участки пульпы. Степень воспаления пульпы коррелирует с количеством бактериальных раздражителей и их близостью к пульпе [140, 165]. В конце концов, бактериальная инфекция достигает пульпы и распространяется по витальной пульпе, что приводит к дегенерации пульпы и инициированию периапикального воспаления. Такой же процесс воспаления с последующей потенциальной инфекцией в конечном итоге происходит и в периапикальных отростках, особенно после полного некроза пульпы.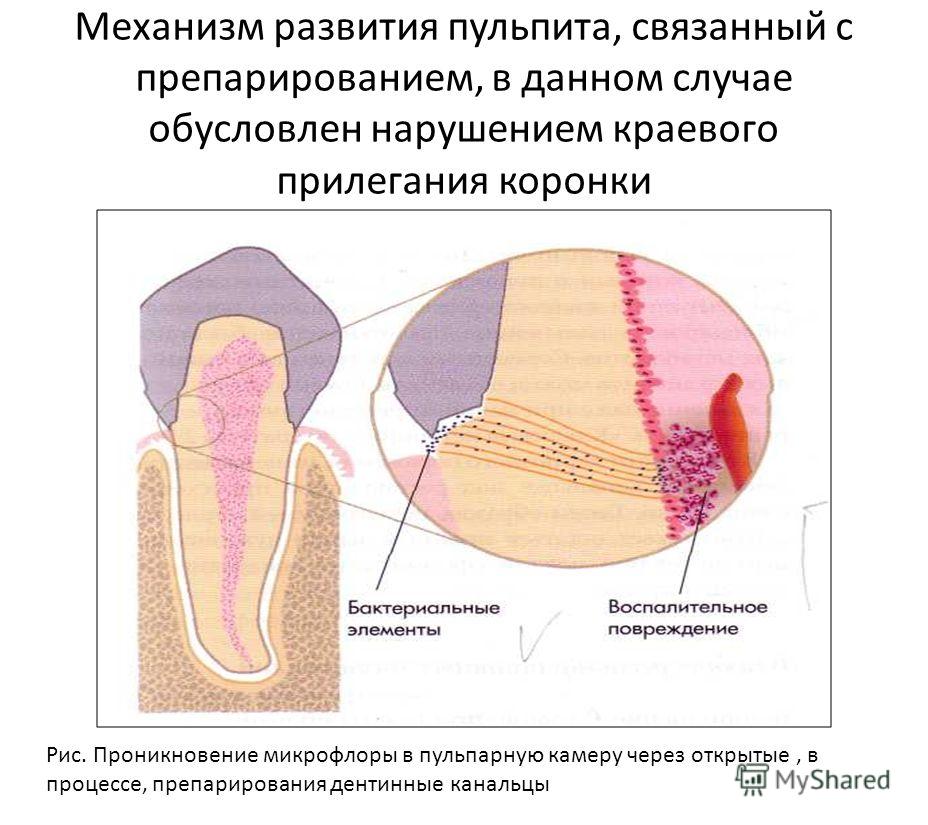 Апикальная инфекция может привести к формированию острого или хронического абсцесса, особенно когда вирулентные бактерии достигают периапикальной области в достаточном количестве. Следовательно, и пульпа, и периапикальные ткани претерпевают стадию воспалительных изменений, прежде чем физически заразятся бактериями. Одной из основных целей диагностического процесса с клинической точки зрения является определение того, воспалены или инфицированы пораженная пульпа и периапекс, потому что это повлияет на анестезиологические соображения, экстренное и радикальное лечение, а также на определение прогноза.
Апикальная инфекция может привести к формированию острого или хронического абсцесса, особенно когда вирулентные бактерии достигают периапикальной области в достаточном количестве. Следовательно, и пульпа, и периапикальные ткани претерпевают стадию воспалительных изменений, прежде чем физически заразятся бактериями. Одной из основных целей диагностического процесса с клинической точки зрения является определение того, воспалены или инфицированы пораженная пульпа и периапекс, потому что это повлияет на анестезиологические соображения, экстренное и радикальное лечение, а также на определение прогноза.
Исследования показали, что при контакте с бактериями полости рта воспаление пульпы и последующая дегенерация, как правило, опосредованы врожденным иммунитетом. Доказательства этого получены на мышиных моделях, где было показано, что скорость некроза пульпы одинакова у животных с дефицитом адаптивных иммунных клеток, таких как Т- и В-клетки, и у нормальных животных [55, 222]. Однако адаптивный иммунитет, особенно В-клетки и иммуноглобулины, защищают от тяжелых инфекций, вызванных большим количеством патогенных бактерий [212].
Мощные бактериальные молекулы, такие как бактериальный пептидогликан, липополисахарид (LPS) (также известный как эндотоксин) грамотрицательных бактерий и липотейхоевая кислота (LTA) грамположительных бактерий, способны вызывать значительное воспаление пульпы и периапикальных тканей. Например, исследования на животных показали, что размещение LPS в стерильных корневых каналах вызывает периапикальные поражения [34, 45]. ЛПС является мощным медиатором резорбции кости [23], который действует посредством активации пути арахидоновой кислоты, продукции цитокинов и активации комплемента [56]. Кроме того, было показано, что ЛПС активирует рецепторы TLR4 на ноцицепторах тройничного нерва [221] и клинически связан с болью при наличии кариозных поражений [104] и инфицированной пульпы [84, 9].2, 134]. Однако ЛПС ни в коем случае не является единственным бактериальным раздражителем, участвующим в патогенезе пульпита и апикального периодонтита. Исследования, в которых изучалось прогрессирование заболевания пульпы и верхушки корня у моделей с гипочувствительностью к ЛПС, показали, что общее прогрессирование заболевания сравнимо с нормальными животными, что указывает на то, что ЛПС, пептидогликан, бактериальные протеиназы, токсины и другие факторы вирулентности могут способствовать процессу [60].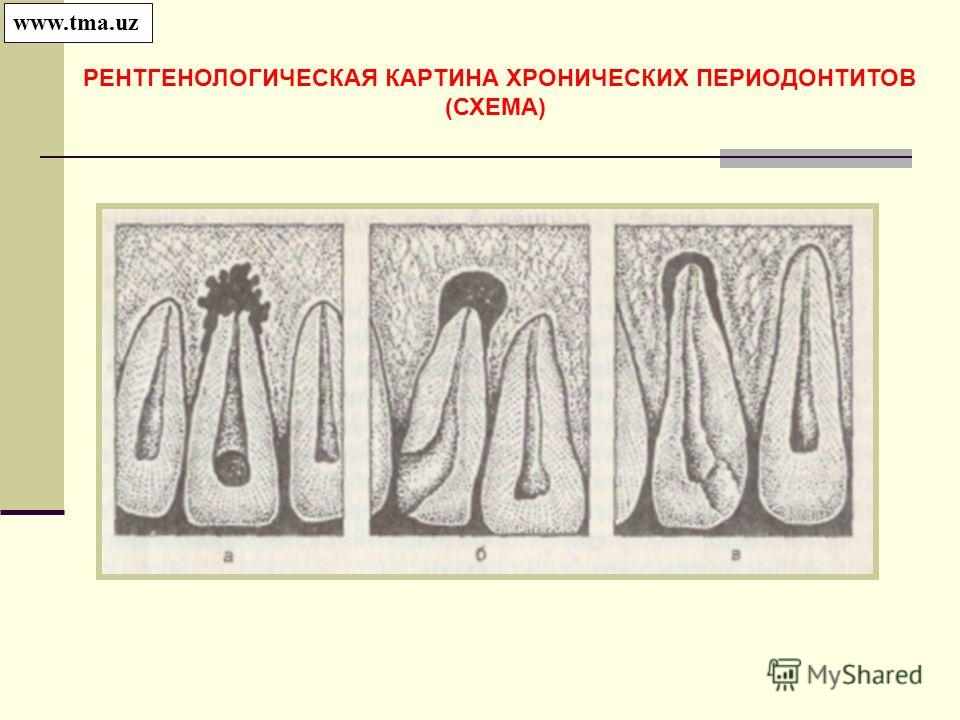
Клинически потеря периапикальной кости обычно видна рентгенологически, когда пульпа некротизирована. Это удивительное открытие, поскольку периапикальное воспаление видно гистологически в исследованиях на животных в период воспаления пульпы. Действительно, было показано, что клинический феномен связан с низкой чувствительностью периапикальной рентгенографии при обнаружении ранних апикальных поражений, и что более чувствительные методы, такие как конусно-лучевая компьютерная томография (КЛКТ), значительно более чувствительны, чем периапикальная рентгенография при обнаружении верхушечный периодонтит при пульпите [1]. Таким образом, пульпа не обязательно должна быть полностью некротизированной для резорбции периапикальной кости и образования периапикального поражения.
3.4 Пульпа зуба
3.4.1 Защитная система в пульпе зуба
Пульпа зуба хорошо приспособлена для обнаружения проникающих патогенов и формирования иммунного ответа на них. Как и во всех других тканях организма, систему защиты пульпы можно разделить на врожденную и адаптивную иммунные реакции. Врожденные ответы не являются антиген-специфичными и включают отток дентинной жидкости наружу и отложение внутриканальцевых иммуноглобулинов [130, 136, 155]. Он также включает резидентные клетки (такие как одонтобласты и фибробласты) и врожденные иммунные клетки (такие как дендритные клетки, естественные клетки-киллеры и Т-клетки). Одонтобласты находятся на границе пульпо-дентинного соединения и имеют отростки, переходящие в дентинные канальцы. В то время как основной функцией одонтобластов является производство матрикса предентина во время формирования зубов и контроль его минерализации, они также играют важную роль в иммунном ответе пульпы. Было высказано предположение, что они представляют собой первую биологически активную линию защиты пульпы и что их роль аналогична роли эпителиальных клеток кожи и слизистых оболочек. Одонтобласты экспрессируют Toll-подобные рецепторы (TLR), класс рецепторов распознавания образов.
Как и во всех других тканях организма, систему защиты пульпы можно разделить на врожденную и адаптивную иммунные реакции. Врожденные ответы не являются антиген-специфичными и включают отток дентинной жидкости наружу и отложение внутриканальцевых иммуноглобулинов [130, 136, 155]. Он также включает резидентные клетки (такие как одонтобласты и фибробласты) и врожденные иммунные клетки (такие как дендритные клетки, естественные клетки-киллеры и Т-клетки). Одонтобласты находятся на границе пульпо-дентинного соединения и имеют отростки, переходящие в дентинные канальцы. В то время как основной функцией одонтобластов является производство матрикса предентина во время формирования зубов и контроль его минерализации, они также играют важную роль в иммунном ответе пульпы. Было высказано предположение, что они представляют собой первую биологически активную линию защиты пульпы и что их роль аналогична роли эпителиальных клеток кожи и слизистых оболочек. Одонтобласты экспрессируют Toll-подобные рецепторы (TLR), класс рецепторов распознавания образов. В частности, они экспрессируют TLR-1, 2, 4, 6 и 9.[44, 95, 217]. Стимуляция этих TLR активирует MyD88-зависимый путь, который запускает активацию NF-kB и MAPK, что приводит к экспрессии провоспалительных генов и генов хемокинов, таких как CCL2, CCL5, CCL7, CXCL8 и CXCL10 [199]. Одонтобласты также экспрессируют белки семейства лейцин-богатых повторов (NLR) с нуклеотидсвязывающим доменом, такие как NOD2, которые распознают пептидогликановые компоненты, общие как для грамположительных, так и для грамотрицательных бактерий [198]. Активированные одонтобласты высвобождают молекулы, такие как оксид азота (NO), бета-дефензины (BD) и белок, связывающий липосахариды (LBP), IL-6, CXCL1, CXCL 2, CXCL 8, CCL2 и IL-10 [41, 42, 44, 111, 154, 217]. Некоторые из них диффундируют через дентин к кариозному поражению, чтобы уничтожить болезнетворные микроорганизмы (такие как NO и BD) или уменьшить их патогенность (например, LBP). Другие диффундируют в пульпу, где активируют и мобилизуют иммунные клетки [44] (рис.
В частности, они экспрессируют TLR-1, 2, 4, 6 и 9.[44, 95, 217]. Стимуляция этих TLR активирует MyD88-зависимый путь, который запускает активацию NF-kB и MAPK, что приводит к экспрессии провоспалительных генов и генов хемокинов, таких как CCL2, CCL5, CCL7, CXCL8 и CXCL10 [199]. Одонтобласты также экспрессируют белки семейства лейцин-богатых повторов (NLR) с нуклеотидсвязывающим доменом, такие как NOD2, которые распознают пептидогликановые компоненты, общие как для грамположительных, так и для грамотрицательных бактерий [198]. Активированные одонтобласты высвобождают молекулы, такие как оксид азота (NO), бета-дефензины (BD) и белок, связывающий липосахариды (LBP), IL-6, CXCL1, CXCL 2, CXCL 8, CCL2 и IL-10 [41, 42, 44, 111, 154, 217]. Некоторые из них диффундируют через дентин к кариозному поражению, чтобы уничтожить болезнетворные микроорганизмы (такие как NO и BD) или уменьшить их патогенность (например, LBP). Другие диффундируют в пульпу, где активируют и мобилизуют иммунные клетки [44] (рис. 3.1).
3.1).
Фибробласты также играют роль в иммунной защите пульпы, помимо их роли в синтезе и обновлении внеклеточного матрикса. Они экспрессируют несколько рецепторов распознавания образов, таких как TLRs-2, 4, 5 и NOD1,2 [83, 103, 126, 199]. После активации они высвобождают медиаторы, такие как TNFa, CXCL8 и др. [102]. Интересное исследование сравнило ответы фибробластов и одонтобластоподобных клеток на различные агонисты TLR [199]. Липотейхоевая кислота (LTA), специфический агонист TLR2, индуцировала активацию CXCL-2 и -10 в одонтобластоподобных клетках, но не в фибробластах. В то время как LPS, специфический агонист TLR4, индуцировал экспрессию CCL7, CCL26 и CXCL11 в фибробластах, но не в одонтобластоподобных клетках, это позволяет предположить, что одонтобласты и фибробласты вызывают специфические иммунные ответы, по-разному влияя на различные иммунные клетки в пульпе.
Резидентные иммунные клетки в пульпе включают лейкоциты, мононуклеарные фагоциты, дендритные клетки и естественные клетки-киллеры (NK) [71]. Эти клетки постоянно исследуют окружающую среду для обнаружения вторгающихся патогенов. Как только патоген обнаружен, количество иммунных клеток резко возрастает. Нейтрофилы являются одними из самых ранних клеток, которые рекрутируются, за ними следуют моноциты, которые дифференцируются в макрофаги [32, 80, 90, 131]. Дендритные клетки и NK-клетки также накапливаются в месте инфекции, где они захватывают бактериальные антигены или разрушают внедрившийся патоген [44, 9].6, 101, 129, 233]. Взаимодействия между дендритными клетками и NK-клетками приводят к взаимной активации и увеличению продукции цитокинов обоими типами клеток. Эти врожденные иммунные клетки также активируют адаптивный иммунный ответ [107, 224]. Дендритные клетки мигрируют в регионарные лимфатические узлы, где они представляют антигены и активируют CD4+ T-клетки (известные как Th0-клетки) [17].
Эти клетки постоянно исследуют окружающую среду для обнаружения вторгающихся патогенов. Как только патоген обнаружен, количество иммунных клеток резко возрастает. Нейтрофилы являются одними из самых ранних клеток, которые рекрутируются, за ними следуют моноциты, которые дифференцируются в макрофаги [32, 80, 90, 131]. Дендритные клетки и NK-клетки также накапливаются в месте инфекции, где они захватывают бактериальные антигены или разрушают внедрившийся патоген [44, 9].6, 101, 129, 233]. Взаимодействия между дендритными клетками и NK-клетками приводят к взаимной активации и увеличению продукции цитокинов обоими типами клеток. Эти врожденные иммунные клетки также активируют адаптивный иммунный ответ [107, 224]. Дендритные клетки мигрируют в регионарные лимфатические узлы, где они представляют антигены и активируют CD4+ T-клетки (известные как Th0-клетки) [17].
В дополнение к врожденным иммунным ответам, описанным выше, нервы, иннервирующие пульпу, также обнаруживают патогены и реагируют на них. Элегантное исследование с использованием нейронов тройничного нерва человека и крысы, а также пульпы зубов крыс продемонстрировало экспрессию CD14 и TLR4 в нервах, иннервирующих пульпу [221]. Последующие исследования показали, что ЛПС сенсибилизирует ионный канал TRPV1 посредством активации TLR4 в сенсорных нейронах тройничного нерва [40, 52]. Эти исследования, наряду с более ранними исследованиями реакции нейронов на воздействие на пульпу, подтверждают роль нейрогенного воспаления при пульпите [105, 108, 211].
Элегантное исследование с использованием нейронов тройничного нерва человека и крысы, а также пульпы зубов крыс продемонстрировало экспрессию CD14 и TLR4 в нервах, иннервирующих пульпу [221]. Последующие исследования показали, что ЛПС сенсибилизирует ионный канал TRPV1 посредством активации TLR4 в сенсорных нейронах тройничного нерва [40, 52]. Эти исследования, наряду с более ранними исследованиями реакции нейронов на воздействие на пульпу, подтверждают роль нейрогенного воспаления при пульпите [105, 108, 211].
Рисунок 3.1 Иллюстрация двух ключевых аспектов защитного механизма, устанавливаемого одонтобластами. В ответ на бактерии (B) в кариозном дентине одонтобласты (синие) высвобождают медиаторы, такие как оксид азота (NO), бета-дефенсины (BD), липосахарид-связывающий белок (LBP), IL-6, CXCL1, CXCL 2, CXCL 8, CCL2 и Ил-10. Некоторые из этих медиаторов диффундируют через дентин к кариозному поражению, чтобы уничтожить патогены или снизить их патогенность. Другие диффундируют в пульпу, где активируют и мобилизуют иммунные клетки. (Воспроизведено с разрешения из [51].)
(Воспроизведено с разрешения из [51].)
3.4.1.1 Адаптивный иммунитет
Как упоминалось ранее, дендритные клетки активируют CD4+ Т-клетки в лимфатических узлах. Последние затем дифференцируются в эффекторные CD+4-хелперные клетки или индуцированные регуляторные Т-клетки (рис. 3.2). По мере продвижения кариозного поражения к пульпе увеличивается накопление Т-клеток [50, 79, 91]. Здоровая пульпа содержит небольшое количество В-клеток, количество которых увеличивается по мере прогрессирования кариеса и воспаления [71, 79]. Преобладающими иммуноглобулинами, продуцируемыми В-клетками, в воспаленной пульпе являются IgG1, за которыми следуют IgA и IgE [30, 80].
3.4.2 Классификация пульпита
Наиболее общепринятые диагностические классификации основаны на нашем текущем понимании прогноза лечения. Диагноз основывается на симптомах пациента (наличие, продолжительность, тяжесть и тип), наличии кариеса или реставраций, реакции на тесты на чувствительность пульпы, а также клинических и рентгенологических исследованиях. Нормальная пульпа — это зуб, в котором зуб бессимптомный, отвечает на все клинические тесты (пальпацию, перкуссию, холод или электрические раздражители) в пределах нормы и имеет нормальный рентгенологический вид. Нормальная пульпа может содержать кальцинаты.
Нормальная пульпа — это зуб, в котором зуб бессимптомный, отвечает на все клинические тесты (пальпацию, перкуссию, холод или электрические раздражители) в пределах нормы и имеет нормальный рентгенологический вид. Нормальная пульпа может содержать кальцинаты.
Воспаление пульпы обычно подразделяют на обратимый и необратимый пульпит. Первый относится к состоянию легкого воспаления, которое можно «обратить». Другими словами, пульпа способна к заживлению, если проводится соответствующая терапия, такая как удаление раздражителя. Этиология обратимого пульпита включает кариес, травму и недавняя или дефектная реставрация. Клинические осмотры показывают отсутствие чувствительности при пальпации и перкуссии, короткую, непродолжительную реакцию на температурные раздражители и иногда боль при накусывании. Рентгенологическая картина зубов с обратимым пульпитом нормальна.
Когда воспаление пульпы является более тяжелым и прогнозируется, что восстановление нормальной пульпы маловероятно, состояние пульпы классифицируется как «необратимый пульпит»! Эти зубы часто симптоматичны и связаны со спонтанной болью и/или болью, которая сохраняется после устранения термического раздражителя. Зубы могут быть чувствительны к перкуссии и часто имеют нормальный рентгенологический вид.
Зубы могут быть чувствительны к перкуссии и часто имеют нормальный рентгенологический вид.
Рис. 3.2 Иллюстрация роли дендритных клеток (ДК) в активации адаптивного иммунного ответа. Незрелые ДК обычно становятся зрелыми ДК после встречи с антигенами (Ag). Зрелые ДК презентируют антигены наивным CD4+ клеткам, которые затем клонально размножаются и дифференцируются в эффекторные Т-хелперы (Th1, Th3 или Th7) или в индуцированные регуляторные Т-клетки (iT-reg). Альтернативно, незрелые DC частично созревают с образованием толерогенных DC (Tol-DC), которые, в свою очередь, индуцируют дифференцировку клеток iT-reg. TGF — трансформирующий фактор роста; ИЛ — интерлейкин; ИФН — интерферон, Ig — иммуноглобулин. (Воспроизведено с разрешения из [51].)
Этиологические факторы включают глубокий кариес, глубокие реставрации и трещины. Эти пульпы подразделяются на «симптоматические необратимые пульпиты». Напротив, некоторые зубы с кариозными обнажениями или травмами не имеют симптомов. Основываясь на нашем текущем понимании, эти воспаленные пульпы имеют плохой прогноз и, как ожидается, станут некротическими. Эти пульпы подразделяются на «бессимптомные необратимые пульпиты».
Основываясь на нашем текущем понимании, эти воспаленные пульпы имеют плохой прогноз и, как ожидается, станут некротическими. Эти пульпы подразделяются на «бессимптомные необратимые пульпиты».
На данный момент нет достаточных доказательств того, что необратимый пульпит действительно необратим. Основываясь исключительно на истории болей пациентов и доступных в настоящее время диагностических инструментах, невозможно определить, затрагивает ли дегенеративный воспалительный процесс всю пульпу или он ограничен только частью пульпы. Как описано далее в этой главе, гистологическая оценка человеческой пульпы с клинически диагностированным «необратимым» воспалением показала, что в некоторых зубах воспалилась ткань пульпы в одном, но не во всех рогах пульпы [167]. С разработкой новых материалов для покрытия пульпы оказалось, что частичная или полная пульпотомия является жизнеспособным вариантом лечения и что экстирпация всей пульпы может не потребоваться в зубах с необратимым пульпитом [8, 48].
3.4.3 Гистологическая и молекулярная оценка пульпита
Как упоминалось ранее, множественные клетки в пульпе экспрессируют рецепторы распознавания патогенов и быстро реагируют на микробную инфекцию. В недавнем исследовании изучалась гистологическая и молекулярная реакция на повреждение и инфекцию пульпы при воздействии на пульпу крыс PBS или LPS [166]. Ткани исследовали через 3 часа, 9 часов и 3 дня после воздействия. В качестве контроля использовали пульпу интактных зубов. Инфильтрация воспалительными клетками наблюдалась уже в 9часов после воздействия, а остеодентинная матрица была отмечена через 3 дня после воздействия. По сравнению с пульпой, подвергшейся воздействию PBS, площадь пульпы, инфильтрированной воспалительными клетками, и отложения остеодентина были больше в пульпе, подвергшейся воздействию LPS (рис. 3.3). Аналогичные изменения были отмечены при экспрессии сиалофосфопротеина дентина. Анализ методом проточной цитометрии выявил увеличение лейкоцитов и дендритных клеток, в то время как процентное содержание Т-клеток и NK-клеток осталось неизменным. В том же исследовании изучалась экспрессия воспалительных генов. Лечение LPS увеличивало экспрессию IL-6, IL-1 p, IL-10, TNFa, iNOS, CCL2, CXCL1 и CXCL2 через 3 часа. MMP3 активировался в 9 лет.часов и 3 суток после воздействия ЛПС.
В том же исследовании изучалась экспрессия воспалительных генов. Лечение LPS увеличивало экспрессию IL-6, IL-1 p, IL-10, TNFa, iNOS, CCL2, CXCL1 и CXCL2 через 3 часа. MMP3 активировался в 9 лет.часов и 3 суток после воздействия ЛПС.
В клиническом обсервационном исследовании изучали гистологический статус пульпы с клинически диагностированным необратимым воспалением (n=32), обратимым воспалением (n=59) и нормальным (n=4) [167]. В большинстве (84,4%) пульпы с диагнозом необратимого воспаления обнаруживались участки коагуляции или разжижения некроза с бактериальной колонизацией и выраженной лейкоцитарной инфильтрацией в частях коронковой пульпы. Воспалительные/иммунные реакции были гораздо менее выраженными в том, что осталось от коронковой пульпы, и в некоторых зубах; в контралатеральных рогах пульпы отмечались нормальные невоспаленные ткани (рис. 3.4).
В остальной части пульпы, диагностированной как необратимо воспаленная (15,6%), наблюдалось локализованное скопление воспалительных клеток без некроза тканей и бактериальной инфекции – гистологический диагноз соответствовал обратимому пульпиту. Практически во всех (96,6%) пульпах диагностирован обратимый пульпит, гистологический диагноз соответствовал клиническому. В этих пульпах было отмечено накопление хронических воспалительных клеток от легкой до умеренной степени и образование третичного дентина.
Практически во всех (96,6%) пульпах диагностирован обратимый пульпит, гистологический диагноз соответствовал клиническому. В этих пульпах было отмечено накопление хронических воспалительных клеток от легкой до умеренной степени и образование третичного дентина.
В другом клиническом обсервационном исследовании изучалась экспрессия генов у пациентов с пульпитом, страдающих от слабой до сильной боли, а также в нормальных зубах [67]. Гены, участвующие в иммунном ответе, взаимодействии цитокинов и цитокиновых рецепторов и передаче сигналов, взаимодействиях интегрина с клеточной поверхностью и другие, экспрессировались на относительно более высоких уровнях в группе пациентов с пульпитом по сравнению с нормальной пульпой (рис. 3.5 и 3.6).
Кроме того, несколько генов, которые, как известно, модулируют боль и воспаление, показали дифференциальную экспрессию у пациентов с бессимптомной и легкой болью (> 30 мм по визуальной аналоговой шкале) по сравнению с пациентами с умеренной или сильной болью (таблица 3. 1).
1).
Рис. 3.3 Окрашивание трихромом по Массону и иммуногистохимический анализ пульпы крыс, подвергшихся воздействию LPS или PBS. В качестве контроля использовали неэкспонированную пульпу. Стрелка на панели (а) показывает место, где зуб был ампутирован, и обнажена пульпа. По сравнению с PBS (d: малое увеличение; e: большее увеличение) воспалительный экссудат был больше после воздействия LPS (g: малое увеличение; h: большее увеличение). Заживление раны с отложением коллагеновой матрицы (j: малое увеличение; k большее увеличение) было отмечено на 3-й день в группе PBS. Экспрессия сиалофосфопротеина дентина (DSPP) увеличивалась через 3 и 9 часов.-часовые моменты времени (r). (Воспроизведено с разрешения из [166].)
Рис. 3.4. Гистологический анализ зуба с клинически диагностированным необратимым пульпитом. Больной, мужчина 30 лет, поступил с жалобами на сильную боль. (а) Периапикальная рентгенограмма зуба. (b) Подготовка щечно-язычной плоскости для сечения. (c) Обзор пульповой камеры, показывающий абсцесс. Обратите внимание, что контралатеральный рог пульпы выглядит нормальным. (d) Увеличенный вид абсцесса. Обратите внимание на некротические остатки (исходное увеличение 16x). (e) Частичный вид абсцесса (исходное увеличение 40x). (f) Большее увеличение прямоугольной области в E (исходное увеличение 400x). Вставка Изображение абсцесса с большим увеличением (исходное увеличение 400x), указанное стрелкой на D. Обратите внимание на скопление PMN и бактерий. (Воспроизведено с разрешения из [167].)
(c) Обзор пульповой камеры, показывающий абсцесс. Обратите внимание, что контралатеральный рог пульпы выглядит нормальным. (d) Увеличенный вид абсцесса. Обратите внимание на некротические остатки (исходное увеличение 16x). (e) Частичный вид абсцесса (исходное увеличение 40x). (f) Большее увеличение прямоугольной области в E (исходное увеличение 400x). Вставка Изображение абсцесса с большим увеличением (исходное увеличение 400x), указанное стрелкой на D. Обратите внимание на скопление PMN и бактерий. (Воспроизведено с разрешения из [167].)
Рисунок 3.5. Результаты анализа обогащения набора генов между пульпитом и нормальными образцами. Воспаленная пульпа была собрана у пациентов с диагнозом необратимый пульпит (n=20). Контролем служила нормальная пульпа зубов, удаленных по разным причинам (n=20). Полногеномный микрочиповый анализ проводили с использованием многоканального прибора Affymetrix GeneTitan. Каждая полоса представляет функциональные категории и количество значительно регулируемых генов между пульпитом и нормальными группами (q<0,05). (Воспроизведено с разрешения из [67].)
(Воспроизведено с разрешения из [67].)
Рисунок 3.6. Результаты анализа обогащения набора генов между группами, которые не сообщали об отсутствии или слабой боли (>30 мм по ВАШ), и теми, которые сообщали об умеренной или сильной боли по ВАШ, связанной с пульпитом. Образцы были собраны и проанализированы, как описано на рис. 3.5. Каждая полоса представляет функциональные категории и количество значительно регулируемых генов между группами боли от отсутствия до слабой и от умеренной до сильной (q<0,05). (Воспроизведено с разрешения из [67].)
В ограниченном количестве клинических исследований изучались молекулярные маркеры в крови пульпы на уровне белка. Иммуноглобулины IgG, IgA, Ig M, а также эластаза и PGE 2 повышены в воспаленной пульпе по сравнению со здоровой пульпой [2]. Экспрессия цитокина IL-8 повышена в воспаленной симптоматической пульпе по сравнению с нормальной пульпой и бессимптомной пульпой с обнажением кариеса [49]. Содержание дентинной жидкости также может отражать молекулярные изменения в пульпе. Интересное клиническое исследование сравнило экспрессию MMP9в дентинной жидкости, собранной из зубов с диагнозом необратимый пульпит (n=19), по сравнению с нормальным контролем (n=12) [235]. MMP9 представляет собой протеолитический фермент, секретируемый нейтрофилами, и может быть маркером разрушения тканей. Данные показывают явное повышение уровня MMP9 в симптоматических зубах по сравнению с контролем.
Содержание дентинной жидкости также может отражать молекулярные изменения в пульпе. Интересное клиническое исследование сравнило экспрессию MMP9в дентинной жидкости, собранной из зубов с диагнозом необратимый пульпит (n=19), по сравнению с нормальным контролем (n=12) [235]. MMP9 представляет собой протеолитический фермент, секретируемый нейтрофилами, и может быть маркером разрушения тканей. Данные показывают явное повышение уровня MMP9 в симптоматических зубах по сравнению с контролем.
Таблица 3.1 Избранные гены с повышенной или пониженной экспрессией у пациентов с пульпитом. Черный — с пониженной регулировкой; Красный — активизирован; Зеленый — без разницы.
|
Генный символ |
Пульпит по сравнению с нормой |
От отсутствия боли до слабой или от умеренной до сильной боли |
Генная функция (genecards. |
|
АМЕЛКС |
Биоминерализация эмали |
||
|
КАЛКРЛ |
Метаболизм костей |
||
|
CCL20 |
Хемотаксис |
||
|
CD14 |
Врожденный иммунный ответ |
||
|
CD163 |
Рецептор острой фазы |
||
|
КД79А |
Функция В-клеточного рецептора |
||
|
COL10A1 |
Образование коллагена |
||
|
COL11A2 |
Образование коллагена |
||
|
КОЛ12А1 |
Образование коллагена |
||
|
КОЛ14А1 |
Образование коллагена |
||
|
КОЛ15А1 |
Образование коллагена |
||
|
КОЛ15А1 |
Образование коллагена |
||
|
КОЛ18А1 |
Образование коллагена |
||
|
COL1A1 |
Образование коллагена |
||
|
COL1A2 |
Образование коллагена |
||
|
КОЛ21А1 |
Образование коллагена |
||
|
COL4A1 |
Образование коллагена |
||
|
COL4A2 |
Образование коллагена |
||
|
CXCL3 |
Хемотаксис |
||
|
ДЭФА1Б/1А |
Антимикробная активность |
||
|
DEFA3 |
Антимикробная активность |
||
ДСПП |
Образование дентина |
||
|
Ил10РА |
Ил-10 сигналка |
||
|
ИЛ1А |
Воспалительная реакция |
||
|
ИЛ1Б |
Воспалительная реакция |
||
|
ИЛ6 |
Воспаление, созревание В-клеток |
||
|
Ил8 |
Хемотаксис |
||
|
фунтов стерлингов |
Врожденный иммунный ответ |
||
|
ММП13 |
Распад коллагена |
||
|
ММП20 |
Деградация амелогенина |
||
|
ММП9 |
Распад коллагена |
||
|
НОД2 |
Врожденный иммунный ответ |
||
|
НР5А2 |
Противовирусная активность |
||
|
ПТГС2 |
Образование простагландинов |
||
|
СКН8А |
Проницаемость для ионов натрия |
||
|
TLR1 |
Врожденный иммунный ответ |
||
|
TLR2 |
Врожденный иммунный ответ |
||
|
TLR3 |
Врожденный иммунный ответ |
||
|
TLR4 |
Врожденный иммунный ответ |
||
|
TLR6 |
Врожденный иммунный ответ |
||
|
TLR8 |
Врожденный иммунный ответ |
||
|
TLR9 |
Врожденный иммунный ответ |
||
|
ТНФА |
Воспалительная реакция |
Роль эпигенетических модификаций при пульпите только начинает изучаться. Эпигенетические модификации включают метилирование ДНК, модификации гистонов и регуляцию некодирующих РНК. На сегодняшний день метилирование ДНК при воспалении пульпы было изучено только в двух исследованиях. Один из них касался паттерна метилирования IFN у и отмечал частичное метилирование или неметилирование в образцах воспаленной пульпы человека [25]. В другом исследовании не сообщалось об отсутствии различий в метилировании CD14 и TLR2 в нормальной и воспаленной пульпе [24]. Недавние исследования предполагают, что метилирование гистонов на h4K27 играет роль в воспалении пульпы и репаративных процессах [89]., 230].
Эпигенетические модификации включают метилирование ДНК, модификации гистонов и регуляцию некодирующих РНК. На сегодняшний день метилирование ДНК при воспалении пульпы было изучено только в двух исследованиях. Один из них касался паттерна метилирования IFN у и отмечал частичное метилирование или неметилирование в образцах воспаленной пульпы человека [25]. В другом исследовании не сообщалось об отсутствии различий в метилировании CD14 и TLR2 в нормальной и воспаленной пульпе [24]. Недавние исследования предполагают, что метилирование гистонов на h4K27 играет роль в воспалении пульпы и репаративных процессах [89]., 230].
МикроРНК (миР) представляют собой небольшие (18–22 нуклеотида) одноцепочечные некодирующие олигонуклеотиды РНК. Наша лаборатория первой сообщила об экспрессии miR в воспаленной пульпе [236]. Воспаленная пульпа была из кариозных зубов с диагнозом симптоматического или бессимптомного необратимого пульпита (n=18). Нормальная пульпа была удалена из здоровых третьих моляров или зубов, удаленных для ортодонтических целей (n = 12). По сравнению с нормальной пульпой, 36 miR человека были нарушены в воспаленной пульпе. +В отдельном исследовании in vitro мы продемонстрировали, что одна из микроРНК, дифференциально экспрессирующаяся при пульпите, — miR181a модулирует экспрессию цитокина IL-8 [68], демонстрируя тем самым роль микроРНК в модуляции иммунного ответа на микробные инфекции пульпы .
По сравнению с нормальной пульпой, 36 miR человека были нарушены в воспаленной пульпе. +В отдельном исследовании in vitro мы продемонстрировали, что одна из микроРНК, дифференциально экспрессирующаяся при пульпите, — miR181a модулирует экспрессию цитокина IL-8 [68], демонстрируя тем самым роль микроРНК в модуляции иммунного ответа на микробные инфекции пульпы .
3.5 Периапикальные ткани
3.5.1 Защитная система в периапикальных тканях
Как отмечалось ранее, резорбция периапикальной кости и образование периапикального поражения начинаются до полного некроза пульпы. По мере распространения раздражителей в пульпе важно, чтобы апикальная кость рассасывалась и замещалась мягкой тканью, что может вызвать сильный иммунный ответ. Основной функцией периапикального поражения является защита организма от проникновения бактерий из дегенерирующей пульпы. При этом периапикальное поражение защищает от двух серьезных заболеваний: острых распространяющихся инфекций и остеомиелита (рис. 3.7).
3.7).
Хотя эти состояния могут возникать с некоторой частотой, их частота и тяжесть, безусловно, в большинстве случаев модулируются верхушечным иммунным ответом. Развитие апикального поражения, которое можно наблюдать рентгенологически у пациентов, занимает от нескольких недель до месяцев. В моделях на животных размер поражения неуклонно увеличивается, а затем стабилизируется по мере того, как бактериальное раздражение и защитные механизмы достигают стабильной стадии [64]. В некоторых случаях периапикальные поражения могут достигать очень больших размеров (рис. 3.8). Считается, что размер поражения может быть связан с типами и количеством бактериальных раздражителей, развитием апикальной кисты, а также типами и концентрациями медиаторов воспаления в очаге поражения. Имеющиеся данные свидетельствуют о том, что окончательный размер поражения является регулируемым механизмом, который связан с большим количеством микробных факторов и факторов хозяина [200].
Рис. 3.7 Рентгенограмма пациента, перенесшего нехирургическое эндодонтическое лечение левого клыка нижней челюсти, а также первого и второго премоляров. Моляр нормально реагировал. Пациент начал испытывать онемение в этой области, и ему была проведена операция на конце корня премоляра. Отчет о биопсии показал интенсивную воспалительную реакцию и множественные костные фрагменты с пустыми лакунами. Диагноз — остеомиелит.
3.7 Рентгенограмма пациента, перенесшего нехирургическое эндодонтическое лечение левого клыка нижней челюсти, а также первого и второго премоляров. Моляр нормально реагировал. Пациент начал испытывать онемение в этой области, и ему была проведена операция на конце корня премоляра. Отчет о биопсии показал интенсивную воспалительную реакцию и множественные костные фрагменты с пустыми лакунами. Диагноз — остеомиелит.
3.5.1.1 Острые инфекции
Острые эндодонтические инфекции составляют около 56% всех нетравматических стоматологических неотложных состояний [163]. В США эндодонтические инфекции приводят к более чем 400 000 амбулаторных посещений отделений неотложной помощи в год [148]. Эндодонтические абсцессы являются причиной около 8000 госпитализаций в год [5], были причиной смерти 66 госпитализированных пациентов в течение 8 лет, согласно одному исследованию [185]. Учитывая, что в США 27-41% взрослого населения имеют по крайней мере один зуб с апикальным периодонтитом [22], очевидно, что, несмотря на большое количество, тяжелые, опасные для жизни эндодонтические инфекции затрагивают небольшое количество случаев. Наиболее распространенными клиническими проявлениями симптоматических случаев являются случаи, когда имеется симптоматический апикальный периодонтит, связанный с симптоматическим необратимым пульпитом или с некрозом пульпы, или острые апикальные абсцессы с локализованным отеком, лимфаденопатией и минимальными конституциональными симптомами. По данным одного исследования, 57% всех случаев симптоматического необратимого пульпита связаны с симптоматическим апикальным периодонтитом [151]. Наоборот, было показано, что около 40% случаев некроза пульпы и хронического апикального периодонтита развиваются с минимальной болью [139].].
Наиболее распространенными клиническими проявлениями симптоматических случаев являются случаи, когда имеется симптоматический апикальный периодонтит, связанный с симптоматическим необратимым пульпитом или с некрозом пульпы, или острые апикальные абсцессы с локализованным отеком, лимфаденопатией и минимальными конституциональными симптомами. По данным одного исследования, 57% всех случаев симптоматического необратимого пульпита связаны с симптоматическим апикальным периодонтитом [151]. Наоборот, было показано, что около 40% случаев некроза пульпы и хронического апикального периодонтита развиваются с минимальной болью [139].].
Неясно, какие конкретные факторы участвуют в развитии симптоматического апикального периодонтита или тяжелых эндодонтических инфекций. Многочисленные исследования изучали возможность того, что специфические вирулентные эндодонтические патогены могут быть связаны с эндодонтическими инфекциями. Например, в ряде исследований показана ассоциация Fusobacterium nucleatum и Parvimonas micra [27, 61, 178], а также чернопигментированных бактерий, принадлежащих к родам Prevotella и Porphyromonas [75, 77, 208, 209]. ] с болью. Молекулярные исследования, в которых используются более чувствительные методы, показали, что спирохеты, принадлежащие к Treponema spp. (в основном T. denticola) в значительной степени связаны с наличием боли и апикальных острых инфекций, особенно при первичных инфекциях [117, 176, 189]. Связь между этим микроорганизмом и острыми эндодонтическими инфекциями является примером точности и чувствительности молекулярной микробиологии, потому что представители рода Treponema, как и многие другие спирохеты, очень требовательны и поэтому их трудно идентифицировать при культивировании [58]. Молекулярные исследования также идентифицировали другие роды микроорганизмов, которые связаны с болью, такие как Dialister, Filifactor, Olsenella, Granulicatella и Synergistes [171, 19].2]. Однако современное глубокое секвенирование бактериальных образцов от эндодонтических инфекций ясно показало, что бактериальное сообщество содержит сотни или тысячи бактериальных таксонов [87, 121, 190]. Более того, эти исследования показали, что относительное обилие наиболее распространенных отдельных таксонов очень низкое, а доминирующие микроорганизмы отсутствуют.
] с болью. Молекулярные исследования, в которых используются более чувствительные методы, показали, что спирохеты, принадлежащие к Treponema spp. (в основном T. denticola) в значительной степени связаны с наличием боли и апикальных острых инфекций, особенно при первичных инфекциях [117, 176, 189]. Связь между этим микроорганизмом и острыми эндодонтическими инфекциями является примером точности и чувствительности молекулярной микробиологии, потому что представители рода Treponema, как и многие другие спирохеты, очень требовательны и поэтому их трудно идентифицировать при культивировании [58]. Молекулярные исследования также идентифицировали другие роды микроорганизмов, которые связаны с болью, такие как Dialister, Filifactor, Olsenella, Granulicatella и Synergistes [171, 19].2]. Однако современное глубокое секвенирование бактериальных образцов от эндодонтических инфекций ясно показало, что бактериальное сообщество содержит сотни или тысячи бактериальных таксонов [87, 121, 190]. Более того, эти исследования показали, что относительное обилие наиболее распространенных отдельных таксонов очень низкое, а доминирующие микроорганизмы отсутствуют. Поэтому неясно, как профиль микробного сообщества влияет на развитие симптомов. Также вероятно, что эти сложные микробные сообщества по-разному взаимодействуют с реакцией хозяина у разных пациентов, что делает точную идентификацию или истинных виновников довольно сложной задачей.
Поэтому неясно, как профиль микробного сообщества влияет на развитие симптомов. Также вероятно, что эти сложные микробные сообщества по-разному взаимодействуют с реакцией хозяина у разных пациентов, что делает точную идентификацию или истинных виновников довольно сложной задачей.
Рис. 3.8. Пациент-подросток с диагнозом некроз пульпы и бессимптомный апикальный периодонтит левого латерального резца верхней челюсти. Пациент вернулся на лечение только через год. Обратите внимание на значительное увеличение размера поражения за это время. (Воспроизведено с разрешения [57].)
Вирусные инфекции могут усугублять или усиливать симптомы эндодонтических инфекций. Более ранние исследования показали, что инфицирование цитомегаловирусом человека или вирусом Эпштейна-Барр было связано с более крупными и симптоматическими периапикальными поражениями [174, 175, 19].5]. Однако недавний систематический обзор и метаанализ не выявили значительной связи между этими вирусами и симптомами [93]. Следует отметить, что инфекция ветряной оспы часто сопровождается постгерпетической болью, которая может клинически проявляться как зубная боль. Эта вирусная инфекция была связана с патогенезом патологии пульпы и верхушки в нескольких отчетах о случаях, сериях случаев и недавнем систематическом обзоре [76, 94, 156, 187].
Следует отметить, что инфекция ветряной оспы часто сопровождается постгерпетической болью, которая может клинически проявляться как зубная боль. Эта вирусная инфекция была связана с патогенезом патологии пульпы и верхушки в нескольких отчетах о случаях, сериях случаев и недавнем систематическом обзоре [76, 94, 156, 187].
3.5.1.2 Хронические инфекции
Верхушечный периодонтит, по-видимому, является очень распространенным заболеванием среди стоматологических пациентов и лиц, не являющихся пациентами (таблица 3.2).
Как отмечалось ранее, это еще одно свидетельство того, что большинство эндодонтических патологий протекает бессимптомно и представляет собой гомеостатическую связь между микробными раздражителями и реакцией хозяина. Однако хроническое или бессимптомное заболевание может обостряться, приводя к острым инфекциям. Считается, что это происходит из-за изменений в составе микробного сообщества или бактериальной нагрузки. Это также может быть связано с изменениями в реакции хозяина, например, если иммунная система подвергается стрессу или нарушению. В этой области доступно очень мало объективных данных из клинических исследований из-за этической сложности изучения прогрессирования поражения без лечения у пациентов.
В этой области доступно очень мало объективных данных из клинических исследований из-за этической сложности изучения прогрессирования поражения без лечения у пациентов.
Таблица 3.2 Распространенность апикальных поражений, связанных как минимум с одним зубом, у взрослого населения в отдельных репрезентативных исследованиях. Звездочкой обозначены популяции стоматологических клиник.
|
Бергстром и др. 1987 [15] |
(Швеция) |
48% |
|
Одесжо и др. 1990 [150] |
(Швеция) |
43% |
|
Де Клин и др. 1993 [35] |
(Нидерланды) |
45%* |
|
Сондерс и др. |
(Шотландия) |
41%* |
|
Киркеванг и др. 2001 [109] |
(Дания) |
42% |
|
Буше и др. 2002 [19] |
(Франция) |
63%* |
|
Кабак и Эббот 2005 [97] |
(Беларусь) |
80%* |
|
Палмквист 1986 [153] |
(Швеция) (>65 лет) |
72% |
|
Айнамо и др. |
(Финляндия) (>75 лет) |
41% |
|
Каплан и др., 2006 [22] |
(США) (<45 лет) |
27% |
|
Каплан и др., 2006 [22] |
(США) (>45 лет) |
41% |
Имеется большой объем данных по животным моделям или роли различных иммунологических факторов в размере хронических периапикальных поражений. Большинство этих животных моделей имеют хронические периапикальные поражения, которые являются типичными поражениями, которые развиваются при обнажении и экстирпации пульпы. У животных могут развиться острые инфекции в редких случаях, например, при неконтролируемом сахарном диабете [62] или при тяжелом комбинированном иммунодефиците, когда они также заражены эндодонтическими патогенами [212]. Эта тенденция к развитию хронического поражения в нормальных условиях иллюстрирует успех иммунных реакций в предотвращении тяжелых распространяющихся инфекций или остеомиелита, вызванного периапикальными инфекциями. Однако в этих моделях поражения различаются по размеру и скорости прогрессирования в зависимости от множества микробных факторов и факторов реакции хозяина.
Эта тенденция к развитию хронического поражения в нормальных условиях иллюстрирует успех иммунных реакций в предотвращении тяжелых распространяющихся инфекций или остеомиелита, вызванного периапикальными инфекциями. Однако в этих моделях поражения различаются по размеру и скорости прогрессирования в зависимости от множества микробных факторов и факторов реакции хозяина.
Животные с дефицитом TLR-4, который распознает LPS, имеют меньшие периапикальные поражения в одни моменты времени, но не в другие [60, 85]. Интересно, что у животных с дефицитом TLR-2, которые распознают липотейхоевую кислоту грамположительных бактерий, индуцированные периапикальные поражения больше, а не меньше, чем у контрольной группы [33]. Недавно сообщалось, что дефицит TLR-2 может усиливать передачу сигналов CD-14 и TLR-4, что может объяснить увеличенный размер периапикального поражения в этих случаях [169]. Кроме того, эндодонтические патогены, такие как F. nucleatum, могут вызывать выработку цитокинов, которая опосредована передачей сигналов митогенактивируемой протеинкиназы p38 (MAPK), которая не зависит от TLR, нуклеотид-связывающего домена олигомеризации-1 (NOD-1), NOD- 2 и сигнальный путь ядерного фактора каппа B (NF-kB) [162]. В совокупности эти исследования показывают, что периапикальные поражения возникают из-за многих разнообразных бактерий, для которых действуют разные модели распознавания.
В совокупности эти исследования показывают, что периапикальные поражения возникают из-за многих разнообразных бактерий, для которых действуют разные модели распознавания.
В патогенезе хронических периапикальных поражений, в ответ на нормальную микрофлору полости рта, отсутствие Т- и В-клеток [55, 210], фактора комплемента С5 [86], интерлейкина-4 (ИЛ-4) [38, 180], гамма-интерферон (IFN), IL-12 или IL-18 [179], по-видимому, не влияют на патогенез периапикальных поражений.
Однако периапикальные поражения имеют больший размер при дефиците молекул адгезии, таких как молекула межклеточной адгезии-1 (ICAM-1) [38] или P/E-селектины [100], IL-6 [9, 88], IL-10 [38, 180] или хемокины, такие как CCR2 [70] и CCR5 [38], которые имеют решающее значение для миграции циркулирующих воспалительных клеток в очаг воспаления.
Эстроген защищает от распространения периапикальных поражений [72, 228].
Этот эффект можно модулировать антиэстрогенными препаратами, такими как ралоксифен [74]. Напротив, такие препараты, как бисфосфонаты, например алендронат [186, 228, 229] и метформин (гипогликемическое средство) [127], уменьшают резорбцию кости при периапикальных поражениях. Есть много других лекарств и состояний хозяина, которые могут влиять на скорость расширения, симптомы окончательного размера при апикальном периодонтите (и, возможно, на заживление после лечения), и поэтому это является предметом активных исследований.
Напротив, такие препараты, как бисфосфонаты, например алендронат [186, 228, 229] и метформин (гипогликемическое средство) [127], уменьшают резорбцию кости при периапикальных поражениях. Есть много других лекарств и состояний хозяина, которые могут влиять на скорость расширения, симптомы окончательного размера при апикальном периодонтите (и, возможно, на заживление после лечения), и поэтому это является предметом активных исследований.
3.5.2 Классификация апикального периодонтита
3.5.2.1 Гистопатологическая классификация апикального периодонтита
лечение корневых каналов. В связи с этим апикальный периодонтит был классифицирован на три основных гистопатологических состояния: апикальная гранулема, апикальная киста и апикальный абсцесс. Другие менее распространенные апикальные образования включают реакцию на инородное тело (например, на частицы пищи, стоматологические материалы или силеры), апикальный рубец (который формируется из фиброзной ткани и может возникнуть после хирургического лечения больших апикальных поражений) или холестеатому (которая является поражением). заполнены расщелинами, которые образуются из кристаллов холестерина вместе с гигантскими клетками).
заполнены расщелинами, которые образуются из кристаллов холестерина вместе с гигантскими клетками).
3.5.2.1.1 Апикальная гранулема
Апикальная гранулема получила это обозначение из-за присутствия воспалительных клеток, таких как нейтрофилы, лимфоциты, плазматические клетки, макрофаги и тучные клетки, которые могут окружать более крупные многоядерные гигантские клетки или пенистые клетки , придавая вид гранул. Другие гранулематозные заболевания включают туберкулез, проказу и саркоидоз. Апикальные гранулемы могут также включать остатки эпителиальных клеток Маллассеза. Это остатки эпителиального корневого влагалища Гертвига, участвующего в эмбриологическом развитии корня.
Апикальные гранулемы являются первичными поражениями, участвующими в формировании апикального иммунного ответа. Даже при других гистопатологических состояниях, таких как кисты или абсцессы, часть поражения, обычно на периферии, представляет собой апикальную гранулему и считается, что она привела к возникновению кисты или абсцесса. Апикальная гранулема содержит клеточные и молекулярные факторы, участвующие в упомянутом выше иммунном ответе. Дифференциальное количество присутствующих воспалительных клеток может зависеть от метода, используемого для исследования, от того, является ли поражение первичным или персистирующим апикальным периодонтитом, а также от того, является ли оно моделью человека или животных. Исследования на людях показали, что макрофаги [202, 203] или лимфоциты [14] могут доминировать в периапикальной гранулеме. Исследования на животных показывают, что Т-хелперы преобладают на начальных фазах развития поражения, а Т-супрессоры преобладают на более поздних фазах поражения [201, 225]. Недавно было показано, что Т-регуляторные (T-reg) клетки играют важную роль в модуляции или контроле распространения периапикального поражения. Ингибирование T-reg приводило к значительному увеличению тяжести периапикального поражения, что было связано с активацией провоспалительных Т-хелперов 1 и Т-хелперов 17 [66].
Апикальная гранулема содержит клеточные и молекулярные факторы, участвующие в упомянутом выше иммунном ответе. Дифференциальное количество присутствующих воспалительных клеток может зависеть от метода, используемого для исследования, от того, является ли поражение первичным или персистирующим апикальным периодонтитом, а также от того, является ли оно моделью человека или животных. Исследования на людях показали, что макрофаги [202, 203] или лимфоциты [14] могут доминировать в периапикальной гранулеме. Исследования на животных показывают, что Т-хелперы преобладают на начальных фазах развития поражения, а Т-супрессоры преобладают на более поздних фазах поражения [201, 225]. Недавно было показано, что Т-регуляторные (T-reg) клетки играют важную роль в модуляции или контроле распространения периапикального поражения. Ингибирование T-reg приводило к значительному увеличению тяжести периапикального поражения, что было связано с активацией провоспалительных Т-хелперов 1 и Т-хелперов 17 [66].
Считается, что периапикальная гранулема содержит небольшое количество бактерий или не содержит их непосредственно внутри. Исследования на животных не выявили бактерий в апикальной гранулеме [64, 223], а в поражениях человека (которые предположительно имеют более длительный индукционный период к моменту взятия образца, чем в большинстве исследований на животных) гистологически обнаруживается низкая распространенность бактерий [143, 168]. . Стойкие поражения могут иметь более высокую распространенность бактерий в поражении [205-207]. Когда они присутствуют, бактерии обычно окружены интенсивными воспалительными клетками, в основном нейтрофилами и макрофагами [64]. Иногда внутри гранулемы видна область некроза, окруженная интенсивным воспалительным клеточным ответом, и это поражение называется апикальным абсцессом. Одно исследование показало, что 35% апикальных поражений, удаляемых вместе с зубом, представляют собой апикальные абсцессы [146].
Исследования на животных не выявили бактерий в апикальной гранулеме [64, 223], а в поражениях человека (которые предположительно имеют более длительный индукционный период к моменту взятия образца, чем в большинстве исследований на животных) гистологически обнаруживается низкая распространенность бактерий [143, 168]. . Стойкие поражения могут иметь более высокую распространенность бактерий в поражении [205-207]. Когда они присутствуют, бактерии обычно окружены интенсивными воспалительными клетками, в основном нейтрофилами и макрофагами [64]. Иногда внутри гранулемы видна область некроза, окруженная интенсивным воспалительным клеточным ответом, и это поражение называется апикальным абсцессом. Одно исследование показало, что 35% апикальных поражений, удаляемых вместе с зубом, представляют собой апикальные абсцессы [146].
3.5.2.1.2 Апикальная киста
Апикальная киста возникает в результате пролиферации остатков эпителия Маллассе в гранулеме (рис. 3.9). Эпителий первоначально образует тяжи, которые со временем сливаются. Увеличение массы эпителиальных клеток может создать дефицит питания в центре массы, вызывая некроз ткани и разжижение с образованием кисты с кистозной жидкостью. В качестве альтернативы эпителиальные тяжи могут окружать часть гранулематозной ткани, вызывая образование кисты [213]. Считается, что расширение кисты происходит из-за давления со стороны жидкости внутри кисты, особенно из-за того, что клетки эпителия могут секретировать костно-резорбтивные цитокины [123, 214]. Кисты могут клинически достигать очень больших размеров и вызывать смещение корней соседних зубов.
Увеличение массы эпителиальных клеток может создать дефицит питания в центре массы, вызывая некроз ткани и разжижение с образованием кисты с кистозной жидкостью. В качестве альтернативы эпителиальные тяжи могут окружать часть гранулематозной ткани, вызывая образование кисты [213]. Считается, что расширение кисты происходит из-за давления со стороны жидкости внутри кисты, особенно из-за того, что клетки эпителия могут секретировать костно-резорбтивные цитокины [123, 214]. Кисты могут клинически достигать очень больших размеров и вызывать смещение корней соседних зубов.
Диагноз апикальной кисты варьирует. Некоторые патологоанатомы определяют, что поражение представляет собой кисту, всякий раз, когда они видят признаки пролиферации эпителия в представленной ткани. Другие диагностируют кисту только тогда, когда видят неповрежденную эпителиальную выстилку, окружающую заполненную жидкостью полость, которая может содержать холестериновые щели. Эта изменчивость в определении диагноза привела к большим различиям между исследованиями, в которых изучалась распространенность гранулем и кист (таблица 3. 3).
3).
Дальнейшая классификация апикальных кист требует дифференциации кист «Bay» [188] или «Pocket» [164] от истинных апикальных кист. В кистах залива или кармана верхушка корня выступает в кисту, и корневой канал открывается прямо в просвет кисты. В истинной апикальной кисте эпителиальная выстилка кисты и соединительная ткань кажутся непрерывными и отделенными от верхушки корня.
Рис. 3.9. Биоптаты тканей, извлеченных во время апикальной операции в случае незаживающего апикального периодонтита, диагностированного патологоанатомом как периапикальная киста. ( а ) Эпителиальная пролиферация в тяжи внутри гранулематозной ткани (исходное увеличение 100x). (б) Эпителиальная пролиферация (исходное увеличение 200x).
Таблица 3.3 Распространенность кист и гранулем в нескольких часто цитируемых исследованиях.
|
Размер образца |
Кисты % |
Гранулемы % |
|
|
Прибе и др. |
101 |
54 |
46 |
|
Паттерсон и др. 1964 [157] |
510 |
14 |
20 |
|
Бхаскар 1966 [16] |
2308 |
42 |
48 |
|
Лалонд и Любке 1968 [113] |
800 |
44 |
45 |
|
Мортенсен и др. 1970 [142] |
396 |
41 |
59 |
|
Блок и др. |
230 |
7 |
93 |
|
Винсток 1980 [227] |
9804 |
8 |
83 |
|
Стокдейл и Чендлер 1988 [204] |
1108 |
17 |
77 |
|
Спатафор и др. 1990 [196] |
1659 |
42 |
52 |
|
Наир и др. 1996 [164] |
256 |
15 |
50 |
|
Койвисто и др. |
9723 |
33 |
40 |
Диагноз апикальной кисты по сравнению с гранулемой можно поставить только гистологически на основании биоптата или удаленного зуба. Попытки провести это различие с помощью рентгенографии [226] и даже конусно-лучевой компьютерной томографии (КЛКТ) [172] не увенчались успехом. В этом отношении могут быть полезны недавние попытки использовать специальные индексы и алгоритмы для оценки КЛКТ [78]. Имеются некоторые общие рентгенографические признаки апикального просветления, которые позволяют предположить, что это киста, такие как большой размер, окруженный хорошо кортикальной границей и выталкивающий корни соседних зубов. Учитывая сложность клинической диагностики кисты по сравнению с гранулемой, было трудно доказать или опровергнуть эффективность нехирургического лечения корневых каналов при лечении апикальных кист. В 19В 50-х и 1960-х годах считалось, что хирургическая энуклеация необходима для лечения апикальных кист, как и в случае с другими типами кист. Однако позже были выдвинуты аргументы, что, поскольку кисты были довольно распространены в диагностике апикального периодонтита, тот факт, что нехирургическое лечение корневых каналов в случаях с апикальным периодонтитом было более успешным, чем средняя распространенность апикальных гранулем, означает, что должно быть разумное количество кисты, которые зажили без хирургического лечения. Совсем недавно было установлено, что распространенность истинных апикальных кист (в отличие от карманных кист) невелика и что они устойчивы к нехирургическому лечению [144, 145]. Эти гипотезы еще предстоит доказать, особенно то, что диагностика истинной апикальной кисты в настоящее время невозможна до операции.
В 19В 50-х и 1960-х годах считалось, что хирургическая энуклеация необходима для лечения апикальных кист, как и в случае с другими типами кист. Однако позже были выдвинуты аргументы, что, поскольку кисты были довольно распространены в диагностике апикального периодонтита, тот факт, что нехирургическое лечение корневых каналов в случаях с апикальным периодонтитом было более успешным, чем средняя распространенность апикальных гранулем, означает, что должно быть разумное количество кисты, которые зажили без хирургического лечения. Совсем недавно было установлено, что распространенность истинных апикальных кист (в отличие от карманных кист) невелика и что они устойчивы к нехирургическому лечению [144, 145]. Эти гипотезы еще предстоит доказать, особенно то, что диагностика истинной апикальной кисты в настоящее время невозможна до операции.
Другая важная проблема, связанная с апикальными кистами как патологическим образованием, заключается в том, что с биологической точки зрения несколько исследований, проведенных для различения гранулем и кист в отношении клеточного и молекулярного содержимого, не выявили заметных различий [21, 36, 37, 132, 218]. В одном недавнем исследовании литература по экспрессии генов в апикальных гранулемах и радикулярных кистах была изучена более критически с использованием современных инструментов биоинформатики [160]. В этом исследовании было обнаружено, что в кистах экспрессируются основные гены TP53 (опухолевый белок p53) и EP300 (E1A-связывающий белок p300), тогда как периапикальные гранулемы ассоциированы с IL2R, CCL2, CCL4, CCL5, CCR1, CCR3 и CCR5. гены [160].
В одном недавнем исследовании литература по экспрессии генов в апикальных гранулемах и радикулярных кистах была изучена более критически с использованием современных инструментов биоинформатики [160]. В этом исследовании было обнаружено, что в кистах экспрессируются основные гены TP53 (опухолевый белок p53) и EP300 (E1A-связывающий белок p300), тогда как периапикальные гранулемы ассоциированы с IL2R, CCL2, CCL4, CCL5, CCR1, CCR3 и CCR5. гены [160].
3.5.2.2 Клиническая классификация апикального периодонтита
Клиническая классификация апикального периодонтита менялась с годами и в разных регионах мира. По сути, несколько клинических признаков и симптомов подтверждают диагноз апикального периодонтита. При отсутствии гистопатологического диагноза клинический диагноз используется для определения плана лечения, прогноза, необходимости дальнейшего исследования и тестирования и ответа на лечение.
Пациенты с апикальным периодонтитом могут не иметь симптомов, могут жаловаться на слабую или умеренную боль при жевании и могут проявлять сильную боль с отеком или без отека по отношению к пораженному зубу. Рентгенологические признаки включают область гиподенсивности, связанную с верхушкой (или латеральной границей) пораженного зуба, расширение периодонтальной связки и отсутствие твердой пластинки в области рентгенопрозрачности. Зона рентгенологической гиподенсивности может быть диффузной по протяженности или хорошо очерченной и окруженной кортикальной каймой. Иногда на границе рентгенопрозрачности имеется участок повышенной рентгенологической плотности. Другие признаки заболевания включают свищевой ход, который ведет к области апикальной рентгенопрозрачности.
Рентгенологические признаки включают область гиподенсивности, связанную с верхушкой (или латеральной границей) пораженного зуба, расширение периодонтальной связки и отсутствие твердой пластинки в области рентгенопрозрачности. Зона рентгенологической гиподенсивности может быть диффузной по протяженности или хорошо очерченной и окруженной кортикальной каймой. Иногда на границе рентгенопрозрачности имеется участок повышенной рентгенологической плотности. Другие признаки заболевания включают свищевой ход, который ведет к области апикальной рентгенопрозрачности.
Клинический диагноз апикального периодонтита использует эти признаки и симптомы таким образом, чтобы клиницист мог их распознать и воспроизвести. Точная терминология дополнительно обсуждается в других главах. Тем не менее, в отношении взаимосвязи патогенеза и диагностики апикального периодонтита в результате десятилетий исследований были получены некоторые известные данные. Клинические симптомы могут быть связаны с присутствием определенных видов бактерий или вирусов, как отмечалось ранее (см. также Главу 4 для более подробного обсуждения микробиологии эндодонтических инфекций). Симптомы также могут быть связаны с присутствием в корневом канале компонентов бактериальной клеточной стенки, таких как липополисахарид или эндотоксин [84, 9].2]. Периапикальная боль, вероятно, также связана с несколькими медиаторами воспаления, которые снижают болевой порог, такими как нейропептиды, брадикинин, лейкотриены и эйкозаноиды [26, 138, 215]. Размер периапикального поражения может быть связан с уровнями резорбтивных цитокинов кости, таких как IL-1бета [112].
также Главу 4 для более подробного обсуждения микробиологии эндодонтических инфекций). Симптомы также могут быть связаны с присутствием в корневом канале компонентов бактериальной клеточной стенки, таких как липополисахарид или эндотоксин [84, 9].2]. Периапикальная боль, вероятно, также связана с несколькими медиаторами воспаления, которые снижают болевой порог, такими как нейропептиды, брадикинин, лейкотриены и эйкозаноиды [26, 138, 215]. Размер периапикального поражения может быть связан с уровнями резорбтивных цитокинов кости, таких как IL-1бета [112].
3.5.3 Модуляция иммунного ответа и резорбции кости при апикальном периодонтите
Периапикальные поражения представляют собой динамический процесс резорбции и отложения кости в сочетании с развитием поражения мягких тканей, которое содержит ряд иммунных и структурных клеток (Рисунок 3.10). Иммунные клетки включают лимфоциты, макрофаги, нейтрофилы, плазматические клетки и тучные клетки. Структурные клетки включают фибробласты и остеобласты. Кроме того, эндотелиальные клетки и остеокласты играют важную роль в прогрессировании воспалительного процесса. Иногда присутствуют эпителиальные клетки, которые могут привести к кистозному образованию, как отмечалось ранее.
Кроме того, эндотелиальные клетки и остеокласты играют важную роль в прогрессировании воспалительного процесса. Иногда присутствуют эпителиальные клетки, которые могут привести к кистозному образованию, как отмечалось ранее.
Рис. 3.10. Взаимодействия между остеобластическими клетками и предшественниками остеокластов во время ремоделирования кости (воспроизведено с разрешения [59]).
Врожденные иммунологические клетки и факторы играют решающую роль в начальном развитии периапикальных поражений. Модели индукции поражения на животных показывают присутствие нейтрофилов в месте апикального отверстия. По-видимому, они играют важную роль в контроле проникновения микробов в очаг поражения (рис. 3.11).
Исследования показали, что подавление нейтрофилов вызывает значительное нарушение образования поражений на животных моделях [147, 231]. У пациентов с нейтропенией может быть спонтанный некроз и образование абсцесса в связи с легким кариесом [159]. Роль адаптивного иммунитета становится очевидной, когда хозяин подвергается воздействию значительной бактериальной нагрузки вирулентных бактерий полости рта. Так, исследования, в которых животные с дефицитом Т- и В-клеток (мыши scid) подвергались воздействию 10 10 клеток/мл Prevotella intermedia, Fusobacterium nucleatum, Peptostreptococcus micros (теперь Parvimonas micra) и Streptococcus intermedius [212] или Treponema denticola [54], у скомпрометированных животных развились сильные опухоли и диссеминированные инфекции.
Роль адаптивного иммунитета становится очевидной, когда хозяин подвергается воздействию значительной бактериальной нагрузки вирулентных бактерий полости рта. Так, исследования, в которых животные с дефицитом Т- и В-клеток (мыши scid) подвергались воздействию 10 10 клеток/мл Prevotella intermedia, Fusobacterium nucleatum, Peptostreptococcus micros (теперь Parvimonas micra) и Streptococcus intermedius [212] или Treponema denticola [54], у скомпрометированных животных развились сильные опухоли и диссеминированные инфекции.
Однако в большинстве случаев бактериальные раздражители не столь серьезны, и иммунологическая реакция способна контролировать их без значительных осложнений. Баланс между различными иммунологическими факторами и наступающими микробными раздражителями определяет точный размер периапикального поражения. В большинстве исследований на животных размер поражения достигает определенного рентгенографического или гистологического уровня в течение 4-6 недель, после чего он остается стабильным до конца эксперимента [10, 55, 60]. Этот баланс поддерживается провоспалительными и противовоспалительными клетками, а также молекулярными медиаторами, которые действуют сообща, титруя результирующий ответ. Это так же важно в случае апикального периодонтита, как и при пульпите и других видах воспаления, ограничивая побочные эффекты воспаления. Этот процесс обеспечивает защитную функцию воспаления и ограничивает его разрушительное действие.
Этот баланс поддерживается провоспалительными и противовоспалительными клетками, а также молекулярными медиаторами, которые действуют сообща, титруя результирующий ответ. Это так же важно в случае апикального периодонтита, как и при пульпите и других видах воспаления, ограничивая побочные эффекты воспаления. Этот процесс обеспечивает защитную функцию воспаления и ограничивает его разрушительное действие.
Рис. 3.11 Индуцированное периапикальное поражение в мышиной модели. ( а ) Некроз пульпы и интенсивная воспалительная реакция в апикальном отверстии и спорадически в очаге поражения (исходное увеличение 100x). (b) Более высокое увеличение прямоугольника на (а), показывающее, что большинство воспалительных клеток представляют собой нейтрофилы (исходное увеличение 400x).
Как отмечалось ранее, активная резорбция кости связана с развитием поражений. Резорбция кости включает кинетику, связанную с ядерным фактором каппа В (NF-kB), который повсеместно экспрессируется в периапикальных поражениях [173]. В частности, активатор рецептора NF-kB (RANK) на остеокластах и их предшественниках взаимодействует с лигандом RANK (RANKL) на остеобластах, вызывая резорбцию кости. RANKL настолько важен для модуляции костной ткани, что инактиватор этой молекулы вызывает остеонекроз в модели животных [3]. В то же время остеопротегрин (ОПГ) действует как приманка, чтобы остановить реакцию RANK/RANKL и сохранить структуру кости (рис. 3.10). Это происходит, когда достигается баланс между наступающими раздражителями и реакцией хозяина за счет ограничения резорбции кости, что приводит к стабильному размеру поражения. Прекращение дальнейшего развития поражения за пределами необходимой степени может быть организовано клетками T-reg [66] и различными цитокинами, гормонами и другими факторами (рис. 3.10).
В частности, активатор рецептора NF-kB (RANK) на остеокластах и их предшественниках взаимодействует с лигандом RANK (RANKL) на остеобластах, вызывая резорбцию кости. RANKL настолько важен для модуляции костной ткани, что инактиватор этой молекулы вызывает остеонекроз в модели животных [3]. В то же время остеопротегрин (ОПГ) действует как приманка, чтобы остановить реакцию RANK/RANKL и сохранить структуру кости (рис. 3.10). Это происходит, когда достигается баланс между наступающими раздражителями и реакцией хозяина за счет ограничения резорбции кости, что приводит к стабильному размеру поражения. Прекращение дальнейшего развития поражения за пределами необходимой степени может быть организовано клетками T-reg [66] и различными цитокинами, гормонами и другими факторами (рис. 3.10).
Из этого аргумента следует, что потенциально можно исследовать периапикальное поражение (через корневой канал некротизированной пульпы или непосредственно) на наличие факторов, которые могут указывать на то, активно ли развивается, стабильно или заживает поражение. Сообщается о предварительных работах в этой области. В одном исследовании активные и неактивные поражения были произвольно основаны на соотношении RANKL/OPG в пять раз или выше [69]. Это коррелировало с экспрессией генов из массива из 84 генов заживления ран для 83 гранулем и 25 контрольных образцов периодонтальной связки. Было показано, что активные поражения были связаны с повышенной регуляцией TNF (провоспалительный цитокин) и CXCL11 (хемокин), тогда как неактивные поражения имели повышенную регуляцию SERPINE 1 (фермент ремоделирования), TIMP1 (фермент ремоделирования), COL1A1 (внеклеточный матрикс). компонент), TGF-бета1 (фактор роста) и ITGA4 (молекула клеточной адгезии) [69]. В другом исследовании определение активных и неактивных поражений основывалось на диагнозе хронического апикального абсцесса для активных поражений или бессимптомного (хронического) апикального периодонтита для неактивных поражений [119]. Повреждения анализировали на матриксные металлопротеиназы или их инактиваторы.
Сообщается о предварительных работах в этой области. В одном исследовании активные и неактивные поражения были произвольно основаны на соотношении RANKL/OPG в пять раз или выше [69]. Это коррелировало с экспрессией генов из массива из 84 генов заживления ран для 83 гранулем и 25 контрольных образцов периодонтальной связки. Было показано, что активные поражения были связаны с повышенной регуляцией TNF (провоспалительный цитокин) и CXCL11 (хемокин), тогда как неактивные поражения имели повышенную регуляцию SERPINE 1 (фермент ремоделирования), TIMP1 (фермент ремоделирования), COL1A1 (внеклеточный матрикс). компонент), TGF-бета1 (фактор роста) и ITGA4 (молекула клеточной адгезии) [69]. В другом исследовании определение активных и неактивных поражений основывалось на диагнозе хронического апикального абсцесса для активных поражений или бессимптомного (хронического) апикального периодонтита для неактивных поражений [119]. Повреждения анализировали на матриксные металлопротеиназы или их инактиваторы. Было обнаружено, что активные поражения активируют MMP-2, MMP-7 и MMP-9, тогда как неактивные поражения активируют TIMP-1 [119].
Было обнаружено, что активные поражения активируют MMP-2, MMP-7 и MMP-9, тогда как неактивные поражения активируют TIMP-1 [119].
3.5.4 Заживление апикального периодонтита
После устранения микробных раздражителей путем удаления зуба или их значительного уменьшения путем нехирургического или хирургического эндодонтического лечения наступает периапикальное заживление. Заживление происходит за счет увеличения васкуляризации, образования коллагена, развития костных островков, которые в конечном итоге сливаются, и отложения клеточного цемента (рис. 3.12) [65]. Периапикальное поражение содержит множество факторов роста, необходимых для заживления и минерализации раны. К ним относятся трансформирующие факторы роста (TGF-альфа и TGF-бета) [69]., 216], эпидермальный фактор роста [124], факторы роста эндотелия сосудов [53, 118] и костный морфогенетический белок-2 (BMP-2) [135].
Несколько факторов, связанных с хозяином, могут влиять на скорость заживления периапикальных поражений. Например, в когортных исследованиях было показано, что сахарный диабет [7, 63] и курение [43] связаны с уменьшением периапикального заживления. Изучение роли системных факторов в заживлении периапикальных поражений затруднено тем фактом, что многие пациенты принимают лекарства, которые могут изменить кинетику кости в очаге поражения. Например, было показано, что метформин, который обычно используется для лечения диабета 2 типа [127], бисфосфонаты, которые используются, в частности, при остеопорозе [9].9] и статины [122, 125], которые используются многими пожилыми пациентами, уменьшают размер индуцированных периапикальных поражений в моделях на животных.
Например, в когортных исследованиях было показано, что сахарный диабет [7, 63] и курение [43] связаны с уменьшением периапикального заживления. Изучение роли системных факторов в заживлении периапикальных поражений затруднено тем фактом, что многие пациенты принимают лекарства, которые могут изменить кинетику кости в очаге поражения. Например, было показано, что метформин, который обычно используется для лечения диабета 2 типа [127], бисфосфонаты, которые используются, в частности, при остеопорозе [9].9] и статины [122, 125], которые используются многими пожилыми пациентами, уменьшают размер индуцированных периапикальных поражений в моделях на животных.
Рис. 3.12. Заживление через четыре месяца после нехирургического эндодонтического лечения клыка с индуцированным периапикальным поражением у хорька. Элементы заживления включают кость (B), сосудистую пролиферацию (V) и клеточный цемент (CC). (Воспроизведено с разрешения [65].)
Генетический полиморфизм аллеля IL-1beta2 [141] или некоторых Fc-гамма-рецепторов [193, 194] может быть связано с замедлением заживления апикального периодонтита. Fc-гамма-рецепторы расположены на многих воспалительных клетках, особенно на макрофагах, и связывают Fc-фрагмент иммуноглобулина для облегчения фагоцитоза антигенов, присоединенных к Fab-фрагменту антитела. Однако на данном этапе преждевременно обвинять генетический полиморфизм в снижении заживления, поскольку некоторые результаты не подтверждаются другими исследованиями [6].
Fc-гамма-рецепторы расположены на многих воспалительных клетках, особенно на макрофагах, и связывают Fc-фрагмент иммуноглобулина для облегчения фагоцитоза антигенов, присоединенных к Fab-фрагменту антитела. Однако на данном этапе преждевременно обвинять генетический полиморфизм в снижении заживления, поскольку некоторые результаты не подтверждаются другими исследованиями [6].
3.6 Заключительные замечания
В настоящее время считается, что вялотекущее воспаление пульпы способствует регенерации тканей, т. е. третичному дентиногенезу, в то время как более интенсивное и тяжелое воспаление приводит к некрозу [31, 9].1]. В связи с этим механизмы чрезмерного обызвествления пульпы, например, после травмы и сильно восстановленного зубного ряда, до конца не изучены. Терапия, предназначенная для уменьшения воспалительной реакции пульпы, может помочь сохранить жизнеспособность пульпы, эффективной иммунокомпетентной ткани. В собачьей модели пульпита лечение ММП-3 снижало экспрессию провоспалительного цитокина ИЛ-6 и уменьшало количество макрофагов и антигенпрезентирующих клеток [46]. Таким образом, обращая вспять индуцированное воспаление пульпы. Улучшение понимания молекулярных сетей, которые способствуют регенерации тканей и поддержанию здоровой жизненной пульпы, может принести значительную пользу стоматологическим пациентам и улучшить здоровье полости рта.
Таким образом, обращая вспять индуцированное воспаление пульпы. Улучшение понимания молекулярных сетей, которые способствуют регенерации тканей и поддержанию здоровой жизненной пульпы, может принести значительную пользу стоматологическим пациентам и улучшить здоровье полости рта.
Заживление апикального периодонтита при нехирургическом и хирургическом эндодонтическом лечении обычно происходит медленнее, чем после удаления зуба. Считается, что это может быть связано с более эффективной элиминацией микробных факторов при экстракции. Однако эта задержка заживления при эндодонтических процедурах влияет на способность практикующего врача следить за лечением и проводить дополнительное лечение, когда оно показано. В будущем может стать возможным улучшить периапикальное заживление после эндодонтического лечения путем применения коммерчески доступных факторов роста, таких как Emdogain, или других белков, чтобы прогноз можно было определить через более короткий период времени. Кроме того, оценка уровня активности периапикальных поражений, как отмечалось ранее, может помочь в планировании лечения и прогнозировании развития симптомов. Окончательное понимание патогенеза и заживления пульпы и периапикальных тканей будет включать лучшее понимание эндодонтического микробиома, а также геномных, эпигенетических и медицинских соображений пациента.
Окончательное понимание патогенеза и заживления пульпы и периапикальных тканей будет включать лучшее понимание эндодонтического микробиома, а также геномных, эпигенетических и медицинских соображений пациента.
Ссылки
1 Abella, F. et al. (2012) Оценка периапикального состояния зубов с необратимым пульпитом с помощью конусно-лучевой компьютерной томографии и периапикальных рентгенограмм. J Endod 38: 1588-1591.
2 Адачи, Т. и др. (2007)Связанные с кариесом бактерии и цитокины индуцируют CXCL10 в пульпе зуба. J Dent Res 86: 1217-1222.
3 Агалу, Т.Л. и другие. (2014) Ингибиторы RANKL вызывают остеонекроз челюсти у мышей с периапикальным заболеванием. J Bone Miner Res 29: 843-854.
4 Айнамо, А. и др. (1994) Рентгенологические данные зубов у пожилых людей в Хельсинки, Финляндия. Acta Odontol Scand 52: 243-249.
5 Алларедди, В. и др. (2010) Исходы у пациентов, госпитализированных по поводу периапикального абсцесса в Соединенных Штатах: анализ с использованием общенациональной стационарной выборки. J Am Dent Assoc 141: 1107-1116.
J Am Dent Assoc 141: 1107-1116.
6 Aminoshariae, A. и Kulild, J.C. (2015) Ассоциация полиморфизма функциональных генов с апикальным периодонтитом. Дж Эндод 41:999-1007.
7 Арья, С. и др. (2017) Заживление апикального периодонтита после консервативного лечения у пациентов с сахарным диабетом 2 типа. J Endod 43: 1623-1627.
8 Асгари, С., Эгбал, М.Дж., и Годдуси, Дж. (2014) Двухлетние результаты лечения витальной пульпы постоянных моляров с необратимым пульпитом: продолжающееся многоцентровое рандомизированное клиническое исследование. Клинические устные исследования 18: 635-641.
9 Балто, К., Сасаки, Х., и Сташенко, П. (2001) Дефицит интерлейкина-6 увеличивает воспалительное разрушение кости. Заразить иммунитет 69: 744-750.
10 Балто, К. и др. (2002)Мышиная модель воспалительной резорбции корня, вызванной инфекцией пульпы. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 93: 461-468.
11 Baumgartner, J.C. et al. (2004)Географические различия в бактериях, обнаруженных при эндодонтических инфекциях с помощью полимеразной цепной реакции. Журнал эндодонтии 30: 141-144.
Журнал эндодонтии 30: 141-144.
12 Bergenholtz, G. (1974) Микроорганизмы из некротизированной пульпы травмированных зубов. Одонтол Реви 25: 347-358.
13 Bergenholtz, G. and Lindhe, J. (1978) Влияние экспериментально индуцированного маргинального периодонтита и пародонтального скейлинга на пульпу зуба. J Clin Periodontol 5(1): 59-73.
14 Bergenholtz, G. et al. (1983) Морфометрический анализ хронических воспалительных периапикальных поражений зубов с пломбированными корнями. Oral Surg Oral Med Oral Pathol 55: 295-301.
15 Бергстрем Дж., Элиассон С. и Альберг К.Ф. (1987) Периапикальный статус у субъектов с регулярными привычками ухода за зубами. Community Dent Oral Epidemiol 15: 236-239.
16 Бхаскар С.Н. (1966) Периапикальные поражения — типы, заболеваемость и клинические признаки. Oral Surg Oral Med Oral Pathol 21: 657-671.
17 Бхингаре, А. К. и др. (2014) Дендритные клетки пульпы зуба мигрируют в регионарные лимфатические узлы. Журнал стоматологических исследований 93: 288-293.
Блок 18, Р.М. и другие. (1976)Гистопатологическое, гистобактериологическое и радиографическое исследование периапикальных эндодонтических хирургических образцов. Оральная хирургия, оральная медицина, оральная патология, оральная радиология 42: 656-678.
19 Boucher, Y. et al. (2002) Рентгенологическая оценка распространенности и технического качества лечения корневых каналов во французской субпопуляции. Int Endod J 35: 229-238.
20 Браннстром М. и Линд П.О. (1965) Реакция пульпы на ранний кариес зубов. J Dent Res 44: 1045-1050.
21 Кампос, К. и др. (2013) Характер метилирования IFNG в периапикальных гранулемах и корешковых кистах. J Endod 39: 493-496.
22 Каплан, Д.Дж. и другие. (2006)Поражения эндодонтического происхождения и риск ишемической болезни сердца. Джей Дент Рез 85: 996-1000.
23 Кардосо, Ф.Г. и другие. (2015) Корреляция между объемом апикального периодонтита, определенным с помощью анализа конусно-лучевой компьютерной томографии, и уровнями эндотоксина, обнаруженными при первичной инфекции корневых каналов. J Endod 41: 1015-1019.
J Endod 41: 1015-1019.
24 Кардосо, Ф.П. и другие. (2014) Характер метилирования генов CD14 и TLR2 в пульпе зубов человека. Журнал эндодонтии 40: 384-386.
25 Кардосо, Ф.П. и другие. (2010) Характер метилирования гена IFN-gamma в пульпе зуба человека. Журнал эндодонтии 36: 642-646.
26 Caviedes-Bucheli, J. et al. (2008) Нейропептиды в пульпе зуба: молчаливые главные герои. J Endod 34: 773-788.
27 Чавес де Пас Вильянуэва, Л.Е. (2002)Fusobacterium nucleatum при эндодонтических обострениях. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 93: 179-183.
28 Ченг, Г. С. и Хо, М. В. (2001) Микробная флора зубов после лечения корневых каналов, связанная с бессимптомными периапикальными
рентгенопрозрачными поражениями. Оральная микробиология и иммунология 16: 332-337.
29 Чхур, К.Л. и другие. (2005)Молекулярный анализ микробного разнообразия при прогрессирующем кариесе. Журнал клинической микробиологии 43: 843-849.
30 Купер, П.Р. , Холдер, М.Дж., и Смит, А.Дж. (2014)Воспаление и регенерация в пульпо-дентинном комплексе: палка о двух концах. J Endod 40: S46-51.
, Холдер, М.Дж., и Смит, А.Дж. (2014)Воспаление и регенерация в пульпо-дентинном комплексе: палка о двух концах. J Endod 40: S46-51.
31 Cooper, P.R., et al. (2011) Медиаторы воспаления и регенерации. Adv Dent Res 23: 290-295.
32 Cooper, P.R., et al. (2010)Взаимодействие воспаления и регенерации в комплексе пульпа-дентин. Журнал стоматологии 38: 687-697.
33 да Силва Р.А. и другие. (2012) Мыши с нокаутом Toll-подобного рецептора 2 показали увеличенный размер периапикального поражения и количество остеокластов. J Endod 38: 803-813.
34 Dahlén, G., Magnusson, B.C., и Moller, A. (1981) Гистологическое и гистохимическое исследование влияния липополисахарида, экстрагированного из Fusobacterium nucleatum, на периапикальные ткани у обезьяны Macaca fascicularis. Arch Oral Biol 26: 591-598.
35 Де Клин, М.Дж. и др. (1993) Периапикальный статус и распространенность эндодонтического лечения у взрослого голландского населения. Международный Эндод J 26: 112-119.
36 де Оливейра Родини, К., Батиста, А.С., и Лара, В.С. (2004) Сравнительное иммуногистохимическое исследование присутствия тучных клеток в апикальных гранулемах и периапикальных кистах: возможная роль тучных клеток в развитии периапикальных поражений человека. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 97: 59-63.
37 де Оливейра Родини, К. и Лара, В.С. (2001) Изучение экспрессии макрофагов CD68+ и Т-клеток CD8+ в гранулемах человека и периапикальных кистах. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 92: 221-227.
38 De Rossi, A., Rocha, L.B., and Rossi, M.A. (2008) Интерферон-гамма, интерлейкин-10, молекула межклеточной адгезии-1 и хемокиновый рецептор 5, но не интерлейкин-4, ослабляют развитие периапикальной поражения. J Endod 34: 31-38.
39 de Soet, J.J. и другие. (1995) Сравнение микробной флоры в кариозном дентине клинически выявляемых и невыявляемых окклюзионных поражений. Исследование кариеса 29: 46-49.
40 Диоген А. и др. (2011) LPS сенсибилизирует TRPV1 посредством активации TLR4 в сенсорных нейронах тройничного нерва. Журнал стоматологических исследований 90: 759-764.
Журнал стоматологических исследований 90: 759-764.
41 Dommisch, H. et al. (2005)Экспрессия бета-дефензина человека (hBD-1,-2) в пульпе зуба. Оральная микробиология и иммунология 20: 163-166.
42 Dommisch, H. et al. (2007) Иммунорегуляторные функции бета-дефензина-2 человека в одонтобластоподобных клетках. Int Endod J 40: 300-307.
43 Дойл, С.Л. и другие. (2007) Факторы, влияющие на результаты одиночных имплантатов и эндодонтических реставраций. J Endod 33: 399-402.
44 Дюран, С.Х. и другие. (2006) Липотейхоевая кислота увеличивает экспрессию TLR и функциональных хемокинов, одновременно снижая образование дентина в дифференцированных in vitro одонтобластах человека. J Immunol 176: 2880-2887.
45 Двайер, Т.Г. и Torabinejad, M. (1980) Рентгенологическая и гистологическая оценка действия эндотоксина на периапикальные ткани кошки. J Endod 7: 31-35.
46 Эба, Х. и др. (2012) Противовоспалительное действие матриксной металлопротеиназы-3 на необратимый пульпит зрелых прорезавшихся зубов. PLoS One 7: e52523.
PLoS One 7: e52523.
47 Иган, М. В. и др. (2002) Преобладание дрожжей в слюне и корневых каналах зубов, связанных с апикальным периодонтитом. Международный эндодонтический журнал 35: 321-329.
48 Эгбал М.Дж. и др. (2009)Пульпотомия MTA постоянных моляров человека с необратимым пульпитом. Австралийский эндодонтический журнал 35: 4-8.
49 Эль Салхи М., Азизи Ф. и Рагхупати Р. (2013) Цитокины как диагностические маркеры воспаления пульпы. Международный эндодонтический журнал 46: 573-580.
50 Фабрициус, Л. и др. (1982) Влияние комбинаций ротовых бактерий на периапикальные ткани обезьян. Скандинавский журнал стоматологических исследований 90: 200-206.
51 Farges, J.C. et al. (2015) Механизмы защиты и восстановления пульпы зуба при кариесе. Mediators Inflamm 2015: 230251.
52 Ferraz, C.C.R. и другие. (2011)Липополисахарид из porphyromonas gingivalis повышает чувствительность ноцицепторов, чувствительных к капсаицину. Журнал эндодонтии 37: 45-48.
53 Фонсека-Сильва, Т. и др. (2012)Обнаружение и количественная оценка тучных клеток, фактора роста эндотелия сосудов и плотности микрососудов в воспалительных периапикальных кистах и гранулемах человека. Международный Эндод J45: 859-864.
54 Фоски, Ф. и др. (2006)Treponema denticola при распространении эндодонтических инфекций. J Dent Res 85: 761-765.
55 Fouad, A.F. (1997) Экспрессия IL-1 альфа и TNF-альфа в ранних периапикальных поражениях у нормальных и иммунодефицитных мышей. Дж. Дент Рез. 76: 1548–1554.
56 Фуад А.Ф. (2012) Молекулярные медиаторы воспаления пульпы. В: Seltzer and Bender’s Dental Pulp, 2e. (изд. К. М. Харгривз и Х. Э. Гудис), 241–276. Чикаго, Иллинойс: Quintessence Publishing Co., Inc.
57 Фуад А.Ф. (2016) Инфекции пульпы зуба. В: Инфекции головы/шеи/орофациальных инфекций: мультидисциплинарный подход (под редакцией Дж. Р. Ф. Хаппа и Э. М. Фернейна), 175–188. Сент-Луис, Миссури: Elsevier.
58 Фуад, А.Ф. (2016) Treponema spp. Показано, что они являются важными возбудителями первичных эндодонтических инфекций. JEvid Dent Pract 16: 50-52.
Показано, что они являются важными возбудителями первичных эндодонтических инфекций. JEvid Dent Pract 16: 50-52.
59 Фуад, А.Ф. (2017) Эндодонтическая микробиология и патобиология: современное состояние знаний. Стоматологические клиники Северной Америки 61: 1-15.
60 Фуад, А.Ф. и Акоста, А.В. (2001)Прогрессирование периапикального поражения и экспрессия цитокинов в модели с гипочувствительностью к ЛПС. Int Endod J 34: 506-513.
61 Фуад А.Ф. и др. (2002) Идентификация бактерий, связанных с эндодонтической инфекцией, на основе ПЦР. J Clin Microbiol 40: 3223-3231.
62 Фуад А.Ф. и др. (2002) Прогрессирование периапикального поражения с контролируемой микробной инокуляцией на модели мыши с диабетом I типа. J Endod 28: 8-16.
63 Фуад, А.Ф. и Бурлесон, Дж. (2003) Влияние сахарного диабета на исход эндодонтического лечения: данные из электронной карты пациента. J Am Dent Assoc 134: 43-51; викторина 117-118.
64 Фуад А.Ф., Уолтон Р.Е. и Риттман Б. Р. (1992)Индуцированные периапикальные поражения клыков хорьков: гистологическая и рентгенологическая оценка. Endod Dent Traumatol 8: 56-62.
Р. (1992)Индуцированные периапикальные поражения клыков хорьков: гистологическая и рентгенологическая оценка. Endod Dent Traumatol 8: 56-62.
65 Фуад А.Ф., Уолтон Р.Э. и Риттман Б.Р. (1993) Заживление индуцированных периапикальных поражений у клыков хорьков. J Endod 19: 123-129.
66 Франсискони, К.Ф. и другие. (2016) Характеристика защитной роли регуляторных Т-клеток в развитии экспериментальных периапикальных поражений и их химиоаттракция в качестве терапевтического инструмента. J Endod 42: 120-126.
67 Галисия, Дж. К. и др. (2016) Профиль экспрессии генов пульпита. Гены и иммунитет 17: 239-243.
68 Галисия, Дж. К. и др. (2014)МиРНК-181a регулирует индуцированный агонистом Toll-подобного рецептора воспалительный ответ в фибробластах человека. Гены Иммун 15: 333-337.
69 Гарлет, Г.П. и другие. (2012)Анализ экспрессии генов заживления ран в периапикальных гранулемах человека прогрессирующего и стабильного характера. J Endod 38: 185-190.
70 Гарлет, Т. П. и другие. (2010) Дефицит CCR2 приводит к усилению остеолиза при экспериментальных периапикальных поражениях у мышей. J Endod 36: 244-250.
П. и другие. (2010) Дефицит CCR2 приводит к усилению остеолиза при экспериментальных периапикальных поражениях у мышей. J Endod 36: 244-250.
71 Gaudin, A. et al. (2015)Фенотипический анализ иммунокомпетентных клеток в пульпе здорового человека. Журнал эндодонтии 41: 621-627.
72 Жиль, Ж.А. и другие. (1997) У крыс после овариэктомии повышена потеря костной ткани полости рта. J Endod 23: 419-422.
73 Голдман М., Лаосонторн П. и Уайт Р. Р. (1992) Микроподтекание – целые коронки и пульпа зуба. Журнал эндодонтии 18: 473-475.
74 Gomes-Filho, J.E. et al. (2015)Ралоксифен модулирует регуляторы остеокластогенеза и ангиогенеза в модели периапикального поражения с дефицитом эстрогена. Инт Эндод J 48: 1059-1068.
75 Гомес, Б.П., Друкер, Д.Б., и Лилли, Дж.Д. (1994) Ассоциации определенных бактерий с некоторыми эндодонтическими признаками и симптомами. Int Endod J 27: 291-298.
76 Гун В.В. и Якобсен, П.Л. (1988)Продромальная одонталгия и множественные омертвевшие зубы, вызванные инфекцией опоясывающего герпеса тройничного нерва: отчет о случае. J Am Dent Assoc 116: 500-504.
J Am Dent Assoc 116: 500-504.
77 Гриффи, М.Б. и другие. (1980) Связь Bacteroides melaninogenicus с симптомами, связанными с некрозом пульпы. Oral Surg Oral Med Oral Pathol 50: 457-461.
78 Guo, J. et al. (2013) Оценка надежности и точности использования конусно-лучевой компьютерной томографии для диагностики периапикальных кист из гранулем. J Endod 39: 1485-1490.
79 Hahn, C.L., Falkler, W.A., and Siegel, M.A. (1989) Исследование Т-клеток и В-клеток при патологии пульпы. Журнал эндодонтии 15: 20-26.
80 Хан, К.Л. и Ливер, Ф.Р. (2007)Обновленная информация об адаптивных иммунных реакциях пульпы зуба. Журнал эндодонтии 33: 773-781.
81 Harran Ponce, E. et al. (2002) Последствия переломов коронки с обнажением пульпы: гистопатологическая оценка у собак. Стоматологическая травматология: официальное издание Международной ассоциации стоматологической травматологии 18:196-205.
82 Hernandez Vigueras, S. et al. (2016) Вирусы в пульпе и периапикальное воспаление: обзор. Одонтология 104: 184-191.
Одонтология 104: 184-191.
83 Хирао, К. и др. (2009)Роли TLR2, TLR4, NOd2 и NOd1 в фибробластах пульпы. Журнал стоматологических исследований 88: 762-767.
84 Horiba, N. et al. (1991) Корреляция между эндотоксином и клиническими симптомами или рентгенопрозрачными областями в инфицированных корневых каналах. Oral Surg Oral Med Oral Pathol 71: 492-495.
85 Хоу, Л., Сасаки, Х., и Сташенко, П. (2000) У мышей с дефицитом Toll-подобного рецептора 4 снижается разрушение костей после смешанной анаэробной инфекции. Infect Immun 68: 4681-4687.
86 Хоу Л., Сасаки Х. и Сташенко П. (2000) Дефицит В-клеток предрасполагает мышей к распространению анаэробных инфекций: защита путем пассивного переноса антител. Infect Immun 68: 5645-5651.
87 Сяо, В.В. и другие. (2012)Микробная трансформация нормальной микробиоты полости рта в острые эндодонтические инфекции. BMC Genomics 13: 345.
88 Huang, G.T. и другие. (2001)Влияние дефицита интерлейкина-6 на формирование периапикальных поражений после воздействия на пульпу у мышей. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 92: 83-88.
Oral Surg Oral Med Oral Pathol Oral Radiol Endod 92: 83-88.
89 Хуэй, Т.К. и другие. (2014) ЭЖ3, Потенциальный регулятор воспаления и регенерации пульпы зуба. Журнал эндодонтии 40: 1132-1138.
90 Изуми Т. и др. (1996) Иммуногистохимическое исследование HLA-DR и альфа-1-антихимотрипсин-позитивных клеток в пульпе некариозных и кариозных зубов человека. Архив устной биологии 41: 627-630.
91 Изуми Т. и др. (1995) Иммуногистохимическое исследование иммунокомпетентных клеток пульпы некариозных и кариозных зубов человека. Архив биологии полости рта 40: 609-614.
92 Хасинто, Р.К. и другие. (2005)Количественная оценка эндотоксинов в некротизированных корневых каналах зубов с симптомами и без симптомов. J Med Microbiol 54: 777-783.
93 Яковлевич А. и Андрич М. (2014) Цитомегаловирус человека и вирус Эпштейна-Барр в этиопатогенезе апикального периодонтита: систематический обзор. J Endod 40: 6-15.
94 Яковлевич А. и др. (2017) Роль вируса ветряной оспы в развитии периапикальных патологий и резорбции корней: систематический обзор. J Endod 43: 1230-1236.
J Endod 43: 1230-1236.
95 Цзян Х.В. и другие. (2006) Экспрессия Toll-подобного рецептора 4 в нормальных одонтобластах человека и ткани пульпы зуба. J Endod 32: 747-751.
96 Jontell, M. et al. (1998)Иммунные защитные механизмы пульпы зуба. Crit Rev Oral Biol Med 9: 179-200.
97 Кабак Ю. и Эбботт П.В. (2005) Распространенность апикального периодонтита и качество эндодонтического лечения у взрослого населения Беларуси. Int Endod J 38: 238-245.
98 Какехаши С., Стэнли Х.Р. и Фитцджеральд Р.Дж. (1965) Эффекты хирургического обнажения пульпы зуба у безмикробных и обычных лабораторных крыс. Оральная хирургия, оральная медицина, оральная патология, оральная радиология 20: 340-349.
99 Канг Б. и др. (2013) Периапикальное заболевание и бисфосфонаты вызывают остеонекроз челюстей у мышей. J Bone Miner Res 28: 1631-1640.
100 Кавасима, Н. и др. (1999) Стимулированное инфекцией инфраоссальное воспаление и деструкция кости усиливаются у мышей с нокаутом P-/E-селектина. Иммунология 97: 117-123.
Иммунология 97: 117-123.
101 Кавасима, Н. и др. (2006) NK- и NKT-клетки в тканях пульпы зуба крысы. Оральная хирургия Оральная медицина Оральная патология Оральная радиология и эндодонтия 102: 558-563.
102 Келлер, Дж. Ф. и др. (2010) Активация Toll-подобного рецептора 2 липотейхоевой кислотой индуцирует дифференцированную продукцию провоспалительных цитокинов в одонтобластах человека, фибробластах пульпы зуба и незрелых дендритных клетках. Иммунобиология 215: 53-59.
103 Келлер, Дж. Ф. и др. (2011) Экспрессия NOD2 повышена в воспаленной пульпе зуба человека и стимулированных липотейхоевой кислотой одонтобластоподобных клетках. Врожденный иммунитет 17:29-34.
104 Хаббаз М.Г., Анастасиадис П.Л. и Сикарас С.Н. (2000) Определение эндотоксинов при кариесе: связь с болью в пульпе. Int Endod J 33: 132-137.
105 Хаят Б.Г. и другие. (1988) Реакции нервных волокон на воспаление пульпы и периапикальные поражения моляров крыс, продемонстрированные с помощью иммуноцитохимии пептидов, связанных с геном кальцитонина. Журнал эндодонтии 14: 577-587.
Журнал эндодонтии 14: 577-587.
106 Kianush, N. et al. (2014) Бактериальный профиль кариеса дентина и влияние рН на разнообразие бактериальной популяции. ПлоС один 9: e
107 Кикучи Т. и др. (2004) Дендритные клетки, стимулированные Actinobacillus actinomycetemcomitans, вызывают быстрый ответ гамма-интерферона естественными клетками-киллерами. Инфекция и иммунитет 72: 5089-5096.
108 Кимберли, К.Л. и Byers, M.R. (1988) Воспаление молярной пульпы и пародонта крысы вызывает увеличение пептида, связанного с геном кальцитонина, и разрастание аксонов. Анатомическая запись 222: 289-300.
109 Киркеванг Л.Л. и др. (2001) Частота и распространение эндодонтически пролеченных зубов и апикального периодонтита среди городского населения Дании. Инт Эндод Дж 34: 198-205.
110 Койвисто, Т., Боулз, В.Р., и Рорер, М. (2012) Частота и распределение рентгенопрозрачных поражений челюсти: ретроспективный анализ 9723 случаев. J Endod 38: 729-732.
111 Коркмаз Ю. и др. (2011) Необратимое воспаление связано со снижением уровней альфа(1)-, бета(1)- и альфа(2)-субъединиц рГЦ в одонтобластах человека. Журнал стоматологических исследований 90: 517-522.
и др. (2011) Необратимое воспаление связано со снижением уровней альфа(1)-, бета(1)- и альфа(2)-субъединиц рГЦ в одонтобластах человека. Журнал стоматологических исследований 90: 517-522.
112 Куо, М.Л., Ламстер, И.Б., и Хассельгрен, Г. (1998) Хост-медиаторы в эндодонтических экссудатах. I. Показатели воспаления и гуморального иммунитета. Дж Эндод 24:598-603.
113 Лалонд, Э. Р. и Любке, Р. Г. (1968) Частота и распространение периапикальных кист и гранулем. Оценка 800 образцов. Oral Surg Oral Med Oral Pathol 25: 861-868.
114 Лангеланд, К. (1987) Реакция тканей на кариес. Endod Dent Traumatol 3: 149-171.
115 Лангеланд, К., Родригес, Х., и Дауден, В. (1974) Пародонтоз, бактерии и гистопатология пульпы. Оральная хирургия, оральная медицина, оральная патология, оральная радиология 37: 257-270.
116 Лоутон, Ф.Е. и Майерс, Г.Е. (1947) Контроль теплоты трения при подготовке полости. Британский стоматологический журнал 83: 75-77.
117 Лейте, Ф.Р. и другие. (2015)Распространенность видов трепонем, обнаруженных при эндодонтических инфекциях: систематический обзор и метарегрессионный анализ. J Endod 41: 579-587.
и другие. (2015)Распространенность видов трепонем, обнаруженных при эндодонтических инфекциях: систематический обзор и метарегрессионный анализ. J Endod 41: 579-587.
118 Leonardi, R. et al. (2003)Обнаружение фактора роста эндотелия сосудов/фактора проницаемости сосудов в периапикальных поражениях. J Endod 29: 180-183.
119Летра, А. и др. (2013) MMP-7 и TIMP-1, новые цели в прогнозировании плохого заживления ран при апикальном периодонтите. J Endod 39: 1141-1146.
120 Li, H. et al. (2009)Вирусы герпеса при эндодонтических патологиях: ассоциация вируса Эпштейна-Барр с необратимым пульпитом и апикальным периодонтитом. Журнал эндодонтии 35: 23-29.
121 Ли, Л. и др. (2010)Анализ эндодонтических инфекций с помощью пиросеквенирования с глубоким покрытием. J Dent Res 89: 980-984.
122 Лин Л.Д. и другие. (2013)Симвастатин подавляет экспрессию Cyr61 в остеобластах и прогрессирование апикального периодонтита за счет усиления транскрипционного фактора Forkhead/winged helix box белок O3a. Дж Эндод 39: 619-625.
Дж Эндод 39: 619-625.
123 Лин Л.М., Хуанг Г.Т. и Розенберг П.А. (2007)Пролиферация остатков эпителиальных клеток, образование апикальных кист и регресс апикальных кист после заживления периапикальной раны. J Endod 33: 908-916.
124 Лин, Л. М. и др. (1996)Обнаружение рецептора эпидермального фактора роста в воспалительных периапикальных поражениях. Int Endod J 29: 179-184.
125 Лин С.К. и другие. (2009)Симвастатин как новая стратегия для облегчения периапикальных поражений. J Endod 35: 657-662.
126 Лин З.М. и другие. (2009)Экспрессия нуклеотид-связывающего домена олигомеризации 2 в нормальных клетках зубной пульпы человека и тканях зубной пульпы. Журнал эндодонтии 35: 838-842.
127 Лю Л. и др. (2012) Защитное действие метформина на периапикальные поражения у крыс за счет снижения соотношения активатор рецептора лиганда ядерного фактора каппа В/остеопротегерин. J Endod 38: 943-947.
128 Loesche, WJ (1986) Роль Streptococcus mutans в развитии кариеса у человека. Микробиологические обзоры 50: 353-380.
Микробиологические обзоры 50: 353-380.
129 Магазачи А.А. (2005) Компартментализация естественных клеток-киллеров человека. Молекулярная иммунология 42: 523-529.
130 Maita, E. et al. (1991) Поток жидкости и белка через пульподентинный комплекс собаки in vivo. Arch Oral Biol 36: 103-110.
131 Мангкорнкарн, К. и др. (1991)Проточный цитометрический анализ тканей пульпы зубов человека. Журнал эндодонтии 17: 49-53.
132 Marcal, J.R. et al. (2010) Т-хелперные клетки типа 17 / регуляторный Т-клеточный иммунорегуляторный баланс в корешковых кистах и периапикальных гранулемах человека. Дж Эндод 36:995-999.
133 Martin, F.E. et al. (2002)Количественное микробиологическое исследование кариозного дентина человека с помощью посева и ПЦР в реальном времени: связь анаэробов с гистопатологическими изменениями при хроническом пульпите. Журнал клинической микробиологии 40: 1698-1704.
134 Мартиньо, Ф.К. и другие. (2014)Клиническое исследование видов бактерий и эндотоксинов при эндодонтической инфекции и оценка активности содержимого корневого канала в отношении макрофагов по продукции цитокинов. Clin Oral Investig.
Clin Oral Investig.
135 Мацумото Н. и др. (2014) Гистологическая оценка воздействия геля Эмдогейн на поврежденную верхушку корня у крыс. Дж Эндод 40: 1989-1994.
136 Мэтьюз Б. и Вонгсаван Н. (1994) Взаимодействие нервных и гидродинамических механизмов в дентине и пульпе. Arch Oral Biol 39 Приложение: 87s-95s.
137 Мазур, Б. и Масслер, М. (1964) Влияние заболеваний пародонта на пульпу зуба. Оральная хирургия, оральная медицина и оральная патология 17: 592-603.
138 McNicholas, S. et al. (1991) Концентрация простагландина Е2 в перирадикулярных поражениях человека. J Endod 17: 97-100.
139 Майклсон, П.Л. и Холланд, Г.Р. (2002) Является ли пульпит болезненным? Int Endod J 35: 829-832.
140 Мьор И.А. и Tronstad, L. (1972) Экспериментально индуцированный пульпит. Oral Surg Oral Med Oral Pathol 34: 102-108.
141 Морсани, Дж. М. и др. (2011)Генетическая предрасположенность к стойкому апикальному периодонтиту. J Endod 37: 455-459.
142 Мортенсен Х. , Винтер Дж. Э. и Бирн Х. (1970) Периапикальные гранулемы и кисты. Расследование 1600 дел. Скандинавский журнал стоматологических исследований 78: 241-250.
, Винтер Дж. Э. и Бирн Х. (1970) Периапикальные гранулемы и кисты. Расследование 1600 дел. Скандинавский журнал стоматологических исследований 78: 241-250.
143 Наир, П. (1987) Световые и электронные микроскопические исследования флоры корневых каналов и периапикальных поражений. J Endod 13: 29-39.
144 Наир, П.Н. (1998) Новые взгляды на корешковые кисты: заживают ли они? Int Endod J 31: 155-160.
145 Наир, П.Н. (2006) О причинах персистирующего апикального периодонтита: обзор. Int Endod J 39: 249-281.
146 Наир, П.Н. и другие. (1993) Корешковая киста человеческого зуба с запломбированным корнем: долгосрочное наблюдение после лечения. Int Endod J 26: 225-233.
147 Накамура К. и др. (2002) Влияние нейтропении, вызванной метотрексатом, на воспаление пульпы у крыс. J Endod 28: 287-290.
148 Nalliah, R.P. et al. (2011) Посещения отделений неотложной помощи больниц, связанные с пульпарным и периапикальным заболеванием в Соединенных Штатах в 2006 году. J Endod 37: 6-9.
J Endod 37: 6-9.
149 Невес, Б.Г. и другие. (2016)Молекулярное обнаружение бактерий, связанных с активностью кариеса в поражениях дентина. Клинические исследования полости рта.
150 Одесьо, Б. и др. (1990) Распространенность предшествующего эндодонтического лечения, технические стандарты и возникновение периапикальных поражений у случайно выбранной взрослой общей популяции. Endod Dent Traumatol 6: 265-272.
151 Оватц, С. Б. и др. (2007) Частота случаев механической аллодинии у пациентов с необратимым пульпитом. J Endod 33: 552-556.
152 Озчелик Б. и др. (2000) Гистопатологическая оценка пульпы зуба с переломом коронки. Журнал эндодонтии 26: 271-273.
153 Palmqvist, S. (1986) Состояние здоровья полости рта у населения Швеции в возрасте 65 лет и старше. Swed Dent J Suppl 32: 1-87.
154 Париж, С. и др. (2009)Экспрессия генов бета-дефенсинов человека в здоровой и воспаленной пульпе зубов человека. Журнал эндодонтии 35: 520-523.
155 Pashley, D. H. (1979) Влияние проницаемости дентина и кровотока в пульпе на концентрацию растворенных веществ в пульпе. J Endod 5: 355-361.
H. (1979) Влияние проницаемости дентина и кровотока в пульпе на концентрацию растворенных веществ в пульпе. J Endod 5: 355-361.
156 Патель, К. и др. (2016)Множественные апикальные просветления и внешняя резорбция шейки матки, связанные с вирусом ветряной оспы: отчет о случае. Дж Эндод 42:978-983.
157 Паттерсон С.С., Шафер В.Г. и Хили Х.Дж. (1964) Периапикальные поражения, связанные с эндодонтически лечеными зубами. J Am Dent Assoc 68: 191-194.
158 Peciuliene, V. et al. (2001)Выделение дрожжей и кишечных бактерий в запломбированных корнях зубов с хроническим апикальным периодонтитом. Международный эндодонтический журнал 34: 429-434.
159 Pernu, H.E., Pajari, U.H., and Lanning, M. (1996) Важность регулярного лечения зубов у пациентов с циклической нейтропенией. Продолжение 2 случаев. J Периодонтол 67: 454-459.
160 Poswar, F. de, O. et al. (2015)Биоинформатика, сетевой анализ взаимодействия и нейронные сети для характеристики экспрессии генов радикулярной кисты и периапикальной гранулемы. J Endod 41: 877-883.
J Endod 41: 877-883.
161 Priebe, W.A., Lazansky, J.P., and Wuehrmann, A.H. (1954) Значение рентгенографического снимка в дифференциальной диагностике периапикальных поражений. Oral Surg Oral Med Oral Pathol 7: 979-983.
162 Куах С.Ю., Бергенгольц Г. и Тан К.С. (2013)Fusobacterium nucleatum индуцирует продукцию цитокинов посредством механизма, независимого от Toll-подобных рецепторов. Инт Эндод Дж.
163 Quinonez, C. et al. (2009) Посещения отделения неотложной помощи для стоматологической помощи нетравматического происхождения. Community Dent Oral Epidemiol 37: 366-371.
164 Рамачандран Наир П.Н., Пахарола Г. и Шредер Х.Е. (1996) Типы и частота периапикальных поражений человека, полученных при удалении зубов. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 81: 93-102.
165 Ривз Р. и Стэнли Х.Р. (1966) Взаимосвязь проникновения бактерий и патологии пульпы в кариозных зубах. Оральная хирургия, оральная медицина и оральная патология 22: 59-65.
166 Renard, E. et al. (2016)Иммунные клетки и молекулярные сети при экспериментально индуцированном пульпите. Дж. Дент Рез. 95: 196-205.
et al. (2016)Иммунные клетки и молекулярные сети при экспериментально индуцированном пульпите. Дж. Дент Рез. 95: 196-205.
167 Рикуччи Д., Логин С. и Сикейра Дж. Ф. (2014) Корреляция между клиническими и гистологическими диагнозами пульпы. Журнал эндодонтии 40: 1932-1939.
168 Рикуччи Д. и др. (2006)Эпителий и бактерии в периапикальных поражениях. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 101: 239-249.
169 Rider, D. et al. (2016) Повышенная передача сигналов CD14 (кластер дифференцировки 14) и Toll-подобного рецептора (TLR) 4 ухудшает периапикальное воспаление у мышей с дефицитом TLR2. Анат Рек (Хобокен) 299: 1281-1292.
170 Росас, И.Н. и другие. (2016)Микробиом глубоких кариозных поражений дентина в зубах с симптоматическим необратимым пульпитом. PloS 11: e0154653.
171 Росас, И.Н. и Siqueira, JF, Jr. (2005) Обнаружение новых оральных видов и филотипов при симптоматических эндодонтических инфекциях, включая абсцессы. FEMS Microbiol Lett 250: 279-285.
172 Розенберг П.А. и другие. (2010)Оценка патологоанатомов (гистопатология) и радиологов (конусно-лучевая компьютерная томография), отличающая корешковые кисты от гранулем. J Endod 36: 423-428.
173 Сабети М. и др. (2005)Обнаружение активатора рецептора NF-каппа-бета-лиганда при апикальном периодонтите. J Endod 31: 17-18.
174 Sabeti, M., Simon, J.H., and Slots, J. (2003) Цитомегаловирус и вирус Эпштейна-Барр связаны с симптоматическим периапикальным патозом. Oral Microbiol Immunol 18: 327-328.
175 Сабети, М. и др. (2003)Транскрипция ДНК цитомегаловируса и вируса Эпштейна-Барра при эндодонтических симптоматических поражениях. Оральный микробиол иммунол 18: 104-108.
176 Сакамото М. и др. (2009)Разнообразие спирохет при эндодонтических инфекциях. J Clin Microbiol 47: 1352-1357.
177 Sakurai, K., Okiji, T., and Suda, H. (1999) Совместное увеличение количества нервных волокон и дендритных клеток, экспрессирующих HLA-DR и/или фактор-XIIIa, в пораженных кариесом участках дентина. пульпа зуба человека: иммуногистохимическое исследование. Джей Дент. Рез. 78: 1596-1608.
пульпа зуба человека: иммуногистохимическое исследование. Джей Дент. Рез. 78: 1596-1608.
178 Сантос, А.Л. и др. (2011) Сравнение бактериального разнообразия острых и хронических инфекций корневых каналов зубов. PLoS One 6: e28088.
179 Сасаки Х. и др. (2004) Гамма-интерферон (ИФН-гамма) и индуцирующие ИФН-гамма цитокины интерлейкин-12 (ИЛ-12) и ИЛ-18 не усиливают резорбцию кости, стимулируемую инфекцией, in vivo. Clin Diagn Lab Immunol 11: 106-110.
180 Сасаки Х. и др. (2000) IL-10, но не IL-4, подавляет резорбцию кости, стимулированную инфекцией, in vivo. Дж. Иммунол 165: 3626-3630.
181 Сондерс, В.П. и другие. (1997) Технический стандарт лечения корневых каналов у взрослых шотландцев. Бр Дент J 182: 382-386.
182 Schulze-Schweifing, K., Banerjee, A., и Wade, WG (2014) Сравнение бактериальной культуры и профилирования сообщества 16S рРНК с помощью клонального анализа и пиросеквенирования для характеристики микробиома, связанного с кариесом дентина. Границы клеточной и инфекционной микробиологии 4: 164.
Границы клеточной и инфекционной микробиологии 4: 164.
183 Серлс, Дж. К. (1967) Световая и электронная микроскопическая оценка изменений, вызванных высокоскоростной дрелью в одонтобластах резца крысы. Журнал стоматологических исследований 46: 1344-1355.
184 Зельцер С., Бендер И.Б. и Зионц М. (1963) Взаимосвязь пульпы и заболеваний пародонта. Оральная хирургия, оральная медицина и оральная патология 16: 1474-1490.
185 Shah, A.C. et al. (2013)Исходы госпитализаций по поводу периапикального абсцесса с 2000 по 2008 год: анализ продольных тенденций. J Endod 39: 1104-1110.
186 Шелтон Ф., Ромберг Э. и Фуад А.Ф. (2010) Влияние лечения бисфосфонатами на патогенез эндодонтического патологии. Дж Эндод 36: 556.
187 Sigurdsson, A. and Jacoway, J.R. (1995) Инфекция Herpes zoster, проявляющаяся в виде острого пульпита. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 80: 92-95.
188 Саймон, Дж.Х. (1980) Частота возникновения периапикальных кист по отношению к корневому каналу. J Endod 6: 845-848.
J Endod 6: 845-848.
189 Сикейра, Х.Ф., младший и Росас, И.Н. (2003) Идентификация Treponema maltophilum, T amylovorum, T medium и T lecithinolyticum на основе ПЦР при первичных инфекциях корневых каналов. Арка Орал Биол 48: 495-502.
190 Сикейра, Ж.Ф., младший и Росас, И.Н. (2009)Сообщество как единица патогенности: новая концепция микробного патогенеза апикального периодонтита. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 107: 870-878.
191 Сикейра, Х.Ф., младший и Росас, И.Н. (2009) Повторный взгляд на разнообразие эндодонтической микробиоты. Журнал стоматологических исследований 88: 969-981.
192 Сикейра, Х.Ф., младший и Росас, И.Н. (2013)Микробиология и лечение острых апикальных абсцессов. Clin Microbiol Rev 26: 255-273.
193 Сикейра, Дж.Ф., младший и др. (2009)Взаимосвязь между рецептором Fcgamma и полиморфизмом гена интерлейкина-1 и апикальным периодонтитом после лечения. J Endod 35: 1186-1192.
194 Сикейра, Дж.Ф., младший и др. (2011)Полиморфизм гена Fcgamma RIIIa и апикальный периодонтит после лечения. J Endod 37: 1345-1348.
(2011)Полиморфизм гена Fcgamma RIIIa и апикальный периодонтит после лечения. J Endod 37: 1345-1348.
195 Слотс, Дж., Новзари, Х., и Сабети, М. (2004) Цитомегаловирусная инфекция при симптоматическом периапикальном патологии. Int Endod J 37: 519-524.
196 Spatafore, C.M. и другие. (1990) Отчет о периапикальной биопсии: анализ за 10-летний период. J Endod 16: 239-241.
197 Stanley, HR (1971) Реакция пульпы на стоматологические методы и материалы. Стоматологические клиники Северной Америки 15: 115-126.
198 Staquet, M.J. et al. (2011) Рецепторы распознавания образов в защите пульпы. Adv Dent Res 23: 296-301.
199 Staquet, M.J. et al. (2008) Различные роли одонтобластов и фибробластов в иммунитете. J Dent Res 87: 256-261.
200 Сташенко П., Телес Р. и Д’Суза Р. (1998) Периапикальные воспалительные реакции и их модуляция. Crit Rev Oral Biol Med 9: 498-521.
201 Сташенко П., Ю С.М., Ван С.Ю. (1992) Кинетика резорбтивных реакций иммунных клеток и костей на эндодонтические инфекции. J Endod 18: 422-426.
J Endod 18: 422-426.
202 Стерн, М.Х. и другие. (1982)Выделение и характеристика воспалительных клеток из периапикальной гранулемы человека. Журнал стоматологических исследований 61: 1408-1412.
203 Стерн, М.Х. и другие. (1981)Количественный анализ клеточного состава периапикальной гранулемы человека. J Endod 7: 117-122.
204 Стокдейл, Ч.Р. и Чандлер, Н.П. (1988) Характер периапикального поражения — обзор 1108 наблюдений. Журнал стоматологии 16: 123-129.
205 Субраманиан, К. и Микель, А.К. (2009)Молекулярный анализ стойких перирадикулярных поражений и концов корней выявляет разнообразный микробный профиль. J Endod 35: 950-957.
206 Сунде, П.Т. и другие. (2002)Микробиота периапикальных поражений, рефрактерных к эндодонтической терапии. J Endod 28: 304-310.
207 Сунде, П.Т. и другие. (2003)Флуоресцентная гибридизация in situ (FISH) для прямой визуализации бактерий в периапикальных поражениях зубов с бессимптомным пломбированием корней. Микробиология 149: 1095-1102.
208 Сундквист, Г. (1992) Экология корневой флоры. Журнал эндодонтии 18: 427-430.
209 Sundqvist, G., Johansson, E., and Sjogren, U. (1989) Преобладание видов Bacteroides с черным пигментом при инфекциях корневых каналов. J Endod 15: 13-19.
210 Тани, Н. и др. (1995) Влияние дефицита Т-клеток на формирование периапикальных поражений у мышей: гистологическое сравнение образования периапикальных поражений у мышей BALB/c и BALB/c nu/nu. J Endod 21: 195-199.
211 Тейлор, Ч.П. и Байерс, М.Р. (1990) Иммуноцитохимическое исследование морфологической реакции нервов, содержащих пептид, родственный гену кальцитонина, на образование и заживление микроабсцессов в молярах крыс. Архивы устной биологии 35: 629-638.
212 Телес Р., Ван С.Ю. и Сташенко П. (1997) Повышенная восприимчивость мышей RAG-2 SCID к распространению эндодонтических инфекций. Infect Immun 65: 3781-3787.
213 Тен Кейт, А.Р. (1972) Эпителиальные клетки остатков Малассе и генезис зубной кисты. Oral Surg Oral Med Oral Pathol 34: 956-964.
Oral Surg Oral Med Oral Pathol 34: 956-964.
214 Торабинежад М. (1983) Роль иммунологических реакций в формировании апикальной кисты и судьба эпителиальных клеток после лечения корневых каналов: теория. Int J Oral Surg 12: 14-22.
215 Торабинежад М., Котти Э. и Юнг Т. (1992) Концентрация лейкотриена В4 в симптоматических и бессимптомных периапикальных поражениях. J Endod 18: 205-208.
216 Тайлер Л.В. и другие. (1999)Эозинофильные трансформирующие факторы роста (TGF-альфа и TGF-бета 1) в перирадикулярных поражениях человека. Дж Энод 25:619-624.
217 Veerayutthwilai, O. et al. (2007) Дифференциальная регуляция иммунных ответов одонтобластами. Оральный микробиол иммунол 22: 5-13.
218 Великович, М. и др. (2016)Экспрессия интерлейкина-33 и его рецептора ST2 в периапикальных гранулемах и корешковых кистах. J Oral Pathol Med 45: 70-76.
219 Вианна М.Э. и др. (2006)Идентификация и количественная оценка архей, участвующих в первичных эндодонтических инфекциях. Журнал клинической микробиологии 44: 1274-1282.
Журнал клинической микробиологии 44: 1274-1282.
220 Викерман, М.М. и другие. (2007) Филогенетический анализ видов бактерий и архей при симптоматических и бессимптомных эндодонтических инфекциях. Журнал медицинской микробиологии 56: 110-118.
221 Вадачи Р. и Харгривз К.М. (2006)Ноцицепторы тройничного нерва экспрессируют TLR-4 и CD14: механизм боли из-за инфекции. Джей Дент Рез 85: 49-53.
222 Wallstrom, J.B. et al. (1993) Роль Т-клеток в патогенезе периапикальных поражений. Предварительный отчет. Oral Surg Oral Med Oral Pathol 76: 213-218.
223 Уолтон, Р.Э. и Ardjmand, K. (1992) Гистологическая оценка присутствия бактерий в индуцированных периапикальных поражениях у обезьян. J Endod 18: 216-227.
224 Walzer, T. et al. (2005) Естественные клетки-киллеры и дендритные клетки: T union fait la force» Blood 106: 2252-2258.
225 Wang C.Y. и Сташенко P. (1991) Кинетика костно-резорбтивной активности при развитии периапикального поражения. Журнал стоматологических исследований 70: 1362-1366.
226 White, S.C. et al. (1994) Отсутствие радиометрической дифференциации между периапикальными кистами и гранулемами. Oral Surg Oral Med Oral Pathol 78: 650-654.
227 Winstock, D. (1980) Верхушечная болезнь: анализ диагностики и лечения с особым упором на резекцию корневых поражений и патологию. Анналы Королевского колледжа хирургов Англии 62: 171-179.
228 Xiong, H. et al. (2007) Влияние эстроген-дефицитного состояния и терапии алендронатом на потерю костной массы в результате экспериментальных периапикальных поражений у крыс. J Endod 33: 1304-1308.
229 Xiong, H. et al. (2010) Влияние алендроната на резорбцию альвеолярной кости и ангиогенез у крыс с экспериментальными периапикальными поражениями. Int Endod J 43: 485-491.
230 Сюй, Дж. и др. (2013) KDM6B эпигенетически регулирует одонтогенную дифференцировку зубных мезенхимальных стволовых клеток. Международный журнал устной науки 5: 200-205.
231 Ямасаки М. и др. (1994) Влияние вызванной метотрексатом нейтропении на периапикальное поражение крыс. Oral Surg Oral Med Oral Pathol 77: 655-661.
Oral Surg Oral Med Oral Pathol 77: 655-661.
232 Yoshiba, K., Yoshiba, N., and Iwaku, M. (2003) Реакция антигенпрезентирующих дендритных клеток и нервных волокон класса II на кариес, кариес или лечение кариеса в зубах человека. Журнал стоматологических исследований 82: 422-427.
233 Yoshiba, N. et al. (1998) Иммуногистохимическая локализация антигенов класса II и нервных волокон в кариозных зубах человека: иммунореактивность HLA-DR в шванновских клетках. Архив гистологии и цитологии 61: 343-352.
234 Yoshiba, N. et al. (1996) Иммуногистохимическая локализация HLA-DR-позитивных клеток в непрорезавшихся и прорезавшихся нормальных и кариозных зубах человека. Журнал стоматологических исследований 75: 1585-1589.
235 Zehnder, M., Wegehaupt, F.J., and Attin,
T. (2011) Первое исследование полезности матриксной металлопротеиназы 9 из дентинной жидкости для индикации воспаления пульпы. Журнал эндодонтии 37: 17-20.
236 Zhong, S. et al. (2012)Дифференциальная экспрессия микроРНК в нормальной и воспаленной пульпе человека. Журнал эндодонтии 38: 746-752.
Журнал эндодонтии 38: 746-752.
Предыдущая
СтраницаСледующая
Страница
Хронический пульпит, лечение хронического фиброзного пульпита
Содержание:
Возбудителями хронического пульпита в большинстве случаев являются биологические агенты, в состав которых входят различные возбудители, а также выделяемые ими токсины. По дентинным канальцам по кровеносным и лимфатическим сосудам из кариозной области зуба они переносятся в пульпу. Туда же они могут попасть через отверстие верхушки корня при острых инфекционных заболеваниях и воспалительных процессах.
Инфицирование поверхности пульпы в области кариозного участка вызывает воспалительный процесс, после которого болезнетворные бактерии поражают и корневую пульпу.
Воспаление пульпы часто является следствием физических, механических и химических повреждений.
- При механических травмах в результате удара нередко происходит повреждение сосудисто-нервного пучка в области пародонта, в результате чего обнажается пульпа и нарушается ее питание. Целостность зуба нарушается также при быстром стирании режущей части зуба или жевательной поверхности его коронки. г.
- Термическое повреждение часто является результатом неаккуратного препарирования кариозной зоны или верхней части коронки.
- Воспалительный процесс в пульпе может быть вызван и химическим фактором при воздействии таких препаратов, как эфир или спирт, которые часто применяют для лечения кариозной полости.
- Заболевание также может быть связано с неаккуратным наложением или отсутствием заживляющих или изолирующих повязок, а также с применением тимола в дополнение к прокладочному материалу. г.
Симптомы хронического пульпита
Переход заболевания в хроническую форму всегда является следствием нелеченной острой стадии пульпита. Больному может казаться, что воспалительный процесс прошел, но на самом деле ни одно заболевание не проходит само собой. Организм может лишь помочь облегчить симптомы, но болезнь будет прогрессировать дальше.
Больному может казаться, что воспалительный процесс прошел, но на самом деле ни одно заболевание не проходит само собой. Организм может лишь помочь облегчить симптомы, но болезнь будет прогрессировать дальше.
Боль при хроническом пульпите гораздо терпимее, чем при остром. Она носит ноющий характер и редко иррадиирует по ходу стволов тройничного нерва.
Хронический фиброзный пульпит дает ощущение тяжести в зубе, появляется боль как реакция на раздражители. Это единственная форма пульпита, которая может протекать сама по себе, при отсутствии острой стадии в анамнезе.
Характерным признаком этой формы заболевания является появление ноющих болей при изменении температуры окружающей среды (например, при выходе из теплого помещения на мороз).
При объективном исследовании кариозная полость с пигментированным дентином и точечным сообщением с полостью зуба. Зондирование умеренно болезненное.
Хронический гипертрофический пульпит часто встречается у детей и молодых людей. История острой боли в прошлом.
История острой боли в прошлом.
Больные жалуются на боль и кровотечение из полости при пережевывании пищи.
При осмотре в полостях видна разросшаяся, гипертрофированная пульпа. В процессе гипертрофии могут образовываться грануляции или полип. В обоих случаях образование составляет единое целое с воспаленной пульпой.
Зондирование слабо болезненно, но вызывает кровотечение из патологических образований.
Хронический гангренозный пульпит может развиться из хронического фиброзного или гнойного пульпита при попадании гнилостных бактерий в ткань сосудисто-нервного пучка.
В случае, когда заболевание протекает с открытой полостью зуба, спонтанные боли в анамнезе отсутствуют. Но может спровоцировать горячее питание или другое тепловое воздействие. Неизменным спутником гангренозной формы пульпита является неприятное ощущение расширения зуба.
Самостоятельные боли возникают только при закрытой пульповой камере. При этом нет условий для оттока воспалительного экссудата и патологический процесс переходит в острую стадию.
При объективном исследовании глубокой чувствительности вызывает непродолжительную резкую боль. Полость зуба заполнена распадом пульпы с неприятным запахом. На рентгенограмме периодонтальная щель (пространство между корнем зуба и костной тканью челюсти) увеличена и деформирована.
Хронический конкрементозный пульпит обусловлен образованием петрификатов и зубцов в тканях пульпы в результате активного поступления кальция.
Больные жалуются на спонтанные боли острого, приступообразного характера, иррадиирующие по ходу всех ветвей тройничного нерва.
Клиническая картина сопутствующего пульпита сходна с признаками невралгии тройничного нерва, поэтому перед назначением конкретного лечения врач должен тщательно диагностировать заболевание.
Эта форма воспаления зубного нерва чаще возникает в зубах с повышенной стираемостью твердых тканей (эмали и дентина) и лечится по поводу наличия в прошлом кариозной полости.
Но иногда заболевание возникает и в интактных зубах (без внешних признаков поражения).
При осмотре причинного зуба явных признаков конкрементозного пульпита может не быть, поэтому окончательный диагноз ставится на основании рентгенографии, которая точно покажет наличие дементита в пульповой камере.
Обострение хронического пульпита
Каждая форма хронического пульпита склонна к обострению. Чаще всего обостряется пульпит, протекающий при закрытой полости зуба.
Спонтанная боль, иррадиирующая в разные части головы, а также усиление боли в ночное время свидетельствует о начале острой фазы. По симптоматике данный клинический случай можно диагностировать как острый пульпит. На давность заболевания указывают боли аналогичного характера в прошлом.
Правильная диагностика требует тщательного выяснения анамнеза заболевания и тщательного осмотра причинного зуба.
Лечение хронического пульпита
При лечении пульпита необходимо решить несколько задач:
- устранение болевых симптомов за счет ликвидации воспалительного очага в пульпе
- проведение процедур, способствующих заживлению и формированию дентина
- проведение мероприятий по профилактике развития пародонтита
- восстановление формы зубов и функции жевания
Комбинированный метод лечения заключается в полной очистке проходных каналов от пульпы, после чего проводится ее полная мумификация.
Метод витальной ампутации применяют при электрочувствительности пульпы до 40 мкА, а также при лечении хронического фиброзного пульпита.
Метод экстирпации предполагает удаление пульпы без предварительной некротизации с применением анестезии. Этот метод широко применяется при лечении любой формы пульпита. Его применение противопоказано при полной непроходимости корневых каналов, а также у тяжелобольных с невротическими расстройствами и инфарктом миокарда.
При любом методе лечения рекомендуется проводить процедуру обезболивания, что в данном случае является одним из условий успешного лечения.
Премедикация
Перед лечением всегда рекомендуется провести процедуру седации, предполагающую применение специальных лекарственных средств. Ее основная задача – нормализовать функции ЦНС больного, что исключит условия его неадекватной реакции на последующие манипуляции врача. Оптимальный обезболивающий эффект достигается при введении анестетика инъекционным методом. В качестве анестетиков рекомендуется использовать 2% раствор тримекаина в количестве от 2 до 5 мл., 2% раствор новокаина в количестве 2 мл., или 2-5% раствор лидокаина в количестве 2 мл.
В качестве анестетиков рекомендуется использовать 2% раствор тримекаина в количестве от 2 до 5 мл., 2% раствор новокаина в количестве 2 мл., или 2-5% раствор лидокаина в количестве 2 мл.
Наряду с премедикацией в качестве анестезии при лечении пульпита часто применяют внутрипульпарную анестезию, когда анестетик дополнительно вводят в саму пульпу после применения анестезирующего наркоза. Это очень эффективный метод анестезии.
Лечение пульпита методом витальной ампутации
Опыт лечения показал, что коронковая часть зуба может быть успешно удалена с сохранением жизнедеятельности корневой части пульпы. Метод успешен при лечении хронического фиброзного пульпита у пациентов до 40 лет, а также в многокорневых зубах, где четко выражена граница между корнем и коронковой пульпой. При таком лечении используются те же препараты, что и при биологическом методе лечения. Однако область устьев корневых каналов должна быть закрыта медицинскими прокладками.
Данный метод лечения проходит в несколько этапов:
- Больному необходимо ввести анестетик, после чего, соблюдая все меры асептики, рассекают кариозную полость.

- Требуется удалить коронковую и устьевую часть корневой пульпы, затем провести тщательный гемостаз.
- Аккуратно и без давления наложить медицинскую прокладку и пломбу. Здесь стоит отметить, что перед наложением постоянной пломбы необходимо сначала нанести одонтотропную затвердевающую пасту. г.
По окончании лечения больному рекомендуется назначить УВЧ, СВЧ-терапию, процедуры СНЛЛ.
Хирургическое лечение пульпита
При лечении пульпита в терапевтической стоматологии чаще применяют методы, предусматривающие частичное или полное его удаление. Этот метод считается очень трудоемким в связи с тем, что, кроме удаления самой пульпы, данный метод предполагает дальнейшую медикаментозную и инструментальную обработку коронковой полости зуба, а также корневых каналов, после чего их следует запломбировать специальной пломбой. масса.
Способ лечения пульпита девитальной экстирпацией
Способ включает некротизацию, после чего воспаленную пульпу удаляют. Для некротизации используется мышьяковый ангидрид. Количество мышьяковистого вещества должно соответствовать размеру головки сферического бора номер один.
Для некротизации используется мышьяковый ангидрид. Количество мышьяковистого вещества должно соответствовать размеру головки сферического бора номер один.
Способ наложения девитализирующей пасты
С помощью фиссурного бора необходимо обеспечить доступ в кариозную полость больного с целью очистки ее от опилок, а также размягченного дентина. Устранив боль, необходимо обнажить саму пульпу с помощью шаровидного бора, либо с помощью дентального зонда, если дентин слишком мягкий. На кончик зонда аккуратно наносят необходимую дозу мышьяковистой пасты, а поверх него накладывают ватный тампон, смоченный анестетиком. Завершить препарирование кариозной полости можно будет через 1-2 дня после аппликации мышьяковистого вещества или через 7-10 дней в случаях применения пасты замедленного действия.
Способ вскрытия полости зуба
Полость в резцах и клыках следует вскрывать, начиная с язычной поверхности в случаях, когда по ортопедическим показаниям требуется депульпация, была травма зуба, а также в случаях, когда кариес поражена пришеечная область зуба. Перед вскрытием полости необходимо выполнить все процедуры, связанные с формированием ее формы.
Перед вскрытием полости необходимо выполнить все процедуры, связанные с формированием ее формы.
При проведении асептической обработки очень важно, чтобы слюна не попадала на зуб.
Перед использованием пульпэкстрактора необходимо продезинфицировать устье корневого канала специальным раствором антисептика.
Обработку труднодоступных каналов лучше проводить методом импрегнации (резорцин-формалин). Более доступные корневые каналы можно обрабатывать обычными антисептическими средствами.
Метод витальной экстирпации
Этот метод лечения характеризуется применением проводниковой и инфильтрационной анестезии и анестезии. Под анестезией полностью удаляют коронковую и корневую пульпу, мышьяк не применяется. Часто используют метод коагуляции. К манипуляциям можно приступать уже через 20 минут после анестезии. С помощью стерильного бора широко вскрывают коронковую полость, откуда затем механически извлекают пульпу. Стоит отметить, что данная процедура рекомендуется за одно посещение.
Профилактика хронического пульпита
- В связи с тем, что пульпит является следствием осложнений, вызванных кариозными процессами, своевременное лечение кариеса является наиболее эффективным способом его профилактики.
- Регулярные посещения стоматологического кабинета могут предотвратить образование пульпита.
- Поддержание правильного соотношения потребляемых нутриентов – минимальное количество углеводов и большое количество кальция и витаминов.
- Укрепление зубной эмали за счет регулярного употребления фторированной воды. г.
- Ежедневная гигиена полости рта, полоскание или полоскание рта после каждого приема пищи, а также регулярная чистка зубов утром и вечером.
Не стоит относиться к профилактике с пренебрежением, ведь иногда именно она может помочь сохранить здоровье зубов и красивую улыбку.
- Острый пульпит
- Пульпит: симптомы и лечение
- Пародонтит: симптомы и лечение
Пульпит.
 Это воспаление зубов… | Сумеш Ханал
Это воспаление зубов… | Сумеш Ханал Это воспаление пульпы зуба. Последовательность событий, ведущих к пульпиту:
- Кариес зубов -> Полость эмали -> Пенетрация пульпы зуба -> Пульпит
- На ранней стадии, когда инфекция пульпы ограничена, зуб становится чувствительным к перкуссии, горячему или холодному и боли исчезает сразу после устранения раздражающего раздражителя
- Если инфекция распространяется по всей пульпе: возникает необратимый пульпит: некроз пульпы.
- На этой поздней стадии боль сильная, острая или пульсирующая, усиливающаяся в положении лежа
- После полного некроза пульпы боль может быть постоянной или прерывистой, но чувствительность к холоду теряется
- Очень болезненное состояние, являющееся наиболее частой причиной сильная зубная боль
- При отсутствии лечения: отмирание пульпы -> распространение инфекции на пародонтальное пространство -> пародонтит
Этиология:
- Кариес зубов: , распространяющийся на пульпу: наиболее частая причина
- Травматический:
- Обнажение пульпы
- Механическое повреждение
- Перелом коронки
- Треснувший зуб
- Расщепление премоляра, которое обычно происходит в премолярах из-за жевательного напряжения
- Термическое воздействие позволяет микроорганизмам добраться до пульпы
- Например: выделение тепла во время сверления, особенно если оно выполняется без использования воды: сверхбыстрое проникновение в полость: также с серебряным наполнением
- Для предотвращения теплового эффекта под заполнением Zn(PO4) используется в качестве изолятора
- Неспецифическая инфекция
- Вызванная стрептококком, другими микроорганизмами путем глубокого кариеса или гематогенным путем (бактериальная инвазия)
- Химическая травма
- Цементы (силикатные), ртутные квасцы
декомпрессия в условиях высокогорья
Патогенез:
- Инфекция локализуется в пульповой камере (коронка) и пульповой полости (корне), которые замкнуты, фиксированы и ригидны пространство -> скопление экссудата в пульповой полости -> повышенное давление (ограничение апикального отверстия ) -> усиленное кровообращение -> нарушение венозного возврата и нарушение артериального кровоснабжения -> некроз пульпы.

- При лечении на ранней стадии: обратимая и локализованная
- Поздняя стадия: необратимая
- Пульпит является неспецифической инфекцией , поскольку вовлечено множество бактерий: стрептококк и другие бактерии, присутствующие в кариозной полости, в основном ответственны
Типы пульпита:
- Открытый : полость пульпы и ротовая полость сообщаются
- Закрытый : такого сообщения не существует
- Острый : быстрое начало, тяжелое и кратковременное
- Хронический : медленное развитие, большая продолжительность
Острый закрытый пульпит
- Когда вирулентные микроорганизмы попадают в пульпу в большом количестве, часть пульпы быстро разрушается, что приводит к острой воспалительной реакции.
- Эта реакция приводит к острой гиперемии с выходом жидкости и клеточного экссудата в окружающие ткани
- Формируется минутный абсцесс
- Остальная часть пульпы не повреждена, т.
 е. инфекция остается локализованной
е. инфекция остается локализованной - Однако в тяжелых случаях воспаление не остается локализованным: оно быстро распространяется на пульпу и постепенно разрушает ее.
Хронический закрытый пульпит
- Деструкция пульпы видна на входе в месте инъекции
- Происходит легкая гиперемия и образование абсцесса
- Инфекция может оставаться локализованной в течение длительного времени с оставшейся частью пульпы инфицированной и здоровой
- Другими словами , деструкция прогрессирует медленно и, наконец, через верхушку, достигает периапикальной ткани
- Клинически:
- Острый и хронический пульпит, распознаваемый по типу и степени боли:
- Острый пульпит:
- Ранняя стадия: зуб гиперчувствителен к горячему и холодному
- Позднее: боль становится более постоянной и усиливается в положении лежа или во сне
- Боль возникает из-за: давления на нервные окончания воспалительным экссудатом в закрытой и ригидной пульпарной камере
- ИЛИ высвобождения медиаторов боли (гистамин, 5-НТ) из места повреждения
- Хронические пульпиты:
- Могут протекать бессимптомно
- Однако возможны спонтанные приступы полной боли на холодные и горячие раздражители
- Боль как при остром, так и при хроническом пульпите плохо локализована из-за отсутствия проприоцептивных пульпы и потому, что индивидуальная пульпа не представлена в сенсорном гомункуле.

Острый открытый пульпит
- Возникает на поздней стадии кариеса
- Пульповая камера может вскрываться из-за разрушения части коронки
- Обычно к этому времени пульпа уже мертва, но может оставаться жизнеспособной и пролиферативной
- После острого воздействия и занесения инфекции возникает острая воспалительная реакция, которая приводит к образованию абсцесса и выходу гноя через открытую часть
- Гной ускользает: боль возобновляется
- Быстрое распространение инфекции и деструкция пульпы
Хронический открытый пульпит
- Иногда выживает широко обнаженная пульпа в стадии хронического открытого пульпита, особенно в зубах с открытой верхушкой
- Коронка зуба с пульпой разрушается и замещается грануляционной тканью, которая может пролиферировать, заполняя кариозную полость, а затем подвергаться эпителизации и фиброзу
- Фиброз приводит к образованию узелков, называемых «полипами пульпы», и состояние называется хроническим гипертрофическим пластический) пульпит (CHP)
- CHP: раздражение, инфекция, хроническое воспаление пульпы, пролиферация грануляционной ткани, эпителизация и фиброз
- Безболезненный, возникает обычно при широко открытом верхушке и хорошем кровоснабжении, сохраняющем жизнеспособность
- Патофизиология хронического открытого пульпита:
- Инфекция: хроническое воспаление пульпы: образование грануляционной ткани и пролиферация: эпителизация и фиброз: образование узелков
Исследование и диагностика
- хлорид)
- Сначала зуб чувствителен как к горячему, так и к холодному, но позже холод возобновляется, а горячее ухудшается
- Электротестер пульпы: первый тест на здоровом зубе
- Начните со слабого тока и повышайте его, пока не появится ответ
- Затем проверьте пораженный зуб
- Низкий ток вызывает реакцию на ранней стадии, а сильный ток на поздней стадии
- Помогает оценить степень пульпита
Лечение пульпита
- Удаление: эффективный, но деструктивный способ лечения пульпы
- Не всегда предпочтительный метод лечения
- При тяжелом пульпите ЛА может не помочь
- Однако он безопасен, поскольку не вызывает осложнений, таких как распространение инфекции
- Покрытие пульпы:
- В недавно обнаженной полости пульпы с отверстием >1 мм без какой-либо инфекции или боли: выполняется покрытие пульпы (прямое покрытие пульпы или DPC) Ca(OH)2 наносится на открытые участки
- Если отверстие полости пульпы >1 мм : требуется экстирпация и РКИ.

- Пульпотомия
- Частичное удаление пульпы
- Коронковая пульпа ампутируется, оставляя оставшуюся корневую пульпу для заживления
- Пульпотомия является промежуточным методом лечения, когда апекс широкий (например, у детей с неполным развитием) и РКИ невозможно
- Вновь вскрытая полость пульпы лечится пульпотомией вместо РКИ, которая проводится позже, по мере роста пульпы
Лечение пульпита предлагается в зависимости от пациента
- Отношение: хочет ли он сохранить или удалить зуб
- Финансовое положение: РКИ стоит дорого
- Новейшая методика десенсибилизации: ионофорез (возврат к состоянию чувствительности)
- При возникновении необратимого пульпита: необходима РКИ и удаление содержимого пульповой камеры и корневых каналов с последующей тщательной антисептической очисткой и пломбированием зубов инертным материалом
Осложнения пульпита
- Если инфекция пульпы не уменьшается: образование периапикального абсцесса (боль при жевании)
- Если легкая и хроническая инфекция: периапикальная гранулема или, в конечном итоге, периапикальная киста, вызывающая просветление верхушки корня
- При отсутствии лечения a периапикальный абсцесс может разрушаться в альвеолярную кость, вызывая остеомиелит, проникать и дренировать через десну (папка или флюс) или прорастать вдоль глубоких фасциальных плоскостей, вызывая вирулентный целлюлит (ангина Людвига), поражающий поднижнечелюстное пространство и дно полости рта
- Пожилой пациент с СД и больной, принимающий глюкокортикоиды, может испытывать незначительные боли и лихорадку по мере развития этих осложнений.

Пульпа и периапикальные патологии | Карманная стоматология
-
Схема главы
-
Раздражители
-
Патоз пульпы
-
Классификация болезней пульпы
-
Периапикальный патоз
-
Классификация периапикальных поражений
-
Заживление пульпы и периапикальных тканей
-
Неэндодонтический перирадикулярный патоз
Цели обучения
После прочтения этой главы учащийся должен уметь:
- 1.
Определите этиологические факторы, вызывающие воспаление пульпы.
- 2.
Объясните механизм распространения воспаления в пульпе.
- 3.
Объясните, почему пульпе трудно восстановиться после серьезного повреждения.
- 4.
Перечислите специфические и неспецифические медиаторы воспаления пульпы.

- 5.
Классифицировать заболевания пульпы и их клинические и гистологические особенности.
- 6.
Опишите механизмы и объясните последствия распространения воспаления пульпы на перирадикулярные ткани и последующие воспалительные и иммунологические реакции.
- 7.
Классифицируйте перирадикулярные поражения пульпового происхождения.
- 8.
Выявление и различие между гистологическими особенностями и клиническими признаками и симптомами острого апикального периодонтита, хронического апикального периодонтита, острых и хронических апикальных абсцессов (гнойный апикальный периодонтит) и конденсирующегося остита.
- 9.
Опишите шаги, связанные с восстановлением перирадикулярной патологии после успешного лечения корневых каналов.
г.
- 10.
Идентифицируйте и опишите в целом неэндодонтические патологические поражения, которые могут имитировать эндодонтический перирадикулярный патоз.
Цели обучения
После прочтения этой главы учащийся должен уметь:
- 1.

Определите этиологические факторы, вызывающие воспаление пульпы.
- 2.
Объясните механизм распространения воспаления в пульпе.
- 3.
Объясните, почему пульпе трудно восстановиться после серьезного повреждения.
- 4.
Перечислите специфические и неспецифические медиаторы воспаления пульпы.
- 5.
Классифицировать заболевания пульпы и их клинические и гистологические особенности.
- 6.
Опишите механизмы и объясните последствия распространения воспаления пульпы на перирадикулярные ткани и последующие воспалительные и иммунологические реакции.
- 7.
Классифицируйте перирадикулярные поражения пульпового происхождения.
- 8.
Выявление и различие между гистологическими особенностями и клиническими признаками и симптомами острого апикального периодонтита, хронического апикального периодонтита, острых и хронических апикальных абсцессов (гнойный апикальный периодонтит) и конденсирующегося остита.

- 9.
Опишите шаги, связанные с восстановлением перирадикулярной патологии после успешного лечения корневых каналов.
- 10.
Идентифицируйте и опишите в целом неэндодонтические патологические поражения, которые могут имитировать эндодонтический перирадикулярный патоз.
Раздражители
Раздражение пульпы или околокорневых тканей может привести к воспалению. Эти раздражители могут быть широко классифицированы как неживые или живые. Неживые причины воспаления могут быть механическими, термическими или химическими. Жизнеспособные раздражители включают микроорганизмы и вирусы.
Механические раздражители
Механические раздражители, такие как глубокое препарирование полости, удаление тканей зуба без надлежащего охлаждения, ударная травма, окклюзионная травма, глубокий пародонтальный кюретаж и ортодонтическое перемещение зубов, могут привести к изменениям подлежащей пульпы. Временные изменения, такие как аспирация одонтобластов в дентинные канальцы, обычно обратимы в здоровой пульпе (рис. 4.1). Однако в типичных клинических ситуациях ткань пульпы уже воспалена из-за наличия кариеса или предшествующих восстановительных процедур. Если не принять надлежащих мер предосторожности, препарирование полости или коронки может повредить расположенные ниже одонтобласты. Количество канальцев на единицу площади поверхности и диаметр канальцев увеличиваются ближе к пульпе (рис. 4.2). В результате проницаемость дентина больше ближе к пульпе, чем вблизи дентиноэмалевого соединения (DEJ) или цементо-дентинного соединения (CDJ). Следовательно, вероятность раздражения пульпы увеличивается по мере удаления большего количества дентина (т. е. по мере углубления препарирования полости и ее приближения к пульпе). Повреждение пульпы примерно пропорционально количеству удаленной ткани зуба, а также глубине удаления. Кроме того, оперативные процедуры без охлаждающей воды вызывают большее раздражение, чем те, которые выполняются под струей воды. Изучение реакций и сосудистых изменений, возникающих при экспериментально индуцированном остром и хроническом пульпите, показало повышение проницаемости и расширение сосудов на ранних стадиях пульпита.
4.1). Однако в типичных клинических ситуациях ткань пульпы уже воспалена из-за наличия кариеса или предшествующих восстановительных процедур. Если не принять надлежащих мер предосторожности, препарирование полости или коронки может повредить расположенные ниже одонтобласты. Количество канальцев на единицу площади поверхности и диаметр канальцев увеличиваются ближе к пульпе (рис. 4.2). В результате проницаемость дентина больше ближе к пульпе, чем вблизи дентиноэмалевого соединения (DEJ) или цементо-дентинного соединения (CDJ). Следовательно, вероятность раздражения пульпы увеличивается по мере удаления большего количества дентина (т. е. по мере углубления препарирования полости и ее приближения к пульпе). Повреждение пульпы примерно пропорционально количеству удаленной ткани зуба, а также глубине удаления. Кроме того, оперативные процедуры без охлаждающей воды вызывают большее раздражение, чем те, которые выполняются под струей воды. Изучение реакций и сосудистых изменений, возникающих при экспериментально индуцированном остром и хроническом пульпите, показало повышение проницаемости и расширение сосудов на ранних стадиях пульпита. Исследования на моделях грызунов, предназначенные для определения воздействия тепловыделения на пульпу зуба, показали, что повышение температуры пульпы выше 42°C активирует белки теплового шока (HSP). HSP-70 играет защитную роль, и его уровень возвращается к исходному уровню в течение нескольких часов после устранения теплового раздражителя.
Исследования на моделях грызунов, предназначенные для определения воздействия тепловыделения на пульпу зуба, показали, что повышение температуры пульпы выше 42°C активирует белки теплового шока (HSP). HSP-70 играет защитную роль, и его уровень возвращается к исходному уровню в течение нескольких часов после устранения теплового раздражителя.
через эмаль и в 1 мм дентина привело к аспирации одонтобластов (стрелки) в канальцы и инфильтрации пульпы полиморфноядерными (ПЯН) лейкоцитами и лимфоцитами. Образец был взят через 48 часов после изготовления коронки.
Рис. 4.2Микрофотография, иллюстрирующая многочисленные дентинные канальцы на стенке дентина, прилегающей к просвету канала. Плотность канальцев увеличивается ближе к пульпарной стороне стенки дентина.
Ударные травмы с переломами коронки или корня или без них могут вызвать повреждение пульпы (см. главу 11). Тяжесть травмы и степень апикального закрытия корня являются важными факторами способности пульпы к восстановлению. Зубы, подвергшиеся легкой или средней травме, а также зубы с несформированными верхушками имеют больше шансов на выживание пульпы по сравнению с зубами с тяжелыми травмами или зубами с закрытыми верхушками. Приложение сил, выходящих за пределы физиологической переносимости периодонтальной связки (ПСС) во время ортодонтического перемещения зубов, приводит к нарушению кровоснабжения и иннервации тканей пульпы. Результирующие изменения включают атрофию клеток и изменение нервных аксонов. Кроме того, ортодонтическое перемещение может инициировать резорбцию апекса, обычно без изменения жизнеспособности. Глубокое удаление зубного камня и кюретаж могут повредить апикальные сосуды и нервы, что приведет к повреждению пульпы (см. главу 7).
Зубы, подвергшиеся легкой или средней травме, а также зубы с несформированными верхушками имеют больше шансов на выживание пульпы по сравнению с зубами с тяжелыми травмами или зубами с закрытыми верхушками. Приложение сил, выходящих за пределы физиологической переносимости периодонтальной связки (ПСС) во время ортодонтического перемещения зубов, приводит к нарушению кровоснабжения и иннервации тканей пульпы. Результирующие изменения включают атрофию клеток и изменение нервных аксонов. Кроме того, ортодонтическое перемещение может инициировать резорбцию апекса, обычно без изменения жизнеспособности. Глубокое удаление зубного камня и кюретаж могут повредить апикальные сосуды и нервы, что приведет к повреждению пульпы (см. главу 7).
Перирадикулярные ткани могут быть механически раздражены и воспалены в результате ударной травмы, гиперокклюзии, эндодонтических процедур и несчастных случаев, экстирпации пульпы, переинструментации корневых каналов, перфорации корня и чрезмерного растяжения пломбировочного материала корневого канала. Интрузионные повреждения с большей вероятностью приведут к некрозу пульпы, чем латеральные или экструзионные (рис. 4.3). Во время препарирования канала может возникнуть механическое раздражение инструментами. Неточное определение длины канала обычно является причиной переинструментирования и последующего воспаления. Кроме того, отсутствие адекватной апикальной резистентной формы, создаваемой во время очистки и формирования, может вызвать чрезмерное выпячивание пломбировочного материала в периапикальные ткани, вызывая физические и химические повреждения (рис. 4.4).
Интрузионные повреждения с большей вероятностью приведут к некрозу пульпы, чем латеральные или экструзионные (рис. 4.3). Во время препарирования канала может возникнуть механическое раздражение инструментами. Неточное определение длины канала обычно является причиной переинструментирования и последующего воспаления. Кроме того, отсутствие адекватной апикальной резистентной формы, создаваемой во время очистки и формирования, может вызвать чрезмерное выпячивание пломбировочного материала в периапикальные ткани, вызывая физические и химические повреждения (рис. 4.4).
Графическое изображение кровообращения в пульпе после различных видов вывихов зубов. Циркуляция пульпы измеряется в единицах перфузии в течение 36-недельного периода наблюдения.
Рис. 4.4Неправильная инструментальная обработка и экструзия пломбировочных материалов в периапикальные ткани вызывают перирадикулярное воспаление (стрелки).
Химические раздражители
К химическим раздражителям пульпы относятся различные очищающие, стерилизующие и десенсибилизирующие вещества для дентина в дополнение к некоторым веществам, присутствующим во временных и постоянных реставрационных материалах и прокладках для полостей. Антибактериальные агенты, такие как нитрат серебра, фенол с камфорой и без нее и эвгенол, использовались в попытке «стерилизовать» дентин после препарирования полости. Эффективность многих из этих продуктов в качестве стерилизаторов дентина сомнительна, а их цитотоксичность может вызывать воспалительные изменения в подлежащей пульпе зуба. Другие раздражающие агенты включают чистящие средства для полости рта, такие как спирт, хлороформ, перекись водорода и различные кислоты; химические вещества, присутствующие в десенсибилизаторах; вкладыши и основания полостей; временные и постоянные реставрационные материалы.
Антибактериальные агенты, такие как нитрат серебра, фенол с камфорой и без нее и эвгенол, использовались в попытке «стерилизовать» дентин после препарирования полости. Эффективность многих из этих продуктов в качестве стерилизаторов дентина сомнительна, а их цитотоксичность может вызывать воспалительные изменения в подлежащей пульпе зуба. Другие раздражающие агенты включают чистящие средства для полости рта, такие как спирт, хлороформ, перекись водорода и различные кислоты; химические вещества, присутствующие в десенсибилизаторах; вкладыши и основания полостей; временные и постоянные реставрационные материалы.
Антибактериальные ирриганты, используемые при очистке и формировании корневых каналов, внутриканальные препараты и некоторые соединения, присутствующие в материалах для обтурации, являются примерами потенциальных химических раздражителей околокорневых тканей. Большинство ирригантов и медикаментов токсичны и не биосовместимы. Тревино и его коллеги проверили влияние 17% этилендиаминтетрауксусной кислоты (ЭДТА) отдельно или в сочетании с гипохлоритом натрия (NaOCl) или хлоргексидином на жизнеспособность стволовых клеток, выделенных из апикального сосочка. Их результаты показали, что ЭДТА лучше всего поддерживает жизнеспособность клеток (89).% выживаемости клеток), затем следует протокол с использованием NaOCl (выживаемость клеток 74%). Напротив, добавление хлоргексидина приводило к отсутствию жизнеспособности клеток. ЭДТА оказывает аналогичное благоприятное воздействие на клетки пульпы зуба при использовании в качестве кондиционирующего агента для дентина. При тестировании воздействия противомикробных препаратов на клетки пульпы зуба исследователи показали, что гидроксид кальция и более низкие концентрации паст с антибиотиками способствуют выживанию и пролиферации клеток, но более концентрированные формы паст с антибиотиками оказывают пагубное воздействие.
Их результаты показали, что ЭДТА лучше всего поддерживает жизнеспособность клеток (89).% выживаемости клеток), затем следует протокол с использованием NaOCl (выживаемость клеток 74%). Напротив, добавление хлоргексидина приводило к отсутствию жизнеспособности клеток. ЭДТА оказывает аналогичное благоприятное воздействие на клетки пульпы зуба при использовании в качестве кондиционирующего агента для дентина. При тестировании воздействия противомикробных препаратов на клетки пульпы зуба исследователи показали, что гидроксид кальция и более низкие концентрации паст с антибиотиками способствуют выживанию и пролиферации клеток, но более концентрированные формы паст с антибиотиками оказывают пагубное воздействие.
Микробные раздражители
Хотя механические и химические раздражения носят преимущественно преходящий характер, наиболее важной причиной воспаления являются микробы. Микроорганизмы, присутствующие при кариесе зубов, являются основным источником раздражения пульпы зуба и околокорневых тканей. Кариозный дентин и эмаль содержат многочисленные виды бактерий, такие как Streptococcus mutans, лактобактерии и Actinomyces spp. Более поздние исследования с использованием молекулярных методов выявили участие нескольких других родов в развитии кариозных поражений, в том числе Veillonella, Bifidobacterium, и Propionibacterium spp.
Кариозный дентин и эмаль содержат многочисленные виды бактерий, такие как Streptococcus mutans, лактобактерии и Actinomyces spp. Более поздние исследования с использованием молекулярных методов выявили участие нескольких других родов в развитии кариозных поражений, в том числе Veillonella, Bifidobacterium, и Propionibacterium spp.
Прямое воздействие микроорганизмов на пульпу не является предпосылкой для реакции пульпы и воспаления. Микроорганизмы при кариесе продуцируют токсины, проникающие в пульпу через канальцы. Исследования показали, что даже небольшие повреждения эмали способны привлекать воспалительные клетки в пульпе. Первоначальная реакция пульпы на эти раздражители опосредована врожденным иммунным ответом. Эта ранняя реакция на кариес приводит к очаговому накоплению хронических воспалительных клеток, таких как макрофаги, лимфоциты и плазматические клетки. По мере продвижения распада к пульпе интенсивность и характер инфильтрата меняются. Когда происходит фактическое обнажение, ткань пульпы локально инфильтрируется полиморфноядерными (PMN) лейкоцитами с образованием области разжижающего некроза в месте воздействия (рис. 4.5). После обнажения пульпы бактерии колонизируют и сохраняются в месте некроза. Ткань пульпы может оставаться воспаленной в течение длительного времени и может подвергаться возможному или быстрому некрозу. Это зависит от нескольких факторов: (1) вирулентности бактерий, (2) способности высвобождать воспалительные жидкости во избежание заметного повышения внутрипульпарного давления, (3) резистентности хозяина, (4) объема циркуляции и, что важно, фактор, (5) лимфодренаж. Yamasaki и коллеги сделали обнажение пульпы у крыс и показали, что некроз постепенно распространяется от верхней части пульпы к апикальной части. Периапикальное поражение возникло после воспаления и некроза пульпы.
Когда происходит фактическое обнажение, ткань пульпы локально инфильтрируется полиморфноядерными (PMN) лейкоцитами с образованием области разжижающего некроза в месте воздействия (рис. 4.5). После обнажения пульпы бактерии колонизируют и сохраняются в месте некроза. Ткань пульпы может оставаться воспаленной в течение длительного времени и может подвергаться возможному или быстрому некрозу. Это зависит от нескольких факторов: (1) вирулентности бактерий, (2) способности высвобождать воспалительные жидкости во избежание заметного повышения внутрипульпарного давления, (3) резистентности хозяина, (4) объема циркуляции и, что важно, фактор, (5) лимфодренаж. Yamasaki и коллеги сделали обнажение пульпы у крыс и показали, что некроз постепенно распространяется от верхней части пульпы к апикальной части. Периапикальное поражение возникло после воспаления и некроза пульпы.
Локализованная воспалительная реакция, содержащая в основном полиморфноядерные лейкоциты в месте кариозного обнажения пульпы. Остальная часть коронковой пульпы практически свободна от воспалительных клеток.
Остальная часть коронковой пульпы практически свободна от воспалительных клеток.
(любезно предоставлено доктором Дж. Х. Саймоном)
В результате воздействия на полость рта и кариеса пульпа содержит бактерии и их побочные продукты. Пульпа зуба обычно не может устранить эти повреждающие раздражители. В лучшем случае защитные механизмы временно препятствуют распространению инфекции и разрушению тканей. Если раздражители сохраняются, последующее повреждение становится обширным и распространяется по всей пульпе. Впоследствии бактерии или их побочные продукты и другие раздражители из некротизированной пульпы диффундируют из канала периапикально, что приводит к развитию воспалительных поражений (рис. 4.6).
Рис. 4.6Выход раздражителей (закрашенная стрелка) из корневого канала в периапикальную ткань вызывает воспаление (незаштрихованная стрелка) и замещение нормальных периапикальных структур гранулематозной тканью.
Бактерии играют важную роль в патогенезе пульповых и перирадикулярных заболеваний. В ряде исследований установлено, что пульпарный или перирадикулярный патоз не развивается без наличия бактериальной контаминации. Какехаши и его коллеги создали обнажение пульпы у обычных и безмикробных крыс. Эта процедура у стерильных крыс вызывала лишь минимальное воспаление в течение 72-дневного периода исследования. Ткань пульпы у этих животных не была девитализована, а к 14 дню формировался кальцифицирующий мостик с нормальной тканью на вершине дентинного мостика (рис. 4.7, 9).1843 А ). Напротив, у обычных крыс инфекция, некроз пульпы и образование абсцесса происходили к восьмому дню (рис. 4.7, B ). Другие исследователи изучали роль бактерий в развитии перирадикулярных поражений путем герметизации неинфицированных и инфицированных пульп в корневых каналах обезьян. Через 6-7 месяцев клинические, рентгенографические и гистологические исследования зубов, запломбированных неинфицированной пульпой, показали отсутствие патологии в апикальных тканях, тогда как зубы, запломбированные некротизированной пульпой, содержащей определенные бактерии, показали периапикальное воспаление.
В ряде исследований установлено, что пульпарный или перирадикулярный патоз не развивается без наличия бактериальной контаминации. Какехаши и его коллеги создали обнажение пульпы у обычных и безмикробных крыс. Эта процедура у стерильных крыс вызывала лишь минимальное воспаление в течение 72-дневного периода исследования. Ткань пульпы у этих животных не была девитализована, а к 14 дню формировался кальцифицирующий мостик с нормальной тканью на вершине дентинного мостика (рис. 4.7, 9).1843 А ). Напротив, у обычных крыс инфекция, некроз пульпы и образование абсцесса происходили к восьмому дню (рис. 4.7, B ). Другие исследователи изучали роль бактерий в развитии перирадикулярных поражений путем герметизации неинфицированных и инфицированных пульп в корневых каналах обезьян. Через 6-7 месяцев клинические, рентгенографические и гистологические исследования зубов, запломбированных неинфицированной пульпой, показали отсутствие патологии в апикальных тканях, тогда как зубы, запломбированные некротизированной пульпой, содержащей определенные бактерии, показали периапикальное воспаление. Бактериологическое исследование, проведенное Сундквистом по изучению флоры некротизированной пульпы человека, подтверждает выводы Какехаши и его коллег, а также Мёллера и коллег. В этих исследованиях изучались ранее травмированные зубы с некротизированной пульпой, с апикальным поражением и без него. Зубы без апикальных поражений были асептическими, в то время как зубы с периапикальным поражением имели положительные бактериальные культуры.
Бактериологическое исследование, проведенное Сундквистом по изучению флоры некротизированной пульпы человека, подтверждает выводы Какехаши и его коллег, а также Мёллера и коллег. В этих исследованиях изучались ранее травмированные зубы с некротизированной пульпой, с апикальным поражением и без него. Зубы без апикальных поражений были асептическими, в то время как зубы с периапикальным поражением имели положительные бактериальные культуры.
A, В обнаженной пульпе (P) стерильной крысы воспаления не наблюдается. Пищевые частицы и другой мусор (D) упакованы в камеру. B, Периапикальное поражение видно у обычной крысы после обнажения пульпы.
(любезно предоставлено доктором Х. Стэнли)
Недавние исследования показали положительную корреляцию между присутствием некоторых вирусов и симптоматическими апикальными патологиями. Периапикальные поражения, содержащие цитомегаловирус (ЦМВ) и вирус Эпштейна-Барра (ВЭБ), с большей вероятностью будут симптоматическими, чем поражения, не содержащие эти вирусы. Хотя некоторые исследователи предполагают прямую этиологическую роль, эту причинно-следственную связь еще предстоит продемонстрировать на экспериментальных моделях.
Хотя некоторые исследователи предполагают прямую этиологическую роль, эту причинно-следственную связь еще предстоит продемонстрировать на экспериментальных моделях.
Было предложено несколько механизмов идентификации бактерий как раздражителей иммунной системы. Обнаружение этих патогенов может происходить посредством взаимодействия между патоген-ассоциированными молекулярными паттернами (PAMP) и специфическими рецепторами, широко известными как рецепторы распознавания паттернов (PRR). PRR распознают PAMP и инициируют защиту хозяина. Связанные с G-белком рецепторы и Toll-подобные рецепторы (TLR) являются частью врожденного иммунного ответа и активируют фагоцитарные функции, обеспечивая проглатывание микробами. Рецепторы, связанные с G-белком, связываются с хемокинами, липидными медиаторами (например, фактором активации тромбоцитов, простагландином E2 и лейкотриеном B 9).0137 4 ) или бактериальные белки, вызывающие экстравазацию лейкоцитов и продукцию бактерицидных веществ. TLR представляют собой трансмембранные белки, которые экспрессируются клетками врожденной иммунной системы. Эти рецепторы распознают вторгшиеся микробы и активируют сигнальные пути, которые запускают иммунные и воспалительные реакции для уничтожения захватчиков. На сегодняшний день обнаружено не менее 13 TLR с различными способностями к распознаванию. В таблице 4.1 представлены некоторые из идентифицированных в настоящее время TLR и их специфические взаимодействия.
TLR представляют собой трансмембранные белки, которые экспрессируются клетками врожденной иммунной системы. Эти рецепторы распознают вторгшиеся микробы и активируют сигнальные пути, которые запускают иммунные и воспалительные реакции для уничтожения захватчиков. На сегодняшний день обнаружено не менее 13 TLR с различными способностями к распознаванию. В таблице 4.1 представлены некоторые из идентифицированных в настоящее время TLR и их специфические взаимодействия.
Таблица 4.1
Примеры Toll-подобных рецепторов (TLR) и связанных с ними активаторов
| PAMP | ПРР | Патоген |
|---|---|---|
| ЛПС, липид А | TLR4 | Грамотрицательные бактерии |
| Флагеллин | TLR5 | Бактерии жгутиковые |
| дцРНК | TLR3 | Вирус |
| одноцепочечная РНК | TLR7,8 | Вирус |
| ДНК CpG | TLR9 | Бактерии, ДНК |
| ПАМП | ПРР | Патоген |
PAMP, Патоген-ассоциированные молекулярные структуры; PRR, рецепторов распознавания образов.
Патоз пульпы
Помимо анатомической конфигурации и разнообразия наносимых раздражителей, пульпа реагирует на эти раздражители так же, как и другие соединительные ткани. Здоровая пульпа обладает огромной способностью к самовосстановлению и заживлению; однако часто со временем и при воздействии раздражителей ткань пульпы повреждается из-за состояния воспаления или фиброза. Повреждение пульпы приводит к гибели клеток и воспалению. Степень воспаления пропорциональна интенсивности и тяжести повреждения тканей. Легкие травмы, такие как начальный кариес или препарирование неглубоких полостей, вызывают незначительное воспаление пульпы или не вызывают его вовсе. Напротив, глубокий кариес, обширные оперативные вмешательства или постоянные раздражители обычно вызывают более тяжелые воспалительные изменения. В зависимости от тяжести и продолжительности повреждения и способности хозяина реагировать, реакция пульпы варьирует от преходящего воспаления (обратимый пульпит) до необратимого пульпита, а затем до полного некроза. Эти изменения часто происходят без боли и без ведома пациента или стоматолога.
Эти изменения часто происходят без боли и без ведома пациента или стоматолога.
Воспалительный процесс
Дентин действует как физический барьер против ирригантов и предотвращает прямой контакт между воспалительными клетками, присутствующими в пульпе, и раздражителями, такими как бактерии. Когда толщина оставшегося дентина составляет менее 1,1–1,5 мм (например, из-за кариеса), количество воспалительных клеток в пульпе увеличивается.
Раздражение пульпы зуба приводит к активации различных биологических систем, таких как неспецифические воспалительные реакции, опосредованные метаболитами гистамина, брадикинина и арахидоновой кислоты. Также высвобождаются продукты лизосомальных гранул PMN (эластаза, катепсин G и лактоферрин); ингибиторы протеазы (например, антитрипсин); и нейропептиды (например, пептид, родственный гену кальцитонина [CGRP] и субстанция P [SP]). Фагоциты не требуются до тех пор, пока не произойдет прямой контакт между кариесом и пульпой; на самом деле, пока толщина дентина остается более 2 мм, экспрессия генов, связанных с PMN, не повышается.
В отличие от соединительной ткани в других частях тела, нормальная и здоровая пульпа зубов не содержит тучных клеток. Однако эти клетки обнаруживаются в воспаленной пульпе (рис. 4.8). Тучные клетки содержат гистамин, лейкотриены и факторы, активирующие тромбоциты. Физическое повреждение тучных клеток или связывание двух молекул иммуноглобулина Е (IgE) антигеном на их клеточных поверхностях приводит к высвобождению гистамина и/или других биоактивных веществ, присутствующих в гранулах тучных клеток. Присутствие гистамина в стенках кровеносных сосудов и заметное повышение уровня гистамина указывают на важность гистамина при воспалении пульпы.
Рис. 4.8Тучные клетки хорошо видны в виде окрашенных в темный цвет клеток в этой воспаленной пульпе человеческого зуба.
Кинины, вызывающие множество признаков и симптомов острого воспаления, образуются при контакте калликреинов плазмы или тканей с кининогенами. Брадикинин, SP и нейрокинин А были идентифицированы в ткани пульпы зуба с помощью высокоэффективной жидкостной хроматографии. В исследовании in vitro брадикинин вызывал высвобождение иммунореактивного CGRP (iCGRP) из пульпы бычьих зубов; эта активность усиливается простагландином E2 (PGE 2 ). В результате повреждения клеток фосфолипаза А2 вызывает высвобождение арахидоновой кислоты из клеточных мембран. Метаболизм арахидоновой кислоты приводит к образованию простагландинов, тромбоксанов и лейкотриенов. Различные метаболиты арахидоновой кислоты были обнаружены при экспериментально индуцированном пульпите. Наличие этих метаболитов в воспаленной пульпе свидетельствует об участии метаболитов арахидоновой кислоты в воспалительных реакциях пульпы зуба.
В исследовании in vitro брадикинин вызывал высвобождение иммунореактивного CGRP (iCGRP) из пульпы бычьих зубов; эта активность усиливается простагландином E2 (PGE 2 ). В результате повреждения клеток фосфолипаза А2 вызывает высвобождение арахидоновой кислоты из клеточных мембран. Метаболизм арахидоновой кислоты приводит к образованию простагландинов, тромбоксанов и лейкотриенов. Различные метаболиты арахидоновой кислоты были обнаружены при экспериментально индуцированном пульпите. Наличие этих метаболитов в воспаленной пульпе свидетельствует об участии метаболитов арахидоновой кислоты в воспалительных реакциях пульпы зуба.
Пульпа зуба плотно иннервирована чувствительными волокнами, содержащими иммуномодулирующие нейропептиды, такие как SP и CGRP. Исследования показали, что денервация пульпы моляра крысы, вызванная аксотомией нижнего альвеолярного нерва, приводит к усилению повреждения ткани пульпы и уменьшению инфильтрации иммунокомпетентных клеток. Эти данные указывают на то, что пульповые нервы носят защитный характер и могут участвовать в рекрутировании воспалительных и иммунокомпетентных клеток в поврежденную пульпу.
Повреждения пульпы легкой и средней степени тяжести приводят к прорастанию чувствительных нервов с увеличением iCGRP. Однако тяжелые травмы имеют противоположный эффект, приводя либо к снижению, либо к полному исчезновению iCGRP и SP. Эксперименты показывают, что нейропептиды пульпы претерпевают динамические изменения после травмы. Кроме того, недавние исследования показали, что стимуляция пульпы зуба кариесом приводит к образованию различных интерлейкинов и привлечению воспалительных клеток к месту повреждения.
Иммунологические ответы
При начальной инвазии пульпо-дентинного комплекса микробными раздражителями активируется врожденная иммунная система. Врожденная иммунная система доступна сразу и не требует сложного метода отбора клеток, которые реагируют на захватчиков, а не на хозяина, и нет существования или развития памяти. Если врожденный иммунный ответ не может устранить повреждение, в игру вступает адаптивная иммунная система с клеточным и специфическим ответом антител.
Дендритные клетки (ДК) являются главными регуляторами иммунной системы и присутствуют в нормальной пульпе и разбросаны по ней. В здоровой пульпе одонтобласты представляют собой клетки, непосредственно контактирующие с вышележащим дентином. Когда пульпа раздражена, одонтобластные отростки ощущают инвазию и вызывают рекрутирование ДК. ДК фагоцитируют захватчиков и представляют антигены для стимуляции Т-лимфоцитов.
В дополнение к неспецифическим воспалительным реакциям иммунные реакции также могут инициировать и закреплять вредные изменения пульпы. Потенциальные антигены включают бактерии и их побочные продукты внутри кариеса зубов, которые непосредственно (или через дентинные канальцы) могут инициировать различные типы реакций. Нормальная и невоспаленная пульпа зуба содержит иммунокомпетентные клетки, такие как Т- и В-лимфоциты (в меньшем количестве), макрофаги и значительное количество дендритных клеток, экспрессирующих молекулы класса II, которые морфологически сходны с макрофагами. Повышенный уровень иммуноглобулинов в воспаленной пульпе (рис. 4.9).) показывают, что эти факторы участвуют в защитных механизмах, участвующих в защите этой ткани. Реакции типа Артюса встречаются в пульпе зуба. Кроме того, присутствие в воспаленной пульпе иммунокомпетентных клеток, таких как Т-лимфоциты, макрофаги и клетки, экспрессирующие молекулы класса II, которые выглядят как дендритные клетки (рис. 4.10), указывает на то, что в этой ткани также могут возникать отсроченные реакции гиперчувствительности. Несмотря на свои защитные механизмы, иммунные реакции в пульпе могут привести к образованию небольших очагов некроза и, в конечном итоге, к полному некрозу пульпы.
Повышенный уровень иммуноглобулинов в воспаленной пульпе (рис. 4.9).) показывают, что эти факторы участвуют в защитных механизмах, участвующих в защите этой ткани. Реакции типа Артюса встречаются в пульпе зуба. Кроме того, присутствие в воспаленной пульпе иммунокомпетентных клеток, таких как Т-лимфоциты, макрофаги и клетки, экспрессирующие молекулы класса II, которые выглядят как дендритные клетки (рис. 4.10), указывает на то, что в этой ткани также могут возникать отсроченные реакции гиперчувствительности. Несмотря на свои защитные механизмы, иммунные реакции в пульпе могут привести к образованию небольших очагов некроза и, в конечном итоге, к полному некрозу пульпы.
Некоторые плазматические клетки положительно окрашиваются на IgM в воспаленной пульпе зуба человека, что указывает на иммунологическую активность.
Рис. 4.10Много дендритных клеток (стрелки) присутствуют в воспаленной пульпе зуба.
(любезно предоставлено доктором М. Джонтеллом)
Прогрессирование поражения
Легкие травмы могут не привести к значительным изменениям пульпы. Однако повреждения пульпы от средней до тяжелой степени приводят к локализованному воспалению и высвобождению высокой концентрации медиаторов воспаления. Увеличение количества ингибиторов протеазы в пульпе со средним и сильным воспалением указывает на наличие естественных модификаторов. Вследствие выброса большого количества медиаторов воспаления возникают повышение проницаемости сосудов, сосудистый стаз, миграция лейкоцитов к месту повреждения. Данные текущих исследований показывают, что сенсорный нейропептид, CGRP, отвечает за увеличение кровотока при воспалении пульпы.
Однако повреждения пульпы от средней до тяжелой степени приводят к локализованному воспалению и высвобождению высокой концентрации медиаторов воспаления. Увеличение количества ингибиторов протеазы в пульпе со средним и сильным воспалением указывает на наличие естественных модификаторов. Вследствие выброса большого количества медиаторов воспаления возникают повышение проницаемости сосудов, сосудистый стаз, миграция лейкоцитов к месту повреждения. Данные текущих исследований показывают, что сенсорный нейропептид, CGRP, отвечает за увеличение кровотока при воспалении пульпы.
Повышенное капиллярное давление и повышенная проницаемость капилляров перемещают жидкости из кровеносных сосудов в окружающие ткани. Если удаление жидкости венулами и лимфатическими путями не совпадает с фильтрацией капилляров, образуется экссудат. Пульпа заключена в жесткие окружающие ткани, образуя систему с низкой податливостью; поэтому небольшое повышение тканевого давления вызывает пассивную компрессию и даже полный коллапс венул в месте повреждения пульпы. Повышение давления происходит в небольших «разделенных» областях и прогрессирует медленно. Следовательно, пульпа зуба не дегенерирует при сильном повышении давления с последующим странгуляцией.
Повышение давления происходит в небольших «разделенных» областях и прогрессирует медленно. Следовательно, пульпа зуба не дегенерирует при сильном повышении давления с последующим странгуляцией.
Боль часто вызывается несколькими факторами. Высвобождение медиаторов воспаления вызывает болевой синдром непосредственно за счет снижения порога чувствительных нервов. Эти вещества также вызывают боль опосредованно за счет увеличения как вазодилатации артериол, так и проницаемости сосудов венул, что приводит к отеку и повышению тканевого давления. Это давление действует непосредственно на сенсорные нервные рецепторы.
Повышенное тканевое давление, неспособность пульпы к расширению и отсутствие коллатерального кровообращения могут привести к некрозу пульпы и развитию последующего перирадикулярного патологии.
Классификация болезней пульпы
Поскольку корреляция между гистологическими данными о патологии пульпы и клиническими симптомами незначительна или отсутствует, диагностика и классификация заболеваний пульпы основываются на клинических признаках и симптомах, а не на гистопатологических данных. Состояние пульпы можно классифицировать как нормальную пульпу, обратимый и необратимый пульпит, гиперпластический пульпит, некроз и ранее леченную пульпу. Реакции твердых тканей включают кальцификацию и резорбцию.
Состояние пульпы можно классифицировать как нормальную пульпу, обратимый и необратимый пульпит, гиперпластический пульпит, некроз и ранее леченную пульпу. Реакции твердых тканей включают кальцификацию и резорбцию.
Обычная целлюлоза
Зуб с нормальной пульпой клинически не проявляет симптомов и нормально реагирует на тесты на жизнеспособность. В таком зубе не выявляют рентгенологических признаков патологии.
Обратимый пульпит
По определению, обратимый пульпит представляет собой клиническое состояние, связанное с субъективными и объективными данными, указывающими на наличие легкого воспаления в ткани пульпы. Если причина устранена, воспаление прекращается, и пульпа возвращается в нормальное состояние.
Слабые или кратковременные раздражители могут вызвать обратимый пульпит, такой как начальный кариес, эрозия шейки матки или окклюзионная стираемость; большинство оперативных процедур; глубокий пародонтальный кюретаж; и переломы эмали, приводящие к обнажению дентинных канальцев.
Симптомы
Обратимый пульпит обычно протекает бессимптомно. Однако, когда они присутствуют, симптомы обычно следуют определенной схеме. Применение раздражителей, таких как холодная или горячая жидкость или воздух, может вызвать острую преходящую боль. Удаление этих раздражителей, которые обычно не вызывают боли или дискомфорта, приводит к немедленному облегчению. Холодные и горячие раздражители вызывают разные болевые реакции в нормальной пульпе. При воздействии тепла на зубы с невоспаленной пульпой первоначальная реакция задерживается; интенсивность болей нарастает по мере повышения температуры. Напротив, боль в нормальной пульпе в ответ на холод проявляется немедленно; интенсивность имеет тенденцию к снижению, если холодовой раздражитель сохраняется. Основываясь на этих наблюдениях, реакции пульпы как в норме, так и при болезни, по-видимому, в значительной степени являются результатом изменений внутрипульпарного давления.
Лечение
Удаление раздражающих веществ, а также герметизация и изоляция обнаженного дентина или пульпы обычно приводят к уменьшению симптомов и купированию воспалительного процесса в ткани пульпы (рис. 4.11). Тем не менее, если раздражение пульпы продолжается или усиливается по причинам, изложенным ранее, развивается воспаление от умеренного до тяжелого, что приводит к необратимому пульпиту и, в конечном итоге, к некрозу пульпы.
4.11). Тем не менее, если раздражение пульпы продолжается или усиливается по причинам, изложенным ранее, развивается воспаление от умеренного до тяжелого, что приводит к необратимому пульпиту и, в конечном итоге, к некрозу пульпы.
A, Механически обнаженные рога пульпы нижнечелюстного моляра с признаками обратимого пульпита были закрыты минеральным триоксидным агрегатом. B, Рентгенограмма сразу после операции. C, Контрольная рентгенограмма через 5 лет показывает отсутствие метаморфоза кальцификации в пульповой камере, закрытие апексов и нормальную реакцию при клиническом обследовании.
Необратимый пульпит
Необратимый пульпит может быть классифицирован как симптоматический или бессимптомный. Это клиническое состояние, связанное с субъективными и объективными данными, указывающими на наличие тяжелого воспаления в ткани пульпы. Необратимый пульпит часто является следствием обратимого пульпита или его прогрессированием. Серьезное повреждение пульпы из-за обширного удаления дентина во время оперативных вмешательств или нарушения кровотока в пульпе в результате травмы или ортодонтического смещения зубов также может вызвать необратимый пульпит. Необратимый пульпит – это тяжелый воспалительный процесс, который не проходит, даже если устранить причину. Пульпа неспособна к заживлению и медленно или быстро некротизируется. Необратимый пульпит может быть симптоматическим со спонтанной и затяжной болью. Он также может протекать бессимптомно, без клинических признаков и симптомов.
Необратимый пульпит – это тяжелый воспалительный процесс, который не проходит, даже если устранить причину. Пульпа неспособна к заживлению и медленно или быстро некротизируется. Необратимый пульпит может быть симптоматическим со спонтанной и затяжной болью. Он также может протекать бессимптомно, без клинических признаков и симптомов.
Симптомы
Необратимый пульпит обычно протекает бессимптомно. Однако пациенты могут сообщать о легких симптомах. Необратимый пульпит также может быть связан с периодическими или постоянными эпизодами спонтанной боли (без внешних раздражителей). Боль, возникающая в результате необратимого воспаления пульпы, может быть острой, тупой, локализованной или диффузной и может длиться от нескольких минут до нескольких часов. Локализация боли в пульпе более трудна, чем локализация перирадикулярной боли, и усложняется по мере усиления боли. Применение внешних раздражителей, таких как холод или тепло, может привести к длительной боли.
Соответственно, при наличии сильной боли реакция пульпы отличается от реакции невоспаленных зубов или зубов с обратимым пульпитом. Например, воздействие тепла на зубы с необратимым пульпитом может вызвать немедленную реакцию; также иногда при применении холода реакция не исчезает и продлевается. Применение холода у пациентов с болезненным необратимым пульпитом может вызвать сужение сосудов, падение давления в пульпе и последующее облегчение боли. Хотя было заявлено, что зубы с необратимым пульпитом имеют более низкие пороги к электрической стимуляции, Мамфорд обнаружил сходные пороги восприятия боли в воспаленной и невоспаленной пульпе.
Например, воздействие тепла на зубы с необратимым пульпитом может вызвать немедленную реакцию; также иногда при применении холода реакция не исчезает и продлевается. Применение холода у пациентов с болезненным необратимым пульпитом может вызвать сужение сосудов, падение давления в пульпе и последующее облегчение боли. Хотя было заявлено, что зубы с необратимым пульпитом имеют более низкие пороги к электрической стимуляции, Мамфорд обнаружил сходные пороги восприятия боли в воспаленной и невоспаленной пульпе.
Анализы и лечение
Если воспаление ограничено пульпой и не распространяется периапикально, зубы реагируют в пределах нормы на пальпацию и перкуссию. Распространение воспаления на ПДС вызывает перкуторную чувствительность и позволяет лучше локализовать боль. Лечение или удаление корневых каналов показано для зубов с признаками и симптомами необратимого пульпита.
Гиперпластический пульпит
Только обладатели статуса Gold могут продолжить чтение. Войдите или зарегистрируйтесь, чтобы продолжить
Войдите или зарегистрируйтесь, чтобы продолжить
Острая зубная боль I: боль в пульпе и дентине
Тема: Смерть и смерть
Vitenskap
Матти Нари, Ларс Бьорндал, Мария Пигг, Инге Фристад и Сиваками Ретнам Хауг
Настоящая статья, обзор, целью которого является обновление информации для читателя. на современные знания о пульповой и дентинной боли, является первым в цикл статей на тему «Боль и управление болью».
Специализированная анатомия пульпо-дентинного комплекса и плотных, преимущественно ноцицептивная иннервация пульпы из тройничного нерва нерва объясняют разнообразием болевых ощущений от этого органа.
Кратковременная острая боль типична для боли, опосредованной А-волокнами, в то время как длительная,
тупая/ноющая боль указывает на поражение С-волокон. А-волокна реагируют на
холодные или механические раздражители, такие как холодные напитки или чистка зубов,
в то время как С-волокна в основном активируются медиаторами воспаления. Таким образом,
затяжная боль предполагает наличие необратимого воспаления пульпы.
Таким образом,
затяжная боль предполагает наличие необратимого воспаления пульпы.
При пульпите структурные изменения нервов пульпы (прорастание) происходит, и высвобождение нейропептида вызывает иммунный ответ; нейрогенный воспаление. Болевые ощущения при пульпите могут варьироваться от гиперчувствительности к тепловым раздражителям до сильной пульсирующей, ноющей боли, которая может быть направленный и часто трудно локализуемый, что затрудняет диагностику Ситуация для клинициста.
Поверхностная биопленка усиливает гиперчувствительность открытых поверхностей дентина
потому что раздражители достигают пульпы через открытые канальцы дентина, вызывая
воспаление. Удаление биопленки снижает гиперчувствительность дентина
но дополнительное лечение, направленное на снижение проницаемости дентина,
часто необходимо. Лечение кариеса и пломбирование адекватны
при обратимом пульпите, если пульпа сохранила свою способность
дистанцироваться от бактериальной атаки, производя репаративные
дентин. Однако эндодонтическое лечение необходимо при наличии пульпита.
достигла необратимой стадии.
Однако эндодонтическое лечение необходимо при наличии пульпита.
достигла необратимой стадии.
Боль, локализованная в зубах, является одной из наиболее частых орофациальных болей. жалобы на боль, с распространенностью 12% в общей популяции в течение 6 месяцев (1). Зубная боль может быть связана с различными состояний, которые могут быть острыми или хроническими по своей природе, местными или системного происхождения, но чаще всего является признаком повреждения или заболевание зуба или окружающих его тканей. Хорошее понимание структур и механизмов, лежащих в основе болезненных ощущений. обязательным условием для лечения боли.
Иннервация пульпы и дентина
Пульпа зуба находится в жесткой капсуле, состоящей из дентина
и эмаль. Это создает несовместимую среду, которая делает
ткань пульпы уникальна (2, 3). Пульпа зуба богато иннервирована
преимущественно аксонами тройничного нерва, преимущественно чувствительными
носит характер и в основном направлен на восприятие боли (ноцицепцию). Меньшая популяция пульповых нервов относится к вегетативным симпатическим нервам.
волокна, отходящие от верхнего шейного ганглия и связанные с
сужение сосудов пульпы (4).
Меньшая популяция пульповых нервов относится к вегетативным симпатическим нервам.
волокна, отходящие от верхнего шейного ганглия и связанные с
сужение сосудов пульпы (4).
Чрезвычайно сильная боль — достигает максимальной интенсивности при любой боли
оценка — может быть вызвана активацией внутризубных нервов (5 —
7). Столь интенсивные болевые реакции можно объяснить плотным (рис.
1 и 2) и преимущественно ноцицептивной иннервацией пульпы и
дентин (6, 8). Передача болевых раздражителей через
дентин с его обнаженной поверхности исключительно эффективен и позволяет
даже очень легкие раздражители, такие как струя воздуха и зондирование, должны быть усилены
способ, который может вызвать повреждение тканей и последующую активацию нерва
на границе пульпа-дентин (5). Каждый зуб иннервируется примерно
тысяча аксонов тройничного нерва (9- 11), которые могли разветвляться раньше
входит в апикальное отверстие и может иннервировать более одного зуба.
В корешковой пульпе нервные волокна собраны в пучки, но
как только они достигают коронковой пульпы (8, 12, 13), они делятся на более мелкие
связки. Затем аксоны сильно разветвляются, и каждый может образовывать 50
— 100 терминалей в периферической пульпе, образующих сеть под
слой одонтобластов, известный как сплетение Рашкова. Плотность
нервных окончаний особенно высоко в рогах пульпы, где
до 50 % дентинных канальцев иннервированы. Многие из
канальцы содержат несколько нервных окончаний (8). Есть примерно
20 000 — 30 000 ноцицептивных нервных окончаний/мм2 в пульпе-дентине
пограничная область в самой коронковой пульпе, на которую приходится чрезвычайно
высокая чувствительность дентина.
Затем аксоны сильно разветвляются, и каждый может образовывать 50
— 100 терминалей в периферической пульпе, образующих сеть под
слой одонтобластов, известный как сплетение Рашкова. Плотность
нервных окончаний особенно высоко в рогах пульпы, где
до 50 % дентинных канальцев иннервированы. Многие из
канальцы содержат несколько нервных окончаний (8). Есть примерно
20 000 — 30 000 ноцицептивных нервных окончаний/мм2 в пульпе-дентине
пограничная область в самой коронковой пульпе, на которую приходится чрезвычайно
высокая чувствительность дентина.
Рисунок 1. Схематическое представление
внутризубной иннервации. Нервные пучки входят в пульпу
через апикальное отверстие/отверстия и широко разветвляются, особенно
в коронковой пульпе. Пограничная зона пульпы и дентина на периферии
пульпа (кончики пульпы) представляет собой наиболее плотно иннервированную область, где
нервные окончания также простираются на самое большое расстояние (100–150 мкм) в
дентинные канальцы.
Рис. 2. Иллюстрация показывающее распределение внутризубных А- и С-волокон.
Немиелинизированные С-волокна расположены в собственно пульпе, тогда как миелинизированные А-волокна широко распространены в дентине пульпы граница, проникающая во внутреннюю часть дентина.
Типы нервных волокон: А- и С-волокна, их функции отличия
Различают как миелинизированные (20 — 25 %), так и немиелинизированные (75 —
80 %) афферентные нервные волокна в пульпе (8, 12, 13). Эти два волокна
группы сильно различаются по своим функциональным свойствам (6, 7, 14,
15). Миелинизированные волокна относятся преимущественно к Ad-, но a
часть из них относятся к Ab-группе и являются быстропроводящими (от 3 до 50
— 60 м/с (6, 7, 14, 15). Окончания А-волокон расположены в
периферическая пульпа и внутренний дентин (рис. 1, 2 и табл. 1). Они
ответственны за чувствительность дентина, и их активация в
здоровые зубы вызывают острую и обычно непродолжительную боль, а не
пережить раздражитель (5 — 7, 16).
Существует также ряд более крупных Ad-волокон (примерно 10 %, попадающих в пульпу на верхушке). Они не активны в здоровая пульпа, но становятся активными при наличии воспаления. Этот является примером «периферической сенсибилизации», когда обычно неповрежденный нерв волокна рекрутируются в болевой системе. Все чувствительные нервные волокна которые входят в ветвь пульпы и сужаются по мере продвижения к роговой слой пульпы. В четыре раза больше нервных волокон можно насчитать на уровне середины коронки пульпы, чем на апикальном уровне. Миелинизированный нерв волокна обычно имеют немиелинизированные окончания, что затрудняет дифференцировать окончания быстрых и медленных волокон (13, 17).
Немиелинизированные нервы представляют собой С-волокна с низкой скоростью проведения.
(0,5 — 2,5 м/с), а их окончания располагаются в самой пульпе.
Они преимущественно сенсорные с небольшой популяцией симпатиков.
(10%). Большинство (70 %) аксонов, входящих в верхушку, представляют собой С-волокна.
С клинической точки зрения зрения важно отметить, что резкое, кратковременное, не затяжное, боль из-за стимуляции обнаженного дентина может быть вызвана пульпа здорова или имеет незначительные обратимые повреждения и, таким образом, может успешно можно обойтись без лечения корневых каналов.
С-волокна являются полимодальными и реагируют на несколько различных вредных воздействий. раздражители. В других местах они активируются сильным жаром и холодом. и многие медиаторы воспаления, такие как гистамин и брадикинин (7). В пульпе они активируются при воспалении и все чаще так что на поздних стадиях (7). Кажется, они могут проводить тупая боль или боль при воспалении пульпы (5, 7).
Учитывая ответ характеристики С-волокон, можно сделать вывод, что их активация, вызывая тупую ноющую боль, которая часто является длительной или затяжной в природе, может указывать на то, что пульпа необратимо повреждена и может потребоваться лечение корневых каналов.
Кроме того, нервные волокна выделяют биологически активные пептиды, известные
как нейропептиды, влияющие на нервную активность и функционирование
(18). Нейропептиды в пульпе зуба высвобождаются из нерва.
терминали преимущественно А?- и С-волокон. Существует множество нейропептидов
в пульпе зуба, которые обычно классифицируются как сенсорные, симпатические
или парасимпатические по происхождению нервных волокон. Сенсорный
Симпатические нейропептиды синтезируются в тройничном нерве.
и верхний шейный ганглий соответственно (19).
Нейропептиды в пульпе зуба высвобождаются из нерва.
терминали преимущественно А?- и С-волокон. Существует множество нейропептидов
в пульпе зуба, которые обычно классифицируются как сенсорные, симпатические
или парасимпатические по происхождению нервных волокон. Сенсорный
Симпатические нейропептиды синтезируются в тройничном нерве.
и верхний шейный ганглий соответственно (19).
Сенсорные нейропептиды, например, пептид, родственный гену кальцитонина (CGRP),
вещество P (SP) и нейрокинин A. Нейропептид Y (NPY) высвобождается совместно
с норадреналином из симпатических нервных окончаний. Большинство
обильным нейропептидом в пульпе зуба является CGRP, за которым следует SP.
CGRP является сосудорасширяющим средством, в то время как SP увеличивает проницаемость капилляров.
NPY является вазоконстриктором и модулирует иммунную функцию (20).
При введении в кровоток в экспериментальных исследованиях CGRP,
SP и NKA вызывают вазодилатацию (21), в то время как активация пульпарного
нервы с помощью электрической стимуляции вызывает длительную вазодилатацию
в пульпе за счет высвобождения CGRP (22 — 24).
Изменения функции нерва при воспалении, нейрогенное воспаление, медиаторы воспаления
Структурные изменения нервных волокон возникают в ответ на воспаление.
Нервные волокна сильно разветвляются или разветвляются (25, 26), тем самым увеличивая
высвобождение нейропептидов приводит к «нейрогенному воспалению».
CGRP и SP повышены на начальных стадиях воспаления пульпы,
тогда как NPY увеличивается на хронических стадиях (27). Высвобождены нейропептиды
от чувствительных нейронов действуют не только на сосудистую сеть, но и непосредственно
привлекать и активировать врожденные иммунные клетки (дендритные клетки) и адаптивные
иммунные клетки (Т-лимфоциты) (28, 29). Как только иммунные клетки рекрутируются
к месту воспаления медиаторы воспаления, такие как цитокины,
гистамин, брадикинин, простагландины, лейкотриены и многие
выделяются другие вещества. Прорастание нейронов увеличивает количество нейропептидов
содержание и высвобождение, что приводит к нейрогенному воспалению (30, 31). Рисунок 3 схематично иллюстрирует 5 этапов изменений в
дентинно-пульпарный комплекс в зависимости от прогрессирования кариеса, возможные симптомы
и предложил лечение. Кариес, даже ограниченный слоем эмали
может уже оказывать некоторое незначительное воздействие на пульпу зуба (5), например.
с точки зрения нейрогенного воспаления и начала склероза дентина
может произойти, что соответствует альтерации вдоль одонтобласта
слой (32) (Стадия 1). Прорастание сенсорного нейропептида, содержащего
нервных волокон возникает при более глубоких кариозных поражениях (стадия 2 и 3)
совпадающая с гипер- и термической чувствительностью зуба (26, 31,
33). Это прорастание является обратимым и спадает до нормального после кариеса.
арест или восстановление. Раздражение пульпы зуба из-за
кариес приводит к образованию репаративного дентина одонтобластами. С
прогрессирование кариеса (4 стадия), возможны локальные микроабсцессы
формируются в пульпе зуба с прорастанием нервных волокон. Есть
также увеличивает высвобождение нейропептидов (34).
Рисунок 3 схематично иллюстрирует 5 этапов изменений в
дентинно-пульпарный комплекс в зависимости от прогрессирования кариеса, возможные симптомы
и предложил лечение. Кариес, даже ограниченный слоем эмали
может уже оказывать некоторое незначительное воздействие на пульпу зуба (5), например.
с точки зрения нейрогенного воспаления и начала склероза дентина
может произойти, что соответствует альтерации вдоль одонтобласта
слой (32) (Стадия 1). Прорастание сенсорного нейропептида, содержащего
нервных волокон возникает при более глубоких кариозных поражениях (стадия 2 и 3)
совпадающая с гипер- и термической чувствительностью зуба (26, 31,
33). Это прорастание является обратимым и спадает до нормального после кариеса.
арест или восстановление. Раздражение пульпы зуба из-за
кариес приводит к образованию репаративного дентина одонтобластами. С
прогрессирование кариеса (4 стадия), возможны локальные микроабсцессы
формируются в пульпе зуба с прорастанием нервных волокон. Есть
также увеличивает высвобождение нейропептидов (34).
Рис. 3. Схема 5 стадий развития кариеса от слоя эмали до обнажения пульпы с последующими изменениями в пульпе зуба (сосудистыми, нервными, иммунными, гистологический), возможные симптомы и предлагаемое лечение.
Повышенное высвобождение сенсорных нейропептидов в пульпе зуба вызывает вазодилатацию, что приводит к увеличению местного тканевое давление и повышенная проницаемость капилляров, что приводит к экстравазация и образование отека. Из-за неадекватного характера пульпы зуба, клинически это может ощущаться как пульсирующая боль.
По мере того, как загрязненный деминерализованный кариозный дентин достигает зубной
пульпа (стадия 5), воспаление пульпы становится обширным с частичным
некроз в сочетании с образованием репаративного дентина и витальным воспалением
пульпа апикально. Из-за потери функционального барьера против инфекции
и ограниченная способность к заживлению в коронковой части пульпы
на этой стадии некроз прогрессирует апикально. Симптомов может быть множество
и варьирует на этой стадии, а при отсутствии лечения инфекция и
воспаление прогрессирует, в конечном итоге приводя к полному некрозу пульпы
и верхушечный периодонтит.
Симптомов может быть множество
и варьирует на этой стадии, а при отсутствии лечения инфекция и
воспаление прогрессирует, в конечном итоге приводя к полному некрозу пульпы
и верхушечный периодонтит.
Механизм активации нерва в ответ на дентинную стимуляцию, чувствительность дентина
Как стимулы передаются от периферического дентина к сенсорным окончаниям расположен в области границы пульпы и дентина. предметом интереса на протяжении многих лет. Факты указывают на то, что движение жидкости в дентинных канальцах является решающим фактором в дентинных боль. Раздражители, вызывающие боль, такие как тепло, холод, воздушные потоки и т. зондирование кончиком зонда, обладают способностью вытеснять жидкость в канальцах (35, 36). Это называется гидродинамический механизм чувствительности дентина .
Гидродинамическая теория
Гидродинамическая теория предполагает, что дентинная боль, связанная с
стимуляция чувствительного зуба в конечном итоге включает механотрансдукцию. Недавно классические механотрансдукторы были обнаружены на пульпе.
афференты, обеспечивающие механистическую поддержку этой теории (37).
Таким образом, движение жидкости в дентинных канальцах преобразуется в
электрические сигналы путем активации механочувствительных ионных каналов
расположены в окончаниях аксонов. Используя методы записи по одному волокну,
выявлена положительная корреляция между степенью давления
изменяется и количество нервных импульсов, выходящих из пульпы (38 — 40).
Движение жидкости наружу (отрицательное давление) создает гораздо более сильное
нервной реакции, чем движения внутрь (36, 40).
Недавно классические механотрансдукторы были обнаружены на пульпе.
афференты, обеспечивающие механистическую поддержку этой теории (37).
Таким образом, движение жидкости в дентинных канальцах преобразуется в
электрические сигналы путем активации механочувствительных ионных каналов
расположены в окончаниях аксонов. Используя методы записи по одному волокну,
выявлена положительная корреляция между степенью давления
изменяется и количество нервных импульсов, выходящих из пульпы (38 — 40).
Движение жидкости наружу (отрицательное давление) создает гораздо более сильное
нервной реакции, чем движения внутрь (36, 40).
Кратковременное воздействие холодом или теплом на внешнюю поверхность дентина может
вызывают боль, не зависящую от изменения температуры в пульпе
(38, 41). Реакция на тепловую стимуляцию быстрая, хотя
теплопроводность дентина относительно низкая. Тепло расширяет
жидкость в канальцах, заставляя жидкость течь к пульпе,
в то время как холод заставляет жидкость сжиматься, производя внешнее
поток.
В основном А-волокна активируются быстрым смещение канальцевого содержимого (табл. 1 и рис. 1) (42). Однако С-волокна могут активироваться при нагревании (выше 43°С). Полимодальное С-волокно Ноцицепторы содержат множество рецепторов, которые реагируют на различные типы раздражителей (43, 44). В частности, рецептор, называемый «переходным экспрессируется рецепторный потенциал, подтип vanilloid 1″ или TRPV1, и реагирует на тепло выше 43°C, некоторые медиаторы воспаления, и кислоты (pH <6) (45). Эвгенол активирует и в конечном итоге снижает чувствительность TRPV1, и это может объяснить обезболивающее действие эвгенола оксида цинка. временные реставрации (46).
Таблица 1. Стимулы, способные активировать внутризубные нервы
Было также показано, что стимулы, вызывающие боль, легче
передается с поверхности дентина при обнажении отверстий канальцев
открыты, и жидкость внутри канальцев может свободно вытекать наружу.
Например, кислотная обработка обнаженного дентина для удаления мазка. слой открывает отверстия канальцев и делает дентин намного более чувствительным
к раздражителям, таким как воздушные потоки и зондирование.
слой открывает отверстия канальцев и делает дентин намного более чувствительным
к раздражителям, таким как воздушные потоки и зондирование.
Гидродинамическая теория также применима для объяснения гиперчувствительности
дентин. Был поставлен вопрос, является ли обнаженный дентин просто
чувствительным или становится действительно гиперчувствительным. Однако свидетельства указывают
экспрессируются новые натриевые каналы, способные активировать нервы
в нервной ткани, подвергшейся воспалению. Увеличение плотности
натриевых каналов или их чувствительность могут поэтому способствовать
к гиперчувствительности дентина. Гиперчувствительность обычно возникает
в пришеечной области, где обнажен дентин, потому что защитная
эмаль/цемент не сформированы или изношены или вытравлены (рис.
4 и 5). Одонтобласты и/или клетки пульпы реагируют формированием
откладываются внутриканальцевые отложения или, в конечном итоге, третичный дентин.
Это приводит к сужению или закрытию дентинных канальцев. Смещение
третичного дентина приводит к снижению проводимости по сравнению с
первичный и вторичный дентин. Кроме того, отложение третичных
дентин без вовлечения первичных одонтобластов
пульповые концы обнаженных канальцев также могут снижать чувствительность,
поскольку репаративный дентин в меньшей степени иннервируется чувствительными нервными волокнами.
Однако некоторый гиперчувствительный дентин не десенсибилизируется спонтанно,
что указывает либо на продолжающееся воспалительное изменение, либо на механические изменения
в проходимости дентинных канальцев.
Кроме того, отложение третичных
дентин без вовлечения первичных одонтобластов
пульповые концы обнаженных канальцев также могут снижать чувствительность,
поскольку репаративный дентин в меньшей степени иннервируется чувствительными нервными волокнами.
Однако некоторый гиперчувствительный дентин не десенсибилизируется спонтанно,
что указывает либо на продолжающееся воспалительное изменение, либо на механические изменения
в проходимости дентинных канальцев.
Рисунок 4. Возможный нейрогенный
механизмы, играющие роль в развитии пришеечного дентина
чувствительность: после рецессии десны внешние раздражители могут вызвать
местное воспаление на границе пульпы и дентина, приводящее к прорастанию
нервных окончаний и, как следствие, более обширная иннервация
ткани по сравнению со здоровыми зубами, что может увеличить дентин
чувствительность из-за повышенного высвобождения нейропептидов вместе
со многими другими медиаторами воспаления, которые могут повышать чувствительность
ноцицептивных нервных окончаний.
Рис. 5. Изнашиваемая грань A присутствует на щечной поверхности нижнего клыка. В связи до боли избегали гигиенических процедур. В итоге кариозный поражение начало прогрессировать на границе десны.
Гиперчувствительность дентина, развитие, профилактика и лечение
Распространенность лиц, утверждающих, что у них гиперчувствительность дентина Сообщалось о 3-57% и чаще всего у пациентов от 20 до 40 лет (47).
Бактерии и гиперчувствительность дентина
Фасетка износа или некариозное поражение шейки матки могут быть очень болезненными и
следовательно, пациент может избегать ежедневного использования этого конкретного зуба.
и процедуры гигиены полости рта. Это, в свою очередь, может перерасти даже в
более сильная боль. В случае образования биопленки бактерии
и их метаболиты проникают в дентин, вызывая местное воспаление
изменения в пульпе, включая нейрогенное воспаление, как описано
выше. Из-за боли человек может покинуть это место, не потревожившись. Это может иметь два клинических эффекта; во-первых, измененная чувствительность
нервов, которые становятся более реактивными, включая последовательность
прорастания и, во-вторых, может начаться прогрессирование кариеса
(Рисунок 5). В совокупности бактерии могут играть роль в тяжелых
гиперчувствительность дентина, где только улучшенная профессиональная чистка
шейной области может привести к значительной и постоянной боли
рельеф (48).
Это может иметь два клинических эффекта; во-первых, измененная чувствительность
нервов, которые становятся более реактивными, включая последовательность
прорастания и, во-вторых, может начаться прогрессирование кариеса
(Рисунок 5). В совокупности бактерии могут играть роль в тяжелых
гиперчувствительность дентина, где только улучшенная профессиональная чистка
шейной области может привести к значительной и постоянной боли
рельеф (48).
Ятрогенное развитие гиперчувствительности
Во время экскавации клиницист может чрезмерно растянуть препарированную полость. тем самым обнажая здоровый дентин (рис. 6), где проницаемость дентинных канальцев выше, чем в подлежащем кариозном дентине. Этот сценарий может сопровождаться неоптимальным охлаждением и обезвоживанием. дентина. Следовательно, у пациента может возникнуть тяжелая форма дентина. Гиперчувствительность после экскавации и реставрации.
Рисунок 6. Во время раскопок
кариеса обширная периферическая экскавация может привести к
к выраженной гиперчувствительности дентина после реставрации.
Роль воспаления пульпы в чувствительности дентина
А- и С-волокна пульпы могут быть сенсибилизированы многими внешними раздражителями, которые
может вызвать воспалительную реакцию в тканях пульпы. Прорастание
ноцицептивных нервных окончаний возникает в ответ на воспаление
и может расширить рецептивные поля нервных волокон (43, 49),
что может привести к увеличению перекрытия рецептивных полей (=
область, в которой при стимуляции может активироваться один нейрон).
Таким образом, стимуляция небольшого пятна, например. в дентине может привести к активации
значительно большего числа ноцицепторов пульпы и, следовательно,
повышенная чувствительность по сравнению с невоспаленным зубом (рис. 7).
Более того, воспаление и последующее разрастание аксонов
может привести к более обширной иннервации пульпы и пульпы-дентина
области, которые в норме слабо иннервированы в здоровых зубах. Этот
может быть одним из механизмов, играющих значительную роль в увеличении цервикального
чувствительность (рис. 4). Кроме того, пломбы с открытыми краями могут вызвать
воспаление пульпы, влияющее на чувствительность дентина в других
части мякоти. Открытые дентинные канальцы рядом с такой пломбой
может способствовать диффузии и проникновению внешних раздражителей в
пульпы, что приводит к воспалению, активации, а также прорастанию
нервных окончаний в пульпо-дентинном комплексе (рис. 8). Фактически,
вполне может быть, что воспаление той или иной степени может вообще
играют роль в гиперчувствительности дентина.
4). Кроме того, пломбы с открытыми краями могут вызвать
воспаление пульпы, влияющее на чувствительность дентина в других
части мякоти. Открытые дентинные канальцы рядом с такой пломбой
может способствовать диффузии и проникновению внешних раздражителей в
пульпы, что приводит к воспалению, активации, а также прорастанию
нервных окончаний в пульпо-дентинном комплексе (рис. 8). Фактически,
вполне может быть, что воспаление той или иной степени может вообще
играют роль в гиперчувствительности дентина.
Рисунок 7. Схематическое представление
рецептивных полей одиночных внутризубных нервных волокон в
блок дентина А: здоровый и Б: воспаленный зуб. Три
нервные волокна с нервными окончаниями на границе пульпы и дентина
обозначаются цифрами (1 — 3). Они цветные (синий, красный и
коричневый) и те же цвета используются для обозначения их рецептивных полей.
на обнаженной поверхности дентина. Рецептивные поля (RF)
волокна значительно шире и более широко перекрываются в
B: воспаленный по сравнению с A: здоровый зуб. Следовательно,
раздражение стандартного участка дентина приводит к активации значительно
большее количество нервных волокон и более высокая чувствительность в воспаленной
зуб по сравнению со здоровым.
Следовательно,
раздражение стандартного участка дентина приводит к активации значительно
большее количество нервных волокон и более высокая чувствительность в воспаленной
зуб по сравнению со здоровым.
Рисунок 8. Даже значительно отдаленные протекающие пломбы могут повысить чувствительность дентина из-за нейрогенного воспалительные явления с разветвлением внутризубных аксонов в другие участки пульпы и пульпо-дентинного комплекса. Нейрогенный воспаление и связанное с ним высвобождение нейропептидов вызывает активацию других медиаторов воспаления. Индуцированное воспаление повышает чувствительность ноцицепторов пульпы и, следовательно, чувствительность пульпы и дентина. Соответственно, восстановление старые, даже отдаленные пломбы иногда могут быть необходимы для лечения гиперчувствительности дентина.
Кроме того, пульпа зуба, по-видимому, содержит значительное количество
так называемые «молчащие» или «спящие» ноцицепторы, которые не могут быть активированы
в здоровых, но только в воспаленных зубах (43). электрофизиологический
эксперименты показывают, что примерно 40 % ноцицептивных
афференты могут быть активированы в здоровых зубах, тогда как пропорция
увеличивается до 60 % при воспалении пульпы. Принимая во внимание
общее количество внутризубных афферентов (примерно 1000) в
каждого зуба, такое увеличение количества ноцицепторов является значительным
относительно болевой чувствительности зубов.
электрофизиологический
эксперименты показывают, что примерно 40 % ноцицептивных
афференты могут быть активированы в здоровых зубах, тогда как пропорция
увеличивается до 60 % при воспалении пульпы. Принимая во внимание
общее количество внутризубных афферентов (примерно 1000) в
каждого зуба, такое увеличение количества ноцицепторов является значительным
относительно болевой чувствительности зубов.
Бесшумный и «горячий зуб»
По-видимому, активация ноцицепторов пульпы может варьироваться от
значительной степени (5, 43, 50). Во многих случаях острый пульпит может
крайне болезненно. Однако чаще всего воспаление пульпы может продолжаться
до тотального некроза пульпы с незначительными симптомами или без симптомов вообще
(23, 50, 51) (рис. 3). Это озадачивает, учитывая богатый ноцицептивный
иннервация пульпы. Такая вариация симптомов также может
представляет серьезную диагностическую проблему с клинической точки зрения.
Ряд местных посредников могут быть вовлечены в предотвращение
активация нерва (43, 51). К ним относятся, например. местные опиоиды,
соматостатин, норадреналин и оксид азота (43, 52–54). Эти посредники
также важны для регуляции интенсивности воспаления пульпы.
Ингибирование активности ноцицепторов приводит к уменьшению высвобождения
нейропептидов и других медиаторов воспаления, а также ослабление
или даже полное предотвращение болевых симптомов (43, 51). Кроме того
к местной или периферической сенсибилизации и торможению, описанным
выше, механизмы на уровне ствола мозга или выше в центральной нервной
системы сложные ноцицептивные пути могут играть важную роль
для регуляции боли (центральная сенсибилизация/торможение), как при
развитие и модуляция боли (55).
К ним относятся, например. местные опиоиды,
соматостатин, норадреналин и оксид азота (43, 52–54). Эти посредники
также важны для регуляции интенсивности воспаления пульпы.
Ингибирование активности ноцицепторов приводит к уменьшению высвобождения
нейропептидов и других медиаторов воспаления, а также ослабление
или даже полное предотвращение болевых симптомов (43, 51). Кроме того
к местной или периферической сенсибилизации и торможению, описанным
выше, механизмы на уровне ствола мозга или выше в центральной нервной
системы сложные ноцицептивные пути могут играть важную роль
для регуляции боли (центральная сенсибилизация/торможение), как при
развитие и модуляция боли (55).
Клинические случаи боли в пульпе и дентине и их лечение
Лечение гиперчувствительности дентина
Со ссылкой на классическую литературу, клиническое впечатление
и интерпретация боли в дентине — это то, что будет вызвано
и провоцируется вполне определенными внешними раздражителями. В следующих
клинических сценариях накопление биопленки играет огромную роль
в ведущем к боли.
Сценарий 1
Пациент много лет не посещал стоматолога. Пациент совершенно не может пить или принимать холодные или горячие жидкости в полости рта из-за боли. Клинически у больного плохая гигиена. состояние и большое количество дефектных реставраций. Накопление биомассы отмечают при клиническом обследовании. Не только являются ли реставрации неоптимальными, но и большие части зубов разрушаются с обнаженным дентином. Это создало экосистему с образованием биопленки на обнаженном дентине (рис. 9).а, б). Следующий несколько посещений только с профессиональным удалением биопленки (рис. 9с), пациент поступает с выраженным снижением уровня боли. Из Конечно, в реальной жизни клиницист будет инициировать оба гигиенические процедуры и реставрации, но настоящий случай отражает важное влияние биомассы на обнаженный дентин и гиперчувствительность дентина.
Рисунок 9. Представление пациента
с выраженной гиперчувствительностью дентина и большими полостями, покрытыми
биопленка. A: до окрашивания биопленки, B: после окрашивания биопленки и
C: после профессионального удаления биопленки.
A: до окрашивания биопленки, B: после окрашивания биопленки и
C: после профессионального удаления биопленки.
Сценарий 2
Если введены улучшенные гигиенические процедуры, но без боли
план лечения должен быть направлен на снижение проницаемости дентина
(Таблица 2). Это может быть достигнуто путем физической блокировки
дентинных канальцах или путем деполяризации нервов (56). Широкий ассортимент
материалов для десенсибилизации продано, но без универсального
успех. Гиперчувствительность дентина очень трудно контролировать.
что указывает на то, что материалы либо не имеют постоянного эффекта, либо
что воспалительные изменения настолько глубоки, что естественное заживление
процесс предотвращается. Несколько методов лечения показали
окклюзионный или десенсибилизирующий эффект у животных, но было трудно
для демонстрации в клинике (56). Проблема с материалами, которые
предназначены для блокирования потока жидкости в дентинных канальцах, например
путем осаждения кристаллов соли, заключается в том, что осаждение может
вымывается, растворяется в кислой среде или изнашивается так
что потенциальный эффект окклюзии является временным.
Таблица 2. Методы лечения гиперчувствительных дентин
Имеется много опубликованных исследований зубных паст с солями стронция. и соли калия (57). Некоторые из них сообщают, что эти зубные пасты имеют некоторый десенсибилизирующий эффект, в то время как другие не смогли для демонстрации эффекта. Дизайн этих исследований был под вопросом, и эффект неясен (58). Перед проведением дорогостоящее и инвазивное лечение, практический тест может заключаться в оценке того, индивидуальный пациент чувствует улучшение симптомов, используя эти зубные пасты. Паста, состоящая из аргинина и карбоната кальция, утверждал, что закрывает дентинные канальцы, был введен в качестве мягкого обработка чувствительной зоны. Пока только предварительные результаты доступны от производителя (59, 60).
Если вышеуказанные методы неэффективны, следующим шагом будет герметизация
дентинные канальцы с фторлаком, дентинным праймером и смолой
или с полимерной реставрацией. В некоторых случаях это может закончиться эндодонтической
лечение. Как и в других случаях, первичная профилактика, конечно же,
оптимальное решение, в том числе с использованием щадящей техники чистки
как низкое потребление безалкогольных напитков с низким pH в отличие от попытки
для лечения установленной гиперчувствительной области/поражения.
Как и в других случаях, первичная профилактика, конечно же,
оптимальное решение, в том числе с использованием щадящей техники чистки
как низкое потребление безалкогольных напитков с низким pH в отличие от попытки
для лечения установленной гиперчувствительной области/поражения.
Вывод
Диагностика и лечение дентинной боли часто представляет собой проблему к клиницисту. Пульпа зуба исключительно богато иннервирована. ноцицептивными афферентами, а боль в пульпе и дентине может вызвать значительный дискомфорт пациентов. Многие факторы участвуют в развитие и постоянство болей. Кариес, ятрогенные повреждения, изменения в структуре дентина и проницаемости, вызванной эрозией или зубом стирание, скопление биопленки на незащищенном дентине; все может привести к активации ноцицептивных нервов, что инициирует местное воспаление изменения в пульпе, а также запускает центральные изменения в обработке боли — оба из них сложны, и их может быть трудно обратить вспять.
-
Lipton JA, Ship JA, Ларах-Робинсон D.
 Предполагаемая распространенность и распределение сообщаемой орофациальной боли
В Соединенных Штатах. J Am Dent Assoc. 1993 год; 124(10): 115 — 21.
Предполагаемая распространенность и распределение сообщаемой орофациальной боли
В Соединенных Штатах. J Am Dent Assoc. 1993 год; 124(10): 115 — 21. -
Heyeraas KJ, Kvinnsland I. Тканевое давление и кровоток при воспалении пульпы. Proc Finn Dent Soc. 1992 год; 88 Приложение 1: 393 — 401.
-
Ким С. Нейроваскулярные взаимодействия в пульпе зуба в здоровье и воспаление. Журнал эндодонтии. 1990 г.; 16(2): 48 — 53.
-
Хильдебранд С., Фрид К., Туиску Ф., Йоханссон С.С. Зубы и зубные нервы. Прог Нейробиол. 1995 год; 45(3): 165 — 222.
-
Бреннстрем М. Дентин и пульпа в реставрационной стоматологии. Нака, Швеция: Dental Therapeutics AB1981.
-
Байерс М.Р., Нари М.В. Модели травм зубов: экспериментальные инструменты для понимания нейровоспалительных взаимодействий и полимодальных ноцицепторов функции. Crit Rev Oral Biol Med. 1999 г.; 10(1): 4 — 39.
-
Нархи М.В. Характеристики внутризубных сенсорных единиц и их реакции на стимуляцию.
 Журнал стоматологических исследований.
1985 год; 64 Спец. №: 564 — 71.
Журнал стоматологических исследований.
1985 год; 64 Спец. №: 564 — 71. -
Байерс МР. Сенсорные рецепторы зубов. Int Rev Neurobiol. 1984 год; 25: 39 — 94.
-
Johnsen D, Johns S. Количественный анализ нервных волокон в молочные и постоянные клыки и резцы у человека. Арка Орал биол. 1978 год; 23(9): 825 — 9.
-
Джонсен Д.С., Харшбаргер Дж., Раймер Х.Д. Количественная оценка развития нервной системы премоляров человека. Анатомическая запись. 1983; 205(4): 421 — 9.
-
Читатель А, Мастер ДВ. Ультраструктурное количественное исследование внутризубной иннервации человека. Журнал эндодонтии. 1981 год; 7(11): 493 — 9.
-
Хирвонен Т.Дж. Количественный электронно-микроскопический анализ аксонов на верхушке пульпы клыка у собаки. Акта Анат (Базель). 1987 год; 128(2): 134 — 9.
-
Holland GR, Robinson PP. Количество и размер аксонов в вершина кошачьего клыка. Анатомическая запись. 1983; 205(2): 215 — 22.

-
Ювасярви Э., Книффки К.Д. Холодовая стимуляция зубов: сравнение реакции внутризубных А-дельта- и С-волокон кошки и человека сенсация. Журнал физиологии. 1987 год; 391: 193 — 207.
-
Нари М., Ювасьярви Э., Виртанен А., Хуопаниеми Т., Нгассапа D, Hirvonen T. Роль внутризубных нервных волокон A- и C-типа в Механизмы зубной боли. Proc Finn Dent Soc. 1992 год; 88 Приложение 1: 507 — 16.
-
Нари М.В., Конттури-Нярхи В. Чувствительность и состояние поверхности дентина — исследование СЭМ-реплики (аннотация). Журнал стоматологических исследований. 1994; 73: 122.
-
Beasley WL, Голландия GR. Количественный анализ иннервации пульпа кошачьего клыка. J Комп Нейрол. 1978 год; 178(3): 487 — 94.
-
Магги ССА. Тахикинины и пептид, родственный гену кальцитонина (CGRP) как комедиаторы, высвобождаемые из периферических окончаний чувствительных нервов. Прогресс в нейробиологии. 1995 год; 45(1): 1 — 98.
-
Вакисака С.
 , Акаи М. Иммуногистохимическое исследование нейропептидов
вокруг кровеносного сосуда в пульпе зуба кошки. Журнал эндодонтии.
1989; 15(9): 413 — 6.
, Акаи М. Иммуногистохимическое исследование нейропептидов
вокруг кровеносного сосуда в пульпе зуба кошки. Журнал эндодонтии.
1989; 15(9): 413 — 6. -
Haug SR, Heyeraas KJ. Модуляция воспаления зубов симпатической нервной системой. Журнал стоматологических исследований. 2006 г.; 85(6): 488 — 95.
-
Газелиус Б., Эдвалл Б., Ольгарт Л., Лундберг Дж. М., Хокфельт Т., Фишер Дж.А. Сосудорасширяющие эффекты и сосуществование связанных с геном кальцитонина пептид (CGRP) и вещество P в чувствительных нервах пульпы зубов кошек. Acta Physiol Scand. 1987 год; 130(1): 33 — 40.
-
Газелиус Б., Ольгарт Л. Расширение сосудов пульпы зуба при электростимуляции нижнего альвеолярного нерва в кошке. Acta Physiol Scand. 1980; 108(2): 181 — 6.
-
Ольгарт Л.М., Эдвалл Б., Газелиус Б. Нейрогенные медиаторы в контроль кровотока в пульпе. Журнал эндодонтии. 1989 год; 15(9): 409 — 12.
-
Tonder KH, Naess G. Нервная регуляция кровотока в пульпы зубов у собак.
 Acta Physiol Scand. 1978 год; 104(1): 13 — 23.
Acta Physiol Scand. 1978 год; 104(1): 13 — 23. -
Кимберли С.Л., Байерс М.Р. Воспаление молярной пульпы крысы и периодонт вызывает увеличение пептида, связанного с геном кальцитонина, и разрастание аксонов. Анатомическая запись. 1988; 222(3): 289 — 300.
-
Taylor PE, Byers MR, Redd PE. Прорастание нервных волокон CGRP в ответ на повреждение дентина моляров крыс. Мозг Res. 1988 год; 461(2): 371 — 6.
-
Haug SR, Heyeraas KJ. Влияние симпатэктомии на экспериментально вызывали воспаление пульпы и периапикальные поражения у крыс. Неврология. 2003 г.; 120(3): 827 — 36.
-
Мозг SD. Сенсорные нейропептиды: их роль в воспалении и заживление ран. Иммунофармакология. 1997; 37(2 — 3): 133 — 52.
-
Чиу И.М., фон Хен К.А., Вульф К.Дж. Нейрогенное воспаление и периферическая нервная система в защите хозяина и иммунопатологии. Природа неврология. 2012 г.; 15(8): 1063 — 7.
-
Хауг С.Р., Берггрин Э.
 , Хейераас К.Дж. Эффект одностороннего
симпатэктомия и подготовка полостей на пептидергических нервах и иммунных клетках
в пульпе зубов крыс. Опыт Нейрол. 2001 г.; 169(1): 182 — 90.
, Хейераас К.Дж. Эффект одностороннего
симпатэктомия и подготовка полостей на пептидергических нервах и иммунных клетках
в пульпе зубов крыс. Опыт Нейрол. 2001 г.; 169(1): 182 — 90. -
Taylor PE, Byers MR. Иммуноцитохимическое исследование морфологическая реакция нервов, содержащих ген кальцитонина пептид к образованию и заживлению микроабсцессов в молярах крыс. Арка Оральный биол. 1990; 35(8): 629 — 38.
-
Бьёрндал Л., Дарванн Т., Тилструп А. Количественный свет микроскопическое исследование одонтобластной и субодонтобластной реакций к активному и задержанному кариесу эмали без образования полостей. Кариес Рез. 1998 год; 32(1): 59 — 69.
-
Khayat BG, Byers MR, Taylor PE, Mecifi K, Kimberly CL. Ответы нервных волокон к воспалению пульпы и периапикальным поражениям у крыс моляры, продемонстрированные с помощью иммуноцитохимии пептидов, связанных с геном кальцитонина. Журнал эндодонтии. 1988; 14(12): 577 — 87.
-
Кавьедес-Бучели Х.
 , Ломбана Н., Асуэро-Ольгин М.М., Муньос
ЧР. Количественное определение нейропептидов (пептид, родственный гену кальцитонина,
вещество Р, нейрокинин А, нейропептид Y и вазоактивные кишечные
полипептид), экспрессируемый в здоровой и воспаленной пульпе зуба человека.
Международный эндодонтический журнал. 2006 г.; 39(5): 394 — 400.
, Ломбана Н., Асуэро-Ольгин М.М., Муньос
ЧР. Количественное определение нейропептидов (пептид, родственный гену кальцитонина,
вещество Р, нейрокинин А, нейропептид Y и вазоактивные кишечные
полипептид), экспрессируемый в здоровой и воспаленной пульпе зуба человека.
Международный эндодонтический журнал. 2006 г.; 39(5): 394 — 400. -
Brännström M. Передача и контроль дентинной боли. В: Гроссман Л.Дж., изд. Механизмы и контроль боли. Нью-Йорк: Массон Паблишинг США; 1979.
-
Мэтьюз Б., Вонгсаван Н. Взаимодействие между нейронами и гидродинамические механизмы в дентине и пульпе. Arch Oral Biol. 1994 год; 39 Доп.: 87С-95С.
-
Hermanstyne TO, Markowitz K, Fan L, Gold MS. Механопреобразователи в пульпарных афферентах крыс. Журнал стоматологических исследований. 2008 г.; 87(9): 834 — 8.
-
Нари М., Ювасьярви Э., Хирвонен Т., Хуопаниеми Т. Активация термочувствительных нервных волокон в пульпе зуба кошки. Боль. 1982 год; 14(4): 317 — 26.

-
Вонгсаван Н., Мэтьюз Б. Проницаемость кошачьего дентина в естественных условиях и в пробирке. Arch Oral Biol. 1991 год; 36(9): 641 — 6.
-
Вонгсаван Н., Мэтьюз Б. Взаимосвязь между разрядом внутризубные нервы и скорость тока жидкости через дентин в Кот. Arch Oral Biol. 2007 г.; 52(7): 640 — 7.
-
Троубридж Х.О., Фрэнкс М., Коростофф Э., Эмлинг Р. Сенсорика реакция на термическую стимуляцию зубов человека. Журнал эндодонтии. 1980; 6(1): 405 — 12.
-
Нари М. Активация нервов пульпы зуба кошки и собака с гидростатическим давлением. Proc Finn Dent Soc. 1978 год; 74 Приложение 5 — 7: 1 — 63.
-
Нари М., Ямамото Х., Нгассапа Д. Функция внутризубного ноцицепторов в нормальных и воспаленных зубах. Вышли: Симоно М., Маэда Т., Суда Х., Такахаши К., редакторы. Дентинно-пульповый комплекс. Токио: издательство Quintessence Ко; 1996. с. 136.
-
Нари М., Ямамото Х., Нгассапа Д., Хирвонен Т. Нейрофизиологические Основа и роль воспалительных реакций в гиперчувствительности дентина.
 Arch Oral Biol. 1994; 39 Доп.: 23С-30С.
Arch Oral Biol. 1994; 39 Доп.: 23С-30С. -
Чаудхари П., Мартенсон М.Э., Бауманн Т.К. Ванилоидный рецептор экспрессия и возбуждение капсаицином первичных афферентных рецепторов зубов крысы. нейроны. Журнал стоматологических исследований. 2001 г.; 80(6): 1518 — 23.
-
Ян Б.Х., Пяо З.Г., Ким Ю.Б., Ли Ч., Ли Дж.К., Парк К. и др. Активация ваниллоидного рецептора 1 (VR1) эвгенолом. Журнал стоматологические исследования. 2003 г.; 82(10): 781 — 5.
-
Запад NX. Гиперчувствительность дентина: профилактика и лечение подходы к лечению. Пародонтол 2000. 2008; 48: 31 — 41.
-
Hovgaard O. Гиперчувствительность дентина: физиология и обращение: Институт оральной анатомии и тандсигдомслаэре, Орхусская Тандлэгехойская школа; 1988.
-
Байерс МР. Влияние воспаления на сенсорные нервы зубов наоборот. Proc Finn Dent Soc. 1992 год; 88 Приложение 1: 499 — 506.
-
Зельцер С., Бендер И.Б., Зионц М. Динамика воспаления пульпы: Корреляция между диагностическими данными и фактическими гистологическими данными в Мякоти.
 Oral Surg Oral Med Oral Pathol. 1963; 16: 969 — 77.
Oral Surg Oral Med Oral Pathol. 1963; 16: 969 — 77. -
Ольгарт Л.М. Роль местных факторов в дентине и пульпе в механизмах внутризубной боли. Журнал стоматологических исследований. 1985 год; 64 Спец. №: 572 — 8.
-
Фристад I, Берггрин Э., Хауг С.Р. Дельта (дельта) опиоидные рецепторы в мелких и средних нейронах тройничного нерва, поддерживающих зубной мякоть крыс. Arch Oral Biol. 2006 г.; 51(4): 273 — 81.
-
Ольгарт Л. Нейрогенные компоненты воспаления пульпы. В: Симоно М., Маэда Т., Суда Х., Такахаши К., редакторы. Дентинно-пульповый комплекс. квинтэссенция Публикация Co1996. с. 169 — 75.
-
Stein C. Периферические механизмы опиоидной анальгезии. Анест аналг. 1993 год; 76(1): 182 — 91.
-
Сессле Б.Дж. Нейробиология лицевой и зубной боли: современные знания, будущие направления. Журнал стоматологических исследований. 1987 год; 66(5): 962 — 81.
-
Марковиц К., Пэшли Д.Х. Открытие новых методов лечения чувствительные зубы: долгий путь от биологии к терапии.
 J Оральная реабилитация.
2008 г.; 35(4): 300 — 15.
J Оральная реабилитация.
2008 г.; 35(4): 300 — 15. -
Зельцер С., Бендер И.Б., Зионц М. Динамика воспаления пульпы: корреляции между диагностическими данными и фактическими гистологическими данными в пульпе. Oral Surg Oral Med Oral Pathol. 1963 год; 16: 846 — 71 конд.
-
Поулсен С., Эррбо М., Лескей Мевиль Ю., Гленни А.М. Калий содержащие зубные пасты для гиперчувствительности дентина. Кокрановская система баз данных Ред. 2006 г. (3): CD001476.
-
Panagakos F, Schiff T, Guignon A. Гиперчувствительность дентина: эффективное лечение офисной десенсибилизирующей пастой, содержащей 8 % аргинина и карбоната кальция. Американский журнал стоматологии. 2009 г.; 22 Спец. № А: 3А-7А.
-
Петру И., Хеу Р., Страник М., Лаванда С., Зайдель Л., Камминс Д и др. Революционная терапия гиперчувствительности дентина: как стоматологические продукты, содержащие 8 % аргинина и карбоната кальция для эффективного облегчения чувствительности зубов.
 Журнал клинических
стоматология. 2009 г.; 20(1): 23 — 31.
Журнал клинических
стоматология. 2009 г.; 20(1): 23 — 31.
Matti Närhi
DDS, PhD, профессор физиологии полости рта, кафедра Стоматологии/физиологии, Институт медицины, Университет Восточного Финляндия, Финляндия
Ларс Бьорндал
Ассоциированный профессор, доктор философии, доктор Одонт. Министерство Кариология и эндодонтия, факультет здравоохранения и медицинских наук, Копенгагенский университет, Дания
Мария Пигг
ДДС, доктор Одонт. Старший преподаватель. Отделение эндодонтии и отделение орофациальной боли и функции челюсти, факультет одонтологии, Университет Мальмё, Мальмё, Швеция
Инге Фристад
Доктор наук, профессор. Кафедра клинической стоматологии, Факультет медицины и стоматологии Бергенского университета, НОРВЕГИЯ
Сиваками Ретнам Haug
DDS, доктор Одонт. Доцент и заведующий сектором Эндодонтия
Кафедра клинической стоматологии медико-стоматологического факультета. Университет Бергена, Норвегия
Автор, ответственный за переписку: Матти Нэри, электронная почта: matti. [email protected]
[email protected]
Этот документ прошел рецензирование.
Нари М., Бьорндал Л., Пигг М., Фристад I, Хауг С.Р. Острая зубная боль I: боль в пульпе и дентине. Ни Tannlegeforen Tid. 2016; 126: 10-8.
Пульпотомия по сравнению с пульпэктомией при лечении обнажения витальной пульпы молочных резцов. Систематический обзор и метаанализ.
- DOI:10.12688/f1000research.16142.3
- Идентификатор корпуса: 195828606
@article{Gadallah3018PulpotomyVP,
title={Пульпотомия по сравнению с пульпэктомией при лечении обнажения витальной пульпы молочных резцов. Систематический обзор и метаанализ.},
автор = {Ламия Гадалла, Махмуд Хамди, Адель Эль Бардиси и Мохамед Абу Эль Язид},
журнал={F1000Research},
год = {2018},
объем = {7},
страницы={
1560
}
} - Lamia Gadallah, M. Hamdy, Mohamed Abou El Yazeed
- Опубликовано 25 июня 2019 г.

- Medicine
- F1000Research
Предыстория. Кариес в раннем детстве является серьезной проблемой общественного здравоохранения. Когда кариес распространяется на пульпу, пробуют различные формы лечения пульпы, чтобы стимулировать восстановление зубов. Хотя пульпотомия является методом выбора при обнажении пульпы живого молочного зуба, многие стоматологи склонны выполнять пульпэктомию в жизненно важных молочных резцах. Это исследование было направлено на оценку эффекта пульпотомии и пульпекомии при лечении кариозного обнажения витальной пульпы молочных резцов. Методы: Мы…
Посмотреть на PubMed
doi.org
Современные методы лечения литературного пульпита: обзор литературы
- E. Brusnitsyna, E. V. Barabanshchikova, T. Zakirov, E. S. Ioshchenko
-
. Medicine, M.Chyse McIence, M.Cearicy Medicine, Machine Macicer, E. S. Ioshchenko
-
. Medicine, M.Chytice McIence Mphisonge Machine, E. S. Ioshchenko
-
.
 Medicine McInecy Medicine, E.S. 2021
Medicine McInecy Medicine, E.S. 2021
Биологически обоснованные методы лечения пульпита, максимально сохраняющие жизнеспособность пульпы, в настоящее время считаются предпочтительными.
Генотоксичность герметиков для корневых каналов: обзор литературы
- Fábio Miguel dos Santos Costa, M. H. Fernandes, S. R. Batistuzzo de Medeiros
-
Medicine
Clinical Oral Investigations
- 2020
All published data showed some evidence of genotoxicity for most of the commercial root canal sealers; однако были обнаружены противоречивые результаты, в основном для AH Plus, наиболее изученного герметика.
Сравнительный клинический и радиологический анализ пульпотомии и удаления зубов с формокрезолом, МТА и биодентином
- Larissa Maria Monteiro de Albuquerque, C. C. Silva, Wenys Cláudio Gomes Da Silva, A. Araújo
-
Medicine
, Общество и развитие
- 2021
 é o Biodentine и Mineral Trioxide Aggregate, devendo a escolha ser feita de acordo with o critério do profissional e caso do paciente.
é o Biodentine и Mineral Trioxide Aggregate, devendo a escolha ser feita de acordo with o critério do profissional e caso do paciente. Пульпэктомия в сравнении с пульпотомией при лечении временных моляров с хроническим пульпитом
- Брусницына Е., Закиров Т., Иошенко Е., Сайпеева М., Татьяна Стати
-
Медицина
БИО Web of Conferences
- 2020
пульпэктомия и пульпотомия молочных моляров при хроническом фиброзном пульпите и не выявили существенных различий между группами.
ПОКАЗЫВАЮТСЯ 1-10 ИЗ 21 ССЫЛОК
СОРТИРОВАТЬ ПОРелевантностьНаиболее влиятельные документыНедавность
Лечение пульпы при обширном кариесе молочных зубов.
- V. Smaïl-Faugeron, A. Glenny, F. Courson, P. Durieux, M. Muller-Bolla, H. Fron Chabouis
-
Медицина
База данных систематических обзоров Cochrane 912 71910 818910 80009 20809 Кокрановский обзор рандомизированных контролируемых испытаний, в которых сравнивались вмешательства, сочетающие метод лечения пульпы с медикаментами или приспособлениями у детей с обширным кариесом пульпы молочных зубов, показал, что были обнаружены доказательства среднего качества для пульпотомии и пульпэктомии.

Лечение пульпы при обширном кариесе молочных зубов.
- V. Smaïl-Faugeron, F. Courson, P. Durieux, M. Muller-Bolla, A. Glenny, H. Fron Chabouis
-
Медицина
База данных систематических обзоров Cochrane 912 71 7910 818910 80009 20409 2 Кокрановский обзор рандомизированных контролируемых испытаний, сравнивающих различные вмешательства на пульпе, сочетающие метод лечения пульпы и медикаментозное лечение у детей с обширным кариесом, затрагивающим пульпу молочных зубов, не обнаружил доказательств того, что прямое покрытие пульпы превосходит другие методы, и общее качество доказательств был низким.
Использование витальной терапии пульпы в молочных зубах с глубоким кариесом.
- V. Dhar, A. Marghalani, Laurel Graham
-
Медицина
Детская стоматология
- 2017
На основе рекомендаций три рекомендации по пульповой терапии, созванные Американской академией стоматологии: непрямая обработка пульпы (IPT), прямое покрытие пульпы (DPC) и пульпотомия.

Исходы пульпотомии витального первичного резца с применением сульфата железа и лечения корневых каналов.
- M. Casas, D. Kenny, D. Johnston, P. Judd, M. Layug
-
Медицина
Journal
- 2004
резец в 2 года; однако через 2 года выживаемость резцов RCT была статистически выше, чем резцов ORS, обработанных FS pul Potomy.
Сравнение совокупной пульпотомии триоксида железа с комбинированным минералом и эвгенольной пульпэктомии оксидом цинка основных резцов верхней челюсти: 18-месячное рандомизированное контролируемое исследование.
- Trang D Nguyen, P. Judd, E. Barrett, N. Sidhu, M. Casas
-
Медицина
Педиатрическая стоматология
- 2017
Минеральный ангрегат с сульфатом железа + AMT+ альтернатива РКИ для витальных молочных резцов при бессимптомном кариозном витальном молочном резце с обнажением пульпы у здоровых детей в возрасте от 18 до 46 месяцев.

Сравнительное исследование клинико-рентгенологических признаков агрегата минерального триоксида и формокрезола на пульпотомированных молочных молярах
- S. Hugar, S. Deshpande
-
Медицина, материаловедение
Современная клиническая стоматология
- 2010
МТА кажется более многообещающим с предсказуемым положительным эффектом в терапии витальной пульпы, чем пульпосолмокрелэктомия в будущем, за исключением пульпотомии фактор стоимости.
Текущие тенденции в терапии пульпы: обзор, анализирующий методы пульпотомии, преподаваемые в программах ординатуры по детской стоматологии.
По данным опроса руководителей программ резидентуры по детской стоматологии, не произошло серьезного отказа от его клинического использования, несмотря на более широкое использование новых лекарств за последние 5 лет.
Руководство по лечению пульпы молочных и несформированных постоянных зубов.

- F. Shiere, S. Frankl, H. R. Fogels
-
Медицина, материаловедение
Детская стоматология
- 2016
Описание и эпидемиология вскармливания.
Приведено подробное клиническое описание кариеса вскармливания, рассмотрены характеристики детей, которые могут быть подвержены риску развития кариеса вскармливания, а также рассмотрены данные о распространенности кариеса вскармливания в странах, которые сообщили о нем, с предложением направлений исследований в области кариеса вскармливания. этиология и распространенность.
Кариес у детей раннего возраста: обзор причин, диагностики и лечения
- H. Çolak, Ç. Т. Дюльгергил, М. Далли, М. М. Хамиди
-
Медицина
Журнал естественных наук, биологии и медицины
- 2013
Подробная информация о РКР, от ее диагностики до лечения, а также взаимосвязи между грудным вскармливанием и ECC, вероятно, будет сложным и смешанным со многими биологическими переменными, такими как стрептококки mutans, гипоплазия эмали, потребление сахаров, а также социальными переменными, включая образование родителей и социально-экономический статус, которые могут повлиять на здоровье полости рта.

