Антибиотики в современной пародонтологической практике
Восемь основных видов антибиотиков были широко изучены и описаны для лечения заболеваний пародонта: тетрациклин, миноциклин, доксициклин, эритромицин, клиндамицин, ампициллин, амоксициллин и метронидазол.
1. Тетрациклин
Фармакология
1. Производится естественным путем из определенных видов Streptomyces или полусинтетических производных.
2. Бактериостатические препараты, эффективнее против быстро размножающихся бактерий и грамположительных бактерий, чем против грамотрицательных бактерий.
3. Концентрация в десневой борозде в 2-10 раз больше, чем в сыворотке.
4. Обладают уникальными не-антибактериальными характеристиками — ингибированием коллагеназы, ингибированием хемотаксиса нейтрофилов, противовоспалительным эффектом, ингибированием микробной адгезии.
Механизм действия
Действуют путем ингибирования синтеза белка путем связывания с 30 S рибосомами в восприимчивом организме.
Клиническое использование
1. Вспомогательный препаратпри лечении локализованного агрессивного пародонтита.
2. Останавливает потерю кости и подавляет уровни A. actinomycetemcomitans в сочетании с скейлингом и сглаживанием корней.
Тетрациклин, миноциклин и доксициклин являются полусинтетическими членами группы тетрациклина, которые использовались при терапии пародонта.
Режим дозирования — 250 мг четыре раза в день.
2.Миноциклин
1. Эффективен против широкого спектра микроорганизмов.
2. Подавляет спирохеты и подвижные палочки так же эффективно, как скейлинг и сглаживание корней, с подавлением до 3 месяцев после терапии.
3. Можно принимать два раза в день, что облегчает соблюдение правил приема.
4. Хотя сопровождается меньшей фототоксичностью и почечной токсичностью, чем тетрациклин, может вызвать обратимое головокружение.
5. Увеличивает уровень препарата десневой жидкости в 5 раз.
6. За исключением влияния миноциклина на актиномицеты, ни один из тетрациклинов по существу не ингибирует рост оральных грамположительных организмов путем системной доставки.
3. Доксициклин
1. Тот же спектр активности, что и у миноциклина.
2. Удобен в приеме, поскольку его необходимо принимать один раз в день, абсорбция из желудочно-кишечного тракта лишь слегка может быть изменена кальцием, ионами металлов или антацидами.
3. Рекомендуемая доза составляет 100 мг 2 раза в день в первый день, затем 100 мг. Чтобы уменьшить желудочно-кишечные расстройства, 50 мг можно принять 2 раза в день.
Сравнение биологических эффектов, пиковых концентраций тетрациклинов после системного введения в обычной дозе для взрослых показано в таблице 1.
4. Метронидазол
Фармакология
1. Синтетическое нитроимидазольное соединение с бактерицидными эффектами в основном применяются против облигатных грамположительных и грамотрицательных анаэробов. Campylobacterrectus является единственным факультативным анаэробным и вероятным пародонтальным возбудителем, который восприимчив к низким концентрациям метронидазола.
 gingivalis, Pintermedia и C. rectus , низкая эффективность воздействия на инфекции, вызванные A. actinomycetemcomitans и инфекций E. corrodens , существенно не влияет на подавление роста полезных видов бактерий
gingivalis, Pintermedia и C. rectus , низкая эффективность воздействия на инфекции, вызванные A. actinomycetemcomitans и инфекций E. corrodens , существенно не влияет на подавление роста полезных видов бактерий3. Концентрации, измеренные в десневой жидкости, обычно немного меньше, чем в плазме.
Способ действия
Метронидазол действует путем ингибирования синтеза ДНК.
Клиническое использование
1. Для лечения гингивита, острого некротического язвенного гингивита, хронического периодонтита и агрессивного пародонтита.
2. В качестве монотерапии метронидазол является не эффективным, его следует использовать в сочетании с обработкой поверхности корня, хирургическим вмешательством или с другими антибиотиками. Наиболее часто назначаемый режим составляет 250 мг трижды в день в течение 7 дней.
3. В исследовании, проведенном Haffajee et al обследовались пациенты с глубиной кармана ≥6 мм. Пациенты, получавших метронидазол или азитромицин, показали значительно большее уменьшение глубины кармана и большее усиление прикрепления , чем пациенты, получавше доксициклин.

5.Пенициллин
Фармакология
1. Природные и полусинтетические производные бульонных культур Penicillium mould.
2. Узкий спектр и бактерицидный характер. Основная активность в грамположительном спектре. Только широкого спектра пенициллины, такие как ампициллин и амоксициллин, обладают значительной антибактериальной антимикробной активностью для грамотрицательных видов.
Вмешивается в синтез клеточной стенки бактерий, ингибируют транспептидазы, так что перекрёстное сшивание не происходит.
Клиническое использование
1. В лечении пациентов с агрессивным пародонтитом, как в локализованных, так и в генерализованных формах. Рекомендуемая доза составляет 500 мг трижды в день в течение 8 дней.
2. Показывает высокую антимикробную активность по отношению к бактериям, которые встречаются в зубодесневой жидкости, за исключением E. corrodens, S. sputigena и Peptostreptococcus, ингибирует рост грамположительных факультативных анаэробов.
Исследования показывают, что более 60% взрослых пациентов с пародонтитом, у которых брали пробы на анализ пародонтльной бляшки, проявили β-лактамазную активность.
 По этой причине введение чувствительных к β-лактамазе пенициллинов, включая один амоксициллин, обычно не рекомендуется, а в некоторых случаях может ускорять разрушение пародонта.
По этой причине введение чувствительных к β-лактамазе пенициллинов, включая один амоксициллин, обычно не рекомендуется, а в некоторых случаях может ускорять разрушение пародонта.Амоксициллин-клавуланат (Augmentin). Общепринятой стратегией является введение амоксициллина с ингибитором бета-лактамазы, такой как клавулановая кислота. Аугментин может быть полезен при лечении пациентов с невосприимчивым или локализованным агрессивным пародонтитом.
При направленной тканевой регенерации систематическая терапия амоксициллин-клавулановой кислотой использовалась для подавления пародонтальных патогенов и увеличения усиления клинического прикрепления.
6.Цефалоспорины
Фармакология
1. Используется против инфекций, которых в противном случае можно было бы лечить с помощью пенциллина.
2. Устойчив к ряду β-лактамаз, обычно активных против пенициллина.
Способ действия
Тот же способ действия, что и у пенициллинов, т. е. ингибирование синтеза клеточной стенки бактерий.

Клиническое использование
Цефалексин является цефалоспорином, доступным для введения в пероральной лекарственной форме.
1. Достигает высоких концентраций в зубодесневой жидкости.
2. Эффективно тормозит рост грамотрицательных облигатных анаэробов, не препятствует грамотрицательным факультативным анаэробам.
3. Более новые цефалоспорины с повышенной грамотрицательной эффективностью могут быть полезны при лечении заболеваний пародонта.
7.Клиндамицин
Фармакология
Эффективен против анаэробных бактерий и у пациентов, имеющих аллергию на пенициллин.
Способ действия
Ингибирование синтеза белка путем связывания с 50 S рибосомой.
Клиническое использование
1. Клиндамицин достигает более высоких уровней антимикробной активности, чем другие антибиотики.
2. Gordon и соавторы наблюдали средний прирост клинического прикрепления 1,5 мм и снижение активности болезни у пациентов через 24 месяца после дополнительной терапии клиндамицином.

3. Walker и соаворы показали, что клиндамицин помогает в стабилизации процесса у трудноподдающихся лечению пациентов. Дозировка составляла 150 мг 4р./день в течение 10 дней.
4. Jorgensen и соавторы рекомендовали режим 300 мг 2р./день в течение 8 дней
8.Ципрофлоксацин
Фармакология
1. Фторхинолоновый антибиотик, доступный для перорального введения.
2. Мощный ингибитор грамположительных бактерий (все факультативные и некоторые анаэробные предполагаемые пародонтальные патогены), включая Pseudomonas aeruginosa , с величинами MIC 90 в диапазоне от 0,2 до 2 мкг / мл.
Способ действия
Клиническое использование
1. Способствует созданию микрофлоры, связанной с пародонтальным здоровьем, с минимальным воздействием на виды стрептококков, которые связаны с пародонтальным здоровьем.
2. В настоящее время ципрофлоксацин является единственным антибиотиком в пародонтальной терапии, к которому чувствительны все штаммы A.
3. Также используется в сочетании с нитроимидазолами (метронидазолом и тинидазолом).
9.Макролиды
Фармакология
1. Содержит полилактонное кольцо, к которому прикреплены один или несколько дезоксисахаров.
2. Может быть бактериостатическим или бактерицидным, в зависимости от концентрации препарата и природы микроорганизма.
3. Макролидные антибиотики, используемые для лечения пародонта, включают эритромицин, спирамицин и азитромицин.
4. Основным ограничением эритромицина является его плохая абсорбция тканями. Препараты для системного введения доступны в качестве пролекарств (эритромицинэстолат, стеарат эритромицина или этилсукцинат эритромицина) для облегчения абсорбции. Пролекарство обладает незначительной антибактериальной активностью до тех пор, пока не будет гидролизовано эстеразами в сыворотке.
Способ действия
Ингибирование синтеза белка путем связывания с 50 S рибосомными субъединицами чувствительных микроорганизмов и препятствование трансляции.

Эритромицин
Клиническое использование
1. Очень безопасный препарат, который часто рекомендуется в качестве альтернативы пенициллину для пациентов с аллергией.
2. Уровни десневой жидкости указывают на то, что лишь небольшая часть достигает пародонтального кармана оральным путем.
Он выводится с высокой концентрацией через слюну . Результаты различных клинических испытаний показали хорошую эффективность спирамицина в лечении пародонтита, и метаанализ этих исследований показал высокие уровни доказательств, подтверждающих его эффективность . Было показано, что он уменьшает количество зубодесневой жидкости, глубину кармана и спирохет на поддесневом уровне. Herrera и соавторы в мета-анализе, оценивающем спирамицин, амоксициллин совместно с метронидазолом, и метрамидазол показали статистически значимый дополнительный эффект спирамицина по сравнению с другими антибиотиками в отношении уменьшения глубины зондирования кармана для участков с начальной глубиной зондирования более 6 мм
Клиническое использование
Эффективен против грамположительных организмов, оказывает минимальное влияние на увеличение уровня прикрепления.

Азитромицин
Клиническое использование
1. Эффективен против анаэробов и грамотрицательных палочек.
2. После пероральной дозы 500 мг в течение 3 дней в большинстве тканей в течение 7-10 дней могут быть обнаружены значительные уровни азитромицина.
3. Было высказано предположение, что азитромицин проникает в фибробласты и фагоциты в концентрациях, в 100-200 раз превышающих концентрации внеклеточного компартмента. Азитромицин активно переносится в места воспаления фагоцитами, а затем непосредственно высвобождается в местах воспаления как разрыв фагоцитов при фагоцитозе .
4. Терапевтическое применение требует разовой дозы 250 мг / день в течение 5 дней после начальной загрузочной дозы 500 мг.
10.Аминогликозиды
1. Ингибируют синтез белка путем связывания необратимым с конкретным белком или белками 30 S-рибосомной субъединицы.
2. Неактивны в анаэробных условиях, потому что внутриклеточный перенос сильно нарушен в отсутствие кислорода.
 Поэтому все анаэробные бактерии очень устойчивы, хотя они содержат рибосомы, чувствительные к этим антибиотикам.
Поэтому все анаэробные бактерии очень устойчивы, хотя они содержат рибосомы, чувствительные к этим антибиотикам.
Консервативное лечение пародонта
Более 70% населения страдает от различных заболеваний пародонта – т.е. тканей, окружающих зуб. Гингивит, пародонтоз и пародонтит коварны тем, что пациент самостоятельно не может заметить начинающуюся патологию и ждет появления выраженных симптомов, а болезнь в это время быстро прогрессирует. Заболевания десен беспокоят даже детей, начиная с младшего школьного возраста – детский гингивит встречается не реже взрослого. А гингивит беременных встречается еще чаще.
В чем заключается основная причина заболеваний пародонта?
При плохой гигиене мягкий зубной налет окаменевает, образуя зубной камень, который может располагаться как над десной, так и между зубом и десной, ниже ее уровня. Такие отложения называют поддесневыми. Именно они провоцируют появление зубодесневых карманов, в которых начинают активно размножаться микробы, содержащиеся в зубном налете. Это вызывает воспаление, кровотечение и приводит к углублению карманов, расшатыванию зубов, а затем к их потере.
Это вызывает воспаление, кровотечение и приводит к углублению карманов, расшатыванию зубов, а затем к их потере.
С чего начинается консервативное лечение заболеваний пародонта?
При лечении заболеваний десен и околозубных тканей очень важно вовремя пройти оценку состояния пародонта для ранней постановки диагноза, чтобы не допустить генерализации патологического процесса и более легкого и эффективного лечения.
Основными симптомами, которые должны насторожить пациента и послужить поводом обращения к пародонтологу являются кровотечение при чистке зубов и неприятный запах изо рта.
По результатам диагностики у пародонтолога разрабатывается индивидуальный план лечения, которое включает общие и местные воздействия на очаг воспаления.
Когда применяют консервативное лечение заболеваний пародонта?
1. При легкой и среднетяжелой форме гингивита и пародонтита. Это помогает избежать хирургического вмешательства.
2. При тяжелых формах заболеваний пародонта ДО и ПОСЛЕ хирургического лечения.
Что входит в консервативное лечение заболеваний пародонта?
Консервативное лечение направлено на купирование воспаления, устранение зубодесневых карманов и введение процесса в фазу стойкой ремиссии. Оно состоит из следующих манипуляций:
- гигиенических
- терапевтических
- физиотерапевтических
- ортопедических
- ортодонтических
Очень важно, чтобы лечение проводилось по плану, комплексно и поэтапно – это позволит достигнуть результата в более сжатые сроки.
Что ожидает пациента при консервативном лечении заболеваний пародонта?
Объем консервативного лечения определяется врачом-пародонтологом для каждого пациента индивидуально, в зависимости от его состояния. Мы указываем общую схему такого лечения.
1 этап – устранение общих факторов, провоцирующих заболевание десен.
- 1. Любое лечение заболеваний десен всегда начинается с профессиональной гигиены полости рта — очищения зубов и зубодесневых карманов от над- и поддесневых зубных камней, мягких зубных отложений.
 До и после гигиены проводится антисептическая обработка десен и карманов.
До и после гигиены проводится антисептическая обработка десен и карманов. - 2. Проводится обязательное обучение пациента самостоятельной домашней зубной гигиене, подбираются средства для ее проведения (паста, зубная щетка, ополаскиватели, флосс и пр.) В дальнейшем, врач постоянно контролирует ее качество, проводя регулярное окрашивание зубных отложений специальной жидкостью для их индикации.
- 3. Следующий этап – лечение кариеса и его осложнений для устранения очагов размножения патологической флоры, коррекция травмирующих слизистые ткани пломб.
- 4. Ортопедическое лечение — сюда входит шинирование и частичное пришлифовывание по показаниям.
- 5. Ортодонтическое лечение направленное на устранение патологий прикуса, например, глубокое резцовое перекрытие, глубокий и травматический (травмирующий) прикус, когда зубы «кусают» не в зубы, а в слизистую, постоянно нанося травму
2 этап – устранение воспалительного процесса в тканях десны
- 1.
 Наложение на десна и в карманы противовоспалительных и противомикробных средств
Наложение на десна и в карманы противовоспалительных и противомикробных средств - 2. Назначение антимикробных препаратов общего действия.
- 3. Назначение физиотерапевтических процедур.
3 этап – устранения зубодесневых карманов
-
1. Закрытый кюретаж.
Данная процедура – это профессиональная очистка зубодесневых карманов от зубных отложений при помощи специальных ручных инструментов — кюрет, выполняемая врачом под местной анестезией в несколько посещений. Она проводится при глубине кармана до 6-8 мм, и может рассматриваться как следующий, более радикальный этап профессиональной гигиены полости рта.
Процедура назначается только при отсутствии гноетечения, уменьшении воспаления и перевода заболевания из острой в хроническую стадию. После процедуры дёсна пациента и карманы обрабатываются антисептиком, может быть наложена пародонтальная повязка.
В легких и среднетяжелых случаях, эта процедура останавливает заболевание – в результате исчезает отек, зуд, кровотечение, небольшие зубодесневые карманы самостоятельно закрываются.
А тяжелых случаях, закрытый кюретаж является обязательным показанием перед хирургическим лечением тканей пародонта – он заметно уменьшает количество инфекции и ускоряет последующее послеоперационное заживление.
4 этап – восстановительный период
- 1. Тщательная домашняя гигиена и контроль за ней в соответствии со всеми рекомендациями врача-пародонтолога и врача-гигиениста.
- 2. Назначение препаратов, которые способствуют регенерации тканей и восстановлению обменных процессов в тканях пародонта.
5 этап — диспансерное наблюдение за состоянием пациента.
- 1. Профилактические визиты в клинику для контроля и прохождения плановых процедур профессиональной гигиены с целью не допустить повторного появления зубных отложений.
- 2. Курсовое прохождение медикаментозного и физиотерапевтического лечения для поддержания здоровья десен. Его назначают по индивидуальным показаниям.
Очень часто параллельно со специфическим стоматологическим лечением пациенту требуется лечение его основного сопутствующего заболевания у профильного специалиста.
Диагностика у хирурга
Хирургическое лечение пародонта
Закрытие рецессии
При пародонтозе антибиотики: назначение, разновидности, применение
.
Самая мучительная и неприятная боль – зубная. Поход к стоматологу – один из страшных моментов в жизни многих людей. И совершенно неважно, сколько тебе лет. Один вид стоматологического кресла приводит в тихий ужас многих, уже заранее знаешь что тебя ждет. Но, если болевые ощущения граничат с мучениями, хроническим недосыпанием и недоеданием, разве можно терпеть? Нет. Помимо кариеса и других повреждений зубной эмали, существует ряд заболеваний, связанных с воспалительным процессом полости рта. Одной из таких является пародонтоз.
Пародонтоз — расхождение зубов
Как он выглядит
Чаще всего, пародонтоз путают с пародонтитом. Они имеют схожесть, но есть и существенная разница. При пародонтите проходит воспалительный процесс, а при пародонтозе такового нет. Это говорит о том, что курс лечения тоже будет разниться.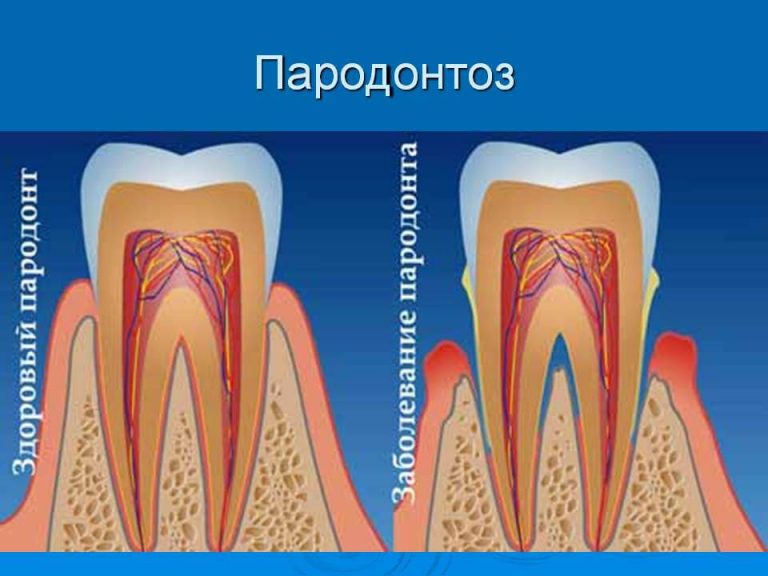 Причины возникновения пока не выяснены, но специалисты утверждают, что появление такого заболевания происходит на уровне генетики.
Причины возникновения пока не выяснены, но специалисты утверждают, что появление такого заболевания происходит на уровне генетики.
Если один из родителей или близких родственников страдает пародонтозом, то и у потомства оно также будет наблюдаться.
Начало заболевания малозаметно
Необходимо заметить, что, чаще всего, страдают данной болезнью люди:
- имеющие проблемы с желудочно-кишечным трактом;
- страдающие атеросклерозом или тромбозом;
- есть в анамнезе диагноз «сахарный диабет»;
- с авитаминозом.
Ко всему прочему люди, соблюдающие диеты и направленные на сильное похудение, где запрещается употребление мяса и молочных продуктов любой категории, помимо похудения получают в награду и пародонтоз, и прочие стоматологические проблемы.
Любое нарушение питания влияет на появление аномалий в ротовой полости.
Изменения в деснах при пародонтоза
Не следует считать, что микроорганизмы и бактерии – виновники болезни. Они вовсе не первопричина, а следствие положения дел. Они способствуют ухудшению состояния десен. Если же десна воспалились и начали кровоточить — это уже другое заболевание, а именно пародонтит. Налет на эмали, языке и деснах появляется в любом случае, что же касается причин пародонтоза, то они гораздо глубже.
Они вовсе не первопричина, а следствие положения дел. Они способствуют ухудшению состояния десен. Если же десна воспалились и начали кровоточить — это уже другое заболевание, а именно пародонтит. Налет на эмали, языке и деснах появляется в любом случае, что же касается причин пародонтоза, то они гораздо глубже.
Дифференциальный диагноз между пародонтитом и пародонтозом
Как понять, что проблема в ротовой полости не что иное, как пародонтоз? Существует ряд проявлений:
- околозубная часть десен медленно опускается, болевых ощущений как таковых нет, разрушаются стенки ближе к корню;
- шейка зуба просматривается все четче и без специальных инструментов в стоматологии;
- ткани десны очень сильно зудят, чешутся, появляется раздражение;
- появление реакции на холодную и горячую пищу, колющие ощущения во время еды сладкого или кислого;
- зубы становятся подвижными – это чувствуется не только во время прикусывания твердых продуктов, но также при чистке зубной щеткой;
- цвет десны бледнеет – это происходит из-за отсутствия достаточного кровотока в области десен и их подпитки;
- возникновение постоянной боли с характерным ноющим чувством около шейки зубов;
последняя стадия пародонтоза – потеря зуба.
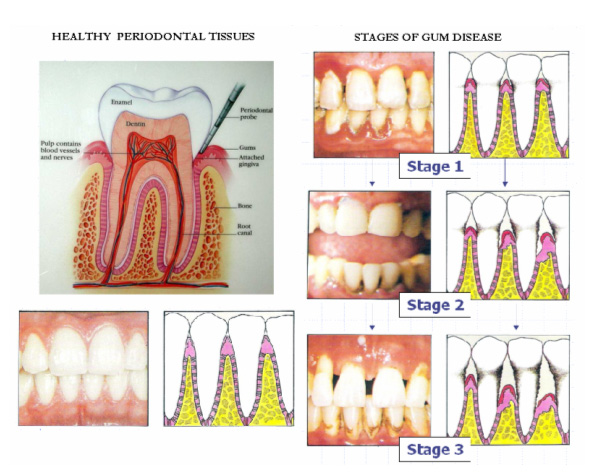
Выпадение зубов при запущенном пародонтозе
Особенностью заболевания является то, что оно осложняется прочими заболеваниями полости рта. Вызвано это появлением бактерий, которые при начальной форме были несущественны. Появится и грибок или вирус.
Чтобы диагностировать пародонтоз, потребуется обязательно сделать рентген. На снимке четко будет видна атрофия костных тканей в области десны, все изменения с этим связанные, а также дополнительные признаки атрофии.
Рентген снимок — диагностика пародонтоза на ранней стадии
Хронический пародонтоз с сопутствующими заболеваниями полости рта требует дополнительно провести анализы, такие, как мазок.
Лечение пародонтоза необходимо уже при первых симптомах и проявлениях заболевания, так как зубная эмаль начинает разрушаться уже на начальной стадии. Потери зубов также не исключены.
Можно ли терпеть?
Если вы понимаете, что заболевание уже появилось, врач подтвердил ваши догадки, то принимать антибиотики сразу не целесообразно, потому что их назначают уже при осложнениях и наличии бактериального налета на зубах и деснах. В зависимости от того, к какой группе принадлежат бактерии и микробы, будут назначены и лекарства. Следует заметить, что антибиотиками нарушается и микрофлора. Происходит ухудшение работы пищеварительной системы, а также иммунная система ослабевает. Ну и последнее, какие бы лекарственные формы не были, они дают толчок к развитию грибковых заболеваний.
В зависимости от того, к какой группе принадлежат бактерии и микробы, будут назначены и лекарства. Следует заметить, что антибиотиками нарушается и микрофлора. Происходит ухудшение работы пищеварительной системы, а также иммунная система ослабевает. Ну и последнее, какие бы лекарственные формы не были, они дают толчок к развитию грибковых заболеваний.
Никто не говорит, что все неприятные моменты следует терпеть. Если у вас наблюдается начальная стадия заболевания, лучше обратиться к другим методам лечения, которые будут направлены на купирование разрушающего процесса.
Специальные зубные пасты при пародонтозе
К сожалению, комплексных препаратов для лечения всех стадий пародонтоза пока не разработали. Чаще всего, применяют несколько систем для лечения недуга.
Сюда входит и массаж десен, способный восстановить кровообращение в тканях. Выполнять его совершенно не сложно в домашних условиях. Достаточно подобрать правильную для этого процесса зубную щетку (мягкая по жесткости). Для улучшения эффекта наносят специальные зубные пасты и гели. К таким относятся: Холисал и Метрагил.
Для улучшения эффекта наносят специальные зубные пасты и гели. К таким относятся: Холисал и Метрагил.
Антибиотики при пародонтозе – последнее спасение. А до этого существует лечение ультразвуковыми волнами, магнитными и электролечение. Среди прочих методов физиотерапии назначается дарсонвализация. В прочем все они должны восстанавливать и улучшать обменные процессы и кровообращение в тканях. Чем лучше происходит регенерация мягких тканей в полости рта, тем быстрее происходит купирование и лечение заболевания. Если же все указанные способы не устраивают, можно воспользоваться антисептиками.
Есть и народные рецепты. Использование пихтового настоя или настоек цветков календулы, масло чайного дерева, прополис. Все эти средства останавливают раздражение и разрушения. Десны перестают зудеть и опускаться. Все способы помогают только при начальных стадиях.
Настойка чистотела втирается в десна
Когда приходит время антибиотиков
Антибиотики при лечении пародонтоза появляются только при возникновении бактерий как на зубах, так и на деснах, либо болезнь перешла в запущенную форму и переросла в пародонтит. К каждой стадии, к каждому виду бактерий должен применяться только свой антибиотик. Его назначают исключительно после обследований и диагностических мероприятий.
К каждой стадии, к каждому виду бактерий должен применяться только свой антибиотик. Его назначают исключительно после обследований и диагностических мероприятий.
При пародонтозе антибиотики применяются только широкого спектра действия. Такие лекарственные формы способны уничтожать большое количество микробов и грибковых заболеваний. Перед применением обязательно необходимо сделать тест на принятие медикамента, так как принять препарат без пробы – риск получить аллергическую реакцию. Не все знают, на какой антибиотик или другое лекарство есть аллергия. Если пациент уже сталкивался с лечением антибиотиками, то он может знать реакцию своего организма.
Гепариновая мазь — эффективное средство от пародонтоза
Антибиотики при лечении пародонтоза могут применяться в разных формах:
- в таблетках или капсулах;
- как крем или как гель;
- жидкость для полоскания;
- в виде растворов для инъекций.
Чаще всего, назначают антибиотики в виде таблеток и капсул. Уже подмечено неоднократно, что именно в такой форме действуют они лучше. Препаратов достаточно много, но только два из них эффективные: Доксициклин и Метронидазол. Если их прописывать одновременно с Хлоргексидином, то это прекрасная возможность полностью нейтрализовать заболевание.
Уже подмечено неоднократно, что именно в такой форме действуют они лучше. Препаратов достаточно много, но только два из них эффективные: Доксициклин и Метронидазол. Если их прописывать одновременно с Хлоргексидином, то это прекрасная возможность полностью нейтрализовать заболевание.
Средства для полоскания полости рта при пародонтозе
Некоторыми специалистами признаются, как более современные и продуктивные для лечения, следующие медикаменты:
- сумамед;
- эрициклин и рондомицин;
- азитромицин.
Прием в домашних условиях без назначения врача запрещается, так как необходимо знать конкретную дозировку и способы приема.
Рисковать своим здоровьем (частые аллергические реакции, провоцирующие отек Квинке) не совсем целесообразно. Неправильная дозировка приведет к разрушительным действиям в таких органах, как печень и почки.
Метронидазол назначают при воспаленном пародонтозе
Назначение делает врач уже в тех случаях, когда совершенно нет другого решения.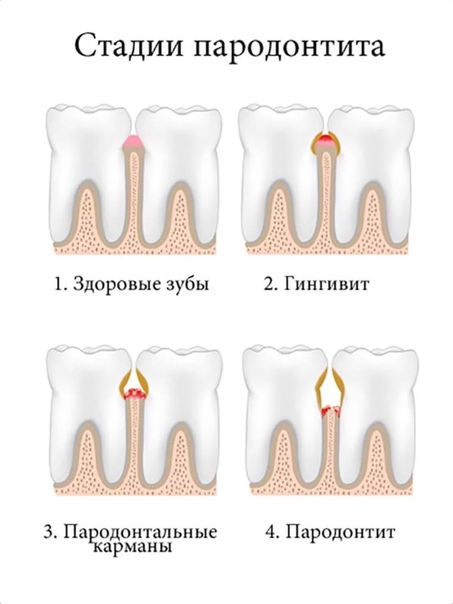 Зубы стали подвижными, а десна оголила большую часть корней. Такие процессы необходимо не только устранять, но и попытаться вернуть к более или менее нормальному виду. Но, может понадобиться и вмешательство хирурга.
Зубы стали подвижными, а десна оголила большую часть корней. Такие процессы необходимо не только устранять, но и попытаться вернуть к более или менее нормальному виду. Но, может понадобиться и вмешательство хирурга.
Антибиотики при пародонтозе могут назначать и при средней тяжести воспалительного процесса в тканях.
Виды и свойства антибиотиков при осложнениях
Не следует думать, что лекарства с повышенной антибактериальной способностью можно принимать только в виде инъекций. Они так быстрее воздействуют на кровоток, дают эффект и действуют значительно быстрее. Но, и пероральные препараты способны сделать невозможное, а именно истребить болезнетворные микробы.
Назначен Трихопол?
Тогда эффективность при лечении обеспечена. Максимальный результат в короткие сроки объясняется составом. Спектр действия всех компонентов большой и виды патогенных организмов будут побеждены в большей степени (если не все сразу). Схему приема и дозы может сказать только врач, который должен рассчитать дозировку, в зависимости от возраста и веса пациента. Хотя в инструкции к медикаменту есть особые указания на этот счет. Пить во время еды и не принимать за один день более трех таблеток. Лечение может длиться максимум неделю. Существует и ряд ограничений по приему Трихопола (беременность и период кормления грудью). Могут возникнуть аллергические реакции, нарушение работы почек. Лечебный эффект должен быть уже через 36 часов после приема первой капсулы. Но, если и на третий день эффекта не будет, то лучше отменить прием и воспользоваться другими препаратами для лечения пародонтоза.
Хотя в инструкции к медикаменту есть особые указания на этот счет. Пить во время еды и не принимать за один день более трех таблеток. Лечение может длиться максимум неделю. Существует и ряд ограничений по приему Трихопола (беременность и период кормления грудью). Могут возникнуть аллергические реакции, нарушение работы почек. Лечебный эффект должен быть уже через 36 часов после приема первой капсулы. Но, если и на третий день эффекта не будет, то лучше отменить прием и воспользоваться другими препаратами для лечения пародонтоза.
Препарат Трихопол имеет многогранное действие
Доксициклин
При лечении Доксициклином бактерии и микробы быстро погибают. По цене доступен каждому. Как и большинство антибиотиков, пьют после еды или во время нее. Максимальная доза в сутки – 3 капсулы. Ни в коем случае не растворять в воде. Большего результата достигнуть можно, если глотать целую таблетку. Если интересует, как действует, то можно обратиться к листку-вкладышу, где доступно все прописано.
Данный препарат очищает весь человеческий организм от микроорганизмов.
Соответственно, потребуется дополнительная терапия, чтобы заселить благоприятной флорой кишечник. Не следует употреблять таблетки людям, имеющим проблемы с печенью или почками, беременным и детям. В сочетании с другими лекарственными формами могут дать побочные эффекты, которые приводят к нарушению работы всего организма, причем по большей части страдает центральная нервная система.
Линкомицин
Следующий в списке антибиотик при пародонтозе – Линкомицин. Хотя цена более, чем доступна, но и вред от препарата велик, поэтому при назначении Линкомицина следует соблюдать все, что скажет врач, и дополнительно перепроверить все назначения, прочитав инструкцию к препарату. Самое главное – не рисковать и не принимать одновременно с Линкомицином еще лекарственные формы. Если пациент пользуется кремами или гелями от пародонтоза, то их потребуется отменить (в крайнем случае, проконсультируйтесь с врачом).
Линкомицин — сильный антибиотик
Мази с антибиотиками
Антибиотики при пародонтозе у взрослых могут быть не только в виде таблеток и капсул. К примеру, противомикробная мазь тоже является прекрасным средством для решения проблем. Она действует по большей степени только на мягких тканях, укоряет их регенерацию. По доступности существует ряд гелей, которые, чаще всего, применяют для лечения пародонтоза. К таким относят гепариновую мазь и Метрогил, Троксевазин и Элюгель.
Гель Метрогил Дента втирают в десна
Что можно добавить
Если возникли проблемы с деснами и зубами, то лучше не ждать осложнений, а начинать профилактические мероприятия и лечение. Касаемо лечебных курсов терапии, то здесь помогут только стоматологи. В профилактике помогут не лекарства, а зубные пасты. Они будут поддерживать тот результат, который был достигнут во время лечения. Вылечиться ими нельзя. Существует ряд паст, в состав которых входят антисептики и антибиотики. Их использовать можно не более двух недель.
Гель Холисал применяют для дезинфекции полости рта
Для профилактики и закрепления результата можно применять гели с антисептическим свойством или противовоспалительным.
Если же обращение было слишком поздно, то остается только один способ – хирургическое вмешательство. Чтобы этого избежать, необходимо следить за чистотой полости рта и обращаться своевременно в стоматологию.
Лечение пародонтита в Омске. Лечение десен. — Наши услуги — Авторская стоматология в Омске
Сохань С.С.
Хочу поблагодарить моего врача Мальцеву Валентину Григорьевну за профессионализм и хорошее отношение. Вообще в целом стоматологическая клиника «Элита» является одной из лучших клиник в Сибири. Сп …
Читать далееСуховеев. А.К.
Выношу благодарность Хамову Михаилу Александровичу за хорошую работу с клиентом. Так держать.
Читать далееРодионов Ю. П.
А мы опять сошли с ума, Всё, кроме масок, как и прежде, Вновь миром правит кутерьма, Вновь вспоминаем о надежде. И символ года сняв с лица, Тост произносим о здоровье, Порой для красного словца, Н …
Читать далееБилецкая Н.Ю.
Огромная благодарность Чеснокову В.А. и всей команде специалистов. Моя улыбка, ровные зубы их заслуга. Спасибо за труд, внимательное отношение. Михаилу Александровичу за моральную поддержку, добры …
Читать далееДементьева Е.А.
С Благодарностью к Вашей клинике и лично Савиновой Ольге Анатольевне. Спасибо за Ваш труд. Спасает проблемные зубы, за которые не берется ни один доктор. Очень внимательное отношение, доброе, что …
Читать далееПикалина З.Г.
Обслуживаюсь в клинике очень давно .Ни в какую другую просто не хочется. Здесь так мило, добро, тепло. Начиная с регистратуры и заканчивая обслуживающим персоналом -улыбка, доброжелательность на …
Читать далееОльга
Хочу выразить огромную благодарность всему коллективу клиники, а особенно Савиновой Ольге Анатольевне, Хамову Михаилу Александровне, Ковалевой Александре Владимировне. Лечусь в клинике уже много л …
Лечусь в клинике уже много л …
Страгис Анна
Спасибо чудесному доктору — Савиновой Ольге Анатольевне! Профессионал с большим сердцем!
Читать далееГорбунова Диана Львовна
Хочу поблагодарить замечательного доктора, профессионала с большой буквы и просто чудесного человека, очень доброго и заботливого, Ксению Сергеевну Хвостову! Ответственное отношение к решению проб …
Читать далееТитаренко О.А.
Большая благодарность Савиновой Ольге Анатольевне за оперативную, грамотную помощь. Я лечусь у Ольги Анатольевны почти 20 лет и ни разу не пожалела, что выбрала такого замечательного доктора.
Читать далееАнтибиотики при пародонтозе у взрослых
Пародонтоз – это атрофический (деструктивный) процесс, сопровождающийся глубоким поражением пародонта (околозубных тканей).
Иногда путают пародонтоз, пародонтит или периодонтит. Первые два вида заболевания характеризуются поражением околозубной ткани: десны, кости, связки и слизистой оболочки – пародонта. Разница в том, что при пародонтозе процесс не сопровождается воспалением, а при пародонтите – сопровождается. Соответственно, подходы к лечению различаются.
Разница в том, что при пародонтозе процесс не сопровождается воспалением, а при пародонтите – сопровождается. Соответственно, подходы к лечению различаются.
Не выяснены окончательно причины пародонтоза. В основном называют генетическую предрасположенность и неправильный гигиенический уход за ротовой полостью. Пародонтоз развивается на фоне хронических заболеваний органов пищеварения с нарушением секреции, болезней сосудов (атеросклероз, тромбоз), сахарного диабета, авитаминоза. Вызвать его могут длительные или частые жесткие диеты с целью похудения, в которых исключаются мясные, молочные продукты. Аномалия трофики (питания) тканей ротовой полости – также одна из причин поражения пародонта.
Пародонтоз и его клиническая картина
Вопреки расхожему мнению бактерии и другие микроорганизмы не являются первопричиной пародонтоза. Они могут усугубить его течение, но никогда не выступают возбудителями болезни. Такое мнение распространено, вероятно, из-за того, что путают пародонтоза с пародонтитом, который как раз вызывается микробами и имеет полную картину инфекционного заболевания: воспалительный процесс, кровотечение, нагноения, распад тканей.
Также при пародонтите отмечается хорошая фиксация зубов, малое количество зубных налетов и отложений, выделение гноя из десневых карманов и т.д.
В некоторых случаях пародонтит может предшествовать пародонтозу или сопровождать его.
Читайте далее: Проверенные данные об антибиотиках при зубной боли, опухшей десне
Основные симптомы пародонтоза проявляются следующим образом:
- Ткани около зуба постепенно безболезненно и бессимптомно разрушаются и «оседают».
- Обнажаются шейки зубов; это уже можно увидеть в зеркале при самоосмотре.
- В деснах чувствуется зуд, раздражение.
- Зубы реагируют на горячее и холодное, сладкое и кислое.
- Продолжающееся обнажение шеек зубов приводит к нарушению их фиксации.
- Десны приобретают бледную окраску из-за существенного нарушения кровообращения и трофики.
- Отмечается прогрессирующая атрофия тканей и выраженное расшатывание зубов.
- Возникает малоинтенсивная ноющая боль.
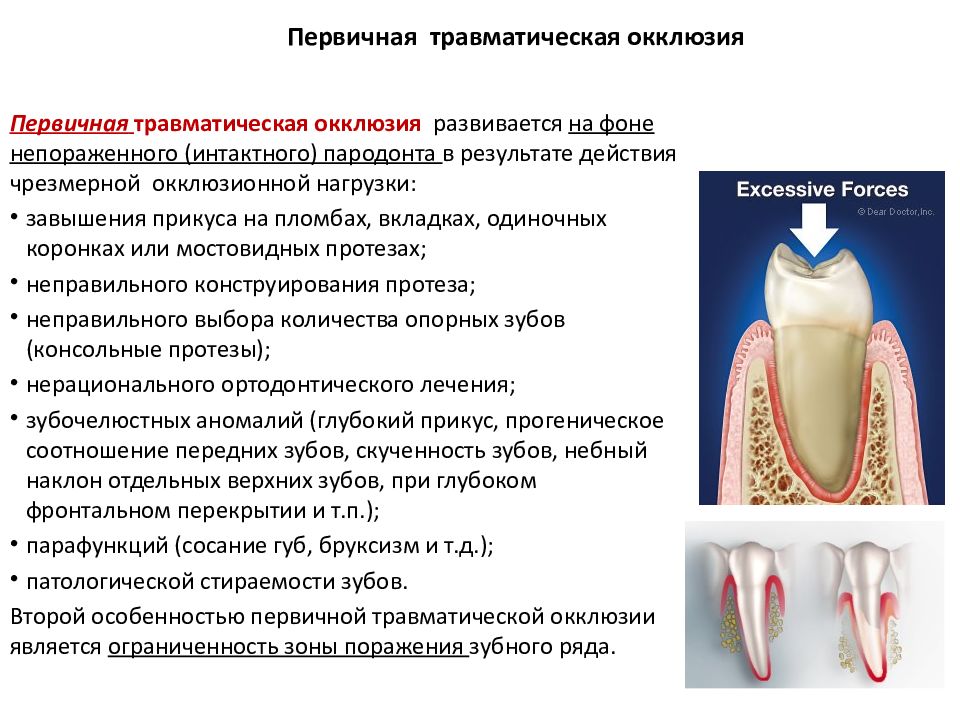
- Начинают выпадать зубы.
Пародонтоз может осложниться кариесом, пародонтитом, стоматитом, — рядом других заболеваний. Природа сопутствующих заболеваний может быть бактериальной (чаще всего), грибковой (чуть реже) и вирусной (относительно редко).
Для диагностики пародонтоза проводят обязательное рентген-обследование. Оно обычно показывает атрофию костной ткани десен (появление мелкоячеистого рисунка), склеротические изменения в ней, выявление очагов остеопороза и другие атрофические признаки.
При сопутствующих заболеваниях берут мазок из ротовой полости и другие материалы для анализов.
Важно! При появлении десневых карманов, нагноениях вокруг зубов, подвижности зубного ряда нужно немедленно обращаться к врачу – гигиенисту или стоматологу. Это явные признаки пародонтита, который чреват потерей зубов уже на первых стадиях течения болезни.
Наглядное видео:
Когда целесообразно лечение пародонтоза антибиотиками
Назначение антибиотиков при отсутствии признаков бактериального воспаление нецелесообразно.
- Во-первых, они помогают только при осложненном бактериальной инфекцией пародонтозе, для чего нужно получить результат мазка и уточнить возбудителя. Против каждой группы микробов есть своя группа антибиотиков.
- Во-вторых, не контролируемый прием антибиотиков может привести к усилению симптомов пародонтоза.
- В-третьих, антибиотики при длительном использовании провоцируют развитие грибковых заболеваний, что может спровоцировать обострение пародонтоза.
В связи с этим, чаще всего используют гели с антибиотиками для местного использования метрогил-дента и т.д.).
Лечение заболевания пародонтоз
Лечение заболевание проводится комплексно. Главная цель лечебных мероприятий – остановка атрофически-деструктивных процессов в тканях и стабилизация состояния пациента.
Нарушенное кровообращение восстанавливается массажем. Его пациент проводит самостоятельно после чистки зубов, используя специальную мягкую щетку. На щетку можно нанести специальные антисептические гели и пасты: метрогил дента®, холисал® и т. д.
д.
Физиотерапия
Широко применяются ультразвуковая терапия, электро- и магнитолечение, дарсонвализация и другие методы физиотерапии. Они направлены, в основном, на восстановление кровообращения и, как следствие, питания тканей, усиление регенерационных процессов пародонта.
Фито препараты
Пародонтоз обычно хорошо поддается лечению антисептиками, без приема таких сильных средств, как антибиотики.
Действенно точечное применение абисила (терпены – ненасыщенные углеводороды – сибирской пихты). Он улучшает питание и регенерацию тканей. Таким же образом применяют настойку календулы, тыквеол® (содержимое капсулы), масло чайного дерева, циклоферон® в форме линимента (бальзама для наружного применения), холисал, солкосерил (дентальная паста), люголь®, камистад®, метрогил дента®, метродент®, настойку прополиса. Все эти препараты улучшают кровообращение в мягких тканях, благотворно влияют на трофику, снимают зуд и раздражение, обеззараживают.
Подробнее ниже.
Спреи
Полость рта орошают спреями анти-ангин формула®, терафлю лар®, тантум верде®, стопангин®, максиколд лор®, мирамистин®, пропосол®. Спреи оказывают антисептическое воздействие, некоторые из них – охлаждают и снимают боль и зуд. Детям до трех лет распылители для спрея лучше заменить шприцем без иголки во избежание вдыхания препарата в момент распыления.
Леденцы
Для рассасывания рекомендуют таблетки, леденцы и пастилки с антисептическим, регенерирующим и слабым обезболивающим действием:
- аджисепт®,
- галавит®,
- гексализ®,
- фалиминт®,
- шалфей®,
- терасил®,
- суприма-лор®,
- стрепсилс (плюс, интенсив и так далее)®,
- септолете®,
- гексорал®,
- дрилл®,
- лизобакт®,
- новосепт форте®,
- ринза лорсепт анестетикс®.
Таблетки и пастилки обеззараживают, способствуют регенерации тканей, снимают неприятные ощущения, некоторые из них – обезболивают.
Полоскания
Для полоскания показаны ацилакт®, гексикон®, йокс-тева® (усиливает действие антибиотиков против стрептококков), водный раствор эвкалиптового масла и настойки эвкалипта, фурасол®, стоматофит®. Полоскание эффективно очищает полость рта от остатков пищи, действует мягче, чем зубная щетка (особенно это важно, когда обнаженные шейки зубов и поврежденные десны чутко реагируют на внешние раздражители), обеззараживает и освежает.
Оперативное лечение
Если антибактериальная терапия не помогла и заболевание прогрессирует, то назначается лазерное лечение; в тяжелых случаях или при отсутствии результатов консервативных методов проводится оперативное вмешательство.
Антибиотики при пародонтозе
Лечение пародонтоза антибиотиками показано, если:
- Пародонтоз осложнен бактериальной инфекцией.
- На зубах имеется выраженный бактериальный налет.
- Заболевание сочетается с пародонтитом.
Нормальная микрофлора ротовой полости представлена преимущественно анаэробной и факультативно — анаэробной флорой. В умеренном количестве присутствуют кокковые бактерии. В норме они не вызывают воспаления, но при чрезмерном росте их колонии возникают стоматиты, пульпиты, абсцессы мягких тканей полости рта.
Если бактерии, свойственные микрофлоре ротовой полости, начали патологический рост, либо произошло заражение посторонними микроорганизмами, назначаются антибиотики:
Макролиды
Из макролидов назначают экозитрин®. Это препарат из подгруппы экоантибиотиков – лекарств нового поколения, которые сохраняют нормальную микрофлору, не нарушают пищеварение и стул.
Терапевтическая переносимость эко антибиотиков гораздо выше, нежели у базовых препаратов предыдущего поколения. Также из макролидной группы назначают кларитромицин® и вильпрафен®. Они действуют эффективно и быстро, имеют мало побочных эффектов.
Метронидазол
®Наиболее эффективно применение гелей и паст с метронидазолом®. Также данный препарат может применяться в таблетированной форме (строго по показаниям).
Метронидазол® в комбинации с другими препаратами назначается при подозрении на микст-инфекцию. Это противомикробный препарат синтетического происхождения.
Прочие препараты
- Из хинолонов (фторхинолонов) прекрасно справляется с инфекциями полости рта Ципролет А®.
- Из антигрибковых антибиотиков для профилактики бактериальной и грибковой инфекций показаны леворин®, нистатин®. Эти препараты хороши тем, что препятствуют возникновению микозов на слизистой оболочке рта.
- Из антибиотиков других групп применяют граммидин®, грамицидин®. Они хороши тем, что разрешены детям, борются сразу с несколькими группами бактерий и усиливают действие других противомикробных средств.
Если врач только лишь на основе визуального осмотра ставит диагноз, без результатов анализов назначает антибиотики от пародонтоза десен, стоит подумать о посещении другого медработника. Для качественного и эффективного лечения диагноз нужно поставить минимум на основе рентгеновского снимка; в идеале – после проведения лабораторных анализов. А антибиотики при пародонтозе у взрослых и тем более детей назначаются только в случае, когда другие методы оказались бесполезны либо принесли лишь временное облегчение.
3 наиболее эффективных варианта
Только врач назначает антибиотики, которые нужно принимать при пародонтозе!
Наиболее эффективным и самым на сегодняшний день безопасным считается экозитрин®. Неплохой эффект дает вильпрафен®. Можно рекомендовать также граммидин®. Он подходит для лечения пародонтоза в комплексе и взрослым, и детям.
Правила приема антибиотиков
- Для профилактики развития дисбактериоза кишечника необходимо применять пробиотики.
- Антибиотики не сочетаются с алкоголем.
- Рекомендовано соблюдать облегченную диету.
- Таблетки запиваются только водой (запивать препараты чаем, соками, кофе и т.д. запрещено).
- Важно соблюдать назначенные схемы приема и дозировки.
Альтернативные методы лечения пародонтоза
Полосканиями настоями и отварами целебных трав помогают при комплексном лечении. Широко применяются травы:
- Зверобой – оказывает вяжущее и противовоспалительное действие.
- Эвкалипт – облегчает раздражение и зуд; антисептик и стимулирует регенеративные процессы в тканях.
- Ромашка – обеззараживает и снимает раздражение и воспаление.
- Кора дуба – имеет вяжущий эффект и эффективно заживляет микроповреждения полости рта.
- Календулы цветки – хорошо подсушивают, обеззараживают и заживляют повреждения мягких тканей.
- Шалфей – природный антисептик.
Полоскания и аппликации салфетками, пропитанными настоями трав, показаны для профилактики и на начальных стадиях болезни. Когда врач назначит медикаментозное лечение, а пациент хочет продолжать терапию народными средствами, нужно обговорить допустимые препараты нетрадиционной медицины, которые усилят действием фармацевтических средств или хотя бы не снизят их эффект.
Полностью излечить пародонтоз можно только на ранних стадиях. Если запустить болезнь, она приведет к потере зубов и необратимым процессам в костной ткани десны, при которых даже имплантировать зубы будет трудно или невозможно.
Читайте далее: Все 7 групп антибиотиков в стоматологии
Врач инфекционист высшей категории с многолетним опытом работы.
Специалист в области терапии инфекционных заболеваний различной этиологии, методах лабораторной диагностики биоматериала.
Новые возможности местной антибактериальной терапии воспалительных заболеваний пародонта на фоне патологии органов пищеварения | Булкина Н.В., Островская Л.Ю.
Многочисленные клинические наблюдения свидетельствуют о том, что заболевания желудочно–кишечного тракта (ЖКТ) сопровождаются патологическими изменениями тканей пародонта [2]. Патология полости рта диагностируется у 92% больных с заболеваниями ЖКТ, и в основном она представлена пародонтитом.
Главной особенностью заболеваний пародонта на фоне хронического поражения ЖКТ является более ранняя, чем у лиц без фоновой патологии, генерализация патологического процесса, т.е. уже на ранних стадиях в патологический процесс вовлекается пародонт всех зубов, отмечаются более интенсивные явления воспаления, нередко сопровождающиеся выделением гноя из пародонтальных карманов. У больных с сочетанной гастродуоденальной патологией течение пародонтита часто носит непрерывно рецидивирующий характер, отмечается резистентность к традиционной терапии, ремиссия заболевания отличается нестойкостью [1].Согласно современной точке зрения воспалительные заболевания пародонта относятся к инфекционным хроническим воспалительным заболеваниям, поэтому нормализация микрофлоры является непременным условием их рациональной терапии. Хорошо известно, что при хроническом гингивите и пародонтите происходит отчетливый сдвиг в сторону преобладания анаэробной флоры: по данным Slots J., при воспалении в пародонтальных карманах количество штаммов анаэробных бактерий увеличивается до 70–80%, тогда как в норме количество анаэробов не превышает 20–30%.
В последние годы большое значение в развитии язвенной болезни придается инфекционному фактору – Helycobacter pylory – HP [3,6,8,13]. Имеются данные об обнаружении этих бактерий в микросреде зубных бляшек и слюне. Пародонтальные карманы могут служить естественным резервуаром для Helycobacter pylory, так как при этом обеспечиваются микроаэробные условия [9]. Не вызывает сомнения тот факт, что хеликобактериоз инициируется попаданием Helycobacter pylory в полость рта по орально–оральному или фекально–оральному пути передачи и депонируется в ней, как в постоянном резервуаре [5,10,12].
Ряд исследователей рассматривают присутствие НР в полости рта, как источник реинфекции слизистой оболочки желудка у больных язвенной болезнью двенадцатиперстной кишки (ЯБДК) [4,11]. Другие [7], обнаружив тотальную инфицированность НР, полагают, что данный микроорганизм в полости рта является комменсалом.
Таким образом, наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается или на фоне сниженного иммунитета, или сам приводит к его изменению [9].
Этим и объясняется целесообразность применения антибактериальных средств. Вместе с тем широкое (а подчас необоснованное и бесконтрольное) применение химиопрепаратов приводит к формированию штаммов с резистентностью к антибиотикам. Установлено, что их селекция происходит, в частности, при резких перепадах концентрации препаратов, что наблюдается при местном применении различных антибактериальных лекарственных форм (в виде полосканий, паст и гелей, легко смываемых слюной). Разрешение этой проблемы может быть реализовано следующими путями:
– использование антисептических препаратов, которые в отличие от антибиотиков обладают широким антибактериальным спектром и не индуцируют резистентность микробов;
– создание пролонгированных лекарственных форм на основе компонентов, сорбирующихся на слизистой оболочке полости рта или создающих депо длительное время в пародонтальных карманах.
На сегодняшний день «золотым стандартом» анаэробицидных средств является метронидазол, демонстрирующий, в частности, высокую эффективность при воспалительных заболеваниях пародонта, в особенности в сочетании с хлоргекседином.
Метронидазол – производное нитроимидазола, обладающего антипротозойным и антибактериальным действием против анаэробных бактерий, простейших, вызывающих пародонтит: Porphyromonas gingivalis, Prevotella intermedia, P. denticola, Fusobacterium fusiformis, Wolinella recta, Treponema sp., Eikenella corrodens, Borrelia vincenti, Bacteroides melaninogenicus, Selenomonas sp. Восстановленная 5–нитрогруппа метронидазола взаимодействует с ДНК клетки микроорганизмов, ингибируя синтез их нуклеиновых кислот, что ведет к гибели микроорганизмов.
Хлоргекседин – антисептик бактерицидного действия против широкого круга вегетативных форм грамотрицательных и грамположительных микроорганизмов, а также дрожжей, дерматофитов и липофильных вирусов. На споры бактерий действует только при повышенной температуре. В низких концентрациях хлоргекседин вызывает нарушение осмотического равновесия бактериальных клеток и выход из них калия и фосфора, что приводит к бактериостатическому эффекту. Сохраняет активность в присутствии крови и гноя. Не токсичен, не кумулируется в организме, отсутствует канцерогенное действие.
Гель для десен «Метрогил дента профессиональный» – единственный препарат в готовом к стоматологическому применению виде, который содержит метронидазол 25% и хлоргекседин в форме 0,1% раствора хлоргекседина глюконата в стабильных концентрациях.
«Метрогил дента профессиональный» имеет приятный вкус, водорастворим, поэтому не препятствует оттоку экссудата. Гель обладает высокой текучестью, поэтому может полностью заполнять пародонтальный карман. После контакта с десневой жидкостью, содержащей эстеразы, происходит гидролиз неактивного метронидазола бензоата. Метронидазол оказывает анаэробицидное действие на бактерии, находящиеся в пародонтальных карманах или зубодесневой борозде.
В своей работе мы изучили особенности состояния тканей пародонта у больных язвенной болезнью, а также оценили эффективность влияния местного применения препарата «Метрогил дента профессиональный» с целью стабилизации данной сочетанной патологии.
Нами были обследованы 70 больных ЯБДК, ассоциированной с НР, в сочетании с воспалительными заболеваниями пародонта в возрасте от 18 до 45 лет, из них с хроническим катаральным гингивитом – 30, генерализованным пародонтитом легкой степени – 19, средней – 11, тяжелой – 10.
Все больные были разделены по группам. В первой группе (группа сравнения) местное лечение заболеваний пародонта включало снятие зубных отложений с последующим полированием поверхностей. Во второй группе (35 человек) наряду с общепринятыми мероприятиями проводили аппликацию «Метрогил дента профессиональный».
Всем пациентам с ЯБДК проводили эрадикационную терапию, включавшую ингибитор протонной помпы омепразол по 20 мг 2 раза в сутки и два антибактериальных препарата: кларитромицин 500 мг 2 раза в сутки и амоксициллин по 1 г 2 раза в сутки в течение 7 дней. Контроль эрадикации осуществляли через 8 недель после окончания терапии.
При гингивите и пародонтите легкой степени после удаления зубных отложений, проведения кюретажа и медикаментозной обработки десневого края, гель «Метрогил дента профессиональный» вводился в пародонтальные карманы 2 раза в сутки, курс лечения составил 5–7 дней. Отмечалось выраженное противовоспалительное действие препарата, которое выражалось в уменьшении гиперемии и отека десневого края уже на 2–й день применения препарата у больных катаральным гингивитом, в снижении кровоточивости десен, что подтверждалось положительной динамикой индексных показателей (ГИ, РМА).
Лечебный эффект при пародонтите легкой степени достигался на 5–7–й день аппликаций препаратом «Метрогил дента профессиональный» на приеме с одновременными аппликациями «Метрогил дента» в домашних условиях в течение 5–7 дней. Десневые сосочки приобрели нормальную форму и величину, восстановился их цвет, исчезла кровоточивость. У 87,3% больных с хроническим генерализованным пародонтитом к 5–7 дню индекс гигиены достоверно снижался и составил 1,8±0,07. Также уменьшался индекс РМА, который составил 9,8±0,6 по сравнению с началом лечения 67,8±2,3. Кровоточивость десен исчезла. Индекс ПИ достоверно не изменялся.
Проведение стоматологических мероприятий в сочетании с лечением заболеваний органов пищеварения, в том числе и эрадикационной терапией, привело к восстановлению структуры пародонта у обследованных пациентов.
Анализ результатов терапии больных группы сравнения показал, что продолжительность курса лечения удлинялась на 7–9 дней. Наблюдалось снижение индексов гигиены и РМА до 1,9±0,1 и 12,01±0,48 соответственно.
В течение месяца у всех пациентов с фоновой патологией пищеварительного тракта также была достигнута клинико–эндоскопическая ремиссия. Положительная динамика клинической картины подтверждена данными морфологического исследования слизистой оболочки желудка.
При исследовании мазков–отпечатков с зубного налета отмечено, что частота обнаружения НР у пациентов с хроническим гингивитом составляет 25%, у пациентов с хроническим пародонтитом – 32,3%.
Эрадикация НР в антральном отделе желудка была достигнута у 80% пациентов с НР–ассоциированной ЯБДК в сочетании с хроническим гингивитом и у 78,5% в сочетании с хроническим пародонтитом.
В течение полугода у 30,8% больных наблюдалось рецидивирование ЯБДК, что сочеталось с обострением хронического пародонтита. Среди пациентов с ЯБДК с развитием рецидива заболевания у 70% больных эрадикация НР в антральном отделе желудка и ротовой полости была неэффективной, а у 30% пациентов, несмотря на уничтожение микроорганизма в антральном отделе желудка, сохранялось персистирование НР в полости рта, что, очевидно, служило источником реинфекции слизистой оболочки желудка и причиной рецидива пептической язвы.
Следовательно, одним из факторов достижения стабильной ремиссии заболеваний пародонта у больных с фоновой H. pylori–ассоциированной патологией верхних отделов пищеварительного тракта является успешная эрадикация микроорганизма в желудке и полости рта с ликвидацией на этом фоне воспалительных изменений в слизистой оболочке желудка.
Заключение
Проведенное исследование подтверждает важность комплексного лечения заболеваний пародонта и НР–ассоциированной патологии верхних отделов пищеварительного тракта с проведением эрадикационной терапии, направленной на уничтожение микроорганизма и в полости рта, и в антральном отделе желудка. Эрадикация НР в полости рта служит важным звеном вторичной профилактики как язвенной болезни двенадцатиперстной кишки, так и воспалительных заболеваний пародонта. Использование геля «Метрогил дента профессиональный» позволяет сократить сроки наступления стабилизации воспалительно–деструктивных процессов в тканях пародонта и способствует эрадикации Нр в полости рта.
Литература
1. Балобанова И.Г., Чуршина Т.В., Балобанов В.Ю. О взаимосвязи пародонтита с гастродуоденальной и гепатобилиарной патологией у лиц молодого возраста // Современные тенденции развития гастроэнтерологии: (Тез. докл. науч.– практич. конф., 20–21 апр. 1995 г.) Ижевск, 1995. С.11–12.
2. Григорьян А.С., Грудянов А.И., Рабухина Н.А., Фролова О.А. Болезни пародонта //Руководство для врачей. – Москва, 2004. – 287с.
3. Ивашкин В.Т., Лапина Т.Л. Инфекция Helicobacter pylori:современное состояние проблемы // Русский медицинский журнал. – 1996. – №3. – С.140–150.
4. Цимбалистов А.В., Робакидзе Н.С. Влияние стоматологического статуса больных язвенной болезнью на инфицированность полости рта и слизистой оболочки желудка Helicobacter pylori // Клиническая стоматология. – 2001. – №1. – С.16–18.
5. Desai H.G., Gill H.H., Shankarai K., Mehta P.R., Prabhu S.R. Dental plaque: a permanent reservoir of Helycobacter pylori?// Scand. J. Gastroenterol. – 1991. – 26(11): 1205–8.
6. Graham D.Y. Campylobacter pylori and peptic ulcer disease // Gastroenterology. – 1989. – Vol.96. – P.615–625.
7. Karczewska E., Konturek J.E., Konturek P.C. et al. Oral cavity as a potential source of gastric reinfection by Helicobacter pylori // Dig. Dis. Sci. – 2002. – Vol.47, N5. – P.978–986.
8. Price A.B., Levi J., Dolby J.M. et al. Campylobacter pyloridis in peptic ulcer disease: microbyology, pathology and scanning electron microscopy // Cut. – 1985. – Vol.21, N3. – P.1183–1188.
9. Schein W., Meryn S. Helycobacter pylori and the mouth cavity – overview and perspectives // Wien – Klin. – Wochenschr. – 1994. – 106(17): 547–9.
10. Shames B., Krajden S., Fuksa M., Babida C., Penner J.L. Evidance for the occurance of the same strain of Campylobacter pylori in the stomach and dental plaque // J. Clin. Microbiol. – 1989. – 27(12): 2849–50.
11. Song Q., Haller B., Ulrich D., A. et al. Quantitation of Helicobacter pylori in dental plaque samples by competitive polymerase chain reaction // J. Clin. Pathol. – 2000. – Vol.53, N3. – P.218–222.
12. Thomas J.E., Gibson G.R., Darboe M.K., Dale A., Weaver L.T. Isolation of Helycobacter pylori from human faeces // Lancet. – 1992. – 340(8829): 1194–5.
13. Wyatt J.I. Campylobacter pylori, duodenitis and duodenal ulceration./ In: Rathbone B.J., Heatley R.V.(eds) Campylobacter pylori and gastroduodenal disease. – Blackwell. – Oxford, 1989. – P.117–124.
.
Виды пародонтита
Очаговый пародонтит
Очаговый пародонтит это форма воспалительного процесса расположенная локализовано, то есть отдельно на определенном участке пародонта, в области одного, двух или нескольких зубов, при условии полного или относительного здоровья остальных пародонтальных тканей. Чаще всего причиной его становятся местная травматизация, например: завышенная пломба, или нависающая, натирание некорректно установленной коронки или мостовидного протеза. Чаще всего локализованный пародонтит проявляется в острой форме, то есть начинается резко, непредвиденно, внезапно, с быстро нарастающими клиническими симптомами.
Генерализованный пародонтит
Генерализованный пародонтит, иначе именуемый диффузным, характеризуется патологическими изменениями пародонтальных тканей в области практически всех или всех зубов в зубном ряду. Чаще носит хроническую форму, имеет бактериальную этиологию, начало заболевания, как правило, бессимптомно, безболезненно.
Генерализованный пародонтит
Острый пародонтит
Острый пародонтит воспалительный процесс в пародонтальных тканях полости рта характеризующийся резким появлением боли, отека, кровоточивости, нередко появлением гнойного экссудата или сукровичных выделений из десневого кармана.
Хронический пародонтит
Хронический пародонтит – форма воспалительного процесса протекающего в тканях пародонта, циклического характера (смена рецидивов – обострений и ремиссий – затуханий).
Хронический пародонтит
Хронический генерализованный пародонтит
Хронический генерализованный пародонтит – форма болезни, имеющая диффузный характер поражения пародонтальных тканей. Характеризуется сменой ремиссий и рецидивов.
Гнойный пародонтит
Гнойный пародонтит – патологическое состояние пародонта, при котором из образованных десневых карманов выделяется гнойный экссудат. Запущенный гнойный пародонтит может стать причиной развития абсцесса.
Абсцедирующий пародонтит
Абсцедирующий пародонтит, осложненная форма пародонтита, характеризующаяся развитием гнойного очага – абсцесса.
Агрессивные формы пародонтита
Агрессивные формы пародонтита – формы пародонтита с нетипичным течением, вызванные микроорганизмами способными быстрее и сильнее проникать в ткани пародонта, обладающими наиболее выраженными патогенными свойствами.
Классификация агрессивных форм пародонтита
- Хронический пародонтит взрослых
- Рано возникающий пародонтит (РВП)
- Препубертатный пародонтит
- Ювенильный пародонтит (пародонтоз)
- Быстропрогрессирующий пародонтит
- Тип А.
- Тип В.
- Рефрактерный пародонтит
- Язвенно-некротический гингиво-пародонтит
- Пародонтит, ассоциированный с системными заболеваниями
Пародонтит взрослых
Название данного подтипа говорит само за себя. Пародонтит взрослых это патологическая медленно развивающаяся форма пародонтита поражающая лиц старше 35 лет. Чаще всего потеря костной ткани у таких пациентов происходит по горизонтальному типу, однако не исключается и вертикальная – угловая потеря.
Характерной особенностью данного заболевания является его этиология, а именно провокация его развития грамм-отрицательными бактериями.
Пародонтит у взрослого человека
При обследовании пациентов с данной формой заболевания, патологически измененные клетки крови не обнаруживаются. В многообразии пародонтологических болезней именно данный недуг является самым распространенным среди взрослого населения.
Пародонтит препубертатный
Препубертатным пародонтитом по праву считается пародонтит, возникающий после прорезывания постоянных зубов. Сама по себе данная форма заболевания встречается достаточно редко, однако ее распространенность все-таки позволила выделить две формы: локализованную и генерализованную.
Ювенильный пародонтит (десмодонтоз)
Ювенильный пародонтит (десмодонтоз)
У некоторого, незначительного количества подростков встречается ЛЮП – локализованный ювенильный пародонтит. Как правило, начало развития патологии приходится на пубертатный период. Классическим вариантом развития заболевания является вертикальная потеря кости у первых моляров, нередко в данный процесс вовлекаются и резцы. Примечательно то, что выраженная потеря кости может развиваться практически бессимптомно.
Налета в значительном количестве не обнаруживается. Симптоматики воспалительного процесса нет, или она очень скудная.
Отдельные пародонтологи, поддерживают теорию о семейной предрасположенности, так как при данном заболевании в крови обнаруживаются нейтрофилы или моноциты функционально не полноценные, однако оба типа клеток при данной патологии дефектов иметь не могут.
Также отмечается в 3 раза увеличенная частота случаев ЛЮП у лиц женского пола.
Иногда причиной данного состояния может стать одна из форм неспецифических анаэробных бактерий, относящихся к грамм-отрицательным. Что подтверждается положительной динамикой при лечении ЛЮП антибиотиками в составе комплексной терапии.
Помимо прочего, для юношеского пародонтита, не редкость и генерализованная форма, когда в патологический процесс вовлекается полностью зубной ряд.
Быстро прогрессирующий пародонтит
Данная форма пародонтита характерна для лиц, вышедших из пубертатного периода, и младше 35 лет. Характеризуется выраженной потерей альвеолярной кости, в генерализованной форме – вокруг большинства зубов. В данном случае потеря кости может происходить как по вертикальному, так и по горизонтальному типу, а также в их комплексе.
Быстро прогрессирующий пародонтит
Для данного заболевания также характерно несоответствие количества налета и степени деструктивных изменений кости. Некоторые случаи развития быстропрогрессирующего пародонтита можно ассоциировать с наличием таких системных заболеваний, как сахарный диабет, или синдром Дауна, однако они нередко встречается у лиц, не имеющих подобных системных патологий.
Быстро прогрессирующий пародонтит внутри своей формы подразделяется еще на два типа, оба они характеризуются быстрой генерализованной потерей кости и прикрепления, а делятся по возрастной категории пациентов. А именно:
- к типу А относят пародонтит, развившийся у пациентов в возрасте от 14-26 лет
- к типу В относят быстропрогрессирующий пародонтит поражающий пародонт у пациентов в возрасте от 26 до 35 лет.
Независимо от типа, заболевание часто рецидивирует, несмотря на успешность и качество проведенной терапии.
Рефрактерный пародонтит
Язвенно-некротический гингиво-пародонтит
Рефрактерный пародонтит это особый вид пародонтита, который, несмотря на постоянное проведение терапевтических мероприятий, продолжает развиваться, что сопровождается потерей костной ткани одновременно в нескольких участках.
Язвенно-некротический гингиво-пародонтит
Чаще всего данное заболевание является следствием нелеченого острого язвенно-некротического гингивита, особенно длительно продолжающихся и рецидивирующих форм, а также при недостаточном их лечении. Эпизодически повторяющаяся активность патологии приводит к разрушению тканей пародонта, и как следствие к образованию, как межзубных, так и десневых кратеров. Также цикличность течения заболевания негативно отражается на возможности адекватного ухода и лечения.
Антибиотики в лечении агрессивного пародонтита
J Pharm Bioallied Sci. 2012 Авг; 4 (Дополнение 2): S252 – S255.
Abinaya Prakasam
Отделение пародонтологии, Стоматологический колледж и больница JKK Натараджа, Комарапалаям, Индия
С. Сугумари Элаварасу
Отделение пародонтологии, Стоматологический колледж и больница JKK Натараджа, Комарапалаям , Индия 1 Отделение пародонтологии, Стоматологический колледж и больница Тагора, Вандалур, Ченнаи, Тамилнад, Индия
Отделение пародонтологии, Стоматологический колледж и больница JKK Натараджа, Комарапалаям, Индия
1 Отделение пародонтологии, Стоматологический колледж и больница Тагора, Вандалур, Ченнаи, Тамилнад, Индия
Получено 1 декабря 2011 г .; Пересмотрено 2 января 2012 г .; Принята в печать 26 января 2012 г.
Авторские права: © Journal of Pharmacy and Bioallied SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа правильно цитируется.
Эта статья цитируется в других статьях в PMC.Abstract
Агрессивный пародонтит, хотя и встречается не редко, но является довольно неизвестным заболеванием. Мало что известно о его оптимальном управлении.В то время как большинство пациентов с распространенными формами заболеваний пародонта предсказуемо хорошо реагируют на традиционную терапию (инструкции по гигиене полости рта (OHI), безоперационная обработка раны, хирургия и поддерживающая пародонтальная терапия (SPT)), пациенты с диагнозом агрессивной формы пародонтоза часто делают это. не отвечает предсказуемо / благоприятно на традиционную терапию из-за ее сложной многофакторной этиологии. Протоколы лечения агрессивного пародонтита в значительной степени эмпирически. Существуют убедительные доказательства того, что дополнительное лечение антибиотиками часто приводит к более благоприятному клиническому ответу, чем обычная терапия.В этой статье основное внимание уделяется роли дополнительного использования фармакологических средств в улучшении прогноза и результатов лечения пациентов с агрессивным пародонтитом.
КЛЮЧЕВЫЕ СЛОВА: Антибиотики, агрессивный пародонтит, дополнительное применение системных антибиотиков, модуляция хозяина
Агрессивный пародонтит, по определению, вызывает быстрое разрушение пародонтального прикрепительного аппарата и поддерживающей альвеолярной кости. Он может быть локализованным или обобщенным.Двумя общими чертами обеих форм являются (1) быстрая потеря прикрепления и разрушение кости у клинически здорового пациента и (2) семейная агрегация [1]. Эти пациенты часто имеют ограниченные микробные отложения, которые кажутся несовместимыми с серьезностью разрушения тканей. Однако присутствующие отложения часто имеют повышенные уровни Aggregatibacter (ранее Actinobacillus ), actinomycetemcomitans , [2] или Porphyromonas gingivalis .Эти пациенты могут также иметь аномалии фагоцитов и гиперчувствительный фенотип моноцитов / макрофагов. Эти клинические, микробиологические и иммунологические особенности предполагают, что пациенты с диагнозом агрессивный пародонтит будут иметь плохой прогноз. Чувствительность агрессивного пародонтита к традиционному лечению пародонта непредсказуема, и общий прогноз для этих пациентов хуже, чем для пациентов с хроническим пародонтитом.
Однако при определении прогноза клиницист должен учитывать дополнительные особенности локализованной формы заболевания.Локализованный агрессивный пародонтит обычно возникает примерно в возрасте полового созревания и локализуется на первых молярах и резцах [3]. Пациент часто демонстрирует сильный ответ сывороточных антител на инфекционные агенты, что может способствовать локализации поражений. При ранней диагностике их можно лечить консервативно с помощью ОГИ и системной антибиотикотерапии, что дает отличный прогноз. При более запущенном заболевании прогноз все еще может быть хорошим, если поражение лечить с помощью хирургической обработки раны, местных и системных антибиотиков и регенеративной терапии.Напротив, пациенты с генерализованной формой заболевания также молоды с генерализованной потерей межзубного прикрепления и плохим ответом антител. Часто присутствуют вторичные способствующие факторы, такие как курение сигарет. Эти факторы в сочетании с изменением защиты хозяина, наблюдаемым у многих из этих пациентов, могут привести к тому, что заболевание не будет хорошо поддается традиционной пародонтальной терапии (удаление зубного камня с выравниванием корня, инструкция по гигиене полости рта и хирургическое вмешательство). Следовательно, у этих пациентов часто бывает справедливый, плохой или сомнительный прогноз, и следует рассмотреть возможность использования системных антибиотиков для контроля болезни.
Антимикробная терапия
Присутствие пародонтальных патогенов, в частности A. actinomycetemcomitans , считается причиной того, что агрессивный пародонтит не поддается лечению только традиционной терапией. Известно, что эти патогены остаются в тканях [4] после терапии и повторно инфицируют карман. Идентификация A. actinomycetemcomitans как главного виновника и открытие того, что этот организм проникает в ткани, открыли другую перспективу патогенеза агрессивного пародонтита и дали новую надежду на терапевтический успех, а именно применение антибиотиков.Считалось, что использование системных антибиотиков необходимо для устранения патогенных бактерий из тканей. [4]
Имеются убедительные доказательства того, что дополнительное лечение антибиотиками часто приводит к более благоприятному клиническому ответу, чем только механическая терапия. Действительно, несколько авторов сообщили об успешном лечении агрессивного пародонтита с помощью антибиотиков в качестве дополнения к стандартной терапии.
Сравнение эмпирической терапии с микробиологическим тестированием
Выбор антибиотиков может быть эмпирическим или основываться на информации о природе патогенных микроорганизмов и / или их профиле чувствительности к антибиотикам.В настоящее время нет прямых доказательств того, что микробиологическая диагностика и целенаправленный выбор режима антибиотиков дает дополнительную пользу по сравнению с эмпирическим использованием [5]. На практике антибиотики часто используются эмпирически без микробиологического тестирования. Исследования, проведенные для оценки эффективности микробного тестирования, пришли к выводу, что полезность микробного тестирования может быть ограничена и что эмпирическое использование антибиотиков, таких как комбинация амоксициллина и метронидазола, может быть более клинически обоснованным и экономически эффективным, чем идентификация бактерий и чувствительность к антибиотикам. тестирование.Использование таких мер может быть рассмотрено всякий раз, когда агрессивный пародонтит не помогает или если деструкция продолжается, несмотря на хорошие терапевтические усилия.
Обоснование антибактериальной терапии
Обоснованием использования фармакологических средств для лечения агрессивных форм пародонтоза является устранение инициирующих факторов и пораженных тканей с помощью традиционной терапии и дополнение ее системными фармакологическими средствами для устранения патогенов, оставшихся в тканях.В таких случаях следует подчеркнуть, что использование антибиотиков так же важно, как и традиционная терапия. [6] Механическое лечение может непредсказуемо устранить предполагаемые патогены, такие как A. actinomycetemcomitans , из субдесневой области из-за того, что они недоступны для механического вмешательства, особенно в таких областях, как вогнутости корней, развилки и их способность проникать в ткани пародонта и дентинные канальцы. Устойчивость в недоматных областях, таких как тыльная сторона языка или миндалины, снова является важной проблемой.
Хотя использование антибиотиков в лечении пародонта, вероятно, всегда будет противоречивым, отчеты Американской академии пародонтологии и Европейской федерации пародонтологии содержат ценные рекомендации по их применению. В обоих этих отчетах после исчерпывающего литературного поиска было установлено, что пациентам с агрессивным пародонтитом, по-видимому, полезно дополнительное применение системных антибиотиков во время лечения.
Системное введение антибиотиков
Идеальный антибиотик для использования в профилактике и лечении заболеваний пародонта должен быть специфичным для пародонтальных патогенов, аллогенным и нетоксичным, существенным, не используемым для лечения других заболеваний и недорогим.[7] В настоящее время идеального такого антибиотика не существует. [6] Хотя бактерии полости рта чувствительны ко многим антибиотикам, ни один антибиотик в концентрациях, достигаемых в биологических жидкостях, не подавляет все предполагаемые пародонтальные патогены. Действительно, предполагается, что для устранения всех предполагаемых патогенов из некоторых пародонтальных карманов может потребоваться комбинация лекарств.
Тетрациклины
Тетрациклины широко используются для лечения рефрактерных форм пародонтоза, включая локализованный агрессивный пародонтит.Они обладают способностью концентрироваться в тканях пародонта и подавлять рост A. actinomycetemcomitans . [8] Кроме того, они проявляют антиколлагеназный эффект, который может ингибировать разрушение тканей и способствовать регенерации костей. Механическое удаление зубного камня и зубного налета с поверхности корней может не уничтожить бактерии из тканей пародонта. Системный тетрациклин может уничтожать тканевые бактерии, и было показано, что он останавливает потерю костной массы и подавляет уровень микробов в сочетании с масштабированием и строганием корней.[9] Рекомендуемая дозировка составляет 250 мг 4 раза в день (4 раза в день).
Доксициклин
Важность доксициклина проистекает из того факта, что он имеет более высокую доступность в десневой щели по сравнению с другими препаратами, в 7–20 раз больше, чем любой другой препарат [10]. Второй по важности фактор — это двойной механизм действия. В качестве антибиотика он оказывает более значительное действие против A. actinomycetemcomitans , что позволяет использовать его при агрессивном пародонтите [10].
Кроме того, его действие не ограничивается антимикробной активностью, но включает следующие свойства модуляции хозяина:
-
Антиколлагеназа
-
Противовоспалительное
-
Ингибирование резорбции кости
-
Способствует повторному прикреплению
-
Химически модифицированный тетрациклин (CMT).
Концепция низких доз доксициклина (LDD)
Поскольку доксициклин можно назначать только один раз в день, это делает его более совместимым с пациентами. Соответствие также приветствуется, потому что абсорбция из желудочно-кишечного тракта изменяется лишь незначительно. Рекомендуемая доза в качестве противоинфекционного средства составляет 100 мг два раза в день в первый день, а затем 100 мг один раз в день в течение 21 дня.
Метронидазол
Метронидазол не является препаратом выбора для лечения инфекций A. actinomycetemcomitans . Однако он эффективен против них при использовании в сочетании с другими антибиотиками.[11] Он также эффективен против анаэробов, таких как P. gingivalis и Prevotella intermedia . [6] Исследования показали, что в сочетании с амоксициллином или амоксициллин-клавуланатом калия метронидазол может быть полезен при лечении пациентов с агрессивный пародонтит.
Амоксициллин
Было обнаружено, что амоксициллин полезен при лечении пациентов с агрессивным пародонтитом как в локальной, так и в генерализованной формах [12]. Рекомендуемая дозировка — 500 мг 3 раза в день в течение 8 дней.[6]
Амоксициллин – клавуланат калия
Комбинация амоксициллина и клавуланата калия делает антибиотик устойчивым к ферментам пенициллиназы, продуцируемым некоторыми бактериями. Было обнаружено, что он полезен при лечении локальной формы агрессивного пародонтита [11], а также для остановки потери альвеолярной кости.
Ципрофлоксацин
Ципрофлоксацин активен в отношении грамотрицательных палочек, включая все факультативные и некоторые анаэробные предполагаемые патогены пародонта.Поскольку он демонстрирует минимальный эффект на Streptococcus видов, которые связаны со здоровьем пародонта, его введение может способствовать формированию микрофлоры, связанной со здоровьем пародонта. В настоящее время ципрофлоксацин является единственным антибиотиком в пародонтологической терапии, к которому чувствительны все штаммы A. actinomycetemcomitans. Он также использовался в сочетании с метронидазолом. [13]
Макролиды
Азитромицин эффективен против анаэробов и грамотрицательных бактерий.Концентрация азитромицина в образцах тканей из поражений пародонта значительно выше, чем у нормальной десны. [14] Также было высказано предположение, что это лекарство проникает в фибробласты и фагоциты, предполагая, что он активно транспортируется фагоцитами к участкам воспаления, а затем высвобождается непосредственно в участки воспаления, когда фагоциты разрываются во время фагоцитоза. [15]
Последние данные свидетельствуют о том, что азитромицин может быть эффективной дополнительной терапией для повышения уровня привязанности у пациентов с агрессивным пародонтитом.Лечебная дозировка составляет разовая доза 250 мг / сут в течение 5 дней после начальной ударной дозы 500 мг.
Серийная и комбинированная терапия
Инфекции пародонта содержат большое количество бактерий; следовательно, ни один антибиотик не может быть эффективным против всех предполагаемых патогенов. [16] Эта «смешанная инфекция» может включать множество аэробных, микроаэрофильных и анаэробных бактерий, как грамотрицательных, так и грамположительных. Этот сценарий делает обязательным использование более одного антибиотика либо последовательно, либо в комбинации.[11] Комбинация метронидазол-амоксициллин и метронидазол-амоксициллин-клавуланат калия вызвала отличное уничтожение многих микроорганизмов при локализованном агрессивном пародонтите, который безуспешно лечился тетрациклином и механической обработкой раны [11]. Комбинация метронидазол-ципрофлоксацин эффективна против A. actinomycetemcomitans ; метронидазол нацелен на облигатные анаэробы, а ципрофлоксацин — на факультативные анаэробы. Это очень мощная комбинация против смешанных инфекций.Эта комбинация обеспечивает терапевтический эффект за счет уменьшения или устранения патогенных микроорганизмов и предлагает профилактический эффект, вызывая преимущественно стрептококковую микрофлору. [13]
Антибиотики, обладающие бактериостатическим действием (например, тетрациклин), обычно требуют наличия быстро делящихся микроорганизмов, чтобы быть эффективными. Они не работают должным образом, если одновременно вводится бактерицидный антибиотик (например, амоксициллин). Когда требуются оба этих препарата, их лучше назначать последовательно, а не в комбинации.
Современные подходы
Местная доставка
Использование метода местной доставки для введения антибиотика предлагает новый подход к лечению «локализованных» инфекций пародонта. Основное преимущество заключается в том, что меньшие дозы местных агентов могут быть доставлены внутрь кармана, что позволяет избежать побочных эффектов системных антибактериальных агентов, одновременно увеличивая воздействие на целевые микроорганизмы до более высоких концентраций и, следовательно, более терапевтических уровней лекарства.[17]
Полная дезинфекция полости рта
Другой подход к антимикробной терапии в борьбе с инфекцией, связанной с пародонтитом, — это концепция полной дезинфекции полости рта. Процедура состоит из полной хирургической обработки раны, которая проводится за два приема в течение 24 часов. Помимо удаления зубного камня и выравнивания корня, язык чистят гелем хлоргексидина (1%) в течение 1 мин, полоскание рта раствором хлоргексидина (0,2%) в течение 2 мин и орошение пародонтальных карманов раствором хлоргексидина (1%). .Было отмечено значительное уменьшение глубины кармана и увеличение клинического прикрепления у пациентов с агрессивным пародонтитом в течение 8 месяцев после лечения, а также значительное уменьшение количества патогенов пародонта в течение 8 месяцев после лечения [17].
Модуляция хозяина
Новым подходом к лечению агрессивного пародонтита является введение агентов, которые модулируют реакцию хозяина. Использование субантимикробной дозы доксициклина (SDD) [18] может помочь предотвратить разрушение прикрепления пародонта, контролируя активацию матриксных металлопротеиназ, особенно коллагеназы, как из инфильтрирующих клеток, так и из резидентных клеток пародонта, в первую очередь нейтрофилов.SDD, как дополнение к повторной механической санации раны, привело к клиническому улучшению у пациентов с генерализованным агрессивным пародонтитом. Другие агенты, такие как CMT, флубипрофен, индометацин и напроксен, могут снижать выработку медиатора воспаления. Ожидаются дальнейшие исследования использования таких агентов.
План лечения
Лечение агрессивного пародонтита должно начинаться с удаления зубного камня и выравнивания корня в сочетании с системными антибиотиками. Рекомендуется [19], чтобы (i) начало антибиотикотерапии проводилось за 24 часа до начала удаления зубного камня и выравнивания корня и (ii) выравнивание корня выполнялось в течение короткого периода времени, в течение которого назначается антибиотик.
Период переоценки 4–6 недель, по-видимому, действителен для пациента с агрессивным пародонтитом. Если, однако, нет значительного ответа на начальную терапию, врач может выбрать повторное удаление десневого зубного камня с другой схемой приема антибиотиков. Если реакция на начальную терапию способствует переходу к хирургической фазе, следует назначить системный антибиотик и дать пациенту указание начать прием антибиотика примерно за 1 час до операции [20]. Полоскания с хлоргексидином должны быть прописаны и продолжены в течение нескольких недель, чтобы помочь заживлению и увеличить контроль над зубным налётом.
Профилактика пародонта
В конечном счете, успех клинициста в лечении пациентов с агрессивным пародонтитом в основном зависит от программы обслуживания. Рекомендуется ежемесячная поддерживающая терапия в течение первых 6 месяцев после завершения активного лечения, а затем два раза в месяц поддерживающая терапия в течение еще шести месяцев. Если состояние пациента стабильно в течение этого первого года, интервалы обслуживания могут быть увеличены до 3 месяцев. Поддесневое удаление зубного камня в сочетании с местной доставкой антибиотиков является хорошим способом лечения отдельных участков рецидива заболевания, в то время как удаление зубного камня на всю полость рта и системное лечение антибиотиками или терапией модуляции хозяина можно использовать для лечения генерализованного рецидива.[19]
Заключение
Агрессивный пародонтит представляет собой проблему для клинициста, поскольку он встречается нечасто, а предсказуемость успеха лечения варьируется от пациента к пациенту. Эти необычные состояния часто плохо поддаются традиционной терапии из-за сложной природы заболевания. Лучшим лечением для этих пациентов, по-видимому, является сочетание обычного лечения с антимикробной терапией (системное и / или местное введение) и тщательного последующего наблюдения.Модуляция дополнительного хозяина, хотя и только появляющаяся, может оказаться многообещающей при лечении пациентов с агрессивным пародонтитом.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
Список литературы
1. Hart Tc. Генетические факторы риска возникновения пародонтита. J Periodontol. 1996; 67: 355. [PubMed] [Google Scholar] 2. Тонетти М.С., Момбелли А. Пародонтит с ранним началом. Летопись Периодонтола.1999; 4: 39. [PubMed] [Google Scholar] 3. Армитаж ГК, Куллинан депутат. Сравнение клинических особенностей хронического и агрессивного пародонтита. Пародонтология. 2000, 2010; 53: 12. [PubMed] [Google Scholar] 4. Кристерсон Л.А., Викешо У.М., Альбини Б., Замбон Дж.Дж., Дженко Р.Дж. Тканевая локализация Actinobacillus actinomycetemcomitans при пародонтите человека. II. Корреляция между иммунофлуоресценцией и методами культивирования. J Periodontol. 1987; 58: 540. [PubMed] [Google Scholar] 5. Haffajee AD, Socransky SS, Gunsolley JC.Системная противоинфекционная пародонтальная терапия. Систематический обзор. Летопись Периодонтола. 2003; 8: 115. [PubMed] [Google Scholar] 6. Йоргенсен М.Г., Слотс Дж. Практическая антимикробная пародонтальная терапия. Компендируйте Contin Educ Dent. 2000; 21: 111. [PubMed] [Google Scholar] 7. Гибсон В. Антибиотики и заболевания пародонта: выборочный обзор литературы. J Am Dent Assoc. 1982; 104: 213. [PubMed] [Google Scholar] 8. Вайнштейн Л. Противомикробные средства: тетрациклины и хлорамфеникол. В: Гудман Л.С., Гилман А., редакторы.Фармакологические основы терапии. 5 изд. Нью-Йорк: Макмиллан; 1975. [Google Scholar] 9. Гордон Дж. М., Уокер CB, Мерфи Дж. Концентрация тетрациклина в десневой жидкости человека после однократного приема. J Clin Periodontol. 1981; 8: 117. [PubMed] [Google Scholar] 10. Слоты J, Рамс TE. Антибиотики и пародонтологическая терапия: достоинства и недостатки. J Clin Periodontol. 1990; 17: 479. [PubMed] [Google Scholar] 11. Рамс Т.Е., Слотс Дж. Антибиотики в пародонтологической терапии: обновление. Компендируйте Contin Educ Dent.1992; 13: 1130. [PubMed] [Google Scholar] 12. Вайнштейн Л. Противомикробные средства: пенициллины и цефалоспорины. В: Гудман Л.С., Гилман А., редакторы. Фармакологические основы терапии. 5 изд. Нью-Йорк: Макмиллан; 1975. [Google Scholar] 13. Рамс Т.Е., Фейк Д., Слотс Дж. Лечение рецидивирующего пародонтита у взрослых ципрофлоксацином / метронидазолом. Абстрактный. J Dent Res. 1992; 71: 319. [Google Scholar] 14. Малиция Т., Техада М.Р., Геларди Э., Сенези С., Габриэле М., Джука М.Р. и др. Распределение азитромицина в тканях пародонта.J Periodontol. 1997; 68: 1206. [PubMed] [Google Scholar] 15. Hoepelman IM, Schneider MME. Азитромицин: первый азалид тканевого селективного действия. Int J Antimicrob Agents. 1995; 5: 145. [PubMed] [Google Scholar] 16. Уокер CB, Гордон JM, Магнуссон I, Кларк WB. Роль антибиотиков в лечении рефрактерного пародонтита. J Periodontol. 1993; 64: 772. [PubMed] [Google Scholar] 17. Мориера Р.М., Ферес-Филхо Э.Дж. Сравнение между очисткой полости рта и полировкой корня и базовой терапией агрессивного пародонтита по квадрантам: клинические результаты за 6 месяцев.J Periodontol. 2007; 78: 1683. [PubMed] [Google Scholar] 18. Катон Дж., Блейден Т., Чиансио С. Лечение субантимикробной дозой Доксициклин улучшает эффективность масштабирования и выравнивания корней у пациентов с пародонтитом взрослых. J Periodontol. 2000; 71: 521. [PubMed] [Google Scholar] 19. Deas DE, Mealey BL. Ответ на лечение хронического и агрессивного пародонтита. Пародонтология. 2000, 2010; 53: 154. [PubMed] [Google Scholar] 20. Мили Б.Л., Клоккевольд ПР, Коргель Дж. Учебник клинической пародонтологии Каррансы.Эд 9. Vol. 38. Elsevier Science; 2003. Пародонтологическое лечение пациентов с ограниченными возможностями; п. 527. [Google Scholar]Системная антибактериальная терапия в пародонтологии
Dent Res J (Исфахан). 2012 сентябрь-октябрь; 9 (5): 505–515.
Anoop Kapoor
1 Отделение пародонтологии оральной имплантологии, Стоматологический колледж и больница Бходжи, Бадди, Химачал-Прадеш, Индия
Ранжан Малхотра
2 Отделение пародонтологии и стоматологической имплантологии, Национальный колледж и стоматологическая больница Гулабгар. , Дерабасси, р-н.SAS Nagar, Мохали (Пенджаб), Индия
Vishakha Grover
2 Отделение пародонтологии и оральной имплантологии, Национальный стоматологический колледж и больница, Гулабгарх, Дерабасси, р-н. SAS Nagar, Мохали (Пенджаб), Индия
Deepak Grover
2 Отделение пародонтологии и оральной имплантологии, Национальный стоматологический колледж и больница, Гулабгарх, Дерабасси, р-н. SAS Nagar, Мохали (Пенджаб), Индия
1 Отделение пародонтологии оральной имплантологии, Стоматологический колледж и больница Бходжи, Бадди, Химачал-Прадеш, Индия
2 Отделение пародонтологии и оральной имплантологии, Национальный стоматологический колледж и больница, Гулабгарх, Дерабасси, р-н.SAS Nagar, Мохали (Пенджаб), Индия
Адрес для корреспонденции: Доктор Ануп Капур, Отделение пародонтологии и оральной имплантологии, Стоматологический колледж и больница Бходжи, Бадди, Химачал-Прадеш, Индия. Электронная почта: moc.ffider@roopak_poonardПоступила в редакцию января 2012 г .; Принята в печать 2012 г., май.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Системные антибиотики в сочетании со скейлингом и выравниванием корня (SRP) могут предложить дополнительное преимущество по сравнению с одним SRP при лечении периодонтита с точки зрения потери клинического прикрепления (CAL) и изменения глубины кармана, а также снижения риска дополнительных Потеря CAL. Однако антибиотики не являются безобидными лекарствами. Их использование должно быть оправдано на основе четко установленной потребности и не должно заменять адекватное местное лечение.Цель этого обзора — обсудить обоснование, правильный выбор, дозировку и продолжительность антибактериальной терапии, чтобы оптимизировать эффективность лекарственной терапии.
Ключевые слова: Пародонтит, пародонтит, шелушение и выравнивание корней, системная антибактериальная терапия
ВВЕДЕНИЕ
В течение последних двух десятилетий стоматологи и микробиологи использовали пародонтологическую антибактериальную терапию как мощное дополнение к традиционной механической обработке раны для терапевтического лечения заболевания пародонта [1,2], свидетельствующие о бактериальной специфичности пародонтита, накапливаются и усиливаются.Антибиотики — это природные или синтетические органические вещества, которые в низких концентрациях подавляют или убивают селективные микроорганизмы [1].
Концепция пародонтологической терапии антибиотиками сосредоточена на патогенной микробиоте, пациенте и лекарстве. [3] Существует множество антибиотиков, которые можно использовать для лечения пародонтальных инфекций, но часто неясно, какой антибиотик принесет наибольшую пользу пациенту с конкретной пародонтальной инфекцией с минимальными побочными эффектами.
Обсуждение ниже касается обоснования, правильного выбора, дозировки и продолжительности антибактериальной терапии, чтобы оптимизировать эффективность лекарственной терапии.
ОБОСНОВАНИЕ АНТИБИОТИЧЕСКОЙ ТЕРАПИИ
Механическое и хирургическое лечение в сочетании с надлежащими мерами гигиены полости рта может остановить или предотвратить дальнейшую потерю прикрепления пародонта у большинства людей за счет уменьшения общей наддесневой бактериальной массы. [4] Однако, несмотря на тщательное стоматологическое лечение, у некоторых людей по-прежнему наблюдается разрушение пародонта, что может быть связано со способностью основных пародонтальных патогенов, таких как Porphyromonasgingivalis, Aggregatibacteractinomycetemcomitans, Fusobacterium-nucleatum, Treponemadenticola , бактероидов, проникать в ткани пародонта или оставаться в тканях пародонта или оседать в них. другие зубные структуры вне досягаемости пародонтальных инструментов или из-за слабых защитных механизмов организма.[4] Кроме того, предполагаемые патогены пародонта («красный комплекс») имеют тенденцию находиться в части биопленки, прикрепленной к эпителиальной поверхности пародонтального кармана, и пациент не может добраться до этого места во время гигиены полости рта. [5]
Основными кандидатами на системную противомикробную терапию являются пациенты, у которых наблюдается потеря привязанности после кажущейся адекватной традиционной терапии, или пациенты с агрессивными формами пародонтита или связанные с предрасполагающими заболеваниями или рефрактерным пародонтитом.[6] Пациентам с острыми или тяжелыми инфекциями пародонта (пародонтальный абсцесс, острый некротический гингивит / пародонтит) также может помочь терапия антибиотиками. [3]
Системная пародонтальная антибиотикотерапия направлена на усиление механического лечения пародонта и поддержку системы защиты хозяина в преодолении инфекции путем уничтожения поддесневых патогенов, которые остаются после традиционной механической пародонтальной терапии. [4] Восприимчивость бактерий к антибиотикам может быть ключом к эффективности системных антибиотиков при лечении заболеваний пародонта.Некоторые химиотерапевтические агенты также могут уменьшать разрушение коллагена и костей благодаря своей способности ингибировать фермент коллагеназу. Пациенты с гингивитом или стабильным пародонтитом взрослых обычно хорошо реагируют на механическую пародонтологическую терапию и не получают дополнительной пользы от терапии антибиотиками.
РУКОВОДСТВО ПО ПРИМЕНЕНИЮ АНТИБИОТИКОВ ПРИ ПЕРИОДОНТАЛЬНОМ ЗАБОЛЕВАНИИ
-
Клинический диагноз и ситуация диктуют необходимость возможной антибактериальной терапии в качестве дополнения к борьбе с активным заболеванием пародонта, поскольку диагноз пациента может измениться со временем.[5]
-
Продолжающаяся активность заболевания является показанием к вмешательству на пародонте и возможному микробиологическому анализу путем отбора образцов зубного налета. Также случаи рефрактерного или агрессивного пародонтита могут указывать на необходимость антимикробной терапии.
-
При использовании для лечения заболеваний пародонта антибиотики выбираются на основе медицинского и стоматологического статуса пациента, принимаемых лекарств и результатов микробного анализа, если он проводится.
-
Образцы микробов можно получить из отдельных карманов с недавней активностью заболевания или из объединенных поддесневых участков.Объединенный поддесневой образец может дать хорошее представление о диапазоне пародонтальных патогенов, на которые будет нацелена антибактериальная терапия. [3]
-
Взятие образцов зубного налета может быть выполнено при первичном осмотре, выравнивании корня, повторной оценке или на приеме поддерживающей пародонтальной терапии.
-
Было также показано, что антибиотики имеют ценность в снижении потребности в хирургии пародонта у пациентов с хроническим пародонтитом.
-
Системная антибиотикотерапия должна быть дополнением к комплексному плану лечения пародонта.Для эффективности против бактерий, расположенных в биопленках, может потребоваться сила антибиотика, в 500 раз превышающая системную терапевтическую дозу. Следовательно, важно физически разрушить эту биопленку, чтобы антибиотики могли проникнуть в пародонтальные патогены [5].
-
Slots и др. . [7] описали серию шагов с использованием противоинфекционных агентов для улучшения регенеративного заживления. Они рекомендуют начинать прием антибиотиков за 1-2 дня до операции и продолжать в течение как минимум 8 дней, однако ценность этого режима не подтверждена документально.
-
Haffajee и др. . [8] пришли к выводу, что данные подтверждают аналогичные эффекты для большинства антибиотиков. Риски и преимущества применения антибиотиков в качестве дополнения к пародонтальной терапии необходимо обсудить с пациентом перед применением антибиотиков.
ВЫБОР АНТИБИОТИКА
После установления потребности в применении антибиотика пациенту часто бывает трудно решить, какой из множества доступных антибиотиков выбрать. Факторами, определяющими выбор антибиотиков, являются: [9]
-
Возраст пациента: это может повлиять на фармакокинетику многих антибиотиков e.грамм. тетрациклины накапливаются в развивающихся зубах и костях.
-
Функция почек и печени: осторожное использование и изменение дозы антибиотика становится необходимым, когда орган его удаления поврежден.
-
Местные факторы: Условия, преобладающие в очаге инфекции, сильно влияют на действие антибиотиков, например, наличие гноя и выделений, некротического материала и инородного тела, низкий pH.
-
Лекарственная аллергия: необходимо получить анамнез предыдущего воздействия антибиотика и любых аллергических реакций.
-
Нарушение защиты хозяина: у человека с нормальной защитой хозяина бактериостатический антибиотик может излечить, тогда как интенсивная терапия бактерицидными препаратами обязательна для людей с нарушенной защитой хозяина.
-
Беременность: следует избегать приема всех антибиотиков во время беременности из-за риска для развивающегося плода.
-
Соображения, связанные с организмом: Хотя терапия в большинстве случаев является эмпирической, необходимо учитывать вероятность наиболее вероятного патогена.
-
Лекарственные факторы: сюда входят специфические свойства антибиотиков, такие как спектр активности (узкий / широкий), тип активности (бактерицидный / бактеристатический), чувствительность организма (значения минимальной ингибирующей концентрации), относительная токсичность, фармакокинетический профиль, способ применения, данные о клинической эффективности и стоимости препарата.
Микробный состав поддесневого налета значительно варьируется от пациента к пациенту.
Описание реакции окрашивания по Граму и анаэробных требований инфекционной микробиоты пародонта стало первым руководством по выбору антимикробной терапии.
Определение типа пародонтальной инфекции (экзогенная / эндогенная) может иметь важное значение при выборе правильной стратегии антимикробной терапии в пародонтологии. [4]
При выборе системного антибиотика для пародонтологической терапии следует особо учитывать два критических фактора: [10] Концентрация десневой жидкости и минимальная ингибирующая концентрация (МИК).
-
Концентрация десневой жидкости (C GCF ) предоставляет информацию о пиковых уровнях, достигаемых системной доставкой в первичную экологическую нишу для пародонтальных патогенов, пародонтальный карман.
-
Минимальная ингибирующая концентрация 90% (MIC 90 ) — это определение in vitro концентрации, которое будет ингибировать рост 90% бактериальных штаммов тестируемых видов. Антимикробная активность может быть определена как соотношение между C GCF и MIC 90
100 (C GCF / MIC 90 ) = антимикробная активность, выраженная в процентах для каждого антибиотика и каждого организма.
Антибиотики, которые могут подавлять рост организма на 90%, появляются на линии 100%. Наиболее эффективными антибиотиками для лечения определенного патогена пародонта являются те, которые равны или превышают 100% -ное значение.
Заболевания пародонта, при которых можно использовать антибиотики:
-
Хронический пародонтит: антибиотикотерапия обычно рекомендуется пациентам с прогрессирующим разрушением пародонта даже после традиционного механического лечения, пациентам, не отвечающим на пародонтологическую терапию (рефрактерный пародонтит), и пациентам с рецидивирующим заболеванием .[1,4] При обзоре соответствующей литературы [2–5] было предложено использование следующих антибиотиков:
Тетрациклин, доксициклин, метронидазол, клиндамицин, амоксициллин + клавулиновая кислота (аугментин), азитромицин, метронидазол + амоксициллин, спирамицин.
-
Агрессивный пародонтит: Локализованный агрессивный пародонтит (LAP), в основном связанный с Aggregatibacteractinomycetemcomitan , можно контролировать или искоренять с помощью системной комбинированной терапии метронидазолом и амоксициллином.[1] При локализованном и генерализованном агрессивном пародонтите рекомендуются следующие антибиотики: [2,3,5]
Тетрациклин, доксициклин, миноциклин, метронидазол, амоксициллин + клавулиновая кислота (аугментин), метронидазол + амоксициллин.
-
Некротические заболевания пародонта: Пациенты с умеренным или тяжелым НУГ или некротическим язвенным периодонтитом (НЯП), местной лимфаденопатией и системным поражением нуждаются в терапии антибиотиками. Рекомендуемые антибиотики — амоксициллин, метронидазол и комбинация амоксициллин + метронидазол.[1,3,5]
-
Пародонтальный абсцесс: Антибактериальная терапия показана при пародонтальных абсцессах с системными проявлениями (лихорадка, недомогание, лимфаденопатия). Антибиотики для лечения абсцессов следует назначать в сочетании с хирургическим разрезом и дренированием [3].
Схемы приема антибиотиков для взрослых пациентов с острыми пародонтальными абсцессами [3]
-
Амоксициллин: ударная доза 1,0 г с последующей поддерживающей дозой 500 мг / т.я бы. в течение 3 дней с последующим обследованием пациента, чтобы определить, требуется ли дальнейшая антибактериальная терапия или корректировка дозировки.
-
При аллергии на ß-лактамные препараты: Азитромицин: ударная доза 1,0 г в 1-й день, затем 500 мг / раз в день. на 2-й и 3-й дни; или Клиндамицин: ударная доза 600 мг в день 1, затем 300 мг / q.i.d. в течение 3 дней.
ПРИНЦИПЫ ДОЗИРОВКИ АНТИБИОТИКОВ [11]
-
Применяйте высокие дозы в течение короткого времени: Успех антибиотика зависит от поддержания концентраций в крови и тканях выше минимальной ингибирующей концентрации для целевого организма.Высокие концентрации более важны для аминогликозидов, метронидазола и хинолонов (антибиотики, зависящие от концентрации), тогда как длительное воздействие антимикробного агента на организм более критично для бета-лактамов (антибиотиков, зависящих от времени).
-
Используйте пероральную нагрузочную дозу антибиотика: без ударной дозы для достижения максимального терапевтического уровня в крови и тканях при пероральном введении требуется 6-12 часов.
-
Достигните уровня антибиотика в крови в 2-8 раз превышающего минимальную ингибирующую концентрацию: такие уровни в крови необходимы для компенсации тканевых барьеров, препятствующих проникновению антибиотика в место инфекции.
-
Используйте частые интервалы дозирования: это важно для старых бета-лактамных антибиотиков, таких как пенициллин V и цефалоспорины первого поколения (цефалексин, цефрадин), чтобы поддерживать относительно постоянный уровень в крови.
-
Определите продолжительность терапии по ремиссии заболевания: прием антибиотика прекращается, когда защитные силы пациента-хозяина получили контроль над инфекцией и инфекция, с достаточной степенью уверенности, исчезнет или разрешится.Системно применяемые бактериостатические антибиотики обычно требуют более длительных периодов введения, чтобы быть эффективными по сравнению с их бактерицидными аналогами.
ОБЫЧНО ИСПОЛЬЗУЕМЫЕ АНТИБИОТИКИ В ПЕРИОДОНТИИ
Восемь основных групп антибиотиков были тщательно изучены для лечения заболеваний пародонта; тетрациклин, миноциклин, доксициклин, эритромицин, клиндамицин, ампициллин, амоксициллин и метронидазол. [10] Ниже приводится краткий обзор этих групп лекарств:
Тетрациклин
Фармакология
-
Произведено естественным путем из определенных видов Streptomyces или получено полусинтетическим путем.
-
Бактериостатические препараты, эффективные против быстро размножающихся бактерий и грамположительных бактерий, чем грамотрицательные бактерии.
-
Концентрация в десневой щели в 2-10 раз выше, чем в сыворотке [5].
-
Обладают уникальными неантибактериальными характеристиками — ингибированием коллагеназы [12], ингибированием хемотаксиса нейтрофилов, противовоспалительным действием [10], ингибированием прикрепления микробов [13] и кондиционированием поверхности корня [14].
Механизм действия
Действует путем ингибирования синтеза белка путем связывания с 30 S-рибосомами в восприимчивом организме.[9]
Клиническое применение
-
Вспомогательные средства при лечении локализованного агрессивного пародонтита (LAP).
-
Остановить потерю костной массы и подавить уровни A. actinomycetemcomitans в сочетании с масштабированием и строганием корня.
Тетрациклин, миноциклин и доксициклин являются полусинтетическими членами группы тетрациклинов, которые использовались в пародонтологической терапии.
Тетрациклин
Режим дозирования — 250 мг четыре раза в день, недорогой, меньшее соблюдение.
Миноциклин
-
Эффективен против широкого спектра микроорганизмов.
-
Подавляет спирохеты и подвижные стержни так же эффективно, как шелушение и выравнивание корня, с очевидным подавлением до 3 месяцев после терапии.
-
Можно давать два раза в день, что способствует соблюдению требований.
-
Хотя он связан с меньшей фототоксичностью и почечной токсичностью, чем тетрациклин, может вызывать обратимое головокружение.
-
Повышает уровень десневой жидкости в 5 раз выше уровня в крови.[15]
-
За исключением действия миноциклина на актиномицетов, ни один из тетрациклинов существенно не ингибирует рост оральных грамположительных организмов путем системной доставки.
Доксициклин
-
Тот же спектр активности, что и миноциклин.
-
Соблюдение режима приветствуется, поскольку его следует принимать один раз в день, абсорбция из желудочно-кишечного тракта лишь незначительно изменяется из-за кальция, ионов металлов или антацидов. [5]
-
Рекомендуемая доза составляет 100 мг 2 раза в день в первый день, затем 100 мг о.d. Чтобы уменьшить расстройство желудочно-кишечного тракта, можно принимать 50 мг два раза в день.
Примечание: сравнение биологических эффектов, пиковых концентраций после системного введения и обычной дозировки тетрациклинов для взрослых было проиллюстрировано на.
Таблица 1
Сравнение биологических эффектов, пиковых концентраций после системного введения и обычных дозировок тетрациклинов для взрослых (все значения в мкг / мл) [10]
Метронидазол
Фармакология
-
Синтетическое соединение нитроимидазола с бактерицидным действием в первую очередь воздействуют на облигатные грамположительные и грамотрицательные анаэробы. Campylobacterrectus — единственный факультативный анаэроб и вероятный патоген пародонта, чувствительный к низким концентрациям метронидазола.
-
Спектр высокоактивного лечения инфекций Fusobacterium и Selenomonas , лучший кандидат для инфекций Peptostreptococcus , приемлемый кандидат для инфекций P. gingivalis, Pintermedia и C. rectus , плохой выбор для A.actinomycetemcomitans и E. разъедает инфекцию , существенно не подавляет рост полезных видов [10].
-
Концентрации, измеренные в десневой жидкости, обычно немного ниже, чем в плазме.
Механизм действия
Метронидазол действует путем ингибирования синтеза ДНК.
Клиническое применение
-
Для лечения гингивита, острого язвенно-некротического гингивита, хронического пародонтита и агрессивного пародонтита.
-
В качестве монотерапии метронидазол менее эффективен, его следует использовать в сочетании с выравниванием корня, хирургическим вмешательством или с другими антибиотиками. Чаще всего назначают по 250 мг три раза в день в течение 7 дней.
-
В исследовании Haffajee et al. . [16] участки с начальной глубиной кармана ≥6 мм показали значительно большее уменьшение глубины кармана и большее усиление прикрепления у субъектов, получавших метронидазол или азитромицин, чем у субъектов, получавших доксициклин.
Пенициллин
Фармакология
-
Натуральные и полусинтетические производные бульонных культур плесени пеницилла.
-
Узкий спектр действия и бактерицидный характер. Основная активность в грамположительном спектре. Только пенициллины расширенного спектра, такие как ампициллин и амоксициллин, обладают значительной антибактериальной антимикробной активностью в отношении грамотрицательных видов [10].
Механизм действия
Вмешивается в синтез клеточной стенки бактерий, ингибирует транспептидазы, так что перекрестное связывание не происходит.
Клиническое применение
-
В ведении пациентов с агрессивным пародонтитом как в локальной, так и в генерализованной формах. Рекомендуемая дозировка — 500 мг 3 раза в день в течение 8 дней.
-
Проявляет высокую антимикробную активность на уровнях, которые встречаются в GCF для всех пародонтальных патогенов, кроме E. corrodens, S. sputigena и Peptostreptococcus, подавляет рост грамположительных факультативных анаэробов. [10]
Исследования показывают, что более 60% взрослых пациентов с пародонтитом, взятых в пробах, содержат зубной налет, который проявляет активность β-лактамазы.По этой причине введение пенициллинов, чувствительных к β-лактамазе, включая только амоксициллин, обычно не рекомендуется и в некоторых случаях может ускорить разрушение пародонта.
Амоксициллин-клавуланат (Аугментин) — общепринятой стратегией является введение амоксициллина с ингибитором бета-лактамазы, таким как клавулановая кислота. Штаммы, продуцирующие бета-лактамазу, обычно чувствительны к этому препарату. Аугментин может быть полезен при лечении пациентов с рефрактерным или локализованным агрессивным пародонтитом.
При управляемой регенерации тканей системная терапия амоксициллин-клавулановой кислотой использовалась для подавления патогенов пародонта и увеличения клинического прикрепления [3].
Цефалоспорины
Фармакология
-
Используется для инфекций, которые в противном случае можно было бы лечить с помощью пенициллина.
-
Устойчив к ряду β-лактамаз, обычно активен против пенициллина.
Способ действия
Механизм действия такой же, как у пенициллинов, т.е.е. ингибирование синтеза клеточной стенки бактерий. Однако они связываются с белками, отличными от тех, которые связывают пенициллины. [15]
Клиническое применение
Цефалексин представляет собой цефалоспорин, доступный для перорального приема.
-
Достигает высоких концентраций в GCF.
-
Эффективно подавляет рост грамотрицательных облигатных анаэробов, не подавляет грамотрицательные факультативные анаэробы. [10]
-
Новые цефалоспорины с повышенной грамотрицательной эффективностью могут быть полезны при лечении заболеваний пародонта.
Клиндамицин
Фармакология
Эффективен против анаэробных бактерий и у пациентов с аллергией на пенициллин.
Механизм действия
Подавление синтеза белка путем связывания с 50 S рибосомой.
Клиническое применение
-
Клиндамицин обладает более высоким антимикробным действием, чем другие антибиотики.
-
Gordon et al . [17] наблюдали среднее увеличение клинического прикрепления на 1.5 мм и снижение активности заболевания у пациентов через 24 месяца после дополнительной терапии клиндамицином.
-
Walker и др. . [18] показали, что клиндамицин способствует стабилизации рефрактерных пациентов. Дозировка составляла 150 мг 4 раза в день в течение 10 дней.
-
Jorgensen и Slots [19] рекомендовали режим 300 мг 2 раза в день в течение 8 дней.
Ципрофлоксацин
Фармакология
-
Фторированный 4-хинолоновый антибиотик, доступный для перорального применения.
-
Сильный ингибитор грамотрицательных бактерий (все факультативные и некоторые анаэробные предполагаемые пародонтальные патогены), включая Pseudomonas aeruginosa , со значениями MIC 90 в диапазоне от 0,2 до 2 мкг / мл. [10]
Механизм действия
Ингибирование репликации и транскрипции бактериальной ДНК путем ингибирования фермента ДНК-гиразы, фермента, уникального для прокариотических клеток. [9]
Клиническое применение
-
Облегчает формирование микрофлоры, связанной со здоровьем пародонта, минимальное воздействие на виды стрептококков, которые связаны со здоровьем пародонта.
-
В настоящее время ципрофлоксацин является единственным антибиотиком в пародонтальной терапии, к которому чувствительны все штаммы A. actinomycetemcomitans .
-
Также используется в сочетании с нитроимидазолами (метронидазол и тинидазол).
Макролиды
Фармакология
-
Содержат полилактоновое кольцо, к которому присоединены один или несколько дезоксисахаров.
-
Может быть бактериостатическим или бактерицидным, в зависимости от концентрации препарата и природы микроорганизма.
-
Макролидные антибиотики, используемые для лечения пародонта, включают эритромицин, спирамицин и азитромицин.
-
Принципиальным ограничением эритромицина является его плохая абсорбция тканями. Препараты для системного введения доступны в виде пролекарств (эстолат эритромицина, стеарат эритромицина или этилсукцинат эритромицина) для облегчения абсорбции. Пролекарство имеет слабую антибактериальную активность, пока не будет гидролизовано эстеразами сыворотки. [10]
Механизм действия
Подавляет синтез белка путем связывания с 50 S рибосомными субъединицами чувствительных микроорганизмов и препятствует трансляции.
Эритромицин
Клиническое применение
-
Чрезвычайно безопасный препарат, который часто рекомендуется как альтернатива пенициллину для пациентов с аллергией.
-
Уровни десневой жидкости предполагают, что только небольшая часть достигает пародонтального кармана оральным путем.
Спирамицин
В высоких концентрациях выделяется со слюной. [5] Результаты различных клинических испытаний показали хорошую эффективность спирамицина при лечении пародонтита, а метаанализ этих исследований выявил высокий уровень доказательств, подтверждающих его эффективность.[2,4,8] Было показано, что он снижает объем жидкости десневой щели, глубину кармана и уровень поддесневых спирохет. [1] Herrera и др. . [6] в амета-анализе, оценивающем спирамицин, амоксициллин плюс метронидазол и метронидазол, показали статистически значимый дополнительный эффект спирамицина по сравнению с другими антибиотиками в отношении уменьшения глубины кармана при зондировании для участков с начальной глубиной зондирования более 6 мм.
Клиническое применение
Эффективен против грамположительных организмов, оказывает минимальное влияние на повышение уровня прикрепления.
Азитромицин
Клиническое применение
-
Эффективен против анаэробов и грамотрицательных бактерий.
-
После перорального приема 500 мг 1 раз в день в течение 3 дней значительные уровни азитромицина могут быть обнаружены в большинстве тканей в течение 7-10 дней.
-
Было высказано предположение, что азитромицин проникает в фибробласты и фагоциты в концентрациях, в 100-200 раз превышающих концентрацию во внеклеточном пространстве. Азитромицин активно транспортируется фагоцитами к участкам воспаления, а затем напрямую высвобождается в участки воспаления по мере разрыва фагоцитов во время фагоцитоза.[5]
-
Для терапевтического использования требуется однократная доза 250 мг / день в течение 5 дней после начальной ударной дозы 500 мг.
Аминогликозиды
-
Подавляют синтез белка путем необратимого связывания с конкретным белком или белками 30 S субъединицы рибосомы.
-
Неактивны в анаэробных условиях, поскольку внутриклеточный транспорт серьезно нарушается в отсутствие кислорода. Следовательно, все анаэробные бактерии заметно устойчивы, даже если они содержат рибосомы, чувствительные к этим антибиотикам.[15]
Примечание: побочные эффекты некоторых антибиотиков, используемых при лечении заболеваний пародонта, описаны в.
Таблица 2
Отдельные побочные эффекты антибиотиков, используемых при лечении заболеваний пародонта [4]
Есть пять устрашающих проблем, которые замедляют прогресс антибактериальной терапии: [2]
-
Заболевания пародонта неоднородны;
-
Клинический диагноз ставится на основании клинических признаков, а не молекулярной патологии;
-
Фактический причинный фактор (ы) окончательно не идентифицирован;
-
Отсутствие микробиологического отбора проб.
-
Существует множество различных протоколов применения антибиотиков, но мало хорошо спланированных рандомизированных контролируемых испытаний, в которых проверяется эффективность этих протоколов.
Инфекции пародонта можно рассматривать как смешанные инфекции, в которых задействованы различные аэробные, микроаэрофильные и анаэробные бактерии, как грамотрицательные, так и грамположительные, чувствительные к различным лекарствам. Следовательно, в некоторых клинических ситуациях кажется лучше использовать более одного антибиотика, чтобы покрыть все пародонтальные патогены.
Комбинация антибиотиков может помочь [4]
-
Расширить антимикробный диапазон терапевтического режима за пределы того, что достигается любым отдельным антибиотиком.
-
Для предотвращения или предупреждения возникновения бактериальной устойчивости с помощью агентов с перекрывающимися антимикробными спектрами.
-
Для снижения дозы отдельных антибиотиков за счет использования возможного синергизма между двумя лекарствами против целевых организмов.
Недостатками комбинирования антибиотиков являются: [4]
-
Увеличение побочных реакций
-
Антагонистические лекарственные взаимодействия с неправильно подобранными антибиотиками.
ПОСЛЕДОВАТЕЛЬНЫЕ СИСТЕМНЫЕ АНТИБИОТИКИ
Антибиотики, обладающие бактериостатическим действием (например, тетрациклин), обычно требуют наличия быстро делящихся микроорганизмов. Они не работают должным образом, если одновременно вводится бактерицидный антибиотик (например, амоксициллин или метронидазол). Когда требуются оба типа лекарств, их лучше назначать последовательно, а не в комбинации, чтобы избежать неблагоприятного взаимодействия, но получить пользу от обоих. [5]
В одном из таких исследований шести пациентам с рецидивирующим прогрессирующим периодонтитом давали обычную для взрослых дозу доксициклина в течение 4 дней, а затем амоксициллин с клавуланатом в течение 5 дней.Пятерым подобным пациентам давали только доксициклин в течение 10 дней. Через 25 недель у пациентов, получавших последовательную комбинацию, наблюдалось значительно большее уменьшение глубины кармана, чем у пациентов, получавших только доксициклин. [2]
В другом исследовании все пациенты с рецидивирующим пародонтитом получали регулярные двухмесячные и последовательные дозы доксициклина и метронидазола. В группе комбинированных антибиотиков у 9% наблюдался рецидив периодонтита, тогда как у 42% группы плацебо наблюдались признаки рецидива заболевания.Хотя эти различия кажутся статистически значимыми, через 7 месяцев после приема метронидазола никакой разницы в микробиоте между группами обнаружить не удалось. [2]
КОМБИНИРОВАННАЯ ТЕРАПИЯ
Было показано, что комбинация метронидазола и амоксициллина (МА) является эффективным антибиотиком для борьбы с инфекциями пародонта, ассоциированными с Aggregatibacter actinomycetemcomitans и Porphyromonas gingivalis [20].
Один важный клинический результат исследования Winkel et al .[21] было наблюдение, что пациенты с поддесневым P. gingivalis на исходном уровне, получавшие метронидазол + амоксициллин, показали примерно половину количества карманов размером> 5 мм после терапии по сравнению с P. gingivalis положительными пациентами, получавшими плацебо. Guerreo и др. . [22] использовали сопоставимый протокол лечения пациентов с агрессивным пародонтитом и показали значительно лучшее улучшение всех пародонтальных параметров у пациентов, получавших антибиотики, по сравнению с пациентами, получавшими плацебо, через 6 месяцев после лечения.
Эти исследования показали, что как при хроническом, так и при агрессивном пародонтите антибиотики приводят к лучшему разрешению воспаления пародонта, большей глубине зондирования и уменьшению потери прикрепления.
Метронидазол и клиндамицин, по-видимому, более эффективны в уничтожении анаэробных пародонтопатических бактерий, чем доксициклин или только механическая терапия. [23]
Комбинация метронидазола и ципрофлоксацина эффективна против A. actinomycetemcomitans .Метронидазол нацелен на облигатные анаэробы, а ципрофлоксацин — на факультативные анаэробы. Это мощная комбинация против смешанных инфекций. Исследования этой комбинации препаратов при лечении рефрактерного пародонтита документально подтвердили заметное клиническое улучшение [24].
МЕДИЦИНСКИЕ УСЛОВИЯ, НЕОБХОДИМЫЕ ПРИМЕНЕНИЕ ПРЕДОПЕРАЦИОННЫХ АНТИБИОТИКОВ
Пациенты с неконтролируемым диабетом, трансплантацией органов, трансплантацией костного мозга, протезированием суставов, лейкемией, нейтропенией, тромбоцитопенией подвергаются большему риску развития инфекции после стоматологических процедур из-за снижения иммуносупрессии иммунных клеток.[25,26] Пациенты с хронической почечной недостаточностью также нуждаются в профилактике антибиотиками для предотвращения эндартериита артериовенозной фистулы или шунта. [25] Предотвратить инфекционный эндокардит у пациентов с инфекционным эндокардитом в анамнезе, протезами сердечных клапанов, большим врожденным пороком сердца (тетралогия Фалло, транспозиция магистральных артерий, хирургически сконструированные системные легочные шунты или кондуиты), приобретенная клапанная функция (например, ревматическая болезнь сердца) , гипертрофическая кардиомиопатия, пролапс митрального клапана с клапанной регургитацией, утолщение створок или и то, и другое, рекомендуется профилактика антибиотиками.[25]
Пародонтологические процедуры, рассматриваемые как процедуры высокого риска у этих пациентов, включают зондирование, удаление зубного камня, выравнивание корня, поддесневое введение волокон или полоски антибиотика, интралигаментарные местные инъекции анестетика, профилактическую чистку зубов или имплантатов с ожидаемым кровотечением, пародонтологическую операцию, установка зубных имплантатов. [27] Амоксициллин чаще всего используется для антибиотикопрофилактики. Рекомендуемая доза составляет 2 г для взрослых и 50 мг / кг для детей перорально за час до процедуры.Пациентам, которые не могут принимать пероральные препараты, ампициллин вводят внутримышечно или внутривенно в дозе 2,0 г взрослым и 50 мг / кг детям в течение 30 минут до процедуры. У пациентов с аллергией на пенициллин предпочтительными антибиотиками являются клиндамицин (взрослые, 600 мг; дети, 20 мг / кг перорально за час до процедуры), цефалексин или цефадроксил (взрослые, 2,0 г; дети, 50 мг / кг перорально за час до процедуры). ), Азитромицин или кларитромицин (взрослые, 500 мг; дети, 15 мг / кг перорально за час до процедуры).Пациентам с аллергией на пенициллин, которые не могут принимать пероральные препараты, назначают клиндамицин (взрослые, 600 мг; дети, 15 мг / кг внутривенно за час до процедуры) или цефазолин (взрослые, 1,0 г; дети, 25 мг / кг внутримышечно или внутривенно в течение За 30 минут до процедуры). [27]
КЛИНИЧЕСКИЕ ПРИЧИНЫ НЕДОСТАТОЧНОСТИ АНТИБИОТИКА
Клинические причины неэффективности антибиотиков следующие: [11]
-
Неправильный выбор антибиотика
-
Появление устойчивых к антибиотикам микроорганизмов
-
Слишком низкая концентрация в крови антибиотик
-
Медленный рост микроорганизмов
-
Нарушение защитных сил хозяина
-
Несоблюдение пациентом режима
-
Антагонизм антибиотика
-
Неспособность антибиотика проникнуть в очаг
Ограниченная васкуляризация или снижение кровотока -
Неблагоприятные местные факторы (снижение pH ткани или напряжение кислорода)
-
Неспособность устранить источник инфекции (отсутствие разреза и дренажа)
РЕЗЮМЕ
Установлено это си стволовые антибиотики могут значительно усилить эффект механической пародонтологической терапии в сочетании с мерами, улучшающими гигиену полости рта.Клинические исследования системной антибактериальной терапии у взрослых пациентов с пародонтитом, рефрактерным пародонтитом, агрессивным пародонтитом представлены в . Как было предложено Herrera и др. . [6] и Haffajee и др. . [8], средний «прирост» прикрепления 0,3-0,4 мм может показаться небольшим, но он был основан на изменении во рту, включая участки с неглубокие глубины зондирования, улучшение которых после терапии можно было бы ожидать умеренно. В качестве ориентира, пациенты с пародонтитом, наблюдаемые после лечения и на поддерживающей пародонтальной терапии в течение примерно 12 лет, испытали среднегодовую среднюю потерю прикрепления всего рта, равную 0.От 042 мм (субъекты с нормальной восприимчивостью) до 0,067 мм (субъекты с высокой восприимчивостью). [28] Таким образом, «прирост» уровня привязанности на 0,3 мм был бы эквивалентен обращению вспять 4-7 лет прогрессирования болезни в популяции, получавшей лечение и поддерживающуюся [8].
Таблица 3
Клинические исследования системной антибиотикотерапии у взрослых пациентов с пародонтитом с недавней активностью заболевания до начала терапии антибиотиками [29]
Все антибиотики, используемые в пародонтологической терапии, подавляют рост основных пародонтальных патогенов P.gingivalis, C. rectus и Capnocytophaga . Напротив, ни один из них не особенно эффективен в ингибировании E. corrodens (лучше всего миноциклин и доксициклин). Миноциклин, по-видимому, является наиболее эффективным антибиотиком, который достигает уровней, которые должны быть полностью ингибирующими (активность антибиотика = 600%) для большинства патогенов пародонта, но также может подавлять рост полезных видов [10]. Амоксициллин почти так же эффективен, как миноциклин.Тетрациклин — наиболее часто используемый антибиотик, но, по-видимому, является относительно плохим выбором для лечения инфекций A. actinomycetemcomitans , для которых он использовался наиболее часто. Эритромицин — плохой выбор для лечения любой патогенной инфекции полости рта. Метронидазол уникально эффективен при лечении инфекций Selenomonassputigena и Peptostreptococcus и равен миноциклину при лечении инфекций Fusobacterium .
ЗАКЛЮЧЕНИЕ
Инфекции пародонта могут вовлекать множество патогенов с разной чувствительностью к противомикробным препаратам и разными типами резистентности.При пародонтальных инфекциях тканевые барьеры и биопленки следует удалять механической обработкой до или с помощью антибиотиков. Для успешного лечения пародонта необходимо тщательно определить статус заболевания пародонта и режим антимикробной терапии. Если противомикробные препараты против заболеваний пародонта не будут использоваться разумно, мы можем вскоре столкнуться с новой породой оральных микроорганизмов с повышенной защитой, которая обеспечит выживание вида, позволит повысить патогенность и передать генетический материал, кодирующий повышенную вирулентность и устойчивость к антибиотикам, другим оральным микроорганизмам. и неоральные микроорганизмы.
Сноски
Источник поддержки: Нет.
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Слоты Дж., Тинг М. Системные антибиотики в лечении заболеваний пародонта. Периодонтол 2000. 2002; 28: 106–76. [PubMed] [Google Scholar] 2. Эллен Р.П., Маккулок, Калифорния. Доказательства против эмпиризма: рациональное использование системных антимикробных препаратов для лечения пародонтита. Периодонтол 2000. 1996; 10: 29–44. [PubMed] [Google Scholar] 3.Слотс Дж. Комитет по исследованиям, науке и терапии. Системные антибиотики в пародонтологии. J Periodontol. 2004. 75: 1553–65. [PubMed] [Google Scholar] 4. ван Винкельхофф AJ, Рамс TE, Слотс Дж. Системная антибактериальная терапия в пародонтологии. Периодонтол 2000. 1996; 10: 45–78. [PubMed] [Google Scholar] 5. Жолковский Д.Л., Чианцио С. Химиотерапевтические средства. В: Carranza FA, Newman MG, Takei HH, Klokkevold PR, редакторы. Клиническая пародонтология. 10-е изд. Филадельфия: У. Б. Сондерс; 2006. С. 798–812. [Google Scholar] 6.Herrera D, Sanz M, Jepsen S, Needleman I, Roldan S. Систематический обзор эффекта системных противомикробных препаратов в качестве дополнения к масштабированию и выравниванию корней у пациентов с пародонтитом. J Clin Periodontol. 2002; 29: 136–59. [PubMed] [Google Scholar] 7. Слоты Дж., Макдональд Э.С., Новзари Х. Инфекционные аспекты регенерации пародонта. Периодонтол 2000. 1999; 19: 164–72. [PubMed] [Google Scholar] 8. Haffajee AD, Socransky SS, Gunsolley JC. Системная противоинфекционная терапия пародонта: систематический обзор. Ann Periodontol.2003. 8: 115–81. [PubMed] [Google Scholar] 9. Tripathi KD. Противомикробные препараты: общие соображения. В: Трипати К.Д., редактор. Основы медицинской фармакологии. 5-е изд. Нью-Дели: Jaypee Publishers; 2003. С. 627–40. [Google Scholar] 10. Гудсон Дж. М.. Антимикробные стратегии лечения заболеваний пародонта. Периодонтол 2000. 1994; 5: 142–68. [PubMed] [Google Scholar] 11. Pallasch TJ. Фармакокинетические принципы антимикробной терапии. Периодонтол 2000. 1996; 10: 5–11. [PubMed] [Google Scholar] 12.Голуб Л.М., Рамамурти Н., Макнамара Т.Ф., Гомес Б., Вольф М., Казино А и др. Тетрациклины подавляют активность тканевой коллагеназы. Новый механизм лечения пародонтоза. J Periodontal Res. 1984; 19: 651–5. [PubMed] [Google Scholar] 13. Ланц М.С., Рэй Т., Кришанасами С., Персон Д.Е. Субингибирующие концентрации тетрациклина изменяют связывание фибриногена Bucferoidesinterrnedius. Противомикробные агенты Chemother. 1987; 31: 1915–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Викешо У.М., Бейкер П.Дж., Кристерсон Л.А., Дженко Р.Дж., Лайалл Р.М., Хик С. и др.Биохимический подход к регенерации пародонта: обработка тетрациклином улучшает состояние поверхности дентина. J Periodont Res. 1986; 21: 322–9. [PubMed] [Google Scholar] 15. Уокер CB. Избранные противомикробные средства: механизмы действия, побочные эффекты и лекарственные взаимодействия. Периодонтол 2000. 1996; 10: 12–28. [PubMed] [Google Scholar] 16. Haffajee AD, Torresyap G, Socransky SS. Клинические изменения после четырех различных пародонтологических методов лечения хронического пародонтита: результаты за 1 год. J Clin Periodontol.2007; 34: 243–53. [PubMed] [Google Scholar] 17. Гордон Дж., Уокер С., Ламстер I, Вест Т., Сокранский С., Сейгер М. и др. Эффективность клиндамицина гидрохлорида при рефрактерном периодонтите — результаты через 12 месяцев. J Periodontol. 1985; 56: 75–80. [PubMed] [Google Scholar] 18. Уокер CB, Гордон JM, Магнуссон I, Кларк WB. Роль антибиотиков в лечении рефрактерного пародонтита. J Periodontol. 1993; 64: 772–81. [PubMed] [Google Scholar] 19. Йоргенсон М.Г., Слотс Дж. Ответственное использование противомикробных препаратов в пародонтологии.J Calif Dent Assoc. 2000. 28: 185–93. [PubMed] [Google Scholar] 20. ван Винкельхофф AJ, Винкель EG. Антибиотики в пародонтологии: правильно или неправильно? J Periodontol. 2009. 80: 1555–8. [PubMed] [Google Scholar] 21. Винкель EG, ван Винкельхофф AJ, Тиммерман MF, Ван дер Фельден U, ван дер Вейден GA. Амоксициллин плюс метронидазол в лечении взрослых пациентов с пародонтитом. Двойное слепое плацебо-контролируемое исследование. J Clin Periodontol. 2001. 28: 296–305. [PubMed] [Google Scholar] 22. Герреро А., Гриффитс Г.С., Нибали Л., Суван Дж., Молес Д.Р., Лорелл Л. и др.Дополнительные преимущества системного амоксициллина и метронидазола при нехирургическом лечении генерализованного агрессивного пародонтита: рандомизированное плацебо-контролируемое клиническое исследование. J Clin Periodontol. 2005. 32: 1096–107. [PubMed] [Google Scholar] 23. Сигуш Б., Байер М., Клингер Г., Пфистер В., Глокманн Э. Двухэтапная безоперационная процедура и системные антибиотики в лечении быстро прогрессирующего пародонтита. J Periodontol. 2001. 72: 275–83. [PubMed] [Google Scholar] 24. Рамс Т.Е., Фейк Д., Слотс Дж. Лечение рецидивирующего пародонтита у взрослых ципрофлоксацином / метронидазолом.J Dent Res. 1992; 71: 319. [Google Scholar] 25. Мили Б.Л., Клоккевольд П.Р., Отомо-Коргель Дж. Пародонтологическое лечение пациентов с нарушениями здоровья. В: Carranza FA, Newman MG, Takei HH, Klokkevold PR, редакторы. Клиническая пародонтология. 10-е изд. Филадельфия: У. Б. Сондерс; 2006. С. 650–64. [Google Scholar] 26. Маленький JW, Фалас Д.А., Миллер С.С., Родус Н.Л. 7-е изд. Сент-Луис: Мосби Эльзевьер; 2008. Стоматологическое лечение пациента с ограниченными возможностями здоровья; С. 1–40. [Google Scholar] 27. Тонг, округ Колумбия, Ротвелл, BR. Антибиотикопрофилактика в стоматологии: обзор и практические рекомендации.J Am Dent Assoc. 2000; 131: 366–74. [PubMed] [Google Scholar] 28. Rosling B, Serino G, Hellstrom MK, Socransky SS, Lindhe J. Продольные изменения тканей пародонта во время поддерживающей терапии. Результаты исследований субъектов с нормальной и высокой предрасположенностью к заболеваниям пародонта. J Clin Periodontol. 2001; 28: 241–9. [PubMed] [Google Scholar]Лечение антибиотиками — Центр имплантологии и пародонта
Если пародонтолог сказал вам, что у вас пародонтит, первым шагом в вашем лечении будет удаление зубного камня и полировка корня.Цель лечения пародонта — тщательно очистить очаги бактерий и предотвратить дальнейшее повреждение. Для многих пациентов это, наряду с хорошим домашним уходом и регулярной чисткой, поможет улучшить здоровье полости рта и сохранить его на всю жизнь. Однако в тяжелых случаях пародонтоза этого может быть недостаточно.
Антибиотики могут быть полезным инструментом в сочетании с хирургическим вмешательством и другой пародонтальной терапией, если у вас есть:
- Тяжелые формы пародонтита (запущенная болезнь десен) ,00
- Заболевания пародонта, состояние которых не улучшилось с помощью только других видов лечения
- Заболевания пародонта и ослабленная иммунная система
Устные лекарства
Для полного уничтожения бактерий, вызывающих инфекцию, могут потребоваться пероральные антибиотики, которые обычно назначаются при острой инфекции.Хотя длительное использование пероральных антибиотиков обычно не рекомендуется из-за риска бактериальной резистентности, оно может быть эффективным для контроля агрессивных заболеваний пародонта.
Местное лекарство
В отличие от пероральных препаратов, которые обладают системным действием, местное нанесение антибиотиков на поверхность десен не повлияет на все ваше тело. Ваш пародонтолог может порекомендовать использовать антибиотики местного действия для контроля бактериальной инфекции, которые могут включать полоскание рта антибиотиками или введение нитей и гелей, содержащих антибиотики, в пространство между зубами и деснами или в карманы после глубокой чистки.
Антибиотики лечат бактериальную инфекцию, вызывающую заболевание пародонта, но их также можно использовать для:
- Предлагает защиту для пациентов с сердечными заболеваниями, перенесших стоматологическую операцию, предотвращая инфекции сердечно-сосудистой системы
- Помогите предотвратить дальнейшее инфицирование десен
- Уменьшает воспаление, которое может еще больше повредить ткань десны
Если состояние вашего пародонта не улучшается даже при регулярных осмотрах, чистках и домашнем уходе, спросите пародонтолога, подходит ли вам добавление антибактериальной терапии.
Лечение антибиотиками | Тампа, Флорида
Заболевание пародонта — это прогрессирующее заболевание, которое при отсутствии лечения приводит к тяжелому воспалению и потере зубов. Лечение антибиотиками можно использовать в сочетании с масштабированием и планированием корня, выскабливанием, хирургическим вмешательством или как отдельное лечение, чтобы помочь уменьшить количество бактерий до и / или после многих распространенных пародонтальных процедур.
Существует несколько различных видов лечения антибиотиками, в том числе оральные формы и гели для местного применения, которые наносятся непосредственно в карманы десен.Исследования показали, что в случае острой пародонтальной инфекции, рефрактерных заболеваний пародонта, препубертатных заболеваний пародонта и ювенильных заболеваний пародонта лечение антибиотиками было невероятно эффективным.
Антибиотики могут быть назначены в низких дозах для длительного использования или в качестве краткосрочного лекарства для предотвращения повторной колонизации бактерий.
Пероральные антибиотики
Пероральные антибиотики имеют тенденцию влиять на все тело и назначаются реже, чем гель для местного применения.Вот некоторые подробности о нескольких различных типах пероральных антибиотиков:
-
Тетрациклиновые антибиотики — Антибиотики, в состав которых входят гидрохлорид тетрациклина, доксициклин и миноциклин, являются основными препаратами, используемыми при лечении пародонта. Они обладают антибактериальными свойствами, уменьшают воспаление и блокируют коллагеназу (белок, разрушающий соединительную ткань).
-
Макролидные антибиотики — Эта группа антибиотиков доказала свою эффективность в уменьшении воспаления, а также может уменьшить рост бактерий, связанных с пародонтитом.
-
Метронидазол — Этот антибиотик обычно используется в сочетании с амоксициллином или тетрациклином для борьбы с воспалением и размножением бактерий при тяжелом или хроническом периодонтите.
Гели и полоски для местного применения
Самым большим преимуществом прямой доставки антибиотиков к поверхности десен является то, что это не влияет на все тело. Гели для местного применения и методы прямой доставки, как правило, предпочтительнее их пероральных аналогов и чрезвычайно эффективны при использовании после процедур удаления зубного камня и выравнивания корня.Вот некоторые из наиболее часто используемых антибиотиков прямой доставки:
-
Arestin ® — Этот антибиотик миноциклина поставляется в мини-капсулах, которые гигиенист доставляет непосредственно в десны после удаления зубного камня и планирования корня, а также при последующих посещениях для ухода за пародонтом.
-
PerioChip ® — Этот чип помещается в собственно карман десны после процедуры строгания корня.PerioChip® медленно высвобождает хлоргексидин, мощный антибактериальный антисептик. PerioChip ® в большинстве случаев уменьшает глубину кармана у больных пародонтитом.
-
Actisite ® — Эта тонкая полоска похожа на зубную нить и содержит гидрохлорид тетрациклина. Нить временно помещают непосредственно между зубом и десной, чтобы убить бактерии и уменьшить глубину карманов десен. Иногда на 10 дней накладывают несколько нитей, чтобы усилить действие антибиотика.
-
Elyzol ® — Этот антибиотик метронидазола выпускается в форме геля и полоски. Он уникален тем, что способен уничтожать паразитов, а также бактерии полости рта.
-
Atridox ® — Этот гель доксициклина повторяет контуры поверхности десен и затвердевает над ними. В течение нескольких дней этот гель постепенно высвобождает антибиотик. Заметные улучшения пародонта обычно наблюдаются после системного или перорального лечения антибиотиками. Ваш пародонтолог или стоматолог назначит и порекомендует вам лечение антибиотиками, необходимое для выздоровления вашего пародонта.
Если у вас есть какие-либо вопросы о пародонтозе или лечении антибиотиками, обратитесь к своему стоматологу.
Дополнительное использование антибиотиков и противомикробных препаратов в пародонтологической терапии
Удаление зубного камня и выравнивание корня — наиболее эффективный и наиболее рекомендуемый метод лечения в составе нехирургической пародонтальной терапии. 1,2 Однако лечение пародонта может поддерживаться дополнительными терапиями, предназначенными для уменьшения хронического воспаления с помощью местных или системных агентов и / или дополнительных терапий с модуляцией хозяина при заболеваниях пародонта. 2
Дополнительная терапия с модуляцией хозяина — это лечение, которое потенциально снижает разрушение тканей за счет изменения факторов ответа хозяина. 3 Единственным лекарством, одобренным Управлением по контролю за продуктами и лекарствами США (FDA), является субантимикробная доза доксициклина.Это системный препарат, применяемый для модуляции хозяина в качестве дополнения к шелушению и выравниванию корней при лечении периодонтита. 4 Эта дополнительная терапия модуляции хозяина представляет собой ингибитор коллагеназы, состоящий из 20 мг капсулы доксициклина гиклата для перорального системного введения. Исследования показывают, что пациенты с пародонтитом, которые ежедневно использовали этот режим доксициклина, снижали повышенную активность коллагеназы в десневой десневой щели. 5
Бактерицидный метронидазол эффективен против анаэробных микроорганизмов при заболеваниях пародонта.Он используется в качестве дополнительной терапии при гингивите, язвенно-некротическом гингивите, хроническом пародонтите и агрессивном пародонтите. Как и другие вспомогательные методы лечения, метронидазол следует использовать в сочетании со скейлингом и выравниванием корня, хирургическим вмешательством или другими антибиотиками. Чаще всего его назначают в таблетках по 250 мг и принимают три раза в день в течение 7 дней. Из-за режима дозирования соблюдение пациентом режима приема препарата может быть затруднено. Haffajee et al. 6 обнаружили, что пациенты с пародонтальными карманами ≥ 6 мм испытали значительное уменьшение глубины карманов и увеличение прикрепления при использовании метронидазола.Когда метронидазол назначают в качестве комбинированной терапии с амоксициллином, пациент получает разнообразное действие и увеличивает спектр антимикробной активности. Комбинация амоксициллин (250 мг) -метронидазол (75 мг), принимаемая три раза в день в течение 8 дней, является одной из наиболее распространенных комбинаций антибиотиков в пародонтологии. Berglundh et al. 7 показали, что у пациентов с пародонтитом улучшилось состояние пародонта, уменьшилось количество патогенов пародонта и уменьшился размер поражения при приеме амоксициллин-метронидазола.
Использование системных антибиотиков в качестве дополнительной терапии к шелушению и выравниванию корня может обеспечить дополнительные преимущества по сравнению с чисткой и строганием корня при лечении пародонтита, включая потерю клинического прикрепления и изменение глубины кармана, а также снижение риска разрушения структур пародонта. Однако использование системной антибактериальной терапии не заменяет процедуры удаления зубного камня и корня или тщательный уход за пациентом.
МЕСТНЫЕ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Системы местной доставки лекарств используются в пародонтальных карманах и могут подавлять или устранять патогенные микроорганизмы пародонта, а также модулировать воспалительную реакцию тканей.Однако они не заменяют необходимость тщательного удаления зубного камня и строгания корня. Системы местной доставки лекарств помещаются в пародонтальные карманы. Дополнительное использование местных систем доставки лекарств со свойствами контролируемого высвобождения может обеспечить определенный, но ограниченный положительный ответ на пародонтальные карманы. Кроме того, успех местной доставки лекарств зависит от клинических данных, реакции на лечение, желаемых клинических результатов, а также от стоматологических данных и истории болезни пациентов. 8 Основным преимуществом является их способность доставлять терапевтические уровни антибактериальных агентов непосредственно в пародонтальные карманы без системных побочных эффектов.Однако способность контролировать высвобождение лекарств в определенном месте в течение длительного периода является ключевым фактором их успеха. 9
Желатиновая матрица, содержащая 2,5 мг хлоргексидина глюконата, представляет собой поддесневую систему доставки с контролируемым высвобождением. Он используется в качестве дополнительной терапии в сочетании с инструментами для ухода за пародонтом с карманами ≥ 5 мм, которые кровоточат при зондировании. Хлоргексидин вводится в пародонтальный карман. При контакте с поддесневыми жидкостями он становится липким и связывается с эпителием кармана.Хлоргексидин высвобождается в течение 7-10 дней, чип рассасывается, и его не нужно удалять. Puri et al 9 сообщили, что использование этой системы улучшило здоровье пародонта и уменьшило рецидивы пародонтальных патогенов.
Другой вариант — гель, состоящий из 10% доксициклин-гиклата. Раствор смешивается в двух шприцах и вводится в пародонтальный карман вокруг зуба. Раствор затвердевает при контакте с десневой щелевой жидкостью. По мере биоразложения доксициклин доставляется на место в больших количествах в течение от 7 до 14 дней. 10 Deo et al. 11 обнаружили, что эта терапия уменьшала глубину кармана и увеличивала клинические уровни прикрепления в большей степени, чем только масштабирование и строгание корня.
Продукт с замедленным высвобождением содержит антибиотик миноциклина гидрохлорид, который является тетрациклиновым антибиотиком широкого спектра действия и одним из наиболее активных антибиотиков против большинства микроорганизмов, связанных с заболеваниями пародонта. Он имеет наиболее заметную субстантивность и представляет собой биорассасывающуюся систему устойчивой местной доставки лекарств в одноразовом полипропиленовом аппликаторе 2% гидрохлорида миноциклина. 12 Одним из его преимуществ является то, что лекарство можно вводить в более высокую концентрацию поддеснево на 24 часа с замедленным высвобождением. После первого применения концентрация препарата экспоненциально снижается. 12 Доказательства подтверждают, что дополнительные местные противомикробные препараты с контролируемым высвобождением повышают эффективность удаления зубного камня и выравнивания корней. 13
ПРОТИВОМИКРОБНЫЕ ПРОМЫВКИ
Противомикробные полоскания оказались полезным дополнением к ежедневному уходу за полостью рта. 14 Доступно бесчисленное множество антимикробных ополаскивателей, включая те, которые содержат цетилпиридиния хлорид, диоксид хлора, хитозан-аргининамид, масло мяты перечной, масло чайного дерева, масло цедры лимона и алоэ вера, но большинство исследований проводилось на ополаскивателях для рта, содержащих хлоргексидин и эфирные масла. масла. Хотя дельмопинол не является противомикробным средством, он доступен в составе средства для полоскания рта и предназначен для предотвращения накопления зубного налета. Недавнее исследование показало, что хлоргексидин и жидкости для полоскания рта с эфирным маслом подавляют разрастание биопленок и уменьшают воспаление десен по сравнению с плацебо. 15 Антимикробные полоскания могут предоставить пациентам эффективные, безопасные и практичные средства контроля репопуляции патогенных бактерий и гингивита. Однако, поскольку жидкости для полоскания рта не проникают в глубокие участки пародонта, их полезность при лечении пародонтита ограничена.
Были изучены потенциальные риски использования антимикробных ополаскивателей для рта. Включение антибактериальных ингредиентов может повлиять на микробы полости рта, критические для образования оксида азота, и, в свою очередь, предрасполагать пациентов к метаболическим нарушениям, включая диабет. 16 Джошипура и др. 16 обнаружили, что у пользователей антимикробных ополаскивателей дважды в день повышен риск преддиабета / диабета 2 типа. Однако все испытуемые имели избыточный вес / ожирение и имели факторы риска диабета. Кроме того, более 60% участников исследования уже имели умеренное или тяжелое заболевание пародонта. 16 В то время как некоторые исследования показали повышенный риск рака полости рта при использовании антимикробных ополаскивателей, 17 метанализ не выявил связи между ополаскивателем для рта и раком полости рта, независимо от частоты использования. 18
ОБРАЗОВАНИЕ ПАЦИЕНТОВ
Пациенты с поражением пародонта или не соблюдающие инструкции по уходу за собой должны быть проинформированы об антибиотиках и антимикробных полосканиях в качестве дополнения к их режимам гигиены полости рта. Кроме того, взаимосвязь между здоровьем полости рта и общим здоровьем продемонстрирует важность межпрофессионального подхода к укреплению здоровья полости рта во время обучения пациентов. Консультации по вопросам питания, отказ от курения, оценка риска диабета и скрининг рака полости рта должны быть частью обучения пациентов.Эти дополнительные компоненты к инструкциям по уходу за собой могут помочь клиницистам определить, принесут ли пользу пациентам антибиотики или антимикробные полоскания. Стоматологи-гигиенисты обладают квалификацией для проведения общего просвещения по вопросам укрепления здоровья и профилактики заболеваний, и им не следует ограничивать свою деятельность только здоровьем полости рта. 19
ЗАКЛЮЧЕНИЕ
Исследования показывают, что использование дополнительных местных противомикробных препаратов с контролируемым высвобождением улучшает эффективность удаления зубного камня и выравнивания корней. 13 Следует отметить, что использование дополнительных процедур для улучшения лечения пародонта не является альтернативным методом тщательного ухода за собой или ухода за пародонтом. Специалисты в области гигиены полости рта должны определять эффективность дополнительных методов лечения заболеваний пародонта, исходя из потребностей отдельных пациентов.
ССЫЛКИ
- Page R. Микробиологическое обоснование дополнительной терапии пародонтита. J Int Acad Periodontol .2004. 6: 143–149.
- Бадер Х. Дополнительная пародонтальная терапия: обзор современных методов. Доступно по адресу: dentalcetoday.com/courses/81%2FPDF%2FDTCE_July_127.1_drft2.pdf. По состоянию на 27 августа 2018 г.
- Шинвари М., Танвир Ф., Хайдер П., Бин Саид М. Терапия модуляции хозяина в пародонтологии: роль в качестве дополнительной пародонтальной терапии. J Coll Врачи Surg Pak . 2014; 24: 676–684.
- Кейтон Дж., Райан МЭ. Клинические исследования по лечению заболеваний пародонта с использованием доксициклина в субантимикробных дозах (SDD). Pharmacol Res. 2011; 63: 114–120.
- Голуб Л.М., Макнамара Т.Ф., Райан М.Э. и др. Дополнительное лечение субантимикробными дозами доксициклина: влияние на активность коллагеназы десневой жидкости и потерю прикрепления при пародонтите у взрослых. J Clin Periodontol. 2001; 28: 146–156.
- Haffajee A, Torresyap G, Socransky S. Клинические изменения после четырех различных пародонтологических методов лечения хронического пародонтита: результаты за 1 год. J Clin Periodontol. 2007; 34: 243–253.
- Berglundh T, Krok L, Liljenberg B, Westfelt E, Serino G, Lindhe J. Использование метронидазола и амоксициллина в лечении запущенных заболеваний пародонта. Проспективное контролируемое клиническое исследование. J Clin Periodontol .1998; 25: 354–362.
- ДаРоча Х., Сильва С., Сантьяго Ф., Мартинс Л., Диас П., ДеМахалхаес Д. Местные системы доставки лекарств при лечении пародонтита: обзор литературы. J Int Acad Periodontol . 2015; 17: 82–90.
- Puri K, Dodwad V, Bhat K, Puri N. Влияние Periochip с контролируемым высвобождением на клинические и микробиологические параметры у пациентов с хроническим пародонтитом. J Indian Soc Periodontol. 2013: 17: 605–611.
- Мухатар А., Вандана К. Сравнительная оценка системы доставки атригеля (10% доксициклин-гиклат) Атридокс со скейлингом и выравниванием корня и комбинированной терапией при лечении пародонтита: клиническое исследование. J Indian Soc Periodontol. 2012: 16: 43–48.
- Deo V, Ansari S, Mandia S, Bhongade M. Терапевтическая эффективность субгингивального введения доксициклина гиклата в качестве дополнения к нехирургическому лечению хронического пародонтита. J Oral Maxillofac Res . 2011; 2: e3.
- Аббас С., Махендра Дж., Ари Г. Мазь с миноциклином в качестве местного лекарственного средства при лечении генерализованного хронического пародонтита — клиническое исследование. J Clin Diagn Res . 2016; 10: ZC15 – ZC19.
- Финкельман Р., Полсон А. Фактические соображения относительно клинического использования местных противомикробных препаратов с контролируемым высвобождением в пародонтологической терапии. Дж Дент Хиг . 2013; 87: 249–264.
- Моран Дж., Пал Д., Ньюкомб Р., Эдди М. Сравнение фенольной и 0,2% хлоргексидиновой жидкости для полоскания рта на развитие зубного налета и гингивита. Clin Prevent Dent . 1991; 13: 31–35.
- Goutham BS, Manchanda K, Sarkar AD, Prakash R, Jha K, Mohammed S. Сравнительное исследование эффективности двух коммерчески доступных полосканий для полости рта — хлоргексидина и листерина на зубном налете и гингивите. J Int Oral Health . 2013; 5: 56–61.
- Джошипура К., Муньос-Торрес Ф, Мору-Бермудес Э., Патель, Р.Использование жидкости для полоскания рта без рецепта и риск преддиабета / диабета. Оксид азота . 2017; 71: 1420.
- Элиот М.Н., Мишо Д.С., Ланжевен С.М., МакКлин М.Д., Келси К.Т. Пародонтоз и использование жидкости для полоскания рта являются факторами риска плоскоклеточного рака головы и шеи. Контроль причин рака. 2013; 24: 1315–1322.
- Gandini S, Negri E, Boffetta P, La Vecchia C, Boyle P. Количественный метаанализ эпидемиологических исследований риска рака полости рта и рака полости рта. Ann Agric Environ Med. 2012; 19: 173–180.
- Орн К. Роль стоматологов-гигиенистов в профилактике здоровья полости рта. Oral Health Prev Dent . 2004; 2 (Дополнение 1): 277–281.
Из Размеры стоматологической гигиены . Сентябрь 2018; 16 (9): 18,20.
Drs. Suway and Toscano, Зубные имплантаты, косметическая и лазерная пародонтология
Лечение антибиотиками можно использовать в сочетании с удалением зубного камня и выравниванием корня, выскабливанием, хирургическим вмешательством или как отдельное лечение.
Для лечения антибиотиками используются пероральные формы и гели для местного применения, которые наносятся непосредственно в карманы десен. Исследования показали, что в случае острой пародонтальной инфекции, рефрактерных заболеваний пародонта, препубертатных заболеваний пародонта и ювенильных заболеваний пародонта лечение антибиотиками было невероятно эффективным.
Антибиотики могут быть назначены в низких дозах для длительного использования или в качестве краткосрочного лекарства для предотвращения повторной колонизации бактерий.
Пероральные антибиотики
-
Тетрациклиновые антибиотики — Антибиотики, которые включают гидрохлорид тетрациклина, доксициклин и миноциклин, являются распространенными препаратами, используемыми при лечении пародонта.Они обладают антибактериальными свойствами, уменьшают воспаление и блокируют коллагеназу (белок, разрушающий соединительную ткань).
-
Макролидные антибиотики — Эта группа антибиотиков доказала свою эффективность в уменьшении воспаления, а также может уменьшить рост бактерий, связанных с пародонтитом.
-
Метронидазол — Этот антибиотик обычно используется в сочетании с амоксициллином или тетрациклином для борьбы с заболеваниями пародонта, которые более устойчивы к другим методам лечения.
Местные антибиотики
Самым большим преимуществом прямой доставки антибиотиков в пораженные пародонтальные карманы является то, что не затрагивается все тело. Гели для местного применения и методы прямой доставки, как правило, предпочтительнее их пероральных аналогов и чрезвычайно эффективны при использовании после процедур удаления зубного камня и выравнивания корня. Вот некоторые из наиболее часто используемых антибиотиков прямой доставки:
-
Atridox ® — Этот гель доксициклина повторяет контуры поверхности десен и затвердевает над ними.В течение нескольких дней этот гель постепенно высвобождает антибиотик.
-
PerioChip ® — Этот чип помещается в собственно карман десны после процедуры строгания корня. PerioChip® медленно высвобождает хлоргексидин, мощный антибактериальный антисептик. PerioChip ® в большинстве случаев уменьшает глубину кармана у больных пародонтитом. Arestin ® — Этот антибиотик миноциклина выпускается в мини-капсулах, которые доставляются в десны после удаления зубного камня и планирования корня.
Заметные улучшения пародонта обычно наблюдаются после системного или перорального лечения антибиотиками. Врачи могут включить или порекомендовать лечение антибиотиками, если это необходимо для лечения вашего состояния пародонта.
Если у вас есть какие-либо вопросы о пародонтозе или лечении антибиотиками, звоните в офис.
Jenkintown Periodontics & Dental Implants, LLC
Д-р Нил Б.Suway & Dr. Jeremy Toscano
Зубные имплантаты, косметическая и лазерная пародонтология
261 Old York Road Suite 319
Jenkintown, PA 19046
Телефон: (215) 887-6060
Удобно добраться до Филадельфии, Абингтон, Уиллоу Гроув, Элкинс Парк, Челтнем, Хоршем, Уорминстер и Хатборо
Годовые результаты рандомизированного контролируемого клинического исследования по оценке эффектов нехирургической пародонтальной терапии хронического пародонтита в сочетании с трех- или семидневным системным введением амоксициллина / метронидазола
Абстрактные
Фон
Оценить клинические исходы через 12 месяцев после системного введения амоксициллина (AMX) и метронидазола (MET) в дополнение к поддесневой санации (SD) у пациентов с тяжелым хроническим пародонтитом (sChP).
Материалы и методы
102 пациента с sChP лечились случайным образом следующим образом: SD в течение 2 дней подряд и плацебо в течение 7 дней (группа A), SD + AMX + MET (оба 500 мг x 3 раза в день 3 раза в день) в течение 3 дней (группа B), SD + AMX + МЕТ (оба 500 мг x 3 три раза в день) в течение 7 дней (группа C). Исходно, через 3, 6 и 12 месяцев после лечения оценивались глубина зондирования кармана (PD), уровень клинического прикрепления (CAL), поражение фуркации, кровотечение при зондировании (BOP), оценка налета во рту (FMPS). определенный.Уменьшение количества участков с PD ≥ 6 мм было определено как основная переменная результата.
Результаты
75 пациентов завершили исследование. Через 12 месяцев все три группы лечения показали статистически значимое улучшение (p <0,001) среднего PD, CAL, BOP и количества участков с PD ≥6 мм по сравнению с исходным уровнем. Средние остаточные PD были статистически значимо ниже, а прирост CAL статистически значимо больше в двух группах антибиотиков по сравнению с плацебо. При снижении ПД (p = 0.012) и прирост CAL (p = 0,017) были статистически значимо выше в группе C по сравнению с группой A, только в группе 3-дневной AB было выявлено статистически значимо меньше участков с PD ≥6 мм на расстоянии 12 м (p = 0,003). Уменьшение количества участков с PD ≥ 6 мм (первичный результат) не показало статистически значимых различий между 3 группами лечения. Однако в обеих группах антибиотиков значительно больше пациентов по сравнению с группой плацебо достигли низкого риска прогрессирования заболевания через 12 месяцев (≤4 участков с PD ≥5 мм).
Заключение
Через 12 месяцев оба протокола дополнительных антибиотиков привели к статистически значимо большему клиническому улучшению по сравнению с плацебо.
Образец цитирования: Cosgarea R, Heumann C, Juncar R, Tristiu R, Lascu L, Salvi GE, et al. (2017) Годовые результаты рандомизированного контролируемого клинического исследования по оценке эффектов нехирургической пародонтальной терапии хронического пародонтита в сочетании с трех- или семидневным системным введением амоксициллина / метронидазола.PLoS ONE 12 (6): e0179592. https://doi.org/10.1371/journal.pone.0179592
Редактор: Питер Эйкхольц, Центр стоматологической, оральной и челюстно-лицевой медицины, ГЕРМАНИЯ
Поступила: 4 ноября 2016 г .; Принята к печати: 18 мая 2017 г .; Опубликован: 29 июня 2017 г.
Авторские права: © 2017 Cosgarea et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Авторы не получали специального финансирования на эту работу.
Конкурирующие интересы: Авторы заявили об отсутствии конкурирующих интересов.
Введение
Принято считать, что хронический пародонтит (ХП) представляет собой вызванное зубным налетом воспалительное заболевание, которое поражает опорные структуры зубов.Если не лечить, прогрессирующее разрушение этих тканей может в конечном итоге привести к потере зубов [1]. Таким образом, основным направлением пародонтальной терапии является удаление бактериальных отложений с поверхности корней посредством механической обработки раны [т.е. масштабирование и планирование корня (-SRP)], направленное на устранение воспаления, остановку прогрессирования заболевания и восстановление здоровья пародонта. Несколько авторов представили доказательства того, что персистентность Aggregatibacter actinomycetemcomitans (A . actinomycetemcomitans) , Porphyromonas gingivalis (P . gingivalis) и некоторые другие виды бактерий связаны с прогрессированием деструкции тканей [2–4], в то время как лучшие клинические результаты были получены, когда эти бактерии не были обнаружены [5–7] . Следовательно, уменьшение или даже полное устранение микробной нагрузки представляется необходимым для получения долгосрочной клинической стабильности [8, 9].
Для достижения этих целей безоперационную пародонтологическую терапию часто комбинируют с дополнительными антибактериальными средствами i.е. антибиотики и антисептики [3, 10–13]. Большое количество исследований предоставило доказательства того, что дополнительное применение амоксициллина (AMX) и метронидазола (MET) к SRP имело положительный эффект на подавление A . actinomycetemcomitans и другие пародонтопатогенные бактерии из пораженных пародонтом участков [14–18]. Статистически и клинически значимо лучшие клинические результаты с точки зрения уменьшения глубины кармана (PD) и увеличения уровня клинического прикрепления (CAL) наблюдались, когда комбинация AMX + MET вводилась дополнительно к SRP по сравнению с лечением только SRP [10, 11, 19–29].Кроме того, эта дополнительная схема лечения антибиотиками привела к статистически значимому снижению количества пародопатогенных бактерий и воспалительных цитокинов по сравнению с одним SRP [19–31].
Несмотря на то, что большое количество исследований было сосредоточено на клинических, микробиологических и воспалительных эффектах дополнительного применения AMX и MET к SRP, единого мнения относительно оптимальной дозировки и продолжительности действия этих антибиотиков не существует. В то время как некоторые авторы исследовали дополнительное введение 375 мг AMX и 250/500 мг MET 3 3 раза в сутки в течение 7–8 дней для SRP [19–21, 32, 33], другие оценивали эффект AMX и MET в дозировке 500 мг. мг 3 три раза в день в течение 7 дней [18, 22, 29] или 500 мг AMX и 400/250 мг MET 3 три раза в день в течение 10–14 дней [17, 23–27, 34].Поскольку после приема антибиотиков в течение более длительного периода (например, до 7 дней и дольше) сообщалось о нескольких побочных эффектах, таких как изменение вкуса, головная боль, диарея, тошнота / рвота, гиперчувствительность, почечная и печеночная токсичность и т. Д. [ 19, 35, 36], представляется важным, чтобы антибиотики принимались в минимальной бактерицидной концентрации в течение минимального времени [37]. Было высказано предположение, что такие концепции могут максимизировать положительные эффекты антибиотиков, ограничивая возникновение упомянутых побочных эффектов.Более того, использование высоких концентраций антибиотиков в течение короткого времени может снизить вероятность развития микробной устойчивости к антибиотикам. Кроме того, длительные протоколы приема антибиотиков могут нести более высокий риск нарушения пациентом режима, а соблюдение пациентом режима приема прописанных лекарств без надзора является важным для успеха терапии [38, 39].
Устойчивость бактерий к антибиотикам была признанной проблемой почти с начала эры антибиотиков, демонстрируя непрерывный глобальный рост [40–43]; однако только в последние 20 лет регулярно регистрировалось появление опасных, устойчивых штаммов, влияющих на успех антимикробной терапии опасных для жизни инфекций [44, 45].Устойчивые к антибиотикам инфекции оказывают огромное негативное влияние на общественное здоровье и экономику: то есть в Соединенных Штатах ежегодно 2 миллиона человек заражаются устойчивыми к антибиотикам бактериями и 23 000 умирают от этих инфекций [46]; кроме того, дополнительные расходы на лечение оцениваются в 1,6 млрд. евро и 2,5 млн. евро дополнительных больничных дней в Европе [45, 47] и 20 млрд. долларов и 8 млн. долларов дополнительных больничных дней в США [45, 46, 48]. Новые резистентные штаммы или резистентные факторы в бактериальных популяциях могут появиться, особенно при назначении низких доз лекарств, что приводит к плохой комплаентности к лекарствам или неполному проникновению лекарства во все ткани [49–51].Тем не менее, исследования устойчивости к противомикробным препаратам показали снижение частоты устойчивости после отмены антибиотиков [52–54]. Кроме того, только временное увеличение процента устойчивых поддесневых видов наблюдалось при увеличении введения антибиотика, через 90 дней после антибактериальной терапии процент устойчивых к антибиотикам штаммов вернулся к исходным значениям [53].
Учитывая пагубные последствия длительных курсов антибактериальной терапии (например,грамм. неблагоприятные инфекции, плохое соблюдение пациентом режима лечения, эволюция и распространение микроорганизмов, устойчивых к антибиотикам, дополнительные высокие затраты и госпитализация), ученые / врачи в нескольких областях общей медицины пытались оптимизировать продолжительность терапии, делая упор на оптимальную комбинацию антибиотиков [55], внедрение более коротких схем лечения с высокими дозами [55–63].
В пародонтологической терапии — контролируемые клинические исследования, оценивающие потенциальную эффективность кратковременного введения AMX и MET по сравнению со стандартным протоколом (например,грамм. использования не менее 7 дней) отсутствуют. Недавно мы оценили клинические результаты 3-дневного режима AMX и MET в дополнение к SRP при тяжелом хроническом пародонтите через 6 месяцев, показав, что 3-дневное и 7-дневное дополнительное введение этих антибиотиков привело к статистически значимым лучшим клиническим улучшениям по сравнению с одним SRP в течение 6 месяцев. 6 месяцев [11]. Однако в настоящее время неизвестно, в какой степени результаты, полученные при кратковременном введении AMX и MET, остаются стабильными в течение более длительного периода времени (например,грамм. до одного года).
Таким образом, целью настоящего исследования была оценка клинических результатов, полученных через 1 год после нехирургической пародонтальной терапии (проводимой в течение 2 дней подряд) в сочетании с системным введением AMX и MET в течение 3 или 7 дней у пациентов с тяжелой хронической болезнью. пародонтит (ПКП).
Материалы и методы
Это исследование было разработано как рандомизированное, плацебо-контролируемое, двойное замаскированное клиническое исследование, проверяющее гипотезу о том, что «системное применение AMX и MET в течение 3 или 7 дней в качестве дополнения к SD приводит к лучшим клиническим результатам по сравнению с только с SD »[11].
Мощность исследования рассчитывалась с учетом разницы по крайней мере 5 участков с PD ≥ 6 мм [26, 27, 64] и стандартного отклонения 6 участков [19, 27] между группами AB и плацебо, соответственно. Мощность исследования 92% для уровня статистической значимости 0,05 была достигнута для 30 субъектов на группу лечения; однако с учетом возможного отсева в 13% мы набрали по 34 пациента на каждую группу лечения.
Утверждение этического комитета факультета медицины и фармации Клуж-Напока (Заявка № 514/09.01.2012, утверждено 09.01.2012) был получен протокол исследования, проведенного в соответствии с Хельсинкской декларацией (1964 г., редакция 2008 г.). Исследование было зарегистрировано в реестре исследований ISRCTN (идентификатор исследования ISRCTN17605083). Поскольку набор пациентов начался в январе 2012 года и в то время регистрация исследования не была обязательной для многих журналов, исследование было зарегистрировано с задержкой после начала набора участников. Авторы подтверждают, что все текущие и связанные испытания этого препарата / вмешательства зарегистрированы.
Субъектов
Подробно клинический протокол был представлен ранее [11]. Вкратце, 102 пациента, обращавшиеся за стоматологическим лечением в стоматологической университетской клинике (Университет «Юлиу Хатиегану», Клуж-Напока), были включены и лечились следующим образом: набор пациентов продолжался в период с 10.01.2012 по 01.03.2014, поддесневая обработка раны проводилась в период с 20.01.2012. –30.06.2014, период наблюдения — с 03.02.2012 (2 недели после обработки раны) по 05.06.2015. Были рассмотрены следующие критерии включения: возраст старше 30 лет, пациенты должны иметь в полости рта не менее 12 естественных зубов с клиническими (по крайней мере, одно место / квадрант с PD ≥6 мм) и рентгенологическими признаками генерализованного тяжелого хронического пародонтита [65] , хороший уровень гигиены полости рта (оценка налета на всю полость рта ≤ 25% до стандартного отклонения) [66], системное здоровье без каких-либо заболеваний, которые могут повлиять на тяжесть / прогрессирование пародонтита (например,грамм. Синдром Дауна, ВИЧ, сахарный диабет 1 и 2 типа), отсутствие пострадиационного облучения в области головы / шеи, отсутствие инфекционных / сердечных заболеваний, требующих профилактического приема антибиотиков перед стоматологическим лечением, отсутствие заболеваний печени. Субъекты, выкуривающие не менее 10 сигарет в день в течение последних пяти лет, были определены как курильщики [67]. Пациенты, которые получали нехирургическую пародонтологическую терапию в течение предыдущих 12 месяцев, получали системную или местную терапию антибиотиками в течение предшествующих 3 месяцев при приеме лекарств, которые могли взаимодействовать с AMX или MET (например,д., производные кумарина, содержащие производные спирта, производные 5-фтор-урацил / дисульфирама, пероральные растворы ампренавира, пероральный раствор лопинавира / ритонавира) или при приеме лекарств с возможным влиянием на пародонт (циклоспорин А, соединения фенитоина, блокаторы кальциевых каналов ), или беременные / кормящие пациенты были исключены из исследования. Все подходящие субъекты были тщательно проинформированы о цели, рисках и преимуществах их участия в исследовании, а также о протоколе лечения, и информированное письменное согласие на участие в исследовании было получено от всех участников до начала исследования.
Клинический протокол
Согласно списку, сгенерированному компьютером, все включенные субъекты были распределены в одну из трех групп лечения: контрольная группа А, получавшая SD + плацебо [плацебо трижды в день (TID) в течение 7 дней; группа B, получавшая SD и системный AMX + MET (оба антибиотика по 500 мг 3 раза в день в течение 3 дней, плацебо 3 раза в день в течение остальных 4 дней; и группа C, получавшая SD и системный AMX + MET (оба антибиотика по 500 мг 3 раза в день в течение 7 дней ( Рис. 1. Сокрытие выделения было гарантировано использованием непрозрачных конвертов.
До SD (исходный уровень), через 3, 6 и 12 месяцев после SD с помощью ручного пародонтального зонда (PCPUNC 15, Hu Friedy, Chicago, IL, USA) оценивали следующие параметры: FMPS [66], кровотечение при зондировании ( BOP) [68], глубины кармана (PPD) и уровня клинического прикрепления (CAL). Кроме того, вовлечение фуркации (FI) также измерялось с помощью ручного зонда фуркации (зонд Nabers -PQ2N, Hu Friedy, Чикаго, Иллинойс, США). Сеансы, включающие инструкции по гигиене полости рта и наддесневую чистку, проводились до тех пор, пока пациенты не достигли показателя FMPS ≤ 25%.Все клинические записи и инструкции по гигиене полости рта были выполнены одним экспертом (RJ), не знающим назначения лечения. Впоследствии SRP проводился в течение 2 дней подряд одним опытным пародонтологом (RC), который также не знал о групповом распределении. Все участки с PD ≥ 4 мм были масштабированы и выровнены до дна кармана с помощью машинных скалеров (Kavo Sonicflex Scaler, Kavo Dental GmbH, Бибербах, Германия) и кюретов Gracey (Hu Friedy, Чикаго, Иллинойс, США). Затем обработанные карманы тщательно промывали 0.12% раствор диглюконата хлоргексидина. В течение 14 дней субъекты полоскались 0,2% раствором хлоргексидина диглюконата (Corsodyl ® , GlaxoSmithKline, Brentford, Лондон, Великобритания, два раза в день в течение 2 минут) и чистили зубы 0,2% зубной пастой хлоргексидина диглюконата (Elugel ® , Пьер Фабр, Париж, Франция). В конце сеансов SD пациенты были распределены другим врачом (RT) в одну из трех групп лечения, получили свои лекарства и инструкции по приему (подробное описание таблеток в бутылках см. [11]).Через две недели после SD пациентов спрашивали о соблюдении режима приема исследуемых препаратов и возможных побочных эффектах после приема таблеток. Впоследствии пациенты были отозваны через 3, 6 и 12 месяцев, когда были оценены следующие параметры: FMPS, BOP, PD, CAL, FI. На этих приемах был удален только наддесневой камень, оставив любые остаточные пародонтальные карманы с PD = 4 мм и BOP или PD ≥ 5 мм без повторного инструментария.
Пять пациентов, каждый с минимум 10 зубами с хотя бы одним участком с PD ≥ 6 мм на зуб, были использованы для калибровки исследователя.Пациенты были обследованы дважды в 2 приема с интервалом 48 часов. Калибровка была принята, когда эти измерения были подобны миллиметру при> 90% (средняя надежность внутри обследуемого: PD: 0,87, CAL: 0,76, анализ Cohen’s Kappa). Экзаменатор не знал о назначении лечения.
Статистический анализ
Все данные были введены в базу данных (LI) и дважды проверены на наличие ошибок путем сравнения с исходными картами пациентов (RT, RC). Статистический анализ был выполнен опытным профессиональным статистиком (CH) с использованием статистических программ (SPSS statistics 21, IBM, Армонк, Нью-Йорк, США и R Core Team, 2016.R: Язык и среда для статистических вычислений. R Фонд статистических вычислений, Вена, Австрия).
Статистической единицей был пациент; Первичной переменной результата было уменьшение (Δ) количества участков на пациента с PD ≥ 6 мм, рассчитанное между исходным уровнем и 12 месяцами. Вторичными переменными были средние изменения в FMPS, BOP, PD, AL, количество участков с PD ≥ 6 мм, с PD ≥ 5 мм и общее количество участков с PD = 4 положительными при зондировании и участками с PD ≥ 5 мм через 12 месяцев. а также количество субъектов с низким риском прогрессирования заболевания (≤4 участков с PD≥5 мм) [69].Статистически значимыми считались p- значений <0,05.
Все участки с PD ≥ 4 мм на исходном уровне рассматривались для статистического анализа. Внутригрупповые клинические сравнения между периодами наблюдения анализировали с помощью парного t-критерия и критерия знаковых рангов Вилкоксона. Сравнения между группами в различные моменты времени проводились с поправкой на исходные значения и курение с использованием поправок ANCOVA и Бонферрони.
Было проанализировано остаточное количество участков с PD ≥ 5 мм, и в соответствии с ним пациенты были разделены на низкий (≤4 участка), средний (5–8 участков) и высокий (≥9 участков) риск прогрессирования заболевания [69].Групповые сравнения проводились с использованием точного критерия Фишера.
С помощью регрессионного анализа Пуассона установлена связь между количеством участков с PD ≥ 6 мм через 12 месяцев и переменными лечением (антибиотики в течение 3 или 7 дней), курением, полом, BOP, FMPS, на исходном уровне и через 12 месяцев. месяцев, исходное среднее значение PD, исходное среднее значение AL, тяжесть заболевания ≥10 участков с PD ≥ 6 мм на исходном уровне.
Результаты
Субъектов
Всего 102 человека (средний возраст 43.37 ± 9,85, 65 женщин, 35 курильщиков), удовлетворяющих критериям включения (34 на группу лечения), были включены в это исследование и проходили лечение и наблюдение в соответствии с протоколом в период с января 2012 года по июнь 2015 года. Так, 27 пациентов были исключены из окончательного анализа согласно протоколу (PP). Причины отсева: несоблюдение назначений (n = 16), прием антибиотиков по другим медицинским причинам (n = 9), переезд в другой город (n = 2).В конце концов, 75 субъектов [средний возраст 42,59 ± 9,68 года, 45 женщин (60%), 22 курильщика (29,33%)] были включены в окончательный анализ (рис. 1). Распределение пациентов не выявило статистически значимых различий между группами в отношении пола, статуса курения и исходных клинических параметров (таблицы 1 и 2). Соблюдение пациентом режима приема таблеток оценивалось через две недели после стандартного отклонения, и было отмечено отличное соблюдение режима приема таблеток с небольшими различиями во времени [11]. Нежелательные явления, произошедшие во время или после периода приема лекарств, были зарегистрированы во всех группах лечения: 1-2 пациента в каждой группе лечения имели головные боли, мышечно-скелетные боли, нарушения вкуса и головокружение; 1 пациент в группе плацебо и в группе B жаловался на желудочно-кишечные расстройства, в то время как у 1 пациента в группе плацебо и у 1 пациента в группе C была лихорадка.Только 1 пациент в группе B имел респираторные расстройства, а I пациент в группе плацебо жаловался на дрожь. Ни у одного из пациентов не было признаков аллергии или кандидоза [11].
Таблица 2. Средние значения и сравнения групп (ANOVA с поправкой на курение и ANCOVA с поправкой на исходные значения и курение для 12-месячных переменных) и их изменения (Δ) между исходным уровнем и 12 месяцами (среднее ± стандартное отклонение) (анализ PP, внутригрупповые сравнения между исходным уровнем и 12 м с помощью парного t-критерия и критерия знаковых рангов Вилкоксона).
https://doi.org/10.1371/journal.pone.0179592.t002
Клинические данные
Клинические данные через 3 и 6 месяцев после нехирургического лечения пародонта были представлены в предыдущей публикации [11]. Через 6 месяцев 91 из 102 включенных субъектов завершили оценку, и статистически значимые клинические улучшения (p <0,05) по сравнению с исходным уровнем наблюдались во всех группах лечения для всех оцениваемых клинических параметров. Эти статистически значимые улучшения сохранялись до одного года во всех трех группах, даже если меньшее количество субъектов (75 из 102 субъектов) завершили исследование (p <0.05, парный t-критерий и критерий знаковых рангов Вилкоксона). На исходном уровне не было зарегистрировано статистически значимых различий между группами лечения ни по одному из исследованных клинических параметров (таблицы 1 и 2, p> 0,05). BOP был статистически значимо снижен во всех группах лечения по сравнению с исходным уровнем. Однако никаких статистически значимых различий между группами не наблюдалось на исходном уровне и через 12 месяцев. Во всех трех группах FMPS продемонстрировал статистически незначимое увеличение через 12 месяцев по сравнению с исходным уровнем без каких-либо межгрупповых различий (Таблица 2).
Через 12 месяцев обе группы антибиотиков привели к статистически значимым улучшениям по сравнению с группой плацебо в отношении общего среднего PD, а также среднего снижения PD и PD (Δ base-12m) для участков с PD 4-6 мм и глубоких участков с PD. ≥7 мм (таблица 2). Общее среднее снижение PD (Δ base-12m) было значительно выше только в группе C по сравнению с группой A. Прирост CAL (Δ base-12m) через 12 месяцев был значительно выше в группе 7-дневного AB по сравнению с плацебо для всех сайтов с PD≥4мм, а также для участков с PD 4-6мм.Однако для участков с PD ≥ 7 мм статистически значимых различий между тремя группами не наблюдалось. Кроме того, через 12 месяцев в группе 3-дневной АВ наблюдалось значительно меньше участков с PD ≥6 мм, с PD ≥5 мм и с PD = 4 мм и BOP + по сравнению с контрольной группой (Таблица 2). Тем не менее, уменьшение количества участков с PD ≥ 6 мм (первичная переменная результата) не показало статистических различий между тремя группами пациентов. Статистически значимых изменений ни по одному из оцениваемых клинических параметров между двумя группами антибиотиков не наблюдалось (p> 0.05).
Через 12 месяцев у курильщиков было статистически значимо меньше улучшений по сравнению с некурящими в отношении среднего PD и значительно меньшее снижение PD, среднее CAL и среднее увеличение CAL во всех категориях PD (p <0,05, Таблица 2). Для участков с PD ≥ 7 мм у курильщиков были значительно более высокие средние PD и CAL через 12 месяцев; однако не было статистически значимых различий для снижения PD и увеличения CAL (p> 0,05, таблица 2). Более того, у курильщиков было меньше участков с PD ≥ 5 мм, PD ≥ 4 мм и BOP + (p <0.05, таблица 2).
Анализируя риск прогрессирования заболевания [69], все пациенты во всех группах лечения изначально находились в группе высокого риска (таблица 3). При всех наблюдениях снижение было отмечено во всех группах лечения, так что через 12 месяцев самый низкий процент (20,8%) пациентов с высоким риском прогрессирования заболевания наблюдался в группе 3-дневной АБ, за которой следовали 7- группа дня AB с 40% и, наконец, группа плацебо с 46,2%. Сравнивая группы по количеству субъектов, достигших низкого риска прогрессирования заболевания, представленных ≤4 участков с PD ≥5 мм, в обеих группах антибиотиков присутствовало больше пациентов по сравнению с группой плацебо (таблица 3).Однако в PP-анализах только в группе 3-дневного AB наблюдалось значительно больше пациентов с низким риском через 12 месяцев по сравнению с группой плацебо без значительных различий между группами B и C (Таблица 4). Разница между группами A и C присутствовала только в популяции ITT (p = 0,049). Коррекция Бонферрони (3 теста, сравнивающих группы A-B, A-C, B-C) приведет к значительным различиям только между группами A и B (ITT и PP).
Таблица 3. Пациенты (количество и%) с низким (≤4 количество остаточных участков с PD≥5 мм ≤4), умеренным (количество остаточных участков с PD≥5 мм: 5-8) и высоким (количество остаточных участков с PD ≥5 мм ≥9) риск прогрессирования заболевания [69].https://doi.org/10.1371/journal.pone.0179592.t003
Через 12 месяцев регрессионный анализ показал статистически значимую положительную корреляцию между остаточным количеством участков с PD ≥ 6 мм и группой плацебо (группа B имела 0,28 и группа C 0,70 раза больше ожидаемого количества остаточных участков с PD ≥ 6 мм через 12 месяцев, чем группа A), мужской пол и курильщики. Другими значимыми переменными были процентное соотношение ПБ на исходном уровне и через 12 месяцев, исходный повышенный уровень ПБ и начальное среднее значение CAL (Таблица 5).
Обсуждение
В настоящем исследовании оценивались клинические исходы в течение 12 месяцев после 3 или 7 дней системного введения AMX и MET в дополнение к SD по сравнению с нехирургическим лечением пародонта только у пациентов с тяжелым ХП. 3-дневное системное введение AMX и MET дало сравнимые клинические результаты с 7-дневным режимом AMX и MET в качестве дополнения к SD.
Поскольку в нескольких клинических испытаниях оценивались различные периоды введения антибиотиков в дополнение к нехирургической пародонтальной терапии, например, от 7 [19, 22, 29, 70] до 14 дней [17, 26, 27, 71], нет единого мнения относительно оптимального Существует режим антибиотикотерапии, цель настоящего исследования состояла в том, чтобы предоставить дополнительные данные для определения оптимальной дозировки и продолжительности лечения антибиотиками в дополнение к нехирургическому лечению пародонта.Принимая во внимание тот факт, что возможное появление новых устойчивых штаммов может произойти во время или после единичной длительной инфекции, связанной с терапией антибиотиками, и учитывая широкое использование антибиотиков в нашем обществе, устойчивость к противомикробным препаратам стала в настоящее время глобальным бременем [49, 50] . Поскольку в нескольких областях общей медицины удалось максимально ограничить и оптимизировать схему приема антибиотиков за счет сокращения продолжительности приема антибиотиков и увеличения дозировки [55–57, 63, 72], представляется целесообразным, чтобы аналогичные меры были приняты в стоматологии. ограничение лечения антибиотиками пациентами, которые получают от него наибольшую пользу, и установление оптимального режима лечения (минимальная бактерицидная концентрация и продолжительность) [37].Более того, это должно быть одной из основных целей исследований, поскольку значительное увеличение доли устойчивых штаммов к наиболее часто используемым антибиотикам в стоматологии, особенно к AMX и MET, которые оказались наиболее эффективными при лечении тяжелых форм пародонтита. , уже были зарегистрированы [73–79]. Учитывая эти аспекты и зная, что распространение патогенов пародонта в других частях тела может привести к серьезным опасным для жизни заболеваниям (таким как абсцессы головного мозга, инфекции легких, эндокардит, инфекции мягких тканей) [80], представляется чрезвычайно важным оптимизировать Дополнительное применение антибиотиков при лечении заболеваний пародонта.
Хотя уже существует несколько исследований по оценке и сравнению дозировок 250-500 мг AMX и MET в дополнение к нехирургическому лечению пародонта и продолжительностью 7–14 дней [15, 17–19, 22, 26, 27, 29, 32, 71, 81, 82] и демонстрируя значительные клинические и частично микробиологические преимущества в группах антибиотиков по сравнению с одной только механической терапией, мы сочли целесообразным оценить эффективность краткосрочного курса антибиотиков продолжительностью 3 дня [11]. Однако эта продолжительность может быть проблемой, связанной с развитием устойчивости к противомикробным препаратам.Тем не менее, мы решили проверить эту продолжительность действия антибиотика, основываясь на наблюдениях из исследования Feres et al. [53], где было показано, что временное повышение устойчивости бактерий было ниже в течение 3 дней по сравнению с 7-дневным режимом антибиотикотерапии. Кроме того, были получены положительные результаты при кратковременных курсах лечения острого стрептококкового фарингита у детей [83, 84], при острых инфекциях мочевыводящих путей [85], внутрибрюшных инфекциях и инфекциях в отделениях общей хирургии [86, 87].
В настоящем исследовании через 12 месяцев все группы лечения показали статистически значимое снижение (Δ) количества участков с PD ≥6 мм по сравнению с исходным уровнем (p <0,05) (первичная переменная результата, таблица 2) [11]; не было обнаружено статистически значимых различий между тремя группами лечения, даже несмотря на то, что снижение было выше в двух группах антибиотиков по сравнению с контрольной группой (таблица 2). Это может быть объяснено тем фактом, что в настоящем исследовании через 12 месяцев более высокий отсев числа пациентов по сравнению с априори рассчитанной мощностью исследования наблюдался во всех группах лечения (менее 30 пациентов / группу через 12 месяцев), что приводило к низкому показателю. оценка мощности для первичного результата (апостериорный анализ: для группы сравнения AB 35%, для AC 64%).Широкие диапазоны отклонений для количества участков с PD ≥ 6 мм на исходном уровне (14 65–17,58 участков) также могли повлиять на тот факт, что не было получено значительных различий между 3 группами по их уменьшению (Δ). Однако через 12 месяцев только в группе 3-дневного приема антибиотика было выявлено статистически значимо меньшее количество остаточных глубоких участков (PD ≥ 6 мм) по сравнению с группой плацебо (p = 0,003), даже несмотря на то, что группа плацебо показала на исходном уровне менее глубокие участки. сайтов (25,5 ± 17,36) по сравнению с 2 группами антибиотиков (3 дня AB 29.37 ± 14,65, 7 дней АБ 35,92 ± 17,58, таблица 2). Тем не менее, поскольку количество остаточных глубоких участков (PD ≥ 6 мм) было вторичной переменной результата, эти результаты следует интерпретировать с осторожностью. Сходные результаты были получены также для остаточного числа участков с PD ≥ 5 мм или с PD ≥ 4 мм и BOP +, где только в группе 3-дневного AB выявлено статистически значимо меньше участков по сравнению с плацебо. Тот факт, что в группе 7-дневного приема антибиотиков остаточное количество таких участков (с PD ≥ 6 мм, PD ≥ 5 мм, PD ≥ 4 мм и BOP +) не было статистически значимо ниже по сравнению с группой плацебо, может быть связан с большим количеством такие участки на исходном уровне в группе C по сравнению с группой A [для PD≥6 мм: плацебо 25.50 ± 17,36 (среднее ± стандартное отклонение), 7-дневная группа AB 35,92 ± 17,58 (среднее ± стандартное отклонение)], даже если на исходном уровне не было получено статистически значимых различий между тремя группами лечения (таблица 2).
Наши 12-месячные результаты подтверждают данные, полученные Feres et al., 3-дневная группа AB в нашем исследовании, показывающая сопоставимое остаточное количество участков с PD ≥ 6 мм (1,66 ± 2,26) с 14-дневной группой AMX и MET группы Feres. и другие. (1.2 — 2.2) [27]. Сопоставимые результаты для глубоких участков были также зарегистрированы Harks et al., Где пациенты, получавшие AMX и MET в течение 7 дней, показали 27.5 месяцев 0,9 ± 1,6% участков с PD ≥ 7 мм [81] и по Rooney et al. через 6 месяцев (в группе AMX + MET было 1,3 ± 2,6% участков с PD ≥ 6 мм) [16]. Более того, если посмотреть на количество участков с PD ≥ 5 мм, наши данные аналогичны данным, полученным Feres et al. через 12 месяцев (Feres et al. AMX + MET группа: 4,7 ± 6,0, в нашем исследовании 3-дневная группа AB: 4,71 ± 5,4 сайта) и Silva et al. получены через 3 месяца (Silva et al. AMX + MET в течение 14 дней 5,3 ± 4,4) [26, 27]. Однако Cionca et al. показали через 6 месяцев, что группа AMX + MET имела остаточное количество участков с PD> 5 мм и BOP + 0.4 ± 0,8 [19] намного меньше, чем количество таких сайтов в обеих группах AB из нашего исследования (группа B: 6,41 ± 6,25, группа C: 10,97 ± 8,94). Как сообщалось ранее, исходные состояния пародонта в настоящем исследовании отличаются от таковых Cionca et al. в которую вошли пациенты с умеренным и тяжелым ХП, по крайней мере, с четырьмя зубами с PD> 4 мм и CAL ≥ 2 мм, в отличие от генерализованных тяжелых форм ХП, включенных в настоящее исследование [11, 19]. Это отражено в исходном количестве участков с PD ≥ 5 мм, которое было как минимум вдвое больше в каждой группе лечения настоящего исследования по сравнению с соответствующими значениями в исследовании Cionca et al.[19], а также тем фактом, что все пациенты в настоящем исследовании изначально имели более 9 участков с PD ≥ 5 мм (Таблица 3).
Все три группы лечения получили через 12 месяцев статистически значимое снижение PD и увеличение CAL по сравнению с исходным уровнем. Тем не менее, средние значения PD через 12 месяцев были значительно ниже в обеих группах AB по сравнению с плацебо (p <0,05, таблица 2). Однако среднее снижение PD и увеличение CAL были статистически значимо выше только в группе 7-дневной AB по сравнению с плацебо.Это может быть связано с тем, что эта группа представлена на исходном уровне, даже если статистически незначима, более глубокие участки по сравнению с двумя другими группами (группа A и B), как видно из исходных средних значений для каждой категории PD (общее среднее значение PD, PD 4-6 мм, PD> 7 мм, таблица 2). Кроме того, большее количество глубоких участков (PD ≥ 7 мм) на исходном уровне в 7-дневной группе антибиотиков, даже если оно статистически незначимо по сравнению с двумя другими группами, могло повлиять на результаты снижения PD и увеличения CAL, учитывая, что более глубокие участки могут получить больше пользы от режима AB по сравнению с более мелкими [15, 19, 26, 27, 32].Однако снижение PD для участков с PD между 4-6 мм и для участков с PD ≥ 7 мм было статистически значимо выше в обеих группах AB по сравнению с группой плацебо, без статистически значимых различий при сравнении 3- и 7-дневного AB. группы (таблица 2). Сопоставимые результаты с точки зрения среднего PD были получены Feres et al. через 12 месяцев (плацебо: 3,05 ± 0,59 мм, AMX + MET в течение 14 дней: 2,54 ± 0,40 мм), Cionca et al. через 6 месяцев (плацебо: 3,1 ± 0,3 мм, AMX + MET в течение 7 дней 3,0 ± 0,2 мм) [19, 27].Harks et al. полученные через 27,5 месяцев в обеих группах лечения несколько более низкие средние значения PD по сравнению с данными в настоящем исследовании (плацебо: 2,6 ± 0,7 мм, AMX + MET в течение 7 дней: 2,3 ± 0,5 мм) [81], причем эти различия, возможно, являются Это объясняется исходными средними значениями PD, которые были примерно на 2 мм ниже, чем в нашем исследовании (Таблица 2), и тем фактом, что они сообщили о результатах вдвое более длительного периода наблюдения (27,5 месяцев) по сравнению с нашим исследованием (12 месяцев). Кроме того, среднее снижение PD, полученное в нашем исследовании во всех группах лечения, было сходным с таковым, полученным в группах SRP и AB Goodson et al.через 24 месяца (только SRP: 1,81 ± 0,23 мм, SRP + AMX + MET в течение 14 дней: 2,36 ± 0,2 мм) [71]. Более того, усиление CAL в группе AB Goodson et al. (1,53 ± 0,16 мм) также было сопоставимо с полученным в нашем исследовании (3-дневная группа AB: 1,59 ± 0,65, 7-дневная группа AB: 1,71 ± 0,54 мм). Чуть меньший прирост CAL наблюдался Cionca et al., Feres et al. и Harks et al. [19, 27, 81]. Эти различия могут быть связаны с примерно на 2 мм более высокими исходными значениями CAL у пациентов, включенных в настоящее исследование, по сравнению с таковыми в вышеупомянутых исследованиях.
Исследования, определяющие клиническую эффективность лечения, используют различные критерии для определения успеха [88], такие как изменения PD и CAL, количество и пропорции умеренных и глубоких участков [15, 16, 19, 27, 81]. Поскольку ХП является воспалительным заболеванием, вызванным бактериальной инфекцией, наиболее важной частью его терапии является лечение инфекции и устранение воспаления для остановки прогрессирования заболевания и улучшения прогноза зубов. Использование полного рта PD и CAL в качестве переменных результата в нескольких исследованиях [15, 17, 26, 27, 32], оценивающих эффективность лечения антибиотиками в нехирургической пародонтальной терапии, может быть недостаточно репрезентативным для эффективности лечения антибиотиками. , поскольку неглубокие участки имеют меньшую дополнительную пользу от антибиотиков, чем глубокие участки [15, 19, 26, 27, 32], и могут не подчеркивать лечебный эффект для глубоких участков, которые, как было показано, имеют высокий риск прогрессирования заболевания [64, 69, 89].В этом смысле средние значения PD и CAL, а также их уменьшение / усиление могут не быть наиболее подходящими параметрами для оценки устранения воспаления и эффективности лечения.
Поскольку прогрессирование заболевания с большей вероятностью происходит в глубоких участках, представляется актуальным оценить остаточное количество таких участков или изменить атрибуцию пациента с тяжелого на низкий риск прогрессирования заболевания. Учитывая это, мы проанализировали как остаточное количество глубоких участков (PD ≥ 6 мм), так и отнесение пациента к риску прогрессирования заболевания [69].Независимо от группового распределения, все пациенты имели исходный высокий риск прогрессирования заболевания. После лечения процент таких пациентов непрерывно снижался во всех группах до 12 месяцев. Более тщательный анализ распределения риска между группами показал, что почти половина пациентов в группе плацебо все еще имела высокий риск прогрессирования, в то время как в группе 3-дневной АБ было наименьшее количество пациентов с высоким риском. Наконец, 70% пациентов в группе 3-дневного AB достигли клинической конечной точки низкого прогрессирования заболевания (<4 участков с PD ≥ 5 мм), за ними следовала группа 7-дневного AB с более чем 40% и группа плацебо с только 20%, что было статистически значимо ниже только по сравнению с 3-дневной группой AB (анализ PP).Кроме того, аналогичные проценты для групп A и C были получены для числа пациентов, у которых сохранялся высокий риск прогрессирования заболевания (≥9 участков с PD ≥ 5 мм) и большего количества участков с PD ≥ 5 мм через 12 месяцев. Тот факт, что группа C не получила в PP-анализах значительно меньше пациентов с низким риском по сравнению с группой A, может быть связан с большим количеством участков с PD ≥ 5 мм и участков с PD ≥ 6 мм на исходном уровне, даже если эта разница не достигли статистической значимости. Эти значения сопоставимы со значениями, полученными в исследованиях, исследующих этот параметр: Feres et al.через 12 месяцев (плацебо: 22,5%, AMX + MET: 66,7%), Harks et al. через 27,5 месяцев (плацебо 36,5%, AMX + MET: 63,1%) [27, 81].
В настоящем исследовании у курильщиков в течение 12 месяцев наблюдалось статистически значимо меньшее клиническое улучшение по сравнению с некурящими, и это наблюдалось для большинства оцениваемых параметров (таблица 2). Это согласуется с данными других исследований, оценивающих безоперационное лечение пародонта, которые показали значительно более низкие клинические улучшения у курильщиков [15, 90–92].Более того, это отражено в результатах регрессионного анализа Пуассона (Таблица 4), где курение вместе с антибиотиками (как 3-, так и 7-дневный режим антибиотиков), женский пол, BOP на исходном уровне и через 12 месяцев, начальное маргинальное кровотечение десен ( GBI) и исходная CAL статистически влияли на остаточное количество участков с PD ≥ 6 мм через 12 месяцев. Это согласуется с данными других исследований, в которых лечение антибиотиками оказалось единственной переменной, которая существенно повлияла на клинический результат [19, 27].
Тенденция к лучшим клиническим исходам после 7 дней AMX и MET, наблюдаемая через 6 месяцев [11], сохранялась через 12 месяцев. Как упоминалось ранее и в нашей предыдущей публикации, мы оценили исследование с 30 участниками в каждой группе лечения, чтобы выявить разницу в 5 участков с PD ≥ 6 мм [19, 27, 64] для мощности 90% (уровень значимости 0,05 ). Поскольку настоящее исследование было разработано как испытание превосходства двух протоколов антибиотиков над только механической обработкой раны, нельзя исключать, что прямое сравнение между 3- и 7-дневным протоколом может быть недостаточно эффективным, и поэтому это сравнение должно быть интерпретируется с осторожностью.Таким образом, на основании настоящих результатов нельзя сделать никаких выводов относительно прямого сравнения 3- и 7-дневного протокола приема антибиотиков. Очевидно, что для адекватного решения этой важной проблемы необходимо провести будущие проспективные рандомизированные контролируемые клинические исследования с соответствующим дизайном и с участием достаточного количества пациентов.
Ограничение настоящего исследования представляет собой высокий коэффициент отсева ниже 30 (согласно первоначальному расчету мощности исследования), рекомендующий тщательную интерпретацию настоящих результатов.Высокий процент отсева во всех 3 группах был связан с тем фактом, что несколько пациентов либо пропустили свои контрольные визиты, либо принимали антибиотики в течение периода наблюдения по другим медицинским причинам, либо подвергались дальнейшему хирургическому лечению (например, дентальные имплантаты) своими пациентами. направление стоматологов. Вывод о том, что через 12 месяцев исследование не смогло выявить статистически значимых различий для основной переменной результата между любой из групп лечения, может, с одной стороны, быть связано с высоким уровнем отсева, что привело к низкой мощности исследования через 12 месяцев. .Однако, с другой стороны, широкие диапазоны стандартного отклонения количества глубоких участков (PD ≥ 6 мм) на исходном уровне также могли повлиять на результаты. Тем не менее, следует отметить, что большинство исследованных переменных выявили статистически значимые клинические улучшения (Таблица 2) в обеих группах антибиотиков по сравнению с группой плацебо, но эти результаты необходимо тщательно интерпретировать как вторичные исходы.
В заключение, настоящее исследование показало, что: а) у пациентов с тяжелым хроническим пародонтитом нехирургическая пародонтальная терапия в сочетании с трех- или семидневным системным введением амоксициллина (AMX) и метронидазола (MET) дает статистически значимые клинические улучшения. по сравнению с безоперационной терапией.
Дополнительная информация
S1 Таблица. ITT-анализ: средние значения и сравнения групп (ANCOVA с поправкой на исходные значения и курение) и их изменения (Δ) между исходным уровнем и 12 месяцами (среднее ± стандартное отклонение).
ITT = намерение лечить, PD = глубина кармана, CAL = клинический уровень прикрепления, BOP = кровотечение при зондировании; FMPS = оценка налета на всю полость рта по О’Лири [66], м: месяцы, основание: исходный уровень. s статистически значимых p значений.
https: // doi.org / 10.1371 / journal.pone.0179592.s001
(DOCX)
Благодарности
Авторы хотели бы поблагодарить медсестер-исследователей Ливию Индолеан и Эрику Батиз за ввод данных и проверку ошибок.
Ссылки
- 1. Сокранский СС, Хаффаджи А.Д. Бактериальная этиология деструктивных заболеваний пародонта: современные концепции. J Periodontol. 1992; 63: 322–31. pmid: 1573546
- 2. Момбелли А., Гмур Р., Гобби С., Ланг Н.П. Actinobacillus actinomycetemcomitans при пародонтите у взрослых.I. Топографическое распределение до и после лечения. Журнал пародонтологии. 1994; 65: 820–6. pmid: 79
- 3. Момбелли А., Шмид Б., Рутар А., Ланг Н.П. Паттерны персистенции Porphyromonas gingivalis, Prevotella intermedia / nigrescens и Actinobacillus actinomyetemcomitans после механической терапии пародонтоза. J Periodontol. 2000. 71: 14–21. pmid: 10695934
- 4. Renvert S, Wikstrom M, Dahlen G, Slots J, Egelberg J. Влияние хирургической обработки корня на устранение Actinobacillus actinomycetemcomitans и Bacteroides gingivalis из пародонтальных карманов.Журнал клинической пародонтологии. 1990; 17: 345–50. pmid: 2204636
- 5. Дален Г., Викстром М., Ренверт С. Лечение заболеваний пародонта на основе микробиологической диагностики. 5-летнее наблюдение за индивидуальными паттернами. Журнал пародонтологии. 1996. 67: 879–87. pmid: 8884645
- 6. Гросси С.Г., Замбон Дж.Дж., Хо А.В., Кох Г., Данфорд Р.Г., Махтей Э.Е. и др. Оценка риска заболеваний пародонта. I. Индикаторы риска потери привязанности. Журнал пародонтологии.1994; 65: 260–7. pmid: 8164120
- 7. Хаффаджи А.Д., Сокранский СС. Микробные этиологические агенты деструктивных заболеваний пародонта. Пародонтология 2000. 1994; 5: 78–111. pmid: 9673164
- 8. Карвалью Л.Х., Д’Авила Г.Б., Леао А., Гонсалвес С., Хаффаджи А.Д., Сокрански С.С. и др. Снятие зубного камня и выравнивание корня, системное применение метронидазола и профессиональное удаление зубного налета при лечении хронического пародонтита у населения Бразилии II — микробиологические результаты. Журнал клинической пародонтологии.2005; 32: 406–11. pmid: 15811059
- 9. Cugini MA, Haffajee AD, Smith C, Kent RL Jr., Socransky SS. Влияние удаления зубного камня и выравнивания корня на клинико-микробиологические параметры заболеваний пародонта: результаты за 12 месяцев. Журнал клинической пародонтологии. 2000. 27: 30–6. pmid: 10674959
- 10. Keestra JA, Grosjean I., Coucke W, Quirynen M, Teughels W. Нехирургическая пародонтальная терапия системными антибиотиками у пациентов с нелеченым хроническим пародонтитом: систематический обзор и метаанализ.J Periodontal Res. 2015; 50: 294–314. pmid: 25142259
- 11. Cosgarea R, Juncar R, Heumann C, Tristiu R, Lascu L, Arweiler N, et al. Нехирургическое лечение пародонта в сочетании с 3-7-дневным системным введением амоксициллина и метронидазола у пациентов с тяжелым хроническим пародонтитом. Плацебо-контролируемое рандомизированное клиническое исследование. J Clin Periodontol. 2016; 43: 767–77. pmid: 27027501
- 12. Haffajee AD, Socransky SS, Gunsolley JC. Системная противоинфекционная пародонтальная терапия.Систематический обзор. Ann Periodontol. 2003. 8: 115–81. pmid: 14971252
- 13. Herrera D, Sanz M, Jepsen S, Needleman I, Roldan S. Систематический обзор эффекта системных противомикробных препаратов в качестве дополнения к масштабированию и выравниванию корней у пациентов с пародонтитом. J Clin Periodontol. 2002; 29 Дополнение 3: 136–59; обсуждение 60–2.
- 14. van Winkelhoff AJ, Abbas F, Pavicic MJ, de Graaff J. Хронический конъюнктивит, вызванный пероральными анаэробами, эффективно лечится системным метронидазолом плюс амоксициллин.Журнал клинической микробиологии. 1991; 29: 723–5. pmid: 18
- 15. Винкель Э.Г., Ван Винкельхофф А.Дж., Тиммерман М.Ф., Ван дер Фельден У., Ван дер Вейден Г.А. Амоксициллин плюс метронидазол в лечении взрослых пациентов с пародонтитом. Двойное слепое плацебо-контролируемое исследование. J Clin Periodontol. 2001. 28: 296–305. pmid: 11314884
- 16. Rooney J, Wade WG, Sprague SV, Newcombe RG, Addy M. Дополнительные эффекты к нехирургической пародонтальной терапии системного метронидазола и амоксициллина по отдельности и в комбинации.Плацебо-контролируемое исследование. J Clin Periodontol. 2002; 29: 342–50. pmid: 11966932
- 17. Матараццо Ф, Фигейредо Л.С., Круз С.Е., Фавери М., Ферес М. Клинические и микробиологические преимущества системного метронидазола и амоксициллина при лечении курильщиков с хроническим пародонтитом: рандомизированное плацебо-контролируемое исследование. J Clin Periodontol. 2008. 35: 885–96. pmid: 18727657
- 18. Герреро А., Гриффитс Г.С., Нибали Л., Суван Дж., Молес Д.Р., Лорелл Л. и др. Дополнительные преимущества системного амоксициллина и метронидазола при нехирургическом лечении генерализованного агрессивного пародонтита: рандомизированное плацебо-контролируемое клиническое исследование.J Clin Periodontol. 2005. 32: 1096–107. pmid: 16174275
- 19. Cionca N, Giannopoulou C, Ugolotti G, Mombelli A. Амоксициллин и метронидазол в качестве дополнения к полному удалению зубного камня и полировке корней хронического пародонтита. J Periodontol. 2009; 80: 364–71. pmid: 19254119
- 20. Cionca N, Giannopoulou C, Ugolotti G, Mombelli A. Микробиологические испытания и результаты чистки рта и выравнивания корня с амоксициллином / метронидазолом или без него при хроническом пародонтите.Журнал пародонтологии. 2010; 81: 15–23. pmid: 20059413
- 21. Рибейро Эдель П., Биттенкур С., Занин И.К., Бови Амброзано Г.М., Саллум Е.А., Носити Ф.Х. и др. Ультразвуковая санация всего рта, связанная с амоксициллином и метронидазолом в лечении тяжелого хронического пародонтита. Журнал пародонтологии. 2009. 80: 1254–64. pmid: 19656025
- 22. Гриффитс Г.С., Айоб Р., Герреро А., Нибали Л., Суван Дж., Молес Д. Р. и др. Амоксициллин и метронидазол в качестве дополнительного лечения генерализованного агрессивного пародонтита при начальной терапии или повторном лечении: рандомизированное контролируемое клиническое исследование.J Clin Periodontol. 2011; 38: 43–9. pmid: 21062335
- 23. Хеллер Д., Варела В.М., Сильва-Сенем М.С., Торрес М.С., Ферес-Филхо Е.Дж., Коломбо А.П. Влияние системных противомикробных препаратов в сочетании с антиинфекционной механической обработкой раны на микробиоту генерализованного агрессивного пародонтита: 6-месячное рандомизированное контролируемое исследование. Журнал клинической пародонтологии. 2011; 38: 355–64. pmid: 21303403
- 24. Местник М.Дж., Ферес М., Фигейредо Л.К., Соарес Дж., Телес Р.П., Фермиано Д. и др. Эффекты дополнительного приема метронидазола и амоксициллина при лечении генерализованного агрессивного пародонтита: годичное двойное слепое плацебо-контролируемое рандомизированное клиническое исследование.Журнал клинической пародонтологии. 2012; 39: 955–61. pmid: 22882646
- 25. Mestnik MJ, Feres M, Figueiredo LC, Duarte PM, Lira EA, Faveri M. Краткосрочные преимущества дополнительного использования метронидазола плюс амоксициллин в микробном профиле и клинических параметрах субъектов с генерализованным агрессивным пародонтитом. Журнал клинической пародонтологии. 2010; 37: 353–65. pmid: 20447259
- 26. Сильва М.П., Ферес М., Сиротто Т.А., Соарес Г.М., Мендес Дж. А., Фавери М. и др.Клинические и микробиологические преимущества одного метронидазола или амоксициллина в качестве дополнительных средств при лечении хронического пародонтита: рандомизированное плацебо-контролируемое клиническое исследование. J Clin Periodontol. 2011; 38: 828–37. pmid: 21762197
- 27. Ферес М., Соарес Г.М., Мендес Дж. А., Сильва М. П., Фавери М., Телес Р. и др. Метронидазол отдельно или с амоксициллином в качестве дополнения к нехирургическому лечению хронического пародонтита: годичное двойное слепое плацебо-контролируемое рандомизированное клиническое исследование.J Clin Periodontol. 2012; 39: 1149–58. pmid: 23016867
- 28. Варела В.М., Хеллер Д., Сильва-Сенем М.С., Торрес М.С., Коломбо А.П., Ферес-Филхо Э.Дж. Системные противомикробные препараты в дополнение к повторной механической и антисептической терапии агрессивного пародонтита: 6-месячное рандомизированное контролируемое исследование. Журнал пародонтологии. 2011; 82: 1121–30. pmid: 21235333
- 29. Yek EC, Cintan S, Topcuoglu N, Kulekci G, Issever H, Kantarci A. Эффективность комбинации амоксициллина и метронидазола для лечения генерализованного агрессивного пародонтита.J Periodontol. 2010; 81: 964–74. pmid: 20214441
- 30. Goutoudi P, Diza E, Arvanitidou M. Влияние пародонтальной терапии на уровни интерлейкина-1бета и интерлейкина-10 в трещинной жидкости при хроническом пародонтите. Журнал стоматологии. 2004; 32: 511–20. pmid: 15304296
- 31. де Лима Оливейра А.П., де Фавери М., Гурски Л.С., Местник М.Дж., Ферес М., Хаффаджи А.Д. и др. Влияние пародонтальной терапии на цитокины GCF у пациентов с генерализованным агрессивным пародонтитом. Журнал клинической пародонтологии.2012; 39: 295–302. pmid: 22126282
- 32. Эмке Б., Мотер А., Бейклер Т., Милиан Э., Флеммиг Т.Ф. Дополнительная антимикробная терапия пародонтита: долгосрочное влияние на прогрессирование заболевания и колонизацию полости рта. J Periodontol. 2005. 76: 749–59. pmid: 15898936
- 33. Флеммиг Т.Ф., Милиан Э., Карч Х., Клайбер Б. Дифференциальный клинический результат лечения после системного применения метронидазола и амоксициллина у пациентов, носящих Actinobacillus actinomycetemcomitans и / или Porphyromonas gingivalis.Журнал клинической пародонтологии. 1998. 25: 380–7. pmid: 9650874
- 34. Родригес А.С., Лоренкао Д.С., Лима Нето Л.Г., Паннути С.М., Хирата Р.Д., Хирата М.Х. и др. Клиническая и микробиологическая оценка с помощью полимеразной цепной реакции в реальном времени безоперационного лечения агрессивного пародонтита, связанного с амоксициллином и метронидазолом. Журнал пародонтологии. 2012; 83: 744–52. pmid: 22060046
- 35. Шехаб Н, Патель ПР, Сринивасан А, Будниц Д. Посещение отделения неотложной помощи при нежелательных явлениях, связанных с приемом антибиотиков.Клинические инфекционные заболевания: официальное издание Общества инфекционных болезней Америки. 2008; 47: 735–43.
- 36. Уокер CB. Избранные противомикробные средства: механизмы действия, побочные эффекты и лекарственные взаимодействия. Пародонтология 2000. 1996; 10: 12–28. pmid: 9567935
- 37. Фогельман Б., Крейг В.А. Кинетика антимикробной активности. J Pediatr. 1986; 108: 835–40. pmid: 3701535
- 38. Лопес Н.Дж., Гамонал Дж. А., Мартинес Б. Повторное лечение пародонтита метронидазолом и амоксициллином.Последующее исследование. Журнал пародонтологии. 2000. 71: 79–89. pmid: 10695942
- 39. Loesche WJ, Grossman N, Giordano J. Метронидазол при пародонтите (IV). Влияние комплаенса пациента на параметры лечения. Журнал клинической пародонтологии. 1993; 20: 96–104. pmid: 8436638
- 40. Надь Э, Урбан Э, Север СЕ. Чувствительность к противомикробным препаратам изолятов группы Bacteroides fragilis в Европе: 20-летний опыт. Клиническая микробиология и инфекции: официальное издание Европейского общества клинической микробиологии и инфекционных заболеваний.2011; 17: 371–9.
- 41. Снидман Д.Р., Якобус Н.В., Макдермотт Л.А., Голан Й., Хехт Д.В., Гольдштейн Э.Дж. и др. Уроки, извлеченные из исследования анаэробов: историческая перспектива и обзор самых последних данных (2005–2007 гг.). Клинические инфекционные заболевания: официальное издание Общества инфекционных болезней Америки. 2010; 50 Приложение 1: S26–33.
- 42. Робертс С.А., Шор К.П., Павиур С.Д., Голландия Д., Моррис А.Дж.. Чувствительность к антимикробным препаратам анаэробных бактерий в Новой Зеландии: 1999–2003 гг.Журнал антимикробной химиотерапии. 2006; 57: 992–8. pmid: 16507560
- 43. Karlowsky JA, Walkty AJ, Adam HJ, Baxter MR, Hoban DJ, Жанель Г.Г. Распространенность устойчивости к противомикробным препаратам среди клинических изолятов группы Bacteroides fragilis в Канаде в 2010–2011 гг .: эпиднадзорное исследование CANWARD. Противомикробные средства и химиотерапия. 2012; 56: 1247–52. pmid: 22203594
- 44. Lassmann B, Gustafson DR, Wood CM, Rosenblatt JE. Повторное появление анаэробной бактериемии.Клинические инфекционные заболевания: официальное издание Общества инфекционных болезней Америки. 2007; 44: 895–900.
- 45. Ярмарка Р. Дж., Тор Ю. Антибиотики и устойчивость к бактериям в 21 веке. Perspect Medicin Chem. 2014; 6: 25–64. pmid: 25232278
- 46. Профилактика CfDCa. Угрозы устойчивости к антибиотикам в США, 2013 г. Доступно по адресу: http://www.cdc.gov/drugresistance/threat-report-2013/.
- 47. EuropeanMedicineAgency.Бактериальный вызов: время реагировать. Призыв сократить разрыв между бактериями с множественной лекарственной устойчивостью в ЕС и разработкой новых антибактериальных средств: Европейское агентство медицины; 2013. Доступно по адресу: http://ecdc.europa.eu/en/publications/Publications/0909_TER_The_Bacterial_Challenge_Time_to_React.pdf.
- 48. Профилактика. CfDCa. Всемирный день здоровья: информационный бюллетень для СМИ. 2013 г. Доступно по адресу: http://www.cdc.gov/media/release/2011/f0407_antimicrobialresistence.pdf.
- 49.Либерман Т.Д., Мишель Дж. Б., Айнгаран М., Поттер-Байно Дж., Ру Д., Дэвис М. Р. Мл. И др. Параллельная бактериальная эволюция у нескольких пациентов позволяет идентифицировать гены-кандидаты патогенности. Нат Жене. 2011; 43: 1275–80. pmid: 22081229
- 50. Musher DM, Dowell ME, Shortridge VD, Flamm RK, Jorgensen JH, Le Magueres P и др. Возникновение устойчивости к макролидам при лечении пневмококковой пневмонии. N Engl J Med. 2002; 346: 630–1. pmid: 11856810
- 51. Липсич М, Левин БР.Популяционная динамика антимикробной химиотерапии. Противомикробные средства и химиотерапия. 1997; 41: 363–73. pmid: 93
- 52. Barbosa TM, Levy SB. Влияние использования антибиотиков на развитие и устойчивость. Обновления лекарственной устойчивости: обзоры и комментарии по противомикробной и противоопухолевой химиотерапии. 2000; 3: 303–11.
- 53. Ферес М., Хаффаджи А.Д., Аллард К., Сом С., Гудсон Дж. М., Сокранский С.С. Устойчивость поддесневых видов к антибиотикам во время и после антибактериальной терапии.J Clin Periodontol. 2002; 29: 724–35. pmid: 123
- 54. Сеппала Х., Клаукка Т., Вуопио-Варкила Дж., Муотиала А., Хелениус Х., Лагер К. и др. Влияние изменений в потреблении макролидных антибиотиков на устойчивость к эритромицину стрептококков группы А в Финляндии. Финская исследовательская группа по устойчивости к противомикробным препаратам. Медицинский журнал Новой Англии. 1997. 337: 441–6. pmid: 9250845
- 55. Джоши Дж. Химиотерапия туберкулеза в 21 веке: назад к истокам.Легкая Индия. 2011; 28: 193–200. pmid: 21886955
- 56. Milo G, Katchman EA, Paul M, Christiaens T, Baerheim A, Leibovici L. Продолжительность антибактериального лечения неосложненной инфекции мочевыводящих путей у женщин. Кокрановская база данных Syst Rev.2005: CD004682. pmid: 15846726
- 57. Данбар Л.М., Вундеринк Р.Г., Хабиб М.П., Смит Л.Г., Тенненберг А.М., Хашаб М.М. и др. Короткий курс левофлоксацина в высоких дозах при внебольничной пневмонии: новая парадигма лечения. Clin Infect Dis.2003. 37: 752–60. pmid: 12955634
- 58. Частре Дж., Вольф М., Фагон Дж. Ю., Шевре С., Томас Ф., Вермерт Д. и др. Сравнение 8-дневной и 15-дневной антибактериальной терапии респираторно-ассоциированной пневмонии у взрослых: рандомизированное исследование. Джама. 2003; 290: 2588–98. pmid: 14625336
- 59. де Бур WA, ван Эттен RJ, Schade RW, Ouwehand ME, Schneeberger PM, van Unnik AJ, et al. Однодневная усиленная четырехкратная терапия лансопразолом для лечения инфекции Helicobacter pylori. Пищевая фармакология и терапия.1997; 11: 109–12.
- 60. Грин С.М., Ротрок С.Г. Однократное внутримышечное введение цефтриаксона при остром среднем отите у детей. Педиатрия. 1993; 91: 23–30. pmid: 8416502
- 61. Гуч В.М. 3-й, Блэр Э., Пуополо А., Пастер Р.З., Шварц Р.Х., Миллер Х.С. и др. Эффективность пятидневной терапии суспензией цефуроксима аксетила для лечения острого среднего отита. Журнал детских инфекционных болезней. 1996; 15: 157–64. pmid: 8822290
- 62. Barnett ED, Teele DW, Klein JO, Cabral HJ, Kharasch SJ.Сравнение цефтриаксона и триметоприм-сульфаметоксазола при остром среднем отите. Группа изучения среднего отита Большого Бостона. Педиатрия. 1997; 99: 23–8. pmid: 8989332
- 63. Шраг С.Дж., Пена С., Фернандес Дж., Санчес Дж., Гомес В., Перес Э. и др. Влияние короткого курса терапии высокими дозами амоксициллина на носительство резистентного пневмококка: рандомизированное исследование. ДЖАМА. 2001. 286: 49–56. pmid: 11434826
- 64. Matuliene G, Pjetursson BE, Salvi GE, Schmidlin K, Bragger U, Zwahlen M, et al.Влияние остаточных карманов на прогрессирование пародонтита и выпадение зубов: результаты после 11 лет лечения. J Clin Periodontol. 2008. 35: 685–95. pmid: 18549447
- 65. Армитаж GC. Разработка системы классификации заболеваний и состояний пародонта. Летопись пародонтологии / Американская академия пародонтологии. 1999; 4: 1–6.
- 66. О’Лири Т.Дж., Дрейк Р.Б., Нейлор Дж. Э. Запись контроля зубного налета. Журнал пародонтологии. 1972; 43: 38. pmid: 4500182
- 67.Ammenheuser MM, Hastings DA, Whorton EB Jr., Ward JB Jr. Частоты мутантных лимфоцитов hprt у курильщиков, некурящих и бывших курильщиков. Экологический и молекулярный мутагенез. 1997. 30: 131–8. pmid: 9329637
- 68. Айнамо Дж., Бэй И. Проблемы и предложения по регистрации гингивита и налета. Международный стоматологический журнал. 1975. 25: 229–35. pmid: 1058834
- 69. Ланг Н.П., Тонетти М.С. Оценка пародонтального риска (PRA) для пациентов, получающих поддерживающую пародонтологическую терапию (SPT).Здоровье полости рта Prev Dent. 2003; 1: 7–16. pmid: 15643744
- 70. van Winkelhoff AJ, Winkel EG, Vandenbroucke-Grauls CM. О дозировке антибиотиков в клинических исследованиях. J Clin Periodontol. 1999; 26: 764–6. pmid: 10589814
- 71. Goodson JM, Haffajee AD, Socransky SS, Kent R, Teles R, Hasturk H, et al. Контроль пародонтальных инфекций: рандомизированное контролируемое исследование I. Первичный результат: увеличение прикрепления и уменьшение глубины кармана на обработанных участках. J Clin Periodontol.2012; 39: 526–36. pmid: 22512461
- 72. Катчман Е.А., Майло Дж., Пол М., Кристиаенс Т., Баерхейм А., Лейбовичи Л. Трехдневная и более длительная антибиотикотерапия цистита у женщин: систематический обзор и метаанализ. Am J Med. 2005. 118: 1196–207. pmid: 16271900
- 73. Ardila CM, Гранада, MI, Guzman IC. Устойчивость к антибиотикам поддесневых видов у больных хроническим пародонтитом. J Periodontal Res. 2010. 45: 557–63. pmid: 20546113
- 74. Харамилло А., Арсе Р.М., Эррера Д., Бетанкур М., Ботеро Дж. Э., Контрерас А.Клинико-микробиологическая характеристика пародонтальных абсцессов. J Clin Periodontol. 2005; 32: 1213–8. pmid: 16268997
- 75. Кулик Е.М., Ленкейт К., Шено С., Мейер Дж. Антимикробная чувствительность пародонтопатогенных бактерий. J Antimicrob Chemother. 2008; 61: 1087–91. pmid: 18326855
- 76. Ольсвик Б., Хансен Б.Ф., Теновер Ф.К., Олсен И. Устойчивые к тетрациклину микроорганизмы, полученные от пациентов с рефрактерным заболеванием пародонта. J Clin Periodontol.1995; 22: 391–6. pmid: 7601921
- 77. van Winkelhoff AJ, Herrera D, Oteo A, Sanz M. Антимикробные профили пародонтальных патогенов, выделенных у пациентов с пародонтитом в Нидерландах и Испании. J Clin Periodontol. 2005; 32: 893–8. pmid: 15998275
- 78. van Winkelhoff AJ, Herrera Gonzales D, Winkel EG, Dellemijn-Kippuw N, Vandenbroucke-Grauls CM, Sanz M. Устойчивость к противомикробным препаратам поддесневой микрофлоры у пациентов с пародонтитом взрослых. Сравнение Нидерландов и Испании.J Clin Periodontol. 2000. 27: 79–86. pmid: 10703651
- 79. Уокер CB. Приобретение антибиотикорезистентности микрофлоры пародонта. Периодонтол 2000. 1996; 10: 79–88. pmid: 9567938
- 80. Эррера Д., Контрерас А., Гамонал Дж., Отео А., Харамилло А., Сильва Н. и др. Поддесневые микробные профили у пациентов с хроническим пародонтитом из Чили, Колумбии и Испании. J Clin Periodontol. 2008; 35: 106–13.
- 81. Харкс И., Кох Р., Эйкхольц П., Хоффманн Т., Ким Т.С., Кохер Т. и др.Влияют ли системные антибиотики на прогрессирование пародонтита? Клиническое рандомизированное исследование. J Clin Periodontol. 2015; 42: 832–42. pmid: 26250060
- 82. van Winkelhoff AJ, Rodenburg JP, Goene RJ, Abbas F, Winkel EG, de Graaff J. Метронидазол плюс амоксициллин в лечении пародонтита, связанного с Actinobacillus actinomycetemcomitans. J Clin Periodontol. 1989. 16: 128–31. pmid: 2921374
- 83. Альтамими С., Халил А., Халаиви К.А., Милнер Р., Пусик М.В., Аль-Осман М.А.Короткая по сравнению со стандартной длительностью антибактериальная терапия острого стрептококкового фарингита у детей. Кокрановская база данных Syst Rev.2009: CD004872. pmid: 1 43
- 84. Алтамими С., Халил А., Халаиви К.А., Милнер Р.А., Пусик М.В., Аль-Осман М.А. Краткосрочные антибиотики позднего поколения по сравнению с более длительным приемом пенициллина при остром стрептококковом фарингите у детей. Кокрановская база данных Syst Rev.2012: CD004872. pmid: 22895944
- 85. Майкл М., Ходсон Э.М., Крейг Дж. С., Мартин С., Мойер В. А..Краткосрочная и стандартная пероральная антибактериальная терапия острой инфекции мочевыводящих путей у детей. Кокрановская база данных Syst Rev.2003: CD003966. pmid: 12535494
- 86. Хедрик Т.Л., Эванс Х.Л., Смит Р.Л., Макеларни С.Т., Шульман А.С., Чонг Т.В. и др. Можем ли мы определить идеальную продолжительность антибактериальной терапии? Хирургическая инфекция (Larchmt). 2006; 7: 419–32.
- 87. Sawyer RG, Claridge JA, Nathens AB, Rotstein OD, Duane TM, Evans HL, et al. Испытание краткосрочного курса антимикробной терапии внутрибрюшной инфекции.N Engl J Med. 2015; 372: 1996–2005. pmid: 25992746
- 88. Лундгрен Д., Асклоу Б., Торстенссон Н., Харефельдт А.М. Показатели успешности пародонтологического лечения в зависимости от выбора критериев оценки. Представление лестницы критериев оценки для использования рентабельности. J Clin Periodontol. 2001; 28: 23–30. pmid: 11142663
- 89. Матулиене Г., Студер Р., Ланг Н.П., Шмидлин К., Пьетурссон Б.Е., Салви Г.Е. и др. Значение оценки пародонтального риска рецидива пародонтита и потери зубов.J Clin Periodontol. 2010; 37: 191–9. pmid: 20041980
- 90. Ван дер Вельден У., Варуфаки А., Хаттер Дж. У., Сюй Л., Тиммерман М. Ф., Ван Винкельхофф А. Дж. И др. Влияние курения и пародонтологического лечения на поддесневую микрофлору. Журнал клинической пародонтологии. 2003. 30: 603–10. pmid: 12834497
- 91. Hughes FJ, Syed M, Koshy B., Bostanci N, McKay IJ, Curtis MA, et al. Факторы прогноза в лечении генерализованного агрессивного пародонтита: II. Влияние курения на исходный результат.
