Быстропрогрессирующий пародонтит — лечение в Москве в клинике Бюро32
Одной из атипичных форм заболеваний десен является быстропрогрессирующий пародонтит. Заболевание поражает преимущественно молодых людей в возрасте от 20 до 35 лет, хотя встречается и у пожилых пациентов. Иногда диагностируется у детей и подростков. Его опасность – в быстром развитии за короткий промежуток времени. Только своевременное обращение к врачу позволит избежать потери зубов!
Симптомы быстропрогрессирующего пародонтита
На начальной стадии больной ощущает слабый дискомфорт. Десны краснеют и опухают, при надавливании болят. Иногда с этими проявлениями можно справиться самостоятельно, используя антибактериальные ополаскиватели и отвары трав. Но если воспаление не проходит, необходимо как можно быстрее обратиться к врачу, чтобы исключить быстропрогрессирующий пародонтит.
Его признаки:
- кровоточивость десен во время чистки зубов и приема пищи;
- неприятный запах изо рта;
- опухшие, красные и болезненные десны;
- скопление зубного камня, сукровицы и гноя в пародонтальных карманах;
- повышенная температура.

Если заболевание начинает сказываться на общем самочувствии, рекомендовано провести диагностику на наличие быстропрогрессирующего пародонтита.
В нашей клинике предоставляется услуга современного пародонтального обследования. Всесторонняя диагностика позволит проанализировать состояние челюстных костей и оценить степень поражения каждого зуба. Бывает, что зуб болит, но внешне выглядит целым, при этом ткани десны – на вид здоровые. В этом случае дополнительно проводится рентген.
ПАРОДОНТОЛОГИЯ
| Профессиональная гигиена зубов | 7 900 р. |
| Двухступенчатая профессиональная чистка | от 5 000 р. |
| Удаление налета с применением системы Air Flow | 3 000 р. |
| Кюретаж закрытый | от 2 000 р. |
| Кюретаж открытый | от 4 600 р. |
| Закрытие рецессии десны | от 17 500 р. |
| Лечение пародонтита препаратом Emdogain | 32 000 р. за три зуба. |
Профессиональное лечение быстропрогрессирующего пародонтита
Специалисты стоматологической клиники «Бюро 32» в Москве располагают современным оборудованием, в том числе ультразвуковой системой вектор и лазерной установкой. Полость рта очищается от патогенной микрофлоры, пародонтальные карманы обрабатываются до стерильного состояния. После этого в них закладываются противомикробные составы, возможно назначение дополнительной медикаментозной терапии.
Для лечения быстропрогрессирующего пародонтита в стоматологии понадобится несколько сеансов. Впоследствии необходимо производить контрольные обследования в течение, как минимум, года, чтобы предупредить повторные воспалительные изменения. При соблюдении гигиены зубы быстро перестанут шататься и укрепятся в деснах, а десны, в свою очередь, приобретут здоровый вид.
Цена лечения быстропрогрессирующего пародонтита зависит от тактики выбранной терапии и других факторов. Наш стоматолог озвучит стоимость услуг после диагностики и оценки объема предстоящих работ.
Только в тесном сотрудничестве с врачом возможно достижение гарантированного результата. Запишитесь на прием +7(495)945-05-55 и обсудите со специалистом перспективы и методы терапии быстропрогрессирующего пародонтита.
| ВРАЧИ Врачи всех направлений. Опыт работ каждого специалиста более 15 лет. Врачи клиник – обладатели международных дипломов и сертификатов. | ИНДИВИДУАЛЬНЫЙ ПОДХОД Для нас важен каждый пациент, поэтому в клинике «Бюро 32» мы сначала ищем причину возникшей проблемы, а потом решаем эту проблему самыми современными методами. |
| ВСЕ В ОДНОМ МЕСТЕ Весь комплекс лечения и профилактики – от компьютерной диагностики до сложных операций, проводится в стенах клиники. | ЛЕЧЕНИЕ ПО СИСТЕМЕ «ВСЕ ВКЛЮЧЕНО» В стоимость каждой процедуры в клинике включена диагностика, а цена не меняется в зависимости от количества промежуточных процедур и манипуляций. 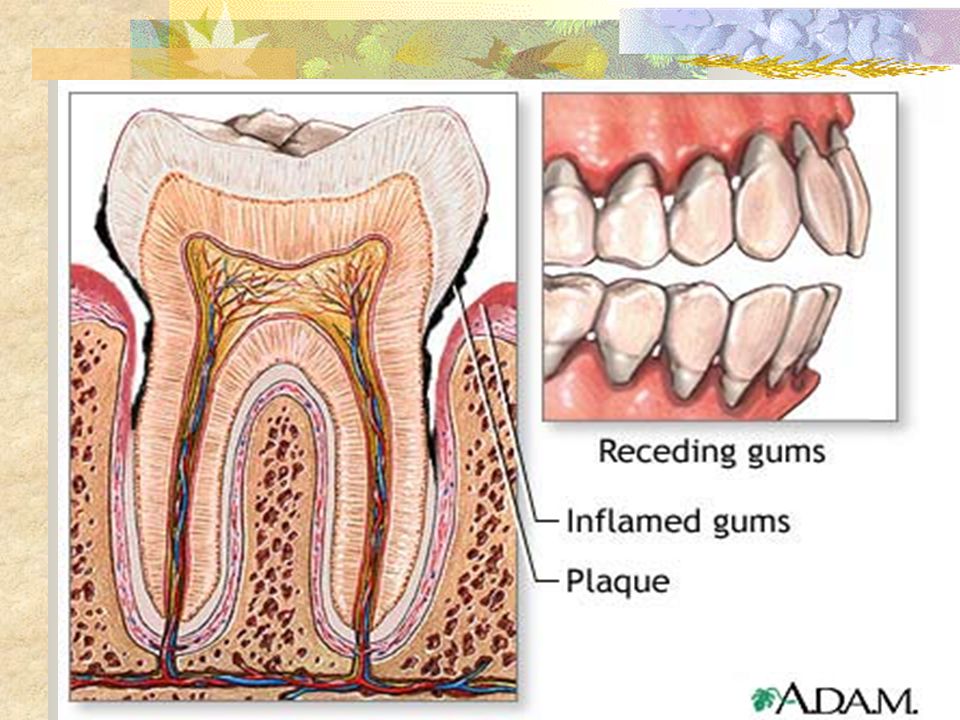 |
| ОБОРУДОВАНИЕ В клинике используется новейшее оборудование: дентальный микроскоп Karl Kaps, компьютерный томограф Sirona, цифровой рентген с визиографом, аппарат для отбеливания Zoom4. | РАСПОЛОЖЕНИЕ Нашу клинику легко найти: «Бюро 32» находится в центре Москвы рядом с метро Беговая. |
ДОПОСЛЕ
Комбинированное лечение. Костная пластика, закрытие рецессии десны и тотальное восстановление зубного ряда при помощи имплантатов и коронок из оксида циркония.
Прием ведут
ЧЕРНЯК ИОСИФ ИЗОЛЬДОВИЧ
Глава клиники «Бюро 32». Врач высшей категории, стоматолог-хирург, имплантолог, стоматолог-ортопед.
Записаться на прием
ПШЕНКО ПОЛИНА ДМИТРИЕВНА
Врач стоматолог-терапевт, микроскопист.
Записаться на прием
Отзывы
72. Пародонтит быстро прогрессирующий. Клиника, диагностика, дифференциальная диагностика, лечение.
Атипичность
БПП проявляется тем, что активное
разрушение тканей пародонта начинается
в молодом возрасте: с 17–20 лет, практически
не поддаётся лечению с помощью традиционных
средств и отличается крайне неблагоприятным
прогнозом.
Клиника: БПП отличается рядом признаков: деструктивные изменения в тканях пародонта начинаются в постювенильном или молодом возрасте; генерализованное разрушение костного субстрата при неадекватно умеренной в большинстве случаев воспалительной реакции в тканях пародонта; более тяжёлое поражение пародонта по сравнению с пациентами аналогичного возраста при сопоставимом скоплении зубного налёта; неэффективность либо незначительный и кратковременный эффект от проводимого ранее лечения. Первый симптом воспалительного заболевания пародонта (кровоточивость дёсен при чистке зубов) появляется у пациентов за 5–6 лет до явлений выраженной деструкции костной ткани. Обычно пациенты обращаются в клинику уже на поздних стадиях заболевания, связывая подвижность и перемещение зубов с началом болезни пародонта, поэтому нельзя с уверенностью утверждать, что предшествует заболеванию: либо банальный гингивит, либо ювенильный пародонтит.
Течение
заболевания волнообразное, с периодами
частых обострений (чаще 1 раза в 3 мес) и
коротких ремиссий. ДИАГНОСТИКА:
Диагноз
быстропрогрессирующего пародонтита
может быть поставлен на основании очень
тщательного анамнеза и данных клинического
обследования, рентгенологического, а
при возможности — микробиологического
и иммунологического исследований. Для
БПП характерны:
ДИАГНОСТИКА:
Диагноз
быстропрогрессирующего пародонтита
может быть поставлен на основании очень
тщательного анамнеза и данных клинического
обследования, рентгенологического, а
при возможности — микробиологического
и иммунологического исследований. Для
БПП характерны:
-начало заболевания от 18 до 35 лет;
-некоторые пациенты имеют в анамнезе ювенильный пародонтит;
-отсутствие параллелизма между активностью воспаления и глубиной деструктивных изменений в тканях пародонта;
-поражение пародонта имеет генерализованный характер.
-иногда заболевание сопровождается системными проявлениями, такими как понижение веса тела, депрессия и общее недомогание;
-при фазово-контрастной микроскопии в составе микрофлоры пародонтальных карманов пациентов с БПП отмечают преобладание подвижных и извитых форм факультативных анаэробов; у 80% пациентов и более микрофлора пародонтальных карманов устойчива к антибиотикам;
-при иммунологическом исследовании периферической крови пациентов с БПП выявляют нарушения в иммунном статусе, который в отличие от типичных форм пародонтита не претерпевает достоверных изменений в ходе лечения;
-при
рентгенологическом исследовании
(ортопантомография) определяют
генерализованное поражение костной
ткани альвеолярных отростков челюстей,
обширные очаги остеопороза с размытыми
нечёткими границами, что косвенно
свидетельствует об активности
воспалительно-деструктивного процесса.
В
отличие от БПП, юношеские и препубертатные
формы пародонтитов проявляются в более
раннем возрасте. При юношеском пародонтите
чаще всего поражается пародонт в области
резцов и первых моляров. Препубертатный
пародонтит следует дифференцировать
с воспалительными заболеваниями
пародонта, обусловленными такими
системными заболеваниями, как сахарный
диабет 1-го и 2-го типа, нарушения функции
щитовидной железы, заболевания крови
(лейкоз, агранулоцитоз, циклическая
нейтропения). Необходимо также
дифференцировать БПП с язвенным
пародонтитом при СПИДе. БПП дифференцируют
не только с приобретёнными тяжёлыми
патологиями, но и с врождёнными
заболеваниями: хроническая гранулёматозная
болезнь, дефицит лейкоцитарной адгезии,
недостаточность лейкоцитарных гранул,
болезнь Дауна, синдром Папийона–Лефевра
и др.
ЛЕЧЕНИЕ
При составлении плана лечения необходимо учитывать два ведущих причинных фактора: микробный и травматический.
Основные тактические подходы к лечению включают: мотивацию пациента к проведению оптимальной гигиены полости рта, поэтапное механическое инструментальное удаление над- и поддесневых зубных отложений с последующим кюретажем ПК, адекватную антибиотикотерапию, комплекс хирургических вмешательств; поддерживающее лечение.
К особенностям относят большую резистентность процесса к вмешательствам, а соответственно более длительное лечение при более скромных результатах. Кроме того, в силу вышеприведённых особенностей определение чувствительности микрофлоры к антибиотикам, определение функциональной активности нейтрофилов и консультация у специалистов общего профиля для пациентов с ББП обязательны.
Наиболее
весомый эффект при ББП обеспечивает
проведение хирургических вмешательств,
направленных на устранение карманов и
местных травматических факторов: мелкого
преддверия полости рта, патологии
прикрепления уздечек губ, тяжей слизистой
оболочки переходных складок.
Антибиотики следует выбирать на основании антибиотикограмм. При БПП — тетрациклин по 0,25 г
4 раза в день с нистатином по 500 000 ЕД (или разовом назначении флуконазола) на протяжении 14–21 дней (в зависимости от клинической динамики) или тинидазол (при отсутствии противопоказаний со стороны печени) по схеме: после приёма пищи по 1 таблетке через каждые 15 мин, всего 4 таблетки — 1 раз (!).на стадии обострения рекомендуют использовать АБ из группы макролидов: азитромицин по 500 мг 1 раз в день в течение 3–5 дней; рокситромицин по 150 мг 2 раза в день в течение 10 дней; для профилактики кандидоза — нистатин по 500 000 ЕД 2 раза в день или 1 таблетку флуконазола. применение таблетированных форм пробиотиков: бифидобактерии бифидум и лактобактерии ацидофильные — по 10 доз в день в течение 14 дней на активной фазе лечения; по 5 доз в день в течение 1 мес во время поддерживающего лечения.
Второй
этап лечения — хирургический. Он
отличается только более длительной
противовоспалительной подготовкой, но
именно проведение лоскутных операций,
описанных выше, наиболее существенно
влияет на количество патогенной
микрофлоры.
И до, и после хирургического вмешательства лицам с БПП целесообразно использовать методику подслизистого введения озонированного натрия хлорида (натрия хлорида изотонического раствора для инъекций 0,9%♠) с целью уменьшения воспалительных осложнений, снижения боли в послеоперационном периоде, а также исключения вероятности формирования грубых рубцов после френуло- и вестибулопластики.
Пациенты с ББП должны проходить курс поддерживающего лечения каждые 3 мес, т.е. 4 раза в год.
Систематическое наблюдение за пациентами и своевременное корригирующее лечение позволяют у лиц с ББП добиться достаточно ощутимых результатов.
К вопросу об этиологии и патогенезе быстропрогрессирующего пародонтита Текст научной статьи по специальности «Фундаментальная медицина»
ОБЗОР ЛИТЕРАТУРЫ
© КОЛЛЕКТИВ АВТОРОВ, 2012 УДК 616.314.17-002-039.36-02-092
Н. В. Булкина, А. П. Ведяева
к ВОПРОСУ ОБ этиологии и ПАТОГЕНЕЗЕ БЫСТРОПРОГРЕССИРУЮЩЕГО ПАРОДОНТИТА
Кафедра терапевтической стоматологии ГБОУ ВПО Саратовский ГМУ им. В. И. Разумовского Минздравсоцразвития России
В. И. Разумовского Минздравсоцразвития России
В последние годы участились заболевания пародонта, имеющие агрессивное, практически непрерывно рецидивирующее, течение. Профилактика и повышение эффективности комплексного лечения быстропрогрессирующего паро-донтита являются актуальными проблемами современной стоматологии. Большие трудности обусловлены широким распространением данной патологии и отсутствием единой концепции этиологии и патогенеза. Ключевые слова: быстропрогрессирующий пародонтит, иммунодефицит, аутоиммунная реакция
Bulkina N. V., Ved’aeva A.P.
TO THE QUESTION ABOUT THE ETIOLOGY AND PATHOGENESIS OF RAPIDLY PROGRESSIVE PERIODONTAL
In recent years, more frequent periodontal disease with an aggressive, almost constantly recurrent course. The problems of prevention, to increase the efficiency of complex treatment quickly periodontitis is actuol problems of modern dentistry. Great difficulties because of the prevalence of this pathology, the absence of a unified concept of the etiology and pathogenesis Key words: rapidly growing periodontitis, immunodeficiency, autoimmune reaction
В последние годы все чаще встречаются заболевания пародонта, имеющие агрессивное, практически непрерывно рецидивирующее течение [3, 5-8, 12, 15, 19, 28]. Проблемы профилактики и повышения эффективности комплексного лечения быстропрогрессиру-ющего пародонтита (БПП) представляют актуальную проблему современной стоматологии. Большие трудности обусловлены широкой распространенностью указанной патологии, отсутствием единой концепции этиологии и патогенеза [1, 5, 6].
Проблемы профилактики и повышения эффективности комплексного лечения быстропрогрессиру-ющего пародонтита (БПП) представляют актуальную проблему современной стоматологии. Большие трудности обусловлены широкой распространенностью указанной патологии, отсутствием единой концепции этиологии и патогенеза [1, 5, 6].
Атипичность указанной формы пародонтита проявляется в том, что активное разрушение опорных тканей зубов начинается в молодом возрасте. Заболевание сопровождается глубоким разрушением кости и периодонта, очень часто — обильным и стойким гноетечением и разрастанием грануляционной ткани в пародонтальных карманах, а с другой стороны — незначительным воспалением в мягких тканях. Практически не поддается лечению с помощью традиционных средств и в относительно короткий промежуток времени (5-7 лет) приводит к полной потере зубов, вследствие чего отличается крайне неблагоприятным прогнозом [1, 14, 16, 34].
Анализируя причины и механизмы агрессивного течения пародонтита, безусловно, необходимо учитывать современные научные представления о регулирующей роли иммунной системы в развитии патологических состояний. Эти процессы развиваются в сочетании со снижением иммунных механизмов защиты всех уровней, определяющих возможность раз-
Эти процессы развиваются в сочетании со снижением иммунных механизмов защиты всех уровней, определяющих возможность раз-
Ведяева Анна петровна — канд. мед. наук, ассистент каф., тел. 8(903)328-44-65, e-mail: [email protected]
вития воспалительных изменений, которые усугубляют друг друга по типу порочного круга [2, 5, 10].
Микробный фактор является определяющим в развитии быстропрогрессирующего пародонтита. По мнению ряда авторов, главными патогенными микроорганизмами, вызывающими заболевания па-родонта, и в частности БПП, являются Actinobacillus actinomycetemcomitans, Prevotella intermedia, Porphy-romonas gingivalis, Campylobacter rectalis, которые входят в состав зубной бляшки и отличаются наиболее высокой агрессивностью и способностью проникать в ткани пародонта [30, 32]. Эти микроорганизмы участвуют в формировании иммунного ответа организма на их внедрение в ткани пародонта, вызывая развитие аутоиммунного воспаления или иммунодефицитно-го состояния. Патогенные бактерии секретируют в тканевую среду большое число биологически активных веществ, в том числе ряд ферментов, например протеиназы, металлопротеазы, трипсиноподобный фермент и т.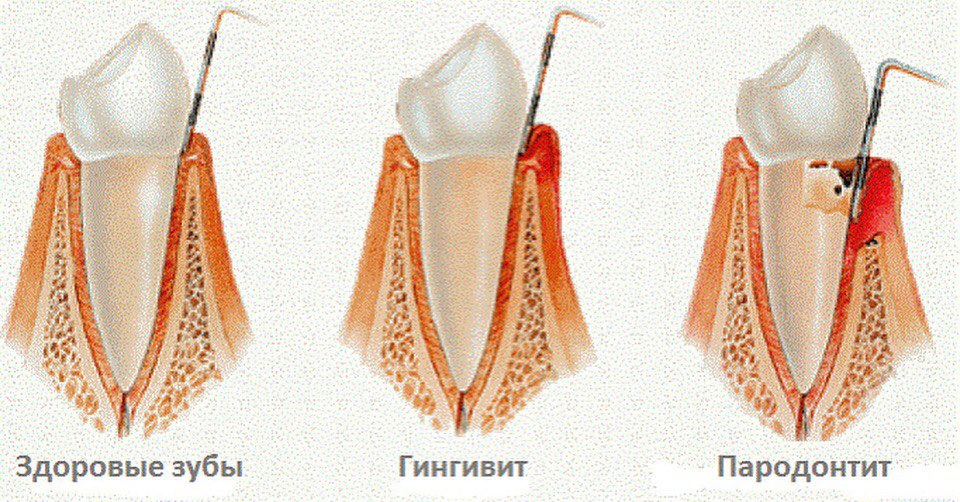 д. В частности, Porphyromonas gingivalis является продуцентом аргинин-1-протеазы, которая обладает способностью активировать гуморальное звено иммунной реакции. Установлена также способность Porphyromonas gingivalis продуцировать про-теиназы, вызывающие разрушение С5-компонента комплемента. Также патогенные микроорганизмы индуцируют образование комплекса провоспалитель-ных цитокинов, в частности IL-1, TNF-ß, PG-E2, IL-6, IL-8, обусловливающих развитие прогрессирующих деструктивных изменений в тканях пародонта [29, 30]. Так, под воздействием цитокинов меняются пропорции остеолитических и остеобластных ферментов, активируются остеокласты и металлопротеиназа остеоидной ткани [8].
д. В частности, Porphyromonas gingivalis является продуцентом аргинин-1-протеазы, которая обладает способностью активировать гуморальное звено иммунной реакции. Установлена также способность Porphyromonas gingivalis продуцировать про-теиназы, вызывающие разрушение С5-компонента комплемента. Также патогенные микроорганизмы индуцируют образование комплекса провоспалитель-ных цитокинов, в частности IL-1, TNF-ß, PG-E2, IL-6, IL-8, обусловливающих развитие прогрессирующих деструктивных изменений в тканях пародонта [29, 30]. Так, под воздействием цитокинов меняются пропорции остеолитических и остеобластных ферментов, активируются остеокласты и металлопротеиназа остеоидной ткани [8].
ОБЗОР ЛИТЕРАТУРЫ
В соответствии с данными литературы большая роль в этиологии и патогенезе БПП отводится формированию локального и системного иммунодефи-цитного состояния, во многом предопределяющего развитие воспалительных заболеваний пародонта [15, 17, 32]. В условиях хронического воспалительного процесса в пародонте происходит неизбежное повреждение эпителиального барьера, что в совокупности с микробной агрессией приводит к активации эпителиальных клеток. -6, TNF-a) и большого количества плазматических клеток на участках, поврежденных БПП, приводит к деструкции пародонта и альвеолярной кости [15]. Провоспалительные ци-токины вызывают повреждение сосудистой стенки и нарушение микроциркуляции, которые проявляются нарастанием числа спавшихся капилляров, пристеночным выпадением бесструктурных электронно-плотных масс, образованием тромбов, нарушением трофического транспорта через сосудистую стенку. Учитывая изложенные выше данные о системном характере воспалительного процесса, следует отметить, что при БПП активируются механизмы поражения сосудистой стенки, в том числе на уровне микроциркуляториого русла с последующим нарушением ее антитромбогенных свойств и функциональной активности эндотелиоцитов и тромбоцитов с последующим ухудшением клинической картины заболевания, стоматологического статуса, качества жизни пациентов [5].
-6, TNF-a) и большого количества плазматических клеток на участках, поврежденных БПП, приводит к деструкции пародонта и альвеолярной кости [15]. Провоспалительные ци-токины вызывают повреждение сосудистой стенки и нарушение микроциркуляции, которые проявляются нарастанием числа спавшихся капилляров, пристеночным выпадением бесструктурных электронно-плотных масс, образованием тромбов, нарушением трофического транспорта через сосудистую стенку. Учитывая изложенные выше данные о системном характере воспалительного процесса, следует отметить, что при БПП активируются механизмы поражения сосудистой стенки, в том числе на уровне микроциркуляториого русла с последующим нарушением ее антитромбогенных свойств и функциональной активности эндотелиоцитов и тромбоцитов с последующим ухудшением клинической картины заболевания, стоматологического статуса, качества жизни пациентов [5].
Между тем в большинстве клинико-экспе-риментальных работ делается акцент на недостаточность фагоцитарной активности полиморфно-ядерных лейкоцитов (ПМЯЛ), а также мононуклеа-ров, обеспечивающих первую линию защиты против инфекционных патогенных факторов и индукцию иммунного ответа при различных заболеваниях инфекционной и неинфекционной природы, в том числе при быстропрогрессирующем пародонтите [13, 22, 24]. При этом дефект функциональной активно-
При этом дефект функциональной активно-
сти ПМЯЛ носит системный характер и наблюдается у 75-83% пациентов с БПП, что свидетельствует о снижении неспецифической резистентности организма [23]. Нейтрофильные лейкоциты, обладающие большим деструктивным потенциалом, могут стать причиной повреждения тканей пародонта вследствие экзоцитоза радикалов кислорода и ферментов при остром воспалении или обострении хронического. Нейтрофилы также фагоцитируют микроорганизмы, разрушают иммунные комплексы и продукты тканевого распада. Стимулированные нейтрофильные лейкоциты служат источником медиаторов, которые влияют на активность других патогенетических звеньев воспаления, зачастую усугубляя его течение. У всех больных быстропрогрессирующим пародон-титом обнаружено глубокое угнетение всех звеньев фагоцитоза. В то же время установлено, что паро-донтопатоген, продуцируемый Р. gingivаlis, ингиби-рует трансэндотелиальную миграцию лейкоцитов и стимулирует активацию коллагеназ, продуцируемых ПМЯЛ [18, 27, 29]. В ряде исследований установлено, что чрезмерная активация ПМЯЛ в очагах поражения пародонта под влиянием провоспалительных цитокинов приводит к быстропрогрессирующей дезорганизации его тканей [35]. Респираторный «взрыв» в ПМЯЛ, возникающий при их адгезии на сосудистом эндотелии, определяет цитотоксичность ПМЯЛ в отношении окружающих тканей у пациентов с БПП [27, 31, 33]. При сравнительной оценке функциональной активности лейкоцитов установлено, что ПМЯЛ у больных БПП выделяют больше эластазы, чем у лиц с типичными формами воспалительных заболеваний пародонта.
В ряде исследований установлено, что чрезмерная активация ПМЯЛ в очагах поражения пародонта под влиянием провоспалительных цитокинов приводит к быстропрогрессирующей дезорганизации его тканей [35]. Респираторный «взрыв» в ПМЯЛ, возникающий при их адгезии на сосудистом эндотелии, определяет цитотоксичность ПМЯЛ в отношении окружающих тканей у пациентов с БПП [27, 31, 33]. При сравнительной оценке функциональной активности лейкоцитов установлено, что ПМЯЛ у больных БПП выделяют больше эластазы, чем у лиц с типичными формами воспалительных заболеваний пародонта.
В ряде работ отечественных и зарубежных авторов отмечена несостоятельность локальных и системных гуморальных факторов неспецифической резистентности, фагоцитоза, а также специфических иммунологических механизмов защиты, обеспечиваемых В- и Т-системами лимфоцитов [11, 20, 21, 29, 32]. При детальном изучении механизмов иммунитета выявлены угнетение Т-звена и стимуляция В-звена иммунитета, накопление токсичных цитокинов в десневой жидкости и в тканях пораженного пародонта. А в десневой жидкости и в тканях десны, коррелирующее с тяжестью клинических проявлений пародонтита [17, 26, 28, 32]. Результаты проведенных далее исследований подтвердили важную роль недостаточности гуморального и клеточного звена иммунитета в патогенезе быстропро-грессирующего пародонтита. Так, в периферической
А в десневой жидкости и в тканях десны, коррелирующее с тяжестью клинических проявлений пародонтита [17, 26, 28, 32]. Результаты проведенных далее исследований подтвердили важную роль недостаточности гуморального и клеточного звена иммунитета в патогенезе быстропро-грессирующего пародонтита. Так, в периферической
крови больных пародонтитом выявлено существенное снижение содержания Т-лимфоцитов, в частности Т-лимфоцитов-хелперов (CD4+-клетки), а также и цитотоксических лимфоцитов (CD8+-клетки). При этом содержание хелперных Т-лимфоцитов было снижено в 1,6 раза, а относительное количество цитотоксических Т-лимфоцитов — в 1,4 раза [27, 32]. Безусловно, снижение уровня CD4+-Т-хелперов в периферической крови является одним из патогенетических факторов подавления индукции иммунного ответа и вовлечения в иммунный ответ антиген-чувствительных клонов В- и Т-лимфоцитов. В то же время падение уровня CD8+-T-лимфоцитов в крови свидетельствует о системной недостаточности эфферентного звена клеточного иммунного ответа, обеспечивающего киллерный эффект [14, 22]. Однако данные о характере изменений уровня и активности CD8+-Т-лимфоцитов при БПП противоречивы. Так, в ряде работ отмечено, что выраженная деструкция тканей пародонта, наблюдаемая у пациентов с БПП, может объясняться высоким локальным цитотокси-ческим эффектом CD8+-клеток в ротовой полости [24, 25].
Однако данные о характере изменений уровня и активности CD8+-Т-лимфоцитов при БПП противоречивы. Так, в ряде работ отмечено, что выраженная деструкция тканей пародонта, наблюдаемая у пациентов с БПП, может объясняться высоким локальным цитотокси-ческим эффектом CD8+-клеток в ротовой полости [24, 25].
Многочисленные исследования подтвердили аутоиммунную природу повреждения и дезинтеграции функции тканей пародонта на фоне системной лимфоидно-клеточной сенсибилизации с функциональной несостоятельностью клеток мононуклеарно-фагоцитарной системы и сниженной общей реактивностью организма. Доказано появление в крови больных антигена, свойственного пародонту, и антител к нему. Продукты тканевой деструкции активируют процессы аутосенсибилизации и переключение функции заинтересованных иммунокомпетентных клеток на выработку провоспалительных, цитотоксических, вазопрессорных и других цитокинов, что ведет к хро-низации и прогрессированию процессов тканевой деструкции. Следует отметить, что более чем у 40% пациентов с БПП в крови обнаружены циркулирующие иммунные комплексы, которые, фиксируясь на базальной мембране сосудистой стенки и отслаивая эндотелий, могут служить индукторами развития эн-дотелиальной дисфункции, расстройств коагуляци-онного и сосудисто-тромбоцитарного звена системы гемостаза [1, 2, 11, 13].
Резюмируя приведенные выше данные в целом, следует отметить многокомпонентность механизмов развития быстропрогрессирующего пародон-тита, когда инициирующее действие бактериально-токсических факторов, безусловно, реализуется лишь на фоне недостаточности неспецифических механизмов резистентности и специфических иммунологических механизмов защиты.
ЛИТЕРАТУРА
1. Безрукова И. В. Быстропрогрессирующий пародонтит. Этиология. Клиника. Лечение: Дис. … д-ра мед. наук. — M., 2001.
2. Безрукова И. В., Грудянов А. И. Агрессивные формы паро-донтита. — M., 2003. — С. 11-66.
3. Булкина Н. В., Понукалина Е. В., Карпенко И. Н. // Арх. пат. -2009. — № 1. — С. 57-60.
4. Булкина Н. В., Ведяева А. П. Саратов. науч.-мед. журн. -2009. — № 2 (5). — С. 238-242.
5. Булкина Н. В., Ведяева А. П., Смирнову Д. А. // Mаэстро сто-матол. — 2011. — № 2. — С. 16-22.
6. Григорян А. С., Фролова О. А. // Стоматология. — 2006. — № 3. — С. 11-17.
7. Дмитриева Л. А. Современные аспекты клинической паро-донтологии. — M., 2001.
— M., 2001.
8. Иванов B. C. Заболевания пародонта. — 4-е изд. — M., 2001.
9. Киричук В. Ф., Симонян Т. В. // Рос. стоматол. журн. — 2008.
— № 3. — С. 48-50.
10. КолесоваН. А., Политун А. М., КолесоваН. В. И Соврем. стоматол. — 2006. — № 1. — С. 61-64.
11. КузникБ. И., Цыбиков Н. Н., ВитковскийЮ. А. И Тромбоз, гемостаз и реол. — 2005. — № 2 (22). — С. 3-16.
12. Ласкарис Д., Скалли К. Атлас по пародонтологии. Проявление местных и системных поражений — M., 2005. — С. 60-87.
13. Левин М. Я., Орехова Л. Ю. И Пародонтология. — 1996. — № 1. -С. 19-26.
14. Орехова Л. Ю. Иммунологические механизмы в патогенезе воспалительных заболеваний пародонта: Дис. … д-ра мед. наук. -СПб., 1997.
15. Орехова Л. Ю. Заболевания пародонта. — M., 2004.
16. Оспанова Г. Б., Овчинникова О. В., Богатырков Д. В. и др. / Клин. стоматол. — 2001. — № 1. — С. 52-56.
17. Плахтий Л. Я., Бекмурзова А. И., Валиева М. В. И Стоматолог. -2005. — № 5. — С. 41-44.
18. Феди П., Вернино А., Грей Д. Пародонтологическая азбука. — 2006.
19. Фролова Л. Б. И Казан. мед. журн. — 2010. — № 2. — С. 218-223.
20. Цепов Л. М., Николаев А. И., Михеева Е. А. И Пародонтология. -2004. — № 1 (30). — С. 3-7.
21. Шмагель К. В., Беляева О. В., Черешнев В. А. И Стоматология. -2003. — № 1. — С. 61-64.
22. Beck J. P., Ojfenbacker S. H Periodontology. — 2001. — Vol. 6, N 1. -P. 9-16.
23. Caruso F. Minerva Stomatol. — 1990. — Vol. 39, N 6. — P. 439-445.
24. CelenligilH. H Clin. Periodontal. — 1990. — Vol. 17, N 4. — P. 207-210.
25. Conde M. C., Pan S. H Dent. Res. — 2000. — Vol. 79. — P. 391.
26. Ebersole J. L., Cappely D. H Dent. Restavret. — 1995. — Vol. 74, N 5. — P. 658-666.
27. Gainet J. H Lab. Invest. — 1998. — Vol. 78, N 6. — P. 755-762.
28. HujfajeeA. D., Socransky S. S. H Periodontology. — 2000. — Vol. 5, N 1. — P. 78-161.
29. Kantarci A., Oyaizuk K., Van Duck T. E. H J. Periodontol. — 2003. -Vol. 74, N 1. — P. 66-75.
-Vol. 74, N 1. — P. 66-75.
30. Kornmann K. S., Newman M. G. H Periodontology. 2000. — Vol. 10.
— P. 18-23.
31. Macey M. G. H Cytometry. — 1998. — Vol. 34, N 3. — P. 152-158.
32. Renvert S., Wikatom M. H Clin. Periodontol. — 1996. — Vol. 23, N 5.
— P. 562-571.
33. TramontiniN. L., KuipersP. J., Huber C. M. et al. / Inflammation. -2002. — Vol. 26. — P. 311-319.
34. Vitkov L., Krautgarther W. D., Hanning M. H Oral Microbiol. Immunol. — 2005. — Vol. 20. — P. 317-327.
35. Yalsin S. H J. Periodontol. — 2001. — Vol. 72. — P. 411-416.
Поступила 03.07.12
хирургия
ЗАПИСЬ НА ПРИЕМ К ВРАЧУ
ЗАПИСЬ НА ПРИЕМ К ВРАЧУ
Ваша заявка успешно отправлена !
График работы: Пн.- Пт. 9.00-19.00
A- A A+
Лечение пародонтальных кармановОткрытый и закрытый кюретажПластика уздечек языка, верхней и нижней губыУглубление предверия полости ртаПрименение остеотропных препаратов для остеогенеза
- Пародонтология – раздел стоматологии, который изучает болезни десен и разрабатывает эффективные способы лечения десен.

Согласно последним исследованиям ВОЗ, более 90% населения старше 40 лет страдают серьёзным заболеванием — пародонтитом. Пародонтит «молодеет» и до 40 лет процент поражаемости не намного ниже.
- Основные признаки пародонтита:
Расшатанность зубов, Кровоточивость десен и запах изо рта, Изменение положения зубов, появление щелей между зубами,Болезненность при жевании, Вязкая слюна
- Ткань здоровых десен имеет светло-розовую окраску без каких-либо видимых невооруженным глазом «точек». Она не кровоточит при чистке зубов, при условии, что вы правильно чистите зубы и используете подходящую для этого зубную щетку. Воспаленная же ткань десен имеет темно-красную окраску и часто кровоточит при малейших прикосновениях к ней зубной щеткой. Если у вас часто бывает неприятный привкус во рту или неприятный запах, причиной этого могут быть зубные отложения и застрявшие в зубных промежутках или в зубодесневых карманах остатки пищи.
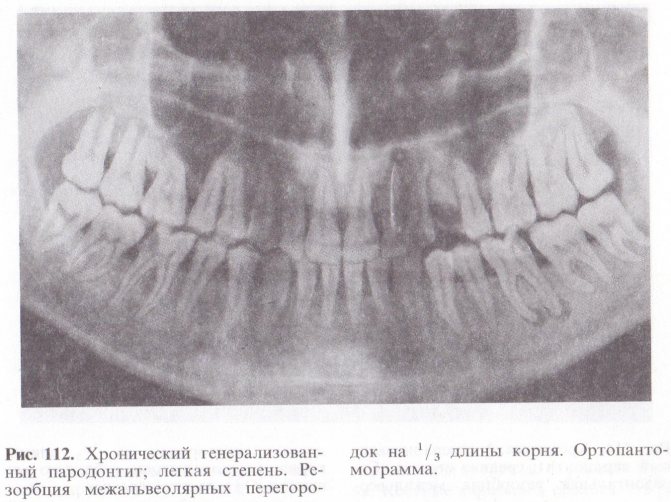
И то и другое часто приводит к пародонтиту. Также образование зубного камня способствует развитию язвы желудка. Кроме того, пародонтит может стать одной из причин преждевременных родов, образования сгустков крови и сердечнососудистых заболеваний. Заболевания пародонта повышают риск сердечного приступа в три раза, причем эта опасность с возрастом увеличивается.
- Без лечения процесс проникает глубже и разрушает пародонтальную связку, возникает пародонтальный карман в который, в свою очередь, откладывается налет и камень и стимулирует дальнейшее прогрессирование процесса. Пародонтальные ткани (окружающие зуб десна, костная ткань) разрушаются, и зуб начинает шататься, теряя костную опору в челюсти. На этом этапе может наблюдаться так же изменение положения зубов, появление щелей между ними.
Одной из разновидностей пародонтита является быстропрогрессирующий пародонтит. При нем выявляется мало зубного налета, но происходит быстрое и глубокое распространение воспалительного процесса в костной ткани с образованием очень глубоких карманов.
 Такое заболевание развивается быстро, в течение 1-5 лет. Одна из причин развития заболевания — определенные виды микроорганизмов. Глубина карманов может достигать 8-10 мм и более. Такое активное течение процесса приводит к ранней потере зубов. Лечение этого вида пародонтита необходимо начать сразу же после выявления заболевания.
Такое заболевание развивается быстро, в течение 1-5 лет. Одна из причин развития заболевания — определенные виды микроорганизмов. Глубина карманов может достигать 8-10 мм и более. Такое активное течение процесса приводит к ранней потере зубов. Лечение этого вида пародонтита необходимо начать сразу же после выявления заболевания. Быстропрогрессирующий пародонтит может развиваться у детей, подростков и у взрослых до 35 лет. У детей заболевание носит локальный характер и поражает, в основном, постоянные шестые зубы или центральные резцы. Образование зубного камня способствует развитию язвы желудка. Кроме того, пародонтит может стать одной из причин преждевременных родов, образования сгустков крови и сердечнососудистых заболеваний. Заболевания пародонта повышают риск сердечного приступа в три раза, причем эта опасность с возрастом увеличивается.
- Поскольку лечение пародонтита – процесс сложный и весьма дорогостоящий, то лучше предотвратить воспаление десен, чем заниматься его лечением.
 Что вызывает воспаление десен? Наиболее распространенная причина воспаления десен – зубной камень. Зубной камень – вот наш враг номер один! Если мы хотим избежать необходимости лечения десен, мы должны вовремя справиться с зубным камнем. Необходима регулярная профессиональная гигиена полости рта. Наша клиники предоставляют полный комплекс услуг по профессиональной гигиене полости рта, выполняемых на современном оборудовании.
Что вызывает воспаление десен? Наиболее распространенная причина воспаления десен – зубной камень. Зубной камень – вот наш враг номер один! Если мы хотим избежать необходимости лечения десен, мы должны вовремя справиться с зубным камнем. Необходима регулярная профессиональная гигиена полости рта. Наша клиники предоставляют полный комплекс услуг по профессиональной гигиене полости рта, выполняемых на современном оборудовании.
- Если же заболевание привело к значительной потери костных и мягких тканей, при пародонтологическом лечении приходиться прибегать к операции. Хирургическая пародонтология позволяет восстановить утраченную костную ткань, укрепить зуб и продлить срок его службы на десятки лет, что доказано нашими клиническими результатами. Этот метод пародонтологического лечения требует от врача очень высокой квалификации, профессиональных навыков и предполагает использование высоких технологий, а от пациента – доверие и желание достичь результата.
Адрес:
г. Оренбург, ул.Терешковой, д. 77/2,
Оренбург, ул.Терешковой, д. 77/2,
оф. 8 (ост.Автовокзал)
Скорая помощь (24×7)
Тел: 8(922) 836-34-61
Тел/факс: 8(3532) 56-09-69
График работы
Понедельник-Пятница с 9.00 до 19.00
Суббота,воскресенье — выходной
Агрессивные формы пародонтита: быстропрогрессирующий, маргинальный
Содержание
- Особенности заболевания
- Классификация
- Пародонтит маргинального характера
- Лечение
- Альтернативный метод
- Какие еще есть варианты лечения?
- Рекомендации
.
Содержание
Пародонтит — достаточно распространенное стоматологическое заболевание. Оно протекает в виде воспалительного процесса, локализующегося в пародонтальных тканях. Болезнь сопровождается прогрессирующей деструкцией кости и тканей периодонта, а также появлением пародонтальных карманов. Это достаточно серьезное заболевание зубов, которое проявляется в разных формах. Многие из них агрессивные и приводят к потере зубов.
Агрессивный пародонтит требует особого подхода в лечении. При появлении любых непривычных симптомов в ротовой полости, нужно сразу обращаться к врачу.
Агрессивный пародонит развивается очень быстро
Особенности заболевания
Агрессивные формы развиваются по причине усиленного размножения патогенной микрофлоры. Воспаления могут иметь определенные группы болезнетворных микроорганизмов. Болезнь может развиваться как у взрослых, так и у детей. Как правило, у детей пародонтоз развивается на одном или двух зубах, в то время как у взрослых он чаще всего глобальный.
Пародонтит, который активно прогрессирует, отличается от обычных форм определенными особенностями. К основным из них относятся:
- генерализованное поражение пародонта;
- чувство слабости и недомогание;
- снижение массы тела;
- состояние депрессии;
- ухудшение защитных функций иммунной системы;
- обширное поражение костной ткани.
Агрессивные пародонтиты являются формами пародонтита, при которых наблюдается стремительное и глубокое распространение воспаления в костной ткани. А также образуются глубокие карманы.
А также образуются глубокие карманы.
Агрессивная форма пародонтита у пациентки 22 лет
Как правило, заболевание достигает пика своего развития очень быстро. Это может происходить и за год. При других формах пародонтит может протекать и десять лет.
Из-за быстрого течения болезни, многие сталкиваются к ранней потере зубов. Очень важно вовремя начать лечение. Как правильно, такие агрессивные формы встречаются не так часто, как маргинальный пародонтит.
Классификация
Агрессивные формы болезни, представлены в нескольких видах.
- Пародонтит взрослых. Это хроническая форма заболевания, которая встречается в возрасте стершее 35 лет. Течение болезни медленное. Ее причина в активности грамотрицательных бактерий, костная ткань при такой патологии поражается как горизонтально, так и вертикально. Такая форма наиболее распространенная.
- Препубертатный. Возникает достаточно редко. Как правило, развивается в период после прорезывания коренных зубов.
 Патология может проявляться в двух формах. Первая протекает локально и поражает только отдельные зубы, а вторая генерализовано – весь зубной ряд.
Патология может проявляться в двух формах. Первая протекает локально и поражает только отдельные зубы, а вторая генерализовано – весь зубной ряд. - Ювениальный. Чаще всего, такая форма встречается у девушек в пубертатный период. Как правило, поражению подвержены моляры и резцы. Костная ткань разрушается без наличия выраженной симптоматики. Наличие налета незначительное. По мнению специалистов, это заболевание имеет наследственный характер. Иногда развитие нарушения вызвано неспецифическими анаэробными бактериями из грамотрицательной группы. Болезнь хорошо поддается лечению при приеме антибиотиков.
- Быстропрогрессирующий. Как правило, диагностируется у пациентов, которым менее 35 лет. Наблюдается разрушение альвеолярной кости и незначительное количество налета. Болезнь часто появляется у людей, которые больны сахарным диабетом и синдромом Дауна. Быстропрогрессирующий пародонтит бывает двух видов. К первому относится тип А, проявляющийся в возрасте 14-26 лет. Тип В диагностируется у пациентов, в возрасте 26-35 лет.
 Даже после тщательного лечения наблюдаются периоды обострения. Быстропрогрессирующий пародонтит — одна из самых сложных форм.
Даже после тщательного лечения наблюдаются периоды обострения. Быстропрогрессирующий пародонтит — одна из самых сложных форм. - Язвенно-некротический гингиво-пародонтит. Как показывает стоматологическая практика, данная форма заболевания развивается в результате недолеченного устраненного язвенно-некротического гингивита. Наблюдается усиленное поражение ткани пародонта и появление впадин между деснами и зубами.
- Рефрактеральный. Особенностью патологии является непрерывный процесс рецидивов. Даже после тщательного лечения, пародонтит возвращается и вызывает деструкцию костной ткани.
В классификации также выделяют пародонтит, который связан с болезнями системного характера. Он развивается уже на фоне имеющихся патологий.
Ювенальная форма агрессивного пародонтита
Пародонтит маргинального характера
Достаточно распространенной формой заболевания является маргинальный пародонтит. Он представлен в виде воспалительного процесса, который локализуется в связке зуба около зубного края. Маргинальный пародонтит может быть вызван травмированием края перидонта: когда что-то острое застрянет между зубом и десной. А также к причинам относятся:
Маргинальный пародонтит может быть вызван травмированием края перидонта: когда что-то острое застрянет между зубом и десной. А также к причинам относятся:
- травмирование в результате удара;
- неправильно выполненное пломбирование и протезирование;
- постоянное скопление пищи между зубами;
- регулярное травмирование края перидонта зубной нитью.
Маргинальный пародонтит сопровождается болезненными ощущениями к краям десны и ее покраснением. Как правило, он диагностируется при обращении пациентов с перечисленными жалобами.
Маргинальный пародонтит протекает в виде рецидивов, сменяющихся периодами затихания. Наблюдается повышенная деструкция пародонта.
Агрессивные формы являются очень серьезными и требуют тщательного лечения. Если пренебречь проведением терапии, потеря зубов неизбежна.
Агрессивный пародонтит может протекать бессимптомно и часто пациенты слишком поздно обращаются с уже развившимся заболеванием. Поэтому, нужно постоянно посещать консультации врача и следить за состоянием своих зубов.
Генерализованный пародонтит на рентген снимке
Лечение
Агрессивные пародонтиты лечатся достаточно долго. Очень часто используются антибиотики, так как большая часть форм патологии вызвана активностью патогенной микрофлоры. Первый этап лечения начинается с таких действий:
- чистка зубов;
- удаление налета;
- удаление зубных камней;
- полировка корней.
На протяжении двух дней выполняется кюретаж закрытого типа. В течении этого времени происходит полировка корня или его удаление. Для этого применяется ультразвуковой аппарат. Необходимость процедуры заключается в следующем: очистка придесенных карманов и уменьшение количества патогенной микрофлоры.
После того, как выполнен первый этап лечения, пациенты избавляются от чувства жжения и усиленной кровоточивости десен. Зубы становятся крепче.
Закрытый кюретаж убирает десневые карманы
После такой процедуры, может усилиться восприимчивость зубов к холодному. Это связано с тем, что вместе с налетом снимается и часть зубной эмали. Спустя 1-2 недели данный симптом проходит. Чтобы снизить чувствительность, можно воспользоваться специальными пастами. И также наблюдается оголение корней, которое связано с глубокими карманами в десне.
Это связано с тем, что вместе с налетом снимается и часть зубной эмали. Спустя 1-2 недели данный симптом проходит. Чтобы снизить чувствительность, можно воспользоваться специальными пастами. И также наблюдается оголение корней, которое связано с глубокими карманами в десне.
Альтернативный метод
Одним из вариантов лечения является шинирование. Оно применяется в тех случаях, когда зубы уже стали подвижными. С помощью специальной конструкции осуществляется закрепление зубов. Оно может быть как постоянным, так и временным. Агрессивный пародонтит требует длительной терапии.
После того как проходит полгода, начинается второй этап терапии. За это время, при незапущенной степени заболевания, устраняются небольшие пародонтальные каналы, а большие становятся меньше.
В тех случаях, когда глубина карманов находится в пределах 5 мм, требуется хирургическое вмешательство, так как другие методы уже не актуальны. Во время оперативного вмешательства выполняется завершающая очистка эмали. Убирается налет и зубные камни. Выполняется замена ткани зуба, разрушенной в результате воспалительного процесса.
Убирается налет и зубные камни. Выполняется замена ткани зуба, разрушенной в результате воспалительного процесса.
Как завершается?
Третий этап лечения носит поддерживающий характер. В этот момент необходимо обеспечить условия, при которых болезнетворные организмы не смогут вызвать воспалительный процесс и тем самым поспособствовать повторному развитию заболевания. Необходимо избегать рецидивов, так как болезнь будет протекать намного сложнее, как и процесс лечения.
Шинирование зубов — завершающая стадия лечения
На завершающем этапе терапии рекомендуется придерживаться таких профилактических мер:
- посещать стоматолога и проводить профилактическое лечение;
- каждый день чистить зубы;
- улучшать иммунитет полости рта, что позволит избежать размножения бактерий;
- проводить профессиональную чистку зубов в стоматологии.
При соблюдении всех рекомендаций, а также своевременному обращению к врачу, заболевание лечится и есть возможность сохранить зубы без их дальнейшей потери.
Какие еще есть варианты лечения?
Лечение агрессивных форм пародонтита должно быть комплексным. Необходимо не только устранить симптомы, но и обеспечить комплекс мер, которые будут направлены на общее укрепление организма, чтобы ускорить выздоровление. Может проводиться ортодонтическое лечение. Оно поможет устранить следующие проблемы:
- глубокий кариес, а также его осложнение;
- неправильное положение зубов и их отсутствие;
- деформированный прикус.
После решения этих проблем, процесс лечения становится намного эффективнее. В тех случаях, когда патология привела к потере зубов, требуется протезирование. Оно предусматривает выполнение таких действий:
- лечение десен в местах потери зубов;
- изготовление зубных протезов;
- установление протезов.
Протезы, как хороший вариант
Протезирование — длительный процесс. Протезы позволяют равномерно распределить нагрузку на зубы и обеспечить жевательную функцию. Они обеспечивают эстетический эффект. После полного устранения воспалительного процесса, выполняется протезирование постоянного характера. Изначально могут применяться временные, съемные протезы. Протезирование возможно только при таких условиях:
Они обеспечивают эстетический эффект. После полного устранения воспалительного процесса, выполняется протезирование постоянного характера. Изначально могут применяться временные, съемные протезы. Протезирование возможно только при таких условиях:
- отсутствие зубных камней и налета;
- полное устранение воспаления;
- соблюдение правил гигиены ротовой полости;
- глубина придесенных карманов должна быть не больше 4 мм;
- наличие плотной десны вокруг зуба;
- полностью вылеченный кариес;
- правильный прикус.
Если зубы очень подвижны, применяются элементы, которые будут их фиксировать. При повышенной нагрузке на протезы могут использоваться имплантаты, выступающие в качестве опоры.
Перед установкой имплантатов, нужно полностью вылечить воспаление. Выполняется тщательное обследование, чтобы исключить наличие противопоказаний. Дополнительно проводится терапия хронических заболеваний.
Имплантация зубов осуществляется при их потере
Как правило, имплантаты применяются в тех случаях, когда присутствует плохой прогноз. Если есть риск потери зуба, того его удаляют, но сохраняют костную ткань, которая расположена вокруг него.
Если есть риск потери зуба, того его удаляют, но сохраняют костную ткань, которая расположена вокруг него.
При установке имплантата может увеличиваться объем костной ткани, которая часто уменьшается при агрессивных формах пародонтита.
Рекомендации
Каким будет прогноз, зависит от того, какая форма заболевания у пациента и на каком этапе ее развития он обратился к специалисту. При запущенных формах пародонтита требуется протезирование или имплантация, так как сохранить свои зубы уже не удается.
Агрессивные формы пародонтита развиваются очень быстро, поэтому нужно обращаться к стоматологу как можно быстрее. Опасность болезни в том, что она негативно воздействует на весь организм. Полностью вылечить патологию можно только при соблюдении особых рекомендаций.
- Строгое соблюдение всех предписаний стоматолога.
- Проведение полного курса терапии. Нельзя прекращать лечение, так как болезнь будет продолжать прогрессировать, что приведет к различным осложнениям.

- Правильное проведение гигиены ротовой полости.
- Постоянное посещение врача и консультирование по лечению.
Агрессивные формы пародонтита, несмотря на их пугающее название, все же лечатся. Очень важно при появлении первых симптомов, нужно обратиться к стоматологу и провести лечение.
Заболевания пародонта и меры их профилактики | #04/01
Заболевания пародонта, так же как и кариес зубов, получили очень широкое распространение. По данным ВОЗ, около 95% взрослого населения планеты и 80% детей имеют те или иные признаки заболевания пародонта.
Что
же такое пародонт? Пародонт — это комплекс тканей, которые окружают зуб
и обеспечивают его фиксацию в челюстных костях. В этот комплекс
включают десну, периодонтальную связку, соединяющую корень зуба с
костной лункой, костную ткань альвеолярных отростков и цемент корня
зуба. При различных заболеваниях пародонта в патологический процесс
может вовлекаться какая-либо часть пародонтального комплекса либо весь
пародонт в целом. Характер патологического процесса также бывает
различным: дистрофический, воспалительный или опухолевый.
Характер патологического процесса также бывает
различным: дистрофический, воспалительный или опухолевый.
Среди всех заболеваний пародонта 90-95% приходится на воспалительные, такие как гингивит и пародонтит. Поэтому именно на них мы остановимся наиболее подробно.
Гингивит — это воспалительный процесс в тканях десневого края, при котором поражаются только поверхностные ткани десны.
Пародонтит — это воспалительный процесс, в который вовлекаются все структуры пародонта. Он характеризуется разрушением зубодесневого соединения и прогрессирующей деструкцией альвеолярных отростков челюстных костей.
Фактически гингивит и пародонтит — это две взаимосвязанные формы заболевания, поскольку воспалительный процесс возникает сначала в тканях десны, и постепенно в него вовлекаются подлежащие структуры пародонта: зубодесневая связка и альвеолярная кость.
В настоящее время
установлены основные местные патогенетические факторы, лежащие в основе
воспалительных заболеваний пародонта. Это скопление зубного налета
(микробный фактор), нарушение строения преддверия полости рта,
зубочелюстные аномалии и супраконтакты.
Это скопление зубного налета
(микробный фактор), нарушение строения преддверия полости рта,
зубочелюстные аномалии и супраконтакты.
Воспалительный процесс в тканях десны изначально возникает из-за массивных микробных скоплений и выделяемых ими ферментов и токсинов. Пока воспаление ограничивается только десной, а подлежащие ткани не затронуты, мы имеем дело с гингивитом, который протекает с периодами обострения и ремиссии, с различной степенью активности у разных пациентов.
| Рисунок 1. Хронический гингивит. |
Различие в характере течения гингивита определяется
состоянием защитных механизмов общего характера у пациентов. Именно
поэтому, при абсолютном признании микробного фактора в качестве
причинного, никогда не подвергалась сомнению «заинтересованность» всего
организма в развитии и течении этого, казалось бы, сугубо местного
процесса.
Какие жалобы предъявляют пациенты при гингивите?
Чаще всего это жалобы на кровоточивость десен.
Кровоточивость десен во время чистки зубов отмечают практически все пациенты с гингивитом. Могут быть жалобы также на боль и кровоточивость десен во время приема пищи. Общее состояние за редким исключением не нарушено.
При осмотре пациентов, как правило, определяется большое количество мягкого зубного налета, особенно в области шеек зубов. Десневой край обычно гиперемирован, отечен, десна легко кровоточит при зондировании.
Поскольку при гингивите воспалены только поверхностные, хорошо доступные для обзора и направленных лечебных вмешательств ткани, лечение этого заболевания очень эффективно.
Основным методом лечения и профилактики гингивита является удаление микробных скоплений, то есть гигиенические мероприятия.
Гигиенические
средства — пасты и зубные щетки — основное оружие против воспалительных
заболеваний пародонта. Более того, они одинаково эффективно действуют
как против воспаления в пародонте, так и против кариеса, так как
микробный фактор и в том и в другом случае является основным.
Более того, они одинаково эффективно действуют
как против воспаления в пародонте, так и против кариеса, так как
микробный фактор и в том и в другом случае является основным.
Однако,
несмотря на наличие столь действенного и доступного профилактического и
лечебного средства, проблема воспалительных заболеваний пародонта
остается очень актуальной. Уже в детском возрасте в 30-80% случаев
диагностируется начальная стадия заболевания в виде поверхностного
воспаления — гингивита, для течения которого характерно чередование
периодов интенсивной воспалительной реакции и относительно
благополучного состояния пародонта. С возрастом интенсивность и
распространенность воспалительной реакции в пародонте нарастает: у
подростков с гингивитом в 2-6% случаев отмечаются деструктивные
изменения в пародонте. Позже частота поверхностных воспалительных
изменений, проявляющихся в виде гингивита, уменьшается, и значительно
увеличивается распространенность более глубоких деструктивных явлений в
пародонте различных степеней тяжести.
| Рисунок 2. Хронический пародонтит. |
Проблема адекватного гигиенического ухода за полостью рта, привития необходимых гигиенических навыков детям крайне сложна. На сегодняшний день на отечественном рынке представлены гигиенические средства (пасты и щетки) довольно высокого качества. Вопрос в другом: чтобы добиться необходимой очистки зубов и десен, необходимо не менее 20 раз провести щеткой по одной поверхности зуба, общее время чистки зубов — с наружной и внутренней сторон — должно составлять не менее трех минут, иначе микробная бляшка сохраняется. Кроме того нужно обязательно обрабатывать межзубные промежутки с помощью флоссов (зубных нитей). К этому необходимо приучать детей с самого раннего возраста, чтобы сформировать у них потребность в такой чистке зубов не менее двух раз в день.
Пока ребенок не будет
устойчиво мотивирован к такого рода уходу, трудно ожидать ощутимых
результатов в отношении состояния десен и зубов. Следует помнить, что
качество очистки зубов в большей степени зависит от индивидуальных
мануальных навыков. Многие дети при всем желании просто не могут хорошо
вычистить зубы, даже если очень стараются. Сказанное впрямую относится
к детям с нарушениями общего развития.
Следует помнить, что
качество очистки зубов в большей степени зависит от индивидуальных
мануальных навыков. Многие дети при всем желании просто не могут хорошо
вычистить зубы, даже если очень стараются. Сказанное впрямую относится
к детям с нарушениями общего развития.
Какой же из этой ситуации
может быть выход? Врач должен регулярно проводить соответствующую
обработку или назначать препараты, эффективно подавляющие активность
микроорганизмов и замедляющие формирование микробных скоплений. В этих
целях на сегодня наиболее эффективен препарат хлоргексидина биглюконат,
резко ингибирующий жизнедеятельность всех микробных скоплений, которые
вызывают повреждение тканей пародонта и твердых тканей зуба. Кроме
того, он активно подавляет вирусы герпеса, грибов, оказывает слабый
обезболивающий эффект. Недостаток этого средства — устойчивый горький
вкус, что ограничивает применение данного препарата, особенно у детей. Недавно появившийся на нашем рынке препарат корсодил лишен указанного
недостатка. В силу этого он получил широкое распространение во многих
странах мира. Окрашивание поверхностей языка и пломб — свойство
хлоргексидина — явление временное, которое достаточно быстро проходит.
Зато эффект от применения хлоргексидина и в качестве лечебного, и в
качестве профилактического средства очень высок и стабилен. Пациенты
применяют препарат самостоятельно, курс лечения составляет 5-7 дней.
Недавно появившийся на нашем рынке препарат корсодил лишен указанного
недостатка. В силу этого он получил широкое распространение во многих
странах мира. Окрашивание поверхностей языка и пломб — свойство
хлоргексидина — явление временное, которое достаточно быстро проходит.
Зато эффект от применения хлоргексидина и в качестве лечебного, и в
качестве профилактического средства очень высок и стабилен. Пациенты
применяют препарат самостоятельно, курс лечения составляет 5-7 дней.
Как
только воспаление преодолевает основной барьер — зубодесенное
соединение, — оно устремляется в подлежащие ткани — на периодонт и
альвеолярную кость. Являясь логическим продолжением гингивита, эта
форма обретает абсолютно новые черты. Во-первых, формируется
пародонтальный карман, в котором микробные скопления оказываются
надежно скрыты и не удаляются во время чистки зубов. Во-вторых, в
глубине пародонтальных карманов активно размножаются наиболее
агрессивные микробные виды — анаэробы, спирохеты, повреждающий
потенциал которых чрезвычайно высок. В-третьих, из карманов и сами
микроорганизмы, и их ферменты и токсины с легкостью проникают в
подлежащие структуры, растворяя их. Как следствие, снижается
устойчивость зубов, они становятся подвижными, а механическая нагрузка
на зубы при жевании оказывается травматичной. Вследствие этой травмы
разрушение опорного аппарата зуба идет особенно быстро, что, в свою
очередь, еще больше способствует распространению микробных скоплений.
Формируется пародонтит.
В-третьих, из карманов и сами
микроорганизмы, и их ферменты и токсины с легкостью проникают в
подлежащие структуры, растворяя их. Как следствие, снижается
устойчивость зубов, они становятся подвижными, а механическая нагрузка
на зубы при жевании оказывается травматичной. Вследствие этой травмы
разрушение опорного аппарата зуба идет особенно быстро, что, в свою
очередь, еще больше способствует распространению микробных скоплений.
Формируется пародонтит.
| Рисунок 3. Быстропрогрессирующий пародонтит. |
Жалобы, которые обычно предъявляют пациенты, — подвижность зубов, кровоточивость десен, неприятный запах изо рта, веерообразное расхождение верхних фронтальных зубов, оголение шеек зубов.
При осмотре отмечается гиперемия десневого края, часто с цианотичным оттенком, десна неплотно прилегает к шейке зубов.
При зондировании определяются пародонтальные карманы различной глубины, в зависимости от степени тяжести процесса. Имеются над-и поддесневые зубные отложения. При выраженном процессе могут иметь место гнойные выделения из пародонтальных карманов и значительная подвижность зубов. Рентгенологически при пародонтите отмечается снижение высоты альвеолярного отростка за счет резорбции костной ткани межальвеолярных перегородок.
Лечение пародонтита направлено в первую очередь на
удаление микробных скоплений, зубного камня и грануляций из
пародонтальных карманов. При значительной глубине пародонтальных
карманов их тщательная обработка возможна только хирургическим путем. А
после проведения операции основная задача — не допустить вновь
активного проникновения микробных масс вглубь. Этого добиться уже
сложнее, но опять-таки главным методом профилактики в этом случае
является качественная контролируемая гигиена полости рта, назначение
эффективных антимикробных полосканий, среди которых корсодил сегодня
признан наиболее эффективным.
Есть ряд форм воспалительных заболеваний пародонта, отличающихся повышенной агрессивностью. Основное их отличие — в присутствии специфических микроорганизмов и их сочетаний.
Препубертатный пародонтит. Процесс возникает в детском возрасте, в него вовлекаются зубы постоянного и даже молочного прикуса. Раннее развитие и агрессивное течение обусловлено тем, что у таких пациентов имеются дефекты общей защиты — моноцитов и полиморфноядерных лейкоцитов. В таких случаях тактика специалистов сводится к более тщательному антимикробному контролю. Но результат может быть обеспечен только усилиями специалистов общего профиля — в случае, если удается устранить дефекты клеток крови с помощью направленного медикаментозного воздействия.
Очаговый ювенильный пародонтит.
При этой форме парадонтита происходит избирательное поражение опорного
аппарата первых постоянных зубов. Заболевание вызывается видом Actinobacillus Actinomycetes comitans.
В большинстве случаев возникает у детей, родители которых являются
носителями микроорганизма. Процесс протекает при минимальной
воспалительной реакции. Быстрое его распространение обусловлено тем,
что данный вид микроорганизмов обладает способностью подавлять
хемотаксис лейкоцитов, а антитела в таких условиях не успевают
образовываться. Поэтому последующие постоянные зубы повреждаются редко,
так как позднее успевают сформироваться и проявить свое защитное
действие специфические антитела. Лечение включает активную
антибиотикотерапию — на протяжении не менее 3 недель — в сочетании с
местными вмешательствами. Длительность и необходимость общей
антибиотикотерапии обусловлены тем, что микроорганизмы не только
населяют зубодесневую бороздку, а в последующем — пародонтальный
карман, но еще и проникают вглубь тканей и костных структур, где
достаточно стойко сохраняются.
Заболевание вызывается видом Actinobacillus Actinomycetes comitans.
В большинстве случаев возникает у детей, родители которых являются
носителями микроорганизма. Процесс протекает при минимальной
воспалительной реакции. Быстрое его распространение обусловлено тем,
что данный вид микроорганизмов обладает способностью подавлять
хемотаксис лейкоцитов, а антитела в таких условиях не успевают
образовываться. Поэтому последующие постоянные зубы повреждаются редко,
так как позднее успевают сформироваться и проявить свое защитное
действие специфические антитела. Лечение включает активную
антибиотикотерапию — на протяжении не менее 3 недель — в сочетании с
местными вмешательствами. Длительность и необходимость общей
антибиотикотерапии обусловлены тем, что микроорганизмы не только
населяют зубодесневую бороздку, а в последующем — пародонтальный
карман, но еще и проникают вглубь тканей и костных структур, где
достаточно стойко сохраняются.
Быстропрогрессирующий пародонтит, а также пародонтит, устойчивый к лечебным вмешательствам, — вызывается специфической микрофлорой: Porphyromonas gingivalis (ранее — бактериоиды) Actinobacillus Actinomycetes comitans и Prevotella intermedia. Причем обычно имеет место именно их сочетание. В этом случае указанные микроорганизмы проявляют резко положительное синергическое взаимовлияние, и микробный состав не только обусловливает резкое деструктивное влияние на ткани, но и подавляет эффект защитных клеток. Кроме того, характерна инвазия этих микроорганизмов вглубь тканей.
| Рисунок 4. Пародонтоз. |
Врачебная тактика состоит в тщательной механической
обработке пародонтальных карманов и интенсивной антимикробной терапии.
Эффективно местное применение метронидазола или тетрациклина внутрь. Лоскутные операции целесообразно проводить не ранее чем через 3-4
недели после начала антимикробной терапии, иначе — при сохранении
жизнеспособности перечисленных микроорганизмов — хирургическое лечение
окажется неэффективным. Хороший эффект после хирургического лечения
оказывает корсодил. Учитывая относительную местную ареактивность, самым
надежным критерием эффективности лечения является микробиологический
анализ содержимого пародонтальных карманов и тканевых биоптатов. Из
этого следует, что в ряде случаев лечение таких пациентов целесообразно
проводить только в специализированных учреждениях, имеющих необходимую
базу. И конечно же, никакое лечение не может оказаться результативным,
тем более когда речь идет об отдаленном прогнозе, если отсутствует
надлежащий уход за полостью рта.
Лоскутные операции целесообразно проводить не ранее чем через 3-4
недели после начала антимикробной терапии, иначе — при сохранении
жизнеспособности перечисленных микроорганизмов — хирургическое лечение
окажется неэффективным. Хороший эффект после хирургического лечения
оказывает корсодил. Учитывая относительную местную ареактивность, самым
надежным критерием эффективности лечения является микробиологический
анализ содержимого пародонтальных карманов и тканевых биоптатов. Из
этого следует, что в ряде случаев лечение таких пациентов целесообразно
проводить только в специализированных учреждениях, имеющих необходимую
базу. И конечно же, никакое лечение не может оказаться результативным,
тем более когда речь идет об отдаленном прогнозе, если отсутствует
надлежащий уход за полостью рта.
Одно из заболеваний, в основе
которых лежит дистрофический процесс, — пародонтоз. Пародонтоз
представляет собой атрофически-дистрофический процесс в тканях
пародонта. Это заболевание имеет довольно скудную симптоматику. Что же
приводит пациентов к врачу?
Это заболевание имеет довольно скудную симптоматику. Что же
приводит пациентов к врачу?
В основном это косметический дефект, выражающийся в том, что происходит обнажение корней зубов и увеличение их клинической коронки. Пациенты жалуются на то, что «десна оседает, а зубы становятся длинными», особенно это беспокоит их во фронтальном отделе. В ряде случаев больных беспокоит зуд в деснах, а также болевые ощущения со стороны обнаженных шеек зубов.
При осмотре чаще всего наблюдается равномерность атрофических проявлений в области всех зубов и вовлечение в процесс непосредственно зубных тканей — это выражается в наличии так называемых клиновидных дефектов. Данная патология отличается медленным течением и относительной асимптоматичностью.
Причина
этой патологии неясна, ее рассматривают либо как преждевременное
развитие инволюционных процессов, либо как проявление общих нарушений в
пародонте, то есть синдрома или симптома общих нарушений. Однако очень
конкретная и четко выраженная клиника позволяет выделять данную форму
заболевания.
Однако очень
конкретная и четко выраженная клиника позволяет выделять данную форму
заболевания.
Адекватного лечения пародонтоза не существует, поскольку не установлена причина заболевания. Врач проводит только симптоматическое лечение — устраняет повышенную чувствительность зубов, назначает массаж или аутомассаж десен с целью коррекции трофических нарушений, а также проводит пломбирование клиновидных дефектов. Стремясь пойти навстречу пожеланиям пациентов, некоторые хирурги проводят вестибулопластические операции. Однако этого делать не следует, поскольку эффект от таких вмешательств оказывается очень кратковременным.
Что на самом деле эффективно, так это применение
средств, устраняющих болевую чувствительность обнаженных щеек зубов.
Для этого используют фтор-лак, флюогель, порошок питьевой соды. В
настоящее время на рынке появилась паста сенсодин, которая успешно
снимает повышенную чувствительность зубов, и пациент может использовать
ее самостоятельно. Врач должен предупредить пациентов с таким
заболеванием о том, что им нельзя пользоваться жесткой щеткой и
проводить горизонтальные движения, чтобы не усиливать глубину
клиновидных дефектов.
Врач должен предупредить пациентов с таким
заболеванием о том, что им нельзя пользоваться жесткой щеткой и
проводить горизонтальные движения, чтобы не усиливать глубину
клиновидных дефектов.
Опухолевые и опухолеподобные поражения также относятся к числу заболеваний, которые трудно прогнозировать, так как они развиваются только у лиц, имеющих склонность к данному процессу. А толчком к началу развития процесса могут быть гормональные сдвиги, в частности накопление соматотропного гормона в периоды полового созревания или беременности, наличие хронического травматического фактора, предшествующее воспаление. Однако все это лишь дополнительные факторы риска, провоцирующие развитие подобных поражений у лиц, предрасположенных к данному процессу.
Меры лечения и
профилактики состоят в устранении травмы, воспаления и, при
необходимости, в хирургическом удалении разросшихся тканей (при
фиброматозе десен, гипертрофическом гингивите, эпулисе, межкорневой
гранулеме). В настоящее время появился еще один достаточно серьезный
фактор, провоцирующий развитие подобного рода патологии: использование
молодыми людьми анаболиков при занятиях культуризмом и
профессиональными силовыми видами спорта. Возможности врача здесь
скромны: разъяснение и совет.
В настоящее время появился еще один достаточно серьезный
фактор, провоцирующий развитие подобного рода патологии: использование
молодыми людьми анаболиков при занятиях культуризмом и
профессиональными силовыми видами спорта. Возможности врача здесь
скромны: разъяснение и совет.
Что реально приводит в таких случаях к положительному результату? Максимально тщательная гигиена полости рта, использование самими пациентами эффективных антисептических и антибактериальных полосканий после активного лечебного курса.
Быстропрогрессирующий пародонтит. Особое клиническое состояние
Отчеты о клинических случаях
. 1983 г., апрель; 54 (4): 197–209.
doi: 10.1902/jop.1983.54.4.197.
Р. К. Пейдж, Л. К. Альтман, Дж. Л. Эберсоул, Г. Э. Вандестин, У. Х. Дальберг, Б. Л. Уильямс, С. К. Остерберг
Уильямс, С. К. Остерберг
- PMID: 6574228
- DOI: 10.1902/jop.1983.54.4.197
Отчеты о клинических случаях
R C Page et al. J Пародонтол. 1983 Апрель
. 1983 г., апрель; 54 (4): 197–209.
doi: 10.1902/jop.1983.54.4.197.
Авторы
Р. К. Пейдж, Л. К. Альтман, Дж. Л. Эберсоул, Г. Э. Вандестин, В. Х. Дальберг, Б. Л. Уильямс, С. К. Остерберг
- PMID: 6574228
-
DOI:
10.
 1902/jop.1983.54.4.197
1902/jop.1983.54.4.197
Абстрактный
Мы сообщаем о рентгенографических, клинических, анамнестических и лабораторных наблюдениях за семью пациентами, отобранными для иллюстрации особенностей и характеристик быстро прогрессирующего пародонтита, с целью выделения этого заболевания в качестве отдельной клинической единицы. Эта форма пародонтита чаще всего встречается у молодых людей в возрасте от 20 до 20 лет, но может возникать и у лиц постпубертатного возраста примерно до 35 лет. Во время активной фазы ткани десны сильно воспалены, наблюдается кровоизлияние, разрастание маргинальной десны, экссудация. Разрушение происходит очень быстро, с потерей большей части альвеолярной кости в течение нескольких недель или месяцев. Эта фаза может сопровождаться общим недомоганием, похуданием и депрессией, хотя эти симптомы наблюдаются не у всех больных. Заболевание может прогрессировать без ремиссии до потери зубов или, наоборот, оно может стихнуть и затихнуть с терапией или без нее. Фаза покоя характеризуется наличием клинически нормальной десны, которая может плотно прилегать к корням зубов с выраженной потерей костной ткани и глубокими пародонтальными карманами. Фаза затишья может быть постоянной, она может сохраняться в течение неопределенного периода или активность болезни может вернуться. Большинство пациентов с быстро прогрессирующим пародонтитом имеют сывороточные антитела, специфичные для различных видов Bacteroides, Actinobacillus или обоих видов, и проявляются дефектами хемотаксиса нейтрофилов или моноцитов. Пораженные пациенты обычно положительно реагируют на лечение путем удаления зубного камня и открытого или закрытого выскабливания, особенно в сочетании со стандартными дозами антибиотиков в течение обычных периодов времени. Небольшое меньшинство пациентов не отвечает ни на какое лечение, включая антибиотики, и болезнь неумолимо прогрессирует до потери зубов даже при агрессивной пародонтологической терапии и поддерживающей терапии. В настоящее время до начала лечения невозможно определить, какие люди будут реагировать на терапию, а какие нет.
Фаза покоя характеризуется наличием клинически нормальной десны, которая может плотно прилегать к корням зубов с выраженной потерей костной ткани и глубокими пародонтальными карманами. Фаза затишья может быть постоянной, она может сохраняться в течение неопределенного периода или активность болезни может вернуться. Большинство пациентов с быстро прогрессирующим пародонтитом имеют сывороточные антитела, специфичные для различных видов Bacteroides, Actinobacillus или обоих видов, и проявляются дефектами хемотаксиса нейтрофилов или моноцитов. Пораженные пациенты обычно положительно реагируют на лечение путем удаления зубного камня и открытого или закрытого выскабливания, особенно в сочетании со стандартными дозами антибиотиков в течение обычных периодов времени. Небольшое меньшинство пациентов не отвечает ни на какое лечение, включая антибиотики, и болезнь неумолимо прогрессирует до потери зубов даже при агрессивной пародонтологической терапии и поддерживающей терапии. В настоящее время до начала лечения невозможно определить, какие люди будут реагировать на терапию, а какие нет.
Похожие статьи
-
Взаимосвязь межкорешковой ширины и потери альвеолярной кости. Радиометрическое исследование популяции пародонтита.
Хайнс П.Дж., Томас Р.Г., Ньютон Дж.В. Хайнс П.Дж. и соавт. J Пародонтол. 1988 г., февраль; 59 (2): 73–79. doi: 10.1902/jop.1988.59.2.73. J Пародонтол. 1988 год. PMID: 3162268
-
Потеря альвеолярной кости у пациентов с длительной поддерживающей терапией.
Layport CA, Greco GW, McFall WT Jr. Лейпорт, Калифорния, и др. J Пародонтол. 1990 июль; 61 (7): 434-7. doi: 10.1902/jop.1990.61.7.434. J Пародонтол. 1990. PMID: 2388140
-
Клинические, микробиологические и иммунологические исследования семьи с высокой распространенностью раннего пародонтита.

Vandesteen GE, Williams BL, Ebersole JL, Altman LC, Page RC. Vandesteen GE и соавт. J Пародонтол. 1984 март; 55(3):159-69. doi: 10.1902/jop.1984.55.3.159. J Пародонтол. 1984. PMID: 6584592
-
Болезни пародонта: обзор для врачей.
Фенеси К.Е. Фенеси К.Е. Гора Синай J Med. 1998 г., октябрь-ноябрь; 65 (5-6): 362-9. Гора Синай J Med. 1998. PMID: 9844364 Обзор.
-
Рентгенологическая интерпретация хронического пародонтита.
Hirschmann PN. Хиршманн ПН. Инт Дент Дж. 1987 март; 37(1):3-9. Инт Дент Дж. 1987. PMID: 3294597 Обзор.
Посмотреть все похожие статьи
Цитируется
-
Защита альвеолярной кости путем нацеливания на ось Sh4BP2-SYK в остеокластах.

Киттака М., Йошимото Т., Шлоссер С., Роттапель Р., Каджия М., Курихара Х., Рейхенбергер Э.Дж., Уэки Ю. Киттака М. и др. Джей Боун Шахтер Рез. 2020 фев; 35 (2): 382-395. дои: 10.1002/jbmr.3882. Epub 2019 24 октября. Джей Боун Шахтер Рез. 2020. PMID: 31613396 Бесплатная статья ЧВК.
-
Оценка фагоцитарной активности полиморфноядерных лейкоцитов у больных хроническим и агрессивным пародонтитом с помощью нитросинего тетразолия.
Гути Дж.Р., Шаширеха А., Гунтакала В.Р., Палапарти Р. Гути Дж. Р. и др. J Indian Soc Periodontol. 2019 июль-август; 23(4):316-321. doi: 10.4103/jisp.jisp_399_18. J Indian Soc Periodontol. 2019. PMID: 31367127 Бесплатная статья ЧВК.
-
Диморфная анемия и психическая депрессия как результат системных проявлений генерализованного агрессивного пародонтита: первый клинический случай.

Махаджан А., Аси К., Тхакур Н., Расила Д. Махаджан А. и др. J Indian Soc Periodontol. 2017 сен-октябрь;21(5):412-416. дои: 10.4103/jisp.jisp_248_16. J Indian Soc Periodontol. 2017. PMID: 294
Бесплатная статья ЧВК.
-
Результаты имплантационной терапии у пациентов с агрессивным пародонтитом в анамнезе. Систематический обзор и метаанализ.
Теодоридис К., Григориадис А., Менексес Г., Вурос И. Теодоридис С. и др. Clin Oral Investig. 2017 март; 21 (2): 485-503. doi: 10.1007/s00784-016-2026-6. Epub 2016 24 декабря. Clin Oral Investig. 2017. PMID: 28013438 Обзор.
-
Роль психотерапии в лечении генерализованного агрессивного пародонтита.
Приядаршини Д., Надиг П., Дешпанде Н.
 , Дешпанде А.
Приядаршини Д. и соавт.
BMJ Case Rep. 2014 г., 17 июля; 2014 г.: bcr2013200851. doi: 10.1136/bcr-2013-200851.
Представитель BMJ, 2014 г.
PMID: 25035440
Бесплатная статья ЧВК.
, Дешпанде А.
Приядаршини Д. и соавт.
BMJ Case Rep. 2014 г., 17 июля; 2014 г.: bcr2013200851. doi: 10.1136/bcr-2013-200851.
Представитель BMJ, 2014 г.
PMID: 25035440
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Грантовая поддержка
- DE-02600/DE/NIDCR NIH HHS/США
- DE-04881/DE/NIDCR NIH HHS/США
- DE-07063/DE/NIDCR NIH HHS/США
и т. д.
Стоматологическая практика Образовательная исследовательская группа
КЛАССИФИКАЦИЯ ЗАБОЛЕВАНИЙ ПАРОДОНА
|
Признание того, что заболевания, поражающие ткани пародонта, могут проявляться в различных формах, стало большим шагом вперед в нашем понимании природы и прогноза этих заболеваний за последнее десятилетие. |
C между разными странами не было достигнуто единодушие в отношении точной номенклатуры, которую следует использовать; тем не менее, в этом информационном листке представлен обзор того, как классифицировать заболевания пародонта, с целью помочь вам в регистрации соответствующего пародонтального диагноза в истории болезни каждого пациента.
G Ингивит – это воспалительное состояние тканей десны. Поражения гингивита можно классифицировать как:
Хронический маргинальный гингивит определяется как воспаление маргинальных тканей десны и характеризуется покраснением, отеком и кровоточивостью. По сути, это обратимое состояние. Хотя гингивит обычно предшествует формированию периодонтита, это никоим образом не является неизбежным следствием гингивита.
Острый язвенно-некротический гингивит (ANUG) представляет собой воспалительное деструктивное заболевание десен, чаще встречающееся у молодых людей, характеризующееся интерпроксимальными некротическими язвами, покрытыми остатками, болезненными при прикосновении и легко кровоточащими. ANUG, по-видимому, связана с плохим контролем зубного налета с уже существующим маргинальным гингивитом, курением и эмоциональным стрессом.
P эриодонтит — воспалительное заболевание пародонта, характеризующееся наличием пародонтальных карманов и активной резорбцией кости. Пейдж и Шредер (1982) определяют пять различных форм пародонтита:
- препубертатный периодонтит
- ювенильный пародонтит
- быстропрогрессирующий пародонтит
- пародонтит взрослых
- острый язвенно-некротический гингиво-периодонит
T Наиболее распространенным из них является пародонтит взрослых . Считается, что это начинается после 30 лет и может затронуть любой или все зубы с вертикальной или горизонтальной структурой потери костной массы. Это редко приводит к потере зубов, хотя у некоторых пациентов на некоторых стадиях наблюдается быстрое разрушение прикрепления пародонта. Острые обострения заболевания могут накладываться на хроническую форму с образованием гноя, что может привести к пародонтальному абсцессу. Лечение большинства пациентов с пародонтитом у взрослых относительно несложно для стоматолога общей практики. Выявление других форм заболеваний пародонта должно быть обязанностью стоматолога общей практики; однако следует серьезно рассмотреть вопрос о направлении к пародонтологу для лечения этих состояний.
Считается, что это начинается после 30 лет и может затронуть любой или все зубы с вертикальной или горизонтальной структурой потери костной массы. Это редко приводит к потере зубов, хотя у некоторых пациентов на некоторых стадиях наблюдается быстрое разрушение прикрепления пародонта. Острые обострения заболевания могут накладываться на хроническую форму с образованием гноя, что может привести к пародонтальному абсцессу. Лечение большинства пациентов с пародонтитом у взрослых относительно несложно для стоматолога общей практики. Выявление других форм заболеваний пародонта должно быть обязанностью стоматолога общей практики; однако следует серьезно рассмотреть вопрос о направлении к пародонтологу для лечения этих состояний.
Препубертатный периодонтит — чрезвычайно редкое заболевание, приводящее к раннему отслоению молочных зубов с воспалением тканей пародонта или без него. Обычно это связано с системными заболеваниями, такими как синдром Папийона-Лефевра.
Юношеский периодонтит хорошо задокументирован и характеризуется тяжелым поражением пародонта, ограничивающимся преимущественно первыми постоянными молярами и/или резцами. Считается, что начало болезни совпадает с периодом полового созревания, когда она очень активна, но впоследствии деструкция может замедлиться или спонтанно прекратиться. Распространенность заболевания оценивается примерно в одном случае на тысячу детей. Клинически ткани десны могут выглядеть совершенно нормально, с очень небольшим налетом. Таким образом, диагностика в значительной степени зависит от использования пародонтального зонда в качестве рутинной части стоматологического осмотра и тщательного изучения любых сделанных рентгенограмм. Ювенильный пародонтит обычно поддается пародонтологическому лечению; однако это может включать обширное выравнивание корней, антибактериальную терапию и хирургический доступ.
Быстро прогрессирующий пародонтит поражает молодых людей в возрасте до 35 лет. Это вызывает обширное разрушение тканей пародонта, поражающее большинство зубов, и может привести к ранней потере зубов. Заболевание имеет активную и неактивную фазы. Во время активной фазы у пациента часто отмечаются воспаленные и опухшие десневые ткани, которые обильно кровоточат при осторожном зондировании. Также может отмечаться повышенная подвижность зубов. Эта активная фаза может длиться две-три недели, прежде чем вернуться в неактивную фазу.
Это вызывает обширное разрушение тканей пародонта, поражающее большинство зубов, и может привести к ранней потере зубов. Заболевание имеет активную и неактивную фазы. Во время активной фазы у пациента часто отмечаются воспаленные и опухшие десневые ткани, которые обильно кровоточат при осторожном зондировании. Также может отмечаться повышенная подвижность зубов. Эта активная фаза может длиться две-три недели, прежде чем вернуться в неактивную фазу.
I Если пациент посещает во время неактивной фазы, может быть очень мало клинических признаков, указывающих на степень деструкции пародонта. Опять же, для выявления этого состояния необходимо тщательное зондирование пародонта и изучение рентгенограмм. Эта форма пародонтита обычно требует агрессивного лечения, при этом вероятными компонентами лечения являются улучшение гигиены полости рта, полировка корней, антибактериальная терапия и пародонтальная хирургия. Раннее выявление и направление к специалисту могут дать пациенту наилучший прогноз.
Последняя категория пародонтита, острый язвенно-некротический гингиво-периодонтит , обычно связана с ВИЧ-ассоциированным пародонтитом. Это часто наблюдается на поздних стадиях ВИЧ-инфекции, когда у пациента сильно ослаблен иммунитет. Он начинается с типичных признаков ANUG, но быстро распространяется, поражая нижележащие ткани пародонта, вызывая некроз кости и быстрое отслоение зубов. Пациенты часто жалуются на глубокую боль в костях.
T Его краткий обзор является руководством по формированию пародонтологического диагноза для каждого из ваших пациентов. Для получения более подробной информации вы можете обратиться по адресу:
1. Страница RC, Schroeder HE. Пародонтит у человека и других животных. Karger: Basel, 1982.
2. Williams DM, Hughes FJ, Odell EW, Farthing PM. Патология пародонтоза. Издательство Оксфордского университета, 1992.

или обратитесь в Исследовательский отдел стоматологической практики Университета Аделаиды.
TO TOP
Связь агрессивного и хронического периодонтита с системными проявлениями и зубными аномалиями у населения Иордании: исследование случай-контроль | Медицина головы и лица
- Исследования
- Открытый доступ
- Опубликовано:
- Ханса Т Абабнех 1 ,
- Anas H Taha 1 ,
- Muna S Abbadi 1 ,
- Jumana A Karasneh 2 &
- …
- Yousef S Khader 3
Медицина для головы и лица том 6 , номер статьи: 30 (2010) Процитировать эту статью
-
8006 доступов
-
Сведения о показателях
Abstract
История вопроса
Взаимосвязь между зубными аномалиями и периодонтитом не была документирована более ранними исследованиями. Хотя психологические факторы вовлечены в этиопатогенез пародонтита, до сих пор было опубликовано очень мало информации о связи тревоги и депрессии с агрессивным пародонтитом. Целью данного исследования было изучение ассоциации хронического пародонтита и агрессивного пародонтита с некоторыми системными проявлениями и зубочелюстными аномалиями.
Хотя психологические факторы вовлечены в этиопатогенез пародонтита, до сих пор было опубликовано очень мало информации о связи тревоги и депрессии с агрессивным пародонтитом. Целью данного исследования было изучение ассоциации хронического пародонтита и агрессивного пародонтита с некоторыми системными проявлениями и зубочелюстными аномалиями.
Методы
Всего было включено 262 пациента (100 с хроническим пародонтитом, 81 с агрессивным пародонтитом и 81 контрольная группа), посещавших пародонтологические клиники Иорданского университета науки и технологии, Центр обучения стоматологии. Всем испытуемым было проведено полное пародонтологическое и рентгенографическое обследование для оценки состояния пародонта и проверки на наличие любой из следующих стоматологических аномалий: инвагинатус, эвагинат, врожденное отсутствие боковых резцов или штифтообразные боковые резцы. Участников опросили по поводу следующего: депрессивное настроение, утомляемость, потеря веса или потеря аппетита; состояние тревоги и депрессии оценивали с использованием госпитальной шкалы тревоги и депрессии (HAD).
Результаты
Пациенты с агрессивным пародонтитом сообщали о большем количестве системных симптомов (51%), чем пациенты с хроническим пародонтитом (36%) и контрольная группа (30%) ( p < 0,05). Пациенты с агрессивным пародонтитом имели более высокую склонность как к тревоге, так и к депрессии, чем пациенты с хроническим пародонтитом и контрольная группа. Стоматологические аномалии достоверно ( p < 0,05) чаще встречались у больных как с хроническим, так и с агрессивным пародонтитом (15% и 16% соответственно) по сравнению с контрольной группой.
Заключение
В этой группе иорданцев системные симптомы были тесно связаны с агрессивным пародонтитом, а зубные аномалии были положительно связаны как с агрессивным, так и с хроническим пародонтитом.
Отчеты экспертной оценки
История вопроса
Пародонтит — многофакторное заболевание, которое включает инфекцию и воспаление поддерживающих тканей пародонта, приводящее к их разрушению [1]. В данной статье основное внимание уделяется двум типам пародонтита: хроническому пародонтиту (ХП) и агрессивному пародонтиту (АП) и их связи с некоторыми стоматологическими аномалиями и психологическим стрессом. Пейдж и коллеги в 1983 [2] сообщили, что быстропрогрессирующий пародонтит (БПП, в настоящее время называемый генерализованным ОП) прогрессирует в чередующиеся фазы активности и затишья заболевания. Они сообщили, что активная фаза RPP связана с системными проявлениями, такими как депрессия, недомогание, потеря веса и потеря аппетита у некоторых людей.
В данной статье основное внимание уделяется двум типам пародонтита: хроническому пародонтиту (ХП) и агрессивному пародонтиту (АП) и их связи с некоторыми стоматологическими аномалиями и психологическим стрессом. Пейдж и коллеги в 1983 [2] сообщили, что быстропрогрессирующий пародонтит (БПП, в настоящее время называемый генерализованным ОП) прогрессирует в чередующиеся фазы активности и затишья заболевания. Они сообщили, что активная фаза RPP связана с системными проявлениями, такими как депрессия, недомогание, потеря веса и потеря аппетита у некоторых людей.
Существует множество заболеваний зубочелюстной системы, которые могут поражать коронки или корни зубов, так что могут быть затронуты размер, форма или количество зубов. Dens invaginatus является необычным пороком развития, который демонстрирует широкий спектр анатомических вариаций [3]. Считается, что он возникает из-за складчатости зубного сосочка или искривления эмалевого органа в процессе развития зубов [4–6]. Сообщаемая распространенность dens invaginatus колеблется от 0,04 до 10% [7]. Наиболее пораженными постоянными зубами являются верхнечелюстные боковые резцы, часто двусторонние, за которыми следуют центральные резцы, клыки, премоляры и моляры [8]. Клиницисты чаще всего используют классификацию, предложенную Oehlers (19).57) [5], который классифицирует dens invaginatus на:
Наиболее пораженными постоянными зубами являются верхнечелюстные боковые резцы, часто двусторонние, за которыми следуют центральные резцы, клыки, премоляры и моляры [8]. Клиницисты чаще всего используют классификацию, предложенную Oehlers (19).57) [5], который классифицирует dens invaginatus на:
-
Тип I: выстланная эмалью инвагинация внутри коронки, не выходящая за пределы цементно-эмалевой границы (ЦЭГ).
-
Тип II: инвагинация эмали в корень, за пределы ЦЭГ, оканчивающаяся слепым мешком.
-
Тип III: расширение инвагинации, покрытой эмалью, через корень с образованием дополнительного апикального или латерального отверстия; обычно прямой связи с пульпой нет.
Dens evaginatus или бугорок когтя — относительно редкая одонтогенная аномалия, возникающая при морфодифференцировке зубов [9]. Дополнительный бугорок различается по размеру, форме, длине и способу прикрепления к коронке. Он варьируется от увеличенного цингулума до большого, хорошо очерченного бугорка [10]. Обычно это связано с небными аспектами передних зубов верхней челюсти [11], но может также присутствовать на окклюзионных аспектах боковых зубов, особенно у людей азиатского происхождения [12].
Дополнительный бугорок различается по размеру, форме, длине и способу прикрепления к коронке. Он варьируется от увеличенного цингулума до большого, хорошо очерченного бугорка [10]. Обычно это связано с небными аспектами передних зубов верхней челюсти [11], но может также присутствовать на окклюзионных аспектах боковых зубов, особенно у людей азиатского происхождения [12].
Колышковидные (конические) боковые резцы верхней челюсти представляют собой относительно распространенные стоматологические аномалии [13–16], которые могут встречаться у здоровых людей или быть частью других заболеваний, таких как синдром Дауна [17]. В своем исследовании иорданских студентов-стоматологов Albashaireh & Khader (2006) [15] сообщили, что распространенность штифтовых боковых резцов составляет 2,3%.
Гиподонтию, врожденное отсутствие зубов, делят на два класса: синдромальные и несиндромальные, в зависимости от причины гиподонтии [18]. Верхние боковые резцы и вторые премоляры являются наиболее часто поражаемыми зубами [19]. ]. В Иордании сообщается о 5,5% распространенности гиподонтии [15].
]. В Иордании сообщается о 5,5% распространенности гиподонтии [15].
Целью данного исследования было изучение связи определенных системных проявлений с ОП и ХП, оценка состояния тревоги и депрессии при обоих типах пародонтита с использованием госпитальной шкалы тревоги и депрессии (HAD) и изучение связи CP и AP с некоторыми зубными аномалиями. Насколько нам известно и основано на обширном поиске в Medline, связь между AP/CP и зубными аномалиями, такими как dens invaginatus, dens evaginatus, штифтообразной формой и отсутствием боковых резцов, никогда не сообщалась в литературе.
Методы
Это исследование было предпринято с пониманием и согласием каждого участника и проводилось в полном соответствии с этическими принципами Хельсинкской декларации Всемирной медицинской ассоциации http://www.wma.net/en/30publications/ 10policies/b3/index.html. Исследование было независимо рассмотрено и одобрено Советом по этике Иорданского университета науки и технологий (JUST). Письменные формы согласия на интервью и обследование были подписаны всеми участниками или родителями участников в возрасте до 18 лет. Исследуемая популяция этого исследования случай-контроль состояла из 262 человек и включала 100 пациентов с ХП, 81 случай ОП и 81 контрольную группу. Было 125 мужчин и 137 женщин в возрасте от 14 до 71 года и среднем возрасте 31,3 (± 11,4 SD) года. Клиническое обследование проводилось в пародонтологической клинике Учебного центра JUST Dental. В исследование были включены системно здоровые лица, не получавшие пародонтологического лечения в течение последних трех месяцев до обследования. Из исследования были исключены лица с сахарным диабетом или заболеваниями крови, пациенты, длительно принимающие какие-либо лекарства, беременные женщины, пациенты, ранее или продолжающие ортодонтическое лечение, и дети в возрасте до 14 лет.
Исследуемая популяция этого исследования случай-контроль состояла из 262 человек и включала 100 пациентов с ХП, 81 случай ОП и 81 контрольную группу. Было 125 мужчин и 137 женщин в возрасте от 14 до 71 года и среднем возрасте 31,3 (± 11,4 SD) года. Клиническое обследование проводилось в пародонтологической клинике Учебного центра JUST Dental. В исследование были включены системно здоровые лица, не получавшие пародонтологического лечения в течение последних трех месяцев до обследования. Из исследования были исключены лица с сахарным диабетом или заболеваниями крови, пациенты, длительно принимающие какие-либо лекарства, беременные женщины, пациенты, ранее или продолжающие ортодонтическое лечение, и дети в возрасте до 14 лет.
Демографические и социально-экономические данные участников были записаны в специальную форму обследования, и всех участников опросили, часто ли они испытывали какие-либо из следующих системных симптомов: утомляемость (без очевидной причины), потеря аппетита, потеря веса и депрессивное настроение. . Эмоциональный статус дополнительно оценивали у всех испытуемых по шкале HAD [20] (рис. 1). Эта шкала представляет собой инструмент самооценки, разработанный для выявления тревоги и депрессии у амбулаторных больных [20]. Шкала HAD состоит из 14 утверждений (7 для беспокойства, обозначенных как «A» и 7 для депрессии, обозначенных как «B»), с 4 возможными ответами для каждого утверждения. Каждый ответ оценивается от 0 до 4 баллов. Минимальный подбалл для каждой категории («А» или «В») равен нулю, а максимальный подбалл равен 21. По подбаллу шкалы HAD участники были разделены на три группы, как это рекомендовано авторами [20]; те, кто набрал ≤ 7 баллов, считались свободными от тревоги или депрессии, те, кто набрал 8–10 баллов, считались имеющими сомнительную тревогу или депрессию, а те, чей подсчет был ≥ 11, считались страдающими тревогой или депрессией.
. Эмоциональный статус дополнительно оценивали у всех испытуемых по шкале HAD [20] (рис. 1). Эта шкала представляет собой инструмент самооценки, разработанный для выявления тревоги и депрессии у амбулаторных больных [20]. Шкала HAD состоит из 14 утверждений (7 для беспокойства, обозначенных как «A» и 7 для депрессии, обозначенных как «B»), с 4 возможными ответами для каждого утверждения. Каждый ответ оценивается от 0 до 4 баллов. Минимальный подбалл для каждой категории («А» или «В») равен нулю, а максимальный подбалл равен 21. По подбаллу шкалы HAD участники были разделены на три группы, как это рекомендовано авторами [20]; те, кто набрал ≤ 7 баллов, считались свободными от тревоги или депрессии, те, кто набрал 8–10 баллов, считались имеющими сомнительную тревогу или депрессию, а те, чей подсчет был ≥ 11, считались страдающими тревогой или депрессией.
Копия госпитальной шкалы тревоги и депрессии (HAD) .
Полноразмерное изображение
Для каждого субъекта полное пародонтальное обследование выполнялось одним из трех экспертов (AHT, MSA и KTA). Обследование пародонта включало измерение уровня клинического прикрепления (CAL) и индекса зубного налета (PI) по Silness и Löe [21]. Для измерения CAL каждый зуб осматривали, «проходя» пародонтологическим зондом по всей окружности зуба; третьи моляры и оставшиеся корни были исключены. CAL измеряли в шести местах на зуб (мезио-, средне- и дистально-щечный; мезио-, средне- и дистально-язычный/небный). Надежность между исследователями рассчитывалась с использованием альфа-статистики в отношении глубины зондирования и CAL в 16 квадрантах. Диагноз ХП и ОП был основан на значениях CAL и подтвержден рентгенологически с использованием внутриротовых периапикальных и прикусных рентгенограмм. Пародонтит определяли как наличие потери прикрепления (CAL) > 2 мм более чем на одном зубе. Всем участникам были сделаны прикусные рентгенограммы задних зубов и париапикальные рентгенограммы передних зубов, чтобы определить наличие и характер потери альвеолярной кости и подтвердить (или исключить) наличие периодонтита.
Обследование пародонта включало измерение уровня клинического прикрепления (CAL) и индекса зубного налета (PI) по Silness и Löe [21]. Для измерения CAL каждый зуб осматривали, «проходя» пародонтологическим зондом по всей окружности зуба; третьи моляры и оставшиеся корни были исключены. CAL измеряли в шести местах на зуб (мезио-, средне- и дистально-щечный; мезио-, средне- и дистально-язычный/небный). Надежность между исследователями рассчитывалась с использованием альфа-статистики в отношении глубины зондирования и CAL в 16 квадрантах. Диагноз ХП и ОП был основан на значениях CAL и подтвержден рентгенологически с использованием внутриротовых периапикальных и прикусных рентгенограмм. Пародонтит определяли как наличие потери прикрепления (CAL) > 2 мм более чем на одном зубе. Всем участникам были сделаны прикусные рентгенограммы задних зубов и париапикальные рентгенограммы передних зубов, чтобы определить наличие и характер потери альвеолярной кости и подтвердить (или исключить) наличие периодонтита. Чтобы дифференцировать ХП и ОП, в качестве диагностических критериев использовали клинические данные, включая состояние десен, CAL, тяжесть и (в меньшей степени) характер потери костной массы, а также возраст субъекта. Когда субъект имел CAL > 2 мм вокруг по крайней мере двух зубов, один из которых был первым моляром, или когда наблюдалась потеря прикрепления вокруг первых моляров и/или резцов, у которых в раннем возрасте (т.е. <45 лет) наблюдалась потеря костной массы, особенно если характерный дугообразный дефект (дефекты) был обнаружен на рентгенограммах, случай был диагностирован как ОП. Несоответствие между количеством отложений зубного налета и количеством деструкции пародонта (при наличии) и положительный семейный анамнез дополнительно подтвердили диагноз ОП. С другой стороны, ДЦП был диагностирован, когда CAL> 2 мм вокруг по крайней мере двух зубов, как правило, в более старших возрастных группах (т.е.> 45 лет). У молодых людей с легким прикреплением и потерей костной массы, у которых отложения бляшек соответствовали степени разрушения, был поставлен диагноз ДЦП.
Чтобы дифференцировать ХП и ОП, в качестве диагностических критериев использовали клинические данные, включая состояние десен, CAL, тяжесть и (в меньшей степени) характер потери костной массы, а также возраст субъекта. Когда субъект имел CAL > 2 мм вокруг по крайней мере двух зубов, один из которых был первым моляром, или когда наблюдалась потеря прикрепления вокруг первых моляров и/или резцов, у которых в раннем возрасте (т.е. <45 лет) наблюдалась потеря костной массы, особенно если характерный дугообразный дефект (дефекты) был обнаружен на рентгенограммах, случай был диагностирован как ОП. Несоответствие между количеством отложений зубного налета и количеством деструкции пародонта (при наличии) и положительный семейный анамнез дополнительно подтвердили диагноз ОП. С другой стороны, ДЦП был диагностирован, когда CAL> 2 мм вокруг по крайней мере двух зубов, как правило, в более старших возрастных группах (т.е.> 45 лет). У молодых людей с легким прикреплением и потерей костной массы, у которых отложения бляшек соответствовали степени разрушения, был поставлен диагноз ДЦП. Случаи неопределенности в диагностике ОП или ХП в данное исследование не включались.
Случаи неопределенности в диагностике ОП или ХП в данное исследование не включались.
Исследуемые зубные аномалии включали dens invaginatus, dens evaginatus, врожденное отсутствие и штыревую форму боковых резцов. Врожденно отсутствующие зубы были зарегистрированы после проверки их врожденного отсутствия участниками, и их отсутствие было подтверждено с помощью периапикальных рентгенограмм. Было отмечено наличие стержнеобразных боковых резцов, и все зубы были исследованы как клинически, так и рентгенологически на наличие dens evaginatus и dens invaginatus. Случаи Dens evaginatus классифицировали по Oehlers (1957) [5].
Статистический анализ
Все переменные были введены в персональный компьютер, и для обработки и анализа данных использовалось программное обеспечение Statistical Package for Social Sciences (SPSS Version 11, Chicago, Illinois). Были произведены частотное распределение и перекрестная таблица. Рассчитывали средние значения и стандартное отклонение и использовали критерий хи-квадрат. Различия считались значимыми, когда р < 0,05.
Различия считались значимыми, когда р < 0,05.
Результаты
Коэффициент альфа Кронбаха составил 0,9.4 для CAL, что свидетельствует об отличном согласии между исследователями.
Среднее значение CAL для случаев ХП составляло 2,17 мм (± 1,53 SD), тогда как среднее значение CAL для случаев AP составляло 2,76 мм (± 1,77 SD). У контрольных субъектов не было выявлено потери прикрепления (средний CAL = 0 мм) и рентгенологических признаков потери альвеолярной кости.
Социально-демографические характеристики
Как показано в таблице 1, наибольшую долю пациентов с ДЦП составляли мужчины в возрасте от 36 до 45 лет, работающие, но с низким доходом и имеющие образование вплоть до средней школы (т.е. ≤12 лет). Субъекты ДЦП и контрольная группа достоверно различались по возрасту, роду занятий, месту жительства и образованию. Самый высокий процент субъектов AP были молодыми (≤25 лет), были женщинами, были безработными, имели низкий доход, жили в городской местности и получили образование до средней школы. Члены группы AP значительно отличались от контрольной группы по возрасту, полу, роду занятий, доходу и образованию. При сравнении групп ХП и АП были выявлены статистически значимые различия между обеими группами по возрасту, полу, роду занятий, месту жительства и образованию (табл. 1).
Члены группы AP значительно отличались от контрольной группы по возрасту, полу, роду занятий, доходу и образованию. При сравнении групп ХП и АП были выявлены статистически значимые различия между обеими группами по возрасту, полу, роду занятий, месту жительства и образованию (табл. 1).
Полная таблица
Контрольная выборка состояла из 81 системно здорового иорданца без пародонтита; 45 мужчин и 36 женщин в возрасте от 14 до 37 лет со средним возрастом 22,2 года (± стандартное отклонение), у которых не было клинических или рентгенологических признаков прикрепления или потери костной массы в любом месте. Возраст контрольной группы не ограничивался 37 годами, но практически невозможно было найти здоровых пародонтологов в возрасте 40 лет и старше.
Системные проявления
Около 51% пациентов с ОП сообщили, что у них часто возникают один или несколько системных симптомов (в основном утомляемость и депрессивное настроение), которые они не могут связать с заболеванием или внешними факторами. Меньший процент случаев ХП (36%) и контрольной группы (около 29%) сообщили о наличии таких симптомов. Частота системных проявлений была значительно выше у пациентов с ОП, чем в контроле ( p = 0,019). Не было обнаружено существенных различий в частоте системных симптомов между пациентами с ХП и контролем (9).0288 р = 0,7). Однако между случаями ХП и ОП наблюдалась незначительно значимая разница ( p = 0,059). В таблице 2 показано дифференцированное распределение системных проявлений, о которых сообщалось в исследуемой популяции. Наиболее распространенной системной жалобой в 3 группах была усталость, сопровождаемая депрессивным настроением. Несмотря на то, что пациенты с ОП чаще сообщали о депрессивном настроении, чем в двух других группах, разница не была статистически значимой.
Меньший процент случаев ХП (36%) и контрольной группы (около 29%) сообщили о наличии таких симптомов. Частота системных проявлений была значительно выше у пациентов с ОП, чем в контроле ( p = 0,019). Не было обнаружено существенных различий в частоте системных симптомов между пациентами с ХП и контролем (9).0288 р = 0,7). Однако между случаями ХП и ОП наблюдалась незначительно значимая разница ( p = 0,059). В таблице 2 показано дифференцированное распределение системных проявлений, о которых сообщалось в исследуемой популяции. Наиболее распространенной системной жалобой в 3 группах была усталость, сопровождаемая депрессивным настроением. Несмотря на то, что пациенты с ОП чаще сообщали о депрессивном настроении, чем в двух других группах, разница не была статистически значимой.
Полноразмерная таблица
Тревога и депрессия с использованием шкалы HAD
Показатели тревоги и депрессии суммировались независимо, чтобы получить «оценку тревоги» и «оценку депрессии» для каждого субъекта. В таблице 3 показано количество и процентное соотношение лиц в каждой категории баллов по шкале HAD. Группа с самым высоким процентом в этом исследовании набрала 7 или меньше баллов как за тревогу, так и за депрессию. В то время как почти равные доли пациентов с ОП (31%) и ХП (32%) имели сомнительную тревогу, гораздо меньшая доля контрольной группы (14%) имела сомнительную тревогу. Однако более высокий процент пациентов с ОП (31%) имел выраженную тревогу, чем пациенты с ХП (21%) и контрольная группа (22%). Что касается оценки депрессии, более высокий процент (26%) случаев ОП имел сомнительную депрессию, а также определенную депрессию (11%), чем у пациентов с ХП и контроля. Таблица 3 также показывает, что у большего количества пациентов с ОП (31%) тревожность была выше, чем депрессия (11%).
В таблице 3 показано количество и процентное соотношение лиц в каждой категории баллов по шкале HAD. Группа с самым высоким процентом в этом исследовании набрала 7 или меньше баллов как за тревогу, так и за депрессию. В то время как почти равные доли пациентов с ОП (31%) и ХП (32%) имели сомнительную тревогу, гораздо меньшая доля контрольной группы (14%) имела сомнительную тревогу. Однако более высокий процент пациентов с ОП (31%) имел выраженную тревогу, чем пациенты с ХП (21%) и контрольная группа (22%). Что касается оценки депрессии, более высокий процент (26%) случаев ОП имел сомнительную депрессию, а также определенную депрессию (11%), чем у пациентов с ХП и контроля. Таблица 3 также показывает, что у большего количества пациентов с ОП (31%) тревожность была выше, чем депрессия (11%).
 Статистически значимая разница была обнаружена при тревоге ( p = 0,039) и депрессии ( = 0,039).0288 p = 0,001) баллы пациентов с ОП сравнивали с контролем. Однако не было обнаружено существенных различий в средних баллах HAD при сравнении случаев ХП и ОП с контролем (таблица 3).
Статистически значимая разница была обнаружена при тревоге ( p = 0,039) и депрессии ( = 0,039).0288 p = 0,001) баллы пациентов с ОП сравнивали с контролем. Однако не было обнаружено существенных различий в средних баллах HAD при сравнении случаев ХП и ОП с контролем (таблица 3). Стоматологические аномалии
Стоматологические аномалии наблюдались в 28 случаях исследуемой популяции; в 15% случаев ХП (15 человек) и в 16% случаев ОП (13 человек), но не наблюдались ни у одного из контрольных субъектов (табл. 4). Все случаи dens invaginatus наблюдались одно- и билатерально на верхних боковых резцах и были клинически и рентгенологически типом I. Все случаи dens evaginatus были небольшими бугоркообразными расширениями поясной извилины верхних боковых резцов и не мешали окклюзии. Среди случаев ОП (табл. 5) 8 пациентов (90,9%) имели dens invaginatus, один (1,2%) имел dens evaginatus, 2 (2,46%) имели двусторонние штифтовые боковые резцы и 2 пациента (2,46%) имели врожденное отсутствие верхнего бокового резца. Среди случаев ДЦП 6 пациентов (6%) имели инвагинальный придаток, 2 (2%) — dens evaginatus и 7 (7%) — одностороннее врожденное отсутствие зубов (2 нижних вторых премоляра и 5 верхних боковых резцов). И AP, и CP были значительно более связаны с зубными аномалиями, чем контрольная группа ( p <0,05), в то время как разница между двумя группами пародонтита была незначительной ( р = 0,72). Кроме того, группы больных не имели существенных отличий от контроля или друг от друга при сравнении каждой из зубных аномалий в отдельности ( p > 0,05).
Среди случаев ДЦП 6 пациентов (6%) имели инвагинальный придаток, 2 (2%) — dens evaginatus и 7 (7%) — одностороннее врожденное отсутствие зубов (2 нижних вторых премоляра и 5 верхних боковых резцов). И AP, и CP были значительно более связаны с зубными аномалиями, чем контрольная группа ( p <0,05), в то время как разница между двумя группами пародонтита была незначительной ( р = 0,72). Кроме того, группы больных не имели существенных отличий от контроля или друг от друга при сравнении каждой из зубных аномалий в отдельности ( p > 0,05).
Полноразмерная таблица
Таблица 5 Зубные аномалии при CP и AP.Полноразмерная таблица
Обсуждение
Распределение хронического и агрессивного пародонтита, обнаруженное в этом исследовании, соответствовало общим закономерностям, описанным в других работах [22–24]. Самый высокий процент пациентов с ХП был старше (> 35 лет), чем самый высокий процент пациентов с ОП (< 25 лет). Это подтверждает, что ОП обычно проявляется в более раннем возрасте у восприимчивых лиц. В то время как ХП был распределен почти поровну между мужчинами и женщинами в этом исследовании, большую часть пациентов с ОП составляли женщины. Обследования заболеваний пародонта обычно показывают, что у взрослых мужчин риск развития ДЦП выше, чем у женщин [25]. Это различие может быть отражением лучшей практики гигиены полости рта и более широкого использования услуг по уходу за полостью рта среди женщин, а не врожденных различий между мужчинами и женщинами в отношении восприимчивости к ХП [26]. Выявлено, что частота обеих форм пародонтита у студентов значительно ниже, чем у работающих и неработающих. Социально-экономический уровень является хорошим маркером различных факторов риска пародонтита, таких как гигиена полости рта, оказание стоматологической помощи и поведение. Предыдущие исследования зафиксировали различия в здоровье пародонта в зависимости от факторов социально-экономического статуса (СЭС), таких как доход и образование, показывая, что более низкий СЭС был связан с повышенным риском пародонтита [27].
Это подтверждает, что ОП обычно проявляется в более раннем возрасте у восприимчивых лиц. В то время как ХП был распределен почти поровну между мужчинами и женщинами в этом исследовании, большую часть пациентов с ОП составляли женщины. Обследования заболеваний пародонта обычно показывают, что у взрослых мужчин риск развития ДЦП выше, чем у женщин [25]. Это различие может быть отражением лучшей практики гигиены полости рта и более широкого использования услуг по уходу за полостью рта среди женщин, а не врожденных различий между мужчинами и женщинами в отношении восприимчивости к ХП [26]. Выявлено, что частота обеих форм пародонтита у студентов значительно ниже, чем у работающих и неработающих. Социально-экономический уровень является хорошим маркером различных факторов риска пародонтита, таких как гигиена полости рта, оказание стоматологической помощи и поведение. Предыдущие исследования зафиксировали различия в здоровье пародонта в зависимости от факторов социально-экономического статуса (СЭС), таких как доход и образование, показывая, что более низкий СЭС был связан с повышенным риском пародонтита [27]. Однако в настоящее время считается, что образование оказывает большее влияние, чем доход, на уровень заболеваемости пародонтитом населения [28].
Однако в настоящее время считается, что образование оказывает большее влияние, чем доход, на уровень заболеваемости пародонтитом населения [28].
В этом исследовании изучались некоторые системные проявления, такие как утомляемость, потеря аппетита, потеря веса и депрессивное настроение в связи с ХП и ОП. Значительная часть пациентов с диагнозом ОП сообщила, что они испытывали (одно или несколько из этих) системных проявлений, причем наиболее часто сообщаемыми симптомами были утомляемость и депрессивное настроение. Эти выводы согласуются с выводами Page et al. [2], которые предположили, что РПП (генерализованный ОП) протекает в фазах активности и покоя и что активная фаза РПП у части лиц включает системные проявления, такие как депрессия, общее недомогание, снижение массы тела и снижение аппетита [2]. . Мы также заметили, что частота этих системных проявлений значительно выше у пациентов с ОП, чем в контрольной группе или у пациентов с ХП (маргинальная значимость). Оценка состояния тревоги и депрессии у участников этого исследования с использованием шкалы HAD показала, что субъекты с диагнозом ОП проявляли значительно большую тревогу и депрессию по сравнению с пациентами с ДЦП и контрольной группой. Было бы интересно узнать, как пародонтит (особенно АП) связан с тревогой и депрессией. Большая часть литературы исследовала влияние психологического стресса на пародонтит, но влияние пародонтита на психологическое состояние не привлекало особого внимания. Настоящее исследование демонстрирует простую связь между пародонтитом и тревогой и депрессией, и для прояснения этого вопроса необходимы будущие лонгитюдные и междисциплинарные исследования. Кроме того, в настоящем исследовании люди с ОП, как правило, имели более высокие баллы по тревоге, чем по депрессии. Тревога у пациентов с ОП может частично возникать из-за их опасений потерять зубы в молодом возрасте. Также стоит отметить, что большинство пациентов с ОП были безработными, имели низкий доход и имели только (до) среднее образование; безработица, низкий доход и образование могут вызывать нестабильность в жизни и усиливать тревогу. Однако из настоящих результатов неясно, предрасполагают ли наличие пародонтита и неблагоприятный прогноз состояния зубов в этой группе лиц к тревоге и депрессии, или же эти психологические симптомы являются истинными компонентами заболевания (ОП и, возможно, ХП) как предположили Пейдж и его коллеги [2], и необходимы дальнейшие исследования для изучения этой связи.
Было бы интересно узнать, как пародонтит (особенно АП) связан с тревогой и депрессией. Большая часть литературы исследовала влияние психологического стресса на пародонтит, но влияние пародонтита на психологическое состояние не привлекало особого внимания. Настоящее исследование демонстрирует простую связь между пародонтитом и тревогой и депрессией, и для прояснения этого вопроса необходимы будущие лонгитюдные и междисциплинарные исследования. Кроме того, в настоящем исследовании люди с ОП, как правило, имели более высокие баллы по тревоге, чем по депрессии. Тревога у пациентов с ОП может частично возникать из-за их опасений потерять зубы в молодом возрасте. Также стоит отметить, что большинство пациентов с ОП были безработными, имели низкий доход и имели только (до) среднее образование; безработица, низкий доход и образование могут вызывать нестабильность в жизни и усиливать тревогу. Однако из настоящих результатов неясно, предрасполагают ли наличие пародонтита и неблагоприятный прогноз состояния зубов в этой группе лиц к тревоге и депрессии, или же эти психологические симптомы являются истинными компонентами заболевания (ОП и, возможно, ХП) как предположили Пейдж и его коллеги [2], и необходимы дальнейшие исследования для изучения этой связи.
В настоящем исследовании было исследовано несколько зубных аномалий, включая инвагинатные и эвагинативные зубья, штифтовые боковые резцы и врожденное отсутствие боковых резцов. Интересно, что зубные аномалии, исследованные в этом исследовании, наблюдались только у субъектов с ХП и ОП, в отличие от контрольной группы, у которой не было ни одной из исследованных зубных аномалий. Кроме того, частота dens invaginatus, наблюдаемая среди групп AP (16%) и CP (15%), была значительно выше, чем в общей популяции в Иордании (2,9%).5%) [27]. Считается, что аномалии развития зубов детерминированы генетически, поскольку они очень воспроизводимы по форме, проявляют склонность к некоторым расовым группам и часто встречаются вместе [12]. Считается, что развитие зубов находится под строгим генетическим контролем, который определяет положение, количество и форму различных зубов [19]. Кроме того, зубные аномалии, такие как, например, боковые резцы в форме штифта, являются хорошо документированными компонентами многочисленных системных заболеваний и синдромов, таких как синдром Дауна [17], синдром зубов и ногтей Виткопа [28], синдром Сетре-Чотцена [29]. ), подслизистая расщелина неба [30] и гипогидротическая эктодермальная дисплазия [31]. По мере постепенного выявления генетической основы различных стоматологических аномалий [9] одновременно становится все более ясным, что предрасположенность к различным видам пародонтита связана с генетическими полиморфизмами в генах, кодирующих определенные цитокины и другие компоненты иммунной системы, такие как ИЛ- 1 [32] и Ил-10 [33].
), подслизистая расщелина неба [30] и гипогидротическая эктодермальная дисплазия [31]. По мере постепенного выявления генетической основы различных стоматологических аномалий [9] одновременно становится все более ясным, что предрасположенность к различным видам пародонтита связана с генетическими полиморфизмами в генах, кодирующих определенные цитокины и другие компоненты иммунной системы, такие как ИЛ- 1 [32] и Ил-10 [33].
Таким образом, кажется логичным постулировать, что определенные зубные аномалии могут быть компонентами АР и ЦП у некоторых людей, возникающими в результате специфических, возможно родственных, генетических полиморфизмов. Это исследование, однако, показывает простую связь и не может подтвердить или исключить такое предположение. Необходимы генетические и широкомасштабные эпидемиологические исследования, направленные на изучение связи ОП и ХП с отдельными зубными аномалиями.
Выводы
Сделан вывод, что системные проявления утомляемости, депрессивного настроения, снижения аппетита и похудания были тесно связаны с ОП. Установлено, что зубочелюстные аномалии dens invaginatus, dens evaginatus, колышковидная форма и врожденное отсутствие боковых резцов ассоциированы с агрессивным и хроническим пародонтитом. Наличие этих зубных аномалий должно побудить клиницистов провести тщательное обследование пародонта, а пациенты с агрессивным пародонтитом могут быть кандидатами на направление к профессиональной психологической помощи.
Установлено, что зубочелюстные аномалии dens invaginatus, dens evaginatus, колышковидная форма и врожденное отсутствие боковых резцов ассоциированы с агрессивным и хроническим пародонтитом. Наличие этих зубных аномалий должно побудить клиницистов провести тщательное обследование пародонта, а пациенты с агрессивным пародонтитом могут быть кандидатами на направление к профессиональной психологической помощи.
Сокращения
- АП :
-
Агрессивный пародонтит
- КАЛ :
-
Уровень клинической привязанности
- ЦЭЖ :
-
Цементоэмалевая стыковка
- КП :
-
Хронический пародонтит
- Весы HAD :
-
Больничная шкала тревоги и депрессии
- Ил-1 :
-
Интерлейкин 1
- Ил-10 :
-
Интерлейкин 10
- иорданских динаров :
-
Иорданский динар
- ИП :
-
Индекс зубного налета
- РПП :
-
Быстро прогрессирующий пародонтит
- СЭС :
-
Социально-экономический статус.

Каталожные номера
-
Kinane DF: Причины и патогенез заболеваний пародонта. Пародонтология 2000. 2001, 25: 8-20. 10.1034/j.1600-0757.2001.22250102.х.
КАС Статья пабмед Google ученый
-
Page RC, Altman LC, Ebersole JL, Vandesteen GE, Dahlberg WH, Williams BL, Osterberg SK: Быстро прогрессирующий периодонтит. Отдельное клиническое состояние. Джей Перио. 1983, 54: 197-209. 10.1902/jop.1983.54.4.197.
КАС Статья Google ученый
-
Зильберман А., Коэнка Н., Саймон Дж. Х.: Анатомический редизайн для лечения invaginatus типа III с открытыми верхушками: обзор литературы и описание случая. J Am Dent Assoc. 2006, 137: 180-185.
Артикул пабмед Google ученый
«> -
Oehlers FA: Dens invaginatus, часть I: варианты процесса инвагинации и связь с формами передней коронки. Oral Surg Oral Med Oral Pathol. 1957, 10: 1204-1218. 10.1016/0030-4220(57)
-4.КАС Статья пабмед Google ученый
-
Oehlers FA: Корешковая разновидность dens invaginatus. Oral Surg Oral Med Oral Pathol. 1958, 11: 1251-1260. 10.1016/0030-4220(58)-0.
КАС Статья пабмед Google ученый
-
Hovland EJ, Блок RM: Нераспознавание и последующее эндодонтическое лечение инвагинального зуба. Дж Эндод. 1977, 3: 360-362. 10.1016/S0099-2399(77)80067-8.
КАС Статья пабмед Google ученый
«> -
Аль-Омари М.А., Хаттаб Ф.Н., Дарвазех А.М., Даммер П.М.: Клинические проблемы, связанные с необычными случаями бугорка когтя. Int Endod J. 1999, 32: 183-190. 10.1046/j.1365-2591.1999.00212.х.
КАС Статья пабмед Google ученый
-
Хаттаб Ф.Н., Ясин О.М., аль-Нимри К.С.: Бугорок когтя – клиническое значение и лечение: отчеты о случаях. Квинтэссенция Инт. 1995, 26: 115-120.
КАС пабмед Google ученый
-
Lorena SC, Oliveira DT, Odellt EW: Множественные зубные аномалии в области резцов верхней челюсти. J Устные науки. 2003, 45: 47-50.

Артикул пабмед Google ученый
-
Левитан М.Е., Химель В.Т.: Dens evaginatus: обзор литературы, патофизиология и комплексная схема лечения. Дж Эндод. 2006, 32: 1-9. 10.1016/j.joen.2005.10.009.
Артикул пабмед Google ученый
-
Yonezu T, Hayashi Y, Sasaki J, Machida Y: Распространенность врожденных аномалий молочных зубов у японских детей. Булл Токио Дент Кол. 1997, 38: 27-32.
КАС пабмед Google ученый
-
Bäckman B, Wahlin YB: Вариации количества и морфологии постоянных зубов у 7-летних шведских детей. Int J Paediatr Dent. 2001, 11: 11-17.
Артикул пабмед Google ученый
-
Albashaireh ZS, Khader YS: Распространенность и характер гиподонтии постоянных зубов, размер и форма коронки, деформация верхних боковых резцов в выборке иорданских стоматологических пациентов.
 Сообщество Dent Health. 2006, 23: 239-243.
Сообщество Dent Health. 2006, 23: 239-243. ПабМед Google ученый
-
Wu H, Feng HL: Исследование количества и морфологических аномалий постоянных зубов у 6 453 молодых людей в возрасте от 17 до 21 года. Чжунхуа Коу Цян И Сюэ За Чжи. 2005, 40: 489-490.
ПабМед Google ученый
-
Cheng RH, Leung WK, Corbet EF, King NM: Состояние полости рта у взрослых с синдромом Дауна в Гонконге. Стоматолог Spec Care. 2007, 27: 134-138. 10.1111/j.1754-4505.2007.tb00335.x.
Артикул пабмед Google ученый
-
Пембертон Т.Дж., Мендоза Г., Джи Дж., Патель П.И.: Унаследованные зубные аномалии: обзор и перспективы будущей роли клиницистов. J Calif Dent Assoc. 2007, 35: 324-326. 328-333
ПабМед Google ученый
«> -
Зигмонд А.С., Снейт Р.П.: Госпитальная шкала тревоги и депрессии. Acta Psychiatr Scand. 1983, 67: 361-370. 10.1111/j.1600-0447.1983.tb09716.x.
КАС Статья пабмед Google ученый
-
Silness J, Löe H: Заболевания пародонта у беременных. II. Взаимосвязь между гигиеной полости рта и состоянием пародонта. Акта Одонтол Сканд. 1964, 22: 121-135. 10.3109/00016356408993968.
КАС Статья пабмед Google ученый
-
Pihlstrom BL: Оценка пародонтального риска, диагностика и планирование лечения. Пародонтология 2000.
 2001, 25: 37-58. 10.1034/j.1600-0757.2001.22250104.х.
2001, 25: 37-58. 10.1034/j.1600-0757.2001.22250104.х. КАС Статья пабмед Google ученый
-
Albandar JM, Rams TE: Факторы риска пародонтита у детей и молодых людей. Пародонтология 2000. 2000, 29: 207-222. 10.1034/j.1600-0757.2002.2
.х. -
Боррелл Л.Н., Папапану П.Н.: Аналитическая эпидемиология периодонтита. Дж. Клин Пародонтол. 2005, 32: 132-158. 10.1111/j.1600-051X.2005.00799.х.
Артикул пабмед Google ученый
-
Albandar JM: Эпидемиология и факторы риска заболеваний пародонта. Дент Клин Норт Ам. 2005, 49: 517-32. 10.1016/j.cden.2005.03.003. v-vi
Артикул пабмед Google ученый
-
Боррелл Л.Н., Берт Б.А., Соседи Х.
 В., Тейлор Г.В.: Социальные факторы и пародонтит у пожилых людей. Am J Общественное здравоохранение. 2004, 94: 748-754. 10.2105/AJPH.94.5.748.
В., Тейлор Г.В.: Социальные факторы и пародонтит у пожилых людей. Am J Общественное здравоохранение. 2004, 94: 748-754. 10.2105/AJPH.94.5.748. Артикул пабмед ПабМед Центральный Google ученый
-
Хамаша А.А., Аломари К.Д.: Распространенность dens invaginatus у взрослых иорданцев. Int Endod J. 2004, 37: 307-310. 10.1111/j.0143-2885.2004.00797.х.
КАС Статья пабмед Google ученый
-
Altug-Atac AT, Iseri H: Синдром зубов и ногтей Виткопа и ортодонтия. Угол Ортод. 2008, 78: 370-380. 10.2319/100406-403.1.
Артикул пабмед Google ученый
-
Marchesi A, Leoni R: Множественные шиповидные зубы, связанные с акроцефалосиндактилией. Вариант синдрома Сетре-Чотцена? Клинический случай. Минерва Стоматол. 1993, 42: 169-172.
КАС пабмед Google ученый
«> -
Шигли А., Редди Р.В., Хугар С.М., Дешпанде Д. Гипогидротическая эктодермальная дисплазия: уникальный подход к эстетическому и протезному лечению: клинический случай. J Indian Soc Pedod Prev Dent. 2005, 23: 31-34. 10.4103/0970-4388.16024.
КАС Статья пабмед Google ученый
-
Корнман К.С., Крейн А., Ван Х.И., ди Джовин Ф.С., Ньюман М.Г., Пирк Ф.В., Уилсон Т.Г., Хиггинботтом Ф.Л., Дафф Г.В.: Генотип интерлейкина-1 как фактор тяжести заболеваний пародонта у взрослых. Дж. Клин Пародонтол. 1997, 24: 72-77. 10.1111/j.1600-051X.1997.tb01187.x.
КАС Статья пабмед Google ученый
«>
Кронфельд Р: Dens in dente. Джей Дент Рез. 1934, 14: 49-66. 10.1177/00220345340140010801.
Артикул Google ученый
Алани А., Бишоп К. Dens invaginatus. Часть 1: классификация, распространенность и этиология. Int Endod J. 2008, 41: 1123-1136. 10.1111/j.1365-2591.2008.01468.х.
КАС Статья пабмед Google ученый
Arte S, Nieminen P, Apajalahti S, Haavikko K, Thesleff I, Pirinen S: Характеристики резцово-премолярной гиподонтии в семьях. Джей Дент Рез. 2001, 80: 1445-1450. 10.1177/00220345010800051201.
КАС Статья пабмед Google ученый
Артикул Google ученый
Helióvaara A, Ranta R, Rautio J: Стоматологические аномалии постоянного прикуса у детей с подслизистой расщелиной неба. Акта Одонтол Сканд. 2004, 62: 129-131.
Артикул пабмед Google ученый
Берглунд Т., Донати М., Хан-Зорик М., Хэнсон Л.А., Падюков Л.: Ассоциация полиморфизма гена -1087 IL 10 с тяжелым хроническим пародонтитом у шведских европеоидов. Дж. Клин Пародонтол. 2003, 30: 249-254. 10.1034/j.1600-051X.2003.10274.x.
Артикул пабмед Google ученый
Ссылки на скачивание
Благодарности
Авторы выражают благодарность Иорданскому университету науки и технологий за спонсорство этой работы в виде гранта через деканство научных исследований. Особая благодарность стоматологическому факультету и Учебному центру JUST Dental, Ирбид, Иордания, за помощь в клиническом и рентгенографическом обследовании участников этого исследования. Мы благодарим г-жу Сумайя Хамайсе и г-жу Ясмин Джарадат за их помощь во время сбора данных.
Информация об авторе
Авторы и организации
-
Отделение пародонтологии, кафедра профилактической стоматологии, стоматологический факультет, Иорданский университет науки и технологий, Иордания
Ханса Т.
 Абабне, Анас Х. Таха и Муна С. Аббади
Абабне, Анас Х. Таха и Муна С. Аббади - 4
- 4
Отделение оральной медицины, кафедра оральной хирургии, оральной медицины, оральной патологии и радиологии, стоматологический факультет, Иорданский университет науки и технологии, Иордания
Jumana A Karasneh
-
Общественная медицина и общественное здравоохранение, Медицинский факультет, Иорданский научно-технический университет, Иордания
Yousef S Khader
Авторы
- You cansa T Ababneh 90 публикаций 30 публикаций 20090 публикаций 200011 Khansa T Ababneh 90 также ищите этого автора в PubMed Google Scholar
- Anas H Taha
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Muna S Abbadi
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jumana A Karasneh
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Yousef S Khader
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Автор, ответственный за переписку
Ханса Т Абабне.
Дополнительная информация
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Вклад авторов
KTA предложил план исследования, руководил и участвовал в сборе данных и написал рукопись. И AHT, и MSA проводили сбор данных и обследование пациентов, а также участвовали в написании рукописи. JAK предложил дизайн исследования и участвовал в анализе данных. YSK провел статистический анализ. Все авторы прочитали и одобрили рукопись.
Оригинальные файлы изображений, представленные авторами
Ниже приведены ссылки на оригинальные файлы изображений, представленные авторами.
Исходный файл авторов для рисунка 1
Права и разрешения
Открытый доступ Международная лицензия (https://creativecommons.org/licenses/by/2.0), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Перепечатки и разрешения
Об этой статье
Признаки и симптомы заболеваний пародонта | Troy, Alabama
Заболевание пародонта (также известное как пародонтит и заболевание десен) является прогрессирующим заболеванием и основной причиной потери зубов среди взрослых в развитых странах. Заболевание пародонта возникает, когда токсины, обнаруженные в зубном налете, начинают раздражать или воспалять десну (ткань десны). Возникающая в результате бактериальная инфекция, часто известная как гингивит, может в конечном итоге привести к разрушению ткани десны и подлежащей кости. Если пародонтоз не лечить, он также может привести к расшатыванию или потере зубов.
Существует много распространенных типов заболеваний пародонта, включая агрессивный, хронический, некротизирующий пародонтит и пародонтит, связанный с системными заболеваниями. Каждый из этих типов заболеваний пародонта имеет свои отличительные характеристики и симптомы, и все они требуют немедленного лечения у стоматолога, чтобы остановить последующую потерю костной ткани и тканей.
Общие признаки и симптомы
Чрезвычайно важно отметить, что заболевание пародонта может прогрессировать без каких-либо признаков или симптомов, таких как боль. Вот почему регулярные стоматологические осмотры чрезвычайно важны. Ниже описаны некоторые из наиболее распространенных признаков и симптомов пародонтита.
Если у вас есть какие-либо из этих признаков или симптомов, необходимо как можно скорее обратиться за консультацией к стоматологу общей практики или пародонтологу:
-
Необъяснимое кровотечение – Кровотечение при чистке зубов, чистке зубной нитью или приеме пищи является одним из наиболее распространенных симптомов пародонтальной инфекции. Токсины зубного налета вызывают бактериальную инфекцию, которая делает ткани склонными к кровотечениям.
-
Боль, покраснение или отек – Пародонтальная инфекция может присутствовать, если десны опухшие, красные или болезненные без видимой причины.
 Важно остановить прогрессирование инфекции до того, как будут затронуты ткани десны и кости челюсти. Также очень важно лечить инфекцию до того, как она попадет в кровоток в другие части тела.
Важно остановить прогрессирование инфекции до того, как будут затронуты ткани десны и кости челюсти. Также очень важно лечить инфекцию до того, как она попадет в кровоток в другие части тела.
-
Более длинные зубы – Пародонтоз может привести к рецессии десны. Токсины, вырабатываемые бактериями, могут разрушать поддерживающие ткани и кости, из-за чего зубы выглядят длиннее, а улыбка – более «зубастой».
-
Неприятный запах изо рта/неприятный запах изо рта – Хотя запах изо рта может исходить от задней части языка, легких и желудка, пищи, которую мы потребляем, или от употребления табака, неприятный запах изо рта также может быть вызван старыми частицами пищи, которые находятся между зубами и под десной. Более глубокие карманы десен могут содержать больше мусора и бактерий, вызывающих неприятный запах.
-
Шатающиеся зубы/изменение прикуса – Признаком быстро прогрессирующего пародонтита является расшатывание или смещение зубов в пораженной области.
 По мере разрушения костной ткани зубы, которые когда-то были прочно прикреплены к челюстной кости, расшатываются или могут сместиться.
По мере разрушения костной ткани зубы, которые когда-то были прочно прикреплены к челюстной кости, расшатываются или могут сместиться.
-
Гной – Гной, просачивающийся из межзубных промежутков, является явным признаком прогрессирующей пародонтальной инфекции. Гной является результатом того, что организм пытается бороться с бактериальной инфекцией.
Лечение заболеваний пародонта
Крайне важно остановить прогрессирование заболеваний пародонта до того, как они вызовут дальнейшее повреждение тканей десны и челюстной кости. Стоматолог первоначально оценивает весь рот, чтобы установить прогресс заболевания. После постановки диагноза стоматолог может лечить бактериальную инфекцию антибиотиками в сочетании с нехирургическим или хирургическим лечением или с обоими.
В случае заболевания пародонта средней степени тяжести карманы (под линией десны) зубов будут полностью очищены от мусора с помощью процедуры, называемой скейлингом и шлифованием корней. Карманы могут быть заполнены антибиотиками, чтобы способствовать хорошему заживлению и убить оставшиеся бактерии.
Карманы могут быть заполнены антибиотиками, чтобы способствовать хорошему заживлению и убить оставшиеся бактерии.
Тяжелый пародонтит можно лечить несколькими способами, например:
-
Лазерная обработка – Может использоваться для уменьшения размера карманов между зубами и деснами.
-
Тканевая и костная пластика – При разрушении значительного количества костной или десневой ткани стоматолог может выбрать пересадку новой ткани путем введения мембраны для стимуляции роста ткани.
-
Операция по устранению карманов – Стоматолог может провести «лоскутную операцию» для непосредственного уменьшения размера десневых карманов.
Если у вас есть дополнительные вопросы о признаках и симптомах заболеваний пародонта, свяжитесь с нами!
Виды заболеваний пародонта | Gladewater, Texas
Дом
Заболевание пародонта (также известное как пародонтит и болезнь десен ) — это прогрессирующее заболевание, поражающее опорную и окружающую ткань десны, а также подлежащую челюстную кость. Если не лечить заболевание пародонта, оно может привести к расшатыванию, нестабильности зубов и даже их потере. Заболевания пародонта на самом деле являются основной причиной потери зубов у взрослых в развитых странах, и к ним нельзя относиться легкомысленно.
Если не лечить заболевание пародонта, оно может привести к расшатыванию, нестабильности зубов и даже их потере. Заболевания пародонта на самом деле являются основной причиной потери зубов у взрослых в развитых странах, и к ним нельзя относиться легкомысленно.
Заболевание пародонта начинается, когда токсины, содержащиеся в зубном налете, начинают атаковать мягкие или десневые ткани, окружающие зубы. Эта бактерия внедряется в десну и быстро размножается, вызывая бактериальную инфекцию. По мере прогрессирования инфекции она начинает проникать глубже в ткани, вызывая воспаление или раздражение между зубами и деснами. Реакцией организма является разрушение инфицированной ткани, поэтому десны опускаются. Образовавшиеся карманы между зубами углубляются, и, если лечение не проводится, ткань, из которой состоит челюстная кость, также отступает, что приводит к нестабильности зубов и потере зубов.
Типы заболеваний пародонта
Существует множество разновидностей заболеваний пародонта и множество способов проявления этих вариаций. Все они требуют немедленного лечения у пародонтолога, чтобы остановить прогрессирование и сохранить ткань десны и кость.
Все они требуют немедленного лечения у пародонтолога, чтобы остановить прогрессирование и сохранить ткань десны и кость.
Вот некоторые из наиболее распространенных заболеваний пародонта, а также методы лечения, обычно применяемые для их устранения:
Гингивит
Гингивит — самая легкая и наиболее распространенная форма пародонтита. Это вызвано токсинами в зубном налете и приводит к заболеваниям пародонта. Люди с повышенным риском развития гингивита включают беременных женщин, женщин, принимающих противозачаточные таблетки, людей с неконтролируемым диабетом, потребителей стероидов и людей, которые контролируют судороги и артериальное давление с помощью лекарств.
Лечение: гингивит легко вылечить с помощью надежного сочетания домашнего ухода и профессиональной чистки. Стоматолог может выполнить процедуры полировки корней и глубокого удаления зубного камня, чтобы очистить карманы от мусора. Комбинация антибиотиков и лекарственных средств для полоскания рта может быть использована для уничтожения любых оставшихся бактерий и способствует хорошему заживлению карманов.
Комбинация антибиотиков и лекарственных средств для полоскания рта может быть использована для уничтожения любых оставшихся бактерий и способствует хорошему заживлению карманов.
Хронические заболевания пародонта
Хронические заболевания пародонта являются наиболее распространенной формой заболевания и гораздо чаще встречаются у людей старше 45 лет. Хронические заболевания пародонта характеризуются воспалением ниже линии десны и прогрессирующим разрушением десны и костная ткань. Может показаться, что зубы постепенно растут в длину, но на самом деле десны постепенно опускаются.
Лечение: К сожалению, в отличие от гингивита, хроническое заболевание пародонта не может быть полностью излечено, поскольку поддерживающая ткань не может быть восстановлена. Тем не менее, стоматолог может остановить прогрессирование заболевания, используя процедуры удаления зубного камня и полировки корней в сочетании с антимикробным лечением. При необходимости пародонтолог может провести хирургическое лечение, такое как операция по уменьшению кармана, а также тканевые трансплантаты для укрепления кости и улучшения эстетического вида полости рта.
При необходимости пародонтолог может провести хирургическое лечение, такое как операция по уменьшению кармана, а также тканевые трансплантаты для укрепления кости и улучшения эстетического вида полости рта.
Агрессивное заболевание пародонта
Агрессивное заболевание пародонта характеризуется быстрой потерей прикрепления десны, быстрой потерей костной ткани и семейной агрегацией. Само заболевание по сути такое же, как хронический пародонтит, но прогрессирование происходит намного быстрее. Курильщики и лица с семейным анамнезом этого заболевания подвергаются повышенному риску развития агрессивного периодонтита.
Лечение. Лечение агрессивного пародонтоза такое же, как и лечение хронического пародонтита, но при агрессивном пародонтите гораздо чаще требуется хирургическое вмешательство. Эту форму заболевания труднее остановить и вылечить, но стоматолог выполнит удаление зубного камня, полировку корней, противомикробные и, в некоторых случаях, лазерные процедуры, пытаясь сохранить ценные ткани и кости.
Заболевание пародонта, связанное с системными заболеваниями
Заболевание пародонта может быть симптомом заболевания или состояния, поражающего остальную часть тела. В зависимости от основного заболевания заболевание может вести себя как агрессивное заболевание пародонта, быстро разрушая ткани. Сердечно-сосудистые заболевания, диабет и респираторные заболевания являются наиболее распространенными сопутствующими факторами, хотя есть и много других. Даже в тех случаях, когда зубы покрыты небольшим налетом, многие заболевания усиливают и ускоряют прогрессирование заболеваний пародонта.
Лечение: Первоначально необходимо контролировать состояние здоровья, вызвавшее начало заболевания пародонта. Стоматолог остановит прогрессирование заболевания, используя те же методы лечения, которые используются для борьбы с агрессивными и хроническими заболеваниями пародонта.
Некротическая болезнь пародонта
Эта форма заболевания быстро прогрессирует и чаще встречается у людей, страдающих ВИЧ, иммуносупрессией, недоеданием, хроническим стрессом или курящих. Отмирание тканей (некроз) часто поражает периодонтальную связку, ткани десны и альвеолярную кость.
Отмирание тканей (некроз) часто поражает периодонтальную связку, ткани десны и альвеолярную кость.
Лечение: Некротизирующие заболевания пародонта встречаются крайне редко. Поскольку это может быть связано с ВИЧ или другим серьезным заболеванием, вероятно, стоматолог проконсультируется с врачом перед началом лечения. Для лечения этой формы заболевания обычно используются скейлинг, строгание корней, таблетки с антибиотиками, лекарственные жидкости для полоскания рта и фунгицидные препараты.
Если у вас есть какие-либо вопросы или опасения по поводу различных типов заболеваний пародонта и методов лечения, обратитесь к своему стоматологу.
Назад
Клонирование и характеристика основного поверхностного белка (MspTL) Treponema lecithinolyticum, ассоциированного с быстро прогрессирующим пародонтитом | FEMS Microbiology Letters
Abstract
Ген, кодирующий главный поверхностный белок (MspTL) Treponema lecithinolyticum , пародонтопатогена, был клонирован и секвенирован. Ген mspTL имеет открытую рамку считывания (ORF) длиной 1770 п.н., кодирующую белок из 590 аминокислот с расчетной молекулярной массой 65 кДа, который имеет типичную для прокариотов сигнальную последовательность (19).аминокислоты). MspTL показал высокий уровень гомологии с главным белком оболочки (MspA) Treponema maltophilum , филогенетически ближайшим родственником T. lecithinolyticum . Саузерн-блоттинг показал, что ген mspTL существует в единственной копии, а нозерн-блоттинг показал, что транскрипт mspTL является моноцистронным. Другая ORF, расположенная ниже mspTL , имела ту же ориентацию и кодировала предполагаемый белок, в котором первый N-концевой 29была идентифицирована 1 аминокислота. Гомологическая область этого белка также является частью локуса T. maltophilum mspA .
Ген mspTL имеет открытую рамку считывания (ORF) длиной 1770 п.н., кодирующую белок из 590 аминокислот с расчетной молекулярной массой 65 кДа, который имеет типичную для прокариотов сигнальную последовательность (19).аминокислоты). MspTL показал высокий уровень гомологии с главным белком оболочки (MspA) Treponema maltophilum , филогенетически ближайшим родственником T. lecithinolyticum . Саузерн-блоттинг показал, что ген mspTL существует в единственной копии, а нозерн-блоттинг показал, что транскрипт mspTL является моноцистронным. Другая ORF, расположенная ниже mspTL , имела ту же ориентацию и кодировала предполагаемый белок, в котором первый N-концевой 29была идентифицирована 1 аминокислота. Гомологическая область этого белка также является частью локуса T. maltophilum mspA .
Белок наружной мембраны, Оральный Трепонема , Пародонтит, Treponema lecithinolyticum
1 Введение
Оральные трепонемы гетерогенны, и известно, что некоторые из них тесно связаны с заболеваниями пародонта [5,16]. Сообщалось, что поверхностные белки оральных трепонем оказывают разнообразные цитопатические эффекты на несколько типов клеток, таких как эпителиальные клетки, фибробласты, макрофаги или полиморфноядерные лейкоциты (PMN) [6,12,15,18,22]. Основные поверхностные белки (Msps) трепонем ротовой полости гетерогенны в отношении их антигенности и мономерной молекулярной массы в диапазоне от 42 до 64 кДа [9].,10,23,24]. Но известно, что они обладают некоторыми общими физическими и функциональными характеристиками.
Сообщалось, что поверхностные белки оральных трепонем оказывают разнообразные цитопатические эффекты на несколько типов клеток, таких как эпителиальные клетки, фибробласты, макрофаги или полиморфноядерные лейкоциты (PMN) [6,12,15,18,22]. Основные поверхностные белки (Msps) трепонем ротовой полости гетерогенны в отношении их антигенности и мономерной молекулярной массы в диапазоне от 42 до 64 кДа [9].,10,23,24]. Но известно, что они обладают некоторыми общими физическими и функциональными характеристиками.
Msp Treponema denticola , который является наиболее интенсивно изучаемым видом среди оральных трепонем, был идентифицирован как адгезины [7,8] или порообразующие молекулы [15]. Также сообщалось, что T. denticola Msp запускает специфическое высвобождение матриксных металлопротеиназ (ММП) из PMN человека и участвует в их активации [6]. Таким образом, считается, что поверхностные белки участвуют в патогенезе заболеваний пародонта, включая деградацию внеклеточного матрикса ММР, и накопление данных о поверхностных белках должно дать больше информации об их структурных и функциональных характеристиках. Это может способствовать пониманию патогенеза оральных трепонем при заболеваниях пародонта.
Это может способствовать пониманию патогенеза оральных трепонем при заболеваниях пародонта.
Treponema lecithinolyticum — недавно описанная пероральная трепонема, проявляющая сильную фосфолипазную активность [27]. Молекулярно-эпидемиологическое исследование показало, что этот новый вид с высокой частотой присутствует в образцах поддесневого зубного налета у пациентов с быстро прогрессирующим пародонтитом [16,27].
Целью данного исследования было клонирование и характеристика Msp T. lecithinolyticum . Мы идентифицировали Msp T. lecithinolyticum , обозначенный как MspTL (590 аминокислотных остатков) путем клонирования геномной ДНК в векторе лямбда ZAP Express.
2 Materials and methods
2.1 Bacterial strains and cloning vectors
Treponema strains included in this study were T. lecithinolyticum (ATCC 700332), T. maltophilum (ATCC 51939), T. denticola (ATCC 33521), T. pectinovorum (ATCC 33768), T. socranskii subsp. buccale (ATCC 35534), T. socranskiy подвид. paredis (ATCC 35535), T. socranskiy subsp. socranskiy (ATCC 35536) и T. vincentii (ATCC 35580). Все штаммов Treponema выращивали в анаэробных условиях на среде OMIZ-Pat, как описано ранее [27]. Чистоту культур проверяли с помощью фазово-контрастной микроскопии. Вектор
maltophilum (ATCC 51939), T. denticola (ATCC 33521), T. pectinovorum (ATCC 33768), T. socranskii subsp. buccale (ATCC 35534), T. socranskiy подвид. paredis (ATCC 35535), T. socranskiy subsp. socranskiy (ATCC 35536) и T. vincentii (ATCC 35580). Все штаммов Treponema выращивали в анаэробных условиях на среде OMIZ-Pat, как описано ранее [27]. Чистоту культур проверяли с помощью фазово-контрастной микроскопии. Вектор
Lambda ZAP Express™, предварительно расщепленный штаммом Eco RI (Stratagene, Ла-Хойя, Калифорния, США) и штаммом Escherichia coli XL1-Blue MRF’, использовали для клонирования и создания геномной библиотеки Т. лецитинолитический . Штамм E. coli XLOLR использовали для вырезания in vivo фагемидного вектора pBK-CMV из экспресс-вектора лямбда ZAP. Штаммы E. coli культивировали в среде LB с добавлением 12,5 мкг/мл -1 тетрациклина.
2.2 Иммунизация и очистка поликлональных антител
Трехдневную культуру (200 мл) T. lecithinolyticum собирали центрифугированием при 5000× g в течение 10 мин (4°C) и промывали фосфатом -забуференный физиологический раствор (PBS). Осадок клеток суспендировали в небольшом объеме PBS и обрабатывали ультразвуком с помощью ультразвука в течение 3 мин при выходной мощности 10 Вт с интервалом 30 с. Концентрации белка определяли с использованием реагента для анализа белка кумасси (Pierce Chemical Co., Рокфорд, Иллинойс, США). Кур-несушек (белый леггорн, возраст 21 неделя) иммунизировали внутримышечно Целые клетки T. lecithinolyticum , обработанные ультразвуком (1 мг белка), эмульгированные в 0,5 мл адъюванта (Specol, Институт зоотехники и здоровья, Лелистад, Нидерланды). Были сделаны две бустерные инъекции с интервалом в 3 недели. Яйца собирали через 10 дней после последней бустерной инъекции и хранили при 4°C до использования.
Яичные желтки отделены от белков. После удаления липидной оболочки желтковую смесь разбавляли четырьмя объемами дистиллированной воды, а затем многократно (четыре раза) замораживали и оттаивали. Антитело получали центрифугированием при 5000× г в течение 30 мин и осаждали сульфатом аммония, как описано ранее [19]. Для удаления антител, перекрестно реагирующих с антигенами E. coli , антитела желтка адсорбировали против озвучивания целых клеток E. coli XL1-Blue MRF’ с помощью аффинной хроматографии с использованием активированной бромцианом сефарозы 4B, как описано ранее [19]. Элюат, содержащий очищенный анти- T. lecithinolyticum IgY, хранили при -20°C до использования.
2.3 Конструирование и иммуноскрининг геномной библиотеки
Культуру T. lecithinolyticum (200 мл), выращенную до экспоненциальной фазы, собирали и промывали, как описано выше. Хромосомную ДНК экстрагировали по стандартному протоколу [19] и частично расщепляли рестриктазами Hae III, Rsa I и Alu I. Фрагменты ДНК размером от 2 до 10 т.п.н. очищали из агарозных гелей с использованием набор для извлечения из геля (Qiagen, Валенсия, США). После прикрепления адаптеров Eco RI к очищенным фрагментам ДНК их лигировали в вектор лямбда ZAP Express, предварительно расщепленный Eco RI и упакованный с комплектом для клонирования Gigapack II Gold (Stratagene, Ла-Хойя, Калифорния, США). Библиотеку высевали на E. coli XL1-Blue MRF’ и планшеты инкубировали в течение ночи при 37°C. Нитроцеллюлозные фильтры, пропитанные 10 мМ изопропил-β-d-тиогалактопиранозидом (ИПТГ), наслаивали на агар чашек и инкубировали при 37°С еще 4 часа. Затем фильтры снимали с планшетов и инкубировали в блокирующем буфере (ТНТ: 10 мМ Трис-HCl (pH 8,0), 150 мМ NaCl, 0,05% Tween 20 и 3% бычий сывороточный альбумин (БСА)) в течение 30 мин. Затем фильтры инкубировали в блокирующем буфере, содержащем анти- T. lecithinolyticum IgY на 1 час. После промывки TNT, содержащим 0,1% BSA, фильтры инкубировали в течение 1 ч в PBS, содержащем конъюгированный со щелочной фосфатазой (AP) козий антикуриный IgY (Jackson ImmunoResearch, West Grove, PA, USA) в разведении 1:1000.
Фрагменты ДНК размером от 2 до 10 т.п.н. очищали из агарозных гелей с использованием набор для извлечения из геля (Qiagen, Валенсия, США). После прикрепления адаптеров Eco RI к очищенным фрагментам ДНК их лигировали в вектор лямбда ZAP Express, предварительно расщепленный Eco RI и упакованный с комплектом для клонирования Gigapack II Gold (Stratagene, Ла-Хойя, Калифорния, США). Библиотеку высевали на E. coli XL1-Blue MRF’ и планшеты инкубировали в течение ночи при 37°C. Нитроцеллюлозные фильтры, пропитанные 10 мМ изопропил-β-d-тиогалактопиранозидом (ИПТГ), наслаивали на агар чашек и инкубировали при 37°С еще 4 часа. Затем фильтры снимали с планшетов и инкубировали в блокирующем буфере (ТНТ: 10 мМ Трис-HCl (pH 8,0), 150 мМ NaCl, 0,05% Tween 20 и 3% бычий сывороточный альбумин (БСА)) в течение 30 мин. Затем фильтры инкубировали в блокирующем буфере, содержащем анти- T. lecithinolyticum IgY на 1 час. После промывки TNT, содержащим 0,1% BSA, фильтры инкубировали в течение 1 ч в PBS, содержащем конъюгированный со щелочной фосфатазой (AP) козий антикуриный IgY (Jackson ImmunoResearch, West Grove, PA, USA) в разведении 1:1000. После трех промывок в PBS/0,2% Tween 20 мембраны проявляли 5-бром-4-хлор-3-индолилфосфатом (165 мкг мл -1 ) и нитросиним тетразолием (330 мкг мл -1 ). Бляшки, показывающие сильные положительные реакции, были отобраны и дополнительно проанализированы. Фагемиды pBK-CMV, содержащие 9ДНК-вставки 0927 T. lecithinolyticum вырезали in vivo из экспресс-вектора лямбда ZAP с интерференционно-устойчивым хелперным фагом ExAssist в соответствии с инструкциями производителя (Stratagene, La Jolla, CA, USA). Полученные фагмиды очищали согласно протоколам минипрепарата плазмидной ДНК [19]. Фагемида pBK-CMV, несущая фрагмент ДНК T. lecithinolyticum длиной 2,5 т.п.н., была обозначена как pTL6-2.
После трех промывок в PBS/0,2% Tween 20 мембраны проявляли 5-бром-4-хлор-3-индолилфосфатом (165 мкг мл -1 ) и нитросиним тетразолием (330 мкг мл -1 ). Бляшки, показывающие сильные положительные реакции, были отобраны и дополнительно проанализированы. Фагемиды pBK-CMV, содержащие 9ДНК-вставки 0927 T. lecithinolyticum вырезали in vivo из экспресс-вектора лямбда ZAP с интерференционно-устойчивым хелперным фагом ExAssist в соответствии с инструкциями производителя (Stratagene, La Jolla, CA, USA). Полученные фагмиды очищали согласно протоколам минипрепарата плазмидной ДНК [19]. Фагемида pBK-CMV, несущая фрагмент ДНК T. lecithinolyticum длиной 2,5 т.п.н., была обозначена как pTL6-2.
2.4 Приготовление фракции наружной мембраны (OMF)
Для получения OMF клетки T. lecithinolyticum собирали центрифугированием при 6000× g в течение 10 мин при 4°C и суспендировали в PBS. Суспензии подвергали осторожному встряхиванию и центрифугировали при 6000× g в течение 15 мин при 4°С. Супернатанты, содержащие наружную мембрану, осаждали центрифугированием при 29 000× g в течение 30 мин при 4°С.
Суспензии подвергали осторожному встряхиванию и центрифугировали при 6000× g в течение 15 мин при 4°С. Супернатанты, содержащие наружную мембрану, осаждали центрифугированием при 29 000× g в течение 30 мин при 4°С.
2,5 SDS-электрофорез в полиакриламидном геле (SDS-PAGE) и иммуноблоттинг
SDS-PAGE проводили по стандартной методике, как описано ранее [19].]. После SDS-PAGE белки окрашивали кумасси бриллиантовым синим. Для иммуноблоттинга белки, разделенные с помощью SDS-PAGE (10% гель), переносили электрофоретически на нитроцеллюлозные мембраны с использованием полусухого блоттинга (Trans-Blot × SD, Bio-Rad, Hercules, CA, USA), блокировали 5% обезжиренного молока в PBS/0,2% Tween 20 и инкубировали с анти- T. lecithinolyticum IgY или моноспецифическим антителом, реагирующим с укороченным рекомбинантным MspTL (trMspTL; см. ниже) в течение 1 часа. Остальные процедуры выполняли, как описано для иммуноскрининга геномной библиотеки. В некоторых случаях мембраны окрашивали 0,1% амидочерью в течение 1 мин.
В некоторых случаях мембраны окрашивали 0,1% амидочерью в течение 1 мин.
2.6 Экстракция MspTL детергентами и химикатами
Целые клетки или аликвоты T. lecithinolyticum OMF (10 мкг белка) обрабатывали 0,1 М Na 2 CO 3 , 0,6 М NaCl и 0,6 М NaCl. , которые, как известно, удаляют периферические белки с мембраны.
2.7 Аффинная очистка моноспецифического антитела против trMspTL
Моноспецифическое антитело, реагирующее с trMspTL, получали аффинной очисткой из анти- T. lecithinolyticum IgY. Соникаты E. coli , содержащие pTL6-2, подвергали SDS-PAGE и переносили на нитроцеллюлозные мембраны. Контрольную дорожку вырезали и trMspTL локализовали с помощью иммуноблоттинга с использованием анти- T. lecithinolyticum IgY. Кусок мембраны, соответствующий trMspTL, вырезали, блокировали 5% обезжиренным молоком и инкубировали с анти- T. lecithinolyticum IgY при комнатной температуре в течение 5 часов. Антитело, реагирующее с trMspTL, элюировали путем инкубации с элюирующим буфером (0,2 М глицина, рН 2,8 и 1 мМ EGTA) при комнатной температуре в течение 20 мин. Элюат нейтрализовали 1/10 объема 1 М трис-основания. После добавления 1/10 объема 10×PBS и азида натрия (0,02%) аффинно-очищенное антитело хранили при 4°C до использования для иммуноблоттинга.
lecithinolyticum IgY при комнатной температуре в течение 5 часов. Антитело, реагирующее с trMspTL, элюировали путем инкубации с элюирующим буфером (0,2 М глицина, рН 2,8 и 1 мМ EGTA) при комнатной температуре в течение 20 мин. Элюат нейтрализовали 1/10 объема 1 М трис-основания. После добавления 1/10 объема 10×PBS и азида натрия (0,02%) аффинно-очищенное антитело хранили при 4°C до использования для иммуноблоттинга.
2.8 ПЦР-амплификация и анализ последовательности
ПЦР-амплификацию проводили для получения 5′-конца гена mspTL с использованием специфического праймера (PR1: 5′-AAA CGC CAT AGA TAA AGG TGG AAT-3′) и вырожденный праймер (PF1: 5′-CCG GTA AAA TCT GTA TTT TTC GGC TTC-3′), полученный из гомологичной области геномной последовательности T. maltophilum (K. Heuner, неопубликованные данные). Реакционная смесь содержала по 20 пмоль каждого праймера, 200 мкМ смеси dNTP, 2,5 ЕД Taq ДНК-полимераза и реакционный буфер в общем объеме 100 мкл. Затем проводили ПЦР в термоциклере в течение 30 циклов: стадия денатурации при 95°С в течение 1 мин, стадия отжига при 60°С в течение 1 мин и стадия удлинения при 72°С в течение 1 мин.
Затем проводили ПЦР в термоциклере в течение 30 циклов: стадия денатурации при 95°С в течение 1 мин, стадия отжига при 60°С в течение 1 мин и стадия удлинения при 72°С в течение 1 мин.
Секвенирование нуклеотидов проводили с использованием набора для циклического секвенирования с флуоресцентно-мечеными дидезоксинуклеозидтрифосфатами (Applied Biosystems, Inc., Фостер-Сити, Калифорния, США) и автоматического секвенатора ДНК (Applied Biosystems, модель 373A). И нуклеотидная, и выведенная аминокислотная последовательности сравнивались со всеми записями в текущих базах данных, включая SWISS-PROT, PIR, EMBL и GenBank, с использованием программ FASTA [17] и BLAST [1].
Для Саузерн- и Нозерн-блот-гибридизации меченный дигоксигенином (DIG) зонд, охватывающий всю кодирующую область гена mspTL , был получен в реакции ПЦР с использованием DIG-11-dUTP (Boehringer Mannheim, Germany). Реакционная смесь для ПЦР (100 мкл) содержала по 20 пмоль каждого праймера (PmspF1: 5′-TTA TGA AAA AGA TCC TTG CAT-3′; PmspR1: 5′-CAG AGC GAT TTT CGC CTT T-3′, рис. 1А) , 200 мкМ каждого из dATP, dGTP, dCTP и 140 мкМ dTTP, 60 мкМ DIG-dUTP, 2,5 ед. ДНК-полимеразы Taq и реакционный буфер. Для ПЦР был выбран тот же температурный цикл, что и описанный выше. Продукт ПЦР фильтровали с использованием концентратора с отсечением по молекулярной массе 30 кДа (Centricon 30, Amicon, Денвер, Колорадо, США) для удаления праймеров.
1А) , 200 мкМ каждого из dATP, dGTP, dCTP и 140 мкМ dTTP, 60 мкМ DIG-dUTP, 2,5 ед. ДНК-полимеразы Taq и реакционный буфер. Для ПЦР был выбран тот же температурный цикл, что и описанный выше. Продукт ПЦР фильтровали с использованием концентратора с отсечением по молекулярной массе 30 кДа (Centricon 30, Amicon, Денвер, Колорадо, США) для удаления праймеров.
1
Открыть в новой вкладкеСкачать слайд
Рестрикционная карта геномного участка mspTL (A) и нуклеотидная последовательность некодирующих участков гена mspTL (B). Показаны вставка размером 2,5 т.п.н. (pTL6-2) и ПЦР-фрагмент, амплифицированный с 5′-конца mspTL . ORFU1 расположен ниже гена mspTL . Обозначены сайты рестрикции: E для Eco RI, H для Hin dIII, Ha для Hae III, K для Kpn I, P для Pst I и S для Sma I. PF1 и PR1 являются праймерами, используемыми для ПЦР для получения 5′-конца гена mspTL , а PmspF1 и PmspR1 для полногенного зонда, используемого для Саузерн- и Нозерн-блоттинга. Инициирующий и стоп-кодон гена mspTL выделены жирным шрифтом. Показаны консенсусный сайт связывания рибосомы (RBS) и инвертированные повторы (подчеркнуты) ниже остановки трансляции.
Инициирующий и стоп-кодон гена mspTL выделены жирным шрифтом. Показаны консенсусный сайт связывания рибосомы (RBS) и инвертированные повторы (подчеркнуты) ниже остановки трансляции.
2.9 Саузерн-блот-гибридизация и нозерн-блот-анализ
Для Саузерн-блот-гибридизации геномную ДНК T. lecithinolyticum расщепляли с помощью Hin dIII и Pst I соответственно. Фрагменты разделяли на 0,8% агарозном геле и переносили на нейлоновую мембрану в 20×SSC (175,3 г NaCl и 88,2 г цитрата натрия, растворенные в 1 л dH 2 O). После иммобилизации ДНК путем УФ-сшивки (254 нм, 3 мин) проводили прегибридизацию при 65°С в течение 1 ч в растворе для гибридизации (5×SSC, 0,1% N -лауроилсаркозин, 0,02% SDS, 1% блокирующий реагент (Boehringer Mannheim, Германия)). После добавления 30 мкл меченного DIG ПЦР-зонда, денатурированного нагреванием в течение 5 мин при 100°С, проводили гибридизацию при 65°С в течение ночи. Мембрану дважды промывали при 65°C в течение 15 мин в промывочном растворе (0,1×SSC, 0,1% SDS). Гибридизированные зонды детектировали с помощью AP-конъюгированного анти-DIG-антитела и хемилюминесцентного субстрата для AP с использованием набора для люминесцентной детекции DIG (Boehringer Mannheim, Германия).
Мембрану дважды промывали при 65°C в течение 15 мин в промывочном растворе (0,1×SSC, 0,1% SDS). Гибридизированные зонды детектировали с помощью AP-конъюгированного анти-DIG-антитела и хемилюминесцентного субстрата для AP с использованием набора для люминесцентной детекции DIG (Boehringer Mannheim, Германия).
Для нозерн-блоттинга общую РНК T. lecithinolyticum выделяли с использованием Trizol (Life Technologies, Rockville, MD, USA), монофазного раствора фенола и гуанидинизотиоцианата. Т. lecithinolyticum (50 мл), выросшие до экспоненциальной фазы, собирали, как описано выше. Осадок клеток ресуспендировали в 1 мл реагента Trizol, лизировали повторным пипетированием и проводили последующую экстракцию в соответствии с инструкциями производителя. Количество РНК определяли по поглощению при 260 нм. РНК (20 мкг) подвергали электрофорезу на 1% агарозном геле, содержащем формальдегид, как описано ранее [19].]. После электрофореза гель промывали в dH 2 O без РНКазы, а затем погружали в 20×SSC. РНК переносили на нитроцеллюлозную мембрану капиллярной элюцией в 20×SSC и затем иммобилизовали УФ-облучением (254 нм, 3 мин). Мембрану гибридизовали с ПЦР-зондом, меченным DIG, как описано в Саузерн-блот-анализе.
РНК переносили на нитроцеллюлозную мембрану капиллярной элюцией в 20×SSC и затем иммобилизовали УФ-облучением (254 нм, 3 мин). Мембрану гибридизовали с ПЦР-зондом, меченным DIG, как описано в Саузерн-блот-анализе.
2.10 Нуклеотидная последовательность инвентарного номера
Нуклеотидная последовательность гена mspTL была отправлена в GenBank под инвентарным номером AY026951.
3 Результаты
3.1 Выделение и секвенирование гена
mspTL Геномную библиотеку T. lecithinolyticum в векторе лямбда ZAP Express подвергали скринингу с анти- T. lecithinolytic Ig0927 Tum lecitholyticum . Было отобрано несколько рекомбинантных лямбда-фагов с сильным сигналом и секвенированы вставки. Когда полученные аминокислотные последовательности сравнивали с помощью программ FASTA и BLAST, одна из них показала значительную гомологию с T. maltophilum mspA 9.0928 и был дополнительно проанализирован. Фагемидный вектор pBK-CMV, содержащий эту вставку, был обозначен pTL6-2 (фиг. 1А) и вырезан in vivo из рекомбинантного фага лямбда. pTL6-2 содержал вставку размером 2,5 т.п.н., которая состояла из двух укороченных открытых рамок считывания (ORF), разделенных 133 п.н. ORF, которая показала значительную гомологию с T. maltophilum mspA , не имела 5′-конца гена, который был получен с помощью ПЦР-амплификации из T. lecithinolyticum геномной ДНК с использованием одного вырожденного и одного специфического праймера. Полученный продукт ПЦР секвенировали. Объединив эту последовательность с последовательностью укороченного гена, была получена полная ORF из 1770 п.н. (кодирующая MspTL), и полный ген был обозначен как 9.0927 мспТЛ . Рестрикционная карта локуса mspTL показана на рис. 1А. Консенсусный сайт связывания рибосомы (AAGGAGG) располагался на 14 п.н. выше инициирующего кодона ATG. Последовательность ниже стоп-кодона ТАА представляет собой инвертированные повторы, за которыми следует цепочка Т-остатков, типичный ро-независимый терминатор транскрипции (рис.
maltophilum mspA 9.0928 и был дополнительно проанализирован. Фагемидный вектор pBK-CMV, содержащий эту вставку, был обозначен pTL6-2 (фиг. 1А) и вырезан in vivo из рекомбинантного фага лямбда. pTL6-2 содержал вставку размером 2,5 т.п.н., которая состояла из двух укороченных открытых рамок считывания (ORF), разделенных 133 п.н. ORF, которая показала значительную гомологию с T. maltophilum mspA , не имела 5′-конца гена, который был получен с помощью ПЦР-амплификации из T. lecithinolyticum геномной ДНК с использованием одного вырожденного и одного специфического праймера. Полученный продукт ПЦР секвенировали. Объединив эту последовательность с последовательностью укороченного гена, была получена полная ORF из 1770 п.н. (кодирующая MspTL), и полный ген был обозначен как 9.0927 мспТЛ . Рестрикционная карта локуса mspTL показана на рис. 1А. Консенсусный сайт связывания рибосомы (AAGGAGG) располагался на 14 п.н. выше инициирующего кодона ATG. Последовательность ниже стоп-кодона ТАА представляет собой инвертированные повторы, за которыми следует цепочка Т-остатков, типичный ро-независимый терминатор транскрипции (рис. 1В).
1В).
Для определения количества копий гена mspTL ДНК T. lecithinolyticum расщепляли с помощью Hin 9.0928 dIII и Pst I, и исследовали с помощью цельногенного зонда, меченного DIG. Отсутствие сайтов Pst I внутри гена приводило к одной полосе, тогда как присутствие одного сайта Hin dIII внутри гена приводило к двум полосам (рис. 2А). Полоса Hin dIII размером около 2 т.п.н. соответствовала размеру рестрикционного фрагмента, показанного на фиг.1А. Результат подразумевает, что только одна копия гена mspTL присутствует в T. lecithinolyticum 9.0928 хромосома.
2
Открыть в новой вкладкеСкачать слайд
Саузерн-блоттинг (A) Hin dIII (дорожка 1) и Pst I (дорожка 2) расщепленной геномной ДНК T. lecithinolyticum . Для обнаружения гена mspTL использовали меченный DIG цельный генный зонд, полученный с помощью ПЦР. Нозерн-блоттинг (B) мРНК mspTL . Тотальную РНК (20 мкг) T. lecithinolyticum гибридизовали с тем же зондом, что и при Саузерн-блоттинге. Стандарты размеров молекул ДНК и РНК показаны справа.
Тотальную РНК (20 мкг) T. lecithinolyticum гибридизовали с тем же зондом, что и при Саузерн-блоттинге. Стандарты размеров молекул ДНК и РНК показаны справа.
Размер мРНК mspTL определяли с помощью Нозерн-блоттинга. Как показано на фиг. 2B, меченный DIG цельный генный зонд гибридизуется с одним транскриптом размером приблизительно 2 т.п.н., который включает кодирующую область mspTL размером 1770 п.н. . Этот размер соответствовал размеру транскрипта mspTL , рассчитанному по последовательности ДНК. Промотор и сайт начала транскрипции еще предстоит идентифицировать в богатой AT ДНК непосредственно выше mspTL .
Другая ORF (ORFU1, рис. 1A), расположенная ниже mspTL в той же ориентации, кодировала предполагаемый белок, в котором была идентифицирована первая N-концевая 291 аминокислота. Этот белок показал значительное сходство (52–57%) с консервативными гипотетическими белками различных бактерий, включая Methanococcus jannaschii (MJ0326), Pseudomonas aeruginosa (PA4719), Borrelia burgdorferi (BBB22) и Bacillus subtilis. (ЕББ). Функция 9Сообщалось, что белок 0927 P. aeruginosa является вероятным переносчиком [21]. Гомологичная область ORFU1 также входит в состав локуса T. maltophilum mspA [11].
(ЕББ). Функция 9Сообщалось, что белок 0927 P. aeruginosa является вероятным переносчиком [21]. Гомологичная область ORFU1 также входит в состав локуса T. maltophilum mspA [11].
3.2 Анализ пептида MspTL
Полный пептид MspTL содержал 590 аминокислот и имел расчетную молекулярную массу 65 кДа. Он имел типичную для прокариот сигнальную последовательность (19 аминокислотных остатков) с двумя положительно заряженными аминокислотами после первого метионина и гидрофобным ядром, предшествующим предполагаемому сайту расщепления сигнальной пептидазой I, расположенному между 19 остатками.и 20. Предполагаемый зрелый белок состоял из 571 аминокислоты с молекулярной массой 63 кДа. MspTL не содержит цистеина. Непроцессированный пептид показал наивысшую идентичность (53%) и сходство (59%) с T. maltophilum MspA, который, как сообщается, является термомодифицируемым, детергентно- и трипсин-стабильным белком основной оболочки [10]. На рис. 3 представлено попарное выравнивание MspTL и MspA.
На рис. 3 представлено попарное выравнивание MspTL и MspA.
3
Открыть в новой вкладкеСкачать слайд
Выравнивание аминокислотных последовательностей MspTL из T. lecithinolyticum и MspA T. maltophilum . Идентичные остатки (|), консервативные (:) или нейтральные замены (.) указаны между выровненными последовательностями. Номера остатков указаны справа от последовательностей аминокислот.
Индукция E. coli , несущих pTL6-2, с помощью IPTG приводила к экспрессии белка trMspTL с молекулярной массой приблизительно 60 кДа, лишенного 65-аминокислотного N-конца зрелого нативного MspTL, как показано на анализ последовательности нуклеотидов. Уникальная полоса 60 кДа, представляющая этот белок, была визуализирована с помощью SDS-PAGE и идентифицирована с помощью иммуноблоттинга с использованием анти- T. lecithinolyticum антитела IgY (рис. 4). Аффинно-очищенные антитела, специфичные к trMspTL, реагировали только с белком массой 63 кДа цельноклеточных ультразвуковых препаратов T. lecithinolyticum (рис. 5). Этот белок массой 63 кДа является наиболее распространенным белком в OMF T. lecithinolyticum .
lecithinolyticum (рис. 5). Этот белок массой 63 кДа является наиболее распространенным белком в OMF T. lecithinolyticum .
4
Открыть в новой вкладкеСкачать слайд
Идентификация MspTL с помощью SDS-PAGE (A) и иммуноблота (B). Белки разделяли методом SDS-PAGE и переносили на нитроцеллюлозную мембрану. Мембрану разрезали пополам, одна половина была окрашена амидо-черным, а другая реагировала с анти- Т. lecithinolyticum IgY. Дорожки: 1, ультразвуковые препараты целых клеток T. lecithinolyticum ; 2, OMF T. lecithinolyticum ; 3, обработанные ультразвуком целые клетки E. coli XLORL/pTL6-2.
5
Открыть в новой вкладкеСкачать слайд
SDS-PAGE (A) и иммуноблот (B) озоновых препаратов цельных трепонемных клеток (10 мкг). Дорожки: 1, Т. denticola ; 2, еще не классифицированный оральный Treponema sp.; 3, Т. lecithinolyticum ; 4, Т. maltophilum ; 5, Т. pectinovorum ; 6, T. socranskiy subsp. буккаль ; 7, T. socranskiy subsp. Паредис ; 8, T. socranskiy subsp. сокранский ; 9, Т. vincentii . Аффинно-очищенные антитела, специфичные к trMspTL, использовали для иммуноблоттинга.
pectinovorum ; 6, T. socranskiy subsp. буккаль ; 7, T. socranskiy subsp. Паредис ; 8, T. socranskiy subsp. сокранский ; 9, Т. vincentii . Аффинно-очищенные антитела, специфичные к trMspTL, использовали для иммуноблоттинга.
Обработка OMF или целых клеток T. lecithinolyticum 0,1 М Na 2 CO 3 , 0,6 М NaCl или 1,6 М мочевины для удаления периферических белков из мембраны не приводила к выделению MspTL ( данные не показаны).
MspTL содержал последовательность прикрепления клеток (RGD в положении 312) и два предполагаемых сайта гликозилирования (Asn-X-Ser/Thr) (положение 46: NRT; положение 543: NTT).
4 Обсуждение
В этом исследовании мы клонировали, секвенировали и анализировали белок внешней мембраны, названный MspTL, из T. lecithinolyticum . Анализ SDS-PAGE и иммуноблоттинг показали, что MspTL является основным компонентом OMF, высвобождаемым из целых клеток при осторожном встряхивании. Хорошо известно, что наружные мембраны трепонем хрупкие, и промывание их в PBS высвобождает наружные мембраны [2].
Хорошо известно, что наружные мембраны трепонем хрупкие, и промывание их в PBS высвобождает наружные мембраны [2].
Поиски в базе данных показали, что MspTL показывает самую высокую степень гомологии (идентичность 53%) с MspA, ассоциированным с внешней оболочкой T. maltophilum [10]. Основываясь на филогенетическом анализе с использованием сравнения последовательностей 16S рРНК, T. maltophilum наиболее тесно связан с T. lecithinolyticum [4], что означает, что филогенетические отношения, установленные с помощью анализа 16S рРНК, могут быть применены к другим генам в тех же организмах. . MspTL показал только около 30% идентичности с Msps T. denticola ATCC 33520 и ATCC 35405.
Гомологическая область ORFU1 также входит в состав локуса T. maltophilum mspA [10]. ORFU1, расположенный ниже mspTL , показал значительную гомологию с ORF 431 (45 кДа) T. maltophilum , которая также расположена ниже гена mspA [11]. Хотя T. lecithinolyticum не обладал геном, гомологичным ORF 262 (30 кДа) T. maltophilum , расположенным между mspA и ORF 431, близость этих генов и их гомологов у T. lecithinolyticum указывает на степень структурной консервативности этих генов у двух видов. Полная длина ORFU1 была получена Heuner et al. и показал 85% идентичность и 93% сходство с ORF 431 T. maltophilum , который показал значительное сходство с консервативными интегральными мембранными белками различных бактерий [11]. Хойнер и др. показали, что mspA 9Область гена 0928 консервативна среди трепонем IV группы, включая T. lecithinolyticum и T. maltophilum [11].
Хотя T. lecithinolyticum не обладал геном, гомологичным ORF 262 (30 кДа) T. maltophilum , расположенным между mspA и ORF 431, близость этих генов и их гомологов у T. lecithinolyticum указывает на степень структурной консервативности этих генов у двух видов. Полная длина ORFU1 была получена Heuner et al. и показал 85% идентичность и 93% сходство с ORF 431 T. maltophilum , который показал значительное сходство с консервативными интегральными мембранными белками различных бактерий [11]. Хойнер и др. показали, что mspA 9Область гена 0928 консервативна среди трепонем IV группы, включая T. lecithinolyticum и T. maltophilum [11].
MspTL не содержит остатков цистеина. Этот факт перекликается с Msps некоторых других оральных трепонем [9,10]. Отсутствие остатков цистеина означает отсутствие любых возможных внутримолекулярных дисульфидных связей, которые могли бы способствовать нативной конформации белка.
Физические свойства того, что MspTL не был экстрагирован такими реагентами, как 0,1 М Na 2 CO 3 , 0,6 М NaCl и 1,6 М мочевины также наблюдали в MompA T. pectinovorum [23] и MspA T. maltophilum [10].
pectinovorum [23] и MspA T. maltophilum [10].
Связывание бактерий с клетками-хозяевами имеет решающее значение в патогенезе [7,8,25]. MspTL содержит последовательность Arg-Gly-Asp (RGD), которая отвечает за многие взаимодействия присоединения клеток [20] и может быть вовлечена во взаимодействие между T. lecithinolyticum и поверхностями клеток млекопитающих. В предварительном тесте с цельными бактериальными ультразвуковыми препаратами было обнаружено, что MspTL участвует в связывании с культивируемыми фибробластами десны человека (данные не представлены). Однако дальнейшее исследование с интактными 9Клетки 0927 T. lecithinolyticum необходимы для подтверждения того, что MspTL является ассоциированным с мембраной адгезином в нативной топологии.
Два потенциальных сайта гликозилирования, Asn-Arg-Thr и Asn-Thr-Thr, были идентифицированы в MspTL. Прокариотические гликопротеины встречаются у различных бактерий, включая белки S-слоя [14], жгутиковые белки [26] и белки внешней мембраны [13]. Сообщалось, что белок внешней оболочки T. denticola GM-1 64 кДа гликозилирован [24]. Сообщалось, что некоторые гликопротеины связаны со спайками [14] и синтезируются в качестве предшественников с сигнальным пептидом, который также показан в MspTL. Является ли MspTL гликозилированным, еще предстоит определить.
Сообщалось, что белок внешней оболочки T. denticola GM-1 64 кДа гликозилирован [24]. Сообщалось, что некоторые гликопротеины связаны со спайками [14] и синтезируются в качестве предшественников с сигнальным пептидом, который также показан в MspTL. Является ли MspTL гликозилированным, еще предстоит определить.
Таким образом, MspTL с молекулярной массой 65 кДа был идентифицирован в OMF T. lecithinolyticum . Было обнаружено, что ген mspTL присутствует в геноме в виде единственной копии и транскрибируется моноцистронно. Организация генома области mspTL оказалась консервативной у филогенетически родственных организмов [4,10,16].
Проводятся дальнейшие исследования по очистке MspTL и характеристике его функции. В предварительном исследовании OMF 9Было показано, что 0927 T. lecithinolyticum активирует латентную форму MMP-2, секретируемую из первично культивируемых клеток HGF и периодонтальной связки [3]. Вопрос о том, участвует ли MspTL в активации MMP-2, находится в стадии изучения.
Благодарности
Благодарим Ю.-Х. Ким за техническую помощь. Это исследование было частично поддержано грантом (F00045) Корейского исследовательского фонда для Б.-К.С.
Ссылки
[1]
Altschul
S.F.
Мэдден
T
Шаффер
А.А.
Чжан
З
Миллер
В
Липман
Д.Дж.
(
1997
)
Gapped BLAST и PSI-BLAST: новое поколение программ поиска белков в базе данных
.
Рез. нуклеиновых кислот.
25
,
3389
–
3402
.
[2]
Каймано
М.Дж.
Бурелл
К. В.
В.
Баннистер
Т.Д.
Кокс
Д.Л.
Радольф
Дж.Д.
(
1999
)
Основной белок оболочки Treponema denticola преимущественно периплазматический и имеет лишь ограниченное воздействие на поверхность
.
Заразить. Иммун.
67
,
4072
–
4083
.
[3]
Чой
Б.К.
Юнг
Дж.Х.
Suh
H.Y.
Ю
Ю.Дж.
Чо
К.С.
Чай
Дж.К.
Ким
К.К.
(
2001
)
Активация матриксной металлопротеиназы-2 новыми видами оральных спирохет, Treponema lecithinolyticum
.
J. Пародонтология.
72
.
[4]
Чой
Б.К.
Paster
B.J.
Dewhirst
F.E.
Göbel
U.B.
(
1994
)
Разнообразие культивируемых и некультивируемых спирохет полости рта у больного тяжелым деструктивным пародонтитом
.
Заразить. Иммун.
62
,
1889
–
1895
.
[5]
Dewhirst
F.E.
Tamer
M.A.
Ericson
R.E.
Лау
К.Н.
Леванос
В.А.
Boches
С.К.
Galvin
J.L.
Paster
B.J.
(
2000
)
Разнообразие пародонтальных спирохет по анализу 16S рРНК
.
Пероральный микробиол. Иммунол.
15
,
196
–
202
.
[6]
Уитто
В.-Й
Хаапасало
М
Лоунатмаа
К
Конттинен
Гренье
Д
Сорса
Т
(
1996
)
Мембранные компоненты Treponema denticola вызывают высвобождение протеиназы из полиморфноядерных лейкоцитов человека
.
Дж. Дент. Рез.
75
,
1986
–
1993
.
[7]
Эллен
П.Р.
Доусон
Дж.Р.
(
1994
)
Treponema denticola как модель полярной адгезии и цитопатогенности спирохет
.
Trends Microbiol.
2
,
114
–
119
.
[8]
Fenno
J.C.
Muller
K.H.
МакБрайд
Б.К.
(
1996
)
Анализ последовательности, экспрессия и связывающая активность рекомбинантного основного белка внешней оболочки (Msp) Treponema denticola
.
J. Бактериол.
178
,
2489
–
2497
.
[9]
Фенно
Дж. К.
Вонг
Г.В.К.
Ханнам
вечера
Мюллер
К.-Х
Леунг
В. К.
К.
МакБрайд
Б.К.
(
1997
)
Консервация msp , гена, кодирующего основной белок наружной мембраны ротовой полости Treponema spp.
.
J. Бактериол.
179
,
1082
–
1089
.
[10]
Heuner
K
Choi
B.-K
Schade
R
Moter
A
Göbel
U.B.
(
1999
)
Клонирование и характеристика гена ( mspA ) , кодирующего основной белок оболочки Treponema maltophilum АТСС 51939 Т
.
J. Бактериол.
181
,
1025
–
1029
.
[11]
Heuner
K
Meltzer
U
Choi
B.-K
Göbel
900.B.
(
2001
)
Белки, ассоциированные с внешней оболочкой ротовой спирохеты Treponema maltophilum
.
FEMS Microbiol. лат.
197
,
187
–
193
.
[12]
Ко
К.С.
Glogauer
M
McCulloch
C.A.
Эллен
Р. П.
(
1998
)
Treponema denticola Наружная мембрана ингибирует поток кальция в фибробластах десны
.
Заразить. Иммун.
66
,
703
–
709
.
[13]
де Корт
Г
Салиманс
М.М.
Ван дер Бент-Клутвийк
P
Ван Хест
C
Ван Буссел
M.J.
Ван де Клундерт
3 J.A.
(
1999
)
Гликозилирование белка внешней мембраны Enterobacter cloacae OmpX в эукариотических клетках
.
FEMS Microbiol. лат.
177
,
305
–
311
.
[14]
Котиранта
A
Лоунатмаа
K
Хаапасало
M
(
2000
)
Эпидемиология и патогенез инфекций Bacillus cereus
.
Микроб. Заразить.
2
,
189
–
198
.
[15]
Мазерс
Д.А.
Люн
В.К.
Fenno
J.C.
McBride
B.C.
(
1996
)
Главный поверхностный белковый комплекс Treponema denticola деполяризует и индуцирует ионные каналы в клеточных мембранах HeLa
.
Заразить. Иммун.
64
,
2904
–
2910
.
[16]
Moter
A
Hoenig
C
Choi
B.-K
Göbel
.B.
(
1998
)
Молекулярная эпидемиология трепонем полости рта, связанных с пародонтозом
.
Дж. Клин. микробиол.
36
,
1399
–
1403
.
[17]
Pearson
W.R.
Lipman
D.J.
(
1988
)
Усовершенствованные инструменты для сравнения биологических последовательностей
.
Проц. Натл. акад. науч. США
85
,
2444
–
2448
.
[18]
Rosen
G
Sela
M.N.
Халаби
А
Барак
В
Шапира
Л
(
1999
)
Активация мышиных макрофагов липопротеином и липоолигосахаридом Treponema denticola
.
Заразить. Иммун.
67
,
1180
–
1186
.
[19]
Sambrook
J.
Fritsch
E.F.
Maniatis
Т.
(
1989
)
Молекулярное клонирование: лабораторное руководство
, 2-е изд.
Лаборатория Колд-Спринг-Харбор
,
Колд-Спринг-Харбор, Нью-Йорк
.
[20]
Stockbauer
К.Е.
Магун
Л
Лю
М
младший
Бернс
Э.Х.
Губба
S
Рениш
S
Бодри
S.C.
Baker
E
Coburn
J
Leong
J. M.
M.
Musser
J.M.
(
1999
)
Природный вариант фактора вирулентности цистеиновой протеазы группы А Streptococcus с мотивом аргинин-глицин-аспарагиновой кислоты (RGD) предпочтительно связывает интегрины человека α и 6 5 α 1 β 5 IIb β 3
.
Проц. Натл. акад. науч. США
96
,
242
–
247
.
[21]
Стовер
С.К.
Фам
X.Q.T.
Erwin
A.L.
Mizoguchi
S.D.
Warrener
P
Hickey
MJ
Brinkman
F.S.L.
Hufnagle
W.O.
Ковалик
Д.Дж.
Lagrou
M
Garber
R. L.
L.
Goltry
L
Tolentino
E
Westbrook-Wadman
S
Brody
L.L.
Coulter
S.N.
Фолгер
К.Р.
Ларбиг
К
Лим
Р.М.
Смит
К.А.
Спенсер
Д. Х.
Вонг
Г.К.С.
Полсен
И.Т.
Reizer
J
Saier
M.H.
Хэнкок
Р.Э.В.
Олсон
М.В.
(
2000
)
Полная последовательность генома Pseudomonas aeruginosa PA01, оппортунистического патогена
.
Природа
406
,
959
–
964
.
[22]
Уитто
В.Дж.
Кастрюля
Ю. М.
М.
Люн
В.К.
Ларджава
H
Эллен
Р.П.
Финли
Б.Б.
(
1995
)
Цитопатическое действие Treponema denticola химотрипсиноподобной протеиназы на мигрирующие и многослойные эпителиальные клетки
.
Заразить. Иммун.
63
,
3401
–
3410
.
[23]
Walker
S.G.
Ebersole
J.L.
Holt
S.C.
(
1997
)
Идентификация, выделение и характеристика основного белка наружной мембраны (MompA) массой 42 кДа из Treponema pectinovorum ATCC 33768
.
J. Бактериол.
179
,
6441
–
6447
.
[24]
Weinberg
A
Holt
S.C.
.
J. Бактериол.
173
,
6935
–
6947
.
[25]
Whittaker
CJ
Klier
C.M.
Коленбрандер
Ч.Е.
(
1996
)
Механизмы адгезии бактериями полости рта
.
год. Преподобный Микробиолог.
50
,
513
–
552
.
