Что такое моляр тутового дерева?
Молярная шелковица — это физически дефектные постоянные моляры. Деформация вызвана врожденным сифилисом. Для этого типа аномалий характерны карликовые коренные зубы с остриями, покрытыми шаровидными эмалями. Эти зубы функциональны, но могут быть косметически закреплены с помощью коронок, мостов или имплантатов.
Прямо над линией десен молярная шелковица выглядит нормально. Деформация становится очевидной по направлению к острой или верхней шлифовальной поверхности зуба. Здесь размер моляра шелковицы уменьшается во всех аспектах, создавая пухлую версию обычного моляра. Считается, что причиной молярной атрофии является гипоплазия эмали или дефицит зубной эмали. Базовый дентин и пульпа зуба нормальны, но эмалевое покрытие или молярная оболочка тонкие и деформированные, создавая меньшую версию типичного зуба.
Шлифовальная поверхность моляра тутового дерева также повреждена. Обычно шлифовальная поверхность коренного зуба имеет ямку и окружена круглым выступом в верхней части зуба, который используется для шлифования. Деформация бугорка моляра шелковицы характеризуется чрезвычайно неглубокой или полностью отсутствующей ямкой. Вместо этого область ямы заполнена шаровидными структурами, сгруппированными по всей верхней поверхности острого выступа. Этот тип уродства также считается вызванным гипоплазией эмали.
Молярная шелковица обычно функциональна и не нуждается в лечении. Если уродство является серьезным или человек обеспокоен зубами, есть несколько вариантов. Зубы могут быть покрыты постоянной литой коронкой, коронкой из нержавеющей стали, или могут быть удалены коренные зубы, и вместо моляра тутового дерева может быть установлен имплант или мост.
Молярная шелковица вызвана врожденным сифилисом, который передается от матери ребенку в матке через плаценту. Поскольку этот конкретный симптом врожденного сифилиса проявляется позднее в детстве с прорезыванием постоянных коренных зубов, он является маркером поздней стадии заболевания.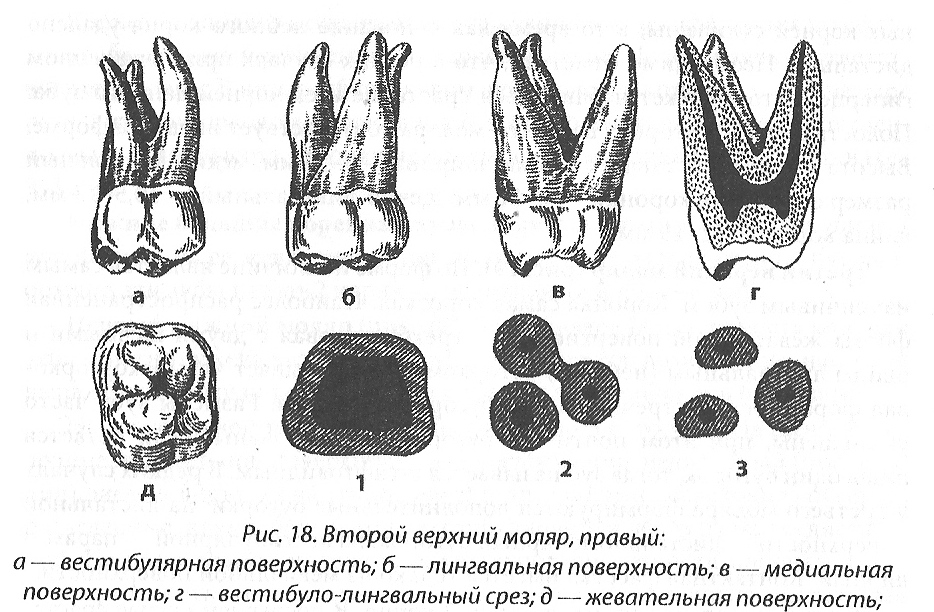
ДРУГИЕ ЯЗЫКИ
Специализированное научно-практическое издания для ветеринарных врачей и студентов ветеринарных ВУЗов.
Автор: Левина О. А., ветеринарный врач-стоматолог Ветеринарной клиники ортопедии, травматологии и интенсивной терапии, г. Санкт-Петербург.Прикус (occlusio) – соотношение зубных рядов при наиболее плотном смыкании челюстей, то есть соотношения зубов в одной челюсти, а также соотношения зубов в противоположных челюстях.
Малокклюзия может возникать по причине несоответствия длины и/или ширины челюсти (скелетная малокклюзия), а также по причине неправильного расположения зубов в зубном ряду или их комбинации (дентальная малокклюзия). Развитие окклюзии определяется как генетическими, так и приобретенными факторами. Известно, что длина челюсти, положение зачатка зуба и размер зуба наследуются (Stockard, 1941).
 Считается, что скелетная малокклюзия является унаследованной патологией (если не удается идентифицировать иную причину неправильного развития, например травму). Дентальная же малокклюзия условно считается приобретенной патологией, в том случае если не отслеживается у других особей в этой линии разведения.
Считается, что скелетная малокклюзия является унаследованной патологией (если не удается идентифицировать иную причину неправильного развития, например травму). Дентальная же малокклюзия условно считается приобретенной патологией, в том случае если не отслеживается у других особей в этой линии разведения.Оценка окклюзии
При оценке окклюзии важно осмотреть всю ротовую полость и не заострять свое внимание исключительно на окклюзии резцов. Фактически окклюзия клыков, премоляров и моляров дает нам больше ответов при оценке прикуса у собаки.Форма головы влияет на позиционирование зубов. Малокклюзия может быть у собак, имеющих любую из трех форму головы (долихоцефал, мезоцефал и брахицефал), но чаще всего встречается у брахицефальных пород.
У мезоцефальной собаки нижняя челюсть короче и уже, чем верхняя челюсть. Следовательно, нижнечелюстные резцы и моляры прикрываются их верхнечелюстными антагонистами. Нормальный прикус взрослой собаки-мезоцефала характеризуется следующими показателями:
- Окклюзия резцов:
- Верхнечелюстные резцы располагаются ростральнее нижнечелюстных.
- Кончики нижнечелюстных резцов упираются в основание коронок верхних резцов.
- Срединная линия верхней и нижней челюсти должны совпадать (фото 1).
- Окклюзия клыков:
- Нижнечелюстной клык заполняет диастему (пространство) между верхним третьим резцом и верхним клыком, не касаясь ни одного их них. Его ось располагается точно посередине между верхним клыком и третьим резцом.
- Линии, проведенные вдоль оси верхнего, нижнего и верхнего третьего клыков, должны быть параллельными (фото 2).
- Разобщение премоляров:
- Острые кончики премоляров направлены точно в сторону межзубного пространства противоположной аркады. Причем первый премоляр нижней челюсти является наиболее ростральным (фото 2).
- Окклюзия моляров и премоляров:
- Мезиобуккальная поверхность первого нижнего моляра скрыта верхним четвертым премоляром.

- Дистальная окклюзионная поверхность нижнего моляра нижней челюсти закрыта небной окклюзионной поверхностью первого моляра верхней челюсти.
Скелетная малокклюзия. Мандибулярная прогнатия
При прогнатическом прикусе нижняя челюсть длиннее верхней челюсти, а некоторые или все зубы нижней челюсти смещены рострально по отношению к верхнечелюстным зубам.Степень малокклюзии варьируется следующим образом:
- нормальная резцовая окклюзия – клыки нижней челюсти соприкасаются с верхнечелюстными резцами, премоляры рострально смещены;
- верхние и нижние резцы соприкасаются режущими поверхностями, клыки нижней челюсти соприкасаются с верхнечелюстными резцами, премоляры рострально смещены;
- обратный ножницеобразный прикус – нижние резцы расположены ростральнее верхних на 0,5–5 см и более, нижние клыки могут находиться как ростральнее, так и каудальнее верхних третьих резцов, премоляры и моляры смещены в одинаковой степени (фото 3).
Мандибулярная прогения
Мандибулярный брахигнатический прикус, часто называемый недокусом, возникает, когда нижняя челюсть короче верхней (фото 4)При этой патологии прикуса наблюдаются следующие изменения:
- верхние резцы расположены ростральнее по отношению к нижним резцам на 0,5–5 см и более;
- верхние клыки расположены каудальнее, но касаются нижнечелюстных клыков, выровнены с нижними клыками или находятся ростральнее по отношению к нижнечелюстным клыкам;
- нижнечелюстные премоляры каудально смещены относительно верхнечелюстных премоляров.
 Криворотость развивается с отклонением от срединной линии.
Криворотость развивается с отклонением от срединной линии.Узкая нижняя челюсть
У некоторых собак нижняя челюсть слишком узкая по отношению к верхней челюсти (фото 5). В результате этого нижнечелюстные клыки упираются в твердое небо. Животное может оказаться неспособным закрыть рот, и обычно происходит повреждение слизистой оболочки твердого неба. В тяжелых случаях возможно повреждение самого твердого неба и формирования ороназального отверстия.Дентальная малокклюзия
Передний перекрестный прикусЗадний перекрестный прикус – это состояние, при котором верхнечелюстные премоляры (а иногда и моляры) перекрывают буквально нижнечелюстные премоляры и моляры. Если у животного при этом удобный и функциональный прикус, то лечение не показано. Однако в случае наличия дискомфорта или травмы из-за неправильного прикуса травмирующие зубы должны быть удалены. Ортодонтическое лечение обычно не показано при данной патологии.
Нормального физиологического очищения зубов нижней челюсти зубами верхней челюсти не происходит, и поэтому моляры нижней челюсти нуждаются в более тщательном уходе из-за постоянного накопления зубных отложений.
Ростральное смещение верхнечелюстных клыков
– верхние клыки расположены ростральнее нижних клыков. Часто они повернуты перпендикулярно по отношению к их нормальному росту. Есть мнение, что это генетически обусловленная патология. Персистирующие временные зубы могут усугубить положение вещей (фото 7).Медиальное смещение нижних клыков
Считается, что персистирующие временные зубы являются первопричиной этого состояния. Однако данное утверждение является спорным, поскольку у миниатюрных пород собак, у которых распространены персистирующие временные зубы, данная патология встречается не часто. У долихоцефальных пород эта патология распространена по причине узости нижней челюсти (фото 8).
Однако данное утверждение является спорным, поскольку у миниатюрных пород собак, у которых распространены персистирующие временные зубы, данная патология встречается не часто. У долихоцефальных пород эта патология распространена по причине узости нижней челюсти (фото 8).Лечение патологий прикуса (исправление прикуса)
Считается, что исправление прикуса выполняется только по прихоти владельца, обусловленного желанием получить собаку шоу-класса. Может быть, во многих случаях это действительно так, однако имеется огромное количество патологий прикуса, при которых у собаки может развиться хроническая травма мягких и твердых тканей зубов, в результате чего животное лишится возможности нормально смыкать челюсти, а соответственно, и питаться. В результате нарушается физиологическая функциональность зубочелюстной системы, и в этих случаях мы имеем возможность помочь таким животным (рис. 9).Для того чтобы ортодонтические аппараты развивали силу давления или тяги на определенный участок челюсти, при их конструировании необходимо создать точку опоры и точку приложения силы. Точка опоры должна быть значительно устойчивее по сравнению с той частью зубочелюстной системы, которая подлежит перемещению. По законам механики более устойчивая опора будет оставаться на месте, а тело в точке приложения силы (как менее устойчивое) может перемещаться. Если точка опоры и точка приложения силы будут одинаковой устойчивости, то возникает взаимодействие сил: обе точки нагружаются в одинаковой мере, но в противоположном направлении. В качестве опоры могут быть использованы отдельные группы зубов. На верхней челюсти в качестве опорного зуба используется верхний четвертый премоляр, на нижней – первый моляр, поскольку эти зубы самые крупные в своей аркаде. При перемещении резцов используются соответствующие клыки.
При воздействии на зуб продолжительного давления происходит перестройка костной ткани. В месте давления корня зуба на кость происходит ее лизис, а с противоположной стороны корня происходит образование новой костной ткани. В результате зуб передвигается в нужном нам направлении. Эти два процесса должны находиться в равновесии, иначе лизис будет превосходить над формированием новой кости. Чаще всего лизис все же превалирует над формированием новой ткани, поэтому в большинстве случаев требуется установка ретейнеров после ортодонтического лечения. Они позволяют закрепить результат.
Осложнения ортодонтического лечения чаще всего включают пульпит, внешнюю резорбцию корня, подвижность зубов, боль. Все эти осложнения, как правило, возникают по причине того, что во время перемещения зубов была применена слишком сильная непрерывная тяга.
Литература:
- Cedric Tutt. Small Animal Dentistry: A manual of techniques, 2006.
- Cecilia Gorrel, Susanne Andersson, Leen Verhaert. Veterinary Dentistry for the General Practitioner, second edition, 2013.
Лечение зубов мудрости | Стоматология Космодента
Ответственные люди всегда отслеживают состояние своих зубов, вовремя занимаются их лечением и пытаются сделать всё от них зависящее, чтобы сохранить их здоровье. Но третьи моляры это особенные зубы. Они прорезываются очень поздно и часто доставляют владельцу много проблем.
Зуб мудрости всегда занимает в зубном ряду восьмое место и называется третьим моляром. Прорезывание его приходится на двадцатый год жизни человека, который к этому времени является зрелым и условно «мудрым». Именно поэтому у зуба мудрости такое название. Но у кого-то восьмерки не прорезываются вовсе, так как уже не выполняют свои изначальные функции, которые заключались в размельчении пищи высокой твердости.
Устройство и сроки существования восьмерок
Выглядит третий моляр примерно также как и остальные моляры, но особенность его в том, что она поздно прорезывается, чаще всего для неё нет места и приходится заниматься расталкиванием соседних зубов, а ещё восьмёрки слишком сложно лечить из-за их труднодоступности, но это и не имеет смысла, поэтому их просто удаляют. Служат восьмёрки не очень долго, хоть и прорезываются позже других. За ними сложно ухаживать и они часто растут под наклоном. В связи с этим такие зубы быстро портятся и в итоге удаляются. Часто они оказываются поражены кариесом, ещё не прорезавшись полностью, так как лезли очень долго и сложно. А порой они прекрасно себя чувствуют и им хватает места и ухода.
Служат восьмёрки не очень долго, хоть и прорезываются позже других. За ними сложно ухаживать и они часто растут под наклоном. В связи с этим такие зубы быстро портятся и в итоге удаляются. Часто они оказываются поражены кариесом, ещё не прорезавшись полностью, так как лезли очень долго и сложно. А порой они прекрасно себя чувствуют и им хватает места и ухода.
Функции и капюшон
О функциях восьмых зубов можно говорить долго. Кто-то считает, что раз они были раньше и появляются сейчас, то не нужно удалять их без причины. А ещё иногда зуб мудрости помогает фиксировать зубной протез. Какие-то врачи считают, что лучше удалить третьи моляры сразу же после прорезывания, ведь, по сути, они являются рудиментом.
Капюшон это десневой карман, который нависает над зубом мудрости при прорезывании. В этом кармане скапливается пища и создает предпосылки для размножения вредоносных бактерий. Очень часто капюшон и десна воспаляются, затрагивая и другие сопредельные зоны. Тогда обязательно нужно обращаться к врачу для устранения проблемы, а именно иссечения капюшона. Это удаление части десны и промывание её антисептиком.
Чем болеют зубы мудрости и как их лечить?
Обычно восьмерки страдают от банального кариеса, ведь они неудобно расположены и поэтому сложно за ними ухаживать. Зона с кариесом часто возникает в самой труднодоступной зоне и вылечить зуб становится невозможно. Понимая, что качественного лечения организовать не удастся, хороший стоматолог предложит удалить такой зуб. Не в коем случае нельзя оттягивать лечение зуба в случае обнаружения проблем. Иначе это может привести к пульпиту или периодонтиту, что является показанием к однозначному удалению.
Если восьмерки расположены правильно и ничего не мешает их лечению, можно попытаться это сделать, посетив врача вовремя. При решении удалить нерв доктор назначит лечение антибиотиками для остановки воспалительного процесса. Если зуб болит, то анальгетики применяют для ожидания визита к стоматологу и пломбирования каналов, после которого боли исчезнут. Главное — никогда не откладывать посещение клиники.
Главное — никогда не откладывать посещение клиники.
Зубы мудрости могут доставлять очень много проблем. Лучше всего будет отслеживать их состояние и своевременно удалить их в случае сложностей.
| Оставить заявку | Записаться |
Верхний моляр
Добрый день! Моему ребенку 2 года. Первый зуб прорезался только в 11 месяцев. Уже в 1,3 года на 4 передних верхних зубах появилась полоска, которая быстро переросла в траншею. В платной клинике нам предложили поставить на каждый зуб пломбу, но ребенок решительно отказался открывать там рот. Закатывался в истерике, удержать вдвоем не смогли, в итоге нам посеребрили 3-х кратно, но уже через 3 месяца эти зубы просто рассыпаются на глазах, двух практически не осталось уже.
Я не знаю с чем это связано. Ребенок был на грудном вскармливании до 1,5 лет, бутылки не было, соску тоже мы не знаем, соки он не пьет, поправлялись всегда очень хорошо. Зубы чистим, с криками, конечно, но стабильно 2 раза в день пастой Rocs.
Вчера заметила на коренных, на передней стенке та же самая проблема, эмаль как будто трескается… Расстроилась… Не знаю что и делать, куда бежать. Жалко ребенка.
Помогите, пожалуйста, может каких-то элементов не хватает в организме, хотя питание достаточно рациональное, кушает с удовольствием, сладкого не даем. Очень хочется сохранить оставшиеся зубы.
Заранее спасибо!
ОТВЕТ СПЕЦИАЛИСТА
Здравствуйте! Проблема, о которой Вы говорите, довольно распространенная. И причин здесь много. Во-первых, Ваша беременность: принимали ли вы какие-то препараты, лежали ли на сохранении и т.д. Питание ребенка. То, что вы чистите зубы два раза в день — очень хорошо. Но, нужно смотреть, правильно ли вы это делаете, не травмируете ли эмаль. Правильно ли подобрана ли щетка, ребенок еще маленький, может быть, вам пока еще нужна силиконовая. Можно попробовать поменять пасту. Вовремя нужно проводить профилактические процедуры, когда еще нет больших разрушений, даже лучше, когда еще зубы не повреждены. Особенно, если есть такая предрасположенность. Мы чаще применяем эмаль-ликвид, средство, содержащее кальций и фтор, которые укрепляют эмаль зубов. Но эта процедура не одноразовая, её нужно проводить по схеме, которую назначит врач именно для вас. Что касается препаратов для внутреннего применения, то для начала вы должны посоветоваться с педиатром. Сейчас детки очень аллергичные и не всем эти препараты подходят. Возможно, нужно будет сдать какие-то анализы, чтобы посмотреть картину изнутри. Подводя всё вышесказанное, скажу, что в Вашем случае нужна совместная работа стоматолога, педиатра и ваша. Тогда, я уверена, Вы добьетесь положительного результата. Здоровья Вам и вашему малышу!
Особенно, если есть такая предрасположенность. Мы чаще применяем эмаль-ликвид, средство, содержащее кальций и фтор, которые укрепляют эмаль зубов. Но эта процедура не одноразовая, её нужно проводить по схеме, которую назначит врач именно для вас. Что касается препаратов для внутреннего применения, то для начала вы должны посоветоваться с педиатром. Сейчас детки очень аллергичные и не всем эти препараты подходят. Возможно, нужно будет сдать какие-то анализы, чтобы посмотреть картину изнутри. Подводя всё вышесказанное, скажу, что в Вашем случае нужна совместная работа стоматолога, педиатра и ваша. Тогда, я уверена, Вы добьетесь положительного результата. Здоровья Вам и вашему малышу!
MB2 в верхних молярах — как определить его наличие в зубе
Главная цель эндодонтического лечения — тщательное формирование и очистка всех корневых каналов с последующим введением инертного наполнителя.
Основной причиной заболеваний после эндодонтического лечения является отсутствие условий для локализации, полной обработки и правильной обтурации каждого участка системы корневых каналов. Поэтому для успешного эндодонтического лечения необходимо знать анатомию системы корневых каналов и ее часто встречающиеся вариации. Первые верхние моляры самые изученные зубы по сравнению с другими, и принято считать, что они имеют 3 корня и 3 корневых канала (MB, DB, P). Но в большинстве исследований сообщается о наличии второго канала (MB2) в мезиально-щечном корне этих зубов более чем в 50% случаев. Эта информация заставляет задуматься: есть ли в конкретном зубе MB2? Также стоит учитывать, что наиболее часто причиной неудач в эндодонтическом лечении является пропущенный MB2. Поэтому в своей статье я расскажу о том, как его найти, чтобы вы могли в каждом клиническом случае с уверенностью определить имеет ли первый верхний моляр 3 корня и 4 канала (MB1, MB2, DB, P) или только 3 канала.
Видео — Схема расположения МВ2
1. Анатомия
Анатомия
Наиболее важное условие для поиска MB2 – понимание анатомии. Прописная истина: мы знаем только то, что видим, и видим только то, что знаем. Поэтому, если мы после обработки зуба, проведения конусно-лучевой компьютерной томографии, посещения лекций и прочтения статей знаем, что MB2 встречаются, мы в силах их обнаружить. John Stropko в 1999 году в эндодонтическом журнале опубликовал исследование с изучением 1732 стандартно пролеченных верхних моляров. Было отмечено, что MB2 был найден в 73,2% случаев в первых молярах, в 50,7% случаев во вторых молярах и в 20% случаев в третьих молярах. Из них оказалось, что MB2 был отдельным каналом в 54,9% первых моляров и в 45,6% вторых моляров и сливался с другим каналом во всех третьих молярах. Но удивительно, что эти цифры возросли до 93% в первых молярах и 60,4% во вторых молярах, когда оператор стал более опытным, начал использовать подходящее клиническое оборудование и работать под увеличением. Из исследования Stropko можно сделать важный вывод о том, что более чем в 90% случаев MB2 первых верхних моляров идентифицируется не путем простого обнаружения в зубе, а посредством тщательного поиска. Исследователь кропотливо искал его для изучения строения зубов. Это очень важный момент, поскольку, если мы не задумываемся, что в зубе может быть MB2, мы не будем его искать. Но если мы знаем о возможности существования такого дополнительного канала, мы будем предполагать его наличие, пока не докажем обратное.
2. Увеличение
Увеличение подразумевает улучшение видимости. Как я уже упоминал ранее, мы знаем только то, что видим, поэтому увеличение имеет решающее значение при поиске MB2. Buhrley и др. в 2002 году в эндодонтическом журнале опубликовали данные о влиянии увеличения на обнаружение MB2 в верхних молярах. Они установили, что без увеличения можно найти дополнительный канал в 17,2% случаев, в то время как со стоматологическими линзами этот процент значительно возрастает до 62,5%, а при использовании стоматологического микроскопа до 71,1% случаев.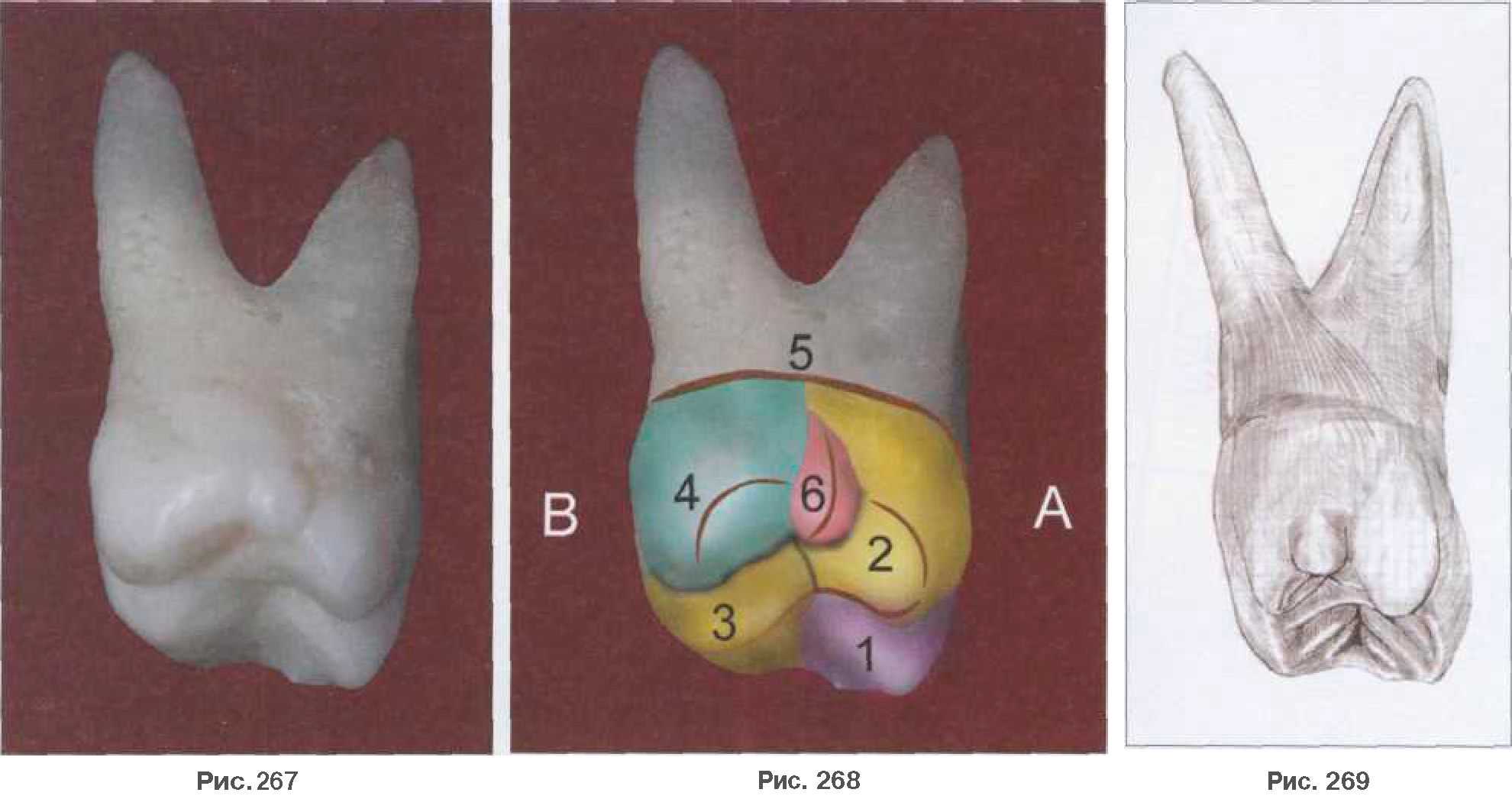 Эта информация означает, что увеличение при поиске MB2 – обязательное условие, а стоматологический микроскоп – лучший инструмент для увеличения. Кроме того, необходимо хорошее освещение, которое также улучшает видимость.
Эта информация означает, что увеличение при поиске MB2 – обязательное условие, а стоматологический микроскоп – лучший инструмент для увеличения. Кроме того, необходимо хорошее освещение, которое также улучшает видимость.
3. Рентгенография
Рентгенограммы очень важны для поиска MB2. Многие стоматологи начинают работу, имея на руках одиночный снимок. Зачастую этого недостаточно. При проведении рентгенографии с трех разных углов (техника SLOB) мы имеем возможность лучше видеть строение зуба.
Изображение 1 – На первом снимке (А) все выглядит нормально, но когда делаются рентгенограммы под другими углами (В), можно заметить, что пропущен MB2
изображение 2
4. Доступ к полости зуба
Известно, что создание доступа к полости зуба – это первый шаг всех эндодонтических манипуляций, и он всегда имеет важное значение. Я встречал множество клинических случаев пропущенных каналов, в которых основной причиной ошибок в идентификации дополнительных каналов был неправильно сформированный доступ к полости. Я не собираюсь в этой статье обсуждать детали формирования эндодонтического доступа, но подчеркну, что полный доступ с выровненными и финированными аксиальными стенками необходим для успешной работы. Я не утверждаю, что доступ должен быть большим, ведь можно добиться адекватного доступа, не принося в жертву здоровые структуры зуба. Иногда для получения хорошего доступа требуется удалить все имеющиеся реставрации, в том числе и коронки. Этот шаг обеспечивает лучшее ориентирование в полости зуба и служит профилактикой перфорации в процессе поиска корневых каналов.
Обнаружение MB2
Теперь, когда мы обсудили ключевые моменты при поиске дополнительного канала, давайте поговорим о стратегии и технике. Как известно, не каждый MB2 легко идентифицировать. Редко бывает так, что мы просто берем файл и находим такой канал. Чаще всего, приходится выполнить большую работу по его поиску, прохождению и расширению. В этой статье я поделюсь некоторыми советами и хитростями, которые могут быть полезны при работе с MB2.
Тест белой линии
В некротизированых зубах при создании доступа с помощью бора либо ультразвуковой технологии образуются опилки, которые могут скапливаться в анатомических пространствах, таких как бороздки на дне полости зуба. Это создает картину «белой линии». Мы должны быть очень внимательными в отношении таких линий, так как их можно использовать при поиске устья дополнительного канала.
Тест красной линии
Подобно некротизированым зубам, в витальных зубах можно ориентироваться на тест «красной линии». После создания доступа и раскрытия пульпарной полости в витальном зубе, естественно, она будет кровоточить. После остановки кровотечения и экстирпации тканей можно заметить небольшие капельки крови, выступающие из бороздок на дне полости зуба. Они также могут служить индикатором наличия дополнительного канала.
Тест на пузырьки
Тест на пузырьки упоминался множество раз с начала эпохи микроскопической эндодонтии. Для проведения этого теста в пульпарную полость вводят раствор гипохлорита натрия, который диссоциирует на ионы натрия и хлорида с выделением свободного кислорода при контакте с органическими тканями. Реакция заметна как появление пузырьков на дне полости зуба, и ее можно увидеть в микроскоп. Это еще одна подсказка при исследовании строения зуба.
Цветовой тест
Важно помнить также и о цветовом тесте. Один из трех законов анатомии пульпарной камеры, опубликованных в эндодонтическом журнале Krasner и др. в 2004 году, — закон изменения цвета. Линии, появляющиеся при развитии и слиянии корней, или корневая карта, представляют собой узкие полосы на дне полости зуба и выглядят более темными по сравнению с окружающей тканью. Они приводят нас к дополнительным каналам.
Можно заметить, что дно полости зуба всегда более темное по сравнению с окружающими дентинными стенками, а линии, появившееся при развитии и слиянии корней (корневая карта) еще темнее.
Тест на красители
красители тоже могут быть полезны. В данном случае можно использовать метиленовый синий. Поместите несколько капель красителя в полость зуба, а затем промойте водой. краситель задерживается в трещинах и углублениях, которые помогут определить внутреннюю анатомию.
В данном случае можно использовать метиленовый синий. Поместите несколько капель красителя в полость зуба, а затем промойте водой. краситель задерживается в трещинах и углублениях, которые помогут определить внутреннюю анатомию.
Обработка MB2
После создания доступа можно провести несколько вышеописанных тестов, которые помогут найти MB2. В некоторых случаях с использованием микроскопа устье дополнительного канала может быть определено после выполнения тестов. Но так происходит не всегда. Есть еще два важных этапа выявления MB2.
Первый этап заключается в поиске всех основных каналов первого верхнего моляра. В описанном случае это будут мезиально-щечный (MB1), дистально-щечный (DB) и небный (P) каналы. Для более легкой идентификации трех устьев стоит помнить анатомический ключ:
1. MB1 располагается немного дистальнее вершины мезиально-щечного бугра.
2. DB располагается дистальнее и несколько более небно по отношению к
мезиально-щечному. Как правило, его устье находится в области щечной
фиссуры.
3. P расположен дистальнее вершины мезиально-небного бугра.
Второй этап заключается в определении местоположения MB2. Обычно он локализуется более небно по сравнению с основным MB1 и немного мезиальнее по отношению к линии, проведенной между MB1 и P.
В большинстве зубов даже после определения устья МВ2 этот канал по—прежнему трудно пройти, пока не удалить некоторое количество дентина в области его устья в апикальном направлении. Для этого можно пользоваться низкоскоростными борами с длинным хвсютодиком, такими как раскрывающие боры Мunсе. Они очень удобны в работе, так как громоздкая шпика наконечника удалена от рабочей оси, что освобождает пинию обзора вдоль хвостовика бора. Это позволяет видеть не заднюю часть наконечника, а вращение бора. Ультразвуковые наконечники также могут быть очень эффективны в плане хорошей видимости без перекрытия рабочего поля громоздкой головкой наконечника. Можно использовать пьезоэлектрическую ультразвуковую установку с соответствующими наконечниками, такую как Start-X З. При этом видимость будет лучше при использовании гладкого угловот инструмента с возможнсюгью наблюдения за его работой. Ротационные инструменты с очень высокой режущей способностью также одни из моих самых любимых для раскрытия дополнительного канала Используйте ротационные инструменты, такие как ProTaper SX, WaveOne Gold или Reciproc blue, с помощью очищающих движений в направлении от фуркации для удаления треуголника дентина на уровне устья канала и уменьшения корональной интерференции.
При этом видимость будет лучше при использовании гладкого угловот инструмента с возможнсюгью наблюдения за его работой. Ротационные инструменты с очень высокой режущей способностью также одни из моих самых любимых для раскрытия дополнительного канала Используйте ротационные инструменты, такие как ProTaper SX, WaveOne Gold или Reciproc blue, с помощью очищающих движений в направлении от фуркации для удаления треуголника дентина на уровне устья канала и уменьшения корональной интерференции.
Роль эндодонтического зонда Endo explorer в поиске МВ2 мало описана, однако он тоже может быть весьма полезным. Очень приятно скалывать небольшой участок надлежащет дентина, а иногда это еще и намного безопаснее, чем использование бора для его высверливания. При использовании эндодонтического зонда рекомендуется крепко прижимать его кончик к вышележащему дентину Сам кончик инструмента довольно прочныи После удаления участка дентина мы надеемся увидеть небольшое отверстие в МВ2 и готовы проходить и обрабатывать этот канал В обработке канала нет каких-либо отличий от работы с другими каналами. Используйте механический инструмент для создания ковровой дорожки, ручной файл небольшого размера или инструмент Micro opener Micro opener представляет собой стальной файл, прикрепленный к ручке. Такая эрономичная ручка позволяет держать пальцы оператора дне поля зрения, не перекрывая обзор.
Перевод выполнен специально для форума Stomatologija.su
Источник:
http://www.styleitaliano.org/mb2-in-maxillary-molars—does-it-really-exist-
Шинирование — один за всех и все за одного! В данной статье мы поговорим про процедуру, пугающую многих пациентов. Итак, для начала разберем — что такое шинирование. Все очень просто! Эта процедура делается с целью укрепления зубов, предотвращения «расшатывания» зубов и для того, чтобы дать тканям вокруг зубов (пародонт) восстановиться. Способы шинирования зубов Существует множество различных способов шинирования зубов: мостовидные протезы, съемные конструкции, стекловолоконные нити и даже шинирование брекет-системами.
 Да-да! Именно брекет-системами. Ведь при помощи брекетов можно не только двигать зубы, но еще и заставить их стоять неподвижно. У каждого метода есть свои светлые и темные стороны. Например, для шинирования при помощи «мостов» приходится обтачивать коронковые части зубов, а брекет-системы зачастую «кусают» пациентов своей стоимостью. И у всех видов шинирования есть один общий минус! И это гигиена. Но ваш доктор всегда расскажет и покажет, как правильно ухаживать за полостью рта, чтобы минимализировать возможность каких-либо осложнений. Стекловолоконная нить — лучший выбор Что же тогда выбрать, спросите вы? На сегодняшний день, самым оптимальным видом шинирования является стекловолоконная нить. Она фиксируется на внутреннюю поверхность зубов при помощи пломбировочного материала. При этом вся нагрузка поступающая на конкретный зуб сразу равномерно распределяется по всем зашинированным зубам. При правильном уходе шину можно носить несколько лет, при этом постепенно будут восстанавливаться ткани вокруг зубов и следовательно, усиливаться устойчивость зубов. 8 Сентября 2017
Да-да! Именно брекет-системами. Ведь при помощи брекетов можно не только двигать зубы, но еще и заставить их стоять неподвижно. У каждого метода есть свои светлые и темные стороны. Например, для шинирования при помощи «мостов» приходится обтачивать коронковые части зубов, а брекет-системы зачастую «кусают» пациентов своей стоимостью. И у всех видов шинирования есть один общий минус! И это гигиена. Но ваш доктор всегда расскажет и покажет, как правильно ухаживать за полостью рта, чтобы минимализировать возможность каких-либо осложнений. Стекловолоконная нить — лучший выбор Что же тогда выбрать, спросите вы? На сегодняшний день, самым оптимальным видом шинирования является стекловолоконная нить. Она фиксируется на внутреннюю поверхность зубов при помощи пломбировочного материала. При этом вся нагрузка поступающая на конкретный зуб сразу равномерно распределяется по всем зашинированным зубам. При правильном уходе шину можно носить несколько лет, при этом постепенно будут восстанавливаться ткани вокруг зубов и следовательно, усиливаться устойчивость зубов. 8 Сентября 2017 В данной статье мы поговорим про процедуру, пугающую многих пациентов. Итак, для начала разберем — что такое шинирование. Все очень просто! Эта процедура делается с целью укрепления зубов, предотвращения «расшатывания» зубов и для того, чтобы дать тканям вокруг зубов (пародонт) восстановиться.
Способы шинирования зубов
Существует множество различных способов шинирования зубов: мостовидные протезы, съемные конструкции, стекловолоконные нити и даже шинирование брекет-системами. Да-да! Именно брекет-системами. Ведь при помощи брекетов можно не только двигать зубы, но еще и заставить их стоять неподвижно.
У каждого метода есть свои светлые и темные стороны. Например, для шинирования при помощи «мостов» приходится обтачивать коронковые части зубов, а брекет-системы зачастую «кусают» пациентов своей стоимостью. И у всех видов шинирования есть один общий минус! И это гигиена. Но ваш доктор всегда расскажет и покажет, как правильно ухаживать за полостью рта, чтобы минимализировать возможность каких-либо осложнений.
Но ваш доктор всегда расскажет и покажет, как правильно ухаживать за полостью рта, чтобы минимализировать возможность каких-либо осложнений.
Стекловолоконная нить — лучший выбор
Что же тогда выбрать, спросите вы? На сегодняшний день, самым оптимальным видом шинирования является стекловолоконная нить. Она фиксируется на внутреннюю поверхность зубов при помощи пломбировочного материала. При этом вся нагрузка поступающая на конкретный зуб сразу равномерно распределяется по всем зашинированным зубам.
При правильном уходе шину можно носить несколько лет, при этом постепенно будут восстанавливаться ткани вокруг зубов и следовательно, усиливаться устойчивость зубов.
Вкладки
Иногда зуб разрушен настолько, что пломба занимает бОльшую часть его коронковой части.
Слишком большие пломбы неправильно распределяют нагрузку на зуб, и есть высокий риск откола стенок.
Зачастую с такими крупными реставрациями врачу не удается сделать высокоэстетичную и функциональную работу.
Существует более надежная и эстетичная альтернатива большим пломбам — вкладка.
Что такое вкладка?
Вкладка — микропротез, который заменяет фрагмент зуба. Ее изготавливают из очень прочной керамики. Керамическая вкладка позволяет полностью восстановить жевательную функцию и эстетику даже при значительной утрате тканей. Если пломба со временем стирается и требует обновления, то вкладка стабильна в полости рта и выдерживает естественную, ежедневную нагрузку.
Постановка вкладки — это зубосохраняющая процедура, которая позволяет минимально препарировать зуб, следовательно сохранить его жизнеспособность. Для применения такой конструкции необходима достаточная толщина хотя бы двух стенок зуба и сохранность эмали. Это обеспечит хорошую адгезию (сцепление) и гарантию того, что стенки не сломаются.
Показания к применению вкладок
Показания к применению вкладок весьма обширны и во многом перекликаются с основаниями к использованию методик прямого пломбирования эстетическими пломбировочными материалами:
- Вкладки используются как один из вариантов восстановления возникших разрушений, травм и повышенной стираемости «живых» и депульпированных зубов.
- Вкладки с перекрытием бугров (оверлей) могут являться альтернативой применению коронок при восстановлении значительных дефектов жевательной поверхности зуба.
Условия для установки вкладок:
- Вкладки применяются даже при большой степени разрушения зуба — более 50%. Лучше, чтобы такой зуб был витальным, то есть недепульпированным — с живым нервом.
- Керамические вкладки устанавливают только на жевательные зубы (моляры и премоляры). Форма клыков и резцов не позволяет реставрировать их таким способом.
- Вкладку можно установить при отсутствии одной, двух или даже трех стенок. Однако ее использование предполагает наддесневое препарирование, поэтому стенки не должны отсутствовать до самого края десны.
- Для постановки конструкции нужна достаточная толщина стенок зуба. Если они совсем тонкие, то быстро сломаются. В такой ситуации стенку вообще лучше убрать и восстановить вкладкой.
Изготовление вкладок
Вкладки изготавливаются из инновационной дисиликатлитиевой стеклокерамики E-max, система CAD/CAM.Это обеспечивает высокую эстетику и исключительную прочность реставрации.
Широкий диапазон уровней прозрачности, оттенков и размеров блоков предоставляет большое разнообразие возможностей.
Вкладку создают в зуботехнической лаборатории с учетом правильной анатомической формы зуба, цвета его эмали, состояния соседних зубов и всех особенностей прикуса пациента.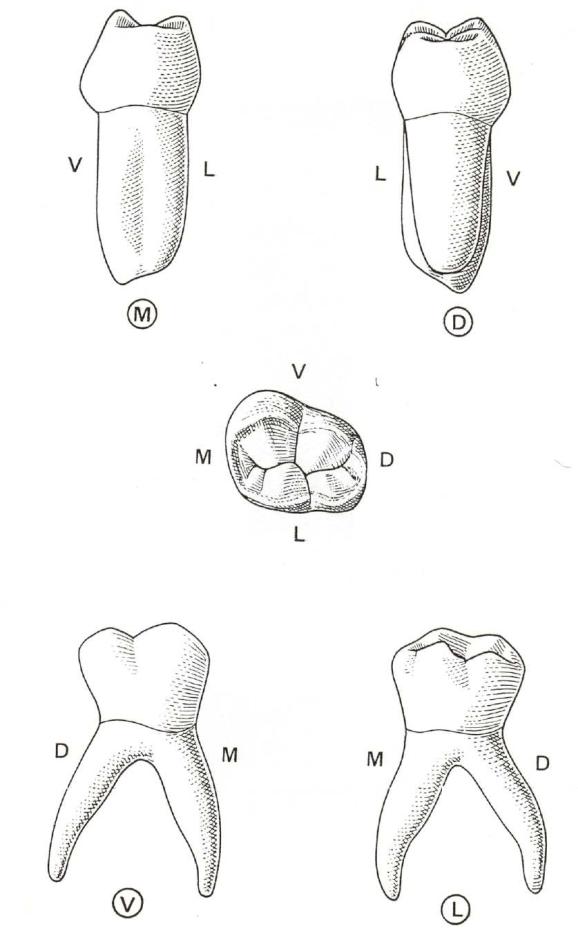
Изготовление вкладки состоит из нескольких этапов:
- Удаляются старые пломбы, формируется полость для будущей вкладки.
- Снимается оптический оттиск с помощью сканера 3D Shape Trios, потом данные передаются в зуботехническую лабораторию, где изготавливается вкладка методом компьютерного фрезерования
- Когда вкладка готова (при необходимости это может быть уже через пару часов), пациент второй раз посещает стоматолога, который примеряет и фиксирует вкладку.
Преимущества керамических вкладок перед пломбами:
- Долговечность. Пломба со временем стирается, керамика остается стабильной в полости рта, поскольку значительно прочнее композита. Средний срок использования вкладок и накладок приближен к коронкам, тогда как средний срок использования композитных реставраций — около 5 лет.
- Керамическая вкладка за счет своей неизменности «держит» прикус в правильном положении, в то время как стираемость пломбы приводит к его нарушению.
- Лучшая прочность и изностойкость, биологическая совместимость по сравнению с прямыми реставрациями в результате более полной полимеризации материала и низкой подверженности процессам биодеградации в условиях полости рта (более высокой стойкости к механическому износу и гидролизу).
- Пломба создается врачом прямо в полости рта пациента, поэтому не всегда удается восстановить правильную анатомическую форму зуба. Вкладку делают в зуботехнической лаборатории по индивидуальным слепкам человека, поэтому результат — всегда идеальное продолжение натурального зуба, а стало быть эффективное восстановление его жевательной поверхности.
- Эстетика вкладок перед пломбами неоспорима! Цвет керамики полностью совпадает с оттенком натурального зуба и имеет все его оптические свойства, например, пропускает свет. Вкладка специально прокрашивается, чтобы зуб имел натуральные оттенки.
- Технология фиксации керамической вкладки полностью исключает нарушение краевого прилегания.
 Иными словами, по ее кромке никогда не появится щель, в которую быстро проникают микроорганизмы, образуя кариес. В случае с большой пломбой такая вероятность существует.
Иными словами, по ее кромке никогда не появится щель, в которую быстро проникают микроорганизмы, образуя кариес. В случае с большой пломбой такая вероятность существует. - Существенно меньшая нагрузка на оставшиеся твердые ткани стенок сформированной полости. Композитные материалы во время фотополимеризации подвергаются объемной усадке (0,8–1,8%) в направлении источника света. При достаточно большом размере пломбы это приводит к появлению внутренних напряжений в самой реставрации, что может явиться причиной трещин в ослабленных стенках полости.
Относительными недостатками микропротезов, как и любых непрямых конструкций, являются:
- большее количество этапов и длительность лечения,
- необходимость участия в процессе зуботехнической лаборатории, использование дополнительных материалов и дорогостоящего оборудования,
- более высокая стоимость лечения.
Таким образом, вкладка-это минимально инвазивное препарирование, отличная эстетика, клинический долгосрочный результат и научно подтвержденный результат!
Результаты работ по установке вкладок:
Задать вопрос
Задать вопрос специалисту
Обратный звонок
Мы перезвоним в удобное для вас время.
Записаться на прием
Результаты работы
Отзывы
Отзывы о сети стоматологических клиник Вероника
Сопутствующие услуги
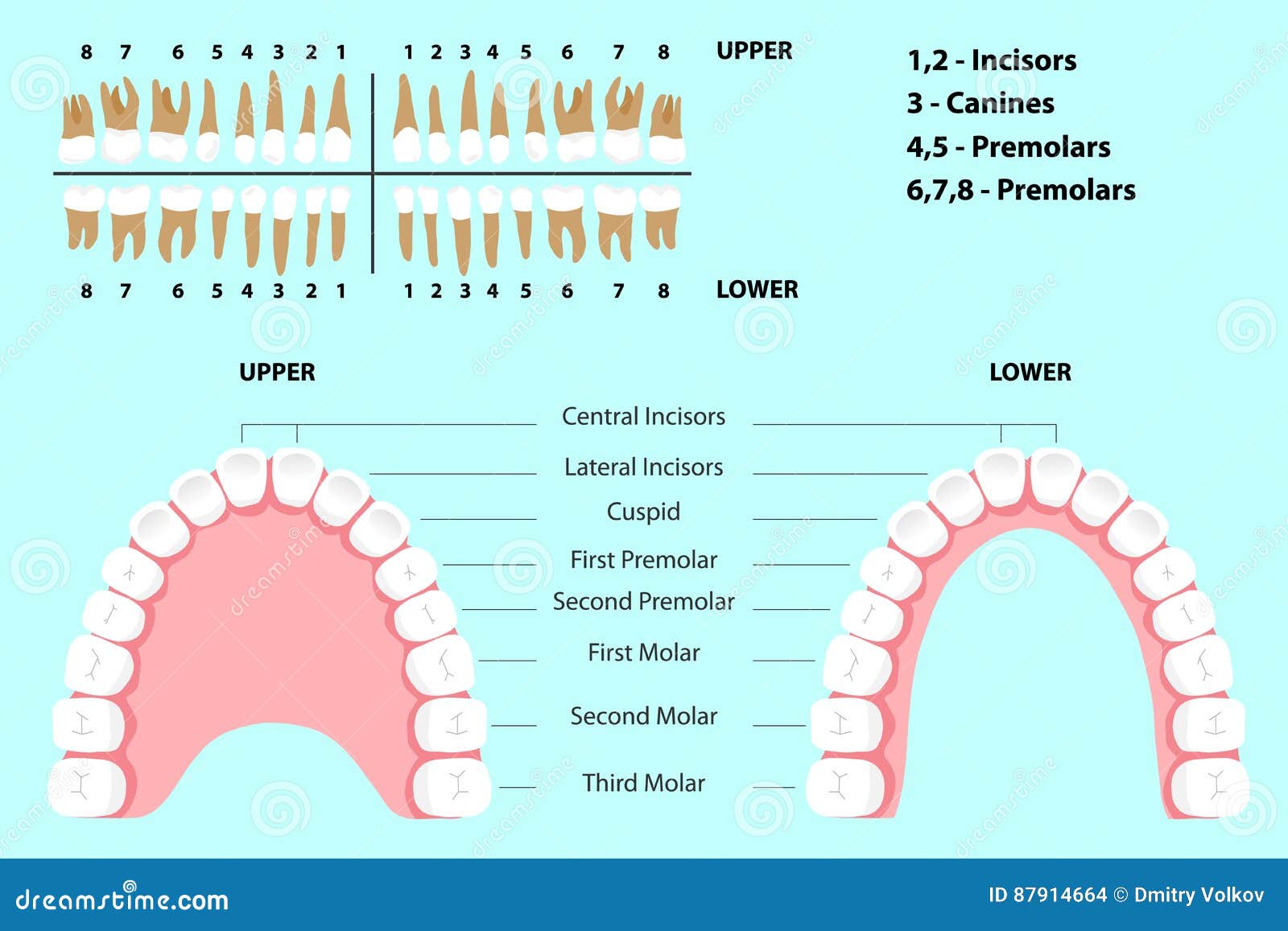
Определение моляра по Merriam-Webster
месяц | \ ˈMō-lər \ : зуб с закругленной или плоской поверхностью, приспособленный для шлифования. конкретно
: один из щечных зубов млекопитающих за резцами и клыками — см. Иллюстрацию зуба.
конкретно
: один из щечных зубов млекопитающих за резцами и клыками — см. Иллюстрацию зуба.
2 : , относящиеся к коренным зубам или расположенные рядом с ними
1 : моль вещества или относящиеся к нему молярный объем газа
2
: , содержащее один моль растворенного вещества в одном литре раствора.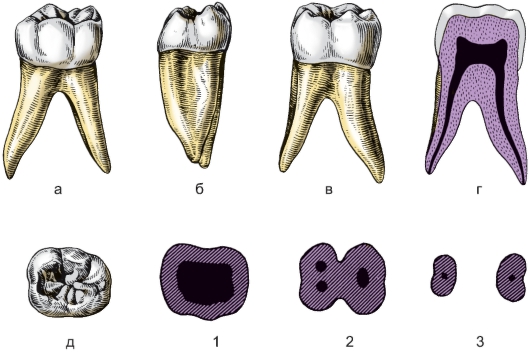
концентраторов | Безграничная химия
Молярность
Молярность определяется как количество молей растворенного вещества на объем всего раствора.
Цели обучения
Расчет концентрации раствора с использованием молярности.
Основные выводы
Ключевые моменты
- Молярность (M) указывает количество молей растворенного вещества на литр раствора (моль / литр) и является одной из наиболее распространенных единиц, используемых для измерения концентрации раствора.
- Молярность может использоваться для расчета объема растворителя или количества растворенного вещества.
- Связь между двумя растворами с одинаковым количеством молей растворенного вещества может быть представлена формулой c 1 V 1 = c 2 V 2 , где c — концентрация, а V — объем.
Ключевые термины
- разбавление : Процесс, при котором раствор становится менее концентрированным путем добавления большего количества растворителя.
- Единица СИ : Современная форма метрической системы, широко используемой в науке (сокращенно СИ от французского: Système International d’Unités).
- молярность : Концентрация вещества в растворе, выраженная в количестве молей растворенного вещества на литр раствора.
- концентрация : относительное количество растворенного вещества в растворе.
В химии концентрация раствора часто измеряется молярностью (M), которая представляет собой количество молей растворенного вещества на литр раствора. Эта молярная концентрация (c i ) рассчитывается путем деления молей растворенного вещества (n i ) на общий объем (V):
[латекс] \ text {c} _ \ text {i} = \ frac {\ text {n} _ \ text {i}} {\ text {V}} [/ latex]
Единица измерения молярной концентрации в системе СИ — моль / м 3 . Однако моль / л является более распространенной единицей измерения молярности.Раствор, содержащий 1 моль растворенного вещества на 1 литр раствора (1 моль / л), называется «один молярный» или 1 М. Единицу моль / л можно преобразовать в моль / м 3 , используя следующее уравнение:
1 моль / л = 1 моль / дм 3 = 1 моль-дм −3 = 1 M = 1000 моль / м 3
Расчет молярности
Для расчета молярности раствора количество молей растворенного вещества необходимо разделить на общее количество литров полученного раствора. Если количество растворенного вещества указано в граммах, мы должны сначала рассчитать количество молей растворенного вещества, используя молярную массу растворенного вещества, а затем рассчитать молярность, используя количество молей и общий объем.
Расчет молярности с учетом молей и объема
Если в воде (растворителе) растворено 10,0 граммов NaCl (растворенного вещества) для получения 2,0 л раствора, какова молярность этого раствора?
Во-первых, мы должны перевести массу NaCl в граммах в моль. Делаем это путем деления на молекулярную массу NaCl (58,4 г / моль).
[латекс] 10,0 \ text {граммы NaCl} \ times \ frac {\ text {1 моль}} {58,4 \ text {г / моль}} = 0,17 \ text {моль NaCl} [/ латекс]
Затем мы делим количество молей на общий объем раствора, чтобы получить концентрацию.
[латекс] \ text {c} _ \ text {i} = \ frac {\ text {n} _ \ text {i}} {\ text {V}} [/ latex]
[латекс] \ text {c} _ \ text {i} = \ frac {0,17 \ text {моль NaCl}} {2 \ text {литры раствора}} [/ латекс]
[латекс] \ text {c} _ \ text {i} = 0,1 \ text {M} [/ latex]
Раствор NaCl представляет собой 0,1 М раствор.
Расчет молей с учетом молярности
Чтобы рассчитать количество молей в растворе с учетом молярности, мы умножаем молярность на общий объем раствора в литрах.
Сколько молей хлорида калия (KCl) в 4.0 л 0,65 М раствора?
[латекс] \ text {c} _ {\ text {i}} = \ frac {\ text {n} _ {\ text {i}}} {\ text {V}} [/ latex]
[латекс] 0,65 \ text {M} = \ frac {\ text {n} _ \ text {i}} {4.0 \ text {L}} [/ latex]
[латекс] \ text {n} _ \ text {i} = (0,65 \ text {M}) (4,0 \ text {L}) = 2,6 \ text {моль KCl} [/ латекс]
В 0,65 М растворе, занимающем 4,0 л, содержится 2,6 моля KCl.
Расчет объема с учетом молярности и молей
Мы также можем рассчитать объем, необходимый для достижения определенной массы, в граммах с учетом молярности раствора.Это полезно для определенных растворенных веществ, которые не могут быть легко собраны с помощью весов. Например, диборан (B 2 H 6 ) является полезным реагентом в органическом синтезе, но также очень токсичен и легковоспламеняем. Диборан безопаснее использовать и транспортировать, если растворен в тетрагидрофуране (ТГФ).
Сколько миллилитров 3,0 М раствора Bh4-THF необходимо для получения 4,0 г Bh4?
Сначала мы должны преобразовать граммы BH 3 в моль, разделив массу на молекулярную массу.
[латекс] \ frac {4.0 \ text {g} \ text {BH} _3} {13.84 \ text {g / mol} \ text {BH} _3} = 0.29 \ text {moles} \ text {BH} _3 [ / латекс]
Как только мы узнаем, что нам нужно получить 0,29 моль BH 3, , мы можем использовать это и данную молярность (3,0 M) для расчета объема, необходимого для достижения 4,0 г.
[латекс] \ text {c} _ {\ text {i}} = \ frac {\ text {n} _ {\ text {i}}} {\ text {V}} [/ latex]
[латекс] 3.0 \ text {M} = \ frac {0.29 \ text {moles BH} _3} {\ text {V}} [/ latex]
[латекс] \ text {V} = 0.1 \ text {L} [/ latex]
Теперь, когда мы знаем, что в 0,1 л содержится 4,0 г BH 3 , мы знаем, что нам нужно 100 мл раствора, чтобы получить 4,0 г BH 3 .
Разведение
Разбавление — это процесс уменьшения концентрации растворенного вещества в растворе, обычно путем добавления большего количества растворителя. Это соотношение представлено уравнением c 1 V 1 = c 2 V 2 , где c 1 и c 2 — начальная и конечная концентрации, а V 1 и V 2 — начальный и конечный объемы раствора.
Пример 1
У ученого есть 5,0 М раствор соляной кислоты (HCl), и для его нового эксперимента требуется 150,0 мл 2,0 М HCl. Сколько воды и 5,0 M HCl должен использовать ученый, чтобы получить 150,0 мл 2,0 M HCl?
c 1 V 1 = c 2 V 2
c 1 и V 1 — концентрация и объем исходного раствора, который представляет собой 5,0 М HCl. c 2 и V 2 — концентрация и объем желаемого раствора, или 150.0 мл 2,0 М раствора HCl. Объем пока не нужно переводить в литры, потому что обе части уравнения используют мл. Следовательно:
[латекс] (5.0 \ text {M HCl}) (\ text {V} _1) = (2.0 \ text {M HCl}) (150.0 \ text {mL}) [/ латекс]
V 1 = 60,0 мл 5,0 M HCl
Если для приготовления желаемого раствора используется 60,0 мл 5,0 М HCl, можно рассчитать количество воды, необходимое для правильного разбавления раствора до нужной молярности и объема:
150.0 мл — 60,0 мл = 90,0 мл
Для того, чтобы ученый приготовил 150,0 мл 2,0 М HCl, ему потребуется 60,0 мл 5,0 М HCl и 90,0 мл воды.
Пример 2
Воду добавляли к 25 мл исходного раствора 5,0 М HBr до тех пор, пока общий объем раствора не достиг 2,5 л. Какова молярность нового раствора?
Нам дано следующее: c 1 = 5 ° M, V 1 = 0,025 л, V 2 = 2,50 л. Нас просят найти c 2 , что является молярностью разбавленного раствора. решение.
(5,0 м) (0,025 л) = c 2 (2,50 л)
[латекс] \ text {c} _2 = \ frac {(5.0 \ text {M}) (0.025 \ text {L})} {2.50 \ text {L}} = 0,05 \ text {M} [/ latex]
Обратите внимание, что все единицы объема были преобразованы в литры. Мы рассчитали, что у нас будет 0,05 М раствор, что соответствует нашим ожиданиям, учитывая, что мы разбавили 25 мл концентрированного раствора до 2500 мл.
Моляльность
Моляльность — это свойство раствора, которое указывает количество молей растворенного вещества на килограмм растворителя.
Цели обучения
Рассчитайте моляльность раствора и объясните, почему это коллигативное свойство
Основные выводы
Ключевые моменты
- Моляльность — это свойство раствора, которое определяется как количество молей растворенного вещества на килограмм растворителя.
- Единица измерения моляльности в системе СИ — моль / кг. Раствор с моляльностью 3 моль / кг часто описывается как «3 моль» или «3 моль». Однако, следуя системе единиц СИ, теперь предпочтительнее моль / кг или связанная с ней единица СИ.
- Поскольку объем раствора зависит от температуры и давления окружающей среды, масса может иметь большее значение для измерения растворов. В этих случаях подходящим измерением является молярность (а не молярность).
Ключевые термины
- моляльность : Концентрация вещества в растворе, выраженная как количество молей растворенного вещества на килограмм растворителя.
- коллигативное свойство : свойство растворов, которое зависит от отношения количества частиц растворенного вещества к количеству молекул растворителя в растворе, а не от типа присутствующих химических соединений.
- интенсивное свойство : свойство вещества, не зависящее от количества вещества.
Измерения массы (молярности) в зависимости от объема (молярности)
Моляльность — это интенсивное свойство растворов, и она рассчитывается как количество молей растворенного вещества, деленное на килограммы растворителя. В отличие от молярности, которая зависит от объема раствора, молярность зависит только от массы растворителя. Поскольку объем может изменяться из-за температуры и давления, молярность также зависит от температуры и давления.В некоторых случаях использование веса является преимуществом, поскольку масса не зависит от условий окружающей среды. Например, моляльность используется при работе с диапазоном температур.
Определение моляльности
Моляльность, b (или m), раствора определяется как количество вещества растворенного вещества в молях, n растворенного вещества , деленное на массу в кг растворителя, м растворитель :
[латекс] \ text {bM} _ {\ text {solute}} = \ frac {\ text {n} _ {\ text {solute}}} {\ text {m} _ {\ text {растворитель}}} [/ латекс]
Моляльность основана на массе, поэтому ее можно легко преобразовать в массовое отношение, обозначенное w:
.[латекс] \ text {bM} _ {\ text {solute}} = \ frac {\ text {n} _ {\ text {solute}}} {\ text {m} _ {\ text {растворитель}}} = \ frac {\ text {w} _ {\ text {solute}}} {\ text {w} _ {\ text {Solute}}} [/ latex]
По сравнению с молярной концентрацией или массовой концентрацией приготовление раствора заданной моляльности проще, поскольку для этого требуется только хороший масштаб; и растворитель, и растворенное вещество являются массами, а не измеряются по объему.Во многих слабых водных растворах молярность и моляльность аналогичны, поскольку один килограмм воды (растворителя) занимает один литр объема при комнатной температуре, а небольшое количество растворенного вещества мало влияет на объем растворителя.
Водный раствор соли : Поваренная соль легко растворяется в воде с образованием раствора. Если массы соли и воды известны, можно определить моляльность.
Единицы
Единица измерения моляльности в системе СИ — моль / кг, или моль растворенного вещества на кг растворителя.Раствор с моляльностью 1 моль / кг часто описывается как «1 моль» или «1 моль». Однако, следуя системе единиц СИ, Национальный институт стандартов и технологий, который является органом США по измерениям, считает термин «моляль» и символ единицы измерения «м» устаревшими и предлагает использовать моль / кг. или другая связанная единица СИ.
Расчет моляльности
Моляльность легко вычислить, если мы знаем массу растворенного вещества и растворителя в растворе. Моляльность — это интенсивное свойство, поэтому оно не зависит от измеряемого количества.Это верно для всех концентраций гомогенного раствора, независимо от того, исследуем ли мы образец одного и того же раствора объемом 1,0 л или 10,0 л. Концентрация или моляльность остается постоянной.
Расчет молярности с учетом массы
Если мы массируем 5,36 г KCl и растворяем это твердое вещество в 56 мл воды, какова молярность раствора? Помните, что моляльность составляет моль растворенного вещества / кг на растворитель. KCl — это наше растворенное вещество, а вода — наш растворитель. Сначала нам нужно рассчитать количество родинок в 5.36 г KCl:
[латекс] \ text {моль KCl} = 5,36 \ text {g} \ times (\ frac {1 \ text {moles}} {74,5 \ text {g}}) = 0,0719 \ text {моль KCl} [/ латекс ]
Нам также необходимо преобразовать 56,0 мл воды в эквивалентную массу в граммах, используя известную плотность воды (1,0 г / мл):
[латекс] 56,0 \ \ text {mL} \ times (\ frac {1.0 \ text {g}} {\ text {mL}}) = 56,0 \ \ text {g} [/ latex]
56,0 г воды эквивалентно 0,056 кг воды. Имея эту информацию, мы можем разделить моли растворенного вещества на кг растворителя, чтобы найти моляльность раствора:
[латекс] \ text {molality} = (\ frac {\ text {moles}} {\ text {кг растворителя}}) = (\ frac {0.0719 \ text {моль KCl}} {0,056 \ text {кг воды}}) = 1,3 \ \ text {m} [/ latex]
Моляльность нашего раствора KCl и воды составляет 1,3 м. Поскольку раствор очень разбавленный, молярность почти идентична молярности раствора, которая составляет 1,3 М.
Расчет массы с учетом моляльности
Мы также можем использовать моляльность, чтобы найти количество вещества в растворе. Например, сколько уксусной кислоты в мл необходимо для приготовления 3,0 м раствора, содержащего 25,0 г KCN?
Сначала мы должны преобразовать образец KCN из граммов в моль:
[латекс] \ text {моль KCN} = 25.0 \ text {g} \ times (\ frac {1 \ text {moles}} {65.1 \ text {g}}) = 0,38 \ text {moles} [/ latex]
Затем можно использовать моль KCN для определения килограмма уксусной кислоты. Мы умножаем количество молей на величину, обратную данной моляльности (3,0 моль / кг), чтобы наши единицы соответственно сокращались. В результате получаем желаемую массу уксусной кислоты, которая нам нужна для приготовления нашего 3 м раствора:
.[латекс] 0,38 \ text {моль KCl} \ times (\ frac {\ text {кг уксусной кислоты}} {3,0 \ text {моль KCl}}) = 0,12 \ text {кг уксусной кислоты} [/ латекс]
Получив массу уксусной кислоты в кг, переводим из кг в граммы: 0.12 кг равняется 120 г. Затем мы используем плотность уксусной кислоты (1,05 г / мл при 20 o C) для преобразования в требуемый объем в мл. Мы должны умножить на обратную величину плотности, чтобы добиться этого:
[латекс] 120,0 \ text {g уксусная кислота} \ times (\ frac {\ text {mL}} {1.05 \ text {g}}) = 114,0 \ text {мл уксусной кислоты} [/ латекс]
Следовательно, нам требуется 114 мл уксусной кислоты для приготовления 3,0 м раствора, содержащего 25,0 г KCN.
Молярность vs.молярность : В этом уроке вы узнаете, чем отличаются молярность и молярность.
Молярная доля и молярный процент
Мольная доля — это количество молекул данного компонента в смеси, деленное на общее количество молей в смеси.
Цели обучения
Рассчитайте мольную долю и мольный процент для данной концентрации смеси
Основные выводы
Ключевые моменты
- Мольная доля описывает количество молекул (или молей) одного компонента, деленное на общее количество молекул (или молей) в смеси.
- Мольная доля полезна, когда два реактивных компонента смешиваются вместе, так как соотношение двух компонентов известно, если известна мольная доля каждого.
- Умножение мольной доли на 100 дает молярный процент, который описывает то же самое, что и мольная доля, только в другой форме. Мольные доли могут быть получены из различных концентраций, включая составы молярности, молярности и массовых процентов.
Ключевые термины
- моль : основная единица СИ для количества вещества; количество вещества, которое содержит столько элементарных объектов, сколько атомов в 0.012 кг углерода-12.
- мольная доля : отношение количества молей одного компонента в смеси к общему количеству молей.
Молярная доля
В химии мольная доля, x i , определяется как количество молей компонента, n i , деленное на общее количество молей всех компонентов в смеси, n тот :
[латекс] \ text {x} _ {\ text {i}} = \ frac {\ text {n} _ {\ text {i}}} {\ text {n} _ {\ text {tot}}} [/ латекс]
Мольные доли безразмерны, а сумма всех мольных долей в данной смеси всегда равна 1.
Свойства мольной доли
Мольная доля очень часто используется при построении фазовых диаграмм. Имеет ряд преимуществ:
- Он не зависит от температуры, в отличие от молярной концентрации, и не требует знания плотности фазы (фаз).
- Смесь с известными мольными долями может быть приготовлена путем взвешивания соответствующих масс компонентов.
- Мера симметричная; в мольных долях x = 0.1 и x = 0,9, роли «растворителя» и «растворенного вещества» обратимы.
- В смеси идеальных газов мольную долю можно выразить как отношение парциального давления к общему давлению смеси.
Мольная доля в растворе хлорида натрия : Мольная доля увеличивается пропорционально массовой доле в растворе хлорида натрия.
Молярный процент
Умножение мольной доли на 100 дает мольный процент, также называемый процентным соотношением количество / количество (сокращенно n / n%).Для общей химии все мольные проценты смеси составляют в сумме 100 мольных процентов. Мы можем легко преобразовать молярный процент обратно в мольную долю, разделив на 100. Таким образом, мольная доля 0,60 равна 60,0% молярного процента.
Расчеты с молярной долей и мольным процентом
Молярная доля в смесях
Смесь газов была образована путем объединения 6,3 моль O 2 и 5,6 моль N 2 . Какая мольная доля азота в смеси?
Сначала мы должны найти общее количество молей с n итого = n N2 + n O2 .
[латекс] \ text {n} _ {\ text {total}} = 6.3 \ \ text {moles} +5.6 \ \ text {moles} = 11.9 \ \ text {moles} [/ latex].
Далее мы должны разделить моли N 2 на общее количество молей:
[латекс] x (\ text {мольная доля}) = (\ frac {\ text {моль} \ text {N} _2} {\ text {моль} \ text {N} _2 + \ text {моль} O_2} ) = (\ frac {5.6 \ text {moles}} {11.9 \ text {moles}}) = 0.47 [/ latex]
Мольная доля азота в смеси составляет 0,47.
Молярная доля в растворах
Молярная доля также может применяться в случае растворов.Например, 0,100 моль NaCl растворяют в 100,0 мл воды. Какая мольная доля NaCl?
Нам дано количество молей NaCl, но объем воды. Сначала мы преобразуем этот объем в массу, используя плотность воды (1,00 г / мл), а затем преобразуем эту массу в моль воды:
[латекс] 100 \ \ text {mL} \ H_2O \ times (\ frac {1.0 \ text {g}} {1 \ text {mL}}) = 100.0 \ \ text {g} \ \ text {H} _2 \ text {O} \ times (\ frac {1 \ text {moles}} {18.0 г}) = 5.55 \ text {moles} \ text {H} _2 \ text {O} [/ latex]
С помощью этой информации мы можем найти общее количество присутствующих родинок: 5.55 + 0,100 = 5,65 моль. Если разделить моли NaCl на общее количество молей, мы найдем мольную долю этого компонента:
[латекс] \ text {x} = (\ frac {0.100 \ text {moles}} {5.65 \ text {moles}}) = 0,0176 [/ латекс]
Мы находим, что мольная доля NaCl составляет 0,0176.
Молярная доля многокомпонентных смесей
Мольные доли также могут быть найдены для смесей, состоящих из нескольких компонентов. К ним относятся не иначе, чем раньше; опять же, общая мольная доля смеси должна быть равна 1.
Например, раствор образуется при смешивании 10,0 г пентана (C 5 H 12 ), 10,0 г гексана (C 6 H 14 ) и 10,0 г бензола (C 6 H 6 ). Какая мольная доля гексана в этой смеси?
Сначала мы должны определить количество молей, присутствующих в 10,0 г каждого компонента, с учетом их химической формулы и молекулярной массы. Количество молей каждого находится путем деления его массы на соответствующую молекулярную массу.Мы обнаружили, что имеется 0,138 моль пентана, 0,116 моль гексана и 0,128 моль бензола.
Мы можем найти общее количество молей, взяв сумму всех молей: 0,138 + 0,116 + 0,128 = 0,382 общих молей. Если разделить моли гексана на общее количество молей, мы вычислим мольную долю:
[латекс] \ text {x} = (\ frac {0,116 \ text {moles}} {0,382 \ text {moles}}) = 0,303 [/ латекс]
Мольная доля гексана составляет 0,303.
Молярная доля от моляльности
Мольную долю можно также рассчитать по моляльности.Если у нас есть 1,62 м раствор столового сахара (C 6 H 12 O 6 ) в воде, какова мольная доля столового сахара?
Поскольку нам дана моляльность, мы можем преобразовать ее в эквивалентную мольную долю, которая уже является массовым соотношением; помните, что моляльность = моль растворенного вещества / кг растворителя. Учитывая определение моляльности, мы знаем, что у нас есть раствор, содержащий 1,62 моля сахара и 1,00 кг (1000 г) воды. Поскольку мы знаем количество молей сахара, нам нужно найти количество молей воды, используя его молекулярный вес:
[латекс] 1000 \ \ text {g} \ \ text {H} _2 \ text {O} \ times (\ frac {1 \ \ text {мол}} {18.0 \ \ text {g}}) = 55,5 \ text {moles} \ text {H} _2 \ text {O} [/ latex]
Общее количество молей — это сумма молей воды и сахара, или 57,1 молей всего раствора. Теперь мы можем найти мольную долю сахара:
[латекс] \ text {x} = (\ frac {1,62 \ text {молей сахара}} {57,1 \ text {молей раствор}}) = 0,0284 [/ латекс]
При мольной доле 0,0284 мы видим, что имеем 2,84% раствор сахара в воде.
Молярная доля от массового процента
Мольную долю можно также рассчитать из массовых процентов.Какова мольная доля коричной кислоты, которая имеет массовый процент 50,00% мочевины в коричной кислоте? Молекулярная масса мочевины составляет 60,16 г / моль, а молекулярная масса коричной кислоты составляет 148,16 г / моль.
Во-первых, мы предполагаем общую массу 100,0 г, хотя можно принять любую массу. Это означает, что у нас есть 50,0 г мочевины и 50,0 г коричной кислоты. Затем мы можем вычислить количество присутствующих молей, разделив каждый на его молекулярный вес. У нас 0,833 моль мочевины и 0,388 моль коричной кислоты, так что у нас 1.Всего 22 моля.
Чтобы найти мольную долю, разделим количество молей коричной кислоты на общее количество молей:
[латекс] \ text {x} = (\ frac {.388 \ text {моль коричной кислоты}} {1,22 \ text {моль раствор}}) = 0,318 [/ латекс]
Мольная доля коричной кислоты составляет 0,318.
Что такое молярная масса? — Определение, формула и примеры — Видео и стенограмма урока
Как найти молярную массу для соединений
Соединения — это вещества, состоящие из более чем одного элемента.Например, некоторые распространенные соединения включают соль, глюкозу, уксусную кислоту (или уксус) и бикарбонат натрия (или пищевую соду).
Хлорид натрия состоит из двух элементов: натрия и хлора. Давайте использовать это соединение, хлорид натрия, в качестве нашего первого примера расчета молярной массы соединений. Первое, что нам нужно сделать, это найти натрий и хлор в периодической таблице.
Шаг 1: Найдите атомные массы отдельных элементов в периодической таблице.
Первое, что нам нужно, это найти отдельные атомные массы для каждого элемента.Если вы посмотрите записи для натрия и хлора в таблице, мы обратим внимание на цифры, которые появляются в верхнем левом углу (см. Видео). Они представляют собой атомную массу. Элемент натрия имеет атомную массу 22,98976 г / моль. Элемент хлор имеет атомную массу 35,453 г / моль.
Шаг 2: Подсчитайте количество атомов для каждого элемента
Для соединения хлорида натрия, поскольку нет нижних индексов (маленькие числа внизу символа каждого элемента), это означает, что имеется только один натрий и только один хлор. атом для этого соединения.
Шаг 3: Найдите молярную массу
Теперь, когда мы знаем, сколько атомов имеется у каждого элемента, мы можем найти молярную массу.
Сначала мы вычисляем массу атомов натрия, которая составляет 22,98976 граммов на моль. Затем мы проделаем то же самое с массой атомов хлора, которая составляет 35,453 грамма на моль. Затем мы складываем эти две массы вместе, чтобы найти общую массу молекул хлорида натрия. Получается 58,44276 граммов на моль, которые мы можем округлить до 58.44 грамма на моль.
Пример: расчет молярной массы соединения
Давайте рассмотрим более сложный пример.
Найдите молярную массу уксусной кислоты .
Есть три элемента — углерод, водород и кислород — поэтому найдите их атомные массы в периодической таблице: 12,0107 грамма на моль для углерода, 1,00794 грамма на моль для водорода и 15,9994 грамма на моль для кислорода.
Далее, мы должны учитывать, что каждый элемент в химическом соединении имеет нижний индекс, поэтому у каждого атома более одного.У нас есть два атома углерода, четыре атома водорода и два атома кислорода.
Теперь мы можем найти молярную массу каждого элемента. Для углерода мы умножаем его молярную массу 12,0107 грамма на моль на два, потому что у нас есть два атома углерода. Это равняется 24,0214 грамма на моль. Для водорода мы умножаем молярную массу 1,00794 на 4. Это равняется 4,03176 грамма на моль. Наконец, для кислорода мы умножаем молярную массу 15,9994 на 2. Это равняется 31,9988 грамма на моль.
Теперь, чтобы закончить, мы должны сложить все эти массы вместе, что дает нам в общей сложности 60.05196 грамм на моль для нашего соединения.
Расчет количества граммов по молярной массе
Ранее мы упоминали, что в научной лаборатории мы измеряем вес вещества в граммах. Иногда нам известно только количество молей присутствующего вещества. Проблема в том, что мы не можем измерить эти родинки с помощью прибора, чтобы определить массу. Здесь и появляется молярная масса. Мы можем использовать это, чтобы преобразовать любое количество молей в граммы, используя простую формулу. Количество граммов равно молярной массе элемента или соединения, умноженной на количество молей.
Допустим, нам нужно получить вес в граммах 1,5 моля пищевой соды. Как мы это делаем? Нам нужно получить молярную массу сложной пищевой соды, в данном случае 84 грамма на моль, и умножить ее на 1,5.
Когда мы умножаем количество молей на молярную массу, единица «моль» отменяется, и мы остаемся с единицей «граммы». В данном случае у нас 126 граммов пищевой соды.
Что, если мы хотим получить вес 0,5 моля соли или хлорида натрия в граммах? Молярная масса соли составляет 58,44 грамма на моль. Когда мы умножаем эти два вместе, мы получаем, что масса 0,5 моля соли составляет 29,22 грамма.
Резюме урока
Молярная масса — это масса всех атомов в молекуле в граммах на моль. Чтобы вычислить молярную массу молекулы, мы сначала получаем атомные веса отдельных элементов периодической таблицы.Затем мы подсчитываем количество атомов и умножаем его на массы отдельных атомов. Наконец, мы складываем все атомные массы вместе, чтобы получить молярную массу.
Молярная масса также является важным коэффициентом пересчета из молей в граммы. Для этого умножаем количество молей вещества на молярную массу. Этот коэффициент пересчета важен при количественном определении веса в граммах в научных экспериментах.
Быстрые заметки
- Молярная масса — это масса всех атомов молекулы в граммах на моль.
- Молярную массу можно использовать для расчета массы соединения и перевода молей в граммы.
Результаты обучения
После изучения урока примените свои знания о молярной массе, чтобы сделать следующее:
- Обсудите значение молярной массы и молярной массы
- Использовать молярную массу для определения массы соединения
- Перевести моль вещества в граммы
Что такое молярное решение?
Молярность — еще одно стандартное выражение концентрации раствора.Молярные растворы используют грамм молекулярной массы растворенного вещества при расчете молярной концентрации в литре (л) раствора.
Молекулярная масса грамма (GMW) вещества (иногда называемая «формульной массой») — это сумма объединенных атомных масс всех атомов в молекуле, выраженная в граммах. Например, GMW NaCl равен атомному весу (эти атомные веса могут быть найдены в периодической таблице или как формула веса на бутылке с веществом) Na (22.99) и атомный вес Cl (35,45), всего 58,44 г.
1 молярный (M) раствор будет содержать 1,0 GMW вещества, растворенного в воде, чтобы получить 1 литр конечного раствора. Следовательно, 1М раствор NaCl содержит 58,44 г.
Пример:
HCl часто используется в гистохимии ферментов. GMW HCl будет атомной массой H, добавленной к атомной массе Cl: H = 1 + Cl = 35,45 = 36,45 г. В литре 1M раствора HCl содержится 36,45 г.
Буфер дигидрофосфата натрия (NaH 2 PO 4 ) также используется в гистохимии ферментов. литра 1M раствора NaH 2 PO 4 будет содержать Na (22,99) + 2 H (1×2 = 2) + P (30,97) + 4 O (16×4 = 64) для общего GMW , равного 119,98. грамм.
Чтобы просто рассчитать количество или вес вещества, необходимого для желаемого молярного раствора, можно использовать следующую формулу:
Вес в граммах = желаемая молярность x необходимый объем в литрах x GMW
— — OR —
(W = M x V x GMW)
Пример:
500 мл 0.Для процедуры необходим 1М раствор NaOH. Рассчитайте количество растворенного вещества (NaOH), необходимое для приготовления раствора. (атомные массы: Na = 22,99; O = 16; H = 1)
X g = 0,1M x 500 мл x GMW 39,99
X = 0,1 x 0,5 x 39,99
X = 1,99995 или 2
2,0 г NaOH необходимо разбавить до 500 мл, чтобы приготовить 0,1М раствор.
В чем разница между молярной массой и молекулярной массой?
Обновлено 14 февраля 2020 г.
Автор: Riti Gupta
Проверено: Lana Bandoim, B.С.
Все дело в агрегатах. Понимание разницы между молекулярной массой и молярной массой сводится к разнице в том, что считается и в единицах измерения.
Молекулярная масса — это масса молекулы вещества. Его также можно назвать молекулярной массой. Единицы измерения молекулярной массы — атомные единицы массы (а.е.м.).
Молярная масса — масса одного моля вещества. Молярная масса указывается в граммах на моль или г / моль.
В чем разница между молекулой и кротом?
Молекула — самая маленькая частица в элементе или соединении, которая все еще обладает свойствами этой молекулы или соединения. Например, CO 2 или диоксид углерода представляет собой соединение. Самая маленькая частица углекислого газа — это отдельная молекула CO 2 . Если вы попытаетесь разделить его дальше на элементы, участвующие в CO 2, , это больше не будет CO 2 .
моль (моль) — это просто число.В частности, это число 6.022×10 23 , которое также известно как число Авогадро. Таким образом, моль CO 2 составляет 6.022×10 23 молекул CO 2 . Однако моль не обязательно относится к молекулам. Как было сказано ранее, это просто число. Это означает, что если вы видите моль фламинго (животное), значит, это фламинго 6.022×10 23 . Неважно, что вы измеряете.
Другими словами, моль — это просто удобный способ сказать 6.022×10 23 в том же смысле, что дюжина — это удобный способ сказать двенадцать.
Как рассчитать молекулярный вес?
Во-первых, вам понадобится масса отдельных соединений. Это число находится под элементом в таблице периодов. Например, молекулярная масса кислорода составляет 16,00 а.е.м.
Когда вы знаете массу отдельных компонентов соединения, вы можете определить молекулярную массу.
Например, молекулярная масса воды (H 2 O) равна:
Масса водорода равна 1.008 а.е.м., а масса кислорода — 16,00 а.е.м. Подсчет этого дает:
Суммирование молекулярных масс каждого элемента вместе дает:
Таким образом, молекулярная масса воды составляет 18,02 а.е.м.
Как рассчитать молярную массу вещества?
Теперь, когда вы уже знаете, как рассчитать молекулярную массу, вычислить молярную массу очень просто. Почему? Как только вы знаете молекулярную массу, вы также знаете и молярную массу.
Молекулярная масса натрия 22.99 а.е.м. Молярная масса натрия составляет 22,99 грамма на моль (г / моль). Это так просто!
Так как же тогда вычислить молярную массу воды?
Вам необходимо знать молярную массу элементов, входящих в состав воды. Молярная масса водорода составляет 1,008 г / моль, как указано в таблице периодов. Молярная масса кислорода составляет 16,00 г / моль. Итак:
Помните, вы должны учитывать две части водорода на один кислород, поэтому перед молярной массой кислорода стоит два.Вставка молярной массы каждого элемента дает:
Молярная масса воды составляет 18,02 г / моль. Вы заметите, что это то же число, что и у вас для молекулярной массы, но единицы измерения другие.
Как определить молярную концентрацию
Обновлено 4 марта 2020 г.
Рити Гупта
Проверено: Lana Bandoim, B.S.
Уметь рассчитывать концентрацию раствора — один из основных навыков, необходимых ученому.Не зная, с каким количеством вещества вы работаете, вы не можете контролировать проводимые реакции.
Концентрация раствора: определение
Концентрация раствора в основном указывается в молярности или молях на литр. Сокращенное обозначение молярности — M , единицы концентрации — моль / л .
Определение молярности означает, что вы можете найти молярность раствора, если знаете общее количество молей растворенного вещества и общий объем раствора.Итак, чтобы рассчитать концентрацию раствора (в молярности), вам нужно разделить моли растворенного вещества на общий объем.
Расчет молярной концентрации раствора
Допустим, у вас есть 10 моль NaCl, а общий объем раствора составляет 5 л. Чтобы определить молярность этого раствора, вам нужно разделить общее количество молей растворенного вещества (NaCl) на общий объем:
Это означает, что ваш 5 л раствор, содержащий 10 моль NaCl, является 2 М раствором NaCl. Здесь «М» произносится вслух как «коренной зуб».«
Что делать, если у вас есть раствор, содержащий 10 граммов NaCl в 5 л раствора?
Чтобы найти концентрацию этого нового раствора, вам необходимо преобразовать из граммов в моль. молярная масса (выраженная в граммах / моль) NaCl. Молярная масса вещества находится путем сложения молярной массы отдельных компонентов. Для NaCl двумя компонентами являются натрий и хлорид.
Чтобы найти молярную массу любого из них, вам нужно заглянуть под их символы в таблице Менделеева.Молярная масса натрия составляет 22,99 г / моль, а молярная масса хлора составляет 35,45 г / моль. В сумме это дает молярную массу NaCl, которая составляет 58,44 г / моль.
Теперь вы можете найти концентрацию 5-литрового раствора, который содержит 10 граммов NaCl.
Начните с преобразования граммов в моль:
Затем вам нужно разделить количество молей на общий объем, чтобы найти концентрацию:
Это означает, что если у вас есть 10 граммов NaCl в 5-литровом растворе, вы получите иметь 0.034 М раствор NaCl.
Что делать, если у вас есть раствор, содержащий 1000 миллиграммов NaCl в 5 л раствора?
В этом случае вам нужно сначала перевести миллиграммы в граммы. В 1 грамме 1000 миллиграммов.
Теперь, когда вы знаете, что 1000 миллиграммов соответствует 1 грамму, вы можете преобразовать граммы в моль, используя молярную массу:
Наконец, вы можете взять количество молей и разделить на общий объем:
Таким образом, 1000 граммов NaCl в 5 л общего раствора совпадает с 0.0034 М раствор NaCl.
Общие уравнения для определения концентрации
Ниже показана обобщенная версия шагов, показанных выше, или «Формула концентрации ».
Учитывая количество растворенного вещества и литры раствора, молярность рассчитывается по формуле:
Учитывая количество растворенного вещества в граммах, следующее уравнение дает концентрацию:
Учитывая количество растворенного вещества в миллиграммах, следующее уравнение дает концентрацию:
Как рассчитать молярную концентрацию раствора | FAQ
Единица молярной концентрации [моль / л (М)] традиционно широко используется в качестве метода концентрации.Это количество молей целевого вещества (растворенного вещества), растворенных в 1 литре раствора. Вот как рассчитать концентрацию.
(вес 1 литра раствора) x (чистота) ÷ молекулярная масса
[удельный вес раствора (г / мл) x 1000 (мл) x чистота (вес / вес%) / 100 ÷ молекулярный вес]
Например, рассчитаем молярную концентрацию 2-меркаптоэтанола (HSCH 2 CH 2 OH). Необходимая информация следующая.
- Удельный вес (или плотность) = 1.114 г / мл
- Чистота (или содержание) = 100 мас.% (Предположительно)
- Молекулярный вес = 78,13
Рассчитав это значение, применив это значение к приведенному выше уравнению, вы можете узнать молярную концентрацию.
1,114 г / мл x 1000 мл x 100 мас.% / 100 ÷ 78,13 = 14,26 моль / л
Чтобы рассчитать концентрацию, как указано выше, необходимо знать три точки: «удельный вес (или плотность)», «чистота (или содержание)» и «молекулярный вес». Приведенная ниже таблица представляет собой краткую справочную таблицу общих концентраций кислоты и основания.В кислотах и щелочах используется «нейтрализационное титрование», часто используется «нормальность (N)».
【Краткая справочная таблица общих концентраций кислот и оснований】
| Соединение | Молекулярная формула | Молекулярный вес | Purity (w / w %) |
Удельный вес (20 ℃) |
Концентрация (моль / л) |
эквивалент | Нормальность (N) |
|---|---|---|---|---|---|---|---|
| Соляная кислота | HCl | 36.46 | 20% | 1,10 | 6,0 | 1 | 6,0 |
| 35% | 1,17 | 11,2 | 11,2 | ||||
| Азотная кислота | HNO 3 | 63,01 | 60% | 1,37 | 13,0 | 1 | 13,0 |
| 65% | 1,39 | 14,3 | 14,3 | ||||
| 70% | 1.41 | 15,7 | 15,7 | ||||
| Сульфат | H 2 SO 4 | 98,08 | 100% | 1,83 | 18,7 | 2 | 37,3 |
| Фосфорная кислота | H 3 PO 4 | 98,00 | 85% | 1,69 | 14,7 | 3 | 44,0 |
| 90% | 1,75 | 16.1 | 48,2 | ||||
| Ацетат | CH 3 COOH | 60,05 | 100% | 1,05 | 17,5 | 1 | 17,5 |
| Хлорная кислота | HClO 4 | 100,46 | 60% | 1,54 | 9,2 | 1 | 9,2 |
| 70% | 1,67 | 11,6 | 11,6 | ||||
| Вода с перекисью водорода | H 2 O 2 | 34.01 | 30% | 1,11 | 9,8 | – | |
| 35% | 1,13 | 11,6 | |||||
| Аммиачная вода | NH 3 | 17,03 | 25% | 0,91 | 13,4 | 1 | 13,4 |
| 28% | 0,90 | 14,8 | 14,8 | ||||
【Краткий справочник по концентрации и единицам измерения】
● Как выразить концентрацию раствора
| Выражение | Комментарий |
|---|---|
| Массовая процентная концентрация | «г» растворенного вещества в 100 г. раствора.Во многих случаях выражается как мас.%, Мас.% И% для плотности. |
| Объемная процентная концентрация | «м-число» растворенного вещества в 100м растворе. Выражается как об. / Об., Когда смесь или растворенное вещество являются жидкими. |
| Массовая зависимость от концентрации в процентах от объема | Количество растворенного веществаг в 100 мл раствора. Выражается в% мас. / Об. |
| Нормальность | грамм эквивалентного количества растворенного вещества в 1 л раствора. Выражается как N для анализа емкости. |
| Объемная удельная концентрация | Концентрация косвенно выражается объемным соотношением разбавленного жидкого реагента. Он используется в JIS и других. Пример: Серная кислота (1 + 2) → Серная кислота показана разбавленной 2 объемами воды. |
| Массовая доля концентрации | Концентрация, косвенно выраженная через массовое соотношение, при котором растворяется твердый реагент. Он используется в JIS и других. Пример: хлорид натрия (1 + 19) → Растворено в 19 вес. Воды по отношению к 1 NaCl. |
| Молярность | Моль количество целевого вещества (растворенного вещества) в 1 л раствора. Выражается как моль / или М. |
● Префикс, представляющий несколько
| Экспресс | Экспресс малая | |||
|---|---|---|---|---|
| 100 = 10 2 | часов (Hecto) | 1/100 = 10 -2 | c (Centi) | % (Percent) |
| 1000 = 10 3 | k (килограмм) | 1/1000 = 10 -3 | м (Милли) | ‰ (Permili) |
| 100 万 = 10 6 | M (Mega) | 1/100 万 = 10 -6 | мкм (Micro) | частей на миллион |
| 1 миллиард = 10 9 | G (Гига) | 1/10 миллиарда = 10 -9 | n (Nano) | частей на миллиард |
| 1 триллион = 10 12 | T (Tera) | 1/1 триллиона = 10 -12 | p (Pico) | п.п. |
| 1000 триллионов = 10 15 | p (Peta) | 1/1000 триллиона = 10 -15 | f (Femto) | чел. / Кв. |
● ppm Таблица преобразования
| частей на миллиард | частей на миллион | % | мг / г | мг / л |
|---|---|---|---|---|
| 1000 | 1 | 0.0001 | 0,001 | 1 |
| 10 000 | 10 | 0,001 | 0,01 | 10 |
| 100 000 | 100 | 0,01 | 0,1 | 100 |
| 1000000 | 1 000 90 530 | 0,1 | 1 | 1 000 90 530 |
| 10 000 000 | 10 000 | 1 | 10 | 10 000 |
