Ципролет капли глазные 0,3% 5мл
Международное непатентованное название. Ципрофлоксацин
Лекарственная форма. Капли глазные 0,3%
Состав. 1 мл препарата содержит
активное вещество — ципрофлоксацина (в виде ципрофлоксацина гидрохлорида) – 3мг,
вспомогательные вещества: бензалкония хлорид, динатрия эдетат, натрия хлорид, натрия гидроксид, кислота хлороводородная, вода для инъекций.
Фармакотерапевтическая группа. Препараты для лечения заболеваний глаз. Противомикробные препараты другие. Ципрофлоксацин. Код АТХ S01АХ13
Фармакокинетика
Ципрофлоксацин при местном применении в виде глазных капель хорошо проникает в ткани глаза. После однократной инстилляции его концентрация во влаге передней камеры глаза через 10 минут составляет 0,1 мг/мл. Максимальная концентрация во влаге передней камеры определенная через 1 час и составляет 0,19 мг/мл. По истечении 2-х часов концентрация начинает снижаться, однако антибактериальное его действие в тканях роговицы сохраняется до 6 часов, во влаге передней камеры до 4-х часов. При лечении в течение 7 дней, в среднем, 4 раза в день в оба глаза, средняя концентрация составляет менее 2 нг/мл.
При лечении в течение 7 дней, в среднем, 4 раза в день в оба глаза, средняя концентрация составляет менее 2 нг/мл.
После инстилляции возможна системная абсорбция препарата.
Период полувыведения из сыворотки крови при местном применении составляет 4-5 часов. Препарат выводится через почки преимущественно (до 50 %) в неизмененном виде и до 10 % в виде метаболитов; порядка 15 % выводится через кишечник; у кормящих грудью матерей — частично выводится с грудным молоком.
Фармакодинамика
Ципрофлоксацин — антибактериальный препарат из группы фторхинолонов, обладает широким спектром антибактериального действия, оказывает бактерицидный эффект. Препарат ингибирует фермент ДНК-гиразу бактерий, вследствие чего нарушается репликация ДНК и синтез клеточных белков бактерий. Ципрофлоксацин действует как на размножающиеся микроорганизмы, так и на находящиеся в стадии покоя.
Спектр антибактериального действия ципрофлоксацина включает грамотрицательные микроорганизмы: Esherichia coli, Salmonella spp. , Shigella spp., Proteus spp. (индолположительный и индолотрицательный), Morganella morganii, Citrobacter spp., Klebsiella spp., Enterobacter spp., Vibrio spp., Campylobacter spp., Hafnia spp., Providencia stuartii, Haemophilus influenzae, Pasteurella multocida, Pseudomonas spp., Gardnerella spp., Legionella pneumophila, Neisseria spp., Moraxella catarrhalis, Acinetobacterspp., Brucella spp., Chlamidia spp.
, Shigella spp., Proteus spp. (индолположительный и индолотрицательный), Morganella morganii, Citrobacter spp., Klebsiella spp., Enterobacter spp., Vibrio spp., Campylobacter spp., Hafnia spp., Providencia stuartii, Haemophilus influenzae, Pasteurella multocida, Pseudomonas spp., Gardnerella spp., Legionella pneumophila, Neisseria spp., Moraxella catarrhalis, Acinetobacterspp., Brucella spp., Chlamidia spp.
К ципрофлоксацину чувствительны также грамположительные микроорганизмы:
Staphylococcus spp., Streptococcus pyogenes, St. Agalactiae, Corynebacterium diphtheriae, Listeria monocitogenes. Препарат малотоксичен.
Показания к применению
Бактериальные воспалительные заболевания глаза и его придатков
— острый и подострый конъюнктивит
— кератит
— передний увеит
— блефарит и другие воспалительные заболевания век
— дакриоцистит
— профилактика и лечение инфекционных осложнений после ранений глаза и его придатков и при операциях на глазном яблоке
Способ применения и дозы
Местно. Препарат закапывают по 1-2 капли в конъюнктивальный мешок. Частота инстилляций зависит от тяжести воспалительного процесса.
Препарат закапывают по 1-2 капли в конъюнктивальный мешок. Частота инстилляций зависит от тяжести воспалительного процесса.
При острых бактериальных конъюнктивитах, простых, чешуйчатых и язвенных блефаритах Ципромед назначают от 4-х до 8 раз в день в зависимости от тяжести заболевания. Курс лечения от 5 до 14 дней.
При кератитах препарат назначается по 1 капле не менее 6 раз в день, при наличии положительного эффекта максимальный курс лечения в зависимости от тяжести поражения роговицы составляет 2-4 недели.
При поражении роговицы синегнойной палочкой Ципромед назначают как можно чаще — не менее 8-12 раз в день по 1 капле. Курс лечения зависит от течения болезни и обычно составляет около 2-3 недель.
При передних увеитах препарат закапывают 8-12 раз в день по 1 капле.
При острых дакриоциститах и каналикулитах Ципромед назначают 6-12 раз в день, при хронических — 4-8 раз в день по 1 капле.
При ранениях глаза и его придатков для профилактики вторичной инфекции Ципромед назначают в течение 1-2 недель по 1 капле 4-8 раз в день.
Для профилактики воспалительных заболеваний после хирургических вмешательств с перфорацией глазного яблока Ципромед назначают 4-6 раз в день по 1 капле на весь срок послеоперационного периода, обычно от 5 дней до 1 месяца.
Побочные действия
Местные:
Часто
— зуд глаза, раздражение глаза
— дискомфорт в глазу, ощущение инородного тела в глазу, абнормальные ощущения в глазу
— образование корок по краю века
— гиперемия конъюнктивы, гиперемия глаза
— остаток препарата
Нечасто
— кератит, кератопатия, окрашивание роговицы
— аллергия глаза
— снижение остроты зрения, затуманивание зрения, светобоязнь
— отек века
— инфильтрация роговицы
— боль в глазу
— увеличение слезоточивости
Системные:
Часто: извращение вкуса
Нечасто
— постназальный синдром
— тошнота
— дерматит
— герпетический кератит, простой герпес глазного нерва, ячмень
— гиперчувствительность
— головная боль
Противопоказания
— повышенная чувствительность к компонентам препарата или к другим хинолонам
— детский возраст до 8 лет
Лекарственные взаимодействия. Раствор ципрофлоксацина несовместим с лекарственными препаратами со значением рН 3-4, которые физически или химически нестабильны.
Раствор ципрофлоксацина несовместим с лекарственными препаратами со значением рН 3-4, которые физически или химически нестабильны.
Особые указания
Препарат для местного офтальмологического применения, не использовать для инъекций или приема внутрь.
Следует прекратить применение препарата Ципромед капли глазные при первых проявлениях кожной сыпи или любого другого признака повышенной чувствительности.
Серьезные в некоторых случаях летальные реакции повышенной чувствительности (анафилактические реакции), иногда после первой дозы, наблюдались у больных, принимавших системные хинолоны. Некоторые реакции сопровождались сердечно-сосудистой недостаточностью, потерей сознания, покалыванием, отеком гортани или лица, одышкой, крапивницей и зудом. Серьезные острые реакции гиперчувствительности требуют незамедлительную неотложную терапию эпинефрином (адреналином) и другие меры реанимации, включая прием кислорода, внутривенных растворов, внутривенных антигистаминных средств, кортикоидов, сосудосуживающие факторы и искусственную вентиляцию легких, в случае клинической необходимости.
Известно о случаях проявления от умеренной до тяжелой степени фототоксичности в виде реакций солнечного ожога у пациентов, находившихся под прямыми солнечными лучами во время системного приема некоторых представителей класса хинолонов. Следует избегать чрезмерного солнечного света. При проявлении случаев фототоксичности следует прекратить лечение.
Как и с другими антибактериальными препаратами, длительное применение может привести к избыточному количеству невосприимчивых бактериальных штаммов или грибков. В случае возникновения суперинфекции следует начать соответствующую терапию.
При системном лечении фторхинолонами, в том числе ципрофлоксацином, особенно у пожилых пациентов и у пациентов принимающих совместно кортикостероиды, возможны случаи воспаления и разрывов сухожилий. Поэтому лечение каплями глазными Ципромед должно быть прекращено при первых признаках воспаления сухожилий.
Беременность и период лактации
Ципромед следует применять во время беременности только в случае, когда потенциальная польза для матери превышает возможный риск для плода.
При применении препарата в период грудного вскармливания следует прекратить кормление грудью.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами. Сразу после закапывания препарата возможно снижение чёткости зрения и замедление психических реакций, что может уменьшить способность к активному участию в уличном движении, обслуживанию машин или к выполнению работ без опоры. В ещё большей степени это имеет место при одновременном применении препарата с алкоголем.
Передозировка
Симптомы: При случайном приеме Ципромеда внутрь специфические симптомы отсутствуют. Возможны тошнота, рвота, диарея, головная боль, обморок, чувство тревоги.
Лечение: обильно промыть под чистой проточной водой. При необходимости проводят симптоматическую терапию.
Условия хранения. Хранить в защищенном от света месте при температуре не выше 25С. Не замораживать. Хранить в недоступном для детей месте!
Не замораживать. Хранить в недоступном для детей месте!
Срок хранения. 2 года
Период применения после вскрытия флакона 1 месяц.
Не использовать после истечения срока годности, указанного на упаковке!
ᐉ Ципролет А таблетки покрытые пленочной оболочкой 500 мг + 600 мг №10 (8901148224339)
Фармакологические свойства
Фармакодинамика. фармакологические свойства препарата ципролет а обусловлены фармакологическими свойствами каждого его вещества. механизм действия ципрофлоксацина обусловлен угнетением бактериального фермента днк-гиразы бактерий. результатом такого угнетения является нарушение объемной структуры днк бактерий и делает невозможным дальнейшее деление бактериальных клеток. ципрофлоксацин активен в отношении грамположительных и грамотрицательных бактерий.
Спектр действия ципрофлоксацина охватывает такие микроорганизмы:
аэробные грамотрицательные бактерии — Escherichia coli, Klebsiella pneumoniae, Salmonella typhi, Рroteus mirabilis, Proteus vulgaris, Shigella sonnei, Shigella boydii, Shigella dysenteriae, Shigella flexneri, Enterobacter cloacae, Morganella morganii, Providencia rettgeri, Providencia stuartii, Citrobacter diversus, Citrobacter freundii, Serratia marcescens, Campylobacter jejuni, Pseudomonas aeruginosa, Neisseria gonorrhoeae, Haemophilus influenzae, Haemophilus parainfluenzae, Bacillus anthracis.
аэробные грамположительные бактерии — стафилококки, включая штаммы, продуцирующие пенициллиназу, и штаммы, резистентные к метициллину, стрептококки, в том числе Streptococcus рneumoniae, Listeria monocytogenes, Corynebacterium spp.
Тинидазол является производным 5-нитроимидазола с замещенным имидазоловым компонентом, который способен действовать против анаэробных бактерий и простейших. Механизм действия тинидазола на анаэробные бактерии и простейшие связывают с проникновением препарата в клетки микроорганизмов и с повреждением ДНК или угнетением ее синтеза.
Тинидазол является активным как в отношении простых, так и облигатных анаэробных бактерий. Простейшие микроорганизмы, чувствительные к тинидазолу, включают Trichomonas vaginalis, Entamoeba histolytica и Giardia lamblia.
Тинидазол активен по отношению к Gardnerella vaginalis и большинству анаэробных бактерий, включая Bacteroides fragilis, Bacteroides melaninogenicus, Bacteroides spp., Clostridium spp.
Фармакокинетика. Ципрофлоксацин быстро всасывается после перорального приема. Биодоступность составляет около 70%. Пища не влияет на степень абсорбции ципрофлоксацина, но может замедлить скорость всасывания. Cmax ципрофлоксацина в плазме крови достигается через 1–2 ч. Ципрофлоксацин достигает терапевтических концентраций почти во всех тканях и жидкостях организма. Связывание с белками плазмы крови незначительное — 20–40%. Т½ составляет 3–5 ч.
Тинидазол быстро и полностью всасывается при приеме внутрь.
После приема тинидазола в дозе 2 г внутрь концентрация в плазме крови достигала пика в 40–51 мкг/мл в течение 2 ч и снижалась до 11–19 мкг/мл через 24 ч. Т Тинидазол выделяется печенью и почками. В течение 5 дней 60–65% введенной дозы выводится с мочой, причем 20–25% — в неизмененном виде. Около 12% дозы выводится с калом.
Тинидазол выделяется печенью и почками. В течение 5 дней 60–65% введенной дозы выводится с мочой, причем 20–25% — в неизмененном виде. Около 12% дозы выводится с калом.
Показания
Инфекции, вызванные чувствительными к препарату микроорганизмами, включая смешанные аэробно-анаэробные инфекции, протозойные инфекции: дыхательных путей — плеврит, эмпиема плевры, абсцесс легких; лор-органов — хронический синусит, мастоидит; кожи и мягких тканей — инфицированные язвы, абсцессы, целлюлит, инфекции мягких тканей у больных сахарным диабетом; жкт — бактериальная диарея, дизентерия, амебиаз, другие смешанные инфекции жкт; интраабдоминальные инфекции; гинекологические инфекции; инфекции костей — хронический остеомиелит; стоматологические инфекции.
Применение
Обычная доза препарата ципролет а для взрослых — 1 таблетка 2 раза в сутки. применяют у взрослых внутрь за 1 ч до или через 2 ч после еды. таблетки следует глотать не разжевывая, запивая небольшим количеством жидкости. для больных с клиренсом креатинина 31–60 мл/мин максимальная суточная доза препарата должна составлять 2 таблетки в сутки, для больных с клиренсом креатинина ≤30 мл/мин — 1 таблетка в сутки. при инфекциях тяжелого течения органов брюшной полости, дыхательных путей, при хроническом остеомиелите максимальная суточная доза — 3 таблетки в сутки. курс лечения зависит от тяжести инфекции и результатов бактериологических исследований. обычный курс лечения при острых инфекциях составляет 5–7 дней, но в случае лечения хронических рецидивирующих инфекций курс лечения составляет 10–14 дней. рекомендуется продолжать прием препарата в течение по крайней мере 3 дней после нормализации температуры тела или устранения симптомов болезни.
для больных с клиренсом креатинина 31–60 мл/мин максимальная суточная доза препарата должна составлять 2 таблетки в сутки, для больных с клиренсом креатинина ≤30 мл/мин — 1 таблетка в сутки. при инфекциях тяжелого течения органов брюшной полости, дыхательных путей, при хроническом остеомиелите максимальная суточная доза — 3 таблетки в сутки. курс лечения зависит от тяжести инфекции и результатов бактериологических исследований. обычный курс лечения при острых инфекциях составляет 5–7 дней, но в случае лечения хронических рецидивирующих инфекций курс лечения составляет 10–14 дней. рекомендуется продолжать прием препарата в течение по крайней мере 3 дней после нормализации температуры тела или устранения симптомов болезни.
Противопоказания
Повышенная чувствительность к ципрофлоксацину или другим фторхинолонам, повышенная чувствительность к тинидазолу или другим производным 5-нитроимидазола, органические неврологические нарушения, заболевания крови в анамнезе, период беременности и кормления грудью, детский возраст.
Побочные эффекты
Со стороны пищеварительного тракта: тошнота, диарея, повышение уровня печеночных трансаминаз (алат, асат), щф, рвота, диспептические явления, аномальные значения тестов на функцию печени, анорексия, метеоризм, гипербилирубинемия, оральный кандидоз, желтуха, холестатическая желтуха, псевдомембранозный колит, некроз печени, панкреатит, гепатит, металлический привкус, боль в животе, обложенный язык, глоссит, стоматит.
Со стороны нервной системы: головокружение, расстройства сна, ажитация, спутанность сознания, мигрень, галлюцинации, повышенное потоотделение, парестезии, эмоциональные нарушения (беспокойство, страх, тревога), нарушения сна, судороги, гиперестезия, депрессия, тремор, неустойчивая походка, психоз, повышение внутричерепного давления, атаксия, подергивание, головная боль, периферическая нейропатия, сенсорные нарушения.
Со стороны сердечно-сосудистой системы: тахикардия, мигрень, синкопе (обморок), вазодилатация, артериальная гипотензия, васкулит.
Со стороны системы кроветворения: эозинофилия, лейкопения, анемия, лейкоцитоз, измененные значения уровня протромбина, тромбоцитопения, тромбоцитоз, гемолитическая анемия, петехии, агранулоцитоз, панцитопения, угнетение функции костного мозга.
Со стороны опорно-двигательного аппарата: артралгия, миалгия, отек суставов, миастения, тендинит (преимущественно ахиллова сухожилия), повреждения сухожилий.
Со стороны мочеполовой системы: повышение уровня креатинина, азота мочевины в крови, ОПН, нарушение функции почек, вагинальный кандидоз, гематурия, кристаллурия, интерстициальный нефрит, потемнение мочи.
Со стороны дыхательной системы: диспноэ, отек гортани.
Реакции гиперчувствительности и изменения со стороны кожи: кожная сыпь, зуд, макулопапулезная сыпь, крапивница, аллергические реакции, медикаментозная лихорадка, анафилактические реакции (в том числе анафилактический шок), реакция, подобная сывороточной болезни, петехии, мультиформная эритема, узелковая эритема, синдром Стивенса — Джонсона, токсический эпидермальный некролиз, фоточувствительность, ангионевротический отек.
Нарушение метаболизма: отеки, гипергликемия, повышенная активность амилазы, повышенная активность липазы.
Со стороны органов чувств: нарушение вкуса, шум в ушах, временная глухота, нарушение зрения, диплопия, хроматопсия, паросмия, нарушение ощущения запахов.
Со стороны организма в целом: боль в животе, кандидоз, астения, боль в конечностях, боль в спине, боль в груди, приливы.
Особые указания
Во время лечения препаратом не следует употреблять алкогольные напитки. больным эпилепсией, с приступами судорог в анамнезе, с сосудистыми заболеваниями и органическими поражениями головного мозга в связи с опасностью развития побочных реакций со стороны цнс, препарат ципролет а следует назначать только по жизненным показаниям. при появлении во время лечения побочных реакций со стороны цнс применение препарата следует прекратить. при возникновении во время или после лечения препаратом ципролет а тяжелой и длительной диареи следует исключить диагноз псевдомембранозного колита, который требует немедленной отмены препарата и назначения соответствующей терапии.
Способность влиять на скорость реакции при управлении транспортными средствами или работе с другими механизмами. Во время лечения следует воздерживаться от управления транспортными средствами и/или другими механизмами, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Во время лечения следует воздерживаться от управления транспортными средствами и/или другими механизмами, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Применение в период беременности и кормления грудью. Препарат противопоказан в период беременности и кормления грудью.
Дети. Эффективность и безопасность применения препарата в педиатрической практике не установлены, поэтому у детей его не применяют.
Взаимодействия
Одновременное применение препарата ципролет а с препаратами железа, сукральфатом и антацидными средствами, содержащими магний, алюминий, кальций, и препаратами с большой буферной емкостью (например антиретровирусные средства) снижает интенсивность всасывания ципрофлоксацина. в связи с этим ципролет а следует назначать за 1–2 ч до или через 4 ч после приема указанных препаратов. указанное ограничение не касается класса блокаторов h3-гистаминовых рецепторов. одновременное применение теофиллина и ципрофлоксацина приводит к повышению концентрации теофиллина в плазме крови и удлинению его т½. при одновременном применении препарата с циклоспорином в отдельных случаях отмечают увеличение содержания креатинина в плазме крови. ципролет а повышает концентрацию и удлиняет т½ непрямых антикоагулянтов и пероральных гипогликемических средств. ципрофлоксацин влияет на метаболизм кофеина, увеличивая его т½. при одновременном применении ципрофлоксацина и фенитоина сообщалось об изменениях уровня фенитоина в плазме крови (повышение или понижение). сочетанное применение препарата ципролет а и пробенецида сопровождается повышением концентрации ципрофлоксацина в плазме крови. метоклопрамид ускоряет абсорбцию препарата ципролет а, вследствие чего сокращается период достижения cmax ципрофлоксацина в плазме крови (на биодоступность последнего это не влияет).
при одновременном применении препарата с циклоспорином в отдельных случаях отмечают увеличение содержания креатинина в плазме крови. ципролет а повышает концентрацию и удлиняет т½ непрямых антикоагулянтов и пероральных гипогликемических средств. ципрофлоксацин влияет на метаболизм кофеина, увеличивая его т½. при одновременном применении ципрофлоксацина и фенитоина сообщалось об изменениях уровня фенитоина в плазме крови (повышение или понижение). сочетанное применение препарата ципролет а и пробенецида сопровождается повышением концентрации ципрофлоксацина в плазме крови. метоклопрамид ускоряет абсорбцию препарата ципролет а, вследствие чего сокращается период достижения cmax ципрофлоксацина в плазме крови (на биодоступность последнего это не влияет).
Передозировка
В случае острой передозировки были сообщения о нефротоксичности. специфический антидот неизвестен. в случае передозировки следует промыть желудок. пациента следует тщательно наблюдать и проводить поддерживающую терапию, включая мониторинг функции почек и введение антацидов, содержащих магний, алюминий или кальций, которые могут уменьшить всасывание ципрофлоксацина. следует поддерживать адекватный водный режим. тинидазол легко выводится при диализе. ципрофлоксацин с помощью гемодиализа или перитонеального диализа выводится в небольшом количестве (10%).
следует поддерживать адекватный водный режим. тинидазол легко выводится при диализе. ципрофлоксацин с помощью гемодиализа или перитонеального диализа выводится в небольшом количестве (10%).
Условия хранения
В сухом, защищенном от света месте, при температуре не выше 25 °с.
Влияние антимикробных каркасов, содержащих ципрофлоксацин, на жизнеспособность стволовых клеток пульпы зуба — исследования in vitro
- Список журналов
- Рукописи авторов HHS
- PMC5338688
Arch Oral Biol. Авторская рукопись; доступно в PMC 2017 6 марта.
Опубликовано в окончательной редакции как:
Arch Oral Biol. 2015 авг; 60 (8): 1131–1137.
Published online 2015 May 16. doi: 10.1016/j.archoralbio.2015.05.002
doi: 10.1016/j.archoralbio.2015.05.002
PMCID: PMC5338688
NIHMSID: NIHMS850052
PMID: 26042622
, a , b and a, *
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности
Цель
Комбинация антибиотиков, включая, помимо прочего, метронидазол (МЕТ) и ципрофлоксацин (ЦИП), была показана для уничтожения бактерий в некротизированных несформированных постоянных зубах перед регенеративным лечением. процедуры. Клинически было показано, что пасты с антибиотиками могут привести к существенной гибели стволовых клеток. Цель этого исследования состояла в том, чтобы синтезировать каркасы, содержащие различные концентрации CIP, для повышения жизнеспособности клеток при сохранении антимикробных свойств.
Дизайн
Электроформованные каркасы на основе полидиоксанона (ПДС) обрабатывали с уменьшающимися концентрациями CIP (25 – 1 мас.%) и морфологически оценивали с помощью сканирующей электронной микроскопии (СЭМ). Были проведены анализы цитотоксичности, чтобы определить, приведет ли количество CIP, высвобождаемое из каркасов, к токсичности стволовых клеток пульпы зуба человека (hDPSC). Точно так же были проведены анализы WST-1 для оценки влияния высвобождения CIP на пролиферацию hDPSC. Чистые каркасы PDS и насыщенный двойной раствор антибиотика MET/CIP (DAP) служили как положительным, так и отрицательным контролем соответственно. Антибактериальная эффективность против E. faecalis ( Ef ) был протестирован.
Были проведены анализы цитотоксичности, чтобы определить, приведет ли количество CIP, высвобождаемое из каркасов, к токсичности стволовых клеток пульпы зуба человека (hDPSC). Точно так же были проведены анализы WST-1 для оценки влияния высвобождения CIP на пролиферацию hDPSC. Чистые каркасы PDS и насыщенный двойной раствор антибиотика MET/CIP (DAP) служили как положительным, так и отрицательным контролем соответственно. Антибактериальная эффективность против E. faecalis ( Ef ) был протестирован.
Результаты
Наблюдалось значительное снижение жизнеспособности hDPSC при концентрациях 5–25 мас.%. Однако концентрации ниже 5 мас.% не ухудшали жизнеспособность клеток. Данные анализов WST-1 показали отсутствие вредного воздействия на пролиферацию клеток каркасов, содержащих 2,5 мас.% CIP или менее. Значительные противомикробные свойства наблюдались у CIP-каркасов при более низких концентрациях (, т.е. , 1 и 2,5 мас.%).
Заключение
Полученные данные показали, что пониженная концентрация CIP, включенного в каркасы на основе PDS, сохраняет его антимикробные свойства, одновременно повышая жизнеспособность и пролиферацию стволовых клеток пульпы зуба.
Ключевые слова: антибиотики, матриксы, цитосовместимость, стволовые клетки, эндодонтия, регенерация
Пульпа играет жизненно важную роль в развитии зубов, так как содержит одонтобласты, высокоспециализированные клетки, синтезирующие дентин. 1 Травматические повреждения или бактериальная инфекция пульпы зуба приводят к воспалению и, если его не остановить, к некрозу. 2 У детей некроз пульпы способствует гибели одонтобластов, что приводит к нарушению развития корня. 3
Традиционно при травматических повреждениях зубов с незавершенным апикальным развитием проводилась апексификация путем внутриканального введения гидроксида кальция или, совсем недавно, агрегата минерального триоксида. 3,4 Тем не менее, в то время как апексификационная терапия способствует только апикальному закрытию, она не способствует развитию корня. 4 Между тем, клинические данные ( например, , развитие корней с утолщением стенок дентина) накапливаются после лечения некротизированных несформированных зубов методом реваскуляризации. 5–8
5–8
По существу, в пропагандируемой в настоящее время процедуре регенеративной эндодонтии комбинация антибиотиков, включая, помимо прочего, метронидазол (МЕТ) и ципрофлоксацин (ЦИП), была показана для достижения максимальной эрадикации бактерий. 3,5,9–11 Уничтожение микробов должно быть достигнуто с минимальной инструментальной обработкой корневого канала для сохранения недифференцированных клеток. 3,11 После деконтаминации корневых каналов подход, основанный на тканевой инженерии, происходит путем провоцирования преднамеренного кровотечения в периапикальной области, где формируется матрица на основе фибрина, которая в конечном итоге служит каркасом для поддержки прикрепления, пролиферация и дифференцировка стволовых клеток из апикальных сосочков благодаря вкладу эндогенно-продуцируемых факторов роста. 2,4 Самое главное, по данным литературы, демонстрация образования пульпоподобной ткани после реваскуляризации наблюдалась только в недавнем исследовании. 12 Между тем, в подавляющем большинстве исследований, включая данные как на животных моделях, так и в клинических случаях, в целом сообщается, что новообразованная инвагинированная ткань состоит из периапикальной ткани, содержащей костеподобную твердую ткань, а утолщение стенок корневого канала связано с образование цементоподобной ткани. 13,14
12 Между тем, в подавляющем большинстве исследований, включая данные как на животных моделях, так и в клинических случаях, в целом сообщается, что новообразованная инвагинированная ткань состоит из периапикальной ткани, содержащей костеподобную твердую ткань, а утолщение стенок корневого канала связано с образование цементоподобной ткани. 13,14
Несмотря на обнадеживающие данные, внутреннюю изменчивость клеточных популяций у разных пациентов, а также количество и разнообразие факторов роста, 3 в сочетании с крайней токсичностью стволовых клеток, связанной с использованием ирригантов и антибиотиков, 15,16 предложили возможность использования фиброзных каркасов, содержащих антибиотики, способных функционировать в качестве системы доставки лекарств для устранения инфекции корневых каналов при сохранении жизнеспособности стволовых клеток. 17,18 Исходя из вышеупомянутых соображений, целью этого исследования было синтезирование с помощью электропрядения каркасов на основе волокон, содержащих различные концентрации CIP, для повышения жизнеспособности стволовых клеток пульпы зуба при сохранении противомикробных свойств.
2.1. Синтез ципрофлоксацинсодержащих волокнистых каркасов
Ципрофлоксацинсодержащие (CIP, Sigma-Aldrich, Сент-Луис, Миссури, США) полимерные растворы на основе полидиоксанона (PDSII ® , Ethicon Inc, Somerville, NJ, USA) готовили для синтезировать каркасы с выбранными концентрациями CIP, следуя стандартным процедурам, как недавно сообщалось. 17–20 Сначала шовные нити PDS фиолетового цвета разрезали на кусочки одинаковой длины (, т.е. , 3 см) и обесцвечивали путем погружения в дихлорметан (Sigma-Aldrich) на 48 часов. Во-вторых, очищенный от красителя PDS растворяли в 1,1,1,3,3,3-гексафтор-2-пропаноле (HFP, Sigma-Aldrich) в концентрации 10 мас.% в течение ночи при интенсивном перемешивании. В последнюю очередь в приготовленные растворы ПДС добавляли порошок CIP в возрастающих концентрациях (1, 2,5, 5, 10, 15, 20 и 25 мас. %, по отношению к массе полимера – 9 %).0013, т.е. , 6, 15, 30, 60, 90, 120 и 150 мг соответственно), а затем перемешивали в течение ночи. Отдельные CIP-содержащие растворы PDS и чистый PDS (контроль) формовали в волокна (далее называемые каркасами) при комнатной температуре (КТ) на покрытой алюминиевой фольгой вращающейся (120 об/мин) оправке из нержавеющей стали, загружая растворы в пластиковые шприцы. (Becton-Dickinson & Company, Франклин Лейкс, Нью-Джерси, США) с металлической иглой с тупым концом 27G с использованием предварительно оптимизированных параметров (9).0013, т. е. , скорость потока 2 мл/ч, расстояние между наконечником и коллектором 18 см и 15–18 кВ). Перед испытанием каркасы сушили в вакууме при комнатной температуре не менее 48 ч. 17–20 Сканирующая электронная микроскопия (SEM, JSM-5310LV, JEOL, Tokyo, Japan) использовалась для оценки морфологии волокон синтезированных каркасов. Диаметр волокна оценивали с использованием программного обеспечения Image-J (NIH, Bethesda, MD, USA). 17–20
Отдельные CIP-содержащие растворы PDS и чистый PDS (контроль) формовали в волокна (далее называемые каркасами) при комнатной температуре (КТ) на покрытой алюминиевой фольгой вращающейся (120 об/мин) оправке из нержавеющей стали, загружая растворы в пластиковые шприцы. (Becton-Dickinson & Company, Франклин Лейкс, Нью-Джерси, США) с металлической иглой с тупым концом 27G с использованием предварительно оптимизированных параметров (9).0013, т. е. , скорость потока 2 мл/ч, расстояние между наконечником и коллектором 18 см и 15–18 кВ). Перед испытанием каркасы сушили в вакууме при комнатной температуре не менее 48 ч. 17–20 Сканирующая электронная микроскопия (SEM, JSM-5310LV, JEOL, Tokyo, Japan) использовалась для оценки морфологии волокон синтезированных каркасов. Диаметр волокна оценивали с использованием программного обеспечения Image-J (NIH, Bethesda, MD, USA). 17–20
2.2. Культура клеток для анализа жизнеспособности и пролиферации
Модифицированная среда Игла Дульбекко с низким содержанием глюкозы (DMEM, Gibco, Гранд-Айленд, Нью-Йорк, США) с добавлением 10 % FBS (Hyclone Laboratories Inc, Logan, UT) и 1 % пенициллин-стрептомицина (Sigma -Aldrich) помещают во влажный инкубатор при 37°C, с 5% CO 2 , использовали для культивирования стволовых клеток пульпы зуба человека (hDPSC, AllCells LLC, Аламеда, Калифорния, США), полученных из постоянных третьих моляров. 17,18 Среду меняли каждые 2–3 дня, использовали клетки пассажей 4–6.
17,18 Среду меняли каждые 2–3 дня, использовали клетки пассажей 4–6.
2.3. Анализы цитотоксичности
Для оценки потенциально токсического воздействия каркасов, содержащих CIP, на стволовые клетки пульпы зуба человека, проводятся анализы цитотоксичности в соответствии с рекомендациями Международной организации по стандартизации (ISO, 1993) 21 . Все каркасы (15×15 мм 2 ) сначала стерилизовали УФ-излучением (30 мин с каждой стороны), а затем погружали на 30 мин в 70% этанол. 17,18 После промывания стерильным PBS (5 мин, 2×) были приготовлены экстракты из отдельных каркасов. Анализ оценивает токсическое действие любого вымываемого соединения (соединений) (, например, , высвобожденный ципрофлоксацин) при контакте с клетками. Стерильные матриксы (соотношение поверхностей = 1 см 2 /мл среды) инкубировали в среде DMEM при 37°C в течение 2 дней в атмосфере 5% CO 9 .0123 2 влажная атмосфера. 17,18 В качестве отрицательного контроля готовили экстракты стерильного полиэтилена сверхвысокой молекулярной массы (СВМПЭ). Супернатанты фильтровали через мембрану Millipore ® и из экстрактов получали серийные разведения. Разведения готовили также для 0,3 об.% раствора фенола, который служил в качестве положительного контроля. 17,18 Тесты на цитотоксичность для каждого разведения проводили в четырехкратной повторности. Вкратце, hDPSC при плотности 3×10 3 /лунку высевали и оставляли прикрепляться в лунках 96-луночных планшетов для тканевых культур. Через 4 ч среду заменяли экстрактами различной концентрации. 17,18 По 100 мкл каждого экстракта пипетировали в каждую лунку. Контрольные колонки из четырех лунок готовили со средой без клеток (холостые) и со средой с клетками, но без экстракта (100% выживаемость). Планшеты инкубировали во влажной атмосфере с 5% CO 2 . Затем через 3 дня добавляли 20 мкл реагента CellTiter 96 AQueous One Solution Reagent (Promega Corporation, Мэдисон, Висконсин, США). 17,18 Реагент реагировал в течение 2 часов в тех же условиях.
Супернатанты фильтровали через мембрану Millipore ® и из экстрактов получали серийные разведения. Разведения готовили также для 0,3 об.% раствора фенола, который служил в качестве положительного контроля. 17,18 Тесты на цитотоксичность для каждого разведения проводили в четырехкратной повторности. Вкратце, hDPSC при плотности 3×10 3 /лунку высевали и оставляли прикрепляться в лунках 96-луночных планшетов для тканевых культур. Через 4 ч среду заменяли экстрактами различной концентрации. 17,18 По 100 мкл каждого экстракта пипетировали в каждую лунку. Контрольные колонки из четырех лунок готовили со средой без клеток (холостые) и со средой с клетками, но без экстракта (100% выживаемость). Планшеты инкубировали во влажной атмосфере с 5% CO 2 . Затем через 3 дня добавляли 20 мкл реагента CellTiter 96 AQueous One Solution Reagent (Promega Corporation, Мэдисон, Висконсин, США). 17,18 Реагент реагировал в течение 2 часов в тех же условиях. Включенный краситель измеряли, считывая оптическую плотность при 490 нм в ридере для микропланшетов относительно пустой колонки. 17,18
Включенный краситель измеряли, считывая оптическую плотность при 490 нм в ридере для микропланшетов относительно пустой колонки. 17,18
2.4. Анализы пролиферации (WST-1)
hDPSC собирали путем трипсинизации, подсчитывали и высевали на 13-мм обработанные покровные стекла для клеточных культур (Thermanox, Thermo Fisher Scientific Inc, Рочестер, штат Нью-Йорк, США) в 24-луночные планшеты при плотности 10 4 /лунка (1500 мкл питательной среды). Между тем, леса (15×15 мм 2 , n=4–6/группа) помещали в пластиковый контейнер CellCrown TM (Scaffdex, Тампере, Финляндия), дезинфицировали 70% этанолом в течение 30 минут и дважды промывали стерильным PBS (Sigma). После 4-часового периода инкубации, чтобы обеспечить прикрепление клеток, в лунки вносили CellCrowns с каркасами. Расстояние между ячейками и каркасом в 2 мм было достигнуто с помощью пластиковых колец в целях стандартизации. Контрольные (пустые) колонки были приготовлены в среде без клеток и в среде с клетками, но без каркаса (выживаемость 100%). Насыщенный раствор (50 мг/мл) CIP в DMEM готовили путем перемешивания в течение 4 ч при комнатной температуре с последующим центрифугированием (3000 об/мин) в течение 15 мин. Прозрачный супернатант стерилизовали фильтрованием с использованием шприцевого фильтра 0,22 мкм. 9Анализ 0011
Насыщенный раствор (50 мг/мл) CIP в DMEM готовили путем перемешивания в течение 4 ч при комнатной температуре с последующим центрифугированием (3000 об/мин) в течение 15 мин. Прозрачный супернатант стерилизовали фильтрованием с использованием шприцевого фильтра 0,22 мкм. 9Анализ 0011
WST-1 (Roche Diagnostics, Мангейм, Германия) использовали для оценки влияния каркасов, содержащих CIP, на пролиферацию hDPSC до 7 дней воздействия клеток/каркаса. 20 Через 3, 5 и 7 дней коронки CellCrown с каркасами удаляли. В каждой лунке оставляли 500 мкл DMEM. Затем в каждую лунку добавляли реагент WST-1 в соотношении 10:1 (, т.е. , 50 мкл). После 2-часовой инкубации в 5%CO 2 во влажной атмосфере при 37°C 100 мкл от общего объема каждой лунки переносили в 9 лунок.6-луночные планшеты. 20 Полная среда с клетками без воздействия каркаса и полная среда без клеток были назначены в качестве положительного и отрицательного контроля соответственно. Оптическую плотность (ОП) включенного красителя определяли, измеряя оптическую плотность при 450 нм в устройстве для считывания микропланшетов относительно пустой колонки. 20 Пролиферацию рассчитывали как отношение ОП от экспериментального значения к положительному контролю; оба были вычтены из отрицательного контроля. 20
20 Пролиферацию рассчитывали как отношение ОП от экспериментального значения к положительному контролю; оба были вычтены из отрицательного контроля. 20
2.5. Антимикробное тестирование
Анализы диффузии в агаре использовались для определения антимикробной эффективности каркасов, содержащих CIP, против Enterococcus faecalis ( Ef) (ATCC 29212). 17,18 Согласно нашим недавним результатам, приготовленные аналогичным образом CIP-содержащие каркасы в концентрациях 5 и 25 мас.% продемонстрировали значительную антимикробную активность в отношении Ef . 17 Таким образом, здесь мы предложили исследовать, могут ли каркасы, содержащие более низкие концентрации CIP ( напр. , 1 и 2,5% масс., по-прежнему будут сохранять противомикробные свойства. Ef культивировали в аэробных условиях в течение 24 ч в 5% CO 2 при 37°C в бульоне для инфузии мозга и сердца (BHI). 17,18 Затем стерилизованные УФ-излучением дискообразные (диаметром 6 мм) образцы (n=4) из 3 экспериментальных групп (, т. е. , 1, 2,5 и 5 мас.% CIP) помещали на чашки с кровяным агаром. содержащие Ef бактериальных газонов. 17,18 Хлоргексидин (0,12%) и 0,9% стерильный физиологический раствор использовали в качестве положительного и отрицательного контроля соответственно. Через 3 дня инкубации регистрировали зоны ингибирования (в мм). 17,18
е. , 1, 2,5 и 5 мас.% CIP) помещали на чашки с кровяным агаром. содержащие Ef бактериальных газонов. 17,18 Хлоргексидин (0,12%) и 0,9% стерильный физиологический раствор использовали в качестве положительного и отрицательного контроля соответственно. Через 3 дня инкубации регистрировали зоны ингибирования (в мм). 17,18
2.6. Статистический анализ
Односторонний дисперсионный анализ (ANOVA) с последующим множественным сравнением Тьюки использовался для оценки различий в диаметре волокон. При этом данные о жизнеспособности клеток (цитотоксичности) и пролиферации анализировали с использованием двустороннего дисперсионного анализа. Сравнение зон ингибирования проводили с использованием смешанной модели ANOVA. Уровень значимости был установлен на уровне p<0,05.
Репрезентативные СЭМ-микрофотографии синтезированных микро/нановолокнистых каркасов показаны на . Средний диаметр волокна колебался от 1139±348 нм (ПДС, контроль) до 748±231 нм (25 мас. % CIP). Как правило, концентрации CIP выше 5 мас.% приводили к образованию волокон значительно (p<0,001) меньшего диаметра, чем PDS.
% CIP). Как правило, концентрации CIP выше 5 мас.% приводили к образованию волокон значительно (p<0,001) меньшего диаметра, чем PDS.
Открыть в отдельном окне
Репрезентативные СЭМ-микрофотографии каркасов (5000×): (A) чистый PDS, (B) 1 масс.% CIP, (C) 2,5 масс.% CIP, (D) 5 масс. %CIP, (E) 10% масс. CIP, (F) 15% масс. CIP, (G) 20% масс. CIP и (H) 25% масс. CIP.
Основываясь на предполагаемом клиническом использовании современных каркасов, содержащих антибиотики, в качестве стратегии дезинфекции перед процедурами регенеративной эндодонтии, было оценено цитотоксическое действие всех каркасов, чтобы определить, действительно ли количество выпущенного CIP приведет к клеточной токсичности. Анализы цитотоксичности выявили значительное снижение жизнеспособности клеток при концентрациях 5-25 мас.% (). Затем мы обрабатывали скаффолды, содержащие CIP, при более низких концентрациях (  Анализ был проведен снова с использованием аналогичных контролей, но с CIP-содержащими каркасами с концентрациями от 1 до 5 мас.%. показывает данные о жизнеспособности клеток, где видно, что концентрации ниже 5 мас.% не ухудшают жизнеспособность hDPSC. Точно так же мы оценили косвенные эффекты высвобождения CIP из каркасов на способность к пролиферации hDPSC путем инкубации клеток в присутствии каркасов до 7 дней. Данные показали, что каркасы, содержащие от 5 до 25 мас. % CIP ингибировал пролиферацию клеток за все время (). Ингибирующее действие на пролиферацию hDPSC не наблюдалось после воздействия каркасов, содержащих 1 и 2,5 мас.% CIP (). Данные о цитосовместимости, представленные в этом исследовании, согласуются с нашей предыдущей работой. Однако, поскольку снижение концентрации CIP до 1 и 2,5 мас.% не выявило значительного влияния на жизнеспособность/пролиферацию клеток, мы предложили изучить, действительно ли эти каркасы обладают противомикробными свойствами. Данные по диффузии в агар продемонстрировали значительное ингибирование роста E.
Анализ был проведен снова с использованием аналогичных контролей, но с CIP-содержащими каркасами с концентрациями от 1 до 5 мас.%. показывает данные о жизнеспособности клеток, где видно, что концентрации ниже 5 мас.% не ухудшают жизнеспособность hDPSC. Точно так же мы оценили косвенные эффекты высвобождения CIP из каркасов на способность к пролиферации hDPSC путем инкубации клеток в присутствии каркасов до 7 дней. Данные показали, что каркасы, содержащие от 5 до 25 мас. % CIP ингибировал пролиферацию клеток за все время (). Ингибирующее действие на пролиферацию hDPSC не наблюдалось после воздействия каркасов, содержащих 1 и 2,5 мас.% CIP (). Данные о цитосовместимости, представленные в этом исследовании, согласуются с нашей предыдущей работой. Однако, поскольку снижение концентрации CIP до 1 и 2,5 мас.% не выявило значительного влияния на жизнеспособность/пролиферацию клеток, мы предложили изучить, действительно ли эти каркасы обладают противомикробными свойствами. Данные по диффузии в агар продемонстрировали значительное ингибирование роста E. faecalis связаны с использованием CIP-содержащих каркасов при концентрациях ниже 5 мас.% ().
faecalis связаны с использованием CIP-содержащих каркасов при концентрациях ниже 5 мас.% ().
Открыть в отдельном окне
Цитотоксические эффекты экстрактов, приготовленных из каркасов с выбранными концентрациями CIP. hDPSC подвергались воздействию увеличивающейся концентрации экстрактов, а именно 6,25%, 12,5%, 25%, 50% и 100%. Жизнеспособность клеток (%) определяли через 72 часа. * Достоверные отличия от контроля установлены при p < 0,05.
Открыть в отдельном окне
Пролиферация (%) hDPSCs после воздействия CIP-содержащих каркасов (5 – 25 мас.%). Пролиферацию определяли на 3, 5 и 7 дни. Данные анализировали с использованием однофакторного дисперсионного анализа и тестов множественного сравнения Тьюки. * Достоверные различия между опытными группами и контролем в один и тот же момент времени установлены на уровне p < 0,05.
Открыть в отдельном окне
Пролиферация (%) hDPSC после воздействия CIP-содержащих каркасов (1 – 5 мас.%). Пролиферацию определяли на 3, 5 и 7 дни. Достоверные отличия от контроля (PDS) и других групп были установлены на уровне p < 0,05 и представлены строчными буквами.
Достоверные отличия от контроля (PDS) и других групп были установлены на уровне p < 0,05 и представлены строчными буквами.
Открыть в отдельном окне
Влияние каркасов, содержащих CIP, на ингибирование роста Ef . (A-B) Репрезентативные макрофотографии анализов диффузии в агаре на Ef с 1 мас.%, 2,5 мас.% и 5 мас.% CIP-содержащих каркасов. В качестве отрицательного и положительного контроля использовали стерильный физиологический раствор (Sal) и 0,12% раствор хлоргексидина (CHX). (C) Данные анализа диффузии в агар на 3-й день (n = 4). Значимые различия между группами отмечены звездочкой (p < 0,05).
Искоренение инфекции из некротизированных зубов является жизненно важным шагом перед процедурами регенеративной эндодонтии. 3,5,9–11 В настоящее время хорошо известно, что смеси антибиотиков, такие как так называемые двойные (МЕТ и CIP) и тройные (МЕТ, CIP и миноциклин) пасты антибиотиков, превосходно обеспечивают защиту от бактерий. свободная ниша 9–11 ; однако они снижают жизнеспособность стволовых клеток пульпы зуба, участвующих в регенерации тканей. 15,16 В последнее время наша группа предложила стратегию доставки лекарств, основанную на использовании содержащих антибиотик электропрядных каркасов, обладающих значительным клиническим потенциалом в эндодонтии для этапа дезинфекции, включенного в текущую клинически пропагандируемую регенеративную стратегию. 17,18 В совокупности наши недавние данные доказали, что различные антибиотики ( т.е. , составы MET, CIP и MET/CIP bi-mix) могут быть успешно сплетены в волокнистые каркасы со значительной антимикробной эффективностью против чувствительных бактерии. 17–19 Тем не менее, несмотря на значительно более низкие концентрации антибиотиков, высвобождаемых из этих каркасов, по сравнению с фактическими концентрациями антибиотиков, используемыми в клинической практике, мы также сообщили о значительном негативном влиянии на выживаемость hDPSCs после воздействия CIP-содержащих каркасов, а не MET-содержащих подмости. 17
15,16 В последнее время наша группа предложила стратегию доставки лекарств, основанную на использовании содержащих антибиотик электропрядных каркасов, обладающих значительным клиническим потенциалом в эндодонтии для этапа дезинфекции, включенного в текущую клинически пропагандируемую регенеративную стратегию. 17,18 В совокупности наши недавние данные доказали, что различные антибиотики ( т.е. , составы MET, CIP и MET/CIP bi-mix) могут быть успешно сплетены в волокнистые каркасы со значительной антимикробной эффективностью против чувствительных бактерии. 17–19 Тем не менее, несмотря на значительно более низкие концентрации антибиотиков, высвобождаемых из этих каркасов, по сравнению с фактическими концентрациями антибиотиков, используемыми в клинической практике, мы также сообщили о значительном негативном влиянии на выживаемость hDPSCs после воздействия CIP-содержащих каркасов, а не MET-содержащих подмости. 17
Хинолоны, включая CIP, представляют собой антибиотики широкого спектра действия, обычно используемые против широкого спектра как грамположительных, так и грамотрицательных бактерий. 22 Механизм действия 23 включает ингибирование бактериальной ДНК топоизомеразы II (гиразы) и топоизомеразы IV, которые являются ферментами, участвующими в раскручивании бактериальной ДНК в процессе репликации. К сожалению, было также показано, что CIP снижает жизнеспособность эукариотических клеток, что приводит к многочисленным побочным эффектам 24,25 , такие как тендинопатии 26 и периферическая невропатия 27,28 , из-за снижения синтеза белков, кодируемых митохондриальной дезоксирибонуклеиновой кислотой (мтДНК). Анализ мтДНК из клеток, обработанных CIP, выявил наличие сайт-специфических двухцепочечных разрывов ДНК 29 , которые были приписаны ингибированию активности митохондриальной топоизомеразы II, функционально и структурно сходные с таковыми у бактерий. 30 Таким образом, взятые вместе, клетки млекопитающих чувствительны к токсическим эффектам CIP, особенно клетки с высокой скоростью пролиферации, , т.
22 Механизм действия 23 включает ингибирование бактериальной ДНК топоизомеразы II (гиразы) и топоизомеразы IV, которые являются ферментами, участвующими в раскручивании бактериальной ДНК в процессе репликации. К сожалению, было также показано, что CIP снижает жизнеспособность эукариотических клеток, что приводит к многочисленным побочным эффектам 24,25 , такие как тендинопатии 26 и периферическая невропатия 27,28 , из-за снижения синтеза белков, кодируемых митохондриальной дезоксирибонуклеиновой кислотой (мтДНК). Анализ мтДНК из клеток, обработанных CIP, выявил наличие сайт-специфических двухцепочечных разрывов ДНК 29 , которые были приписаны ингибированию активности митохондриальной топоизомеразы II, функционально и структурно сходные с таковыми у бактерий. 30 Таким образом, взятые вместе, клетки млекопитающих чувствительны к токсическим эффектам CIP, особенно клетки с высокой скоростью пролиферации, , т. е. , гемопоэтические стволовые клетки человека 31,32 , эмбриональные стволовые клетки (чЭСК) 33 и родственные зубам клетки. 15,16 Следует отметить, что цитотоксические эффекты, связанные с CIP, также зависят от дозировки и времени воздействия. В недавнем исследовании in vitro эмбриональные стволовые клетки смогли восстановить исходную метаболическую активность после отмены CIP 33 ; таким образом, снижение концентрации препарата и/или времени воздействия может значительно улучшить жизнеспособность стволовых клеток. Основываясь на вышеизложенном, здесь мы исследовали, будет ли синтез с помощью электропрядения CIP-содержащих каркасов с пониженными концентрациями CIP повышать жизнеспособность стволовых клеток пульпы зуба, сохраняя при этом антимикробные свойства. В нашем предыдущем исследовании 17 , мы продемонстрировали, что CIP в концентрации 5 мас.% имел противомикробную эффективность, сравнимую с 25 мас.%. Данные, полученные здесь, показали, что каркасы, содержащие более низкие концентрации CIP (, например, , 1 и 2,5 мас.
е. , гемопоэтические стволовые клетки человека 31,32 , эмбриональные стволовые клетки (чЭСК) 33 и родственные зубам клетки. 15,16 Следует отметить, что цитотоксические эффекты, связанные с CIP, также зависят от дозировки и времени воздействия. В недавнем исследовании in vitro эмбриональные стволовые клетки смогли восстановить исходную метаболическую активность после отмены CIP 33 ; таким образом, снижение концентрации препарата и/или времени воздействия может значительно улучшить жизнеспособность стволовых клеток. Основываясь на вышеизложенном, здесь мы исследовали, будет ли синтез с помощью электропрядения CIP-содержащих каркасов с пониженными концентрациями CIP повышать жизнеспособность стволовых клеток пульпы зуба, сохраняя при этом антимикробные свойства. В нашем предыдущем исследовании 17 , мы продемонстрировали, что CIP в концентрации 5 мас.% имел противомикробную эффективность, сравнимую с 25 мас.%. Данные, полученные здесь, показали, что каркасы, содержащие более низкие концентрации CIP (, например, , 1 и 2,5 мас. %), не только сохраняли антимикробные свойства, но, что более важно, значительно снижали негативное влияние на жизнеспособность/пролиферацию hDPSC.
%), не только сохраняли антимикробные свойства, но, что более важно, значительно снижали негативное влияние на жизнеспособность/пролиферацию hDPSC.
В заключение, данные этого исследования показали, что уменьшение количества CIP, включенного в каркасы на основе PDS, повышает жизнеспособность и пролиферацию hDPSC при сохранении их антимикробных свойств.
Это исследование было частично поддержано стартовыми фондами Школы стоматологии IU (MCB). Авторы отрицают любые конфликты интересов, связанные с этим исследованием.
1. Чиего ДиДжей. В: Развитие полости рта и гистология. Эйвери Дж. К., редактор. Медицинские издательства Тиме; Нью-Йорк: 2003. С. 190–212. [Google Scholar]
2. Albuquerque MT, Valera MC, Nakashima M, Nör JE, Bottino MC. Стратегии регенеративной эндодонтии, основанные на тканевой инженерии. Джей Дент Рез. 2014;93:1222–31. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Харгривз К.М., Диоген А., Тейшейра Ф.Б. Возможности лечения: биологические основы регенеративных эндодонтических процедур. Дж Эндод. 2013;39(3 Приложение):S30–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Эндод. 2013;39(3 Приложение):S30–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Дамле С.Г., Бхаттал Х., Лумба А. Апексификация передних зубов: сравнительная оценка агрегата минерального триоксида и пасты гидроксида кальция. J Clin Pediatr Dent. 2012; 36: 263–8. [PubMed] [Google Scholar]
5. Banchs F, Trope M. Реваскуляризация несформированных постоянных зубов при апикальном периодонтите: новый протокол лечения? Дж Эндод. 2004;30:196–200. [PubMed] [Google Scholar]
6. Bose R, Nummikoski P, Hargreaves K. Ретроспективная оценка рентгенологических результатов несформированных зубов с некротизированными системами корневых каналов, пролеченных с помощью регенеративных эндодонтических процедур. Дж Эндод. 2009; 35:1343–9. [PubMed] [Google Scholar]
7. Петрино Дж. А., Бода К. К., Шамбаргер С., Боулз В. Р., Маккланахан С. Б. Проблемы регенеративной эндодонтии: серия случаев. Дж Эндод. 2010;36:536–4. [PubMed] [Google Scholar]
8. Gomes-Filho JE, Duarte PC, Ervolino E, Mogami Bomfim SR, Xavier Abimussi CJ, Mota da Silva Santos L, Lodi CS, Penha De Oliveira SH, Dezan E, Jr, Cintra LT. Гистологическая характеристика инженерных тканей в канальном пространстве закрытых верхушечных зубов с апикальным периодонтитом. Дж Эндод. 2013;39: 1549–56. [PubMed] [Google Scholar]
Гистологическая характеристика инженерных тканей в канальном пространстве закрытых верхушечных зубов с апикальным периодонтитом. Дж Эндод. 2013;39: 1549–56. [PubMed] [Google Scholar]
9. Hoshino E, Kurihara-Ando N, Sato I, Uematsu H, Sato M, Kota K, Iwaku M. Антибактериальная чувствительность in vitro бактерий, взятых из инфицированного корневого дентина, к смеси ципрофлоксацин метронидазол и миноциклин. Int Endod J. 1996; 29: 125–30. [PubMed] [Google Scholar]
10. Sato I, Ando-Kurihara N, Kota K, Iwaku M, Hoshino E. Стерилизация инфицированного дентина корневого канала путем местного применения смеси ципрофлоксацина, метронидазола и миноциклина in situ. Инт Эндод Дж. 1996;29:118–24. [PubMed] [Google Scholar]
11. Диоген А.Р., Рупарел Н.Б., Тейшейра Ф.Б., Харгривз К.М. Трансляционная наука в области дезинфекции для регенеративной эндодонтии. Дж Эндод. 2014;40(4 Приложение):S52–7. [PubMed] [Google Scholar]
12. Shimizu E, Jong G, Partridge N, Rosenberg PA, Lin LM.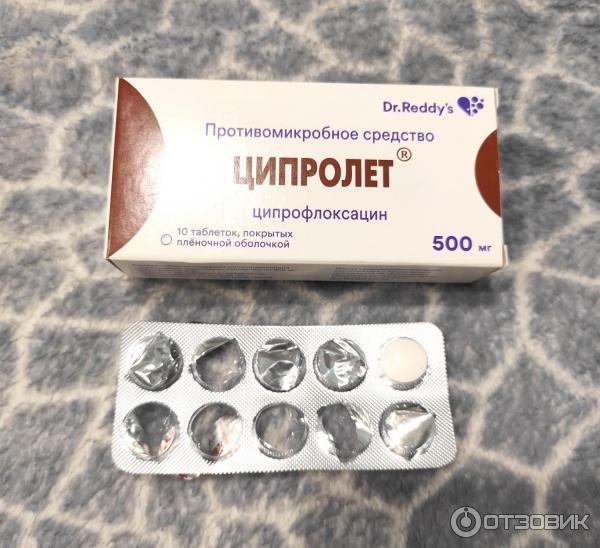 Гистологическое наблюдение несформированного постоянного зуба человека с необратимым пульпитом после процедуры реваскуляризации/регенерации. Дж Эндод. 2012; 38:1293–1297. [PubMed] [Академия Google]
Гистологическое наблюдение несформированного постоянного зуба человека с необратимым пульпитом после процедуры реваскуляризации/регенерации. Дж Эндод. 2012; 38:1293–1297. [PubMed] [Академия Google]
13. Мартин Г., Рикуччи Д., Гиббс Д.Л., Лин Л.М. Гистологические данные реваскуляризированного/ревитализированного незрелого постоянного моляра с апикальным периодонтитом с использованием богатой тромбоцитами плазмы. Дж Эндод. 2013; 39: 138–44. [PubMed] [Google Scholar]
14. Becerra P, Ricucci D, Loghin S, Gibbs JL, Lin LM. Гистологическое исследование незрелого постоянного премоляра человека с хроническим апикальным абсцессом после реваскуляризации/ревитализации. Дж Эндод. 2014;40:133–9. [PubMed] [Google Scholar]
15. Ruparel NB, Teixeira FB, Ferraz CC, Diogenes A. Прямое влияние внутриканальных препаратов на выживаемость стволовых клеток апикального сосочка. Дж Эндод. 2012;38:1372–5. [PubMed] [Академия Google]
16. Чуэнсомбат С., Хемалилакул С., Чаттипакорн С. , Срисуван Т. Цитотоксические эффекты и антибактериальная эффективность комбинации 3-антибиотиков: исследование in vitro. Дж Эндод. 2013;39:813–9. [PubMed] [Google Scholar]
, Срисуван Т. Цитотоксические эффекты и антибактериальная эффективность комбинации 3-антибиотиков: исследование in vitro. Дж Эндод. 2013;39:813–9. [PubMed] [Google Scholar]
17. Bottino MC, Kamocki K, Yassen GH, Platt JA, Vail MM, Ehrlich Spolnik KJ, Gregory RL. Биоактивные нановолоконные каркасы для регенеративной эндодонтии. Джей Дент Рез. 2013;92:963–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Palasuk J, Kamocki K, Hippenmeyer L, et al. Bi-mix противомикробные каркасы для регенеративной эндодонтии. Дж Эндод. 2014;40:1879–84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Bottino MC, Arthur RA, Waeiss RA, Kamocki K, Gregson KS, Gregory RL. Биоразлагаемые нановолокнистые системы доставки лекарств: влияние метронидазола и ципрофлоксацина на пародонтопатогены и комменсальные бактерии полости рта. Clin Oral Investig. 2014;18:2151–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Bottino MC, Yassen GH, Platt JA, Labban N, Windsor LJ, Spolnik KJ, Bressiani AHA. Новый трехмерный каркас для регенеративной эндодонтии: материалы и биологические характеристики. J Tissue Eng Regen Med. 2013 г.: 10.1002/term.1712. [Epub перед печатью] [PubMed] [CrossRef] [Google Scholar]
Новый трехмерный каркас для регенеративной эндодонтии: материалы и биологические характеристики. J Tissue Eng Regen Med. 2013 г.: 10.1002/term.1712. [Epub перед печатью] [PubMed] [CrossRef] [Google Scholar]
21. Международная организация по стандартизации. Часть 5: Тесты на цитотоксичность: методы in vitro. 1993. ИСО 10993-5. Биологическая оценка медицинских изделий. [Google Scholar]
22. Блондо Ж.М. Расширенная активность и полезность новых фторхинолонов: обзор. Клин Тер. 1999; 21:3–40. [PubMed] [Google Scholar]
23. Хупер, округ Колумбия. Механизмы действия и резистентность старых и новых фторхинолонов. Клин Инфекция Дис. 2000; 31 (Приложение 2): S24–8. [PubMed] [Академия Google]
24. Бриасулис А., Агарвал В., Пирс В.Дж. Удлинение интервала QT и torsade de pointes, вызванные фторхинолонами: нечастые побочные эффекты от часто используемых лекарств. Кардиология. 2011; 120:103–10. [PubMed] [Google Scholar]
25. Carbon C. Сравнение побочных эффектов левофлоксацина с другими фторхинолонами. Химиотерапия. 2001; 47 (Приложение 3): 9–14. [PubMed] [Google Scholar]
Химиотерапия. 2001; 47 (Приложение 3): 9–14. [PubMed] [Google Scholar]
26. Льюис Т., Кук Дж. Фторхинолоны и тендинопатии: руководство для спортсменов и спортивных врачей и систематический обзор литературы. Джей Атл Трейн. 2014;49: 422–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Али А.К. Риски периферической невропатии и синдрома Гийена-Барре, связанные с воздействием системных фторхинолонов: анализ фармаконадзора. Энн Эпидемиол. 2014; 24: 279–85. [PubMed] [Google Scholar]
28. Коэн Дж.С. Периферическая невропатия, связанная с фторхинолонами. Энн Фармакотер. 2001; 35:1540–7. [PubMed] [Google Scholar]
29. Лоуренс Дж. В., Клэр Д. С., Вайсиг В., Роу Т. С. Замедленная цитотоксичность и расщепление митохондриальной ДНК в клетках млекопитающих, обработанных ципрофлоксацином. Мол Фармакол. 1996;50:1178–88. [PubMed] [Google Scholar]
30. Gadelle D, Filee J, Buhler C, Forterre P. Филогеномика ДНК-топоизомераз типа II. Биоэссе. 2003; 25: 232–42. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
31. Somekh E, Douer D, Shaked N, Rubinstein E. Влияние ципрофлоксацина и пефлоксацина in vitro на рост нормальных гемопоэтических клеток-предшественников человека и клеток лейкемических клеточных линий. J Pharmacol Exp Ther. 1989; 248: 415–8. [PubMed] [Google Scholar]
32. Hahn T, Barak Y, Liebovich E, Malach L, Dagan O, Rubinstein E. Ципрофлоксацин ингибирует рост гемопоэтических клеток человека: синергизм с фактором некроза опухоли и интерфероном. эксп Гематол. 1991;19:157–60. [PubMed] [Google Scholar]
33. Роморини Л., Рива Д.А., Блюгерманн С., Видела Ричардсон Г.А., Скасса М.Е., Севлевер Г.Е., Мирюка С.Г. Действие антибиотиков на Mycoplasma sp. на статус недифференцированных эмбриональных стволовых клеток человека, жизнеспособность и рост клеток плюрипотентности. PloS Один. 2013;8:e70267. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Индийская ассоциация стоматологов
Индийская ассоциация стоматологов- +91(22) 43434545
- ho@ida.
 org.in
org.in
-Выберите категорию-MemberStateLocalAdmin
Забыли пароль?
Ингибируют бактериальную ДНК-гиразу или фермент топоизомеразу IV, тем самым ингибируя Репликация и транскрипция ДНК.
Торговое название: Цифран, Циплокс, Ципробид, Ципролет 250, 500, 750 мг таб, 200/100мл в/в. настой.
Ципрофлоксацин используется для лечения подтвержденных серьезных и опасных для жизни бактериальных инфекций. инфекции, такие как:
- Инфекции мочевыводящих путей.
- Острый неосложненный цистит у женщин.
- Хронический бактериальный простатит.
- Инфекции нижних дыхательных путей.
- Острый синусит.
- Инфекции кожи и структур кожи.
- Инфекции костей и суставов.
- Инфекционная диарея.
- Брюшной тиф (брюшной тиф), вызываемый Salmonella typhi.
- Желудочно-кишечный тракт – Тошнота, рвота, неприятный вкус, анорексия.
- ЦНС — головокружение, головная боль, беспокойство, тревога, тремор движений.
- Гиперчувствительность – сыпь, зуд, фотосенсибилизация, крапивница, отек губ. и т. д.
- Тендинит и разрыв сухожилия.
В основном используется при инфекциях мочевыводящих путей и половых путей и бактериальной диарее.
Торговое название: Norbactin, Norflox 200, 400, 600, вкладка 800 мг; Глазные капли 3 мг/мл.
- Он особенно используется при лечении хронического бронхита и других респираторных заболеваний. тракта и ЛОР-инфекции.
- Он также используется для лечения гонореи и негонококкового уретрита.
Торговое название: Lomecon, Lomaday 400 мг табл.
Торговое название: Заноцин, Тарвид 100, 200, 400 мг таб.; 200 мг/100 мл в/в инфузии.
- Внебольничная пневмония.
- Хронический бронхит.
- Инфекции нижних и верхних дыхательных путей.
Национальная награда Sushruta за здоровье полости рта
Познакомьтесь с дружелюбным стоматологом: доктор Сильные ЗубыФайлы cookie помогают нам предоставлять наши услуги. Используя наши услуги, вы соглашаетесь на использование нами файлов cookie.
Поболтай с нами
Имя
Электронная почта
Мобильный
Отправить
Амол
-
Lorem Ipsum — это просто текст-пустышка полиграфической и наборной индустрии.

