инструкция по применению, доставка на дом
Характеристики
| Минимальная допустимая температура хранения, °С | 25 °C |
| Максимальная допустимая температура хранения, °С | 10 °C |
| Срок годности | 5 мес |
| Фармакологическая группа | Местный анестетик |
| Количество в упаковке | 10 шт |
Описание
Раствор для инъекций прозрачный, бесцветный или почти бесцветный, без запаха.
Действующие вещества
Лидокаин
Форма выпуска
Ампулы
Состав
Лидокаина гидрохлорид (в форме лидокаина гидрохлорида моногидрата 43 мг) 20 мг.
Вспомогательные вещества: натрия хлорид для парентеральных форм — 12 мг, вода д/и — до 2 мл.
Фармакологический эффект
Лидокаин является короткодействующим местным анестетиком амидного типа. В основе его механизма действия лежит уменьшение проницаемости мембраны нейрона для ионов натрия. В результате этого снижается скорость деполяризации и повышается порог возбуждения, приводя к обратимому местному онемению. Лидокаин применяют в целях достижения проводниковой анестезии в различных участках тела и контроля аритмий. Обладает быстрым началом действия (около одной минуты после в/в введения и 15 мин после в/м), быстро распространяется в окружающие ткани. Действие продолжается 10-20 мин и около 60-90 мин после в/в и в/м введения соответственно.
Фармакокинетика
Всасывание
Лидокаин быстро абсорбируется из ЖКТ, однако вследствие эффекта «первого прохождения» через печень лишь небольшое его количество достигает системного кровотока. Системная абсорбция лидокаина определяется местом введения, дозой и его фармакологическим профилем. Cmax в крови достигается после межреберной блокады, далее (в порядке снижения концентрации), после введения в поясничное эпидуральное пространство, плечевое сплетение и подкожные ткани. Основным фактором, определяющим скорость абсорбции и концентрацию в крови, является общая введенная доза, независимо от участка введения. Имеется линейная зависимость между количеством введенного лидокаина и Cmax анестетика в крови.
Cmax в крови достигается после межреберной блокады, далее (в порядке снижения концентрации), после введения в поясничное эпидуральное пространство, плечевое сплетение и подкожные ткани. Основным фактором, определяющим скорость абсорбции и концентрацию в крови, является общая введенная доза, независимо от участка введения. Имеется линейная зависимость между количеством введенного лидокаина и Cmax анестетика в крови.
Распределение
Лидокаин связывается с белками плазмы, включая &alpha,1-кислый гликопротеин (АКГ) и альбумин. Степень связывания вариабельна, составляя приблизительно 66%. Плазменная концентрация АКГ у новорожденных низкая, поэтому у них отмечается относительно высокое содержание свободной биологически активной фракции лидокаина.
Лидокаин проникает через ГЭБ и плацентарный барьер, вероятно, посредством пассивной диффузии.
Метаболизм
Лидокаин метаболизируется в печени, около 90% введенной дозы подвергается N-дезалкилированию с образованием моноэтилглицинксилидида (MEGX) и глицинксилидида (GX), оба вносят вклад в терапевтические и токсические эффекты лидокаина.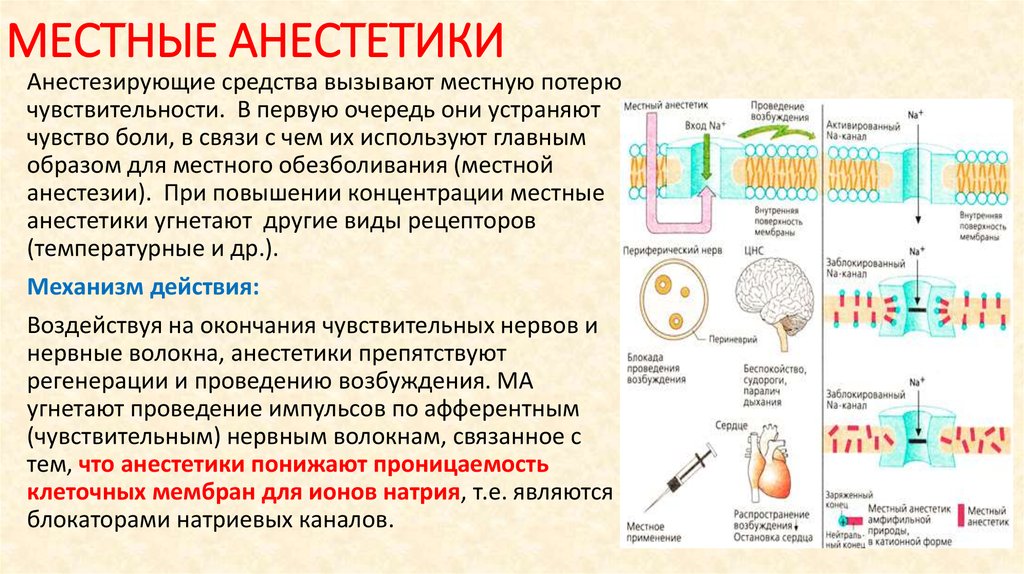 Фармакологические и токсические эффекты MEGX и GX сопоставимы с таковыми лидокаина, но выражены слабее. GX обладает более длинным, чем лидокаин, Т1/2 (около 10 ч) и может кумулировать при многократном введении.
Фармакологические и токсические эффекты MEGX и GX сопоставимы с таковыми лидокаина, но выражены слабее. GX обладает более длинным, чем лидокаин, Т1/2 (около 10 ч) и может кумулировать при многократном введении.
Метаболиты, образующиеся в результате последующего метаболизма, выводятся с мочой.
Выведение
Терминальный Т1/2 лидокаина после в/в болюсного введения здоровым взрослым добровольцам составляет 1-2 ч. Терминальный Т1/2 GX составляет около 10 ч, MEGX — 2 ч. Содержание неизмененного лидокаина в моче не превышает 10%
Фармакокинетика у особых групп пациентов
Вследствие быстрого метаболизма на фармакокинетику лидокаина могут оказывать влияние состояния, нарушающие функцию печени. У пациентов с нарушением функции печени Т1/2 лидокаина может повышаться в 2 и более раз.
Нарушение функции почек не влияет на фармакокинетику лидокаина, но может привести к кумуляции его метаболитов.
У новорожденных отмечается низкая концентрация АКГ, поэтому связывание с белками плазмы может снижаться. В связи с потенциально высокой концентрацией свободной фракции применение лидокаина у новорожденных не рекомендуется.
В связи с потенциально высокой концентрацией свободной фракции применение лидокаина у новорожденных не рекомендуется.
Показания
Местная и регионарная анестезия, проводниковая анестезия при больших и малых вмешательствах.
Противопоказания
AV-блокада III степени. Гиповолемия. Повышенная чувствительность к любому из компонентов препарата и к анестетикам амидного типа.
Применение при беременности и кормлении грудью
Лидокаин разрешается применять при беременности и в период грудного вскармливания. Необходимо строго придерживаться назначенного режима дозирования. При осложнениях или кровотечении в анамнезе проведение эпидуральной анестезии лидокаином в акушерстве противопоказано.
Лидокаин применяли у большого числа беременных женщин и женщин детородного возраста. Какие-либо репродуктивные нарушения не зарегистрированы, т.е. повышения частоты пороков развития не отмечалось.
Вследствие потенциального достижения высокой концентрации местных анестетиков у плода после парацервикальной блокады у него могут развиться нежелательные реакции, такие как фетальная брадикардия. В связи с этим лидокаин в концентрации, превышающей 1%, в акушерстве не применяют.
В связи с этим лидокаин в концентрации, превышающей 1%, в акушерстве не применяют.
В исследованиях на животных вредное воздействие на плод не обнаружено.
Лидокаин в небольшом количестве проникает в грудное молоко, биодоступность очень низкая, таким образом, ожидаемое количество, поступающее с грудным молоком, очень небольшое, следовательно, потенциальный вред для ребенка очень низкий. Решение о возможности применения лидокаина в период грудного вскармливания принимает врач.
Данные о влиянии лидокаина на фертильность у человека отсутствуют.
Способ применения и дозы
Режим дозирования следует подбирать в зависимости от реакции пациента и места введения. Препарат следует вводить в наименьшей концентрации и в наименьшей дозе, дающей требуемый эффект. Максимальная доза для взрослых не должна превышать 300 мг.
Объем раствора, подлежащий введению, зависит от размера анестезируемого участка. Если есть потребность во введении большего объема с низкой концентрацией, то стандартный раствор разводят физиологическим солевым раствором (0. 9% раствор натрия хлорида). Разведение осуществляют непосредственно перед введением.
9% раствор натрия хлорида). Разведение осуществляют непосредственно перед введением.
Побочные действия
Со стороны иммунной системы
Реакции гиперчувствительности (аллергические или анафилактоидные реакции, анафилактический шок) — см. также нарушения со стороны кожи и подкожных тканей. Кожная аллергическая проба на лидокаин считается ненадежной.
Со стороны нервной системы и психические расстройства
К неврологическим симптомам системной токсичности относятся головокружение, нервозность, тремор, парестезия вокруг рта, онемение языка, сонливость, судороги, кома.
Реакции со стороны нервной системы могут проявляться ее возбуждением или угнетением. Признаки стимуляции ЦНС могут быть непродолжительными или не возникать вовсе, вследствие чего первыми проявлениями токсичности могут служить спутанность сознания и сонливость, сменяющиеся комой и дыхательной недостаточностью.
К неврологическим осложнениям спинальной анестезии относятся преходящие неврологические симптомы, такие как боль в пояснице, ягодицах и ногах. Эти симптомы развиваются, как правило, в течение 24 ч после анестезии и разрешаются в течение нескольких дней.
Эти симптомы развиваются, как правило, в течение 24 ч после анестезии и разрешаются в течение нескольких дней.
После спинальной анестезии лидокаином и сходными средствами описаны отдельные случаи арахноидита и синдрома конского хвоста со стойкой парестезией, дисфункцией кишечника и мочевыводящих путей или параличом нижних конечностей. Большинство случаев обусловлено гипербарической концентрацией лидокаина или длительной спинальной инфузией.
Со стороны органа зрения
Признаками токсичности лидокаина могут быть затуманенное зрение, диплопия и преходящий амавроз. Двусторонний амавроз также может быть следствием случайного введения лидокаина в ложе зрительного нерва в ходе офтальмологических процедур. После ретро- или перибульбарной анестезии сообщалось о воспаление глаза и диплопии.
Со стороны органа слуха и лабиринта: звон в ушах, гиперакузия.
Со стороны сердечно-сосудистой системы
Сердечно-сосудистые реакции проявляются артериальной гипотензией, брадикардией, угнетением миокарда (отрицательный инотропный эффект), аритмиями, возможны остановка сердца или недостаточность кровообращения.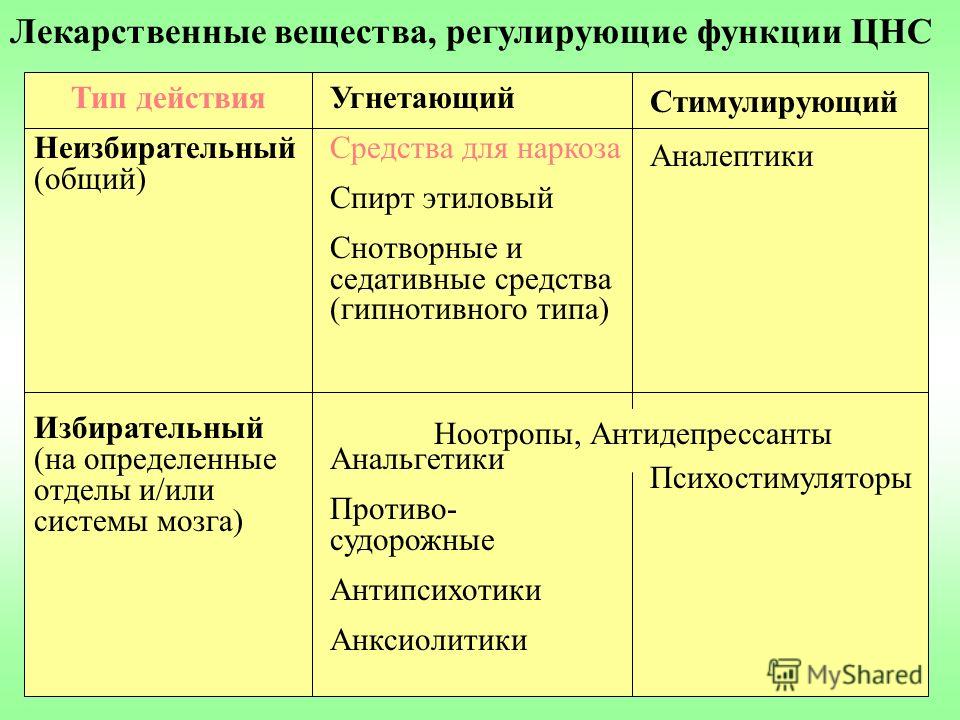
Со стороны дыхательной системы: одышка, бронхоспазм, угнетение дыхания, остановка дыхания.
Со стороны пищеварительной системы: тошнота, рвота.
Со стороны кожи и подкожных тканей: сыпь, крапивница, ангионевротический отек, отек лица.
Взаимодействие с другими препаратами
Токсичность лидокаина увеличивается при его одновременном применении с циметидином и пропранололом вследствие повышения концентрации лидокаина, это требует снижения дозы лидокаина. Оба препарата снижают печеночный кровоток. Кроме того, циметидин ингибирует микросомальную активность. Ранитидин незначительно снижает клиренс лидокаина, что приводит к повышению его концентрации.
Повышение сывороточной концентрации лидокаина также могут вызывать антиретровирусные средства (например, ампренавир, атазанавир, дарунавир, лопинавир).
Гипокалиемия, вызываемая диуретиками, может снижать действие лидокаина при их одновременном применении.
Лидокаин следует с осторожностью применять у пациентов, получающих другие местные анестетики или средства, структурно сходные с местными анестетиками амидного типа (например, антиаритмическими средствами, такими как мексилетин, токаинид), поскольку системные токсические эффекты носят аддитивный характер.
Отдельные исследования лекарственного взаимодействия между лидокаином и антиаритмическими препаратами III класса (например, амиодароном) не проводились, однако рекомендуется соблюдать осторожность.
У пациентов, одновременно получающих антипсихотические средства, удлиняющие или способные удлинять интервал QT (например, пимозид, сертиндол, оланзапин, кветиапин, зотепин), прениламин, эпинефрин (при случайном в/в введении) или антагонисты серотониновых 5НТ 3 рецепторов (например, трописетрон, доласетрон), может повышаться риск желудочковых аритмий.
Одновременное применение хинупристина/далфопристина может увеличивать концентрацию лидокаина и повышать, таким образом, риск желудочковых аритмий, одновременного применения следует избегать.
У пациентов, одновременно получающих миорелаксанты (например, суксаметоний), может повышаться риск усиленной и пролонгированной нервно-мышечной блокады.
После применения бупивакаина у пациентов, получавших верапамил и тимолол, сообщалось о развитии сердечно-сосудистой недостаточности, лидокаин близок по структуре к бупивакаину.
Допамин и 5-гидрокситриптамин снижают порог судорожной готовности для лидокаина.
Опиоиды, вероятно, обладают просудорожным действием, что подтверждается данными о том, что лидокаин снижает судорожный порог для фентанила у человека.
Комбинация опиоидов и противорвотных средств, иногда применяемая в целях получения седативного эффекта у детей, может снизить судорожный порог и повысить угнетающее действие лидокаина на ЦНС.
Применение эпинефрина вместе с лидокаином может снизить системную абсорбцию, но при случайном в/в введении резко возрастает риск желудочковой тахикардии и фибрилляции желудочков.
Одновременное применение прочих антиаритмических средств, бета-адреноблокаторов и блокаторов медленных кальциевых каналов может дополнительно снижать AV-проведение, внтурижелудочковую проводимость и сократимость.
Одновременное применение сосудосуживающих средств увеличивает длительность действия лидокаина.
Одновременное применение лидокаина и алкалоидов спорыньи (например, эрготамина) может вызвать тяжелую артериальную гипотензию.
Необходимо соблюдать осторожность при применении седативных средств, поскольку они могут повлиять на действие местных анестетиков на ЦНС.
Следует соблюдать осторожность при длительном применении противоэпилептических средств (фенитоин), барбитуратов и других ингибиторов микросомальных ферментов печени, поскольку это может привести к снижению эффективности и, как следствие, повышенной потребности в лидокаине. С другой стороны, в/в введение фенитоина может усилить угнетающее действие лидокаина на сердце.
Анальгезирующий эффект местных анестетиков может усиливаться опиоидами и клонидином.
Этанол, особенно при длительном злоупотреблении, может снижать действие местных анестетиков.
Лидокаин не совместим с амфотерицином В, метогекситоном и нитроглицерином.
Смешивать лидокаин с другими лекарственными препаратами не рекомендуется.
Особые указания
Введение лидокаина должны осуществлять специалисты, обладающие опытом проведения и оборудованием для реанимации.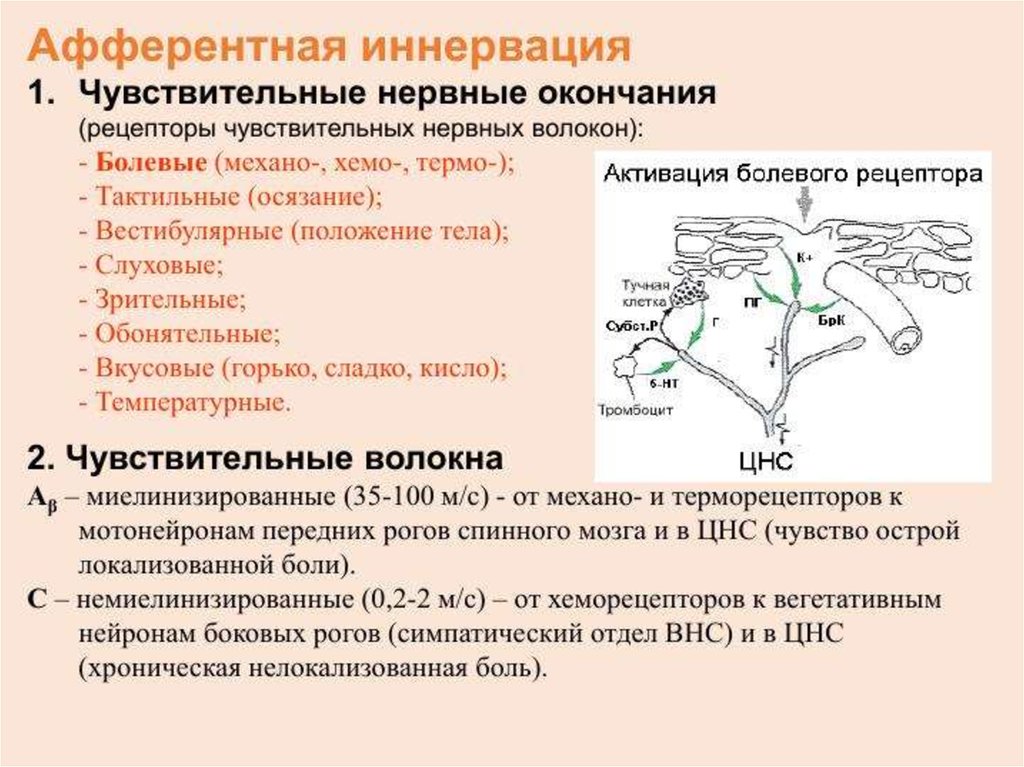 При введении местных анестетиков необходимо располагать оборудованием для проведения реанимации.
При введении местных анестетиков необходимо располагать оборудованием для проведения реанимации.
Лидокаин следует с осторожностью применять у пациентов с миастенией gravis, эпилепсией, хронической сердечной недостаточностью, брадикардией и угнетением дыхания, а также в комбинации с препаратами, взаимодействующими с лидокаином и приводящими к повышению его биодоступности, потенцированию эффектов (например, фенитоином) или удлинению выведения (например, при печеночной или терминальной почечной недостаточности, при которой могут кумулировать метаболиты лидокаина).
За пациентами, получающими антиаритмические препараты III класса (например, амиодарон), необходимо установить тщательное наблюдение и ЭКГ-мониторинг, поскольку влияние на сердце может потенцироваться.
В пострегистрационном периоде поступали сообщения о хондролизе у пациентов, которым проводили длительную внутрисуставную инфузию местных анестетиков после операции. В большинстве случаев хондролиз отмечался в плечевом суставе. Вследствие множества вносящих вклад факторов и противоречивости научной литературы относительно механизма реализации эффекта, причинно-следственная связь не выявлена. Длительная внутрисуставная инфузия не является разрешенным показанием к применению лидокаина.
Вследствие множества вносящих вклад факторов и противоречивости научной литературы относительно механизма реализации эффекта, причинно-следственная связь не выявлена. Длительная внутрисуставная инфузия не является разрешенным показанием к применению лидокаина.
В/м введение лидокаина может повышать активность креатинфосфокиназы, что может затруднить диагностику острого инфаркта миокарда.
Показано, что лидокаин может вызывать порфирию у животных, применение препарата у пациентов с порфирией следует избегать.
При введении в воспаленные или инфицированные ткани эффект лидокаина может снижаться. Перед началом в/в введения лидокаина необходимо устранить гипокалиемию, гипоксию и нарушение кислотно-основного состояния.
Некоторые процедуры местной анестезии могут приводить к серьезным нежелательным реакциям, независимо от применяемого местного анестетика.
Проводниковая анестезия спинномозговых нервов может приводить к угнетению сердечно-сосудистой системы, особенно на фоне гиповолемии, поэтому при проведении эпидуральной анестезии пациентам с сердечно-сосудистыми нарушениями следует соблюдать осторожность.
Эпидуральная анестезия может приводить к артериальной гипотензии и брадикардии. Риск можно снизить предварительным введением кристаллоидных или коллоидных растворов. Необходимо немедленно купировать артериальную гипотензию.
В некоторых случаях парацервикальная блокада при беременности может приводить к брадикардии или тахикардии у плода, в связи с чем, требуется тщательный мониторинг ЧСС у плода.
Введение в область головы и шеи может привести к непреднамеренному попаданию в артерию с развитием церебральной симптоматики (даже в низких дозах).
Ретробульбарное введение в редких случаях может приводить к попаданию в субарахноидальное пространство черепа, приводя к серьезным/тяжелым реакциям, включая сердечно-сосудистую недостаточность, апноэ, судороги и временную слепоту.
Ретро- и перибульбарное введение местных анестетиков несет низкий риск стойкой глазодвигательной дисфункции. К основным причинам относят травму и (или) местное токсическое действие на мышцы и (или) нервы.
Тяжесть подобных реакций зависит от степени травмы, концентрации местного анестетика и продолжительности его экспозиции в тканях. В связи с этим любой местный анестетик необходимо применять в наименьшей эффективной концентрации и дозе.
Лидокаин, раствор для инъекций, не рекомендуется применять у новорожденных. Оптимальная сывороточная концентрация лидокаина, позволяющая избежать такой токсичности, как судороги и аритмии, у новорожденных не установлена.
Условия хранения
Препарат следует хранить в недоступном для детей месте при температуре от 15° до 25°С.
Отпуск по рецепту
Да
Medznat
Лидокаин является короткодействующим местным анестетиком амидного типа.
ВСТУПЛЕНИЕ
Лидокаин является короткодействующим местным анестетиком амидного типа. В основе его механизма действия лежит уменьшение проницаемости мембраны нейрона для ионов натрия.
Показания к применению
Местная и регионарная анестезия, проводниковая анестезия при больших и малых вмешательствах.
ДОЗИРОВКА
Режим дозирования следует подбирать, основываясь на реакции пациента в месте введения. Препарат следует вводить в наименьшей концентрации и наименьшей дозе, дающей требуемый эффект. Максимальная доза для взрослых не должна превышать 300 мг.
Объем раствора, подлежащий введению, зависит от размера анестезируемого участка. Если есть потребность во введении большего объема с низкой концентрацией, то стандартный раствор разводят солевым раствором (0,9 % раствор натрия хлорида). Разведение осуществляют непосредственно перед введением.
Детям, пожилым и ослабленным пациентам препарат вводят в меньших дозах, соответствующих их возрасту и физическому состоянию.
У взрослых и детей 12-18 лет однократная доза лидокаина (за исключением спинальной анестезии) не должна превышать 5 мг/кг, при максимальной — 300 мг.
Дозы, рекомендуемые для взрослых:
|
10 мг/мл |
20 мг/мл | ||
|
Инфильтрационная анестезия: | |||
|
Малые вмешательства |
2-10 мл (20-100 мг) | ||
|
Болышие вмешательства |
10-20 мл (100-200 мг) |
5-10 мл (100-200 мг) | |
|
Проводниковая анестезия |
3-20 мл (30-200 мг) |
1. | |
|
Анестезия пальцев рук/ног |
2-4 мл (20-40 мг) |
2-4 мл (40-80 мг) | |
|
Эпидурульная, люмбальная |
25-30 мл (250-300 мг) | ||
|
Каудальная, грудная блокада |
20-30 мл (200-300 мг) | ||
|
Регионарная анестезия |
Не более 5 мл (50 мг) |
Не более 2,5 мл (50 мг) | |
Дети младше 1 года:
Опыт
применения у детей младше 1 года ограничен. Максимальная доза у детей 1-12 лет
составляет 5 мг/кг массы тела 1% раствора.
ФАРМАКОКИНЕТИКА
Абсорбция
Лидокаин быстро абсорбируется из желудочно-кишечного тракта, однако вследствие эффекта «первичпого прохождения» через печень лишь небольшое его количество достигает системного кровотока. Системная абсорбция лидокаина определяется местом введения, дозой и его фармакологическим профилем. Максимальная концентрация в крови достигается после межреберной блокады, далее (в порядке снижения концентрации), после введения в поясничное эпидуральное пространство, плечевое сплетение и подкожные ткани. Основным фактором, определяющим скорость абсорбции и концентрацию в крови, является общая введенная доза, независимо от участка введения. Имеется линейная зависимость между количеством введенного лидокаина и результирующей максимальной концентрацией анестетика в крови.
Максимальная концентрация в крови достигается после межреберной блокады, далее (в порядке снижения концентрации), после введения в поясничное эпидуральное пространство, плечевое сплетение и подкожные ткани. Основным фактором, определяющим скорость абсорбции и концентрацию в крови, является общая введенная доза, независимо от участка введения. Имеется линейная зависимость между количеством введенного лидокаина и результирующей максимальной концентрацией анестетика в крови.
Распределение
Лидокаин связывается с белками плазмы, включая альфа1-кислый гликопротеин (АКГ) и альбумин. Степень связывания вариабельна, составляя приблизительно 66 %. Плазменная концентрация АКГ у новорожденных низкая, поэтому у них отмечается относительно высокое содержание свободной биологически активной фракции лидокаина. Лидокаин проникает через гематоэнцефалический и плацентарный барьеры, вероятно, посредством пассивной диффузии.
Meтаболизм
Лидокаин метаболизируется в печени, около 90 % введенной дозы подвергается N-дезадкилированию с образованием моноэтилглицинксилидида (MEGX) и глицинксилида (GX), оба вносят вклад в терапевтические и токсические эффекты лидокаина. Фармакологические и токсические эффекты MEGX и GX сопоставимы с таковыми лидокаина, но выражены слабее. GX обладает более длинным, чем лидокаин, периодом полувыведения (около 10 часов) и может кумулировать при многократном введении. Метаболиты, образующиеся в результате последующего метаболизма, выводятся с мочой, содержание неизменного лидокаина в моче не превышает 10 %.
Фармакологические и токсические эффекты MEGX и GX сопоставимы с таковыми лидокаина, но выражены слабее. GX обладает более длинным, чем лидокаин, периодом полувыведения (около 10 часов) и может кумулировать при многократном введении. Метаболиты, образующиеся в результате последующего метаболизма, выводятся с мочой, содержание неизменного лидокаина в моче не превышает 10 %.
Выведение
Tepминальный период полувыведения лидокаина после внутривенного болюсного введения здоровым взрослым добровольцам составляет 1-2 часа. Терминальный период полувыведсния GX составляет около 10 часов, MEGX — 2 часа.
Особые группы пациентов
Вследствие быстрого метаболизма на фармакокинетику лидокаина могут оказывать влияние состояния, нарушающие функцию печени. У пациентов с печеночной дисфункцией период полувыведения лидокаина может повышаться в 2 и более раз.
Нарушение функции почек не влияет на фармакокинетику лидокаина, но может приводить к кумуляции его метаболитов. У новорождённых отмечается низкая концентрация АКГ, поэтому связь с белками плазмы может снижаться. Вследствие потенциально высокой концентрации свободной фракции применение лидокаина у новорожденных не рекомендуется.
У новорождённых отмечается низкая концентрация АКГ, поэтому связь с белками плазмы может снижаться. Вследствие потенциально высокой концентрации свободной фракции применение лидокаина у новорожденных не рекомендуется.
ПРОТИВОПОКАЗАНИЯ
- Гиперчувствительность к анестетикам амидного ряда
- Атриовентрикулярная (AV) блокада 3 степени.
- Гиповолемия.
С осторожностью
Хроническая сердечная недостаточность II ФК, артериальная гипотензия, гиповолемия, атриовентрикулярная блокада I степени, синусовая брадикардия, тяжелая печеночная и/или почечная недостаточность, тяжелая миастения, эпилептиформные судороги (в т.ч. в анамнезе), сниженный печеночный кровоток, ослабленные или пожилые больные (старше 65 лет), дети до 18 лег (вследствие замедленного метаболизма возможно накопление препарата).
Применение во время беременности и в период грудного вскармливания
Данные о влиянии лидокаина на фертильность человека отсутствуют.
Беременность
Лидокаин разрешается применять во время беременности и грудного вскармливания. Необходимо строго придерживаться назначенного режима дозирования. При осложнениях или кровотечении в анамнезе проведение эпидуральной анестезии лидокаином в акушерстве противопоказано.
Необходимо строго придерживаться назначенного режима дозирования. При осложнениях или кровотечении в анамнезе проведение эпидуральной анестезии лидокаином в акушерстве противопоказано.
Лидокаин применяли у большого числа беременных женщин и женщин детородного возраста. Какие-либо репродуктивные нарушения не зарегистрированы, т.е. повышения частоты пороков развития не отмечалось.
Вследствие потенциального достижения высокой концентрации местных анестетиков у плода после парацервикальной блокады у него могут развиться нежелательные реакции, такие как фетальная брадикардия. В связи с этим лидокаин в концентрации, превышающей 1%, в акушерстве не применяют.
В исследованиях на животных вредное воздействие на плод не обнаружено.
Грудное вскармливание
Лидокаин в небольшом количестве проникает в грудное молоко, его пероральная биодоступиость очень низкая. Таким образом, ожидаемое количество, поступающее с грудным молоком, очень небольшое, следовательно, потенциальный вред для ребенка очень низкий.
Решение о возможности применения лидокаина в период грудиого вскармливания принимает врач.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ПРЕПАРАТАМИ
Токсичность лидокаина увеличивается при его одновременном применении с циметидином и пропранололом вследствие повышения концентрации лидокаина, это требует снижения дозы лидокаина. Оба препарата снижают печеночный кровоток. Кроме того, циметидин ингибирует микросомальиую активность. Ранитидин незначительно снижает клиренс лидокаина, что приводит к повышению его концентрации в крови. Повышение сывороточной концентрации лидокаина также могут вызывать антиретровирусные средства (например, ампренавир, атазанавир, дарунавир, лопинавир).
Гипокалиемия, вызываемая диуретикамии, может снижать действие лидокаина при их одновременном применении (см. раздел «Особые указания»).
Лидокаин следует применять с осторожностью у пациентов, получающих другие местные анестетики или средства, структурно сходные с местными анестетиками амидного типа (например, аптиаритмиками, такими как мексилитин, токаинид), поскольку системные токсические эффекты носят адаптивный характер.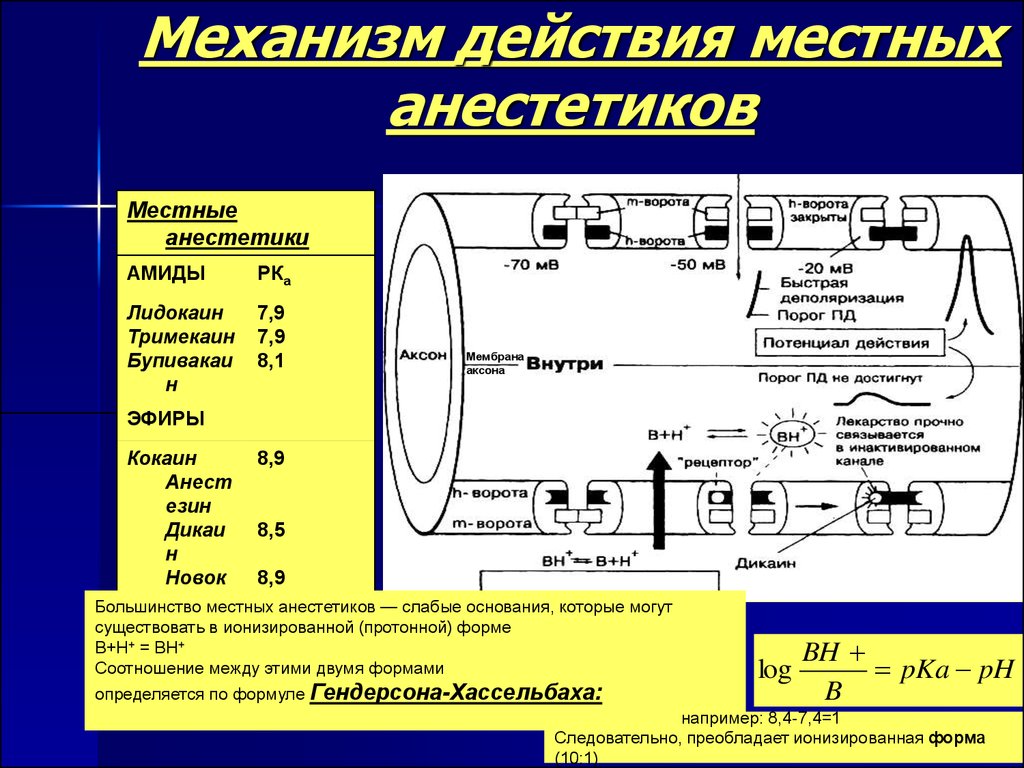
Отдельные исследования лекарственного взаимодействия между лидокаином и антитритмиками III класса (например, амиодароном) не проводились, однако рекомендуется соблюдать осторожность.
У пациентов, одновременно получающих антипсихотические средства, удлиняющие или способные удлинять интервал QT (например, пимозид, сертиндол, оланзапин, кветиапин, зотепин), прениламин, эпинефрин (при случайном внутривенном введении) или антагонисты 5-НТз-серотониновых рецепторов (например, трописетрон, доласетрон), может повышаться риск развития желудочковых аритмий.
Одновременное примененение хинупристина/далфопристина может увеличивать концентрацию лидокаина и повышать, таким образом, риск развития желудочковых аритмий; их одновременного применения следует избегать.
У пациеитов, получающих миорелаксанты (например, суксометоний), может повышаться риск усиленной и пролонгированной нервно-мышечной блокады.
После применения бупивакаина у пациентов, получавших верапамил и тимолол, сообщалось о развитии сердечно-сосудистой недостаточности; лидокаин близок по структуре к бупивакаину. Допамин и 5-гидрокситриптамин снижают порог судорожной готовности у пациентов, получающих лидокаин.
Допамин и 5-гидрокситриптамин снижают порог судорожной готовности у пациентов, получающих лидокаин.
Опиоиды, вероятно, обладают просудорожным действием, что подтверждается данными, что лидокаин снижает судорожный порог к фентанилу у человека.
Комбинация опиоидов и противорвотных средств, иногда применяемых в целях седации у детей, может снизить судорожный порог к лидокаину и повысить его угнетающее действие на ЦНС.
Применение эпинефрина вместе с лидокаином может снизить системную абсорбцию, но при случайном внутривенном введении возрастает риск желудочковой тахикардии и фибрилляции желудочков.
Одновременное применение прочих антиаритмических препаратов, бета-адреноблокаторов и блокаторов «медленных» кальциевых каналов может дополнительно снижать AV-проведение, проведение по желудочкам и сократимость.
Одновременное применение сосудосуживающих средств увеличивает длительность действия лидокаина.
Одновременное применение лидокаина и акалоидов спорыньи (например, эрготамина) может вызвать тяжелую артериальную гипотензию.
Необходимо соблюдать осторожность при применении седативных средств, поскольку они могут повлиять на действие местных анестетиков на ЦНС.
Необходимо соблюдать осторожность при длительном применении противоэпилептических средств (фенитоин), барбитуратов и других ингибиторов микросомальных ферментов печени, поскольку это может привести к снижению эффективности и, как следствие, повышенной потребности в лидоканне.
С другой стороны, внутривенное введение фенитоина может усилить угнетающее действие лидокаина на сердце.
Анальгезирующий эффект местных анестетиков может усиливаться опиоидами и клонидином. Этиловый спирт, особенно при длительном злоупотреблении, может снижать действие местных анестетиков.
Лидокаин не совместим с амфотерицином В, метогекситоном, нитроглицерином.
Смешивать лидокаин с другими лекарственными препаратами не рекомендуется.
ПОБОЧНЫЕ ЭФФЕКТЫ
Нежелательные реакции описаны в соответствии с системно-органными классами MedDRA. Частота определена следующим образом:
Частота определена следующим образом:
Подобно другим местным анестетикам, нежелательные реакции на лидокаин редки и, как правило, обусловлены повышенной плазменной концентрацией вследствие случайного внутрисосудистого введения, превышения дозы или быстрой абсорбции из участков с обильным кровоснабжением, либо вследствие гиперчувствителыюсти, идиосинкразии или сниженной переносимости пациента. Реакции системной токсичности, главным образом, проявляются со стороны центральной нервной и (или) сердечно-сосудистой системы (см. также раздел «Передозировка»)
Нарушения со стороны иммунной системы
Реакции гиперчувствительности (аллергические или анафилактоидные реакции, анафилактический шок) — см. также нарушения со стороны кожи и подкожных тканей. Кожная аллергическая проба на лидокаин считается надежной.
Нарушения со стороны нервной системы и психические расстройства
К неврологическим признакам системной токсичности относятся головокружение, нервозность, тремор, парестезия вокруг рта, онемение языка, сонливость, судороги, кома.
Реакции со стороны нервной системы могут проявляться ее возбуждением или угнетением. Признаки стимуляции центральной нервной системы могут быть непродолжительными или не возникать вовсе, вследствие чего первыми проявлениями токсичности могут служить снутанность сознания и сонливость, сменяющиеся комой и дыхательной недостаточностью.
К неврологическим осложнениям спинальной анестезии относятся преходящие неврологические симптомы, такие как боль в пояснице, ягодицах и ногах. Эти симптомы развиваются, как правило, в течение 24 часов после анестезии и разрешаются в течение нескольких дней. После спинальной анестезии лидокаином и сходными средствами описаны отдельные случаи арахноидита и синдрома конского хвоста со стойкой парестезией, дисфункцией кишечника и мочевыводящих путей или параличом нижних конечностей. Большинство случаев обусловлено гипербаричсской концентрацией лидокаина или длительной спинальной инфузией.
Нарушения со стороны органа зрения
Признаками лидокаиновой токсичности могут быть затуманенное зрение, диплопия и преходящий амавроз.
Двусторонний амавроз также может быть следствием случайного введения в ложе зрительного нерва в ходе офтальмологических процедур. После ретро- и перибульбарной анестезии сообщалось о воспалении глаза и диплопии (см. раздел «Особые указания»)
Нарушения со стороны органа слуха и лабиринта
Шум и ушах, гиперакузия.
Нарушения со стороны сердечно-сосудистой системы
Сердечно-сосудистые реакции проявляются артериальной гипотензией, брадикардией, угнетением миокарда (отрицательный инотроипый эффект), аритмиями; возможны остановка сердца или недостаточность кровообращения.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Одышка, бронхоспазм, угнетение дыхания, остановка дыхания.
Нарушения со стороны желудочно-кишечного тракта
Тошнота, рвота.
Нарушения со стороны кожи и подкожных тканей
Сыпь, крапивница, ангионевротический отек, отек лица.
Передозировка
Симптомы
Токсичность со стороны центральной нервной системы проявляется симптомами, нарастающими по тяжести. Сначала может развиться парестезия вокруг рта, онемение языка, головокружение, гиперакузия и шум в ушах. Нарушение зрения и мышечный тремор или мышечные подергивания свидетельствуют о более серьезной токсичности и предшествуют генерализованным судорогам. Эти признаки не следует путать с невротическим поведением. Затем могут наступить потеря сознания и большие судорожные припадки продолжительностью от нескольких секунд до нескольких минут. Судороги приводят к быстрому нарастанию гипоксии и гиперкапнии, обусловленных повышенной мышечной активностью и нарушением дыхания. В тяжелых случаях может развиться апноэ. Ацидоз усиливает токсичность местных анестетиков.
В тяжелых случаях возникают нарушения со стороны сердечно-сосудистой системы. При высокой системной концентрации могут развиться артериальная гипотензия, брадикардия, аритмия и остановка сердца, которые могут оказаться летальными.
Разрешение передозировки происходит вследствие перераспределения местного анестетика из центральной нервной системы и его метаболизма и может протекать достаточно быстро (если не была введена очень большая доза препарата).
Лечение
При возникновении признаков передозировки введение анестетика следует немедленно прекратить.
Судороги, угнетение центральной нервной системы и кардиотоксичность требуют медицинского вмешательства. Главные цели терапии заключаются в поддержании оксигенации, прекращении судорог, поддержании кровообращения и купировании ацидоза (в случае его развития). В соответствующих случаях необходимо обеспечить проходимость дыхательных путей и назначить кислород, а также наладить вспомогательную вентиляцию легких (масочную или с помощью мешка Амбу). Поддержание кровообращения осуществляется посредством вливания плазмы или инфузионных растворов. При необходимости длительного поддержания кровообращения следует рассмотреть возможность введения вазопрессоров, однако они повышают риск возбуждения центральной нервной системы. Контроль судорог можно достичь посредством внутривенного введения диазепама (0,1 мг/кг) или тиопентала натрия (1-3 мг/кг), при этом следует учитывать, что противосудорожные средства могут также угнетать дыхание и кровообращение. Продолжительные судороги могут препятствовать вентиляции легких и оксигенации пациента, в связи с чем следует рассмотреть возможность ранней эндотрахеальной интубации. При остановке сердца приступают к стандартной сердечно-легочной реанимации. Эффективность диализа при лечении острой передозировки лидокаином очень низкая.
Контроль судорог можно достичь посредством внутривенного введения диазепама (0,1 мг/кг) или тиопентала натрия (1-3 мг/кг), при этом следует учитывать, что противосудорожные средства могут также угнетать дыхание и кровообращение. Продолжительные судороги могут препятствовать вентиляции легких и оксигенации пациента, в связи с чем следует рассмотреть возможность ранней эндотрахеальной интубации. При остановке сердца приступают к стандартной сердечно-легочной реанимации. Эффективность диализа при лечении острой передозировки лидокаином очень низкая.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
Введение лидокаина должны осуществлять специалисты, обладающие опытом проведения и оборудованием для реанимации. При введении местных анестетиков необходимо располагать оборудованием для проведения реанимации.
Его следует с осторожностью применять у пациентов с миастенией gravis, эпилепсией, хронической сердечной недостаточностью, брадикардией и угнетением дыхания, а также в комбинации с препаратами, взаимодействующими с лидокаином и приводящими к повышению его биодоступности, потенцированию эффектов (например, фенитоином) или удлинению выведения (например, при печеночной или терминальной почечной недостаточности, при которой могут кумулировать метаболиты лидокаина).
За пациентами, получающими антиаритмические препараты III класса (например, амиодарон), необходимо установить тщательное наблюдение и ЭКГ-мониторинг, поскольку влияние на сердце может потенцироваться.
Поступали пострегистрациоиные сообщения о хондролизе у пациентов, которым осуществляли длительную внутрисуставную инфузию местных анестетиков после операции. В большинстве случаев хондролиз отмечался в плечевом суставе.
Вследствие множества вносящих вклад факторов и противоречивости научной литературы относительно механизма реализации эффекта, причинно-следственная связь не выявлена. Длительная внутрисуставная инфузия не является разрешенным показанием к применению лидокаина.
Внутримышечное введение лидокаина может повышать активность креатинфосфокиназы, что может затруднить диагностику острого инфаркта миокарда.
Показано, что лидокаин может вызывать порфирию у животных, его применения у лиц с порфирией следует избегать.
При введении в воспаленные или инфицированные ткани эффект лидокаина может снижаться. Перед началом внутривенного введения лидокаина необходимо устранить гипокалиемию, гипоксию и нарушение кислотно-основного состояния.
Перед началом внутривенного введения лидокаина необходимо устранить гипокалиемию, гипоксию и нарушение кислотно-основного состояния.
Некоторые процедуры местной анестезии могут приводить к серьезным нежелательным реакциям, независимо от применяемого местного анестетика.
Проводниковая анестезия спинномозговых нервов может приводить к угнетению сердечно-сосудистой системы, особенно на фоне гиповолемии, поэтому при проведении эпидуральной анестезии пациентам с сердечно-сосудистыми нарушениями следует соблюдать осторожность. Эпидуральная анестезия может привести к артериальной гипотензии и брадикардии. Риск можно снизить предварительным введением кристаллоидных или коллоидных растворов. Необходимо немедленно купировать артериальную гипотензию.
В некоторых случаях парацервикальная блокада при беременности может приводить к брацикардии или тахикардии у плода, в связи с чем требуется тщательный мониторинг частоты сердцебиения у плода (см. раздел «Применение во время беременности и в период грудного вскармливания»).
Введение в область головы и шеи может привести к непреднамеренному попаданию в артерию с развитием церебральной симптоматики даже в низких дозах.
Ретробульбарное введение в редких случаях может приводить к попаданию в субарахноидальное пространство черепа, приводя к серьезным/тяжелым реакциям, включая сердечно-сосудистую недостаточность, апноэ, судороги и временную слепоту.
Ретро- и перибульбарное введение местных анестетиков несет низкий риск стойкой глазодвигательной дисфункции. К основным причинам относят травму и(или) местное токсическое действие на мышцы и(или) нервы.
Тяжесть подобных реакций зависит от степени травмы, концентрации местного анестетика и продолжительности его экспозиции в тканях. В связи с этим любой местный анестетик необходимо применять в наименьшей эффективной концентрации и дозе.
Раствор для инъекций лидокаина не рекомендуется применять у новорожденных. Оптимальная сывороточная концентрация лидокаина, позволяющая избежать такой токсичности как судороги и аригмиии, у новорожденных не установлена.
Следует избегать внутрисосудистого введения, если таковое напрямую не показано.
Применение с осторожностью:
- у пациентов с коагулопагией. Терапия антикоагулянтам и (например, гепарином) НПВП, или плазмозаменителями повышает склонность к кровотечениям. Случайное повреждение сосудов может привести к тяжелым кровотечениям. При необходимости следует проверить время кровотечения, активированное частичное тромбопластиновое время (АЧТВ) и содержание тромбоцитов;
- пациенты с полной и неполной блокадой внутрисердечной проводимости, поскольку местные анестетики могут угнетать AV-проведение;
- необходимо тщательно наблюдать за пациентами с судорожными расстройствами на предмет симптоматики со стороны ЦНС. Низкие дозы лидокаина также могут повышать судорожную готовность. У пациентов с синдромом Мелькерссона-Розенталя аллергические и токсические реакции со стороны нервной системы в ответ на введение местных анестетиков могут развиваться чаще;
- третий триместр беременности.

Лидокаин, раствор для инъекций, 10, 20 мг/мл не разрешен для интратекального введения (субарахноидальной анестезии).
Влияние на способность управлять транспортными средствами и работу с механизмами
После введения местных анестетиков может отмечаться преходящее снижение чувствительности и(или) моторный блок. До разрешения этих эффектов пациентам не рекомендуется управлять транспортными средствами и работать с механизмами.
Клинические данные
Ссылка на инструкцию по применению препарата Лидокаин
http://grls.rosminzdrav.ru
Местные анестетики: системная токсичность — OpenAnesthesia
Токсичность местных анестетиков может проявляться в органах тела, правильное функционирование которых зависит от натриевых каналов. К ним относятся центральная нервная система и сердце. ЦНС более чувствительна к действию местных анестетиков, чем сердечная система, и обычно первыми проявляются признаки/симптомы токсичности.
Фармакологические данные (таблицы см. на изображении)
на изображении)
Воздействие на системы органов
Центральная нервная система
Начальными симптомами со стороны ЦНС являются шум в ушах, нечеткость зрения, головокружение, парез языка и онемение вокруг рта. Возбуждающие признаки, такие как нервозность, возбуждение, беспокойство и мышечные подергивания, являются результатом блокады тормозных путей. Подергивание мышц предвещает начало тонико-клонических судорог. Ранние признаки/симптомы переходят в угнетение ЦНС с невнятной речью, сонливостью, потерей сознания, а затем остановкой дыхания. У пациентов, получавших препараты, угнетающие ЦНС, может наблюдаться только угнетение ЦНС без предшествующих симптомов возбуждения.
Воздействие на ЦНС зависит от различных клинических факторов, в том числе:
Гиперкапния – повышение PaCO 2 снижает судорожный порог при введении местной анестезии. Сопутствующее увеличение мозгового кровотока позволяет доставить больше местного анестетика в ЦНС. Увеличение внутриклеточного рН приводит к захвату ионов местным анестетиком. Ацидоз, вызванный гиперкапнией, снижает связывание местных анестетиков с белками, делая больше лекарств доступным для ЦНС.
Ацидоз, вызванный гиперкапнией, снижает связывание местных анестетиков с белками, делая больше лекарств доступным для ЦНС.
Угнетение ЦНС. Пациенты в сознании, получающие препараты, угнетающие ЦНС, такие как бензодиазепины или внутривенные анестетики, имеют более высокий судорожный порог и могут не проявлять судорожной активности до наступления полного угнетения ЦНС.
Сердечно-сосудистая система
Местные анестетики оказывают прямое воздействие на сердце и периферические кровеносные сосуды. Они блокируют быстрые натриевые каналы в быстропроводящих тканях волокон Пуркинье и желудочков, что приводит к снижению скорости деполяризации. Местные анестетики также сокращают эффективный рефрактерный период и продолжительность потенциала действия. Высокие концентрации могут уменьшать время проведения, что приводит к удлинению интервалов PR и расширению комплексов QRS и даже к брадикардии/остановке синусового узла. Желудочковые аритмии, включая фибрилляцию, чаще возникают при применении бупивакаина, чем лидокаина. Местные анестетики обладают дозозависимым отрицательным инотропным эффектом. Этот угнетающий эффект прямо пропорционален относительной силе препарата (см. таблицу). Пациенты с ацидозом и/или гипоксией подвержены большему риску сердечно-депрессивного действия местных анестетиков. Кардиотоксичность местных анестетиков можно сравнить с использованием соотношения доз КК/ЦНС, которое представляет собой отношение дозы, вызывающей сердечный коллапс (КК), к дозе, вызывающей судороги/судороги. Чем ниже число, тем более кардиотоксичен препарат (например, CC/CNS для бупивакаина составляет приблизительно 3 против 7 для лидокаина). Важно отметить, что у пациентов, находящихся под общей анестезией, обычно проявляется кардиотоксичность как первый признак токсичности местных анестетиков.
Местные анестетики обладают дозозависимым отрицательным инотропным эффектом. Этот угнетающий эффект прямо пропорционален относительной силе препарата (см. таблицу). Пациенты с ацидозом и/или гипоксией подвержены большему риску сердечно-депрессивного действия местных анестетиков. Кардиотоксичность местных анестетиков можно сравнить с использованием соотношения доз КК/ЦНС, которое представляет собой отношение дозы, вызывающей сердечный коллапс (КК), к дозе, вызывающей судороги/судороги. Чем ниже число, тем более кардиотоксичен препарат (например, CC/CNS для бупивакаина составляет приблизительно 3 против 7 для лидокаина). Важно отметить, что у пациентов, находящихся под общей анестезией, обычно проявляется кардиотоксичность как первый признак токсичности местных анестетиков.
Относительная активность местного анестетика Прокаин 1 Хлоропрокаин 1 Кокаин 2 Лидокаин 2 Прилокаин 2 Мепивакаин 2 Этидокаин 6 Бупивакаин 8 Тетракаин 8 и снижение УВО. Кокаин — единственный местный анестетик, вызывающий сужение сосудов в любых дозах.
Различные блокады нервов
Вообще говоря, после данной инъекции с таким же количеством местного анестетика, уровни в сыворотке самые высокие после межреберных блокад, за которыми следуют эпидуральные/каудальные блокады, за которыми следуют блокады плечевого сплетения и бедренного/седалищного нерва, за которыми следуют подкожные блокады инъекции. Этот порядок соответствует сосудистому снабжению каждой ткани. См. ключевое слово ниже.
Абсорбция местных анестетиков (от большей к меньшей)
- Внутривенно
- Межреберный
- Каудальная эпидуральная анестезия
- Поясничная эпидуральная анестезия
- Плечевое сплетение
- Подкожный
Беременность
Было показано, что бупивакаин обладает повышенной кардиотоксичностью у беременных женщин, что приводит к уменьшению соотношения доз CC/CNS.
Метгемоглобинемия
Побочным эффектом, уникальным для прилокаина, является метгемоглобинемия при дозах не менее 600 мг.
Лидокаин: A Focus
Системная токсичность местных анестетиков: современные перспективы
1. Эль-Богдадли К., Пава А. Плоская блокада, выпрямляющая позвоночник: плоская и простая. Анестезия. 2017;72(4):434–438. [PubMed] [Google Scholar]
2. Фореро М., Адхикари С.Д., Лопес Х., Цуй С., Чин К.Дж. Плоскостной блок, выпрямляющий позвоночник. Reg Anesth Pain Med. 2016;41(5):621–627. [PubMed] [Google Scholar]
3. Ильфельд Б.М. Непрерывные блокады периферических нервов: обзор опубликованных данных. Анест Анальг. 2011;113(4):904–925. [PubMed] [Google Scholar]
4. Pawa A, Wight J, Onwochei DN, et al. Комбинированные блокады грудного паравертебрального и грудного нервов при операциях на молочной железе под седацией: серия проспективных наблюдений. Анестезия. 2018;73(4):438–443. [PubMed] [Google Scholar]
5.
6. Dillane D, Finucane BT. Системная токсичность местных анестетиков. Can J Anesth Can D’Anesthésie. 2010;57(4):368–380. [PubMed] [Академия Google]
7. Баттерворт Дж.Ф. Модели и механизмы кардиотоксичности местных анестетиков: обзор. Reg Anesth Pain Med. 2010;35(2):167–176. [PubMed] [Google Scholar]
8. Такер Г.Т. Фармакокинетика местных анестетиков. Бр Джей Анаст. 1986;58(7):717–731. [PubMed] [Google Scholar]
9. Becker DE, Reed KL. Местные анестетики: обзор фармакологических соображений. Анест Прог. 2012;59(2):90–102. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Butterworth JF, Strichartz GR. Молекулярные механизмы местной анестезии: обзор. Анестезиология. 1990;72(4):711–734. [PubMed] [Google Scholar]
11. Гробан Л., Долински С.Ю. Различия в сердечной токсичности между ропивакаином, левобупивакаином, бупивакаином и лидокаином.
12. Komai H, Mcdowell TS. Ингибирование местными анестетиками токов калия, активируемых напряжением, в нейронах ганглиев задних корешков крыс. Анестезиология. 2001;94(6):1089–1095. [PubMed] [Google Scholar]
13. Валенсуэла С., Дельпон Э., Тамкун М.М., Тамарго Дж., Снайдерс Д.Дж. Стереоселективная блокада калиевых каналов сердца человека (Kv1.5) энантиомерами бупивакаина. Биофиз Дж. 1995;69(2):418–427. [PMC free article] [PubMed] [Google Scholar]
14. Coyle DE, Sperelakis N. Бупивакаин и лидокаин блокируют опосредованные кальцием потенциалы медленного действия в желудочковой мышце морской свинки. J Pharmacol Exp Ther. 1987; 242(3):1001–1005. [PubMed] [Google Scholar]
15. Clarkson CW, Hondeghem LM. Механизм угнетения сердечной проводимости бупивакаином. Анестезиология. 1985;62(4):396–405. [PubMed] [Google Scholar]
16. Fettiplace MR, Kowal K, Ripper R, et al. Передача сигналов инсулина при индуцированной бупивакаином сердечной токсичности: сенсибилизация во время восстановления и потенцирование с помощью липидной эмульсии.
17. Piegeler T, Votta-Velis EG, Bakhshi FR, et al. Защита эндотелиального барьера местными анестетиками: ропивакаин и лидокаин блокируют активацию Src эндотелиальных клеток, индуцированную фактором некроза опухоли-а. Анестезиология. 2014;120(6):1414–1428. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Piegeler T, Votta-Velis EG, Liu G, et al. Антиметастатический потенциал местных анестетиков, связанных с амидом: ингибирование миграции клеток аденокарциномы легкого и воспалительной передачи сигналов Src независимо от блокады натриевых каналов. Анестезиология. 2012;117(3):548–559. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Butterworth JF, 4th, Brownlow RC, Leith JP, Prielipp RC, Cole LR. Бупивакаин ингибирует продукцию циклического 3′,5′-аденозинмонофосфата. Возможный фактор, способствующий сердечно-сосудистой токсичности. Анестезиология. 1993;79(1):88–95. [PubMed] [Google Scholar]
20. Пишкин О., Айдын Б.Г., Пишкин А.Б.Г. Влияние предварительной обработки инсулином + глюкозой на кардиотоксичность бупивакаина у крыс. Hum Exp Toxicol. 2018;37(5):451–457. [PubMed] [Академия Google]
Пишкин О., Айдын Б.Г., Пишкин А.Б.Г. Влияние предварительной обработки инсулином + глюкозой на кардиотоксичность бупивакаина у крыс. Hum Exp Toxicol. 2018;37(5):451–457. [PubMed] [Академия Google]
21. Roth D, Pace NL, Lee A, et al. Физикальное обследование дыхательных путей для выявления проблем с обеспечением проходимости дыхательных путей у внешне здоровых взрослых пациентов. Cochrane Database Syst Rev. 2018;5(5):CD008874. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Шульце С.М., Хеммингс Б.А., Ниссен М., Чопп О. Передача сигналов PI3K/AKT, MAPK и AMPK: протеинкиназы в гомеостазе глюкозы. Эксперт Rev Mol Med. 2012;14:e1. [PubMed] [Google Scholar]
23. Zink W, Graf BM. Токсичность местных анестетиков: место ропивакаина и левобупивакаина. Курр Опин Анаэстезиол. 2008;21(5):645–650. [PubMed] [Академия Google]
24. Watanabe Y, Dohi S, Iida H, Ishiyama T. Влияние бупивакаина и ропивакаина на чувствительность барорефлекса с респираторным ацидозом и алкалозом или без них у крыс. Анест Анальг. 1997;84(2):398–404. [PubMed] [Google Scholar]
Анест Анальг. 1997;84(2):398–404. [PubMed] [Google Scholar]
25. Neal JM, Bernards CM, Butterworth JF, et al. Практические рекомендации ASRA по системной токсичности местных анестетиков. Reg Anesth Pain Med. 2010;35(2):152–161. [PubMed] [Google Scholar]
26. Эль-Богдадли К., Чин К.Дж. Системная токсичность местных анестетиков: непрерывное профессиональное развитие. Джан Джей Анаст. 2016;63(3):330–349. [PubMed] [Google Scholar]
27. Гитман М., Баррингтон М.Дж. Системная токсичность местных анестетиков: обзор последних сообщений о случаях заболевания и реестров. Reg Anesth Pain Med. 2018;43(2):124–130. [PubMed] [Google Scholar]
28. Грегорио Г., Нил Дж. М., Розенквист Р. В., Вайнберг Г. Л. Клиническая картина системной токсичности местных анестетиков: обзор опубликованных случаев с 1979 по 2009 год. Reg Anesth Pain Med. 2010;35(2):181–187. [PubMed] [Google Scholar]
29. Малрой М.Ф. Системная токсичность и кардиотоксичность местных анестетиков: заболеваемость и меры профилактики. Reg Anesth Pain Med. 2002;27(6):556–561. [PubMed] [Академия Google]
Reg Anesth Pain Med. 2002;27(6):556–561. [PubMed] [Академия Google]
30. Гробан Л. Влияние на центральную нервную систему и сердце токсичности амидных местных анестетиков длительного действия в модели интактных животных. Reg Anesth Pain Med. 2003;28(1):3–11. [PubMed] [Google Scholar]
31. Бреслин Д.С., Мартин Г., Маклеод Д.Б., Д’Эрколе Ф., Грант С.А. Токсичность центральной нервной системы после введения левобупивакаина для блокады поясничного сплетения: отчет о двух случаях. Reg Anesth Pain Med. 2003;28(2):144–147. [PubMed] [Google Scholar]
32. Weiss E, Jolly C, Dumoulin JL, et al. Судороги у 2 пациенток после двусторонней блокады поперечной плоскости живота под ультразвуковым контролем для обезболивания кесарева сечения. Reg Anesth Pain Med. 2014;39(3): 248–251. [PubMed] [Google Scholar]
33. Rosenberg PH, Veering BT, Urmey WF. Максимально рекомендуемые дозы местных анестетиков: многофакторная концепция. Reg Anesth Pain Med. 2004;29(6):564–575. [PubMed] [Google Scholar]
34. Pere PJ, Ekstrand A, Salonen M, et al. Фармакокинетика ропивакаина у больных с хронической почечной недостаточностью. Бр Джей Анаст. 2011;106(4):512–521. [PubMed] [Google Scholar]
Pere PJ, Ekstrand A, Salonen M, et al. Фармакокинетика ропивакаина у больных с хронической почечной недостаточностью. Бр Джей Анаст. 2011;106(4):512–521. [PubMed] [Google Scholar]
35. Pere P, Salonen M, Jokinen M, Rosenberg PH, Neuvonen PJ, Haasio J. Фармакокинетика ропивакаина у пациентов с уремией и без уремии после подмышечной блокады плечевого сплетения. Анест Анальг. 2003;96 (2): 563–569. [PubMed] [Google Scholar]
36. Vasques F, Behr AU, Weinberg G, Ori C, di Gregorio G. Обзор случаев системной токсичности местных анестетиков с момента публикации рекомендаций Американского общества регионарной анестезии. Reg Anesth Pain Med. 2015;40(6):1–705. [PubMed] [Google Scholar]
37. Yu RN, Houck CS, Casta A, Blum RH. Институциональные изменения политики для предотвращения сердечной токсичности, связанной с блокадой полового члена бупивакаином у младенцев. Отчет по делу 2016;7(3):71–75. [PubMed] [Академия Google]
38. Barrington MJ, Kluger R. Ультразвуковой контроль снижает риск системной токсичности местных анестетиков после блокады периферических нервов. Reg Anesth Pain Med. 2013;38(4):289–297. [PubMed] [Google Scholar]
Reg Anesth Pain Med. 2013;38(4):289–297. [PubMed] [Google Scholar]
39. Tucker GT, Moore DC, Bridenbaugh PO, Bridenbaugh LD, Thompson GE. Системная абсорбция мепивакаина при обычно используемых процедурах регионарной блокады. Анестезиология. 1972;37(3):277–287. [PubMed] [Google Scholar]
40. Trabelsi B, Charfi R, Bennasr L, et al. Фармакокинетика бупивакаина после двусторонней блокады поперечной плоскости живота под ультразвуковым контролем после кесарева сечения под спинальной анестезией. Int J Obstet Анест. 2017;32:17–20. [PubMed] [Академия Google]
41. Муроути Т., Ивасаки С., Ямакаге М. Хронологические изменения концентрации ропивакаина и обезболивающих эффектов между блокадой поперечной плоскости живота и блокадой прямой кишки. Reg Anesth Pain Med. 2015;40(5):568–571. [PubMed] [Google Scholar]
42. Yasumura R, Kobayashi Y, Ochiai R. Сравнение концентраций левобупивакаина в плазме после блокады поперечной плоскости живота и блокады влагалища прямой мышцы живота. Анестезия. 2016;71(5):544–549. [PubMed] [Google Scholar]
Анестезия. 2016;71(5):544–549. [PubMed] [Google Scholar]
43. Toju K, Shiraishi K, Hakozaki T, Isosu T, Murakawa M. Концентрация ропивакаина в плазме после подреберной блокады поперечной плоскости живота под ультразвуковым контролем у взрослых. Джей Анест. 2015;29(1): 146–148. [PubMed] [Google Scholar]
44. Bardsley H, Gristwood R, Baker H, Watson N, Nimmo W. Сравнение сердечно-сосудистых эффектов левобупивакаина и rac-бупивакаина после внутривенного введения здоровым добровольцам. Бр Дж Клин Фармакол. 1998;46(3):245–249. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Corvetto MA, Echevarría GC, De La Fuente N, Mosqueira L, Solari S, Altermatt FR. Сравнение концентраций левобупивакаина в плазме с адреналином и без него при блокаде поперечной плоскости живота. Reg Anesth Pain Med. 2012;37(6):633–637. [PubMed] [Академия Google]
46. Миранда П., Корветто М.А., Альтерматт Ф.Р., Аранеда А., Эчеваррия Г.К., Кортинес Л.И. Фармакокинетика всасывания левобупивакаина с адреналином и без него во время блокады TAP: анализ доз на основе связанного риска токсичности местных анестетиков. Eur J Clin Pharmacol. 2016;72(10):1221–1227. [PubMed] [Google Scholar]
Eur J Clin Pharmacol. 2016;72(10):1221–1227. [PubMed] [Google Scholar]
47. Neal JM, Barrington MJ, Fettiplace MR, et al. Рекомендации Третьего Американского общества регионарной анестезии и медицины боли по системной токсичности местных анестетиков: краткое изложение 2017. Reg Anesth Pain Med. 2018;43(2):113–123. [PubMed] [Академия Google]
48. Gurnaney H, Kraemer FW, Maxwell L, Muhly WT, Schleelein L, Ganesh A. Амбулаторная непрерывная блокада периферических нервов у детей и подростков: продольное 8-летнее одноцентровое исследование. Анест Анальг. 2014;118(3):621–627. [PubMed] [Google Scholar]
49. Kumar SK, Rao V, Morris RG, Watts RW, Westley IS, Ropivacaine WIS. Концентрации ропивакаина (общего и несвязанного) и AGP после блока поперечной плоскости живота для обезболивания после абдоминальной хирургии. Мониторинг наркотиков. 2014;36(6):759–764. [PubMed] [Google Scholar]
50. Брайдон А.С., Сувацоглу Р., Аббас М., Уотсон Д.Г., Макдональд Д.А., Гилл А.М. Уровни ропивакаина в плазме после местной инфильтрационной анальгезии в высоких дозах при тотальном эндопротезировании коленного сустава. Анестезия. 2015;70(7):784–790. [PubMed] [Google Scholar]
Уровни ропивакаина в плазме после местной инфильтрационной анальгезии в высоких дозах при тотальном эндопротезировании коленного сустава. Анестезия. 2015;70(7):784–790. [PubMed] [Google Scholar]
51. Fenten MG, Bakker SM, Touw DJ, et al. Фармакокинетика 400 мг ропивакаина после периартикулярной местной инфильтрационной анальгезии при тотальном эндопротезировании коленного сустава. Acta Anaesthesiol Scand. 2017;61(3):338–345. [PubMed] [Академия Google]
52. Affas F, Eksborg S, Wretenberg P, Olofsson C, Stiller CO. Фармакокинетика ропивакаина после местного инфильтрационного обезболивания при эндопротезировании тазобедренного сустава. Анест Анальг. 2014;119(4):996–999. [PubMed] [Google Scholar]
53. Аффас Ф. Эффективность и безопасность местного инфильтрационного обезболивания при эндопротезировании коленного и тазобедренного суставов. Сканд Джей Пейн. 2016;13:59–66. [PubMed] [Google Scholar]
54. Fenten MG, Rohrbach A, Wymenga AB, Stienstra R. Системная токсичность местных анестетиков после местного инфильтрационного обезболивания после замены полиэтиленовой большеберцовой вставки: отчет о клиническом случае. Reg Anesth Pain Med. 2014;39(3): 264–265. [PubMed] [Google Scholar]
Reg Anesth Pain Med. 2014;39(3): 264–265. [PubMed] [Google Scholar]
55. Рубин Д.С., Мацумото М.М., Вайнберг Г., Рот С. Системная токсичность местных анестетиков при тотальном эндопротезировании суставов: заболеваемость и факторы риска в Соединенных Штатах из национальной стационарной выборки 1998–2013 гг. Reg Anesth Pain Med. 2018;43(2):131–137. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Hu D, Onel E, Singla N, Kramer WG, Hadzic A. Фармакокинетический профиль липосомальной инъекции бупивакаина после однократного введения в область хирургического вмешательства. Клин по расследованию наркотиков. 2013;33(2):109–115. [PubMed] [Google Scholar]
57. Rice D, Heil JW, Biernat L. Фармакокинетический профиль и переносимость липосомального бупивакаина после многократного введения через локальную подкожную инфильтрацию у здоровых добровольцев. Клин по расследованию наркотиков. 2017;37(3):249–257. [PubMed] [Google Scholar]
58. Джоши Г.П., Пату Г., Харитонов В. Безопасность липосомного бупивакаина при различных путях введения у животных. Джей Боль Рез. 2015; 8: 781–789. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Безопасность липосомного бупивакаина при различных путях введения у животных. Джей Боль Рез. 2015; 8: 781–789. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Бербридж М., Джаффе Р.А. Exparel®: новый местный анестетик с особыми требованиями безопасности. Анест Анальг. 2015;121(4):1113–1114. [PubMed] [Google Scholar]
60. Харитонов В. Обзор совместимости липосомального бупивакаина с другими лекарственными средствами и часто используемыми материалами для имплантатов. аспирантура мед. 2014;126(1):129–138. [PubMed] [Google Scholar]
61. Аггарвал Н. Связь системной токсичности местных анестетиков с экспарелом (бупивакаиновая липосома) – оценка фармаконадзора. Экспертное заключение Drug Safe. 2018;17(6):1–7. [PubMed] [Академия Google]
62. Svedman KJ, Coldiron B, Coleman WP, et al. Руководство ASDS по уходу за тумесцентной липосакцией. Дерматол Хирург. 2006;32(5):709–716. [PubMed] [Google Scholar]
63. Klein JA, Jeske DR. Расчетные максимальные безопасные дозы тумесцентного лидокаина. Анест Анальг. 2016;122(5):1350–1359. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Анест Анальг. 2016;122(5):1350–1359. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Вайнберг Г. Системная токсичность местных анестетиков и липосакция: взгляд назад, взгляд вперед. Анест Анальг. 2016;122(5):1250–1252. [PubMed] [Академия Google]
65. Бэкон Б., Сильвертон Н., Кац М., Хит Э., Булл Д.А., Хариг Дж., Тонна Дж.Е. Системная токсичность местного анестетика, вызванная остановкой сердца после топизации для чреспищеводной эхокардиографии и последующего лечения с помощью экстракорпоральной сердечно-легочной реанимации. J Cardiothorac Vasc Anesth. 31 января 2018 г.: S1053-0770(18)30048-X. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Gaïes E, Jebabli N, Lakhal M, Klouz A, Salouage I, Trabelsi S. Отсроченные судороги после инстилляции лидокаина для бронхоскопии. Преподобный Мал Респир. 2016;33(5):388–390. [PubMed] [Google Scholar]
67. Ву Ф.Л., Раззаги А., Соуни П.Ф. Судороги после лидокаина для бронхоскопии: история болезни и обзор использования лидокаина при анестезии дыхательных путей. Фармакотерапия. 1993;13(1):72–78. [PubMed] [Google Scholar]
Фармакотерапия. 1993;13(1):72–78. [PubMed] [Google Scholar]
68. Weibel S, Jokinen J, Pace NL, et al. Эффективность и безопасность внутривенного введения лидокаина для послеоперационного обезболивания и восстановления после операции: систематический обзор с последовательным анализом испытаний. Бр Джей Анаст. 2016;116(6):770–783. [PubMed] [Академия Google]
69. Вудрафф С., Вечорек П.М., Шрикер Т., Винет Б., Бэкман С.Б. Распыленный лидокаин для местной анестезии дыхательных путей у пациентов с морбидным ожирением: 1% по сравнению с 2% анестезией. 2010;65(1):12–17. [PubMed] [Google Scholar]
70. Эфтимиу Дж., Хигенботтам Т., Холт Д., Кокрейн Г.М. Плазменные концентрации лигнокаина во время фиброоптической бронхоскопии. грудная клетка. 1982;37(1):68–71. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Кандил Э., Меликман Э., Адинофф Б. Инфузия лидокаина: многообещающий терапевтический подход к хронической боли. Джей Анест Клин Рез. 2017;8(1) [бесплатная статья PMC] [PubMed] [Google Scholar]
72. Eipe N, Gupta S, Penning J. Внутривенный лидокаин при острой боли: доказательная клиническая информация. BJA Образование. 2016;16(9):292–298. [Google Scholar]
Eipe N, Gupta S, Penning J. Внутривенный лидокаин при острой боли: доказательная клиническая информация. BJA Образование. 2016;16(9):292–298. [Google Scholar]
73. Wong GK, Joo DT, Mcdonnell C. Липидная реанимация у ребенка с дефицитом карнитина после внутрисосудистой миграции эпидурального катетера. Анестезия. 2010;65(2):192–195. [PubMed] [Google Scholar]
74. Халдар Р., Дубей М., Растоги А., Сингх П.К. Внутривенный лидокаин для притупления реакции на экстубацию: палка о двух концах. Am J Ther. 2016;23(2):e646–e648. [PubMed] [Академия Google]
75. Guay J. Нежелательные явления, связанные с внутривенной регионарной анестезией (блокада Бира): систематический обзор осложнений. Джей Клин Анест. 2009;21(8):585–594. [PubMed] [Google Scholar]
76. Orebaugh SL, Kentor ML, Williams BA. Неблагоприятные исходы, связанные с блокадой периферических нервов под контролем нейростимулятора и под контролем УЗИ под наблюдением стажеров: обновление базы данных в одном месте. Reg Anesth Pain Med. 2012;37(6):577–582. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Reg Anesth Pain Med. 2012;37(6):577–582. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Литман Р.С., Смит В.И., Мейнленд П. Новые решения для снижения количества ошибок при приеме лекарств по неправильному пути. Педиатр Анест. 2018;28(1):8–12. [PubMed] [Google Scholar]
78. Комитет по анализу управления рисками Французского общества анестезиологии и интенсивной терапии (SFAR), Французского общества клинической фармации (SFPC) Пириу В., Тейссен А., Арсалье-Даре С. Предотвращение ошибок при приеме лекарств в анестезии и интенсивной терапии (сокращенная версия) Anaesth Crit Care Pain Med. 2017;36(4):253–258. [PubMed] [Академия Google]
79. Vasques F, Behr AU, Weinberg G, Ori C, di Gregorio G. Обзор случаев системной токсичности местных анестетиков с момента публикации рекомендаций Американского общества регионарной анестезии: для кого это может касаться. Reg Anesth Pain Med. 2015;40(6):698–705. [PubMed] [Google Scholar]
80. Mochizuki T, Sato S. Гипокапния продлевает брадикардию, вызванную бупивакаином или левобупивакаином в изолированных сердцах крыс. Джан Джей Анаст. 2008;55(12):836–846. [PubMed] [Академия Google]
Джан Джей Анаст. 2008;55(12):836–846. [PubMed] [Академия Google]
81. Fettiplace MR, Lis K, Ripper R, et al. Мультимодальный вклад в детоксикацию острой фармакотоксичности с помощью микроэмульсии триглицеридов. J Управление выпуском. 2015;198:62–70. [Бесплатная статья PMC] [PubMed] [Google Scholar]
82. Rahman S, Li J, Bopassa JC, et al. Фосфорилирование GSK-3β опосредует интралипид-индуцированную кардиозащиту от ишемии/реперфузии. Анестезиология. 2011;115(2):242–253. [Бесплатная статья PMC] [PubMed] [Google Scholar]
83. Lou P-H, Lucchinetti E, Zhang L, et al. Механизм опосредованного Интралипидом® ингибирования кардиозащитного комплекса IV активным метаболитом, пальмитоилкарнитином, генерирует активные формы кислорода и активирует реперфузионные киназы спасения травм. ПЛОС Один. 2014;9(1):e87205. [Бесплатная статья PMC] [PubMed] [Google Scholar]
84. Stehr SN, Ziegeler JC, Pexa A, et al. Влияние инфузии липидов на функцию миокарда и биоэнергетику при токсичности l-бупивакаина в изолированном сердце крысы. Анест Анальг. 2007;104(1):186–192. [PubMed] [Google Scholar]
Анест Анальг. 2007;104(1):186–192. [PubMed] [Google Scholar]
85. Fettiplace MR, Ripper R, Lis K, et al. Быстрый кардиотонический эффект инфузии липидной эмульсии*. Крит Уход Мед. 2013;41(8):e156–e162. [PubMed] [Google Scholar]
86. Weinberg G. Текущие данные поддерживают использование липидной спасательной терапии при системной токсичности местных анестетиков. Acta Anaesthesiol Scand. 2017;61(4):365–368. [PubMed] [Академия Google]
87. Harvey M, Cave G. Эмульсия липидов при токсичности местных анестетиков. Курр Опин Анаэстезиол. 2017;30(5):632–638. [PubMed] [Google Scholar]
88. Fettiplace MR, McCabe DJ. Эмульсия липидов улучшает выживаемость на животных моделях токсичности местных анестетиков: метаанализ. Клин Токсикол. 2017;55(7):617–623. [PubMed] [Google Scholar]
89. Руководство по безопасности Ассоциации анестезиологов Великобритании и Ирландии AAGBI: Управление тяжелой токсичностью местных анестетиков. [По состоянию на 08 июля 2018 г.]. https://www. aagbi.org/sites/default/files/la_toxicity_2010_0.pdf.
aagbi.org/sites/default/files/la_toxicity_2010_0.pdf.
90. Wang QG, Wu C, Xia Y, et al. Адреналин ухудшает легочный газообмен в крысиной модели кардиотоксичности, вызванной бупивакаином: пороговая доза адреналина. Reg Anesth Pain Med. 2017;42(3):342–350. [PubMed] [Google Scholar]
91. LipidRescue ™ реанимация [домашняя страница в Интернете] [По состоянию на 08 июля 2018 г.]. Доступно по адресу: http://www.lidrescue.org.
92. Берде С.Б., Стрихартц Г.Р. Местные анестетики. В: Миллер Р.Д., редактор. Анестезия Миллера. восьмой. Филадельфия: Эльзевир; 2015. с. 1043. [Google Академия]
93. Dadure C, Sola C, Dalens B, Capdevila X. Регионарная анестезия у детей. В: Миллер Р.Д., редактор. Анестезия Миллера. восьмой. Филадельфия: Эльзевир; 2015. с. 2718. [Google Scholar]
94. Американская академия педиатрии; Американская академия детской стоматологии. Кот С.Дж., Уилсон С., Рабочая группа по седации. Рекомендации по мониторингу и ведению педиатрических пациентов во время и после седации при диагностических и терапевтических процедурах: обновление.

 5-10
мл (30-200 мг)
5-10
мл (30-200 мг)