Десквамация — это… Что такое Десквамация?
десквамация — шелушение, отслаивание, слущивание Словарь русских синонимов. десквамация сущ., кол во синонимов: 3 • отслаивание (5) • … Словарь синонимов
ДЕСКВАМАЦИЯ — (от лат. desquamo снимаю чешую) 1) чешуйчатое отслаивание горных пород со скалистых поверхностей под влиянием резких колебаний температур (главным образом суточных), преимущественно в пустынях и высокогорных районах.2) Слущивание клеток с… … Большой Энциклопедический словарь
ДЕСКВАМАЦИЯ — [desquamare снимать чешую] шелушение и отслаивание г. п. под влиянием резких колебаний температур. Обычно наблюдается в пустынях и в высокогорных р нах. В результате Д. образуется скопление плоских остроугольных обломков п. Син.: шелушение горных … Геологическая энциклопедия
ДЕСКВАМАЦИЯ — (от лат. squama чешуя), отпадение, слущивание клеток с поверхности. Д. как явление постоянное наблюдается напр. на поверхности кожи, где происходит слущивание клеток ороговевшего эпителия (чешуек). Физиологическую Д. эпителия можно обнаруяшть… … Большая медицинская энциклопедия
десквамация — Шелушение и отслаивание горных пород под влиянием резких колебаний температуры. Обычно проявляется в пустынях и высокогорных областях. [Словарь геологических терминов и понятий. Томский Государственный Университет] Тематики геология, геофизика… … Справочник технического переводчика
десквамация — Отслаивание тонких округлых чешуй с обнаженных скалистых поверхностей горных пород под влиянием резких, главным образом суточных, колебаний температуры … Словарь по географии
десквамация — (лат. desquamare снимать чешую) 1) мед. шелушение кожи, отпадение, слущивание клеток покровных тканей; 2) геол. отслаивание вещества горных пород чешуйками под влиянием резких колебаний температуры (напр.
десквамация — (от лат. desquamo снимаю чешую), 1) чешуйчатое отслаивание горных пород со скалистых поверхностей под влиянием резких колебаний температур (главным образом суточных), преимущественно в пустынях и высокогорных районах. 2) Слущивание клеток с… … Энциклопедический словарь
десквамация — rus десквамация (ж) eng desquamation, exfoliation fra desquamation (f), exfoliation (f) deu Desquamation (f), Abschuppung (f), Exfoliation (f) spa descamación (f), exfoliación (f) … Безопасность и гигиена труда. Перевод на английский, французский, немецкий, испанский языки
десквамация — (desquamatio; от лат. desquamo, desquamatum снимать чешую) физиологический или патологический процесс слущивания эпителиальных клеток … Большой медицинский словарь
7.6. Заболевания языка
7.6. Заболевания языка
Поражение слизистой оболочки языка наряду с поражением других отделов полости рта наблюдается при многих стоматитах, однако есть заболевания, которые проявляются только на языке.
Десквамативный глоссит («географический» язык). Предполагают, что пятнистая десквамация эпителия спинки языка обусловлена нарушением нервной трофики, возможно, в связи с глистной инвазией, экссудативным диатезом, желудочно-кишечными и другими заболеваниями. Многие дети практически здоровы. Обычно такая десквамация выявляется уже на первом году жизни.
Клиническая
картина.
На спинке или боковой поверхности языка
появляется пятно беловато-желтого
или сероватого цвета вследствие набухания
и мацерации эпителия, последний вскоре
отторгается, оставляя участок слизистой
оболочки, на котором сохранены лишь
нижние слои эпителиального пласта.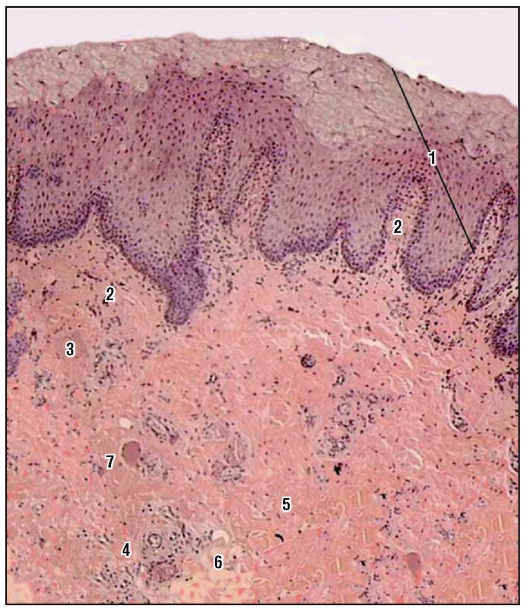
Рис. 7.18. Десквамативный глоссит.
Для «географического» языка характерны быстрое слущивание эпителия и быстрое, в течение 2—3 дней, восстановление величины нитевидных сосочков, поэтому рисунок на языке очень изменчив. Общее состояние ребенка не изменяется, болевых ощущений нет или они связаны с приемом раздражающей пищи.
Дифференцировать «географический» язык надо от десквамативных процессов на спинке языка, наблюдающихся при нарушении витаминного баланса, заболеваниях желудочно-кишечного тракта, эндокринной и нервной систем, при длительном приеме лекарств. В этих случаях характерно появление на языке обширных участков десквамации эпителия в виде полос и пятен, не меняющих своих очертаний в течение нескольких дней и недель и не имеющих по периферии типичного ободка, набухшего перед слущиванием эпителия. Восстановление эпителиального покрова происходит медленно в связи с улучшением общего состояния организма.
Лечение. Необходимо разъяснить родителям безопасность такого состояния языка. Болевые ощущения, сопровождающие у некоторых детей очаговую десквамацию, обычно прекращаются, вероятно, за счет улучшения трофика тканей через 4—5 дней от начала приема внутрь пантотената кальция (по 0,03—0,1 г 3 раза в день). Препарат принимают в течение месяца, при показаниях курс лечения можно повторять 2—3 раза в год.
Ромбовидный
глоссит. Это
заболевание встречается у детей
очень редко. По средней линии спинки
языка в заднем отделе имеется участок
ромбовидной формы, лишенный нитевидных
сосочков и потому выделяющийся на общем
фоне более яркой розовой окраской.
Лечение не требуется, но необходимо обследовать ребенка для выявления органной патологии.
Складчатый язык. Эта аномалия развития у детей младшего возраста встречается очень редко, главным образом при болезни Дауна. В препубертатном и пубертатном периодах вместе с ростом всего организма происходит увеличение размера языка за счет разрастания мышечного слоя. На поверхности языка появляются продольные и поперечные борозды, в глубине которых сохраняются нитевидные сосочки. Жалоб дети не предъявляют.
Дифференцировать складчатый язык нужно от трещин воспалительного характера (в последнем случае в глубине их определяется эрозирование ткани), а также от лим-фангиомы языка.
Лечение не требуется.
Черный «волосатый» язык. Эта патология обусловлена гиперплазией нитевидных сосочков языка, которые покрываются толстым роговым слоем и удлиняются от нескольких миллиметров до 1 см и более. Окраска сосочков темно-желтая, буро-коричневая, до черной. У детей эта патология встречается редко и обычно развивается после каких-либо заболеваний и приема антибиотиков. В соскобах с поверхности языка находят разнообразную микрофлору, в том числе и дрожжеподобные грибы, хотя клинических признаков молочницы обнаружить не удается. У детей понижен аппетит, старшие дети чувствуют разрастание сосочков как инородное тело на языке.
МОРФОЛОГИЧЕСКАЯ ТРАНСФОРМАЦИЯ КИШЕЧНОГО ТРАНСПЛАНТАТА ПОСЛЕ ЦИСТЭКТОМИИ С ОРТОТОПИЧЕСКОЙ ПЛАСТИКОЙ МОЧЕВОГО ПУЗЫРЯ | Ситдыкова
Аннотация
Введение. Неизученным является гистоморфологическое состояние и механизмы трансформации кишечного эпителия ортотопического мочевого пузыря.Цель исследования. Изучение морфологических адаптативно-компенсаторные изменений в стенке кишечного трансплантата (КТ) и их связь с гомеостазом на различных этапах после оперативного лечения.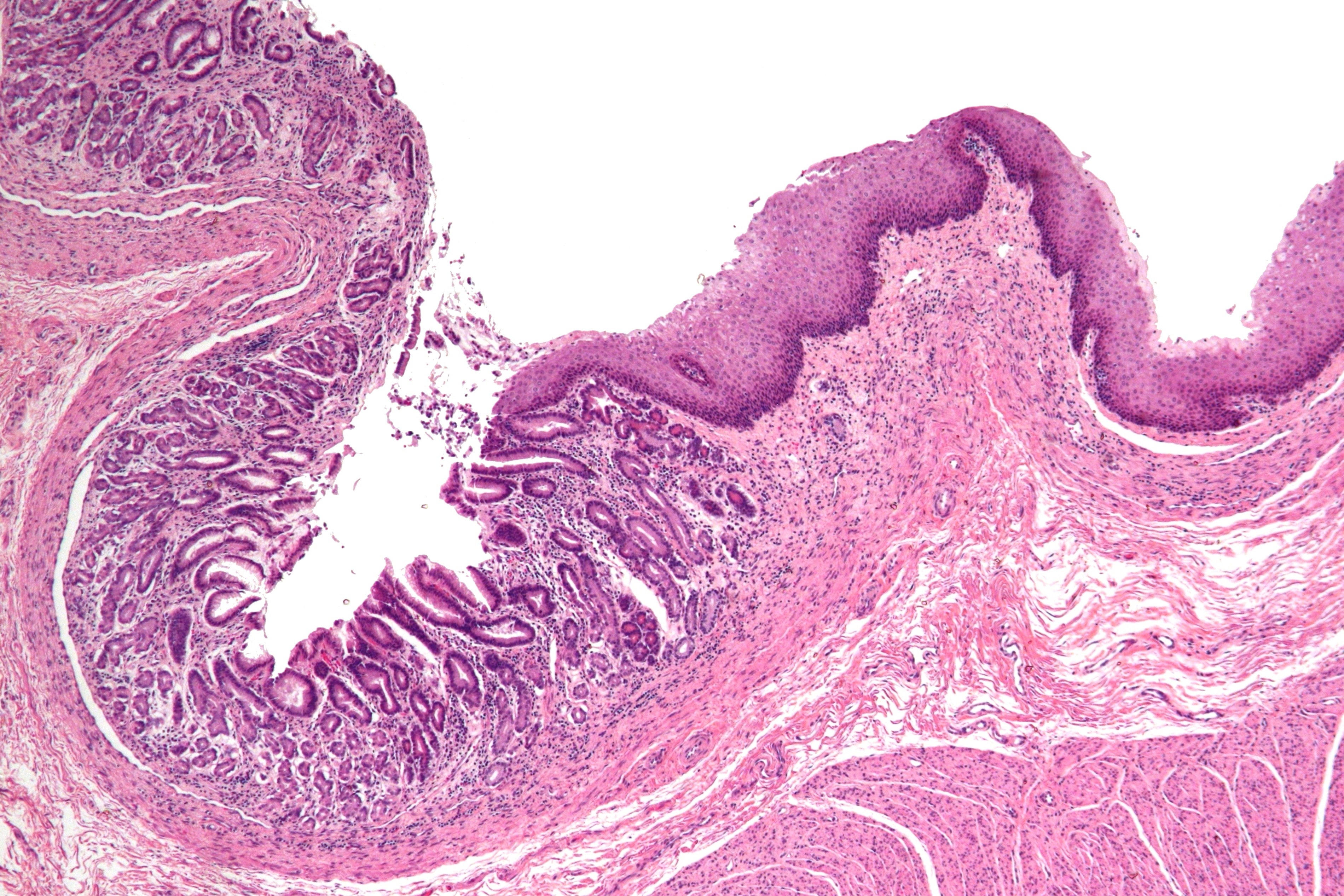
Материал и методы. Исследовано морфологическое состояние стенки кишечного трансплантата (КТ) у 42 больных, подвергшихся цистэктомии с формированием ортотопического кишечного мочевого пузыря (15-подвздошная кишка, 27 – сигмовидная) на сроках от 1,0 до 6,5 мес. и 1 года и более после оперативного лечения.
Результаты. Морфологические изменения, происходящие в стенке КТ начинаются с момента попадания в его просвет мочи, что происходит в сочетании с изменением стереотипной динамики органа. Выраженные изменения наблюдаются во всех отделах стенки тонкой и толстой кишки. Происходит регенерация и перестройка эпителия, выражающаяся в атрофии и уменьшении числа всасывающих цилиндрических клеток и увеличении количества слизеобразующих бокаловидных элементов, завершающаяся к 12 мес. и более после операции. Это в сочетании с уменьшением числа и размеров ворсин и крипт, редукцией лимфатического русла и склерозом кровеносных сосудов и стромы блокирует всасывание. Увеличение количества слизеобразующих бокаловидных клеток, обеспечивает создание барьера, защищающего слизистую КТ от воздействия мочи.
Заключение. Морфологические изменения, происходящие в стенке КТ под воздействием мочи, способствуют сохранению гомеостаза и являются идентичными при толсто- и тонкокишечном варианте пластики мочевого пузыря.
Раскрытие информации: Исследование не имело спонсорской поддержки. Авторы заявляют об отсутствии конфликта интересов.
Введение
Радикальная цистэктомия с лимфодис- секцией и различными видами кишечной деривации мочи является золотым стандартом лечения пациентов с мышечно-инвазивным раком мочевого пузыря [1]. Несмотря на достаточно большое количество клинических наблюдений больных после цистэктомии с формированием изолированного кишечного трансплантата, остается недостаточно неизученным гистоморфологическое состояние и механизмы трансформации кишечного эпителия ортотопического мочевого пузыря [2-5].
Цель исследования — изучение морфологических адаптативно-компенсаторные изменений в стенке кишечного трансплантата (КТ) и их связь с гомеостазом на различных этапах после оперативного лечения.
Материалы и методы
Исследовано морфологическое состояние стенки КТ у 42 больных, подвергшихся операции цистэктомии с формированием ортотопического кишечного мочевого пузыря (15-подвздошная кишка, 27 — сигмовидная) на сроках от 1 до 6,5 мес. и 1 года и более после операции. У всех пациентов использована оригинальная методика «создания «У»-образного, анти- или изоперистальтического артифициального кишечного мочевого пузыря из изолированного отрезка тонкого или толстого кишечника по методике Э.Н. Ситдыкова. Гистологический материал забирался путем эндоскопической «холодной» щипковой биопсии и исследовался с помощью окраски гематоксилином, эозином по Ван-Гизону и муцикармином.
Результаты
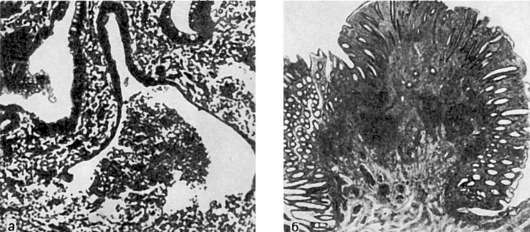
Изменения, происходящие в стенке КТ начинаются с момента попадания в его просвет необычного для кишки содержимого, т.е. мочи, что происходит в сочетании с изменением стереотипной динамики органа. Выраженные изменения наблюдаются во всех отделах стенки тонкой кишки. Эпителий практически отсутствует во всех полях зрения, а единичные клетки эпителиального покрова обнаруживаются лишь в глубине крипт (рис. 1).
Рисунок 1. Тонкокишечный трансплантат (3 месяца после операции). Некроз поверхностных отделов ворсин, десквамация эпителия, небольшие группы эпителиальных клеток в глубине крипт.
Figure 1. Small intestine graft (3 months after surgery). Necrosis of villi’s surface areas, desquamation of epithelium, small groups of epithelial cells in the depth of crypts.
В оставшихся клетках местами наблюдается пикноз ядер с их гиперхромией, набухание или уменьшение размеров цитоплазмы, в которой отмечаются явления вакуольной дистрофии. Значительная часть оставшихся клеток теряет связь с базальной мембраной, десквамируются и находятся вблизи неё. Количество кишечных ворсин неравномерно уменьшается, высота ворсин снижается, что сопровождается расширением основания. Они представляют собой небольшие холмообразные возвышения, причём крипты не определяются за счёт выравнивания собственной пластинки кишки. Подслизистый слой и строма ворсин несколько отёчны, что сопровождается спадением лимфатических сосудов. Кровеносные сосуды, напротив, полнокровны с выраженным периваскулярным отёком. По мере приближения к просвету кишки наблюдаются тромбозы сосудов, выраженные в зонах фибриноидных некрозов поверхностных отделов слизистой, местами достигая тотального поражения (рис. 2).
Количество кишечных ворсин неравномерно уменьшается, высота ворсин снижается, что сопровождается расширением основания. Они представляют собой небольшие холмообразные возвышения, причём крипты не определяются за счёт выравнивания собственной пластинки кишки. Подслизистый слой и строма ворсин несколько отёчны, что сопровождается спадением лимфатических сосудов. Кровеносные сосуды, напротив, полнокровны с выраженным периваскулярным отёком. По мере приближения к просвету кишки наблюдаются тромбозы сосудов, выраженные в зонах фибриноидных некрозов поверхностных отделов слизистой, местами достигая тотального поражения (рис. 2).
Рисунок 2. Тонкокишечный трансплантат (3 месяца после операции). Тромбоз кровеносного русла поверхностных отделов слизистой кишки.
Figure 2. Small intestinal graft (3 months after surgery). Thrombosis of the bloodstream in the superficial parts of the intestinal mucosa.
Строма ворсинок диффузно инфильтрирована с преобладанием плазмоцитов, лимфоцитов и макрофагов, с незначительным количеством эозинофилов и сегментоядерных лейкоцитов. Небольшая часть клеточного инфильтрата, диффузно располагается и в подслизистом слое, но число клеток вблизи базальной мембраны низкая, в мышечном слое встречаются лишь единичные лимфоидные элементы. С другой стороны, в подслизистом слое оказываются наиболее выраженные локальные лимфоидные скопления, местами формирующие очаги типа фолликулов без центров размножения.
Изменения, происходящие в стенке толстой кишки в период от 1 до 6,5 месяцев, имеют аналогичные по характеру и выраженности проявления, описанные в КТ, сформированном из тонкой кишки. Наблюдается выраженная десквамация эпителия слизистой оболочки в основном в апикальных отделах кишечных ворсин, сопровождающаяся некрозом стромы. У основания кишечных ворсин и криптах сохраняются небольшие пласты эпителия, а часть клеток здесь находится в состоянии некробиоза или некроза. Сами клетки меняют свои типичные продолговатые очертания и оказываются деформированными или округлыми. Эпителиальные клетки располагаются в виде монослоя цилиндрических клеточных элементов, среди которых нередки дистрофия и некрозы с полным разрушением слизистой (рис. 3).
Сами клетки меняют свои типичные продолговатые очертания и оказываются деформированными или округлыми. Эпителиальные клетки располагаются в виде монослоя цилиндрических клеточных элементов, среди которых нередки дистрофия и некрозы с полным разрушением слизистой (рис. 3).
Рисунок 3. Толстокишечный трансплантат (6 месяцев после операции). Десквамация эпителия поверхностных отделов слизистой уплощенной поверхности кишки.
Figure 3. Colon graft (6 months after surgery). Epithelium desquamation in the superficial parts of the gut’s mucosa flattened surface.
Высота ворсин снижается, а верхние отделы их уплощаются. В некоторых участках ворсины принимают горизонтальное положение, тесно прилегая одна к другой, образуя ровную внутреннюю поверхность. На отдельных участках наблюдаются фибриноидные некрозы, которые распространяются на большую глубину и захватывают расположенные поверхностно кровеносные сосуды, часть из которых тромбирована. Большое количество кровеносных сосудов в подслизистом слое гиперемировано, в то время как лимфатические капилляры, как правило, находятся в спавшемся состоянии. В участках разрушения поверхностных отделов слизистой в зонах некрозов наблюдается интенсивная лимфоидная инфильтрация. В других участках клеточная инфильтрация носит преимущественно диффузный характер и представлена лимфоцитами и макрофагами. В строме ворсин и подслизистом слое наблюдается выраженный отёк, менее заметный в мышечном слое.
На сроках более 12 месяцев после операции наблюдается постепенное восстановление слизистой тонкокишечного КТ. Целостная эпителиальная выстилка покрывает практически всю внутреннюю поверхность резервуара, и лишь апикальные отделы единичных ворсин оказываются лишенными эпителиального покрова в виде площадок. Слизистая представлена преимущественно бокаловидными клетками. Эти клетки имеют гиперхромные ядра, расположенные в базальном отделе и цитоплазму, расширенную в виде большой капли в апикальном отделе. Между слизистыми клетками располагаются цилиндрические всасывающие клетки, имеющие признаки атрофии. В апикальной части отдельных ворсин число таких атрофичных клеток значительно возрастает, и они образуют своеобразное клеточное покрытие в виде плотного слоя («частокол») веретеновидных клеточных элементов (рис. 4).
Между слизистыми клетками располагаются цилиндрические всасывающие клетки, имеющие признаки атрофии. В апикальной части отдельных ворсин число таких атрофичных клеток значительно возрастает, и они образуют своеобразное клеточное покрытие в виде плотного слоя («частокол») веретеновидных клеточных элементов (рис. 4).
Рисунок 4. Тонкокишечный трансплантат (12 месяцев после операции). Слой («частокол») веретеновидных цилиндрических клеток на утолщенной верхушке ворсины.
Figure 4. Small intestine graft (12 months after surgery). Layer («palisade») of fusiform cylindrical cells on a thickened apex of the villus.
В тоже время уплощенные апикальные отделы части ворсин оказываются лишенными эпителиального покрова. В этих участках нередко наблюдаются фибриноидные некрозы и тромбозы сосудов поверхностной зоны. Размеры ворсин, особенно их высота, заметно снижаются, что сопровождается уменьшением их поперечного размера. Соответственно снижается и число ворсин на единицу площади КТ.
Слизистая толстокишечного ортотопического мочевого пузыря через 12 месяцев восстанавливалась в большей части, лишь ламинарные отделы ворсин иногда оказывались лишенными эпителиальной выстилки. Клетки, выстилающие как поверхностные отделы, так и большую часть в глубине крипт, по своему морфологическому строению идентичны слизистым (бокаловидным) (рис. 5).
Рисунок 5. Толстокишечный трансплантат (12 месяцев после операции). Слизистые клетки, образующие выстилку кишечного резервуара.
Figure 5. Colon graft (12 months after surgery). Mucous cells that form the lining of the intestinal reservoir.
В строме ворсин и подслизистом слое с небольшим количеством рыхловолокнистой соединительной ткани диффузно располагаются единичные лимфоциты, макрофаги и лимфоидные фолликулы. Лимфатические сосуды не определяются, а количество кровеносных снижено и часть из них склерозирована и тромбирована в поверхностных отделах стенки КТ.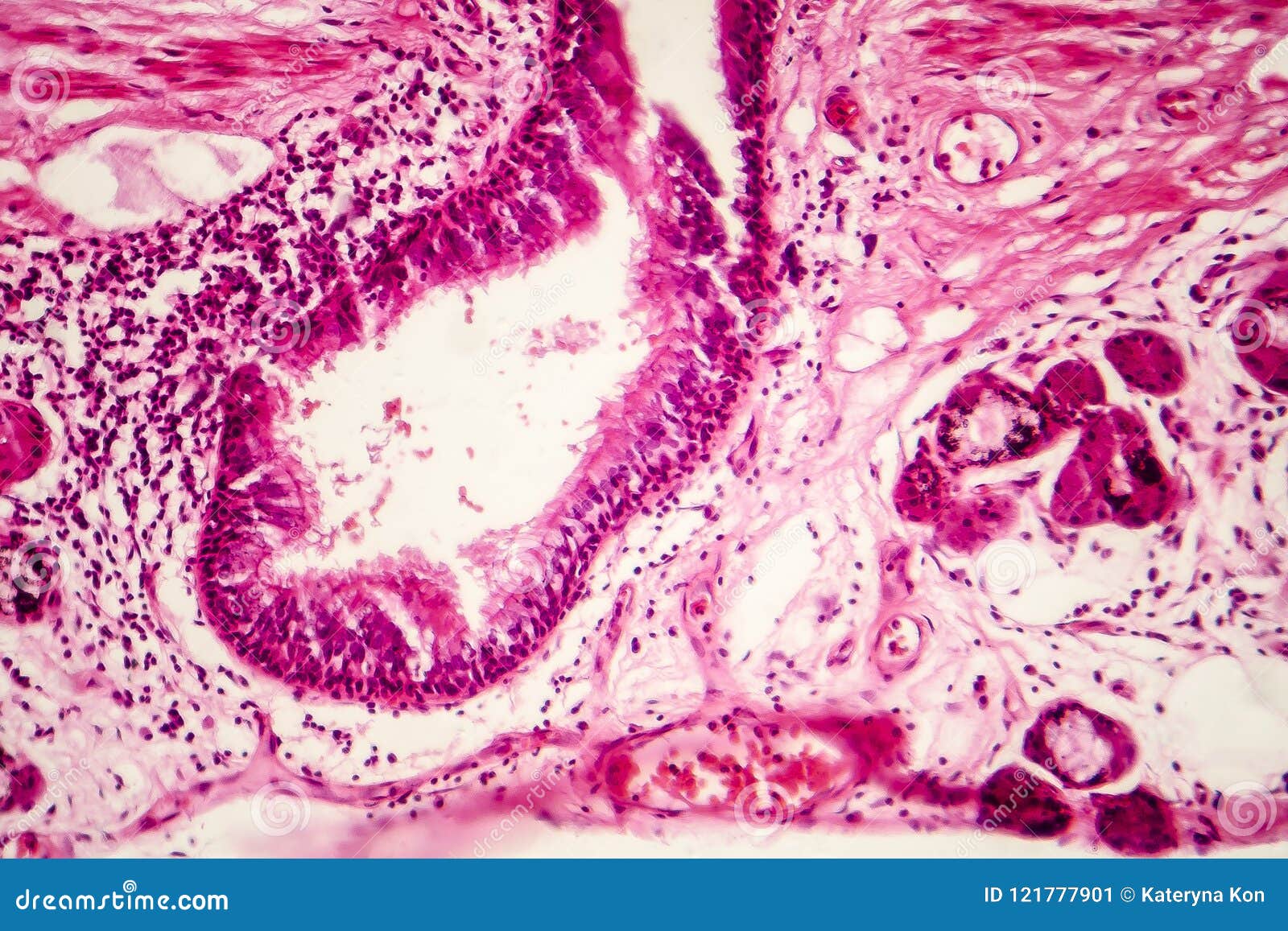 Мышечный слой не претерпевает значительных морфологических изменений, кроме небольшой атрофии мышечных элементов. В отдельных участках поверх уплощенных ворсин и кишечных ямок нарастает монослой из кишечного эпителия с большим количеством цилиндрических клеток (рис. 6).
Мышечный слой не претерпевает значительных морфологических изменений, кроме небольшой атрофии мышечных элементов. В отдельных участках поверх уплощенных ворсин и кишечных ямок нарастает монослой из кишечного эпителия с большим количеством цилиндрических клеток (рис. 6).
Рисунок 6. Толстокишечный трансплантат (12 месяцев после операции). Монослой цилиндрических клеток нарастающий на поверхность слизистой.
Figure 6. Colon graft (12 months after surgery). Monolayer of cylindrical cells are accrescenting on the mucosa surface.
Обнаруженные изменения идентичны острому альтеративно-десквамативному энтериту и колиту, что предполагает нарушение всасывания преимущественно за счет потери эпителиального покрова кишки. С другой стороны, резкое венозное полнокровие способствует не только нарушению всасывания, но и, напротив, может приводить к выделению определенного количества жидкости из стенки поврежденной кишки. Следовательно, уже на ранних этапах повреждение слизистой КТ сопровождается блокированием всасывания, что делает физиологичным выполнение им своих функций при определенных вторичных изменениях стенок.
Через год происходит регенерация и перестройка эпителия, выражающаяся в атрофии и уменьшении числа всасывающих цилиндрических клеток и увеличении количества слизеобразующих бокаловидных элементов. Это в сочетании с уменьшением числа и размеров ворсин и крипт, редукцией лимфатического русла и склерозом кровеносных сосудов и стромы блокирует всасывание. Увеличение количества слизеобразующих бокаловидных клеток, обеспечивает создание барьера, защищающего слизистую КТ от воздействия мочи.
Заключение
Морфологические изменения, происходящие в стенке КТ под воздействием мочи, способствуют сохранению гомеостаза и являются идентичными при толсто- и тонкокишечном варианте пластики мочевого пузыря.1. Рак мочевого пузыря (классика и новации). Под ред. Когана М.И. М.:Медфорум; 2017.
Рак мочевого пузыря (классика и новации). Под ред. Когана М.И. М.:Медфорум; 2017.
2. Цветов Е.П. Морфологические изменения трансплантата при кишечной пластике мочевого пузыря. Новый хирург. Архив. 1961;1:48-54.
3. Шахов Е.В. Гистологическая характеристика тонкокишечного трансплантата используемого для пластики мочевого пузыря в эксперименте. Материалы 2-го Всесоюз.симпозиума. Горький; 1973.
4. Комяков Б.К., Аничков Н.М., Бодарева Н.В. Морфологическая адаптация артифициального мочевого пузыря. Материалы Пленума РОУ. Краснодар, 2010.
5. Перепечай В.А. Оптимизация хирургического лечения мышечно-инвазивного и местнораспространенного рака мочевого пузыря. Дисc. …докт.мед.наук. Ростов-на-Дону. 2016:420.
6. Yuan J, Lin H, Li P, Zhang R, Luo A, Berardinelli F, Dai Y, Wang R. Molecular mechanisms of vacuum therapy in penile rehabilitaTIon: a novel animal study. EurUrol. 2010;58:773-80. DOI:10.1016/j.eururo.2010.07.005
7. Lin H, Yang W, Zhang J, Dai Y, Wang R. Penile rehabilitaTIon with a vacuum erecTIle device in an animal model is related to an anTIhypoxic mechanism: blood gas evidence. Asian J Androl. 2013;15:387. DOI:10.1038/aja.2013.18
8. Yuan J, Hoang A, Romero C, Lin H, Dai Y, Wang R. Vacuum therapy in erecTIle dysfuncTIon-science and clinical evidence. Int J Impot Res. 2010;22:211-9. DOI:10.1038/ijir.2010.4
Тактика терапевтического и хирургического лечения хронических поверхностных эрозий роговицы.
Авторы: Павлова Т. Н., Олейник В. В.,Ротанов Д.А., Научный консультант доцент Шилкин А.Г.
Ветеринарным врачам офтальмологам в клинической практике достаточно часто приходится встречаться с таким тяжелым и длительно протекающим заболеванием, как хронические поверхностные эрозии роговицы. Существуют различные названия у данного заболевания. Такие как: постоянные роговичные эрозии, возвратные эпителиальные эрозии, «ленивые» язвы, «неизлечимые» язвы боксеров и многие другие (Morgan R, Abrams K. A comparison of six different therapies for persistent corneal erosions in dogs and cats. Vet Comp Ophthalmol 1994 ). Впервые эта болезнь была описана у боксеров в 1965 г., но в настоящее время известны случаи заболевания у собак более 40 пород. Породная предрасположенность выявлена у боксеров, пекинесов, мопсов и стаффордширских терьеров, причем, как правило, боксеры и стаффордширские терьеры имеют более обширный дефект эпителия, чем пекинесы и мопсы. В большинстве случаев заболевание отмечается у животных старше 5 лет и не носит ярко выраженной сезонности. Также это заболевание встречается у кошек и лошадей, но регистрируется гораздо реже.
Клиническими признаками поверхностных эрозий роговицы на ранних стадиях являются роговичная триада (стойкий блефароспазм, эпифора, светобоязнь) и иногда пролапс третьего века. При хроническом течении заболевания проявления клинической картины заметно снижаются.
При биомикроскопии роговицы выявляются участки отслоившегося поверхностного эпителия на границе патологического и здорового участка, при этом целостность стромы роговицы сохранена, повреждения её тканей не наблюдается. На ранних стадиях поверхностные слои роговицы остаются неизменными или несколько отечными. При длительном течении процесса обнаженный слой стромы имеет склонность к дегенерации. Молодые эпителиальные клетки обладают низкими адгезивными свойствами к поврежденной строме, что приводит к рецидивам эрозии. При окраске раствором флуоресцеина натрия наблюдается не только зеленое окрашивание зоны дефекта, но и окрашивание отслоенного роговичного эпителия, степень и характер которого служит своеобразным прогностическим тестом скорости возможной регенерации.
Сложность хронических поверхностных эрозий роговицы заключается в низкой эффективности медикаментозного лечения и высоком проценте рецидивов.
Задачами нашей работы было:
- Проанализировать патогенез хронических эрозий роговицы;
- Изучить различные методы лечения;
- Подобрать оптимальную схему медикаментозного лечения роговичных эрозий.
- Определить технику хирургического вмешательства эрозий роговицы не поддающихся медикаментозной терапии.
Патогенез хронических эрозий роговицы.
Патогенез стойкой эрозии роговицы до сих пор до конца не изучен. В обычных условиях клетки эпителия роговицы плотно крепятся к подлежащей базальной мембране с помощью клеточных контактов – полидесмосом. ( Kirschner S. Persistent Corneal Ulcers: What to do when ulcers wont heal? Vet Clin N Am 1990). Известно, что у некоторых страдающих стойкой эрозией роговицы животных их количество на клетках эпителия снижено, в структуре базальной мембраны имеются нарушения. Таким образом, нормальная адгезия клеток эпителия роговицы к строме нарушается из-за дефектов в базальной части клеток или в самой строме. При анализе пораженных эрозией поперечных срезов роговицы методом световой микроскопии, легко выявляются участки отслоения эпителия. В некоторых случаях базальная мембрана эпителия роговицы не изменяется, но базальные клетки разбухают, между ними появляются заполненные жидкостью промежутки, накапливается мембраноподобный материал. В других случаях ясно заметны аномалии структуры базальной мембраны эпителия и резко сниженное число полидесмосом. . ( Gelatt K., Samuelson D. Recurrent corneal erosions and epithelial dystrophy in the Boxer dog. J Am Anim Hosp Assoc 1982)
Другие исследователи, анализируя патогенез развития поверхностных эрозий, пришли к выводу, что ведущим компонентом является нейротрофическая дистрофия стромы роговицы. ( Murphy CJ, Marfurt CF, McDermott A, et al. Spontaneous chronic corneal epithelial defects in dogs: Clinical features, innervation,and effect of topical SP,with or without IGF-1. Invest Ophthalmol Vis Sci 2001).
Invest Ophthalmol Vis Sci 2001).
Методы лечения.
Существует множество различных методов лечения стойких эрозий роговицы – от медикаментозных до хирургических.
Для лечения хронических эрозий в ветеринарной практике в некоторых случаях применяют эпидермальный фактор роста, аспротинин (ингибитор плазмина и других сериновых протеаз), сыворотку крови пациента, спленопид (противовоспалительный и иммуномодулирующий эффект). В гуманитарной офтальмологии на сегодняшний день для лечения этого заболевания используют мягкие контактные линзы, субконъюнктивальные блокады тауфона, местные инстиляции пилокарпина, периферические плазменные потоки газа оксида азота. В качестве хирургического лечения применяют покрытие из амниона, переднюю послойную инвертную кератопластику, пересадку прямых мышц глаза.
Мы со своей стороны придерживаемся более классических методов лечения длительно незаживающих эрозий роговицы.
В качестве медикаментозной терапии мы используем комбинацию антимикробных препаратов фторхинолонового ряда (Ципровет, Вигамокс, Зимар) в сочетании с препаратами, улучшающими питание роговицы (Баларпан, Оквис, Витасик, Корнерегель), а также с местными иммуностимулирующими препаратами (Полудан, Реаферон). Антибиотики назначаются с целью профилактики вторичного воспаления. При диагностировании эрозии без явного септического компонента назначаются антисептики: Витабакт, Окомистин. Если десквамация роговичного эпителия наблюдается на обширном участке («сползает чулком»), то назначаем препараты обладающие дубящим эффектом (цинка сульфат с борной кислотой). Обнаружить обширную десквамацию можно по прониканию раствора флуоресцеина между эпителием и стромой роговицы.
При выраженной отечности стромы и эпителия роговицы, в некоторых случаях, назначаем дексаметазон в разведении от 1:1 до 1:10 в зависимости от клинической картины, кратким курсом при ежедневном контроле. Назначение мазей (Тетрациклин, Колбиоцин, Флоксал) на наш взгляд нецелесообразно, так как их применение в значительной степени снижает перенос кислорода и несколько угнетает окислительно- востановительные процессы в тканях роговицы, что в свою очередь приводит к дегенерации волокон стромы, тем самым затягивая стоки эпителизации дефекта.
Наиболее опасны эрозии роговицы с активной десквамацией эпителия. При этом обширные эрозии (больше шести миллиметров) с плотной адгезией эпителия по краям дефекта роговицы, имеют лучшие шансы на заживление без хирургии, чем маленькие эрозии ( меньше 5 миллиметров) с плохо прилегающим эпителием.
Помимо медикаментозной терапии, в некоторых случаях мы применяли методику туширования эпителиального дефекта спиртовым раствором бриллиантового зеленого или спиртовым раствором йода 5%, с целью активизации петлистой сосудистой сети и улучшения трофики роговицы .Процедура проводится следующим образом: после проведения местной анестезиии роговичным шпателем от периферии к центру удаляли некротизированный эпителий, и затем тушировали эрозированную поверхность ватным тампоном, пропитанным спиртовым раствором бриллиантового зеленого или спиртовым раствором йода 5%. Данную манипуляцию целесообразно проводить не более 2-х раз. В случае отсутствия положительной динамики необходимо оперировать животных. Метод туширования роговицы используем редко, так как в 25% случаев наблюдается обратный эффект –химический ожег роговицы или увеличение размера эрозии. Как правило эту манипуляцию производим пожилым животным, которым противопоказана общая анестезия.
При отсутствии положительной динамики в течение 7 дней после проведения медикаментозной терапии и туширования эрозии требуется хирургическое лечение. На наш взгляд затягивание хирургии негативно сказывается на состоянии
роговицы и приводит к её дегенерации, что провоцирует к ухудшению приживления трансплантата.
Хирургические методы лечения:
Мы в своей практике используем несколько методов хирургического лечения, таких как сетчатая кератотомия, трансплантация биотрансплантата фирмы Cook, аллопланта и конъюнктивального лоскута на ножке.
Сетчатая кератотомия. Принцип метода. Во многих иностранных источниках эту процедуру рекомендуют проводить под местной анестезией, но по нашему мнению данная манипуляция связана со значительным риском неконтролируемого повреждения роговицы. Для предотвращения осложнений, данную процедуру проводим под общей анестезией. Все манипуляции на пораженном глазу осуществляли под операционным микроскопом. На первом этапе производили удаление некротизированного эпителия под большим увеличением микроскопа кратного 16, затем с помощью роговичного шпателя наносим насечки сначала в горизонтальном затем в вертикальном направлении на расстоянии 1 мм. Нежелательно для этой манипуляции использовать лезвие, которое прорезает волокна стромы роговицы, что во первых ухудшает регенерацию роговичных тканей, а в после операционном периоде приводит к образованию грубых рубцов роговицы. Операция завершается тушированием оперированной поверхности раствором бриллиантового зеленого. Послеоперационный период составляет 14-16 дней. Сетчатую кератотомию мы используем в случае отсутствия выраженного отека стромы роговицы . Цель данной операции заключается в удалении «больных или усталых» клеток по краям эпителиального дефекта, что способствует усилению функции деления кератоцитов за счет репаративного ответа после травмы, и регенерации клеток эпителия.
Для предотвращения осложнений, данную процедуру проводим под общей анестезией. Все манипуляции на пораженном глазу осуществляли под операционным микроскопом. На первом этапе производили удаление некротизированного эпителия под большим увеличением микроскопа кратного 16, затем с помощью роговичного шпателя наносим насечки сначала в горизонтальном затем в вертикальном направлении на расстоянии 1 мм. Нежелательно для этой манипуляции использовать лезвие, которое прорезает волокна стромы роговицы, что во первых ухудшает регенерацию роговичных тканей, а в после операционном периоде приводит к образованию грубых рубцов роговицы. Операция завершается тушированием оперированной поверхности раствором бриллиантового зеленого. Послеоперационный период составляет 14-16 дней. Сетчатую кератотомию мы используем в случае отсутствия выраженного отека стромы роговицы . Цель данной операции заключается в удалении «больных или усталых» клеток по краям эпителиального дефекта, что способствует усилению функции деления кератоцитов за счет репаративного ответа после травмы, и регенерации клеток эпителия.
Если вышеописанная манипуляция не приводит к эпителизации дефекта, то единственным методом остается проведение передней послойной кератопластики с применением конъюнктивального лоскута на ножке, аллопланта или биотрансплантата толщиной 50 мкр фирмы СооК .
От выбора материала для трансплантации зависит скорость приживления и оптический результат после операции. Все вышеперечисленные материалы имеют свои преимущества и недостатки.
Всего за период с 2004 по 2012 года нами было прооперированно 67 собак и кошек разных половозрастных групп.
- Биотрасплантат Сооk
- Аллоплант
- Конъюнктивальный лоскут на ножке
- Собак 40
- Собак 4
- Собак 10
- Кошек 7
- Кошек 1
- Кошек 5
Наиболее оптимальным по нашим наблюдениям является биотрансплантат фирмы Соок (для данной операции использовали трансплантат толщиной 50 мкр, наиболее тонкий в линейке трансплантатов Соок). Операции проводили по стандартной методике. Диаметр трансплантата варьировал от 5 до 10 мм. Операции и послеоперационный период протекали без особенностей и осложнений не отмечалось. Снятие швов проводили через 14-20 дней.
Операции проводили по стандартной методике. Диаметр трансплантата варьировал от 5 до 10 мм. Операции и послеоперационный период протекали без особенностей и осложнений не отмечалось. Снятие швов проводили через 14-20 дней.
Результаты.
Приживление конъюнктивального лоскута отмечалось у 100% прооперированных животных (15 животных:10 собак, 5 кошей) , но недостатком этого материала являлется образование выраженного помутнения роговицы в зоне пересадки , что значительно снижением оптические функции глаза.
После применения аллопланта у 5 животных (4 собак, 1 кошек) мы получили следующие результаты:
- у 2 животных произошло резорбирование трансплантата, что потребовало дополнительного медикаментозного лечения, тем самым удлинив срок лечения, и эпителизация соответственно наступила в сроки от 3 до 5 недель;
- у 1 животного произошло резорбирование трансплантата и углубление язвенного дефекта, что в дальнейшем потребовало пересадки биотрансплантата фирмы Соок;
- у 2 животных послеоперационный период протекал без осложненией и в результате получили практически полное восстановление прозрачности роговицы.
- Аллоплант имеет неплохое приживление, но принимая во внимание высокую стоимость аллопланта и при этом гарантии отсутствия осложнений, является ограничивающим фактором в использовании данного материала.
После применения биотрансплантата фирмы Соок у 47 животных ( 40 собак, 7 кошек) мы получили следующие результаты:
- У 10 животных с обширными эрозиями более 6 мм, произошло частичное преждевременное резорбирование центральной зоны трансплантата, что потребовало дополнительной медикаментозной терапии и увеличило срок восстановления роговицы до 5-6 недель;
- У 31 животного произошло полное приживление и биодеструкция трансплантата. Роговица восстановила свою оптическую прозрачность.
- У 6 животных произошло полное приживление, но в области трансплантации незначительно отмечается незначительное помутнение в виде облачка ,что несколько снижает оптические функции глаза.

Выводы.
Лечение эрозий роговицы должно быть последовательно и дифференцированно. На первом этапе лечения назначается медикаментозная терапия . Отсутствие положительной динамики в течение 7 дней является показанием к проведению хирургической операции – сетчатой кератэктомии. При выраженной деструкции поверхностных роговичных слоев и рецидивировании процесса после сетчатой кератотомии единственным методом лечения является кератопластика. Мы считаем, что самые лучшие результаты были получены после проведения трансплантации с применением биотрансплантата фирмы Соок (50 мкр).
SUMMARY
Tactics of therapeutic and surgical treatment of chronic superficial erosion of a cornea.
Pavlova T. N, OlejnikV.V. Rotanov D.A.
The scientific adviser senior lecturer Shilkin A.G.
The center of veterinary ophthalmology of doctor Shilkina A.G., Moscow .
The resume. In theses techniques of conservative and surgical treatment of chronic ulcers of a cornea which are used in our clinic are reflected.
Заболевания шейки матки. Виды заболеваний. Диагностика и лечение.
I. Экзо – и эндоцервициты
Это воспаление слизистой оболочки экзо – и эндоцервикса, причиной которого может быть как условно-патогенная микрофлора (стрептококки, стафилококки, кишечная палочка), так и урогенитальная инфекция (мико-, уреаплазмоз, трихомониаз, хламидиоз, вирусные инфекции).
Специфических клинических симптомов воспаления не существует, чаще всего заболевание проявляется появлением более обильных выделений из половых путей (бели), очень редко тупыми болями внизу живота, связанными в основном с сопутствующими заболеваниями (уретрит, цистит).
Диагностика
При гинекологическом осмотре обнаруживается гиперемия вокруг наружного зева, слизистые или гнойные выделения.
Кольпоскопия помогает не только диагностировать цервицит, но иногда и уточнить его этиологию.
Так по кольпоскопической картине можно дифференцировать воспаление хламидийной, вирусной, кандидозной и трихомонадной этиологии.
При трихоманадном цервиците, наблюдается так называемый симптом «земляничного цервикса», когда на шейки при кольпоскопии визуализируются мелкие петехиальные кровоизлияния.
Трихомонадный диффузный цервицит
Кандидозный цервицит сопровождается чередованием «шероховатых» зон с «лакированной» поверхностью, а так же появлением типичных творожистых выделений на шейки и стенках влагалища.
Кандидозный цервицит
Типичным симптомом вирусного цервицита является симптом «большой эрозии», когда вся поверхность шейки матки ярко-красного цвета с изъявлениями.
Хламидийный цервицит сопровождается отеком эктопированого цилиндрического эпителия, очагами некроза и изъязвления, слизисто-гноевидными выделениями.
Для уточнения этиологии воспаления так же необходимо сдать мазок на флору, бак посев и чувствительность к антибиотикам из цервикального канала, соскоб на урогенитальную инфекцию методом ПЦР и РАР-тест для исключения фоновых и предраковых заболеваний.
Лечение зависит от возбудителя, вызвавшего воспаление и его чувствительности к антибиотикам.
Учитывая то, что чаще всего причиной являются несколько возбудителей, в лечении используют препараты местного действия, обладающие противовоспалительным, антибактериальным и противогрибковым эффектом (Полижинакс, Тержинан, Клион-Д, Бетадин).
При гонорейной, трихомонадной, герпетической этиологии цервицита в комплексе используют пероральные антибактериальные или противовирусные препараты.
II. Истинная эрозия шейки матки
Довольно часто врачи используют термин «эрозия шейки матки», тем самым обозначая, отклонения от нормы при осмотре невооруженным глазом. В основном эти «отклонения» оказываются обычной эктопией или псевдоэрозией.
Истинная эрозия — это нарушение целостности эпителия (язва) и в репродуктивном периоде встречается редко.
При этом происходит дистрофия и десквамация многослойного плоского эпителия с обнажением подэпителиальной стромы.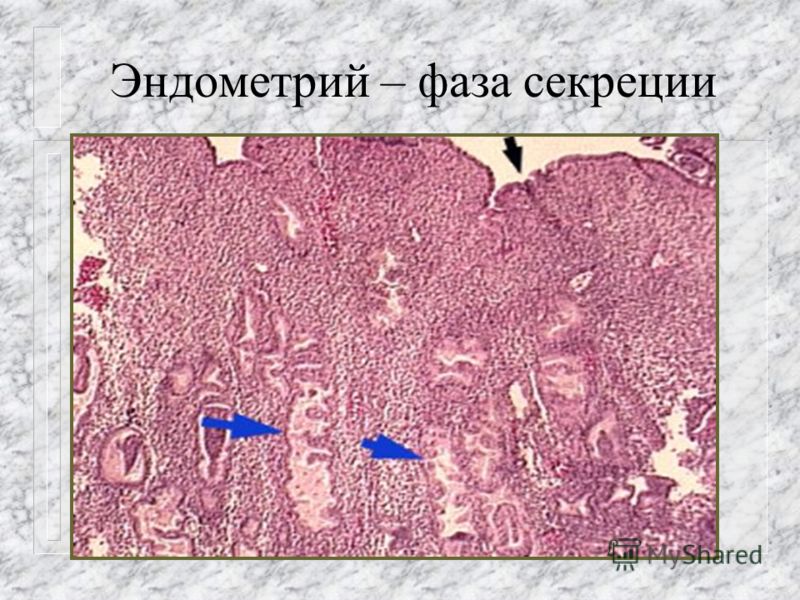
Причины истинной эрозии шейки матки.
1. Воспалительный процесс. Длительные выделения при кольпитах и цервицитах различной этиологии приводят к патологическим изменениям слизистой шейки матки, повышению проницаемости эпителия для микроорганизмов, его дистрофии и десквамации.
2. Травмы шейки матки. Механические повреждения шейки матки в родах и патологическая реакция на шовный материал, используемый для реконструкции разрывов, травматизация шейки матки зеркалами при осмотре могут быть одной из причин появления истинной эрозии шейки матки.
3. Ожоги шейки матки. После лечения шейки матки различными методиками (химио-, электро-, криодестукция), как правило, происходит отторжения струпа, в результате чего образуется эрозивная поверхность, которая постепенно эпителизируется.
4. Трофические нарушения. Группой риска для возникновения этого заболевания является пациентки с выпадением матки, когда ткани трамируются о белье, а также пациентки после лучевой терапии.
5. Гормональный дисбаланс. Немалую роль в появлении истинной эрозий играет дефицит женских половых гормонов в постменопаузе. Недостаток эстрагенов приводит к истончению слизистой, снижению секреции желез, сухости и, как следствие, ткани становятся более ранимыми.
6. Другие причины. Нарушения иммунитета, аллергические реакции, авитаминозы и нехватка минеральных веществ также могут способствовать появлению эрозии.
При кольпоскопии истинная эрозия выглядит, как дефект эпителия с четкими краями и неровным, бугристым дном.
В норме, если исключить воспалительный процесс поддерживающий эрозию, через 1-2 недели она начинает эпителизироваться.
Поэтому основным методом лечения, как истинной эрозии, является устранение воспалительного компонента. При лечении истинной эрозии шейки в постменопаузе используют комбинированное лечение, включающее исключение травмирующего фактора, противоспалительную и гормональную терапию.
Не стоит забывать о цитологическом исследовании шейки матки перед лечением, для исключения более серьезной патологии.
Подробнее об эрозии шейки матки: причины, симптомы, диагностика, лечение.
III. Лейкоплакия шейки матки
Это поражение слизистой экзоцервикса, заключающееся в утолщении слизистой и нарушении процессов её ороговения, при этом на поверхности шейки матки образуются белые пленки или бляшки, плоские или возвышающиеся над поверхностью.
Виды
При кольпоскопии выделяют три формы лейкоплакии шейки матки:
- плоская лейкоплакия – белесоватые участки находятся на одном уровне с нормальным многослойным плоским эпителием;
- бородавчатая лейкоплакия – поверхность шейки матки выглядит бугристой за счет наслоения пораженных участков друг на друга и возвышения их над поверхностью;
- эрозивная лейкоплакия – при кольпоскопии помимо лейкоплакии на шейке матки в пораженной зоне определяются эрозивные участки или трещины.
По гистологическому заключению выделяют простую лейкоплакию шейки матки (или без атипии) и лейкоплакию с атипией.
Простая лейкоплакия характеризуется утолщением базального и зернистого слоя многослойного плоского эпителия и явлениями паракератоза.
Причина этого процесса до конца не выяснена, но среди возможных причин выделяют нарушение гормонального фона женщины, травмы шейки матки, инфекционные и химические факторы.
Лейкоплакия с атипией относится к предраковым заболеваниям и заключается в появление базально-клеточной гиперактивности и атипичных клеток. В 15-75% случаев она может переходить в преинвазивный плоскоклеточный рак.
Кольпоскопия в этом случае не позволяет точно дифференцировать заболевание.
Единственным методом диагностики является цитологическое, а лучше гистологическое исследование.
Для этого проводят РАР-тест или биопсию участка лейкоплакии.
При подтверждении простой лейкоплакии на гистологическом уровне, никакого лечения не требуется, кроме наблюдения и проведения РАР-теста раз в год.
При обнаружении атипичных клеток при гистологическом исследовании, методом лечения является радиоволновое «прижигание» лейкоплакии на шейке матке на 5-7 день менструального цикла, в запущенных случаях применяется конизация шейки матки.
Применение тампонов с облепиховым маслом, алоэ и шиповником не допустимо, т.к. провоцирует бурный рост злокачественных клеток!
IV. Эндометриоз шейки матки
По данным литературы почти в 20% случаев эндометриоз шейки матки является результатом диатермокоагуляции. Так же некоторые исследователи к причинам развития эндометриоза шейки матки относят пластические операции, аборты и роды. Предполагают, что эндометрий внедряется в поврежденную слизистую шейки матки, формируя очаги гетеротопии.
При локализации эндометриоза только на влагалищной части шейки матки, заболевание может протекать бессимптомно, либо сопровождаться появлением мажущих темно-коричневых выделений до и после менструации.
При внедрении эндометриоидных очагов в слизистую цервикального канала присоединяется болевой синдром, меняющий свою интенсивность в зависимости от фазы цикла.
При кольпоскопии очаги эндометриоза выглядят, как кисты красноватого цвета, размерами до 5 мм, а в дни менструации они увеличиваются в размере и становятся багрово-синюшными.
Также перед лечением необходимо провести биопсию очагов с гистологическим заключением, для исключения злокачественных процессов.
Радикальным методом лечения эндометриоза шейки матки, так же как и других форм этого заболевания, является хирургический. На 6-7 день цикла проводят лазерную или радиоволновую деструкцию очагов.
Рецидив заболевания после этого встречается крайне редко.
V. Предраковые заболевания шейки матки
Рак шейки матки по данным литературы занимает 3-е место среди злокачественных заболеваний репродуктивной системы у женщин. Ежегодно регистрируется до 500000 новых случаев рака шейки матки в мире.
Но рак возникает не молниеносно, проходят десятки лет, прежде чем предрак перейдет в злокачественный процесс. Его можно предотвратить, если вовремя диагностировать и пролечить предраковые изменения.
Сложность в диагностике заключается в том, что даже выраженный процесс протекает бессимптомно, поэтому так важно проходить обследование у гинеколога хотя бы раз в год.
Многие исследования доказывают, что формирование предраковых процессов начинается с инфицирования вирусом папилломы человека, который впоследствии нарушает структурное строение клеток, больше всего затрагивая ядра клеток.
Кондиломы
По классификации Bethesda system их относят к LSIL (плоскоклеточные интраэпителиальные поражения низкой степени значимости).
Кондиломы возникают в результате папилломовирусной инфекции и представляют собой разрастания соединительной ткани, покрытой многослойным плоским эпителием.
Выделяют остроконечные и плоские кондиломы.
Плоские кондиломы в 10% случаев могут малигнизироваться в течение 2-х лет, они незаметны невооруженным глазом и диагностируются при расширенной кольпоскопии.
Лечение кондилом заключается в лазерной хирургии пораженных очагов с дальнейшей противовирусной и иммуномодулирующей терапией.
Дисплазия легкой степени (CIN I)Изменения структуры клеток затрагивают только нижние слои многослойного плоского эпителия.
Как правило, эти изменения возникают вследствие воспалительного процесса и, либо проходят после противовоспалительной терапии, либо регрессируют сами.
В 10-15% случаев могут переходить в дисплазию средней степени.
Дисплазия средней степени (CIN II)Характеризуются тем, что изменения в клетках затрагивают уже более высокие слои.
В 20% случаев переходит в CIN III, а в 5% может переходить в рак шейки матки.
Дисплазия тяжелой степени (CIN III) и рак in situПри CIN III изменения в клетках характеризуются появлением больших ядер или нескольких ядер на всех пластах слизистой. Лишь в самых поверхностных слоях можно обнаружить признаки созревания и дифференцировки нормальных клеток.
При раке in situ клетки по структуре не отличаются от раковых, но эти изменения ещё не вышли за пределы слизистой оболочки.
Учитывая то, что разные степени дисплазии могут сочетаться, для уточнения стадии и перед лечением необходимо проводить прицельную биопсию подозрительных участков с последующим гистологическим исследованием.
Лечение
При CIN I-II лечение начинают с противовоспалительных препаратов с последующим повторным цитологическим исследованием через 2-е недели.
Также при обнаружении папилломовирусной инфекции в комплексе можно использовать противовирусную и иммуномодулирующую терапию.
Если при повторном исследовании изменения сохраняются, проводят лазерную коагуляцию шейки матки, как наиболее эффективный метод лечения.
Это амбулаторная процедура, проводимая на 4-7 день цикла. Полная эпителизация коагулированной поверхности наступает через 4-6 недель после процедуры.
В последующем необходимо динамическое наблюдение с цитологическим исследованием раз в 6 месяцев.
При CIN III и раке in situ выжидательная тактика неприемлема, необходимо сразу проводить конизацию шейки матки – ампутация шейки матки с последующим гистологическим исследованием материала.
Процедура проводится в стационаре под наркозом. При этом можно использовать различные методики: радиоволновая, лазерная, электрохирургическая или просто хирургическая.
Недостатком лазерной методики является то, что происходит обугливание краев материала, что затрудняет дальнейшую диагностику, но при этом риск развития кровотечения значительно ниже, чем после использования хирургического метода.
В последние годы широко применяют радиоволновой или аргоноплазменный метод с помощью специальной петли, который устраняет оба эти недостатка.
После проведения манипуляции также необходимо диспансерное наблюдение 1 р в 3 месяца.
Подробнее о дисплазии шейки матки: классификация, причины, симптомы, диагностика и лечение.
VI. Рак шейки матки
Клинические симптомы появляются только на поздних стадиях, на ранних — заболевание протекает бессимптомно!
При этом все симптомы неспецифичны и могут быть признаком множества других гинекологических заболеваний.
Наиболее часто появляются жалобы на:
- Кровотечения после полового акта, осмотра гинеколога
- Кровянистые выделения в постменопаузе
- Изменение продолжительности и характера менструаций
- Боли или дискомфорт внизу живота
Поэтому диагностика рака шейки матки столь затруднительна. Основными методами ранней диагностики заболевания являются систематическое прохождение РАР-теста и кольпоскопии.
Лечение заключается в комплексном применении хирургических, лучевых и химиотерапевтических мероприятий.
Хирургическое лечение, в настоящее время, заключается в более щадящей, по сравнению с операцией Вертгейма-Мейгса, гистерэктомии – удалении матки с шейкой. Вопрос о придатках решают индивидуально, в зависимости от возраста и распространенности процесса.
В последние годы, все больше исследований доказывает более эффективное применение совместно лучевой и химиотерапии. Хотя такое лечение приводит к более тяжелым осложнениям и труднее переносится пациентками.
Прогноз при этом заболевании достаточно благоприятный. На ранних стадиях 5-ая выживаемость составляет более 90%, при второй-третьей стадии от 30 до 60%, а при четвертой около 10%.
Изменения эпителиальной выстилки конъюнктивы при непереносимости контактных линз по данным импрессионной цитологии | Егорова Г.Б., Федоров А.А., Митичкина Т.С., Шамсудинова А.Р.
Резюме Цель: изучить состояние эпителиальной выстилки конъюнктивы при непереносимости контактных линз (КЛ) и неэффективности традиционных методов медикаментозной коррекции (слезозаменители, корнеопротекторы).
Цель: изучить состояние эпителиальной выстилки конъюнктивы при непереносимости контактных линз (КЛ) и неэффективности традиционных методов медикаментозной коррекции (слезозаменители, корнеопротекторы).Методы исследования: было обследовано 16 пациентов с миопией, кератоконусом III-IV стадии, вторичными эктазиями после кераторефракционных операций, дистрофией роговицы. У всех пациентов непереносимость КЛ сочеталась с признаками синдрома «сухого глаза». Для оценки состояния эпителия конъюнктивы век был использован модифицированный метод импрессионной цитологии.
Результаты: при анализе полученных отпечатков эпителия выявлены признаки выраженной плоскоклеточной метаплазии эпителиоцитов, локальной, а затем и диффузной дистрофии, а также признаки аллергической и воспалительной реакций.
Заключение: длительное ношение КЛ может явиться фактором риска возникновения осложнений, особенно у пациентов с наиболее сложной патологией роговицы. Алгоритм лечения должен включать слезозаменители, эпителиотропные, антисептические, противоаллергические средства.
Ключевые слова: контактные линзы, эпителий конъюнктивы, импрессионная цитология.
Abstract
Changes of conjunvtival epithelial layer in patients with intolerance of contact lenses according to a data
of impression cytology
G.B. Egorova, A.A. Fedorov,
T.S. Mitichkina, A.R. Shamsutdinova
FGBU NII of Eye Diseases RAMN, Moscow
Purpose: to study a condition of conjunctival epithelial layer in patients with intolerance of contact lenses (CL) and absence of standard medical treatment ( tear substitutes, corneoprotectors).
Methods: Patients with myopia, keratoconus of III-IV stages, secondary ecstasies after keratorefractive surgery, corneal dystrophies were examined. In all patients intolerance of contact lenses was combined with symptoms of dry eye syndrome. For evaluation of a condition of a conjunctival epithelium impression cytology method was applied.
Results: 16 patients were enrolled into the study. Analysis of epithelium imprints showed a signs of evident squamous metaplasia of epithelial cells, local and diffuse dystrophy. There were also signs of allergic and inflammatory reactions registered.
Conclusion: Prolonged wearing of CL could be a risk factor of complications, particularly in patients with complex corneal pathology. Treatment should include tear substitutes, epithelioropic, antiseptic, antiallergic drugs.
Key words: contact lenses, conjunctival epithelium, impression cytology.
Видимая поверхность глаза представлена передним эпителием роговицы, в области лимба переходящим в эпителий бульбарной конъюнктивы. В соответствии с функциональными особенностями этих двух поверхностей имеются существенные различия в структуре их покровного эпителия.
Эпителий, покрывающий поверхность роговицы, представлен 5–6 слоями клеток неороговевающего эпителия. Клетки базального слоя мигрируют из лимбальной ростковой зоны к центру, продолжая делиться. В процессе дифференцировки они перемещаются кнаружи, образуя слои крыловидных и плоских клеток. Свободная поверхность плоских клеток содержит микроворсинки для удержания муцинового слоя прекорнеальной слезной пленки. По мере отмирания эти клетки десквамируются и удаляются с током слезы.
Бульбарная конъюнктива покрыта многослойным плоским неороговевающим эпителием с включениями из бокаловидных клеток, секретирующих муцин. Вблизи лимба роговицы эпителий конъюнктивы без резкой границы переходит в передний эпителий роговицы. Эпителиальная выстилка глазной поверхности во взаимодействии с прекорнеальной слезной пленкой обеспечивает функции защиты, транспорта кислорода и питательных веществ.
Воздействие неблагоприятных факторов окружающей среды, в том числе КЛ, глазных капель может приводить к трансформации конъюнктивального эпителия по типу плоскоклеточной метаплазии, кератинизации, потери способности формировать бокаловидные клетки, приводя к уменьшению их плотности вплоть до полного исчезновения. Все это неизбежно ведет к снижению слезопродукции и изменению состава слезы, т.е. к развитию синдрома «сухого глаза» [7].
Для лечения этого состояния необходим комплексный подход. Достаточно эффективным методом является слезозаместительная терапия препаратами (желательно) без консервантов. Для восстановления структуры и функции эпителиального слоя применяются медикаментозные средства, содержащие декспантенол. Как правило, лечебные мероприятия с использованием этих средств являются достаточными при ношении КЛ, их применение позволяет купировать симптомы «сухого глаза» и обеспечить комфорт использования средств контактной коррекции [2, 3].
Однако в ряде случаев, несмотря на проводимую слезозаместительную терапию и применение корнеопротекторов, возникает непереносимость КЛ. Это проявляется в виде гиперемии конъюнктивы век и глазного яблока, отека конъюнктивы и неравномерности ее поверхности, а при выраженной степени эпителиопатии – повышенной десквамации эпителиальных клеток вплоть до эрозии роговицы.
Подобные клинические ситуации возникают при длительном многолетнем ношении КЛ, сопровождающемся значительным снижением слезопродукции, кератоконусе, вторичных эктазиях после кераторефракционных операций, дистрофиях роговицы. Контактные линзы в этих ситуациях являются дополнительным фактором негативного воздействия на глазную поверхность и состояние слезной пленки. Однако именно для этой категории пациентов контактная коррекция является основным методом коррекции рефракционных нарушений [1].
Для определения тактики лечения при непереносимости КЛ необходимо комплексное обследование пациента с обязательной оценкой состояния эпителия роговицы и конъюнктивы. Одним из методов, позволяющим оценить состояние эпителиальной выстилки, является метод импрессионной цитологии, основанный на переносе с помощью миллипорового фильтра поверхностного слоя клеток на предметное стекло, с последующим их прокрашиванием и исследованием под иммерсией в световом микроскопе. Метод позволяет изучать морфологию эпителиоцитов, оценивать наличие бокаловидных клеток, а также клеток воспаления, выявить признаки аллергической реакции, наличие инфекции [4].
Преимуществами метода импрессионной цитологии по сравнению с общепринятым методом соскоба с конъюнктивы являются его малоинвазивность, простота выполнения, возможность повторного взятия отпечатка и отсутствие необходимости применения анестетиков, которые могут вызвать изменения изначальной картины эпителиального пласта [5]. Метод импрессионной цитологии применим также для взятия отпечатков эпителия роговицы и других слизистых поверхностей. Правда, в первом случае без местных анестетиков не обойтись, что в свою очередь потребует при интерпретации полученной картины поправки на цитотоксическое действие препарата на эпителий роговицы [6, 8].
Цель работы: изучить состояние эпителиальной выстилки конъюнктивы при непереносимости КЛ и неэффективности традиционных методов медикаментозной коррекции (слезозаменители, корнеопротекторы).
Материал и методы исследования
Под наблюдением находилось 16 пациентов (31 глаз), из них 5 (10 глаз) пациентов – с миопией, более 5 лет использующие КЛ (3 пациента – с ЖГКЛ, 2 – с МКЛ), 6 пациентов (12 глаз) – с кератоконусом III-IV стадии, 2 больных (3 глаза) – с вторичными эктазиями после кераторефракционных операций, 3 пациента (6 глаз) – с дистрофией роговицы. У всех пациентов непереносимость КЛ сочеталась с признаками синдрома «сухого глаза», эпителиопатией, гиперемией конъюнктивы век и глазного яблока.
Для оценки состояния эпителия конъюнктивы век был использован модифицированный метод импрессионной цитологии. Полоску миллипорового фильтра (диаметр пор – 0,25 мкм) стандартных размеров при помощи анатомического пинцета помещали в нижний свод конъюнктивальной полости, после чего проводили смещение нижнего века до соприкосновения с поверхностью глазного яблока под небольшим давлением. При последующем отведении нижнего века извлекали полоску фильтра с «отпечатанными» на обеих ее поверхностях эпителиальными клетками как бульбарной, так и тарзальной конъюнктивы. Отпечатки тотчас же переносили на специально подготовленное предметное стекло, фиксировали 95% метиленовым спиртом в течение 1–3 мин. и окрашивали по Романовскому – Гимзе. После высушивания материал исследовали под световым микроскопом. Исследование и фоторегистрация цитологических препаратов проводились на «Фотомикроскопе III» (фирма Opton, Германия) при увеличении ×400.
Результаты исследования
При анализе полученных отпечатков эпителия тарзальной и бульбарной конъюнктивы век выявлены признаки выраженной плоскоклеточной метаплазии (кератинизации) эпителиоцитов, локальной, а затем и диффузной дистрофии, приводящей к повышенной десквамации поверхностного слоя эпителия. Данные исследования позволяют судить и о наличии воспалительной реакции конъюнктивы.
Клинический пример 1. Больной К., 21 год. Диагноз: кератоконус II стадии OD, I стадии OC. Острота зрения OD = 0,06; с жесткой газопроницаемой КЛ (ЖГКЛ) = 0,8. Острота зрения OC = 0,08; с ЖГКЛ = 0,8.
Срок ношения ЖГКЛ – 3 года. Максимальное время ношения линз в течение дня – 2-3 ч, затем возникают дискомфорт, чувство жжения, покраснение глаз, чувство инородного тела. Пациент вынужден снимать КЛ.
Методом импрессионной цитологии выявлены выраженная кератинизация эпителия (зерна кератогиалина в цитоплазме), отсутствие бокаловидных клеток (рис. 1).
Клинический пример 2. Больная М., 58 лет. Диагноз: дистрофия роговицы, вторичная конусовидная деформация ОU. Острота зрения OD = 0,04; с ЖГКЛ = 0,5. Острота зрения OC = 0,06; с ЖГКЛ = 0,4.
Срок ношения ЖГКЛ – 10 лет. В течение последних 2 лет отмечает ухудшение переносимости КЛ, сухость глаз, дискомфорт, несмотря на постоянное использование слезозаместительных препаратов и корнеопротекторов.
При цитологическом исследовании выявлена частичная атрофия эпителиоцитов (светлые отечные клетки) (указано стрелками «а») на фоне относительно сохранных клеток в левой части препарата (указано стрелкой «б») (рис. 2).
Клинический пример 3. Больной С., 24 года. Диагноз: кератоконус II-III стадии OD, II стадии OC. Острота зрения OD = 0,02; с ЖГКЛ = 0,8. Острота зрения OC = 0,2; с ЖГКЛ = 0,9. Пациент не переносит ЖГКЛ.
Цитологический метод исследования позволил выявить диффузную атрофию клеток эпителиального пласта с расширением межклеточных пространств и наличие воспалительных клеток (рис. 3).
Клинический пример 4. Больная Е., 39 лет. Диагноз: кератоконус, субклиническая стадия OU. Острота зрения OD = 0,08 c sph – 4,5 = 1,0. Острота зрения OC = 0,8 c sph – 5,5= 0,0. Пациентка не переносит ЖГКЛ.
Цитологически выявлена выраженная тотальная атрофия поверхностного слоя клеток эпителия с их последующей десквамацией (рис. 4).
Заключение
Таким образом, метод импрессионной цитологии позволяет оценить наличие и степень плоскоклеточной метаплазии эпителия конъюнктивы век и глазного яблока, состояние плотности бокаловидных клеток – характерные признаки синдрома «сухого глаза», нередко сопровождающего ношение КЛ. Нарастание дистрофии, десквамации клеток приводит к снижению барьерных свойств эпителия, появлению воспалительной реакции, нередко к развитию инфекции. Наличие плотных слизистых нитей в препарате свидетельствует о присоединении аллергической реакции.
Таким образом, длительное ношение КЛ может явиться фактором риска возникновения осложнений, особенно у пациентов с наиболее сложной патологией роговицы. Именно эта категория больных нуждается в коррекции аномалий рефракции КЛ и выработке алгоритма лечения и реабилитации.
Комплекс лечения должен включать:
– слезозаместительную терапию, причем слезозаменители не должны содержать консервантов;
– эпителиотропные средства (солкосерил, дексантенол), необходимые для восстановления регенераторной функции эпителия;
– противовоспалительную терапию (антисептические средства) для профилактики и лечения воспаления;
– при наличии аллергической реакции – противоаллергические средства.
При выраженном снижении уровня слезопродукции, признаках хронического воспалительного процесса и наличии аллергического компонента можно ожидать положительного результата от местного применения 0,05% эмульсии циклоспорина (Restasis; Allergan Inc, Irvine, California). Лечение 0,05% эмульсией циклоспорина требует изучения и контроля действия препарата. Одним из методов оценки его терапевтической эффективности может служить данный цитологический метод исследования.
Литература
1. Егорова Г.Б. Оптимизация контактной коррекции первичных и вторичных аметропий: Дисс…. д-ра мед. наук. М., 2005. С. 214.
2. Егорова Г.Б., Федоров А.А., Митичкина Т.С. Оценка эффективности применения слезозаменителей при симптоматическом синдроме сухого глаза // Офтальмологические ведомости. 2011. Т. IV. № 4. С. 8–12.
3. Егорова Г.Б., Федоров А.А., Митичкина Т.С. Возможности метода импрессионной цитологии в диагностике и оценке эффективности медикаментозной коррекции синдрома сухого глаза при ношении контактных линз // Вестник офтальмологии. 2012. Т. 128. №1. С. 33–35.
4. Федоров А.А., Шерстнева Л.В. Клинико-цитологические параллели при воспалительных заболеваниях конъюнктивы // Вестник офтальмологии. 1997. Т. 113. № 1. С. 33–36.
5. Федоров А.А. Морфологические основы научных исследований в офтальмологии // Вестник офтальмологии. 2013. Т. 129. № 5. С. 10–21.
6. Murube J., Rivas L. Impression cytology on conjunctiva and cornea in dry eye patients establishes a correlation between squamous metaplasia and dry eye clinical severity // Eur J Ophthalmol. 2003. Vol. 13. N 2. Р. 115–127.
7. Pflugfelder S.C., Beuerman R.W., Stern M.E. Dry Eye and Ocular Surface Disorders. Marcel Dekker, Inc. New York – Basel, 2004. P. 428.
8. Singh R. et al. Impression cytology of the ocular surface // Br. J. of Ophthalmol. 2005. Vol. 89. N 7. P. 1655–1659.
.
Histomorphological changes in various rat tissues following chronic exposure to copper-zinc-pyrite ore | Ziyakayeva
Актуальность изучения воздействия тяжёлых металлов в составе медно-цинковых колчеданных руд на человека обусловлена наличием на территории Республики Башкортостан одного из крупнейших предприятий горнодобывающей промышленности — Учалинского горно-обогатительного комбината. Основной фактор вредного воздействия производственной среды на работников данного предприятия — медно-цинковая колчеданная мелкодисперсная пыль, в которой в качестве сопутствующих компонентов присутствуют сера, свинец, кадмий, ртуть, мышьяк, сурьма, хром. Из всех перечисленных химических элементов наиболее опасны для организма кадмий и свинец [1, 2].
При свинцовой интоксикации снижается синтез эритропоэтина в почках, нарушаются пролиферация и дифференцировка стволовых клеток костного мозга, угнетается костномозговой эритропоэз, нарушается синтез гемоглобина, снижается осмотическая резистентность эритроцитов [3, 4].
Кадмий, накапливаясь в клетках паренхиматозных органов, связывает карбоксильные, амино- и сульфгидрильные группы, что приводит к нарушению межклеточных взаимодействий, некрозу и апоптозу [5, 6].
Известно, что геохимическая специфика горного производства оказывает негативное воздействие на здоровье людей, работающих и проживающих на территории рудных месторождений [7]. Что касается медно-цинковых колчеданных руд, то большинство исследований посвящено оценке профессиональной заболеваемости на горнодобывающих предприятиях, в то время как экспериментальному гистоморфологическому анализу изменений, возникающих в тканях под воздействием руд цветных металлов, уделено недостаточно внимания: в современной литературе представлены только результаты метаболизма и структурной перестройки костной ткани и печени [1, 8, 9].
Цель нашего исследования — изучение хронического воздействия медно-цинковой колчеданной руды на гистоморфологическое состояние ткани лёгких, органов желудочно-кишечного тракта и почек в длительном модельном эксперименте.
Материал и методы исследования. Экспериментальное исследование выполнено на 60 белых нелинейных крысах-самцах с исходной массой тела 200±30 г в возрасте 3–4 мес. Работа проведена в соответствии с принципами Базельской декларации. Согласно международным правилам этичного обращения с животными, крысы содержались в виварии университета в стандартных клетках (n=6) в условиях свободного доступа к воде и еде при температуре воздуха в виварии 24±2 °С в соответствии с правилами СП 2.2.1.3218 и Директивой 2010/63/EU по охране животных, используемых в научных целях. Исследование одобрено локальным этическим комитетом ФГБОУ ВО «Башкирский государственный университет» Минздрава РФ, протокол №5 от 13.09.2017.
Для анализа токсического действия солей тяжёлых металлов медно-цинковой колчеданной руды на организм животного использовали модель дозированного перорального введения измельчённой руды [8, 10]. Образец исследуемой руды был предоставлен ОАО «Учалинский горно-обогатительный комбинат» (г. Учалы, Россия). Количество свинца в исследуемом образце руды составляло 0,06%, кадмия — 0,0088%.
Для создания экспериментальной модели хронической интоксикации опытной группе животных (n=40) в течение 4 мес ежедневно за час до стандартного кормления per os вводили водную суспензию порошка медно-цинковой колчеданной руды в дозе 600 мг/кг массы тела животного. Вводимую дозу рассчитывали, исходя из предельно допустимых концентраций тяжёлых металлов в зерне и хлебе [11]. В ходе эксперимента дозу руды корректировали каждый раз после очередного взвешивания животных, которое производили каждые 14–15 дней. В контрольную группу вошли 20 крыс, которые не подвергались воздействию руды.
Для гистоморфологического исследования на 30-е, 60-е, 90-е и 120-е сутки эксперимента у контрольных и подопытных крыс были взяты кусочки желудка, тонкой и толстой кишки, печени, лёгких и почек размером 0,5×0,5 см. Ткани фиксировали в 10% забуференном растворе формалина, и после соответствующей гистологической проводки готовили срезы толщиной 7 мкм с последующим окрашиванием их гематоксилином и эозином (ЗАО «ЭКОлаб», Россия) [10, 12]. Визуальный гистоморфологический анализ микропрепаратов осуществляли на микроскопе AXIO Lab.A1 (ZEISS, Германия) при увеличении объектива ×40. Всего было исследовано 100 микропрепаратов.
Результаты. В проведённых гистоморфологических исследованиях органов крыс, подвергнутых хронической интоксикации медно-цинковой колчеданной рудой, мы наблюдали признаки воспалительных и дегенеративных процессов, динамика развития которых в разных органах имела свои особенности.
В слизистой оболочке желудка при хроническом воздействии медно-цинковой колчеданной руды структурные нарушения развивались уже на 30-е сутки: в препаратах появлялись слущенные и полуразрушенные эпителиальные клетки, количество которых увеличилось к 60-м суткам (рис. 1). В это же время в собственном слое и подслизистой основе слизистой оболочки желудка была выявлена лимфоидная инфильтрация. К 120-м суткам в препаратах наряду с признаками десквамации эпителия и диффузной лимфоцитарной инфильтрацией присутствовали крупные лимфоидные фолликулы, занимающие всю толщину слизистой оболочки желудка.
Рис. 1. Слизистая оболочка желудка: А — контроль; Б — 30-е сутки, начальная стадия десквамации эпителия; В — 60-е сутки, слущенные эпителиоциты на поверхности слизистой оболочки; Г — 120-е сутки, десквамация эпителия, инфильтрация слизистой оболочки лимфоидными клетками. Окраска гематоксилином и эозином. Микрофотография. Окуляр ×10, объектив ×40
В тонкой кишке животных первые признаки морфологических изменений обнаруживали позднее — на 60-е сутки воздействия медно-цинковой колчеданной руды (рис. 2). Они проявлялись в деструкции эпителиального слоя слизистой оболочки и сопровождались заметной инфильтрацией стенки кишечника лимфоцитами. В стенке толстой кишки также происходило увеличение количества отдельных лимфоцитов и солитарных лимфоидных фолликулов. К 120-м суткам у подопытных животных в слизистых оболочках тонкой и толстой кишки определялись диффузная лимфоцитарная инфильтрация и очаговый некроз.
Рис. 2. Тонкая кишка: А — контроль; Б — 60-е сутки, скопление лимфоцитов между криптами; В — 90-е сутки, лимфоидная инфильтрация слизистой оболочки; Г — 120-е сутки, формирование лимфоидных фолликулов и признаки некроза. Окраска гематоксилином и эозином. Микрофотография. Окуляр ×10, объектив ×40
Воспалительные и дегенеративные процессы, вызванные введением в организм соединений тяжёлых металлов в составе медно-цинковой колчеданной руды, наиболее отчётливо были выражены в печени подопытных животных (рис. 3). Признаки структурной перестройки органа появились уже к 30-м суткам интоксикации, когда по ходу печёночной триады и внутри долек печени сформировались очаги скопления лимфоидных клеток. К 60-м суткам в препаратах возникала гидропическая дистрофия гепатоцитов, ткань печени была насыщена лимфо-макрофагальными инфильтратами. К 90-м суткам хронического воздействия медно-цинковой руды в печени подопытных крыс развилась жировая дистрофия. К 120-м суткам в печени были выявлены признаки некроза: в центре долек присутствовали разные по площади очаги аутолитического распада клеток и жиробелковый детрит, по периферии долек располагались гепатоциты в состоянии жировой дистрофии.
Рис. 3. Печень: А — контроль; Б — 60-е сутки, гидропическая дистрофия печени; В — 90-е сутки, полнокровие синусоидных капилляров и жировая дистрофия гепатоцитов; Г — 120-е сутки, очаговая гиперемия внутридольковых синусоидных капилляров, признаки аутолиза и некроза гепатоцитов. Окраска гематоксилином и эозином. Микрофотография. Окуляр ×10, объектив ×40
Несмотря на то обстоятельство, что в нашем эксперименте подопытные животные получали медно-цинковую руду перорально, воспалительные изменения возникли не только в органах желудочно-кишечного тракта, но и в лёгочной ткани (рис. 4). На 30-е сутки эксперимента в лёгких зарегистрированы скопление лимфоидных клеток и застой крови в капиллярах, окружающих альвеолы, а интерстициальная соединительная ткань была инфильтрирована нейтрофилами и макрофагами. К 60-м суткам хронического воздействия медно-цинковой колчеданной руды в лёгочной ткани на фоне воспалительных явлений появились признаки бронхопневмонии. На 90-е сутки в значительной части лёгочной ткани развились отёк и клеточная инфильтрация стенок бронхиол и альвеолярного пространства. Все перечисленные признаки воспалительного процесса в лёгких присутствовали и на 120-е сутки эксперимента.
Рис. 4. Лёгкие: А — контроль; Б — 30-е сутки, очаговая инфильтрация лейкоцитами интерстициальной ткани; В — 60-е сутки, десквамация эпителия бронхов, инфильтрация их стенок лимфоцитами; Г — 120-е сутки, выраженная инфильтрация интерстициальной ткани и кровеносных сосудов лимфоцитами и макрофагами. Окраска гематоксилином и эозином. Микрофотография. Окуляр ×10, объектив ×40
Анализ гистоморфологического строения почки уже на 30-е сутки интоксикации компонентами медно-цинковой колчеданной руды выявил наличие воспалительного процесса в ткани, окружающей канальцы нефрона (рис. 5). К 60-м суткам эксперимента у крыс развился тубулоинтерстициальный нефрит с очаговой инфильтрацией интерстициальной ткани. В последующие дни выраженность деструктивных процессов в почках подопытных животных нарастала. К 120-м суткам на гистологических срезах были выявлены изменения микроциркуляторного русла (венозная гиперемия с последующим увеличением проницаемости стенок капилляров, усиленная экссудация плазмы крови, миграция лейкоцитов в периваскулярную зону), а также множественная очаговая лейкоцитарная инфильтрация интерстициальной ткани. Таким образом, хроническая интоксикация медно-цинковой колчеданной рудой привела к развитию выраженного тубулоинтерстициального нефрита и тубулопатии с признаками хронического пиелонефрита.
Рис. 5. Почки: А — контроль; Б — 30-е сутки, венозная гиперемия в зоне почечных канальцев; В 60-е сутки, коллоидоподобное содержимое в канальцах нефрона почек; Г — 120-е сутки, цилиндры в почечных канальцах. Окраска гематоксилином и эозином. Микрофотография. Окуляр ×10, объектив ×40
Обсуждение. Полученные нами данные свидетельствуют о выраженном токсическом действии компонентов медно-цинковой колчеданной руды на организм млекопитающих. Помимо меди, цинка и серы, руда содержит свинец, селен, теллур, кадмий, никель, кобальт, мышьяк, сурьму, таллий и барий. Тяжёлые металлы и их соединения проникают в организм через воздух, воду, пищу, накапливаются в нём и оказывают токсическое воздействие на разные органы и ткани.
Показано, что при хроническом введении компонентов руды у экспериментальных животных нарушаются функции эндокринной системы: снижается уровень тестостерона, йодсодержащих гормонов щитовидной железы и паратгормона, увеличивается синтез глюкокортикоидов [8]. На клеточном уровне под влиянием цинка, свинца, кадмия происходит активация перекисного окисления липидов, изменяется проницаемость мембран, снижаются адгезивные способности клеток, тормозятся процессы пролиферации и дифференцировки гемопоэтических клеток, клеток печени и костной ткани [1, 9, 10, 13–15].
Гистоморфологические изменения, описанные в нашем исследовании, являются результатом неспецифического повреждающего действия компонентов медно-цинковой колчеданной руды, вызывающего, по всей видимости, признаки системного воспалительного ответа в различных тканях.
Отдельного внимания заслуживает обнаруженный нами феномен инфильтрации лимфоидными клетками паренхиматозных органов и слизистых оболочек при хронической интоксикации животных медно-цинковой колчеданной рудой. Известно, что лимфоциты не только защищают организм от чужеродных антигенов, но и регулируют морфогенез, поддерживая механизмы обновления тканей в физиологических условиях и запуская при необходимости резервную программу репаративной регенерации [16, 17].
Выводы
- Длительное пероральное введение крысам тяжёлых металлов в составе медно-цинковой колчеданной руды привело к выраженным воспалительным и дегенеративным изменениям в лёгочной ткани, органах желудочно-кишечного тракта и почках.
- Интоксикация медно-цинковой колчеданной рудой вызывает выраженную лимфоцитарную тканевую реакцию.
Участие авторов. З.К.Р. — проведение эксперимента, анализ полученных результатов, написание и оформление статьи; К.А.Ф. — руководитель исследования; К.Ф.А. и Ф.М.Я. — морфологическое исследование, описание гистологических препаратов и приготовление микрофотографий.
Источник финансирования. Исследование не имело спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов по представленной статье.
Desquamation — обзор | ScienceDirect Topics
Патогенез и иммунитет
Вирус поражает слизистую дыхательных путей, вызывая лизис и десквамацию респираторного эпителия, инфильтраты мононуклеарных клеток и изменение мукоцилиарного клиренса. Трахеобронхит — типичная особенность, часто связанная с длительными нарушениями функции легких легких и гиперреактивностью дыхательных путей. Первичная вирусная пневмония гриппа приводит к диффузному поражению альвеол, альвеолярному кровотечению и экссудату, гиалиновым мембранам и реактивному фиброзу.В смертельных случаях пандемического гриппа A (h2N1) 2009 г. были выявлены патологические изменения синдрома полиорганной дисфункции, такие как застой и отек мозга, воспаление миокарда, фибриноидные изменения артериол, тромбоз ветвей легочных и селезеночных артерий, приводящие к клиновидным инфарктам селезенки. 36,58
Репликация вируса в верхних дыхательных путях обычно достигает пика в течение 1-2 дней после появления симптомов и, в зависимости от возраста и предыдущего иммунитета, продолжается примерно 3-8 дней.Тяжесть заболевания широко коррелирует с вирусной нагрузкой на верхние дыхательные пути. Симптомы конституционального гриппа частично связаны с высвобождением провоспалительных цитокинов и хемокинов. Уровни интерферона (IFN-α и IFN-γ), фактора некроза опухоли (TNF-α), интерлейкинов и хемокинов (IL-1β, IL-6, IL-8, IL-10, MCP-10, MIP-1α и MIP-1β) увеличиваются в носовых секретах, а IFN, IL-6 и TNF-α увеличиваются в крови при гриппе человека. 36 Тропизм штамма вируса гриппа зависит, среди прочего, от комбинации чувствительности его НА к расщеплению протеазами и доступности тканей протеаз, что делает вирус инфекционным. 59 Внелегочное распространение вируса у людей редко документируется, но системное распространение является обычным признаком высокопатогенных вирусов птиц у кур, а иногда и у грызунов или других млекопитающих-хозяев. Сывороточные и секреторные антитела, направленные на HA и NA, появляются через 10 дней после инфицирования и коррелируют с надежной защитой от повторного заражения гомологичным штаммом. Вызванная вакциной защита от гомотипического вируса может длиться до 2–3 лет. Инфекция также вызывает клеточный иммунитет, обнаруживаемый через 3–6 дней, что, по-видимому, важно для выздоровления. 36 Ответ цитотоксических Т-лимфоцитов против внутренних белков может обеспечивать некоторую степень гетероподтипического иммунитета.
Сезонный грипп A (h2N1) реплицируется в основном в верхних дыхательных путях, тогда как грипп A 2009 г. (h2N1) реплицируется как в верхних, так и нижних дыхательных путях. 60 Патологоанатомические исследования у пациентов с пандемией A (h2N1) были аналогичны таковым с инфекцией A (H5N1), включая диффузное альвеолярное повреждение, гемофагоцитоз, лимфоидную атрофию и повышенные уровни воспалительных маркеров, таких как IL-6 и MCP-1 в паренхима легкого.Была обнаружена значительная корреляция между тяжестью заболевания и уровнями провоспалительных цитокинов, таких как IL-6, IL-10 и IL-15. 60
Десквамация — обзор | ScienceDirect Topics
Патогенез и иммунитет
Вирус поражает слизистую дыхательных путей, вызывая лизис и десквамацию респираторного эпителия, инфильтраты мононуклеарных клеток и изменение мукоцилиарного клиренса. Трахеобронхит — типичная особенность, часто связанная с длительными нарушениями функции легких легких и гиперреактивностью дыхательных путей.Первичная вирусная пневмония гриппа приводит к диффузному поражению альвеол, альвеолярному кровотечению и экссудату, гиалиновым мембранам и реактивному фиброзу. В смертельных случаях пандемического гриппа A (h2N1) 2009 г. были выявлены патологические изменения синдрома полиорганной дисфункции, такие как застой и отек мозга, воспаление миокарда, фибриноидные изменения артериол, тромбоз ветвей легочных и селезеночных артерий, приводящие к клиновидным инфарктам селезенки. 36,58
Репликация вируса в верхних дыхательных путях обычно достигает пика в течение 1-2 дней после появления симптомов и, в зависимости от возраста и предыдущего иммунитета, продолжается примерно 3-8 дней.Тяжесть заболевания широко коррелирует с вирусной нагрузкой на верхние дыхательные пути. Симптомы конституционального гриппа частично связаны с высвобождением провоспалительных цитокинов и хемокинов. Уровни интерферона (IFN-α и IFN-γ), фактора некроза опухоли (TNF-α), интерлейкинов и хемокинов (IL-1β, IL-6, IL-8, IL-10, MCP-10, MIP-1α и MIP-1β) увеличиваются в носовых секретах, а IFN, IL-6 и TNF-α увеличиваются в крови при гриппе человека. 36 Тропизм штамма вируса гриппа зависит, среди прочего, от комбинации чувствительности его НА к расщеплению протеазами и доступности тканей протеаз, что делает вирус инфекционным. 59 Внелегочное распространение вируса у людей редко документируется, но системное распространение является обычным признаком высокопатогенных вирусов птиц у кур, а иногда и у грызунов или других млекопитающих-хозяев. Сывороточные и секреторные антитела, направленные на HA и NA, появляются через 10 дней после инфицирования и коррелируют с надежной защитой от повторного заражения гомологичным штаммом. Вызванная вакциной защита от гомотипического вируса может длиться до 2–3 лет. Инфекция также вызывает клеточный иммунитет, обнаруживаемый через 3–6 дней, что, по-видимому, важно для выздоровления. 36 Ответ цитотоксических Т-лимфоцитов против внутренних белков может обеспечивать некоторую степень гетероподтипического иммунитета.
Сезонный грипп A (h2N1) реплицируется в основном в верхних дыхательных путях, тогда как грипп A 2009 г. (h2N1) реплицируется как в верхних, так и нижних дыхательных путях. 60 Патологоанатомические исследования у пациентов с пандемией A (h2N1) были аналогичны таковым с инфекцией A (H5N1), включая диффузное альвеолярное повреждение, гемофагоцитоз, лимфоидную атрофию и повышенные уровни воспалительных маркеров, таких как IL-6 и MCP-1 в паренхима легкого.Была обнаружена значительная корреляция между тяжестью заболевания и уровнями провоспалительных цитокинов, таких как IL-6, IL-10 и IL-15. 60
Процесс десквамации и внешний слой кожи
Шелушение — это естественный процесс, при котором клетки кожи создаются, удаляются и заменяются. Процесс десквамации происходит в самом внешнем слое кожи, называемом эпидермисом. Сам эпидермис состоит из четырех уникальных слоев. Каждый из этих слоев играет определенную роль в десквамации.
PeopleImages / DigitalVision / Getty ImagesРождение клеток кожи
Иногда это называется оборотом клеток, десквамация происходит каждую секунду дня, и вы даже этого не замечаете.
Новые клетки кожи создаются в зародышевом слое, который является самым глубоким слоем эпидермиса. Этот слой еще называют базальным слоем.
Клетки кожи начинают свою жизнь как один слой толстых столбчатых клеток. Эти клетки отвечают за создание каждой клетки вашей кожи.
Клетки в этом слое делятся. Половина из них остается в зародышевом слое. Остальные клетки начинают миграцию на поверхность кожи.
Сделано кератин
Их следующая остановка — шиповатый слой. Здесь клетки кожи меняют свою форму столбца на форму, которая больше похожа на многоугольник.
Шиповидный слой также называют «колючим слоем», потому что эти многоугольные клетки действительно выглядят довольно колючими, если вы посмотрите на них под микроскопом.
Именно здесь, в шиповатом слое, клетки кожи начинают вырабатывать кератин, жесткие волокнистые белки, составляющие основную структуру кожи. (Кератин также является основным компонентом ваших волос и ногтей.)
Ячейки выравниваются
Клетки кожи продолжают продвигаться вверх от остистого слоя и попадают в гранулированный слой. В этом слое клетки начинают выравниваться. Они тоже потеряли свое ядро.
Этот слой также называют «зернистым слоем».«Хотите угадать, почему? Да, потому что здесь клетки приобретают зернистый вид.
Клетки достигают поверхности, а затем отслаиваются
Клетки кожи достигли своего конечного пункта назначения — рогового слоя. Как только клетки достигают этого верхнего слоя кожи, они, по сути, мертвы.
Клетки рогового слоя очень плоские и плотно упакованы. Эти плоские мертвые клетки непрерывно отпадают по мере того, как новые клетки выходят на поверхность. Таким образом, ваша кожа постоянно обновляется.
Куда деваются все эти мертвые клетки кожи? Вы можете быть удивлены, узнав, что большая часть пыли в вашем доме на самом деле состоит из мертвых клеток кожи.
Весь процесс десквамации, от рождения клеток до слущивания, занимает от 14 до 28 дней.
Роль аномального шелушения при акне
Считается, что у людей с акне процесс шелушения идет наперекосяк. Мертвые клетки кожи остаются дольше, чем должны, закупоривая поры и способствуя возникновению высыпаний.Вот почему отшелушивающие процедуры помогают улучшить состояние кожи.
Тяжелая форма астмы — заболевание эпителия
Астма — важное клинически распространенное заболевание во всем мире. Несмотря на лучшее знание патогенеза, механизмы, лежащие в основе индукции и сохранения болезни, в значительной степени неизвестны. Сейчас принято считать, что воспаление дыхательных путей и структурные изменения бронхов являются важными признаками. Взаимосвязь между этими структурными изменениями и клиническими и функциональными отклонениями явно заслуживает дальнейшего изучения.Эти результаты привели к усилению использования ингаляционных кортикостероидов в качестве основного метода лечения астмы. Тем не менее, есть пациенты со стойкими симптомами, измененной функцией легких и высокой частотой обострений, несмотря на долгосрочное наблюдение специалиста и постоянное оптимальное лечение. Эти тяжелые пациенты имеют серьезные физические недостатки в повседневной жизни и несут большую часть расходов, связанных с астмой 1. Поэтому очень важно лучше понять механизмы, приводящие к этому тяжелому фенотипу.
Почти столетие назад Эллис 2 подчеркнул, что патологию астмы можно исследовать, исследуя мокроту живых пациентов или легкие пациентов, умерших во время приступа. Из этих источников роль бронхиального эпителия была прояснена путем описания удлиненных эпителиальных клеток в мокроте и наличия аномалий псевдослоистого и мерцательного эпителия в большинстве случаев со смертельным исходом, хотя они значительно варьировались в отношении местоположения и степени 2. Роль. Игра эпителиальных клеток была пересмотрена более подробно только 15 лет назад, и их реакция на воспаление и повреждение была явно обнаружена как ненормальная при астме 3.
Аллергены — это потенциально вредные факторы, которые могут взаимодействовать и повреждать эпителий бронхов, что приводит к развитию долгосрочных заболеваний, таких как астма. В исследовании с использованием провокационного теста in vivo было показано, что они влияют на гомеостаз бронхиального эпителия, вызывая пролиферацию 4. Вирусные инфекции являются хорошо известными индукторами большинства обострений астмы у детей и взрослых. Они взаимодействуют с бронхиальным эпителием и участвуют в структурных изменениях дыхательных путей, что приводит к гиперсекреции и гиперреактивности бронхов, которые длятся ≥1 года в некоторых моделях на животных, имитируя сохранение болезни человека 5.Несколько различных механизмов, связанных с воспалением, вызывают повреждение эпителия при астме. Медиаторы, выделяемые воспалительными клетками, такие как катионные белки, различные протеолитические ферменты, металлопротеиназы и вещества, реагирующие с кислородом, являются потенциальными виновниками. Бронхиальный отек и сосудистая утечка способствуют хрупкости эпителиального слоя астматических бронхов. Процессы раннего восстановления пытаются восстановить целостность ткани. Динамика этих событий сложна, включая активацию и гибель клеток, а также пролиферацию, миграцию и дифференцировку.Восстанавливающий эпителий производит различные факторы роста, которые способны активировать структурные клетки подслизистой оболочки, включая фибробласты и гладкомышечные клетки. Это межклеточное сотрудничество привело некоторых авторов к предположению, что структурные изменения дыхательных путей, наблюдаемые при астме, вызваны реактивацией эпителиальной мезенхимальной трофической единицы, которая контролирует морфогенез дыхательных путей в антенатальной жизни 6.
При астме бронхиальный эпителий видоизменяется, становится хрупким и активированным.Аномалии включают потерю самого поверхностного слоя эпителия, разрушение реснитчатых клеток, повышенную регуляцию высвобождения фактора роста и сверхэкспрессию рецепторов, таких как рецепторы эпидермального фактора роста (EGFR). Грубая морфология эпителия наблюдается на эндобронхиальных биопсиях была спорной. Отслаивание эпителия, о котором ранее сообщали исследователи, изучавшие эндобронхиальные биопсии, теперь считается, по крайней мере частично, результатом процедуры отбора проб.Несмотря на этот потенциальный смешивающий фактор, хрупкость эпителия остается реальностью 7. Ни одно исследование не продемонстрировало способность ингаляционных кортикостероидов полностью восстанавливать нормальный эпителиальный слой 8.
В этом выпуске журнала European Respiratory Journal , Hamilton et al . 9 сообщают об изменении фосфорилирования эпителиального тирозина эпителиальных клеток бронхов, полученных при фиброоптической бронхоскопии у живых астматиков с тяжелой формой заболевания.Эндобронхиальные биопсии или эксплантация очищенных клеток использовались для анализа различных сигнальных путей. Интересно, что эти изменения были довольно уникальными для клеток тяжелых пациентов по сравнению с нормальными субъектами и пациентами с более легкой формой заболевания. На уровни фосфотирозина не влияло 6-недельное лечение ингаляционными кортикостероидами. Было обнаружено, что эпидермальный фактор роста, тирозинкиназа, активируется в эпителии тяжелых астматиков, и экспериментов in vitro продемонстрировали неспособность кортикостероидов подавлять фосфорилирование EGFR и некоторых нижестоящих или связанных белков, таких как митоген-активированный белок. киназа.
При тяжелой астме экспрессия рецепторов, таких как EGFR, повышается и не зависит от текущих методов лечения, включая кортикостероиды 10. Маркеры выживания и пролиферации клеток коэкспрессируются с маркерами активации, такими как ядерный фактор-κB, в эпителий эндобронхиальных биоптатов, полученных от кортико-зависимых пациентов. У пациентов с тяжелой астмой слой эпителия был толще, чем у пациентов с легкой формой заболевания, и было идентифицировано мало апоптотических клеток.Это исследование было важным, чтобы предположить, что при тяжелой астме эпителиальные клетки были связаны с аномальным процессом восстановления, несмотря на отсутствие десквамации эпителия 10. Следует отметить, что повышенная регуляция ингибитора циклин-зависимой киназы, p21WAF, в астматическом эпителии может способствовать к этой длительной активации, несмотря на отсутствие потери контроля над этой пролиферацией 11. Этот фермент регулирует скорость пролиферации клеток и не зависит от кортикостероидов. Это может быть вызвано различными медиаторами и факторами роста, включая трансформирующий фактор роста-β, который, как было обнаружено, чрезмерно продуцируется в дыхательных путях при астме 12.Сочетание анализа эндобронхиальной биопсии с результатами, полученными ex vivo с использованием первичных культур очищенных эпителиальных клеток, способствует установлению эпителиальных аномалий как потенциального внутреннего фактора патофизиологии тяжелой астмы.
Разрешение воспаления — это хорошо скоординированный, активный процесс, который контролируется эндогенными противовоспалительными медиаторами. Эти медиаторы могут отключать хемоаттракцию и активацию лейкоцитов и обращать вспять сосудистые аномалии.Трансцеллюлярный метаболизм арахидоновой кислоты за счет взаимодействия липоксигеназы дает начало липоксиновому семейству метаболитов эйкозаноидов. Бронхиальный эпителий богат 15 продуктами, производными липоксигеназы, что указывает на его потенциал в качестве источника этих естественных противовоспалительных продуктов. Недавно было обнаружено, что тяжелая астма связана с потерей выработки липоксина-A4 по сравнению с легкой контролируемой астмой 13. Липидные медиаторы тогда являются потенциально важными компонентами разрешения воспаления, избегая дальнейшего усиления, ведущего к ремоделированию ткани.Эти результаты дают некоторое обоснование для разработки стабильных миметиков, которые могут влиять на ключевые аспекты хронического воспаления при астме.
Эти данные способствуют выделению эпителия как важнейшего партнера при тяжелой астме и могут указывать на внутриклеточные сигнальные пути бронхиального эпителия как потенциальные мишени для новых терапевтических вмешательств, когда глюкокортикоиды и β 2 -агонисты длительного действия имеют ограниченную эффективность.
Рецидивирующие эрозии роговицы | Канадская ассоциация оптометристов
Что такое периодическая эрозия роговицы (RCE)?
Роговица — это прозрачное куполообразное покрытие глаза.RCE возникает, когда внешний слой роговицы, известный как эпителий, расслаивается или отслаивается. Обычно эпителий плотно прилегает к находящемуся под ним слою роговицы. Глаз становится очень болезненным при RCE, так как роговица очень чувствительна к любому разрушению клеток. Боль часто усиливается при пробуждении. Когда веки закрыты во время сна, уменьшение поступления кислорода вызывает небольшой отек эпителия. Этот отек может привести к прилипанию эпителия к нижней поверхности века.После пробуждения эта рыхлая ткань отслаивается при открывании век, что вызывает сильную боль. Боль может длиться от пары часов до нескольких дней с частотой повторения несколько раз в год. Часто, если они проходят быстро, симптомы RCE часто игнорируются. Следует проконсультироваться с врачом-оптометристом, чтобы правильно диагностировать и лечить рецидивирующую эрозию роговицы, чтобы свести к минимуму испытываемый дискомфорт и предложить решения для предотвращения рецидива.
Что вызывает RCE?
Большинство случаев RCE связано с предшествующей травмой роговицы, например, предыдущей царапиной.Другие случаи связаны с основными эпителиальными дистрофиями. Как упоминалось ранее, обычно эпителий плотно прилегает к нижележащему слою. Иногда после травмы возникают недостаточные или дефектные соединения для прикрепления эпителия к остальной части роговицы, в результате чего эпителий подвержен шелушению. Пациенты с дистрофией роговицы, естественно, имеют рыхлый эпителий. Обычно это присутствует при рождении, но не проявляется до раннего взросления. Важно отметить, что пациенты редко испытывают стойкую потерю зрения из-за RCE.
Как вы относитесь к RCE?
Лечение RCE включает в себя то, что доктор оптометрии накладывает на пораженный глаз пластырь с кислородопроницаемой контактной линзой с повязкой, а также использует антибиотики и противовоспалительные глазные капли. Искусственные слезы также используются для смазывания глаз. В зависимости от тяжести RCE, местные мази иногда наносят на глаза на ночь перед сном, чтобы уменьшить вероятность отслоения эпителия утром. В некоторых случаях у пациентов возникают повторные эпизоды эрозий.Лечение может включать либо перевязку контактных линз на несколько месяцев, либо возможное хирургическое вмешательство офтальмолога в крайних случаях. В случае травмы роговицы важно, чтобы глаз обработал окулист, чтобы снизить вероятность возникновения RCE.
Изображение Джеймса Хейлмана, доктора медицины (собственная работа) [CC BY-SA 3.0 (http://creativecommons.org/licenses/by-sa/3.0) или GFDL (http://www.gnu.org/copyleft/) fdl.html)], через Wikimedia Commons
Определение десквамации по Merriam-Webster
des · qua · mate | \ ˈDe-skwə-ˌmāt \слущенный; шелушение
Другие слова из
десквамат шелушение \ ˌDe- skwə- ˈmā- shən \ имя существительноеПервое известное применение десквамата
1828, в значении, определенном выше
История и этимология дескваматы
Latin desquamatus , причастие прошедшего времени desquamare по шкале, от de- + squama по шкале
Узнать больше about
desquamateСтатистика для
дескваматПроцитируйте эту запись
«Десквамация.” Словарь Merriam-Webster.com , Merriam-Webster, https://www.merriam-webster.com/dictionary/desquamate. По состоянию на 24 марта 2021 г.
ГНД Чикаго APA Мерриам-ВебстерДополнительные определения для десквамация
des · qua · mate | \ ˈDes-kwə-ˌmāt \слущенный; шелушение
Медицинское определение
дескваматы: для отслаивания в виде чешуек : масштаб для отслаивания слущенных эпителиальных клеток
Другие слова из десквамат
шелушение \ ˌDes- kwə- ˈmā- shən \ имя существительноеКомментарии к записи десквамат
Что побудило вас посмотреть на десквамация ? Сообщите, пожалуйста, где вы это читали или слышали (включая цитату, если возможно).
Многослойный эпителий: характеристика, функция, типы
Некератинизированный
Важно понимать, что разница между «некератинизированным» и «ороговевшим» многослойным плоским эпителием (SSE) заключается не в отсутствии или наличии кератина соответственно. Вместо этого различие заключается в количестве ороговевших клеток, присутствующих внутри эпителия, потому что оба типа действительно содержат этот тип волокнистого белка.
Некератинизированный SSE состоит из переменного числа слоев. Клетки в более глубоком, базальном слое обычно кажутся кубовидными с прозрачной цитоплазмой из-за содержания в них гликогена. Клетки в поверхностном слое являются плоскими или плоскими. Базальный слой прикреплен к базальной мембране , листу белков внеклеточного матрикса. Он также содержит стволовых клеток, , которые имеют решающее значение в процессе самообновления. Стволовые клетки непрерывно делятся в базальном слое и мигрируют к апикальному слою.Они заменяют старые клетки в этом слое, которые, в свою очередь, впоследствии отслаиваются в виде безъядерных плоских клеток.
Некератинизированный эпителий обычно несет слизистую оболочку, которая служит дополнительным защитным и смазывающим слоем эпителия. Его можно увидеть в некоторых частях ротовой полости, глотке, пищеводе, дистальных отделах мочеточников, влагалище и наружных женских гениталиях. Некератинизированный эпителий действительно содержит некоторые ороговевшие клетки, однако количество отложений кератина будет варьироваться в зависимости от уровня высыхания и истирания, которому он может подвергаться.Например, у людей с хроническим курением или употреблением алкоголя в анамнезе эпителий ротоглотки и верхних отделов пищеварительного тракта может стать атипично ороговевшим. Кроме того, сжатие или скрежетание зубами о некератинизированный эпителий слизистой оболочки щеки может привести к образованию мозолистой ткани.
Поскольку количество кератина в этом подклассе многослойного эпителия довольно низкое, клетки плоской формы сохраняют свои нормальные характерные ядра и метаболические функции.
Кератинизированный
Кератинизированный многослойный плоский эпителий важен для тканей, подвергающихся регулярному физическому истиранию, а также из-за возможности высыхания (высыхания) и потери воды. Ороговевший эпителий состоит из многочисленных слоев мертвых плоских клеток, которые специально структурированы, чтобы быть водонепроницаемыми и уменьшать испарение из подлежащих тканей. Поэтому они составляют важную часть эпидермиса или внешней кожи. Они также встречаются в определенных областях ротовой полости (например,грамм. твердое небо, тыльная сторона языка), где еда, речь и дыхание могут привести к значительной потере воды. Кератинизированные клетки чаще всего идентифицируют по их безъядерному виду.
Кожа
В то время как некератинизированные SSE содержат относительно небольшое количество кератина, ороговевшие подклассы полны им. Лучшим примером ороговевшего ССЭ является эпидермис кожи. Он состоит либо из четырех отдельных слоев тонкой кожи, либо из пяти слоев толстой кожи.Их называют, начиная с самого глубокого:
- базальный слой
- шиповидный слой
- зернистый слой
- stratum lucidum (характерно для толстой кожи)
- роговой слой
Базовый слой
Базальный слой (базальный слой) состоит из стволовых клеток, которые непрерывно делятся путем митоза, давая начало кератиноцитам. Эти базальных кератиноцитов имеют небольшое количество базофильной цитоплазмы, плотно упакованные ядра и кубовидную или низко столбчатую форму.Они расположены в один слой и содержат сильно нерегулярные и складчатые базальные поверхности с большим количеством гемидесмосом , которые отвечают за прикрепление базального слоя к lamina lucida базальной мембраны.
Базальный слой также содержит рассеянные меланоцитов . Эти клетки содержат специфические гранулы, называемые меланосомами , которые отвечают за производство предшественника пигмента меланина .Этот пигмент придает коже характерный цвет и защищает от ультрафиолета. При обычном окрашивании H&E меланоциты имеют округлую форму с прозрачной цитоплазмой. Однако при более подробных исследованиях становится ясно, что меланоциты содержат некоторые специфические цитоплазматические отростки , которые проходят между кератиноцитами внутри шиповидного слоя. Эти процессы используются для переноса меланосом в кератиноциты, которые в конечном итоге располагаются как крышка над их ядрами.
Шиповатый слой
Шиповатый слой (шиповатый слой) состоит из кератиноцитов, которые мигрировали из базального слоя, расположенного ниже.Шиповидный слой на самом деле многослойный 90-120, а не один дискретный и однослойный. Кератиноциты также синтезируют цитокератинов (промежуточные филаменты), которые впоследствии агрегированы в тонофибрилл . Поверхность этих клеток содержит десмосом, , которые образуют межклеточные соединения. В этом слое кератиноциты имеют форму многогранника, имеют округло-овальные ядра, выступающие ядрышки и цитоплазмы. Они также синтезируют цитокератинов (промежуточные филаменты), которые впоследствии агрегированы в тонофибрилл .
Stratum spinosum (гистологический препарат)Stratum granulosum
Продолжая миграцию кератиноцитов, они попадают в гранулированный слой (зернистый слой). По мере созревания клетки синтезируют гранулы кератогиалина неправильной формы (плотно базофильные), которые содержат различные белки, такие как инволюкрин, лорикрин и филаггрин. Эти типы белков взаимодействуют с ранее продуцированными тонофибриллами, в результате чего образуются поперечно сшитые промежуточные филаменты, называемые кератином .
Кератиноциты также образуют пластинчатых тел , которые представляют собой гранулы трубчатой или яйцевидной формы, которые собираются комплексом Гольджи. Фактически, эти тельца представляют собой гетерогенные смеси или сборки липидов-носителей, ферментов, обрабатывающих липиды, белков и протеаз. Они могут быть связаны с мембраной и, следовательно, покрывать мембрану клетки или секретироваться во внеклеточное пространство. Их содержимое позволяет пластинчатым телам образовывать эпидермальный водный барьер , который является гидрофобным.Этот общий процесс называется ороговением (ороговение). Это считается особым типом апоптоза, потому что типичная фрагментация клеток заменяется накоплением кератина. В эпидермисе кератинизация происходит постоянно. Однако его скорость может быть вызвана чрезмерным истиранием . Некоторые примеры включают неправильно подогнанные зубы в полости рта (некератинизированный SSE) или высокий уровень трения кожи (ороговевший SSE), приводящий к мозолям. В целом, высокое количество кератина делает эпидермис чрезвычайно устойчивым к постоянному механическому истиранию.
Stratum lucidum
Просветленный слой виден только в толстой коже , обеспечивая защиту от повышенного трения. Этот слой содержит видимые эозинофильных клеток , но в целом этот слой очень преломлен и плохо окрашивается. Клетки содержат большое количество кератина , следовательно, ядро и другие органеллы имеют нарушенную морфологию.
Stratum lucidum (гистологическое слайд)Роговой слой
Роговой слой — это самый верхний неживой клеточный слой эпидермиса, состоящий из терминально дифференцированных кератиноцитов .Они заполнены кератиновыми промежуточными волокнами, что придает им более неправильную и плоскую форму, чем обычно.
