Удаление новообразований слизистой оболочки полости рта лазером в СПб
ВНИМАНИЕ
Обратите внимание!
По техническим причинам временно не работает прицельная внутриротовая рентгенография зубов.
Приносим извинения за временные неудобства.
Обратите внимание!
В связи с большим потоком обращений, возможны перебои в работе телефонной линии.
Для связи с оператором оставьте заявку, или пишите в онлайн консультант.
26 и 27 февраля в клинике «Медицентр» по адресу г. Мурино, Охтинская аллея д. 18 проводятся ремонтные работы, прием пациентов осуществляется только в случаях оказания неотложной помощи.
Приносим извинения за временные неудобства.
directions
Удаляем новообразования слизистой оболочки рта при помощи современного стоматологического лазерного оборудования. Для проведения операции мы используем углекислотный инфракрасный СО2-лазер, благодаря которому процедура проходит безболезненно и бескровно.
В настоящее время на сайте ведутся работы по изменению прайс-листа, актуальную информацию уточняйте по тел: 640-55-25 или оставьте заявку, с Вами свяжется оператор.
Цены на услуги
- Прием (осмотр, консультация) врача -стоматолога — хирурга повторный B01.067.002 850a
- Прием (осмотр, консультация) врача-стоматолога — хирурга первичный B01.067.001 1360a
- Удаление доброкачественного образования слизистой оболочки полости рта до 0,5 см 1530a
- Удаление доброкачественного образования слизистой оболочки полости рта более 0,5 см 2465a
Информация и цены, представленные на сайте, являются справочными и не являются публичной офертой.
Наши клиники в Санкт-Петербурге
Получить подробную информацию и записаться на прием Вы можете по телефону
Преимущества нашей клиники
- Профессиональный персонал. В нашей клинике работает медперсонал, прошедший специальную медицинскую подготовку и имеющий большой опыт.
- Высокоточное оборудование. Современный СО2-лазер позволяет проводить операции с высокой точностью.
- Быстрота процедуры. Длительность операции по удалению папиллом во рту составляет не больше пяти минут.
- Безболезненность.
 Для обезболивания при удалении опухолей мы используем качественные анестетики.
Для обезболивания при удалении опухолей мы используем качественные анестетики. - Легкая реабилитация. Рана после проведения процедуры затягивается в течение нескольких дней.
Показания к лазерному удалению опухолей во рту
Применение лазерного аппарата назначают при следующих доброкачественных опухолях слизистой оболочки рта:
- папиллома;
- фиброма;
- миома;
- гранулема;
- гемангиома;
- эритроплакия.
Противопоказания к удалению новообразований во рту
Удаление опухолей полости рта не проводится в следующих случаях:
- заболевания крови;
- сахарный диабет;
- злокачественные опухоли;
- проблемы иммунной системы.
Подготовка к операции
После первого посещения специалиста понадобится сдать ряд анализов, на основании которых стоматолог установит, можно ли проводить операцию.
Анализы, которые нужно сдать:
Перед процедурой не рекомендуется наносить на папилломы лекарственные гели и мази.
Как проводится лазерное удаление папиллом во рту
Процедура удаления опухолей во рту проводится под местной анестезией. После того, как стоматолог сделает обезболивающий укол, он вводит в рот пациента наконечник лазерного аппарата и аккуратно срезает новообразование. Узко сфокусированный луч не повредит мягкие ткани, окружающие папиллому.
Длительность операции зависит от количества опухолей. На удаление одного новообразования потребуется 2-3 минуты. Процедура абсолютно бескровная, так как лазерный луч прижигает ткани и предотвращает кровотечение.
После того, как новообразование будет удалено, на его месте останется небольшая ранка. Врач обработает ее заживляющим гелем и раствором перманганата калия.
Реабилитация после операции
После удаления опухолей полости рта на два-три часа откажитесь от приема пищи. Пока рана не затянется полностью, следует избегать острых, кислых и соленых продуктов.
Пока рана не затянется полностью, следует избегать острых, кислых и соленых продуктов.
Через несколько дней от следов воздействия лазера не останется следа. Возможно появление небольшого рубца, который исчезнет через 3 месяца.
936,855,898,852,946,1292
Тарасова Ольга 07.12.2020 20:55medi-center.ru
Клоконос Никита Сергеевич хороший врач, внимательный, обязательно спросит, как, хорошо ли, ответственно относится к работе. Делал ультразвуковую чистку зубов и лечил два кариеса. Большое спасибо центру, что берет на работу хороших специалистов.
Большое спасибо стоматологу Андрееву Петру Александровичу! Была на проф. гигиене, доктор все рассказал, дал рекомендации, ответил на все вопросы. Впечатление очень положительное, спасибо и до скорых встреч, Медицентр ????
Келих Анна Александровна 30.
medi-center.ru
Выражаю огромную благодарность врачам клиники «Медицентр», в особенности Степанчуку Максиму Андреевичу. Лечится у Максима Андреевича — одно удовольствие. Чуткое и внимательное отношение к пациентам, отзывчивость и переживание за свою работу. Я очень долго искала такую клинику и такого врача! Чуткий подход к пациенту, отзывчивость и доброта, согласитесь, такое не часто встретишь в наше время. Спасибо всем, кто облегчает наши страдания. Доктора клиники «Медицентр» — это настоящая команда во главе с заведующим стоматологического отделения Ветухом Вадимом Сергеевичем! Еще раз спасибо за добросовестную работу!!!
Забавникова Ю.С 11.07.2020 00:10medi-center.ru
Посетила стоматолога Андреева Петра Александровича. Очень классный врач!!! Спасибо ему огромное за качественную, душевную, а главное (для меня) безболезненную работу над моими зубами! Очень терпеливый и понимающий человек. Кажется, среди огромного кол-ва стоматологов я нашла своего врача!!! 🙂
Очень классный врач!!! Спасибо ему огромное за качественную, душевную, а главное (для меня) безболезненную работу над моими зубами! Очень терпеливый и понимающий человек. Кажется, среди огромного кол-ва стоматологов я нашла своего врача!!! 🙂
Спасибо большое за лечение, была у доктора Андреева П.А. Замечательный доктор, сделал все очень хорошо, сохранил почти безнадежный зуб, теперь на лечение только в эту клинику.
В данном центре делали удаление 8-го зуба, попала на прием к доктору Сари и очень этому рада, что именно он делал данную операцию. Удаление зуба было сложное, но благодаря терпению, высокому профессионализму, внимательности и пониманию проблем пациента результат и цель все таки были достигнуты. Рекомендую доктора Араби Сари теперь всем своим знакомым, и мне действительно важно быть уверенной в профессионализме специалиста а также, теперь уже всегда со спокойствием и доверием понимаю, что любую проблему по стоматологии мне помогут решить и я знаю к кому обратиться)
Симптомы, диагностика и лечение эритроплакии
Эритроплакия – это облигатная предраковая болезнь и представляет собой более опасную патологию в плане возможности развития злокачественности, в отличие лейкоплакии. Пациентами в основном являются мужчины и женщины старше 50 лет.
Пациентами в основном являются мужчины и женщины старше 50 лет.
Как правило, пациенты не испытывают ни болевых ощущений, ни дискомфорта. Только у некоторых возникает беспокойство относительно возникшего ярко-красного пятна на слизистой оболочке ротовой полости. Для определения вредных привычек у пациентов (например, пристрастие к употреблению алкоголя, курение и т.д.) нужно собрать анамнез.
Представленная патология характеризуется наличием элементов поражения в виде ярко-красных пятен и небольших узелков мягкой консистенции, при пальпации которых возникают болезненные ощущения. Если провести тщательное обследование полости рта пациента, можно обнаружить такие пятна в нескольких местах. Ярко-красный цвет пятен обусловлен атрофией слизистой.
Такие пятна чаще всего возникают в следующих областях:
- За последними молярами,
- На ротоглотке,
- На слизистой оболочке переходной складки нижней челюсти, дна полости рта и языка.
В редких случаях у одного пациента могут наблюдаться симптомы и эритроплакии, и лейкоплакии.
Диагностика и лечение эритроплакии
Длительное течение болезни приводит, как правило, к неблагоприятному исходу, так как пятна довольно быстро становятся злокачественными. Для благоприятного исхода заболевания следует сразу обратиться к врачу для правильной постановки диагноза и начала адекватного лечения.
Эритроплакию можно спутать с контактным стоматитом, десквамативным глосситом, гемангиомой, саркомой Капоши, лейкоплакией и плоскоклеточной карциономой.
Для правильной постановки диагноста лучше всего провести гистологическое исследование.
Лечится эритроплакия только хирургическим способом.
Хирургическое лечение доброкачественных новообразований полости рта
Хирургическое лечение доброкачественных новообразований полости рта
Ярема Владимир Иванович
Врач хирург-онколог маммолог, профессор кафедры госпитальной хирургии лечебного факультета Московского Государственного Медико-Стоматологического Университета
В основном, встречающиеся в полости рта новообразования являются доброкачественными. Среди них в поле зрения хирурга наиболее часто попадают фибромы, фибролипомы, папилломы, гемангиомы (рис.1), лейкоплакия, реже плеоморфные аденомы, красный плоский лишай, эритроплакия и некоторые другие заболевания. К доброкачественным процессам, локализованным на красной кайме губ (нижняя губа поражается гораздо чаще верхней), помимо вышеперечисленных, относятся различные хейлиты, кератопапилломы и другие.
Среди них в поле зрения хирурга наиболее часто попадают фибромы, фибролипомы, папилломы, гемангиомы (рис.1), лейкоплакия, реже плеоморфные аденомы, красный плоский лишай, эритроплакия и некоторые другие заболевания. К доброкачественным процессам, локализованным на красной кайме губ (нижняя губа поражается гораздо чаще верхней), помимо вышеперечисленных, относятся различные хейлиты, кератопапилломы и другие.
Плоскоклеточная папиллома проявляется на слизистой оболочке полости рта в виде одиночного образования на ножке с белесоватой ворсинчатой поверхностью, иногда напоминает цветную капусту. Папиллома растет медленно, боли не причиняет. При частой травматизации процесс может переходить в злокачественный.
Фиброматозный и ангиоматозный эпулис наиболее часто встречается на слизистой оболочке альвеолярного отростка полости рта. Причиной возникновения является хроническое механическое раздражение. В основном выявляется у лиц старше 50 лет. Рентгенологическое исследование при эпулисах, исходящих из мягких тканей, не выявляет патологических костных изменений.
Рентгенологическое исследование при эпулисах, исходящих из мягких тканей, не выявляет патологических костных изменений.
В лечении фиброзных разрастаний ведущую роль играет устранение причины, вызвавшей их возникновение. Операцию проводят при неэффективности консервативного лечения.
Фиброматоз в полости рта проявляется как фиброматоз десен в виде диффузного разрастания их и десневых сосочков. Встречается сравнительно редко, наблюдается у лиц молодого и среднего возраста. Клинически определяется валикообразное увеличение десны, покрывающее частично или полностью коронки зубов.
Зернистоклеточная опухоль(«зернисто-клеточная миобластома») является доброкачественной опухолью. Ранее ее происхождение связывали с развитием из мышечной ткани и трактовали как миому из миобластов (Абрикосов А.И., 1925). В настоящее время термин «миобластома» используется только для удобства, а генез опухоли остается неясным. Опухоль ограниченная, безболезненная, иногда носит дольчатый характер, по консистенции эластичная, может располагаться в глубине тканей или поверхностно, непосредственно под эпителиальным, покровом.
Миксома – доброкачественная опухоль неясного генеза, часто имеет инфильтративный рост. Встречается редко. Клинически диагностировать трудно, окончательный диагноз устанавливают после патоморфологического исследования.
Гемангиома –доброкачественное неотграниченное поражение, состоящее из пролиферирующих кровеносных сосудов. Происхождение гемангиом до настоящего времени окончательно не выяснено. Большая часть их является врожденной, и ее относят к аномалиям развития (Петров Н.Н., 1955).
Гранулема беременных – хирургическому лечению в период беременности, как правило, не подлежит, за исключением возникновения функциональных нарушений.
Травматическая неврома – опухолеподобное поражение, локализуется по переходной складке нижнего свода преддверия полости рта соответственно месту выхода подбородочного нерва. Встречается преимущественно у пожилых лиц с полной адентией и атрофией альвеолярного отростка нижней челюсти, пользующихся съемным зубным протезом. Возникновение невромы связано с постоянной травмой краем протеза подбородочного нерва у выхода из одноименного отверстия.
Возникновение невромы связано с постоянной травмой краем протеза подбородочного нерва у выхода из одноименного отверстия.
Клинически определяется округло-овальное образование размером до 0,5 см, болезненное, плотно эластичной консистенции. Располагается под слизистой оболочкой переходной складки с вестибулярной стороны соответственно нижним премолярам.
Хирургическое лечение обычно не проводят, так как иссечение невромы ведет к потере чувствительности тканей подбородочной области и нижней губы, которая воспринимается больным менее тягостно, чем болезненность самой травматической невромы. Лечение направлено на устранение постоянного раздражения ее краем протеза.
Таким образом, оперативное лечение доброкачественных новообразований полости рта проводят: при частых травмах любых опухолей и опухолевидных образований, при подготовке к протезированию, при неэффективности консервативной терапии, при частом рецидивировании, с косметической целью и для уточнения диагноза.
Среди доброкачественных процессов, подлежащих обязательному хирургическому лечению, выделяют предраковые заболевания, к которым относятся: бородавчатый (узелковый) предрак красной каймы губ, абразивный преканцерозный хейлит Манганотти (рис.5), лейкоплакия, красный плоский лишай, эритроплакия и некоторые другие.
Лейкоплакия характеризуется ороговением слизистой оболочки с наличием воспалительного компонента. Клинически определяется в виде белого пятна. Имеется несколько форм. Наиболее опасна веррукозная лейкоплакия.
В ранней стадии клинически определить начало злокачественного процесса на фоне лейкоплакии не представляется возможным.
В зависимости от формы лейкоплакии лечение начинают с устранения местных раздражающих факторов (отказ от курения, приема алкоголя, горячей, острой пищи) и применения консервативных методов (апликации масляными растворами витаминов групп А, В и прочее).
Эритроплакиявстречается редко, в основном у мужчин. Проявляется в виде довольно четко ограниченного очага ярко-красного цвета неправильной формы, с бархатистой поверхностью, на которой встречаются участки помутнения в виде серо-белого налета. При длительном существовании отмечается атрофия слизистой оболочки. Пораженный участок при пальпации безболезненный, подлежащие ткани не уплотнены.
Проявляется в виде довольно четко ограниченного очага ярко-красного цвета неправильной формы, с бархатистой поверхностью, на которой встречаются участки помутнения в виде серо-белого налета. При длительном существовании отмечается атрофия слизистой оболочки. Пораженный участок при пальпации безболезненный, подлежащие ткани не уплотнены.
Плоский лишай (красный плоский лишай) – хроническое заболевание кожи и слизистой оболочки рта, сопровождается ороговением поверхностного слоя эпителия, часто поражается изолированно только слизистая оболочка щеки, реже языка, десен, неба, губ. В начальной стадии заболевания возникают папулы в виде красных точек, затем они становятся серо-белого цвета, сливаются друг с другом.
В очаге поражения могут образоваться эрозии, изъязвления. Наличие этих признаков вместе с очагами гиперкератоза, а также инфильтрации основания поражения являются подозрительным на переход процесса в злокачественный.
Консервативное лечение плоского лишая начинают специалисты дерматологи и терапевты стоматологи. Назначают инъекции 1% раствора никотиновой кислоты, поливитамины (A, D), кортикостероиды и другие препараты. Необходимо также устранить местные раздражающие факторы (острая и горячая пища, табак, алкоголь).
Назначают инъекции 1% раствора никотиновой кислоты, поливитамины (A, D), кортикостероиды и другие препараты. Необходимо также устранить местные раздражающие факторы (острая и горячая пища, табак, алкоголь).
Особенности операций при доброкачественных новообразованиях
мягких тканей полости рта
При расположении доброкачественных процессов на слизистой оболочке полости рта проводят хирургическое иссечение новообразований в пределах здоровых тканей с обязательным гистологическим исследованием удаленного материала. При их незначительных размерах (около 1 см) хирургическое иссечение последних не представляет каких-либо трудностей. Швы накладывают обычно рассасывающимся шовным материалом. При новообразованиях, расположенных на губе возможно выполнение клиновидной резекции из-за более качественного косметического эффекта.
Хирургическое иссечение новообразований слизистой оболочки полости рта более 1 см в диаметре часто представляет из себя электрорезекцию тканей (за исключением губы) в пределах здоровых тканей с пластикой перемещенным слизисто-подслизистым лоскутом. Объемные операции на слизистых оболочках полости рта проводятся под наркозом с тампонадой глотки. Для питания в послеоперационном периоде довольно часто устанавливается назо-гастральный зонд. При распространенном поражении дна полости рта, для удобства доступа, язык прошивают лавсановыми нитями и смещают кверху. Язычные артерии при необходимости прошивают и перевязывают лавсаном.
Объемные операции на слизистых оболочках полости рта проводятся под наркозом с тампонадой глотки. Для питания в послеоперационном периоде довольно часто устанавливается назо-гастральный зонд. При распространенном поражении дна полости рта, для удобства доступа, язык прошивают лавсановыми нитями и смещают кверху. Язычные артерии при необходимости прошивают и перевязывают лавсаном.
Иногда в рану на слизистой оболочке устанавливают турунду с йодоформом (например, при иссечении опухолей твердого неба, из-за неподвижности слизистой оболочки и невозможности ушивания последней).
При хирургическом удалении эпулиса интактные зубы, находящиеся в пределах образования, стараются сохранить.
Лечение больных фиброматозом десен заключается в поэтапном иссечении патологической ткани до кости, включая надкостницу, одномоментно в пределах 6–8 зубов.
Удаление опухолей, расположенных в толще мягких тканей щеки со стороны полости рта производят либо под местной анестезией, либо под наркозом (зависит от размера опухоли и близости ее к слизистой оболочке).
С помощью электроножа производят разрез непосредственно над опухолевидным образованием мягких тканей щеки. Тупо и остро из мягких тканей щеки выделяют и удаляют опухолевидное образование. Производят гемостаз и ушивают рану кетгутовыми швами, после чего ее обрабатывают раствором бриллиантовой зелени или марганцовки.
Эти опухоли удаляются наружным доступом в редких случаях (при этом нужно помнить о анатомических особенностях расположения лицевого нерва).
Особо хочется отметить методы лечения гемангиом, поскольку они различаются в зависимости от распространенности последней.
В лечении обширных, распространенных кавернозных и ветвистых гемангиом широко используют комбинированный метод, включающий, на первом этапе склерозирующую терапию, на втором – хирургическое вмешательство, направленное на иссечение склерозированных иизмененных избыточных тканей.
Склерозирующая терапия основана на развитии асептического воспаления, ведущего к склерозированию и запустеванию сосудистых полостей. Для лечения используют химические препараты – 2% раствор салицилового спирта и чаще 70° этиловый спирт (Агапов B.C., 1990 и др.), который вводят в опухолевую ткань в количестве 5–90 мл в зависимости от размера гемангиомы. Он, попадая в полости и просветы сосудов, вызывает свертывание крови и слипчивое воспаление. После введения спирта тут же накладывают давящую повязку. В течение последующих 6–8 дней наблюдается отек и болезненный инфильтрат, затем наступает рубцевание. Повторное введение спирта проводят не ранее, чем через 2–4 недели после первой инъекции. В результате повторных курсов лечения опухоль уменьшается или исчезает.
Для лечения используют химические препараты – 2% раствор салицилового спирта и чаще 70° этиловый спирт (Агапов B.C., 1990 и др.), который вводят в опухолевую ткань в количестве 5–90 мл в зависимости от размера гемангиомы. Он, попадая в полости и просветы сосудов, вызывает свертывание крови и слипчивое воспаление. После введения спирта тут же накладывают давящую повязку. В течение последующих 6–8 дней наблюдается отек и болезненный инфильтрат, затем наступает рубцевание. Повторное введение спирта проводят не ранее, чем через 2–4 недели после первой инъекции. В результате повторных курсов лечения опухоль уменьшается или исчезает.
Склерозирующая терапия проводится как самостоятельный метод с прошиванием опухоли и с перевязкой приводящих и отводящих сосудов.
Электрокоагуляцию опухоли осуществляют с помощью электрокоагулятора, лучшие результаты дает внутритканевая коагуляция биактивными электродами. Электроды в виде двух игл вводят так, чтобы небольшая гемангиома оказалась между ними. В случае большой опухоли вкол электродов производят по периметру опухоли. В результате коагуляции поверхностных гемангиом образуется струп, при глубоких – инфильтрат, заканчивающийся рубцеванием. Возможно применение криовоздействия.
Послеоперационные осложнения
Осложнения после операций встречаются в основном в виде гематом, при нагноении которых назначается антибактериальная терапия, если есть, то снимаются швы и разводятся края раны для создания оптимального оттока гнойного отделяемого.
Из альтернативных методов лечения при доброкачественных новообразованиях полости рта применяют криодеструкцию или лазерную коагуляцию. Хороший эффект достигается применением СО2-лазера в режиме испарения.
Доброкачественные новообразования костей и хрящевой ткани
Одонотогенные новообразования – являются органоспецифическими, происхождение их связано с зубообразующими тканями, локализуются только в челюстных костях.
К доброкачественным одонтогенным опухолям, подлежащим хирургическому лечению, в первую очередь, относится амелобластома – доброкачественная одонтогенная эпителиальная опухоль, способная к инвазивному росту. Наблюдается в основном у лиц среднего возраста, в 80% случаев поражается нижняя челюсть. Безболезненная деформация челюсти нарастает постепенно, в течение нескольких лет, в виде вздутия.
Стандартная рентгенологическая картина характеризуется деструкцией кости в виде множественных очагов разрежения с четкими границами (поликистозный характер разрежения).
Вторая из опухолей, требующих скорейшего хирургического лечения это миксома-доброкачественная опухоль, обладающая местным инвазивным ростом. Она не имеет капсулы и, разрушая кость, прорастает в мягкие ткани.
Цементомы, амелобластическая фиброма, аденоматоидная одонтогенная опухоль, сложная и составная одонтома также являются одонтогенными опухолями, но встречаются гораздо реже.
Кисты челюстей – по частоте стоят на первом месте среди других одонтогенных образований. Киста представляет собой полость, выстланную оболочкой, которая состоит из соединительно-тканного слоя, прилегающего к кости, и эпителиального, обращенного в полость. Последняя обычно выполнена жидкостью. Рост кисты происходит за счет наличия внутрикистозного давления, которое приводит к атрофии окружающей костной ткани и пролиферации эпителия, что при отсутствии лечения может привести к патологическим переломам.
Последняя обычно выполнена жидкостью. Рост кисты происходит за счет наличия внутрикистозного давления, которое приводит к атрофии окружающей костной ткани и пролиферации эпителия, что при отсутствии лечения может привести к патологическим переломам.
Корневая (радикулярная) киста, как правило, обнаруживается в области разрушенного или леченного зуба.
Зубосодержащая (фолликулярная) киста развивается из эмалевого органа непрорезавшегося зуба, преимущественно третьего большого коренного и клыка.
Первичная киста (кератокиста) может переходить в злокачественную форму. Встречается редко.
Возникновение неодонтогенных кист челюсти связано с нарушением эмбриогенеза лица. Это щелевые (фиссуральные) кисты, локализуются на верхней челюсти, встречаются редко. К ним отнесены: киста носо-небного (резцового) канала, шаровидно-верхнечелюстная киста и носо-губная (носо-альвеолярная) киста.
Хирургическое лечение кист проводят, в основном, в амбулаторных условиях.
Костные опухоли. Из костных опухолей наибольшее число падает на гигантоклеточную опухоль. Редко встречающиеся новообразования (остеоид-остеома, хондрома, хондробластома, гемангиоэндотелиома и др.).
Гигантоклеточная опухоль (остеокластома) – доброкачественная опухоль, поражает различные кости скелета. Развивается внутрикостно. В центре опухоли замедляется движение крови, эритроциты оседают и распадаются, гемоглобин превращается в гемосидерин, придавая опухоли бурую окраску.
В челюстных костях встречается довольно часто, составляет 24% всех костных опухолей и опухолеподобных поражений. Отмечается преимущественная локализация в области нижней челюсти соответственно малым коренным зубам. На верхней челюсти опухоль развивается редко.
Опухоль выявляют только тогда, когда возникает выбухание участка челюсти или становятся подвижными зубы в пределах новообразования.
Диагностика гигантоклеточной опухоли только на основании клинико-рентгенологической картины не всегда возможна.
Для цитологического исследования пунктат получают через истонченную или отсутствующую кортикальную пластинку челюсти. В сомнительном случае проводят открытую биопсию.
Остеома –доброкачественное образование из зрелой костной ткани. Выделяют периферическую и центральную остеому. Периферическая остеома в виде костного образования округлой, реже неправильной формы соединяется с челюстью узким или довольно широким основанием, приводит к деформации лица.
Центральная остеома, исходящая из эндоста, располагается в глубине челюстной кости, имеет небольшой размер (до 1,5 см), протекает бессимптомно. Растут чрезвычайно медленно.
Функциональные расстройства могут возникнуть при локализации остеомы на верхней челюсти в виде диплопии, затруднения носового дыхания, располагаясь на скуловой дуге, вызывает ограничение открывания рта.
Остеоид-остеома, остеобластома и оссифицирующаяся фиброма (фиброостеома)– различаются клинически и рентгенологически, встречаются редко. Распространенные опухоли вызывают деформацию челюсти.
Распространенные опухоли вызывают деформацию челюсти.
К операциям прибегают в основном по эстетическим и функциональным показаниям, а также в случае необходимости зубного протезирования.
Хрящеобразующие опухоли продуцируют патологическую хрящевую ткань. Они занимают до 5% случаев всех костных новообразований.
Хондрома – локализуется преимущественно в переднем отделе верхней челюсти в виде изолированного солитарного узла. Растет медленно, деформирует челюсть. При периферической форме проявляется в виде четкого, бугристого, плотного на ощупь, безболезненного образования, связанного с подлежащей костью. Энхондрома развивается незаметно в глубине кости, приводят к подвижности и смещению зубов в стороны. Диагностируется значительно позже, когда опухоль, разрушив кость, распространяется кнаружи. Слизистая оболочка полости рта обычно не изменяется. При длительном существовании отмечена возможность злокачественного превращения хондромы в хондросаркому.
Остеохондрома (костно-хрящевой экзостоз) – доброкачественное образование, покрытое хрящом, локализуется на суставной головке нижней челюсти. Встречается редко. В начальном периоде заболевания возникает хруст или неприятные ощущения в области одного из височно-нижнечелюстных суставов. Постепенно (в течение 1–2 лет) развивается и нарастает деформация лица, нарушается прикус, становится затрудненным откусывание и пережевывание пищи.
Центральная гигантоклеточная гранулема (гигантоклеточная репаративная гранулема) – опухолеподобное поражение кости с локализацией исключительно в альвеолярной части челюсти в виде ограниченного опухолевидного образования на десне.
Идентичное поражение, развивающееся только в мягких тканях десны без вовлечения в процесс кости, называют периферической гигантоклеточной гранулемой и рассматривают в группе опухолеподобных поражений мягких тканей. Ранее оба эти вида относили к гигантоклеточному эпулису.
Фиброзная дисплазия – опухолеподобное поражение кости, заключающееся в очаговом нарушении костеобразования. Заболевание чаще выявляется у детей, однако иногда, медленно прогрессирует в течение многих лет и обнаруживается уже у взрослого человека.
Клинические проявления мало характерны. Отмечают более частое поражение верхней челюсти, при этом возникает деформация за счет безболезненного, медленно увеличивающегося выбухания костной плотности.
Полиоссальное поражение костей мозгового, лицевого черепа и челюстей дает картину костной львиности лица.
Рентгенологическая картина довольно типична. Определяется диффузное увеличение пораженного отдела кости с деструкцией костной ткани в виде чередования мелких участков уплотнения и разрежения, наблюдается, так называемая, картина «матового стекла».
В случае стабилизации процесса, которая, как правило, наблюдается десятками лет, ограничиваются лишь динамическим наблюдением. Операция возможна только при возникновении функциональных нарушений.
Аневризмальная костная киста – относится к опухолеподобным поражениям, встречается редко. Поражает в основном молодых лиц, при этом наблюдается сравнительно быстро увеличивающееся (в течение нескольких месяцев) выбухание участка кости, которое может быть безболезненным. Такие симптомы дают подозрение на злокачественное течение.
При пункции образования шприц свободно наполняется кровью. В некоторых случая трудно дифференцировать от гигантоклеточной опухоли.
Неврилеммома, десмопластическая фиброма и хондробластома встречаются очень редко, протекают как другие доброкачественные внутрикостные опухоли. Диагноз чаще устанавливают после микроскопического исследования удаленной опухоли.
Особенности операций при доброкачественных новообразованиях
костей и хрящевой ткани
Операции при кистах – цистотомия и цистэктомия
Показаниями к цистэктомии являются: 1)киста, как следствие порока развития одонтогенного эпителия, 2)киста небольших размеров, расположенная в пределах 1-2 интактных зубов, 3)обширная киста нижней челюсти, при которой отсутствуют зубы в ее зоне и сохранено достаточной толщины (до 1 см) основание челюсти, препятствующее патологическому перелому, 4)киста больших размеров на верхней челюсти, не имеющая зубов, с сохраненной костной стенкой дна полости носа, а также прилегающая к верхнечелюстной пазухе или оттесняющая ее, без явлений воспаления пазухи.
Показания к цистотомии: 1)киста, в полость которой проецируется 3 и более интактных зубов, на рентгенограмме у корней последних не определяется периодонтальная щель, 2) большие кисты верхней челюсти с разрушением костного дна полости носа и небной пластинки, 3) обширные кисты нижней челюсти с резким истончением (толщиной кости менее 1–0,5 см) основания челюсти, при этом частичное сохранение кистозной оболочки является одной из мер профилактики патологического перелома.
Предоперационная подготовка зубов для цистотомии в отличие от цистэктомии касается только «причинного зуба», остальные, хотя и вовлечены в зону кисты, после цистотомии остаются прикрытыми ее оболочкой. Показанием к ороназальной цистэктомии служит отсутствие зубов в пределах кисты, либо вовлечение лишь одного- двух в ее зону. Ороназальную цистотомию применяют при наличии большого количества интактных зубов, проецирующихся в полость кисти.
Пластическая цистэктомияприменяется при отсутствии гарантии первичного заживления раны после цистэктомии, а также в случае рецидива кисты. Операция может быть исходом цистэктомии, осложнившейся нагноением.
Операция может быть исходом цистэктомии, осложнившейся нагноением.
Двухэтапная операция кисты.Вариант хирургического вмешательства, сочетающий оба основных вида операций, при котором в 1-й этап проводят декомпрессионную операцию по типу цистотомии. 2-й этап, когда через определенный промежуток времени произойдет восстановление истонченной или отсутствующей костной ткани, заканчивается цистэктомией. Показанием к операции на верхней челюсти служит киста, сопровождающаяся разрушением костного дна полости носа, на нижней челюсти, занимающая тело и ветвь. В 1-й этап создают сообщение с полостью рта по типу цистотомии, но меньшего диаметра, однако достаточное для осуществления оттока из кистозной полости на продолжительный срок. 2-й этап операции проводится через различные промежутки времени в среднем от 0,5 года до 1,5–2 лет. Двухэтапная операция является сберегающей, не травматичной, проводят ее амбулаторно. Позволяет сохранить контуры и размеры челюсти, несмотря на обширность поражения, и приводит к полному излечению больного.
С целью профилактики патологического перелома в послеоперационном периоде больным проводится двучелюстное шинирование.
Операции при опухолях.
Хирургическое лечение большинства доброкачественных опухолей заключается в их удалении в пределах здоровых тканей (иногда фрезой, пилой Джильи или при помощи долота.
Ввиду того, что выскабливание опухоли часто ведет к рецидиву и возможно ее злокачественное перерождение, то предпочтительна резекция челюстей.
В зависимости от распространенности опухоли резекция нижней челюсти может быть с сохранением (экономной) и с нарушением ее непрерывности (возможна одномоментная костная пластика). У соматически отягощенных больных применяют метод экскохлеации опухоли с обработкой подлежащей кости борами, высверливания элементов опухоли из едва заметных бухт. В последнее время у этой группы больных стали применять более щадящий метод – декомпрессионную операцию по типу цистотомии, которая снимает внутриполостное давление и, создавая постоянный отток экссудата из кистозных полостей, предупреждает развитие острого гнойного воспаления.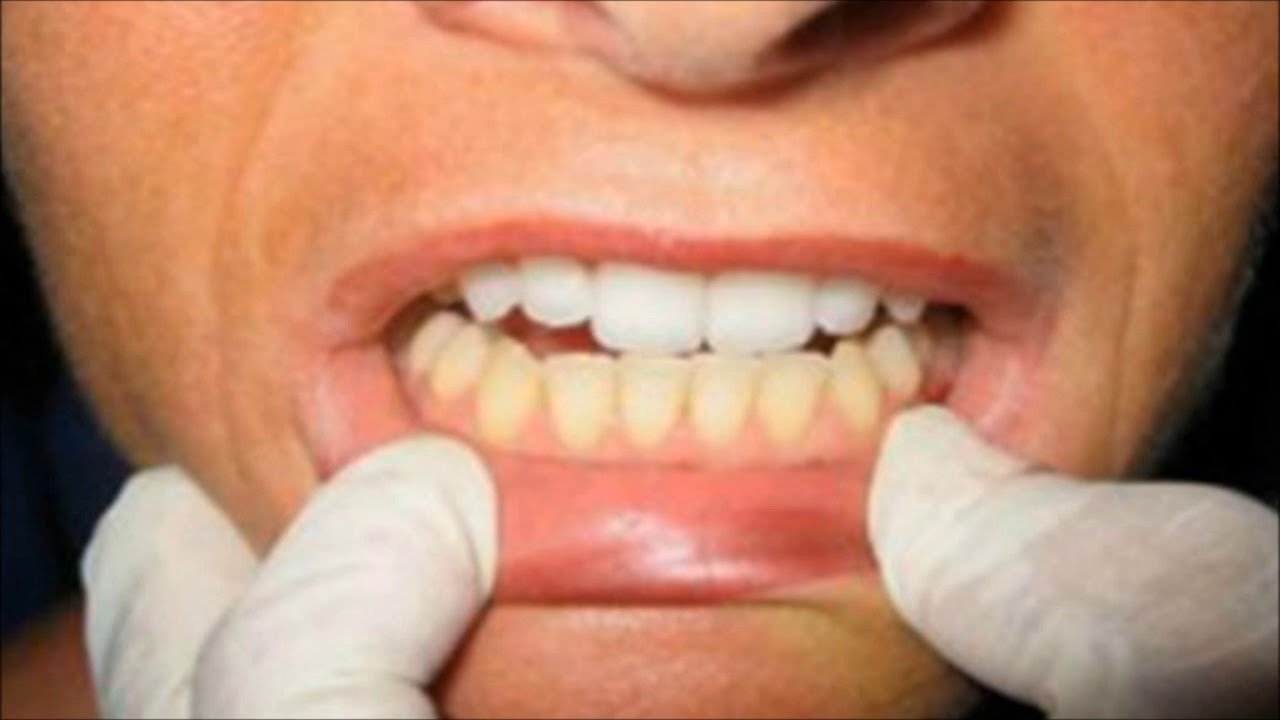
Лечение остеоид-остеомы и остеобластомы проводится в виде выскабливания патологической ткани до здоровой, при этом в случае остеоид-остеомы рекомендуется с помощью фрезы удалять окружающую склерозированную кость.
При остеохондроме выполняют хирургическое иссечение новообразования вместе с мыщелковым отростком. Наилучшие результаты дает одномоментная, артропластика гомотрансплантатом.
При цементобластоме и цементирующейся фиброме хирургическое лечение заключается в вылущивании опухоли с капсулой. В случаях периапикальной цементной дисплазии и гигантоформной цементомы, являющимися опухолеподобными поражениями, возможно лишь динамическое наблюдение и оперативное лечение проводят лишь при необходимости (невозможность зубного протезирования ввиду деформации челюсти).
Резекция нижней челюсти проводится под наркозом. Доступ наружный, возможен и внутренний. Необходимо помнить о том, что в подчелюстной области проходит лицевая артерия и нижняя ветка лицевого нерва.
После выделения тела нижней челюсти пилой Джильи производят перепиливание последнего у 1–2 резца. Кровотечение из кости останавливают коагуляцией, при невозможности – воском.
Кровотечение из кости останавливают коагуляцией, при невозможности – воском.
Ветвь перепиливают проволочной пилой или перекусывают кусачками.
При доброкачественных опухолях образовавшийся дефект челюсти восстанавливают различными способами одномоментно, при злокачественных – это целесообразно делать через определенное время (чаще после 1 года) с предварительным обследованием больного.
На верхней челюсти с диагностической и лечебной целью выполняют гайморотомию. Разрез делают по переходной складке в области 4–5 премоляров. Бором или долотом вскрывают гайморову пазуху.
Удаляют имеющееся там образование и в полость устанавливают йодоформную турунду.
Она выводится через нижний носовой ход, а рана на слизистой оболочке в области переходной складки ушивается кетгутом.
Турунда удаляется после премедикации через 7–8 дней после операции.
Литература
- Белоусов А.
 Е. Пластическая, реконструктивная и эстетическая хирургия. – СПб.: Гиппократ, 1998. – 744 c.
Е. Пластическая, реконструктивная и эстетическая хирургия. – СПб.: Гиппократ, 1998. – 744 c. - Карапетян И.С, Губайдуллина Е.Я., Цегельник Л.Н. Опухоли и опухолеподобные поражения органов полости рта, челюстей, лица и шеи. МИА, Москва, 2004, 232 с.
- Неробеев А.Л. Boccтaнoвлeниe ткaнeй гoлoвы и шeи cлoжными apтepиaлизиpoвaнными лocкyтaми. – M.: Meдицинa, 1988.
- Пачес А.И. Опухоли головы и шеи. – 4-е изд. – М.: Медицина, 2000. 430 с.
- Уртаев Б.М., Гусов Т.Ю., Ярема Р.И. Лимфологическая профилактика воспалительных осложнений при протезировании зубов несъемными ортопедическими конструкциями // Хирург. – 2007. – № 2. – С. 42–46.
- Ярема В.И., Ярема Р.И. Хирургическая коррекция дефектов орофарингеальной области методом аутотрансплантации анатомических структур шеи // Хирург. – 2007. – № 6. – С. 8–17.
- Kay S. Microvaskular surgery // Surgery (Int. Edition).
 – 1991. – Vol. 12. – P. 2130–2136.
– 1991. – Vol. 12. – P. 2130–2136. - Maurer P., Eckert A.W., Schubert J. Functional rehabilitation following resection of the floor of the mouth: the nasolabial flap revisited // J. Cranio-maxillofacial Surg. – 2002. – Vol. 30 (6). – P. 369–372.
Вернуться
Диагностика предраковых изменений полости рта в Кирове
ЛЮМИНЕСЦЕНТНАЯ СТОМАТОСКОПИЯ
Люминесцентная (аутофлуоресцентная) стоматоскопия – оптический метод визуализации патологических изменений слизистой оболочки рта.
Современные клинические исследования подтверждают, что в месте злокачественного перерождения слизистой оболочки происходит резкое уменьшение интенсивности её аутофлуоресцентного (эндогенного) свечения, обусловленное морфологическими и биохимическими изменениями, характерными для развития дисплазии и рака.
С целью активного выявления предопухолевых заболеваний и ранних стадий злокачественных новообразований органов и тканей рта в программе онкоскрининга наряду с традиционным осмотром рта и пальпацией регионарных лимфоузлов проводится люминесцентная (аутофлуоресцентная) стоматоскопия.
Онкоскрининг необходимо проходить:
- Ежегодно всем лицам.
- При наличии факторов риска – 2 раза в год.
- При отягощенной наследственности – 1-2 раза в год.
- При наличии предраковых изменений полости рта (лейкоплакия, эритроплакия ) – 2-4 раза в год.
- При наличии хронических травм слизистой полости рта (частое прикусывание)– 2-4 раза в год.
Как проводиться обследование?
- При освещении полости рта стоматоскопом возникает эндогенное или аутофлуоресцентное свечение, которое врач может наблюдать через специальные очки в условиях затемнения
- Нормальная слизистая оболочка рта имеет зеленое свечение различной интенсивности
- Очаги раннего предрака и рака имеют аномальное свечение
- Выявление аномального свечения позволяет проявить онкологическую настороженность при первичном осмотре пациента
Гистология — стандарт в диагностике предрака и ранних форм рака слизистой оболочки рта!
Наши врачи-стоматологи не ставят диагноз, доктора проявляют онкологическую настороженность!
Записаться на обследование можно на сайте https://centrmedi. ru/ или по телефону 8(8332) 755-355.
ru/ или по телефону 8(8332) 755-355.
Обследование проводит врач-стоматолог-пародонтолог клиники MEDI Чигарских Анна Сергеевна.
MEDI — МЕДИ
Онкология
© А.А. Доманин, А.Ф. Солнышкина, 2011
УДК 616.311-006.6-07
Тверская государственная медицинская академия
Рост заболеваемости раком и предраковыми поражениями слизистой оболочки полости рта (СОПР), поражение лиц трудоспособного возраста, высокий процент послеоперационных осложнений и рецидивов, проблемы классификации, сложности морфологической верификации и прогнозирования свидетельствуют об актуальности этой проблемы. Согласно Международной гистологической классификации опухолей (ВОЗ, № 4), эти заболевания отнесены к группе патологических процессов полости рта и ротоглотки. Однако эксперты ВОЗ прямо указывают, что ни с теоретической, ни с практической точки зрения их не следует рассматривать как единую группу.
Целью данного исследования явилось комплексное клинико-морфологическое изучение предраковых поражений СОПР, особенностей их эпидемиологии, вскрытие механизмов морфогенеза, нарастания дисплазии и закономерностей озлокачествления, выявление критериев для ранней диагностики и прогнозирования. Материалом служили результаты патоморфологического исследования биопсийного и операционного материала от 719 больных (409 мужчин и 310 женщин) с различными заболеваниями СОПР и губы, находившихся в лечебных учреждениях г. Твери, среди которых пациентов с предопухолевы-ми процессами было 139.
Материалом служили результаты патоморфологического исследования биопсийного и операционного материала от 719 больных (409 мужчин и 310 женщин) с различными заболеваниями СОПР и губы, находившихся в лечебных учреждениях г. Твери, среди которых пациентов с предопухолевы-ми процессами было 139.
Полученные результаты продемонстрировали, что предопухолевые заболевания СОПР и губы представляют собой собирательную группу нозологических форм, которые можно разделить на факультативный и облигатный предрак, каждая из которых может быть самостоятельным заболеванием либо последовательной морфогенетической стадией единого процесса. Их доля в общей структуре заболеваемости СОПР составляет 19,3%.
В Тверской области из числа предраковых процессов встречаются: плоская, бляшечная, бородавчатая, эрозивно-язвенная лейкоплакии (вместе составляют 46,0% всех предопухолевых и опухолевых состояний этой анатомической зоны), для которых характерно прогрессивное нарастание диспластических изменений и возможна малигнизация; папилломатоз (43,9%), эритроплакия (2,9%) и эритроплазия Кейра (2,2%), а также болезнь Боуэна (2,9%).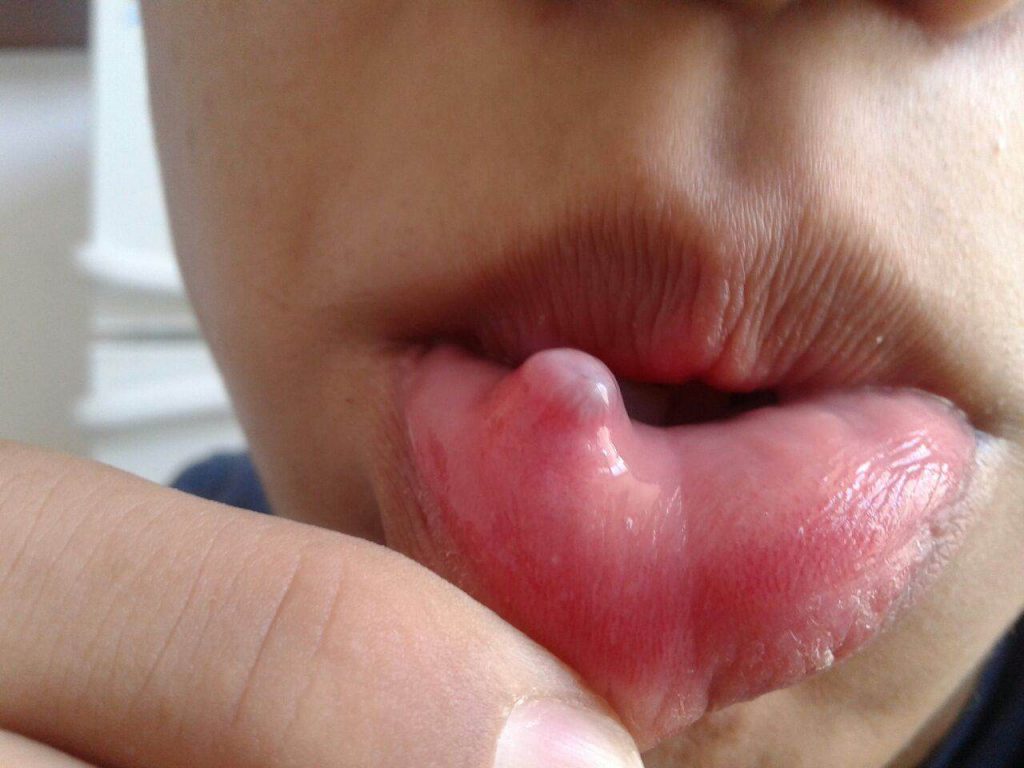 К облигатному предра-ку следует относить эритроплазию Кейра, а болезнь Боуэна верифицировать как рак in situ.
К облигатному предра-ку следует относить эритроплазию Кейра, а болезнь Боуэна верифицировать как рак in situ.
К характерным особенностям предопухолевых поражений данной анатомической зоны относятся: преимущественное поражение лиц трудоспособного возраста и мужского пола; позднее обращение пациентов за медицинской помощью, несмотря на доступность для визуального обследования; частое сочетание разных структурных форм патологии в пределах одного очага поражения; выраженный полиморфизм и сложность дифференциальной пато-морфологической диагностики различных вариантов предрака. Патоморфологическое своеобразие данной группы заболеваний проявляется полиморфизмом многослойного плоского эпителия, наличием дистрофических и диспластических его изменений, кой-лоцитозом (признак вирусного генеза заболеваний, встречающийся при некоторых формах предрака СОПР в 80%), короткодистантным ангиогенезом с ангиоматозом и редкими аваскулярными зонами, дисциркуляторными нарушениями, различными величинами пролиферативного (Ki-67) и антиапопто-тического (bcl-2) индексов, нетипичной иммунокле-точной реакцией разной интенсивности с обилием эозинофильных лейкоцитов, активность которых имеет прогностическое значение из-за способности синтезировать мелатонин и мексамин.
Принимая во внимание частое сочетание различных форм предраковой патологии в пределах одного очага поражения с разной степенью дисплазии и риском озлокачествления, необходимо считать обязательным патогистологическое изучение всех тканей поврежденной зоны на серийных гистотопографи-ческих срезах, не допуская фрагментации операционного материала. Следует максимально тщательно проводить дифференциальную микроскопическую диагностику предраковых процессов СОПР и губы, учитывая ее сложность, выраженный полиморфизм заболеваний, темпы увеличения степени дисплазии эпителия, потенциальную опасность малигнизации.
Энергетический дисбаланс клеток в зоне поражения (феномен Вабурга) определяет их метаболические сдвиги, структурное своеобразие, приобретение атипичного фенотипа, повреждение тиолового механизма деления, нетипичность динамики клеточных реакций в зоне патологии как своеобразный ответ эпителиоцитов на повреждения различного рода в виде нарушений дифференцировки, увеличивающий неустойчивость генома. Имеется прямая зависимость между увеличением индекса пролиферации клеток и показателями экспрессии онкопротеина bcl-2 — антагониста апоптоза, активность которых отражает степень дифференцировки эпителиальных клеток.
В зависимости от того, на каком уровне эпителиального пласта канцерогенные факторы оказывают свое влияние, следует ожидать возникновения разных гистологических вариантов рака: от базальноклеточ-ного до плоскоклеточного разной степени зрелости, поскольку каждый слой эпителия секретирует свой тип цитокератина. Иммуногистохимическое изучение экспрессии цитокератинов продемонстрировало, что даже при дисплазии эпителиальные клетки способны приводить к увеличению сложности цитокератино-вого набора, что отражает неполноценность синтеза этих соединений.
Для проведения своевременной микроскопической диагностики и особенно клинического прогнозирования целесообразно рекомендовать в качестве дополнительных методов морфологического исследования анализ проявлений койло-цитоза, кинетики иммуноклеточных инфильтратов и ангиогенеза, тканевой эозинофилии, индекса пролиферации эпителия (Ki-67), экспрессии онко-протеина bcl-2, ингибирующего апоптоз, изменения цитокератинового «профиля» при данных патологических процессах.
Опухоли головы и шеи. Аспекты ранней диагностики и лечения
Количество пациентов, у которых выявляется онкологическая патология головы и шеи растет с каждым годом. Ежегодно в мире диагностируется более 400000 случаев заболеванием раком головы и шеи. В Кореличском районе диагноз рак органов головы и шеи выявляется у 5-6 человек ежегодно…
В структуре заболеваемости злокачественными новообразованиями рак головы и шеи составляет 3-4%, а в структуре смертности от злокачественных новообразований удельный вес опухолей слизистой полости рта и ротоглотки составляет 2,8%.
В половом отношении рак чаще развивается у мужчин, чем у женщин в 5-7 раз, соотношение 7:1, в возрастном эквиваленте чаще в возрасте 50-70 лет. По Кореличскому району статистика мужчины и женщины составляет 9:1, возраст 48-75 лет.
Локализация первичного очага в полости рта располагается следующим образом: язык 50-75%, дно полости рта 20-35%, другие структуры полости рта до 15%.
Причиной возникновения и фактором риска развития заболевания более чем у 90% случаев является курение и употребление алкоголя. У излеченных пациентов риск рецидива заболевания у курящих составляет 40-60%.
Предраковые заболевания, те заболевания, которые при отсутствии своевременного лечения приводят к озлокачествлению. К ним относятся: лейкоплакия – хроническое повреждение слизистой полости рта, вид – участок слизистой бледного цвета, ткани вокруг бледно-розовые; эритроплакия – участок слизистой с рыхлыми красными пятнами; дисплазия – участки слизистой полости рта, возвышающиеся над слизистой, бледного цвета.
Выживаемость после лечения зависит от ранней диагностики и на какой стадии выявлено заболевание. Так общая выживаемость больных раком слизистой оболочки полости рта и ротоглотки составляет 40%. Пятилетняя выживаемость при I стадии 80-85%; II стадии 70-75%; III стадии до 65%; при IV стадии до 30%.
Для раннего выявления патологического процесса нужна совместная работа пациента и врача.
Для самоконтроля и раннего выявления заболевания необходимо обратить внимание на наличие: патологического ощущения в полости рта, боли и/или помехи в глотке, постоянная осиплость, дисфагия (затрудненное глотание), образования в полости рта, на шее и носу, заложенность носа и в ухе, кровянистые выделения из носа.
Если хотя бы 1 из этих симптомов сохраняется более 3 недель необходимо обратиться к врачу. Раннее обращение к специалисту и ранняя постановка диагноза спасают ЖИЗНЬ. Не отказывайтесь.
Врач оториноларинголог
Князик А.И.
Елецкая стоматологическая поликлиника | Новости
Рак полости рта: причины, симптомы, лечение и прогнозы при раке щеки, неба, языка, десны, дна полости рта
Причины
Не установлено точной причины, приводящей к появлению новообразований во рту. Исследователи лишь выявили ряд факторов, которые в значительной мере повышают вероятность развития этого заболевания. Ключевыми среди них являются вредные привычки — курение, жевание насвая или бетеля, а также злоупотребление алкоголем.
Дополнительными факторами являются:
-Хронические механические травмы ротовой полости.
-Использование некачественных или плохо подогнанных зубных протезов.
-Плохая обработка пломб и травмы зубов — острые края пломб и сломанных зубов вызывают постоянное травмирование слизистой щек и языка.
-Травмы десен стоматологическими инструментами.
-Плохое соблюдение гигиены.
-Применение в зубном протезировании металлических протезов из разных металлов — между разными металлами может возникать гальваническое напряжение, что ведет к повреждению клеток и их малигнизации.
Отмечена повышенная частота развития этой патологии у лиц, работающих в тяжелых и вредных условиях: в постоянном контакте с вредными веществами, в условиях с повышенной или чрезмерно низкой температурой и высокой влажностью.
Воздействие острой и горячей пищи также способствует формированию опухолей на слизистой оболочке рта. Усугубляет ситуацию дефицит в пище витамина A и наличие в полости рта воспаления или предракового заболевания.
Предраковые заболевания, способные переродиться в рак слизистой полости рта
Лейкоплакия . Выглядит как белесое пятнышко на слизистой в любой области полости рта: на небе, на щеках возле губ с внутренней стороны. Характеризуется участками ороговения эпителия.
Эритроплакия . Характеризуется появлением красных очагов, обильно пронизанных кровеносными сосудами. До половины случаев эритроплакии трансформируются в онкологию.
Дисплазия — собственно предрак. Исследование диспластических очагов под микроскопом показывает, что часть клеток уже приобрела черты злокачественности. В случае игнорирования этой патологии в 99% случаев через несколько месяцев развивается рак полости рта.
Симптомы и стадии рака ротовой полости
На самой начальной стадии рак слизистой рта может ничем не беспокоить, лишь часть пациентов ощущает какой-то необычный дискомфорт во рту. При осмотре можно увидеть трещину на слизистой, небольшой бугорок или уплотнение. Около трети раковых больных жалуются на невыраженные боли, которые маскируются под симптомы воспалительных заболеваний: глоссита, гингивита.
Прогресс заболевания обычно сопровождается усилением болевого синдрома, даже если воспаление уже прошло. Боль может иррадиировать в лоб, висок, челюсть. Очень часто больные связывают эти боли с зубными.
Несвоевременная диагностика позволяет болезни перейти в запущенную стадию, когда развиваются следующие симптомы рака полости рта:
-Появляется язва или нарост на слизистой.
-Распад опухоли сопровождается неприятным гнилостным запахом.
-Боль становится постоянной.
В запущенных случаях к симптомам опухоли рака слизистой оболочки полости рта присоединяется деформация лица за счет прорастания патологической ткани в окружающие структуры: мышцы и кости. Нарастают симптомы интоксикации: пациенты жалуются на общую слабость, быструю утомляемость, тошноту.
Классификация
По своей микроскопической структуре рак слизистой полости рта относится к плоскоклеточному типу. Выделяют несколько его форм:
-Ороговевающий плоскоклеточный рак. Выглядит как скопление ороговевшего эпителия («раковые жемчужины»). Составляет до 95% случаев развития патологии данной локализации.
-Неороговевающий плоскоклеточный. Проявляется разрастанием раковых клеток эпителия без участков ороговения.
-Низкодифференциированный(карцинома). Это самая злокачественная и труднодиагностируемая форма.
-Рак слизистой рта in situ. Самая редкая форма.
В зависимости от особенностей роста опухоли, различают следующие ее формы:
-Язвенная — это одна или несколько язв, постепенно разрастающихся и склонных к росту и слиянию. Обычно дно язв покрыто налетом неприятного вида.
-Узловатая — характеризуется появлением на слизистой плотного нароста в виде узла, покрытого белесыми пятнами.
-Папиллярная — проявляется быстрорастущими, плотными наростами, напоминающими бородавки. Выросты обычно сопровождает отек подлежащих тканей.
Отдельные формы рака слизистой ротовой полости
-Рак языка. Типичным местом локализации патологии является боковая поверхность языка, реже опухоль обнаруживается на корне языка, спинке или на нижней поверхности. Злокачественная опухоль уже на ранних стадиях ведет к расстройству жевания и глотания, что облегчает диагностику.
-Рак слизистой щеки. Эта опухоль часто маскируется под афтозные язвы, находящиеся на линии рта на щеках. Увеличение язвы в диаметре и прорастание ее в жевательные мышцы приводит к ограничению в открытии рта, что является типичным симптомом рака щеки.
-Рак неба и десны верхней челюсти. На небе образуется быстрорастущий узел со склонностью к изъязвлению. Может отмечаться раннее появление болевого синдрома, особенно в тех ситуациях, когда поражаются более глубокие ткани.
-Рак слизистой оболочки дна полости рта. Первые признаки заболевания практически всегда остаются незамеченными. Опухоль рано прорастает в окружающие ткани, в том числе и в костные. Онкопроцесс часто сопровождается повышенной саливацией (слюнотечением), опасен развитием кровотечений. Разрастание опухоли с поражением костной ткани нижней челюсти сопровождается деформацией лица.
-Рак слизистой на альвеолярных отростках. На ранней стадии сопровождается проблемами с зубами — пациентов беспокоит зубная боль, зубы расшатываются и выпадают, опухают десны. Типичное явление — кровотечение из лунки выпавшего зуба.
Диагностика
Диагноз ставится на основании жалоб пациента и после осмотра слизистой рта. Подтвердить диагноз помогает биопсия опухоли. Технологичные методы диагностики, такие как УЗИ или томография, при данных опухолях не очень информативны. Чтобы выявить поражение костных тканей нижней и верхней челюстей больному назначают рентген лицевого скелета.
Чаще первыми новообразования в полости рта замечают врачи стоматологи в связи с особенностями своей профессии. При выявлении первых признаков онкологии во рту пациент обязательно направляется на консультацию к онкологу.
Профилактика
Главное профилактическое значение в борьбе с раком слизистой ротовой полости имеет отказ от вредных привычек. Обязательно следует бросить курить, жевать бетель, употреблять насвай. Рекомендуется отказаться от алкоголя.
Снижение травматизации щек, языка, десен также позволяет снизить риск возникновения опухолей описываемой локализации. Все зубы должны быть вылечены, установленные пломбы должны быть обработаны. При необходимости в протезировании следует очень тщательно подбирать протез, чтобы он был удобен в эксплуатации и не доставлял дискомфорта.
Из рациона должны быть исключены продукты с раздражающим действием, не следует употреблять очень горячую пищу. При появлении первых признаков и симптомов онкологии ротовой полости необходимо сразу обратиться к специалисту.
С регулярностью не реже одного раза в год, а при выявлении предраковых состояний каждый квартал, нужно проходить профилактические осмотры у стоматолога и онколога.
Подготовил врач-стоматолог-хирург Кузьмин Д.К.
(по материалам интернета)
Лейкоплакия и эритроплакия — предраковые плоские поражения полости рта: определение, этиология, эпидемиология
Гейл Н., Пильч Б.З., Сидранский Д. и др. Поражения предшественников эпителия. В: Barnes L, Eveson JW, Reichart P, Sidranksy D, eds. Классификация опухолей Всемирной организации здравоохранения. Патология и генетика опухолей головы и шеи . Лион, Франция: IARC Press; 2005. 177-9.
Speight PM. Обновленная информация о дисплазии эпителия полости рта и прогрессировании рака. Голова Шея Патол . 2007 Сентябрь 1 (1): 61-6. [Медлайн].
Sciubba J, Scully C. Лейкоплакия полости рта. BMJ Best Practice (подписка). Доступно по адресу http://bestpractice.bmj.com/best-practice/monograph/621/highlights/summary.html. Обновлено: 8 июля 2016 г .; Доступ: 13 апреля 2017 г.
Грир РО. Патология злокачественных и предраковых поражений эпителия полости рта. Otolaryngol Clin North Am . 2006 Apr. 39 (2): 249-75, v. [Medline].
Вениг BM. Плоскоклеточный рак верхних отделов пищеварительного тракта: предшественники и проблемные варианты. Мод Pathol . 2002 15 марта (3): 229-54. [Медлайн].
Эль-Наггар А.К., Рейхарт, Пенсильвания. Пролиферативная веррукозная лейкоплакия и предраковые состояния. В: Barnes L, Eveson JW, Reichart P, Sidranksy D, eds. Классификация опухолей Всемирной организации здравоохранения. Патология и генетика опухолей головы и шеи .Лион, Франция: IARC Press; 2005. 180.
Gillenwater AM, Vigneswaran N, Fatani H, Saintigny P, El-Naggar AK. Пролиферативная веррукозная лейкоплакия (ПВЛ): обзор неуловимого патологического образования !. Адв. Анат Патол . 2013 Ноябрь 20 (6): 416-23. [Медлайн].
Gillenwater AM, Vigneswaran N, Fatani H, Saintigny P, El-Naggar AK. Пролиферативная бородавчатая лейкоплакия: распознавание и дифференциация от обычной лейкоплакии и имитации. Голова Шея . 2014 ноябрь 36 (11): 1662-8. [Медлайн].
Ярдимчи Г., Кутлубай З., Энгин Б., Тузун Ю. Предраковые поражения слизистой оболочки рта. World J Clin Cases . 2014 16 декабря. 2 (12): 866-72. [Медлайн].
Пай SI, Westra WH. Молекулярная патология рака головы и шеи: значение для диагностики, прогноза и лечения. Анну Рев Патол . 2009. 4: 49-70. [Медлайн].
Джонсон Н., Шмид С., Франчески С. и др.Плоскоклеточная карцинома. В: Barnes L, Eveson JW, Reichart P, Sidranksy D, eds. Классификация опухолей Всемирной организации здравоохранения. Патология и генетика опухолей головы и шеи . Лион, Франция: IARC Press; 2005. 168-75.
McLemore MS, Haigentz M Jr, Smith RV и др. Плоскоклеточный рак головы и шеи у ВИЧ-инфицированных пациентов: предварительное исследование вирусных ассоциаций. Голова Шея Патол . 2010 июн. 4 (2): 97-105. [Медлайн].
Napier SS, Speight PM.Естественная история потенциально злокачественных поражений и состояний полости рта: обзор литературы. Дж. Орал Патол Мед . 2008 г., 37 (1): 1-10. [Медлайн].
Швам З.Г., Джадсон Б.Л. Улучшенный прогноз для пациентов с плоскоклеточным раком полости рта: анализ национальной базы данных по раку 1998-2006 гг. Оральный онкол . 2016 Январь 52: 45-51. [Медлайн].
Llewellyn CD, Johnson NW, Warnakulasuriya KA. Факторы риска плоскоклеточного рака полости рта у молодых людей — комплексный обзор литературы. Оральный онкол . 2001 июл. 37 (5): 401-18. [Медлайн].
Munde A, Karle R. Пролиферативная веррукозная лейкоплакия: обновление. J Cancer Res Ther . 2016 апр-июн. 12 (2): 469-73. [Медлайн].
Speight PM, Абрам Т.Дж., Флориано П.Н. и др. Согласие между наблюдателями в оценке дисплазии: к усиленному золотому стандарту клинических исследований патологии. Oral Surg Oral Med Oral Pathol Oral Radiol . 2015 Октябрь 120 (4): 474-82.e2. [Медлайн].
Гудсон М.Л., Слоан П., Робинсон К.М., Кокс К., Томсон П.Дж. Поражения-предшественники полости рта и злокачественная трансформация — кто, где, что и когда ?. Br J Oral Maxillofac Surg . 2015 Ноябрь 53 (9): 831-5. [Медлайн].
Веред М., Аллон I, Даян Д. Маспин, p53, p63 и Ki-67 в эпителиальных поражениях языка: от гиперплазии через дисплазию до карциномы. Дж. Орал Патол Мед . 2009 Март 38 (3): 314-20. [Медлайн].
Уэйн С., Робинсон РА. Плоская дисплазия верхних отделов пищеварительного тракта: корреляция с экспрессией p16, p53, pRb и Ki-67. Arch Pathol Lab Med . 2006 Сентябрь 130 (9): 1309-14. [Медлайн].
Курокава Х., Мацумото С., Мурата Т. и др. Иммуногистохимическое исследование подавления синдекана-1 и экспрессии белка p53 или антигена Ki-67 при лейкоплакии полости рта с или без эпителиальной дисплазии. Дж. Орал Патол Мед .2003 Октябрь, 32 (9): 513-21. [Медлайн].
Сайто Т., Накадзима Т., Моги К. Иммуногистохимический анализ белков p16, pRb, p53, p27 и Ki-67, связанных с клеточным циклом, при раке полости рта и предраке с особым упором на бородавчатую карциному. Дж. Орал Патол Мед . 1999 Май. 28 (5): 226-32. [Медлайн].
Каннан С., Баларам П., Чандран Дж. Дж. И др. Дифференциальная экспрессия белков цитокератина во время опухолевой прогрессии в слизистой оболочке полости рта. Биол эпителиальных клеток . 1994. 3 (2): 61-9. [Медлайн].
Рам Прассад В.В., Нирмала Н.Р., Котян МС. Иммуногистохимическая оценка экспрессии цитокератина 19 при различных гистологических степенях лейкоплакии и плоскоклеточного рака полости рта. Индийский J Dent Res . 2005 январь-март. 16 (1): 6-11. [Медлайн].
Филлис Т., Йогшис М., Кляйнхайнц Дж., Брандт Б., Йоос У., Бюргер Х. Изменение цитокератина при лейкоплакии полости рта и плоскоклеточной карциноме полости рта. Онкол Реп . 2007 сентября 18 (3): 639-43. [Медлайн].
Анджеро Ф, Беренци А., Бенетти А. и др. Экспрессия белков p16, p53 и Ki-67 при прогрессировании эпителиальной дисплазии полости рта. Anticancer Res . 2008 сен-окт. 28 (5A): 2535-9. [Медлайн].
Cruz IB, Snijders PJ, Meijer CJ, et al. Экспрессия p53 над базальным клеточным слоем в слизистой оболочке полости рта является ранним событием злокачественной трансформации и имеет прогностическое значение для развития плоскоклеточного рака полости рта. Дж. Патол . 1998 Апрель 184 (4): 360-8. [Медлайн].
Питияге Г., Тилакаратне В.М., Тавассоли М., Варнакуласурия С. Молекулярные маркеры дисплазии эпителия полости рта: обзор. Дж. Орал Патол Мед . 2009 ноябрь 38 (10): 737-52. [Медлайн].
Зиберс Т.Дж., Бергшоф В.Е., Отте-Холлер И. и др. Хромосомная нестабильность предсказывает прогрессирование предраковых поражений полости рта. Оральный онкол . 2013 декабрь 49 (12): 1121-8. [Медлайн].
de Carvalho Fraga CA, Farias LC, de Oliveira MV, et al. Повышенные уровни белка VEGFR2 и MMP9 связаны с классификацией эпителиальной дисплазии. Патол Рес Прак . 2014 Декабрь 210 (12): 959-64. [Медлайн].
Kil TJ, Kim HS, Kim HJ, Nam W, Cha IH. Генетические аномалии при прогрессировании лейкоплакии полости рта и рака полости рта. Asian Pac J Cancer Предыдущая . 2016. 17 (6): 3001-6. [Медлайн].
Axell T, Pindborg JJ, Smith CJ, van der Waal I.Белые поражения ротовой полости с особым акцентом на предраковые и связанные с курением поражения: выводы международного симпозиума, проведенного в Упсале, Швеция, 18-21 мая 1994 г. Международная совместная группа по вопросам белых поражений полости рта. Дж. Орал Патол Мед . 1996 25 февраля (2): 49-54. [Медлайн].
Сильверман С. Младший, Горский М., Лозада Ф. Лейкоплакия полости рта и злокачественная трансформация. Контрольное обследование 257 пациентов. Рак . 1984, 1 февраля. 53 (3): 563-8. [Медлайн].
Shafer WG, Waldron CA. Эритроплакия полости рта. Рак . 1975 Сентябрь, 36 (3): 1021-8. [Медлайн].
Варнакуласурия С., Рейбель Дж., Буко Дж., Дабелстин Э. Системы классификации дисплазии эпителия полости рта: прогностическая ценность, полезность, слабые места и возможности для улучшения. Дж. Орал Патол Мед . 2008 г., 37 (3): 127-33. [Медлайн].
Arduino PG, Surace A, Carbone M и др.Результат дисплазии ротовой полости: ретроспективное больничное исследование с участием 207 пациентов с длительным периодом наблюдения. Дж. Орал Патол Мед . 2009 Июль 38 (6): 540-4. [Медлайн].
Hogewind WF, van der Kwast WA, van der Waal I. Оральная лейкоплакия с акцентом на злокачественную трансформацию. Контрольное исследование 46 пациентов. J Craniomaxillofac Surg . 1989 г., 17 (3): 128-33. [Медлайн].
Holmstrup P, Vedtofte P, Reibel J, Stoltze K.Долгосрочные результаты лечения предраковых поражений полости рта. Оральный онкол . 2006 май. 42 (5): 461-74. [Медлайн].
Hsue SS, Wang WC, Chen CH, Lin CC, Chen YK, Lin LM. Злокачественная трансформация у 1458 пациентов с потенциально злокачественными заболеваниями слизистой оболочки полости рта: последующее исследование, проведенное в тайваньской больнице. Дж. Орал Патол Мед . 2007 января, 36 (1): 25-9. [Медлайн].
Schepman KP, van der Meij EH, Smeele LE, van der Waal I.Злокачественная трансформация лейкоплакии полости рта: последующее исследование стационарного населения из 166 пациентов с лейкоплакией полости рта из Нидерландов. Оральный онкол . 1998 июл. 34 (4): 270-5. [Медлайн].
Варнакуласурия С., Ариявардана А. Злокачественная трансформация лейкоплакии полости рта: систематический обзор обсервационных исследований. Дж. Орал Патол Мед . 2016 Март 45 (3): 155-66. [Медлайн].
Мохд Бакри М., Мохд Хуссайни Х, Рэйчел Холмс А., Дэвид Кэннон Р., Мэри Рич А.Пересмотр связи между кандидозной инфекцией и карциномой, особенно плоскоклеточным раком полости рта. J Устный микробиол . 2010 21 декабря 2: [Medline].
Gerber S, Gengler C, Grätz KW, Kruse AL. Влияние замороженных срезов на конечные хирургические границы при плоскоклеточном раке полости рта и губ: ретроспективный анализ за 11-летний период. Голова шеи Онкол . 2011 30 декабря. 3:56. [Медлайн].
Stott-Miller M, Houck JR, Lohavanichbutr P, et al.Уровни металлопротеиназы матрикса опухоли и слюны являются сильными диагностическими маркерами плоскоклеточного рака полости рта. Биомаркеры эпидемиологии рака Предыдущая . 2011 Декабрь 20 (12): 2628-36. [Медлайн].
Галлаб Н.А., Шейкер О.Г. Уровни хемерина и ММР-9 в сыворотке и слюне при плоскоклеточном раке полости рта и предраковых поражениях полости рта. Clin Oral Investigation . 2017 21 апреля (3): 937-47. [Медлайн].
Хван Дж. Т., Гу Ю. Р., Шен М. и др.Индивидуальная пятилетняя оценка риска прогрессирования предраковых поражений полости рта до рака. Oral Surg Oral Med Oral Pathol Oral Radiol . 2017 Март 123 (3): 374-81. [Медлайн].
Чаудхари М., Гадбайл А.Р., Видхале Г. и др. Сравнение экспрессии миофибробластов при плоскоклеточной карциноме полости рта, бородавчатой карциноме, эпителиальной дисплазии высокого риска, эпителиальной дисплазии низкого риска и нормальной слизистой оболочке полости рта. Голова Шея Патол . 2012 Сентябрь 6 (3): 305-13.[Медлайн].
типов | Рак полости рта
Большинство видов рака ротовой полости и ротоглотки представляют собой плоскоклеточный рак. Но есть и менее распространенные виды.
Плоскоклеточный рак ротовой полости и ротоглотки
Плоскоклеточный рак (SCC) — это рак, начинающийся из плоскоклеточных клеток. Около 95 из 100 (95%) всех случаев рака ротоглотки являются SCC. Большинство видов рака ротовой полости также относятся к SCC. Плоские клетки — это плоские, похожие на кожу клетки, покрывающие внутреннюю часть рта, носа, гортани и горла.Карцинома означает рак.
Веррукозная карцинома — это необычный тип плоскоклеточного рака. Он распространяется на другие части тела, но может очень глубоко проникнуть в окружающие ткани.
Другие виды рака ротовой полости и ротоглотки
Другие типы рака полости рта и ротоглотки включают следующие.
Рак слюнной железы
На слизистой оболочке рта и ротоглотки расположены второстепенные слюнные железы. Шишка в этой области чаще бывает доброкачественной (доброкачественной).Но в этих железах может развиться рак. В основном это разновидность рака, называемая аденокарциномой. Аденокарциномы — это тип рака, который начинается в железистой ткани.
Аденоидно-кистозная опухоль
Это редкий тип опухоли, которая может развиваться из железистой ткани слюнных желез или рта. Околоушная железа — наиболее частое место, где обнаруживают этот тип рака.
Базальноклеточный рак
Эти виды рака развиваются из базальных клеток и могут быть обнаружены на губах.
Лимфома
Лимфомы — это злокачественные опухоли, которые возникают из клеток лимфатической системы. Основание языка и миндалины состоят из лимфатической ткани, которая может перерасти в рак. На шее также много лимфатических узлов. Безболезненное увеличение лимфатического узла — наиболее частый признак лимфомы. Лечение лимфомы будет сильно отличаться от лечения рака полости рта или ротоглотки.
Меланома
Меланомы развиваются из клеток, вырабатывающих пигмент, которые придают коже ее цвет.Меланомы головы и шеи могут возникать где угодно на коже или внутри носа или рта (полости рта). Если у вас меланома рта или губы, вам будет полезна информация о лучевой терапии или хирургии рака ротовой полости и ротоглотки.
Доброкачественные новообразования во рту и ротоглотке
Рост или опухоль не всегда являются раком. Незлокачественные новообразования называют доброкачественными.
Основное различие между раком и доброкачественной опухолью состоит в том, что рак может распространяться, а доброкачественная опухоль — нет.Некоторые опухоли рта и ротоглотки доброкачественные и не распространяются на другие части тела.
Предраковые изменения во рту и ротоглотке
Два разных заболевания могут вызвать аномальные участки во рту или горле. С самого начала они безвредны, но, если их не лечить, у небольшого числа людей они могут перерасти в рак. Врачи называют эти состояния предраковыми. Их:
- лейкоплакия
- эритроплакия
Лейкоплакия и эритроплакия
Лейкоплакия — это белое пятно во рту.Эритроплакия — это красная область во рту, которая легко кровоточит. Эти белые или красные пятна могут быть безвредными. Но они также могут быть предраковыми и содержать аномальные клетки. Эти аномальные клетки называются дисплазией. Без лечения они могут перерасти в рак.
Ваш врач берет образец клеток (биопсия), чтобы определить, что это за пятна.
Лишь около 5 из 100 человек (5%) с диагнозом лейкоплакия имеют раковые или предраковые изменения. Но около 50 из 100 (50%) очагов эритроплакии могут стать злокачественными.
Риски и причины
Наиболее частыми причинами лейкоплакии и эритроплакии являются курение и жевание табака. Он также может развиться, если у вас плохо подогнанные зубные протезы, которые постоянно натирают десны, внутреннюю часть рта или языка.
Важно регулярно проходить стоматологические осмотры, если у вас есть зубные протезы. А отказ от алкоголя или отказ от курения может помочь уменьшить белые пятна.
Лечение
Вам может потребоваться лечение, если отказ от курения и алкоголя не помогает или если в поражении проявляются первые признаки рака.Если у вас дисплазия, существует риск развития рака ротовой полости. Если ваш врач устранит дисплазию, риск рака ротовой полости обычно исчезает. Ваш врач может удалить пятна с помощью лазера или скальпеля.
Исследователи пробуют группу препаратов, называемых ретиноидами, от лейкоплакии. Ретиноиды состоят из витамина А. Они используются для лечения тяжелых угрей и других кожных заболеваний. Они могут быть эффективны при лечении лейкоплакии, но могут иметь серьезные побочные эффекты.
Бета-каротин — это антиоксидант, который в организме превращается в витамин А.Небольшие исследования показали, что это может быть эффективным средством лечения пятен лейкоплакии. Лечение все еще экспериментальное и обычно не назначается в NHS.
Если вы курите, у вас повышен риск рецидива лейкоплакии и эритроплакии. Ваш врач настоятельно посоветует вам бросить курить.
Клиническая характеристика узкополосной визуализации эритроплакии полости рта и ее корреляция с патологией | BMC Cancer
Эритроплакия — это резко очерченное ярко-красное бархатистое поражение, описанное Кейра в 1911 г. как происходящее на головке полового члена и представляющее предраковый процесс из-за частого развития карциномы [13].Точный момент появления эритроплакии для описания конкретного типа заболевания слизистой оболочки полости рта не подтвержден документально. Прямая связь между эритроплакией полости рта и развитием рака полости рта не предполагалась до 1960-1970-х годов [22]. Распространенность эритроплакии полости рта составляет 0,02–0,83%, что намного меньше 0,2–4,9% лейкоплакии полости рта [22–24]. Термин лейкоплакия используется для обозначения клинического белого пятна или налета на слизистой оболочке полости рта, которые не могут быть удалены соскабливанием и не могут быть классифицированы клинически или микроскопически как другое заболевание [25].Кейра использовал термин «эритроплазия» для обозначения красной области аналогично французскому термину «лейкоплазия» [22]. Концепция эритроплакии сходна с концепцией лейкоплакии; однако воспалительная или травматическая этиология должна быть исключена перед дальнейшей диагностикой эритроплакии [26]. С точки зрения клинических проявлений эритроплакия отличается от лейкоплакии отсутствием беловатого пятна, которое под микроскопом оказалось гиперкератотическим поражением. Патологически гиперкератоз или паракератоз в случаях эритроплакии полости рта в настоящем исследовании не обнаружены.Процесс гиперкератоза вовлечен в патогенный процесс лейкоплакии, но этот же процесс может не быть вовлечен в эритроплакию. Кроме того, эпителий при эритроплакии полости рта часто атрофичен и не имеет ороговения [1,27]. Эритроплакия имеет самый высокий риск развития карциномы, тогда как при лейкоплакии полости рта он встречается реже [28]. В исследовании, проведенном Shafer et al., 91% биоптатов эритроплакии выявляют дисплазию, карциному in situ или карциному патологически [13].Эти четкие различия между этими двумя формами заболевания важны, потому что большинство поражений эритроплакии представляют собой предраковые или злокачественные состояния более серьезной степени.
Гистопатологическое исследование эритроплакии — единственный метод, который может быть использован для определения наличия сопутствующей дисплазии, карциномы in situ или карциномы внутри эритроплакии, что аналогично лейкоплакии полости рта. До проведения хирургической биопсии статус эпителия обычно неизвестен.NBI — это эндоскопический метод, основанный на отличительных оптических фильтрах, которые сужают полосу пропускания света для улучшения визуализации внутриэпителиального микроциркуляторного русла поверхности слизистой оболочки, который поднимается перпендикулярно от разветвляющегося сосуда, и едва различим при наблюдении нормального эпителия с помощью BWL [10,18, 29]. Было показано, что он полезен для улучшения раннего выявления раковых поражений в верхних отделах пищеварительного тракта, включая пищевод, глотку и полость рта; Аномальная сосудистая архитектура NBI слизистой оболочки полости рта проявляется в виде увеличенного числа извитых, расширенных, скрученных, удлиненных и штопорных мелких кровеносных сосудов различного калибра [5,6,8–10,18,30].Эндоскоп с NBI использовался для оценки лейкоплакии полости рта, наиболее часто встречающегося предракового поражения полости рта, а разнообразные интраэпителиальные микрососудистые паттерны, показанные NBI, оказались полезным инструментом для выявления дисплазии высокой степени, карциномы in situ и карциномы в оральная лейкоплакия в наших предыдущих работах [5,6,8,9]. Корреляции между клиническим проявлением эритроплакии полости рта и гистопатологией до сих пор не обнаружено. Поскольку NBI характеризуется улучшенной визуализацией внутриэпителиального микроциркуляторного русла, демонстрация микрососудистых структур под эпителием слизистой оболочки при освещении NBI может пролить свет на взаимосвязь между IPCL и патологией эритроплакии полости рта.
В настоящем исследовании только три случая имели тип IV IPCL (деструктивный паттерн внутриэпителиальной микрососудистой сети), и все они были инвазивной карциномой (рис. 6, 7, 8). Среди 25 случаев IPCL типа III (скрученный и удлиненный паттерн внутриэпителиального микроциркуляторного русла) 14 случаев (56%) были HGD / Tis / CA. Напротив, IPCL типа I и типа II состояли из 44 случаев, но только четыре (9,1%) были HGD / Tis / CA. Корреляция между различными типами интраэпителиального микроциркуляторного русла NBI и патологическими результатами с постепенным увеличением степени тяжести была хорошей ( r Пирсона = 0.7, таблица 2).
Три установленных критерия морфологии IPCL NBI были использованы в клинической практике. Характеристики этих критериев были исследованы и проанализированы на лейкоплакии полости рта в нашей предыдущей работе [6]. Критерий I состоял из коричневатых пятен и демаркационной линии с нерегулярным микроваскулярным узором, критерий II состоял из хорошо разграниченной коричневатой области с толстыми темными пятнами и / или извилистыми сосудами, а критерий III состоял из удлинения, скручивания и извилистого разрушения рисунка IPCL.В этом исследовании мы использовали эти критерии для анализа и сравнения различий в эритроплакии полости рта. По сравнению с лейкоплакией наблюдение за интраэпителиальным микроциркуляторным руслом более выгодно, потому что легко наблюдается микрососудистая морфология NBI (рис. 1, 2, 3, 4, 5, 6, 7, 8). В случае лейкоплакии полости рта, внутриэпителиальная папиллярная капиллярная петля обычно не может наблюдаться из-за того, что гиперкератоз лейкоплакии полости рта препятствует проникновению света, и необходимо сосредоточить внимание на слизистой оболочке вокруг белесого пятна [ 5,6,8,9].Было высказано предположение, что одна из причин, почему эритроплакия полости рта выглядит красной под BWL, включала ослабленный и атрофический эпителий с собственной сосудистой пластинкой, лежащей близко к поверхности, и сосочками соединительной ткани, содержащими набухшие капилляры, поднимающиеся между сетчатыми гребнями близко к поверхности [13, 22]. В исследовании Carlie et al было обнаружено значительное усиление васкуляризации при прогрессировании заболевания при раке полости рта. В исследовании было замечено, что изменение паттернов IPCL может быть связано с чрезмерным ангиогенезом как в предраковых, так и в раковых поражениях [31,32].Комбинация набухших капилляров с повышенной васкуляризацией объясняет морфологию микрососудистой архитектуры при освещении NBI. Было обнаружено, что коричневатые пятна с извилистыми сосудами или без них используются для выявления рака in situ на слизистой оболочке ротоглотки и гипофаринкса [18] и раковых поражений в полости рта [15], однако низкое отношение шансов критерия I NBI (OR = 0,12, ДИ 95%: 0,03–0,40) и критерии II (ОШ = 0,80, ДИ 95%: 0,18–3,55) показали, что эти закономерности могут не быть решающими индикаторами HGD / Tis / CA при эритроплакии полости рта.Коричневые области, обнаруженные NBI или критерием I в этом исследовании, могут представлять доброкачественные патологии, такие как ангиодисплазия, эрозивные изменения слизистой оболочки или перекрытие нормальной васкуляризации, каждая из которых может вызывать ложноположительные результаты [33]. Частота выявления HGD / Tis / CA критериев III (OR = 15,46, CI95%: 3,81–72,84) была значительно лучше, чем критерии I и II ( p <0,001, таблица 3). По результатам диагностических тестов по III критерию прогностическая ценность отрицательного результата составила 90.91%, но положительная прогностическая ценность составила 60,71%. Это открытие с хорошей отрицательной прогностической ценностью объясняет, что низкая частота HGD / Tis / CA, когда скрученный удлиненный рисунок IPCL не был продемонстрирован NBI. Раннее обнаружение HGD / Tis / CA напрямую связано с менее агрессивным лечением и лучшим прогнозом. Для тех, кто не подходит для биопсии или не желает проходить хирургическую биопсию, NBI может быть многообещающим, быстрым и безопасным инструментом для предоставления дополнительной важной информации о эритроплакии полости рта перед хирургическим вмешательством.
Насколько нам известно, данное исследование является первым, которое иллюстрирует корреляцию между патологией и морфологическими картинами изображений NBI у большой группы пациентов. Образы NBI, видимо, субъективны. Обязательно обучение, чтобы научиться наблюдать морфологию со всех сторон и избегать случайного светового рефлекса от слизи или мусора из ротовой полости. В исследовании, проведенном Puxeddu et al., . , сочетание NBI и Storz Professional Image Enhancement System (SPIES) с контактной эндоскопией при патологии гортани и гортани a для увеличения сосудистого рисунка исследуемых поражений и уменьшения вариаций между и внутри наблюдателей является многообещающим инструментом.Точность дифференциального диагноза между нормальной тканью и гиперплазией по сравнению с легкой дисплазией и карциномой составляет 97,6% [34]. Необходимы дальнейшие исследования применения этой системы к поражениям слизистой оболочки полости рта для улучшения выявления патологической дисплазии и карциномы. Отсутствие универсальных диагностических стандартов для морфологии микрососудов NBI остается проблемой, и необходимы крупномасштабные проспективные исследования для дальнейшей проверки этого инструмента. Кроме того, нам известны некоторые ограничения нашего исследования.Во-первых, размер выборки невелик из-за низкой частоты эритроплакии полости рта и короткого периода времени для сбора данных. Во-вторых, гистопатологическая дисплазия эпителия представляет собой спектр, и в настоящее время не установлено никаких определенных критериев, чтобы четко разделить этот спектр на низкую, среднюю и высокую степень. Возможны существенные различия в оценке степени эпителиальной дисплазии между наблюдателями и внутри наблюдателя [14]. В некоторых случаях мы попытались уменьшить вышеупомянутые вариации, используя иммуногистохимическое окрашивание мышиным моноклональным антителом Ki-67 и попросив двух патологов прийти к соглашению по каждому случаю.Третье ограничение — ретроспективный характер исследования. Чтобы прийти к более определенному выводу, необходимо крупномасштабное многоцентровое или международное межстрановое исследование.
Средства диагностики для выявления предраковых состояний полости рта
Johnson NW, Warnakulasuriya S, Gupta PC et al . Глобальное неравенство в отношении здоровья полости рта в отношении заболеваемости и исходов рака полости рта: причины и решения. Adv Dent Res 2011; 23 (2): 237–246.
Артикул Google ученый
Сигел Р., Найшадхам Д., Джемал А.Статистика рака. CA Cancer J Clin 2012; 62 (1): 10–29.
Артикул Google ученый
Napier SS, Speight PM. Естественная история потенциально злокачественных поражений и состояний полости рта: обзор литературы. J Oral Pathol Med 2008; 7 (1): 1–10.
Артикул Google ученый
ван дер Ваал И.Потенциально злокачественные поражения слизистой оболочки полости рта и ротоглотки; терминология, классификация и современные концепции менеджмента. Oral Oncol 2009; 45 (4/5): 317–323.
Артикул Google ученый
Llewellyn CD, Johnson NW, Warnakulasuriya KA. Факторы риска плоскоклеточного рака полости рта у молодых людей — подробный обзор литературы. Oral Oncol 2001; 37 (5): 401–418.
Артикул Google ученый
Линген М.В., Пинто А., Мендес RA и др. . Генетика / эпигенетика предраковых заболеваний полости рта: текущее состояние и будущие исследования. Болезни полости рта 2011; 17 (Дополнение 1): 7–22.
Артикул Google ученый
Альбо Д., Граник М.С., Джала Н. и др. . Связь ангиогенеза с биологической активностью при плоскоклеточном раке головы и шеи человека. Ann Plast Surg 1994; 32 (6): 588–594.
Артикул Google ученый
Гийо М., Чжан Л., По С и др. . Возможное использование количественного фенотипа ткани для прогнозирования риска злокачественных новообразований полости рта. Cancer Res 2008; 68 (9): 3099–3107.
Артикул Google ученый
Ho PS, Chen PL, Warnakulasuriya S и др. .Злокачественная трансформация потенциально злокачественных заболеваний полости рта у мужчин: ретроспективное когортное исследование. BMC Cancer 2009; 9 : 260–267.
Артикул Google ученый
Barnes L, Eveson JW, Reichart P et al . Всемирная организация здравоохранения. Классификация опухолей. Патология и генетика опухолей головы и шеи . Лион: IARC Press, 2005: 283–328.
Google ученый
Arduino PG, Surace A, Carbone M и др. .Результат дисплазии ротовой полости: ретроспективное больничное исследование с участием 207 пациентов с длительным периодом наблюдения. J Oral Pathol Med 2009; 38 (6): 540–544.
Артикул Google ученый
Механна Х.М., Раттай Т., Смит Дж. и др. . Лечение и последующее наблюдение дисплазии полости рта — систематический обзор и метаанализ. Голова Шея 2009 г .; 31 (12): 1600–1609.
Артикул Google ученый
Leemans CR, Boudewijn JM, Braakhuis JM et al .Молекулярная биология рака головы и шеи. Nat Rev Cancer 2011; 11 (1): 9–22.
Артикул Google ученый
Бреммер Дж. Ф., Браакхуис Б. Дж., Бринк Дж. и др. . Неинвазивный генетический скрининговый тест для выявления предопухолевых поражений полости рта. Lab Invest 2005; 85 (12): 1481–1488.
Артикул Google ученый
Bremmer JF, Graveland AP, Braakhuis BJ et al .Скрининг на предрак полости рта с помощью неинвазивной генетической цитологии. Cancer Prev Res 2009; 2 (1): 128–133.
Артикул Google ученый
Шпицер Т., Хамзани Ю., Бахар Г. и др. . Анализ слюны на биомаркеры рака полости рта. Br J Cancer 2009; 101 (7): 1194–1198.
Артикул Google ученый
Лю Дж, Дуань Ю.Слюна: потенциальная среда для диагностики и мониторинга заболеваний. Oral Oncol 2012; 48 (7): 569–577.
Артикул Google ученый
Mehrotra R, Gupta DK. Захватывающие новые достижения в диагностике рака полости рта: пути к раннему выявлению. Голова шеи Oncol 2011; 3 : 33–40.
Артикул Google ученый
Ланге CJ.Изучение биомаркеров рака головы и шеи. Cancer 2012; 118 (16): 3882–3892.
Артикул Google ученый
Карнелио С., Родригес С.Дж., Шеной Р. и др. . Краткий обзор распространенных предраковых поражений полости рта с акцентом на их ведение и профилактику рака. Indian J Surg 2011; 73 (4): 256–261.
Артикул Google ученый
Сильверман С. Младший, Горский М., Лозада Ф.Лейкоплакия полости рта и злокачественная трансформация. Контрольное обследование 257 пациентов. Cancer 1984; 53 (3): 563–568.
Артикул Google ученый
Silverman S Jr. Демография и распространенность рака полости рта и глотки: результаты, тенденции, проблемы. J Am Dent Assoc 2001; 132 (Дополнение 1): 7S – 11S.
Артикул Google ученый
Cabay JR, Morton AH Jr, Epstein JB.Пролиферативная веррукозная лейкоплакия и ее прогрессирование в карциному полости рта: обзор литературы. J Oral Pathol Med 2007; 36 (5): 255–261.
Артикул Google ученый
Вилла А, Вилла С, Абати С. Рак полости рта и эритроплакия полости рта: обновленная информация и значение для клиницистов. Aust Dent J 2011; 56 (3): 253–256.
Артикул Google ученый
Феллер Л., Леммер Дж.Лейкоплакия полости рта в связи с инфекцией ВПЧ: обзор. Int J Dent 2012; 2012 : 540561.
Артикул Google ученый
Гринде Б., Ольсен И. Роль вирусов в заболеваниях полости рта. J Oral Microbiol 2010; 2 : 2127–2135.
Артикул Google ученый
D’Souza G, Dempsey A. Роль ВПЧ при раке головы и шеи и обзор вакцины против ВПЧ. Prev Med 2011; 53 (Дополнение 1): S5 – S11.
Артикул Google ученый
Оствальд С., Руцац К., Шведер Дж. В. и др. . Вирус папилломы человека 6/11, 16 и 18 при карциномах полости рта и доброкачественных поражениях полости рта. Med Microbiol Immunol 2003; 192 (3): 145–148.
Артикул Google ученый
Hennessey PT, Westra HW, Califano JA.Вирус папилломы человека и плоскоклеточный рак головы и шеи: последние данные и клинические последствия. J Dent Res 2009; 88 (4): 300–306.
Артикул Google ученый
Wise-Draper TM, Wells SI. Белки папилломавирусов E6 и E7 и их клеточные мишени. Front Biosci 2008; 13 : 1003–1017
Артикул Google ученый
Насман А., Аттнер П., Хаммарштедт Л. и др. .Заболеваемость карциномой миндалин, положительной по вирусу папилломы человека (ВПЧ), в Стокгольме, Швеция: эпидемия вирусно-индуцированной карциномы? Int J Cancer 2009; 125 (2): 362–366.
Артикул Google ученый
Schlecht HP. Оральная опасность заражения вирусом папилломы человека интимной близости. J Am Med Assoc 2012; 307 (7): 724–725.
Артикул Google ученый
Ho PS, Yang YH, Shieh TY и др. .Употребление арека квида, сигарет и алкоголя связано с коморбидностью субмукозного фиброза полости рта и рака полости рта. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2007; 104 (5): 647–652.
Артикул Google ученый
Шахид РА. Приезд в Америку: орех бетель и субмукозный фиброз полости рта. J Am Dent Assoc 2010; 141 (4): 423–428.
Артикул Google ученый
Bhattacharyya I, Chehal HK.Белые поражения. Otolaryngol Clin N Am 2011; 44 (1): 109–131.
Артикул Google ученый
Sugerman PB, Savage NW, Walsh LJ и др. . Патогенез красного плоского лишая полости рта. Crit Rev Oral Biol Med 2002; 13 (4): 350–365.
Артикул Google ученый
Sugerman PB, Savage NW, Zhou X и др. .Красный плоский лишай полости рта. Clin Dermatol 2000; 18 (5): 533–539.
Артикул Google ученый
Le Cleach L, Chosidow O. Клиническая практика. Красный плоский лишай. N Engl J Med 2012; 366 (8): 723–732.
Артикул Google ученый
ван дер Ваал И. Красный плоский лишай и поражения ротовой полости; критическая оценка с акцентом на диагностические аспекты. Med Oral Patol Oral Cirt Bucal 2009; 14 (7): E310 – E314.
Google ученый
Ho MW, Risk JM, Woolger JA и др. . Клинические детерминанты злокачественной трансформации при дисплазии эпителия полости рта. Oral Oncol 2012; 48 (10): 969–976.
Артикул Google ученый
Мессади Д.В., Уайлдер-Смит П., Волински Л.Повышение выживаемости при раке полости рта: роль стоматологов. J Calif Dent Assoc 2009; 37 (11): 789–798.
PubMed PubMed Central Google ученый
Стил Т.О., Мейерс А. Раннее выявление предраковых образований и рака полости рта. Otolaryngol Clin N Am 2011; 44 (7): 221–229.
Артикул Google ученый
Наир Д., Прути Р., Павар У и др. .Рак полости рта: предраковые состояния и скрининг — обновленная информация. J Can Res Therap 2012; 8 (Дополнение 1): s57 – s66.
Google ученый
Fedele S. Средства диагностики при скрининге рака полости рта. Голова шеи Oncol 2009; 1 : 5–10.
Артикул Google ученый
Эпштейн Дж. Б., Сильверман С. Младший, Эпштейн Дж. Д. и др. .Анализ биоптатов поражений полости рта, выявленных и оцененных визуальным осмотром, хемилюминесценцией и толуидиновым синим. Oral Oncol 2008; 44 (6): 538–544.
Артикул Google ученый
Lingen MW, Kalmar JR, Karrison T и др. . Критическая оценка диагностических средств для обнаружения рака полости рта. Oral Oncol 2008; 44 (1): 10–22.
Артикул Google ученый
Канифоль М.П., Пох С.Ф., Гийяр М. и др. .Визуализация и другие новые технологии как факторы, влияющие на профилактику рака полости рта. Ann NY Acad Sci 2007; 1098 : 167–183.
Артикул Google ученый
Паттон Л.Л., Эпштейн Дж. Б., Керр АР. Дополнительные методы для обследования рака полости рта и диагностики поражений: систематический обзор литературы. J Am Dent Assoc 2008; 139 (7): 896–905.
Артикул Google ученый
Су WW, Yen AM, Chiu SY и др. .РКИ на уровне сообщества по скринингу на рак полости рта с применением толуидинового синего. J Dent Res 2010; 89 (9): 933–937.
Артикул Google ученый
Аван К.Х., Ян Ю.Х., Морган Р.Р. и др. . Использование толуидинового синего в качестве вспомогательного средства диагностики при обнаружении потенциально злокачественных заболеваний полости рта — клиническая и гистологическая оценка. Oral Dis 2012; 18 (8): 728–733.
Артикул Google ученый
Sciubba JJ. Улучшение выявления предраковых и раковых поражений полости рта. Компьютерный анализ щеточной биопсии полости рта. Совместная исследовательская группа OralCDx в США. J Am Dent Assoc 1999; 130 (10): 1445–1457.
Артикул Google ученый
Рик GM. Биопсия ротовой полости: проблема ложных срабатываний. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2003; 96 (3): 252–258.
Артикул Google ученый
Свирский Дж. А., Бернс Дж. К., Карпентер В. М. и др. . Сравнение результатов компьютерной кистевой биопсии с последующей биопсией скальпеля и гистологией. Gen Dent 2002; 50 (6): 500–503.
PubMed Google ученый
Scheifele C, Schimdt-Westhausen A, Detrich T et al .Чувствительность и специфичность методики OralCDx: оценка 103 случаев. Oral Oncol 2004; 40 (8): 824–828.
Артикул Google ученый
Хубер М.А., Бсоул С.А., Тережалмы ГТ. Промывка уксусной кислотой и хемилюминесцентное освещение в качестве дополнения к обычному исследованию мягких тканей полости рта для выявления дисплазии: пилотное исследование. Quintessence Int 2004; 35 (5): 378–384.
PubMed Google ученый
Kerr AR, Sirois DA, Epstein JB. Клиническая оценка хемилюминесцентного освещения: дополнение к исследованиям слизистой оболочки полости рта. J Clin Dent 2006; 17 (3): 59–63.
PubMed Google ученый
Эпштейн Дж. Б., Горский М., Лонки С. и др. . Эффективность оральной люменоскопии ™ (ViziLite®) в визуализации повреждений слизистой оболочки полости рта. Spec Care Dent 2006; 26 (4): 171–174.
Артикул Google ученый
МакИнтош Л., Маккалоу М.Дж., Фарах К.С. Оценка рассеянного света и полоскания уксусной кислотой (Microlux / DL) при визуализации поражений слизистой оболочки полости рта. Oral Oncol 2009; 45 (12): 227–231.
Артикул Google ученый
Lam S, MacAulay C, Palcic B.Выявление и локализация раннего рака легких методами визуализации. Комод 1993; 103 (1 приложение): 12S – 14S.
Артикул Google ученый
Park SY, Follen M, Milbourne A и др. . Автоматизированный анализ изображений цифровой кольпоскопии для обнаружения неоплазии шейки матки. J Biomed Opt 2008; 13 (1): 014029.
Артикул Google ученый
Kennedy JC, Pottier RH.Эндогенный протопорфирин IX, клинически полезный фотосенсибилизатор для фотодинамической терапии. J Photochem Photobiol B 1992; 14 (4): 275–292.
Артикул Google ученый
Эбихара А, Лиав Л.Х., Красиева ТБ. Обнаружение и диагностика рака полости рта с помощью флуоресценции, индуцированной светом. Lasers Surg Med 2003; 32 (1): 17–24.
Артикул Google ученый
Шанц С.П., Колли В., Сэвидж HE и др. . In vivo нативная клеточная флуоресценция и гистологические характеристики рака головы и шеи. Clin Cancer Res 1998; 4 (5): 1177–1182.
PubMed Google ученый
Суини Л., Дин Н. Р., Магнусон Дж. С. и др. . Оценка автофлуоресценции и отражательной способности тканей для скрининга рака полости рта. Отоларингол Хирургия головы и шеи 2012; 145 (6): 956–960.
Артикул Google ученый
Lane PM, Gilhuly T, Whitehead P et al . Простое устройство для прямой визуализации флуоресценции тканей ротовой полости. J Biomed Opt 2006; 11 (2): 024006.
Артикул Google ученый
Poh CF, Ng SP, Williams PM и др. . Прямая флуоресцентная визуализация клинически скрытых предраковых заболеваний полости рта с высоким риском с помощью простого портативного устройства. Голова Шея 2007; 29 (1): 71–76.
Артикул Google ученый
Балеви Б. Принятие решений на основе фактов: должен ли стоматолог общего профиля использовать VELscope для рутинного скрининга на рак полости рта? J Can Dent Assoc 2007; 73 (7): 603–606.
PubMed Google ученый
Камилс Ф, Макинтош Л., Георгиу А и др. .Эффективность аутофлуоресцентной визуализации тканей (Velscope) при визуализации поражений слизистой оболочки полости рта. Голова Шея 2012; 34 (6): 856–862.
Артикул Google ученый
Аван К. Х., Морган ПР, Варнакуласурия С. Оценка системы визуализации на основе автофлуоресценции (VELscope TM ) для выявления потенциально злокачественных заболеваний полости рта и доброкачественного кератоза. Oral Oncol 2011; 47 (4): 274–277.
Артикул Google ученый
Роблайер Д., Курачи С., Степанек В. и др. . Объективное обнаружение и определение неоплазии полости рта с помощью автофлуоресцентной визуализации. Cancer Prev Res 2009; 2 (5): 423–431.
Артикул Google ученый
Фолкман Дж., Уотсон К., Ингбер Д. и др. . Индукция ангиогенеза при переходе от гиперплазии к неоплазии. Nature 1989; 339 (6219): 58–61.
Артикул Google ученый
Хасина Р., Линген МВт. Ангиогенез при раке полости рта. J Dent Educ 2001; 65 (11): 1282–1290.
PubMed Google ученый
Шварц Р.А., Гао В., Редден Вебер С. и др. . Неинвазивная оценка поражений ротовой полости с помощью оптической спектроскопии, чувствительной к глубине: простое устройство для прямой визуализации флуоресценции тканей полости рта. Cancer 2009; 115 (8): 1669–1679.
Артикул Google ученый
Макги С.А., Миркович Дж., Мардиросян В. и др. . Модельный спектроскопический анализ полости рта: влияние анатомии. J Biomed Opt 2008; 13 (6): 064034.
Артикул Google ученый
Koch FP, Kaemmerer PW, Biesterfeld S et al .Эффективность автофлуоресценции для выявления подозрительных поражений полости рта — проспективное слепое клиническое исследование. Clin Oral Investigation 2011; 15 (6): 975–982.
Артикул Google ученый
Forde MD, Koka S, Eckert SE и др. . Системные оценки с использованием слюны: общие соображения и текущие оценки части 1. Int J Prosthodont 2006; 19 (1): 43–52.
PubMed Google ученый
Пеше MA, Spitalnik SL.Слюна и лаборатория клинической патологии. Ann NY Acad Sci 2007; 1098 : 192–199.
Артикул Google ученый
Li Y, St John MA, Zhou X et al . Диагностика транскриптома слюны для выявления рака полости рта. Clin Cancer Res 2004; 10 (24): 8442–8450.
Артикул Google ученый
Wong DT.На пути к простому тесту на основе слюны для обнаружения рака полости рта жидкость (слюна), которая является зеркалом тела, является идеальной средой для исследования здоровья и наблюдения за заболеваниями. Expert Rev Mol Diagn 2006; 6 (3): 267–272.
Артикул Google ученый
Wong DT. Диагностика слюны на основе нанотехнологий, протеомики и геномики. J Am Dent Assoc 2006; 137 (3): 313–321.
Артикул Google ученый
Потенциально злокачественные поражения полости рта
Специальные выпуски
сентябрь 2011 г.
Том 32, Выпуск 2
Потенциально злокачественные поражения полости рта
Линн В. Соломон, DDS, MS
Реферат
Успехи в исследованиях потенциально злокачественных поражений полости рта приводят к более ранней диагностике, соответствующему лечению и более длительному наблюдению.Знание терминологии, связанной с этими поражениями и клиническими предупреждающими знаками, облегчает общение между клиницистами, их пациентами и другими специалистами. При обнаружении потенциально злокачественного новообразования клиницист должен начать соответствующее расследование, включая анамнез пациента, биопсию и гистологическое исследование, которые позволят поставить диагноз, связанный с вероятностью прогрессирования заболевания. При определении метода лечения необходимо учитывать множество факторов, таких как степень поражения, расположение в зоне повышенного риска, надежность пациента для последующих посещений, история предыдущей плоскоклеточной карциномы полости рта, такие привычки. как употребление табака, так и системные проблемы, такие как иммуносупрессия.
По мере того, как достижения в исследованиях привели к большему пониманию потенциально злокачественных поражений в полости рта, клиницисты должны понимать и уметь сообщать об относительных рисках этих поражений, а также обучать пациентов стратегиям лечения. В этой статье обсуждаются терминология, клинические предупреждающие признаки и необходимые шаги для обнаружения потенциально злокачественного поражения полости рта.
Терминология
Ротовая полость включает ярко-красные границы губ, слизистые оболочки губ, слизистые оболочки щек, вестибулы щеки, альвеолярные гребни и десны, дно рта, ротовой язык и твердое небо.Наиболее распространенной формой рака полости рта является плоскоклеточный рак, на который приходится около 94% всех злокачественных новообразований полости рта. Плоскоклеточные клетки представляют собой эпителиальные клетки, которые образуют поверхностное покрытие слизистой оболочки рта; Таким образом, плоскоклеточная карцинома полости рта (OCSCC) представляет собой злокачественное новообразование поверхностных эпителиальных клеток. Потенциально злокачественное поражение — это поражение, которое имеет больший риск стать ОКРК, чем клинически нормальная слизистая оболочка полости рта.
Предраковое заболевание
OCSCC возникает как временная сумма многих молекулярных и биохимических клеточных аномалий, а также изменений иммунной системы и изменений в основной фиброваскулярной строме. 1 По мере накопления первоначальных клеточных аномалий они отражаются в изменениях клинического вида пораженных эпителиальных тканей, известных как предраковые заболевания. Под предраком понимается клинически видимое предраковое поражение, которое представляет собой доброкачественную, морфологически измененную ткань, которая имеет более высокий, чем обычно, риск злокачественной трансформации. 2 Предраковые поражения клинически могут проявляться в виде белых, красных или смешанных бело-красных изменений эпителиальной поверхности.
Потенциально злокачественное поражение
Терминология «предраковое поражение» подразумевает, что поражение будет следовать необратимому и неизбежному прогрессированию до ОКРК.Исследования показывают, что, несмотря на наличие статистических данных для прогнозирования конкретных клинических и микроскопических изменений, связанных с развитием ОКРК, для каждого отдельного поражения клиницисты могут только оценить вероятность прогрессирования. 3 Таким образом, чем предраковое поражение, предпочтительнее термин, который более точно отражает текущее понимание: потенциально злокачественное поражение.
Предраковое состояние
Предраковое состояние — это заболевание или привычка пациента, которая не обязательно меняет клинический вид местной ткани, но связана с более высоким, чем обычно, риском развития потенциально злокачественного поражения или рака в пораженной ткани. . 2 Тщательный медицинский, стоматологический и социальный анамнез необходим для выявления пациентов, у которых повышается индекс клинического подозрения на потенциально злокачественные поражения. Злоупотребление алкоголем или табаком, наличие нескольких партнеров орального секса, ранний сексуальный опыт, употребление марихуаны, 4 предыдущих OCSCC и иммуносупрессия (например, ВИЧ / СПИД, трансплантация органов или подавление костного мозга) связаны с повышенным риск OCSCC.
Потенциал злокачественной трансформации
Этот термин означает статистический риск наличия рака в потенциально злокачественном поражении или состоянии либо при первоначальном диагнозе, либо в будущем, обычно выражаемый в процентах. 2
Предупреждающие знаки
Клинические предупреждающие признаки потенциально злокачественного поражения полости рта отражают лежащие в основе клеточные аномалии. Эти клинические изменения обычно имеют белый или красный цвет. Белый клинический вид эпителия называется лейкоплакией, а красный клинический вид — эритроплакией. Лейкоплакия и эритроплакия — это строго клинические термины, означающие «белое пятно» и «красное пятно» соответственно, и оба являются диагнозами исключения.Это означает, что лейкоплакия или эритроплакия «не могут быть охарактеризованы клинически или патологически как любое другое заболевание», согласно Всемирной организации здравоохранения. 5
Leukoplakia
Белые потенциально злокачественные образования встречаются гораздо чаще, чем красные, однако они с меньшей вероятностью будут диспластическими или трансформироваться в OCSCC со временем. Задача состоит в том, чтобы исключить другие потенциальные причины клинически очевидного поражения белого цвета, такие как фрикционный кератоз, гиперпластический кандидоз, morsicatio (хроническое покалывание языка, щеки или губы), красный плоский лишай, лейкоэдема, кератоз табачного мешочка, никотиновый стоматит и белый губчатый невус.Клинический диагноз лейкоплакии требует, чтобы все эти другие состояния были исключены из истории болезни, дополненной биопсией с микроскопическим исследованием при необходимости. Микроскопически диагноз лейкоплакии может варьироваться от гиперкератоза без дисплазии, акантоза (утолщения поверхностного эпителиального слоя), эпителиальной дисплазии (легкой, средней, тяжелой), карциномы in situ или даже плоскоклеточной карциномы. В одном исследовании более 80% из 3000 случаев лейкоплакии не имели дисплазии.» 6 Эта статистика в некоторой степени специфична для конкретного места, потому что в определенных местах с» высоким риском «(кратко изложено ниже) лейкоплакии чаще являются потенциально злокачественными. 6,7
Поверхность лейкоплакии может быть гладкой и однородной ( , и), или морщинистые, или гофрированные с однородной текстурой на всем протяжении (). Неоднородная лейкоплакия может проявляться папиллярной поверхностью (бородавчатая лейкоплакия) или участками эритематозных изменений, которые называются эритролейкоплакией ().Эритролейкоплакия может проявляться в виде обширной области смешанного красного и белого изменения поверхности или в виде однородных небольших беловатых папул на эритематозной основе (например, пятнистая лейкоплакия). Области бородавчатого изменения, покраснения или изъязвления при лейкоплакии имеют большую вероятность злокачественной трансформации в OSCC, чем лейкоплакия без этих изменений. В одном исследовании негомогенные лейкоплакии показали семикратное увеличение риска злокачественной трансформации по сравнению с гомогенными лейкоплакиями. 8
Эритроплакия
Красные потенциально злокачественные образования гораздо реже, чем белые поражения, однако с большей вероятностью они будут диспластическими или со временем трансформироваться в ОКРК. 9 Эритроплакия — это плоское пятно или пятно, поверхность слизистой оболочки которого имеет красный бархатистый или мелкозернистый вид (). Границы истинной эритроплакии обычно хорошо разграничены, в отличие от границ воспалительного процесса, при котором границы имеют тенденцию сливаться с окружающей нормальной тканью. Эритроплакические поражения могут быть симптоматичными, когда пациенты едят горячую или острую пищу, и чаще всего возникают в местах с высоким риском ОКРК (перечислены ниже). Основными различиями в клинической эритроплакии являются воспалительные процессы, травмы или ожоги, которые должны быть исключены на основании истории болезни в сочетании с результатами биопсии, исключающей инфекцию, физическое или химическое повреждение, дерматозы или иммунные реакции. 10 Гистологический диагноз истинной эритроплакии может включать атрофию эпителия (истончение поверхностного эпителиального слоя), изъязвление, дисплазию эпителия, карциному in-situ или плоскоклеточный рак. В одном исследовании 91% эритроплакических поражений были инвазивными OCSCC, карциномой in-situ или тяжелой эпителиальной дисплазией. 11
Расположение, расположение, расположение
Потенциально злокачественные поражения полости рта с наибольшей вероятностью злокачественной трансформации в OCSCC в следующих местах:
- Киноварь нижней губы
- Язык (боковые границы> вентральный язык> основание > dorsum)
- Дно рта
- Ретромолярный треугольник / мягкое небо / столбы миндалин и небные миндалины
Хотя мягкое небо и небные миндалины технически не находятся в ротовой полости, они примыкают к ретромолярному треугольнику и при обширных поражениях может быть трудно определить, откуда возникло собственно ротовая полость или ткани ротоглотки.Ткани ротоглотки, которые являются участками высокого риска для плоскоклеточного рака ротоглотки (OPSCC), — это небные миндалины и язычные миндалины, расположенные у основания языка. OPSCC связан с инфекцией вируса папилломы человека. 12 Это не означает, что потенциально злокачественные новообразования никогда не возникают на других участках полости рта. Тем не менее, участки высокого риска — это те, в которых эти поражения требуют более частого наблюдения.
Шаги, которые нужно предпринять после открытия
История пациента
Вот некоторые вопросы, которые могут быть полезны для исследования аномалии ротовой полости:
Знаете ли вы какие-либо изменения во рту?
Симптоматические поражения часто являются результатом воспалительного процесса, в то время как потенциально злокачественные поражения обычно протекают бессимптомно.
Если да, как давно вы знаете об этих изменениях?
Давнее (от нескольких лет до десятилетий) изменение или изменение, которое не прогрессировало с момента первого открытия, с меньшей вероятностью может быть потенциально злокачественным поражением.
Случалось ли такое раньше? Поражение приходит и уходит или присутствует всегда?
История обострения и ремиттирующего поражения или того, которое демонстрирует циклическое возникновение, менее согласуется с потенциально злокачественным поражением.
Повреждение увеличилось с тех пор, как вы его впервые заметили?
Потенциально злокачественные новообразования со временем изменяются. Белые поражения могут смешиваться с красным компонентом или образовывать бородавчатую поверхность. Поражения могут стать более обширными, твердыми или изъязвленными, особенно если они претерпевают злокачественную трансформацию.
Есть ли дискомфорт или боль, связанные с поражением?
Ранние потенциально злокачественные поражения обычно протекают бессимптомно, однако появление дискомфорта или боли может указывать на злокачественную трансформацию.
Начали ли вы принимать какие-либо новые лекарства или изменили ли режим ухода за полостью рта?
Временная связь нового фактора окружающей среды с появлением аномалии ротовой полости предполагает, что они могут быть связаны. Если возможно, можно попытаться прекратить изменение окружающей среды, чтобы увидеть, исчезнет ли потенциально злокачественное поражение.
Вы употребляете табачные изделия или жуете бетель квид?
Многие лейкоплакии связаны с употреблением табака, и отказ от этой привычки может привести к исчезновению поражения. 10
После опроса и клинического обследования может быть определена возможная причина поражения (например, контакт с острым бугорком зуба, плохо подогнанные зубные приспособления, гиперчувствительность к средствам для ухода за зубами или пищевым продуктам, инфекционный процесс, трение при жевании беззубого тела гребень, или травма). Важно задокументировать и контролировать поражение. 13 Если есть вероятность, что поражение является реактивным, следует назначить соответствующее лечение и повторно оценить область через 7–14 дней. 14 К счастью, подавляющее большинство поражений проходят через 2 недели. Однако, если поражение увеличилось в размерах, изменило характеристики или не подействовало на лечение, как ожидалось, подходящим лечением является биопсия с гистологическим исследованием. Лучше подтвердить, что поражение не является потенциально предраковым, чем подождать, пока потенциально злокачественное поражение не станет злокачественным.
Биопсия
Послеоперационная биопсия удаляет репрезентативную часть поражения и рекомендуется, если поражение большое.При выполнении биопсии эритролейкоплакии область красного изменения должна быть включена в образец, отправленный патологу. Эксцизионная биопсия удаляет все клинически видимые поражения и рекомендуется, если поражение небольшое. Избегать биопсии можно только в том случае, если она может серьезно угрожать здоровью или безопасности пациента. Результат биопсии определяет, какие меры последующего наблюдения необходимы. Только хирургическая биопсия архитектурно неповрежденной ткани может диагностировать потенциально злокачественные поражения и ОКРК.
Гиперкератоз / гиперпластический кандидоз
После биопсии некоторые белые поражения могут быть микроскопически определены как простой гиперкератоз (утолщение поверхностного кератинового слоя) с нормальными эпителиальными клетками (). Иногда биопсия выявляет инфекцию эпителиальной поверхности кандидозными организмами (). Гиперпластический кандидоз часто вызывает воспалительную реакцию со значительной клеточной атипией, видимой под микроскопом. В этих случаях после курса соответствующей противогрибковой терапии поражение следует повторно оценить. 15 Если поражение не рассосалось, может потребоваться повторная биопсия, чтобы исключить оппортунистическую кандидозную колонизацию гиперкератотического потенциально злокачественного поражения.
Дисплазия эпителия полости рта и карцинома in situ
Микроскопический диагноз дисплазии эпителия означает наличие цитологических и / или архитектурных аномалий эпителия. Диагноз дисплазии будет разделен на легкую, среднюю или тяжелую. 16 Легкая дисплазия эпителия ограничивается нижней третью толщины эпителия ().Умеренная дисплазия эпителия составляет более одной трети, но менее двух третей толщины эпителия (). Тяжелая дисплазия эпителия затрагивает более двух третей толщины эпителия (), в то время как карцинома in-situ означает, что вся толщина эпителия аномальна (), хотя злокачественные клетки еще не стали местно инвазивными. Усложняя прогнозирование того, какие поражения подвергнутся злокачественной трансформации, диспластические поражения могут стать инвазивными OCSCC без предварительного проявления тяжелой эпителиальной дисплазии или полнослойной карциномы in situ.В метаанализе объединенных данных 992 пациентов, частота злокачественной трансформации дисплазии от легкой до умеренной оценивается в 10,3%, в то время как частота злокачественной трансформации от умеренной до тяжелой дисплазии составляет 24,1%. 17
Результаты биопсии
Биопсия с отрицательным результатом на OCSCC не должна рассматриваться как ненужная процедура. Если ткань без дисплазии, это хорошая новость для пациента. В некоторых случаях биопсия выявляет такой диагноз, как мигрирующая эритема, волосатая лейкоплакия, красный плоский лишай или травматическая язвенная гранулема, что объясняет клиническую аномалию и дает обоснование для дальнейшего лечения.Когда гистологический диагноз клинической лейкоплакии или эритроплакии включает слова «без дисплазии» или «поражение доброкачественное», это означает, что периодического клинического наблюдения за любым оставшимся клиническим поражением при повторных визитах (каждые 6–12 месяцев) достаточно для лечения. Конечно, пациенту следует посоветовать обратиться в офис для обследования, если возникнут какие-либо изменения или симптомы, до следующего визита. Исследования показали, что поражения без дисплазии в конечном итоге показали злокачественную трансформацию примерно в 2% случаев. 8 В случае если гистологический анализ отрицательный на дисплазию или степень тяжести меньше, чем ожидалось, исходя из степени и характеристик клинического поражения, клиницист должен без колебаний связаться с патологом, который прочитал слайды, и обсудить необходимость еще одна биопсия. Возможность ошибки выборки является серьезной проблемой, поскольку потенциально злокачественные новообразования полости рта могут быть гистологически гетерогенными, и может быть предоставлен нерепрезентативный образец. Патолог может сообщить только то, что видно на слайде, даже если поражение может быть очень подозрительным с клинической точки зрения.Эту концепцию иллюстрирует.
Если дисплазия отмечена в диагностической строке отчета о биопсии, это важная информация, потому что, хотя дисплазия не является OCSCC, эта ткань имеет больший потенциал для злокачественной трансформации, чем клинически нормальная ткань. Как отмечалось ранее, частота злокачественных трансформаций дисплазии варьируется в зависимости от степени тяжести, что является важным фактором при планировании лечения. При определении метода лечения необходимо учитывать множество дополнительных факторов, таких как степень поражения, расположение в зоне повышенного риска, надежность пациента для последующих посещений, история предыдущих OCSCC, такие привычки, как курение, злоупотребление марихуаной и / или этанолом, а также системные проблемы, такие как иммуносупрессия.В настоящее время нет доказательств эффективного нехирургического лечения для предотвращения прогрессирования диспластических поражений в ОКРК. 18 В ранее упомянутом метаанализе данных 992 пациентов с диспластическими поражениями, у тех, кому не проводилось хирургическое удаление, уровень злокачественной трансформации составил 14,6%, по сравнению с пациентами, у которых очаги поражения были удалены хирургическим путем, у которых уровень злокачественной трансформации составил 5,4%. 17 Однако важно понимать, что даже хирургическое вмешательство не предотвращает все потенциально злокачественные поражения полости рта от злокачественной трансформации. 8
Заключение
Терминология, связанная с потенциально злокачественными поражениями полости рта, была обобщена, чтобы обеспечить лучшее общение между клиницистами и их пациентами, а также другими специалистами, с которыми можно проконсультироваться, такими как патологи полости рта и хирурги. Фотографии были представлены в качестве примеров клинических предупреждающих признаков потенциально злокачественных поражений полости рта, и были описаны надлежащие шаги, которые необходимо предпринять при обнаружении потенциально злокачественных поражений в полости рта.Вероятность злокачественной трансформации любого отдельного потенциально злокачественного поражения полости рта не может быть определена с уверенностью, хотя гистологическое исследование неповрежденной ткани может установить диагноз, связанный с вероятностью прогрессирования заболевания.
Ссылки
1. Линген М.В., Пинто А., Мендес Р.А., Франчини Р., Чернински Р. и др. Генетика / эпигенетика предраковых заболеваний полости рта: текущее состояние и будущие исследования. Устные сообщения . 2011; 17 Дополнение 1: 7-22.
2. Невилл Б.В., Дамм Д.Д., Аллен С.М., Букот Дж. Э. Патология полости рта и челюстно-лицевой области. Сент-Луис, Миссури: Сондерс; 2009.
3. Speight PM. Обновленная информация о дисплазии эпителия полости рта и прогрессировании рака. Head Neck Pathol. 2007; 1 (1): 61-66.
4. Гиллисон М.Л., Д’Соуза Дж., Вестра В., Шугар Е, Сяо В. и др. Четкие профили факторов риска рака головы и шеи, положительного по вирусу папилломы человека 16-го типа и отрицательного по вирусу папилломы человека 16-го типа. J Ntl Cancer Inst . 2008; 100 (6): 407-420.
5. Барнс Л., Эвесон Дж., Райхарт П., Сидрански Д. Классификация опухолей Всемирной организации здравоохранения: патология и генетика опухолей головы и шеи . Лион, Франция: Международное агентство исследований рака Press; 2005.
6. Waldron CA, Shafer WG. Повторное посещение лейкоплакии. Клинико-патологическое исследование 3256 лейкоплакий полости рта. Рак . 1975; 36 (4): 1386-1392.
7. Мелроуз Р.Дж.Предраковые заболевания слизистой оболочки полости рта. Дж. Калифорния Дент Ассо . 2001; 29 (8): 593-600.
8. Холмструп П., Ведтофте П., Райбель Дж., Штольце К. Долгосрочные результаты лечения предраковых поражений полости рта. Oral Oncol. 2006; 42 (5): 461-474.
9. Невилл Б.В., Day TA. Рак полости рта и предраковые поражения. CA Cancer J Clin . 2002; 52 (4): 195-215.
10. Wright JM. Предраковые поражения и состояния полости рта. Semin Dermatol. 1994; 13: 125-131.
11. Shafer WG, Waldron CA. Эритроплакия полости рта. Рак . 1975; 36 (3): 1021-1028.
12. Westra WH. Меняющееся лицо рака головы и шеи в 21 веке: влияние ВПЧ на эпидемиологию и патологию рака полости рта. Голова Шея Патол . 2009; 3 (6): 78-81.
13. Глик М., Джонсон Н.В. Рак полости рта и ротоглотки: что делать дальше? J Am Dent Assoc . 2011; 142 (8): 892-894.
14.ван дер Ваал I, Аксель Т. Оральная лейкоплакия: предложение по унифицированной отчетности. Оральный онкол . 2002; 38 (6): 521-526.
15. Sitheeque MA, Samaranayake LP. Хронический гиперпластический кандидоз / кандидоз (кандидозная лейкоплакия). Crit Rev Oral Biol Med . 2003; 14 (4): 253-267.
16. Куджан О., Оливер Р.Дж., Хаттаб А., Робертс С.А., Таккер Н., Слоан П. Оценка новой бинарной системы оценки оральной эпителиальной дисплазии для прогнозирования злокачественной трансформации. Оральный онкол . 2006; 42 (10): 987-993.
17. Механна Х.М., Раттай Т., Смит Дж., МакКонки СС. Лечение и последующее наблюдение дисплазии полости рта — систематический обзор и метаанализ. Голова Шея . 2009; 31 (12): 1600-1609.
18. Brennan M, Migliorati CA, Lockhart PB, Wray D., Al-Hashimi I, et al. Ведение дисплазии эпителия полости рта: обзор. Oral Surg Oral Med Oral Pathol Oral Radiol Endod . 2007; 103 Приложение: S19.e1-12.
Об авторе
Lynn W.Solomon, DDS, MS
Доцент,
Кафедра стоматологической и челюстно-лицевой патологии
Школа стоматологической медицины Университета Тафтса
Бостон, Массачусетс
Лейкоплакия и эритроплакия слизистой оболочки рта — краткий обзор
Товио Э.Г., Кармона М.С., Диас А.Дж., Харрис Дж., Ланфранки Х.Э. Expresiones clínicas de los desórdenes Potencialmente Malignos en cavidad oral. Revisión integrationtiva de la literatura. Univ Odontol. 2018 энэ-июн; 37 (78).https://doi.org/10.11144/Javeriana.uo37-78.ecdp. SECCIN: Práctica Clínica TITULILLO: Desórdenes Potencialmente Malignos Expresiones clínicas de los desórdenes Potencialmente Malignos en cavidad oral. Revisión integrationtiva de la literatura RESUMEN Antecedentes: Los desórdenes Potencialmente Malignos (DPM) son aquellas situaciones clínicas en la cavidad bucal que presentan un riesgo aumentado de malignización neoplásica, debido a la exasición de alraciones de factores de factores. Es necesario realizar revisiones de la evidencia de este tipo de desórdenes para desarrollar o actualizar guías de práctica clínica idóneas.Objetivo: Identificar, través de una revisión integrationtiva de la literatura, la Evidencia reciente sobre DPM de la cavidad bucal y su transformación maligna, con el fin de proporcionar recomendaciones de manejo diagnóstico y terapéutico. Методы: Реализуйте свою литературу на основе баз данных PubMed, Elsevier, SciELO y EMBASE, используя комбинацию этих описаний. Результат: La búsqueda inicial arrojó 1743 títulos y la muestra consistió en 67 artículos después de aplicar los criterios de inclusión y exclusión.Las DPM Identificadas fueron liquen plano oral, palatitis nicotínica, hábito de fumar invtido, queilitis actínica, eritroplasia y leucoplasia oral y úlcera traumática crónica. Заключение: Cada tipo de lesión tiene specificto Potencial de Malignización, entre los cuales la eritroplasia, el liquen plano oral variante erosivo y la queilitis actínica poséen el mayor riesgo. РЕФЕРАТ PALABRAS CLAVE Предпосылки: Потенциально злокачественные заболевания (PMD) — это клинические состояния полости рта, которые представляют повышенный риск неопластической малигнизации из-за воздействия факторов риска или генетических изменений.Для разработки или обновления адекватных клинических рекомендаций необходимо проводить научно обоснованные обзоры этого типа расстройств. Цель: посредством комплексного обзора литературы выявить последние данные о ПМД в полости рта и их злокачественной трансформации, чтобы предоставить рекомендации по диагностике и лечению. Методы. Был проведен поиск литературы в PubMed, Elsevier, SciELO и EMBASE с использованием комбинации шести дескрипторов. Результаты. Первоначальный поиск показал 1743 заголовка, а после применения критериев включения и исключения выборка состояла из 67 статей.Среди выявленных ПМД были красный плоский лишай ротовой полости, никотиновый палатит, обратная привычка к курению, актинический хейлит, эритроплакия и лейкоплакия полости рта, а также хроническая травматическая язва.
Контуры патологии — Лейкоплакия
Полость рта и ротоглотка
Потенциально злокачественная и дисплазия
Лейкоплакия
Тема завершена: 15 февраля 2021 г.
Незначительные изменения: 15 февраля 2021 г.
-2021 Copyrightcom, Inc.
PubMed Search : Обзор лейкоплакии полости рта [TI] [PT]
просмотров страниц в 2020 году: 11,719
просмотров страниц в 2021 году на сегодняшний день: 2948
Цитируйте эту страницу: Стоянов И.Я. Лейкоплакия. Сайт PathologyOutlines.com. https://www.pathologyoutlines.com/topic/oralcavityleukoplakia.html. По состоянию на 26 февраля 2021 г.
Определение / общее
- Гиперкератотический (белый) налет / участок слизистой оболочки, демонстрирующий клональность и представляющий собой предшественник плоскоклеточного рака.
- Термин лейкоплакия / лейкоплакия также используется описательно в клинических условиях для обозначения любого белого поражения без очевидного диагноза
- Такое использование может исказить понимание биологии / поведения лейкоплакии из-за преобладания фрикционных / реактивных кератозов в полости рта, которые не всегда клинически распознаются, но не имеют злокачественного потенциала (Head Neck Pathol 2019; 13: 423)
- Определяется ВОЗ как белый налет сомнительного риска, исключающий (другие) известные заболевания или расстройства, не несущие повышенного риска развития рака (J Oral Pathol Med 2007; 36: 575)
- Лейкоплакия может возникать в верхних отделах пищеварительного тракта.
Основные признаки
- Гиперкератотический (белый) бляшек / участок слизистой оболочки, демонстрирующий клональность и представляющий собой предшественник плоскоклеточного рака
- Примерно 40% лейкоплакий демонстрируют ороговевшую дисплазию; для остальных характерен только гиперкератоз
- Годовая частота злокачественной трансформации составляет 3% и наиболее точно прогнозируется наличием дисплазии при биопсии; увеличение продолжительности, увеличение размера и негомогенный внешний вид, также связанные со злокачественной трансформацией
- Лейкоплакия, проявляющая гиперкератоз, который не является фрикционным / реактивным, демонстрирует скорость злокачественной трансформации приблизительно 5%, аналогичную легкой эпителиальной дисплазии
- Гистологический вид лейкоплакии неотличим от пролиферативной (бородавчатой) лейкоплакии и требует клинической корреляции
- Хирургическое удаление снижает риск злокачественной трансформации примерно в 3 раза
Терминология
- Лейкоплазия, эритролейкоплакия, эритроплакия
Кодировка МКБ
- МКБ-10: K13.21 — Лейкоплакия слизистой оболочки рта, в том числе языка
Участки
- Может присутствовать на любой поверхности слизистой оболочки
- Связано с самой высокой частотой злокачественной трансформации, возникающей на вентролатеральном языке или дне рта (Oral Oncol 2009; 45: 317)
Патофизиология
- Лейкоплакия, демонстрирующая ороговевшую дисплазию, характеризующуюся геномными изменениями, включая мутации TP53 и потерю гетерозиготности в 3p и 9p (Cancer Prev Res (Phila) 2012; 5: 1081)
- Лейкоплакия, проявляющая только гиперкератоз, характеризуется геномными изменениями, включая мутации KMT2C, TP53 и TIAM1 (Oral Dis 2019; 25: 1707)
- Модель генетической прогрессии рака головы и шеи не очень хорошо проработана, особенно в отношении ранних предшественников (Clin Cancer Res 2000; 6: 347)
Этиология
- Связано с курением / бездымным табаком, алкоголем и употреблением орехов арека (бетель квид)
- ВПЧ связаны только с очень небольшим процентом случаев (Mod Pathol 2017; 30: 1646)
Клинические признаки
- Гиперкератоз на участках слизистой оболочки, не поддающихся фрикционной / искусственной травме, особенно при резкой границе, считается клинически опасным (J Oral Maxillofac Surg 2017; 75: 723)
- Доказанная биопсией лейкоплакия может клинически казаться гомогенной или негомогенной (Oral Oncol 2009; 45: 317)
- Гомогенная лейкоплакия: однородный тонкий или толстый гиперкератоз, часто резко отграниченный
- Негомогенная лейкоплакия: неправильная текстура с трещинами, узловатыми / бородавчатыми компонентами или компонентами эритематозной эритролейкоплакии (эритролейкоплакия)
- Пролиферативная (бородавчатая) лейкоплакия: необычное и значительно более агрессивное (уровень злокачественной трансформации 60-100%) заболевание, характеризующееся мультифокальным поражением слизистой оболочки полости рта и склонностью к женщинам среднего и пожилого возраста, не употребляющих табак или алкоголь в анамнезе или минимально (Устное сообщение 2018; 24: 749)
- Лучше всего рассматривать как отдельное заболевание на основании различных демографических / клинических проявлений, биологического поведения и соображений ведения пациента
Диагноз
- Биопсия, необходимая для диагностики и стратификации риска
- Лейкоплакия с дисплазией, легко диагностируемая на основе обычных гистопатологических признаков эпителиальной дисплазии (Head Neck Pathol 2019; 13: 423)
- Лейкоплакия без дисплазии требует клинико-патологической корреляции и исключения фрикционных / фактических признаков, выявленных клинически или гистопатологически
Факторы прогноза
- Годовая частота злокачественной трансформации 3% (Oral Oncol 1998; 34: 270)
- Наличие эпителиальной дисплазии, наиболее значимого фактора риска злокачественной трансформации (Oral Oncol 2009; 45: 317, Mod Pathol 2017; 30: S112)
- Тяжелая дисплазия эпителия: 28.4% риск
- Умеренная дисплазия эпителия: риск 22,5%
- Легкая дисплазия эпителия: риск 5,7%
- Гиперкератоз: риск 4,9%
- Сообщенные общие показатели злокачественной трансформации 0,36-34% трудно интерпретировать из-за исторического включения фрикционных / реактивных кератозов в когорты лейкоплакии и вариабельности продолжительности наблюдения (J Oral Pathol Med 2016; 45: 155)
- Продолжительность, увеличение размера и негомогенный внешний вид, связанные с повышенным риском злокачественной трансформации
Лечение
- Хирургическое удаление приводит к 3-кратному снижению риска злокачественной трансформации (Head Neck 2009; 31: 1600)
- Лейкоплакию с дисплазией высокой степени (средней / тяжелой) следует удалять по возможности.
- Тщательное клиническое наблюдение может быть подходящим для обширной лейкоплакии или пациентов с сопутствующими заболеваниями, но в остальном, по-видимому, оно играет ограниченную роль, когда возможно консервативное хирургическое лечение (J Oral Maxillofac Surg 2017; 75: 723)
Клинические изображения
Предоставлено Иваном Дж.Стоянов, D.M.D., M.M.Sc.
Лейкоплакия задней верхней челюсти слева
Лейкоплакия задней верхней челюсти справа
Лейкоплакия левого вентрального языка
Обширная лейкоплакия языка
Микроскопическое (гистологическое) описание
- Лейкоплакия с дисплазией демонстрирует архитектурные и цитологические особенности ороговевшей дисплазии
- Признаки включают гиперкератоз / паракератоз, атрофию эпителия или гиперплазию с луковичными сетчатыми гребнями, гиперплазию базальных клеток с ядерной гиперхромазией или повышенным ядерным цитоплазматическим соотношением, различные супрабазальные или атипичные митозы, дискератоз или стекловидную цитоплазму
- Примерно 33% дисплазий характеризуются воспалительным инфильтратом и не должны ошибочно диагностироваться как красный плоский лишай (Oral Surg Oral Med Oral Pathol Oral Radiol 2014; 117: 511)
- Лейкоплакия без дисплазии проявляет гиперкератоз без гистологических признаков фрикционного / реактивного процесса, но в остальном охарактеризован хуже
- Гистологические признаки включают (Head Neck Pathol 2019; 13: 423):
- Компактный гиперкератоз с гипергранулезом
- Тонкая веррукоидная архитектура
- Атрофия или гиперплазия эпителия
- Если взять образец периферии лейкоплакии, гиперкератоз будет резко разграничен
- Гистологические признаки включают (Head Neck Pathol 2019; 13: 423):
- Некоторые лейкоплакии без дисплазии могут иметь выраженную бородавчатую архитектуру и сообщаться как бородавчатая гиперплазия
Микроскопические (гистологические) изображения
Предоставлено Иваном Дж.Стоянов, D.M.D., M.M.Sc.
Волнистая / веррукоидная структура поверхности
Отсутствие эпителиальной атипии
Гиперкератоз резко отграниченный
Веррукозная гиперплазия
Периферия лейкоплакии
Дисплазия средней степени
Лейкоплакия без дисплазии
Паракератоз и гиперплазия эпителия
Гиперкератоз и атрофия эпителия
Минимальные цитологические диспластические признаки
Описание цитологии
- В настоящее время ограниченная роль цитологии:
- Сложность взятия адекватной ткани у пациентов без анестезии
- Эпителиальная атипия, если присутствует, трудно классифицировать как реактивную или диспластическую при отсутствии архитектурных особенностей
- Паттерны ороговения не поддаются оценке
- Участки полости рта, легко поддающиеся послеоперационной биопсии
Молекулярно-цитогенетическое описание
Молекулярные / цитогенетические изображения
Изображения, размещенные на других серверах:
Лейкоплакия CGH по сравнению с SCC
Гены, участвующие в злокачественной трансформации
Образец отчета о патологии
- Нижняя челюсть, десна, послеоперационная биопсия:
- Гиперкератоз, атрофия эпителия и легкое хроническое воспаление, не реактивное (см. Комментарий)
- Комментарий: Гиперкератоз не проявляет признаков фрикционного / реактивного процесса и напоминает поверхностное ороговение, обычно наблюдаемое при эпителиальных дисплазиях.Цитологическая атипия минимальна / отсутствует в этом образце, но лейкоплакия без дисплазии (гиперкератоз, который не является реактивным) имеет злокачественную трансформацию примерно 5%, что аналогично лейкоплакии с легкой дисплазией. Полученные данные согласуются с клинически наблюдаемой лейкоплакией, которая примерно в 60% случаев протекает без дисплазии. Если клинический контекст подходит, можно также рассмотреть пролиферативную (бородавчатую) лейкоплакию.
Дифференциальный диагноз
- Доброкачественный кератоз альвеолярного гребня :
- Гистологические признаки сходны с простым хроническим лишаем
- Гиперплазия эпителия с бородавчатой / волнообразной поверхностью и клиновидным гипергранулезом
- Компактный гиперкератоз, сужающийся к краям и не очерченный резко
- Удлиненные гребни ретейна, иногда сливающиеся на концах
- Нет эпителиальной атипии
- Фиброз и редкое хроническое воспаление
- Хронический фрикционный / искусственный кератоз :
- Лохматый / мацерированный паракератоз с поверхностной бактериальной колонизацией
- Гиперплазия эпителия с отеком кератиноцитов, но без атипии эпителия
- Вариабельный фиброз, острое и хроническое воспаление и экзоцитоз лейкоцитов
- Красный плоский лишай / лихеноидный мукозит:
- Скваматизация / дегенерация базального слоя клеток с тельцами Civatte (дискератотические кератиноциты)
- Лентовидный лимфоплазматический гистиоцитарный инфильтрат в собственной поверхностной пластинке с лейкоцитарным экзоцитозом и спонгиозом
- Пролиферативная (бородавчатая) лейкоплакия:
- Клинически характеризуется мультифокальной лейкоплакией
- Поражение десен часто
- Пристрастие к женщинам среднего и пожилого возраста, при отсутствии / минимальном воздействии табака или алкоголя
- Причина этой ассоциации неясна
- Гистологически неотличимы от лейкоплакии
- Веррукозная эпителиальная архитектура обычна, но не обязательно присутствует
- Клинически характеризуется мультифокальной лейкоплакией
Вопрос стиля проверки совета директоров № 1
У курильщика 57 лет обнаружена лейкоплакия на левом вентральном языке.Что является наиболее важным предиктором злокачественной трансформации?
- Продолжительность
- Однородный внешний вид
- Неоднородный внешний вид
- Наличие дисплазии эпителия при биопсии
- Размер
Вопрос о стиле проверки совета директоров № 2
Что из следующего верно относительно лейкоплакии без дисплазии?
- Его можно легко распознать по гистологическим признакам фрикционного / реактивного процесса.
- Может подвергаться злокачественной трансформации
- Обычно это связано с инфекцией ВПЧ.
- Диагностика пролиферативной (бородавчатой) лейкоплакии.
- Редко встречается при биопсии лейкоплакии.
