Дифтерия — симптомы, причины и лечение
Лечением данного заболевания занимается Отоларинголог (ЛОР) , Педиатр , Инфекционист
- Что это такое?
- О заболевании
- Виды
- Симптомы
- Причины
- Диагностика
- Мнение эксперта
- Лечение
- Профилактика
- Вопросы и ответы
О заболевании
Дифтерия – что это за болезнь с этиопатогенетической точки зрения? Патология относится к типичным антропонозным инфекциям, которые передаются от человека к человеку. Причинные бактерии проникают в организм обычно через слизистые оболочки зева. В области входных ворот наблюдается активное размножение коринебактерий. Через 2-4 суток с момента заражения начинается выработка бактериальных токсинов, которые оказывают повреждающее воздействие на ткани и приводят к появлению клинической симптоматики.
Дифтерийный токсин вызывает паретическое расширение кровеносных и лимфатических сосудов, что приводит к развитию выраженного отека слизистой и подкожной клетчатки. Поступление экзотоксина в кровоток может приводить к повреждению сердца, сосудов, нервной ткани, мочевой системы.
Заболевание может протекать с разной степенью тяжести. Наиболее типичные проявления – это лихорадка, боли в горле, наличие фибринозного налета. Окончательная диагностика осуществляется на основании лабораторных исследований, направленных на идентификацию возбудителя или его антител.
Лечение заключается во введении нейтрализующей токсин сыворотки и назначении антибиотиков. Одновременно с этим проводится коррекция развившихся нарушений и потенциальных осложнений.
Виды дифтерии
По локализации различают следующие виды дифтерии – гортани, зева, носа, глаз. Помимо распространенных вариантов встречаются и редкие локализации – кожные покровы, половые органы. Возможны также комбинированные формы, когда сочетаются типичные поражения с редкими вариантами.
По степени тяжести дифтерия делится на 3 разновидности:
- легкая, когда патологический процесс локализован в месте внедрения патогенных бактерий;
- среднетяжелая, когда токсины и бактерии распространяются по организму, прорывая локальные защитные барьеры;
- тяжелая, которая делится на подклассы – субтоксический, токсический 3 степеней тяжести и гипертоксический, для которого характерно наиболее тяжелое течение.
Симптомы дифтерии
Инкубационный период заболевания обычно продолжается от 2 до 10 суток.
Локализованная форма инфекции, которая является самым легким вариантом, начинается с повышения температуры тела и появления жалоб на боль в горле при глотании.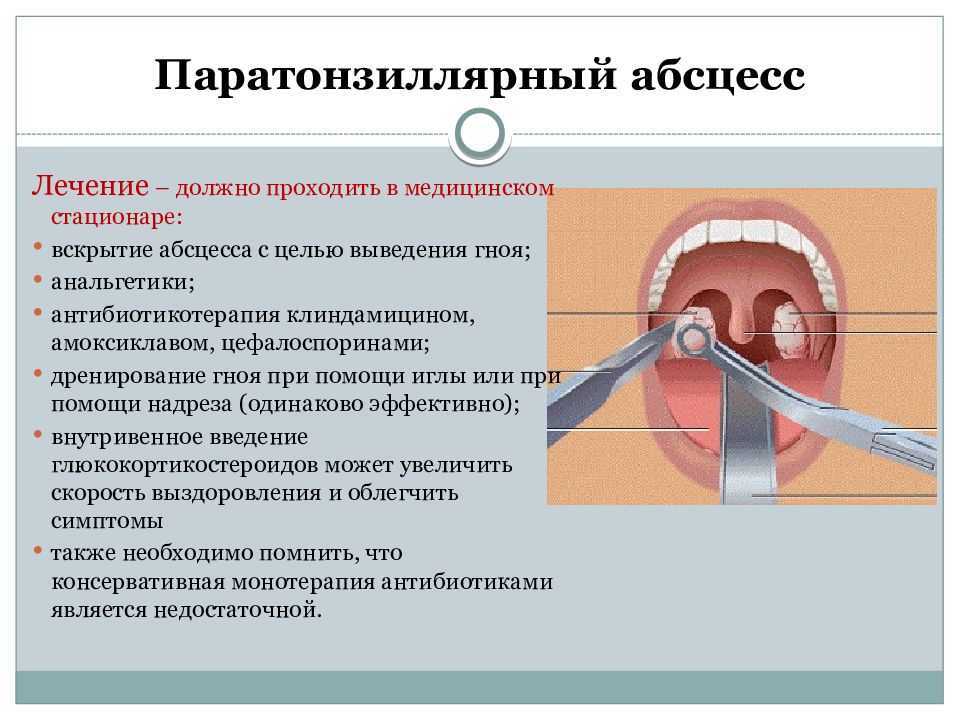 В зависимости от внешнего вида миндалин и ротоглотки локализованную форму делят на пленчатую и островчатую.
В зависимости от внешнего вида миндалин и ротоглотки локализованную форму делят на пленчатую и островчатую.
- При островчатой форме симптомы дифтерии включают в себя отечность миндалин и небных дужек, покраснение с синюшным оттенком, появление участков на миндалинах, покрытых фибринозным налетом.
- При пленчатой форме сначала типичные серо-белые налеты отсутствуют. Так, на первых порах они имеют розовый полупрозрачный цвет. Через 1-2 суток они превращаются в фибринозные пленки.
Только что образованные пленки с поверхности слизистой снимаются без труда. Однако вскоре они уплотняются и после их снятия остаются кровоточащие эрозированные поверхности.
Распространенная форма дифтерии диагностируется в том случае, если воспалительный процесс распространяется на язычок, мягкое небо, слизистую рта, гортань, нос. Это существенно утяжеляет течение заболевания.
Для токсической формы дифтерии характерно внезапное острое начало. Первыми проявлениями заболевания являются высокая лихорадка и выраженные симптомы интоксикации (головная боль, озноб, жажда, общая слабость, плохой аппетит, бледность кожных покровов). У взрослого или ребенка может появляться повторяющаяся рвота, боли в животе, резкая смена настроения (адинамия быстро сменяется возбуждением и наоборот). Беспокоит боль при глотании и в области шеи, определяется болезненность регионарных лимфатических узлов (они становятся плотными и увеличенными). Важным признаком токсической формы является отек зева. Сначала отекают миндалины, затем дужки и небо. Отек не имеет четких границ и сочетается с синюшным покраснением слизистой. Фибринозный налет в начале имеет вид паутинки, но вскоре он уплотняется и становится опалесцирующим.
У взрослого или ребенка может появляться повторяющаяся рвота, боли в животе, резкая смена настроения (адинамия быстро сменяется возбуждением и наоборот). Беспокоит боль при глотании и в области шеи, определяется болезненность регионарных лимфатических узлов (они становятся плотными и увеличенными). Важным признаком токсической формы является отек зева. Сначала отекают миндалины, затем дужки и небо. Отек не имеет четких границ и сочетается с синюшным покраснением слизистой. Фибринозный налет в начале имеет вид паутинки, но вскоре он уплотняется и становится опалесцирующим.
При токсической форме налет всегда выходит за пределы миндалин. Он приводит к появлению неприятного приторно-кислого запаха изо рта. В период разгара присутствует подкожный отек шеи. В зависимости от его распространенности определяется степень тяжести токсической формы. Так, при первой степени отек доходит до середины шеи, при второй – не опускается ниже ключиц, а при третьей – распространяется ниже ключиц.
Гипертоксическая форма может протекать в виде молниеносного или геморрагического варианта.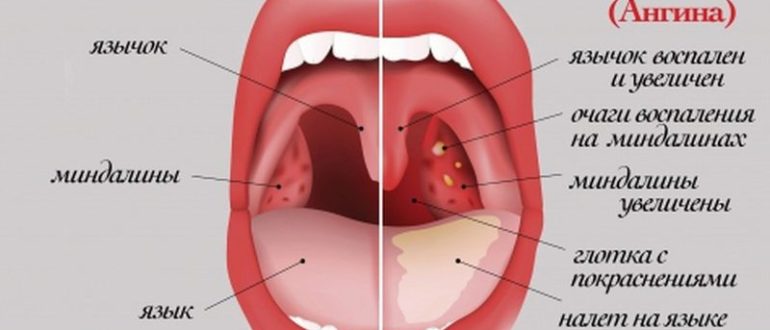
- Для геморрагической формы характерно острое начало, при этом с 3-5-х суток на коже и слизистых появляются геморрагии (петехиальная сыпь). Они имеют вид точечных петехий темного (черного) цвета. В местах инъекций кровь плохо сворачивается, появляются десневые кровотечения. Опасность этой формы в вероятности развития диссеминированного внутрисосудистого свертывания, когда в одних сосудах происходит образование тромбов, а в других – запускаются процессы их лизиса. Риски ДВС-синдрома заключаются в тромбогреморрагических осложнениях.
- При молниеносной форме события развиваются очень быстро. На фоне выраженной интоксикации формируется сосудистая недостаточность и миокардит, которые представляют непосредственную опасность для жизни человека. Кожные покровы при этой форме всегда очень бледные, больной апатичен.
Причины дифтерии
Причины дифтерии – corynebacterium diphtheriae. Дифтерия передается от больного человека здоровому. Путь передачи заболевания – воздушно-капельный. Отмечается сезонный пик заболеваемости. Наибольшее количество случаев дифтерийной инфекции приходится на осенний и зимний периоды.
Отмечается сезонный пик заболеваемости. Наибольшее количество случаев дифтерийной инфекции приходится на осенний и зимний периоды.
Возбудителем дифтерии являются токсигенные штаммы дифтерийных палочек, которые относятся к роду коринебактерий. Дифтерийная палочка продуцирует ряд токсинов, из которых наиболее значимыми в патогенезе являются:
- экзотоксин;
- нейротоксин;
- гемолизин;
- гиалуронидаза;
- нейраминидаза.
Особенно опасным является экзотоксин, который состоит из А- и В-фрагмента. Последний нарушает состояние клеточной оболочки и способствует проникновению А-фрагмента в клетку. Это вещество вмешивается в синтез белка и приводит к гибели клетки.
Дифтерийные палочки обладают значительной устойчивостью к воздействию факторов окружающей среды. Так, в пыли они сохраняются около 5 недель, в воде и молоке – до 3 недель. Кипячение в течение 1 минуты приводит к гибели патогена.
Получить консультацию
Если у Вас наблюдаются подобные симптомы, советуем записаться на прием к врачу.
Узнать подробности о заболевании, цены на лечение и записаться на консультацию к специалисту Вы можете по телефону:
+7 (495) 292-39-72
Заказать обратный звонок Записаться онлайн
Почему «СМ-Клиника»?
1
Лечение проводится в соответствии с клиническими рекомендациями
2
Комплексная оценка характера заболевания и прогноза лечения
3
Современное диагностическое оборудование и собственная лаборатория
4
Высокий уровень сервиса и взвешенная ценовая политика
Методы диагностики дифтерии
После снятия бело-серого пленчатого налета возможна оценка важных дифференциально-диагностических признаков. Фибринозная дифтиритическая пленка не растворяется в воде, не тонет, не утрачивает свою форму и не растирается между стеклами. Диагноз дифтерии базируется на клинических и лабораторных данных.
- Бактериологический посев отделяемого из носа и ротоглотки.
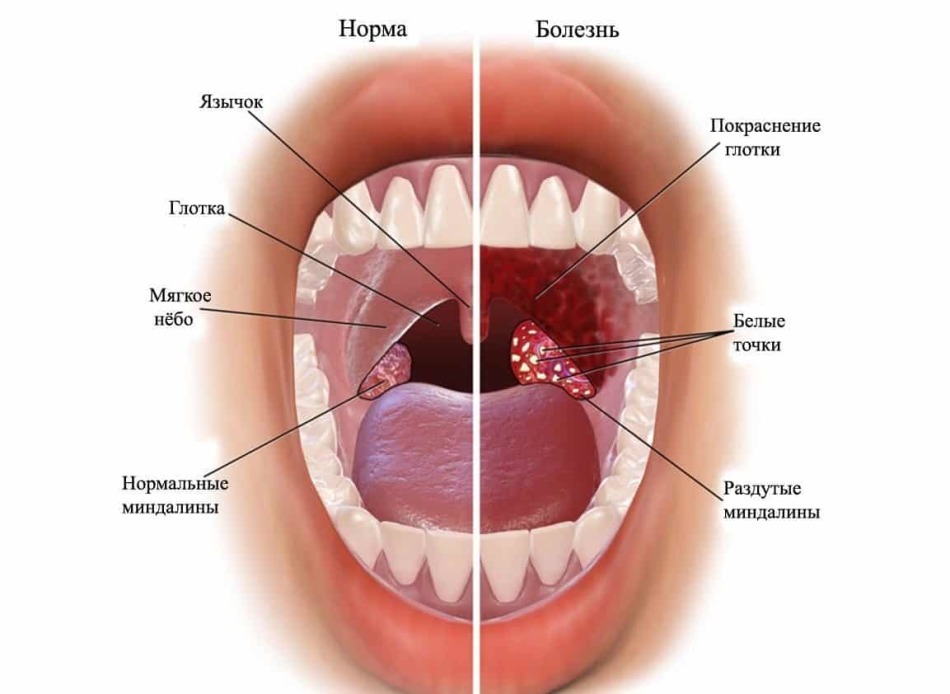 По характеру выросших колоний микробиолог идентифицирует видовую принадлежность возбудителя.
По характеру выросших колоний микробиолог идентифицирует видовую принадлежность возбудителя. - Серологические методы диагностики дифтерии. Позволяют определить в крови уровень специфических антител (иммуноглобулинов).
- Выявление дифтерийного токсина в сыворотке крови. Относится к методу ранней диагностики.
Мнение эксперта
Одним из грозных осложнений заболевания является дифтерийный круп (стенозирующий ларинготрахеит). Это состояние характеризуется резким нарушением проходимости гортани и трахеи, что не позволяет воздуху в полном объеме поступать в легкие. Круп создает условия для развития острой дыхательной недостаточности, поэтому требуется незамедлительное оказание помощи. Круп особенно часто встречается у детей с дифтерийной инфекцией. В течении этого состояния врачи выделяют 3 стадии. На первой стадии появляется громкий лающий кашель, голос становится осипшим (может развиться полная утрата голоса – афония). Во второй стадии дыхание становится очень шумным, появляется втяжение межреберных промежутков и других податливых мест грудной клетки.
Марцишевская Евгения Анатольевна
Врач-педиатр, врач-инфекционист, к.м.н.
Лечение дифтерии
Лечение дифтерии направлено на нейтрализацию дифтерийного токсина, который и определяет патогенные свойства коринебактерий. Для этого вводится антитоксическая противодифтерийная сыворотка. Помимо патогенетического направления комплексная терапия включает в себя:
- коррекцию измененной гемодинамики;
- улучшение обменных процессов в тканях;
- купирование дыхательных расстройств;
- снижение повышенной температуры тела;
- борьба с дисфункцией иммунной системы;
- противовоспалительные кортикостероидные средства (вводятся при тяжелом течении, когда воспаление как защитная реакция начинает представлять прямую опасность для организма человека).

Противодифтерийная сыворотка может проявлять аллергенные свойства, поэтому перед ее первым введением выполняется кожная тест-проба (согласно клиническим рекомендациям по дифтерии). Лечебная доза анатоксина зависит от степени тяжести заболевания. Длительность этиопатогенетического лечения также определяется тяжестью течения бактериального процесса. При локализованной форме обычно достаточно однократного введения, при токсических формах показано повторное введение.
Важным направлением лечения является дезинтоксикация. При легком течении заболевания больному рекомендуется больше пить жидкости комфортной температуры, при токсических формах – внутривенно вводятся кристаллоидные растворы. В случае гипертоксических форм могут быть показаны методы экстракорпоральной детоксикации (плазмаферез, гемосорбция).
В рамках комплексного лечения врач также назначает антибактериальные препараты, которые подавляют жизнедеятельность коринебактерий. Антибактериальный курс продолжается 1-1,5 недели. Таким образом, противодифтерийный анатоксин наносит удар по уже образованному экзотоксину, а антибиотики приводят к гибели бактерий, предупреждая повторное образование опасного токсина.
Таким образом, противодифтерийный анатоксин наносит удар по уже образованному экзотоксину, а антибиотики приводят к гибели бактерий, предупреждая повторное образование опасного токсина.
Меры профилактики дифтерии
Основной мерой профилактики дифтерии является вакцинация. Трехкратное введение вакцины позволяет сформировать стойкий иммунитет к возбудителю заболевания.
На лиц, которые контактировали с больным дифтерией, или носителями причинно значимых бактерий накладывается карантин. Карантин снимается не раньше, чем через 1 неделю, при этом обязательным условием является получение отрицательного результата бактериологического исследования.
Вопросы и ответы
Диагностикой и лечением дифтерийной инфекции занимается врач-инфекционист.
Помимо истинного крупа эта инфекция может приводить к таким последствиям, как поражение сердца (миокардит), воспаление нервных структур и почек.
Это состояние бывает первичным, когда фибринозные налеты изначально появляются на слизистой оболочке носовых ходов, и вторичным, когда воспаление из зева и гортани распространяется в полость носа.
Если женщина не вакцинирована от этой инфекции, то при контакте с патогенными коринебактериями может развиться заболевание.
Дифтерия вызывается не вирусом, а бактериями, поэтому для ее лечения используются антибиотики.
Суджаев Г.А. Закономерности дифтерийного эпидемического процесса в различные периоды иммунизации. Мат. V съезда гигиен., эпидемиол. и инф. Белоруссии. Минск, 1971. С. 431-434.
World Health Organization. The Global Vaccine Action Plan 2011–2020. Introduction and Immunization Landscape Today.
Болотовский В.М., Крюков В.Ю., Титова Н.С. Эпидемиологический надзор за дифтерией и корью. Журн. микробиол. 1986. № 10. С. 21-27.
>
Заболевания по направлению Отоларинголог (ЛОР)
Аденоидит Аллергический ринит Ангина Ангина катаральная Ангина лакунарная Ангина фолликулярная Болезнь Меньера Воспаление лимфоузлов Гайморит Гнойный отит Искривление носовой перегородки Киста в пазухе Ларингит Наружный отит Неврит слухового нерва Нейросенсорная тугоухость Остеома лобной пазухи Отит Отомикоз Отосклероз Перелом носа Перфорация барабанной перепонки Полипы в носу Полисинусит Поллиноз Ринит Ринит вазомоторный Серная пробка Синусит Средний отит Стеноз гортани Сфеноидит Тонзиллит хронический Трахеит Тубоотит (евстахиит) Тугоухость (глухота) Ушной шум (тиннитус) Фарингит Фиброма гортани Фронтит Хронический гайморит Хронический ринит Этмоидит
Заболевания по направлению Инфекционист
Анизакидоз Анкилостомидоз Аскаридоз Балантидиаз Бластомикоз Бруцеллез Вирус Эпштейна-Барра Вирусная инфекция Вирусный гепатит Гастроэнтерит Гастроэнтероколит Гемофильная инфекция Генитальный герпес Грипп Диарея путешественников Дизентерия Дифиллоботриоз Желтуха Коклюш Краснуха
Заболевания по направлению Педиатр
Гемофильная инфекция Коклюш
Все врачи
м. Севастопольская
Севастопольская
м. Чертановская
м. Марьина Роща
м. Войковская
м. Балтийская
м. Улица 1905 года
м. Юго-Западная
Все врачи
Загрузка
Записаться на прием к инфекционисту
поля, отмеченные*, необходимы к заполнению
Имя
Телефон *
Нажимая на кнопку, вы даете согласие на обработку своих персональных данных
Запись через сайт является предварительной. Наш сотрудник свяжется с Вами для подтверждения записи к специалисту.
Мы гарантируем неразглашение персональных данных и отсутствие рекламных рассылок по указанному вами телефону. Ваши данные необходимы для обеспечения обратной связи и организации записи к специалисту клиники.
Лицензии
Перейти в раздел лицензииПерейти в раздел правовая информация
Дифтерия — АЛМ Медицина
Дифтерия – острое инфекционное заболевание с воздушно-капельным путем передачи, характеризующееся токсическим поражением преимущественно сердечно-сосудистой и нервной систем, местным воспалительным процессом с образованием фиброзного налета.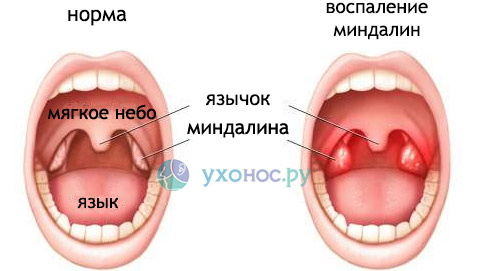
Возбудитель – дифтерийная палочка (Corynebacterium diphteriae). Токсичное действие дифтерийной палочки связано со специфическим экзотоксином, который всасывается в кровь и вызывает общую интоксикацию с поражением миокарда, периферической и вегетативной нервной системы, почек, надпочечников.
Источником заражения дифтерией является только человек – больной или бактерионоситель. Входными воротами инфекции являются слизистые оболочки ротоглотки, носа и гортани. Инкубационный период – от 2 до 10 дней.
В зависимости от локализации различают дифтерию зева, носа, гортани, глаз и др.
Дифтерия зева – бывает локализованная, распространенная и токсическая формы дифтерии зева.
Локализованная форма – фибринозный налет на миндалинах, зев умеренно гиперемирован, боли при глотании выражены умеренно или слабо, регионарные лимфоузлы увеличены незначительно. Общая интоксикация не выражена, температура невысокая.
При распространенной форме – фибринозные налеты переходят на слизистую оболочку небных дужек и язычка, интоксикация выражена, температура высокая, лимфоузлы сильно увеличены.
Токсическая форма дифтерии характеризуется резким увеличением миндалин, отеком слизистой оболочки зева и образованием толстых грязно-белых налетов, общее состояние больного резко нарушено, температура тела высокая(39-400С), общая разбитость, слабость, анорексия, иногда рвота, боли в животе.
Дифтерия гортани (дифтерийный круп) – характеризуется крупозным воспалением слизистой оболочки гортани и трахеи. Течение болезни быстро прогрессирующее. Характерно –высокая температура, нарастающая осиплость голоса, далее прогрессируют симптомы стеноза верхних дыхательных путей – шумное дыхание, напряжение вспомогательной дыхательной мускулатуры. Если своевременно не оказать помощь, больной может умереть от асфиксии.
Дифтерия носа, гортани, конъюнктивы глаз, наружных половых органов в последнее время наблюдается редко.
Осложнения дифтерии возникают в результате воздействия токсина в остром периоде болезни, хотя изменения со стороны пораженных органов проявляются позже, в разные сроки болезни. Наиболее характерные осложнения дифтерии возникают со стороны сердечно-сосудистой системы (миокардит), периферической нервной системы(невриты и полиневриты) и почек (нефротический синдром).
Наиболее характерные осложнения дифтерии возникают со стороны сердечно-сосудистой системы (миокардит), периферической нервной системы(невриты и полиневриты) и почек (нефротический синдром).
Дифференцировать дифтерию необходимо с ангинами, инфекционным мононуклеозом, «ложным крупом», пленчатым аденовирусным конъюнктивитом.
Несмотря на большое разнообразие клинических проявлений, существует ряд общих признаков, типичных для дифтерии – наличие плотной беловато-серой фибринозной пленки на слизистой оболочке ротоглотки, носа, гортани и т.п. Лимфоузлы увеличены в соответствии с местным процессом, плотные на ощупь, умеренно болезненны. Температура тела в зависимости от тяжести заболевания — 37,5-38,50С при легких и среднетяжелых формах и до 400С- при тяжелых формах течения болезни. Резкая болезненность при глотании , яркая гиперемия, длительная лихорадка не характерны для дифтерии и свидетельствуют против этого диагноза.
Подтверждением диагноза служит выделение токсигенных дифтерийных палочек при бактериологическом исследовании.
Лечение дифтерии предусматривает специфическую терапию – внутримышечное введение противодифтерийной сыворотки в дозах, зависящих от степени интоксикации и сроков начала лечения.
Основой успешной борьбы с дифтерией является активная иммунизация (вакцинация). С этой целью используют дифтерийный анатоксин(АД-анатоксин), который входит в состав следующих вакцин: АКДС, Пентаксим, АДС, АДС-м, Инфанрикс.
Больные дифтерией подлежат обязательной госпитализации, в квартире больного после его изоляции проводят окончательную дезинфекцию.
Профилактические прививки предохраняют население от тяжелых форм дифтерии и неблагоприятных исходов.
Сезонные акции
Направления
Стоматология
Взрослая поликлиника
Детская поликлиника
Диагностика
Вызов врача на дом
Онлайн консультации
Медицинский справочник
Что такое
Миокардиты (неревматические)?УзнатьАденоидные камни – «Аденолиты» — PMC
- Список журналов
- Рукописи авторов HHS
- PMC4718572
Дж Отол Ринол. Авторская рукопись; доступно в PMC 2016 19 января.
Авторская рукопись; доступно в PMC 2016 19 января.
Опубликовано в окончательной редакции как:
J Otol Rhinol. 2015 сен; 4(4): 240.
Published online 2015 Jul 13. doi: 10.4172/2324-8785.1000240
PMCID: PMC4718572
NIHMSID: NIHMS723554
PMID: 26798664
, 1, * , 2 и 1
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности
Камни, состоящие из скоплений бактерий, могут быть обнаружены в хронически воспаленных лимфоидных тканях, таких как гипертрофированные миндалины. Хотя в скрытых миндалинах часто обнаруживаются миндалины, камни в аденоидной ткани обнаруживаются редко. Здесь мы представляем интересный случай пациента, перенесшего аденоидэктомию по поводу гипертрофии аденоидов, рецидивирующего недомогания и инфекций верхних дыхательных путей. Интраоперационно в криптах аденоидной ткани обнаружены многочисленные камни ярко-зеленого цвета, напоминающие миндалины в криптах миндалин. При патологии выявляются полимикробные бактериальные агрегаты, окруженные нейтрофилами. Наши данные свидетельствуют о том, что патофизиология аналогична таковой при образовании миндалин. Таким образом, мы должны, по крайней мере, учитывать наличие аденоидных камней и рассматривать аденоидэктомию при симптомах, часто приписываемых миндалинам. Мы ввели термин «аденолиты», чтобы описать это интересное открытие и представить его как потенциальный источник рецидивирующей инфекции.
При патологии выявляются полимикробные бактериальные агрегаты, окруженные нейтрофилами. Наши данные свидетельствуют о том, что патофизиология аналогична таковой при образовании миндалин. Таким образом, мы должны, по крайней мере, учитывать наличие аденоидных камней и рассматривать аденоидэктомию при симптомах, часто приписываемых миндалинам. Мы ввели термин «аденолиты», чтобы описать это интересное открытие и представить его как потенциальный источник рецидивирующей инфекции.
Обнаружение кальцифицированных камней в скрытых складках хронически воспаленных гипертрофированных миндалин не является редким явлением. Однако камни обычно не обнаруживаются в других лимфоидных тканях, таких как аденоиды или язычные миндалины. Поиск литературы в PubMed не выявил публикаций, за исключением одного французского реферата по радиологии, в котором сообщается о рентгеноконтрастных камнях в глотке как о случайных находках в 6% КТ головы/шеи [1]. Тонзиллиты обычно являются результатом хронического воспаления и описываются как биопленки аэробных и анаэробных бактерий, которые со временем кальцифицируются, трудно поддаются лечению антибиотиками и служат очагом рецидивирующей инфекции [2]. Любые бактерии или грибы, вызывающие тонзиллит, могут инициировать процесс кальцификации, что связано с застоем слюны [3]. Они часто связаны с неприятным запахом изо рта, который, как полагают, связан с летучими молекулами серы [4.5]. Студли и др. [2] провели гистологическое исследование и обнаружили слой фибринозного дебриса и воспалительных клеток между тонзиллитом и эпителием крипт. Они также заметили, что миндалины состоят из плотно упакованных полимикробных бактерий, удерживаемых вместе внеклеточным матриксом. Цуэниши и др. [4] использовали ПЦР-анализ 16S-рибосомной ДНК тонзиллитов и определили, что агрегаты являются полимикробными, в частности, одним микробом, F. nucleatum , как известно, производит летучие соединения серы, которые могут вызывать неприятный запах.
Любые бактерии или грибы, вызывающие тонзиллит, могут инициировать процесс кальцификации, что связано с застоем слюны [3]. Они часто связаны с неприятным запахом изо рта, который, как полагают, связан с летучими молекулами серы [4.5]. Студли и др. [2] провели гистологическое исследование и обнаружили слой фибринозного дебриса и воспалительных клеток между тонзиллитом и эпителием крипт. Они также заметили, что миндалины состоят из плотно упакованных полимикробных бактерий, удерживаемых вместе внеклеточным матриксом. Цуэниши и др. [4] использовали ПЦР-анализ 16S-рибосомной ДНК тонзиллитов и определили, что агрегаты являются полимикробными, в частности, одним микробом, F. nucleatum , как известно, производит летучие соединения серы, которые могут вызывать неприятный запах.
Мы представляем интересный случай 30-летней здоровой женщины, главной жалобой которой были заложенность носа, утомляемость и рецидивирующие инфекции верхних дыхательных путей. В анамнезе у нее была длительная инфекция, вызванная вирусом Эпштейна-Барр (ВЭБ) более 10 лет назад, но в остальном ничем не примечательная история болезни и отсутствие предшествующей аденотонзиллэктомии. Физикальное обследование выявило 2+ небных миндалины, которые казались нормальными, в то время как волоконно-оптическая назофиарингоскопия показала значительную гипертрофию аденоидов. У пациента были частые инфекции верхних дыхательных путей и недомогание, а также хроническая заложенность носа, приписываемая гипертрофированным аденоидам. На неприятный запах изо рта не жаловалась. КТ пазух показала нормальные пазухи, увеличенные, но в остальном доброкачественные аденоиды и отсутствие рентгеноконтрастности в ее аденоидном ложе. Было принято решение продолжить аденоидэктомию, чтобы облегчить ее симптомы.
Физикальное обследование выявило 2+ небных миндалины, которые казались нормальными, в то время как волоконно-оптическая назофиарингоскопия показала значительную гипертрофию аденоидов. У пациента были частые инфекции верхних дыхательных путей и недомогание, а также хроническая заложенность носа, приписываемая гипертрофированным аденоидам. На неприятный запах изо рта не жаловалась. КТ пазух показала нормальные пазухи, увеличенные, но в остальном доброкачественные аденоиды и отсутствие рентгеноконтрастности в ее аденоидном ложе. Было принято решение продолжить аденоидэктомию, чтобы облегчить ее симптомы.
Больной доставлен в операционную для эндоскопической трансназальной аденоидэктомии. Во время операции мы обнаружили, что аденоидная ткань была скрытой, и когда мы отсасывали аденоидную массу, были доставлены маленькие камни ярко-зеленого цвета размером 1-2 мм (1-2 мм). Примерно 5-10 камней одинакового размера. Эти камни были отправлены в микробиологию и патологию. Небольшая биопсия аденоида также была отправлена на патологию, и аденоидэктомия была выполнена с использованием электрокоагуляции отсасывающего бови. Через несколько недель пациент был осмотрен для последующего наблюдения с улучшением носового дыхания. Длительное наблюдение по телефону показало, что ее носовое дыхание значительно улучшилось, у нее стало заметно меньше усталости и меньше инфекций верхних дыхательных путей.
Через несколько недель пациент был осмотрен для последующего наблюдения с улучшением носового дыхания. Длительное наблюдение по телефону показало, что ее носовое дыхание значительно улучшилось, у нее стало заметно меньше усталости и меньше инфекций верхних дыхательных путей.
Открыть в отдельном окне
(А) Предоперационный вид гипертрофированной аденоидной ткани через левую хоану, перегородку слева; (B) Вскрытие гипертрофированной аденоидной ткани показывает ярко-зеленый камень; (C) Несколько камней были удалены (масштабная линейка 4 мм).
Патология аденоидной ткани выявляет гипертрофию аденоид и отсутствие малигнизации. Патология конкрементов выявляет плотные бактериальные агрегаты (в том числе нитевидные формы), окруженные нейтрофилами (1), что соответствует тому, что наблюдается в миндалинах. Культуры выросли: 4+ прихотливых грамотрицательных палочек, не идентифицируемых обычными биохимическими методами, 4+ группы Streptococcus milleri (anginosus/constellatus/intermedius), грамотрицательные палочки, ферментирующие лактозу: выделены только из бульона, и 4+ предполагаемой смешанной анаэробной флоры, включая анаэробную грамотрицательную флору палочки отрицательные и анаэробные грамположительные палочки. Рост грамотрицательных палочек и обнаружение нитевидных структур при гистологическом исследовании наводит на мысль о гранулах серы Actinomyces, которые часто обнаруживаются в камнях миндалин [3].
Рост грамотрицательных палочек и обнаружение нитевидных структур при гистологическом исследовании наводит на мысль о гранулах серы Actinomyces, которые часто обнаруживаются в камнях миндалин [3].
Открыть в отдельном окне
(A) Микрофотографии окрашенного H и E среза всего камня демонстрируют преимущественно некротическую ткань с многочисленными плотными базофильными бактериальными агрегатами (B и C, стрелки), окруженными нитевидными (C, стрелка, 600x) структуры и/или лучистый аморфный эозинофильный материал (B, стрелка, 400x), напоминающий гранулемы. Обильные нейтрофилы окружают скопления бактерий. В камне не видно ни жизнеспособной аденоидной ткани, ни очевидных кальцинатов.
Здесь мы описали редкий случай аденоидных камней, удаленных из гипертрофированной аденоидной ткани у здорового в остальном пациента. Тонзиллиты формируются в хронически воспаленных миндалинах и состоят из полимикробных бактериальных агрегатов, окруженных фибринозными остатками и воспалительными клетками. Как и в предыдущих сообщениях о тонзиллитах, камни, которые мы собрали из аденоидов при патологическом исследовании, также содержали полимикробные бактериальные агрегаты, окруженные нейтрофилами. Гипертрофированные аденоиды нашего пациента были очень похожи на типичную гипертрофию аденоидов и были очень загадочными, создавая потенциальные пространства для бактериальных агрегатов и образования биопленки. Мы предполагаем, что механизм аналогичен образованию тонзиллитов в криптах миндалин с биопленочной и воспалительной клеточной инфильтрацией. Это поднимает вопрос о том, могут ли лимфоидные камни служить очагом инфекции или они являются просто результатом продолжающейся хронической инфекции. Например, в недавнем исследовании предполагается, что наличие аденоидной биопленки, а не размер аденоида, коррелирует с хроническим средним отитом [6].
Как и в предыдущих сообщениях о тонзиллитах, камни, которые мы собрали из аденоидов при патологическом исследовании, также содержали полимикробные бактериальные агрегаты, окруженные нейтрофилами. Гипертрофированные аденоиды нашего пациента были очень похожи на типичную гипертрофию аденоидов и были очень загадочными, создавая потенциальные пространства для бактериальных агрегатов и образования биопленки. Мы предполагаем, что механизм аналогичен образованию тонзиллитов в криптах миндалин с биопленочной и воспалительной клеточной инфильтрацией. Это поднимает вопрос о том, могут ли лимфоидные камни служить очагом инфекции или они являются просто результатом продолжающейся хронической инфекции. Например, в недавнем исследовании предполагается, что наличие аденоидной биопленки, а не размер аденоида, коррелирует с хроническим средним отитом [6].
Мы предполагаем, что если камни могут образовываться в аденоидах, они также могут быть источником неприятного запаха изо рта, если они содержат серообразующие бактерии, присутствующие в оральной флоре. К счастью, у нашего пациента не было жалоб на неприятный запах изо рта, и, соответственно, культуры не росли F. nucleatum . Тем не менее, оценка аденоидных камней, возможно, должна быть рассмотрена при жалобах на неприятный запах изо рта.
К счастью, у нашего пациента не было жалоб на неприятный запах изо рта, и, соответственно, культуры не росли F. nucleatum . Тем не менее, оценка аденоидных камней, возможно, должна быть рассмотрена при жалобах на неприятный запах изо рта.
Нас также заинтриговало отсутствие публикаций об аденоидных камнях. Это первый случай, когда авторы столкнулись с подобными выводами. Тем не менее, есть один реферат, в котором сообщается о случайной рентгенологической находке камней в носоглотке в 6% КТ головы и шеи [1]. Чувствительность обнаружения камней миндалин на КТ составляет 46,1% камней размером не менее 3 мм [7], поэтому можно ожидать, что более чем у 12% пациентов будут обнаружены камни где-то в носоглотке. Почему мы не встретили больше камней в аденоидах, непонятно. Возможно, мы не ищем их. В нашем случае у пациента не было рентгенологически видимых камней. Этому есть несколько объяснений. Одна из возможностей заключается в том, что собранные нами камни не содержат грубых кальцинатов. Другая возможность заключается в том, что собранные нами камни довольно малы, размером 1–2 мм, и могут быть слишком малы для обнаружения на КТ. Судя по отчетам, чувствительность ограничивается камнями размером не менее 2–3 мм.
Другая возможность заключается в том, что собранные нами камни довольно малы, размером 1–2 мм, и могут быть слишком малы для обнаружения на КТ. Судя по отчетам, чувствительность ограничивается камнями размером не менее 2–3 мм.
У пациента была длительная инфекция EBV. Хотя предполагалось, что ВЭБ вызывает аденотонзиллярную гипертрофию, например, при посттрансплантационных лимфопролиферативных заболеваниях и мононуклеозе, ограниченные исследования предполагают отсутствие связи между рецидивирующим тонзиллитом и наличием ВЭБ [8]. Мы можем заключить, что корреляция между ВЭБ и аденоидными инфекциями, вероятно, отсутствует.
Можно возразить, что для того, чтобы назвать аденоидный конкремент «аденолитом» (то есть камнем), необходимо, чтобы он содержал рентгеноконтрастные кальцификации. Хотя мы не выявили грубых кальцинатов в образцах, которые мы оценивали, мы не можем исключить наличие микрокальцинатов. Что еще более важно, наши результаты показывают, что микробиологический процесс этих аденоидных камней слишком поразительно похож на процесс образования камней миндалин. Таким образом, мы можем только ожидать, что сильно кальцифицированные аденолиты должны сформироваться, если будет достаточно времени.
Таким образом, мы можем только ожидать, что сильно кальцифицированные аденолиты должны сформироваться, если будет достаточно времени.
В заключение мы представляем редкий и интересный случай камней в аденоидных тканях. Хотя камни часто обнаруживаются в криптах небных миндалин, они редко обнаруживаются в других лимфоидных тканях глотки. Здесь мы сообщаем, что камни в аденоидах действительно могут возникать почти так же, как и в миндалинах, и мы ввели термин «аденолиты» для их описания. Наши данные свидетельствуют о том, что эти агрегаты бактериальной биопленки могут также образовываться в аденоидной ткани. Это повышает вероятность того, что аденолиты служат очагом хронической инфекции и источником неприятного запаха изо рта и требуют удаления аденоидов.
Первый автор получил грант (NIDCD Research Training in Otolaryngology, DC000018).
1. Ben Salem D, Guiu B, Duvillard C, Couaillier JF, Ricolfi F. Миндалины носоглотки: отчет о 31 случае. Дж Радиол. 2007; 88: 259–262. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
2. Stoodley P, Debeer D, Longwell M, Nistico L, Hall-Stoodley L, et al. Тонзиллит: не просто камень, а живая биопленка. Отоларингол Head Neck Surg. 2009; 141:316–321. [PubMed] [Академия Google]
3. Купер М.М., Стейнберг Дж.Дж., Ластра М., Антополь С. Тонзиллярные камни. Отчет о случае и обзор литературы. Челюстно-лицевая хирургия. 1983; 55: 239–243. [PubMed] [Google Scholar]
4. Tsuneishi M, Yamamoto T, Kokeguchi S, Tamaki N, Fukui K, et al. Состав бактериальной флоры миндалин. микробы заражают. 2006; 8: 2384–2389. [PubMed] [Google Scholar]
5. Krespi YP, Shrime MG, Kacker A. Взаимосвязь между неприятным запахом изо рта и бактериями, производящими летучие соединения серы. Отоларингол Head Neck Surg. 2006; 135: 671–676. [PubMed] [Академия Google]
6. Ода М., Кито С., Танака Т., Нисида И., Авано С. и др. Распространенность и визуализационные характеристики обнаруживаемых миндалин на 482 парах последовательных КТ и панорамных рентгенограмм. Здоровье полости рта BMC. 2013;13:54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Здоровье полости рта BMC. 2013;13:54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Saafan ME, Ibrahim WS, Tomoum MO. Роль аденоидной биопленки при хроническом среднем отите с выпотом у детей. Eur Arch Оториноларингол. 2013; 270:2417–2425. [PubMed] [Google Scholar]
8. Endo LH, Ferreira D, Montenegro MC, Pinto GA, Altemani A, et al. Обнаружение вируса Эпштейна-Барр в ткани миндалин у детей и связь с рецидивирующими тонзиллитами. Int J Pediatr Оториноларингол. 2001;58:9–15. [PubMed] [Академия Google]
Анатомические данные о микробных биопленках в тканях миндалин: возможный механизм для объяснения хронизации | Инфекционные болезни | JAMA Отоларингология – Хирургия головы и шеи
Абстрактный
Контекст
Бактерии в биопленках устойчивы к защите хозяина и антибиотикам. Присутствие бактериальных биопленок в ткани и криптах воспаленных миндалин может объяснить хронический и рецидивирующий характер некоторых форм тонзиллита.
Цель Чтобы определить, встречаются ли микробные биопленки в миндалинах с клиническими аномалиями.
Дизайн В этом исследовании мы оценили гистоморфологический вид 19 миндалин человека на наличие признаков образования биопленки с помощью световой и просвечивающей электронной микроскопии.
Субъекты Ткани человека были собраны во время хирургической тонзиллэктомии. Пятнадцать образцов были удалены из-за повторных инфекций в анамнезе, а 4 — из-за гипертрофии и обструкции.
Вмешательства В этом исследовании вмешательства не использовались.
Показатель основного результата Гистологические и ультраструктурные признаки бактериальных биопленок в криптах миндалин.
Результаты
Грамположительные и грамотрицательные бактерии были обнаружены в бесклеточных отложениях среди крипт 11 из 15 инфицированных миндалин.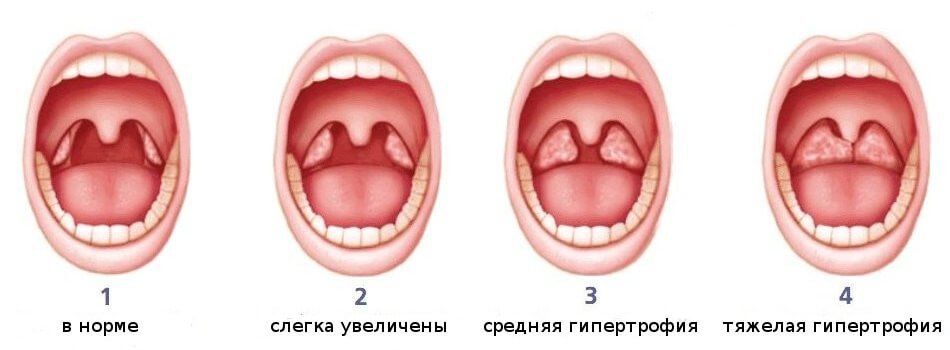 Участки скопления бактерий имели ультраструктурный вид типичного аморфного полисахаридного биопленочного матрикса. Небольшие скопления бактериальных колоний были обнаружены в 3 из 4 миндалин, удаленных по причине гипертрофии.
Участки скопления бактерий имели ультраструктурный вид типичного аморфного полисахаридного биопленочного матрикса. Небольшие скопления бактериальных колоний были обнаружены в 3 из 4 миндалин, удаленных по причине гипертрофии.
Выводы Имеются убедительные анатомические доказательства наличия бактериальных биопленок в миндалинах с хроническими заболеваниями. Поскольку сидячие бактерии в биопленках устойчивы к защите хозяина и антибиотикам, бактериальные биопленки в миндалинах могут объяснить хронический и рецидивирующий характер некоторых форм тонзиллита.
ТОНЗИЛЛИТ ЯВЛЯЕТСЯ одной из наиболее распространенных инфекционных болезней детского возраста. Несмотря на широкое применение антибиотиков для лечения этого заболевания, оно часто бывает упорным и рецидивирующим. Тонзиллэктомия часто выполняется, когда антибактериальная терапия не помогает при этом заболевании. За 19 лет в США было выполнено более 400 000 тонзиллэктомий.96, что делает его одной из самых распространенных хирургических процедур, выполняемых у детей. 1
1
Неспособность антибиотикотерапии уничтожить чувствительные микроорганизмы, вызывающие тонзиллит, остается загадкой. Например, несмотря на адекватное лечение тонзиллита, вызванного β-гемолитическими стрептококками, пенициллином, 20% случаев тонзиллита остаются после лечения бактериологически положительными. 2 Хотя растущая заболеваемость микроорганизмами, продуцирующими β-лактамазу, извлеченными из миндалин, может улучшить выживаемость бактерий, 3 инфекции миндалин могут рецидивировать, даже если они вызваны микроорганизмами, чувствительными к которым in vitro. 2 Эти наблюдения привели нас к гипотезе о том, что бактерии из биопленок в криптах хронически инфицированных миндалин могут сопротивляться эрадикации антибиотиками и защитными механизмами хозяина. В этом исследовании мы оценили миндалины, удаленные во время обычной тонзиллэктомии, на наличие анатомических признаков образования биопленки.
Методы
Образцы миндалин
Миндалины были получены во время плановой тонзиллэктомии и помещены в 10% нейтральный забуференный формалин. Образцы были получены от лиц с рецидивирующим тонзиллитом (n = 15), а также от лиц, перенесших тонзиллэктомию по поводу храпа или апноэ во сне (n = 4). Комитет по обзору исследований человека Вашингтонского университета в Сент-Луисе, Сент-Луис, Миссури, одобрил исследование, и испытуемые дали письменное согласие на пожертвование ткани для исследования.
Образцы были получены от лиц с рецидивирующим тонзиллитом (n = 15), а также от лиц, перенесших тонзиллэктомию по поводу храпа или апноэ во сне (n = 4). Комитет по обзору исследований человека Вашингтонского университета в Сент-Луисе, Сент-Луис, Миссури, одобрил исследование, и испытуемые дали письменное согласие на пожертвование ткани для исследования.
Световая микроскопия
Миндалины сначала помещали в 10% нейтральный забуференный формалин, затем разрезали на срезы толщиной от 2 до 4 мм, которые переносили в фиксатор, состоящий из 4% параформальдегида и 0,05% глутаральдегида в 0,1 М фосфатном буфере, на 24 часа. при 4°С. В качестве альтернативы образцы миндалин помещали непосредственно в неводный растворитель (Fluorinert FC-72; 3M, Сент-Пол, Миннесота) с 1% осмия для сохранения полисахаридной матрицы биопленок, которая легко растворяется в водных растворах. Затем все образцы обезвоживали в градуированных растворах ацетона и заливали эпоксидной смолой (Epon-Araldite; Electron Microscopy Sciences, Fort Washington, Pa). Было получено несколько полутонких срезов (0,5-1,0 мкм) на различной глубине образца и контрастно окрашены толуидиновым синим и основным фуксином. Альтернативную группу срезов окрашивали по Граму с использованием имеющегося в продаже набора для окрашивания (Protocol Gram Stain Set; Biochemical Sciences Inc, Swedesboro, NJ). Срезы исследовали с помощью вертикального светового микроскопа (Olympus BH-2; Olympus America Inc, Мелвилл, штат Нью-Йорк) и изображения получали с помощью цифровой фотосистемы (Sony DKC-5000; Sony Corporation of America, Нью-Йорк, штат Нью-Йорк).
Было получено несколько полутонких срезов (0,5-1,0 мкм) на различной глубине образца и контрастно окрашены толуидиновым синим и основным фуксином. Альтернативную группу срезов окрашивали по Граму с использованием имеющегося в продаже набора для окрашивания (Protocol Gram Stain Set; Biochemical Sciences Inc, Swedesboro, NJ). Срезы исследовали с помощью вертикального светового микроскопа (Olympus BH-2; Olympus America Inc, Мелвилл, штат Нью-Йорк) и изображения получали с помощью цифровой фотосистемы (Sony DKC-5000; Sony Corporation of America, Нью-Йорк, штат Нью-Йорк).
Трансмиссионная электронная микроскопия
Образцы тканей фиксировали и обезвоживали, как описано выше, а затем заливали эпоксидной смолой. Блоки делали тонкими срезами для просвечивающей электронной микроскопии на ультрамикротоме (Reichert Ultracut; Leica Inc, Deerfield, IL). Затем были взяты тонкие срезы для просвечивающей электронной микроскопии из областей, содержащих подозреваемые биопленки, и контрастно окрашены уранилацетатом-цитратом свинца. Их исследовали и сфотографировали с помощью просвечивающего электронного микроскопа (Hitachi H-7500; Hitachi High Technologies America, Плезантон, Калифорния) с возможностью цифровой обработки изображений. Контрастность и яркость изображений были оптимизированы для публикации с помощью программного обеспечения для редактирования изображений (Adobe Photoshop 7.0; Adobe Systems Inc, Сан-Хосе, Калифорния).
Их исследовали и сфотографировали с помощью просвечивающего электронного микроскопа (Hitachi H-7500; Hitachi High Technologies America, Плезантон, Калифорния) с возможностью цифровой обработки изображений. Контрастность и яркость изображений были оптимизированы для публикации с помощью программного обеспечения для редактирования изображений (Adobe Photoshop 7.0; Adobe Systems Inc, Сан-Хосе, Калифорния).
Полученные результаты
Мы считали биопленками плотные скопления бактерий, встроенных в аморфный матрикс. Из миндалин с инфекциями в анамнезе 11 из 15 показали наличие биопленок. Из увеличенных миндалин, которые были удалены по поводу обструкции и не имели активной текущей инфекции, 3 из 4 имели признаки биопленок.
Биопленки чаще всего встречались в криптах миндалин и представляли собой большие плотные скопления смешанных бактерий. Воспалительные клетки обычно обнаруживались на периферии этих бактериальных колоний, но не внутри массы (рис.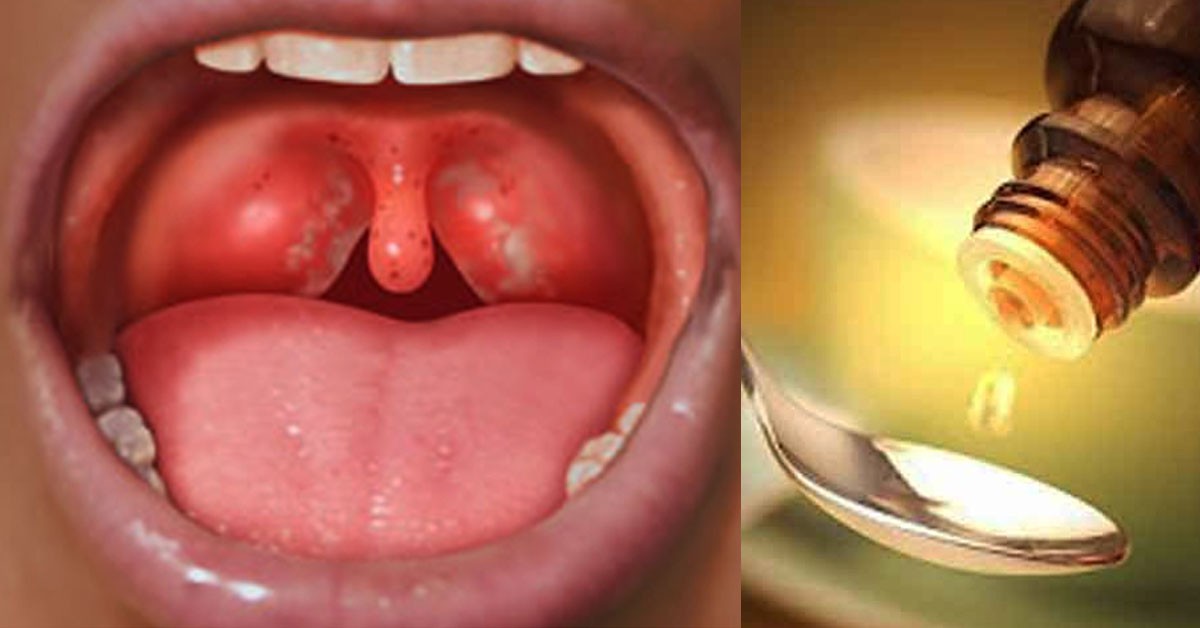 1). Окрашивание по Граму выявило грамположительные и грамотрицательные микроорганизмы, хотя преобладали грамположительные кокки (рис. 1, вставка). Некоторые биопленки имели диаметр несколько миллиметров и были видны невооруженным глазом. Некоторые колонии оказались более сложными, с складками. При электронной микроскопии бактериальные колонии были видны как плотно упакованные бактерии с различным морфологическим внешним видом, включая палочковидные и сферические профили, а также различные модели окрашивания капсул. При ближайшем рассмотрении бактерии были погружены в однородное аморфное фоновое вещество, которое хорошо сохранилось в тканях, обработанных растворителем (рис. 2).
1). Окрашивание по Граму выявило грамположительные и грамотрицательные микроорганизмы, хотя преобладали грамположительные кокки (рис. 1, вставка). Некоторые биопленки имели диаметр несколько миллиметров и были видны невооруженным глазом. Некоторые колонии оказались более сложными, с складками. При электронной микроскопии бактериальные колонии были видны как плотно упакованные бактерии с различным морфологическим внешним видом, включая палочковидные и сферические профили, а также различные модели окрашивания капсул. При ближайшем рассмотрении бактерии были погружены в однородное аморфное фоновое вещество, которое хорошо сохранилось в тканях, обработанных растворителем (рис. 2).
Комментарий
Бактерии, вызывающие болезни человека, обычно рассматриваются как свободно подвижные организмы. Однако большинство бактерий, как правило, виды Escherichia coli , Haemophilus influenzae и Pseudomonas , Staphylococcus и Klebsiella , обладают способностью прилипать к поверхностям на границе раздела твердой и жидкой фаз. 4 ,5 Прикрепившись, бактерии образуют сложную полисахаридную матрицу, в которую они внедряются. Затем колонии бактерий увеличиваются и в результате процесса, называемого определение кворума , образуют большие колонии сидячих бактерий. 6 Сидячие бактерии в биопленках принимают измененный фенотип, при котором они не делятся. Эти биопленки широко распространены в природе и встречаются практически во всех естественных водоемах мира. За последние 10 лет биопленки были признаны важной причиной персистирующих инфекций, включая зубной налет, пневмонит вследствие муковисцидоза, хронический цистит, остеомиелит, средний отит и холестеатому. 6 -11 Наиболее важной характеристикой бактериальных биопленок является то, что бактерии внутри этих колоний становятся очень устойчивыми к антибиотикам и защите хозяина. 12 Например, штамм Klebsiella pneumoniae имел минимальную ингибирующую концентрацию ампициллина 2 мкг/мл в водной суспензии, но тот же штамм, выращенный в виде биопленки, выдерживал концентрации ампициллина 5000 мкг/мл.
4 ,5 Прикрепившись, бактерии образуют сложную полисахаридную матрицу, в которую они внедряются. Затем колонии бактерий увеличиваются и в результате процесса, называемого определение кворума , образуют большие колонии сидячих бактерий. 6 Сидячие бактерии в биопленках принимают измененный фенотип, при котором они не делятся. Эти биопленки широко распространены в природе и встречаются практически во всех естественных водоемах мира. За последние 10 лет биопленки были признаны важной причиной персистирующих инфекций, включая зубной налет, пневмонит вследствие муковисцидоза, хронический цистит, остеомиелит, средний отит и холестеатому. 6 -11 Наиболее важной характеристикой бактериальных биопленок является то, что бактерии внутри этих колоний становятся очень устойчивыми к антибиотикам и защите хозяина. 12 Например, штамм Klebsiella pneumoniae имел минимальную ингибирующую концентрацию ампициллина 2 мкг/мл в водной суспензии, но тот же штамм, выращенный в виде биопленки, выдерживал концентрации ампициллина 5000 мкг/мл.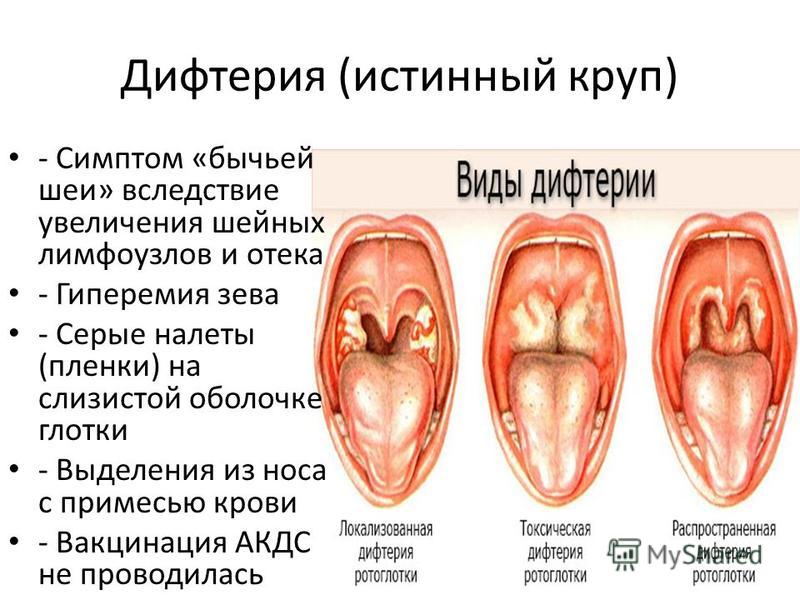 4
4
Вполне вероятно, что прикрепление бактерий к эпителию миндалин является первым шагом в формировании биопленки. 13 Адгезивные бактерии, особенно в криптах миндалин, могут образовывать большие смешанные колонии бактерий. Бактерии в этих биопленках, хотя и защищены от защиты хозяина и антибиотиков, продолжают метаболизироваться и образовывать эндотоксин. Выработка локального эндотоксина в криптах миндалин может привести к хроническому воспалению. Кроме того, при благоприятных местных условиях окружающей среды бактерии внутри биопленки могут стать подвижными, вызывая рецидив острой инфекции. 14
В этом исследовании мы исследовали миндалины, которые были удалены из-за рецидивирующей инфекции, а также увеличения и обструкции. Считается, что в гипертрофированных миндалинах больше патогенных бактерий, чем в здоровых миндалинах. 15 Действительно, когда аспираты нормальных миндалин 16 сравнивают с таковыми гипертрофированных миндалин, гипертрофированные миндалины содержат больше бактериальных изолятов. Исследование, в котором сравнивалась тонзиллярная микробная флора в гипертрофированных миндалинах и миндалинах с рецидивирующей инфекцией, показало, что две группы существенно не различались по количеству изолятов на пациента, будь то аэробные (3,8 против 4,3) или анаэробные (5,2 против 4,7) бактерии. 17 Таким образом, увеличенные миндалины в настоящем исследовании могут не соответствовать нормальному контролю.
Исследование, в котором сравнивалась тонзиллярная микробная флора в гипертрофированных миндалинах и миндалинах с рецидивирующей инфекцией, показало, что две группы существенно не различались по количеству изолятов на пациента, будь то аэробные (3,8 против 4,3) или анаэробные (5,2 против 4,7) бактерии. 17 Таким образом, увеличенные миндалины в настоящем исследовании могут не соответствовать нормальному контролю.
Обнаружение биопленок в миндалинах без истории инфекции повышает вероятность того, что образование биопленок в криптах миндалин является частью нормального процесса иммунного надзора и что смешанные бактериальные биопленки являются частью нормальной флоры миндалин человека. Наиболее подходящими контрольными тканями были бы ткани миндалин от контрольных субъектов того же возраста, у которых никогда не было инфекций верхних дыхательных путей, но такие ткани не были доступны для этого исследования.
Анатомические данные смешанных бактериальных биопленок в криптах миндалин, которые были удалены из-за рецидивирующей инфекции или гипертрофии, повышают вероятность того, что бактерии, секвестрированные защитными средствами хозяина и антибиотиками, могут объяснить неподатливую природу некоторых случаев рецидивирующего тонзиллита.
Наверх
Информация о статье
Автор, ответственный за переписку: Richard A. Chole, MD, PhD, Отделение отоларингологии, Campus Box 8115, Washington University in St Louis, 660 S Euclid Ave, St Louis, MO 63110 (электронная почта: [email protected] ).
Принято к публикации 16 октября 2002 г.
Это исследование было поддержано грантами DC00263-16 и P30 DC04665 Национального института глухоты и других коммуникативных расстройств, Национальных институтов здравоохранения, Бетесда, Мэриленд
Мы благодарим Рут Хьюз. , Jae Jung, Lisette Ramos и Eric Wang из отделения отоларингологии Вашингтонского университета в Сент-Луисе за помощь в подготовке некоторых материалов, использованных в этом исследовании.
Рекомендации
1.
Национальный центр медицинской статистики Амбулаторные и стационарные процедуры в США.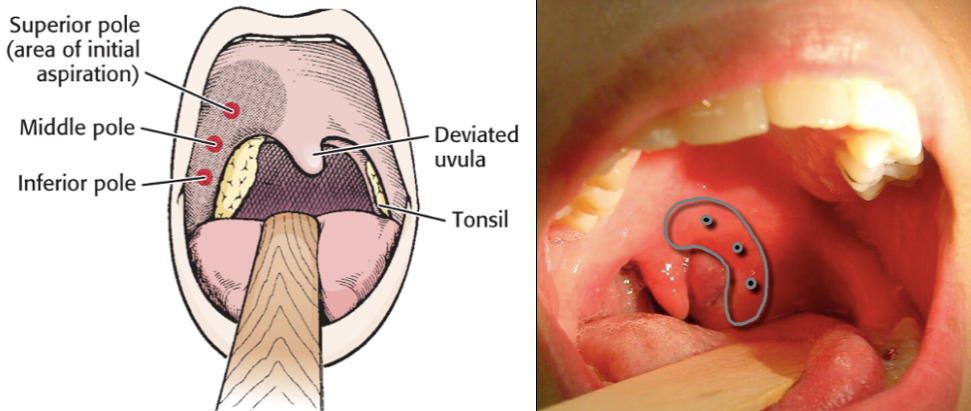 Хаяттсвилл, штат Мэриленд: Национальный центр статистики здравоохранения; 1996.
Хаяттсвилл, штат Мэриленд: Национальный центр статистики здравоохранения; 1996.
2.
Брук I Неспособность пенициллина искоренить тонзиллит бета-гемолитического стрептококка группы А: причины и лечение. J Отоларингол. 2001;30:324-329.Google Scholar
3.
Брук IYocum ПФут Пенсильвания Jr Изменения в основной бактериологии миндалин при рецидивирующем тонзиллите: 1977-1993. Clin Infect Dis. 1995;21:171-176. Google Scholar
4.
Андерль
Дж. Н. Франклин
М.Дж.Стюарт
PS Роль ограничения проникновения антибиотиков в устойчивость биопленки Klebsiella pneumoniae к ампициллину и ципрофлоксацину. Антимикробные агенты Chemother. 2000;44:1818-1824. Google Scholar
Google Scholar
5.
Майсорекар IUMulvey МАХультгрен С.Дж. Гордон JL Молекулярная регуляция обновления уротелия и защиты хозяина при заражении уропатогенным Кишечная палочка . J Biol Chem. 2002;277:7412-7419. Google Scholar
6.
Костертон Дж.В.Стюарт П.С.Гринберг EP Бактериальные биопленки: частая причина персистирующих инфекций. Наука. 1999;284:1318-1322.Google Scholar
7.
Костертон JW Патогенез кистозного фиброза и роль биопленок в персистирующей инфекции. Trends Microbiol. 2001;9:50-52.Google Scholar
8.
Холе
РАФаддис
BT Доказательства наличия микробных биопленок в холестеатомах. Arch Otolaryngol Head Neck Surg. 2002;128:1129-1133.Google Scholar
Arch Otolaryngol Head Neck Surg. 2002;128:1129-1133.Google Scholar
9.
Сообщение JC Прямые доказательства наличия бактериальных биопленок в среднем отите. Ларингоскоп. 2001;111:2083-2094. Google Scholar
10.
Райнер М.Г.Чжан YГорри МакЧен YPost JCEhrlich GD Доказательства бактериальной метаболической активности при культурально-отрицательном среднем отите с выпотом. ЯМА. 1998;279:296-299.Google Scholar
11.
Эрлих GDVeeh РВанг Икс и др. Формирование слизистой биопленки на слизистой оболочке среднего уха в модели среднего отита у шиншилл. ЯМА. 2002;287:1710-1715.Google Scholar
12.
Стюарт ПСКстертон JW Устойчивость бактерий к антибиотикам в биопленках. Ланцет. 2001;358:135-138.Google Scholar
13.
Стенфорс Л.Э.Райсанен S Прикрепление бактерий к эпителию миндалин при остром тонзиллите. Ж Ларынгол Отол. 1991;105:29-32.Google Scholar
14.
Stoodley П. Уилсон Шолл-Студли ЛБойл JDLappin-Скотт HMCosterton JW Рост и отделение кластеров клеток от зрелых смешанных биопленок. Appl Environ Microbiol. 2001;67:5608-5613.Google Scholar
15.
Ричардсон MA Боль в горле, тонзиллит и аденоидит. Med Clin North Am. 1999;83:75-83, viii.Google Scholar
16.
