Флюс – статьи о здоровье
Флюс характеризуется появлением шишки на десне в области корня зуба, и сопровождается сильной болью.
Если говорить простым языком, то флюс – это гнойное воспаление корня зуба.
Сам процесс образования флюса начинается из спровоцированного инфекцией воспаления в области корня зуба, где и образовывается первоначальный гной, который постепенно прокладывает себе путь через костную, а далее мягкую ткани, вырываясь наружу.
Причины
Развитию флюса у людей способствуют следующие факторы:
— воспалительные процессы: пульпит, периодонтит;
— последствия ранений, травм мягких тканей полости рта;
— переломы челюсти;
— инфекции, попадающие через кровеносную систему;
— инфекционные заболевания, передающиеся через лимфатическую систему.
Самое главное в лечении — найти причину появления патологии, чтобы определить оптимальные пути лечения, оперативного вмешательства, комплексного проведения сопутствующих мероприятий.
Симптомы
Cамым явным симптомом флюса, конечно же, является волдырь на десне, либо опухание щеки, но кроме этого, есть и другие симптомы, которые указывают на то, что это заболевание постепенно развивается. Самый первый симптом – это острая зубная боль, которая может захватывать не только непосредственно зуб, а ещё и щеку, шею, голову в целом. Может повышаться температура тела, могут опухать губы и крылья носа.
Зуб должен не просто сильно болеть, острая боль должна чувствоваться, когда на зуб что-то давит, при резком смыкании челюстей или при жевании пищи. Флюс может развиваться не только со стороны десны, которая находится ближе к лицу, он может развиваться и со стороны слизистой рта. При этом десна просто краснеет и имеет небольшой отёк.
Самый первый признак, что начался гнойный флюс зуба – это повышение температуры больного, отсутствие аппетита, общее ухудшение состояния человека. Обязательно на десне или на щеке должна быть опухоль.
Диагностика
Диагноз устанавливают после осмотра больного, его различных клинических данных, в том числе, рентгенологических. Выяснить правильный диагноз помогают лабораторные исследования, определяющие стадию воспалительного процесса.
Лечение
Лечение зубного флюса может предполагать применение одного из двух методов. Первый — медикаментозная терапия или консервативное лечение, проводимое на начальных стадиях развития заболевания. Второй — оперативное лечение, которое является необходимым в тех случаях, когда на начальных этапах развития заболевания не было проведено качественного лечения и на поверхности десны возник гнойник.
Лечение медикаментами может состоять из нескольких этапов:
— Снятие отечности, для чего используются антибиотики, а также различные антибактериальные препараты. Задачей врача является правильный их подбор в зависимость от характера болезни и состояния здоровья пациента.
— Лечение заболевания, которое является причиной развития флюса.
— Если болезнь характеризуется периодическими обострениями, то должны назначаться укрепляющие препараты, такие как глюканат кальция и иммуномодуляторы, а также витамины.
Если медикаментозная терапия не дала желаемого результата, то проводится хирургическое вмешательства. В первую очередь, пациенту вводится обезболивающее. Затем абсцесс вскрывается, для чего делается надрез на десне в районе флюса. Гной удаляется. Десна дренируется, чем обеспечивается постоянный отток гнойных масс.
В том случае, если зуб нельзя восстановить, его необходимо удалить. После этого осуществляется полная очистка раны от гноя и установка дренажа. Далее назначается курс антибиотиков.
Если речь идет о лечении сложных форм периостита, то в конечном счете может быть назначено также лечение лазером, ионофорезом и ультразвуком.
Хлорохин ингибирует поток аутофагии, уменьшая слияние аутофагосомы и лизосомы
[1] Mizushima N, Levine B, Cuervo AM, et al. Аутофагия борется с болезнями посредством клеточного самопереваривания. Природа. 2008.
февраль
28;451(7182):1069–1075. PubMed PMID: 18305538. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Аутофагия борется с болезнями посредством клеточного самопереваривания. Природа. 2008.
февраль
28;451(7182):1069–1075. PubMed PMID: 18305538. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[2] Shintani T, Klionsky DJ.. Аутофагия в норме и болезни: палка о двух концах. Наука. 2004. ноябрь 5;306(5698):990–995. PubMed PMID: 15528435. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[3] Левин Б, Клионский Д. Развитие путем самопереваривания: молекулярные механизмы и биологические функции аутофагии. Ячейка Дев. 2004. Апрель; 6 (4): 463–477. PubMed PMID: 15068787. [PubMed] [Google Scholar]
[4] Levine B, Mizushima N, Virgin HW. Аутофагия в иммунитете и воспалении. Природа. 2011. январь 20;469(7330):323–335. PubMed PMID: 21248839. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[5] Kawamata T, Kamada Y, Kabeya Y, et al.
Организация преаутофагосомной структуры, ответственной за образование аутофагосом. Мол Биол Селл. 2008.
19 мая(5): 2039–2050 гг. PubMed PMID: 18287526.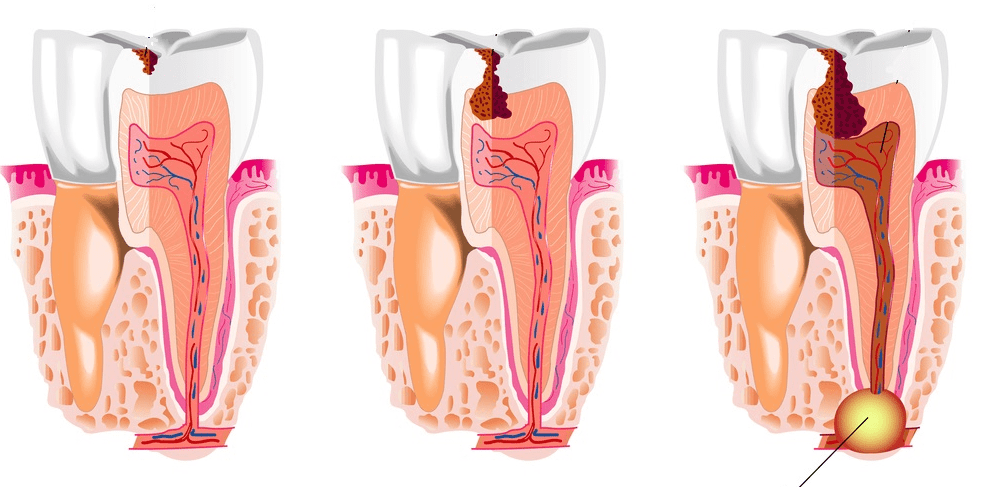 [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
[6] He C, Klionsky DJ. Механизмы регуляции и сигнальные пути аутофагии. Анну Рев Жене. 2009; 43:67–93. PubMed PMID: 19653858. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[7] Yang Z, Klionsky DJ. Аутофагия млекопитающих: основной молекулярный механизм и регуляция передачи сигналов. Curr Opin Cell Biol. 2010. 22 апреля (2): 124–131. PubMed PMID: 20034776. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[8] Мари М., Туз С.А., Реджори Ф. Загадочное происхождение аутофагосомной мембраны. F1000 Биол Респ. 2011;3:25 PubMed PMID: 22162728. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[9] Reggiori F, Ungermann C. Созревание и слияние аутофагосом. Дж Мол Биол. 2017. февраль 17;429(4):486–496. PubMed PMID: 28077293. [PubMed] [Google Scholar]
[10] Накамура С., Йошимори Т.
Новое понимание слияния аутофагосом-лизосом. Дж. Клеточные науки. 2017.
апреля
1;130(7):1209–1216. PubMed PMID: 28302910. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
[11] Klionsky DJ, Abdelmohsen K, Abe A, et al. Руководство по использованию и интерпретации анализов для мониторинга аутофагии (3-е издание). Аутофагия. 2016;12(1):1–222. PubMed PMID: 26799652. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[12] O’Neill PM, Bray PG, Hawley SR, et al. 4-Аминохинолины – прошлое, настоящее и будущее: химическая перспектива. Фармакол Тер. 1998. Январь; 77 (1): 29–58. PubMed PMID: 9500158. [PubMed] [Google Scholar]
[13] Аль-Бари М.А. Аналоги хлорохина в открытии лекарств: новые направления использования, механизмы действия и токсические проявления от малярии до разнообразных заболеваний. J Антимикробная химиотерапия. 2015;70(6):1608–1621. PubMed PMID: 25693996. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[14] Poole B, Ohkuma S. Влияние слабых оснований на внутрилизосомальный рН перитонеальных макрофагов мышей. Джей Селл Биол. 1981. Сентябрь; 90 (3): 665–669. PubMed PMID: 6169733. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[15] Seglen PO, Grinde B, Solheim AE.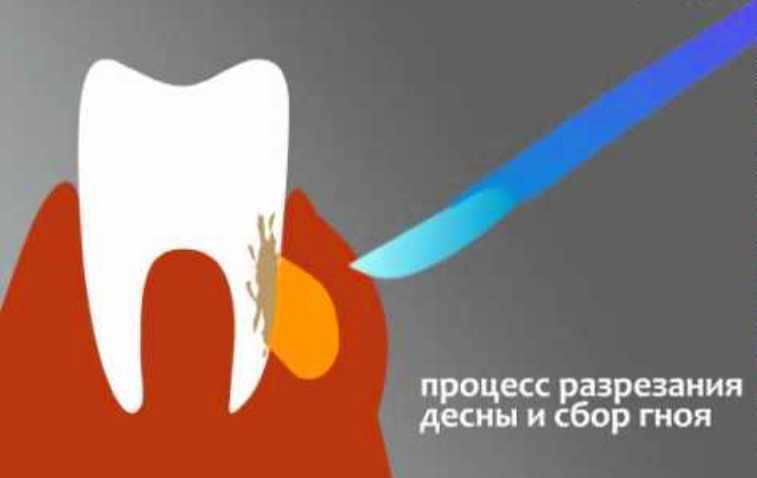 Ингибирование лизосомального пути деградации белка в изолированных гепатоцитах крысы аммиаком, метиламином, хлорохином и лейпептином. Евр Дж Биохим. 1979.
апреля
2;95(2):215–225. PubMed PMID: 456353. [PubMed] [Google Scholar]
Ингибирование лизосомального пути деградации белка в изолированных гепатоцитах крысы аммиаком, метиламином, хлорохином и лейпептином. Евр Дж Биохим. 1979.
апреля
2;95(2):215–225. PubMed PMID: 456353. [PubMed] [Google Scholar]
[16] Mizushima N, Yoshimori T, Levine B. Методы исследования аутофагии млекопитающих. Клетка. 2010. февраль 5;140(3):313–326. PubMed PMID: 20144757. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[17] Galluzzi L, Bravo-San Pedro JM, Levine B, et al. Фармакологическая модуляция аутофагии: терапевтический потенциал и сохраняющиеся препятствия. Nat Rev Drug Discov. 2017. Июль; 16 (7): 487–511. PubMed PMID: 28529316. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[18] Ronan B, Flamand O, Vescovi L, et al. Высокомощный и селективный ингибитор Vps34 изменяет перенос везикул и аутофагию. Nat Chem Biol. 2014. 10 (12) декабря: 1013–1019. PubMed PMID: 25326666. [PubMed] [Google Scholar]
[19] Bago R, Malik N, Munson MJ, et al.
Характеристика VPS34-IN1, селективного ингибитора Vps34, показывает, что фосфатидилинозитол-3-фосфат-связывающая протеинкиназа SGK3 является нижестоящей мишенью фосфоинозитид-3-киназы класса III.
[20] Egan DF, Chun MG, Vamos M, et al. Ингибирование малых молекул киназы аутофагии ULK1 и идентификация субстратов ULK1. Мол Ячейка. 2015. Июль 16;59(2):285–297. PubMed PMID: 26118643. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[21] Petherick KJ, Conway OJ, Mpamhanga C, et al. Фармакологическое ингибирование киназы ULK1 блокирует мишень рапамициновой (mTOR)-зависимой аутофагии у млекопитающих. Дж. Биол. Хим. 2015. Может 1;290(18):11376–11383. PubMed PMID: 25833948. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[22] Manic G, Obrist F, Kroemer G, et al. Хлорохин и гидроксихлорохин для лечения рака. Мол Селл Онкол. 2014;1(1):e29911 PubMed PMID: 27308318. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[23] Maycotte P, Aryal S, Cummings CT, et al.
Хлорохин повышает чувствительность клеток рака молочной железы к химиотерапии независимо от аутофагии. Аутофагия. 2012.
февраль
1;8(2):200–212. PubMed PMID: 22252008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Аутофагия. 2012.
февраль
1;8(2):200–212. PubMed PMID: 22252008. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[24] Cufi S, Vazquez-Martin A, Oliveras-Ferraros C, et al. Противомалярийный хлорохин преодолевает первичную резистентность и восстанавливает чувствительность к трастузумабу при HER2-положительном раке молочной железы. Научный представитель 2013; 3: 2469 PubMed PMID: 23965851. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[25] Eng CH, Wang Z, Tkach D, et al. Макроаутофагия необязательна для роста мутантных опухолей KRAS и эффективности хлорохина. Proc Natl Acad Sci U S A. 2016. январь 5;113(1):182–187. PubMed PMID: 26677873. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[26] Льюис В., Грин С.А., Марш М. и др. Гликопротеины лизосомальной мембраны. Джей Селл Биол. 1985. Июнь; 100 (6): 1839–1847. PubMed PMID: 3922993. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[27] Chen JW, Murphy TL, Willingham MC, et al.
Идентификация двух лизосомальных мембранных гликопротеинов.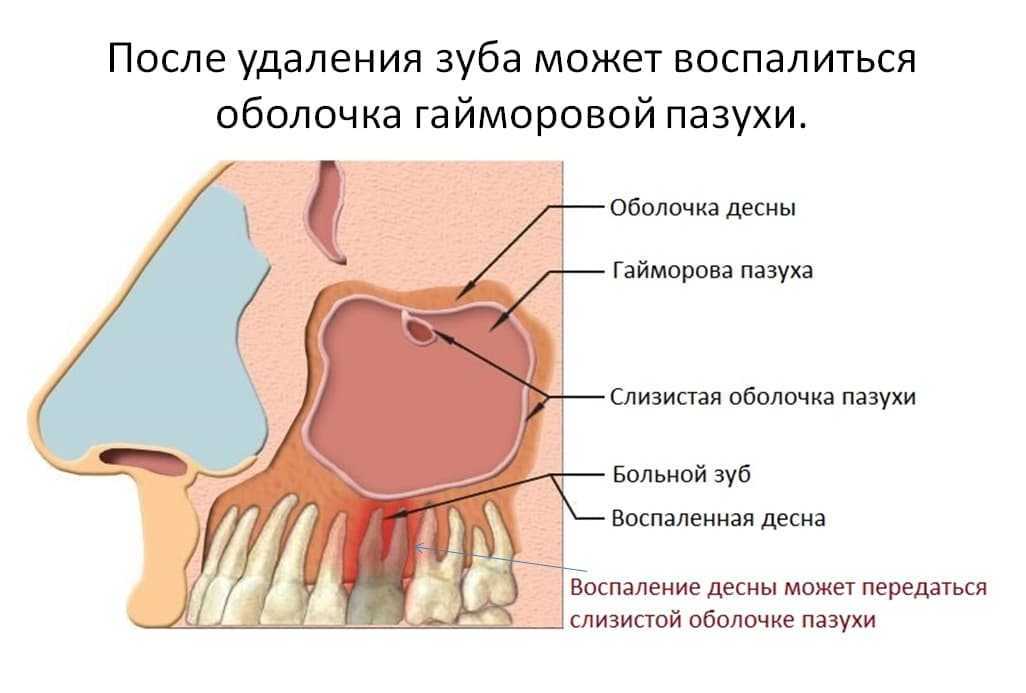 Джей Селл Биол. 1985.
Июль; 101 (1): 85–95. PubMed PMID: 2409098. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Джей Селл Биол. 1985.
Июль; 101 (1): 85–95. PubMed PMID: 2409098. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[28] Bowman EJ, Siebers A, Altendorf K. Бафиломицины: класс ингибиторов мембранных АТФаз микроорганизмов, клеток животных и клеток растений. Proc Natl Acad Sci U S A. 1988. Ноябрь; 85 (21): 7972–7976. PubMed PMID: 2973058. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[29] Jacquin E, Leclerc-Mercier S, Judon C, et al. Фармакологические модуляторы аутофагии активируют параллельный неканонический путь, управляющий нетрадиционным липидированием LC3. Аутофагия. 2017. Может 4;13(5):854–867. PubMed PMID: 28296541. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[30] Lu S, Sung T, Lin N, et al. Лизосомальная адаптация: как клетки реагируют на лизосомотропные соединения. PloS Один. 2017;12(3):e0173771 PubMed PMID: 28301521. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[31] Эскелинен Э.Л.
Быть или не быть? Примеры неправильной идентификации аутофагических компартментов при обычной просвечивающей электронной микроскопии клеток млекопитающих. Аутофагия. 2008.
Февраль; 4 (2): 257–260. PubMed PMID: 17986849. [PubMed] [Google Scholar]
Аутофагия. 2008.
Февраль; 4 (2): 257–260. PubMed PMID: 17986849. [PubMed] [Google Scholar]
[32] Эскелинен Э.Л., Ковач А.Л. Двойные мембраны против липидных бислоев и их значение для правильной идентификации макроаутофагических структур. Аутофагия. 2011. Сентябрь; 7 (9): 931–932. PubMed PMID: 21642767. [PubMed] [Google Scholar]
[33] Браун В.Дж., Константинеску Э., Фаркуар М.Г. Перераспределение маннозо-6-фосфатных рецепторов, индуцированное туникамицином и хлорохином. Джей Селл Биол. 1984. июль; 99 (1 часть 1): 320–326. PubMed PMID: 6330128. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[34] Mu FT, Callaghan JM, Steele-Mortimer O, et al. EEA1, ранний белок, ассоциированный с эндосомами. EEA1 представляет собой консервативный альфа-спиральный белок периферической мембраны, окруженный цистеиновыми «пальцами» и содержащий мотив IQ, связывающий кальмодулин. Дж. Биол. Хим. 1995. Июнь 2;270(22):13503–13511. PubMed PMID: 7768953. [PubMed] [Google Scholar]
[35] Luzio JP, Brake B, Banting G, et al. Идентификация, секвенирование и экспрессия интегрального мембранного белка транс-сети Гольджи (TGN38). Биохим Дж. 1990.
Август
15;270(1):97–102. PubMed PMID: 2204342. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Идентификация, секвенирование и экспрессия интегрального мембранного белка транс-сети Гольджи (TGN38). Биохим Дж. 1990.
Август
15;270(1):97–102. PubMed PMID: 2204342. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[36] Reaves B, Banting G. Нарушение морфологии сети транс-Гольджи после обработки брефельдином А: перераспределение TGN-специфического интегрального мембранного белка, TGN38. Джей Селл Биол. 1992. Январь; 116 (1): 85–94. PubMed PMID: 1730751. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[37] Nakamura N, Rabouille C, Watson R, et al. Характеристика цис-матриксного белка Гольджи, GM130. Джей Селл Биол. 1995. Декабрь; 131 (6 Pt 2): 1715–1726. PubMed PMID: 8557739. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[38] Serafini T, Stenbeck G, Brecht A, et al.
Субъединица оболочки везикул, не покрытых клатрином, происходящих из Гольджи, с гомологией с белком оболочки везикул, покрытым клатрином, бета-адаптином. Природа. 1991.
январь
17;349(6306):215–220. PubMed PMID: 1898984. [PubMed] [Google Scholar]
PubMed PMID: 1898984. [PubMed] [Google Scholar]
[39] Dahms NM, Lobel P, Breitmeyer J, et al. Маннозо-6-фосфатный рецептор 46 кД: клонирование, экспрессия и гомология с маннозо-6-фосфатным рецептором 215 кД. Клетка. 1987. Июль 17;50(2):181–192. PubMed PMID: 2954652. [PubMed] [Google Scholar]
[40] Klier HJ, von Figura K, Pohlmann R. Выделение и анализ человеческого гена маннозо-6-фосфатного рецептора массой 46 кДа. Евр Дж Биохим. 1991. апреля 10;197(1):23–28. PubMed PMID: 1849818. [PubMed] [Google Scholar]
[41] McAfee Q, Zhang Z, Samanta A, et al. Ингибитор аутофагии Lys05 обладает противоопухолевой активностью и воспроизводит фенотип генетического дефицита аутофагии. Proc Natl Acad Sci U S A. 2012. Может 22;109(21):8253–8258. PubMed PMID: 22566612. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[42] Rabinowitz S, Horstmann H, Gordon S, et al.
Иммуноцитохимическая характеристика эндоцитарного и фаголизосомного компартментов перитонеальных макрофагов. Джей Селл Биол. 1992.
Январь; 116 (1): 95–112. PubMed PMID: 1730752. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Джей Селл Биол. 1992.
Январь; 116 (1): 95–112. PubMed PMID: 1730752. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[43] Sorkin A, Helin K, Waters CM, et al. Множественные сайты аутофосфорилирования рецептора эпидермального фактора роста необходимы для активности и интернализации рецепторной киназы. Различное значение тирозина 992 в нативных и укороченных рецепторах. Дж. Биол. Хим. 1992. апреля 25;267(12):8672–8678. PubMed PMID: 1314835. [PubMed] [Google Scholar]
[44] Kabeya Y, Mizushima N, Ueno T, et al. LC3, гомолог дрожжей Apg8p млекопитающих, локализуется в мембранах аутофагосом после процессинга. ЭМБО Дж. 2000. ноябрь 1;19(21): 5720–5728. PubMed PMID: 11060023. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[45] Luhr M, Szalai P, Saetre F, et al. Простой анализ секвестрации груза для количественного измерения неселективной аутофагии в культивируемых клетках. Методы Энзимол. 2017; 587: 351–364. PubMed PMID: 28253965. . [PubMed] [Google Scholar]
[46] Kopitz J, Kisen GO, Gordon PB, et al.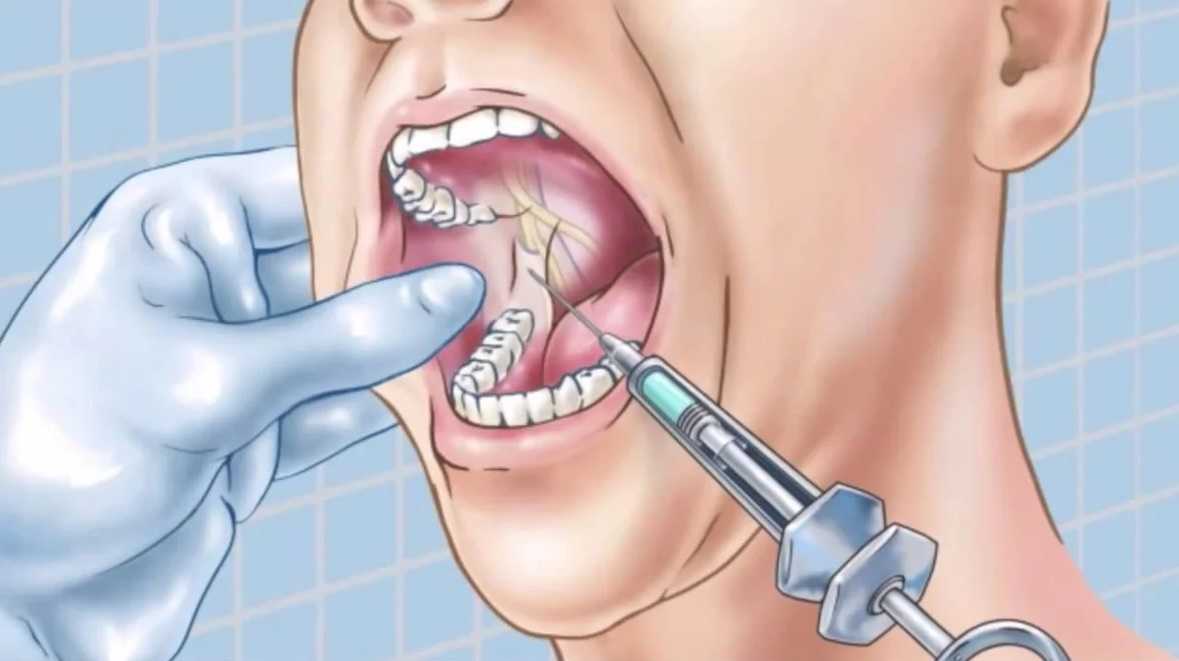 Неселективная аутофагия цитозольных ферментов изолированными гепатоцитами крысы. Джей Селл Биол. 1990.
Сентябрь;111(3):941–953. PubMed PMID: 2391370. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Неселективная аутофагия цитозольных ферментов изолированными гепатоцитами крысы. Джей Селл Биол. 1990.
Сентябрь;111(3):941–953. PubMed PMID: 2391370. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[47] Engedal N, Torgersen ML, Guldvik IJ, et al. Модуляция гомеостаза внутриклеточного кальция блокирует образование аутофагосом. Аутофагия. 2013. 9 (10) октября: 1475–1490. PubMed PMID: 23970164. [PubMed] [Google Scholar]
[48] Thoreen CC, Kang SA, Chang JW, et al. АТФ-конкурентная мишень ингибитора рапамицина у млекопитающих обнаруживает устойчивые к рапамицину функции mTORC1. Дж. Биол. Хим. 2009. Маршировать 20;284(12):8023–8032. PubMed PMID: 19150980. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[49] Florey O, Gammoh N, Kim SE, et al. V-АТФаза и осмотический дисбаланс активируют липидизацию эндолизосом LC3. Аутофагия. 2015;11(1):88–99. PubMed PMID: 25484071. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[50] Kjos I, Borg Distefano M, Saetre F, et al. Rab7b модулирует поток аутофагии, взаимодействуя с Atg4B. Представитель EMBO, 2017 г.
Август
23;18:1727–1739. PubMed PMID: 28835545. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Rab7b модулирует поток аутофагии, взаимодействуя с Atg4B. Представитель EMBO, 2017 г.
Август
23;18:1727–1739. PubMed PMID: 28835545. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[51] Кимура С., Нода Т., Йошимори Т. Рассечение процесса созревания аутофагосом с помощью нового репортерного белка, тандемного флуоресцентно-меченого LC3. Аутофагия. 2007. Сентябрь-октябрь; 3 (5): 452–460. PubMed PMID: 17534139. [PubMed] [Google Scholar]
[52] Young AR, Chan EY, Hu XW, et al. Голодание и ULK1-зависимый цикл Atg9 млекопитающих между TGN и эндосомами. Дж. Клеточные науки. 2006. Сентябрь 15; 119 (Пт. 18): 3888–3900. PubMed PMID: 16940348. [PubMed] [Google Scholar]
[53] Itakura E, Kishi-Itakura C, Mizushima N. Синтаксин 17 SNARE, заякоренный в виде шпильки, нацелен на аутофагосомы для слияния с эндосомами/лизосомами. Клетка. 2012. Декабрь 7; 151(6):1256–1269.. PubMed PMID: 23217709. [PubMed] [Google Scholar]
[54] Цубояма К., Кояма-Хонда И., Сакамаки Ю. и др. Системы конъюгации ATG важны для деградации внутренней аутофагосомной мембраны. Наука. 2016.
ноябрь
25;354(6315):1036–1041. PubMed PMID: 27885029. [PubMed] [Google Scholar]
Системы конъюгации ATG важны для деградации внутренней аутофагосомной мембраны. Наука. 2016.
ноябрь
25;354(6315):1036–1041. PubMed PMID: 27885029. [PubMed] [Google Scholar]
[55] Zhou J, Tan SH, Nicolas V, et al. Активация лизосомальной функции в ходе аутофагии посредством подавления mTORC1 и слияния аутофагосом-лизосом. Сотовый рез. 2013. Апрель; 23 (4): 508–523. PubMed PMID: 23337583. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[56] Baltazar GC, Guha S, Lu W, et al. Кислотные наночастицы доставляются в лизосомы и восстанавливают кислый лизосомальный рН и деструктивную функцию в скомпрометированных клетках ARPE-19. ПЛОС Один. 2012;7(12):e49635 PubMed PMID: 23272048. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[57] Nadanaciva S, Lu S, Gebhard DF, et al. Скрининговый анализ высокого содержания для выявления лизосомотропных соединений. Токсикол в пробирке. 2011. Апрель; 25 (3): 715–723. PubMed PMID: 21184822. [PubMed] [Google Scholar]
[58] Yoon YH, Cho KS, Hwang JJ и др. Индукция расширения лизосом, остановка аутофагии и гибель клеток хлорохином в культивируемых клетках ARPE-19. Invest Ophthalmol Vis Sci. 2010.
ноябрь; 51 (11): 6030–6037. PubMed PMID: 20574031. [PubMed] [Google Scholar]
Индукция расширения лизосом, остановка аутофагии и гибель клеток хлорохином в культивируемых клетках ARPE-19. Invest Ophthalmol Vis Sci. 2010.
ноябрь; 51 (11): 6030–6037. PubMed PMID: 20574031. [PubMed] [Google Scholar]
[59] Chikte S, Panchal N, Warnes G. Использование красителей LysoTracker: проточно-цитометрическое исследование аутофагии. Цитометрия А. 2014. Февраль; 85 (2): 169–178. PubMed PMID: 23847175. . [PubMed] [Google Scholar]
[60] Duvvuri M, Gong Y, Chatterji D, et al. Характеристики проницаемости слабого основания влияют на сайт внутриклеточной секвестрации в лейкемической клеточной линии человека с множественной лекарственной устойчивостью HL-60. Дж. Биол. Хим. 2004. Июль 30;279(31): 32367–32372. PubMed PMID: 15181006. [PubMed] [Google Scholar]
[61] Окума С., Пул Б.
Измерение флуоресцентным зондом внутрилизосомального pH в живых клетках и возмущение pH различными агентами. Proc Natl Acad Sci U S A. 1978.
июль; 75 (7): 3327–3331. PubMed PMID: 28524. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
[62] Marceau F, Bawolak MT, Lodge R, et al. Захват катионов клеточными кислыми компартментами: за пределами концепции лизосомотропных препаратов. Toxicol Appl Pharmacol. 2012. февраль 15;259(1): 1–12. PubMed PMID: 22198553. [PubMed] [Google Scholar]
[63] Yucel-Lindberg T, Jansson H, Glaumann H. Протеолиз в изолированных аутофагических вакуолях поджелудочной железы крыс. Эффекты введения хлорохина. Virchows Arch B Cell Pathol, включая Mol Pathol. 1991;61(2):141–145. PubMed PMID: 1683722. [PubMed] [Google Scholar]
[64] Glaumann H, Ahlberg J, Berkenstam A, et al. Быстрое выделение вторичных лизосом печени крысы — аутофагических вакуолей — после введения хлорохина. Разрешение ячейки опыта. 1986. март; 163 (1): 151–158. PubMed PMID: 3943558. [PubMed] [Google Scholar]
[65] Wisner-Gebhart AM, Brabec RK, Gray RH.
Морфометрические исследования вызванных хлорохином изменений органелл гепатоцитов у крыс. Опыт Мол Патол. 1980.
Октябрь; 33 (2): 144–152. PubMed PMID: 7418864. [PubMed] [Google Scholar]
1980.
Октябрь; 33 (2): 144–152. PubMed PMID: 7418864. [PubMed] [Google Scholar]
[66] Kovacs J, Rez G. Количественные аспекты клеточного аутофагоцитоза. Морфометрические исследования и клеточное фракционирование. Ревис Биол Селуляр. 1989; 20: 63–78. PubMed PMID: 2700098. [PubMed] [Google Scholar]
[67] Kovacs J, Karpati AP. Регрессия аутофагических вакуолей в клетках поджелудочной железы мышей: морфометрическое исследование действия метиламина и хлорохина с последующим лечением циклогексимидом. Cell Biol Int Rep. 1989. Сентябрь; 13 (9): 805–811. PubMed PMID: 2805089. [PubMed] [Google Scholar]
[68] Ковач А.Л., Сеглен П.О. Ингибирование деградации гепатоцитарного белка индукторами накопления аутофагосом. Acta Biol Med Ger. 1982;41(1):125–130. PubMed PMID: 7113543. [PubMed] [Google Scholar]
[69] Ямамото А., Тагава Ю., Йошимори Т. и др.
Бафиломицин А1 предотвращает созревание аутофагических вакуолей, ингибируя слияние между аутофагосомами и лизосомами в клеточной линии гепатомы крыс, клетках H-4-II-E. Функция клеточной структуры. 1998.
Февраль; 23 (1): 33–42. PubMed PMID: 9639028. [PubMed] [Google Scholar]
Функция клеточной структуры. 1998.
Февраль; 23 (1): 33–42. PubMed PMID: 9639028. [PubMed] [Google Scholar]
[70] Jahreiss L, Menzies FM, Rubinsztein DC. Путь аутофагосом: от периферического образования до слияния с лизосомами по принципу «поцелуй-и-беги». Движение. 2008. Апрель; 9 (4): 574–587. PubMed PMID: 18182013. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[71] Mauvezin C, Nagy P, Juhasz G, et al. Слияние аутофагосомы и лизосомы не зависит от опосредованного V-АТФазой подкисления. Нац коммун. 2015. Может 11;6:7007 PubMed PMID: 25959678. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[72] Kumar S, Jain A, Farzam F, et al. Механизм рекрутирования Stx17 в аутофагосомы через IRGM и белки Atg8 млекопитающих. Джей Селл Биол. 2018. март; 217 (3): 997–1013. PubMed PMID: 29420192. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[73] Rivinoja A, Hassinen A, Kokkonen N, et al.
Повышенный рН по методу Гольджи ухудшает терминальное N-гликозилирование, индуцируя неправильную локализацию гликозилтрансфераз Гольджи.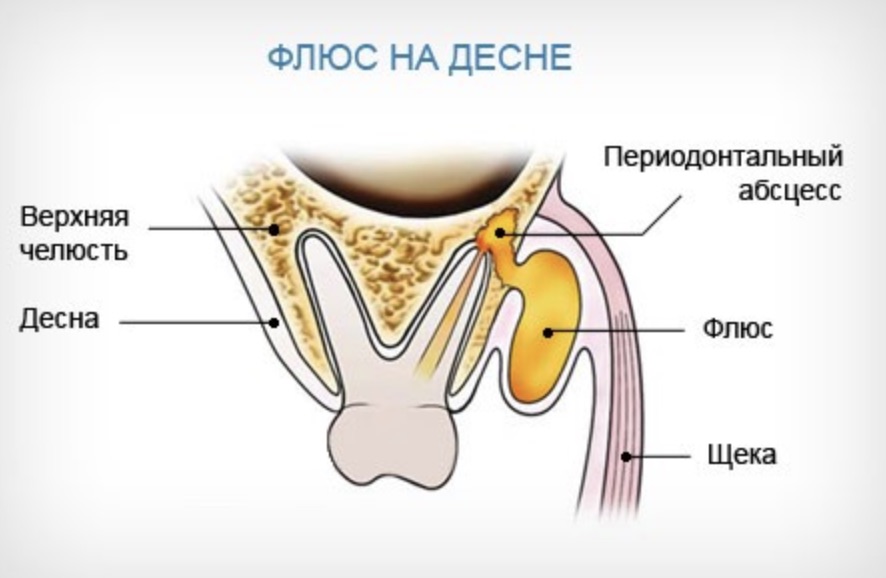 J Cell Physiol. 2009 г..
июль; 220 (1): 144–154. PubMed PMID: 19277980. [PubMed] [Google Scholar]
J Cell Physiol. 2009 г..
июль; 220 (1): 144–154. PubMed PMID: 19277980. [PubMed] [Google Scholar]
[74] Chen PM, Gombart ZJ, Chen JW. Обработка хлорохином клеток ARPE-19 приводит к расширению лизосом и накоплению внутриклеточных липидов: возможные последствия лизосомной дисфункции при дегенерации желтого пятна. Клетка Биоски. 2011. Маршировать 8;1(1):10 PubMed PMID: 21711726. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[75] Kellokumpu S, Sormunen R, Kellokumpu I. Аномальное гликозилирование и измененная структура Гольджи при колоректальном раке: зависимость от рН внутри Гольджи. ФЭБС лат. 2002. апреля 10;516(1–3):217–224. PubMed PMID: 11959136. [PubMed] [Google Scholar]
[76] Thorens B, Vassalli P. Хлорохин и хлорид аммония предотвращают терминальное гликозилирование иммуноглобулинов в плазматических клетках, не влияя на секрецию. Природа. 1986 год. Июнь 5–11;321(6070):618–620. PubMed PMID: 3086747. [PubMed] [Google Scholar]
[77] Zhang X, Wang Y. Контроль качества гликозилирования по структуре Гольджи. Дж Мол Биол. 2016.
Август
14;428(16):3183–3193. PubMed PMID: 26956395. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Контроль качества гликозилирования по структуре Гольджи. Дж Мол Биол. 2016.
Август
14;428(16):3183–3193. PubMed PMID: 26956395. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[78] Hassinen A, Pujol FM, Kokkonen N, et al. Функциональная организация путей N- и O-гликозилирования по Гольджи включает образование рН-зависимых комплексов, которые в раковых клетках нарушены. Дж. Биол. Хим. 2011. ноябрь 4;286(44):38329–38340. PubMed PMID: 21911486. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[79] Razi M, Chan EY, Tooze SA. Ранние эндосомы и эндосомальный коатомер необходимы для аутофагии. Джей Селл Биол. 2009. апреля 20;185(2):305–321. PubMed PMID: 19364919. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[80] Зонку Р., Бар-Пелед Л., Эфеян А. и др. mTORC1 ощущает лизосомальные аминокислоты посредством внутреннего механизма, для которого требуется вакуолярная Н(+)-АТФаза. Наука. 2011. ноябрь 4; 334(6056):678–683. PubMed PMID: 22053050. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[81] Li M, Khambu B, Zhang H, et al. Подавление функции лизосом вызывает аутофагию посредством обратной регуляции активности комплекса MTOR 1 (MTORC1). Дж. Биол. Хим. 2013.
Декабрь
13;288(50):35769–35780. PubMed PMID: 24174532. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Подавление функции лизосом вызывает аутофагию посредством обратной регуляции активности комплекса MTOR 1 (MTORC1). Дж. Биол. Хим. 2013.
Декабрь
13;288(50):35769–35780. PubMed PMID: 24174532. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[82] Барроу-МакГи Р., Киши Н., Жоффр С. и соавт. Кооперация Beta 1-integrin-c-Met обнаруживает внутреннюю передачу сигналов выживания на эндомембранах, связанных с аутофагией. Нац коммун. 2016. Июнь 23;7:11942 PubMed PMID: 27336951. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[83] Martinez-Lopez N, Athonvarangkul D, Mishall P, et al. Белки аутофагии регулируют фосфорилирование ERK. Нац коммун. 2013;4:2799 PubMed PMID: 24240988. . [Бесплатная статья PMC] [PubMed] [Google Scholar]
[84] Button RW, Roberts SL, Willis TL, et al. Накопление аутофагосом вызывает цитотоксичность. Дж. Биол. Хим. 2017. Июль 3;292:13599–13614. PubMed PMID: 28673965. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[85] Carter RE, Sorkin A. Эндоцитоз функциональной химеры рецептора эпидермального фактора роста — зеленого флуоресцентного белка. Дж. Биол. Хим. 1998.
Декабрь
25;273(52):35000–35007. PubMed PMID: 9857032. [PubMed] [Google Scholar]
Эндоцитоз функциональной химеры рецептора эпидермального фактора роста — зеленого флуоресцентного белка. Дж. Биол. Хим. 1998.
Декабрь
25;273(52):35000–35007. PubMed PMID: 9857032. [PubMed] [Google Scholar]
[86] Rote KV, Rechsteiner M. Деградация микроинъецированных белков: эффекты лизосомотропных агентов и ингибиторов аутофагии. J Cell Physiol. 1983. июль; 116 (1): 103–110. PubMed PMID: 6853609. . [PubMed] [Google Scholar]
[87] Martinez-Martin N, Maldonado P, Gasparrini F, et al. Переключение с канонической на неканоническую аутофагию формирует ответы В-клеток. Наука. 2017. февраль 10;355(6325):641–647. PubMed PMID: 28183981. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[88] Codogno P, Mehrpour M, Proikas-Cezanne T. Каноническая и неканоническая аутофагия: вариации на общую тему самопоедания? Nat Rev Mol Cell Biol. 2011. Декабрь 14;13(1):7–12. PubMed PMID: 22166994. [PubMed] [Google Scholar]
[89] Galluzzi L, Baehrecke EH, Ballabio A, et al.
Молекулярные определения аутофагии и родственных процессов. ЕМБО Дж. 2017.
Июль
3; 36 (13): 1811–1836. PubMed PMID: 28596378. [Бесплатная статья PMC] [PubMed] [Google Scholar]
ЕМБО Дж. 2017.
Июль
3; 36 (13): 1811–1836. PubMed PMID: 28596378. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[90] Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. Август 15;227(5259):680–685. PubMed PMID: 5432063. [PubMed] [Google Scholar]
[91] Schneider CA, Rasband WS, Eliceiri KW. NIH Image to ImageJ: 25 лет анализа изображений. Нат Методы. 2012. 9 июля(7): 671–675. PubMed PMID: 22930834. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[92] Verheije MH, Raaben M, Mari M, et al. Репликация РНК коронавируса мышиного гепатита зависит от активации ARF1, опосредованной GBF1. PLoS Патог. 2008. июнь;4(6):e1000088 PubMed PMID: 18551169. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[93] Slot JW, Geuze HJ. Криосрезы и иммуномаркировка. Природный протокол. 2007;2(10):2480–2491. PubMed PMID: 17947990. . [PubMed] [Google Scholar]
Может ли кислотный рефлюкс убить вас, вызвать опасные осложнения?
Кислотный рефлюкс возникает, когда содержимое желудка поднимается вверх по пищеводу — трубке, соединяющей рот с желудком.
Большинство людей время от времени испытывают легкий рефлюкс. Риск осложнений, как правило, низкий, когда рефлюкс незначительный.
Напротив, частый кислотный рефлюкс может быть признаком состояния, известного как гастроэзофагеальная рефлюксная болезнь (ГЭРБ).
Хотя ГЭРБ сама по себе не является опасным для жизни состоянием, она может привести к более серьезным проблемам со здоровьем и осложнениям, если ее не лечить.
Читайте дальше, чтобы узнать о более серьезных осложнениях ГЭРБ.
Легкий или случайный кислотный рефлюкс обычно не вызывает беспокойства. Хотя это может вызвать временный дискомфорт, это не представляет серьезного риска для здоровья.
У людей, которые испытывают кислотный рефлюкс более двух раз в неделю, может быть ГЭРБ, состояние, которое связано с большим количеством симптомов и осложнений.
Общие симптомы ГЭРБ включают:
- неприятный запах изо рта
- боль в груди
- кашель
- затрудненное глотание (дисфагия)
- изжога
- расстройство желудка
- тошнота
- срыгивание
- боль в горле
В отдельных случаях ГЭРБ может привести к осложнениям. Некоторые из них могут быть серьезными, особенно если их не лечить. Многие из этих осложнений связаны друг с другом.
Некоторые из них могут быть серьезными, особенно если их не лечить. Многие из этих осложнений связаны друг с другом.
Давайте подробнее рассмотрим некоторые из наиболее серьезных проблем со здоровьем, которые могут возникнуть из-за ГЭРБ.
Эзофагит
Частый кислотный рефлюкс может вызвать воспаление пищевода, состояние, известное как эзофагит.
Эзофагит затрудняет глотание и иногда вызывает боль. Другие симптомы включают:
- боль в горле
- хриплый голос
- изжога
Хронический, нелеченый эзофагит может вызывать язвы и стриктуры пищевода. Это также может увеличить риск рака пищевода.
Язвы пищевода
Желудочная кислота может повредить слизистую оболочку пищевода, вызывая болезненную язву. Этот тип пептической язвы известен как язва пищевода.
Это может вызвать симптомы, такие как:
- Ощущение жжения в области вашей груди
- Ставка
- При глотании
- Тошнота
- .
 имеет симптомы.
имеет симптомы. При отсутствии лечения язва пищевода может привести к более серьезным осложнениям, таким как перфорация пищевода (отверстие в пищеводе) или кровоточащая язва.
Стриктура пищевода
Если ГЭРБ не лечить, она может вызвать воспаление, образование рубцов или аномальный рост тканей (неоплазию) в пищеводе. В результате ваш пищевод может стать уже и плотнее.
Это состояние, известное как стриктура пищевода, часто затрудняет или вызывает боль при глотании. Это также может затруднить прохождение пищи и жидкости из пищевода в желудок, а дыхание может ощущаться суженным.
В некоторых случаях твердая или плотная пища может застревать в пищеводе. Это может увеличить риск удушья. Кроме того, если вы не можете легко глотать пищу и жидкость, это может привести к недоеданию и обезвоживанию.
Аспирационная пневмония
Желудочная кислота, попадающая в горло или рот, может попасть в легкие при вдыхании. This can lead to aspiration pneumonia, a lung infection that causes symptoms like:
- fever
- deep cough
- chest pain
- shortness of breath
- wheezing
- fatigue
- blue discoloration of the skin
- death
Аспирационная пневмония может стать серьезной и даже смертельной, если ее не лечить.

Лечение обычно включает антибиотики и, в более тяжелых случаях, госпитализацию и поддерживающую дыхательную терапию.
Пищевод Барретта
Продолжающееся повреждение пищевода, вызванное желудочной кислотой, может вызвать клеточные изменения в слизистой оболочке пищевода.
При пищеводе Барретта плоскоклеточные клетки, выстилающие нижнюю часть пищевода, замещаются железистыми клетками. Эти клетки похожи на те, что выстилают ваш кишечник.
Пищевод Барретта развивается примерно у 10–15 процентов людей с ГЭРБ. Он имеет тенденцию поражать мужчин почти в два раза чаще, чем женщин.
Существует небольшой риск того, что клетки этих желез могут стать злокачественными и вызвать рак пищевода.
Рак пищевода
У людей с ГЭРБ несколько повышен риск развития определенного типа рака пищевода, известного как аденокарцинома пищевода.
Этот рак поражает нижнюю часть пищевода, вызывая такие симптомы, как:
- затрудненное глотание
- потеря веса
- боль в груди
- кашель
- сильное расстройство желудка
- сильная изжога
Рак пищевода часто не вызывает симптомов на ранних стадиях.
 Люди обычно замечают симптомы только после того, как рак достиг более поздней стадии.
Люди обычно замечают симптомы только после того, как рак достиг более поздней стадии. Помимо ГЭРБ, другие факторы, которые могут увеличить риск рака пищевода, включают:
- принадлежность к мужскому полу
- возраст старше 55 лет
- употребление табачных изделий
- регулярное употребление алкоголя на грудь или верхнюю часть живота
Вы можете уменьшить кислотный рефлюкс и предотвратить осложнения, выработав следующие привычки:
- Избегайте определенных продуктов. Жирная, жирная, кислая и острая пища с большей вероятностью может привести к рефлюксу. Другие продукты, такие как мята, томатный соус, чеснок, лук, цитрусовые и темный шоколад, также вызывают рефлюкс.
- Измените свои привычки в еде. Старайтесь принимать пищу по крайней мере за 2–3 часа до того, как вы ложитесь или ложитесь спать. Это даст вашему желудку время переварить пищу, которую вы съели. Кроме того, употребление небольших порций и медленное пережевывание пищи может помочь предотвратить чрезмерный рефлюкс.

- Сбросить лишний вес. Если вы носите лишний вес в районе живота, ваш желудок поднимается вверх, что облегчает попадание кислоты в пищевод.
- Ограничьте прием алкоголя и кофеина. Алкоголь и кофеин могут усиливать кислотный рефлюкс.
- Бросьте курить. Курение затрудняет правильное закрытие сфинктера, отделяющего пищевод от желудка, после того, как пища попадает в желудок.
- Спите на наклонной поверхности. Если кислотный рефлюкс и изжога возникают ночью, положите несколько блоков под изголовье кровати так, чтобы верхняя часть тела была немного выше живота. Вы также можете посмотреть на специальные клиновидные подушки, которые сделаны для людей с ГЭРБ.
- Носите более свободную одежду. Узкие штаны могут оказывать дополнительное давление на живот, выталкивая содержимое желудка вверх.
Вам следует обратиться к врачу, если вы испытываете симптомы ГЭРБ чаще, чем пару раз в неделю, даже если ваши симптомы легкие.

Вам также следует обратиться к врачу, если вы регулярно принимаете безрецептурные антациды или лекарства от изжоги. Эти препараты могут помочь нейтрализовать желудочную кислоту, но не устранят воспаление в пищеводе.
Кроме того, чрезмерное использование этих лекарств может вызвать побочные эффекты.
Существует ряд методов лечения кислотного рефлюкса, вызванного ГЭРБ. Ваш врач может предложить сочетание изменений образа жизни и лекарств.
Общие лекарства, используемые для лечения кислотного рефлюкса, включают:
- антациды
- блокаторы h3
- ингибиторы протонной помпы
- прокинетики
Если эти методы лечения не помогают, врач может порекомендовать операцию.
Существует несколько различных типов процедур, используемых для контроля ГЭРБ. Большинство из них сосредоточены на улучшении функции сфинктера, который удерживает желудочную кислоту от подъема вверх по пищеводу.
Эпизодический кислотный рефлюкс обычно не связан с долгосрочными или серьезными осложнениями.

