Гранулематозные заболевания легких | Самсонова
1. Muller H., Kruger S. Immunohistochemical analysis of cell composition and in situ cytokine expression in HIV- and non-HIV-associated tuberculosis lymphadenitis. Immuno- biol. 1994; 191: 354–368.
2. Enelow R.I., Sullivan G.W., Carper H.T., Mandell G.L. Induction of multinucleated giant cell formation from in vitro culture of human monocytes with interleukin-3 and interferon-gamma:comparison with other stimulating factors. Am. J. Respir. Cell Mol. Biol. 1992; 6: 57–62.
3. Струков А.И., Кауфман О.Я. Гранулематозное воспаление и гранулематозные болезни. М.: Медицина; 1989.
4. Statement on sarcoidosis. Joint Statement of the American Thoracic Society (ATS), the European Respiratory Society (ERS) and the World Association of Sarcoidosis and Other Granulomatous Disorders (WASOG) adopted by the ATS Board of Directors and by the ERS Executive Committee, February 1999. Am. J. Respir. Crit. Care Med. 1999; 160 (2): 736–755. DOI: 10.1164/ajrccm.160.2.ats4-99.
DOI: 10.1164/ajrccm.160.2.ats4-99.
5. Gal A.A., Koss M.N. The pathology of sarcoidosis. Curr. Opin. Pulm. Med. 2002; 8 (5): 445–451.
6. Popper H.H., Klemen H., Churg A., Colby T.V. Necrotizing sarcoid granulematosis. Sarcoidosis. 1997; 14 (Suppl. 1): 33.
7. Coleman A., Colby T.V. Histologic diagnosis of extrinsic allergic alveolitis. Am. J. Surg. Pathol. 1988; 12 (7): 514–518.
8. Barrios R.J. Hypersensitivity pneumonitis: histopathology. Arch. Pathol. Lab. Med. 2008; 132 (2): 199–203.
9. Popper H.H. Epithelioid cell granulomatosis of the lung: new insights and concepts. Sarcoidos. Vasc. Diffuse Lung Dis. 1999; 16 (1): 32–46.
10. Aubry M.-C. Necrotizing granulematous inflammation: what does it mean if your special stains are negative? Modern Pathology. 2012; 25: S31–S38. DOI: 10.1038/modpathol.2011.155.
11. Godman G., Churg J. Wegener’s granulomatosis. AMA Arch. Pathol. 1954; 58 (6): 533–553.
12. Yousem S.A., Colby T.V., Carrington C.B. Lung biopsy in rheumatoid arthritis.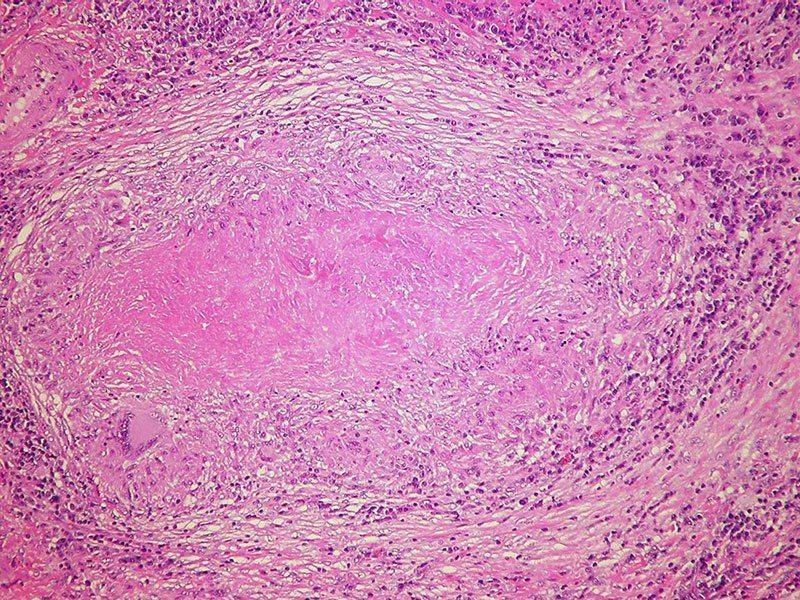 Am. Rev. Respir. Dis. 1985; 131 (5): 770–777. DOI: 10.1164/arrd.1985.131.5.770.
Am. Rev. Respir. Dis. 1985; 131 (5): 770–777. DOI: 10.1164/arrd.1985.131.5.770.
13. Yousem S.A. The surgical pathology of pulmonary infarcts: diagnostic confusion with granulomatous disease, vasculitis, and neoplasia. Mod. Pathol. 2009; 22 (5): 679–685. DOI: 10.1038/modpathol.2009.20.
14. Хмельницкий О.К., Хмельницкая Н.М. Патоморфология микозов человека. СПб: Издательский дом СПб МАПО; 2005.
15. Mukhopadhyay S., Gal A.A. Granulomatous lung disease: an approach to the differential diagnosis. Arch. Pathol. Lab. Med. 2010; 134 (5): 667–690. DOI: 10.1043/1543-2165134.5.667.
16. Travis W.D., Pittaluga S., Lipschik G.Y. et al. Atypical pathologic manifestations of Pneumocystis carinii pneumonia in the acquired immune deficiency syndrome: review of 123 lung biopsies from 76 patients with emphasis on cysts, vascular invasion, vasculitis, and granulomas. Am. J. Surg. Pathol. 1990; 14 (7): 615–625.
17. Weber W.R., Askin F.B., Dehner L.P. Lung biopsy in Pneumocystis carinii pneumonia: a histopathologic study of typical and atypical features. Am. J. Clin. Pathol. 1977; 67 (1): 11–19.
Am. J. Clin. Pathol. 1977; 67 (1): 11–19.
18. Струков А.И., Соловьева И.П. Морфология туберкулеза в современных условиях. М.: Медицина; 1976.
19. Corpe R.F., Stergus I. Is the histopathology of nonphotochromogenic mycobacterial infections distinguishable from that caused by Mycobacterium tuberculosis? Am. Rev. Respir. Dis. 1963; 87: 289–291.
20. Соловьева И.П., Батыров Ф.А., Пономарев А.Б., Федоров Д.Н. Патологическая анатомия туберкулеза и дифференциальная диагностика гранулематозных заболеваний. М.; 2005. Доступно на: http://bit.ly/2uhZO73
21. Danila E., Zurauskas E. Diagnostic value of epithlioid cell granulomas in bronchoscopic biopsies. Intern. Med. 2008; 47 (24): 2121–2126.
22. Iannuzzi M.C., Rybicki B.A., Teirstein A.S. Sarcoidosis. N. Engl. J. Med. 2007; 357 (21): 2153–2165. DOI: 10.1056/NEJMra071714.
23. Rosen Y., Amorosa J.K. Moon S. et al. Occurrence of lung granulomas in patients with stage I sarcoidosis. Am. J. Ro- engenol. 1977; 129 (6): 1083–1085. DOI: 10.2214/ajr.129.6.1083.
DOI: 10.2214/ajr.129.6.1083.
24. Myers J.L., Tazelaar H.D. Challenges in pulmonary fibrosis: Problematic granulomatous lung disease. Thorax. 2008; 63 (1): 78–84. DOI: 10.1136/thx.2004.031047.
25. Ulbright T.M., Katzenstein A.L. Solitary necrotizing granulomas of the lung: differentiating features and etiology. Am. J. Surg. Pathol. 1980; 4 (1): 13–28.
26. Mukhopadhyay S., Farver C.F., Vaszar L.T. et al. Causes of pulmonary granulomas: a retrospective study of 500 cases from seven countries. J. Clin. Pathol. 2012; 65 (1): 51–57. DOI: 10.1136/jclinpath-2011-200336.
ХРОНИЧЕСКИЙ ГЕНЕРАЛИЗОВАННЫЙ (ГРАНУЛЕМАТОЗНЫЙ) КАНДИДОЗ | Степанова Ж.В.
Ключевые слова: Кандидоз гранулематозный – микозы – иммунодефицит – грибы – клиническое течение – общеукрепляющее воздействие – иммунокорригирующие препараты – иммуномодуляторы – детоксицирующие средства – антимикотилен.
Представлены данные о патогенезе, клинических проявлениях и терапии хронического генерализованного (гранулематозного) кандидоза, накопленные в ходе многолетнего изучения данного заболевания, отличающегося длительным, часто рецидивирующим течением, устойчивостью к средствам противогрибковой терапии. Установлено, что ведущим фактором в его развитии являются иммунные нарушения. С учетом выявленных нарушений (иммунных, эндокринных, дефицита микроэлементов) разработан эффективный комплексный метод лечения, включающий патогенетические и антифунгальные препараты общего и наружного действия, а также общеукрепляющие средства.
Установлено, что ведущим фактором в его развитии являются иммунные нарушения. С учетом выявленных нарушений (иммунных, эндокринных, дефицита микроэлементов) разработан эффективный комплексный метод лечения, включающий патогенетические и антифунгальные препараты общего и наружного действия, а также общеукрепляющие средства.
Key words: Granulomatous candidiasis — mycoses — immunodeficiency — fungi — clinical course — conditioning effects — immunomodulating agents -detoxifying agents — antimycolen.
The paper gives data on the pathogenesis, clinical manifestations, and treatment of chronic generalized (granulomatous) candiasis, which have been accumulated during many-year studies of the disease which is characterized by its long-term, frequently reccurent curse and resistance to antimycotic therapy. Immune disorders were found to be the leading factor predisposing to candidiasis. By taking into accout the identified disorders (immune, endocrine disorders, trace deficiencies), an effective combined multimodality treatment with pathogenetic and antifungal agents of systemic and topical action and conditioning has been elaborated.
Ж.В. Степанова, доктор мед. наук, ведущий научный сотрудник отделения микологии Центрального научно-исследовательского кожно-венерологического института Минздрава РФ, Москва
Zh.V. Stepanova, MD, Leading Researcher, Department of Mycology, Central Research Dermatovenereological Institute, Ministry of Health of the Russian Federation
В последние годы в структуре заболеваемости микозами населения развитых стран произошли сдвиги в сторону увеличения доли болезней, обусловленных условно-патогенными грибами; основное место среди них занимает кандидоз. По данным Центра контроля заболеваемости (США), при обследовании больных СПИДом у 41,8% был выявлен кандидоз слизистой полости рта. Своеобразной разновидностью хронического кандидоза является хронический генерализованный (гранулематозный) кандидоз (ХГК), часто возникающий как генетически обусловленное заболевание.
Синонимы: хронический кожно-слизистый кандидоз, кандидагранулема, эндокринно-кандидозный синдром и др.
Патогенез
За последние 20 лет благодаря развитию клинической иммунологии достигнуты определенные успехи в изучении патогенеза ХГК. В настоящее время это заболевание можно с уверенностью причислить к состояниям, связанным с нарушением иммунной системы. Установлено, что при ХГК снижены реакции гиперчувствительности замедленного типа, подавлена реакция лимфоцитов в культуре с митогеном фитогемагглютинина или кандидаантигеном, нарушена способность лимфоцитов вырабатывать лимфокины в присутствии специфического антигена. По нашим данным, почти у 50% больных кандидоз развивается на фоне иммунодефицита: при распространенных формах поражения с сопутствующей патологией внутренних органов доминирующими являются иммунные нарушения, характеризующиеся снижением количественных и функциональных показателей Т-лимфоцитов, изменением содержания В-лимфоцитов, а также нарушением розеткообразующих свойств и фагоцитарной активности нейтрофилов крови.
Рис. 1. Поражение языка.
Некоторые исследователи относят это заболевание к ферментопатиям и считают, что основную роль в нарушении механизма фагоцитарной активности клеток крови в отношении грибов рода Кандида играет повреждение миелопероксидазной системы с невозможностью полного переваривания клеток грибов рода Кандида.
Рис. 2. Поражение ногтей.
Диагностика
Диагноз ХГК ставится на основании клинической картины поражения и подтверждается обнаружением дрожжеподобных грибов в патологическом материале при микроскопическом исследовании. Основным возбудителем является гриб Кандида альбиканс, реже другие виды рода Кандида.
Основным возбудителем является гриб Кандида альбиканс, реже другие виды рода Кандида.
Клиническое течение
Заболевание начинается в первые дни, недели, месяцы или годы жизни, но чаще в возрасте от 3 до 6 мес. При этом могут быть поражены слизистые оболочки рта и гениталий, кожа лица, головы, конечностей, туловища, ногтевые пластинки кистей и стоп, зубы, глаза и внутренние органы. Нами были выявлены некоторые особенности в клиническом течении ХГК. Заболевание может начинаться с поражения слизистой оболочки рта, кожи или ногтей. У некоторых больных поражения слизистой оболочки рта, ногтей остаются в течение нескольких лет единственными проявлениями кандидоза, а высыпания на коже могут появиться даже через 20 лет.
Рис. 3. Очаги эритематосквамозного характера на коже нижних конечностей.
Поражения слизистой оболочки рта и ногтевых пластинок носят однотипный характер. На слизистой щек, губ, неба, десен и языке появляется налет белого цвета; налет сначала творожистый, затем на слизистой щек он становится плотным и напоминает плоскую или эрозивную лейкоплакию. Налет плохо отделяется при поскабливании. Кроме того, могут наблюдаться эрозии и эрозивные участки. В углах рта имеются поверхностные или глубокие трещины с инфильтрацией в основании. Язык утолщенный, складчатый, складки могут быть поперечными и продольными (рис. 1). На красной кайме губ развивается сначала хейлит, а позже макрохейлит одной, реже обеих губ. Поражение со слизистой оболочки рта распространяется на глотку, пищевод. Возможно развитие склерозирующего макроглоссита и макрохейлита. У большинства больных развивается кариозное поражение зубов. Поражения ногтей могут быть единичными, но чаще множественными. Ногтевые валики утолщены, гиперемированы, эпонихион сохраняется, ногтевое ложе бугристое, деформировано и приподнимается за счет подногтевого гиперкератоза (рис. 2). Клинические проявления на коже могут варьировать от эритематосквамозных до гранулематозных очагов с веррукозными разрастаниями и ороговением. Высыпания возникают на любом участке кожного покрова, бывают ограниченными или же распространенными, напоминающими эритродермию.
Налет плохо отделяется при поскабливании. Кроме того, могут наблюдаться эрозии и эрозивные участки. В углах рта имеются поверхностные или глубокие трещины с инфильтрацией в основании. Язык утолщенный, складчатый, складки могут быть поперечными и продольными (рис. 1). На красной кайме губ развивается сначала хейлит, а позже макрохейлит одной, реже обеих губ. Поражение со слизистой оболочки рта распространяется на глотку, пищевод. Возможно развитие склерозирующего макроглоссита и макрохейлита. У большинства больных развивается кариозное поражение зубов. Поражения ногтей могут быть единичными, но чаще множественными. Ногтевые валики утолщены, гиперемированы, эпонихион сохраняется, ногтевое ложе бугристое, деформировано и приподнимается за счет подногтевого гиперкератоза (рис. 2). Клинические проявления на коже могут варьировать от эритематосквамозных до гранулематозных очагов с веррукозными разрастаниями и ороговением. Высыпания возникают на любом участке кожного покрова, бывают ограниченными или же распространенными, напоминающими эритродермию.
Рис. 4. Кандидагранулемы на голове.
В процесс могут быть вовлечены внутренние органы (бронхи, легкие, кишечник, печень, селезенка, почки). Однако последние поражения не всегда кандидозной этиологии, чаще аутоиммунного характера и обусловлены развитием иммунодефицита или эндокринных нарушений, что требует дополнительного обследования и соответствующего лечения у специалистов смежных дисциплин.
Рис. 5. Очаги поражения на коже стоп у больного ХГК.
У больных с гипофункцией паращитовидных желез бывают эпилептиформные припадки с выраженным судорожным компонентом. У некоторых больных присоединяется другое грибковое заболевание – руброфития или трихофития.
В некоторых случаях в одной семье имеется двое или трое детей, страдающих ХГК. Под нашим наблюдением находятся две семьи, в одной больны отец и дочь, в другой – мать и сын. В обоих случаях фоном для развития кандидоза послужили нарушения функции иммунной системы в виде аутоиммунных заболеваний.
Лечение
Лечение больных ХГК должно быть комплексным и включать патогенетические и антифунгальные препараты общего и наружного действия, а также общеукрепляющие средства.
Общеукрепляющие воздействия. Лечение следует начинать с общеукрепляющих мероприятий. Назначают фитин, инъекции алоэ в общепринятых дозах. Особое внимание следует обращать на насыщение организма витаминами, преимущественно группы В (В1, В2, В6, В12), назначать их можно внутрь или внутримышечно. Рекомендуются фолиевая кислота, витамин А в общепринятых дозах, аскорбиновая кислота по 0,1 – 0,2 г 3 раза в день.
Так как у больных ХГК наблюдается гипопротеинемия, им следует назначать анаболические стероиды для улучшения азотистого обмена. Особенно удобен для применения у детей нандролон благодаря пролонгированному действию. Детям его назначают из расчета 0,5 – 1 мг на 1 кг массы 1 раз в 3 – 4 нед, взрослым – по 0,025 – 0,05 г (25 – 50 ЕД) 1 раз в 3 нед. Нандролон вводят внутримышечно, на курс 2 – 3 инъекции.

Патогенетическая терапия
Основное значение в комплексном лечении имеет патогенетическая терапия.
Иммунокорригирующие препараты назначают с учетом выявленных нарушений. В последние годы наиболее перспективным в изучении эффективности иммуномодуляторов в плане индивидуализации терапии является хемилюминесцентный метод.
В качестве иммуномодуляторов при количественной и функциональной недостаточности Т- и В-лимфоцитов используют левамизол, спленин, нуклеинат натрия, арбидол, тактивин и др. При сниженной функциональной активности нейтрофилов назначают метилурацил, взвесь плаценты, пирогенал. Для коррекции гуморального иммунитета применяют иммуно- и гамма-глобулин. Левамизол назначают внутрь из расчета 2,5 мг на 1 кг массы тела больного по следующей схеме: 1 раз в день в течение 3 дней подряд с 4-дневным перерывом на протяжении 3 нед, после 2-недельного перерыва – 3 дня подряд с 4-дневным перерывом в течение 2 нед и вновь 2-недельный перерыв. Продолжительность курса 3 – 3,5 мес. Спленин вводят внутримышечно ежедневно, детям до 3 лет – 0,5 мл, от 4 до 8 лет – 1 мл, от 9 до 14 лет – 1,5–2 мл, старше 14 лет – 2–3 мл, на курс 10 инъекций. Нуклеинат натрия применяют по 0,5–1 г в день в 2–3 приема в течение 2–3 нед. Тактивин вводят подкожно по 1 мл (100 мкг) ежедневно в течение 3 дней, затем 2 раза в той же дозе 1 раз в неделю, через 1–1,5 мес курс лечения можно повторить или вводить по 1 мл через день, на курс 10 инъекций. Нами получен хороший терапевтический эффект при назначении арбидола 24 больным по результатам хемилюминесценции in vitro. Доза для детей составляла по 0,1 г, для взрослых – по 0,2 г 3 раза в день в течение 5 дней с 2-дневным перерывом, затем в той же дозе 1 раз в неделю на протяжении 3 нед. Метилурацил назначают в возрасте до 6 лет по 0,25 г 2 раза в день, от 6 до 10 лет по 0,25 г 3 раза, от 10 до 15 лет по 0,5 г 2 раза, старше 15 лет – 0,5 г 3 раза в день, курс лечения 10 дней. После 7-дневного перерыва лечение можно повторить.
Продолжительность курса 3 – 3,5 мес. Спленин вводят внутримышечно ежедневно, детям до 3 лет – 0,5 мл, от 4 до 8 лет – 1 мл, от 9 до 14 лет – 1,5–2 мл, старше 14 лет – 2–3 мл, на курс 10 инъекций. Нуклеинат натрия применяют по 0,5–1 г в день в 2–3 приема в течение 2–3 нед. Тактивин вводят подкожно по 1 мл (100 мкг) ежедневно в течение 3 дней, затем 2 раза в той же дозе 1 раз в неделю, через 1–1,5 мес курс лечения можно повторить или вводить по 1 мл через день, на курс 10 инъекций. Нами получен хороший терапевтический эффект при назначении арбидола 24 больным по результатам хемилюминесценции in vitro. Доза для детей составляла по 0,1 г, для взрослых – по 0,2 г 3 раза в день в течение 5 дней с 2-дневным перерывом, затем в той же дозе 1 раз в неделю на протяжении 3 нед. Метилурацил назначают в возрасте до 6 лет по 0,25 г 2 раза в день, от 6 до 10 лет по 0,25 г 3 раза, от 10 до 15 лет по 0,5 г 2 раза, старше 15 лет – 0,5 г 3 раза в день, курс лечения 10 дней. После 7-дневного перерыва лечение можно повторить. Взвесь плаценты в виде подкожных инъекций назначают детям до 6 лет в дозе 0,5 мл, от 7 до 10 лет – 1 мл, от 11 до 14 лет – 1,5 мл, старше 14 лет – 2 мл 1 раз в 5–7 дней, 3 – 4 инъекции на курс. Пирогенал вводят внутримышечно, начиная с 30 – 50 МПД, инъекции производят через 1–2 дня, при хорошей переносимости каждую последующую дозу увеличивают на 30 – 50 МПД, на курс 8 – 10 инъекций.
Взвесь плаценты в виде подкожных инъекций назначают детям до 6 лет в дозе 0,5 мл, от 7 до 10 лет – 1 мл, от 11 до 14 лет – 1,5 мл, старше 14 лет – 2 мл 1 раз в 5–7 дней, 3 – 4 инъекции на курс. Пирогенал вводят внутримышечно, начиная с 30 – 50 МПД, инъекции производят через 1–2 дня, при хорошей переносимости каждую последующую дозу увеличивают на 30 – 50 МПД, на курс 8 – 10 инъекций.
Иммуноглобулин человека нормальный назначают внутримышечно в разовой дозе 0,15 – 0,2 мл на 1 кг массы тела больного 1 раз в 3 дня, на курс 3 – 4 инъекции. Гамма-глобулин вводят внутримышечно: детям до 3 лет 1,5 мл, от 3 до 6 лет 2 мл, старше 6 лет 3 мл 2 раза в неделю, 3 – 5 инъекций на курс, в зимне-весенний период инъекции производят 1 раз в 3 нед в течение 3 мес.
Детоксицирующие воздействия. При распространенных и генерализованных процессах, сопутствующей руброфитии показаны внутривенные инфузии гемодеза: детям по 5 – 10 мл на 1 кг массы тела, взрослым по 200 – 250 мл, на курс 3 – 5 вливаний с перерывом в 1 – 2 дня.
Лечение фоновой патологии, снижающей иммунитет. При низком содержании гемоглобина крови применяют препараты железа: железа глицерофосфат, железа лактат, гемостимулин, ферроплекс. Железа глицерофосфат назначают детям по 0,3 – 0,5 г 2 – 3 раза в день, взрослым по 1 г 3 – 4 раза в день после еды (запивать молоком), курс лечения составляет 2 – 3 нед в стационаре, затем после 3 – 4-недельного перерыва препараты дают амбулаторно. Железа лактат детям назначают по 0,1 – 0,5 г 3 раза в день, взрослым – по 0,5 г 3 раза в день после еды, курс лечения 2 – 3 нед. Гемостимулин назначают в порошках или таблетках детям по 0,1 – 0,5 г 3 раза в день во время еды, лечение проводится 3 нед. Ферроплекс, драже, содержащее 50 мг железа сульфата и 30 мг аскорбиновой кислоты, назначают по 1 – 2 драже 3 раза в день взрослым и по 1 драже 3 раза в день детям в возрасте от 4 до 12 лет. Препараты железа больные должны принимать длительно в течение 1,5 – 2 лет с перерывами в 3 – 4 нед, чередуя их, под контролем показателей крови.
Больные с эндокринной патологией должны обязательно находиться под наблюдением эндокринолога и получать корригирующую терапию.
Этиотропная терапия
Для этиологического лечения применяют антибиотики полиенового ряда. Используют амфотерицин B для внутривенного и ингаляционного введения, нистатин, леворин, амфоглюкамин (внутрь и ингаляционно), леворина натриевую соль растворимую, микогептин (в зависимости от возраста больного от 1 000 000 до 8 000 000 ЕД для пероральных препаратов, продолжительность курса от 3 до 4 нед), натамицин. Назначают препараты имидазольного ряда – кетоконазол, флуконазол, интраконазол, флуцитозин.
Наиболее эффективным препаратом полиенового ряда является амфотерицин B. Выпускают его в виде порошка по 50 000 ЕД для внутривенного введения с 5% раствором глюкозы в качестве растворителя и для ингаляций без растворителя. В связи с побочными действиями (нефротоксичность, гепатотоксичность и др.) его применяют по жизненным показаниям у больных сепсисом и с тяжелыми поражениями внутренних органов.
Натамицин – полиеновый антибиотик группы макролидов, к которой относятся также нистатин и амфотерицин B. Преимущество натамицина – отсутствие развития резистентности у грибов. Препарат выпускают в таблетках по 100 мг, назначают взрослым по 1 таблетке 4 раза в день после еды ежедневно, продолжительность курса от одного до нескольких месяцев.
Флуцитозин оказывает фунгистатическое и фунгицидное действие на дрожжеподобные грибы рода Candida. Препарат выпускается в виде таблеток по 0,5 г и раствора для внутривенного вливания.
Назначают флуцитозин внутрь и внутривенно капельно в средней дозе по 37,5 – 50 мг на 1 кг массы тела каждые 6 ч, суточная доза составляет 150 – 200 мг/кг. Продолжительность лечения зависит от тяжести течения заболевания и переносимости препарата. Недостатком препарата является развитие к нему резистентности. Лечение проводят под контролем функции почек, печени и показателей крови.
Наиболее эффективными противогрибковыми препаратами для лечения больных ХГК являются кетоконазол, флуконазол, интраконазол.
Кетоконазол выпускают в таблетках по 200 мг, его назначают детям с массой тела до 20 кг по 50 мг в день, от 20 до 40 кг по 100 мг, взрослым по 200 мг в день. По нашим данным, препарат не уступает по эффективности амфотерицину B: на фоне его приема разрешались существовавшие почти с первых дней жизни высыпания на слизистой оболочке рта, коже, отрастали здоровые ногтевые пластинки. Однако для получения стойкого терапевтического эффекта в первые месяцы дозу препарата следует удвоить, а продолжительность курса должна составлять не менее 1 – 1,5 лет. Лечение проводят под контролем функции печени и почек.
Флуконазол выпускается в капсулах по 50, 100, 150 и 200 мг в виде раствора, содержащего 2 мг/мл флуконазола для внутривенного введения. Препарат назначают взрослым по 400 мг 1 раз в сутки в 1-й день лечения и по 200 мг в последующие дни, при необходимости дозу можно увеличить до 400 мг/сут; детям его назначают из расчета 3–6 мг на 1 кг массы тела. Лечение проводят под контролем функции печени и почек.
Итраконазол выпускают в капсулах по 100 мг, назначают в зависимости от возраста от 100 до 200 мг ежедневно в течение нескольких месяцев.
Наружное лечение
В комплексном лечении больных ХГК большое значение имеет наружная терапия, которая заключается в применении антифунгальных средств: клотримазола, натамицина, пимафукорта, травогена, травокорта, микоспора, циклопирокса, 1 – 2% водных и спиртовых растворов анилиновых красителей (бриллиантового зеленого, метиленового синего), фукорцина, серно-салициловой (соответственно 10 и 3%), серно-дегтярной (10 и 3%), нистатиновой мазей, микозолона, низорала в виде крема и др.
Больным следует рекомендовать соблюдение режима труда и отдыха, ограничение психических и физических нагрузок.
Как показали наши наблюдения, регулярно проводимое комплексное лечение позволяет поддерживать нормальную жизнедеятельность больных. Они могут посещать детские дошкольные учреждения, учиться в школе, в средних специальных и высших учебных заведениях, полноценно трудиться, вступать в брак, иметь детей.
Литература:
1. Антоньев А.А., Бульвахтер Л.А., Глазкова Л.К., Ильин И.И. Кандидоз кожи и слизистых оболочек. – М.: Медицина. – 1985. – С. 16.
2. Степанова Ж.В. Грибковые заболевания. – М.: Крон–Пресс. – 1996. – С. 176.
Хроническая гранулематозная болезнь Информация | Гора Синай
ЦГД; Фатальный гранулематоз детского возраста; Хроническая гранулематозная болезнь детского возраста; Прогрессирующий септический гранулематоз; Дефицит фагоцитов — хроническая гранулематозная болезнь
Хроническая гранулематозная болезнь (ХГБ) — это наследственное заболевание, при котором определенные клетки иммунной системы не функционируют должным образом. Это приводит к повторным и тяжелым инфекциям.
Причины
При ХГБ клетки иммунной системы, называемые фагоцитами, неспособны убивать некоторые виды бактерий и грибков. Это расстройство приводит к длительным (хроническим) и повторным (рецидивирующим) инфекциям. Состояние часто обнаруживают в очень раннем детстве. Более легкие формы могут быть диагностированы в подростковом возрасте или даже во взрослом возрасте.
Это расстройство приводит к длительным (хроническим) и повторным (рецидивирующим) инфекциям. Состояние часто обнаруживают в очень раннем детстве. Более легкие формы могут быть диагностированы в подростковом возрасте или даже во взрослом возрасте.
Факторы риска включают семейный анамнез рецидивирующих или хронических инфекций.
Около половины случаев ХГБ передается из поколения в поколение как сцепленный с полом рецессивный признак. Это означает, что мальчики чаще страдают этим расстройством, чем девочки. Дефектный ген находится на Х-хромосоме. Мальчики имеют 1 Х-хромосому и 1 Y-хромосому. Если у мальчика есть Х-хромосома с дефектным геном, он может унаследовать это заболевание. У девочек 2 Х-хромосомы. Если у девочки есть 1 Х-хромосома с дефектным геном, другая Х-хромосома может иметь рабочий ген, который компенсирует это. Чтобы заболеть, девочка должна унаследовать дефектный ген Х от каждого родителя.
Симптомы
ХГД может вызывать многие виды трудно поддающихся лечению кожных инфекций, в том числе:
- Пузыри или язвы на лице (импетиго)
- Экзема
- Наросты, наполненные гноем (абсцессы)
- Наполненные гноем образования на коже (фурункулы)
ХГД также могут вызывать: как пневмония или абсцесс легкого
Обследования и анализы
Медицинский работник проведет осмотр и может обнаружить:
- Отек печени
- Отек селезенки
- Увеличение лимфатических узлов
Могут быть признаки инфекции костей, которая может поражать многие кости.
Анализы, которые могут быть выполнены, включают:
- Сканирование костей
- Рентген грудной клетки
- Общий анализ крови (CBC)
- Проточная цитометрия для подтверждения заболевания
- Генетическое тестирование для подтверждения диагноза
- Проверка функции лейкоцитов
- Биопсия ткани
Лечение
Антибиотики используются для лечения инфекций, вызванных этим заболеванием. Хроническое использование антибиотиков может быть использовано для предотвращения инфекций. Лекарство под названием интерферон-гамма также может помочь уменьшить количество тяжелых инфекций. Для лечения некоторых абсцессов может потребоваться хирургическое вмешательство.
Единственным лекарством от ХГБ является трансплантация костного мозга или стволовых клеток.
Перспективы (прогноз)
Длительное лечение антибиотиками может помочь уменьшить количество инфекций, но ранняя смерть может наступить из-за повторяющихся легочных инфекций.
Возможные осложнения
ХГД может вызвать следующие осложнения:
- Повреждение костей и инфекции
- Хронические инфекции носа
- Пневмония, которая постоянно рецидивирует и трудно поддается лечению
- Повреждение легких
- Повреждение кожи
- Увеличение лимфатических узлов, которые остаются увеличенными, возникают часто или образуют абсцессы, для дренирования которых требуется хирургическое вмешательство
Когда обращаться к медицинскому работнику
Если у вас или вашего ребенка есть это заболевание и вы подозреваете пневмонию или другую инфекцию, немедленно позвоните своему поставщику.
Сообщите своему врачу, если легочная, кожная или другая инфекция не поддается лечению.
Профилактика
Генетическое консультирование рекомендуется, если вы планируете иметь детей и у вас есть семейная история этого заболевания. Достижения в области генетического скрининга и более широкое использование биопсии ворсин хориона (тест, который может быть проведен женщиной на 10-12 неделе беременности) сделали возможным раннее выявление ХГБ. Однако эти методы еще не получили широкого распространения и не получили полного признания.
Cunningham-Rundles C. Первичные иммунодефицитные заболевания. В: Goldman L, Schafer AI, ред. Медицина Голдман-Сесил . 26-е изд. Филадельфия, Пенсильвания: Elsevier; 2020: глава 236.
В: Goldman L, Schafer AI, ред. Медицина Голдман-Сесил . 26-е изд. Филадельфия, Пенсильвания: Elsevier; 2020: глава 236.
Холланд С.М., Узел Г. Дефицит фагоцитов. В: Рич Р.Р., Флейшер Т.А., Ширер В.Т., Шредер Дж.Р. HW, Frew AJ, Weyand CM, ред. Клиническая иммунология: принципы и практика . 5-е изд. Филадельфия, Пенсильвания: Elsevier; 2019:глава 22.
Последнее рассмотрение: 24.12.2020
Рецензировал: Джатин М. Вьяс, доктор медицинских наук, доцент медицины, Гарвардская медицинская школа; Ассистент медицины, отделение инфекционных заболеваний, медицинский факультет Массачусетской больницы общего профиля, Бостон, Массачусетс. Также рассмотрены Дэвидом Зивом, доктором медицинских наук, MHA, медицинским директором, Брендой Конауэй, редакционным директором, и A.D.A.M. Редакционная коллегия.
Хроническая гранулематозная болезнь (ХГБ) | Бостонская детская больница
Слушать
Хроническая гранулематозная болезнь (ХГБ) — это наследственное заболевание иммунной системы, которое возникает, когда тип лейкоцитов (фагоцитов), которые обычно помогают организму бороться с инфекцией, не работает должным образом. При ХГБ фагоциты не могут убивать попавшие в организм микробы и, следовательно, не могут защитить организм от бактериальных и грибковых инфекций. Дети с ХГБ часто здоровы при рождении, но у них развиваются тяжелые инфекции в младенчестве и в раннем детстве. Редко, при более легких формах диагноз не становится ясным в течение многих лет или десятилетий.
При ХГБ фагоциты не могут убивать попавшие в организм микробы и, следовательно, не могут защитить организм от бактериальных и грибковых инфекций. Дети с ХГБ часто здоровы при рождении, но у них развиваются тяжелые инфекции в младенчестве и в раннем детстве. Редко, при более легких формах диагноз не становится ясным в течение многих лет или десятилетий.
Поскольку дети с ХГБ не могут бороться с инфекциями, они часто сильно заболевают бактериями, которые могут быть легкими или вообще не вызывать заболевания у здорового ребенка. Эти инфекции могут поражать легкие, кожу, печень, лимфатические узлы и кишечник. У детей в ответ на хронические инфекции также могут развиваться массы воспалительной ткани, называемые гранулемами. Эти гранулемы обычно развиваются в коже, желудочно-кишечном тракте и мочеполовом тракте. CGD был назван в честь этих масс воспаления до того, как были обнаружены генетические причины.
Хроническая гранулематозная болезнь (ХГБ) | Симптомы и причины
Каковы симптомы ХГБ?
Большинство детей с ХГБ диагностируют к 5 годам. Наиболее частые симптомы заболевания включают:
Наиболее частые симптомы заболевания включают:
- пневмонию
- абсцессы селезенки и печени
- остеомиелит: инфекция костей
- гнойный артрит: инвазия сустава бактериальной инфекцией, вызывающая артрит
- поверхностные кожные инфекции, такие как целлюлит и импетиго
- грибковые инфекции
Хроническая гранулематозная болезнь (ХГБ) | Диагностика и лечение
Как диагностируется хроническая гранулематозная болезнь?
Хроническая гранулематозная болезнь (ХГБ) диагностируется с помощью:
- функциональных тестов нейтрофилов для определения того, насколько хорошо функционируют эти лейкоциты
- тест на восстановление дигидрородамина Генетическое тестирование
- для подтверждения наличия специфической генной мутации, приводящей к ХГД
После того, как все анализы будут завершены, врачи смогут определить наилучшие варианты лечения.
Как мы лечим больных ХГБ
Дети с ХГБ лечатся в рамках Иммунологической программы Бостонской детской больницы. Наша программа обеспечивает всестороннюю помощь при различных типах нарушений иммунной системы, включая ХГБ, и наши пациенты имеют доступ к некоторым из самых передовых доступных методов диагностики и лечения.
Генная терапия X-CGD
Boston Children’s участвует в клинических испытаниях фазы I/II для оценки безопасности, осуществимости и эффективности генной терапии Х-сцепленного ХГБ. (Испытание активно, но больше не набирает пациентов.) Лечение является результатом многолетнего научного путешествия, в основном в Бостонской детской больнице.
Хорошие ранние результаты генной терапии CGD
В 22 года Бренден попал в Бостонскую детскую больницу и стал первым человеком в США, получившим генетическую терапию хронической гранулематозной болезни. Пока это работает.
Прочитать его историю
Лечение включает сбор стволовых клеток крови пациента и их обработку в узкоспециализированной лаборатории с использованием безвредного вируса для введения в клетки правильной версии дефектного гена gp91-phox .
