Грануляционная ткань | Консультация стоматолога на сайте клиники Импладент
Грануляционная ткань | Консультация стоматолога на сайте клиники ИмпладентГлавная Услуги Консультация онлайн Консультация №135
26.07.2014
Дмитрий
Здравствуйте. Чуть меньше месяца назад мне вырвали нижнюю шестерку. После удаления выполнял все предписания врача, заживление проходило нормально, хотя и довольно медленно, ко вчерашнему дню края лунки сблизились, а внутри ее заполняла субстанция беловатого цвета — как я понял, грануляционная ткань.
Сегодня создалось впечатление, что я ее случайно выполоскал или случилось что-то еще — в любом случае, беловатого образования в лунке больше нет, а пространство, которое оно заполняло, теперь пустует. Обратиться к хирургу на данный момент нет возможности, а в интернете я нашел лишь информацию о выполаскивании кровяного сгустка на ранних стадиях заживления.
Ответ доктора
Здравствуйте, Дмитрий!
Не переживайте, ничего страшного у вас не происходит. Грануляционную ткань вы не могли выполоскать ни при каких обстоятельствах. Скорее всего вы выполоскали гемостатическую губку, которой хирург после удаления заполнил лунку. Главный показатель нормального заживления лунки не длительность процесса, а отсутствие болевых ощущений. Если в лунке сохраняется «ямочка», просто после каждого приема пищи тщательно полощите, пока лунка полностью закроется.
С уважением, Нина Владимировна.
Наши клиники
Запишитесь на приём
Введите ваше имя*
Введите номер вашего телефона*Выберите клинику*
Выберите клиникуТимирязевскаяЩёлковскаяСлавянский бульвар
Нажимая на кнопку, вы даете согласие
на обработку своих персональных данных
Спасибо за доверие
Ваша заявка была успешно отправлена,
мы свяжемся с вами в ближайшее время
для подтверждения и уточнения деталей.
Вернуться на сайт
Выберите клинику
Цены на лечение в стоматологических клиниках Импладент различаются. Для ознакомления с прайс- листом необходимо выбрать интересующую Вас клинику.
Славянский бульвар Щёлковская Тимирязевская
Позвонить в клинику
Тимирязевская Щёлковская Славянский бульвар
Что такое гранулема зубов? — Статьи
Автор:
Marbery Gedrean| Проверил: Штеба Виктория Петровна | Последняя редакция: 01 ноября 2020.
Зубные гранулемы — это небольшие узелки в области зубов. Они состоят из воспалительных клеток, окруженных капсулой, которые образуют так называемую грануляционную ткань. Грануляционная ткань обычно возникает как реакция на повреждающие воздействия, такие как воспаление, инфекции или аллергия.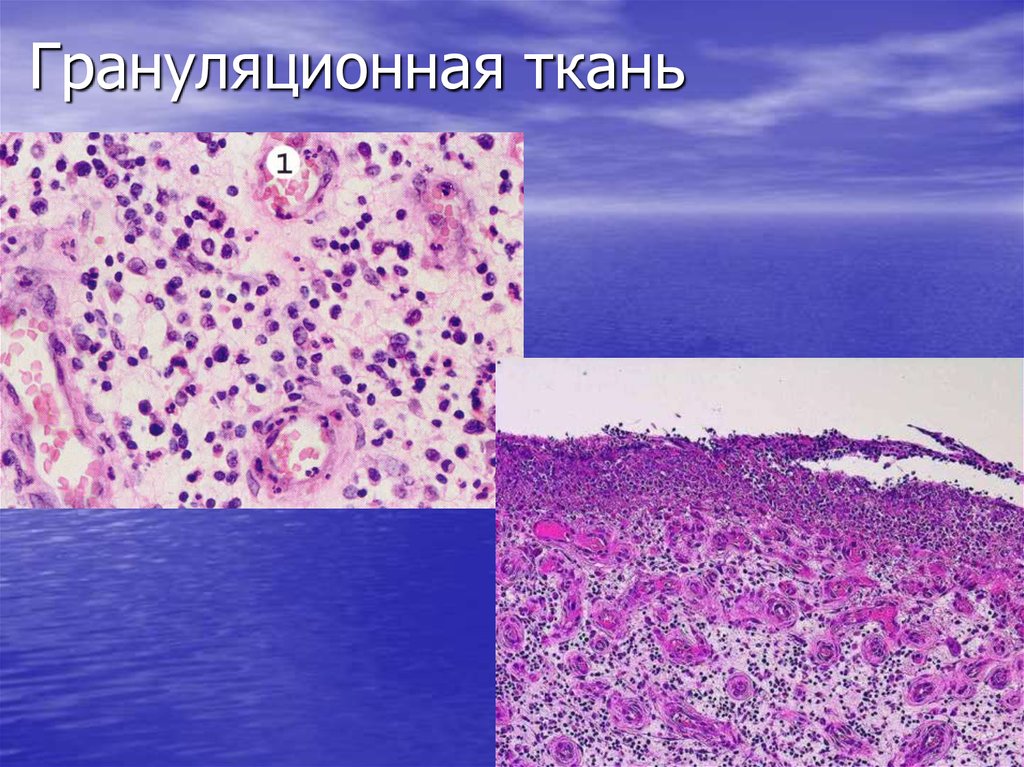
Гранулемы могут формироваться в различных областях зубочелюстной системы. Если они сохраняются и не лечатся своевременно, они могут повреждать окружающие ткани, вызывать некроз тканей и вызывать боль. Зубные гранулемы часто хорошо видны на рентгеновских снимках в виде теней в области кончика корня. Подробный диагноз может поставить только врач-стоматолог на основании симптомов и рентгенологического исследования.
Причины гранулемы зуба
В области зубов часто обнаруживаются эпулис, гранулема верхушки корня и гранулема инородного тела. Эпулис является опухолевидным образованием, которое располагается на линии десен и является реакцией ткани на воспаление, возникающее обычно в десневом кармане. Эпулис также могут вызвать и другие факторы, например длительное механическое раздражение пломбами, коронками или протезами.
При гранулеме верхушки корня воспаление изнутри зуба распространяется на область корня и прилегающую кость. Это создает так называемую грануляционную ткань, которая прикрепляется к верхушке корня в сферической форме и образует капсулу из соединительной ткани.
Это создает так называемую грануляционную ткань, которая прикрепляется к верхушке корня в сферической форме и образует капсулу из соединительной ткани.
Причины гранулем зубов разнообразны и могут включать воспаление зубных нервов или образование десневых карманов с сопутствующим воспалением. Помимо гранулемы верхушки корня, существует также гранулема инородного тела, в которую проникло инородное тело и через какое-то время инкапсулируется. Форма гранулемы в области зубов обусловлена тем, что инородное тело проникает в ткань и вызывает там длительное воспаление. Типичными инородными телами могут быть, например, металлические частицы, древесная стружка или нить.
Лечение гранулемы зуба
При подозрении на гранулемы зубов стоматолог сначала спросит у пациента соответствующие жалобы. Гранулемы корня вызывают симптомы, типичные для воспаления в области зубов. В основном это выпуклости от розового до сине-красноватого цвета, а иногда и боль, которая может быть более или менее сильной. Некоторые гранулемы длительное время остаются безболезненными. При особой форме гранулемы на деснах появляются небольшие узелки, которые легко кровоточат.
Некоторые гранулемы длительное время остаются безболезненными. При особой форме гранулемы на деснах появляются небольшие узелки, которые легко кровоточат.
После сбора анамнеза врач осматривает ротовую полость. Стоматолог может легко увидеть невооруженным глазом кровоточащие гранулемы, такие как эпулис, и ощупать их во время обследования. Гранулемы кончика корня и инородного тела обычно видны только на рентгеновском снимке.
Для лечения гранулемы зуба обычно необходимо хирургическое вмешательство. Пациенту вводят местный анестетик и вырезают образовавшуюся опухоль. Если поражены также десна или корни зуба, необходимо обработать и их, чтобы воспаление или раздражение не могло распространиться снова. Частично может поразиться и костная ткань. Если это так, в большинстве случаев пораженная часть удаляется, чтобы не образовывались новые гранулемы. Важно, чтобы окружающие ткани также были удалены, потому что только в этом случае дальнейший прогноз заболевания будет позитивным. Если воспаление полностью не устранено, курс лечения следует повторить, иначе пациент будет и дальше испытывать болезненные ощущения. Кроме того, гранулемы зубов могут образовываться снова и снова и повреждать прилегающие ткани. Еще одна проблема — образование кист: они могут возникнуть в результате некачественно вылеченных гранулем зубов. Кисты могут повредить кости челюсти, что в худшем случае может привести к расшатыванию зуба. Важно начать терапию как можно раньше, чтобы воспаление не распространилось без необходимости и не повредило слишком много тканей.
Если воспаление полностью не устранено, курс лечения следует повторить, иначе пациент будет и дальше испытывать болезненные ощущения. Кроме того, гранулемы зубов могут образовываться снова и снова и повреждать прилегающие ткани. Еще одна проблема — образование кист: они могут возникнуть в результате некачественно вылеченных гранулем зубов. Кисты могут повредить кости челюсти, что в худшем случае может привести к расшатыванию зуба. Важно начать терапию как можно раньше, чтобы воспаление не распространилось без необходимости и не повредило слишком много тканей.
К сожалению, не существует способов предотвратить гранулемы зубов или предотвратить их развитие. Однако, хороший уход за зубами и гигиена полости рта, а также регулярные стоматологические осмотры у стоматолога, а также посещение врача-гигиениста могут предотвратить кариес и заболевания десен. Поскольку зубные гранулемы чаще возникают на воспаленных зубах, хорошая профилактика кариеса может одновременно предотвратить гранулемы зуба.
Физиология, грануляционная ткань — StatPearls
Введение
Грануляционная ткань является важным компонентом процесса заживления ран. Раны могут заживать первичным натяжением (края ран легко сближаются) и вторичным натяжением (края ран не сближаются). Матрица грануляционной ткани заполнит раны, заживающие вторичным натяжением. Этот тип ткани также присутствует в хронических ранах, которые возникают по разным причинам. В этой статье мы обсудим механизм заживления и восстановления ран, роль грануляционной ткани в этом процессе, патофизиологию, приводящую к хроническим ранам и персистирующей грануляционной ткани, а также клиническое значение грануляционной ткани.
Сотовый уровень
Грануляционная ткань считается сократительным органом, гистологически характеризующимся наличием и пролиферацией фибробластов, кератиноцитов, эндотелиальных клеток, новых тонкостенных капилляров и воспалительной клеточной инфильтрацией внеклеточного матрикса. Образование грануляционной ткани является сложным и требует сложного взаимодействия между типами клеток в месте раны.
Фибробласты
Этот тип клеток отвечает за формирование внеклеточного матрикса грануляционной ткани (ECM). ECM изначально состоит из коллагена III типа, который является быстро вырабатываемой и более слабой формой коллагена, который в конечном итоге заменяется более сильным коллагеном I типа в конце заживления ран и образования рубцов. TGF-β представляет собой фактор роста, продуцируемый как фибробластами, так и кератиноцитами в процессе заживления ран, и было показано, что он вызывает образование грануляционной ткани и дифференцировку миофибробластов.
Кератиноциты
Кератиноциты отвечают за реэпителизацию эпидермиса после повреждения. Способность кератиноцитов к дифференцировке и пролиферации зависит от популяции стволовых клеток в месте раны и стимуляции различными цитокинами и факторами роста (эпидермальный фактор роста, TGF-α и KGF: фактор роста кератиноцитов). Связывание между клетками между кератиноцитами ослабевает во время процесса заживления раны и становится сильнее по его завершению. Сразу после повреждения кератиноциты, прилегающие к ране, подвергаются процессу активации, который изменяет экспрессию генов и способствует их миграции по ложу раны.
Сразу после повреждения кератиноциты, прилегающие к ране, подвергаются процессу активации, который изменяет экспрессию генов и способствует их миграции по ложу раны.
Аутокринным и паракринным образом кератиноциты производят сигналы, которые регулируют активацию кератиноцитов и стимулируют другие типы клеток (фибробласты) во время закрытия раны. ИЛ-1 увеличивает миграцию и пролиферацию кератиноцитов, активирует близлежащие фибробласты, увеличивает KGF (фактор роста кератиноцитов). TNF-α действует аналогично IL-1 и активирует путь FGF (фактор роста фибробластов). TGF-β, продуцируемый кератиноцитами и фибробластами, воздействует на возвращение кератиноцитов к их базально-клеточному фенотипу. Этот сигнальный процесс недостаточен при венозных язвах и способствует незаживлению.
Эндотелиальные клетки
Эндотелиальные клетки ответственны за реваскуляризацию/ангиогенез в месте раны. Первоначально находящиеся в состоянии покоя, резидентные эндотелиальные клетки активируются несколькими ангиогенными факторами, включая фактор роста фибробластов, фактор роста эндотелия сосудов (VEGF), фактор роста тромбоцитов (PDGF), ангиогенин и трансформирующие факторы роста α и β (TGFα и TGFβ). . После активации эндотелиальные клетки претерпевают четыре этапа образования новых кровеносных сосудов:
. После активации эндотелиальные клетки претерпевают четыре этапа образования новых кровеносных сосудов:
-
Продукция протеазы: распад внеклеточного матрикса
-
Хемотаксис
-
Пролиферация
-
Ремоделирование и дифференцировка, которые требуют ангиогенеза
4 4 4 эндотелиальные клетки быстро прорастают в новую ткань из старых неповрежденных кровеносных сосудов, разветвляются и образуют анастомозы с другими сосудами и восстанавливают кровоток. Этот процесс важен для восстановления притока питательных веществ и кислорода к участку, удаления отходов и транспортировки лейкоцитов к участку. Без этого образование грануляционной ткани задерживалось бы, а заживление раны затягивалось бы.Миофибробласты
Миофибробласты отвечают за сократительный процесс при закрытии раны. Когда формируется грануляционная ткань, фибробласты медленно модулируются в миофибробласты, характеризующиеся пучками актиновых микрофиламентов вдоль клеточной плазматической мембраны.
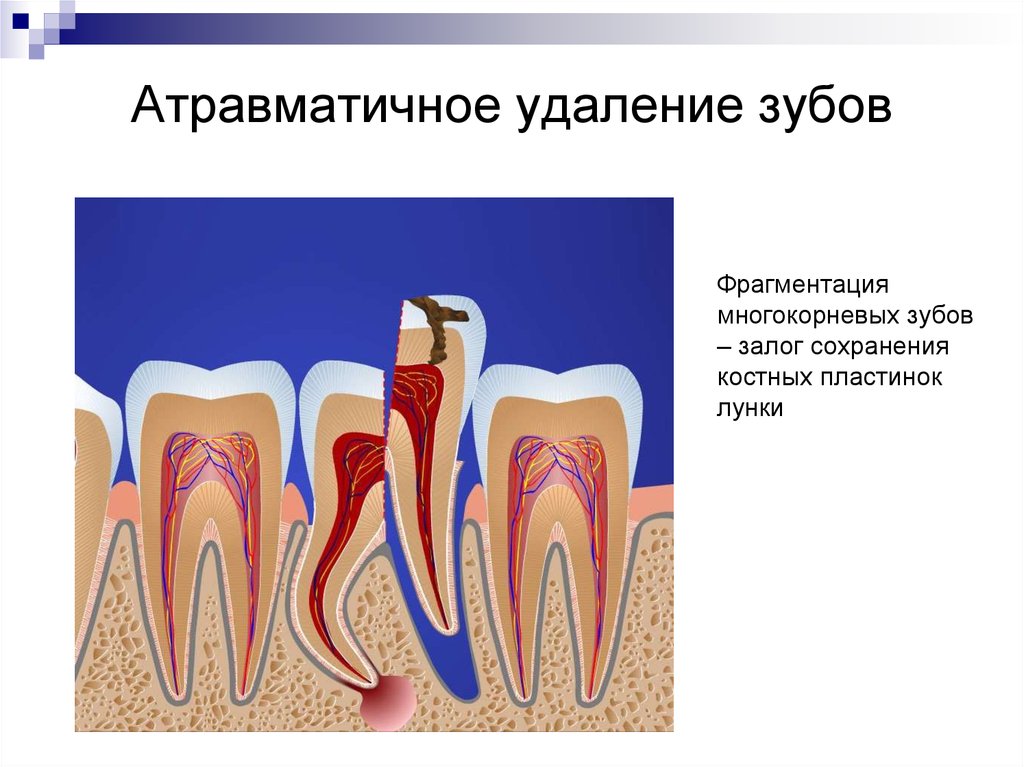
Иммунные клетки
Нейтрофилы (первые в ране) и макрофаги являются первичными иммунными клетками в месте раны, которые способствуют заживлению ран и защищают от вторжения патогенов. Оба типа клеток являются фагоцитарными, что означает, что они поглощают и проглатывают патогены, остатки и поврежденные ткани, обеспечивая защиту и заживление.
Функция
Грануляционная ткань — это тип новой соединительной ткани, а микроскопические кровеносные сосуды выполняют три основные функции.
-
Иммунный: Защищает раневую поверхность от микробной инвазии и дальнейшего повреждения.
-
Пролиферативный: Заполняет рану от основания новой тканью и сосудами.

-
Временная заглушка: Заменяет некротизированную ткань до ее замещения рубцовой тканью.[1][2]
Механизм
Процесс заживления ран сильно различается при сравнении плодов и взрослых. Заживление ран плода обычно характеризуется минимальным рубцеванием или отсутствием рубцевания, незначительным воспалением или его отсутствием (считается, что это связано с отсутствием миофибробластов), быстрой эпителизацией, высоким содержанием коллагена III типа, быстрой миграцией фибробластов и меньшей дегрануляцией фибробластами.
В нормальных условиях у взрослых заживление ран и восстановление тканей происходит в четыре стадии:
-
Гемостаз (образование струпа)
-
Воспалительная стадия (воспаление и образование отека)
Пролиферативная стадия (Формирование грануляционной ткани)
-
Стадия ремоделирования (Формирование рубца)
Гемостаз
На этом этапе заживления раны кровеносные сосуды в месте повреждения сужаются, и вытекающая через раны кровь начинает свертываться и покрываться коркой.
 Процесс коагуляции происходит в результате агрегации тромбоцитов, образующих фибриновую сеть. Фибриновая сеть является основой тромба и служит временной матрицей для мигрирующих клеток. Тромбоциты высвобождают цитокины и факторы роста, которые служат провоспалительными сигналами для привлечения иммунного ответа к месту раны.
Процесс коагуляции происходит в результате агрегации тромбоцитов, образующих фибриновую сеть. Фибриновая сеть является основой тромба и служит временной матрицей для мигрирующих клеток. Тромбоциты высвобождают цитокины и факторы роста, которые служат провоспалительными сигналами для привлечения иммунного ответа к месту раны. Стадия воспаления
Эта стадия начинается, когда нейтрофилы начинают прибывать к месту раны. Нейтрофилы достигают раны в течение нескольких минут и продолжают накапливаться в течение нескольких дней. Роль нейтрофилов заключается в улавливании микроорганизмов, присутствующих в месте раны с самого начала травмы. Нейтрофилы также усиливают провоспалительную реакцию и выделяют свои собственные маркеры.
Моноциты прибывают к месту повреждения в течение двух дней, где дифференцируются в макрофаги. Роль макрофагов заключается в фагоцитозе дебриса, патогенов и нейтрофилов, а также в производстве химических медиаторов (TGF-бета и VEGF), которые служат для рекрутирования фибробластов и эндотелиальных клеток, которые отмечают следующую стадию заживления.
 На этой стадии место повреждения становится гиперемированным и отечным. Этот этап занимает около 72 часов.
На этой стадии место повреждения становится гиперемированным и отечным. Этот этап занимает около 72 часов. Пролиферативная стадия
На этом этапе заживления одновременно происходит реэпителизация и замещение тромба грануляционной тканью. Эта стадия является высококлеточной с первичными типами клеток, включая фибробласты, кератиноциты и эндотелиальные клетки. Фибробласты синтезируют коллаген и внеклеточный матрикс. Сама грануляционная ткань состоит из внеклеточного матрикса, протеогликанов, гиалуроновой кислоты, коллагена и эластина. Цитокины и факторы роста, интерлейкины и факторы ангиогенеза активны в течение этого времени, которое в нормальных условиях может продолжаться от нескольких дней до недель. Грануляционная ткань растет от основания раны и обычно может заполнить рану любого размера. Любые ошибки в формировании грануляционной ткани могут привести к хроническому формированию раны. Инородные тела в месте раны также могут привести к персистирующей грануляционной ткани и плохому заживлению раны с избытком макрофагов, фибробластов и капилляров, реагирующих вокруг инородного материала.

Стадия реконструкции
Последняя стадия заживления ран включает апоптоз и производство новых клеток. Апоптоз и деградация внеклеточного матрикса и незрелого коллагена III типа, а также окончательное образование зрелого коллагена I типа имеют решающее значение для формирования, целостности и прочности рубца. Эта стадия может продолжаться от месяцев до лет. Если на этом этапе есть ошибки, может быть чрезмерное заживление раны, ведущее к гипертрофическому или келоидному рубцеванию, или хроническая рана, приводящая к стойкой грануляционной ткани.
Здоровая грануляционная ткань имеет цвет от розового до красного из-за образования новых капилляров, мягкая на ощупь, влажная, выглядит бугристой и, как правило, безболезненной. Нездоровая грануляционная ткань имеет темно-красный цвет, легко кровоточит при минимальном контакте, болезненна и может быть покрыта блестящей белой или желтой фиброзной тканью, лишенной сосудов, что препятствует заживлению. При появлении «нездоровой» грануляционной ткани следует заподозрить инфекционный процесс или плохое заживление.
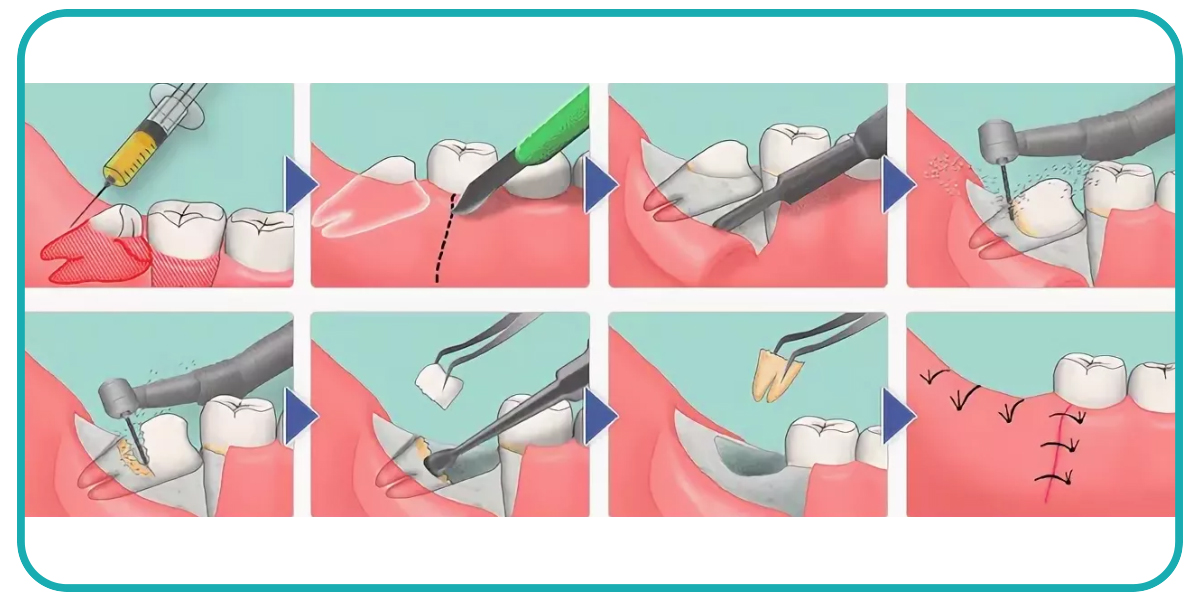 Посев раны и соответствующее лечение в соответствии с результатами посева должны быть завершены как можно скорее. Как только инфекция будет исключена или устранена, некоторые хронические раны могут реагировать на простое прижигание нитратом серебра или местными стероидными препаратами, в то время как раны с покрывающей фиброзной тканью потребуют обработки кюреткой или скальпелем, чтобы обеспечить заживление. 2][3][4][5][6][7]
Посев раны и соответствующее лечение в соответствии с результатами посева должны быть завершены как можно скорее. Как только инфекция будет исключена или устранена, некоторые хронические раны могут реагировать на простое прижигание нитратом серебра или местными стероидными препаратами, в то время как раны с покрывающей фиброзной тканью потребуют обработки кюреткой или скальпелем, чтобы обеспечить заживление. 2][3][4][5][6][7] Патофизиология
Заживление ран может затягиваться при некоторых обстоятельствах. Патофизиология заживления ран, приводящая к избыточной и нездоровой грануляционной ткани и хроническим ранам, сложна. Причины могут включать инфекцию в месте раны, приводящую к чрезмерному набору воспалительных клеток. Инфекции приводят к повышенному высвобождению активных форм кислорода, которые повреждают ткани, а также могут приводить к образованию биопленок, которые способствуют плохому заживлению ран и вызываются бактериальными токсинами. Инфекции могут привести к дальнейшим осложнениям, включая абсцесс, флегмону, остеомиелит и потерю конечностей.

Некроз, плохая перфузия и плохое питание/обмен веществ из-за недостаточного кровоснабжения из-за самой травмы, плохого ангиогенеза и основных состояний (диабет и сосудистая недостаточность) также являются источниками хронических ран и персистирующей грануляционной ткани. 2][3][4][8]
Клиническое значение
Грануляционная ткань может сохраняться при некоторых обстоятельствах в результате основных состояний и/или ошибок на стадиях заживления раны (ошибки в фазе пролиферации и фазе ремоделирования).[1][2][3][4] [6][9][8]
Возможные причины длительного заживления ран включают:
-
Сахарный диабет
-
Ревматоидный артрит
-
Сосудистая или артериальная недостаточность 9 1
5 Дефицит цинка
-
Низкий уровень гормона роста человека
-
Травма
-
Избыток влаги
-
Гипоксия
0005
-
Лекарства (стероиды, НПВП, химиотерапия)
-
Алкоголизм
-
Злоупотребление табаком
4 Возможные причины гипергрануляции 60
-
-
Раневая инфекция
-
Чрезмерное воспаление
-
Инородное тело/материал
-
Физическое раздражение/трение
-
Пиогенная гранулема
-
Полипы пульпы
-
Получите бесплатный доступ к вопросам с несколькими вариантами ответов по этой теме.
-
Комментарий к этой статье.
- 1.
-
Демидова-Райс Т.Н., Хэмблин М.Р., Герман И.М. Острое и нарушенное заживление ран: патофизиология и современные методы доставки лекарств, часть 1: нормальные и хронические раны: биология, причины и подходы к лечению. Уход за кожей Adv. 2012 июль; 25 (7): 304-14. [Бесплатная статья PMC: PMC3428147] [PubMed: 22713781]
- 2.
-
Guo S, Dipietro LA. Факторы, влияющие на заживление ран. Джей Дент Рез. 2010 март;89(3):219-29. [Бесплатная статья PMC: PMC2
6] [PubMed: 20139336] - 3.
-
Pastar I, Stojadinovic O, Yin NC, Ramirez H, Nusbaum AG, Sawaya A, Patel SB, Khalid L, Isseroff RR, Tomic-Canic M. Эпителизация раны Исцеление: всесторонний обзор. Adv Wound Care (Нью-Рошель). 2014 01 июля; 3 (7): 445-464. [Бесплатная статья PMC: PMC4086220] [PubMed: 25032064]
- 4.
-
Jaeger M, Harats M, Kornhaber R, Aviv U, Zerach A, Haik J. Лечение гипергрануляционной ткани в ожоговых ранах местными стероидными повязками: серия кейсов.
 Представитель Int Med Case J. 2016; 9: 241-5. [Бесплатная статья PMC: PMC4986970] [PubMed: 27570466]
Представитель Int Med Case J. 2016; 9: 241-5. [Бесплатная статья PMC: PMC4986970] [PubMed: 27570466] - 5.
-
Дрейфке М.Б., Джаясурия А.А., Джаясурия А.С. Текущие процедуры заживления ран и потенциальный уход. Mater Sci Eng C Mater Biol Appl. 2015 март; 48: 651-62. [Бесплатная статья PMC: PMC4443476] [PubMed: 25579968]
- 6.
-
Hiremath R, Reddy H, Ibrahim J, Harita CH, Shah RS. Инородное тело мягких тканей: полезность УЗИ высокого разрешения. J Clin Diagn Res. 2017 июль;11(7):TC14-TC16. [Бесплатная статья PMC: PMC5583796] [PubMed: 28892999]
- 7.
-
Mo Y, Sarojini H, Wan R, Zhang Q, Wang J, Eichenberger S, Kotwal GJ, Chien S. Внутриклеточная доставка АТФ вызывает быструю регенерацию тканей через активацию цитокинов, хемокинов и стволовых клеток. Фронт Фармакол. 2019;10:1502. [Бесплатная статья PMC: PMC6976531] [PubMed: 32009945]
- 8.
-
Li X, Kim J, Wu J, Ahamed AI, Wang Y, Martins-Green M.
 N — Ацетилцистеин и задействованные механизмы в разрешении хронической раневой биопленки. J Диабет Res. 2020;2020:9589507. [Бесплатная статья PMC: PMC7007959] [PubMed: 32083136]
N — Ацетилцистеин и задействованные механизмы в разрешении хронической раневой биопленки. J Диабет Res. 2020;2020:9589507. [Бесплатная статья PMC: PMC7007959] [PubMed: 32083136] - 9.
-
Livingstone D, Alghonaim Y, Jowett N, Sela E, Mlynarek A, Forghani R. Нитрат серебра, имитирующий инородное тело в слизистой оболочке глотки космос. Мир J Радиол. 2015 28 мая; 7(5):100-3. [Бесплатная статья PMC: PMC4444602] [PubMed: 26029352]
- Список журналов
- Деловой представитель Дент
- v.2016; 2016
- PMC5078642
Грануляционная ткань также может присутствовать в:
Контрольные вопросы
Рис.
Изъязвление венозного застоя в классической нижней медиальной части голени (область голени). Обратите внимание на типичные признаки неглубокого основания раны, неровных краев, здоровой красной грануляционной ткани и окружающего липодерматосклероза. Предоставлено Марком А. Дрейером, DPM, FACFAS (подробнее…)
Рисунок
Пиогенная гранулема H/E 10x. Дольковая морфология изменена вторичными изъязвлениями и воспалительными изменениями. На этой картине эпидермис изъязвлен, а нейтрофилы широко занимают очаг поражения. Над истинной грануляцией имеется эпидермальный воротничок (подробнее…)
Рисунок
Грануляционная ткань, H/E, 20x. На этом изображении истинная грануляционная ткань формируется в ранее существовавшей пиогенной гранулеме/ангиоме. Дольковая морфология пиогенной гранулемы может быть скрыта изъязвлениями и воспалительными изменениями. Предоставлено Фабиолой Фарчи, (подробнее. ..)
..)
Ссылки
Лечение неустойчивой экстракционной лунки для имплантационной терапии у пациента с хроническим пародонтитом
Являясь библиотекой, NLM предоставляет доступ к научной литературе. Включение в базу данных NLM не означает одобрения или согласия с
содержание NLM или Национальных институтов здравоохранения.
Узнайте больше о нашем отказе от ответственности.
Включение в базу данных NLM не означает одобрения или согласия с
содержание NLM или Национальных институтов здравоохранения.
Узнайте больше о нашем отказе от ответственности.
Дело Представитель Вмятина. 2016; 2016: 1746961.
Опубликовано в Интернете 11 октября 2016 г. doi: 10.1155/2016/1746961
, * , и
Информация об авторе Примечания к статье Информация об авторских правах и лицензиях Отказ от ответственности
Поскольку имплантация становится все более распространенной в повседневной практике, сохранение и подготовка беззубых участков имеют ключевое значение. Однако во многих случаях имплантационная терапия может не рассматриваться во время удаления зуба, и не предпринимаются дополнительные меры для сохранения беззубого участка. Несмотря на то, что процесс заживления лунок после удаления хорошо изучен, и можно ожидать заполнения костной ткани, бывают случаи, когда даже при тщательной обработке лунок клиницистами может происходить инфильтрация соединительной ткани в лунки. Это явление, известное как «неустойчивое заживление», может быть связано с факторами, которые приводят к периимплантатному заболеванию, и его следует надлежащим образом контролировать и лечить до хирургической установки имплантата. В этом клиническом случае описывается успешное лечение нестабильного заживления лунки при удалении у 62-летнего пациента европеоидной расы с хроническим пародонтитом и результаты доказательного протокола лечения, проведенного до имплантации. Тщательный предоперационный анализ и конусно-лучевая компьютерная томография могут помочь обнаружить признаки нарушения заживления в будущих местах имплантации и предотвратить хирургические осложнения.
Это явление, известное как «неустойчивое заживление», может быть связано с факторами, которые приводят к периимплантатному заболеванию, и его следует надлежащим образом контролировать и лечить до хирургической установки имплантата. В этом клиническом случае описывается успешное лечение нестабильного заживления лунки при удалении у 62-летнего пациента европеоидной расы с хроническим пародонтитом и результаты доказательного протокола лечения, проведенного до имплантации. Тщательный предоперационный анализ и конусно-лучевая компьютерная томография могут помочь обнаружить признаки нарушения заживления в будущих местах имплантации и предотвратить хирургические осложнения.
За последнее десятилетие оральная реабилитация пациентов с полной или частичной адентией с помощью зубных имплантатов стала рутинной в повседневной клинической практике. Имплантаты помещаются либо в лунки после удаления зубов, либо в лунки после пересадки и заживления, либо в полностью зажившую нативную кость. Характеристики и прогрессирование заживления лунок после экстракции широко изучались на животных моделях и в клинических испытаниях на людях [1–3].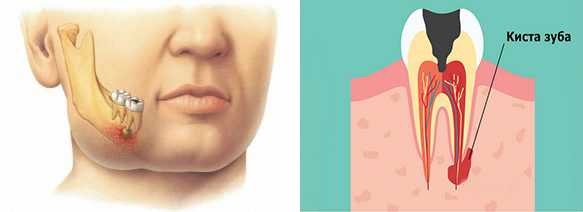 Эти исследования включали клинические и рентгенологические изменения размеров, а также гистологический анализ [4]. В систематическом обзоре существующей литературы оценивалась величина размерных изменений твердых и мягких тканей альвеолярного отростка до 12 месяцев после удаления зубов у человека. Результаты исследований повторного входа человека показывают, что 29-63% потери горизонтальной кости и 11-22% вертикальной потери кости происходят через 6 месяцев после удаления зуба [5]. Текущие данные показывают, что лечение для сохранения альвеолярного гребня во время удаления может минимизировать степень уменьшения размера гребня [6, 7]. Не все пациенты рассматривают или планируют будущую имплантационную терапию во время удаления, поэтому они могут обойтись без процедуры сохранения альвеолярного гребня. В конечном итоге это может повлиять на изменение размеров гребня и процесс заживления после экстракции.
Эти исследования включали клинические и рентгенологические изменения размеров, а также гистологический анализ [4]. В систематическом обзоре существующей литературы оценивалась величина размерных изменений твердых и мягких тканей альвеолярного отростка до 12 месяцев после удаления зубов у человека. Результаты исследований повторного входа человека показывают, что 29-63% потери горизонтальной кости и 11-22% вертикальной потери кости происходят через 6 месяцев после удаления зуба [5]. Текущие данные показывают, что лечение для сохранения альвеолярного гребня во время удаления может минимизировать степень уменьшения размера гребня [6, 7]. Не все пациенты рассматривают или планируют будущую имплантационную терапию во время удаления, поэтому они могут обойтись без процедуры сохранения альвеолярного гребня. В конечном итоге это может повлиять на изменение размеров гребня и процесс заживления после экстракции.
Последовательность заживления клеток и тканей после удаления зуба у человека начинается с образования кровяного сгустка в лунке; затем сгусток замещается грануляционной тканью, после чего происходит формирование остеоида [1]. Гистологическая оценка участков экстракции в первую очередь проводилась на зубах без патологических признаков. В повседневной практике многие удаленные зубы связаны с периодонтом или эндодонтией или удалены у людей с ослабленным здоровьем. В некоторых случаях, даже когда хирурги проводят тщательную обработку лунок, может происходить инфильтрация соединительной ткани в лунки [8]. Некоторые сообщения показали, что бактериальное загрязнение во время установки имплантата и преждевременной нагрузки, микропереломы костей и наличие ранее существовавшего воспаления (бактерии, воспалительные клетки и/или оставшиеся клетки кисты или гранулемы) являются этиологическими факторами ретроградного периимплантита. Ретроградный периимплантит часто сопровождается симптомами боли, болезненности, отека и/или наличия свищевых ходов. Надлежащие методы лечения ретроградного периимплантита до сих пор неясны [9]., 10]. Ким и др. определил «неустойчивое заживление» как заживление, при котором фиброзная рубцовая ткань занимает место экстракции, а не кость после 12 или более недель заживления.
Гистологическая оценка участков экстракции в первую очередь проводилась на зубах без патологических признаков. В повседневной практике многие удаленные зубы связаны с периодонтом или эндодонтией или удалены у людей с ослабленным здоровьем. В некоторых случаях, даже когда хирурги проводят тщательную обработку лунок, может происходить инфильтрация соединительной ткани в лунки [8]. Некоторые сообщения показали, что бактериальное загрязнение во время установки имплантата и преждевременной нагрузки, микропереломы костей и наличие ранее существовавшего воспаления (бактерии, воспалительные клетки и/или оставшиеся клетки кисты или гранулемы) являются этиологическими факторами ретроградного периимплантита. Ретроградный периимплантит часто сопровождается симптомами боли, болезненности, отека и/или наличия свищевых ходов. Надлежащие методы лечения ретроградного периимплантита до сих пор неясны [9]., 10]. Ким и др. определил «неустойчивое заживление» как заживление, при котором фиброзная рубцовая ткань занимает место экстракции, а не кость после 12 или более недель заживления. Неравномерное заживление не является редким осложнением. В своем ретроспективном исследовании авторы показали, что у 5,71 % пациентов, подвергшихся удалению, 4,24 % участков удаления демонстрировали некоторую степень неустойчивого заживления [11]. Соответствующее лечение участков удаления с неравномерным заживлением необходимо до или одновременно с хирургической терапией имплантата для поддержания долгосрочной стабильности имплантата. Цель этой статьи — проиллюстрировать клинический случай и предложить основанный на доказательствах протокол лечения лунок с неравномерным заживлением до установки имплантата.
Неравномерное заживление не является редким осложнением. В своем ретроспективном исследовании авторы показали, что у 5,71 % пациентов, подвергшихся удалению, 4,24 % участков удаления демонстрировали некоторую степень неустойчивого заживления [11]. Соответствующее лечение участков удаления с неравномерным заживлением необходимо до или одновременно с хирургической терапией имплантата для поддержания долгосрочной стабильности имплантата. Цель этой статьи — проиллюстрировать клинический случай и предложить основанный на доказательствах протокол лечения лунок с неравномерным заживлением до установки имплантата.
62-летний мужчина европеоидной расы был направлен в клинику последипломной пародонтологии Школы стоматологии Университета Индианы, Индианаполис, Индиана, США, из кабинета стоматолога общего профиля для лечения пародонта. Пациент сообщил о артериальной гипертензии, закупорке коронарных артерий с заменой стента в 2006 году, остеоартрите и гиперлипидемии. Клиническое обследование выявило увеличение глубины пародонтального зондирования до 6 мм на боковых зубах. Зуб № 30 ранее был удален из-за комбинированного пародонто-эндодонтического поражения (). При рентгенологическом исследовании выявлена горизонтальная потеря костной массы на боковых зубах. Пародонтологический диагноз: генерализованный хронический пародонтит легкой степени с локализованным хроническим пародонтитом средней степени тяжести, ассоциированным с зубами № 2, 3, 14, 15, 18 и 19.[12]. Гигиена полости рта пациентки оценивалась как приемлемая. При первом посещении был зарегистрирован показатель бляшек по О’Лири, равный 29%. Пациенту объяснили возможные лечебные вмешательства при пародонтите и адентическом альвеолярном гребне №30. Они включали (1) инструкции по гигиене полости рта, (2) нехирургическую пародонтальную терапию, (3) хирургическое вмешательство (резективное костное лечение) вокруг жевательных зубов и, после хорошего контроля состояния пародонта пациента, (4) замену № 30 на зуб. реставрация зубов с опорой на имплантаты. Цель противоинфекционной терапии (нехирургическая терапия) состояла в том, чтобы уменьшить бактериальную нагрузку и воспаление.
Зуб № 30 ранее был удален из-за комбинированного пародонто-эндодонтического поражения (). При рентгенологическом исследовании выявлена горизонтальная потеря костной массы на боковых зубах. Пародонтологический диагноз: генерализованный хронический пародонтит легкой степени с локализованным хроническим пародонтитом средней степени тяжести, ассоциированным с зубами № 2, 3, 14, 15, 18 и 19.[12]. Гигиена полости рта пациентки оценивалась как приемлемая. При первом посещении был зарегистрирован показатель бляшек по О’Лири, равный 29%. Пациенту объяснили возможные лечебные вмешательства при пародонтите и адентическом альвеолярном гребне №30. Они включали (1) инструкции по гигиене полости рта, (2) нехирургическую пародонтальную терапию, (3) хирургическое вмешательство (резективное костное лечение) вокруг жевательных зубов и, после хорошего контроля состояния пародонта пациента, (4) замену № 30 на зуб. реставрация зубов с опорой на имплантаты. Цель противоинфекционной терапии (нехирургическая терапия) состояла в том, чтобы уменьшить бактериальную нагрузку и воспаление.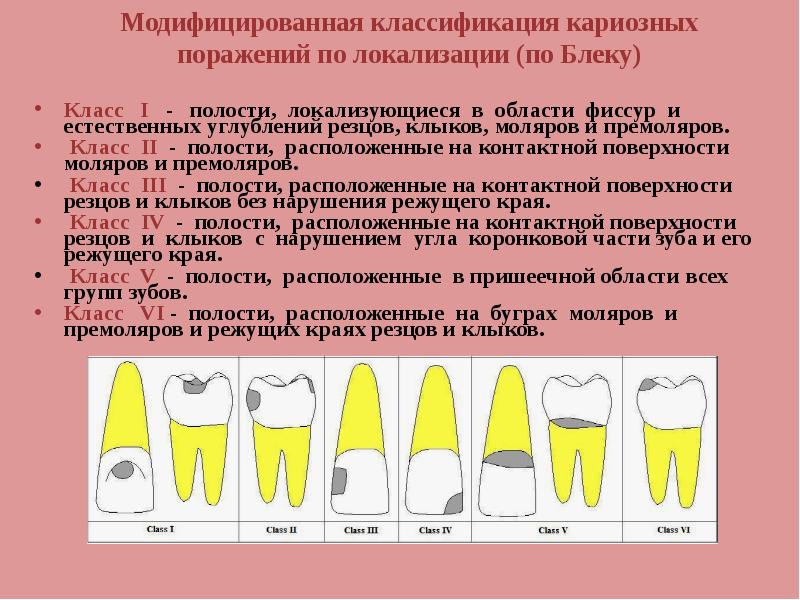 Пациент прошел сеанс пародонтологического обслуживания и получил индивидуальные инструкции по гигиене полости рта. Его гигиена полости рта улучшилась, и оценка налета О’Лири составила 9 баллов.% Было отмечено. Вскоре после визита к пародонтологу была проведена костная резекция в ВЛ, НЛ и ВП квадрантах для достижения меньшей глубины зондирования и улучшения состояния пародонта для задних зубов перед операцией по имплантации на № 30. Пациент решил продолжить имплантационную терапию для № 30 с помощью одиночной коронки с опорой на имплантаты ().
Пациент прошел сеанс пародонтологического обслуживания и получил индивидуальные инструкции по гигиене полости рта. Его гигиена полости рта улучшилась, и оценка налета О’Лири составила 9 баллов.% Было отмечено. Вскоре после визита к пародонтологу была проведена костная резекция в ВЛ, НЛ и ВП квадрантах для достижения меньшей глубины зондирования и улучшения состояния пародонта для задних зубов перед операцией по имплантации на № 30. Пациент решил продолжить имплантационную терапию для № 30 с помощью одиночной коронки с опорой на имплантаты ().
Открыть в отдельном окне
Панорамная рентгенограмма при первичном приеме (№ 30 был сделан направившим стоматологом).
Открыть в отдельном окне
Виды до операции: (а) внутриротовой; (б) периапикальная рентгенограмма.
В день установки имплантата № 30 проводилась инфильтрация 2% лидокаином с 1 : 100 000 адреналина. После крестального разреза над беззубым гребнем № 30 и внутрибороздковых разрезов вдоль дистальной поверхности № 29 и мезиальной поверхности № 31 был отогнут полнослойный лоскут. После отгиба лоскута была отмечена грануляционная ткань, заполняющая область гребня экстракционной лунки №30. Щечная и язычная стенки лунки интактны. Была предпринята попытка тщательной обработки. Получение доступа к дну дефекта было затруднено из-за сложности формы дефекта. Небольшое количество костного гребня было удалено с помощью высокоскоростного наконечника и круглых боров, что позволило хирургу получить доступ к вершине костного дефекта. Грануляционная ткань была удалена из лунки и отправлена на патологоанатомическое исследование для постановки формального диагноза. После тщательной промывки физиологическим раствором гидратированный лиофилизированный костный аллотрансплантат (FDBA: размер частиц 250 µ м–1000 µ м, Sunstar) трансплантировали в лунку и покрыли Bio-Gide (несшитая мембрана из свиного коллагена, Geistlich). Первичное закрытие раны было выполнено одиночными узловыми и горизонтальными матрацными швами с использованием шовного материала Cytoplast 4-0 (1).
После отгиба лоскута была отмечена грануляционная ткань, заполняющая область гребня экстракционной лунки №30. Щечная и язычная стенки лунки интактны. Была предпринята попытка тщательной обработки. Получение доступа к дну дефекта было затруднено из-за сложности формы дефекта. Небольшое количество костного гребня было удалено с помощью высокоскоростного наконечника и круглых боров, что позволило хирургу получить доступ к вершине костного дефекта. Грануляционная ткань была удалена из лунки и отправлена на патологоанатомическое исследование для постановки формального диагноза. После тщательной промывки физиологическим раствором гидратированный лиофилизированный костный аллотрансплантат (FDBA: размер частиц 250 µ м–1000 µ м, Sunstar) трансплантировали в лунку и покрыли Bio-Gide (несшитая мембрана из свиного коллагена, Geistlich). Первичное закрытие раны было выполнено одиночными узловыми и горизонтальными матрацными швами с использованием шовного материала Cytoplast 4-0 (1). Были даны послеоперационные инструкции, и пациенту был назначен амоксициллин по 500 мг три раза в день в течение 1 недели. Ему было рекомендовано полоскать рот по 30 секунд два раза в день 0,12% раствором хлоргексидина глюконата в течение 2 недель. Швы сняты через 2 недели после операции. Участок зажил без осложнений, и отчет о патологии показал, что образец ткани представлен отеком вместе с интенсивным лимфоплазмоцитарным инфильтратом. Основная часть образца состояла из плотных гиалинизированных минерализованных обломков. Диагноз: остаточная хронически воспаленная грануляционная ткань с фиброзной соединительной рубцовой тканью (4).
Были даны послеоперационные инструкции, и пациенту был назначен амоксициллин по 500 мг три раза в день в течение 1 недели. Ему было рекомендовано полоскать рот по 30 секунд два раза в день 0,12% раствором хлоргексидина глюконата в течение 2 недель. Швы сняты через 2 недели после операции. Участок зажил без осложнений, и отчет о патологии показал, что образец ткани представлен отеком вместе с интенсивным лимфоплазмоцитарным инфильтратом. Основная часть образца состояла из плотных гиалинизированных минерализованных обломков. Диагноз: остаточная хронически воспаленная грануляционная ткань с фиброзной соединительной рубцовой тканью (4).
Открыть в отдельном окне
Процедура направленной костной регенерации была проведена в месте неустойчивой экстракции (a–f). После поднятия полнослойного лоскута была отмечена грануляционная ткань, заполняющая ранее удаленный участок (а и б). После тщательной санации и ирригации участок был определен как сдерживаемый дефект (с). FDBA аккуратно уложили в лунку и покрыли несшитой коллагеновой мембраной (d и e). Полное первичное закрытие было достигнуто комбинацией горизонтального матраца и одиночных узловых швов (f).
Полное первичное закрытие было достигнуто комбинацией горизонтального матраца и одиночных узловых швов (f).
Открыть в отдельном окне
Извлеченный препарат и гистопатологическая картина (окраска H&E). Эластичная твердая грануляционная ткань размером примерно 5 × 5 × 3 мм была удалена из места неустойчивой экстракции (а). Фиброзная соединительная ткань с инфильтрацией воспалительными клетками (б).
Через пять месяцев после трансплантации была запланирована установка имплантата. Предоперационная периапикальная рентгенограмма показала увеличение плотности костной ткани в области № 30. После альвеолярного разреза и поднятия лоскута на всю толщину хирургический шаблон был установлен внутри ротовой полости и выполнена остеотомия в соответствии с инструкциями производителя. Мягких тканей и грануляционной ткани в месте остеотомии не обнаружено. Имплантат Zimmer 4,7 × 11,5 ( D × H ) был установлен с усилием введения 35 Н/см (). Устройство Osstell использовалось для измерения стабильности, а ISQ (коэффициент стабильности имплантата) 76 был измерен в буккальном и язычном положениях. Нежелательных явлений на этапе остеоинтеграции отмечено не было. Стоматолог-реставратор поставил индивидуальный абатмент и отлитую из золота коронку. Рентгенограмма и клинические признаки показали стабильность мягких и твердых тканей через год после установки коронки, без каких-либо симптомов или рентгенологических признаков ретроградного периимплантита (1).
Нежелательных явлений на этапе остеоинтеграции отмечено не было. Стоматолог-реставратор поставил индивидуальный абатмент и отлитую из золота коронку. Рентгенограмма и клинические признаки показали стабильность мягких и твердых тканей через год после установки коронки, без каких-либо симптомов или рентгенологических признаков ретроградного периимплантита (1).
Открыть в отдельном окне
Установка имплантата через пять месяцев после процедуры трансплантации. Неравномерно заживающее место удаления показало повышенную рентгеноконтрастность через пять месяцев после операции по пересадке кости (а). Костное заполнение было обнаружено на гребневой части участка (б). Имплантат был установлен в восстановительном положении (c).
Открыть в отдельном окне
Последующее наблюдение в течение года после установки коронки. Нет признаков воспаления или симптомов (а). Потеря альвеолярного гребня или типичный ретроградный периимплантит не были отмечены на периапикальной рентгенограмме (b).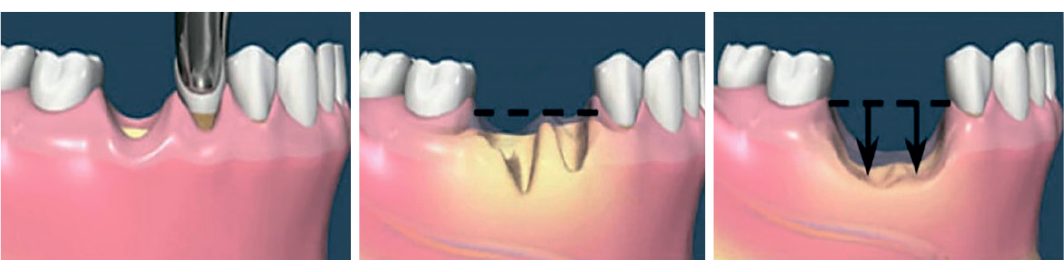
Наблюдения за рентгенопрозрачностью и наличием фиброзной рубцовой ткани, занимающей лунку после удаления, а не кость, исключали установку зубного имплантата в этом месте. Ретроспективное исследование с помощью компьютерной томографии выявило факторы, потенциально препятствующие заживлению в местах после удаления. Это исследование показало, что резцы/клыки верхней челюсти демонстрируют наименьшую распространенность неравномерного заживления, в то время как области моляров нижней челюсти имеют самую высокую распространенность. Результаты многопараметрического анализа показали, что неравномерное заживление с большей вероятностью возникало у пациентов моложе 60 лет (ОШ = 2,23), у пациентов с гипертонией (ОШ = 2,37), в области моляров (ОШ = 4,9).1) и места удаления одиночных зубов (ОШ = 2,98). Этот клинический случай соответствует всем этим условиям, кроме возраста [11].
В данном клиническом случае щечная и язычная кости в месте экстракции у пациента были интактными, а их толщина с обеих сторон превышала 2 мм. Кроме того, беззубый участок был свободен от воспаления, что позволило хирургу добиться первичного закрытия. Первичное закрытие является одним из ключевых моментов, позволяющих добиться оптимальных результатов при направленной костной регенерации. Wang и Boyapati [13] описали эти основные биологические принципы как «PASS» для предсказуемой регенерации кости: «Первичное закрытие раны» для обеспечения бесперебойного и непрерывного заживления раны, «Ангиогенез» для обеспечения необходимого кровоснабжения и недифференцированных мезенхимальных клеток, «Поддержание пространства». для обеспечения достаточного пространства для врастания кости и «Стабильность раны», чтобы вызвать образование тромба и беспрепятственный процесс заживления. Этот случай удовлетворял этим четырем факторам во время процедуры трансплантации, поскольку форма дефекта была сдерживаемой, а здоровые мягкие ткани были доступны для покрытия дефекта. Тем не менее, почти в 85% неравномерно заживающих участков экстракции наблюдается потеря одной или обеих щечных и язычных стенок [11].
Кроме того, беззубый участок был свободен от воспаления, что позволило хирургу добиться первичного закрытия. Первичное закрытие является одним из ключевых моментов, позволяющих добиться оптимальных результатов при направленной костной регенерации. Wang и Boyapati [13] описали эти основные биологические принципы как «PASS» для предсказуемой регенерации кости: «Первичное закрытие раны» для обеспечения бесперебойного и непрерывного заживления раны, «Ангиогенез» для обеспечения необходимого кровоснабжения и недифференцированных мезенхимальных клеток, «Поддержание пространства». для обеспечения достаточного пространства для врастания кости и «Стабильность раны», чтобы вызвать образование тромба и беспрепятственный процесс заживления. Этот случай удовлетворял этим четырем факторам во время процедуры трансплантации, поскольку форма дефекта была сдерживаемой, а здоровые мягкие ткани были доступны для покрытия дефекта. Тем не менее, почти в 85% неравномерно заживающих участков экстракции наблюдается потеря одной или обеих щечных и язычных стенок [11]. Если дефект невозможно локализовать, трудно стабилизировать рану, и для предотвращения коллапса ткани может потребоваться более жесткая мембрана или фиксатор пространства, например мембрана, армированная титаном, или титановая сетка [14]. Кроме того, если дефект является неустранимым и требуется большое наращивание кости для развития места имплантации, предлагается размещение костного трансплантата с медленной скоростью резорбции (Deproteinized Bovine Bone Minerals, DBBM и т. д.) и применение факторов роста. . Невинс и др. использовали рекомбинантный фактор роста тромбоцитов человека BB (rh-PDGF-BB) для регенерации больших участков альвеолярной экстракции с помощью палаточных винтов, DBBM и коллагеновых мембран [15]. В этой серии случаев было обработано восемь участков, и все участки успешно зажили с признаками костеподобной твердой ткани, которая была подтверждена гистологически как живая кость вокруг оставшихся частиц трансплантата.
Если дефект невозможно локализовать, трудно стабилизировать рану, и для предотвращения коллапса ткани может потребоваться более жесткая мембрана или фиксатор пространства, например мембрана, армированная титаном, или титановая сетка [14]. Кроме того, если дефект является неустранимым и требуется большое наращивание кости для развития места имплантации, предлагается размещение костного трансплантата с медленной скоростью резорбции (Deproteinized Bovine Bone Minerals, DBBM и т. д.) и применение факторов роста. . Невинс и др. использовали рекомбинантный фактор роста тромбоцитов человека BB (rh-PDGF-BB) для регенерации больших участков альвеолярной экстракции с помощью палаточных винтов, DBBM и коллагеновых мембран [15]. В этой серии случаев было обработано восемь участков, и все участки успешно зажили с признаками костеподобной твердой ткани, которая была подтверждена гистологически как живая кость вокруг оставшихся частиц трансплантата.
Поскольку неравномерное заживление места экстракции в этом клиническом случае показало достаточный размер щечно-язычного гребня для установки фиксатора имплантата, авторы планировали операцию по имплантации с использованием слепков и периапикальных рентгенограмм. Хирургический план неожиданно изменился во время первой операции. Клиническое обнаружение грануляций и рубцовой ткани в экстракционной лунке было объяснено пациенту во время операции, и план операции был изменен. Однако следует провести более тщательное предоперационное обследование, включая конусно-лучевую компьютерную томографию (КЛКТ), чтобы свести к минимуму риск изменения хирургического плана. Обнаружение неравномерно заживающих экстракционных повреждений до операции полезно как для пациентов, так и для хирургов, чтобы обсудить и создать комплексный план лечения, который включает продолжительность и стоимость необходимого лечения. Американская академия челюстно-лицевой радиологии (AAOMR) опубликовала заявление о позиции в отношении КЛКТ в дентальной имплантологии. AAOMR рекомендует использовать визуализацию поперечных сечений для оценки всех мест установки зубных имплантатов и использовать КЛКТ в качестве предпочтительного метода визуализации для получения этой информации [16]. Решение о проведении КЛКТ-обследования должно быть клинически обосновано и основываться на профессиональном суждении (т.
Хирургический план неожиданно изменился во время первой операции. Клиническое обнаружение грануляций и рубцовой ткани в экстракционной лунке было объяснено пациенту во время операции, и план операции был изменен. Однако следует провести более тщательное предоперационное обследование, включая конусно-лучевую компьютерную томографию (КЛКТ), чтобы свести к минимуму риск изменения хирургического плана. Обнаружение неравномерно заживающих экстракционных повреждений до операции полезно как для пациентов, так и для хирургов, чтобы обсудить и создать комплексный план лечения, который включает продолжительность и стоимость необходимого лечения. Американская академия челюстно-лицевой радиологии (AAOMR) опубликовала заявление о позиции в отношении КЛКТ в дентальной имплантологии. AAOMR рекомендует использовать визуализацию поперечных сечений для оценки всех мест установки зубных имплантатов и использовать КЛКТ в качестве предпочтительного метода визуализации для получения этой информации [16]. Решение о проведении КЛКТ-обследования должно быть клинически обосновано и основываться на профессиональном суждении (т. е. мнение врача о том, что КЛКТ-изображение потенциально может предоставить информацию, необходимую для планирования ортопедического лечения, выбора имплантата и/или хирургической установки).
е. мнение врача о том, что КЛКТ-изображение потенциально может предоставить информацию, необходимую для планирования ортопедического лечения, выбора имплантата и/или хирургической установки).
В этом клиническом случае показано успешное лечение неравномерного заживления места удаления с помощью направленной костной регенерации. Эта терапия привела к оральной реабилитации беззубого участка с помощью реставрации с опорой на дентальный имплантат без каких-либо осложнений в течение одного года после установки протеза. Поврежденные участки экстракции можно лечить адекватно, если соблюдаются основные принципы биологии, такие как принципы «PASS». Тем не менее, дополнительный рентгенографический анализ с КЛКТ для выявления поражения до вскрытия хирургического лоскута очень полезен для диагностики и планирования лечения.
Авторы хотели бы поблагодарить доктора Сьюзан Зант (профессора и заведующего кафедрой патологии полости рта, медицины и радиологии Школы стоматологии Университета Индианы) за предоставление диагноза патологии полости рта и фотографий гистопатологических изображений.
Авторы заявляют об отсутствии конкурирующих интересов, связанных с данным исследованием.
1. Амлер М.Х. Временная последовательность регенерации тканей при экстракционных ранах человека. Хирургия полости рта, медицина полости рта, патология полости рта . 1969; 27(3):309–318. doi: 10.1016/0030-4220(69)
-0. [PubMed] [CrossRef] [Google Scholar]
2. Evian C.I., Rosenberg E.S., Coslet J.G., Corn H. Остеогенная активность кости, удаленной из заживающих экстракционных лунок у человека. Журнал пародонтологии . 1982;53(2):81–85. doi: 10.1902/jop.1982.53.2.81. [PubMed] [CrossRef] [Google Scholar]
3. Pietrokovski J., Massler M. Резорбция альвеолярного гребня после удаления зуба. Журнал ортопедической стоматологии . 1967; 17 (1): 21–27. дои: 10.1016/0022-3913(67)-7. [PubMed] [CrossRef] [Google Scholar]
4. Араужо М. Г., Линде Дж. Изменение размеров гребня после удаления зуба. Экспериментальное исследование на собаке. Журнал клинической пародонтологии . 2005;32(2):212–218. doi: 10.1111/j.1600-051X.2005.00642.x. [PubMed] [CrossRef] [Google Scholar]
Журнал клинической пародонтологии . 2005;32(2):212–218. doi: 10.1111/j.1600-051X.2005.00642.x. [PubMed] [CrossRef] [Google Scholar]
5. Tan W.L., Wong T.L.T., Wong M.C.M., Lang N.P. Систематический обзор изменений размеров твердых и мягких тканей альвеол после удаления у человека. Клинические исследования оральных имплантатов . 2012;23(приложение 5):1–21. doi: 10.1111/j.1600-0501.2011.02375.x. [PubMed] [CrossRef] [Google Scholar]
6. Horowitz R., Holtzclaw D., Rosen P. S. Обзор сохранения альвеолярного гребня после удаления зуба. Журнал доказательной стоматологической практики . 2012;12(3):149–160. doi: 10.1016/S1532-3382(12)70029-5. [PubMed] [CrossRef] [Google Scholar]
7. Horváth A., Mardas N., Mezzomo L.A., Needleman I.G., Donos N. Сохранение альвеолярного гребня. Систематический обзор. Клинические исследования полости рта . 2013;17(2):341–363. doi: 10.1007/s00784-012-0758-5. [PubMed] [CrossRef] [Google Scholar]
8. Hämmerle C. H. F., Chen S. T., Wilson T. G., Jr. Консенсусные заявления и рекомендуемые клинические процедуры в отношении размещения имплантатов в экстракционных лунках. Международный журнал оральных и челюстно-лицевых имплантатов . 2004; 19 (дополнение): 26–28. [PubMed] [Google Scholar]
Hämmerle C. H. F., Chen S. T., Wilson T. G., Jr. Консенсусные заявления и рекомендуемые клинические процедуры в отношении размещения имплантатов в экстракционных лунках. Международный журнал оральных и челюстно-лицевых имплантатов . 2004; 19 (дополнение): 26–28. [PubMed] [Google Scholar]
9. Романос Г. Э., Фроум С., Коста-Мартинс С., Мейтнер С., Тарнов Д. П. Периапикальные поражения имплантатов: этиология и варианты лечения. Журнал оральной имплантологии . 2011;37(1):53–63. doi: 10.1563/aaid-joi-d-09-00067. [PubMed] [CrossRef] [Google Scholar]
10. Quirynen M., Vogels R., Alsaadi G., Naert I., Jacobs R., Steenberghe D.V. Предрасполагающие состояния к ретроградному периимплантиту и рекомендации по лечению. Клинические исследования оральных имплантатов . 2005;16(5):599–608. doi: 10.1111/j.1600-0501.2005.01147.x. [PubMed] [CrossRef] [Google Scholar]
11. Kim J.-H., Susin C., Min J.-H., et al. Лунки удаления: факторы, препятствующие неустойчивому заживлению. Журнал клинической пародонтологии . 2014;41(1):80–85. doi: 10.1111/jcpe.12173. [PubMed] [CrossRef] [Google Scholar]
Журнал клинической пародонтологии . 2014;41(1):80–85. doi: 10.1111/jcpe.12173. [PubMed] [CrossRef] [Google Scholar]
12. Armitage G.C. Разработка системы классификации заболеваний и состояний пародонта. Анналы пародонтологии . 1999;4(1):1–6. doi: 10.1902/annals.1999.4.1.1. [PubMed] [CrossRef] [Google Scholar]
13. Ван Х.-Л., Бояпати Л. Принципы PASS для предсказуемой регенерации кости. Имплантационная стоматология . 2006;15(1):8–17. дои: 10.1097/01.id.0000204762.39826.0f. [PubMed] [CrossRef] [Google Scholar]
14. Урбан И. А., Лозада Дж. Л., Йованович С. А., Нагурски Х., Надь К. Вертикальное увеличение гребня с использованием армированных титаном мембран из плотного ПТФЭ и комбинации аутогенной кости и неорганический минерал, полученный из бычьей кости: проспективная серия случаев у 19 пациентов. Международный журнал оральных и челюстно-лицевых имплантатов . 2014;29(1):185–193. doi: 10.11607/jomi.3346. [PubMed] [CrossRef] [Академия Google]
15.
