Кандидоз (молочница) у детей — Детский врач Гречаниченко Елена Андреевна
Кандидоз у детей— грибковая инфекция, чаще вы слышите название этой инфекции в обиходе как молочница. В последнее время отмечается увеличение заболеваемости кандидозом (молочницей) у детей. Несмотря на разнообразие грибковых инфекций, чаще всего возбудитель кандидозов у детей — грибы рода Candida.
Поражается кожа, слизистая оболочка ротовой полости и желудочно-кишечного тракта, мочеполовой системы.
Родителям надо помнить, что грибковые микроорганизмы являются условно-патогенными, т.е. присутствуют в жизни наших детей всегда и лишь при определенных условиях, нарушении баланса микрофлоры, вызывают заболевание.
Кожа новорожденных карапузиков колонизируется (заселяется) различными микрорганизмами первые несколько недель. Формируются микробиомы, состав которых меняется под действием окружающих факторов( в том числе применение антибиотиков у детей).
Почему возникает кандидоз (молочница) у малышей первого года жизни?
- Нерациональный гигиенический режим: кожа малыша очень нежная, требует мягкой, чистой, натуральной (хлопчатобумажной) одежды и ее смены несколько раз в день.
 Ежедневное купание в теплой воде позволяет эффективно кожу очищать и увлажнять. При несоблюдении этих простых действий нарушается формирование здорового микробиома на коже малыша.
Ежедневное купание в теплой воде позволяет эффективно кожу очищать и увлажнять. При несоблюдении этих простых действий нарушается формирование здорового микробиома на коже малыша. - Перегревание ребенка ведет к усилению потовыделения и мацерации кожи в местах естественных складок. Т. е. одевать детей надо так, чтобы ребенок не мерз ,но и не потел, не перегревался.
Кроме того, у всех детей, независимо от возраста, при нарушении обмена веществ (сахарный диабет), заболеваниях крови и любых онкологических процессах, иммунодефицитных состояниях, частом и длительном применении гормональных или антибактериальных лекарств создаются предпосылки для активного роста грибковых микроорганизмов.
Чем старше ребенок и более зрелая иммунная система, тем меньше риск кандидоза.
Как проявляется кандидоз (молочница)?
Выделяют местный кандидоз.
- молочница ротоглотки — белые творожистые налеты во рту;
- кандидозный стоматит — покраснение, отек и болезненность слизистой ротовой полости с белыми налетами или без них ;
- слизистой наружных половых органов, что сопровождается зудом.

- кандидоз ногтей.
При иммунодефицитах, онкологических процессах, сахарном диабете кандидоз может быть системным: с поражением дыхательных путей, сердечно-сосудистой системы, суставов и даже с развитием менингита (воспаление мозговых оболочек).
Диагностика поверхностного кандидоза, как правило, не представляет сложности для врача.
Чем лечить кандидоз у детей?
На современном фармацевтическом рынке большой выбор противогрибковых средств для местного и системного применения.
В зависимости от возраста, основного диагноза, проявлений кандидоза врач назначает лечение.
Консультация детского врача, частного педиатра в г. Шостка
Если вы заметили у вашего малыша признаки кандидоза, вам нужен осмотр и консультация педиатра с назначение лечения. Вовремя поставленный диагноз может значительно ускорить выздоровление и не допустить осложнения инфекции.
В кабинете «Дитячий лікар» по адресу г. Шостка ул. Короленко, 39 я принимаю пациентов ежедневно.
Шостка ул. Короленко, 39 я принимаю пациентов ежедневно.
Если вам нужна срочная консультация педиатра — перед посещением доктора перезвоните по телефону, указанному на сайте.
Будьте здоровы!
Кандидозный дисбиоз кишечника у детей
Одним из наиболее широко обсуждаемых вопросов не только педиатрической гастроэнтерологии, но педиатрии в целом является вопрос кишечного дисбиоза. При этом мнения, высказываемые авторами, порой диаметрально противоположны: от полного неприятия не только термина, но понятия в целом [17] до разработки новых лечебных препаратов для лечения дисбиоза кишечника [4].
Подходы зарубежных ученых к понятию «дисбиоз» более определенны. Всеми признается возможность существования дисбиоза тонкой кишки, именуемого во всем мире синдромом избыточного роста бактерий, избыточного размножения бактерий или избыточного микробного обсеменения (bacterial overgrowth syndrome) [18, 21]. Этот термин общепринят, расшифрован, изучены причины его возникновения и механизмы развития.
Что же касается толстокишечного дисбиоза, то в Международной классификации болезней 10го пересмотра рубрика «дисбактериоз кишечника» отсутствует и клинические проявления, связываемые в нашем представлении с дисбиозом кишечника (периодические схваткообразные боли по ходу толстой кишки, метеоризм, расстройства стула со склонностью к поносу, запору или их чередование), расцениваются как проявления синдрома раздраженного кишечника (СРК). Тем не менее термин «дисбактериоз (дисбиоз) кишечника» широко используется в отечественной литературе и фактически является общепринятым [1, 8]. При этом целесообразно уточнить локализацию процесса — толстокишечный дисбиоз или дисбиоз толстой кишки.
Термин «дисбиоз» предпочтительнее термина «дисбактериоз». Дисбиоз — это состояние экосистемы (эубиоза), при котором имеет место нарушение функций всех ее компонентов: макроорганизма, его резидентной микрофлоры (причем не только бактерий, но и грибов рода Candida), среды их обитания, а также механизмов взаимодействия [6]. Поэтому в клинической практике целесообразно использовать термины «дисбиоз толстой кишки» и «дисбиоз тонкой кишки». Эти изменения в большинстве случаев вторичны; может быть и по этой причине ни один из терминов не отражен в МКБ10.
Поэтому в клинической практике целесообразно использовать термины «дисбиоз толстой кишки» и «дисбиоз тонкой кишки». Эти изменения в большинстве случаев вторичны; может быть и по этой причине ни один из терминов не отражен в МКБ10.
Дисбиоз кишечника на начальных этапах может не иметь четких кишечных проявлений, однако даже легкие степени кишечного дисбиоза, часто не имеющие клинического эквивалента, негативно сказываются на состоянии макроорганизма, снижая его общую резистентность и сопровождаясь метаболическими и пищеварительными дисфункциями [9, 10].
Кроме различных вариантов микробного толстокишечного дисбиоза, в последние годы все большее внимание привлекает к себе кандидозный дисбиоз [14, 20].
Кандидозный дисбиоз характеризуется увеличением представительства грибов рода Candida в составе микрофлоры кишечника на фоне устойчивого дефицита нормальной бактериальной флоры. Развитию кандидозного дисбиоза кишечника как варианта кандидоза слизистых оболочек способствуют широко распространенная практика применения антибактериальной терапии, создающая условия для уничтожения естественных конкурентов грибов — бактерий, а также увеличение числа пациентов с иммунодефицитными состояниями различного происхождения [12, 13].
Род Candida представляет собой дрожжевые грибы, родственные Ascomycetes, и включает разнообразные виды (Candida spp.), среди которых основное значение как возбудители кандидоза имеют: Candida albicans, Candida tropicalis, Candida parapsilosis, Candida glabrata, Candida dubliniensis, Candida lusitaniae, Candida krusei. Candida spp. представляют собой компонент микрофлоры, симбионтной для человека. У 10–25 % населения, не имеющих клинических признаков грибкового поражения, Candida spp. непостоянно выявляются в полости рта, у 65–80 % — в содержимом кишечника [13].
Термин «кандидоз» подразумевает патологический процесс, основу которого составляет избыточный рост Candida первично в желудочнокишечном тракте и вторично — в других областях — на слизистой оболочке гениталий, бронхов, в паренхиматозных органах [5].
Одним из важнейших факторов риска развития кандидоза кишечника у детей является антибиотикотерапия, особенно длительное применение препаратов широкого спектра действия. Это может приводить к нарушению равновесия в микробном биоценозе кишечника, вследствие чего возможно избыточное развитие кандидозной популяции. Существенную роль играет и несбалансированное нерациональное питание, особенно детей первого года жизни (дефицит в рационе белков, витаминов). В эксперименте на животных показано, что недостаточное поступление белка в организм сопровождается снижением фагоцитарной и бактерицидной активности макрофагального звена, незавершенным фагоцитозом и повышением проницаемости кишечного барьера для Candida albicans [5, 16].
Это может приводить к нарушению равновесия в микробном биоценозе кишечника, вследствие чего возможно избыточное развитие кандидозной популяции. Существенную роль играет и несбалансированное нерациональное питание, особенно детей первого года жизни (дефицит в рационе белков, витаминов). В эксперименте на животных показано, что недостаточное поступление белка в организм сопровождается снижением фагоцитарной и бактерицидной активности макрофагального звена, незавершенным фагоцитозом и повышением проницаемости кишечного барьера для Candida albicans [5, 16].
По современным представлениям, можно выделить два принципиально различных механизма патогенеза кандидоза органов пищеварения: инвазивный и неинвазивный кандидоз [11, 13].
Инвазивный кандидоз кишечника, связанный с трансформацией грибов в псевдомицелий и внедрением последнего в ткани кишечника, развивается у больных с глубокими иммунодефицитными состояниями вследствие основного заболевания.
Однако в практике педиатра чаще встречается неинвазивное поражение — дисбиоз кишечника с избыточным ростом Candida spp. В его основе лежит действие метаболитов грибов, резорбируемых в кишечнике при массивном росте последних в просвете кишки. Около 36 % всех дисбиозов кишечника протекает с избыточным интестинальным ростом Candida spp. [11, 12]. При кандидозном дисбиозе кишечника состояние больных, как правило, удовлетворительное. Симптомы заболевания характеризуются флатуленцией, умеренным абдоминальным дискомфортом, изменением консистенции кала и частоты стула (обычно кал кашицеобразный, чаще 2–3 раза в сутки), отмечаются признаки умеренной интоксикации и тенденция к обострению аллергических процессов.
В его основе лежит действие метаболитов грибов, резорбируемых в кишечнике при массивном росте последних в просвете кишки. Около 36 % всех дисбиозов кишечника протекает с избыточным интестинальным ростом Candida spp. [11, 12]. При кандидозном дисбиозе кишечника состояние больных, как правило, удовлетворительное. Симптомы заболевания характеризуются флатуленцией, умеренным абдоминальным дискомфортом, изменением консистенции кала и частоты стула (обычно кал кашицеобразный, чаще 2–3 раза в сутки), отмечаются признаки умеренной интоксикации и тенденция к обострению аллергических процессов.
Важно отметить, что кандидоз слизистых оболочек кишечника часто протекает как микстинфекция. Это происходит изза того, что дисбиоз (т.е. дефицит облигатных бифидобактерий и лактобацилл) создает условия для адгезии на слизистой оболочке кишечника не только дрожжеподобных грибов, но и условнопатогенной бактериобиоты. Так, частота микстинфекции при дисбиозе кишечника с повышенной пролиферацией грибов рода Candida составляет 63 %. При этом чаще обнаруживают ассоциацию со значительным количеством бактерий с так называемым протеолитическим основным путем метаболизма (условнопатогенными): Esherichia coli, Ristella spp., Clostridium perfringens
При этом чаще обнаруживают ассоциацию со значительным количеством бактерий с так называемым протеолитическим основным путем метаболизма (условнопатогенными): Esherichia coli, Ristella spp., Clostridium perfringens
Клинические варианты проявления роста микромицетов Candida spp. в кишечнике могут быть представлены следующим образом.
Кандидоносительство. Характеризуется транзиторностью, охватывает 60–80 % общей популяции.
Дисбактериоз кишечника с избыточным ростом Candida spp. Избыточное прогрессирование роста микромицетов в просвете кишечника на фоне дефицита нормобиоты. Факторы риска: терапия антибиотиками, острые кишечные инфекции, ферментные энтеропатии.
Кандидозный колит. Трансформация гриба в псевдомицелий и инвазия тканей кишечника на фоне цитопенического синдрома с развитием воспалительных изменений кишечной стенки разной степени тяжести.
Определенная роль кандидозного дисбиоза в патологии детского возраста подтверждена исследованиями, проведенными совместно кафедрой педиатрической гастроэнтерологии и нутрициологии Харьковской медицинской академии последипломного образования (проф. О.Ю. Белоусова) и бактериологической лабораторией (проф. Е.М. Савинова) Института вакцин и сывороток им. И.И. Мечникова НАМН Украины. Изучено состояние кишечного биоценоза у 134 больных с хроническим неспецифическим неязвенным колитом (ХННК). Диагноз заболевания устанавливался на основании ректороманоскопического исследования, выявившего у всех детей явления катарального или катаральнофолликулярного проктосигмоидита. У значительной части больных (86 %) диагноз ХННК подтверждался также результатами морфологического исследования — кафедра патологической анатомии ХМАПО (проф.
Исследования микробного пейзажа кишечника показали, что у всех 134 детей с ХННК имеют место те или иные нарушения кишечного биоценоза, которые носили преимущественно однонаправленный характер. Изменения кишечной микрофлоры при ХННК у детей представлены в табл. 1.
При анализе полученных данных прежде всего обращают на себя внимание количественные нарушения, характеризующиеся умеренным снижением количества бифидо и лактобактерий. Несмотря на относительно незначительное уменьшение облигатной микрофлоры, значение этого показателя нельзя недооценивать, т.к. снижение ферментативной активности бифидо и лактобактерий, а также сдвиг рН кишечника в щелочную сторону обусловливают торможение процессов утилизации организмом ребенка биологически активных веществ, усиление бродильных и гнилостных процессов. Нарушение колонизационной резистентности вызывает адгезию и колонизацию на слизистой оболочке кишечника патогенных и условнопатогенных бактерий и обусловливает поступление токсинов в кровь.
Кроме количественных, выявляются нарушения качественного состава микрофлоры. Прежде всего это касается изменения качественных свойств кишечной палочки: появление форм со сниженной ферментативной активностью и атипичных форм — лактозонегативной, гемолизирующей. Если принять во внимание, что штаммы E.сoli содержат достаточно широкий набор факторов патогенности — эндо, экзо и цитотоксинов, факторы адгезии и тому подобные, то недооценивать ее роль в развитии патологического процесса невозможно [2, 3].
Качественные изменения микрофлоры при ХННК у детей заключались также в появлении условнопатогенной микрофлоры (золотистый и гемолизирующий стафилококк, грибы рода Candida, протей), что свидетельствует об ослаблении защитных возможностей индигенной анаэробной микрофлоры. При этом не может не обращать на себя внимание значительное содержание грибов рода Candida в высокой концентрации.
Таким образом, выявленные изменения биоценоза кишечника свидетельствуют о значительных дисбиотических сдвигах у всех больных ХННК, причем нарушения носят не столько количественный, сколько качественный характер. Количественные изменения состоят в незначительном снижении индигенной микрофлоры, качественные — в снижении ее защитных свойств, росте кишечной палочки с измененными свойствами и условнопатогенной микрофлоры (прежде всего грибов рода Candida). Полученные данные дают основание полагать, что дисбиотические нарушения являются одним из важнейших звеньев формирования патологического процесса при ХННК у детей наряду с нарушениями нервной регуляции пищеварения и иммунологическими расстройствами, причем в ряде случаев именно дисбиоз кишечника может послужить пусковым механизмом патологического процесса, который можно представить следующим образом: дисбиоз ® нарушение слизеобразования ® изменение градиента пролиферации и дифференциации клеток ® изменение местного иммунитета ® развитие транзиторного иммунодефицита ® развитие воспалительного процесса, факторами риска которого являются: длительное течение заболевания, обильный рост условнопатогенных бактерий на фоне дефицита физиологической флоры, снижение местной защиты СО кишечника, угнетение системы местного иммунитета с активацией процесса перекисного окисления липидов.
Количественные изменения состоят в незначительном снижении индигенной микрофлоры, качественные — в снижении ее защитных свойств, росте кишечной палочки с измененными свойствами и условнопатогенной микрофлоры (прежде всего грибов рода Candida). Полученные данные дают основание полагать, что дисбиотические нарушения являются одним из важнейших звеньев формирования патологического процесса при ХННК у детей наряду с нарушениями нервной регуляции пищеварения и иммунологическими расстройствами, причем в ряде случаев именно дисбиоз кишечника может послужить пусковым механизмом патологического процесса, который можно представить следующим образом: дисбиоз ® нарушение слизеобразования ® изменение градиента пролиферации и дифференциации клеток ® изменение местного иммунитета ® развитие транзиторного иммунодефицита ® развитие воспалительного процесса, факторами риска которого являются: длительное течение заболевания, обильный рост условнопатогенных бактерий на фоне дефицита физиологической флоры, снижение местной защиты СО кишечника, угнетение системы местного иммунитета с активацией процесса перекисного окисления липидов. Несмотря на то, что в наших наблюдениях наличие грибов рода Candida не свидетельствует об их безусловной роли в развитии воспалительного процесса (ХННК) в кишечнике, тем не менее и отрицать эту роль не представляется возможным. Повидимому, в развитии воспаления принимает участие смешанная (бактериальная и грибковая) флора, но наличие кандидозного дисбиоза при ХННК тем не менее можно считать доказанным.
Несмотря на то, что в наших наблюдениях наличие грибов рода Candida не свидетельствует об их безусловной роли в развитии воспалительного процесса (ХННК) в кишечнике, тем не менее и отрицать эту роль не представляется возможным. Повидимому, в развитии воспаления принимает участие смешанная (бактериальная и грибковая) флора, но наличие кандидозного дисбиоза при ХННК тем не менее можно считать доказанным.
Вышеизложенное не только пополняет представления о механизмах формирования ХННК у детей, но и определяет необходимость комплексной терапии дисбиоза с учетом его особенностей в каждом конкретном случае заболевания. При диагностике неинвазивного кишечного кандидоза к биопсионному материалу для микологического исследования не прибегают, в качестве стандарта диагностики используют следующие критерии: рост свыше 1000 КОЕ/г Candida spp. при посеве кишечного содержимого, взятого в стерильных условиях, в сочетании с явлениями кишечной диспепсии и положительной клиниколабораторной динамикой при лечении антимикотическими препаратами [5]. К сожалению, правильный забор кишечного содержимого для культурального исследования технически сложен; широко распространенная в нашей стране методика посева кала на дисбактериоз не может служить опорой в оценке реального состава микрофлоры кишечника [13].
К сожалению, правильный забор кишечного содержимого для культурального исследования технически сложен; широко распространенная в нашей стране методика посева кала на дисбактериоз не может служить опорой в оценке реального состава микрофлоры кишечника [13].
В диагностике любой формы кандидоза органов пищеварения важно учитывать наличие у пациента предрасполагающих факторов риска. «Случайное» выявление кандидоза должно послужить стимулом к поиску такого фонового фактора. Важно помнить, что кандидоз может выступать в качестве ранней манифестации общих заболеваний, сопровождающихся развитием иммунодефицита [13]. В большинстве случаев диагнозу «дисбиоз кишечника» должен предшествовать диагноз основного «фонового» заболевания.
Неинвазивную форму кандидоза следует дифференцировать с широким спектром энтеритов и колитов другой этиологии. Косвенным свидетельством в пользу наличия кандидоза кишечника могут выступать внекишечные системные проявления кандидоза.
Обнаружение грибов рода Candida в большом количестве при бактериологическом анализе испражнений в сочетании с симптомом кишечной диспепсии, особенно при безуспешности антибактериальной терапии, может служить показанием для назначения пациенту антимикотических средств в сочетаниии с про и пребиотиками, способствующими восстановлению естественной антимикробной резистентности слизистой оболочки кишечника с целью предотвращения рецидивов дисбиоза [7, 12].
Во время лечения больным рекомендован пищевой рацион с ограничением простых углеводов (сахара, сладких фруктов и ягод, кондитерских изделий, меда, молока, яблок, винограда, белокочанной капусты, бобовых, сладких напитков). По показаниям допускается применение ферментных препаратов, энтеросорбентов, спазмолитиков, энтеросептиков. Назначаются антимикотические препараты, неадсорбирующиеся из просвета кишечника [5].
Лечение кандидозного дисбиоза кишечника не требует назначения резорбируемых имидоазоловых антимикотиков (флуконазол). Чаще всего для селективной деконтаминации кишечника от микромицетов рода Candida назначают нистатин и натамицин (пимафуцин) [5]. В отличие от имидазоловых антимикотиков, нистатин и натамицин (пимафуцин) практически не резорбируются в кишечнике, что обусловливает стабильно высокую их концентрацию именно в просвете кишечника. Самым частым нежелательным эффектом при назначении этих средств является раздражение слизистых оболочек и обусловленные этим тошнота и диарея.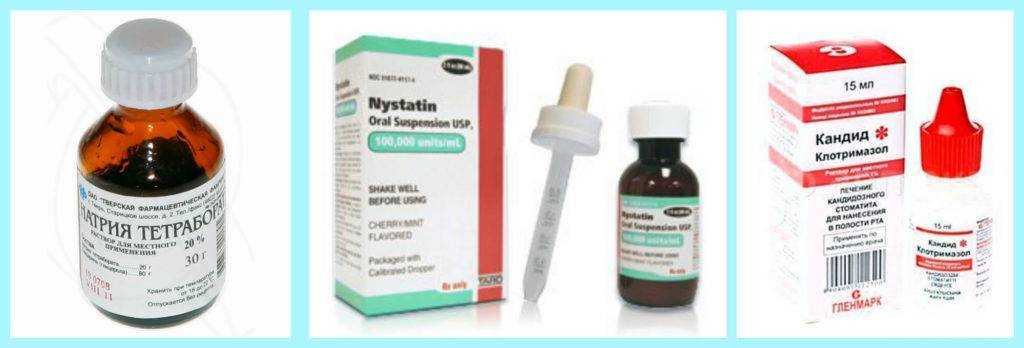 Необходимо отметить, что у пимафуцина эти явления выражены в меньшей степени, чем у нистатина. В отличие от нистатина натамицин (пимафуцин) разрешен для применения у беременных, кормящих, новорожденных, назначают препарат в таблетках взрослым по 100 мг четыре раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим средством длительностью 5–10 дней обычно приводят к элиминации дрожжеподобных грибов из кишечника, однако при сохранении факторов, снижающих эффективность местных антифунгальных барьеров, возможна реинфекция. Поэтому на фоне лечения кандидозного дисбиоза и после его окончания широко используются пре и пробиотики [19].
Необходимо отметить, что у пимафуцина эти явления выражены в меньшей степени, чем у нистатина. В отличие от нистатина натамицин (пимафуцин) разрешен для применения у беременных, кормящих, новорожденных, назначают препарат в таблетках взрослым по 100 мг четыре раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим средством длительностью 5–10 дней обычно приводят к элиминации дрожжеподобных грибов из кишечника, однако при сохранении факторов, снижающих эффективность местных антифунгальных барьеров, возможна реинфекция. Поэтому на фоне лечения кандидозного дисбиоза и после его окончания широко используются пре и пробиотики [19].
Следует помнить, что своевременное выявление и эффективная терапия кандидозного дисбиоза позволит предупредить развитие более тяжелой формы дисбиозного колита, лечение которого потребует значительно большего времени и использования более широкого спектра препаратов.
Список літератури
1. Баранов А.А. Научные и организационные приоритеты в детской гастроэнтерологии // Педиатрия. — 2002. — № 3. — С. 1218.
Научные и организационные приоритеты в детской гастроэнтерологии // Педиатрия. — 2002. — № 3. — С. 1218.
2. Белоусова О.Ю. Хронический неспецифический неязвенный колит у детей. — Х.: Оберіг, 2009. — 184 с.
3. Белоусова О.Ю. Дисбиоз кишечника как фактор риска развития хронических заболеваний кишечника у детей // Здоровье ребенка. — 2011. — № 1. — С. 7375.
4. Бережной В.В. Микроэкологические нарушения у детей и современные возможности повышения эффективности их коррекции / Бережной В.В., Крамарев С.А., Мартынюк В.Ю. // Здоровье женщины. — 2002. — № 4. — С. 7991.
5. Златкина А.Р., Исаков В.А., Иваников И.О. Кандидоз кишечника как новая проблема гастроэнтерологии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2001. — № 6. — С. 3338.
6. Каширская Н.Ю. Значение пробиотиков и пребиотиков в регуляции кишечной микрофлоры // Рус. мед. журн. — 2000. — № 13–14. — С. 3612.
7. Сергеев А.Ю., Сергеев Ю.В. Кандидоз. Природа инфекции, механизмы агрессии и защиты, лабораторная диагностика, клиника и лечение. — М., 2001. — 472 с.
— М., 2001. — 472 с.
8. Урсова Н.И. Проблемы функциональных расстройств билиарного тракта у детей и их коррекция // Русский медицинский журнал. — 2003. — № 3. — С. 138142.
9. Хмельницкий О.К. О кандидозе слизистых оболочек // Архив патологии. — 2000. — Т. 62, № 6. — С. 310.
10. Циммерман Я.С. Гастроэнтерология. — М.: ГЭОТАРМедиа, 2012. — С. 220266.
11. Шевяков М.А., Авалуева Е.Б., Барышникова Н.В. Кишечный кандидоз // Здоровье Украины. — 2009. — 6(1). — С. 4849.
12. Шевяков М.А. Диагностика и лечение кандидоза кишечника // Терапевтический архив. — 2003. — Т. 75, № 11. — С. 7779.
13. Шульпекова Ю.О. Кандидоз кишечника // Русский медицинский журнал. — 2002. — Т. 4, № 1. — С. 2528.
14. Forbes D., Ee L., CamerPesci P., Ward P.B. Faecal Candida and diarrhea // Arch. Dis. Child. — 2001. — Vol. 84. —Р. 328331.
15. Gores G.J. Mechanisms of cellinjury and death sn cholestasis and hepatoprotectson by ursodeocsy choli acid // J. Hepatology. — 2000. — Vol. 32. — P. 1113.
Hepatology. — 2000. — Vol. 32. — P. 1113.
16. Danna P.L., Urban C., Bellin E., Rahal J.J. Role of Candida in pathogenesis of antibioticassociated diarrhoea in elderly patients // Lancet. — 1991. — Vol. 337. — P. 511514.
17. Hyams J.S. Inflammatory bowel disease / Hyams J.S. // Pediatr. Rew. — 2000. — № 21(9). — P. 291295.
18. Levis L.G. Gastroentestinal infection in children / Levis L.J. // Pediatr. — 1994. — V. 5. — P. 573579.
19. PanchevaDimitrova R.Z., GeorgievaShakola M., Tzaneva V. Probiotics and antibioticassociated diarrhea in children // Abstracts of 12 UEGW, Gut. — 2004. — 53 (Suppl. VI). — A137.
20. Segal E. Candida, still number one — what do we know and where are we going from there // Mikol. Lek. — 2004. — 11(2). — Р. 133138.
21. Ott S.J. Reduction in diversity of the colonic mucosa associated bacterial microflora in patients with active inflammatory bowel diseas / S.J. Ott, M. Vusfeld, D.F. Wenderoth et al. // Gut. — 2004. — № 53. — P. 685693.
— № 53. — P. 685693.
Педиатрический инвазивный кандидоз: эпидемиология и диагностика у детей
1. Зиверт Д.М., Рикс П., Эдвардс Дж.Р., Шнайдер А., Патель Дж., Шринивасан А., Каллен А., Лимбагао Б., Фридкин С. Устойчивость к противомикробным препаратам патогены, связанные с инфекциями, связанными со здравоохранением: сводка данных, представленных в Национальную сеть безопасности здравоохранения в Центрах по контролю и профилактике заболеваний, 2009–2010 гг. Заразить. Хосп. Эпидемиол. 2013; 34:1–14. дои: 10.1086/668770. [PubMed] [CrossRef] [Академия Google]
2. Wisplinghoff H., Seifert H., Tallent S.M., Bischoff T., Wenzel R.P., Edmond M.B. Внутрибольничные инфекции кровотока у педиатрических пациентов в больницах США: эпидемиология, клинические особенности и восприимчивость. Педиатр. Заразить. Дис. Дж. 2003; 22: 686–691. doi: 10.1097/01.inf.0000078159.53132.40. [PubMed] [CrossRef] [Google Scholar]
3. Watson R.S., Carcillo J.A., Linde-Zwirble W.T., Clermont G. , Lidicker J., Angus D.C. Эпидемиология тяжелого сепсиса у детей в США. Являюсь. Дж. Дыхание. крит. Уход Мед. 2003;167:695–701. doi: 10.1164/rccm.200207-682OC. [PubMed] [CrossRef] [Google Scholar]
, Lidicker J., Angus D.C. Эпидемиология тяжелого сепсиса у детей в США. Являюсь. Дж. Дыхание. крит. Уход Мед. 2003;167:695–701. doi: 10.1164/rccm.200207-682OC. [PubMed] [CrossRef] [Google Scholar]
4. Creutzig U., Zimmermann M., Reinhardt D., Dworzak M., Stary J., Lehrnbecher T. миелоидный лейкоз: анализ многоцентровых клинических исследований AML-BFM 93 и AML-BFM 98. J. Clin. Онкол. 2004; 22:4384–4393. doi: 10.1200/JCO.2004.01.191. [PubMed] [CrossRef] [Google Scholar]
5. Пагано Л., Кайра М., Кандони А., Оффидани М., Фианчи Л., Мартино Б., Пасторе Д., Пикарди М., Бонини А., Чиеричини А. и др. Эпидемиология грибковых инфекций у пациентов с гемобластозами: исследование SEIFEM-2004. Гематология. 2006;91: 1068–1075. [PubMed] [Google Scholar]
6. Мартин С.Р., Аткисон П., Ананд Р., Линдблад А.С. Исследования педиатрической трансплантации печени 2002: Выживаемость пациентов и трансплантатов и отторжение у педиатрических реципиентов первой трансплантации печени в США и Канаде. Педиатр. Трансплантат. 2004; 8: 273–283. doi: 10.1111/j.1399-3046.2004.00152.x. [PubMed] [CrossRef] [Google Scholar]
Педиатр. Трансплантат. 2004; 8: 273–283. doi: 10.1111/j.1399-3046.2004.00152.x. [PubMed] [CrossRef] [Google Scholar]
7. Profumo R.J. Реципиенты педиатрической трансплантации печени: анализ смертности за 20 лет. Дж. Страхование. Мед. 2006; 38:3–8. [PubMed] [Академия Google]
8. Zaoutis T.E., Argon J., Chu J., Berlin J.A., Walsh T.J., Feudtner C. Эпидемиология и атрибутивные исходы кандидемии у взрослых и детей, госпитализированных в США: анализ склонности. клин. Заразить. Дис. 2005;41:1232–1239. дои: 10.1086/496922. [PubMed] [CrossRef] [Google Scholar]
9. Zaoutis T.E., Prasad P.A., Localio A.R., Coffin S.E., Bell L.M., Walsh T.J., Gross R. Факторы риска и предикторы кандидемии у пациентов педиатрических отделений интенсивной терапии: последствия для профилактика. клин. Заразить. Дис. 2010;51:e38–e45. дои: 10.1086/655698. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Sung L., Lange B.J., Gerbing R.B., Alonzo T.A., Feusner J. Микробиологически подтвержденные инфекции и инфекционная смертность у детей с острым миелоидным заболеванием лейкемия. Кровь. 2007; 110:3532–3539. doi: 10.1182/blood-05-091942, 2007. [PubMed] [CrossRef] [Google Scholar]
Кровь. 2007; 110:3532–3539. doi: 10.1182/blood-05-091942, 2007. [PubMed] [CrossRef] [Google Scholar]
11. Пфаллер М.А., Дикема Д.Дж., Джонс Р.Н., Мессер С.А., Холлис Р.Дж. Тенденции в противогрибковой чувствительности Candida spp. выделены от детей и взрослых пациентов с инфекциями кровотока: SENTRY Antimicrobial Surveillance Program, 1997 до 2000. Дж. Клин. микробиол. 2002; 40: 852–856. doi: 10.1128/JCM.40.3.852-856.2002. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
12. Кркмери В., Лахо Л., Хуттова М., Ондрусова А., Кралинский К., Певалова Л., Длухолуцкий С., Писарчикова М. , Ханзен Дж., Филька Дж. и др. Этиология, противогрибковая чувствительность, факторы риска и исход у 201 ребенка с грибковой инфекцией: данные 12-летнего проспективного национального исследования в Словакии. Дж. Мед. микробиол. 2002; 51: 110–116. doi: 10.1099/0022-1317-51-2-110. [PubMed] [CrossRef] [Академия Google]
13. Хоуп В.В., Сейбел Н.Л., Шварц К.Л., Арриета А., Флинн П. , Шад А., Альбано Э., Кейрнс Дж.Дж., Бьюэлл Д.Н., Гамбо Т. и др. Популяционная фармакокинетика микафунгина у педиатрических пациентов и последствия для противогрибкового дозирования. Антимикроб. Агенты Чемотер. 2007;51:3714–3719. doi: 10.1128/AAC.00398-07. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Шад А., Альбано Э., Кейрнс Дж.Дж., Бьюэлл Д.Н., Гамбо Т. и др. Популяционная фармакокинетика микафунгина у педиатрических пациентов и последствия для противогрибкового дозирования. Антимикроб. Агенты Чемотер. 2007;51:3714–3719. doi: 10.1128/AAC.00398-07. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Blyth C.C., Chen S.C., Slavin M.A., Serena C., Nguyen Q., Marriott D., Ellis D., Meyer W., Sorrell T.C. Не только маленькие взрослые: эпидемиология кандидемии, молекулярная характеристика и чувствительность к противогрибковым препаратам у новорожденных и детей. Педиатрия. 2009 г.;123:1360–1368. doi: 10.1542/пед.2008-2055. [PubMed] [CrossRef] [Google Scholar]
15. Velasco E., Bigni R. Проспективное когортное исследование, оценивающее прогностическое влияние клинических характеристик и сопутствующих состояний госпитализированных взрослых и детей, больных раком с кандидемией. Евро. Дж. Клин. микробиол. Заразить. Дис. 2008; 27:1071–1078. doi: 10.1007/s10096-008-0546-y. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
16. Zaoutis T.E., Coffin S.E., Chu J.H., Heydon K., Zhao H., Greves H.M., Walsh T.J. Факторы риска смертности детей с кандидемией. Педиатр. Заразить. Дис. Дж. 2005; 24: 736–739.. doi: 10.1097/01.inf.0000172938.76561.8e. [PubMed] [CrossRef] [Google Scholar]
17. Сингхи С.С., Редди Т.С., Чакрабарти А. Кандидемия в педиатрическом отделении интенсивной терапии. Педиатр. крит. Уход Мед. 2004; 5: 369–374. doi: 10.1097/01.PCC.0000123550.68708.20. [PubMed] [CrossRef] [Google Scholar]
18. Fisher B.T., Ross R.K., Roilides E., Palazzi D.L., Abzug MJ, Hoffman J.A., Berman D.M., Prasad P.A., Localio A.R., Steinbach W.J., et al. Невозможность проверки многовариантной модели клинического прогнозирования для выявления пациентов педиатрического отделения интенсивной терапии с высоким риском кандидемии. Дж. Педиатр. Заразить. Дис. соц. 2015 год: 10.1093/jpids/piv024. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Хоуп В. В., Кастаньола Э., Гролл А.Х., Ройлидес Э., Акова М., Арендруп М.С., Арикан-Акдагли С., Бассетти М., Билле Дж., Корнели О.А. и др. Руководство ESCMID* по диагностике и лечению заболеваний, вызванных Candida , 2012 г.: Профилактика и лечение инвазивных инфекций у новорожденных и детей, вызванных Candida spp. клин. микробиол. Заразить. 2012; 18:38–52. дои: 10.1111/1469-0691.12040. [PubMed] [CrossRef] [Академия Google]
В., Кастаньола Э., Гролл А.Х., Ройлидес Э., Акова М., Арендруп М.С., Арикан-Акдагли С., Бассетти М., Билле Дж., Корнели О.А. и др. Руководство ESCMID* по диагностике и лечению заболеваний, вызванных Candida , 2012 г.: Профилактика и лечение инвазивных инфекций у новорожденных и детей, вызванных Candida spp. клин. микробиол. Заразить. 2012; 18:38–52. дои: 10.1111/1469-0691.12040. [PubMed] [CrossRef] [Академия Google]
20. Паппас П.Г., Кауфман С.А., Андес Д., Бенджамин Д.К.Дж., Каландра Т.Ф., Эдвардс Дж.Э.Дж., Филлер С.Г., Фишер Дж.Ф., Куллберг Б.Дж., Остроски-Зейхнер Л. и др. Клинические практические рекомендации по лечению кандидоза: обновление 2009 г., подготовленное Американским обществом инфекционистов. клин. Заразить. Дис. 2009; 48: 503–535. дои: 10.1086/596757. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Steinbach W.J., Roilides E., Berman D., Hoffman J.A., Groll A.H., Bin-Hussain I., Palazzi DL, Castagnola E., Halasa Н., Велеграки А. и др. Результаты проспективного международного эпидемиологического исследования инвазивного кандидоза у детей и новорожденных. Педиатр. Заразить. Дис. Дж. 2012; 31:1252–1257. дои: 10.1097/INF.0b013e3182737427. [PubMed] [CrossRef] [Google Scholar]
и др. Результаты проспективного международного эпидемиологического исследования инвазивного кандидоза у детей и новорожденных. Педиатр. Заразить. Дис. Дж. 2012; 31:1252–1257. дои: 10.1097/INF.0b013e3182737427. [PubMed] [CrossRef] [Google Scholar]
22. Сантолая М.Е., Альварадо Т., Кейроз-Теллес Ф., Коломбо А.Л., Зурита Дж., Тирабоски И.Н., Кортес Дж.А., Томпсон Л., Гусман М., Сифуэнтес Дж. ., и другие. Активный эпиднадзор за кандидемией у детей из Латинской Америки: ключевое требование для улучшения результатов заболевания. Педиатр. Заразить. Дис. Дж. 2014; 33:e40–e44. doi: 10.1097/INF.0000000000000039. [PubMed] [CrossRef] [Google Scholar]
23. Пеман Дж., Кантон Э., Линарес-Сицилия М.Дж., Розелло Э.М., Боррелл Н., Руис-Перес-де-Пипаон М.Т., Гвинея Дж., Гарсия Дж. , Porras A., Garcia-Tapia A.M., et al. Эпидемиология и противогрибковая восприимчивость грибковых изолятов кровотока у педиатрических пациентов: испанское многоцентровое проспективное исследование. Дж. Клин. микробиол. 2011;49: 4158–4163. doi: 10.1128/JCM.05474-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2011;49: 4158–4163. doi: 10.1128/JCM.05474-11. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Роилидес Э., Кадилцоглу И., Захидес Д., Бибаши Э. Инвазивный кандидоз у детей. клин. микробиол. Заразить. 1997; 3: 192–197. doi: 10.1111/j.1469-0691.1997.tb00597.x. [PubMed] [CrossRef] [Google Scholar]
25. Zaoutis T.E., Greves H.M., Lautenbach E., Bilker W.B., Coffin S.E. Факторы риска диссеминированного кандидоза у детей с кандидемией. Педиатр. Заразить. Дис. Дж. 2004; 23:635–641. дои: 10.1097/01.инф.0000128781.77600.6ф. [PubMed] [CrossRef] [Google Scholar]
26. Паскуалотто А.К., де Мораес А.Б., Занини Р.Р., Северо Л.К. Анализ независимых факторов риска смерти у детей с кандидемией и установленным центральным венозным катетером. Заразить. Хосп. Эпидемиол. 2007; 28: 799–804. дои: 10.1086/516658. [PubMed] [CrossRef] [Google Scholar]
27. Ной Н., Малик М., Лундинг А., Уиттиер С., Альба Л., Кубин С., Сайман Л. Эпидемиология кандидемии в детской больнице, 2002 г. по 2006 г. Педиатр. Заразить. Дис. Дж. 2009 г.;28:806–809. doi: 10.1097/INF.0b013e3181a0d78d. [PubMed] [CrossRef] [Google Scholar]
по 2006 г. Педиатр. Заразить. Дис. Дж. 2009 г.;28:806–809. doi: 10.1097/INF.0b013e3181a0d78d. [PubMed] [CrossRef] [Google Scholar]
28. Tragiannidis A., Fegeler W., Rellensmann G., Debus V., Müller V., Hoernig-Franz I., Siam K., Pana Z.D., Jürgens H. , Гролл А.Х. Кандидемия в больнице Европейского педиатрического университета: 10-летнее обсервационное исследование. клин. микробиол. Заразить. 2012;18:E27–E30. doi: 10.1111/j.1469-0691.2011.03720.x. [PubMed] [CrossRef] [Google Scholar]
29. Паппас П.Г., Рекс Дж.Х., Ли Дж., Хэмилл Р.Дж., Ларсен Р.А., Паудерли В., Кауфман К.А., Хислоп Н., Мангино Дж.Е., Чепмен С., Горовиц Х.В. , и другие. Проспективное обсервационное исследование кандидемии: эпидемиология, терапия и влияние на смертность госпитализированных взрослых и детей. клин. Заразить. Дис. 2003; 37: 634–643. дои: 10.1086/376906. [PubMed] [CrossRef] [Google Scholar]
30. Zaoutis T.E., Jafri H.S., Huang L.M., Locatelli F., Barzilai A., Ebell W., Steinbach W.J., Bradley J. , Lieberman J.M., Hsiao C.C., и другие. Проспективное многоцентровое исследование каспофунгина для лечения подтвержденных инфекций Candida или Aspergillus у детей. Педиатрия. 2009; 123: 877–884. doi: 10.1542/пед.2008-1158. [PubMed] [CrossRef] [Google Scholar]
, Lieberman J.M., Hsiao C.C., и другие. Проспективное многоцентровое исследование каспофунгина для лечения подтвержденных инфекций Candida или Aspergillus у детей. Педиатрия. 2009; 123: 877–884. doi: 10.1542/пед.2008-1158. [PubMed] [CrossRef] [Google Scholar]
31. Wiley J.M., Seibel N.L., Walsh T.J. Эффективность и безопасность липидного комплекса амфотерицина В у 548 детей и подростков с инвазивными грибковыми инфекциями. Педиатр. Заразить. Дис. Дж. 2005; 24:167–174. дои: 10.1097/01.инф.0000153183.51258.b8. [PubMed] [CrossRef] [Google Scholar]
32. Walsh T.J., Whitcomb P., Piscitelli S., Figg W.D., Hill S., Chanock S.J., Jarosinski P., Gupta R., Pizzo P.A. Безопасность, переносимость и фармакокинетика липидного комплекса амфотерицина В у детей с гепатоспленическим кандидозом. Антимикроб. Агенты Чемотер. 1997; 41:1944–1948. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Липидный комплекс амфотерицина В у детей с инвазивными грибковыми инфекциями. Педиатр. Заразить. Дис. Дж. 1999;18:702–708. doi: 10.1097/00006454-199908000-00010. [PubMed] [CrossRef] [Google Scholar]
Педиатр. Заразить. Дис. Дж. 1999;18:702–708. doi: 10.1097/00006454-199908000-00010. [PubMed] [CrossRef] [Google Scholar]
34. Вюртвейн Г., Гролл А.Х., Хемпель Г., Адлер-Шохет Ф.К., Либерман Дж.М., Уолш Т.Дж. Популяционная фармакокинетика липидного комплекса амфотерицина В у новорожденных. Антимикроб. Агенты Чемотер. 2005; 49: 5092–5098. doi: 10.1128/AAC.49.12.5092-5098.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Queiroz-Telles F., Berezin E., Leverger G., Freire A., van der Vyver A., Chotpitayasunondh T., Konja J. , Diekmann-Berndt H., Koblinger S., Groll A.H., et al. Микафунгин по сравнению с липосомальным амфотерицином В для детей с инвазивным кандидозом: подисследование рандомизированного двойного слепого исследования. Педиатр. Заразить. Дис. Дж. 2008; 27:820–826. doi: 10.1097/INF.0b013e31817275e6. [PubMed] [CrossRef] [Google Scholar]
36. Palazzi DL, Arrieta A., Castagnola E., Halasa N., Hubbard S., Brozovich A.A., Fisher BT, Steinbach WJ Видообразование Candida , противогрибковое лечение и побочные эффекты События при педиатрическом инвазивном кандидозе: результаты 441 инфекции в проспективном многонациональном исследовании. Педиатр. Заразить. Дис. Дж. 2014; 33:1294–1296. doi: 10.1097/INF.0000000000000431. [PubMed] [CrossRef] [Google Scholar]
Педиатр. Заразить. Дис. Дж. 2014; 33:1294–1296. doi: 10.1097/INF.0000000000000431. [PubMed] [CrossRef] [Google Scholar]
37. Датта А., Палацци Д.Л. Candida non-albicans против Candida albicans фунгемия у ненеонатального детского населения. Педиатр. Заразить. Дис. Дж. 2011; 30:664–668. doi: 10.1097/INF.0b013e318213da0f. [PubMed] [CrossRef] [Google Scholar]
38. Dotis J., Prasad P.A., Zaoutis T., Roilides E. Эпидемиология, факторы риска и исход Candida parapsilosis инфекция кровотока у детей. Педиатр. Заразить. Дис. Дж. 2012; 31: 557–560. doi: 10.1097/INF.0b013e31824da7fe. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Benjamin D.K.J., Stoll B.J., Fanaroff A.A., McDonald S.A., Oh W., Higgins R.D., Duara S., Poole K., Laptook A., Гольдберг Р. Кандидоз новорожденных среди детей с экстремально низкой массой тела при рождении: факторы риска, показатели смертности и исходы развития нервной системы в возрасте от 18 до 22 месяцев. Педиатрия. 2006; 117:84–92. doi: 10.1542/пед.2004-2292. [PubMed] [CrossRef] [Google Scholar]
Педиатрия. 2006; 117:84–92. doi: 10.1542/пед.2004-2292. [PubMed] [CrossRef] [Google Scholar]
Педиатрические факторы риска кандидемии, вторичной по отношению к видам Candida glabrata и Candida krusei . Дж. Педиатр. Заразить. Дис. соц. 2013;2:263–266. doi: 10.1093/jpids/pis093. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Garey K.W., Rege M., Pai M.P., Mingo D.E., Suda K.J., Turpin R.S., Bearden DT. Время до начала терапии флуконазолом влияет на смертность пациентов с кандидемией: межведомственное исследование. клин. Заразить. Дис. 2006;43:25–31. дои: 10.1086/504810. [PubMed] [CrossRef] [Академия Google]
42. Моррелл М., Фрейзер В.Дж., Коллеф М.Х. Отсрочка эмпирического лечения инфекции кровотока, вызванной Candida , до получения положительных результатов посева крови: потенциальный фактор риска госпитальной летальности. Антимикроб. Агенты Чемотер. 2005;49:3640–3365. doi: 10.1128/AAC.49.9.3640-3645.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Беренгер Дж., Бак М., Витебски Ф., Сток Ф., Пиццо П.А., Уолш Т.Дж. Лизисно-центрифугированные культуры крови при выявлении тканедоказанного инвазивного кандидоза. Рассеянный против инфекции одного органа. Диагн. микробиол. Заразить. Дис. 1993; 17: 103–109. doi: 10.1016/0732-8893(93)
Беренгер Дж., Бак М., Витебски Ф., Сток Ф., Пиццо П.А., Уолш Т.Дж. Лизисно-центрифугированные культуры крови при выявлении тканедоказанного инвазивного кандидоза. Рассеянный против инфекции одного органа. Диагн. микробиол. Заразить. Дис. 1993; 17: 103–109. doi: 10.1016/0732-8893(93)
-8. [PubMed] [CrossRef] [Google Scholar]
44. Clancy C.J., Nguyen M.H. Обнаружение «недостающих 50%» инвазивного кандидоза: как некультуральная диагностика улучшит понимание спектра заболеваний и трансформирует уход за пациентами. клин. Заразить. Дис. 2013;56:1284–1292. doi: 10.1093/cid/cit006. [PubMed] [CrossRef] [Google Scholar]
45. Lai C.C., Wang C.Y., Liu W.L., Huang Y.T., Hsueh P.R. Время до положительного результата культур крови различных Виды Candida , вызывающие фунгемию. Дж. Мед. микробиол. 2012;61:701–704. doi: 10.1099/jmm.0.038166-0. [PubMed] [CrossRef] [Google Scholar]
46. Cuenca-Estrella M., Verweij P.E., Arendrup M.C., Arikan-Akdagli S., Bille J. , Donnelly J.P., Jensen H.E., Lass-Florl C., Richardson M.D. , Акова М. и др. Руководство ESCMID* по диагностике и лечению заболеваний Candida 2012 г.: Диагностические процедуры. клин. микробиол. Заразить. 2012; 18:9–18. doi: 10.1111/1469-0691.12038. [PubMed] [CrossRef] [Академия Google]
, Donnelly J.P., Jensen H.E., Lass-Florl C., Richardson M.D. , Акова М. и др. Руководство ESCMID* по диагностике и лечению заболеваний Candida 2012 г.: Диагностические процедуры. клин. микробиол. Заразить. 2012; 18:9–18. doi: 10.1111/1469-0691.12038. [PubMed] [CrossRef] [Академия Google]
47. Остроски-Зейхнер Л., Александр Б.Д., Кетт Д.Х., Васкес Дж., Паппас П.Г., Саэки Ф., Кетчум П.А., Вингард Дж., Шифф Р., Тамура Х. и др. Многоцентровая клиническая оценка анализа (1→3)-β-d-глюкана в качестве средства диагностики грибковых инфекций у людей. клин. Заразить. Дис. 2005; 41: 654–659. дои: 10.1086/432470. [PubMed] [CrossRef] [Google Scholar]
48. Held J., Kohlberger I., Rappold E., Busse Grawitz A., Häcker G. Сравнение (1→3)-β-d-глюкана, маннана/ антитела против маннана и Cand-Tec Антиген Candida в качестве сывороточного биомаркера кандидемии. Дж. Клин. микробиол. 2013;51:1158–1164. doi: 10.1128/JCM.02473-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
49. Lunel F.M., Donnelly J.P., van der Lee H.A., Blijlevens N.M., Verweij P.E. Эффективность новых тестов Platelia Candida Plus для диагностики инвазивной инфекции Candida у пациентов, проходящих миелоаблативную терапию. Мед. Микол. 2011;49:848–855. [PubMed] [Академия Google]
Lunel F.M., Donnelly J.P., van der Lee H.A., Blijlevens N.M., Verweij P.E. Эффективность новых тестов Platelia Candida Plus для диагностики инвазивной инфекции Candida у пациентов, проходящих миелоаблативную терапию. Мед. Микол. 2011;49:848–855. [PubMed] [Академия Google]
50. Odabasi Z., Mattiuzzi G., Estey E., Kantarjian H., Saeki F., Ridge R.J., Ketchum P.A., Finkelman M.A., Rex J.H., Ostrosky-Zeichner L. β-d-глюкан в качестве диагностического вспомогательного средства для инвазивных грибковых инфекций: валидация, развитие отсечения и эффективность у пациентов с острым миелогенным лейкозом и миелодиспластическим синдромом. клин. Заразить. Дис. 2004; 39: 199–205. дои: 10.1086/421944. [PubMed] [CrossRef] [Google Scholar]
51. Mularoni A., Furfaro E., Faraci M., et al. Высокий уровень β-d-глюкана у детей с ослабленным иммунитетом и подтвержденным инвазивным грибковым заболеванием. клин. Вакцина Иммунол. 2010; 17:882–883. doi: 10.1128/CVI.00038-10. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Montagna M.T., Coretti C., Lovero G., Franceschi A., Mezzano P., Bandettini R., Viscoli C., Castagnola E. Диагностическая эффективность 1→3-β-d-глюкана у новорожденных и детей больных кандидемией. Междунар. Дж. Мол. науч. 2011;12:5871–5877. doi: 10.3390/ijms12095871. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Montagna M.T., Coretti C., Lovero G., Franceschi A., Mezzano P., Bandettini R., Viscoli C., Castagnola E. Диагностическая эффективность 1→3-β-d-глюкана у новорожденных и детей больных кандидемией. Междунар. Дж. Мол. науч. 2011;12:5871–5877. doi: 10.3390/ijms12095871. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Zhao L., Tang J.Y., Wang Y., Zhou Y.F., Chen J., Li BR, Xue HL Значение β-глюкана в плазме в начале Диагностика инвазивной грибковой инфекции у детей. Чжунго Данг Дай Эр Ке За Чжи. 2009 г.;11:905–908. (на китайском языке) [PubMed] [Google Scholar]
54. Гуджил С., Конголо Г., Дусол Л., Иместурен Ф., Корну М., Леке А., Чоуаки Т. (1–3)-β- Уровни d-глюкана при кандидозной инфекции у новорожденных в критическом состоянии. Дж. Матерн. Фетальная неонатальная мед. 2013; 26:44–48. doi: 10.3109/14767058.2012.722716. [PubMed] [CrossRef] [Google Scholar]
55. Lamoth F., Cruciani M., Mengoli C., Castagnola E., Lortholary O., Richardson M., Marchetti O. Анализ β-глюкановой антигенемии для диагностики инвазивные грибковые инфекции у пациентов с гематологическими злокачественными новообразованиями: систематический обзор и метаанализ когортных исследований Третьей европейской конференции по инфекциям при лейкемии (ECIL-3) Clin. Заразить. Дис. 2012; 54: 633–643. дои: 10.1093/сид/цир897. [PubMed] [CrossRef] [Google Scholar]
Анализ β-глюкановой антигенемии для диагностики инвазивные грибковые инфекции у пациентов с гематологическими злокачественными новообразованиями: систематический обзор и метаанализ когортных исследований Третьей европейской конференции по инфекциям при лейкемии (ECIL-3) Clin. Заразить. Дис. 2012; 54: 633–643. дои: 10.1093/сид/цир897. [PubMed] [CrossRef] [Google Scholar]
56. Хикида С., Танака Ю., Цуру Т., Отани М., Кобаяси Х., Асагири К., Акиёси К., Накамизо Х., Фукахори С., Соэдзима Х. и др. Исследование ДНК грибов полезно в качестве чувствительного параметра для начала и прекращения противогрибковой терапии у детей с ослабленным иммунитетом после операции. Куруме Мед. Дж. 2004; 51: 125–131. doi: 10.2739/kurumemedj.51.125. [PubMed] [CrossRef] [Google Scholar]
57. Ginocchio F., Verrina E., Furfaro E., Cannavo R., Bandettini R., Castagnola E. Случай надежности 1,3-β-d- мониторинг глюкана при лечении перитонеального кандидоза у ребенка, получающего непрерывный перитонеальный диализ. клин. Вакцина Иммунол. 2012;19: 626–627. doi: 10.1128/CVI.00008-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
клин. Вакцина Иммунол. 2012;19: 626–627. doi: 10.1128/CVI.00008-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Санада Ю., Мизута К., Урахаси Т., Ихара Ю., Вакия Т., Окада Н., Ямада Н., Ясуда Ю. , Каварасаки Х. Эффективность измерения β-d глюкана в сыворотке у пациентов с атрезией желчевыводящих путей. Педиатр. Surg. Междунар. 2012;28:993–996. doi: 10.1007/s00383-012-3166-7. [PubMed] [CrossRef] [Google Scholar]
59. Мокаддас Э., Бурхамах М.Х., Хан З.У., Ахмад С. Уровни (1→3)-β-d-глюкана, 9ДНК 0023 Candida и Candida в образцах сыворотки онкологических больных детей, колонизированных видами Candida . Заражение BMC. Дис. 2010;10:292. дои: 10.1186/1471-2334-10-292. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Пинто Дж. М., Султан Р., Дэвис М. А. Ложноположительный анализ (1,3)-β-d-глюкана у пациента с внутричерепной герминомой. Педиатр. Заразить. Дис. Дж. 2015; 34: 676–677. doi: 10.1097/INF.0000000000000690. [PubMed] [CrossRef] [Академия Google]
[PubMed] [CrossRef] [Академия Google]
61. Населли А., Фарачи М., Ланино Э., Морреале Г., Кангеми Г., Бандеттини Р., Кастаньола Э. Стойкость высокого уровня (1,3)-β-d-глюкана после кандидемии после аутологичная периферическая SCT у педиатрического пациента. Пересадка костного мозга. 2015;50:137–138. doi: 10.1038/bmt.2014.206. [PubMed] [CrossRef] [Google Scholar]
62. Montagna M.T., Lovero G., de Giglio O., Iatta R., Caggiano G., Montagna O., Laforgia N. Инвазивные грибковые инфекции в отделениях интенсивной терапии новорожденных Южная Италия: многоцентровое региональное активное наблюдение (проект AURORA) J. Prev. Мед. Гиг. 2010;51:125–130. [PubMed] [Академия Google]
63. Koltze A., Rath P., Schoning S., Steinmann J., Wichelhaus T.A., Bader P., Bochennek K., Lehrnbecher T. Скрининг β-d-глюкана для выявления инвазивных грибковых заболеваний у детей, подвергающихся аллогенной Трансплантация гемопоэтических стволовых клеток. Дж. Клин. микробиол. 2015;53:2605–2610. doi: 10. 1128/JCM.00747-15. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
1128/JCM.00747-15. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
64. Смит П.Б., Бенджамин Д.К.Дж., Александр Б.Д., Джонсон М.Д., Финкельман М.А., Штайнбах В.Дж. Количественная оценка уровня 1,3-β-d-глюкана у детей : Предварительные данные для диагностического использования анализа β-глюкана в педиатрии. клин. Вакцина Иммунол. 2007;14:924–925. doi: 10.1128/CVI.00025-07. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
65. Marchetti O., Lamoth F., Mikulska M., Viscoli C., Verweij P., Bretagne S. Рекомендации ECIL по использованию биологических маркеров для диагностики инвазивных грибковых заболеваний у больных лейкемией и реципиентов гемопоэтической СКТ. Пересадка костного мозга. 2012; 47: 846–854. doi: 10.1038/bmt.2011.178. [PubMed] [CrossRef] [Google Scholar]
Инвазивный кандидоз у младенцев и детей: последние достижения в эпидемиологии, диагностике и лечении
1. Мантадакис Э., Пана З.Д., Заутис Т. Кандидемия у детей: эпидемиология, профилактика и лечение. Микозы. 2018; 61: 614–622. doi: 10.1111/myc.12792. [PubMed] [CrossRef] [Google Scholar]
Микозы. 2018; 61: 614–622. doi: 10.1111/myc.12792. [PubMed] [CrossRef] [Google Scholar]
2. Пана З.Д., Ройлидес Э., Варрис А., Гролл А.Х., Заутис Т. Эпидемиология инвазивных грибковых заболеваний у детей. Дж. Педиатр. Заразить. Дис. 2017;6:С3–С11. doi: 10.1093/jpids/pix046. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Benjamin D.K., Jr., Stoll B.J., Gantz M.G., Walsh M.C., Sánchez P.J., Das A., Shankaran S., Higgins R.D., Auten K.J. , Миллер Н.А. и соавт. Неонатальный кандидоз: эпидемиология, факторы риска и клиническая оценка. Педиатрия. 2010;126:e865–e873. doi: 10.1542/пед.2009-3412. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Aliaga S., Clark R.H., Clark R.H., Laughon M., Walsh T.J., Hope W., Benjamin D.K., Benjamin D.K., Jr., Smith П.Б. Снижение заболеваемости кандидозом у новорожденных в отделениях реанимации новорожденных. Педиатрия. 2014; 133: 236–242. doi: 10.1542/peds.2013-0671. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Статистика инвазивного кандидоза. [(по состоянию на 1 декабря 2018 г.)]; Доступно в Интернете: https://www.cdc.gov/fungal/diseases/candidiasis/invasive/statistics.html
Статистика инвазивного кандидоза. [(по состоянию на 1 декабря 2018 г.)]; Доступно в Интернете: https://www.cdc.gov/fungal/diseases/candidiasis/invasive/statistics.html
6. Бенджамин Д.К., Пул К., Штайнбах В.Дж., Роуэн Дж.Л., Уолш Т.Дж. Неонатальная кандидемия и повреждение органов-мишеней: критическая оценка литературы с использованием метааналитических методов. Педиатрия. 2003; 112: 634–640. doi: 10.1542/peds.112.3.634. [PubMed] [CrossRef] [Google Scholar]
7. Roilides E. Инвазивный кандидоз у новорожденных и детей. Ранний гул. Дев. 2011;87:S75–S76. doi: 10.1016/j.earlhumdev.2011.01.017. [PubMed] [CrossRef] [Google Scholar]
8. Prasad P.A., Fisher B.T., Coffin S.E., Walsh T.J., McGowan K.L., Gross R., Zaoutis T.E. Педиатрические факторы риска кандидемии, вторичной по отношению к видам Candida glabrata и Candida krusei. Дж. Педиатр. Заразить. Дис. 2012;2:263–266. дои: 10.1093/jpids/pis093. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Fierro J. L., Prasad P., Fisher B., Gerber J., Coffin S.E., Walsh T.J., Zaoutis T.E. Глазные проявления кандидемии у детей. Педиатр. Заразить. Дис. Дж. 2013; 32:84–86. doi: 10.1097/INF.0b013e31826f547c. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
L., Prasad P., Fisher B., Gerber J., Coffin S.E., Walsh T.J., Zaoutis T.E. Глазные проявления кандидемии у детей. Педиатр. Заразить. Дис. Дж. 2013; 32:84–86. doi: 10.1097/INF.0b013e31826f547c. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
10. Гамалецу М.Н., Контояннис Д.П., Сипсас Н.В., Морияма Б., Александр Э., Ройлидес Э., Брауз Б., Уолш Т.Дж. Кандидозный остеомиелит: анализ 207 случаев у детей и взрослых (1970–2011) клин. Заразить. Дис. 2012;55:1338–1351. doi: 10.1093/cid/cis660. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Беренгер Дж., Бак М., Витебски Ф., Сток Ф., Пиццо П.А., Уолш Т.Дж. Лизис — центрифугирование культур крови при выявлении диссеминированного инвазивного кандидоза, подтвержденного тканями, по сравнению с инфекцией одного органа. Диагн. микробиол. Заразить. Дис. 1993; 17: 103–109. doi: 10.1016/0732-8893(93)
-8. [PubMed] [CrossRef] [Google Scholar]
12. Хапплер А.Р., Фишер Б.Т., Лернбехер Т., Уолш Т.Дж., Штейнбах В. Дж. Роль молекулярных биомаркеров в диагностике инвазивных грибковых заболеваний у детей. Дж. Педиатр. Заразить. Дис. 2017;6:С32–С44. дои: 10.1093/jpids/pix054. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж. Роль молекулярных биомаркеров в диагностике инвазивных грибковых заболеваний у детей. Дж. Педиатр. Заразить. Дис. 2017;6:С32–С44. дои: 10.1093/jpids/pix054. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. McCarthy M.W., Walsh T.J. Молекулярная диагностика инвазивных микозов центральной нервной системы. Эксперт Преподобный Мол. Диагн. 2016;17:129–139. doi: 10.1080/14737159.2017.1271716. [PubMed] [CrossRef] [Google Scholar]
14. Hamula C.L., Hughes K., Fisher B.T., Zaoutis T.E., Singh I.R., Velegraki A. T2Candida обеспечивает быструю и точную идентификацию видов в педиатрических случаях кандидемии. Являюсь. Дж. Клин. Патол. 2016; 145: 858–861. дои: 10.1093/ajcp/aqw063. [PubMed] [CrossRef] [Google Scholar]
15. Милонакис Э., Клэнси С.Дж., Остроски-Цайхнер Л., Гэри К.В., Алангаден Г.Дж., Васкес Дж.А., Гроегер Дж.С., Джадсон М.А., Винагре Ю.-М., Херд С.О. и др. Магнитно-резонансный анализ T2 для быстрой диагностики кандидемии в цельной крови: клиническое испытание. клин. Заразить. Дис. 2015;60:892–899. doi: 10.1093/cid/ciu959. [PubMed] [CrossRef] [Google Scholar]
клин. Заразить. Дис. 2015;60:892–899. doi: 10.1093/cid/ciu959. [PubMed] [CrossRef] [Google Scholar]
16. Клэнси С.Дж., Паппас П.Г., Васкес Дж., Джадсон М.А., Контояннис Д.П., Томпсон Г.Р., 3-й, Гэри К.В., Реболи А., Гринберг Р.Н., Апевокин С. и др. др. Быстрое и простое обнаружение инфекций при кандидемии, часть 2 (DIRECT2): проспективное многоцентровое исследование панели T2Candida. клин. Заразить. Дис. 2018;66:1678–1686. дои: 10.1093/сид/цикс1095. [PubMed] [CrossRef] [Google Scholar]
17. МакКаллерс Дж. А., Варгас С. Л., Флинн П. М., Раззук Б. И., Шенеп Дж. Л. Кандидозный менингит у детей с раком. клин. Заразить. Дис. 2000; 31: 451–457. дои: 10.1086/313987. [PubMed] [CrossRef] [Google Scholar]
18. Петрайтеен Р., Петрайтис В., Хоуп В.В., Микиен Д., Келахер А.М., Мюррей Х.А., Мья-Сан С., Хьюз Дж.Е., Коттон М.П., Бахер Дж. , и другие. Цереброспинальная жидкость и плазма (1-> 3)-бета-D-глюкан как суррогатные маркеры для обнаружения и мониторинга терапевтического ответа при экспериментальном гематогенном кандидозном менингоэнцефалите. Антимикроб. Агенты Чемотер. 2008; 52:4121–4129. doi: 10.1128/AAC.00674-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Антимикроб. Агенты Чемотер. 2008; 52:4121–4129. doi: 10.1128/AAC.00674-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
(1→3)-β-D-глюкан в спинномозговой жидкости как биомаркер кандидозных и аспергиллезных инфекций центральной нервной системы у детей. Дж. Педиатр. Заразить. Дис. соц. 2016;5:277–286. doi: 10.1093/jpids/piv014. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
20. Ceccarelli G., Ghezzi M.C., Raponi G., Brunetti G., Marsiglia C., Fallani S., Novelli A., Venditti M. Вориконазол лечение менингита Candida tropicalis: персистенция (1,3)-β-D-глюкана в спинномозговой жидкости является маркером клинической и микробиологической неудачи: отчет о клиническом случае. Лекарство. 2016;95:e4474. doi: 10.1097/MD.0000000000004474. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. McCarthy M.W., Walsh T.J. В настоящее время исследуются препараты для лечения инвазивного кандидоза. Мнение эксперта. расследование Наркотики. 2017; 26:825–831. doi: 10.1080/13543784.2017.1341488. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1080/13543784.2017.1341488. [PubMed] [CrossRef] [Google Scholar]
22. Farrugia M.K., Fogha E.P., Miah A.R., Yednock J., Palmer H.C., Guilfoose J. Кандидозный менингит у иммунокомпетентного пациента, выявленный с помощью (1→3)-бета-d -глюкан. Междунар. Дж. Заразить. Дис. 2016;51:25–26. doi: 10.1016/j.ijid.2016.08.020. [PubMed] [CrossRef] [Академия Google]
23. Seibel N.L., Shad A.T., Bekersky I., Groll A.H., Gonzalez C., Wood L.V., Jarosinski P., Buell D., Hope W.W., Walsh T.J., et al. Безопасность, переносимость и фармакокинетика липосомального амфотерицина В у детей с ослабленным иммунитетом. Антимикроб. Агенты Чемотер. 2016;61:e01477-16. doi: 10.1128/AAC.01477-16. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Лестнер Дж. М., Гролл А. Х., Альджаюсси Г., Сейбель Н. Л., Шад А., Гонсалес К., Вуд Л. В., Яросинский П. Ф., Уолш Т. Дж., Хоуп В.В. Популяционная фармакокинетика липосомального амфотерицина В у детей с ослабленным иммунитетом. Антимикроб. Агенты Чемотер. 2016;60:7340–7346. doi: 10.1128/AAC.01427-16. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Агенты Чемотер. 2016;60:7340–7346. doi: 10.1128/AAC.01427-16. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Гролл А.Х., Микиен Д., Петрайтис В., Петрайтене Р., Ибрагим К.Х., Писцителли С.К., Бекерский И., Уолш Т.Дж. Компартментальная фармакокинетика и распределение в тканях противогрибкового эхинокандинового липопептида микафунгина (FK463) у кроликов. Антимикроб. Агенты Чемотер. 2001;45:3322–3327. doi: 10.1128/AAC.45.12.3322-3327.2001. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
26. Петрайтис В., Петрайтене Р., Гролл А.Х., Руссильон К., Хеммингс М., Лиман К.А., Сейн Т., Бахер Дж., Бекерски И., Уолш Т.Дж. и соавт. Сравнительная противогрибковая активность и плазменная фармакокинетика микафунгина (FK463) против диссеминированного кандидоза и инвазивного легочного аспергиллеза у кроликов с устойчивой нейтропенией. Антимикроб. Агенты Чемотер. 2002; 46: 1857–1869.. doi: 10.1128/AAC.46.6.1857-1869.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Андес Д.Р., Дикема Д., Пфаллер М.А., Марчилло К., Бормюллер Дж. Исследование фармакодинамической мишени in vivo для микафунгина против Candida albicans и C. glabrata в модели нейтропенического кандидоза мышей. Антимикроб. Агенты Чемотер. 2008;52:3497–3503. doi: 10.1128/AAC.00478-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Андес Д.Р., Дикема Д., Пфаллер М.А., Марчилло К., Бормюллер Дж. Исследование фармакодинамической мишени in vivo для микафунгина против Candida albicans и C. glabrata в модели нейтропенического кандидоза мышей. Антимикроб. Агенты Чемотер. 2008;52:3497–3503. doi: 10.1128/AAC.00478-08. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Mickiene D., Petraitis V., Petraitiene R., Bacher J., Buell D., Heresi G., Kelaher A.M., Hughes J.E., Cotton М.П., Хоуп В.В. и др. Фармакокинетика и фармакодинамика микафунгина при экспериментальном гематогенном кандидозном менингоэнцефалите: значение терапии эхинокандином у новорожденных. Дж. Заразить. Дис. 2008;197: 163–171. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Simitsopoulou M., Chlichlia K., Kyrpitzi D., Walsh T.J., Roilides E. Фармакодинамические и иммуномодулирующие эффекты микафунгина на реакцию хозяина на биопленки Candida parapsilosis в сравнении к Candida albicans. Антимикроб. Агенты Чемотер. 2018; 62 doi: 10. 1128/AAC.00478-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1128/AAC.00478-18. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Seibel N.L., Schwartz C., Arrieta A., Flynn P., Shad A., Albano E., Keirns J., Lau WM, Facklam Д.П., Бьюэлл Д.Н. и соавт. Безопасность, переносимость и фармакокинетика микафунгина (FK463) у педиатрических пациентов с фебрильной нейтропенией. Антимикроб. Агенты Чемотер. 2005;49: 3317–3324. doi: 10.1128/AAC.49.8.3317-3324.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Сантос Р.П., Санчес П.Дж., Мехиас А., Бенджамин Д.К., младший, Уолш Т.Дж., Патель С., Джафри Х.С. Успешное медикаментозное лечение кожного аспергиллеза у недоношенного ребенка с использованием липосомального амфотерицина В, вориконазола и микафунгина. Педиатр. Заразить. Дис. Дж. 2007; 26: 364–366. doi: 10.1097/01.inf.0000258698.98370.89. [PubMed] [CrossRef] [Google Scholar]
32. Хоуп В., Сейбел Н.Л., Шварц К.Л., Арриета А., Флинн П., Шад А., Альбано Э., Кейрнс Дж.Дж., Буэлл Д.Н., Гамбо Т., и другие. Популяционная фармакокинетика микафунгина у педиатрических пациентов и значение противогрибкового дозирования. Антимикроб. Агенты Чемотер. 2007; 51:3714–3719. doi: 10.1128/AAC.00398-07. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
Популяционная фармакокинетика микафунгина у педиатрических пациентов и значение противогрибкового дозирования. Антимикроб. Агенты Чемотер. 2007; 51:3714–3719. doi: 10.1128/AAC.00398-07. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
33. Queiroz-Telles F., Berezin E., Leverger G., Freire A., van der Vyver A., Chotpitayasunondh T., Konja J. , Diekmann-Berndt H., Koblinger S., Groll A.H., et al. Микафунгин в сравнении с липосомальным амфотерицином В у детей с инвазивным кандидозом: подисследование рандомизированного двойного слепого исследования. Педиатр. Заразить. Дис. Дж. 2008; 27:820–826. doi: 10.1097/INF.0b013e31817275e6. [PubMed] [CrossRef] [Академия Google]
34. Smith P.B., Walsh T.J., Hope W., Arrieta A., Takada A., Kovanda L.L., Kearns G.L., Kaufman D., Sawamoto T., Buell D.N., et al. Фармакокинетика повышенной дозы микафунгина у недоношенных новорожденных. Педиатр. Заразить. Дис. Дж. 2009; 28:412–415. doi: 10.1097/INF.0b013e3181910e2d. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Бенджамин Д.К., Арриета А., Кастро Л., Санчес П.Дж., Кауфман Д., Арнольд Л.Дж., Кованда Л.Л., Савамото Т., Буэлл Д.Н., Хоуп В. и др. Безопасность и фармакокинетика многократного приема микафунгина у детей раннего возраста. клин. Фармакол. тер. 2009 г.;87:93–99. doi: 10.1038/clpt.2009.200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Бенджамин Д.К., Арриета А., Кастро Л., Санчес П.Дж., Кауфман Д., Арнольд Л.Дж., Кованда Л.Л., Савамото Т., Буэлл Д.Н., Хоуп В. и др. Безопасность и фармакокинетика многократного приема микафунгина у детей раннего возраста. клин. Фармакол. тер. 2009 г.;87:93–99. doi: 10.1038/clpt.2009.200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Уолш Т.Дж., Гутель С., Джеллифф Р.В., Голден Дж.А., Литтл Э.А., ДеВо К., Микиен Д., Хейс М., Конте Дж.Э., Jr. Внутрилегочная фармакокинетика и фармакодинамика микафунгина у взрослых пациентов с трансплантацией легких. Антимикроб. Агенты Чемотер. 2010;54:3451–3459. doi: 10.1128/AAC.01647-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Хоуп В., Смит П.Б., Арриета А., Буэлл Д.Н., Рой М., Кайбара А., Уолш Т.Дж., Коэн-Волковиз М., Бенджамин Д.К., младший. Популяционная фармакокинетика микафунгина у новорожденных и детей раннего возраста. Антимикроб. Агенты Чемотер. 2010;54:2633–2637. doi: 10.1128/AAC.01679-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Арриета А.С., Мэддисон П., Гролл А.Х. Безопасность микафунгина в педиатрических клинических испытаниях. Педиатр. Заразить. Дис. Дж. 2011; 30:e97–e102. doi: 10.1097/INF.0b013e3182127eaf. [PubMed] [CrossRef] [Google Scholar]
39. Бохеннек К., Балан А., Мюллер-Шолден Л., Беккер М., Фаровски Ф., Мюллер К., Гролл А.Х., Лернбехер Т. Микафунгин два раза в неделю Противогрибковая профилактика у детей с высоким риском инвазивного грибкового заболевания. Дж. Антимикроб. Чемотер. 2015;70:1527–1530. дои: 10.1093/jac/dku544. [PubMed] [CrossRef] [Google Scholar]
40. Бенджамин Д.К., младший, Кауфман Д.А., Хоуп В.В., Смит П.Б., Арриета А., Манзони П., Кованда Л.Л., Ладемахер К., Исааксон Б., Еднаховски Д. ., и другие. Фаза 3 исследования микафунгина по сравнению с дезоксихолатом амфотерицина В у младенцев с инвазивным кандидозом. Педиатр. Заразить. Дис. Дж. 2018; 37:992–998. doi: 10.1097/INF.0000000000001996. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Кованда Л.Л., Уолш Т.Дж., Бенджамин Д., Арриета А., Кауфман Д., Смит П.Б., Манцони П., Десаи А.В., Кайбара А. , Бонате П. и др. Анализ воздействия микафунгина при кандидозе новорожденных: объединенный анализ двух клинических испытаний. Педиатр. Заразить. Дис. Дж. 2008; 37: 580–585. дои: 10.1097/INF.0000000000001957. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
Кованда Л.Л., Уолш Т.Дж., Бенджамин Д., Арриета А., Кауфман Д., Смит П.Б., Манцони П., Десаи А.В., Кайбара А. , Бонате П. и др. Анализ воздействия микафунгина при кандидозе новорожденных: объединенный анализ двух клинических испытаний. Педиатр. Заразить. Дис. Дж. 2008; 37: 580–585. дои: 10.1097/INF.0000000000001957. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
Фармакокинетическое и фармакодинамическое моделирование анидулафунгина (LY303366): переоценка его эффективности в моделях нейтропенических животных оппортунистических микозов с использованием оптимального отбора проб плазмы. Антимикроб. Агенты Чемотер. 2001; 45: 2845–2855. doi: 10.1128/AAC.45.10.2845-2855.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Бенджамин Д.К., Дрисколл Т., Сейбел Н.Л., Гонсалес С.Е., Роден М.М., Килару Р., Кларк К., Доуэлл Дж.А., Шранц Дж., Уолш Т.Дж. и др. Безопасность и фармакокинетика внутривенного введения анидулафунгина у детей с нейтропенией в группе высокого риска инвазивных грибковых инфекций.

 Ежедневное купание в теплой воде позволяет эффективно кожу очищать и увлажнять. При несоблюдении этих простых действий нарушается формирование здорового микробиома на коже малыша.
Ежедневное купание в теплой воде позволяет эффективно кожу очищать и увлажнять. При несоблюдении этих простых действий нарушается формирование здорового микробиома на коже малыша.