Удаление лейкоплакий слизистой в Уфе
- Главная
- Услуги и направления
- Отоларинголог (ЛОР)
- Удаление лейкоплакий слизистой полости рта
- Специалисты
- Оборудование
- Отзывы
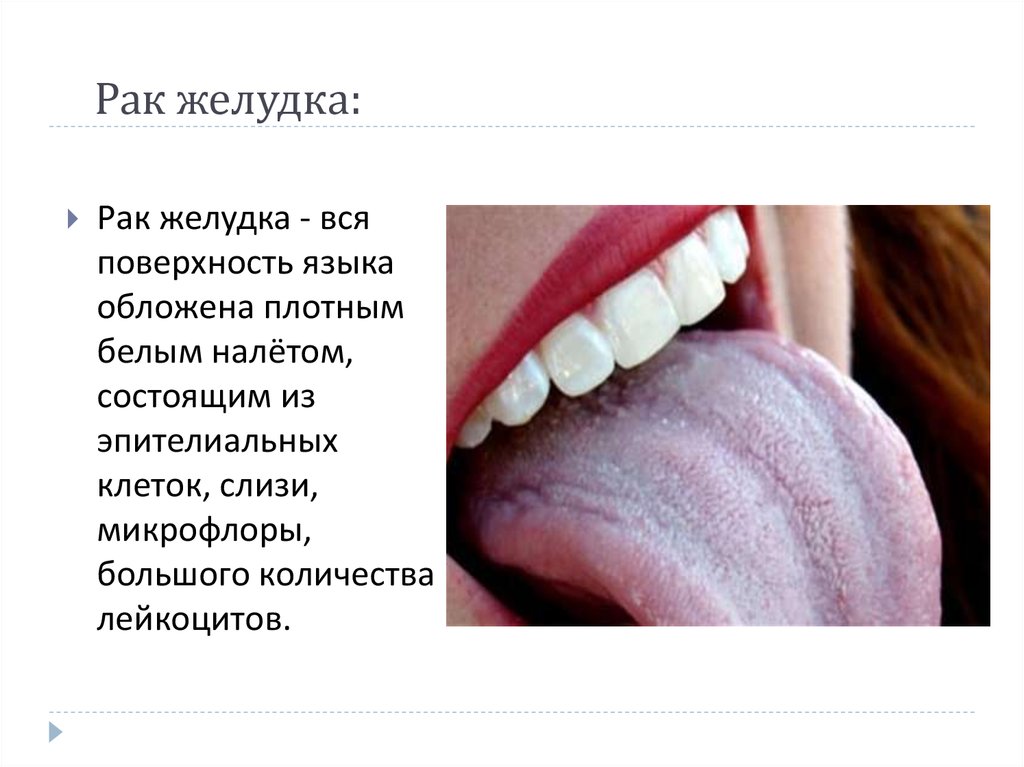
Лейкоплакия ротовой полости — заболевание, характеризующееся поражением слизистых оболочек, ороговением покровного эпителия разной степени выраженности. Чаще лейкоплакия локализуется на слизистой оболочке щёк, преимущественно у углов рта, на нижней губе, реже — на спинке или боковой поверхности языка, альвеолярном отростке и в области дна полости рта.
Причиной возникновения лейкоплакии является реакция слизистой оболочки на разнообразные раздражители.
Внутренние факторы — это прежде всего желудочно-кишечная патология, недостаток или нарушение обмена витамина А, снижение иммунитета и генетическая предрасположенность.
Внешние факторы — хроническая механическая травма(неправильно установленные коронки и мосты), больные зубы в запущенном состоянии, горячий табачный дым, инсоляция и другое.
Локализуется на слизистой оболочке нижней губы, угла рта, дна полости рта, языка, щёк (в двух последних случаях чаще располагается по линии смыкания зубов).
Имеет вид помутнения слизистой оболочки, напоминающего белесую пленку. В зависимости от интенсивности ороговения цвет поражения варьирует от бледно-серого до белого. Поверхность лейкоплакии сухая и слегка шероховатая. На щеках очаги лейкоплакии могут иметь складчатый вид, на дне полости рта — вид морщинистой пленки серовато-белого цвета.
Течение болезни.
Лейкоплакия — очень стойкая и упорная болезнь, характеризующаяся медленным течением и отсутствием болезненных ощущений на ранних стадиях развития.
Более поздние формы развития лейкоплакии отличаются возникновением трещин и эрозии в очаге поражения — тогда больной ощущает боль.
Все формы лейкоплакии потенциально способны озлокачествляться, при этом наибольшая частота озлокачествления наблюдается при локализации процесса на языке.
Лечение лейкоплакий лазерным способом
Все формы лейкоплакии крайне стойки к консервативной терапии, часты рецидивы, поэтому мы предлагаем в сочетании с консервативной терапией, лазерное удаление участков пораженной слизистой.
Удаление выполняется амбулаторно под местной анестезией в течение 15 — 20 минут. Обязательно проводится гистологическое исследование.
На период реабилитации 7-10 дней возможно оформление больничного листа.
Отдаленные результаты после лейкоплакии лазером показывают низкую частоту рецидивов. Удаление хирургическим лазером технически гораздо удобнее по сравнению с криодеструкцией и удалением обычными хирургическими инструментами.
Разина Наталия Викторовна стаж: более 22 лет Врач отоларинголог высшей категории, хирург лазеролог
Лазерный аппарат Лахта-МилонЛечение слизистой оболочки полости рта в Одинцово
- Maxima Clinic
- Стоматология
- Терапия
- Лечение слизистых оболочек полости рта
Вопрос / ответ
Задать вопрос
Слизистая оболочка полости рта постоянно подвергается воздействиям микробов и токсинов, а также – механическим, термическим, химическим. Сама она является чутким индикатором любых неполадок в работе внутренних органов и систем: при ослаблении хоть одного защитного фактора высок риск развития воспалительных заболеваний, характеризующихся болезненностью, отечностью, жжением, покраснением, появлением язвочек и эрозий. Если вы столкнулись с подобными симптомами, незамедлительно обратитесь за помощью к врачу-стоматологу.
Сама она является чутким индикатором любых неполадок в работе внутренних органов и систем: при ослаблении хоть одного защитного фактора высок риск развития воспалительных заболеваний, характеризующихся болезненностью, отечностью, жжением, покраснением, появлением язвочек и эрозий. Если вы столкнулись с подобными симптомами, незамедлительно обратитесь за помощью к врачу-стоматологу.
Какие заболевания слизистой оболочки полости рта бывают?
Самые распространенные: стоматит, глоссит, гингивит, хейлит, лейкоплакия.
Стоматит – общее название воспалительного процесса слизистой полости рта, характеризующегося различными проявлениями (в зависимости от этиологии): покраснением, отеком, появлением эрозированных участков, пузырьков, язвочек.
Гингивит – поражение слизистой оболочки десен, проявляющееся покраснением, кровоточивостью, отечностью.
Глоссит – глубокое или поверхностное воспаление тканей языка, характеризующееся появлением налета, покраснением, жжением, отеком, ограничением подвижности, потерей вкусовых ощущений и повышенным слюноотделением.
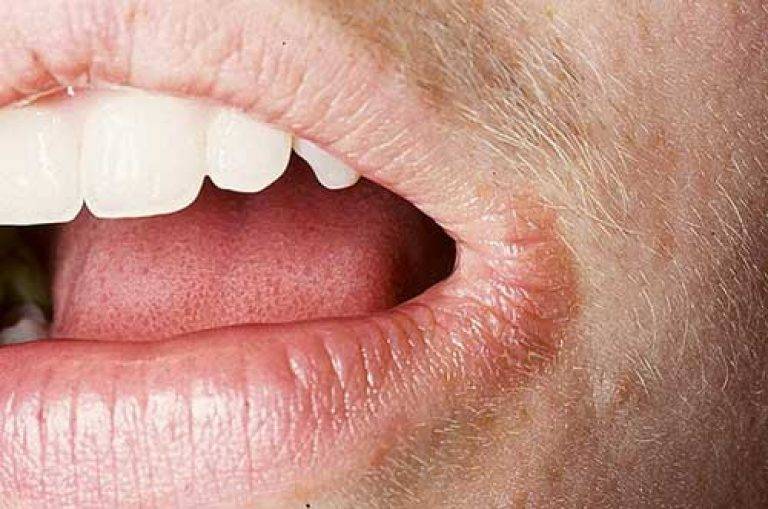
Хейлит (хейлоз) – воспалительный процесс, возникающий на слизистой оболочке полости рта и красной кайме губ. Основные симптомы: покраснение, жжение, боль при открывании рта и приеме пищи, появление язвочек, шелушение губ.
Лейкоплакия полости рта характеризуется образованием бляшек белого, серого или желтого цвета. Обычно заболевание никак не проявляет себя, иногда во рту бывают ощущения сухости и стянутости. В некоторых случаях лейкоплакия может злокачественно перерождаться, поэтому при обнаружении в полости рта каких-либо новообразований обратитесь за консультацией к врачу-стоматологу.
Диагностика и лечение
Чтобы правильно поставить диагноз при воспалении слизистой оболочки полости рта, опытному стоматологу нередко достаточно увидеть клиническую картину и выслушать субъективные жалобы пациента. В некоторых случаях врач может дать направление на аллергопробы или лабораторный анализ (ПЦР, бакпосев соскоба или мазка, гистологическое исследование).
При неподдающихся лечению заболеваниях слизистой оболочки полости рта показаны консультации других специалистов и общее обследование для выявления системных патологий, которые стали триггером болезни.
Факторы, влияющие на состояние слизистой ротовой полости:
- прием антибиотиков и других препаратов;
- нарушения гормонального фона;
- воспалительные процессы зубов и десен;
- травматические повреждения;
- снижение иммунитета;
- наличие воспалительных процессов и инфекций;
- авитаминоз;
- несбалансированное питание;
- генетическая предрасположенность;
- общее обезвоживание;
- вредные привычки (курение, употребление спиртных напитков).
Помимо этого, нередко патологические изменения слизистой полости рта могут быть связаны с нарушениями других органов и систем организма: например, сердечно-сосудистой или ЖКТ; эндокринными расстройствами, аллергией, дерматозами, заболеваниями крови, туберкулезом, СПИДом.
Записаться на прием к врачу-стоматологу MAXIMA CLINIC в Одинцово можно через специальную форму на сайте или по номеру: 8(499)755-55-01.
Заказать оборатный звонок
Ваше имя Номер телефона Отправить Нажимая на кнопку, я соглашаюсь на обработку персональных данныхТеоретические основы автоматизированной диагностики лейкоплакии полости рта: Предварительный отчет Целью данного исследования является предложение эффективного алгоритма анализа текстуры для диагностики лейкоплакии полости рта. В это исследование были включены 35 пациентов с лейкоплакией. Внутриротовые фотографии нормальной слизистой оболочки полости рта и лейкоплакии были сделаны и обработаны для анализа текстуры. Были проанализированы две характеристики текстуры, матрица длин серий и матрица совпадений.
 Разницу проверяли с помощью ANOVA. Проведен факторный анализ и классификация искусственной нейронной сетью. Результаты выявили легкую возможную дифференциацию лейкоплакии от нормальной слизистой оболочки (). Дискриминация нейронной сети показывает полное распознавание лейкоплакии (чувствительность 100%) и специфичность 97%. Этот объективный анализ в нейронной сети показал, что включение 3 текстурных признаков в оптический анализ слизистой оболочки полости рта приводит к правильной диагностике лейкоплакии. Применение текстурного анализа при лейкоплакии является перспективным методом диагностики.
Разницу проверяли с помощью ANOVA. Проведен факторный анализ и классификация искусственной нейронной сетью. Результаты выявили легкую возможную дифференциацию лейкоплакии от нормальной слизистой оболочки (). Дискриминация нейронной сети показывает полное распознавание лейкоплакии (чувствительность 100%) и специфичность 97%. Этот объективный анализ в нейронной сети показал, что включение 3 текстурных признаков в оптический анализ слизистой оболочки полости рта приводит к правильной диагностике лейкоплакии. Применение текстурного анализа при лейкоплакии является перспективным методом диагностики. 1. Введение
Лейкоплакия полости рта представляет собой наиболее распространенное потенциально злокачественное заболевание полости рта [1]. Это белое пятно или бляшка, которые нельзя охарактеризовать ни клинически, ни патологически, как любое другое заболевание. Это классическое определение лейкоплакии, представленное Всемирной организацией здравоохранения. Этиология лейкоплакии многофакторна. Наиболее важными факторами являются алкоголь, курение сигарет, плохая гигиена полости рта, электрогальванические токи и острая пища, раздражающая слизистую оболочку полости рта. Вероятность злокачественного перерождения лейкоплакии находится в пределах от 0,2% до 5% [2]. Из-за риска злокачественного перерождения важно поставить правильный диагноз. Золотым стандартом диагностики по-прежнему остается гистопатологическое исследование, но инвазивность является основным недостатком этого исследования. Флуоресценция или аутофлуоресценция поражений используются в некоторых диагностических системах, таких как ViziLite®, ViziLite®PLUS, VELscope®, Identafi® и Orascoptic DK [3, 4]. Огромная волна электрооптических устройств является основой для изменения онкологической профилактики плоскоклеточного рака полости рта. Существуют простые аналогичные аппараты, такие как VELscope и Microlux, в которых используется флуоресцентный или светодиодный свет. К сожалению, их специфичность очень низкая.
Наиболее важными факторами являются алкоголь, курение сигарет, плохая гигиена полости рта, электрогальванические токи и острая пища, раздражающая слизистую оболочку полости рта. Вероятность злокачественного перерождения лейкоплакии находится в пределах от 0,2% до 5% [2]. Из-за риска злокачественного перерождения важно поставить правильный диагноз. Золотым стандартом диагностики по-прежнему остается гистопатологическое исследование, но инвазивность является основным недостатком этого исследования. Флуоресценция или аутофлуоресценция поражений используются в некоторых диагностических системах, таких как ViziLite®, ViziLite®PLUS, VELscope®, Identafi® и Orascoptic DK [3, 4]. Огромная волна электрооптических устройств является основой для изменения онкологической профилактики плоскоклеточного рака полости рта. Существуют простые аналогичные аппараты, такие как VELscope и Microlux, в которых используется флуоресцентный или светодиодный свет. К сожалению, их специфичность очень низкая.
Цифровые изображения состоят из пикселей. Пиксели строят узоры, которые создают текстуру. Математический и статистический анализ текстурных узоров известен как текстурный анализ (ТА). Методы ТА основаны на математическом анализе матрицы, представляющей распределение яркости пикселей в изображении. Текстурный анализ можно разделить на четыре метода: статистический, структурный, модельный и трансформационный [5, 6]. ТА обычно используется в медицине для анализа рентгеновских снимков, изображений компьютерной томографии или магнитно-резонансных изображений. Внутриротовые цифровые фотографии лейкоплакии кажутся хорошим материалом для анализа текстуры, что будет полезно при ранней диагностике.
Пиксели строят узоры, которые создают текстуру. Математический и статистический анализ текстурных узоров известен как текстурный анализ (ТА). Методы ТА основаны на математическом анализе матрицы, представляющей распределение яркости пикселей в изображении. Текстурный анализ можно разделить на четыре метода: статистический, структурный, модельный и трансформационный [5, 6]. ТА обычно используется в медицине для анализа рентгеновских снимков, изображений компьютерной томографии или магнитно-резонансных изображений. Внутриротовые цифровые фотографии лейкоплакии кажутся хорошим материалом для анализа текстуры, что будет полезно при ранней диагностике.
С одной стороны, в настоящее время в стоматологии популярна внутриротовая макрофотография цифровой камерой с одним объективом или компактной системной камерой. С другой стороны, получение эндоскопического изображения в полости рта возможно и челюстно-лицевыми хирургами, ЛОР-врачами или гастроэнтерологами. Ранее упомянутые методы могут быть потенциальным источником изображений, которые можно анализировать с помощью ТА.
Электронная, теле- и автоматическая диагностика возможна в десятилетие, когда у каждого врача есть смартфон. Соответствующие маленькие камеры и светодиодная подсветка есть во всех телефонах, а многие электрооптические устройства доступны в стоматологических или медицинских центрах. Незначительное развитие отмечается в области специализированного программного обеспечения.
Целью данного исследования было создание базы системы дистанционной диагностики лейкоплакии полости рта.
2. Материалы и методы
2.1. Пациенты
В исследование были включены 35 пациентов с лейкоплакией. Все поражения были гистопатологически верифицированы (со стандартной окраской гематоксилином и эозином) после взятия образца с патологически измененной слизистой оболочки полости рта под местной анестезией. Средний возраст исследуемой группы составил 58 лет. Критерием исключения была дисплазия высокой степени.
Интраоральная фотография нормальной слизистой оболочки полости рта и лейкоплакии была сделана с помощью цифровой камеры Canon EOS 500D (Canon, Ота, Токио, Япония) с макрокольцом 13 мм, 50 мм, объективом f1,8 (Canon, Ота, Токио, Япония). ) и кольцевой фонарик YN-14EX (YONGNUO Photographic Equipment, Longhua District, Shenzhen, China). Все фотографии были сделаны с одного и того же расстояния (для его достижения была зафиксирована дистанция фокусировки), а оптическая ось объектива была перпендикулярна исследуемому поражению. На объектив камеры был наложен поляризованный фильтр, чтобы уменьшить любые отражения. Непосредственно перед фотографированием пораженная слизистая подсушивалась, чтобы уменьшить риск появления отражений.
) и кольцевой фонарик YN-14EX (YONGNUO Photographic Equipment, Longhua District, Shenzhen, China). Все фотографии были сделаны с одного и того же расстояния (для его достижения была зафиксирована дистанция фокусировки), а оптическая ось объектива была перпендикулярна исследуемому поражению. На объектив камеры был наложен поляризованный фильтр, чтобы уменьшить любые отражения. Непосредственно перед фотографированием пораженная слизистая подсушивалась, чтобы уменьшить риск появления отражений.
Все процедуры проводились после получения одобрения Комитета по этике Вроцлавского медицинского университета, Польша (разрешение № KB-367/2014).
2.2. Предварительная обработка изображений
Все графические операции выполнялись в GIMP версии 2.10.8 (программа обработки изображений GNU, https://www.gimp.org/). В центре поражения была выбрана область интереса (ROI) размером 300 × 300 пикселей. Лейкоплакия ROI была выбрана в центре поражения, без ссылки на здоровую слизистую оболочку. Эталонная область интереса слизистой оболочки была выбрана из той же области, например, если поражение было на языке, эталонная область интереса была выбрана на языке. Такой подготовленный фрагмент изображения был отрезан от оригинальной фотографии. Для достижения максимально возможной контрастности фотографии был применен фильтр верхних частот. После этого инструменты уровня использовались для выравнивания гистограммы изображения (для унификации контраста всех изображений). Затем изображения были преобразованы в 4-битную шкалу серого. Файл был сохранен в формате TIFF без каких-либо алгоритмов сжатия. Все графические операции показаны на рис. 1. Область интереса выбиралась без видимых отражений во всех случаях.
Эталонная область интереса слизистой оболочки была выбрана из той же области, например, если поражение было на языке, эталонная область интереса была выбрана на языке. Такой подготовленный фрагмент изображения был отрезан от оригинальной фотографии. Для достижения максимально возможной контрастности фотографии был применен фильтр верхних частот. После этого инструменты уровня использовались для выравнивания гистограммы изображения (для унификации контраста всех изображений). Затем изображения были преобразованы в 4-битную шкалу серого. Файл был сохранен в формате TIFF без каких-либо алгоритмов сжатия. Все графические операции показаны на рис. 1. Область интереса выбиралась без видимых отражений во всех случаях.
2.3. Текстурный анализ
Оптические изображения (300 × 300 пикселей) из 35 случаев были преобразованы в 4-битные графические файлы в градациях серого, импортированные в программное обеспечение MaZda 4.6 (Технический университет Лодзи, Польша), и был выполнен анализ текстуры (рис. 2) [7]. , 8]. Были выбраны шесть текстурных признаков: две из матрицы длин серий (обратные моменты долгосрочного акцента и обратные моменты краткосрочного акцента), две из матрицы совместного появления (энтропия, как показано на рисунке 3, и разностная энтропия, рассчитанная на расстоянии 5 пикселей), и два вейвлет-преобразования Хаара (энергия вейвлета после двумерного фильтра нижних частот и масштаб 5 и масштаб 6 преобразования) [9–11].
2) [7]. , 8]. Были выбраны шесть текстурных признаков: две из матрицы длин серий (обратные моменты долгосрочного акцента и обратные моменты краткосрочного акцента), две из матрицы совместного появления (энтропия, как показано на рисунке 3, и разностная энтропия, рассчитанная на расстоянии 5 пикселей), и два вейвлет-преобразования Хаара (энергия вейвлета после двумерного фильтра нижних частот и масштаб 5 и масштаб 6 преобразования) [9–11].
Пусть p ( i , j ) будет числом раз, когда существует серия длиной j с уровнем серого i . Пусть — количество уровней серого, а N r — количество прогонов [12]. Ниже приведены определения параметров матрицы длин серий p ( i , j ). Акцент на обратных моментах в долгосрочной перспективе: Акцент на обратных моментах в краткосрочной перспективе: где коэффициент C is defined as
The co-occurrence matrix-derived parameters are defined by the equations that follow, where μ x , μ y , and σ x и σ y обозначают среднее и стандартное отклонение сумм строк и столбцов матрицы совпадения соответственно, которые связаны с маргинальными распределениями p x ( i ) и p y ( j ). Энтропия: Разностная энтропия:
Энтропия: Разностная энтропия:
Для дискретного вейвлет-преобразования Хаара выполнен расчет энергии для частотного 2D поддиапазона после прохождения фильтра нижних частот ( L ) в масштабах 5 и 6: где d – вейвлет-коэффициент, и n — количество пикселей в интересующей области (ROI, т. е. все изображение, представленное на рис. 3 в верхнем ряду), оба при 5 -я и 6 -я весы и поддиапазон LL. ROI уменьшаются в последовательных масштабах, чтобы соответствовать размерам изображения поддиапазона. Выходом этой процедуры является вектор признаков, содержащих энергии вейвлет-коэффициентов, рассчитанных в поддиапазоне LL на масштабах 5 th и 6 th .
Дисперсионный анализ проводили в программе Statgraphics Centurion XVI. Затем процедура использует вероятностную нейронную сеть (PNN в программном обеспечении Statgraphics Centurion XVI) для классификации случаев по разным диагнозам на основе 3 входных переменных (входные факторы были сильными отвлекающими факторами анализа этого изображения: краткосрочный акцент, обратные моменты, энтропия и вейвлет). энергии преобразования в масштабе 5 из 35 случаев (рис. 4).
энергии преобразования в масштабе 5 из 35 случаев (рис. 4).
2.4. Статистический анализ
Критерий Шапиро-Уилка был применен для проверки нормальности. Был применен однофакторный дисперсионный анализ (ANOVA). Различие считалось достоверным, если . Statgraphics Centurion 18 ver.18.1.12 (StarPoint Technologies, Inc., Вирджиния, США).
3. Результаты
Сводная статистика отдельных структурных признаков слизистой оболочки полости рта представлена в таблице 1. Частота артефактов краткосрочных акцентов обратных моментов значительно снижается при лейкоплакическом поражении (). Оба метода расчета энтропии выявляют их снижение при патологии (разность энтропии и энтропии, рис. 5). Наложение на текстурный узор самое высокое (энергия самая высокая) для вейвлет-преобразования Хаара, рассматриваемого в масштабах 5 и 6.
Дискриминация нейронной сети показывает (рис. 6) полное распознавание лейкоплакии (чувствительность 100%) и специфичность 97%. Все изображения лейкоплакии были описаны правильно, а одно изображение нормальной слизистой оболочки было классифицировано как патологическое поражение.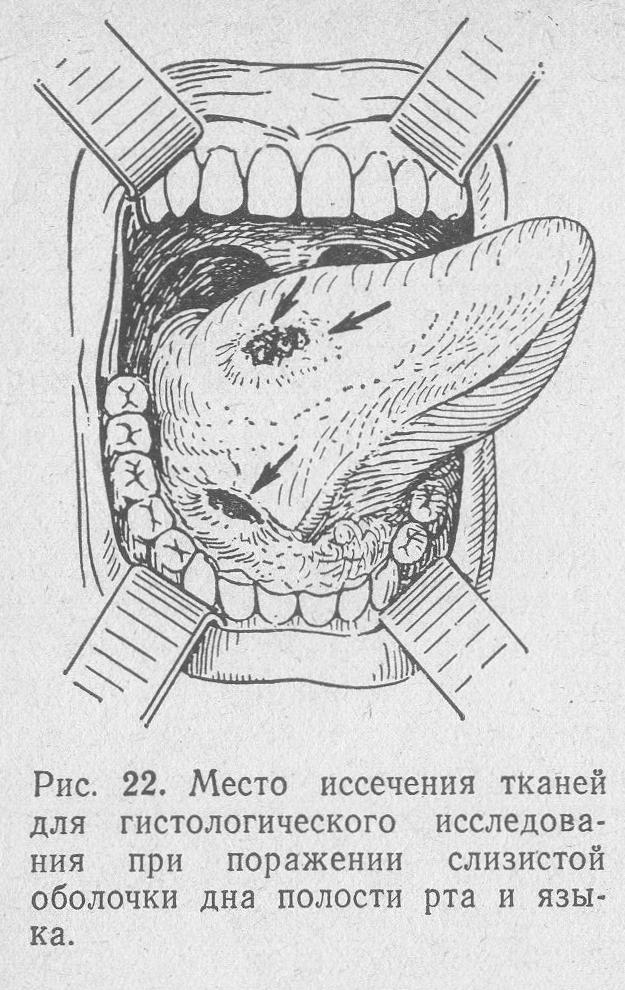
4. Обсуждение
Sambandham et al. применяли систему ViziLite при диагностике лейкоплакии. Их исследование показывает, что чувствительность и специфичность ViziLite составляют около 77,3% и 27,8% соответственно [13]. Макинтош и др. выявили, что система Microlux/DL показала чувствительность 77,8% и специфичность 70,7% при диагностике лейкоплакии [14]. Ибрагим и др. показали, что даже добавление красителя толуидинового синего не улучшало эффективность системы Microlux/DL. В том же исследовании они показали, что чувствительность Microlux/DL составила 100%, а специфичность — 32,4% для визуализации подозрительных предраковых поражений при рассмотрении биопсии как золотого стандарта [15].
Лалла и др. подтвердили, что можно обнаружить дисплазию эпителия полости рта с помощью отражательной спектроскопии (Identafi и DentalEZ). Их исследование показало, что система Identafi при фиолетовом свете обеспечивает чувствительность 12,5% и специфичность 85,4% для обнаружения дисплазии эпителия полости рта. Важно знать, что для интерпретации результатов аутофлуоресцентного исследования требуется высокий уровень клинического опыта [16].
Важно знать, что для интерпретации результатов аутофлуоресцентного исследования требуется высокий уровень клинического опыта [16].
Чан и др. использовали текстурный анализ при обнаружении микрокальцинатов на маммограммах. Их результат показывает, что компьютерный анализ текстуры может извлекать маммографическую информацию, которая не видна при визуальном осмотре. Эти исследования показывают, что уровень специфичности был 39%, а уровень чувствительности 100 % [17]. Наши результаты были одинаковыми по уровню чувствительности, но намного выше по специфичности (97%). Ли и др. Исследования также подтвердили, что маммографический анализ текстуры является надежным методом дифференциальной диагностики доброкачественных и злокачественных опухолей молочной железы. Кроме того, сочетание диагностики на основе изображений и анализа текстуры может значительно повысить эффективность диагностики [18].
Моменты обратного акцента короткого промежутка времени обнаруживают короткие линии пикселей, которые имеют одинаковую яркость. Их присутствие на изображении слизистой является нормальным состоянием. По мере исчезновения коротких линий развивается лейкоплакия. Точно так же энтропия и разностная энтропия указывают области, где существует мелкое гнездо текстуры поверхности слизистой оболочки. При патологическом поражении эта тонкая текстура исчезает, превращаясь в участки белого цвета, т. е. участки лейкоплакии. Результаты вейвлет-преобразования Хаара свидетельствуют о том, что патологические очаги лейкоплакии достаточно протяженны из-за значительного масштаба вейвлет-преобразования (шкала 5 и 6), которые могут накладываться на патологическую текстуру. Это еще раз указывает на то, что слизистая оболочка полости рта утратила свой физиологический тонкий текстурный вид.
Их присутствие на изображении слизистой является нормальным состоянием. По мере исчезновения коротких линий развивается лейкоплакия. Точно так же энтропия и разностная энтропия указывают области, где существует мелкое гнездо текстуры поверхности слизистой оболочки. При патологическом поражении эта тонкая текстура исчезает, превращаясь в участки белого цвета, т. е. участки лейкоплакии. Результаты вейвлет-преобразования Хаара свидетельствуют о том, что патологические очаги лейкоплакии достаточно протяженны из-за значительного масштаба вейвлет-преобразования (шкала 5 и 6), которые могут накладываться на патологическую текстуру. Это еще раз указывает на то, что слизистая оболочка полости рта утратила свой физиологический тонкий текстурный вид.
Этот объективный анализ в нейронной сети показал, что включение 3 текстурных особенностей в оптический анализ слизистой оболочки полости рта приводит к правильной диагностике лейкоплакии. Один нормальный образец слизистой оболочки полости рта был признан патологией, вероятно, в связи с субклиническим развитием патологии в слизистой оболочке.
Предложенные 5 или менее признаков текстуры слизистой оболочки полости рта, наблюдаемых при естественном или искусственном освещении, могут быть использованы для разработки простого приложения для смартфона, позволяющего значительно улучшить вероятность лейкоплакии слизистой оболочки полости рта.
5. Выводы
Применение анализа текстуры лейкоплакии полости рта по сравнению со здоровой слизистой оболочкой является перспективным диагностическим методом, который может быть основой системы дистанционной и полуавтоматической диагностики.
Доступность данных
Данные, подтверждающие результаты этого исследования, можно получить у соответствующего автора по обоснованному запросу.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Авторы выражают благодарность Лодзинскому медицинскому университету (гранты №№ 503/5-061-02/503-51-001 и 503/5-061-02/503-51-002) и Вроцлавскому медицинскому университету (грант № PBMN-152) за их поддержку.
Ссылки
-
S. Suwasini, K. Chatterjee, S.K. Purkait, D. Samaddar, A. Chatterjee и M. Kumar, «Экспрессия белка P53 и антигена Ki-67 при лейкоплакии полости рта с различными гистопатологическими степенями эпителиального дисплазия», Journal of International Society of Preventive and Community Dentistry , том. 8, нет. 6, стр. 513–522, 2018 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
К. С. Арора, А. Найяр, П. Каур, К. С. Арора, А. Гоэл и С. Сингх, «Оценка коллагена при лейкоплакии, подслизистом фиброзе полости рта и плоскоклеточном раке полости рта с использованием поляризационной микроскопии и иммуногистохимии, Asian Pacific Journal of Cancer Prevention , vol. 19, нет. 12, стр. 1075–1080, 2018.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
M.
 Mascitti, G. Orsini, V. Tosco et al., «Обзор современных неинвазивных диагностических устройств в оральной онкологии», Frontiers in Physiology , vol. 9, с. 1510, 2018.
Mascitti, G. Orsini, V. Tosco et al., «Обзор современных неинвазивных диагностических устройств в оральной онкологии», Frontiers in Physiology , vol. 9, с. 1510, 2018. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Л. Л. Паттон, Дж. Б. Эпштейн и А. Р. Керр, «Дополнительные методы обследования полости рта и диагностики поражений: систематический обзор литературы», Журнал Американской стоматологической ассоциации , том. 139, нет. 7, стр. 896–905, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Скоч, Д. Йирак, П. Вихнановска и др., «Классификация МРТ-изображений икроножных мышц с помощью анализа текстуры», Магнитно-резонансные материалы в физике, , том. 16, нет. 6, стр. 259–267, 2004.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д.
 Йирак, М. Дезортова, П. Таймр и М. Хайек, «Анализ текстуры печени человека», Журнал магнитно-резонансной томографии , том. 15, нет. 1, стр. 68–74, 2002.
Йирак, М. Дезортова, П. Таймр и М. Хайек, «Анализ текстуры печени человека», Журнал магнитно-резонансной томографии , том. 15, нет. 1, стр. 68–74, 2002. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
P. Szczypinski, M. Strzelecki и A. Materka, «MaZda — программное обеспечение для анализа текстур», в Proceedings of the ISITC , стр. 245–249, Джоенджу, Южная Корея, ноябрь 2007 г.
Посмотреть по адресу:
Google Scholar
-
П. Щипинский, М. Стшелецкий, А. Матерка и А. Клепачко, «MaZda — программный пакет для анализа текстуры изображения», Компьютерные методы и программы в биомедицине , vol. 94, нет. 1, стр. 66–76, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
J.
 Hadrowicz, P. Hadrowicz, A. Gesing и M. Kozakiewicz, «Возрастные изменения в кости, окружающей зубные имплантаты», Dental and Medical Problems , vol. 51, стр. 27–34, 2014.
Hadrowicz, P. Hadrowicz, A. Gesing и M. Kozakiewicz, «Возрастные изменения в кости, окружающей зубные имплантаты», Dental and Medical Problems , vol. 51, стр. 27–34, 2014. Просмотр по адресу:
Google Scholar
-
М. Колачиньски, М. Козакевич и А. Матерка, «Текстурная энтропия как потенциальная характеристика для количественной оценки заживления челюстной кости процесс», Архив медицинских наук , том. 1, стр. 78–84, 2015 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
М. Козакевич, П. Хадрович, Дж. М. Хадрович и А. Гесинг, «Может ли сила скручивания во время установки зубных имплантатов в сочетании с минеральной плотностью кости поясничного отдела позвоночника быть факторами прогнозирования изменений структуры альвеолярного гребня?» Стоматологические и медицинские проблемы , том.
 51, нет. 4, стр. 448–457, 2014.
51, нет. 4, стр. 448–457, 2014. Посмотреть по адресу:
Google Scholar
-
Р. М. Харалик, К. Шанмугам и И. Х. Динштейн, «Текстурные признаки для классификации изображений», IEEE Transactions on Systems, Man, and Cybernetics , vol. СМС-3, нет. 6, стр. 610–621, 1973.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Т. Самбандхам, К. М. Мастан, М. С. Кумар и А. Джа, «Применение визилита при раке полости рта», Журнал клинических и диагностических исследований: JCDR , vol. 7, нет. 1, стр. 185-186, 2013.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Л. Макинтош, М. Дж. Маккалоу и К. С. Фарах, «Оценка освещения рассеянным светом и ополаскивания уксусной кислотой (микролюкс/DL) при визуализации поражений слизистой оболочки полости рта», Oral Oncology , vol.
 45, нет. 12, стр. e227–e231, 2009.
45, нет. 12, стр. e227–e231, 2009. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
С. С. Ибрагим, С. А. Аль-Аттас, З. Э. Дарвиш, Х. А. Амер и М. Х. Хассан, «Эффективность хемилюминесцентного устройства microlux/DLTM при скрининге потенциально злокачественных и злокачественных поражений полости рта», Азиатско-Тихоокеанский журнал по профилактике рака , том. 15, нет. 15, стр. 6081–6086, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ю. Лалла, М. А. Т. Матиас и К. С. Фарах, «Оценка поражений слизистой оболочки полости рта с помощью аутофлуоресцентной визуализации и отражательной спектроскопии», Журнал Американской стоматологической ассоциации , том. 147, нет. 8, стр. 650–660, 2016.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Х.
 -П. Чан, Б. Сахинер, Н. Петрик и др., «Компьютерная классификация злокачественных и доброкачественных микрокальцинатов на маммограммах: анализ текстуры с использованием искусственной нейронной сети», Physics in Medicine and Biology , vol. 42, нет. 3, стр. 549–567, 1997.
-П. Чан, Б. Сахинер, Н. Петрик и др., «Компьютерная классификация злокачественных и доброкачественных микрокальцинатов на маммограммах: анализ текстуры с использованием искусственной нейронной сети», Physics in Medicine and Biology , vol. 42, нет. 3, стр. 549–567, 1997. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Z. Li, L. Yu, X. Wang et al., «Диагностическая эффективность маммографического анализа текстуры в дифференциальной диагностике доброкачественных и злокачественных опухолей молочной железы», Клинический рак молочной железы , vol. 18, нет. 4, стр. e621–e627, 2018 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Copyright
Copyright © 2020 Kamil Jurczyszyn et al. Это статья с открытым доступом, распространяемая в соответствии с лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Оральная лейкоплакия: современный взгляд на диагностику, лечение, общение с пациентами и исследования
Введение
Заболеваемость раком ротовой полости, в основном представленным плоскоклеточным раком, во всем мире колеблется от менее трех до семи или восьми на 100 000 населения. Заболевания чаще всего поражают людей среднего и пожилого возраста. Наиболее важными этиологическими факторами являются пристрастие к табаку и употребление алкоголя. Вирус папилломы человека играет ограниченную роль в этиологии рака ротовой полости, в отличие от его роли в раке ротоглотки. Лечение состоит из хирургического вмешательства с дополнительной лучевой терапией и химиотерапией или без них. Выживаемость очень сильно зависит от стадии заболевания на момент постановки диагноза. На всех стадиях вместе выживает около 60% пациентов.
Большинству, если не всем, плоскоклеточному раку полости рта предшествуют клинически видимые, но в остальном часто бессимптомные изменения слизистой оболочки полости рта. Такие изменения чаще бывают преимущественно белыми. Такие потенциально злокачественные или, как некоторые предпочитают, потенциально предраковые беловатые поражения обозначаются как лейкоплакии полости рта (рис. 1).
Такие изменения чаще бывают преимущественно белыми. Такие потенциально злокачественные или, как некоторые предпочитают, потенциально предраковые беловатые поражения обозначаются как лейкоплакии полости рта (рис. 1).
Лейкоплакия дна полости рта
Изображение в полный размер
На совещании, проведенном при поддержке Всемирной организации здравоохранения, лейкоплакия полости рта была определена как «преимущественно белая бляшка сомнительного риска, исключающая (другое) известные заболевания или расстройства, которые не несут повышенного риска развития рака» [1]. Было добавлено, что лейкоплакия является клиническим термином и не имеет специфической гистологии. В недавнем отчете было предложено несколько упростить определение лейкоплакии до «преимущественно белого, не поддающегося стиранию поражения слизистой оболочки полости рта, исключающего другие четко определенные преимущественно белые поражения клинически, гистопатологически или с помощью других диагностических методов». вспомогательные средства [2].
вспомогательные средства [2].
Предполагаемая распространенность лейкоплакии полости рта составляет приблизительно 0,1%, но может различаться в разных частях мира. Четких гендерных предпочтений нет. Оральная лейкоплакия в основном возникает в возрасте старше 30–40 лет и гораздо чаще встречается у курильщиков, чем у некурящих. Возможная этиологическая роль алкоголя менее ясна, чем в этиологии рака ротовой полости. Сообщаемый ежегодный риск злокачественной трансформации лейкоплакии полости рта варьирует в многочисленных исследованиях по этому вопросу и колеблется от 2 до 3% или даже намного выше. Рак может развиться на месте или рядом с местом лейкоплакии или в другом месте в полости рта и в области головы и шеи.
Существует множество статистически полезных прогностических факторов злокачественной трансформации, таких как размер поражения, клинический подтип, оральный участок и наличие или отсутствие эпителиальной дисплазии, но они ненадежны для использования у отдельных лиц. пациент. Это также относится к различным молекулярным маркерам, о которых сообщалось в последние десятилетия как о возможных прогностических маркерах злокачественной трансформации [2, 3]. В литературе продолжаются споры о том, эффективно ли лечение лейкоплакии полости рта для предотвращения злокачественной трансформации.
пациент. Это также относится к различным молекулярным маркерам, о которых сообщалось в последние десятилетия как о возможных прогностических маркерах злокачественной трансформации [2, 3]. В литературе продолжаются споры о том, эффективно ли лечение лейкоплакии полости рта для предотвращения злокачественной трансформации.
Диагностические проблемы
На основании настоящего определения диагноз лейкоплакии ставится путем исключения известных, четко определенных поражений и нарушений, которые могут возникать на слизистой оболочке полости рта, как указано в таблице 1 [2]. В результате определения ВОЗ лейкоплакии полости рта точность клинического диагноза во многом зависит от опыта врача. В зависимости от клинической картины и при отсутствии симптомов может быть оправдана постановка диагноза лейкоплакии полости рта без взятия биопсии. Менее опытным клиницистам рекомендуется направить пациента либо к более опытному врачу, либо сделать биопсию, чтобы исключить какое-либо известное, четко определенное заболевание, а также сообщить о возможном наличии и степени эпителиальной дисплазии или даже карциномы (в место). Следует признать, что при больших или множественных лейкоплакиях полости рта инцизионная биопсия не может быть репрезентативной для всего поражения [4]. Кроме того, даже при биопсии беловатых поражений окончательный диагноз лейкоплакии полости рта может оставаться под вопросом, например, в некоторых случаях красного плоского лишая. В настоящее время нет молекулярных маркеров или набора маркеров, которые позволили бы более точно поставить правильный диагноз лейкоплакии полости рта.
Следует признать, что при больших или множественных лейкоплакиях полости рта инцизионная биопсия не может быть репрезентативной для всего поражения [4]. Кроме того, даже при биопсии беловатых поражений окончательный диагноз лейкоплакии полости рта может оставаться под вопросом, например, в некоторых случаях красного плоского лишая. В настоящее время нет молекулярных маркеров или набора маркеров, которые позволили бы более точно поставить правильный диагноз лейкоплакии полости рта.

В идеале диагноз лейкоплакии полости рта должен ставиться в результате тесного сотрудничества клиницистов и патологоанатомов, по крайней мере, при наличии биопсии или хирургического образца. Однако в повседневной практике такое сотрудничество, вероятно, имеет ограниченную ценность из-за отсутствия опыта гистопатологии у клиницистов и отсутствия клинического опыта у патологоанатомов. Тем не менее, клиницист должен предоставить надлежащую клиническую информацию (можно задаться вопросом, что на самом деле является релевантной информацией в случае подозрения на лейкоплакию полости рта) и должен поставить дифференциальный диагноз, если это применимо для патологоанатома. Кроме того, клиницист должен четко указать, какую информацию он ищет, например, наличие эпителиальной дисплазии, поскольку это может, правильно или неправильно, повлиять на дальнейшее ведение пациента. С другой стороны, патологоанатом должен правильно ответить на вопросы, поставленные клиницистом, и должен сообщить о результатах в форме, понятной клиницисту. Отчет патологоанатома рекомендуется четко разделить на две части, причем одна часть используется только для описания и оценки гистопатологических и, если применимо, иммуногистохимических данных.
Отчет патологоанатома рекомендуется четко разделить на две части, причем одна часть используется только для описания и оценки гистопатологических и, если применимо, иммуногистохимических данных.
Проблемы в лечении
Методы лечения
Прекращение курения, если таковое имеется, может привести к регрессии или даже исчезновению поражения. Спонтанный регресс лейкоплакии полости рта встречается редко. В стойких случаях лечение лейкоплакии полости рта традиционно заключалось в хирургическом удалении, если это возможно. В то же время появилось множество других методов лечения, таких как криохирургия, лазерное лечение, либо испарение CO 2 , либо различные нехирургические методы лечения, такие как применение ретиноидов, бета-каротина, добавок витамина С, блеомицина и 5 -фторурацил. Совсем недавно фотодинамическая терапия с использованием местного или системного введения фотосенсибилизатора была добавлена к широкому кругу вариантов лечения. Некоторые из нехирургических методов лечения должны использоваться постоянно и могут иметь серьезные побочные эффекты.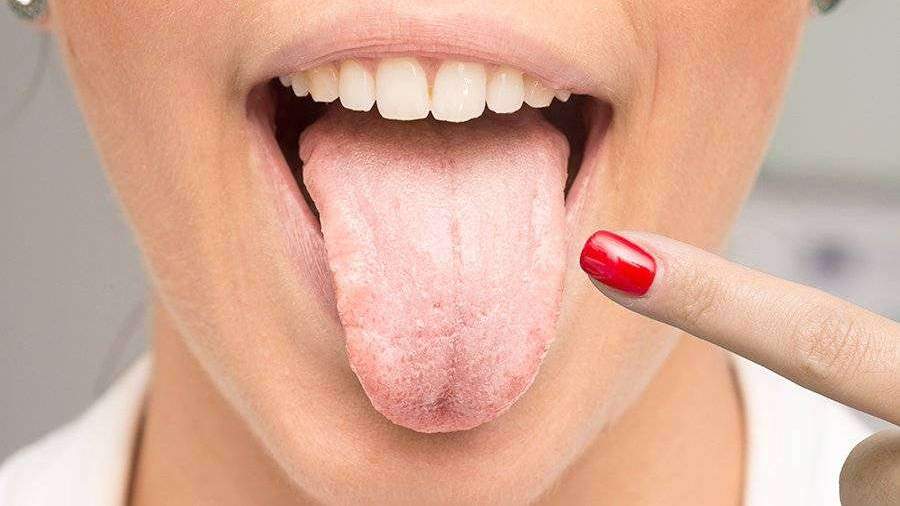
Независимо от типа лечения могут возникать местные рецидивы и новые оральные лейкоплакии могут возникать в других местах ротовой полости, и ни один из методов лечения, по-видимому, не снижает риск злокачественной трансформации [5]. Некоторые авторы подняли вопрос о том, действительно ли хирургическое удаление лейкоплакии полости рта может нести повышенный риск развития рака [6]. Еще в другом исследовании было показано, что отказ от курения после хирургического удаления лейкоплакии полости рта снижает риск злокачественной трансформации [7].
Последующее наблюдение
Как правило, рекомендуется пожизненное наблюдение как у леченных, так и у нелеченых пациентов. Рекомендуемый временной интервал, как сообщается в литературе, варьируется от нескольких месяцев до 1 года. Однако нет исследований, демонстрирующих эффективность такого протокола динамического наблюдения в отношении лучшей выживаемости в случае злокачественной трансформации по сравнению с протоколом, в котором пациенты обращаются сами в случае появления симптомов, являющихся основным признаком неблагоприятных изменений.
Общение с пациентом
Как сообщить пациенту, у которого лейкоплакия? Большинству пациентов не будет интересно слушать академическую лекцию своего врача о различных аспектах лейкоплакии полости рта, но вместо этого они хотят получить информацию в понятной форме, особенно когда речь идет о дальнейшем лечении.
При одиночных небольших поражениях, например, менее 2–3 см, можно рекомендовать выполнение эксцизионной биопсии в первую очередь из-за гистопатологической оценки, а также для успокоения пациента. Пациент должен быть проинформирован о том, что лейкоплакия может рецидивировать в течение периода, варьирующего от нескольких недель, месяцев или нескольких лет. Они также должны знать, что риск развития рака ротовой полости не может быть устранен путем иссечения. Хотя эффективность повторных посещений никогда не демонстрировалась, представляется предпочтительным предлагать такие визиты, главным образом, для успокоения пациента.
При больших или множественных лейкоплакиях требуется более взвешенное обсуждение с пациентами.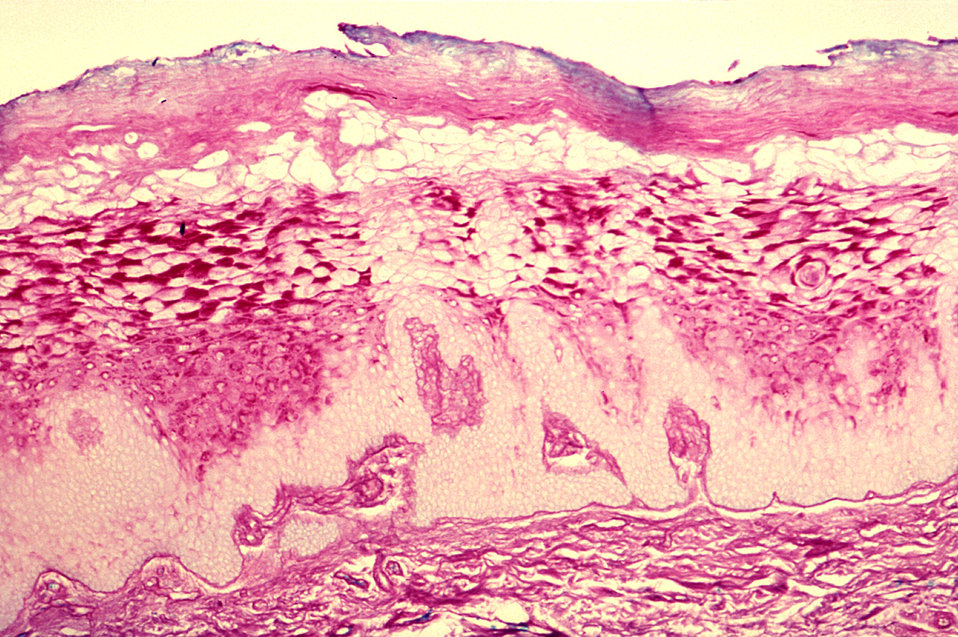 Увеличение заболеваемости в таких случаях должно быть надлежащим образом взвешено по отношению к ожидаемой пользе лечения. При больших, диффузных или множественных лейкоплакиях полости рта можно выбрать выполнение «эксцизионной» биопсии только клинически наиболее подозрительной области, если она имеется, или выполнить множественные биопсии (картирование). В любом случае пациент должен играть важную роль в принятии этого совместного решения. Некоторые предпочтут не проводить активное лечение, в то время как другие настаивают на лечении, даже в случае обширной или множественной лейкоплакии полости рта. Аналогичное расхождение во мнениях может возникнуть в случае повторения. Одни больные не хотят повторно проходить лечение, другие настаивают на повторном лечении.
Увеличение заболеваемости в таких случаях должно быть надлежащим образом взвешено по отношению к ожидаемой пользе лечения. При больших, диффузных или множественных лейкоплакиях полости рта можно выбрать выполнение «эксцизионной» биопсии только клинически наиболее подозрительной области, если она имеется, или выполнить множественные биопсии (картирование). В любом случае пациент должен играть важную роль в принятии этого совместного решения. Некоторые предпочтут не проводить активное лечение, в то время как другие настаивают на лечении, даже в случае обширной или множественной лейкоплакии полости рта. Аналогичное расхождение во мнениях может возникнуть в случае повторения. Одни больные не хотят повторно проходить лечение, другие настаивают на повторном лечении.
Research Perspectives
В последние десятилетия большая часть исследований лейкоплакии ротовой полости была сосредоточена на возможной прогностической ценности злокачественной трансформации в поисках широкого спектра молекулярных маркеров. Другой важный вопрос касается эффективности различных хирургических и нехирургических методов лечения. К сожалению, достигнут довольно незначительный прогресс, и большинство публикаций заканчиваются словами о том, что необходимы дополнительные исследования с привлечением большего числа изучаемых групп населения, носящие проспективный характер и предпочтительно проводимые в межучрежденческом и международном масштабе [2, 3]. Однако в настоящее время такие исследования не представляются целесообразными по разным причинам. Вероятно, основное ограничение состоит в довольно плохом определении лейкоплакии полости рта, включая различные так называемые кератозы. Чтобы решить эту проблему, нужно сначала организовать широко признанную международную встречу по достижению консенсуса по определению.
Другой важный вопрос касается эффективности различных хирургических и нехирургических методов лечения. К сожалению, достигнут довольно незначительный прогресс, и большинство публикаций заканчиваются словами о том, что необходимы дополнительные исследования с привлечением большего числа изучаемых групп населения, носящие проспективный характер и предпочтительно проводимые в межучрежденческом и международном масштабе [2, 3]. Однако в настоящее время такие исследования не представляются целесообразными по разным причинам. Вероятно, основное ограничение состоит в довольно плохом определении лейкоплакии полости рта, включая различные так называемые кератозы. Чтобы решить эту проблему, нужно сначала организовать широко признанную международную встречу по достижению консенсуса по определению.
В будущих исследованиях, вероятно, следует потребовать, чтобы каждое включенное лейкоплакическое поражение было сфотографировано, в то время как эти изображения должны оцениваться группой независимых опытных клиницистов на предмет правильности первоначального клинического диагноза. Аналогично, все образцы биопсии и резекции, если таковые имеются, должны быть повторно оценены независимыми опытными патологоанатомами на предмет правильности исходной гистопатологической оценки. Кроме того, следует использовать классификацию и систему стадирования, принимая во внимание размер лейкоплакии полости рта и отсутствие и наличие эпителиальной дисплазии, а также, возможно, оральный участок [8].
Аналогично, все образцы биопсии и резекции, если таковые имеются, должны быть повторно оценены независимыми опытными патологоанатомами на предмет правильности исходной гистопатологической оценки. Кроме того, следует использовать классификацию и систему стадирования, принимая во внимание размер лейкоплакии полости рта и отсутствие и наличие эпителиальной дисплазии, а также, возможно, оральный участок [8].
Различные методы лечения и результаты должны быть документированы воспроизводимым образом; это также относится к системе слежения. В таблице 2 представлено предложение по унифицированной отчетности, являющейся модификацией того, как сообщалось о результатах лечения рака [9]. Вопрос о нелечении, просто наблюдении – еще один сложный вопрос как с этической, так и с юридической точки зрения. Другие, возможно, важные параметры, которые следует задокументировать, относятся к табачным привычкам и употреблению алкоголя. Пол и возраст также могут быть приняты во внимание в этом типе исследований.
Полная таблица
Организовать проспективные, многоучрежденческие и ориентированные на международный уровень исследования различных аспектов лейкоплакии полости рта вряд ли возможно, в том числе ввиду большого количества пациентов, которых необходимо было бы включить, чтобы применить надлежащие статистические расчеты.
В будущем прогресс может быть неожиданно достигнут благодаря фундаментальным исследованиям в области (орального) канцерогенеза, не обязательно основанным на большом количестве изучаемых групп.
Выводы
Главным образом из-за плохого существующего определения лейкоплакии полости рта в последние годы почти не было достигнуто никакого прогресса в отношении поиска надежных прогностических маркеров злокачественной трансформации. По той же причине, а также из-за отсутствия единого подхода к отчетности невозможно надежно оценить результаты. Учитывая эти недостатки, существует острая необходимость в проведении международного консенсусного совещания для улучшения существующего определения лейкоплакии полости рта и согласования единого отчета о результатах лечения.
Ссылки
-
Варнакуласурия С., Джонсон Н.В., Ван дер Ваал И. Номенклатура и классификация потенциально злокачественных заболеваний слизистой оболочки полости рта. Дж Орал Патол Мед. 2007;36(10):575–80.
Артикул КАС Google ученый
-
van der Waal I. Историческая перспектива и номенклатура потенциально злокачественных или потенциально предраковых поражений эпителия полости рта с акцентом на лейкоплакию полости рта; некоторые предложения по модификации. Oral Surg Oral Med Oral Pathol Oral Radiol. 2018;125(6):577–81.
Артикул Google ученый
-
Никитакис Н.Г., Пентенеро М., Георгаки М., Пох С.Ф., Петерсон Д.Е., Эдвардс П. и др. Молекулярные маркеры, связанные с развитием и прогрессированием потенциально предраковых поражений эпителия полости рта: современные знания и последствия в будущем.
Oral Surg Oral Med Oral Pathol Oral Radiol. 2018;125(6):650–69.
Артикул Google ученый
-
Holmstrup P, Vedtofte P, Reibel J, Stoltze K. Предраковые поражения полости рта; надежна ли биопсия? Дж Орал Патол Мед. 2007;36(5):262–6.
Артикул КАС Google ученый
-
Лоди Г., Франчини Р., Варнакуласурия С., Варони Э.М., Сарделла А., Керр А.Р. и др. Вмешательства по лечению лейкоплакии полости рта для предотвращения рака полости рта. Кокрановская система базы данных, ред. 2016; 7:CD001829. https://doi.org/10.1002/14651858.CD001829.pub4.
Артикул пабмед Google ученый
-
Holmstrup P, Dabelsteen E. Лейкоплакия полости рта; лечить или не лечить. Оральный Дис. 2016;22(6):494–7.
Артикул КАС Google ученый
