Гингивит — тест с ответами
Медицина это наука в которую входит большое количество разнообразных разделов. Оно и понятно ведь будущий специалист в этой области должен иметь высокую квалификацию, ведь от этого зависит жизнь и здоровье человека. Для более лучшей подготовки, мы подготовили тест по медицине на этой странице. Внимание правильные варианты ответов выделены символом [+].
Гингивит – это такое заболевание:
[+] а) воспалительное
[-] б) опухолевидное
[-] в) дистрофическое
Альвеолярная десна:
[-] а) десна, покрывающая альвеолярный отросток и переходная складка
[+] б) десна, покрывающая альвеолярный отросток
[-] в) десневой сосочек и десна вокруг зуба
Маргинальная десна:
[-] а) десна, окружающая зуб
[-] б) десна, покрывающая альвеолярный отросток и небо
[+] в) десневой сосочек и десна вокруг зуба
Альвеолярная десна состоит:
[+] а) из эпителия и надкостницы
[-] б) из эпителия,надкостницы и альвеолярной кости
[-] в) из эпителия и собственного слизистого слоя
При рецессии десны количество десневой жидкости:
[-] а) уменьшается
[-] б) увеличивается
[+] в) не меняется
При катаральном гингивите количество десневой жидкости:
[-] а) уменьшается
[+] б) увеличивается
[-] в) не меняется
Индекс CPITN определяется с помощью такого зонда:
[-] а) штыковидного
[-] б) стоматологического
[+] в) пуговчатого
Индекс CPITN у взрослых, является показателем:
[+] а) нуждаемости в лечении заболеваний пародонта
[-] б) кровоточивости
[-] в) зубного налета
Индекс ПМА определяет:
[-] а) тяжесть пародонтита
[-] б) тяжесть пародонтолиза
[+] в) тяжесть гингивита
На рентгенограмме при гипертрофическом гингивите резорбция межальвеолярной перегородки:
[-] а) на 1/3 длины корня зуба
[+] б) отсутствует
[-] в) на 3/4 длины корня зуба
Катаральный гингивит легкой степени включает воспаление десны:
[+] а) только папиллярной
[-] б) маргинальной и альвеолярной
[-] в) папиллярной и маргинальной
Контрольное обследование послеоперацирннои области после кюретажа целесообразно провести :
[-] а) через полгода
[+] б) через 1 месяц
[-] в) через 10 дней
Количественную выраженность катарального гингивита можно определить с помощью индекса:
[+] а) ПМА
[-] б) пародонтального
[-] в) Грина-Вермильона
Воспаление десны – это характерный признак:
[-] а) пародонтоза
[-] б) фиброматоза десны
[+] в) пародонтита
Наличие ложного десневого кармана характерно:
[+] а) для гипертрофического гингивита
[-] б) для язвенно-некратического гингивита
[-] в) для катарального гингивита
Ранним клиническим признаком воспаления в десне является:
[-] а) деформация десневых сосочков
[+] б) кровоточивость при зондировании
[-] в) карман 4 мм
Каковы клинические признаки хронического катарального гингивита:
[-] а) обнажение корней
[-] б) подцесневой зубной камень
[+] в) кровоточивость при зондировании папиллярной и маргинальной десны
Каков клинический признак гипертрофического гингивита отечной формы:
[-] а) участки некроза маргинальной десны
[+] б) деформация и отек десневых сосочков
[-] в) участки некроза папиллярной десны
Каков клинический признак гипертрофического гингивита фиброзной формы:
[-] а) кровоточивость десны при чистке зубов и откусывании пищи
[-] б) резкая гиперемия и отек десневых сосочков
[+] в) разрастание не измененной в цвете десны
Катаральный гингивит дифференцируют:
[-] а) с фиброматозом
[+] б) с пародонтитом
[-] в) с пародонтозом
Гипертрофический гингивит фиброзной формы дифференцируют:
[+] а) с эпулисом
[-] б) с гингивитом Венсана
[-] в) с герпетическим гингивостоматитом
При фиброзной форме гипертрофического гингивита проводят такое хирургическое лечение:
[-] а) гингивотомию
[+] б) гингивэктомию
[-] в) открытый кюретаж
При отечной форме гипертрофического гингивита проводят:
[-] а) лоскутную операцию
[-] б) открытый кюретаж
[+] в) противоотечное лечение
Наличие пародонтального кармана характерно:
[-] а) для пародонтоза
[+] б) для пародонтита
[-] в) для гингивита
При пародонтите карман определяется:
[-] а) рентгенологически
[-] б) люминесцентно
[+] в) клинически
Гипертрофический гингивит отечной формы дифференцируют:
[-] а) с атрофическим гингивитом
[+] б) с хроническим катаральным гингивитом
[-] в) с герпетическим гингивостоматитом
При лечении хронического катарального гингивита проводят:
[+] а) коррекцию гигиены полости
[-] б) обработку десны резорцином
[-] в) аппликацию протеологических ферментов
Для обезболивания десны при язвенно-некротическом гингивите используют такую анестезию:
[-] а) суггестивную
[-] б) аппликационную
[+] в) проводниковую
Удаление наддесневого зубного камня проводят:
[+] а) до кюретажа карманов
[-] б) после кюретажа
[-] в) в процессе кюретажа
Метронидазол является средством этиотропного лечения:
[-] а) пародонтита
[+] б) язвенно-некротического гингивита
[-] в) гипертрофического гингивита
Тест на тему: «Гингивит» — Медицина, Прочее
Результаты авторизованых пользователей
| Название теста | Дата | Результат | Пользователь |
|---|---|---|---|
| Литература / Тест с ответами: “Подвиги Геракла” | 09-14-2022 05:30:46 pm | 13/20 | Flow Tyun |
| Физика / Итоговое тестирование по физике для 7 класса (с ответами) | 09-14-2022 11:03:42 am | 14/20 | Родион Цой |
| Биология / Тест с ответами: “Уровни организации жизни” | 09-14-2022 09:33:12 am | 13/20 | Никита |
| Биология / Тест с ответами: “Уровни организации жизни” | 09-14-2022 09:28:35 am | 17/20 | Соня Постол |
| Биология / Тест с ответами: “Уровни организации жизни” | 09-14-2022 09:26:50 am | 15/20 | Arsenyi Adamovich |
Все результаты
#1.
 Катаральный гингивит дифференцируют
Катаральный гингивит дифференцируют
A. с фиброматозом
A. с фиброматозомB. с пародонтитом
B. с пародонтитом
C. с пародонтозом
C. с пародонтозом#2. При катаральном гингивите количество десневой жидкости
A. уменьшается
A. уменьшается
B. увеличивается
B. увеличивается
C. не меняется
C. не меняется#3. Наличие ложного десневого кармана характерно
A. для гипертрофического гингивита
A. для гипертрофического гингивита
B. для язвенно-некратического гингивита
B. для язвенно-некратического гингивита
C. для катарального гингивита
C. для катарального гингивита#4.
 Каков клинический признак гипертрофического гингивита фиброзной формы
Каков клинический признак гипертрофического гингивита фиброзной формы
A. кровоточивость десны при чистке зубов и откусывании пищи
A. кровоточивость десны при чистке зубов и откусывании пищи
B. резкая гиперемия и отек десневых сосочков
B. резкая гиперемия и отек десневых сосочков
C. разрастание не измененной в цвете десны
C. разрастание не измененной в цвете десны#5. При лечении хронического катарального гингивита проводят
A. коррекцию гигиены полости
A. коррекцию гигиены полости
B. обработку десны резорцином
B. обработку десны резорцином
C. аппликацию протеологических ферментов
C. аппликацию протеологических ферментов#6. Альвеолярная десна состоит
A. из эпителия и надкостницы
из эпителия и надкостницы
B. из эпителия,надкостницы и альвеолярной кости
B. из эпителия,надкостницы и альвеолярной кости
C. из эпителия и собственного слизистого слоя
#7. При отечной форме гипертрофического гингивита проводят
A. лоскутную операцию
A. лоскутную операцию
B. открытый кюретаж
B. открытый кюретаж
C. противоотечное лечение
C. противоотечное лечение#8. Маргинальная десна
A. десна, окружающая зуб
A. десна, окружающая зуб
B. десна, покрывающая альвеолярный отросток и небо
B. десна, покрывающая альвеолярный отросток и небо
C. десневой сосочек и десна вокруг зуба
десневой сосочек и десна вокруг зуба
#9. Каковы клинические признаки хронического катарального гингивита
A. обнажение корней
A. обнажение корней
B. подцесневой зубной камень
B. подцесневой зубной камень
C. кровоточивость при зондировании папиллярной и маргинальной десны
C. кровоточивость при зондировании папиллярной и маргинальной десны#10. Количественную выраженность катарального гингивита можно определить с помощью индекса
A. ПМА
A. ПМА
B. пародонтального
B. пародонтального
C. Грина-Вермильона
C. Грина-Вермильона#11. Индекс CPITN у взрослых, является показателем
A. нуждаемости в лечении заболеваний пародонта
A. нуждаемости в лечении заболеваний пародонта
нуждаемости в лечении заболеваний пародонта
B. кровоточивости
B. кровоточивости
C. зубного налета
C. зубного налета#12. При рецессии десны количество десневой жидкости
A. уменьшается
A. уменьшается
B. увеличивается
B. увеличивается
C. не меняется
C. не меняется#13. Воспаление десны – это характерный признак
A. пародонтоза
A. пародонтоза
B. фиброматоза десны
B. фиброматоза десны
C. пародонтита
C. пародонтита#14. Удаление наддесневого зубного камня проводят
A. до кюретажа карманов
A. до кюретажа карманов
B. после кюретажа
после кюретажа
C. в процессе кюретажа
C. в процессе кюретажа#15. Гингивит – это такое заболевание
A. воспалительное
A. воспалительное
B. опухолевидное
B. опухолевидное
C. дистрофическое
C. дистрофическое#16. Катаральный гингивит легкой степени включает воспаление десны
A. только папиллярной
A. только папиллярной
B. маргинальной и альвеолярной
B. маргинальной и альвеолярной
C. папиллярной и маргинальной
C. папиллярной и маргинальной#17. На рентгенограмме при гипертрофическом гингивите резорбция межальвеолярной перегородки
A. на 1/3 длины корня зуба
A. на 1/3 длины корня зуба
B. отсутствует
отсутствует
C. на 3/4 длины корня зуба
C. на 3/4 длины корня зуба#18. Индекс CPITN определяется с помощью такого зонда
A. штыковидного
A. штыковидногоB. стоматологического
B. стоматологического
C. пуговчатого
C. пуговчатого#19. Ранним клиническим признаком воспаления в десне является
A. деформация десневых сосочков
A. деформация десневых сосочков
B. кровоточивость при зондировании
B. кровоточивость при зондировании
C. карман 4 мм
C. карман 4 мм#20. Каков клинический признак гипертрофического гингивита отечной формы
A. участки некроза маргинальной десны
A. участки некроза маргинальной десны
B. деформация и отек десневых сосочков
деформация и отек десневых сосочков
C. участки некроза папиллярной десны
C. участки некроза папиллярной десныПоказать результаты
Оцените тест после прохождения!
Нажмите на звезду, чтобы оценить!
Средняя оценка 0 / 5. Количество оценок: 0
Оценок пока нет. Поставьте оценку первым.
Сожалеем, что вы поставили низкую оценку!
Позвольте нам стать лучше!
Расскажите, как нам стать лучше?
Помощь в написании работы
Диагностическое и прогностическое значение исследования десневой жидкости у пациентов с катаральным гингивитом и пародонтитом легкой степени тяжести при проведении профессиональной гигиены полости рта
1. Аболмасов, Н.Н. Системный подход к диагностике, комплексном лечении и профилактике заболеваний пародонта: Дис. докт. мед наук / Н.Н. Аболмасов; Санкт-Петербург, 2005 290 с.
2. Авдеева, М.Г. Интерлейкины и факторы роста / М. Г. Авдеева, В.В. Лебедев, М.Г. Шубич. Справочное учебно-методическое пособие.-Краснодар, 1995.-С.23-58.
Г. Авдеева, В.В. Лебедев, М.Г. Шубич. Справочное учебно-методическое пособие.-Краснодар, 1995.-С.23-58.
3. Аллергия к микробным и соединительным антигенам у больных пародонтозом на фоне инфекционного неспецифического полиартрита / Н.Ф. Данилевский, A.M. Заверная, Н.А. Зелинская и др. // Стоматология.- 1979.- Т.58.- №3.- С.30-32.
4. Антонова, И.Н. Роль профессиональной гигиены полости рта в комплексном подходе к диагностике и лечению воспалительных заболеваний пародонта: Дис.канд. мед. наук / И.Н. Антонова; Санкт-Петербург, 2000 125 с.
5. Атрушкевич, В.Г. Остеопороз в клинике болезней пародонта. Часть 2. Генерализованный пародонтит и системный остеопороз / В.Г. Атрушкевич // Российский стоматологический журнал. 2008. -№1. — С. 48-51.
6. Байбабаев, А.А. Количественные цитологические нормативы эпителия слизистой оболочки ротовой полости у здоровых людей /
7. A.А. Байбабаев // Здравоохранение Таджикистана. 1985. — №5. С. 51-54.
8. Бажанов, Н.Н. Использование гипербарической оксигенации и гелий-неонового лазерного излучения в комплексном лечении больных с одонтогенными флегмонами лица и шеи / Н. Н. Бажанов, Р.Ф. Усманов, К.А. Рогов // Стоматология. 1992. — №2. — С. 38-40.
Н. Бажанов, Р.Ф. Усманов, К.А. Рогов // Стоматология. 1992. — №2. — С. 38-40.
9. Барабаш, Н.Д. Энзимологические механизмы в патогенезе воспалительно-дистрофического поражения пародонта: Автореф. дис. докт. мед. наук / Н.Д. Барабаш: М., 1981.- 23 с.
10. Барер, Г.М. Десневая жидкость. Состав и свойства / Г.М. Барер,
11. B.В. Кочержинский, Э.С. Халитова // Стоматология. 1986. — №4.1. C. 86-90.
12. Барер, Г.М. Использование параметров десневой жидкости в клинике болезней пародонта: Метод, рекомендации / Сост.: Г.М.Барер, В.В. Кочержинский, Э.С. Халитова. М., 1989. — 33 с.
13. Бенюмова, И.А. Цитологическая диагностика выделений из патологических карманов при пародонтозе до и после лечения / И.А. Бенюмова // Вопросы патогенеза, клиники и лечения пародонтоза. -1962.- С.155-164.
14. Бердюгина, О.В. Иммунологический мониторинг резорбции костной ткани при эндопротезировании крупных суставов / О.В. Бердюгина, В.В. Базарный // Клиническая лабораторная диагностика. 2003. — №11. — С. 39-43.
2003. — №11. — С. 39-43.
15. Безрукова, И.В. Клинико-лабораторная оценка эффективности применения в комплексной терапии воспалительных заболеваний пародонта комбинированного препарата цифран СТ / И.В Безрукова, Н.А. Дмитриева, JI.H. Герчиков // Стоматология. №1. — С. 13-15.
16. Болезни пародонта. Патогенез, диагностика, лечение /
17. A.С. Григорьян, А.И. Грудянов, А.И. Рабухина, О.А. Фролова. -М.: Медицинское информационное агентство, 2004. 320 с.
18. Бурханов, Р.А. Новые данные об иммунных механизмах в развитии пародонтоза / Р.А. Бурханов, Ю.М. Зарецкая, В.Н. Исаев и др. //Иммунология. -1984. №3. — С. 78-79.
19. Быков, B.JI. Тканевые и клеточные защитные механизмы слизистой оболочки полости рта / B.JI. Быков // Морфология. 1996. -№6. — С. 14-24.
20. Быков, В.Л. Функциональная морфология эпителиального барьера слизистой оболочки полости рта / В.Л. Быков // Стоматология. 1997. -№3.- С. 12-17.
21. Быков, В.Л. Экспериментальное изучение влияния кортикостероидных препаратов на адгезию грибов рода Candida к эпителиоцитам слизистых оболочек / В. Л. Быков, Е.В. Величко // Микробиология. 1988. — №8. — С. 115-118.
Л. Быков, Е.В. Величко // Микробиология. 1988. — №8. — С. 115-118.
22. Быков, В.Л. Гистология и эмбриология полости рта человека /
23. B.Л. Быков. СПб: Специальная литература, 1996. — 247 с.
24. Быкова, И.А. Цитологическая характеристика отпечатков слизистой оболочки полости рта с применением индекса дифференцировки клеток / И.А. Быкова, А.А. Агаджанян, Г.В. Банченко // Лабораторное дело. 1987. — №1. — С. 33-35.
25. Варава, Г.Н. Клинико-иммунологическое обоснование применения корригирующей иммунотерапии при пародонтозе / Г.Н. Варава, Г.Ф. Белоклицкая, Ю.В. Дяченко // Стоматология. 1982. -№2.-С 36-38.
26. Василенко, A.M. Современная теория боли и нейроиммуно-патология височно-нижнечелюстного сустава / A.M. Василенко // Российский стоматологический журнал. 2000. — №3. — С. 4-10.
27. Величко, Е.В. Адгезия грибов рода Candida к эпителию слизистых оболочек при сахарном диабете / Е.В. Величко, В.Л. Быков //Вестник дерматологии. 1988. — №6. — С. 20-22.
28. Весклер, Г.Н. Клинико-иммунологическое обоснование применения корригирующей иммунотерапии при пародонтозе / Г.Н. Весклер, Г.Ф. Белоклицкая, Ю.В. Дяченко // Стоматология.- 1983. — Т.61. №3. — С. 32-34.
Весклер, Г.Н. Клинико-иммунологическое обоснование применения корригирующей иммунотерапии при пародонтозе / Г.Н. Весклер, Г.Ф. Белоклицкая, Ю.В. Дяченко // Стоматология.- 1983. — Т.61. №3. — С. 32-34.
29. Весклер, Х.М. Микробно-иммуногенетическая концепция патогенеза пародонтоза / Х.М. Весклер, Э.В. Бельчиков // Стоматология. 1973. — №6. — С. 27-30.
30. Власова, Л.Ф. Ультраструктура эпителиоцитов из смывов слизистой оболочки полости рта / Л.Ф. Власова, Л.М. Непомнящих // Бюллетень экспериментальной биологии и медицины. 2000. — Т. 129. -№3 — с. 352-355.
31. Возможности и роль нового цитоморфологического метода в диагностике заболеваний пародонта / А.С. Григорьян, А.И. Грудянов, З.П. Антипова и др. // Пародонтология. -1999. №4(14). — С. 3-7.
32. Воспаление. Руководство для врачей / Под ред. В.В. Серова,
33. B.C. Паукова. М.: Медицина, 1995. — 640 с.
34. Вядро, М.М. Цитокины полу функциональные регуляторы защитных реакций в норме и при патологии / М.М. Вядро,
35. C.М. Навашин // Антибиотики и химиотерапия.- 1989.-Т.34.-№11.-С.863-868.
C.М. Навашин // Антибиотики и химиотерапия.- 1989.-Т.34.-№11.-С.863-868.
36. Гапанович, В.Я. Приспособление для забора материала из полости рта и небных миндалин для цитологических исследований /
37. В.Я. Гапанович, С.В. Глинник, А.Ч. Вуцель // Журнал ушных, носовых, горловых болезней. — 1985.- №5.-С.79.
38. Гемонов, В.В. Защитные свойства поверхностных слоев эпителия слизистой оболочки полости рта / В.В. Гемонов, M.JI. Могильный // Стоматология.- 1996.-Т.75.-№3.-С.4-6.
39. Гемонов, В.В. Атлас по гистологии и эмбриологии органов ротовой полости и зубов / В.В. Гемонов, Э.Н. Лаврова, Л.И. Фалин. -М.: ГОУ ВУНМЦ МЗ РФ, 2003. 96 с.
40. Герасимов, И.Г. Функциональная активность нейтрофилов / И.Г. Герасимов // Клиническа лабораторная диагностика. 2006. — №2. -С. 34-35.
41. Герасимович, И.С. Мотивация к лечению хронического генерализованного пародонтита: Автореф. дис. . канд. мед. наук / И.С. Герасимович: Екатеринбург, 2000. 24с.
42. Горбачева, А.И. Хроническая одонтогенная очаговая инфекция и соматические заболевания / А. И. Горбачева, А.И. Кирсанова // Пародонтология. 2001. — № 4(22). — С. 35-39.
И. Горбачева, А.И. Кирсанова // Пародонтология. 2001. — № 4(22). — С. 35-39.
43. Григорьян, А.С. Роль и место феномена повреждения в патогенезе заболеваний пародонта / А.С. Григорьян // Стоматология. -1999.-№1.-С. 16-20.
44. Григорьян, А.С. Ключевые звенья патогенеза заболеваний пародонта в свете данных цитоморфометрического метода исследований / А.С. Григорьян, А.И. Грудянов // Стоматология. 2001. — №1. — С. 5-8.
45. Григорьян, А.С. Морфогенез ранних стадий воспалительных заболеваний пародонта / А.С. Григорьян, О.А. Фролова, Е.В. Иванова // Стоматология. 2002. — №1. — С. 19-25.
46. Гросси С.Г. Воспалительные процессы полости рта и сердечнососудистые заболевания / С.Г. Гросси //Новое в стоматологии.- 2006.-№1.- С.- 40-44.
47. Грудянов, А.И. Принципы организации и показания лечебной помощи лицам с воспалительными заболеваниями пародонта (Эпидемиол., эксперим., клинич. и соц.-экон. аспекты): Автореф. дис. . д-ра мед. наук / А.И. Грудянов: М., 1992. 46 с.
48. Грудянов, А.И. Методы профилактики заболеваний пародонта и их обоснование / А.И. Грудянов // Стоматология. — 1995. №3. — С. 21-24.
Грудянов, А.И. Методы профилактики заболеваний пародонта и их обоснование / А.И. Грудянов // Стоматология. — 1995. №3. — С. 21-24.
49. Грудянов, А.И. Фагоцитарная активность нейтрофилов десневой крови при пародонтите / А.И. Грудянов, В.В. Овчинникова, JI.E Серебрякова. // Стоматология. — Спецвыпуск. Журналу 85 лет. — С.43-45.
50. Грудянов, А.И. Иммунологические показатели крови при быстро прогрессирующем пародонтите / А.И. Грудянов, И.В. Безрукова // Стоматология. 2000. — №3. — С. 15-17.
51. Гулямов, М.Г. Количественные цитологические нормативы эпителия слизистой оболочки рта у здоровых людей / М.Г. Гулямов,
52. B.И. Польский, А.А. Байбабаев // Здравоохранение Таджикистана.-1989.-№4.- С. 108-109.
53. Дерейко, JI.B. Иммунокорригируюшая терапия в комплексном лечении больных пародонтитом / JI.B. Дерейко // Стоматология. 1987. -№1.-С. 32-33.
54. Десневая жидкость объективный критерий оценки состояния тканей пародонта / Г.М. Барер, В.В. Кочержинский, Э.С. Халитова, Л.М. Лукиных // Стоматология. — 1987. — №1. — С. 28- 30.
Халитова, Л.М. Лукиных // Стоматология. — 1987. — №1. — С. 28- 30.
55. Джемилева, Т. Цитологични данки за ефекта на глюкозоксима при пародонтальни заболявания у оранжерейни работнички / Т. Джемилева, М. Дрянкова // Стоматология. София.-1983.-№6,1. C. 8-13.
56. Дмитриева, Л.А. Особенности синтеза цитокинов у больных с коксартрозами при эндопротезировании тазобедренного сустава
57. JI.A. Дмитриева, Е.Ю. Коршунова, З.В. Кошкарева // Клиническая лабораторная диагностика. 2005. — №2. — С. 38-40.
58. Дмитриева, JI.A. Современные представления о роли микрофлоры в патогенезе заболеваний пародонта / JI.A. Дмитриева, А.Г. Крайнова // Пародонтология. 2004,- №1. — С. 8-15.
59. Дягилева, О.А. Морфофункциональные изменения лейкоцитов десневой крови у больных с воспалительными заболеваниями пародонта / О.А. Дягилева, JI.E. Серебрякова, И.Н. Наумова // Клиническая лабораторная диагностика. 2005. — №10. — С. 53.
60. Ерина, С.В. Цитологическое исследование десневой жидкости при воспалительных заболеваниях пародонта / С. В. Ерина, С.Н. Дьяконова// Лабораторное дело.-1989.-№6.-С.14-15.
В. Ерина, С.Н. Дьяконова// Лабораторное дело.-1989.-№6.-С.14-15.
61. Ерина, С.В. Роль гигиены полости рта в лечении воспалительных заболеваний пародонта (клинико-лаб. исслед.): Дис. . канд. мед. наук. -Воронеж, 1987.- 139 с.
62. Есаян, З.В. Факторы неспецифической и специфической защиты в патогенезе ранних форм поражения пародонта / З.В. Есаян // Стоматология. 2005. — №1. — С. 58-64.
63. Ефанов, О.И. Физиотерапия стоматологических заболеваний / О.И. Ефанов, Т.Ф. Дзанагова // Библиотека практического врача, Медицина. 1984. -294 с.
64. Железникова, Г.Ф. Роль гамма-интерферона в иммунопатогенезе инфекций (обзор литературы) / Г.Ф. Железникова // Клиническая лабораторная диагностика. №4. — 2008. — С. 3-8.
65. Жуматов, У.Ж. Оценка эффективности удаления зубных отложений с использованием ультразвука / У.Ж. Жуматов, З.М. Бекметов // Клиническая стоматология. 2002.- №4.-с.44-45.
66. Жяконис, И.М. Изменения содержания лейкоцитов в капиллярной крови десны у больных гингивитом и пародонтозом / И.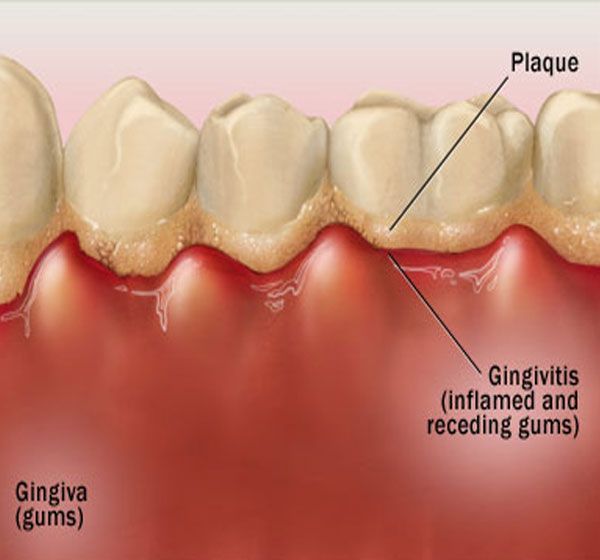 М. Жяконис // Стоматология. 1982. — №1. — С. 26-28.
М. Жяконис // Стоматология. 1982. — №1. — С. 26-28.
67. Жяконис, И.М. Определение Т- и В-лимфоцитов в капиллярной крови десны у больных пародонтозом / И.М. Жяконис, П.А. Пайпалене // Лабораторное дело. 1983. — №3. — С. 7-9.
68. Жяконис, И.М. Содержание иммуноглобулинов в десневой жидкости при пародонтите / И.М. Жяконис // Стоматология. 1985. -№1. — С. 22-24.
69. Заболевания пародонта: Атлас / Н.Ф. Данилевский, Е.А. Магид, Н.А. Мухин, В.Ю. Миликевич. М.: Медицина, 1993. — 320 с.
70. Зеленцова Е.К. Пиограмма десневых карманов / Е.К. Зеленцова // Стоматология.- 1939.-№5.-С.25-34.
71. Иванов B.C. Заболевания пародонта.- М.: Медицинское информационное агенство, 1998.-296с.
72. Иванюшко Т.П. Цитокины в механизмах развития хронического воспаления в пародонте / Т.П. Иванюшко, Л.В. Ганковская, Л.В. Ковальчук //2-ой съезд иммунологов России: Сб. науч. тр. Сочи, 1999.- С.61.
73. Иванюшко Т.П. Комплексное изучение механизмов развития хронического воспаления при пародонтите / Т.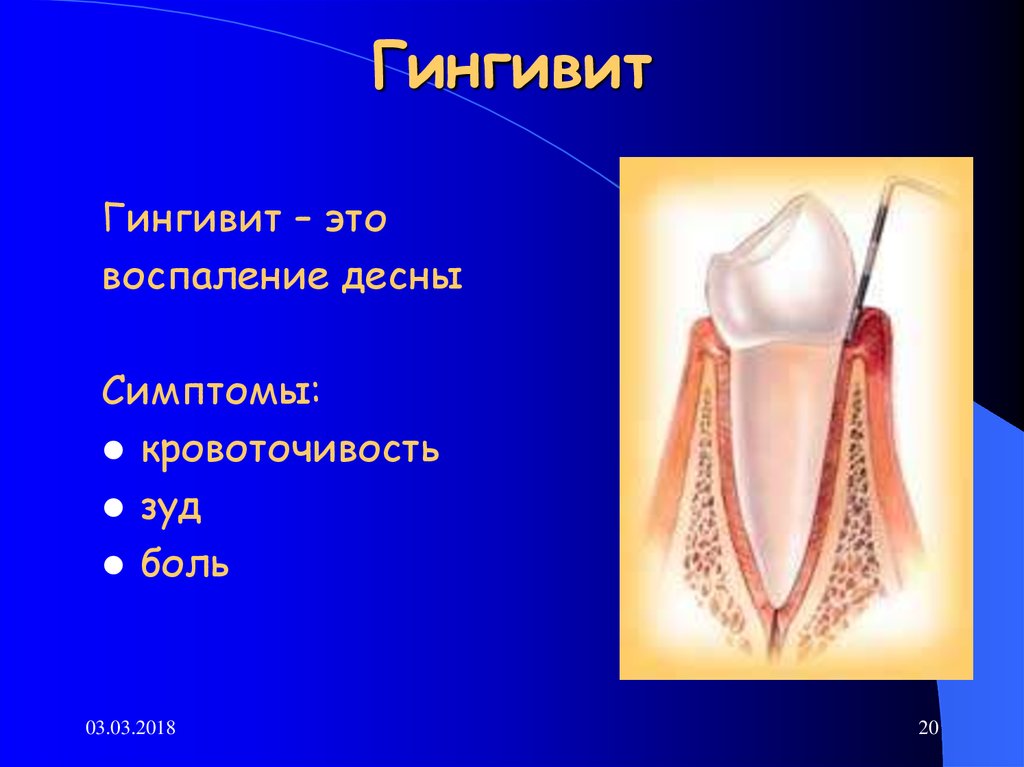 П. Иванюшко, Л.В. Ганковская, Л.В. Ковальчук и др. // Стоматология. 2000. — №4. -С. 13-16.
П. Иванюшко, Л.В. Ганковская, Л.В. Ковальчук и др. // Стоматология. 2000. — №4. -С. 13-16.
74. Иванюшко Т.П. Локальная цитокинотерапия в лечении хронического пародонтита / Т.П. Иванюшко, Г.И. Емиленко, Л.В. Ганковская // Достижения и перспективы стоматологии: Тезисы докл. междун. науч.-практ. конф. М., 1999. — С. 201-203.
75. Иванюшко Т.П. Роль иммунных механизмов в патогенезе пародонтита и обоснование методов локальной иммунотерапии: Дис. докт. мед. наук / Т.П. Иванюшко: ММА им. Сеченова Москва, 2002. -213 с.
76. Иммунологическая реактивность и иммунотерапия больных пародонтозом / Н.Ф. Данилевский, A.M. Заверная, Н.А. Зелинская и др.// Стоматология.- 1988.- т.61.~ №4.- С.24-26.
77. Иммунология Учебник для студентов медицинских вузов / Под ред. Р.В. Петрова М.: Медицина, 1987.-414с.
78. Иорданишвили, А.К. Особенности клинического течения, лечения и профилактики заболеваний забочелюстной системы у летного и плавсостава: Учебное пособие / А.К. Иорданишвили, A. M. Ковалевский. СПб., 1998. — 32 с.
M. Ковалевский. СПб., 1998. — 32 с.
79. Иоффе Е. Зубоврачебные заметки / Е. Иоффе Нью-Йорк, С.-Пб. — 1999.-216 с.
80. Использование ультразвуковых и пескоструйных аппаратов EMS для профилактики и лечения в различных областях стоматологии / Г.М. Барер, И.А. Овчинникова, В.А. Завьялова, Н.Г. Завьялова И Клиническая стоматология.-2001 .-№4.-С.-44-46.
81. Кашкин, К.П. Цитокины и комплемент-регуляторные молекулы иммунной системы / К.П. Кашкин // Аллергология и клиническая иммунология. 1994. — №1. — С.54-57.
82. Кашкин, К.П. Цитокины иммунной системы: основные свойства -иммунопатологическая активность / К.П. Кашкин // Клиническая лабораторная диагностика. 1998.- №11. — С. 21-32.
83. Кетлинский, С.А. Современные аспекты изучения цитокинов / С.А. Кетлинский // 2-ой съезд иммунологов России: Тезисы докладов.-Сочи, 1999. С.46-52.
84. Кимеле Э.В. Цитологическая диагностика в стоматологии / Э.В. Кимеле Рига. — 1984,- 181 с.
85. Киричук, В.Ф. Роль нарушений функциональной активности тромбоцитов в патогенезе микроциркуляторных расстройств у больных катаральным гингивитом / В.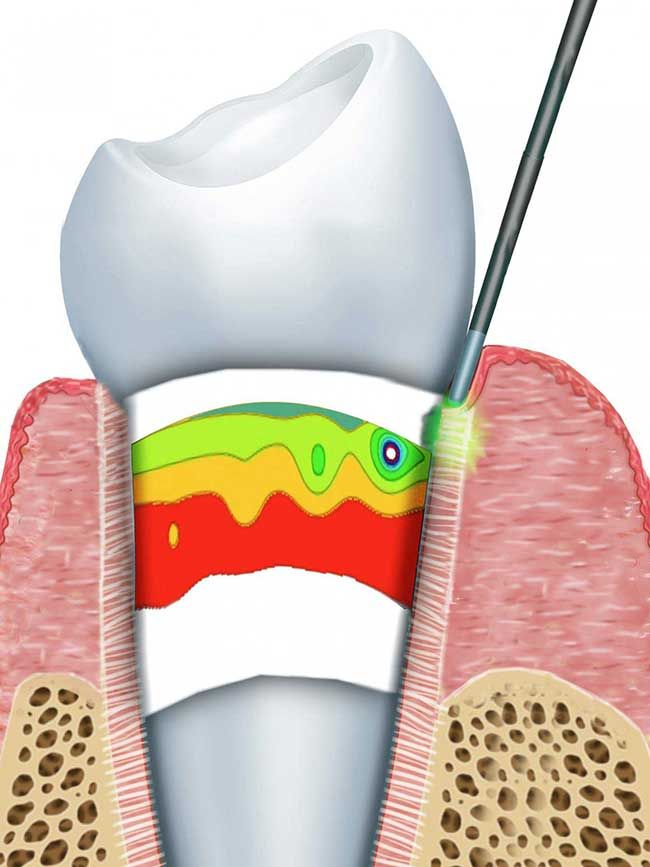 Ф. Киричук, Н.В. Булкина, В.Н. Китаева // Российский стоматологический журнал. 2008. — №1. — С. 22-24.
Ф. Киричук, Н.В. Булкина, В.Н. Китаева // Российский стоматологический журнал. 2008. — №1. — С. 22-24.
86. Киселева, Е.А. Клинико-лабораторное обоснование применения иммунокоррекции в комплексном лечении хронического катарального гингивита / Е.А. Киселева, Е.А. Тё, А.А. Коростелев // Стоматология. — 2007. -№1.-С. 34-37.
87. Клетки крови и костного мозга: Атлас / Г.И. Козинец, З.Г. Шишканова, Т.Г. Сарычева и др.; под ред. Г.И. Козинец. М.: Медицинское информационное агентство, 2004. — 203 с.
88. Клетка: морфология, физиология, патология, методы исследований. Лекция / Б.З. Шенкман, Г.П. Гладилин; Саратовский медицинский институт. Саратов, 1991. — 48 с.
89. Клинико-диагностическое значение исследования слезной жидкости (обзор литературы) / Б.С. Хышиктуев, С.А. Козлов, М.В. Максименя и др. // Клиническая лабораторная диагностика. -2005.-№12.-С. 3-6.
90. Клинико-иммунологические особенности патогенеза катарального гингивита. Сообщение 1 / Ю.М. Максимовский, Т.Д. Чиркова, Т.А.Фролова, и др. // Стоматология. 2003. — №3. -С. 24-27.
Чиркова, Т.А.Фролова, и др. // Стоматология. 2003. — №3. -С. 24-27.
91. Клинико-иммунологическая эффективность применения пасты Parodontax — F в лечении воспалительных заболеваний пародонта / И.В. Анисимова, С.С. Бакшеева, Е.Б. Сорокина, С.А. Николаенко // Клиническая стоматология. 2009. — №1(49).- С. 32 — 34.
92. Клиническая и иммунологическая эффективность линимента циклоферона при пародонтите / Л.А. Соболева, P.P. Сякин,
93. Е.Н. Блинникова и соавт. // Российский стоматологический журнал. — 2009. №2. — С. 25-28.
94. Клинические особенности хронического генерализованного пародонтита / М.Н. Пузин, Е.С. Кипарисова, В.Д. Вагнер и др. // Российский стоматолгический журнал. 2008. — №3. — С. 24-28.
95. Ковальчук, JI.B. Локальная иммунокоррекция цитокинами / Л.В. Ковальчук, Л.В. Ганковская // Аллергология и клиническая иммунология. 1994. №1,- С. 64-70.
96. Ковальчук, Л.В. Иммуноцитокины и локальная иммунокоррекция / Л.В. Ковальчук, Л.В. Ганковская // Иммунология,- 1995. -№1.-с.4-7.
-№1.-с.4-7.
97. Комбинированный метод исследования материала из полости рта на микрофлору / М.А. Горшкова, Е.Н. Егорова, Р.А. Пустовалова, Ж.В. Терещенко // Клиническая лабораторная диагоностика. 2008. -№7.-С. 53-57.
98. Коррекция функциональной активности фагоцитов в очаге воспаления у больных с глубокими флегмонами шеи / Е.А. Цеймах,
99. B.А. Тулупов, Ю.Ю. Гуревич и др. // Стоматология. 2004. — №4.1. C. 37-41.
100. Коррекция местного иммунитета полости рта при хроническом генерализованном пародонтите у больных спленомегалией / Ф.З. Мирсаева, Т.Р. Мирсаев, Л.А. Фарвазова, Л.Ф. Губайбуллина // Российский стоматологический журнал. — 2007. №3.- С. 18-21.
101. Кузьмина, Э.М. Профилактика стоматологических заболеваний / Э.М. Кузьмина // Москва, Изд. МГМСУ.- 2003.- 69-102 с.
102. Куклина, Е.А. Клинико-цитологические параллели при начальных формах поражения пародонта: Дис. канд. мед. наук / Е.А. Куклина: ВГАМН им. Н.Н. Бурденко. Воронеж, 2000. — 150 с.
103. Кулаков, А.А Применение магнитно-лазерного излучения в имплантологии / А.А. Кулаков, А.А. Прохончуков, С.Е Соболева //
Кулаков, А.А Применение магнитно-лазерного излучения в имплантологии / А.А. Кулаков, А.А. Прохончуков, С.Е Соболева //
104. Труды IV Съезда Стоматологической ассоциации России: Сб. науч.тр. -М., 2000. С. 366-368.
105. Кулаженко, Т.В. Гигиеническое воспитание в структуре лечебно-профилактических мероприятий при заболеваниях пародонта / Т.В. Кулаженко // Стоматология. Спецвыпуск. Журналу 85 лет. 2007. -С. 48-51.
106. Куралесина, В.П. Роль профессиональной гигиены полости рта в лечении хронического гингивита: Дисс. канд. мед. наук / В.П. Куралесина ВГАМН им. Н.Н. Бурденко. — Воронеж, 2003 — 124с.
107. Кучумова, Е.Д. Исследование влияния на поверхность зуба различных инструментов для удаления зубных отложений / Е.Д. Кучумова, Я.В. Стюф. // Стоматология. 2006. — №6. — С.27-30.
108. Лебедев, К. А. Образраспознающие рецепторы и их регуляторная роль в иммунных реакциях организма и контроле микробного биоценоза в ротовой полости / К.А. Лебедев, Ю.М. Максимовский, А. В. Митронин, И.Д. Понякина // Стоматолог. -2007. №2.-С. 46-51.
В. Митронин, И.Д. Понякина // Стоматолог. -2007. №2.-С. 46-51.
109. Левицкий А.П. Зубной налет / А.П. Левицкий, И.К. Мезина // Здоровье. 1987.-С. 80.
110. Левченко, Д.М. Профессиональная гигиена полости рта в профилактике болезней пародонта / Д.М. Левченко, И.А. Платонов // Актуальные проблемы медицины. Воронеж, 1993. — Т. 2. — С. 126-127.
111. Лемецкая, Т.И. Клинико-экспериментальное обоснование классификации заболеваний пародонта и патогенетические принципы лечебно-профилактической помощи больным с патологией пародонта: Автореф. дис. . докт. мед. наук / Т.И. Лемецкая; М., 1998. — 62 с.
112. Леонтьев, В.К. Концепция формирования профессиональных стандартов / В.К. Леонтьев, В.Г. Шестаков // Новое в стоматологии. — 1995. -№ 4.-С. 6-8.
113. Леонтьев, В.К. Профилактика стоматологических заболеваний / В.К. Леонтьев, Г.Н. Пахомов // М.: Медицина, 2006. 243-247.
114. Максимовский, Ю.М. Особенности клеточного иммунитета при катаральном гингивите. Сообщение 2 / Ю. М. Максимовский, Т.Д. Чиркова, М.А. Ульянова // Стоматология. 2003. — №4. — С. 29-31.
М. Максимовский, Т.Д. Чиркова, М.А. Ульянова // Стоматология. 2003. — №4. — С. 29-31.
115. Максимовский, Ю.М. Особенности активационного состава иммунокомпетентных клеток крови пародонта при катаральном гингивите. Сообщение 3 / Ю.М. Максимовский, Т.Д. Чиркова, М.А.Ульянова // Стоматология. 2003. — №5. — С. 20-22.
116. Мащенко, И.С. О различии в механизмах развития пародонтита / И.С. Мащенко // Стоматология. 1990. — №1. — С. 29-31.
117. Мащенко, И.С. Клинико-лабораторная характеристика дистрофически-воспалительной формы пародонтоза / И.С. Мащенко // Стоматология. 1980. — №3. — С. 22-24.
118. Метод Пур-детекции пародонтопатогенных бактерий и Streptococcus mutans в биологических образцах из ротовой полости / А.Б. Чухловин, A.M. Соловьева, С.К. Матело и др. // Клиническая лабораторная диагностика. 2007. — №4. — С. 35-38.
119. Мисник, А.В. Состояние местного иммунитета полости рта у пациентов с хроническим деструктивным периодонтитом до и после эндодонтического лечения / А. В. Мисник // Институт стоматологии. — 2008.-№4 (41).-С. 50-52.
В. Мисник // Институт стоматологии. — 2008.-№4 (41).-С. 50-52.
120. Михалева, Л.М. Хронический парод онтит. Клиническая морфология и иммунология / Л.М. Михалева, В.Д. Шаповалов, Т.Г. Бархина. М.: Триада-фарм, 2004. — 126 с.
121. Московский, А.В. Клинико-иммунологические особенности кариеса в сочетании с пародонтитом / А.В. Московский, А.В. Шумский // Российский стоматологический журнал. 2007. — №3. — 23-26.
122. Московский, А.В. Сравнительное исследование иммунокомпетентных клеток пульпы зуба в норме, при кариесе и егоосложнениях в сочетании с пародонтитом / А.В. Московский // Стоматология.- 2007. №1. — С. 31-33.
123. Новый диагностический метод оценки состояния пародонта по данным цитоморфометрии отпечатков с десны / А.С. Григорьян, А.И. Грудянов, З.П. Антипова и др. // Стоматология. 2000. — №5. -С. 4-9.
124. Овруцкий, Г.Д. Пародонтит / Г.Д. Овруцкий, И.Н. Низамутдинов, И.М. Дегтярев // Казань.-1990.-1 Юс.
125. Определение цитокинов методом иммуноферментного анализа / Т. Г. Рябичева, Н.А. Вараксин, Н.В. Тимофеева, М.Ю. Рукавишников // Новости «Вектор-Бест»: Информационный бюллетень.- 2004. -№4 (34).-С. 7-14.
Г. Рябичева, Н.А. Вараксин, Н.В. Тимофеева, М.Ю. Рукавишников // Новости «Вектор-Бест»: Информационный бюллетень.- 2004. -№4 (34).-С. 7-14.
126. Орехова, Л.Ю. Соотношения гуморальных и клеточных аутоиммунных процессов при воспалительных заболеваниях пародонта / Л.Ю. Орехова, М.Я. Левин, Б.Н. Софронов // Пародонтология,- 1997.-№4.-с. 14-15.
127. Ортопедическая стоматология: Руководство для врачей, зубных техников, студентов вузов и мед. училищ / Н.Г. Аболмасов, Н.Н. Аболмасов, В.А. Бычков, А. Аль-Хаким. М.: МЕДпресс-информ, 2002. — 576 с.
128. Оценка уровня дифференцировки клеток эпителия в отпечатках с разных участков слизистой оболочки полости рта здоровых людей / Г.В. Банченко, И.А. Быкова, О.Г. Акопян, А.А. Агаджанян // Стоматология. 1997. — №1. — С. 12-14.
129. Панцулава, И. Профиль циркулирующих цитокинов в здоровой популяции / И. Панцулава, Е. Кобылянский // Аллергология и иммунология. 2004. — №3. — С. 472-474.
130. Пигаревский, В.Е. Полиморфно-ядерный лейкоцит и макрофаг в реакциях воспаления и гиперчувствительности / В. Е. Пигаревский // Арх. патол. 1983. — Т. 45. — №11. — С. 14-22.
Е. Пигаревский // Арх. патол. 1983. — Т. 45. — №11. — С. 14-22.
131. Пескоструйные приборы для профессиональной чистки зубов.// Новое в стоиатологии.-2003.-№8.-с.49-54.
132. Пичугина, JI.B. Внутриклеточные цитокины: проблемы детекции и клиническое значение / JI.B. Пичугина, Б.В. Пинегин // Иммунология. -2008. -№1. С. 55-58.
133. Полная пародонтологическая программа Пьезон: особенности клинического применения / Г.М. Барер, И.А. Овчинникова,
134. B.А. Завьялова, В.Г. Маслий // Клиническая стоматология.- 2002. №4. — С.34-37.
135. Попов, И.Г. Гигиена питания летного состава / И.Г. Попов // Авиационная медицина: Руководство: Под ред. И.Г. Попова, Н.М. Рудного, П.В. Васильева, С.А. Гузулова. М.: Медицина, 1986.1. C. 191-203.
136. Последние достижения в области иммунологии / Под редакцией Р.А. Томпсона М., Медицина, 1983, С. 201-252.
137. Преферанская, Н.Г. Лекарственные средства на основе цитокинов / Н.Г. Преферанская // Российский медицинский журнал. 2008. — №1. -С. 35-38.
2008. — №1. -С. 35-38.
138. Провоспалительные цитокины при герпетической инфекции / О.О. Обухова, Г.В. Башур, Л.А. Трунова и др. // Проблемы клинической медицины. — 2005. №3. — С. 96-99.
139. Продукция интерлейкина-1 и протагландинов моноцитами периферической крови человека / Л.В. Ковальчук, А.Н. Чередеева, В.А. Извекова и др. // Лабораторное дело.- М.,1986.-№11.- С. 657-660.
140. Реактивность буккальных эпителиоцитов: индикация местных и общих нарушений гомеостаза (Обзор литературы) /А.Н. Маянский, М.А. Абаджиди, И.В. Маянская и др. // Клиническая лабораторная диагностика. 2004. — №8. — С. 31-33.
141. Робустова, Т.Г. Иммунная система региона зубо-зубочелюстного сегмента. Обзор / Т.Г. Робустова, К.А. Лебедев, И.Д. Понякина // Стоматология. 1990. — №4. — С. 88-91.
142. Роль цитокинов в механизмах развития хронического воспаления в ткани пародонта / Л.В. Ковальчук, Л.В. Ганковская, М.А. Рогова и др. // Иммунология. 2000. — №6. — С. 24-26.
143. Ройт А. Основы иммунологии. Пер. с англ. / Под ред. Р.Г. Василова.- М.: Медицина, 1991.- 327 с.
Пер. с англ. / Под ред. Р.Г. Василова.- М.: Медицина, 1991.- 327 с.
144. Русакова, Е.Ю. Состояние гигиены полости рта и уровень гигиенических знаний у детей Приморского края / Е.Ю. Русакова, П.А. Железный, А.К. Базин // Российский стоматологический журнал. -2008. -№4. С. 15-17.
145. Рыбаков, А.И. Стоматологические заболевания и их взаимосвязь с внутренними органами / А.И. Рыбаков. // Тбилиси: Сабчота Сакартвело, 1976. 202 с.
146. Рыжков, А.Ю. Клинические и гистохимические параллели в диагностике пародонтита легкой степени тяжести: Дисс. канд. мед. наук / А.Ю. Рыжков: Воронеж, 2004 124с.
147. Сабуров, С.К. Диагностическое и прогностическое значение профессиональной гигиены полости рта в профилактике заболеваний пародонта: Дисс. . канд. мед. наук / С.К. Сабуров: ГМУ им. Абуали ибн Сино. Душанбе, 2004.- 158 с.
148. Саидкаримова, У.А. Динамика цитограммы смешанной слюны больных сиалозами под воздействием низкоинтенсивного лазерного излучения / У.А. Саидкаримова, Е. К. Баландина, Л.О. Астудильо //
К. Баландина, Л.О. Астудильо //
149. Актуальные вопросы интенсивной лазерной медицины: Тезисы докладов 1-й Всерос. науч. конф. М., 1999. — С. 141.
150. Салем, Р. Эффект ультразвуковой обработки пародонтальных карманов в комплексной терапии пародонтита при сахарном диабете: Дисс. канд. мед. наук/Р. Салем: Москва, 2005 113с.
151. Сапин, М.Р. Иммунная система человека / М.Р. Сапин, JI.E. Этинген М.: Медина, 1996.-300 с.
152. Саркисов, Д.С. Общая патология человека: Учебник (2-е изд.) / Д.С. Саркисов, М.А. Пальцев, Н.К. Хитров. М.: Медицина. — 1997. -608 с.
153. Сенников, С.В. Методы определения цитокинов / С.В. Сенников,
154. A.Н. Силков // Цитокины и воспаление. 2005. — Т. 4. — № 1. — С. 22-27.
155. Слободина, Е.В. Диагностические критерии микроциркуляции и экологии полости рта при повышенном риске развития воспалительных заболеваний пародота / Е.В. Слободина, В.А. Румянцев // Клиническая лабораторная диагностика. 2005. — №9. — С. 62-63.
156. Современные средства экзогенной профилактики заболеваений полости рта / JI.A. Хоменко, Н.Б. Биденко, Е.И. Остапко, В.И. Шматко Киев.: «Книга плюс»., 2001. — 207 с.
Современные средства экзогенной профилактики заболеваений полости рта / JI.A. Хоменко, Н.Б. Биденко, Е.И. Остапко, В.И. Шматко Киев.: «Книга плюс»., 2001. — 207 с.
157. Состояние микробиоценоза полости рта у детей в норме и при патологии по результатам изучения микробных метаболитов слюны /
158. B.М. Елизарова, А.В. Горелов, М.Д. Ардатская, А.В. Дикая // Российский стоматологический журнал. 2009. — №2. — С. 12-17.
159. Справочник по стоматологии / Под ред. А.И. Рыбакова. 3-е изд., перераб. и доп. М.: Медицина, 1993.- 576 с.
160. Сравнительная оценка клинического воздействия новой мануальной зубной щетки на удаление зубного налета и снижение проявления гингивита / D.M. Petrone, P. Chaknis, М. Petrone и др. // Новое в стоматологии. 2006. — №3(135). — С. 56-58.
161. Турбовская, С.Н. Сочетанная амплипульс-ультразвуковая терапия у больных с атопическим дерматитом: Афтореф. Дис. .канд. мед. наук / С.Н. Турбовская: М. 2003. -24 с.
162. Улитовский, С.Б. Гигиена полости рта — первичная профилактика стоматологических заболеваний / С. Б. Улитовский. М., 1999.- 144 с.
Б. Улитовский. М., 1999.- 144 с.
163. Улитовский, С.Б.Средства и методы гигиены полости рта / С.Б. Улитовский // Новое в стоматологии. 2001. — №10. — С. 83-85.
164. Улитовский, С.Б. Практическая гигиена полости рта / С.Б. Улитовский. М., 2002.- 230с.
165. Улитовский, С.Б. Гигиенические предпосылки развития гингивита у детей и подростков, находящихся на ортодонтическом лечении / С.Б. Улитовский // Новое в стоматологии. 2003. — №8. -С. 41-42.
166. Улитовский, С.Б. Принципы профилактики основных стоматологических заболеваний / С.Б. Улитовский // Новое в стоматологии. 2003. — №8. — С. 29-39.
167. Улитовский, С.Б. Гигиена полости рта в пародонтологии / С.Б. Улитовский. М.Медкнига. — 2006. — 266 с.
168. Улитовский, С.Б. Гигиена полости рта при заболеваниях пародонта / С.Б. Улитовский // Новое в стоматологии. 2006. -№7(139). — С. 78-80.
169. Улитовский, С.Б. Triumph — Start Brush (или щетка, которая думает) / С.Б. Улитовский // Новое в стоматологии. — 2006. №8(140). — С. 67-700.
№8(140). — С. 67-700.
170. Ультразвуковоя обработка кариозной полости: триумф оперативного мастерства / Г.М. Барер, И.А. Овчинникова,
171. B.А. Завьялова, В.Г. Маслий // Клиническая стоматология.- 2002.- №2.1. C.-20-22.
172. Уртане, И.Ф. Влияние ортодонтического лечения на интенсивность процесса кератинизации эпителиальных клеток слизистой оболочки твердого неба и десен / И.Ф. Уртане // Стоматология. 1980. — №5. — С. 49 — 51.
173. Утешев, Б.С. Интерлейкины, как препараты и объекты фармакологического воздействия (Обзор) / Б.С. Утешев // Антибиотики и химиотерапия.- 1989.-Т.34.-№11.-С. 869-874.
174. Ушаков, Р.В. Микрофлора полости рта и ее значение в развитии стоматологических заболеваний / Р.В. Ушаков, В.Н. Царев // Стоматология для всех.- 1998.- №3.- С. 22-27.
175. Физиотерапия воспалительных заболеваний челюстно-лицевой области: Метод, рекомендации / Сост. О.И. Ефанов, А.Д. Панина, Г.Н. Перегудова. -М.Д986. -45 с.
176. Фрейдлин, И.С. Ключевая позиция макрофагов в цитокиновой регуляторной сети / И. С. Фрейдлин // Иммунология. 1995.-№3.-С.44-48.
С. Фрейдлин // Иммунология. 1995.-№3.-С.44-48.
177. Фрейдлин, И.С. Клетки иммунной системы: развитие, активация, эффекторные функции / И.С. Фрейдлин // 2-ой Съезд иммунологов России: Тезисы докладов. Сочи, 1999.- С. 9-15.
178. Халитова, Э.С. Количественные и качественные показатели десневой жидкости в норме и при патологии тканей пародонта: Автореф. дис. канд. мед. наук /Э.С. Халитова: Москва.- 1989.- 28 с.
179. Характеристика лейкоцитарных маркеров у больных хроническим генерализованным пародонтитом в фазе обострения / А.Е. Романов, Е.Н. Николаева, Е.М. Фомичева и др. // Стоматология. -2003.-№6. -С. 13-16.
180. Хусаинова, И.С. Оценка цитологических показателей буккального эпителия для диагностики функционального состояния человека / И.С. Хусаинова, И.Ю. Варвулева, Н.А. Кожина // Клиническая лабораторная диагностика. 1997. — №3. — С. 10-12.
181. Цимбалистов А.В. Профессиональная гигиена полости рта / А.В.Цимбал истов, Г.Б.Шторина, Е.С. Михайлова СПб.: Изд. «Санкт-Петербургский институт стоматологии». 2002.-48с.
2002.-48с.
182. Цимбалистов, А.В. Иммунологические механизмы в патогенезе непереносимости стоматологических конструкционных материалов /
183. A.В. Цимбалистов, Е.С. Михайлова // Маэстро стоматологии. 2008. -№2 (30).-С. 5-8.
184. Цитологические показатели как критерии оценки состояния пародонта / А.С. Григорьян, А.И. Грудянов, З.П. Антипова и др. // Стоматология.- 1998.-№3.- С.17-21.
185. Цымбалов, О.В. Лейкинферониндуцированная динамика цитохимических показателей ядра и цитоплазмы нейтрофильных гранулоцитов раневого экссудата у больных с флегмонами челюстно-лицевой области / О.В. Цымбалов, Д.Л. Беляев, А.А. Евгелевский,
186. B.А. Демченко // Стоматология. 2000. — №4. — С. 42-45.
187. Чередеев, А.Н. Итоги науки и техники / А.Н. Чередеев, Л.В. Ковальчук // Иммунология.- М., 1989. Т. 19. — 238 с.
188. Шабалова, И.П. Цитологический атлас. Критерии диагностики заболеваний шейки матки: Пособие для врачей / И.П. Шабалова. -Тверь: Губернская медицина, 2001. 120 с.
120 с.
189. Шаповалов, В. Д. Иммунопатологические механизмы формирования воспалительных заболеваний и методические подходы кназначению патогенетической терапии: Дис.докт. мед. наук / В.Д. Шаповалов: ИИФУ «Медбиоэкстрем» при Минздраве РФ. — Москва, 2001.- 191 с.
190. Шмагель, К.В. Современные взгляды на иммунологию пародонтита. Обзор / К.В. Шмагель, О.В. Беляева, В.А. Черешнев // Стоматология. 2003. — №1. — С. 61-64.
191. Щербак, В.А. Цитокины при иммуномодулирующей терапии у детей с хроическим гастродуаденитом / В.А. Щербак, Б.И. Кузник, Ю.А. Витковский // Иммунология, 2005. №6. — С. 342-344.
192. Щербинина, Л.Г. Цитологическая картина содержимого десневых карманов до и после комплексного лечения пародонтоза / Л.Г. Щербинина // Врачебное дело.- 1963.- №9.- С. 99-103.
193. Янушевич, О.О. Состояние тканей пародонта у населения в возрасте 35-44 лет в регионах России / О.О. Янушевич, И.Н. Кузьмина // Российский стоматологический журнал. 2009. — №1. — С. 43 — 45.
194. Adbel-Razzak, M.Y. Immunopathology of T-lymphocyte sybsets in yuvenile and rapidly progressive periodontitis / M.Y. Adbel-Razzak // J. Egypt Dent. 1994. — 40. — №1. — P. 581-588.
195. Allais, G. Биопленка полости рта / G. Allais // Новое в стоматологии. 2006. — № 8(140). — С. 67-70.
196. Anti-inflammatory cytokine IL-10 and T cell cytokine profile in periodontitis granulation tissue / D.F. Lappin, C.P. Macleod, A. Kerr et al. // Clin. Exp. Immunol. 2001. — № 2. — P. 294-300.
197. Bickel, M. The role of interleukin 8 in inflammation and mechanisms of regulation / M. Bickel // J.Periodontal. — 1993. -№ 64(5 Suppl.). — P. 456-460.
198. Birkedal-Hansen, H. Role of matrix metalloproteinases in human periodontal diseases / H. Birkedal-Hansen // Journal of Periodontology.-1993.- Vol.64.- N 5.- P. 474-484.
199. Birkedal-Hansen, H.Role of cytokines and inflammatory mediators in tissue destruction / H. Birkedal-Hansen // Journal of Periodontology.- 1993.-Vol. 26.-N 6.- P.500-510.
26.-N 6.- P.500-510.
200. Brandzaeg, P. Overview of mucosal immune system / P. Brandtzaeg // Curr.Top. Microbiol. Immunol. 1989. — 146. — P. 13 — 28.
201. Branemark, P.F. Tissue integrated prostheses. Osseointegration in clinical dentistry / P.F. Branemark, G.A. Zarb, T. Albrektsson // London: Quintess. Publ. Co Inc. — 1985. — 350 p.
202. Buja, L.M. Apoptosis and necrosis. Basic types and mechanisms of cell death / L.M. Buja, M.L. Eigebradt // Arch. Pathol. Lab. Med. 1993. -V.117.-P. 1208-1214.
203. Burkhardt, A. Intraepithelial lymphocytes and Langerhans cells in the oral mucosa: dynamic aspects / A. Burkhardt // J. Dent. Assoc. South Afi.1992.-V. 47.-P. 200-203.
204. Butcher, F. The regulation of lymphocyte traffic / F. Butcher // Curr. Top. Microbiol. Immunol. 1986. — V.128. — P. 85-122.
205. Carranza, F.A., Clinical Periodontology/ F.A. Carranza, M.G. Newman // Philadelphia W.B. Saunders Co., 1996.- 782 p.
206. Cell surface patterns in normal human oral gingival epithelium. A quantitative scanning electron microscopy approach / G. Moreu, M.C. Sanchez-Quevedo, J.A. Lopez-Escamez et al. // Histol. Histopathol.1993.- V.8.-P. 47-50.
A quantitative scanning electron microscopy approach / G. Moreu, M.C. Sanchez-Quevedo, J.A. Lopez-Escamez et al. // Histol. Histopathol.1993.- V.8.-P. 47-50.
207. Challacombe, S.J. Passage of serum immunoglobulins into the oral cavity / S.J. Challacombe // The Borderline between Caries and Periodontal Disease London.: Acad. Press. — 1980. — V. II. — P. 51-68.
208. Chavrier, C. The elastic system fibers in healthy human gingiva / C. Chavrier// Arch. Oral Biol. 1990. — V. 335. — P. 223-225.
209. Chung, R.M. Interleukin 8 and beta glucuronidase in gingival crevicular fluid / R.M. Chung, J.T. Grbic, I.B. Lamster // J. Clin.Periodontol, 1997. — №24(3). — P. 146-152.
210. Clinical and immunological findings in a family with generalized aggressive periodontitis / G. Aren, N. Gurel, F. Yalcin, E. Firatle // J. Dent. Child (Chic). 2003. — 70. — № 3. — P. 266-271.
211. Cohen, N. Instruction of tolerance by porphyromonas gingivalis on APCs / N. Cohen, J. Morisset, D. Emilie // J. Dent. Res. 2004. — Vol.83. -№5.-P. 429-433.
Emilie // J. Dent. Res. 2004. — Vol.83. -№5.-P. 429-433.
212. Convertion of a stable T-cell lesions to a progressive B-cell lesion the pathogenesis of chronic inflammatory periodontal disease: an Hypothesi / G.I. Seymor, R.N. Powell, W.I. Davies et al. // J. Clin Periodontol. 1979. -V.6. — P. 267-277.
213. Cox, F. Candida albicans adherence in newborn infants / F. Cox // J. Med. Veter. Mycol. 1986. — V. 24. — P. 121-125.
214. Crawford, J.M. Distribution of ICAM-1, LFA-3 and HLA-DR in healthy and diseased gingival tissues / J.M. Crawford // J. Periodont. Res. -1992.-V. 27.-P. 291-298.
215. Cripps, S. Periodontal Disease: Recognition, Interception and Prevention / S. Cripps // Quinttessence Publ. Co Inc. 1984. — 290 p.
216. Cristifero, P. Role of toll-like receptors in infection and immunity: clinical implications / P. Cristifero, S.M. Opal // Drugs. 2006. — Vol.66. -№ 1. — P. 15-29.
217. Davarpanah, M. Periodontal diseases. Clinical forms, epidemiology, etiology, prevention / M. Davarpanah, J.F. Tecuciano, M. Kebir // Rev Prat.-1994.- Vol.44.-P. 374.
Davarpanah, J.F. Tecuciano, M. Kebir // Rev Prat.-1994.- Vol.44.-P. 374.
218. Diamond, R.D. Atlas of fungal instructions / R.D. Diamond. -Philadelphia: Curret. Medicine.- 2000- 236 p.
219. Distribution and phenotype of immune cells in normal human gingiva: active immune response versus unresponsiveness / A. Colasante, S. Rosini, A. Piattelli et al. // J. Oral Path. Med. 1992. — Vol. 21. — P. 12-16.
220. Dongari-Bagtzoglou, A.I. Production of inflammatory mediators and cytokines by human gingival fibroblasts following bacterial challenge / A.I. Dongari-Bagtzoglou, J.L. Ebersole // Journal Peridontol Res.- 1996.-Vol.31.-N2.-P. 90-98.
221. Effect of ultrasonic and sonic scalers of dental plaque microflora in vitro and in vivo / P. Baehni, B. Thilo, B. Chapius, D. Pernet // J. Clin. Periodontal. 1992. — Vol. 19. — P. 455-459.
222. Elley, B.M. Advances in periodontal diagnosis. 5. Potetntial inflammatory and immune markers / B.M. Elley, S.W. Cox // Journal of Br-Dent. , England.- 1998.- Vol.184.- N5.- P. 220-223.
, England.- 1998.- Vol.184.- N5.- P. 220-223.
223. Elley, B.M. Advances in periodontal diagnosis. 7. Proteolytic and hydrolytic enzymes link with periodontitis / B.M. Elley, S.W. Cox // Journal of Br-Dent., England. 1998.-Vol. 184.- N 7. — P. 323-328.
224. Eversole, L.R. The distribution of the antimicrobial protein, calprotectin in normal oral keratinocytes / L.R. Eversole, K.T. Miyasaki, R.E. Christensen // Arch. Oral Biol. 1992. — V. 37. — P. 963-968.
225. Functional hyman T-cell immunity and osteoprotegerin ligand control alveolar bone destruction in periodontal infection / Y.T.A. Teng, H. Nguyen, X.J. Gao et al. // J. Clin. Invest. 2000. — Vol. 106. — №6. — P. 59-67
226. Gao, Z. Patterns of phenotypic expression of human junctional, gingival and reduced enamel epithelia in vivo and in vitro / Z. Gao, I.C. Macken-zie // Epithelial Cell Biol. 1992. — Vol.1. — P. 156-167.
227. Gagnot, G. Ультразвуковое лечение пародонтальных карманов. Новый структурный подход / G. Gagnot, J. Darsel, J.F. Michel // Стоматология сегодня. 2001. — №7(10). — С. 16-17.
Gagnot, J. Darsel, J.F. Michel // Стоматология сегодня. 2001. — №7(10). — С. 16-17.
228. Garant, P.R. The ultrastructure of clinically normal suicular tissues in the beagle dog / P.R. Garant, J.E. Mulvihill // J. Periodont. Res. 1971. -Vol. 6.-P. 252-258.
229. Gee, I.M. The relationship between concentrations Qf proinflammatory cytokines within gingival and the adjacent suicular depth / I.M. Gee, M.A. Tucci, T.P. Edmundson // Journal of Periodontology.- 1998.-Vol. 69.- N 8. P.865-871.
230. Gemmel, E. Cytokine profile of Porphyromonas gingivalis reactive T-lymphocyte line and derived from p. gingivalis -infected subjects / E. Gemmel, M. Kjeldsen// Oral-Dis.-1995.-Vol.l.-№3.-P. 139-146
231. Genco, R. Сердечно-сосудистые заболевания и инфекция в полости рта. In: R. Genco, L.F. Rose, D.W. Cohen, B.L. Mealey eds. Periodontal Medicine. ВС Decker Inc. -2000. P. 63-82.
232. Gibbons, R.J. Bacterial adherence in oral microbial ecology / R.J. Gibbons, J. Van Houte // Annual Rev. Microbiol. 1975. — Vol. 29. -P. 19-44.
Microbiol. 1975. — Vol. 29. -P. 19-44.
233. Gillespie, G.M. Renewal of buccal epithelium /G.M. Gillespie // Oral Surg. 1969. — Vol. 27. — P. 83-89.
234. Gingival suicular leukocytes in periodontitis and in experimental gingivitis in humans / C. Thurre, M. Rovert, G. Cimasoni, P. Baehni // J. Periodont. Res. 1984. — Vol. 19. — P. 457-468.
235. Gingival crevicular interleukin 1 and interleukin — 1 receptor antagonist levels in peruodontally healthy and diseased sites / Y.Ishihara, T. Nishihara, P. Emery et al // J.Periodontal.Res. — 1997. -Vol. 32. — P. 524529.
236. Golding, S. Tenidap-modulated proinflammatory cytokine activation of monocyte cell line / S. Golding, P. Emery, S.P. Young // Immunology. 1995. — Vol. 154 — P. 5384-5390.
237. Growth regulation of serum-free cultures of epithelial cells from normal human buccal mucosa / K. Sundqvist, Y. Liu, K. Arvidson et al. // In Vitro Cell. Develop. Biology-Animal. 1991. — Vol. 21 A. — P. 562-568.
238. Gyorfi, A. Neurogenic inflammation and the oral mucosa /A.Gyorfi, A. Fazekas, L. Rosivall // J. Clin. Periodontol. 1992. — Vol. 19. -P. 731-736.
Neurogenic inflammation and the oral mucosa /A.Gyorfi, A. Fazekas, L. Rosivall // J. Clin. Periodontol. 1992. — Vol. 19. -P. 731-736.
239. Haffage, A.D. Microbial etiological agents of destructive periodontal diseases / A.D. Haffage, S.S. Socransky // Periodotol. 2000. -№10.-p. 78-88.
240. Hancock, E.B. Current epidemiological consideration of periodontal disease / E.B. Hancock., D.H. Newell // Curr. Opin. Periodontol. 1993. -Vol. 3.-P. 3-10.
241. Hillmann, G. Histopathological investigation of gingival tissue from patients with rapidly progressive periodontitis / G. Hillmann, S. Dogan, W. Geurtsen // J.Periodontol. 1998. — №2. — P. 195-208.
242. Hellwig, E. Einfuhrung in die Zahnerhaltung / E. Hellwig, J. Klimek, T. Attin // Munchen: Urban & Schwarzenberg.- 1999. P. 295-306.
243. Hou, L.T. Cloning and characterization of human gingival and periodontal ligament fibroblasts / L.T. Hou, J.A. Yaeger // J. Periodontol. -1993.-Vol. 64.-P. 1209-1218.
244. Hou, L.T. Toll-line receptor 4-deficient mice have reduced bone destruction following mixed anaerobic infection / L.T. Hou, S. Hajime, S. Philip // Infect. Immun. 2000. — Vol. 68. — №8. — P. 123-131.
Hou, L.T. Toll-line receptor 4-deficient mice have reduced bone destruction following mixed anaerobic infection / L.T. Hou, S. Hajime, S. Philip // Infect. Immun. 2000. — Vol. 68. — №8. — P. 123-131.
245. Hunter, N. The interaction of bacterial peptidoglycan with macrophages in chronic inflammation / N.Hunter // J. Dent. Res. 1984. -Vol. 63.-P. 427-430.
246. Individual diversities in interferon gamma production by hyman peripheral blood mononuclear cells stimulated with periodontopathic bacteria / H. Kobayashi, T. Nagasawa, M. Aramaki et al. // J Periodontol Res. 2000. — Vol. 35. — №6. — P. 319-328.
247. Infection patterns incronic and aggressive periodontitis / D.K. Picolos, J. Lerche-Sehm, A. Abron et al. // J. Clin. Periodontal. 2005. — Vol.32. -P. 1055-1061.
248. Interleukin 1 alpha, interleukin — 8 and interferon alpha levels in gingival crevicular fluid / A. Mathur, B. Michalowicz et al. // J.Periodontol Res. — 1996. — Vol. 31 (7). — P. 485-495.
249. IL-8 degradation by Porphyromonas gingivalis proteases / J. Zhang, H. Dong, S. Kashket, M.J. Duncan // Microb. Pathog. 1999. — May. -№26 (5).-P. 275-280.
IL-8 degradation by Porphyromonas gingivalis proteases / J. Zhang, H. Dong, S. Kashket, M.J. Duncan // Microb. Pathog. 1999. — May. -№26 (5).-P. 275-280.
250. Interaction of inflamminatory cells and oral microorganisms VIII Detection of Ieukotoxicactivity of a plaque-derived gram-negative microorganism / P. Bachni, C.C. Tsai, W.P. McAzthar et al. // Infection and Immunity.- 1979.- №24. P.233-243.
251. Interobserver variability in the cytological diagnosis of 1500 Papanicolaou stained carvical monolayer specimens / H. Naujoks, R. Strogmeier, T. Bicker et al. // Pathol. Res. Pract. 1990. — Vol. 186. -P. 150-153.
252. Ivanyi, L. Cell-mediated immunity inperiodontal disease: Citotoxicity, migration inhibition and lymphocyte transformation studies / L. Ivanyi, T. Lehner, J.M.A. Wilton //Immunology.- 1972.- Vol. 226.- P. 141-145.
253. Ivanyi L. Stimulation of lymphocyte transformation by bacterial antigens in patients with periodontal disease / L. Ivanyi, T. Lehner // Arch. Oral. Biol. 1970. -Vol.16. -№11. -P. 1089- 1096.
Oral. Biol. 1970. -Vol.16. -№11. -P. 1089- 1096.
254. Ivanyi, L. Lymphocyte transformation by silicates of dental plaque in human periodontal disease /L. Ivanyi, T. Lehner //Arch. Oral Biol. 1971. -Vol.16. -№ 9.-P. 1117-1121.
255. Ivanyi, L. Cell-mediated immunity in periodontal disease: Citotoxicity, migration inhibition and lymphocyte transformation studies / L. Ivanyi, J.M.A. Wilton, T. Lehner // Immunology. 1972. — Vol. 226. -P.141-145.
256. Jaattela, M. Biologic activities and mechanisms of action of tumor necrosis factor-a (cachectin) / M. Jaattela //Journal of Laboratory Investigation. 1991. — Vol. 64. — №6. — P. 724.
257. Kellar, K.L. Multiplexed microsphere-based flow cytometric immunoassays for human cytokines / K.L. Kellar, J.P. Dougliss // J. Immunol. Meth. 2003. — Vol. 279. — P. 277-285.
258. Kinane, D.F. Pathogenesis of Periodontitis / D.F. Kinane, J. Lindhe // Clinical Periodontology and Implant Dentistry (Third Edition). -Copenhagen.- 1997. P. 189-229.
P. 189-229.
259. Knoh, K.A. Regulation of apoptosis in germinal center В cells / K.A. Knoh, J.T. Gordon // Immunol. Today. 1995. — V. 16(2). — P. 106107.
260. Kovaks, E.J. Regulation of fibroblasl proliferation and collagen synthesis by cytokines / E.J. Kovaks // Immunol. Today. 1991. — V. 12. -P. 17-23.
261. Kvidera, A. Rates of clearance of the epithelial surfaces of mouse oral mucosa and skin /А. Kvidera, I.C. Mackenzie // Epithel. Cell Biol. 1994. -Vol.3. — P. 175-180.
262. Lander, B. Dental used for periodontal patients / B.Lander // J Am Dent Ass. 1990.-Vol. 121 (4). — P. 505-508.
263. Lebendiger, M. Characterization of mononuclear cells in the human oral mucosa / M. Lebendiger, T. Lehner // Arch. Oral Biol. 1981. -Vol. 26.-P. 1041-1052.
264. Lefrancois, L. Extrathymic differentiation of intraepithelial lymphocytes: Generation of separate and unequal T — cell repertoire / L. Lefrancois // Immunol. Today. 1991. — Vol. 12. — P. 436 — 438.
265. Leous, P. Effectiveness of a three-year toothbrashing programon the periodontal status of young adults / P. Leous, L. Kazeko, S. Agievtseva // J. Dental Research. 1996.- Vol. 75, Special issue. — P. 427.
Leous, P. Effectiveness of a three-year toothbrashing programon the periodontal status of young adults / P. Leous, L. Kazeko, S. Agievtseva // J. Dental Research. 1996.- Vol. 75, Special issue. — P. 427.
266. Lindhe, J. Textbook of clinical periodontology / J. Lindhe -Copenhagen, Munksgoal, 1993.-648 p.
267. Listgarten, M.A. Normal development, structure, physiology and repair of gingival epithelium / M.A. Listgarten // Oral Science Review. -1972.-Vol. l.-P. 3-67.
268. Loe, H. The site of mitotic activity in rat and human oral epithelium /Н. Loe, T. Karring, К. Hara // Scand. J. Dent. Res. 1972 — Vol. 80. -P. 11-19.
269. Loe, H. Experimental gingivitis in man / H.Loe, E. Theilade, S.Jensen // J Periodont. 1965. — Vol. 36. — P. 177-187.
270. Loos, B. An evaluation of basic periodontal therapy using sonic and iltrasonic scalers / B. Loos, R. Kieger, J. Egelberg // J. Clin. Periodontol. -1987.-Vol. 14.-P 29-33.
271. Lundqvist, С. T-cell receptor gamma/delta-expressing intraepithelial lymphocytes are present in normal and clinically inflamed human gingiva / C. Periodontal. 1999. — № 8 — P. 935-949.
Periodontal. 1999. — № 8 — P. 935-949.
273. Magno, G. Apoptosis, oncosis, necrosis / G.Magno, J. Joris // Amer. J. Pathol. 1995. — Vol. 146. — P. 3-15.
274. Mariotti, A. Characterization of fibroblasts derived from human periodontal ligament and gingiva /А. Mariotti, D.L. Cochran // Periodontol. -1990,- V. 61.-P. 103-111.
275. Mathur, A. Cell-mediated immune system regulation in periodontal diseases /А. Mathur, B.S. Michalowicz // Crit. Rev. Oral. Biol. Med. -1997. Vol. 8. — №1. — P. 76-89.
276. Medak, H. Atlas of oral cytology / H. Medak // Public Health Service Publiction No. 1949.
277. Merbse, J. IFN-Y inhibits activation-induced expression of E- and P-selectin on endothelial cells / J. Merbse, N. Tsurushita, G. Liu, E.L. Berg //Journal of Immunology. 1998. — Vol. 161. — P. 2457-2464.
278. Murakami, Y. Fibronection in saliva inhibits porphyromonas gingivalis fimbriaiduced expression of inflammatory cytokine gene in mouse macrophages / Y. Murakami, S. Hanazawa // Fems-Immunol-Med-Microbiology. 1998. — Vol. 22. — № 3. — P. 257-262.
Hanazawa // Fems-Immunol-Med-Microbiology. 1998. — Vol. 22. — № 3. — P. 257-262.
279. Nalbant, A. Evidence for apoptosis of the majority of T cells activated in vitro with ctinobacillus actinomycetemcomitans / A. Nalbant, H.H. Zadeh // Oral Microbiol. Immunol. 2000. — Vol. 15. — №5. — P. 290-298.
280. Natural killer (NK) cell activity against human gingival fibroblasts exposed to dental plaque extracts / G.J. Seymour, B.W. Horwood, J. Aaskov, S.N. Powell // J.Periodontal. 1984. — Vol. 55. — № 5. -P. 289-293.
281. Okada, H. T lymphocyte subsets in the inflamed gingival of human abult periodontitis / H. Okada, S. Murakami // Journal Periodontal Res.-1984.-Vol. 19.-P. 595-598.
282. Page, R.S. Pathogenesis of inflammatory periodontal disease. A summary of current work / R.S. Page, H.E. Schroeder // Lab Invest. 1976. -V. 33.-P. 235-249.
283. Pane, W.A. Histopathologic features of initial and early stages of experimental gingivitis in man / W.A. Pane, R.C. Page, A. L. Ogilvie, W.B. Hall // J. Periodont Res. 1975. — Vol. 10. — P. 51-64.
L. Ogilvie, W.B. Hall // J. Periodont Res. 1975. — Vol. 10. — P. 51-64.
284. Peptin, L.F. Preferential V delta 1 expression among NcR gamma/delta-bearing T cells in human oral epithelium / L.F. Peptin,
285. Т. Roger, J. Morisset, M. Seman // Scand. J. Immunol. 1993. — Vol. 37. -P. 289-294.
286. Peritoneal cavity CD5 (Bla) В cells: Citokine induced IgA secretion and homing to intestinal lamina propria in SCID / K.M. Beagley,
287. A.M. Myrray, J.R. McGhee, J.H. Eldridge // Immunol. Cell Biol. 1995. -Vol. 73.-P. 249-255.
288. Phagocytosis of periodonto-pathogenic bacteria by crevicular granulocytes is depressed in progressive periodontitis / S. Eick, W. Pfister,
289. B. Sigusch, E. Straube // Infection. 2000. — Vol. 28. — №5. — P. 301-304.
290. Pober, J.S. IFN-y enhances endothelial activation induced by tumor necrosis factor but not interleukin-1 / J.S. Pober // Journal of Immunology.- 1990. Vol.145. — №6 — P.1727 — 1733.
291. Ratcliff, P.A. The relationship between oral malodor, gingivitis and periodontitis. A review / P.A. Ratcliff, P.W. Johnson // J.Periodontol. -1999.- №5. P.485-489.
The relationship between oral malodor, gingivitis and periodontitis. A review / P.A. Ratcliff, P.W. Johnson // J.Periodontol. -1999.- №5. P.485-489.
292. Reddi, K. Comparison of the pro-inflammatory cytokine -strimulating activity of the surface-associated proteins of periodontopathic bacteria / K. Reddi, M. Wilson // Journal Periodontal Res. 1996.- Vol.31.-№2.- P.120-130.
293. Removal of interproximal subgingival plaque by hand and automatic toothbrushes / J.Y. Taylor, C.L. Wood, J.J. Garnick, W.O. Thompson // J. Periodontol. 1995. — № 66. — P.191-196.
294. Roberts, F.A. Profile of cytokine MRNA expression in chronic adultperiodontitis / F.A. Roberts, K.A. McCaffery, S.M. Michalek // J.Dent.- 1997. Vol. 76(12). — P. 1833-1839.
295. Role of cytokine in the induction of adhesion molecules on cultured human gingival fibroblasts / K. Takahashi, M. Takigawa, S. Takashiba et al. // J. Periodontol. 1994. — Vol. 65. — P. 230-235.
296. Rosenberg, R.M. The effect of root surface roughness on plaque accumulation and gingival inflammation / R. M. Rosenberg, M.M. Ash // J. Periodontol. 1974. — № 18. — P. 146.
M. Rosenberg, M.M. Ash // J. Periodontol. 1974. — № 18. — P. 146.
297. Saito, S. Interactive effects between cytokines on PGE production by human periodontal ligament fibroblasts in vitro / S. Saito, P. Ngan, M. Saito // Journal Dent. Res. 1990. — Vol. 69. — № 8. — P. 1456-1462.
298. Saito, S. Interleukin 1 beta and prostaglandin E are involved in the response of periodontal cells to mechanical stress in vivo and in vitro / S Saito, P. Ngan, M. Saito // Am-Jounal-Orthod-Dentifacial-Orthop.- 1991.-Vol. 99.-P.95.
299. Scannacepieco, F.A. Воспаление тканей пародонта: от гингивита к системному заболеванию / F.A. Scannacepieco // Compend Cont Educ Dent 2004.-Vol. 25(7 Suppl 1).-P. 16-25.
300. Scully, C. Transport and function of polymorphonuclear leucocytes in crevicular fluid / C.Scully // The Borderline between Caries and Periodontal Disease. London.: Acad. Press, 1980. — Vol. II. — P. 69-84.
301. Schroeder, H.E. Transmigration and infiltration of leucocytes in human junctional epithelium / H. E. Schroeder // Helv. Odontol. Acta. -1973.-Vol. 17.-P. 6-18.
E. Schroeder // Helv. Odontol. Acta. -1973.-Vol. 17.-P. 6-18.
302. Schoroeder, H.E. Ultrastructure of the functional epithelium of the human gingiva / H.E. Schoroeder // Helv. Odont. Acta. 1969. — Vol. 13. -P. 63-83.
303. Schoroeder, H.E. Age-related decline of lymphoid tissue components in the oral mucosa of the lip, cheek and soft palate of Macaca fascicularis / H.E. Schroeder, A. Dorig-Schwarzenbach // Cell Tiss. Res. 1984. -Vol. 235.-P. 195-199.
304. Seguier, S. Immunohistological and morphometric analysis of intraepithelial lymphocytes and Langerhans cells in healthy and diseased human gingival tissues / S. Seguier, G. Godeau, N. Brousse // Arch Oral Biol. 2000. — Vol. 45. — №6. — P. 441-452.
305. Seymour, G.J. Experimental gingivitis un humans. A clinical and histological investigation / G.J. Seymour, R.M. Powell, J.F. Aitken // J. Periodontol. 1983. — Vol. 54. — №9. — P. 522-528.
306. Sigusch, B. Altered chemotactic behavior of crevicular PMNs in different forms of periodontitis / B. Sigusch, S. Eick, W. Pfister el al. // J Clin Periodontol. 2001. — Vol. 28. — №2. — P.162-167.
Sigusch, S. Eick, W. Pfister el al. // J Clin Periodontol. 2001. — Vol. 28. — №2. — P.162-167.
307. Sistemik neutrophil response resulting from dental plaque accumulation / M. J. Kowolik, S.A. Dowsett, J. Rodguees et al. // J. periodontal. 2001. — Vol. 72. — №2. — P. 146-151.
308. Socransky, S.S. New concepts of destructive periodontal disease / S.S. Socransky, A.D. Haffajee, J.M. Goodson, J. Lindhe // J. Clin. Periodont. 1984.-Vol.11.-P. 21-32.
309. Soluble antagonists to interleukin-1 (IL-1) and tumor necrosis factor (TNF) inhibits loss of tissue attachment in experimental periodontitis / A.J. Delima, T. Oates, R. Assuma et al. // J Clin Periodontol. 2001. -Vol.28. — №3. p. 233-240.
310. Squier, C.A. The permeability of keratinized and nonkeratinized oral epithelium to lanthanum in vivo / C.A. Squier, L. Rooney // J. Ultrastruct. -1976. Vol.54. — P. 286-295.
311. Stern, I.B. Oral mucous membrane / I.B. Stern // Orban’s Oral Histology and Embryology. Saint Louis. — Mosby. — 1976. — P. 253-327.
— Mosby. — 1976. — P. 253-327.
312. Stirling, D. Qualitative and quantitative PCR: atechnical over — view / D. Stirling // Methods Mol. Biol. 2003. — Vol. 225. — P. 181 -184.
313. Straka, M. Пародонтология 2000 / M. Straka // Новое в стоматологии.- 2002.- №8.- С. 29-31.
314. Structure et organisation des collagenes du tissu gingival /C.Chavrier, M.L. Couble, J.A. Grimaud, H.Magloire // Parodontol. 1985. — Vol.4.-P. 233-236.
315. Tabak, L.A. In defence of the oral cavity: structure, biosynthesis and function of salivary mucins / L.A. Tabak // Annu. Rev. Physiol. 1995. -Vol. 57. — P. 547-564.
316. Taichman, R.S. Effects of interleukin 1 beta and tumor necrosis factor-alpha on osteoblastic exspression of osteocalcin and mineralized extracellular matrix in vitro / R.S. Taichman, P.V. Hauschka // Inflamation.-1992.- Vol.16.- N 6.- P. 587-601.
317. Takahashi, K. Detection of interleukin -1 beta mRNA expressing cells in human gingival crevicular fluid by in situ hybridization / K. Takahashi, I. Poole, D.F. Kinane // Arch. Oral. Biol. -1995. -Vol. 40(10).-P. 941-947.
Takahashi, I. Poole, D.F. Kinane // Arch. Oral. Biol. -1995. -Vol. 40(10).-P. 941-947.
318. Takeichi, O. Human polymorphonuclear leucocytes derived from chronically inflamed tissue express inflammatory cytokines in vivo / O. Takeichi, I. Saito // Cell-Immunology. 1994. — Vol.156. — N2. -P. 296-309.
319. Taugerbeck, R. Ультразвук в стоматологической практике / R. Taugerbeck // Квинтэссенция. 1996. — №3. — С. 22-23.
320. Thl and Th3 cytokine profile in patients with early onset periodontitis and their healthy siblings / J. Bartova, Z. Kratka Opatma, J. Prochaz-kova et al. // Medial Inflam. 2000. — Vol. 9. — №2. — P. 115-120.
321. The mucosal immune system from fundamental concepts to vaccine development / J. Me Ghee, J. Mestecky, M. Detzbaugh et al. // Vaccin. -1992. -Vol.10.-P. 75-88.
322. Thornhill, M.H. IL-4 regulates endothelial cell activation by 1L-1, tumor necrosis factor or ifn-y. / M.H. Thornhill, D.O. Haskard // Journal of Immunology. 1990. — Vol. 145. — №3. — P. 865-872.
— №3. — P. 865-872.
323. Tomasi, T. The discovery of secretory IgA and the mucosal immune system / T. Tomasi // Immunology Today. 1992. — Vol.13. — P. 416-421.
324. Tumor necrosis factor combines with IL-4 or IFN-you selectively enhance endothelial cell adhesiveness for T-cell / M.H. Thornhill., S.M. Wellicom, D.Q. Mahiouz et al. //Journal of Immunology. 1991. -Vol. 146. — №2. — P. 592-598.
325. Wang, S.Y., Stashenko P. Characterization of bone resorbing activity in human periapical lesisons / S.Y. Wang //Journal Endod. 1993. — Vol.19. -N3.-P. 107-111.
326. Waerhaug, J. Effect of rough surfaces upon gingival tissues / J. Waerhaug // Int. Dent. J. 1956. — V. 45. — P. 322.
327. WHO: Oral health surveys basic methods, 4 edition. Gevena, 1997. — 66 p.
328. Wilkins, E.M. Clinical practice of the dental hygienist / E.M. Wilkins // A Lea & Fibiger Book. 1994.-865 p.
329. Williams, R.C. Inhibition of bacterial adherence by secretory immunoglobulin A: a mechanism of antigen disposal / R. C. Williams, R.J. Gibbons // Science. 1972. — Vol. 177. — P. 697-699.
C. Williams, R.J. Gibbons // Science. 1972. — Vol. 177. — P. 697-699.
330. Wilson, T.G. Fundamentals periodontics / T.G. Wilson, K.S. Kornman // Quintessence Publishing Co. 1996. — 564p.
331. Yamamoto, M. Molecular and cellular mechanisms for periodontal diseases: role of Thl and Th3 type cytokines in induction of mucosal inflammation / M.Yamamoto, K. Fujihashi, T. Hiroi // J. Periodontol Res. 1997.-Vol. 32. -№1. — P. 115-119.
332. Zachrisson, B.U. A histological study of experimental gingivitis in man /B.U. Zachrisson // J. Periodont Res. 1968. — №3. — P. 239-302.
Клинико- гистологическое исследование подростков с заболеванием пародонта Текст научной статьи по специальности «Клиническая медицина»
В области передних зубов слизистая оболочка десны воспалена. Индекс РМА до — 65% и после — 38%. Возможно развитие гипертрофического гингивита и образование патологических зубодесневых карманов. Механическое натяжение десневого сосочка напряженной уздечкой может привести к атрофическим процессам в десне и обнажению шейки зуба, кривая Шпее до -2,4 мм и после — 2,1 мм выравнивая, на что указывает 2,1 мм
нормализация. атар ортодонтияльщ емдi бiрге жYргiзудiц непзЫде бiршама нэтиже алуга болады.
атар ортодонтияльщ емдi бiрге жYргiзудiц непзЫде бiршама нэтиже алуга болады.
A.S. RUZDENOVA, G.T. DOSBERDIJEVA
PARIODONTAL CHANGES IN PATHIENTS’ TEETH WITH DEEP BITE
Resume: The most common diseases in clinic are found to be parodontal changes in a period of deep bite. On basis of leading both therapeutical and orthodontical treatment during parodontal changes, it is possible to carry out some results.
The prevalence of this anomaly varies from 6 to 67%. Deep bite causes functional impairment is to reduce the efficiency of mastication, periodontal overload front teeth and often injure oral mucosa, which also contributes to the occurrence and progression of periodontal disease. Therefore, the diagnosis and treatment of deep bite to date remains one of the most difficult and urgent problems of orthodontics. Functional overload in this area leads to changes in the alveolar bone of varying severity, depending on the load and resistance force tissues. Thus in this area radiographically determined decrease alveolar bone height and bone loss.
Found that these changes occur primarily in patients with poor periodontal. Reduced tolerance of periodontal tissue is common, it occurs in diseases of the cardiovascular, endocrine and central nervous system, gastrointestinal tract, collagenosis, beriberi, etc. Given this, it should take a critical presentation of the literature data on the incidence of periodontal tissue damage under the influence of regional functional overload traumatic teeth.
Factors (causes) overload tolerance with reduced periodontal tissue act as his starting device, helping to identify clinical primarily closed pathological process or complicating its course.
In our clinical studies of 23 adult patients with dentoalveolar anomalies periodontal lesions were found in 7 (30.4%). The vast majority of these, 16 (69.6%) periodontium was weakened under the influence of other factors. In all other cases in the pathogenesis of periodontal lesions in the main role played by reduced tolerance of periodontal tissues.
Keywords: periodontal tooth, deep bite, functional disorders, overload periodontal mucosal injury.
УДК 616.314.17-008.1-071.3-018-053.6
Ж.И. РЫСБАЕВА, Р.И. ЮЙ, Г.А. КАРКИМБАЕВА
Казахский Национальный медицинский университет имени СД.Асфендиярова Модуль пропедевтики стоматологии детского возраста и ортодонтии. Кафедра гистологии
КЛИНИКО- ГИСТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ ПОДРОСТКОВ С ЗАБОЛЕВАНИЕМ ПАРОДОНТА
В результате профилактического осмотра 130 детей в возрасте 12-16 лет выявлялась высокая заболеваемость пародонта. Гистологическое исследование десневой жидкости у детей с патологией пародонта выявлялась высокое содержание количества сегментоядерных нейтрофилов и мононуклеаров, что указывает на развитие в пародонте воспалительно-деструктивных реакций. Рентгенологически определялась резорбция межзубных перегородок, остеопороз костной ткани начальные стадии. Ключевые слова: пародонтит, гистология, гингивит, резорбция
Актуальность. Изучение цитограммы десневой жидкости является достаточным точным и надежным способом диагностики и мониторинга пародонтитов. Однако особенности цитограммы десневой жидкости у детей различного возраста не изучались и имеют свои особенности. Цель исследования:
Однако особенности цитограммы десневой жидкости у детей различного возраста не изучались и имеют свои особенности. Цель исследования:
1) провести осмотр подростков в возрасте 12-16 лет
2) выявить особенности клинических признаков заболевания пародонта
137
3) провести цитограмму эпителия десневой жидкости у больных с хроническим катаральным гингивитом .
Материалы и методы исследования. Проведен профилактический осмотр 130 детей школы № 24 г. Алматы в возрасте 12- 16 лет. Гистологически для идентификации эпителиоцитов объектом исследования послужили мазки десневой жидкости от 25 подростков с практически здоровым пародонтом и 25 больных с хроническим катаральным гингивитом в возрасте 12 лет. Для изучения костной ткани проведена ортопантомограмма.
Методы. Десневую жидкость получали с помощью стерильных нитей (размером 10 х 1 мм), приготовленных из марли (Р.И.Юй., Е.Н.Смагулова, 2001). Десну и зубы осторожно протирали ватными тампонами для удаления зубного налета и слюны из устья десневой бороздки. Затем тщательно изолировали
Затем тщательно изолировали
десневую бороздку от слюны ватными тампонами. Стерильные нити с помощью зонда с тупым концом помещали на дно десневой бороздки или десневого кармана в области 8 следующих зубов: 16,13,21,24,36,33,41,44 на 5-8 минут. (рисунок 1)
Рисунок 1 — Методика забора десневой жидкости
Затем марлевые нити извлекали из десневой бороздки или кармана и вращательными движениями по адгезивному предметному стеклу готовили мазки-отпечатки, высушивали,
фиксировали в спирт-ацетоне (1:1) в течение 5 минут и окрашивали по методике Романовского-Гимза . (рисунок 2).
Рисунок 2 — Методика забора десневой жидкости
Результаты. Клинически патология пародонта выявлена у 52,3% (68 детей) из 130 детей. Из них:
1. Хронический катаральный гингивит у 65 детей (95,6 %)
2. Локализованная форма пародонтита 3 (4,4%) (рисунок 3).
При распределении заболевании пародонта по половому признаку следует отметить, что среди мальчиков (49) отмечалось увеличение данной патологии, чем у девочек (19) (рисунок 4).
100 80 60 40 20 0
локализ
ованная
форма
пародон
тита
1 2
Рисунок 3 — Диаграмма распространенности заболевании пародонта
I девочки
Рисунок 4 — Диаграмма распространенности заболевании пародонта по половому признаку
Хронический катаральный гингивит характеризовался гиперемией, отечностью межзубных сосочков в области всех
зубов. Зондирование вызывало кровоточивость. индекс РМА в среднем 62,1 ±0,9, ГИ 2,1±0,8 (рисунок 5, 6).
m
Рисунок 5 — Хронический катаральный гингивит
Рисунок 6 — Хронический катаральный гингивит
Рисунок 7 — Ортопантомограмма
Рентгенологически на ортопантомограмме определялась резорбция костной ткани вершин перегородок или проявлением симптомом легкого остеопороза (рисунок 7). На мазках определялись эпителиоциты различных стадий дифференцировки, в том числе дистрофически измененные,
«фагирующие» и контаминированные микроорганизмами. Кроме того, выявлялись мононуклеары с цитоплазмой, голоядерные мононуклеары и сегментоядерные нейтрофилы. (рисунок 8)
(рисунок 8)
Рисунок 8 — Мазок десневой жидкости. Окраска по Романовскому-Гимза. Х 630.
Увеличение содержания нейтрофилов. Инвазия нейтрофилов в эпителиоцит. Гидропическая дистрофия. Контаминация
микроорганизмами эпителиоцитов 5 ст. дифференцировки. Изменения характеризует заболевания с явлением пародонтита.
Рисунок 9 — Мазок десневой жидкости
Окраска по Романовскому-Гимза. Х 400. Сегментоядерные нейтрофилы и мононуклеары. Контаминация
микроорганизмами эпителиоцита 4 стадии дифференцировки. Изменения характеризует заболевания с явлением пародонтита.
Рисунок 10 — Мазок десневой жидкости. Окраска по Романовскому-Гимза. Х 400 Среди эпителиоцитов преобладают клетки 3 стадии дифференцировки. Изменения характеризует заболевания с явлением пародонтита.
Рисунок 11 — Мазок десневой жидкости
Окраска по Романовскому-Гимза. Х 400. Группа эпителиоцитов 2 стадии дифференцировки. Сегментоядерные нейтрофилы. Изменения характеризует заболевания с явлением пародонтита. Выводы исследования.
Выводы исследования.
1.При профилактическом осмотре детей в возрасте 12- 16 лет выявилось Хронический катаральный гингивит у 65 детей (95,6 %), Локализованная форма пародонтита 3 (4,4%)
2. При диагностике хронического катарального гингивита, несмотря на клинические признаки гистологически определялись более глубокие поражения пародонта, которые характерны для пародонтита.
3. В изученных мазках десневой жидкости у детей с ХКГ по сравнению с контролем значительно увеличивалось количество сегментоядерных нейтрофилов и мононуклеаров, что указывает на развитие в пародонте воспалительно-деструктивных реакций.
4. Отмечалось увеличение числа базальных и парабазальных молодых эпителиоцитов, что характерно для воспаления и
отражает общее омоложение эпителиальных клеток, связанное с их усиленной пролиферацией.
5. В мазках десневой жидкости по сравнению с контролем появлялись эпителиоциты с инвазией лейкоцитами. Их цитоплазма включала один или несколько ядер сегментоядерных нейтрофилов или мононуклеаров. Появление таких клеток свидетельствует о высокой активности воспалительного процесса и агрессивности клеток инфильтрата /SchweigerH.G., 1987/.
Появление таких клеток свидетельствует о высокой активности воспалительного процесса и агрессивности клеток инфильтрата /SchweigerH.G., 1987/.
6. На поверхности эпителиоцитов выявляются разнообразные бактерии, имеющие вид палочек, кокков, нитчатых и извитых организмов мелких размеров.
Таким образом, у детей 12- 16 лет выявлялась высокая заболеваемость пародонта, при котором гистологически выявлялась высокое содержание количества сегментоядерных нейтрофилов и мононуклеаров, что указывает на развитие в пародонте воспалительно-деструктивных реакций. Рентгенологически определялась резорбция межзубных перегородок, остеопороз костной ткани начальные стадии.
СПИСОК ЛИТЕРАТУРЫ
1 Хоменко Л.А. Терапевтическая стоматология детского возраста. — Киев: Книга-плюс, 2007. — 815 с.
2 В.В. Меньшикова Лабораторные методы исследования в клинике // Справочник. — М.: Медицина, 1987. — 336 с.
3 С.В. Дьяченко Организация антибактериальной терапии распространенных заболеваний. алады. ТYйшдi свздер: пародонтит, гистология, гингивит, резорбция
алады. ТYйшдi свздер: пародонтит, гистология, гингивит, резорбция
J.I. RYSBAEVA, R.I. YU, G.A. KARKIMBAEVA
CLINICAL AND HISTOLOGICAL RESEARCHING OF ADOLESCENTS WITH PERIODONTAL DISEASE
Resume: As a result, routine inspection of 130 children between 12-16 years detected a high incidence of periodontal disease in where histologically detected high levels of the amount of segmented neutrophils and mononuclear cells , indicating that the development of inflammatory and destructive periodontal reactions. Radiologically determined resorption interdental septa , osteoporosis bone in initial stages . Keywords: periodontal disease , histology , gingivitis , resorption
Раздел 14 заболевания пародонта
#1.ПАРОДОНТ-ЭТО
-1)зуб, десна, периодонт
+2)десна, периодонт, кость альвеолы
-3)зуб, десна, периодонт, кость альвеолы, цемент корня
#2.АЛЬВЕОЛЯРНАЯ ДЕСНА -ЭТО
-1)десневой сосочек и десна вокруг зуба
-2)десна, окружающая зуб
+3)десна, покрывающая альвеолярный отросток
#3. МАРГИНАЛЬНАЯ ДЕСНА -ЭТО
МАРГИНАЛЬНАЯ ДЕСНА -ЭТО
-1) десневой сосочек и десна вокруг зуба
+2)десна, окружающая зуб
-3)десна, покрывающая альвеолярный отросток
#4.В НОРМЕ НЕ ОРОГОВЕВАЕТ ЭПИТЕЛИЙ
+1)десневой борозды
-2)папиллярной десны
-3)альвеолярной десны
#5.ПРИ ИНТАКТНОМ ПАРОДОНТЕ ДЕСНЕВАЯ БОРОЗДА ОПРЕДЕЛЯЕТСЯ
-1)клинически
+2)гистологически
-3)рентгенологически
#6.ПРИ ИНТАКТНОМ ПАРОДОНТЕ ДЕСНЕВАЯ БОРОЗДА СОДЕРЖИТ
-1)микробные ассоциации
-2)экссудат
+3)десневую жидкость
-4)грануляционную ткань
#7.АЛЬВЕОЛЯРНАЯ ДЕСНА СОСТОИТ ИЗ
-1)эпителия и надкостницы
+2)эпителия и собственно слизистого слоя
-3)эпителия, собственно слизистого и подслизистого слоя
#8.ГИНГИВИТ -ЭТО ЗАБОЛЕВАНИЕ
+1)воспалительное
-2)воспалительно-дистрофическое
-3)дистрофическое
-4)опухолевидное
#9.ПАРОДОНТИТ -ЗАБОЛЕВАНИЕ
-1)воспалительное
+2)воспалительно-дистрофическое
-3)дистрофическое
-4)опухолевидное
#10. ПАРОДОНТОЗ -ЗАБОЛЕВАНИЕ
ПАРОДОНТОЗ -ЗАБОЛЕВАНИЕ
-1)воспалительное
-2)воспалительно-дистрофическое
+3)дистрофическое
-4)опухолевидное
#11.ПАРОДОНТОЗ РАЗЛИЧАЮТ
-1)локализованный
+2)генерализованный
-3)развившийся
#12.ПАРОДОНТОЗ ПО КЛИНИЧЕСКОМУ ТЕЧЕНИЮ РАЗЛИЧАЮТ
-1)острый
+2)хронический
-3)хронический в стадии обострения
-4)в стадии воспаления
#13.РАСТВОР ЭРИТРОЗИНА ПРИМЕНЯЮТ ДЛЯ
+1)определения индекса гигиены
-2)определения индекса ПМА
-3)определения воспаления десны
-4)определения индексаCPITN
#14.РАСТВОР ФУКСИНА ПРИМЕНЯЮТ ДЛЯ
+1)определения индекса гигиены
-2)определения индекса ПМА
-3)определения воспаления
-4)определения индексаCPITN
#15.ИНДЕКС ПИ РУССЕЛЯ ОПРЕДЕЛЯЕТ ТЯЖЕСТЬ
-1)гингивита
+2)пародонтита
-3)пародонтоза
#16.ПРОБА КУЛАЖЕНКО ОПРЕДЕЛЯЕТ СОСТОЯНИЕ
-1)неспецифической резистентности
+2)стойкость капилляров десны к вакууму
-3)воспаление десны
#17. ПРОБА ЯСИНОВСКОГО ОПРЕДЕЛЯЕТ СОСТОЯНИЕ
ПРОБА ЯСИНОВСКОГО ОПРЕДЕЛЯЕТ СОСТОЯНИЕ
+1)неспецифической резистентности
-2)капилляров десны
-3)воспаление десны
#18.ПРОБА ШИЛЛЕРА -ПИСАРЕВА ОПРЕДЕЛЯЕТ СОСТОЯНИЕ
-1)неспецифической резистентности
-2)капилляров десны
+3)воспаление десны
#19.ПОЛЯРОГРАФИЯ ПРИМЕНЯЕТСЯ ДЛЯ ОПРЕДЕЛЕНИЯ
-1)состояния капилляров
-2)микроциркуляции
+3)парциального давления кислорода
-4)парциального давления углекислого газа
#20.РЕОПАРОДОНТОГРАФИЯ ПРИМЕНЯЕТСЯ ДЛЯ ОПРЕДЕЛЕНИЯ
+1)микроциркуляции
-2)парциального давления кислорода
-3)парциального давления углекислого газа
#21.КАПИЛЛЯРОСКОПИЯ ПРИМЕНЯЕТСЯ ДЛЯ ОПРЕДЕЛЕНИЯ
+1)состояния капилляров
-2)микроциркуляции
-3)парциального давления кислорода
-4)парциального давления углекислого газа
#22. ОСНОВНОЙКЛИНИЧЕСКИЙ ПРИЗНАК ХРОНИЧЕСКОГО КАТАРАЛЬНОГО ГИНГИВИТА
+1)кровоточивость при зондировании десневой борозды
-2)гиперемия межзубных сосочков
-3)мягкий зубной налет
-4)наддесневой зубной камень
#23. ПРИ КАТАРАЛЬНОМ ГИНГИВИТЕ КОЛИЧЕСТВО
ДЕСНЕВОЙ ЖИДКОСТИ
ПРИ КАТАРАЛЬНОМ ГИНГИВИТЕ КОЛИЧЕСТВО
ДЕСНЕВОЙ ЖИДКОСТИ
+1)увеличивается
-2)уменьшается
-3)не изменяется
#24.ПРИ ПАРОДОНТИТЕ КОЛИЧЕСТВО ДЕСНЕВОЙ ЖИДКОСТИ
+1)увеличивается
-2)уменьшается
-3)не изменяется
#25.ПРИ ПАРОДОНТОЗЕ КОЛИЧЕСТВО ДЕСНЕВОЙ ЖИДКОСТИ
-1)увеличивается
-2)уменьшается
+3)не изменяется
#26.ИЗМЕНЕНИЯ НА РЕНТГЕНОГРАММЕ ПРИ КАТАРАЛЬНОМ ГИНГИВИТЕ
-1)характерны
+2)не характерны
#27.ИЗМЕНЕНИЯ НА РЕНТГЕНОГРАММЕ ПРИ ГИПЕРТРОФИЧЕСКОМ ГИНГИВИТЕ
-1)характерны
+2)не характерны
#28.ИЗМЕНЕНИЯ НА РЕНТГЕНОГРАММЕ ПРИ ЯЗВЕННО-НЕКРОТИЧЕСКОМ ГИНГИВИТЕ
-1)характерны
+2)не характерны’
#29. ПРИ ФИБРОЗНОЙ ФОРМЕ ГИПЕРТРОФИЧЕСКОГО ГИНГИВИТА ПРОВОДЯТ
-1) гингивотомию
+2) гингивэктомию
-3) кюретаж
#2.ХАРАКТЕРНЫЕ КЛИНИЧЕСКИЕ СИМПТОМЫ ПАРОДОНТИТА
-1)наличие зубного камня и кровоточивость десен
-2)кровоточивость десен и ощущение зуда в десне
-3)кровоточивость и разростание десны
+ 4)наличие пародонтальных карманов и деструкция альвеолы
#31. ЯЗВЕННО-НЕКРОТИЧЕСКИЙ ГИНГИВИТ
ВСТРЕЧАЕТСЯ ПРИ
ЯЗВЕННО-НЕКРОТИЧЕСКИЙ ГИНГИВИТ
ВСТРЕЧАЕТСЯ ПРИ
-1) гастрите
-2) стенокардии
-3) сифилисе
+4) лейкозе
#32. УСКОРЕННАЯ СОЭ ВСТРЕЧАЕТСЯ ПРИ
-1) хроническом катаральном гингивите
-2) локальном гингивите
+3) язвенно-некротическом гингивите
-4) пародонтозе
#33. КЛИНИЧЕСКОЕ ПРОЯВЛЕНИЕ ЯЗВЕННО-НЕКРОТИЧЕСОГО ГИНГИВИТА
-1) зубной налет
+2) некроз межзбных сосочков и десны
-3) гипертрофия десны
-4) цианоз десневого рая
#34. ГИНГИВЭКТОМИЮ ПРИМЕНЯЮТ ПРИ ГИНГИВИТЕ
-1) катаральном
-2) язвенном
+3) гипертрофическом
#35.КАТАРАЛЬНЫЙ ГИНГИВИТ ДИФФЕРЕНЦИРУЮТ С
+1)пародонтитом
-2)фиброматозом
-3)пародонтозом
-4)герпетическим гингивостоматитом
#36.гипертрофический ГИНГИВИТ ОТЕЧНОЙ ФОРМЫдифференцируют С
-1)пародонтитом
+2)фиброматозом
-3)пародонтозом
-4)герпетическим гингивостоматитом
#37. ОСТРЫЙ ЯЗВЕННО-НЕКРОТИЧЕСКИЙ ГИНГИВИТ
ВЕНСАНАдифференцируют
С
ОСТРЫЙ ЯЗВЕННО-НЕКРОТИЧЕСКИЙ ГИНГИВИТ
ВЕНСАНАдифференцируют
С
-1)пародонтитом
-2)фиброматозом
-3)пародонтозом
+4)герпетическим гингивостоматитом
#38.ЛОЖНЫЙ КАРМАН РАСПОЛОЖЕН В ПРЕДЕЛАХ
+1)десны
-2)десны и периодонта
-3)десны, периодонта и кости альвеолы
#39.НАЛИЧИЕ ПАРОДОНТАЛЬНОГО КАРМАНА ХАРАКТЕРНО ДЛЯ
+1)пародонтита
-2)пародонтоза
-3)гипертрофического гингивита
#40.НАЛИЧИЕ РЕЦЕССИИ ДЕСНЫ ХАРАКТЕРНО ДЛЯ
-1)пародонтита
+2)пародонтоза
-3)гипертрофического гингивита
#41.НАЛИЧИЕ ЛОЖНОГО ДЕСНЕВОГО КАРМАНА ХАРАКТЕРНО ДЛЯ
-1)пародонтита
-2)пародонтоза
+3)гипертрофического гингивита
#42.ПАРОДОНТАЛЬНЫЙ КАРМАН ОПРЕДЕЛЯЕТСЯ
+1)клинически
-2)гистологически
-3)рентгенологически
#43.КАРМАН ПРИ ПАРОДОНТИТЕ ЛЕГКОЙ СТЕПЕНИ ТЯЖЕСТИ ДО
+1) 3,5мм
-2) 5мм
-3)более 5мм
#44.КАРМАН ПРИ ПАРОДОНТИТЕ СРЕДНЕЙ СТЕПЕНИ ТЯЖЕСТИ ДО
-1) 3,5мм
+2) 5мм
-3)более 5мм
#45. КАРМАН ПРИ ПАРОДОНТИТЕ ТЯЖЕЛОЙ СТЕПЕНИ
ДО
КАРМАН ПРИ ПАРОДОНТИТЕ ТЯЖЕЛОЙ СТЕПЕНИ
ДО
-1) 3,5 мм
-2) 5мм
+3)более 5мм
#46. ДЛЯ ХРОНИЧЕСКОГО ПАРОДОНТИТА ЛЕГКОЙ СТЕПЕНИ ХАРАКТЕРНО
-1) обнажение шеек и корней зубов
-2) гиперемия десны
-3) цианоз десны
+4) наличие кармана глубиной до 3,5 мм
#47. К ЛОКАЛЬНОМУ ПАРОДОНТИТУ ПРИВОДИТ
-1) плохая гигиена
+2) нависающий трамвирующий край пломбы
-3) прием противосудорожных препаратов
#48. ОТСУТСТВИЕ КОНТРАКТОГО ПУНКТА ПРИВОДИТ К ПАРОДОНТУ
+1) локализованному
-2) генерализованному
#49. НА РЕНТГЕНОГРАММЕ ПРИ КАТАРАЛЬНОМ ГИНГИВИТЕ РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
+1) отсутствует
-2) на 1\3
-3) на 1\2
-4) на 2\3
#50. НА РЕНТГЕНОГРАММЕ ПРИ ГИПЕРТРОФИЧЕСКОМ ГИНГИВИТЕ РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
+1) отсутствует
-2) на1\3
-3) на 1\2
-4) на 2\3
#51. НА
РЕНТГЕНОГРАММЕ ПРИ ОСТРОМ
ЯЗВЕННО-НЕКРОТИЧЕСКОМ ГИНГИВИТЕ
РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
НА
РЕНТГЕНОГРАММЕ ПРИ ОСТРОМ
ЯЗВЕННО-НЕКРОТИЧЕСКОМ ГИНГИВИТЕ
РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
+1) отсутствует
-2) на 1\3
-3) на 1\2
-4) на 2\3
#52. НА РЕНТГЕНОГРАММЕ ПРИ ПАРОДОНТИТЕ ЛЕГКОЙ СТЕПЕНИ РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДЕИ
-1) отсутствует
+2) на 1\3
-3) на 1\2
-4) на 2\3
#53. НА РЕНТГЕНОГРАММЕ ПРИ ПАРОДОНТИТЕ СРЕДНЕЙ СТЕПЕНИ РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
-1) отсутствует
-2) на 1\3
+3) на 1\2
-4) на 2\3
#54. НА РЕНТГЕНОГРАММЕ ПРИ ПЕРОДОНТИТЕ ТЯЖЕЛОЙ СТЕПЕНИ РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНОЙ ПЕРЕГОРОДКИ
-1) отсутствует
-2) на 1\3
-3) на 1\2
+4) на 2\3
#55. РЕЗОРБЦИЯ МЕЖАЛЬВЕОЛЯРНЫХ ПЕРЕГОРОДОК ХАРАКТЕРНА ДЛЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА
-1)гингивита
-2)пародонтоза
+3)пародонтита
#56.ПРИ ПАРОДОНТИТЕ ЛЕГКОЙ СТЕПЕНИ ПОДВИЖНОСТЬ ЗУБОВ
+1) 0- Iстепени
-2) I- IIстепени
-3) II- IIIстепени
#57. ПРИ ПАРОДОНТИТЕ СРЕДНЕЙ СТЕПЕНИ
ПОДВИЖНОСТЬ ЗУБОВ
ПРИ ПАРОДОНТИТЕ СРЕДНЕЙ СТЕПЕНИ
ПОДВИЖНОСТЬ ЗУБОВ
-1) 0-Iстепени
+2) I- IIстепени
-3) II-IIIстепени
#58.ПРИ ПАРОДОНТИТЕ ТЯЖЕЛОЙ СТЕПЕНИ ПОДВИЖНОСТЬ ЗУБОВ
-1) 0- Iстепени
-2) I- IIстепени
+3) II- IIIстепени
#59.КРИТЕРИЕМ ВЫБОРА МЕТОДА ХИРУРГИЧЕСКОГО
ВМЕШАТЕЛЬСТВА ПРИ ЛЕЧЕНИИ ЩРОДОНТИТА ЯВЛЯЕТСЯ
-1)жалобы больного
+2)глубина карманов
-3)длительность заболевания
-4)общее состояние больного
#60.ПРИ ГЛУБИНЕ КАРМАНА ДО 3 — 5ММ ЦЕЛЕСООБРАЗНО ПРОВЕСТИ
+1)кюретаж
-2)открытый кюретаж
-3)лоскутную операцию
#61.ПРИ ГЛУБИНЕ КАРМАНА 4-5ММ ЦЕЛЕСООБРАЗНО ПРОВЕСТИ
-1)кюретаж
+2)открытый кюретаж
-3)лоскутную операцию
#62.ПРИ ГЛУБИНЕ КАРМАНА БОЛЕЕ 5ММ ЦЕЛЕСООБРАЗНО ПРОВЕСТИ
-1)кюретаж
-2)открытый кюретаж
+3)лоскутную операцию
#63.УДАЛЕНИЕ НАДДЕСНЕВОГО ЗУБНОГО КАМНЯ ПРОВОДЯТ
+1)до кюретажа парод онтальных карманов
-2)в процессе кюретажа
-3)после кюретажа
#64. УДАЛЕНИЕ ПОДДЕСНЕВОГО ЗУБНОГО КАМНЯ
ПРОВОДЯТ
УДАЛЕНИЕ ПОДДЕСНЕВОГО ЗУБНОГО КАМНЯ
ПРОВОДЯТ
-1)до кюретажа парод онтальных карманов
+2)в процессе кюретажа
-3)после кюретажа
#65.К ПРОТИВОВОСПАЛИТЕЛЬНЫМ СРЕДСТВАМ ОТНОСЯТСЯ
-1)гепариновая мазь
+2)аспириновая мазь
-3)зовиракс
-4)мазь солкосерила
#66.К ЭПИТЕЛИЗИРУЮЩИМ СРЕДСТВАМ ОТНОСЯТСЯ
-1)гепариновая мазь
-2)аспириновая мазь
-3)бутадиеновая мазь
+4)облепиховое масло
#67.ПРОТЕОЛИТИЧЕСКИЕ ФЕРМЕНТЫ ИСПОЛЬЗУЮТСЯ ПРИ
-1)кровоточивости десны
-2) отеки
+3)некрозе десны
-4)ретракции десны
#68.МЕТРОНИДАЗОЛ ИСПОЛЬЗУЮТ ПРИ ЛЕЧЕНИИ
-1)катарального гингивита
+2)язвенно-некротического гингивита
-3)пародонтоза
-4)гипертрофического гингивита
#69.ПРИ ПОДВИЖНОСТИ ЗУБОВ IIIСТЕПЕНИ ДЕПУЛЬПИРОВАНИЕ
+1)показано
-2)не показано
#70. КЮРЕТАЖ ЭТО-
-1)удаление наддесневого зубного камня
-2)удаление грануляции
-3)удаление поддесневого зубного камня
+4)выскабливание пародонтального кармана
#71. КЮРЕТАЖ КАРМАНОВ ОБЕСПЕЧИВАЕТ УДАЛЕНИЕ
КЮРЕТАЖ КАРМАНОВ ОБЕСПЕЧИВАЕТ УДАЛЕНИЕ
-1) наддесневого и поддесневого зубного камня
-2) наддесневого зубного камня и грануляций
-3) поддесневого зубного камня и грануляций
+4) поддесневого зубного камня , грануляций и десневого эпителия
#72.КРИТЕРИЯМИ КАЧЕСТВЕННО ПРОВЕДЕННОГО КЮРЕТАЖА ЧЕРЕЗ30ДНЕЙ ЯВЛЯЮТСЯ
-1)исчезновение гиперестезии зубов
+2)десна плотно прилегает к зубу
+3)исчезновение гиперестезии при чистке зубов
#73.ПРИ ХРОНИЧЕСКОМ ПАРОДОНТИТЕ В СТАДИИ РЕМИССИИ НАЗНАЧАЮТ
-1)антимикробные препараты
+2)поливитамины
-3)противовоспалительные препараты
#74.ВОСПАЛЕНИЕ ДЕСЕН -ХАРАКТЕРНЫЙ ПРИЗНАК
-1)пародонтоза
+2)пародонтита
#75.ХАРАКТЕРНЫЕ ЖАЛОБЫ БОЛЬНОГО ПРИ ПАРОДОНТОЗЕ
-1)кровоточивость десен
-2)запах изо рта
-3)обильные отложения наддесневого зубного камня
+4)обнажение шеек и корней зубов
#76.ПАРОДОНТОЗ ДИФФЕРЕНЦИРУЮТ С ПАРОДОНТИТОМ В СТАДИИ РЕМИССИИ ПО ДАННЫМ
+1)анамнеза
-2)рентгенологического обследования
-3)клинического определения состояния пародонта
-4)анализа крови на содержание глюкозы
-5)клинического анализа крови
#77. ОКРАСКА ДЕСНЫ ПРИ ПАРОДОНТОЗЕ
ОКРАСКА ДЕСНЫ ПРИ ПАРОДОНТОЗЕ
-1)цианотичная
+2)бледная
-3)гиперемированная
#78.ПАРОДОНТАЛЬНЫЕ КАРМАНЫ ПРИ ПАРОДОНТОЗЕ
-1)до 3мм
-2)от 3до 5мм
-3)более 5мм
+4)отсутствуют
#79.ДЛЯ ПАРОДОНТОЗА ОБИЛИЕ МЯГКОГО ЗУБНОГО НАЛЕТА
-1)характерно
+2)не характерно
#80.ДЛЯ ПАРОДОНТОЗА РАННЯЯ ПОДВИЖНОСТЬ ЗУБОВ
-1)характерна
+2)не характерна
#81.ПРИ ЛЕЧЕНИИ ПАРОДОНТОЗА ИСПОЛЬЗУЮТ
-1)кюретаж пародонтальных карманов
-2)противовоспалительную терапию
+3)электрофорез витамина С
-4)гингивотомию
#82.ДЛЯ ЛЕЧЕНИЯ ГИПЕРЕСТЕЗИИ ТВЕРДЫХ ТКАНЕЙ ЗУБОВ ПРИ ПАРОДОНТОЗЕ РЕКОМЕНДУЮТ ЗУБНЫЕ ПАСТЫ
-1)противовоспалительные
+2)фторсодержащие
-3)солевые
-4)гигиенические
Ультраструктура десны, десневой борозды, десневой жидкости
Похожие презентации:
Здоровье, предболезнь, болезнь и профилактика
Врожденные пороки сердца у детей
Цирроз печени
Приобретенные пороки сердца
Пиелонефрит
Анафилактический шок
Лучевая диагностика заболеваний желудочно-кишечного тракта
Ревматоидный артрит
Инфекции Передаваемые Половым Путем
Бюгельные протезы
1.
 Казахстанско – Российский Медицинский УниверситетКАФЕДРА ТЕРАПЕВТИЧЕСКОЙ СТОМАТОЛОГИИ
Казахстанско – Российский Медицинский УниверситетКАФЕДРА ТЕРАПЕВТИЧЕСКОЙ СТОМАТОЛОГИИСРС
Тема: Ультраструктура десны, десневой борозды,
десневой жидкости.
Выполнил: Сулейманов Омар
Стом. Факультет 505 “А”гр.
Алматы 2016
2. План
ДеснаДесневая жидкость
Десневая борозда
3. Десна
Десна — единственнаяструктура пародонта, которая
видна глазу в норме. Это
слизистая оболочка,
покрывающая альвеолярные
отростки верхней и нижней
челюстей. С оральной
поверхности десна переходит в
слизистую оболочку твёрдого
нёба на верхней челюсти и дна
полости рта — на нижней.
Различают свободную (краевую) десну,
прилежащую к шейке зуба, и
прикреплённую (альвеолярную) десну,
покрывающую альвеолярный отросток.
Краевая десна — наружная стенка
десневой бороздки, она окружает
шейки зубов (рис. 14-1). Ширина зоны
краевой десны зависит от глубины
десневой бороздки. Она неодинакова в
области разных групп зубов, но в
среднем колеблется от 0,5 мм во
фронтальном участке до 1,5 мм в
области моляров.
 В состав краевой
В состав краевойзоны входит и межзубный сосочек.
Межзубный десневой сосочек
образован соединением вестибулярной
и оральной частей десны посредством
соединительнотканных волокон, и на
поперечном срезе все сосочки имеют
вид седла. Форма сосочков в области
разных групп зубов различна:
треугольная — во фронтальных и
трапециевидная — в боковых участках.
Рис. Краевая десна: 1 —
межзубный сосочек, 2 —
свободная десна, 3 —
прикреплённая десна, 4 —
подвижная десна.
Десна состоит из трёх слоёв: из многослойного плоского
эпителия, собственно слизистой оболочки и
подслизистого слоя. Зона прикреплённой десны, или
альвеолярная десна, лишена подслизистого слоя и
срастается с надкостницей. Эпителий десны
многослойный плоский, в отличие от кожи не имеет
блестящего слоя клеток. В нормальных условиях в
эпителии десны наблюдаются ороговение и паракератоз,
которые обеспечивают защиту от механических,
химических и физических воздействий.
 Этот эпителий
Этот эпителийназывают ротовым (оральным). Кроме того, различают
сулькулярный (бороздковый) и соединительный
(эпителиальное прикрепление) эпителий.
Сулькулярный эпителий выстилает десневую бороздку
(сулькус) — щель между поверхностью зуба и
прилежащей к ней десной.
7. ДЕСНЕВАЯ ЖИДКОСТЬ
Десневая жидкостьявляется
физиологической средой
организма сложного
состава, включающей в
себя лейкоциты,
спущенные эпителиальные
клетки,
микро¬организмы,
электролиты, белковые
компоненты и ферменты.
8. Лейкоциты
Наличие лейкоцитов в десневой борозде имеет большое значение в физиоло¬гииполости рта, так как десневая борозда является основным источником поступ¬ления
лейкоцитов в слюну.
Эмиграция лейкоцитов в полость рта имеет возрастной характер, так, у де¬тей до
прорезывания зубов лейкоциты в слюне практически отсутствуют. Они по¬являются
с началом прорезывания зубов и с прорезыванием всех зубов эмиграция достигает
уровня эмиграции лейкоцитов взрослых.
 В более позднем возрасте с умень¬шением
В более позднем возрасте с умень¬шениемчисла зубов количество лейкоцитов в слюне уменьшается. У стариков с беззубой
челюстью эмиграция лейкоцитов значительно снижена.
При интактном пародонте у взрослых в десневой жидкости содержится 95-97%
нейтрофилов, 1-2% лимфоцитов. 2-3% моноцитов. Среди мононуклеарных
лей¬коцитов 24% приходиться на Т-лимфоциты и 58% — на В-лим4юциты. При
воспале¬нии процентное соотношение нейтрофилов. лимфоцитов и моноцитов
остается без изменений, но увеличивается абсолютное число этих клеток.
9. Эпителиальные клетки
Десневая жидкость здоровых людей содержитспущенные эпителиальные клетки. При воспалении число
спущенных эпителиальных клеток увеличивается, что
связано с изменениями метаболизма межклеточного
вещества и с увеличением митотической активности
эпителия десны при воспалении. Спущенные
эпители¬альные клетки могут адсорбироваться на
поверхности зуба и способствовать на¬чальной
колонизации бактерий при образовании зубного налета.

10. Микроорганизмы десневой жидкости
Десневая жидкость в норме нестерильна. Постоянными
представителями микрофлоры
содержимого десневых борозд
являются стрептококки и
стафилококки, фузобактерии,
спирохеты и простейшие. Однако
при патологии пародонта
увеличивается их количество,
изменяется их видовой состав и
повышается их патогенность.
При наличии воспаления в
пародонте микроорганизмы,
выделяемые из десневой жидкости
и зубного поддесневого налета
схожи. Наличие кальция и фосфатов
имеет значение для образования
зубной бляшки.
Стрептококк
Стафилококки
Фузобактерии
(окраска по Грамму)
11. Белковые компоненты десневой жидкости
Белковый состав десневой жидкости и сыворотки кровиодинаков. Содержа¬ние общего белка в десневой жидкости в
среднем составляет 6.1 — 6.8 г/100 мл.
В десневой жидкости содержатся альбумины, глобулины, система
комплемента. Существует мнение о том, что глобуллины и
фибрин могут спо¬собствовать плотному соединению эпителия
десны с эмалью, образуя клейкую плен¬ку и обеспечивая адгезию
клеток зубо-эпителиального прикрепления к поверхнос¬ти чуба.

Десневая жидкость является важным источником ряда
иммуноглобулинов, антител для полости рта. Их концентрация в
десневой жидкости и крови одинакова.
12. Количество десневой жидкости
В течение суток в полость рта поступает от 0.5 до 2,4 мл десневойжидкости. По сравнению с ннтактным пародонтом, при хроническом
катаральном гингивите количество десневой жидкости выше в 4.6 раза,
пародонтите — 10.5 раза. Пародонтоз также характеризует¬ся более
высокими количественными показателями десневой жидкости, которые
превышают уровень ее выделения по сравнению с интактным
пародонтом в 1.8 раза.
Предложено несколько способов получения десневой жидкости.
Наиболее широкое распространение в клинике получил
внутробороздковой метод забора десневой жидкости с помощью
полосок фильтровальной бумаги. Количество десневой жидкости
определяют путем взвешивания бумажных полосок или путем измерения
плошади пропитывания.
13. Десневая бороздка
Десневая бороздка — важноеобразование пародонта.
 Она
Онаформируется только после
прорезывания зуба. Это
необязательная анатомическая
структура, а результат хронического
микробного воздействия на краевой
пародонт с одной стороны и выход
из подлежащих кровеносных
сосудов защитных компонентов
плазмы и форменных элементов
крови в ответ на такие воздействия
— с другой.
English Русский Правила
Гингивит: причины, симптомы и лечение
Гингивит — часто болезненное воспаление десен или десен. Обычно это происходит из-за образования зубного налета на зубах.
Гингивит — это распространенное заболевание, которым в какой-то момент жизни страдает большинство взрослых. Это форма заболевания десен, которая обычно вызывает легкие симптомы. Однако он может перейти в более тяжелое состояние, если человек не лечит его первопричину.
Основные положения о гингивите включают:
- Бактериальные отложения вокруг зубов являются наиболее распространенной причиной гингивита.

- Основным симптомом гингивита являются красные опухшие десны, которые могут кровоточить, когда человек чистит зубы.
- Гингивит часто проходит при хорошей гигиене полости рта, такой как более длительная и частая чистка зубов и регулярная чистка зубной нитью. Кроме того, может помочь антисептическая жидкость для полоскания рта.
В этой статье подробно описаны типы, причины и симптомы гингивита. В нем также обсуждается, что человек может сделать для лечения и профилактики гингивита.
Гингивит представляет собой неразрушающее заболевание пародонта. Люди обычно называют это заболеванием десен. Гингивит — это ранняя форма заболевания десен, обычно проявляющаяся легкими симптомами.
Существует два основных типа гингивита. Гингивит, вызванный зубным налетом, возникает, когда накопление налета раздражает десны человека, что приводит к воспалению, изменению цвета и боли.
Напротив, поражения десен, не вызванные зубным налетом, могут быть результатом бактериальной, вирусной или грибковой инфекции. Аллергические реакции, заболевания и реакции на инородные тела, такие как зубные протезы, также могут вызывать этот тип гингивита.
Аллергические реакции, заболевания и реакции на инородные тела, такие как зубные протезы, также могут вызывать этот тип гингивита.
Оба типа гингивита могут прогрессировать в периодонтит, если человек не лечит его должным образом. Пародонтит является более серьезным заболеванием и может привести к дальнейшим осложнениям, таким как потеря зубов.
Наиболее распространенной причиной гингивита является скопление бактериального налета между зубами и вокруг них. Зубной налет представляет собой биопленку, которая естественным образом накапливается на зубах. Это происходит, когда бактерии прикрепляются к гладкой поверхности зуба.
Этот налет может затвердевать и превращаться в зубной камень возле десен у основания зубов. Он имеет желто-белый цвет. Удалить зубной камень могут только профессиональные стоматологи.
Накопление зубного налета и зубного камня может вызвать иммунный ответ, который приводит к разрушению десны или ткани десны. В конце концов, это может привести к дальнейшим осложнениям, включая потерю зубов.
Узнайте больше о различиях между налетом и зубным камнем здесь.
Другие причины и факторы риска
Несколько основных состояний и внешних факторов могут увеличивать образование зубного налета или повышать риск воспаления десен.
- Изменения гормонов: Это может происходить в период полового созревания, менопаузы, менструального цикла и беременности. Десны могут стать более чувствительными, что повышает риск воспаления.
- Некоторые заболевания: Рак, диабет и ВИЧ связаны с повышенным риском развития гингивита.
- Лекарства: Лекарства, уменьшающие выработку слюны, могут повлиять на здоровье полости рта человека. Дилантин, лекарство от эпилепсии и лекарства от стенокардии, также могут вызывать аномальный рост ткани десны, увеличивая риск воспаления.
- Курение: У заядлых курильщиков чаще развивается гингивит, чем у некурящих.
- Возраст: Риск развития гингивита увеличивается с возрастом.

- Семейный анамнез: Те, чьи родитель или родители страдали гингивитом, также имеют более высокий риск его развития.
Поделиться на PinterestAlgirdas Gelazius/Shutterstock
Признаки и симптомы гингивита могут включать:
- воспаление и изменение цвета десен
- нежные десны, которые могут быть болезненными на ощупь
- кровоточивость десен при чистке щеткой или зубной нитью
- неприятный запах изо рта или неприятный запах изо рта
- опущение десен
- мягкие десны
Стоматолог или специалист по гигиене полости рта проверит наличие симптомов, таких как зубной налет и зубной камень в полости рта.
Они также могут назначить анализы для выявления признаков пародонтита. Это можно сделать с помощью рентгена или зондирования пародонта с помощью инструмента, который измеряет глубину кармана вокруг зуба.
Если диагноз установлен на ранней стадии, а лечение проведено быстро и правильно, человек может лечить гингивит в домашних условиях, соблюдая надлежащую гигиену полости рта.
Узнайте больше о домашних средствах от гингивита здесь.
Однако, если симптомы не проходят или состояние влияет на качество жизни человека, он может обратиться за профессиональной помощью.
Лечение часто включает уход стоматолога и последующие процедуры, проводимые пациентом дома.
Профессиональная стоматологическая помощь
Зубной врач может первоначально провести удаление зубного камня. Это делается для того, чтобы они могли удалить лишний налет и зубной камень. Это может быть неудобно, особенно если скопление зубного камня обширно или десны чувствительны.
После чистки зубов стоматолог объяснит важность гигиены полости рта и способы эффективной чистки зубов щеткой и зубной нитью.
Они могут порекомендовать последующие визиты для наблюдения за налетом и зубным камнем. Это позволит стоматологу быстро выявлять и лечить любые рецидивы.
Исправление любых поврежденных зубов также способствует гигиене полости рта. Некоторые проблемы с зубами, такие как кривые зубы, плохо подогнанные коронки или мосты, могут затруднить правильное удаление зубного налета и зубного камня. Они также могут раздражать десны.
Они также могут раздражать десны.
Человек может предотвратить гингивит в домашних условиях, регулярно соблюдая правила гигиены полости рта. Сюда входят:
- чистка зубов минимум два раза в день
- использование электрической зубной щетки
- чистка зубов зубной нитью минимум один раз в день
- регулярное полоскание рта антисептическим средством для полоскания рта
Лечение гингивита и соблюдение рекомендаций стоматолога обычно позволяет предотвратить осложнения.
Однако заболевание десен может распространяться и поражать ткани, зубы и кости, если его не лечить.
Осложнения включают:
- абсцесс или инфекцию десны или кости челюсти
- периодонтит — более серьезное заболевание, которое может привести к потере кости и зубов
- рецидивирующий гингивит
- траншейный рот, при котором бактериальная инфекция приводит к изъязвлению десен
Гингивит является распространенным заболеванием десен. Это результат накопления бактерий на зубах. Это накопление раздражает окружающие ткани десны и может вызвать воспаление, обесцвечивание и болезненность десен.
Это результат накопления бактерий на зубах. Это накопление раздражает окружающие ткани десны и может вызвать воспаление, обесцвечивание и болезненность десен.
Большинство людей могут вылечить гингивит с помощью регулярных правил гигиены полости рта. Регулярные стоматологические осмотры могут помочь выявить признаки заболевания десен и своевременно их лечить.
Коррекция местного иммунного дисбаланса полости рта в комплексном лечении хронического катарального гингивита у детей
Год и том — Выпуск:
2017. Том 6 — Выпуск 2
Авторы:
Ипполитов Юрий Александрович, Светлана Александровна А. Гаркавец, Татьяна А. Русанова, Светлана Н. Юденкова, Виктория П. Куралесина, Елена О. Алешина, Яна А. Плотникова, Чунг Ч. Чан, Евгений С. Маншин
Рубрика:
Стоматология
Тип статьи:
Research Letter
PDF-файл:
Резюме:
Исходная информация. Заболевания пародонта у подростков считаются актуальными, поскольку частота этих состояний имеет тенденцию к увеличению. Этим условиям особенно подвержены дети, находящиеся в периоде интенсивного роста. Недавние исследования молекулярно-морфологических нарушений, возникающих у детей с хроническим катаральным гингивитом, указывают на необходимость применения иммунокорректоров в комплексном лечении больных с этими заболеваниями, что способствует улучшению как состояния тканей пародонта, так и общего состояния здоровья.
Материал и методы. Обследовано 157 детей в возрасте 12–15 лет. Физикальное обследование ребенка включало данные анамнеза и осмотр полости рта. для диагностики гингивита использовали индекс Российской медицинской ассоциации (РМА); Для оценки состояния гигиены полости рта использовали индекс Грина-Вермиллиона.
Результаты. Изменения общего состояния здоровья подростков, страдающих заболеваниями пародонта, свидетельствуют о снижении защитных механизмов организма. Поэтому заявлено, что лечение обязательно влияет как на сам воспалительный процесс, так и на повышение общего иммунитета. В этом случае наиболее целесообразной мерой считается применение иммунокорректоров, а именно «Имудон».
Этим условиям особенно подвержены дети, находящиеся в периоде интенсивного роста. Недавние исследования молекулярно-морфологических нарушений, возникающих у детей с хроническим катаральным гингивитом, указывают на необходимость применения иммунокорректоров в комплексном лечении больных с этими заболеваниями, что способствует улучшению как состояния тканей пародонта, так и общего состояния здоровья.
Материал и методы. Обследовано 157 детей в возрасте 12–15 лет. Физикальное обследование ребенка включало данные анамнеза и осмотр полости рта. для диагностики гингивита использовали индекс Российской медицинской ассоциации (РМА); Для оценки состояния гигиены полости рта использовали индекс Грина-Вермиллиона.
Результаты. Изменения общего состояния здоровья подростков, страдающих заболеваниями пародонта, свидетельствуют о снижении защитных механизмов организма. Поэтому заявлено, что лечение обязательно влияет как на сам воспалительный процесс, так и на повышение общего иммунитета. В этом случае наиболее целесообразной мерой считается применение иммунокорректоров, а именно «Имудон». Известно, что «Имудон» влияет на восстановление регулярной резидентной флоры ротовой полости человека, а также оказывает противовоспалительное действие. Применение «Имудона» приводит к уменьшению количества пародонтопатогенной слизи. Растворяясь в полости рта, эти таблетки активируют защитные механизмы организма. Благодаря вспомогательным веществам активные компоненты препарата длительное время остаются в полости рта.
Заключение. Установлено соответствие между изменениями иммунологических показаний плазмы крови у детей с хроническим катаральным гингивитом, получающих терапию «Имудоном» до и после лечения.
Известно, что «Имудон» влияет на восстановление регулярной резидентной флоры ротовой полости человека, а также оказывает противовоспалительное действие. Применение «Имудона» приводит к уменьшению количества пародонтопатогенной слизи. Растворяясь в полости рта, эти таблетки активируют защитные механизмы организма. Благодаря вспомогательным веществам активные компоненты препарата длительное время остаются в полости рта.
Заключение. Установлено соответствие между изменениями иммунологических показаний плазмы крови у детей с хроническим катаральным гингивитом, получающих терапию «Имудоном» до и после лечения.
Ключевые слова:
гингивит, подростки, лечение, иммунокорректоры. Коррекция местного иммунного дисбаланса полости рта в комплексном лечении хронического катарального гингивита у детей. Российский открытый медицинский журнал 2017; 6: e0209.
Введение
Заболевания пародонта считаются одними из самых распространенных заболеваний челюстно-лицевой области. Заболеваемость гингивитом составляет почти 100%, болеют преимущественно дети и молодые люди до 25–30 лет. Разработка и внедрение успешных методов лечения заболеваний пародонта являются важной частью отечественных и зарубежных исследований в течение последних 20 лет [1-5]. Микробный фактор, который в клинической практике идентифицируют как зубной налет или мягкие зубные отложения, является основным этиологическим фактором гингивита. Большое значение в микробиологии полости рта имеет разработка клинических мгновенных тестов, исследующих структуру и/или содержимое десневой борозды и ротовой жидкости, прогнозирование продолжительности ремиссии и обострения на основе микробиологических данных. Таким образом, изучение факторного микробного гомеостаза в настоящее время имеет большое теоретическое и практическое значение, так как позволяет выявить механизмы взаимодействия микроорганизмов и тканей в полости рта [2-6]. Установлено, что хронический гингивит у детей представляет особый интерес для профилактики и лечения заболеваний пародонта.
Заболеваемость гингивитом составляет почти 100%, болеют преимущественно дети и молодые люди до 25–30 лет. Разработка и внедрение успешных методов лечения заболеваний пародонта являются важной частью отечественных и зарубежных исследований в течение последних 20 лет [1-5]. Микробный фактор, который в клинической практике идентифицируют как зубной налет или мягкие зубные отложения, является основным этиологическим фактором гингивита. Большое значение в микробиологии полости рта имеет разработка клинических мгновенных тестов, исследующих структуру и/или содержимое десневой борозды и ротовой жидкости, прогнозирование продолжительности ремиссии и обострения на основе микробиологических данных. Таким образом, изучение факторного микробного гомеостаза в настоящее время имеет большое теоретическое и практическое значение, так как позволяет выявить механизмы взаимодействия микроорганизмов и тканей в полости рта [2-6]. Установлено, что хронический гингивит у детей представляет особый интерес для профилактики и лечения заболеваний пародонта. Фармацевтическая эффективность определяется тем, насколько быстро они могут устранить возбудитель или сделать невозможным его негативное воздействие, а также отсутствием рецидивов у детей. Существует проблема недостаточной эффективности применяемых в настоящее время методов лечения. Аспекты, связанные с терапией хронического катарального гингивита, представляются межотраслевыми вопросами между стоматологией и терапией. Пародонтология (термин впервые был использован Оффенбахером в 1998) рассматривается как новый раздел пародонтологии, изучающий взаимовлияние системных заболеваний и воспалительных заболеваний пародонта для разработки новых диагностических критериев, стратегии терапии и целостной профилактической программы заболеваний пародонта [1, 4, 7, 8]. Недавние исследования молекулярно-морфологических нарушений, возникающих при хроническом катаральном гингивите у детей, выявили необходимость применения в комплексной терапии таких больных иммунокорректоров, позволяющих воздействовать как на пародонт, так и на весь организм.
Фармацевтическая эффективность определяется тем, насколько быстро они могут устранить возбудитель или сделать невозможным его негативное воздействие, а также отсутствием рецидивов у детей. Существует проблема недостаточной эффективности применяемых в настоящее время методов лечения. Аспекты, связанные с терапией хронического катарального гингивита, представляются межотраслевыми вопросами между стоматологией и терапией. Пародонтология (термин впервые был использован Оффенбахером в 1998) рассматривается как новый раздел пародонтологии, изучающий взаимовлияние системных заболеваний и воспалительных заболеваний пародонта для разработки новых диагностических критериев, стратегии терапии и целостной профилактической программы заболеваний пародонта [1, 4, 7, 8]. Недавние исследования молекулярно-морфологических нарушений, возникающих при хроническом катаральном гингивите у детей, выявили необходимость применения в комплексной терапии таких больных иммунокорректоров, позволяющих воздействовать как на пародонт, так и на весь организм.
Материалы и методы
Этическая оценка
Все вмешательства, проведенные в ходе исследования, были одобрены Этическим комитетом Воронежского государственного медицинского университета им. ).
Пациенты
Для обоснования обоснованности исследована частота хронического катарального гингивита у детей и зависимость его тяжести от состояния гигиены полости рта. Обследовано 157 детей в возрасте 12-15 лет. По клиническим данным было отобрано 93 детей с хроническим катаральным гингивитом (54 больных хроническим катаральным гингивитом легкой степени и 39 больных хроническим катаральным гингивитом средней степени тяжести) ( Таблица 1).
Кроме того, группа обследованных подростков с хроническим катаральным гингивитом была разделена на две группы: дети, получавшие терапию иммунокорректорами (62 ребенка) и дети, не получавшие такой терапии (31 ребенок).
Таблица 1. Распределение детей по частоте и тяжести гингивита
|
Возраст, лет |
Заболеваемость ging., no. ( % ) |
Отсутствие рыж., шт. (%) |
Мягкий имбирь, нет. (%) |
Умеренный имбирь, № (%) |
|
12 |
15 (38,5) |
24 (61,5) |
7 (17,9) |
8 (20,5) |
|
13 |
26 (57,8) |
19 (42,2) |
14 (31.1) |
12 (26,7) |
|
14 |
24 (64,9) |
13 (35,1) |
8 (21,6) |
16 (43,2) |
|
15 |
28 (77,8) |
8 (22,2) |
5 (13,9) |
23 (63,9) |
лет, лет; ging. , гингивит.
, гингивит.
Методы
Физикальное обследование ребенка включало данные анамнеза и осмотр полости рта. Для диагностики гингивита использовали папиллярно-маргинально-альвеолярный индекс (ПМА) [9] в модификации Parma (1960) [10]; Для оценки состояния гигиены полости рта использовали индекс Грина-Вермиллиона [11].
Выделение микроорганизмов из среды их естественного обитания – тканей и жидкостей полости рта – осуществляли путем культивирования исследуемых материалов на искусственных средах. Используемый метод называется культуральным исследованием. Радиальную иммунодиффузию, или метод Манчини [12], использовали для выявления изменений иммунологических показателей плазмы крови у детей с хроническим катаральным гингивитом.
Дизайн
Профилактические и лечебные мероприятия проводились по следующему графику: -Индекс Vermillion, оценка состояния тканей пародонта с использованием индекса PMA. Лабораторные методы исследования заключались в микробиологическом исследовании содержимого десневой щели и ротовой жидкости, исследовании иммунологических показателей плазмы крови у детей с хроническим катаральным гингивитом до применения терапии иммунокорректорами.
Лабораторные методы исследования заключались в микробиологическом исследовании содержимого десневой щели и ротовой жидкости, исследовании иммунологических показателей плазмы крови у детей с хроническим катаральным гингивитом до применения терапии иммунокорректорами.
На этапе 2 и установлено комплексное лечение хронического катарального гингивита у детей с применением местно-иммунотерапии и иммунокорректора «Имудон». Через три месяца были выполнены лабораторные методы исследования: микробиологическое исследование содержимого десневой щели и ротовой жидкости, исследование иммунологических показателей плазмы у детей с хроническим катаральным гингивитом после проведения местно-иммунотерапии и иммунокорректора «Имудон» соответственно.
Статистический анализ
Первичные данные анализировали с помощью прикладного статистического пакета Statistica 6.0 (Statsoft Inc., США).
Условия нормальности исследуемых данных и дисперсионный критерий распределения признаков в сравниваемых группах оценивали с помощью критерия Шапиро-Уилкса. Было решено, что значение, равное 0,05, станет порогом статистической значимости.
Было решено, что значение, равное 0,05, станет порогом статистической значимости.
Использовались следующие описательные статистики: минимум и максимум (min-max), среднее с его стандартной ошибкой (M±m).
Результаты и обсуждение
Физикальное обследование детей проводили по специально разработанному графику, полученные данные заносили в историю болезни. Доказана зависимость частоты и тяжести гингивита от состояния гигиены полости рта, роль конкремента как фактора, влияющего на этиологию исследуемого заболевания. Для диагностики гингивита использовали индекс РМА, состояние гигиены полости рта оценивали по индексу Грина-Вермилиона ( Рисунок 1).
Рис. 1. Данные индекса Грина-Вермиллиона в зависимости от возраста.
лет, лет.
Как видно из рисунка 1, при хроническом легком катаральном гингивите гигиена полости рта всегда оценивалась как неудовлетворительная (индекс Грина-Вермиллиона: 1,9–2,2), при среднетяжелом хроническом катаральном гингивите – как неудовлетворительная и плохая. (индекс Грина-Вермиллиона: 2,5–2,9). Полученные данные физикального обследования больных показывают, что для повышения эффективности профессиональной гигиены полости рта как метода профилактики воспалительных заболеваний пародонта необходимо каждые 3–4 месяца контролировать гигиену полости рта и состояние тканей пародонта и проводить профилактические мероприятия в сумма, необходимая каждому пациенту. Для оценки местного иммунитета у детей с хроническим катаральным гингивитом применяли однократную радиальную иммунодиффузию или метод Манчини. Забор крови проводился утром натощак. Иммуноглобулины IgA, IgG, IgM плазмы крови определяли по методу Манчини у детей обеих групп – основной и контрольной. Данное исследование проводилось дважды: до и после профилактических и лечебных мероприятий. Находки у детей с хроническим катаральным гингивитом были аномальными с повышенным уровнем иммуноглобулинов в плазме крови. Самые высокие показатели наблюдались у детей с умеренным гингивитом по сравнению с детьми с легким гингивитом (9).
(индекс Грина-Вермиллиона: 2,5–2,9). Полученные данные физикального обследования больных показывают, что для повышения эффективности профессиональной гигиены полости рта как метода профилактики воспалительных заболеваний пародонта необходимо каждые 3–4 месяца контролировать гигиену полости рта и состояние тканей пародонта и проводить профилактические мероприятия в сумма, необходимая каждому пациенту. Для оценки местного иммунитета у детей с хроническим катаральным гингивитом применяли однократную радиальную иммунодиффузию или метод Манчини. Забор крови проводился утром натощак. Иммуноглобулины IgA, IgG, IgM плазмы крови определяли по методу Манчини у детей обеих групп – основной и контрольной. Данное исследование проводилось дважды: до и после профилактических и лечебных мероприятий. Находки у детей с хроническим катаральным гингивитом были аномальными с повышенным уровнем иммуноглобулинов в плазме крови. Самые высокие показатели наблюдались у детей с умеренным гингивитом по сравнению с детьми с легким гингивитом (9). 0184 Таблица 2). Результаты у детей контрольной группы были аналогичны таковым в основной группе. Повторное определение иммуноглобулинов IgA, IgG, IgM плазмы крови проводили через три месяца после начала терапии «Имудоном» у пациентов основной группы и у детей контрольной группы, получавших общепринятое лечение.
0184 Таблица 2). Результаты у детей контрольной группы были аналогичны таковым в основной группе. Повторное определение иммуноглобулинов IgA, IgG, IgM плазмы крови проводили через три месяца после начала терапии «Имудоном» у пациентов основной группы и у детей контрольной группы, получавших общепринятое лечение.
Результаты исследования иммуноглобулинов у детей, получавших терапию «Имудоном», значительно улучшились по сравнению с детьми, получавшими традиционное лечение ( Таблица 3).
Таблица 2. Определение иммуноглобулинов плазмы крови IgA, IgG, IgM у детей до терапии препаратом «Имудон»
|
Параметры |
Группа управления (n =31) |
Дети с хроническим катаральным гингивитом до лечения препаратом «Иммудон» (n= 62) |
|
|
Легкий гингивит |
Умеренный гингивит |
||
|
Ig А, мкМ/л |
21,3±0,2 |
23,7±0,3* |
24,1±0,4* |
|
IgG, мкМ/л |
131,8±0,1 |
133,4±0,2* |
135,3±0,1* |
|
Ig М, мкМ/л |
20,5±0,1 |
19,4±0,2* |
21,3±0,2* |
Данные представлены как среднее значение со стандартной ошибкой (M±m). *Статистически значимые (p<0,05) различия по сравнению со здоровыми детьми.
*Статистически значимые (p<0,05) различия по сравнению со здоровыми детьми.
Таблица 3. Определение иммуноглобулинов плазмы крови IgA, IgG, IgM у детей после терапии препаратом «Имудон»
|
Параметры |
Группа управления (n =31) |
Дети с хроническим катаральным гингивитом после терапии «Иммудоном» (n= 62) |
|
|
Легкий гингивит |
Умеренный гингивит |
||
|
Ig А, мкМ/л |
17,3±0,2 |
10,7±0,2* |
13,5±0,3* |
|
IgG, мкМ/л |
116,8±0,1 |
79,8±0,1* |
82,2±0,1* |
|
Ig М, мкМ/л |
14,5±0,1 |
7,5±0,1* |
9,3±0,1* |
Данные представлены как среднее значение со стандартной ошибкой (M±m). *Статистически значимые (p<0,05) различия по сравнению со здоровыми детьми.
*Статистически значимые (p<0,05) различия по сравнению со здоровыми детьми.
Рис. 2. Средние значения индекса PMA и индекса Грина-Вермиллиона в зависимости от этапа терапии.
У детей контрольной группы, получавших традиционную терапию, также отмечается незначительное улучшение показателей иммуноглобулина. После применения местно-иммунотерапии у подростков с хроническим катаральным гингивитом улучшилось как состояние гигиены полости рта, так и выраженность воспаления (9).0184 Рисунок 2).
По-видимому, средняя интенсивность воспаления (индекс РМА) у всех подростков составляет 24,30±1,16% (индекс Грина-Вермильона: 2,60±0,06) на первом этапе, средняя интенсивность воспаления (индекс РМА) при применении препарата «Имудон» иммунокорректор составляет 10,40±0,43% (индекс Грина-Вермильона: 1,70±0,05) на втором этапе; а через три месяца после терапии «Имудоном» средняя интенсивность воспаления (индекс РМА) у всех подростков составляет 1,80±0,24% (индекс Грина-Вермилиона: 0,9). 0±0,05) соответственно.
0±0,05) соответственно.
В ходе микробиологического исследования ротовой жидкости и жидкости десневой борозды у подростков с хроническим катаральным гингивитом до лечения выявлены следующие основные виды микроорганизмов: стрептококки, стафилококки, микрококковые, Neisseria, Corynebacterium spesits, Enterodacter, Pseudomonas, Candida albicans. Наиболее часто (с частотой 21% и более) были β-гемолитические стрептококки, нейссерии, грибы Candida albicans.
Количественные микробиологические находки Streptococci, Staphylococci, Micrococcaceae, Neisseria, Corynebacterium spesits, видов Enterodacter, видов Pseudomonas и Candida albicans выявили наиболее достоверное снижение после профессиональной гигиены полости рта, сходное с результатами клинических исследований. Так, проанализирована динамика β-гемолитических стрептококков, грибов Neisseria, Candida albicans через три месяца после проведения местноиммунотерапии у подростков с хроническим катаральным гингивитом.
Изменение среднего количества колоний β-гемолитических стрептококков и количества их обнаружения как в ротовой жидкости, так и в жидкости десневой борозды, напрямую зависит от состояния гигиены полости рта; иными словами, улучшение состояния гигиены полости рта приводит к снижению среднего количества колоний β-гемолитических стрептококков в жидкости полости рта и десневой борозды.
Таким образом, доказана возможная роль β-гемолитических стрептококков в развитии зубного налета. Сообщалось также об изменении количественных микробиологических показателей Neisseria и Candida albicans в жидкости полости рта и десневой борозды. Вышеуказанные показатели значительно уменьшились после проведения местно-иммунотерапии и профессиональной гигиены полости рта, а также коррекции гигиенического статуса полости рта у детей контрольной группы. Таким образом, среднее количество колоний Neisseria уменьшилось в ротовой жидкости в 13,6 раза, в жидкости десневой борозды в 32 раза. Уменьшение количества колоний Neisseria и Candida albicans, по-видимому, снижает выраженность воспаления десен у детей с хроническим катаральным гингивитом легкой и средней степени тяжести.
Как видно из вышеизложенного, после проведения профессиональной гигиены полости рта и коррекции гигиенического статуса полости рта улучшение состояния полости рта и уменьшение выраженности воспаления привели к изменению микробиологического состава исследуемых микроорганизмов у подростков с хроническим катаральным гингивитом. Изменения в организме подростков, страдающих заболеваниями пародонта, свидетельствуют о снижении естественных защитных механизмов. В связи с этим лечение должно быть направлено не только на устранение воспалительного процесса, но и на повышение иммунитета. Тогда целесообразно применение иммунокорректоров. Считается, что эти препараты активируют защиту слизистой оболочки полости рта, обеспечивая увеличение количества особого фермента, присутствующего в слюне – лизоцима, который, как известно, обладает микробицидной активностью, стимулируя и увеличивая количество иммуноконкурентных клеток, ответственных за выработку антител. Таким иммунокорректором считается «Имудон». Применение «Имудона» вызывает восстановление резидентной микрофлоры полости рта и оказывает противовоспалительное действие. Применение «Имудона» приводит к уменьшению количества патогенных микроорганизмов на слизистой оболочке пародонта. Растворяясь в полости рта, эти таблетки активизируют естественную иммунную защиту организма.
Изменения в организме подростков, страдающих заболеваниями пародонта, свидетельствуют о снижении естественных защитных механизмов. В связи с этим лечение должно быть направлено не только на устранение воспалительного процесса, но и на повышение иммунитета. Тогда целесообразно применение иммунокорректоров. Считается, что эти препараты активируют защиту слизистой оболочки полости рта, обеспечивая увеличение количества особого фермента, присутствующего в слюне – лизоцима, который, как известно, обладает микробицидной активностью, стимулируя и увеличивая количество иммуноконкурентных клеток, ответственных за выработку антител. Таким иммунокорректором считается «Имудон». Применение «Имудона» вызывает восстановление резидентной микрофлоры полости рта и оказывает противовоспалительное действие. Применение «Имудона» приводит к уменьшению количества патогенных микроорганизмов на слизистой оболочке пародонта. Растворяясь в полости рта, эти таблетки активизируют естественную иммунную защиту организма. Благодаря вспомогательным веществам активные компоненты длительное время воздействуют на слизистую оболочку полости рта. Учитывая все вышеизложенное, можно сделать вывод, что применение «Имудона» в качестве компонента местно-иммунотерапии дает положительный эффект в комплексном лечении хронического катарального гингивита у подростков.
Благодаря вспомогательным веществам активные компоненты длительное время воздействуют на слизистую оболочку полости рта. Учитывая все вышеизложенное, можно сделать вывод, что применение «Имудона» в качестве компонента местно-иммунотерапии дает положительный эффект в комплексном лечении хронического катарального гингивита у подростков.
Заключение
Заболеваемость хроническим катаральным гингивитом у детей в возрасте 12-15 лет остается достаточно высокой и составляет 76,3-86,9%.
Установлено соответствие между изменениями иммунологических показаний плазмы крови у детей с хроническим катаральным гингивитом, получающих терапию «Имудоном» до и после лечения.
Возрастные количественные изменения показателей β-гемолитических стрептококков в жидкости полости рта и десневой борозды у детей с хроническим катаральным гингивитом в динамике исследования были аналогичны полученным после терапии «Имудоном». Количественные признаки Neisseria и Candida albicans в жидкости ротовой полости и десневой борозды снижались постепенно по мере динамики изменения интенсивности воспаления (индекс РМА).
Конфликт интересов: не заявлен.
Ссылки:
- Альбицкая Ю.Н. Особенности биохимических изменений в полости рта у лиц молодого возраста, страдающих кариесом и гингивитом в зависимости от возраста и времени года: Дис. Ростов-на-Дону, Россия, 2005. Русский
- Улитовский С. Распространение средств индивидуальной гигиены полости рта и их роль в профилактике стоматологических заболеваний. DentArt 2004; (1): 21. Русский
- Ипполитов Ю.А. Комплексная терапия хронического генерализованного гингивита с применением бета-терапии: Дисс. Воронеж, Россия, 1996; 256 стр. русский
- Гаркавец С.А. Факторы риска, гомеостаз, интенсивность и заболеваемость кариесом у детей: дис. Воронеж, Россия, 2008 г.; 232 стр. русский
- Куралесина В.П. Роль профессиональной гигиены полости рта в лечении и профилактике хронического гингивита: дис. Воронеж, Россия, 2003; 122 стр. русский
- Цепов Л.М., Николаев А.И.
 , Жажнов Е.Н. Об этиологии и патогенезе воспалительных заболеваний пародонта (обзор). Пародонтология 2000; (2): 9-12. русский
, Жажнов Е.Н. Об этиологии и патогенезе воспалительных заболеваний пародонта (обзор). Пародонтология 2000; (2): 9-12. русский - Камерон А., Уидмер Р., Виноградова Т.Ф. Справочник по детской стоматологии. Москва, Россия: МЕДпресс-информ, 2003. Русский .
- Петрович Ю.А., Пузин М.Н., Сухова Г.В. Свободнорадикальное окисление и антиоксидантная защита слюны и крови при хроническом генерализованном пародонтите. Российский Стоматологический Журнал 2000; (3): 11-13. русский
- Schour J, Massler M. Болезнь десен в послевоенной Италии (1945). J Am Dent Assoc 1947; 35: 475-482. https://www.ncbi.nlm.nih.gov/pubmed/20260900.
- Парма С. Пародонтопатии. Лейпциг: Дж. А. Барт, 1960; 203 стр. немецкий
- Зеленый JC, Vermillion JR. Индекс гигиены полости рта: метод классификации состояния гигиены полости рта. J Am Dent Assoc 1960; 61: 172-179. http://dx.doi.org/10.14219/jada.archive.1960.0177.
- Манчини Г., Карбонара А.
 О., Хереманс Дж.Ф. Иммунохимический количественный анализ антигенов методом однократной радиальной иммунодиффузии. Иммунохимия 1965; 2(3): 235-254. http://dx.doi.org/10.1016/0019-2791(65)
О., Хереманс Дж.Ф. Иммунохимический количественный анализ антигенов методом однократной радиальной иммунодиффузии. Иммунохимия 1965; 2(3): 235-254. http://dx.doi.org/10.1016/0019-2791(65)-2.
Об авторах:
Ипполитов Юрий Александрович – д.м.н., доцент, заведующий кафедрой детской стоматологии и ортодонтии Воронежского областного центра им. Бурденко, Воронеж, Россия. http://orcid.org/0000-0001-9922-137X.
Гарковец Светлана Анатольевна – к.м.н., ассистент кафедры детской стоматологии и ортодонтии, Воронеж Н.Н. Бурденко, Воронеж, Россия.
Русанова Татьяна Анатольевна – к.м.н., ассистент кафедры детской стоматологии и ортодонтии, Воронежский медицинский центр им. Бурденко, Воронеж, Россия.
Юденкова Светлана Николаевна — кандидат медицинских наук, доцент кафедры детской стоматологии и ортодонтии, Воронежский медицинский центр им. Бурденко, Воронеж, Россия.
Виктория Р. Куралесина – к.м.н., доцент кафедры детской стоматологии и ортодонтии, г. Воронеж. Бурденко, Воронеж, Россия.
Куралесина – к.м.н., доцент кафедры детской стоматологии и ортодонтии, г. Воронеж. Бурденко, Воронеж, Россия.
Алешина Елена Олеговна – ассистент кафедры детской стоматологии и ортодонтии, Воронежская клиника им. Бурденко, Воронеж, Россия.
Плотникова Яна Анатольевна – аспирант кафедры детской стоматологии и ортодонтии, Воронежский медицинский центр им. Бурденко, Воронеж, Россия.
Чунг С. Чан – аспирант кафедры детской стоматологии и ортодонтии, Воронеж Н.Н. Бурденко, Воронеж, Россия.
Маньшин Евгений Сергеевич – ординатор кафедры детской стоматологии и ортодонтии, Воронежский медицинский центр им. Н.Н. Бурденко, Воронеж, Россия.
получил 12 апреля 2016 года, пересмотрено 9 февраля 2017 года, принято 5 марта 2017 г.
© 2016, Ippolitov Y.A., Garkavets S.A., Rusanova T.A., Yudenkova S.N., Kuralesina v.p., Aleshina E.O., Plotnikova y………, что S.S.A.A.A. A……,
A……,
© 2016, Российский открытый медицинский журнал
Переписка с Ипполитов Юрий Александрович. Телефон: +7
DOI:
10.15275/rusomj.2017.0209
Автор(ы):
Алешина Елена О. / Чан, Чунг С. / Гаркавец Светлана А. / Ипполитов Юрий А. / Куралесина Виктория П. / Маньшин Евгений С. / Плотникова Яна А. / Русанова Татьяна А. / Юденкова Светлана Н.
[PDF] УРОВЕНЬ ИНТЕРЛЕЙКИНА-18 В РОТОВОЙ ЖИДКОСТИ У МЛАДШИХ ШКОЛЬНИКОВ С ХРОНИЧЕСКИМ КАТАРАЛЬНЫМ ГИНГИВИТОМ И САХАРНЫМ ДИАБЕТОМ I ТИПА.
- .
title={УРОВЕНЬ ИНТЕРЛЕЙКИНА-18 В РОТОВОЙ ЖИДКОСТИ У МЛАДШИХ ШКОЛЬНИКОВ С ХРОНИЧЕСКИМ КАТАРАЛЬНЫМ ГИНГИВИТОМ И САХАРНЫМ ДИАБЕТОМ I ТИПА.},
автор={Алина Максименко и Ольга Шешукова и Ирина Кузь и Наталья А. Ляхова и Ирина М Ткаченко},
журнал={Wiadomosci lekarskie},
год = {2021},
объем={74 6},
страницы={
1336-1340 гг.
 }
}
}
} - Максименко А.В., Шешукова О.В., Ткаченко И.В.
Цель: Нашей научной работы явилось изучение уровня провоспалительного интерлейкина-18 (ИЛ-18) в ротовой жидкости детей с сахарным диабетом (СД) I типа, определение их пародонтального статуса и уровня гигиены полости рта.
ПАЦИЕНТЫ И МЕТОДЫ
Материалы и методы: обследовано 82 ребенка, которые были разделены на группы по наличию гингивита и сахарного диабета. Уровень интерлейкина-18 в ротовой жидкости определяли иммуноферментным методом.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
Результаты: у пациентов…
Просмотр в PubMed
doi.orgФУНКЦИОНИРОВАНИЕ НО-ЦИКЛ В РОТОВОЙ ЖИДКОСТИ У ДЕТЕЙ МЛАДШЕГО ШКОЛЬНОГО ВОЗРАСТА С САХАРНЫМ ДИАБЕТОМ 1 ТИПА В ЛЕЧЕНИИ ХРОНИЧЕСКОГО КАТАРАЛЬНОГО ГИНГИВИТА.
Разработанная схема лечения хронического катарального гингивита у детей с сахарным диабетом 1 типа нормализует поляризацию макрофагов ротовой полости, обусловленную воздействием хронического катарального гедивита как местного патогенетического фактора.

ПОКАЗАНЫ 1-10 ИЗ 21 ССЫЛОК
СОРТИРОВКА ПОРелевантность Наиболее влиятельные статьиНедавность
Уровни интерлейкина-18 и фактора некроза опухоли-альфа в жидкости десневой борозды у детей с диабетом 1 типа и гингивитом
У детей с диабетом с хорошим метаболическим контролем СД1 не влиял на уровни GCF IL-18 и TNF-α при наличии гингивита, однако повышенные уровни GCF T NF-α у детей с гингивитом подтверждают, что TNF-α тесно связан с воспалением десен.
Оценка содержания интерлейкина-18 в жидкости и сыворотке десневой борозды бенгальской популяции со здоровым пародонтом и заболеваниями пародонта
По мере усиления воспаления наблюдалось сопутствующее повышение уровня IL-18 и наоборот после периодонтальной терапии, а в группах после лечения (1B–4B) наблюдалось снижение средней концентрации IL-18 как в GCF, так и в сыворотке.
Уровни интерлейкина-17 и интерлейкина-18 на разных стадиях воспалительного заболевания пародонта
Уровни IL-17 и IL-18 в тканях десны значительно варьируют в зависимости от состояния пародонта и при заболеваниях.

Влияние экспериментального пародонтита, экспериментального диабета и их комбинации на сывороточные уровни адипонектина, лептина, IL-6, IL-18, MCP-1, RANTES и sICAM-1 у крыс.
Можно сделать вывод, что наличие ожирения может препятствовать улучшению клинических параметров пародонта после традиционного пародонтологического лечения у пациентов с сахарным диабетом и пародонтитом.
Влияние экспериментального пародонтита на сывороточные уровни лептина и IL-18 у крыс с диабетом, получавших инсулин
- E. Pepelassi, I. Xynogala, D. Perrea, A. Pantopoulou, G. Agrogiannis, I. Vrotsos
-
Медицина, биология
American Journal of Internal Medicine
- 2019
IL-18 способствует секреции матриксных металлопротеиназ в фибробластах периодонтальной связки человека путем активации передачи сигналов NF-κB.

Полученные данные показывают, что IL-18 способствует секреции MMP1, MMP2, MMP3 и MMP9 в hPDLF путем активации сигнального пути NF-kB, играющего ключевую роль в развитии хронического периодонтита.
Активация белков инфламмасомы NLRP3 у пациентов с пародонтитом и неконтролируемым диабетом 2 типа.
- А. Гарсия-Эрнандес, Анхель Энрике Муньос-Сааведра, Н. Рубио-Инфанте
-
Медицина, биология
Заболевания полости рта
- 2019
Активация генов и белков, участвующих в активации компонентов инфламмасомы NLRP3 у пациентов с пародонтитом и неконтролируемым СД2, предполагает возможную роль в более тяжелых патологических процессах, приводящих к деструкции тканей пародонта, наблюдаемых у этих пациентов.
Обнаружение белков и мРНК IL-18 и IL-1β в эпителиальных клетках ротовой полости человека, индуцированных штаммами Campylobacter concisus.
h3S опосредует повышенную продукцию интерлейкина (IL)-1β и IL-18 в лейкоцитах пациентов с пародонтитом
h3S из поддесневой микробиоты может способствовать воспалительной реакции хозяина посредством секреции провоспалительных цитокинов IL-1β и IL-18, а также может отражать предрасположенность хозяина к развитию пародонтита.

Исследование показателей динамики жидкости ротовой полости на фоне патологической и физиологической стираемости зубов.
Установлено, что минерализующая функция слюны изменяется при возникновении кариесогенной ситуации в полости рта, что приводит к дестабилизации кристаллической структуры ротовой жидкости и указывает на взаимосвязь между ее структурными и минерализующими свойствами.
Идентификация проб жидкости десневой борозды, аналитические методы и оральные биомаркеры для диагностики и мониторинга заболеваний пародонта: систематический обзор
На этой странице
Несколько исследований последних десятилетий были сосредоточены на поиске точного метода диагностики заболеваний пародонта на ранних стадиях. Цель . Оценить из современной научной литературы наиболее распространенный и точный метод сбора образцов жидкости десневой борозды (GCF), методы анализа биомаркеров и вариабельность количественного определения биомаркеров, даже при использовании одного и того же аналитического метода.
 Методология . Был проведен электронный поиск исследований in vivo, в которых были представлены клинические данные о методах, используемых для сбора GCF и анализа биомаркеров. Результаты . Результаты показали, что в 71,1%, 24,7% и 4,1% исследований для сбора жидкости из десневой борозды использовались методы абсорбции, микрокапилляров и промывания соответственно. 73,1% исследователей проанализировали свои образцы с помощью твердофазного иммуноферментного анализа (ИФА). 22,6%, 190,5% и 18,5% исследователей включали интерлейкин-1 бета (IL-1 β ), матриксную металлопротеиназу-8 (ММР-8) и фактор некроза опухоли-альфа (TNF- α ) соответственно. в своих исследованиях в качестве биомаркеров заболеваний пародонта. Заключение . IL-1 β можно отнести к числу наиболее распространенных биомаркеров, которые дают точные результаты и могут использоваться в качестве индикатора прогрессирования заболеваний пародонта. Кроме того, бумажные полоски являются наиболее удобным и точным методом сбора жидкости из десневой борозды, а иммуноферментный анализ можно считать наиболее традиционным методом диагностики биожидкостей.
Методология . Был проведен электронный поиск исследований in vivo, в которых были представлены клинические данные о методах, используемых для сбора GCF и анализа биомаркеров. Результаты . Результаты показали, что в 71,1%, 24,7% и 4,1% исследований для сбора жидкости из десневой борозды использовались методы абсорбции, микрокапилляров и промывания соответственно. 73,1% исследователей проанализировали свои образцы с помощью твердофазного иммуноферментного анализа (ИФА). 22,6%, 190,5% и 18,5% исследователей включали интерлейкин-1 бета (IL-1 β ), матриксную металлопротеиназу-8 (ММР-8) и фактор некроза опухоли-альфа (TNF- α ) соответственно. в своих исследованиях в качестве биомаркеров заболеваний пародонта. Заключение . IL-1 β можно отнести к числу наиболее распространенных биомаркеров, которые дают точные результаты и могут использоваться в качестве индикатора прогрессирования заболеваний пародонта. Кроме того, бумажные полоски являются наиболее удобным и точным методом сбора жидкости из десневой борозды, а иммуноферментный анализ можно считать наиболее традиционным методом диагностики биожидкостей.
1. Введение
Целью данного обзора является оценка проб GCF, аналитических методов и пероральных биомаркеров, используемых для диагностики и мониторинга различных заболеваний пародонта. В нем также делается попытка изучить основные причины различий в количественных оценках биомаркеров среди исследователей путем обзора исследований, основанных на критериях включения и исключения, с января 2005 г. по май 2015 г. клетках и тканях хозяина, что приводит к высвобождению многих цитокинов и хемокинов, вызывающих разрушение структур пародонта [1]. GCF у пациентов с заболеваниями пародонта содержит воспалительные клетки, бактерии, продукты распада тканей, антитела, белки и ферменты системы комплемента, а также многие медиаторы воспаления [2]. ГКФ можно отнести к числу наиболее нетравматичных методов исследования, позволяющих получить информацию о состоянии тканей пародонта, в том числе о состоянии соединительной ткани и степени деструкции твердых тканей [3]. Тяжесть воспаления тканей пародонта можно оценить путем измерения провоспалительных показателей, таких как IL-1, -6 и -8 и TNF-9.
 0863 α , которые играют важную роль в патогенезе заболеваний пародонта [4].
0863 α , которые играют важную роль в патогенезе заболеваний пародонта [4]. Заболевания пародонта должны быть описаны с помощью критериев, которые являются четкими и подходящими для применения любым исследователем, чтобы тот же диагноз мог быть поставлен другими исследователями в тех же условиях [5]. Ранняя диагностика заболеваний пародонта имеет большое значение, что требует быстрого, чувствительного и точного аналитического теста в кресле [6, 7].
Методы диагностики должны предоставлять соответствующую информацию, помогающую дифференцировать различные заболевания пародонта, степень разрушения ткани пародонта и прогнозировать заболевание пародонта. В настоящее время основной метод, используемый в диагностике заболеваний пародонта, зависит, главным образом, от измерения клинических параметров пародонта, включая количество зубного налета (PS) или индекс зубного налета (PI), потерю клинического прикрепления (CAL), глубину зондирования (PD), индекс десны. (GI) или кровотечение при зондировании (BOP), в дополнение к рентгенологическим данным.
 Однако результаты этих клинических параметров скорее свидетельствуют о предшествующем повреждении пародонта, чем уточняют будущее состояние тканей пародонта. Поэтому очень важно найти метод, который может предсказать предстоящее заболевание пародонта. Необходимо исследовать более надежные методы диагностики пародонта [105], такие как тест MMP-8 в кресле, который зависит от принципа иммунохроматографии, который может быть полезен для подтверждения клинических диагностических параметров на поддерживающей фазе [6, 77]. Более того, результаты такого теста повышают точность диагностики заболеваний пародонта и результатов неудачного лечения [106]. Однако этот тест быстр, недорог и прост в выполнении и занимает всего 5 минут [107].
Однако результаты этих клинических параметров скорее свидетельствуют о предшествующем повреждении пародонта, чем уточняют будущее состояние тканей пародонта. Поэтому очень важно найти метод, который может предсказать предстоящее заболевание пародонта. Необходимо исследовать более надежные методы диагностики пародонта [105], такие как тест MMP-8 в кресле, который зависит от принципа иммунохроматографии, который может быть полезен для подтверждения клинических диагностических параметров на поддерживающей фазе [6, 77]. Более того, результаты такого теста повышают точность диагностики заболеваний пародонта и результатов неудачного лечения [106]. Однако этот тест быстр, недорог и прост в выполнении и занимает всего 5 минут [107]. 2. Методология
2.1. Критерии включения и исключения
Критерии включения в настоящее исследование включали (a) клинические исследования, (b) исследования, проведенные как на системно здоровых, так и на системно нездоровых субъектах [пациенты с сахарным диабетом (СД), ишемической болезнью сердца или ревматоидным артритом (РА).
 )] с заболеванием пародонта, (c) исследования, проведенные на курильщиках, тревожных или беременных субъектах, (d) исследования, опубликованные только на английском языке, и (e) исследования, разъясняющие методологию сбора образцов GCF и методы анализа биомаркеров. Критерии исключения включали исследования, специально разработанные для изучения биомаркеров жидкости околоимплантатной борозды (PISF), письма в редакцию, исторические обзоры и комментарии.
)] с заболеванием пародонта, (c) исследования, проведенные на курильщиках, тревожных или беременных субъектах, (d) исследования, опубликованные только на английском языке, и (e) исследования, разъясняющие методологию сбора образцов GCF и методы анализа биомаркеров. Критерии исключения включали исследования, специально разработанные для изучения биомаркеров жидкости околоимплантатной борозды (PISF), письма в редакцию, исторические обзоры и комментарии. 2.2. Протокол поиска
Поиск в базах данных PubMed, Google Scholar и Web of Science с 2005 по 2015 год проводился с использованием комбинаций следующих ключевых слов: «заболевания пародонта», «пародонтит», «оральные биомаркеры», «биомаркеры» и «жидкости десневой борозды». ». Названия и тезисы исследований были идентифицированы с использованием описанного выше протокола, выбраны авторами и проверены на соответствие. Полные тексты исследований были определены по названию и аннотации, а затем независимо оценены авторами (Зейад Назар Маджид, Дасан Сваминатан, А.
 М. Алабси, Коши Филип и Сараванан Пушпараджан) со ссылкой на критерии включения и исключения. Первоначально было выявлено 2765 публикаций, в то время как только 97 исследований, которые соответствовали критериям включения, были включены и обработаны для извлечения данных, как показано на блок-схеме (рис. 1).
М. Алабси, Коши Филип и Сараванан Пушпараджан) со ссылкой на критерии включения и исключения. Первоначально было выявлено 2765 публикаций, в то время как только 97 исследований, которые соответствовали критериям включения, были включены и обработаны для извлечения данных, как показано на блок-схеме (рис. 1). 3. Методы сбора жидкости из десневой борозды
3.1. Техника интракревикулярной промывки
Устройство, используемое для выполнения этого метода, состоит из двух инъекционных игл, вставленных одна в другую. Этот метод сбора GCF был хорошо описан Салоненом и Паунио [108], а основные детали исследований, в которых использовалась техника промывки при сборе GCF, кратко проиллюстрированы в Таблице 1.
3.2. Microcapillary Technique
Для сбора GCF используется калиброванная волюметрическая или некалиброванная микрокапиллярная пипетка с известным объемом. Прадип и др. [23, 24] в своих исследованиях дали хорошее описание того, как выполнять эту технику сбора.
 В этом систематическом обзоре эта методика использовалась в 24 исследованиях (таблица 2).
В этом систематическом обзоре эта методика использовалась в 24 исследованиях (таблица 2). 3.3. Техника абсорбции
В таблице 3 обобщены наиболее важные результаты исследований, в которых использовалась методика абсорбции. Обычно эта техника делится на экстракревикулярную (рис. 2) и интракревикулярную (рис. 3). Первый выполняется путем размещения бумажных полосок над десневой щелью, чтобы уменьшить травму. Второй метод – это интракревикулярная техника, которая используется чаще всего. В зависимости от глубины введения полоски в десневую борозду или пародонтальный карман ее можно разделить на поверхностную и глубокую [109].].
4. Результаты
В этом систематическом обзоре метаанализ результатов не проводился, поскольку неоднородность рассмотренных исследований включала следующие аспекты: выборка GCF, аналитические методы и пероральные биомаркеры, используемые в диагностике и мониторинге парадантоз.
4.1. Методы отбора проб
Что касается методов, используемых для сбора GCF, в наш обзор были включены и проиллюстрированы 97 исследований (таблицы 1, 2 и 3).
 В 69 исследованиях для сбора GCF использовались бумажные полоски (таблица 3), в 24 исследованиях использовались микрокапиллярные пипетки (таблица 2), и только в 4 исследованиях для сбора образцов использовался метод промывания десен (таблица 1).
В 69 исследованиях для сбора GCF использовались бумажные полоски (таблица 3), в 24 исследованиях использовались микрокапиллярные пипетки (таблица 2), и только в 4 исследованиях для сбора образцов использовался метод промывания десен (таблица 1). 4.2. Аналитические методы
Как показано в таблицах 1, 2 и 3, для анализа проб ГКФ было использовано множество методов, чтобы получить желаемые результаты. Аналитический метод ELISA явно был предпочтительным в большинстве исследований. В 71 из 97 рассмотренных нами исследований использовалась методика ELISA для анализа образцов GCF.
4.3. Биомаркеры
Из 97 исследований были рассмотрены IL-1 β (22 исследования), MMP-8 (19 исследований) и TNF- α (18 исследований). Эти результаты показали, что эти концентрации биомаркеров можно использовать для сравнения различных стадий заболеваний пародонта и/или оценки эффективности пародонтальной терапии.
Результаты отбора проб и методов анализа, а также биомаркеров представлены на рисунке 4.

4.4. IL-1
βСравнение уровней GCF IL-1 β между пациентами с заболеваниями пародонта и здоровыми субъектами было проведено для того, чтобы объяснить пригодность использования IL-1 β в качестве биомаркера прогрессирования заболевания пародонта. В это сравнение были включены только 10 исследований из 22 исследований (таблица 4) из-за исключения исследований, которые не продемонстрировали достаточного количества клинических данных, и исследований, проведенных на пациентах с заболеваниями пародонта и системными заболеваниями (например, сахарным диабетом). ) или любые другие условия, которые могут повлиять на результаты (например, беременные женщины и курильщики). Ил-1 9Концентрации 0863 β во всех исследованиях показали значимые различия от умеренных до высоких между здоровыми субъектами и пациентами с ХП или GAgP.
Из 10 исследований, которые были включены для определения различий в уровнях IL-1 β , только 3 исследования [41, 51, 103] показали различия в уровнях IL-1 β между здоровыми субъектами и пациентами с гингивитом.
 Однако эта разница была недостоверна.
Однако эта разница была недостоверна. 4.5. ММР-8
Что касается различий уровней ММР-8 между здоровыми и больными субъектами, только 4 исследования соответствовали критериям включения, таким же, как и для ИЛ-1 β . Во всех исследованиях (таблица 5) были выявлены различия между здоровыми субъектами и больными ДЦП. Хотя эти различия были весьма значительными в исследованиях, проведенных Konopka et al. [67], Рай и соавт. [88] и Teles et al. [98], Якоб и соавт. не сочли его значимым. [11].
4.6. TNF-
αДля различий уровней TNF- α между здоровыми и больными субъектами было включено только 8 исследований, которые соответствовали критериям включения (таблица 6). Рейс и др. [91] показали, что уровни TNF- α были значительно выше в пораженных участках по сравнению с здоровыми участками. Gokul [14] показал очень значимую разницу между здоровыми субъектами и пациентами с гингивитом и ХП. Куртиш и др. [70] показали очень значимую разницу между здоровыми субъектами и пациентами с ХП и GAgP.
 Однако другие исследования показали лишь небольшую разницу в уровне TNF- α между здоровыми и больными субъектами.
Однако другие исследования показали лишь небольшую разницу в уровне TNF- α между здоровыми и больными субъектами. Несмотря на схожесть результатов с результатами большинства исследований, рассмотренных в этом систематическом обзоре, влияние биомаркеров на заболевания пародонта все же различалось. Результаты исследований также определили, как эти биомаркеры могут быть использованы для диагностики или мониторинга состояния заболеваний пародонта, как показано в таблицах 4, 5 и 6. Настоящее исследование показало, что результаты между исследователями различались даже при использовании одни и те же аналитические методы. Чтобы прояснить различия в результатах, было проведено сравнение исследований, в которых использовались одни и те же аналитические методы (таблицы 7 и 8).
Как показано в таблице 7, были включены только пять исследований, в которых использовался один и тот же аналитический метод (стандартный метод ELISA) для количественного определения концентраций IL-1 β .
 Было весьма заметно, что были различия в значениях средних концентраций IL-1 β между исследованиями в одной и той же группе (H, G, CP и GAgP). Например, средняя концентрация IL-1 β среди здоровых субъектов в пяти исследованиях показала различия в средних значениях: 490,81, 195,77, 36,44, 15,5 и 17,8732.
Было весьма заметно, что были различия в значениях средних концентраций IL-1 β между исследованиями в одной и той же группе (H, G, CP и GAgP). Например, средняя концентрация IL-1 β среди здоровых субъектов в пяти исследованиях показала различия в средних значениях: 490,81, 195,77, 36,44, 15,5 и 17,8732. Для сравнения средних значений MMP-8 было задействовано только два исследования (таблица 8). Оба показали относительно близкие результаты, в которых была небольшая разница в средних значениях ММП-8 в каждой исследуемой группе (H, CP).
5. Обсуждение
Этот систематический обзор был разработан для выявления наиболее распространенных и точных методов сбора GCF и анализа биомаркеров, а также для определения надежных биомаркеров, которые можно использовать для выявления заболеваний пародонта.
5.1. GCF Sampling Methods
В этом документе обсуждаются три основных метода сбора GCF: абсорбция, микрокапиллярное пипетирование и метод промывки.
 В нескольких клинических исследованиях, которые были рассмотрены, были различия в методах сбора GCF.
В нескольких клинических исследованиях, которые были рассмотрены, были различия в методах сбора GCF. 5.1.1. Метод абсорбции
Различия можно обобщить следующим образом: (i) В большинстве исследований использовались бумажные полоски, которые считались более эффективными для сбора GCF, поскольку их можно было легко вводить в десневые борозды или пародонтальные карманы, а также для их способность поглощать жидкости. Тем не менее, в нескольких исследованиях для отбора образцов GCF использовались бумажные штифты (размер 30), хотя было показано, что бумажные штифты и бумажные полоски имеют разную скорость поглощения. Исследование, проведенное Guentsch et al. [110] показали, что уровни цитокинов были выше при использовании бумажных полосок. Бумажные штифты чаще используются для сбора поддесневого налета при микробиологическом анализе. (ii) Время, в течение которого бумажные полоски или бумажные штифты оставались в борозде, варьировало от 30 секунд [68, 76, 111] до 1 минуты [112].
 Наиболее часто используемый период составлял 30 секунд, чтобы снизить риск заражения кровью или слюной. (iii) Были разные места, с которых были взяты образцы ЗКФ. Во многих исследованиях образцы GCF собирались только из пораженных участков [72] у пациентов с заболеваниями пародонта, в то время как другие исследователи собирали образцы как здоровых, так и пораженных участков [111].
Наиболее часто используемый период составлял 30 секунд, чтобы снизить риск заражения кровью или слюной. (iii) Были разные места, с которых были взяты образцы ЗКФ. Во многих исследованиях образцы GCF собирались только из пораженных участков [72] у пациентов с заболеваниями пародонта, в то время как другие исследователи собирали образцы как здоровых, так и пораженных участков [111]. Таким образом, важно отметить, что большинство исследований показали, что уровни биомаркеров положительно коррелируют с пародонтальными параметрами (GI, PD и CAL). В то же время было выяснено, что здоровые участки у лиц с заболеваниями пародонта показали повышенные концентрации биомаркеров по сравнению со здоровыми участками у лиц без заболеваний пародонта. Это могло быть связано с тем, что на биомаркеры влиял бактериальный состав соседней поддесневой бляшки [9].8] и тот факт, что развитие пародонтита было локализованным [53].
5.1.2. Микрокапиллярное пипетирование
Время, необходимое для сбора образцов GCF, зависело от желаемого требуемого количества GCF, а также от состояния мест отбора проб (больные или здоровые).
 В большинстве клинических исследований образцы GCF собирали, удерживая микрокапиллярные пипетки у входа в карман в течение 10 минут [22, 85]. По нашему опыту, этой продолжительности было достаточно, если мы собирали образцы ЗКФ с пораженных участков. Однако для сбора образцов у здоровых людей или здоровых участков у пациентов с пародонтитом требовалось 30–50 минут. Эта разница во времени сбора между здоровыми и больными участками была связана с потоком GCF, который был положительно связан с тяжестью заболевания пародонта [113-115]. Длительная продолжительность, необходимая для сбора GCF при использовании микрокапиллярных пипеток, считалась одним из ограничений этого метода, что могло увеличить вероятность заражения слюной и кровью. Это также потребует больше усилий от клинициста и может занять много времени у испытуемых.
В большинстве клинических исследований образцы GCF собирали, удерживая микрокапиллярные пипетки у входа в карман в течение 10 минут [22, 85]. По нашему опыту, этой продолжительности было достаточно, если мы собирали образцы ЗКФ с пораженных участков. Однако для сбора образцов у здоровых людей или здоровых участков у пациентов с пародонтитом требовалось 30–50 минут. Эта разница во времени сбора между здоровыми и больными участками была связана с потоком GCF, который был положительно связан с тяжестью заболевания пародонта [113-115]. Длительная продолжительность, необходимая для сбора GCF при использовании микрокапиллярных пипеток, считалась одним из ограничений этого метода, что могло увеличить вероятность заражения слюной и кровью. Это также потребует больше усилий от клинициста и может занять много времени у испытуемых. 5.1.3. Метод промывки
Результаты этого обзора показали, что техника промывки коллекции GCF не была распространена из-за трудностей, связанных с техникой.
 Кроме того, наблюдался высокий уровень загрязнения кровью из-за повышенной вероятности раздражения десен.
Кроме того, наблюдался высокий уровень загрязнения кровью из-за повышенной вероятности раздражения десен. 5.2. GCF Analytical Method
При отсутствии убедительных доказательств и дефиците данных хорошо спланированных исследований, посвященных методам, используемым при анализе GCF, и после определения преимуществ и недостатков каждого метода, все еще было трудно заявить, что конкретная техника была лучше, чем другие. Это было особенно верно, если мы рассмотрели следующие аспекты: (а) точность и эффективность обнаружения и количественного определения биомаркеров, (б) осуществимость, (в) стоимость и (г) время. Было четко показано, что большинство исследователей использовали метод ИФА в своих клинических исследованиях, вероятно, из-за его простоты. Очень важно уточнить, что использование ИФА не является самой точной методикой. Например, Леппилахти и др. [73] показали, что метод IFMA является более точным, чем использование ELISA.
5.3. Оральные биомаркеры заболеваний пародонта, проанализированные из образцов GCF
На сегодняшний день точный диагноз зависит в основном от клинического осмотра пародонта, рентгенографического исследования и лабораторных тестов для микробного анализа [116], которые позволяют точно оценить и проанализировать уровни потери кости и прикрепления.
 Эти результаты могут быть дополнены анализом GCF, где, как предполагалось во многих исследованиях, GCF является источником бимолекулярной выборки для исследования состояния тканей пародонта [112, 117]. Ингредиенты GCF состоят из многих компонентов, которые были описаны как маркеры развития заболеваний пародонта. К ним относятся ферменты хозяина, модификаторы ответа хозяина и продукты распада тканей [64].
Эти результаты могут быть дополнены анализом GCF, где, как предполагалось во многих исследованиях, GCF является источником бимолекулярной выборки для исследования состояния тканей пародонта [112, 117]. Ингредиенты GCF состоят из многих компонентов, которые были описаны как маркеры развития заболеваний пародонта. К ним относятся ферменты хозяина, модификаторы ответа хозяина и продукты распада тканей [64]. Известно, что биомаркеры являются объективными и измеримыми характеристиками биологических процессов [118], и они могут поддерживать клиническую оценку, то есть, если мы полностью понимаем нормальную физиологию биологических процессов диагностики и прогрессирования заболеваний пародонта [119]. Существует множество биомаркеров, которые могут быть получены из различных биологических жидкостей, таких как кровь, сыворотка, слюна и GCF, а также из различных источников, таких как микробная биопленка зубного налета, продукты распада соединительной ткани, медиаторы воспаления и производные хозяина.
 Например, ММР, присутствующие в GCF, слюне, ополаскивателях для рта и околоимплантатной десневой жидкости (PISF), могут быть использованы для открытия нового аналитического теста в кресле и в месте оказания медицинской помощи, который является нетравматическим методом для диагностика заболеваний пародонта [120, 121].
Например, ММР, присутствующие в GCF, слюне, ополаскивателях для рта и околоимплантатной десневой жидкости (PISF), могут быть использованы для открытия нового аналитического теста в кресле и в месте оказания медицинской помощи, который является нетравматическим методом для диагностика заболеваний пародонта [120, 121]. В этом обзоре мы сосредоточились на биомаркерах GCF из-за их непосредственной близости к ткани пародонта, что сводит к минимуму возможность отражения реакции на другие воспалительные процессы в организме.
Несколько исследований показали, что уровни IL-1 β можно использовать в качестве хорошего биомаркера для дифференциации здоровых и хронических очагов пародонтита [12, 41, 51, 53, 98]. Их также можно использовать для дифференциации здоровых людей от пациентов с AgP [41, 51, 80, 99].]. Из-за небольших различий в уровнях IL-1 β между здоровыми участками и участками с гингивитом [41, 51, 103] их трудно использовать в качестве индикаторов или предикторов для начала заболевания от здорового состояния до гингивита.

Значительно более высокие уровни MMP-8 в GCF наблюдались у пациентов с пародонтитом, чем у здоровых людей [6, 67, 88, 98, 122, 123]. Это изменение уровней ММР-8 может служить индикатором развития заболеваний пародонта. Кроме того, Leppilahti et al. [72] обнаружили, что уровни MMP-8 в GCF на исходном уровне могут предсказывать поведение уровней MMP-8 во время поддерживающей фазы.
Якоб и др. [11], однако, обнаружили отсутствие статистических различий между здоровыми и больными группами, объясняя эти результаты различиями в методах, используемых для сбора GCF.
Результаты этого обзора, как также указано во многих исследованиях, показали минимальное увеличение уровней TNF- α от здоровых до пораженных пародонтом участков [59, 80, 99, 103]. В других исследованиях наблюдалось значительное повышение концентрации TNF- α от здоровых к больным участкам [14, 70, 9].1]. Таким образом, концентрации TNF- α также можно использовать в качестве предиктора прогрессирования заболевания.

Этот систематический обзор был направлен на изучение наиболее разумных факторов, которые приводят к вариабельности результатов в разных исследованиях даже при использовании одних и тех же аналитических методов. Для этого было проведено сравнение средних значений двух биомаркеров (IL-1 β и MMP-8) (таблицы 7 и 8). Были включены исследования, включающие достаточные данные, такие как количество образцов, четкие аналитические методы, количество или количество образцов GCF и точную оценку клинического диагноза с использованием клинико-диагностических параметров (PD, CAL, PI, BOP и GI). в этом сравнении. Исследования, в которых участвовали курильщики и больные диабетом, были исключены, чтобы свести к минимуму влияние на результаты. Например, клинические исследования в разных популяциях показали, что курение увеличивает риск пародонтита, а также что у курильщиков заболевание пародонта прогрессирует быстрее и тяжелее [124]. Тимкив и др. [102] обнаружили, что курение ингибирует экспрессию многих биомаркеров, включая провоспалительные хемокины, регуляторы Т-клеток и естественные клетки-киллеры.
 Это ингибирование привело к уменьшению рекрутирования многих провоспалительных цитокинов и клеток в воспаленные участки пародонта, что привело к неэффективной защите от бактериальной инвазии.
Это ингибирование привело к уменьшению рекрутирования многих провоспалительных цитокинов и клеток в воспаленные участки пародонта, что привело к неэффективной защите от бактериальной инвазии. Кроме того, механизмы, объясняющие связь между диабетом и пародонтитом, до конца не изучены, но охватывают аспекты иммунной функции, воспаления, биологии цитокинов и активности нейтрофилов [125]. Диабет 1 и 2 типа был связан с повышенным уровнем медиаторов воспаления [126], таких как IL-1 β [127] и TNF- α [128].
В таблице 7 показано большое разнообразие средних значений концентраций IL-1 β в исследованиях. Тем не менее, большинство исследователей использовали аналогичные параметры, такие как размер исследуемой популяции, которая может повлиять на среднее значение и стандартное отклонение, методы сбора GCF (в основном бумажные полоски), аналитические методы (стандартный ИФА) и клинические диагностические параметры для классификации выборки исследования (в основном PD, CAL, PI и BOP).
 Однако мы заметили, что компании, производящие наборы для ИФА, применяют разные протоколы для измерения биомаркеров, и реагенты наборов могут различаться по своей способности обнаружения. Еще одним фактором, способствовавшим этой изменчивости, может быть разница в количестве собранных жидкостей GCF, варьирующаяся от 1 до 4 бумажных полосок, собранных у каждого субъекта. Такие различия в объемах GCF также могут вызывать большие различия в частоте обнаружения биомаркеров. Это может быть подтверждено результатами в Таблице 8, которые показали небольшие различия между средними значениями биомаркеров, поскольку в обоих исследованиях использовался один и тот же протокол набора ELISA (R&D System) и одинаковое количество образцов GCF (1 бумажная полоска).
Однако мы заметили, что компании, производящие наборы для ИФА, применяют разные протоколы для измерения биомаркеров, и реагенты наборов могут различаться по своей способности обнаружения. Еще одним фактором, способствовавшим этой изменчивости, может быть разница в количестве собранных жидкостей GCF, варьирующаяся от 1 до 4 бумажных полосок, собранных у каждого субъекта. Такие различия в объемах GCF также могут вызывать большие различия в частоте обнаружения биомаркеров. Это может быть подтверждено результатами в Таблице 8, которые показали небольшие различия между средними значениями биомаркеров, поскольку в обоих исследованиях использовался один и тот же протокол набора ELISA (R&D System) и одинаковое количество образцов GCF (1 бумажная полоска). 6. Ограничения
Из-за неоднородности стратегий, использованных в рассматриваемых исследованиях, таких как выборка, аналитические методы и используемые биомаркеры, метаанализ результатов был невозможен.
7. Заключение
В случае методов сбора GCF бумажные полоски являются самым простым и более точным методом.
 Для анализа образцов GCF трудно определить наиболее точный метод анализа, но в этом обзоре отмечается, что большинство исследователей полагались на метод ELISA.
Для анализа образцов GCF трудно определить наиболее точный метод анализа, но в этом обзоре отмечается, что большинство исследователей полагались на метод ELISA. Можно сделать вывод, что при определении воспалительной активности заболеваний пародонта лучше использовать более одного биомаркера. IL-1 β и ММП-8 можно считать наиболее предпочтительными цитокинами для определения воспалительной активности в пародонте.
Собранный объем GCF и различные компании-производители наборов ELISA являются основными причинами различий среди исследователей.
В целом еще рано полагаться только на пероральные биомаркеры в диагностике заболеваний пародонта, особенно в отсутствие универсальных методов сбора и анализа этих биомаркеров. Однако его можно использовать для поддержки клинических параметров, которые являются наиболее надежными диагностическими методами, а также для мониторинга прогрессирования заболеваний пародонта.
Рекомендации для будущих исследований
Целью исследования оральных биомаркеров является обнаружение возможности их использования для прогнозирования, диагностики и мониторинга заболеваний пародонта или, по крайней мере, их использования в качестве дополнения к традиционному пародонтологическому обследованию и диагностике.
 Мы считаем, что для достижения этого исследователи должны принять во внимание следующие рекомендации в своих будущих исследованиях: (1) Измерение уровней биомаркеров GCF следует проводить с использованием различных методов сбора и анализа, чтобы определить наиболее точную технику. которые могут быть стандартизированы повсеместно. (2) Сравнение уровней биомаркеров GCF в различных этнических группах, состоящих из выборок большого размера, следует рассмотреть для изучения влияния генетических различий на уровни биомаркеров, а также для обеспечения надлежащего статистического анализа. (3) выбор биомаркеров в исследованиях, основанных на GCF, важен. Биомаркеры, которые, как известно, влияют на прогнозирование и прогрессирование заболеваний пародонта, должны быть исследованы на предмет статистической корреляции друг с другом. Примерами биомаркеров, которые могут способствовать этому, являются IL-19.0863 β и MMP-8, при этом Salminen et al. [129] использовали вместе три слюнных биомаркера для диагностики заболеваний пародонта.
Мы считаем, что для достижения этого исследователи должны принять во внимание следующие рекомендации в своих будущих исследованиях: (1) Измерение уровней биомаркеров GCF следует проводить с использованием различных методов сбора и анализа, чтобы определить наиболее точную технику. которые могут быть стандартизированы повсеместно. (2) Сравнение уровней биомаркеров GCF в различных этнических группах, состоящих из выборок большого размера, следует рассмотреть для изучения влияния генетических различий на уровни биомаркеров, а также для обеспечения надлежащего статистического анализа. (3) выбор биомаркеров в исследованиях, основанных на GCF, важен. Биомаркеры, которые, как известно, влияют на прогнозирование и прогрессирование заболеваний пародонта, должны быть исследованы на предмет статистической корреляции друг с другом. Примерами биомаркеров, которые могут способствовать этому, являются IL-19.0863 β и MMP-8, при этом Salminen et al. [129] использовали вместе три слюнных биомаркера для диагностики заболеваний пародонта.
Конкурирующие интересы
Авторы заявили об отсутствии конфликта интересов.
Вклад авторов
Все авторы в равной степени внесли свой вклад в эту работу.
Благодарности
Эта работа была поддержана Исследовательским грантом Министерства высшего образования Малайзии (HIR-MOHE) UM.C/625/1/HIR/MOHE/SC/08 (счет № F000008). -21001) под руководством главного исследователя Коши Филипа и Университета Малайи, Куала-Лумпур, Малайзия, по гранту №. ПГ226-2014Б.
Список литературы
-
S. C. Holt и J. L. Ebersole, «Porphyromonas gingivalis, Treponema denticola и Tannerella Forsythia :« Red Complex », Polypoly Potebogen’t Pategogen’t Pategogentiuts. 38, нет. 1, стр. 72–122, 2005.
Посмотреть по адресу:
Google Scholar
-
G. C. Armitage, «Заболевания пародонта: диагностика», Annals of Periodontology/American Academy of Periodontology , том.
 1, нет. 1, статья 37, 1996.
1, нет. 1, статья 37, 1996. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
N. Bostanci, T. İlgenli, G. Emingil et al., «Уровни жидкости десневой борозды RANKL и OPG при заболеваниях пародонта: последствия их относительного соотношения», Journal of Clinical Periodontology , vol. 34, нет. 5, стр. 370–376, 2007 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Р. Дж. Дженко, «Реакции хозяина при заболеваниях пародонта: современные концепции», Журнал пародонтологии , том. 63, нет. 4, стр. 338–355, 1992.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
A. Savage, K.A. Eaton, D.R. Moles, and I. Needleman, «Систематический обзор определений пародонтита и методов, которые использовались для выявления этого заболевания», Journal of Clinical Periodontology , vol.
 36, нет. 6, стр. 458–467, 2009 г.
36, нет. 6, стр. 458–467, 2009 г. Посмотреть по адресу:
Сайт издателя | Академия Google
-
P. Mäntylä, M. Stenman, D.F. Kinane et al., «Тест-полоска на коллагеназу-2 (MMP-8) жидкости десневой борозды для мониторинга периодонтита в кресле», Journal of Periodontal Research , vol. 38, нет. 4, стр. 436–439, 2003 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
H. Y. Chen, S. W. Cox, B. M. Eley, P. Mäntylä, H. Rönkä и T. Sorsa, «Уровни матричной металлопротеиназы-8 и активность эластазы в жидкости десневой борозды у взрослых пациентов с хроническим периодонтитом», Журнал клинической пародонтологии , том. 27, нет. 5, стр. 366–369, 2000.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Л.
 А. Миранда, А. Г. Ислабао, Р. Г. Фишер, К. М. С. Фигередо, Р. В. Опперманн и А. Густафссон, «Снижение уровня интерлейкина-1 β и эластазы в десневой борозде у лиц, проходящих противовоспалительное лечение. артрит», Journal of Periodontology , vol. 78, нет. 8, стр. 1612–1619., 2007.
А. Миранда, А. Г. Ислабао, Р. Г. Фишер, К. М. С. Фигередо, Р. В. Опперманн и А. Густафссон, «Снижение уровня интерлейкина-1 β и эластазы в десневой борозде у лиц, проходящих противовоспалительное лечение. артрит», Journal of Periodontology , vol. 78, нет. 8, стр. 1612–1619., 2007. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
N. Téllez, N. Aguilera, B. Quiñónez, E. Silva, L. E. González и L. Hernández, «Уровни аргинина и глутамата в жидкости десневой борозды у пациентов с хроническим пародонтитом», Brazilian Dental Журнал , том. 19, нет. 4, стр. 318–322, 2008 г.
Посмотреть по адресу:
Google Scholar
-
Б. Тавебун, П. Лаохапанд, К. Аморнчат и др., «Хост β -фрагменты гена глобина в щелевой жидкости в качестве биомаркера здоровья и заболеваний пародонта», Journal of Periodontal Research , vol.
 45, нет. 1, стр. 38–44, 2010 г.
45, нет. 1, стр. 38–44, 2010 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
M. Yakob, J. Meurman, T. Sorsa и B. Söder, «Treponema denticola ассоциируется с повышенным уровнем MMP-8 и MMP-9 в жидкости десневой борозды», Oral Diseases , vol. . 19, нет. 7, стр. 694–701, 2013.
Просмотр:
Сайт издателя | Google Scholar
-
А. У. Чаудхари, Г. Н. Бякод, П. Ф. Вахмаре и В. М. Кархадкар, «Корреляция уровней интерлейкина-1 β в жидкости десневой борозды с клиническими параметрами хронического периодонтита», , Журнал современной стоматологической практики. , том. 12, нет. 1, стр. 52–59, 2011 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н. Х. Гокхале, А. Б. Ачарья, В.
 С. Патил, Д. Дж. Триведи, С. Сетти и С. Л. Такур, «Уровни резистина в жидкости десневой борозды у пациентов с хроническим пародонтитом и сахарным диабетом 2 типа», Журнал пародонтологии , том. 85, нет. 4, стр. 610–617, 2014.
С. Патил, Д. Дж. Триведи, С. Сетти и С. Л. Такур, «Уровни резистина в жидкости десневой борозды у пациентов с хроническим пародонтитом и сахарным диабетом 2 типа», Журнал пародонтологии , том. 85, нет. 4, стр. 610–617, 2014. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
К. Гокул, «Оценка уровня фактора некроза опухоли в жидкости и сыворотке десневой борозды при здоровье и заболеваниях пародонта: биохимическое исследование», Indian Journal of Dental Research , vol. 23, нет. 3, стр. 348–352, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
М. Гупта, Р. Чатурведи и А. Джейн, «Роль моноцитарного хемоаттрактантного белка-1 (MCP-1) как иммунодиагностического биомаркера в патогенезе хронического пародонтита», Цитокин , об. 61, нет. 3, стр. 892–897, 2013 г.

Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. К. Кумар, Н. Р. Редди, М. Бабу, П. М. Кумар, В. С. Редди и К. В. Чаван, «Оценка уровней простагландина Е 2 в жидкости десневой борозды при здоровье пародонта, заболеваниях и после лечения», Современная клиническая стоматология , том. 4, нет. 3, стр. 303–306, 2013 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Дж. Дж. Куняппу, В. Б. Мэтью, С. Хегде, Р. Кашьяп и Р. Хосадурга, «Оценка уровня щелочной фосфатазы в жидкости десневой борозды как биомаркер для оценки влияния удаления зубного камня и выравнивания корней на хронический периодонтит». : исследование in vivo», Journal of Oral & Manillofacial Pathology , vol. 16, нет. 1, стр. 54–57, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Р.
 Малхотра, В. Гровер, А. Капур и Р. Капур, «Щелочная фосфатаза как маркер заболеваний пародонта», стр. 9.0863 Индийский журнал стоматологических исследований , том. 21, нет. 4, стр. 531–536, 2010.
Малхотра, В. Гровер, А. Капур и Р. Капур, «Щелочная фосфатаза как маркер заболеваний пародонта», стр. 9.0863 Индийский журнал стоматологических исследований , том. 21, нет. 4, стр. 531–536, 2010. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
С. Т. Манойкумар, А. Прадип, Г. Гарг и А. Раджу, «Уровни онкостатина М в жидкости десневой борозды в пародонтальных условиях», Цитокин , том. 50, нет. 3, стр. 248–252, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
S. U. Nayak, D. G. Nayak, A. S. Uppoor и K. K. Pai, «Оценка уровня кортизола в жидкости десневой борозды и слюне у тревожных и нетревожных пациентов с хроническим пародонтитом», Журнал стоматологических исследований , том. 10, нет. 4, с. 474, 2013.
Просмотр по адресу:
Google Scholar
-
С.
 П. Патель, А. Р. Прадип и С. Чоудхри, «Уровни глутатионпероксидазы плазмы (eGPx) в щелевой жидкости при заболеваниях пародонта», Archives of Oral Биология , том. 54, нет. 6, стр. 543–548, 2009 г.
П. Патель, А. Р. Прадип и С. Чоудхри, «Уровни глутатионпероксидазы плазмы (eGPx) в щелевой жидкости при заболеваниях пародонта», Archives of Oral Биология , том. 54, нет. 6, стр. 543–548, 2009 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, Х. Дейзи и П. Хадж, «Уровни моноцитарного хемоаттрактантного белка-1 в жидкости десневой борозды при заболеваниях и здоровье пародонта», Архив устной биологии , том. 54, нет. 5, стр. 503–509, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, Х. Дейзи, П. Хадж, Г. Гарг и М. Торат, «Корреляция уровней интерлейкина-18 жидкости десневой борозды и моноцитарного хемоаттрактантного белка-1 при здоровье и заболевании пародонта», Журнал пародонтологии , том. 80, нет. 9, стр. 1454–1461, 2009.

Посмотреть по адресу:
Сайт издателя | Академия Google
-
А. Р. Прадип, Р. Катария, Н. М. Рагхавендра и А. Шарма, «Уровни пентраксина-3 в жидкости и плазме десневой борозды при здоровье и заболеваниях пародонта», Journal of Periodontology , vol. 82, нет. 5, стр. 734–741, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, М. С. Кумар, М. В. Рамачандрапрасад и К. Шиха, «Уровни неоптерина в десневой борозде у здоровых людей и у пациентов с различными заболеваниями пародонта», Журнал пародонтологии , том. 78, нет. 10, стр. 1962–1967, 2007.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Прадип, Р. С. Манджунат и Р. Катария, «Прогрессирующее заболевание пародонта характеризуется одновременным постепенным повышением уровня жидкости десневой борозды и уровня СРБ в сыворотке», Journal of Investigative and Clinical Dentistry , vol.
 1, нет. 2, стр. 133–138, 2010.
1, нет. 2, стр. 133–138, 2010. Посмотреть по адресу:
Сайт издателя | Академия Google
-
А. Р. Прадип, С. Г. Манджунат, П. П. Свати, К. Шиха и П. Б. Суджата, «Уровни лейкотриена В4 в жидкости десневой борозды при заболеваниях пародонта», Journal of Periodontology , vol. 78, нет. 12, стр. 2325–2330, 2007.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, Д. В. Прапулла, А. Шарма и П. Б. Суджата, «Жидкость десневой борозды и фактор роста эндотелия сосудов сыворотки: их связь со здоровьем пародонта, заболеванием и после лечения», Цитокин , об. 54, нет. 2, стр. 200–204, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, Н. М. Рагхавендра, А.
 Шарма и др., «Связь уровней висфатина в сыворотке и десневой десне со здоровьем пародонта и заболеваниями с сахарным диабетом 2 типа», Journal of Periodontology , vol. 83, нет. 5, стр. 629–634, 2012 г.
Шарма и др., «Связь уровней висфатина в сыворотке и десневой десне со здоровьем пародонта и заболеваниями с сахарным диабетом 2 типа», Journal of Periodontology , vol. 83, нет. 5, стр. 629–634, 2012 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, П. Хадж, С. Чоудхри, С. Патель и Д. Хэппи, «Изучение роли цитокинов Th2: интерлейкина-17 и интерлейкина-18 в здоровье и заболеваниях пародонта», стр. Journal of Oral Science , vol. 51, нет. 2, стр. 261–266, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д. В. Прапулла, П. Б. Суджата и А. Р. Прадип, «Уровни VEGF в жидкости десневой борозды при здоровье и заболеваниях пародонта», Journal of Periodontology , vol. 78, нет. 9, стр. 1783–1787, 2007.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н.
 М. Рагхавендра, А. Р. Прадип, Р. Катария, А. Шарма, Н. С. Рао и С. Б. Наик, «Влияние нехирургической периодонтальной терапии на жидкость десневой борозды и концентрацию висфатина в сыворотке при здоровье и заболевании пародонта», Маркеры заболеваний , vol. 32, нет. 6, стр. 383–388, 2012.
М. Рагхавендра, А. Р. Прадип, Р. Катария, А. Шарма, Н. С. Рао и С. Б. Наик, «Влияние нехирургической периодонтальной терапии на жидкость десневой борозды и концентрацию висфатина в сыворотке при здоровье и заболевании пародонта», Маркеры заболеваний , vol. 32, нет. 6, стр. 383–388, 2012. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
С. Саникоп, С. Патил и П. Агравал, «Щелочная фосфатаза жидкости десневой борозды как потенциальный диагностический маркер заболеваний пародонта», Журнал Индийского общества пародонтологии , том. 16, нет. 4, стр. 513–518, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Шарма, А. Р. Прадип, Н. М. Рагхавендра, П. Арджун и Р. Катария, «Жидкость десневой борозды и уровни цистатина с в сыворотке при заболеваниях и здоровье пародонта», Маркеры заболеваний , vol.
 32, нет. 2, стр. 101–107, 2012 г.
32, нет. 2, стр. 101–107, 2012 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
C.G.D. Sharma and A.R. Pradeep, «Уровни остеопонтина в жидкости десневой борозды при здоровье и заболеваниях пародонта», Journal of Periodontology , vol. 77, нет. 10, стр. 1674–1680, 2006.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
B. Alfant, L. M. Shaddox, J. Tobler, I. Magnusson, I. Aukhil, and C. Walker, «Уровни матриксной металлопротеиназы у детей с агрессивным пародонтитом», стр. Журнал пародонтологии , том. 79, нет. 5, стр. 819–826, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Э. Андерсен, И. М. Дессе, Т. Пернегер и А. Момбелли, «Экспрессия миелоидно-родственного белка (MRP8/14) в жидкости десневой щели при здоровом пародонте, заболеваниях и после лечения», Journal of Пародонтологические исследования , том.
 45, нет. 4, стр. 458–463, 2010.
45, нет. 4, стр. 458–463, 2010. Посмотреть по адресу:
Сайт издателя | Академия Google
-
Э. Балтаджиоглу, Ф. А. Акалин, А. Алвер, О. Дегер и Э. Карабулут, «Уровни карбонила белка в сыворотке и жидкости десневой борозды у пациентов с хроническим пародонтитом», Archives of Oral Biology , vol. 53, нет. 8, стр. 716–722, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
E. Baltacıoğlu, M. A. Kehribar, P. Yuva et al., «Общий оксидантный статус и биомаркеры резорбции кости в сыворотке и жидкости десневой борозды у пациентов с пародонтитом», Журнал пародонтологии , том. 85, нет. 2, стр. 317–326, 2014 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
С. Бесерик, Б. Афакан, В.
 О. Özturk, H. Atmaca и G. Emingil, «Уровни кальпротектина десневой борозды, остеокальцина и сшитых N-концевых телопептидов в норме и при различных заболеваниях пародонта», Disease Markers , vol. 31, нет. 6, стр. 343–352, 2011.
О. Özturk, H. Atmaca и G. Emingil, «Уровни кальпротектина десневой борозды, остеокальцина и сшитых N-концевых телопептидов в норме и при различных заболеваниях пародонта», Disease Markers , vol. 31, нет. 6, стр. 343–352, 2011. Посмотреть по адресу:
Сайт издателя | Академия Google
-
С. Бесерик, В. О. Özturk, H. Atmaca, G. Atilla и G. Emingil, «Жидкость десневой борозды и острофазовые уровни цитокинов в плазме при различных заболеваниях пародонта», Journal of Periodontology , vol. 83, нет. 10, стр. 1304–1313, 2012.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Г. Н. Белибасакис, В.-О. Özturk, G. Emingil и N. Bostanci, «Растворимый триггерный рецептор, экспрессируемый на миелоидных клетках 1 (sTREM-1) в жидкости десневой борозды: связь с клиническими и микробиологическими параметрами», Журнал пародонтологии , том.
 85, нет. 1, стр. 204–210, 2014.
85, нет. 1, стр. 204–210, 2014. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
B. Bıyıkoğlu, N. Buduneli, L. Kardeşler, K. Aksu, M. Pitkala, and T. Sorsa, «Уровни десневой борозды MMP-8 и-13 и TIMP-1 у пациентов с ревматоидным артритом». артрит и воспалительное заболевание пародонта», Journal of Periodontology , vol. 80, нет. 8, стр. 1307–1314, 2009.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Н. Бостанчи, Б. Сайган, Г. Эмингил, Г. Атилла и Г. Н. Белибасакис, «Влияние периодонтального лечения на уровень активатора рецептора NF- κ B лиганда и остеопротегерина и относительное соотношение в жидкости десневой борозды» », Journal of Clinical Periodontology , vol. 38, нет. 5, стр. 428–433, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н.
 Будунели, О. Озчака и А. Налбанцой, «Уровни интерлейкина-33 в жидкости десневой борозды, слюне или плазме не позволяют дифференцировать хронический периодонтит» Журнал пародонтологии , том. 83, нет. 3, стр. 362–368, 2012 г.
Будунели, О. Озчака и А. Налбанцой, «Уровни интерлейкина-33 в жидкости десневой борозды, слюне или плазме не позволяют дифференцировать хронический периодонтит» Журнал пародонтологии , том. 83, нет. 3, стр. 362–368, 2012 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
P. Bullon, B. Goberna, JM Guerrero, JJ Segura, R. Perez-Cano, and A. Martinez-Sahuquillo, «Остеокальцин сыворотки, слюны и жидкости десневой борозды: их связь с пародонтальным статусом и плотность костной ткани у женщин в постменопаузе», Journal of Periodontology , vol. 76, нет. 4, стр. 513–519, 2005.
Просмотр:
Сайт издателя | Google Scholar
-
Ф. О. Б. Корреа, Д. Гонсалвес, К. М. С. Фигередо, А. Густафссон и С. Р. П. Оррико, «Краткосрочная эффективность нехирургического лечения в снижении уровня интерлейкина-1 β и протеаз в десневой борозде».
 жидкости от пациентов с сахарным диабетом 2 типа и хроническим пародонтитом», Journal of Periodontology , vol. 79, нет. 11, стр. 2143–2150, 2008.
жидкости от пациентов с сахарным диабетом 2 типа и хроническим пародонтитом», Journal of Periodontology , vol. 79, нет. 11, стр. 2143–2150, 2008. Посмотреть по адресу:
Сайт издателя | Академия Google
-
R.R. De Oliveira, H.O. Schwartz-Filho, A.B. Novaes Jr. et al., «Противомикробная фотодинамическая терапия при нехирургическом лечении агрессивного периодонтита: цитокиновый профиль в жидкости десневой борозды, предварительные результаты», Journal of Periodontology , том. 80, нет. 1, стр. 98–105, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
G. Emingil, A. Gürkan, G. Atilla и A. Kantarci, «Субантимикробные дозы доксициклина и уровни цитокинов-хемокинов в жидкости десневой борозды», Журнал пародонтологии , том. 82, нет. 3, стр. 452–461, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
G.
 Emingil, B. Han, G. Özdemir et al., «Влияние азитромицина в качестве дополнения к нехирургическому пародонтологическому лечению на микробиологические параметры и биомаркеры жидкости десневой борозды при генерализованном агрессивном пародонтите», Journal пародонтологических исследований , том. 47, нет. 6, стр. 729–739, 2012.
Emingil, B. Han, G. Özdemir et al., «Влияние азитромицина в качестве дополнения к нехирургическому пародонтологическому лечению на микробиологические параметры и биомаркеры жидкости десневой борозды при генерализованном агрессивном пародонтите», Journal пародонтологических исследований , том. 47, нет. 6, стр. 729–739, 2012. Просмотр:
Сайт издателя | Google Scholar
-
А. С. Эртугрул, Х. Сахин, А. Дикилитас, Н. Алпаслан и А. Бозоглан, «Сравнение CCL28, интерлейкина-8, интерлейкина-1 β и фактора некроза опухоли-альфа у субъектов с гингивит, хронический пародонтит и генерализованный агрессивный пародонтит», Journal of Periodontal Research , vol. 48, нет. 1, стр. 44–51, 2013 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
T. Fiorini, C. Susin, JM Da Rocha et al.
 , «Влияние нехирургической пародонтальной терапии на уровни цитокинов в сыворотке и жидкости десневой борозды во время беременности и после родов», Journal of Periodontal Research , vol. 48, нет. 1, стр. 126–133, 2013 г.
, «Влияние нехирургической пародонтальной терапии на уровни цитокинов в сыворотке и жидкости десневой борозды во время беременности и после родов», Journal of Periodontal Research , vol. 48, нет. 1, стр. 126–133, 2013 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ю. Фуджита, Х. Ито, С. Секино и Ю. Нумабе, «Корреляции между уровнями пентраксина 3 или цитокинов в жидкости десневой борозды и клиническими параметрами хронического периодонтита», Стоматология , том. 100, нет. 2, стр. 215–221, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н. Галлаб, Э. Хамди и О. Шейкер, «Уровни малонового диальдегида, супероксиддисмутазы и мелатонина в жидкости десневой борозды у пациентов с агрессивным и хроническим пародонтитом», , Австралийский стоматологический журнал, , том.
 61, нет. 1, стр. 53–61, 2016 г.
61, нет. 1, стр. 53–61, 2016 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
P. F. Goncalves, H. Huang, S. McAninley et al., «Пародонтологическое лечение снижает уровень матриксной металлопротеиназы при локализованном агрессивном пародонтите», Журнал пародонтологии , том. 84, нет. 12, стр. 1801–1808, 2013.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д.-Х. Хан, Х.-С. Шин, Д. Пэк и Х.-Д. Ким, «Уровни матриксных металлопротеиназ в жидкости десневой борозды в поперечном сечении, связанные с пародонтитом и метаболическим синдромом у корейцев», Journal of Clinical Periodontology , vol. 39, нет. 12, стр. 1125–1131, 2012.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
M.
 Hernandez, M.A. Valenzuela, C. Lopez-Otin et al., «Матричная металлопротеиназа-13 сильно выражена в деструктивной активности заболеваний пародонта», Journal of Periodontology , vol. 77, нет. 11, стр. 1863–1870, 2006.
Hernandez, M.A. Valenzuela, C. Lopez-Otin et al., «Матричная металлопротеиназа-13 сильно выражена в деструктивной активности заболеваний пародонта», Journal of Periodontology , vol. 77, нет. 11, стр. 1863–1870, 2006. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Г. С. Химани, М. Л. В. Прабхуджи и Б. В. Картикеян, «Жидкость десневой борозды и концентрация интерлейкина-23 у системно здоровых субъектов: их взаимосвязь со здоровьем и заболеванием пародонта», Journal of Periodontal Research , vol. 49, нет. 2, стр. 237–245, 2014 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
I. Ikezawa, H. Tai, Y. Shimada, Y. Komatsu, JC Galicia и H. Yoshie, «Дисбаланс между растворимыми рецепторами фактора некроза опухоли типа 1 и 2 при хроническом пародонтите», Journal of Клиническая пародонтология , том.
 32, нет. 10, стр. 1047–1054, 2005.
32, нет. 10, стр. 1047–1054, 2005. Посмотреть по адресу:
Сайт издателя | Академия Google
-
Н. Калра, А. Р. Прадип, Н. Приянка и М. Кумари, «Ассоциация фактора стволовых клеток и концентраций высокочувствительного С-реактивного белка в десневой жидкости и сыворотке у пациентов с хроническим периодонтитом с диабетом 2 типа и без него». », Journal of Oral Science , vol. 55, нет. 1, стр. 57–62, 2013 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д. Канер, Ж.-П. Бернимулин, Т. Дитрих, Б.-М. Kleber и A. Friedmann, «Уровни кальпротектина в жидкости десневой борозды предсказывают активность заболевания у пациентов, получающих лечение по поводу генерализованного агрессивного пародонтита», Journal of Periodontal Research , vol. 46, нет. 4, стр. 417–426, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д.
 Канер, Ж.-П. Бернимулин, Б.-М. Kleber, WR Heizmann и A. Friedmann, «Уровни кальпротектина и миелопероксидазы в жидкости десневой борозды во время терапии генерализованного агрессивного периодонтита», Journal of Periodontal Research , vol. 41, нет. 2, стр. 132–139, 2006 г.
Канер, Ж.-П. Бернимулин, Б.-М. Kleber, WR Heizmann и A. Friedmann, «Уровни кальпротектина и миелопероксидазы в жидкости десневой борозды во время терапии генерализованного агрессивного периодонтита», Journal of Periodontal Research , vol. 41, нет. 2, стр. 132–139, 2006 г. Посмотреть по адресу:
Сайт издателя | Академия Google
-
Г. К. Келес, Б. О. Четинкая, И. Исилдак, Х. Копрулу и Г. Ацикгоз, «Уровни фактора активации тромбоцитов в жидкости десневой щели после периодонтальной хирургической терапии», Journal of Periodontal Research , vol. 41, нет. 6, стр. 513–518, 2006 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
S. Khongkhunthian, P. Kongtawelert, S. Ongchai et al., «Сравнения между двумя биохимическими маркерами при оценке тяжести заболеваний пародонта: поперечное исследование», BMC Oral Health , vol.
 14, нет. 1, статья 107, 2014.
14, нет. 1, статья 107, 2014. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
S. Khongkhunthian, N. Srimueang, S. Krisanaprakornkit, K. Pattanaporn, S. Ong-Chai и P. Kongtawelert, «Повышенные уровни эпитопа хондроитинсульфата WF6 в жидкости десневой борозды при хроническом пародонтите», Журнал клинической пародонтологии , том. 35, нет. 10, стр. 871–876, 2008 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Кинни Дж. С., Морелли Т., Ох М. и др., «Биомаркеры щелевой жидкости и прогрессирование заболеваний пародонта», Journal of Clinical Periodontology , vol. 41, нет. 2, стр. 113–120, 2014 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Ł. Konopka, A. Pietrzak и E.
 Brzezińska-Błaszczyk, «Влияние скейлинга и полировки корня на уровни интерлейкина-1 β , интерлейкина-8 и MMP-8 в жидкости десневой борозды у пациентов с хроническим периодонтитом», Journal of Periodontal Research , vol. 47, нет. 6, стр. 681–688, 2012.
Brzezińska-Błaszczyk, «Влияние скейлинга и полировки корня на уровни интерлейкина-1 β , интерлейкина-8 и MMP-8 в жидкости десневой борозды у пациентов с хроническим периодонтитом», Journal of Periodontal Research , vol. 47, нет. 6, стр. 681–688, 2012. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
M. Kraft-Neumärker, K. Lorenz, R. Koch et al., «Полноротовой профиль активного MMP-8 у пациентов с пародонтитом», Journal of Periodontal Research , vol. 47, нет. 1, стр. 121–128, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
М. Кумари, А. Прадип, Н. Приянка, Н. Калра и С. Б. Найк, «Уровни щелевого и сывороточного моноцитарного хемоаттрактантного белка-4 и высокочувствительного С-реактивного белка при здоровье и заболеваниях пародонта». », Архив устной биологии , том.
 59, нет. 6, стр. 645–653, 2014.
59, нет. 6, стр. 645–653, 2014. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
B. Kurtiş, G. Tüter, M. Serdar et al., «Уровни в десневой борозде моноцитарного хемоаттрактантного белка-1 и фактора некроза опухоли-альфа у пациентов с хроническим и агрессивным пародонтитом», Journal of Пародонтология , вып. 76, нет. 11, стр. 1849–1855, 2005.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Б. Куртиш, Г. Тютер, М. Сердар, С. Пинар, И. Демирель и У. Тойман, «Уровни простагландина Е2 и реактивного вещества тиобарбитуровой кислоты в жидкости десневой борозды у курильщиков и некурящих с хроническим пародонтитом». после пародонтальной терапии фазы I и дополнительного применения флурбипрофена», Journal of Periodontology , vol. 78, нет. 1, стр. 104–111, 2007 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
J.
 M. Leppilahti, M. A. Kallio, T. Tervahartiala, T. Sorsa и P. Mäntylä, «Уровни матриксной металлопротеиназы-8 десневой борозды предсказывают исход лечения у курильщиков с хроническим пародонтитом», Журнал пародонтологии , том. 85, нет. 2, стр. 250–260, 2014.
M. Leppilahti, M. A. Kallio, T. Tervahartiala, T. Sorsa и P. Mäntylä, «Уровни матриксной металлопротеиназы-8 десневой борозды предсказывают исход лечения у курильщиков с хроническим пародонтитом», Журнал пародонтологии , том. 85, нет. 2, стр. 250–260, 2014. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Дж. М. Леппилахти, П. А. Эрнандес-Риос, Дж. А. Гамонал и др., «Матричные металлопротеиназы и миелопероксидаза в жидкости десневой борозды обеспечивают специфическую диагностическую ценность для хронического пародонтита», Journal of Clinical Periodontology , vol. 41, нет. 4, стр. 348–356, 2014.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
K. Liu, H. Meng, R. Lu et al., «Начальная пародонтальная терапия снижает системное и местное 25-гидроксивитамин D3 и интерлейкин-1 β у пациентов с агрессивным пародонтитом», Journal of Periodontology , том.
 81, нет. 2, стр. 260–266, 2010.
81, нет. 2, стр. 260–266, 2010. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
E. E. Machtei и M. N. Younis, «Использование 2 схем антибиотикотерапии при агрессивном пародонтите: сравнение изменений клинических параметров и биомаркеров жидкости десневой борозды», Quintessence International , vol. 39, нет. 10, pp. 811–819, 2008.
Просмотр по адресу:
Google Scholar
-
уровни при хроническом пародонтите», Journal of Clinical Periodontology , vol. 41, нет. 3, стр. 252–261, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
P. Mäntylä, M. Stenman, D. Kinane et al., «Мониторинг состояния заболеваний пародонта у курильщиков и некурящих с использованием теста в присутствии пациента, специфичного для матрикса жидкости десневой борозды на металлопротеиназу-8», стр.
 Journal of Periodontal Research , vol. 41, нет. 6, стр. 503–512, 2006 г.
Journal of Periodontal Research , vol. 41, нет. 6, стр. 503–512, 2006 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
A.M. Marcaccini, C.A. Meschiari, L.R. Zuardi et al., «Уровни десневой борозды MMP-8, MMP-9, TIMP-2 и MPO снижаются после периодонтальной терапии», Journal of Clinical Periodontology , том. 37, нет. 2, стр. 180–190, 2010.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
М. Т. С. МакКрудден, Д. Ф. Орр, Ю. Ю и др., «LL-37 в здоровье и заболеваниях пародонта и его восприимчивость к деградации протеиназами, присутствующими в жидкости десневой борозды», Journal of Clinical Periodontology , vol. 40, нет. 10, стр. 933–941, 2013 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
A.
 P. De Lima Oliveira, M. De Faveri, L. C. Gursky et al., «Влияние периодонтальной терапии на цитокины GCF у субъектов с генерализованным агрессивным пародонтитом», Журнал клинической пародонтологии , том. 39, нет. 3, стр. 295–302, 2012 г.
P. De Lima Oliveira, M. De Faveri, L. C. Gursky et al., «Влияние периодонтальной терапии на цитокины GCF у субъектов с генерализованным агрессивным пародонтитом», Журнал клинической пародонтологии , том. 39, нет. 3, стр. 295–302, 2012 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ф. О. Dede, F. O. Özden и B. Avci, «Уровни 8-гидроксидезоксигуанозина в жидкости десневой борозды и слюне у пациентов с хроническим пародонтитом после начального пародонтологического лечения», Journal of Periodontology , vol. 84, нет. 6, стр. 821–828, 2013.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
E. Papathanasiou, F. Teles, T. Griffin et al., «Уровни интерферона- γ в десневой борозде, но не интерлейкина-4 или -33 или стромального лимфопоэтина тимуса, повышены в воспаленных участках у пациентов с заболеваниями пародонта», Journal of Periodontal Research , vol.
 49, нет. 1, стр. 55–61, 2014 г.
49, нет. 1, стр. 55–61, 2014 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
G. Perinetti, M. Paolantonio, B. Femminella, E. Serra и G. Spoto, «Активность щелочной фосфатазы жидкости десневой борозды отражает фазы заживления пародонта/рецидивирующего воспаления у пациентов с хроническим пародонтитом», Журнал пародонтологии , том. 79, нет. 7, стр. 1200–1207, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
R. Pourabbas, A. Kashefimehr, N. Rahmanpour et al., «Влияние фотодинамической терапии на клинические и десневые борозды воспалительных биомаркеров при хроническом пародонтите: рандомизированное клиническое исследование с разделением рта», Journal of Пародонтология , вып. 85, нет. 9, стр. 1222–1229, 2014.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
А.
 Р. Прадип, Н. М. Рагхавендра, М. В. Р. Прасад, Р. Катария, С. П. Патель и А. Шарма, «Концентрация десневой борозды и висфатина в сыворотке: их связь со здоровьем и заболеванием пародонта», Journal of Periodontology , vol. . 82, нет. 9, стр. 1314–1319, 2011.
Р. Прадип, Н. М. Рагхавендра, М. В. Р. Прасад, Р. Катария, С. П. Патель и А. Шарма, «Концентрация десневой борозды и висфатина в сыворотке: их связь со здоровьем и заболеванием пародонта», Journal of Periodontology , vol. . 82, нет. 9, стр. 1314–1319, 2011. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Р. Прадип, Н. С. Рао, П. Баджадж и Э. Агарвал, «8-изопростан: продукт перекисного окисления липидов в жидкости десневой борозды у здоровых людей, страдающих гингивитом и хроническим периодонтитом», Архив устной биологии , том. 58, нет. 5, стр. 500–504, 2013 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н. Приянка, М. Кумари, Н. Калра, П. Арджун, С. Б. Найк и А. Р. Прадип, «Концентрация програнулина в щелевой жидкости и сыворотке и высокочувствительный СРБ при хроническом пародонтите и диабете 2 типа».
 Маркеры заболеваний , vol. 35, нет. 5, стр. 389–394, 2013 г.
Маркеры заболеваний , vol. 35, нет. 5, стр. 389–394, 2013 г. Посмотреть по адресу:
Сайт издателя | Академия Google
-
Б. Рай, Дж. Каур, Р. Джейн и С. К. Ананд, «Уровни десневой щелевой металлопротеиназы-8 и -9 при пародонтите», The Saudi Dental Journal , vol. 22, нет. 3, стр. 129–131, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Б. Рай, С. Харб, Р. Джейн и С. К. Ананд, «Биомаркеры периодонтита в жидкостях полости рта», Journal of Oral Science , vol. 50, нет. 1, стр. 53–56, 2008.
Просмотр:
Сайт издателя | Google Scholar
-
Р. А. Рейнхардт, Дж. А. Стоунер, Л. М. Голуб и др., «Ассоциация биомаркеров жидкости десневой борозды во время обслуживания пародонта с последующим прогрессирующим пародонтитом», Journal of Periodontology , vol.
 81, нет. 2, стр. 251–259, 2010.
81, нет. 2, стр. 251–259, 2010. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
C. Reis, A.V. Da Costa, J.T. Guimarães et al., «Клиническое улучшение после терапии периодонтита: связь со снижением IL-1 и IL-6», Экспериментальная и терапевтическая медицина , том. 8, нет. 1, стр. 323–327, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
W. Rosalem, B. Rescala, R.P. Teles, R.G. Fischer, A. Gustafsson и C.M. Figueredo, «Влияние нехирургического лечения на хронический и агрессивный периодонтит: клинические, иммунологические и микробиологические данные». Журнал пародонтологии , том. 82, нет. 7, стр. 979–989, 2011.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
G.
 E. Salvi, L. M. Franco, TM Braun et al., «Провоспалительные биомаркеры при экспериментальном гингивите у пациентов с сахарным диабетом 1 типа: исследование, подтверждающее концепцию», Journal of Clinical Periodontology , vol. 37, нет. 1, стр. 9–16, 2010 г.
E. Salvi, L. M. Franco, TM Braun et al., «Провоспалительные биомаркеры при экспериментальном гингивите у пациентов с сахарным диабетом 1 типа: исследование, подтверждающее концепцию», Journal of Clinical Periodontology , vol. 37, нет. 1, стр. 9–16, 2010 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
В. Р. Сантос, Ф. В. Рибейро, Дж. А. Лима и др., «Частичное и полное удаление зубного камня и выравнивание корней у пациентов с диабетом 2 типа: 12-месячное наблюдение за клиническими параметрами и уровнями цитокинов и факторы, связанные с остеокластогенезом», Journal of Periodontal Research , vol. 47, нет. 1, стр. 45–54, 2012 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ф. Сарлати, М. Саттари, С. Раззаги и М. Насири, «Активатор рецепторов лиганда ядерного фактора κ B и уровни остеопротегерина в жидкости десневой борозды», Dental Research Journal , vol.
 . 9, нет. 6, pp. 752–757, 2012.
. 9, нет. 6, pp. 752–757, 2012. Посмотреть по адресу:
Google Scholar
-
Т. Сорса, М. Эрнандес, Дж. Леппилахти, С. Мунджал, Л. Нетушил и П. жидкости десневой борозды ММР-8 с помощью различных лабораторных и амбулаторных методов» Болезни полости рта , vol. 16, нет. 1, стр. 39–45, 2010 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Т. Х. Танг, Т. Р. Фитцсиммонс и П. М. Бартольд, «Влияние курения на концентрации рецепторного активатора лиганда ядерного фактора κ B и остеопротегерина в жидкости десневой борозды человека», Журнал клинической пародонтологии, том . . 36, нет. 9, стр. 713–718, 2009 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
Р. Телес, Д. Сакеллари, Ф.
 Телес и др., «Взаимосвязи между биомаркерами жидкости десневой борозды, клиническими параметрами заболеваний пародонта и поддесневой микробиотой», Journal of Periodontology , vol. 81, нет. 1, стр. 89–98, 2010.
Телес и др., «Взаимосвязи между биомаркерами жидкости десневой борозды, клиническими параметрами заболеваний пародонта и поддесневой микробиотой», Journal of Periodontology , vol. 81, нет. 1, стр. 89–98, 2010. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Р. П. Телес, Л. С. Гурски, М. Фавери и др., «Взаимосвязи между поддесневой микробиотой и биомаркерами GCF при генерализованном агрессивном пародонтите», Журнал клинической пародонтологии , том. 37, нет. 4, стр. 313–323, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Х. Токер, А. Акпынар, Х. Айдын и О. Пойраз, «Влияние курения на уровень интерлейкина-1бета, оксидантный статус и антиоксидантный статус в жидкости десневой борозды у пациентов с хроническим пародонтитом до и после пародонтита. лечение», Journal of Periodontal Research , vol.
 47, нет. 5, стр. 572–577, 2012.
47, нет. 5, стр. 572–577, 2012. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Г. Тютер, Б. Куртис и М. Сердар, «Оценка жидкости десневой борозды и уровня высокочувствительного С-реактивного белка в сыворотке у пациентов с хроническим пародонтитом с ишемической болезнью сердца или без нее», Журнал пародонтологии , вып. 78, нет. 12, стр. 2319–2324, 2007.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
К. Д. Тимкив, Д. Х. Танелл, Г. К. Джонсон и др., «Влияние курения на цитокины жидкости десневой борозды при тяжелом хроническом пародонтите», Журнал клинической пародонтологии , том. 38, нет. 3, стр. 219–228, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
A.
 E. Ülker, Ö. Тулуноглу, Н. Озмерикер, М. Кан и С. Демиртас, «Оценка уровней цистатина С, IL-I β и TNF- α в общей слюне и жидкости десневой борозды в возрасте от 11 до 16 лет». -старые дети», Journal of Periodontology , vol. 79, нет. 5, стр. 854–860, 2008.
E. Ülker, Ö. Тулуноглу, Н. Озмерикер, М. Кан и С. Демиртас, «Оценка уровней цистатина С, IL-I β и TNF- α в общей слюне и жидкости десневой борозды в возрасте от 11 до 16 лет». -старые дети», Journal of Periodontology , vol. 79, нет. 5, стр. 854–860, 2008. Просмотр:
Сайт издателя | Google Scholar
-
F.V. Ribeiro, A.C. De Mendoncxa, V.R. Santos, MF Bastos, L.C. Figueiredo, P.M. Duarte, «Цитокины и связанные с костями факторы у системно здоровых пациентов с хроническим пародонтитом и пациентов с диабетом 2 типа и хроническим пародонтитом, Journal of Periodontology , vol. 82, нет. 8, стр. 1187–1196, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Н. Будунели и Д. Ф. Кинане, «Диагностические маркеры хозяина, связанные с разрушением мягких тканей и деградацией кости при пародонтите», Журнал клинической пародонтологии , том.
 38, нет. 11, стр. 85–105, 2011.
38, нет. 11, стр. 85–105, 2011. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Дж. М. Леппилахти, Т. Сорса, М. А. Каллио и др., «Полезность моделей реакции матрикса десневой жидкости десневой борозды на металлопротеиназу-8 в прогнозировании результатов клинического лечения на уровне участка», Journal of Periodontology , vol. . 86, нет. 6, стр. 777–787, 2015.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
A. M. Heikkinen, S. O. Nwhator, N. Rathnayake, P. Mäntylä, P. Vatanen, and T. Sorsa, «Пилотное исследование состояния здоровья полости рта, оцениваемое с помощью теста с ополаскивателем для полости рта с активной матриксной металлопротеиназой-8 у подростков», Журнал пародонтологии , том. 87, нет. 1, стр. 36–40, 2016 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Дж.
 И. Салонен и К. У. Паунио, «Метод внутрищелевой промывки для сбора содержимого борозды», Скандинавский журнал стоматологических исследований , том. 99, нет. 5, стр. 406–412, 1991.
И. Салонен и К. У. Паунио, «Метод внутрищелевой промывки для сбора содержимого борозды», Скандинавский журнал стоматологических исследований , том. 99, нет. 5, стр. 406–412, 1991. Посмотреть по адресу:
Google Scholar
-
Г. С. Гриффитс, «Формирование, сбор и значение жидкости десневой борозды», Пародонтология, 2000, , том. 31, стр. 32–42, 2003 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
A. Guentsch, M. Kramesberger, A. Sroka, W. Pfister, J. Potempa и S. Eick, «Сравнение методов забора жидкости из десневой борозды у пациентов с тяжелым хроническим периодонтитом», Журнал пародонтологии , том. 82, нет. 7, стр. 1051–1060, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ю.
 Шимада, К. Табета, Н. Сугита и Х. Йоши, «Профилирование биомаркеров в жидкости десневой борозды с использованием мультиплексного иммуноанализа с шариками», Archives of Oral Biology , vol. 58, нет. 6, стр. 724–730, 2013.
Шимада, К. Табета, Н. Сугита и Х. Йоши, «Профилирование биомаркеров в жидкости десневой борозды с использованием мультиплексного иммуноанализа с шариками», Archives of Oral Biology , vol. 58, нет. 6, стр. 724–730, 2013. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
И. Бакри, К. В. И. Дуглас и А. Роулинсон, «Влияние стресса на пародонтологическое лечение: лонгитюдное исследование с использованием клинических и биологических маркеров», Журнал клинической пародонтологии , том. 40, нет. 10, стр. 955–961, 2013.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
В. Бут, С. Янг, А. Крачли, Н. С. Тайчман и Э. Палеолог, «Фактор роста эндотелия сосудов при заболеваниях пародонта у человека», Journal of Periodontal Research , vol. 33, нет. 8, pp. 491–499, 1998.
Просмотр по адресу:
Google Scholar
-
L.
 Jin, C. Yu и E. F. Corbet, «Эластазная активность гранулоцитов в статической и текучей жидкости десневой борозды», Journal of Periodontal Research , vol. 38, нет. 3, стр. 303–310, 2003.
Jin, C. Yu и E. F. Corbet, «Эластазная активность гранулоцитов в статической и текучей жидкости десневой борозды», Journal of Periodontal Research , vol. 38, нет. 3, стр. 303–310, 2003. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
К. Т. Смит, Г. С. Ау, П. Л. Фриз, Дж. Б. Осборн и Дж. Л. Столтенберг, «Пять параметров жидкости десневой борозды с восьми поверхностей при заболеваниях пародонта», Journal of Periodontal Research , vol. 27, нет. 5, стр. 466–475, 1992.
Посмотреть по адресу:
Сайт издателя | Академия Google
-
B.L. Pihlstrom, «Оценка пародонтального риска, диагностика и планирование лечения», Periodontology 2000 , vol. 25, нет. 1, стр. 37–58, 2001.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Л.
 Луо, П. Се, П. Гонг, X.-Х. Тан, Ю. Дин и Л.-С. Денг, «Экспрессия HMGB1 и HMGN2 в тканях десны, GCF и PICF у пациентов с пародонтитом и периимплантитом», Archives of Oral Biology , vol. 56, нет. 10, стр. 1106–1111, 2011.
Луо, П. Се, П. Гонг, X.-Х. Тан, Ю. Дин и Л.-С. Денг, «Экспрессия HMGB1 и HMGN2 в тканях десны, GCF и PICF у пациентов с пародонтитом и периимплантитом», Archives of Oral Biology , vol. 56, нет. 10, стр. 1106–1111, 2011. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
W. A. Colburn, VG DeGruttola, D.L. DeMets et al., «Биомаркеры и суррогатные конечные точки: предпочтительные определения и концептуальная основа», Clinical Pharmacology & Therapeutics , vol. 69, нет. 3, стр. 89–95, 2001.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
К. Стримбу и Дж. А. Тавел, «Что такое биомаркеры?» Текущее мнение о ВИЧ и СПИДе , том. 5, нет. 6, стр. 463–466, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
T.
 Sorsa, L. Tjäderhane, YT Konttinen et al., «Матричные металлопротеиназы: вклад в патогенез, диагностику и лечение периодонтального воспаления», Annals of Medicine , vol. 38, нет. 5, стр. 306–321, 2006 г.
Sorsa, L. Tjäderhane, YT Konttinen et al., «Матричные металлопротеиназы: вклад в патогенез, диагностику и лечение периодонтального воспаления», Annals of Medicine , vol. 38, нет. 5, стр. 306–321, 2006 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
T. Sorsa, U.K. Gursoy, S. Nwhator et al., «Анализ матриксных металлопротеиназ, особенно MMP-8, в жидкости десневой борозды, жидкости для полоскания рта и слюне для мониторинга заболеваний пародонта», Пародонтология 2000 , вып. 70, нет. 1, стр. 142–163, 2016 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Д. Ф. Кинане, И. Б. Дарби, С. Саид и др., «Изменения уровней металлопротеиназы-8 матрикса жидкости десневой борозды во время периодонтального лечения и обслуживания», Journal of Periodontal Research , vol.
 38, нет. 4, стр. 400–404, 2003 г.
38, нет. 4, стр. 400–404, 2003 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
C. M. S. Figueredo, A. Areas, L. A. Miranda, R. G. Fischer и A. Gustafsson, «Краткосрочная эффективность нехирургического лечения в снижении активности протеазы в жидкости десневой борозды у пациентов с хроническим периодонтитом», Журнал клинической пародонтологии , том. 31, нет. 8, стр. 615–619, 2004 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Ф. Х. Ночити, М. З. Казати и П. М. Дуарте, «Современный взгляд на влияние курения на прогрессирование и лечение пародонтита», Пародонтология, 2000, , том. 67, нет. 1, стр. 187–210, 2015.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Дж.
 Дж. Тейлор, П. М. Прешоу и Э. Лалла, «Обзор данных о патогенных механизмах, которые могут связывать периодонтит и диабет», Журнал клинической пародонтологии , том. 40, приложение 14, стр. S113–S134, 2013 г.
Дж. Тейлор, П. М. Прешоу и Э. Лалла, «Обзор данных о патогенных механизмах, которые могут связывать периодонтит и диабет», Журнал клинической пародонтологии , том. 40, приложение 14, стр. S113–S134, 2013 г. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
P. Dandona, A. Aljada и A. Bandyopadhyay, «Воспаление: связь между резистентностью к инсулину, ожирением и диабетом», Trends in Immunology , vol. 25, нет. 1, стр. 4–7, 2004 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
S. P. Engebretson, J. Hey-Hadavi, F. J. Ehrhardt et al., «Уровни интерлейкина-1 в жидкости десневой борозды β и контроль гликемии у пациентов с хроническим пародонтитом и диабетом 2 типа», Journal of Periodontology , vol. 75, нет. 9, стр. 1203–1208, 2004.
Посмотреть по адресу:
Сайт издателя | Google Scholar
-
Г.
 Э. Сальви, Дж. Г. Коллинз, Б. Ялда, Р. Р. Арнольд, Н. П. Ланг и С. Оффенбахер, «Моноцитарные модели секреции TNF α у пациентов с ИЗСД с заболеваниями пародонта», Journal of Clinical Periodontology , об. 24, нет. 1, стр. 8–16, 19.97.
Э. Сальви, Дж. Г. Коллинз, Б. Ялда, Р. Р. Арнольд, Н. П. Ланг и С. Оффенбахер, «Моноцитарные модели секреции TNF α у пациентов с ИЗСД с заболеваниями пародонта», Journal of Clinical Periodontology , об. 24, нет. 1, стр. 8–16, 19.97. Посмотреть по адресу:
Сайт издателя | Google Scholar
-
А. Салминен, У. К. Гурсой, С. Паджу и др., «Слюнные биомаркеры бактериальной нагрузки, воспалительной реакции и разрушения тканей при пародонтите», Журнал клинической пародонтологии , том. 41, нет. 5, стр. 442–450, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Copyright
Copyright © 2016 Zeyad Nazar Majeed et al. Это статья с открытым доступом, распространяемая в соответствии с лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.

Устойчивость и сопротивляемость экспериментальному гингивиту: систематический обзорный обзор | BMC Oral Health
- Исследовательская статья
- Открытый доступ
- Опубликовано:
- Чарифа Земури 1 ,
- Николас С. Якубович 2 ,
- Вим Криелаард 1 ,
- Egija Zaura 1 ,
- Michael Dodds 3 ,
- Bettina Schelkle 4 &
- …
- Bruno G. Loos 5
BMC Здоровье полости рта том 19 , Номер статьи: 212 (2019) Процитировать эту статью
-
2823 доступа
-
10 цитирований
-
4 Альтметрика
-
Сведения о показателях
Резюме
Исходная информация
Этот систематический предварительный обзор был направлен на выявление изменений в биомаркерах микробиологического, иммунологического и биохимического происхождения во время экспериментальных исследований гингивита (ЭГ), которые могут указывать на резистентность и резистентность.

Methods
Термин «экспериментальный гингивит» использовался в PubMed с момента создания до 11 апреля 2018 г. Из 411 извлеченных исследований 22 исследования были включены в этот обзор.
Результаты
Были включены исследования, сообщающие данные об изменениях биомаркеров во время и после исследования ЭГ с полным ртом. В двух исследованиях сообщалось об изменениях биомаркеров микробиологического происхождения, в 12 — иммунологического и в восьми — биохимического происхождения. Сообщалось об изменениях в фазе индукции, а иногда и в фазе разрешения. Микробиологический состав как наддесневых, так и поддесневых зубных отложений в ходе ЭГ менялся в более патогенную сторону, но возвращался к более нормальному составу. Это указывает на устойчивость микробиома полости рта. Для иммунологических биомаркеров было сложно получить надежную картину изменений в нескольких исследованиях. IL-1β и IL-6 в слюне и жидкости десневой борозды повышались во время фазы индукции и возвращались в фазе разрешения ниже исходных значений.
 Биохимические параметры цистатина-SN, цистатина-S и лактоферрина в слюне были повышены в конце фазы индукции, однако и здесь не было выявлено четкой закономерности на основании всех доступных исследований.
Биохимические параметры цистатина-SN, цистатина-S и лактоферрина в слюне были повышены в конце фазы индукции, однако и здесь не было выявлено четкой закономерности на основании всех доступных исследований. Выводы
Необходимы дополнительные исследования, чтобы выяснить, какие микробиологические, иммунологические и биохимические биомаркеры могут быть полезны для будущих исследований резистентности и устойчивости полости рта к экспериментальному гингивиту.
Отчеты экспертной оценки
История вопроса
Накопление зубного налета и реакция десен на отсутствие гигиены полости рта варьируются от человека к человеку [1]. Однако при восстановлении практики гигиены полости рта значения индекса зубного налета и десневого индекса быстро снижаются, что указывает на обратимый механизм воспаления десны. Наиболее часто используемым продольным дизайном для моделирования ранних фаз воспаления десен является протокол экспериментального гингивита (ЭГ), первоначально разработанный Löe et al.
Рис. чтобы продемонстрировать, что накопление зубного налета de novo было связано с развитием гингивита [1]. Участников попросили воздержаться от любой формы гигиены полости рта, чтобы вызвать накопление зубного налета, пока не возникнет воспаление десен. Сроки развития гингивита варьировали от 10 до 21 дня. После этого были разработаны различные протоколы с добавлением вмешательства или досудебной фазы. Эта фаза обычно состоит из профессиональной профилактики для достижения нулевого воспаления тканей десны, чтобы можно было изучить только последствия накопления зубного налета. В конечном итоге фаза индукции завершилась профессиональной профилактикой для восстановления здоровья десен. Показав, что удаление зубного налета устраняет воспаление десен, были получены убедительные доказательства того, что зубной налет вызывает гингивит [1]. Недавнее исследование показало незначительное воспаление и отсутствие красного флуоресцентного налета у некоторых участников во время исследования ЭГ, в то время как у других участников был обнаружен высокий уровень зубного налета и воспаления десен [2].
чтобы продемонстрировать, что накопление зубного налета de novo было связано с развитием гингивита [1]. Участников попросили воздержаться от любой формы гигиены полости рта, чтобы вызвать накопление зубного налета, пока не возникнет воспаление десен. Сроки развития гингивита варьировали от 10 до 21 дня. После этого были разработаны различные протоколы с добавлением вмешательства или досудебной фазы. Эта фаза обычно состоит из профессиональной профилактики для достижения нулевого воспаления тканей десны, чтобы можно было изучить только последствия накопления зубного налета. В конечном итоге фаза индукции завершилась профессиональной профилактикой для восстановления здоровья десен. Показав, что удаление зубного налета устраняет воспаление десен, были получены убедительные доказательства того, что зубной налет вызывает гингивит [1]. Недавнее исследование показало незначительное воспаление и отсутствие красного флуоресцентного налета у некоторых участников во время исследования ЭГ, в то время как у других участников был обнаружен высокий уровень зубного налета и воспаления десен [2]. В этом исследовании такие субъекты называются соответственно сильно или слабо реагирующими на воздействие. Субъекты могут иметь высокую устойчивость к возмущениям или ЭГ, при которых в экосистеме полости рта происходят незначительные изменения, поэтому восстановление после испытания будет незначительным. Низкое сопротивление означает, что воздействие на экосистему велико (рис. 1). Устойчивость определяется как свойство экосистемы полости рта восстанавливаться до исходного состояния [3]. В испытании ЭГ участники могут иметь высокую (полную) или низкую (неполную) устойчивость после эксперимента (рис. 1). Факторы, связанные с устойчивостью ткани пародонта/десны к возмущающим факторам, могут включать генетику и/или факторы образа жизни, такие как курение, диета и психосоциальные факторы [4]. В случае ЭГ ранее существовавший воспалительный статус и состояние полости рта в целом на досудебном этапе могли повлиять на исход исследования и, таким образом, определить резильентность [5].
В этом исследовании такие субъекты называются соответственно сильно или слабо реагирующими на воздействие. Субъекты могут иметь высокую устойчивость к возмущениям или ЭГ, при которых в экосистеме полости рта происходят незначительные изменения, поэтому восстановление после испытания будет незначительным. Низкое сопротивление означает, что воздействие на экосистему велико (рис. 1). Устойчивость определяется как свойство экосистемы полости рта восстанавливаться до исходного состояния [3]. В испытании ЭГ участники могут иметь высокую (полную) или низкую (неполную) устойчивость после эксперимента (рис. 1). Факторы, связанные с устойчивостью ткани пародонта/десны к возмущающим факторам, могут включать генетику и/или факторы образа жизни, такие как курение, диета и психосоциальные факторы [4]. В случае ЭГ ранее существовавший воспалительный статус и состояние полости рта в целом на досудебном этапе могли повлиять на исход исследования и, таким образом, определить резильентность [5].
 1
1 Определения устойчивости и устойчивости в текущем систематическом обзорном обзоре ЭГ. На панели a мы определяем сопротивление, т.е. способность оставаться неизменной во время возмущения (стрелки на а и б): Высокое сопротивление определяется как низкий отклик во время фазы индукции (а), а низкое сопротивление определяется как высокий отклик во время фазы индукции. индукционная фаза (б). На панели b мы определяем устойчивость, т. е. способность восстанавливаться до исходного состояния после возмущения: высокая устойчивость определяется как быстрое и полное восстановление на этапе разрешения (с), а низкая устойчивость определяется как медленное или неполное восстановление во время разрешения. фаза (г).
Полноразмерное изображение
Исследование ЭГ было адаптировано многими исследовательскими группами, что привело к принятию различных протоколов для каждой фазы. Эксперимент используется для изучения большого разнообразия результатов от клинических, микробиологических до иммунологических результатов и субъектов, от здоровых субъектов до сравнения системно нездоровых участников исследования или беременных женщин.
 В этом систематическом обзоре мы стремились выявить в исследованиях ЭГ изменения биомаркеров микробиологического, иммунологического и биохимического происхождения, которые могут указывать на резистентность и устойчивость. Мы искали потенциальные маркеры устойчивости и устойчивости в фазах индукции и разрешения соответственно. Полученные данные заносятся в таблицу, а сведения о стойкости и устойчивости или пробелы в литературе представляются для будущих исследований.
В этом систематическом обзоре мы стремились выявить в исследованиях ЭГ изменения биомаркеров микробиологического, иммунологического и биохимического происхождения, которые могут указывать на резистентность и устойчивость. Мы искали потенциальные маркеры устойчивости и устойчивости в фазах индукции и разрешения соответственно. Полученные данные заносятся в таблицу, а сведения о стойкости и устойчивости или пробелы в литературе представляются для будущих исследований. Методы
Дизайн исследования
Предварительная оценка размера и объема доступной исследовательской литературы, касающейся оральной устойчивости к ЭГ, была проведена в соответствии с Руководством для рецензентов JBI Briggs и заявлением PRISMA для прозрачного представления систематических обзоров и метаанализа [ 6, 7] Для обеспечения систематического обзора литературы в процессе обзора использовались контрольный список и руководство PRISMA.
Электронный поиск
Строка поиска была определена и ограничена использованием слов «экспериментальный гингивит» в скобках и запущена в PubMed с момента создания до 11 апреля 2018 г.
 Эта указанная строка поиска ограничила бы ссылки теми, которые сосредоточены только на ЭГ, что привело бы к большому сокращение нерелевантных ссылок по сравнению с другими параметрами строки поиска. Попадания, возникающие в результате стратегии поиска, экспортировались в RAYYAN, веб-приложение систематического обзора [8], для процесса проверки.
Эта указанная строка поиска ограничила бы ссылки теми, которые сосредоточены только на ЭГ, что привело бы к большому сокращение нерелевантных ссылок по сравнению с другими параметрами строки поиска. Попадания, возникающие в результате стратегии поиска, экспортировались в RAYYAN, веб-приложение систематического обзора [8], для процесса проверки. Процесс скрининга
Результаты поиска были проверены C.Z. и Нью-Джерси на основе названия, аннотации и полного текста, а также противоречивых результатов были обсуждены для достижения консенсуса. Извлечение данных было дважды проверено Б.Г.Л. Выбранные исследования для полнотекстового скрининга были экспортированы в EndNote. Полные тексты исследований были получены с помощью EndNote, Google, Research Gate или путем обращения к соответствующему автору. Были включены ссылки, содержащие данные об иммунологических, микробиологических и биохимических показателях. Эти данные были необходимы для указания или косвенного доказательства сопротивления и/или устойчивости полости рта во время и после исследования ЭГ.
 Были исключены исследования ополаскивателей для рта, контрольных групп плацебо, животных, хирургического лечения, антибиотиков, пробиотиков, тех, у кого не было здоровой контрольной популяции, поперечных срезов, любых форм вмешательства во время фазы индукции и экспериментального дизайна разделенного рта. Исследования последнего типа были исключены из-за риска переноса жидкостей и биомаркеров из одной части ротовой полости в другую. Кроме того, системные ответы, вероятно, будут ниже при разделенном дизайне исследования полости рта, чем при ЭГ с полным ртом из-за меньшей площади воспаленной поверхности десны; это может затем повлиять на воспалительный профиль плазмы и GCF.
Были исключены исследования ополаскивателей для рта, контрольных групп плацебо, животных, хирургического лечения, антибиотиков, пробиотиков, тех, у кого не было здоровой контрольной популяции, поперечных срезов, любых форм вмешательства во время фазы индукции и экспериментального дизайна разделенного рта. Исследования последнего типа были исключены из-за риска переноса жидкостей и биомаркеров из одной части ротовой полости в другую. Кроме того, системные ответы, вероятно, будут ниже при разделенном дизайне исследования полости рта, чем при ЭГ с полным ртом из-за меньшей площади воспаленной поверхности десны; это может затем повлиять на воспалительный профиль плазмы и GCF. Управление данными
Данные об организации исследования, параметрах и характеристиках исследования представлены в отдельных таблицах. Данные были обобщены в описательной форме, чтобы предоставить обзор полученных доказательств и сообщаемой устойчивости на основе микробиологического, иммунологического и биохимического происхождения.
 Для каждого исследования мы провели оценку риска систематической ошибки, используя контрольный список JBI для аналитических перекрестных исследований. Мы классифицировали оценки риска систематической ошибки следующим образом: < 4, высокий риск систематической ошибки; 4–5, умеренный риск систематической ошибки; 6–7, низкий риск систематической ошибки.
Для каждого исследования мы провели оценку риска систематической ошибки, используя контрольный список JBI для аналитических перекрестных исследований. Мы классифицировали оценки риска систематической ошибки следующим образом: < 4, высокий риск систематической ошибки; 4–5, умеренный риск систематической ошибки; 6–7, низкий риск систематической ошибки. Результаты
Стратегия поиска дала 411 публикаций, из которых 104 были проверены на основе полнотекстового анализа. Наконец, в текущий обзор были включены 22 уникальных исследования (рис. 2). Подробная информация о включенных исследованиях представлена в таблице 1. Список исключенных исследований на основе полного текста приведен в дополнительном файле 1. Было отмечено, что 18 из этих исследований были исключены на том основании, что полный текст был недоступен. Как правило, они были в небольших стоматологических журналах, доступных только по подписке, и у нас не было доступа к документам. Всего в двух исследованиях сообщалось о микробиологических данных [22, 23], в восьми исследованиях изучались биохимические изменения [10, 12, 13, 14, 21, 24, 25, 26, 27] и в 12 анализировались иммунологические результаты [9].
Рис. 2 , 11, 15,16,17,18,19,20, 28,29,30]. Полные описания всех изучаемых параметров приведены в дополнительном файле 2. Протоколы во включенных исследованиях различались по временным рамкам, охвату фаз и группам сравнения. Нет исследований, специально направленных на выявление факторов, связанных с устойчивостью полости рта к проблемам, возникающим в результате воздержания от мер гигиены полости рта. Пять исследований сравнивали курильщиков и некурящих при испытании ЭГ [18, 23, 24, 25, 29]; статус курения всегда основывался на самоотчете, а не на биохимической оценке. В 15 исследованиях сообщалось о размере выборки менее 20 человек, в то время как в шести других исследованиях участвовало от 21 до 156 субъектов. Студенты использовались в качестве исследуемой группы в 12 исследованиях, девять из которых были посвящены студентам-стоматологам. В двух исследованиях изучались пожилые люди и молодые люди, а в одном исследовании участвовали только дети: с синдромом Дауна и здоровые. Помимо исследования детей (возраст не указан), самым молодым и самым старшим из зарегистрированных возрастов были 18 и 77 лет.
, 11, 15,16,17,18,19,20, 28,29,30]. Полные описания всех изучаемых параметров приведены в дополнительном файле 2. Протоколы во включенных исследованиях различались по временным рамкам, охвату фаз и группам сравнения. Нет исследований, специально направленных на выявление факторов, связанных с устойчивостью полости рта к проблемам, возникающим в результате воздержания от мер гигиены полости рта. Пять исследований сравнивали курильщиков и некурящих при испытании ЭГ [18, 23, 24, 25, 29]; статус курения всегда основывался на самоотчете, а не на биохимической оценке. В 15 исследованиях сообщалось о размере выборки менее 20 человек, в то время как в шести других исследованиях участвовало от 21 до 156 субъектов. Студенты использовались в качестве исследуемой группы в 12 исследованиях, девять из которых были посвящены студентам-стоматологам. В двух исследованиях изучались пожилые люди и молодые люди, а в одном исследовании участвовали только дети: с синдромом Дауна и здоровые. Помимо исследования детей (возраст не указан), самым молодым и самым старшим из зарегистрированных возрастов были 18 и 77 лет. В общей сложности 14 исследований включали предварительную фазу, а девять исследований добавили к эксперименту фазу разрешения. Схема исследования для каждой фазы исследования EG представлена в дополнительном файле 3.
В общей сложности 14 исследований включали предварительную фазу, а девять исследований добавили к эксперименту фазу разрешения. Схема исследования для каждой фазы исследования EG представлена в дополнительном файле 3.
PRISMA Блок-схема процесса поиска и отбора
Изображение в полный размер
Таблица 1 Обзор включенных исследований: описание характеристик исследований и извлеченных данных, стратификация по микробиологическим (A), иммунологическим (B) и биохимическим (C) исходыПолная таблица
Оценка риска систематической ошибки
Десять исследований имели умеренный риск систематической ошибки (4–5 баллов) и 11 исследований имели низкий риск систематической ошибки (6–7 баллов). Ни в одном из исследований не учитывались искажающие факторы при окончательном анализе, поэтому оценка «7» не была достигнута. Полная таблица риска систематической ошибки представлена в дополнительном файле 4.

Микробиологические маркеры
В двух исследованиях изучались микробиологические изменения во время исследования ЭГ и сравнивались результаты у курильщиков и некурящих [22, 23]. Оба исследования были почти одинакового размера, и оба имели профессиональную профилактику на досудебном этапе.
Исследование Salvi et al. [23], используя методы гибридизации ДНК-ДНК в шахматном порядке на образцах поддесневого зубного налета, не выявили различий в общем количестве проб ДНК во время фазы индукции (день 0 по сравнению с днем 21) и после разрешения (день 35 по сравнению с днем 21). Виды были сгруппированы на основе комплексов с цветовой кодировкой, идентифицированных Socransky et al. [31] в исследовании гибридизации в шахматном порядке бактерий, связанных с пародонтозом. Фиолетовые сложные виды ( Veillonella parvula и Actinomyces odontolyticus ) были значительно снижены у некурящих на 21-й день по сравнению с исходным уровнем. Actinomyces sp. (синий комплекс) и желтый комплекс, содержащий оральные стрептококки Streptococcus sanguinis , S.
 oralis , S. mitis , S. gordonii и S. intermedius , увеличивался у некурящих во время разрешения. Напротив, красные сложные виды ( Porphyromonas gingivalis, Treponema denticola, и Таннерелла. forsythia ), которые наиболее тесно связаны с пародонтитом, были значительно повышены у курильщиков в поддесневом налете к 21-му дню ЭГ и значительно уменьшились в фазе разрешения, с 21-го по 35-й день, как у курильщиков, так и у некурящих [23].
oralis , S. mitis , S. gordonii и S. intermedius , увеличивался у некурящих во время разрешения. Напротив, красные сложные виды ( Porphyromonas gingivalis, Treponema denticola, и Таннерелла. forsythia ), которые наиболее тесно связаны с пародонтитом, были значительно повышены у курильщиков в поддесневом налете к 21-му дню ЭГ и значительно уменьшились в фазе разрешения, с 21-го по 35-й день, как у курильщиков, так и у некурящих [23]. Исследование Lie et al. [22] использовали традиционную микробиологическую культуру и идентификацию для исследования девяти различных микробных таксонов в трех различных типах зубного налета: наддесневом, поддесневом или апроксимальном, включая мазки с языка и миндалин. В образцах наддесневого зубного налета общее количество КОЕ значительно увеличилось по сравнению с исходным уровнем до конца фазы ЭГ (14-й день) у некурящих с 1,1 × 10 6 КОЕ до 3,7 × 10 6 КОЕ. Напротив, у курильщиков не было существенной разницы на этом этапе.
 Aggregatibacter (ранее Actinobacillus ) actinomycetemcomitans , Parvimonas micra (ранее Peptostreptococcus micros ) и Streptococcus spp. не различались между группами или с течением времени в фазе индукции. Точно так же не было существенной разницы во времени в уровнях A. actinomycetemcomitans, Campylobacter rectus, Fusobacterium nucleatum, Streptococcus 9.0864 spp. и P. micra в поддесневом налете и всего КОЕ, A. actinomycetemcomitans, Streptococcus spp. и P. micros в апроксимальном налете [22]. Среднее общее количество КОЕ Campylobacter rectus и F. nucleatum увеличилось во время ЭГ у курильщиков и этих видов вместе с Actinomyces spp. и P. intermedia , повышенный у некурящих. Различия варьировались от 3,4-кратного увеличения у Actinomyces вид. у некурящих между 0 и 14 днями до 29-кратного увеличения P. intermedia у некурящих за тот же период времени. Выявлено достоверное увеличение суммы КОЕ в поддесневом зубном налете у курильщиков, но не у некурящих, во время ЭГ с 6,3 × 10 5 КОЕ до 3,4 × 10 6 КОЕ.
Aggregatibacter (ранее Actinobacillus ) actinomycetemcomitans , Parvimonas micra (ранее Peptostreptococcus micros ) и Streptococcus spp. не различались между группами или с течением времени в фазе индукции. Точно так же не было существенной разницы во времени в уровнях A. actinomycetemcomitans, Campylobacter rectus, Fusobacterium nucleatum, Streptococcus 9.0864 spp. и P. micra в поддесневом налете и всего КОЕ, A. actinomycetemcomitans, Streptococcus spp. и P. micros в апроксимальном налете [22]. Среднее общее количество КОЕ Campylobacter rectus и F. nucleatum увеличилось во время ЭГ у курильщиков и этих видов вместе с Actinomyces spp. и P. intermedia , повышенный у некурящих. Различия варьировались от 3,4-кратного увеличения у Actinomyces вид. у некурящих между 0 и 14 днями до 29-кратного увеличения P. intermedia у некурящих за тот же период времени. Выявлено достоверное увеличение суммы КОЕ в поддесневом зубном налете у курильщиков, но не у некурящих, во время ЭГ с 6,3 × 10 5 КОЕ до 3,4 × 10 6 КОЕ. Actinomyces spp. и P. intermedia были повышены как у курильщиков, так и у некурящих. В апроксимальном зубном налете Actinomyces spp. и C. rectus были повышены к концу ЭГ у некурящих, F. nucleatum были повышены у курильщиков и P. intermedia были повышены как у курящих, так и у некурящих. Существенных изменений в количестве микробов между началом и концом ЭГ в образцах с языка или миндалин не наблюдалось [22].
Actinomyces spp. и P. intermedia были повышены как у курильщиков, так и у некурящих. В апроксимальном зубном налете Actinomyces spp. и C. rectus были повышены к концу ЭГ у некурящих, F. nucleatum были повышены у курильщиков и P. intermedia были повышены как у курящих, так и у некурящих. Существенных изменений в количестве микробов между началом и концом ЭГ в образцах с языка или миндалин не наблюдалось [22]. В целом, эти два исследования [22, 23] демонстрируют, что микробиологический состав как наддесневых, так и поддесневых зубных отложений изменяется в ходе ЭГ и во время разрешения, и эти изменения, по-видимому, зависят от курения. Однако исследование Salvi et al. [23] не анализировали изменения у отдельных видов, и поэтому невозможно определить устойчивые маркеры отзывчивости или устойчивости только на основе этих двух исследований.
Иммунологические маркеры
Биопсия и системные данные
Три исследования изучали изменения лейкоцитов в исследовании ЭГ [14, 20, 28].
 У них была 21-дневная фаза индукции, и уровни лейкоцитов как в биоптатах десен, так и в периферической крови не изменились в фазе индукции по сравнению с исходными уровнями. Только в одном исследовании ( N = 8) полиморфноядерные нейтрофилы (ПЯН) в биоптатах десен значительно увеличились с 18,1% в конце исследования ЭГ (т.е. в день 0 фазы разрешения) до 21,9.% на 8-й день фазы разрешения [14]. Это наблюдение противоречит интуиции, однако разница между 18,1 и 21,9% может быть клинически незначимой; фибробласты, лимфоциты, плазматические клетки и макрофаги не показали существенных изменений в фазе разрешения.
У них была 21-дневная фаза индукции, и уровни лейкоцитов как в биоптатах десен, так и в периферической крови не изменились в фазе индукции по сравнению с исходными уровнями. Только в одном исследовании ( N = 8) полиморфноядерные нейтрофилы (ПЯН) в биоптатах десен значительно увеличились с 18,1% в конце исследования ЭГ (т.е. в день 0 фазы разрешения) до 21,9.% на 8-й день фазы разрешения [14]. Это наблюдение противоречит интуиции, однако разница между 18,1 и 21,9% может быть клинически незначимой; фибробласты, лимфоциты, плазматические клетки и макрофаги не показали существенных изменений в фазе разрешения. Известно, что в результате воспалительных реакций sICAM увеличивается в плазме. В одном исследовании sICAM-1 в плазме значительно увеличился в 2,6 раза в фазе индукции и оставался повышенным в течение 2-недельной фазы разрешения [14]. Результаты для sICAM-1 в ЭГ и его разрешение указывают на низкую резистентность и низкую устойчивость к возникающему воспалению десны.
 Здесь мы нашли еще один пример, когда биомаркер дольше оставался в плазме, в то время как десна вернулась в свое здоровое состояние. Интересно, что для цитокина интерферона-γ не было значительных изменений во время фаз индукции и разрешения [14], что свидетельствует об отсутствии значительного участия этого иммунного медиатора в ЭГ.
Здесь мы нашли еще один пример, когда биомаркер дольше оставался в плазме, в то время как десна вернулась в свое здоровое состояние. Интересно, что для цитокина интерферона-γ не было значительных изменений во время фаз индукции и разрешения [14], что свидетельствует об отсутствии значительного участия этого иммунного медиатора в ЭГ. В одном исследовании искали иммуноглобулины в сыворотке. Значения IgG, IgM и IgA у субъектов ЭГ по сравнению с субъектами, которые поддерживали нормальную гигиену полости рта, оставались стабильными в течение индукционного периода [19]. Фаза разрешения не включена.
Слюна
В исследовании Zhou et al. [13], экспрессия интерлейкина (IL)-1β в цельной нестимулированной слюне была значительно выше во время фазы индукции и возвращалась к исходному уровню при разрешении, что позволяет предположить, что здоровье десен улучшилось в конце фазы разрешения до (более) здорового состояния и показывает нормальную устойчивость и воспалительную реакцию на провокацию.
 В одном небольшом исследовании Belstrøm et al. [30], уровни IL-β в стимулированной слюне снижались через 10 дней фазы индукции по сравнению с исходными уровнями. Среднее значение ИЛ-6 в цельной слюне значительно увеличилось с 6,70 пг/мл в начале исследования до 7,86 пг/мл на 21-й день (конец индукции). Значения снизились до 7,05 пг/мл в фазе разрешения, что существенно не отличалось по сравнению с 0-м днем. Кроме того, уровни ИЛ-8 в стимулированной слюне снижались через 4 дня индукции и оставались низкими до фазы разрешения [30]. Примечательно, что уровни ИЛ-2, ИЛ-4, ИЛ-5 и ИЛ-10 в слюне со временем существенно не изменились [12].
В одном небольшом исследовании Belstrøm et al. [30], уровни IL-β в стимулированной слюне снижались через 10 дней фазы индукции по сравнению с исходными уровнями. Среднее значение ИЛ-6 в цельной слюне значительно увеличилось с 6,70 пг/мл в начале исследования до 7,86 пг/мл на 21-й день (конец индукции). Значения снизились до 7,05 пг/мл в фазе разрешения, что существенно не отличалось по сравнению с 0-м днем. Кроме того, уровни ИЛ-8 в стимулированной слюне снижались через 4 дня индукции и оставались низкими до фазы разрешения [30]. Примечательно, что уровни ИЛ-2, ИЛ-4, ИЛ-5 и ИЛ-10 в слюне со временем существенно не изменились [12]. Иммуноглобулины (Ig) изучали в трех исследованиях [11, 18, 19]. Секреция IgA [19] в стимулированной околоушной слюне значительно увеличилась с 20 мкг/мл до 40 мкг/мл в фазе индукции в здоровой исследовательской группе. Однако секреция и концентрация IgA в покоящейся околоушной слюне, подчелюстной/подъязычной слюне (как покоящейся, так и стимулированной) оставались стабильными на этой стадии [18].
 Данные о фазе разрешения отсутствуют [11].
Данные о фазе разрешения отсутствуют [11]. Жидкость десневой борозды
Различные ИЛ изучались в шести исследованиях [13, 15, 16, 17, 19, 28, 29]. В двух из этих исследований [13, 19] не было обнаружено изменений IL-4, IL-5, IL-6, IL-8, IL-10 и IL-12 в жидкости десневой борозды (GCF) на этапе индукции. . В исследовании Heasman et al. [15], IL-1β в GCF из 20 объединенных участков на субъект показал почти 8-кратное увеличение с 16,5 нг/мл в начале исследования до 131 нг/мл на 1-й неделе, после чего оставался примерно на этом уровне до конца эксперимента. 28 дней). Об аналогичной картине сообщили Leishman et al. [17]; интересно, что они включили в свое исследование фазу разрешения и обнаружили, что IL-1β в GCF показал снижение, превышающее исходные уровни (52,9).1 пг/мл) до 9,64 пг/мл в конце фазы разрешения. У курильщиков, участвовавших в исследовании ЭГ, уровень ИЛ-1β в ЗКФ повышался от исходного уровня к 10-му дню индукционной фазы с 6,2 пг/20 с до 13,6 пг/20 с, в то время как у некурящих соответствующие значения составляли 3,99 пг.
 /20 с до 9,8 пг/20 с [19].
/20 с до 9,8 пг/20 с [19]. Другой интерлейкин, IL-2 в GCF, увеличился с 7,81 пг/мл в начале до 11,82 пг/мл в конце индукции [13]. Тем не менее, уровни IL-2 упали ниже исходных значений 0,59 пг/мл [13], что свидетельствует о возвращении к нормальной невоспаленной десне и о том, что исходные ткани десны были несколько воспалены.
Было обнаружено, что уровень выработки ИЛ-4 в GCF снижается после 10 дней индукционной фазы у некурящих с 10,2 пг/20 с до 5,5 пг/20 с и остается стабильным у курильщиков: с 4,4 пг/20 с до 4,1 пг/ 20 лет [19]. Реакция ИЛ-4 не согласуется с данными Leishman et al. [17]. В этом исследовании фаза индукции состояла из 21 дня, в течение которых уровень IL-4 в GCF существенно не менялся с течением времени. Тем не менее, он упал до 0 через 14 дней после разрешения, что указывает на устойчивость к испытанию по маркеру IL-4.
Для IL-8 скорость выброса в GCF значительно увеличилась во время фазы индукции у курильщиков и некурящих (от 21,1 пг/20 с до 56,1 пг/20 с; с 15,1 пг/20 с до 36,5 пг/20с соответственно), при увеличение числа курильщиков [29].
 Это может указывать на то, что у курильщиков реакция хозяина на воспалительный процесс выше, чем у некурящих.
Это может указывать на то, что у курильщиков реакция хозяина на воспалительный процесс выше, чем у некурящих. Исследование, проведенное Tsalikis et al. [28] сравнили уровни TNF-α в GCF у пожилых и молодых участников (61–65 и 20–22 года). Исходные значения не отличались между возрастными группами. На 21-й день фазы индукции и на 7-й день фазы разрешения значения были значительно выше у пожилых участников, в то время как у более молодых участников не было никаких изменений в течение всего эксперимента. Это говорит о том, что пожилой возраст связан с более низкой устойчивостью к ЭГ, чем более молодой возраст. Последние результаты несколько отличаются от результатов другого исследования: в исследовании, проведенном Leishman et al. [17] в исследуемой популяции со средним возрастом 25 лет значения TNF-α в GCF увеличились во время индукции 3-недельного периода (0,98 пг/мл до 1,75 пг/мл) и снизился до 0,11 пг/мл в фазе разрешения, т.е. указывает на высокую устойчивость. Однако противоречивые результаты для TNF-α в GCF между двумя исследованиями [17, 28] затрудняют вывод об общем ответе на ЭГ.

Только в одном исследовании изучались липидные иммунные медиаторы, PGE-2 и TxB2 в образцах GCF. Результат показал, что эти медиаторы не были повышены в течение первых 3 недель. Однако значения значительно увеличились на 4-й неделе индукционной фазы, что свидетельствует о том, что резистентность к ЭГ может быть ослаблена, когда ЭГ продлевается за пределы традиционного 3-недельного периода [15].
Биохимические маркеры
Слюна
Полный протеомный анализ цельной слюны был проведен у здоровых взрослых [27]. Было обнаружено, что несколько белков, перечисленных в таблице 1, демонстрируют по крайней мере двукратное увеличение концентрации во время фазы индукции. Из них было идентифицировано 10 белков, играющих роль в защите клеток и тканей: белок, связывающий витамин D, тиоредоксин, лактоферрин (также известный как лактотрансферрин), рецептор, связанный с G-белком, цистатин-SN, цистатин-S, коллаген альфа 1 (XXVII). цепь, бета-глобин, аннексин А1 и белок ALB. Данных об изменении протеома в фазе разрешения не сообщалось.

Цистатиновая активность слюны, выделение и общий белок были исследованы в одном исследовании ЭГ, в котором участвовали курильщики и некурящие [24]. Средняя концентрация белка в обеих группах существенно не менялась с течением времени. У некурящих активность цистатина, выходная активность цистатина, цистатин С и выходной цистатин С оставались стабильными во время фазы индукции. Однако у курильщиков на 14-й день наблюдалось значительное снижение активности цистатина с 36,2 до 28,8 (единиц/мл) и уменьшение выведения цистатина С (с 0,37 до 0,22 мкг/мин) по сравнению с исходным уровнем. Когда изменения на 14-й день сравнивали между группами, некурящие показали более высокий уровень активности цистатина (49).против 28,8 ЕД/мл), цистатин С (0,63 против 0,44 мкг/мл), выходная активность цистатина (31,6 против 17,5 ЕД/мин) и вывод цистатина С (0,46 против 0,22 мкг/мин). В этом одном исследовании параметров цистатина слюны мы отметили тенденцию этих биомаркеров у некурящих оставаться стабильными во время индукционной фазы ЭГ, что указывает на то, что, возможно, эти слюнные факторы не играют важной роли в резистентности к ЭГ.
 С другой стороны, у курильщиков эти параметры снижаются, что может свидетельствовать о том, что курильщики имеют меньшую способность защиты слюны в исследовании ЭГ.
С другой стороны, у курильщиков эти параметры снижаются, что может свидетельствовать о том, что курильщики имеют меньшую способность защиты слюны в исследовании ЭГ. Из исследования ЭГ Uitto et al. [12], концентрации слюнной эластазы в образцах ополаскивателей для полости рта измеряли на 10-й и 15-й день фазы индукции, и не было сообщено о каких-либо существенных различиях с течением времени. В другом исследовании активность эластазы в образцах слюны значительно увеличилась на 2-й день фазы индукции и оставалась повышенной до 14-го дня, в то время как в фазе разрешения она снова снизилась до исходного уровня [13]. Эти результаты показывают, что активность эластазы является полезным биомаркером резистентности и устойчивости к ЭГ у пародонтально здоровых людей.
Жидкость десневой борозды
Исследование ЭГ, проведенное у 12 здоровых студентов-стоматологов мужского пола, измерило уровни лактоферрина в GCF и выявило значительное увеличение с 0-го дня до конца фазы индукции (14 дней) на 58,8 и 163,2 нг/мкл соответственно.
 [26]. Это согласуется с результатами, полученными Adonogianaki et al. [25], которые также провели исследование GCF у здоровых студентов-стоматологов ( N = 6). В фазе разрешения уровни лактоферрина вернулись к исходным значениям. Лактоферрин при ЗКФ может быть хорошим биомаркером для определения резистентности (увеличение антибактериальной активности) и резильентности при ЭГ.
[26]. Это согласуется с результатами, полученными Adonogianaki et al. [25], которые также провели исследование GCF у здоровых студентов-стоматологов ( N = 6). В фазе разрешения уровни лактоферрина вернулись к исходным значениям. Лактоферрин при ЗКФ может быть хорошим биомаркером для определения резистентности (увеличение антибактериальной активности) и резильентности при ЭГ. В одном исследовании ЭГ ( N = 10) уровни трансферрина не показали значительных изменений в крови и GCF во время фазы индукции [18]. Это не согласуется с исследованием Adonogianaki et al. [25], в которых уровни трансферрина, по-видимому, значительно увеличивались с течением времени, но не возвращались к исходным уровням после разрешения.
Кальпротектин является реагентом острой фазы воспаления, связанного с разрушением тканей и действием нейтрофилов. Изменения значений кальпротектина отражают степень воспаления десен. Значения показали увеличение значения в течение трехнедельного периода ЭГ до 5 мкг / мл, что указывает на воспаление [13].
 Через 1 неделю фазы разрешения биомаркер воспаления снизился до 1,7 мкг/мл, что было ниже исходного значения 2,4 мкг/мл. Последнее свидетельствует о том, что полость рта имеет естественную реакцию на воспаление и восстанавливается до улучшенного состояния по сравнению с исходным. Эти результаты были сходными в исследовании, в котором уровни кальпротектина измерялись в GCF во время фазы индукции [21]. Однако последнее исследование включало профессиональную профилактику в конце индукции, когда уровни значительно увеличились через 1 день после вмешательства. Этот белок может не быть маркером уровня воспаления десны во время ЭГ-испытания, чтобы указывать либо на сопротивляемость, либо на резистентность.
Через 1 неделю фазы разрешения биомаркер воспаления снизился до 1,7 мкг/мл, что было ниже исходного значения 2,4 мкг/мл. Последнее свидетельствует о том, что полость рта имеет естественную реакцию на воспаление и восстанавливается до улучшенного состояния по сравнению с исходным. Эти результаты были сходными в исследовании, в котором уровни кальпротектина измерялись в GCF во время фазы индукции [21]. Однако последнее исследование включало профессиональную профилактику в конце индукции, когда уровни значительно увеличились через 1 день после вмешательства. Этот белок может не быть маркером уровня воспаления десны во время ЭГ-испытания, чтобы указывать либо на сопротивляемость, либо на резистентность. Биопсия и системные данные
Лактоферрин в образцах крови значительно увеличился со 112 нг/мкл в день 0 до 200 нг/мкл через 2 недели фазы индукции и снизился до исходных значений в фазе разрешения [26]. Подобно лактоферрину в GCF, значения образца крови также могут быть хорошим местом для образца для определения устойчивости к ЭГ.

Норман и др. [19] изучали изменения СН50 и компонента комплемента С4 в сыворотке в течение 21-дневной фазы индукции без разрешения. Количество значительно увеличилось в конце индукции по сравнению с исходным уровнем. Молекула компонента комплемента С3, фактор 8, альфа-антитрипсин, микросомальная простагландин-Е-синтаза-1 и циклооксигеназа-2 не менялись в своем значении в течение фазы индукции [16, 21, 24].
В одном исследовании сообщается о моноцитарном хемоаттрактантном белке-1 (MCP-1) и факторе роста эндотелия сосудов (VEGF) у студентов-стоматологов, проходящих ЭГ-исследование [30]. Во время фазы индукции наблюдалось снижение обоих маркеров. Последнее исследование не включало фазу разрешения. Невозможно сделать четких заявлений о маркерах как показателях резистентности или устойчивости во время исследования ЭГ.
Обсуждение
Этот систематический предварительный обзор был направлен на выявление биологических изменений в ротовой полости во время ЭГ-исследований, которые могут свидетельствовать о резистентности и резильентности.
 ЭГ была выбрана потому, что это хорошо зарекомендовавшая себя продольная модель, которая использовалась многими исследователями. Результатом поиска стали исследования с большим разнообразием модификаций оригинального исследования ЭГ [1]. Чтобы снизить уровень неоднородности, исследования с разделенным ртом были исключены, как указано в разделе «Методы» (риск переноса жидкости/биомаркеров, системные ответы). Несмотря на это, результаты экспериментов с полным ртом было трудно сравнивать друг с другом. Постановка EG-фаз и их продолжительность различались между исследованиями. Ни одно из исследований не было направлено на изучение резистентности и/или резильентности к ЭГ. Тем не менее включенные исследования дали некоторое представление об изменениях во время ЭГ-проблемы. Величина изменений может указывать либо на высокую, либо на низкую сопротивляемость и/или сопротивляемость вызову. Только небольшое количество исследований изучало «восстановление» на этапе разрешения, поэтому удалось определить маркеры, которые можно было бы перевести на устойчивость.
ЭГ была выбрана потому, что это хорошо зарекомендовавшая себя продольная модель, которая использовалась многими исследователями. Результатом поиска стали исследования с большим разнообразием модификаций оригинального исследования ЭГ [1]. Чтобы снизить уровень неоднородности, исследования с разделенным ртом были исключены, как указано в разделе «Методы» (риск переноса жидкости/биомаркеров, системные ответы). Несмотря на это, результаты экспериментов с полным ртом было трудно сравнивать друг с другом. Постановка EG-фаз и их продолжительность различались между исследованиями. Ни одно из исследований не было направлено на изучение резистентности и/или резильентности к ЭГ. Тем не менее включенные исследования дали некоторое представление об изменениях во время ЭГ-проблемы. Величина изменений может указывать либо на высокую, либо на низкую сопротивляемость и/или сопротивляемость вызову. Только небольшое количество исследований изучало «восстановление» на этапе разрешения, поэтому удалось определить маркеры, которые можно было бы перевести на устойчивость. Выводы, представленные в этом обзоре в отношении резистентности и устойчивости, очевидно, зависят от продолжительности испытания. Например, исследование Heasman et al. [15] показали, что продление испытания ЭГ до 4 недель дает другие результаты, чем испытания продолжительностью 2 недели. Это может объяснить, почему в исследованиях с короткими фазами индукции и разрешения не было обнаружено четких результатов.
Выводы, представленные в этом обзоре в отношении резистентности и устойчивости, очевидно, зависят от продолжительности испытания. Например, исследование Heasman et al. [15] показали, что продление испытания ЭГ до 4 недель дает другие результаты, чем испытания продолжительностью 2 недели. Это может объяснить, почему в исследованиях с короткими фазами индукции и разрешения не было обнаружено четких результатов. Только два из включенных исследований изучали микробиологические изменения в исследовании ЭГ [22, 23]. Используя микробиологическую культуру, наиболее последовательным изменением во время ЭГ было увеличение P. intermedia , которое наблюдалось в 5/6 протестированных образцах налета (наддесневой налет у некурящих, поддесневой и апроксимальный налет у курильщиков и некурящих) [2]. 24]. P. intermedia входит в состав оранжевого комплекса Сокранского [31]. При рассмотрении этой группы не было обнаружено изменений во время фазы индукции или фазы разрешения [23].
 Actinomyces spp. постоянно увеличивался во время индукции гингивита у некурящих и в поддесневом зубном налете у курильщиков [22]. Actinomyces spp. может служить полезным индикатором резистентности, в зависимости от места отбора проб и статуса курения. Однако это предположение следует интерпретировать с осторожностью, поскольку оно было обнаружено только в одном исследовании с ограниченным числом курильщиков ( n = 11) и некурящих ( n = 14). Более того, мы признаем, что при обзоре/отчете об исследованиях с участием курильщиков биохимическое определение статуса курения было бы идеальным, а не широко применяемым методом самоотчетов. Что касается оценки устойчивости на основе комменсальных полезных видов бактерий полости рта, отсутствуют данные исследований ЭГ всего рта, изучающих изменения в микробиоме. Срочно необходимы более подробные исследования с использованием современных подходов к секвенированию нового поколения для изучения изменений полного микробиома десневых участков и других участков ротовой полости и слюны.
Actinomyces spp. постоянно увеличивался во время индукции гингивита у некурящих и в поддесневом зубном налете у курильщиков [22]. Actinomyces spp. может служить полезным индикатором резистентности, в зависимости от места отбора проб и статуса курения. Однако это предположение следует интерпретировать с осторожностью, поскольку оно было обнаружено только в одном исследовании с ограниченным числом курильщиков ( n = 11) и некурящих ( n = 14). Более того, мы признаем, что при обзоре/отчете об исследованиях с участием курильщиков биохимическое определение статуса курения было бы идеальным, а не широко применяемым методом самоотчетов. Что касается оценки устойчивости на основе комменсальных полезных видов бактерий полости рта, отсутствуют данные исследований ЭГ всего рта, изучающих изменения в микробиоме. Срочно необходимы более подробные исследования с использованием современных подходов к секвенированию нового поколения для изучения изменений полного микробиома десневых участков и других участков ротовой полости и слюны. До сих пор это было сделано только в исследовании дизайна разделенного рта и сосредоточено только на фазе индукции [32].
До сих пор это было сделано только в исследовании дизайна разделенного рта и сосредоточено только на фазе индукции [32]. Несколько иммунологических маркеров были изучены в ходе ЭГ и последующей фазы разрешения. Короче говоря, было практически невозможно получить надежную картину изменений для одного или нескольких из этих маркеров в нескольких исследованиях: маркеры редко измерялись в одном и том же дизайне ЭГ, подтвержденном в достаточном количестве исследований, в различных средах (биопсия). , GCF, стимулированная цельная слюна, нестимулированная цельная слюна, околоушная слюна, поднижнечелюстная слюна) и сообщаемые единицы интереса различались для одного и того же маркера, что затрудняет общие выводы. Одно исследование [13] показало некоторое увеличение числа ПЯЛ в биоптатах десны в фазе индукции ЭГ, но это увеличение не было клинически значимым.
Четыре исследования [12, 13, 15, 28] подтверждают, что IL-1β появляется как нормальная воспалительная реакция на провокацию со значительно более высокими значениями у курильщиков.
 Этот же параметр является маркером устойчивости, поскольку его значения падают ниже базовых уровней. То же самое относится и к ИЛ-6 [12]. Кроме того, уровни IgA могут увеличиваться в фазе разрешения, но это зависит от анализа стимулированной или нестимулированной слюны. Неясно, насколько тесно количество зубного налета (микробная нагрузка) связано с секрецией IgA. Таким образом, мы можем заключить, что обычные провоспалительные маркеры могут увеличиваться во время фазы индукции ЭГ в качестве маркера резистентности, но об этом не всегда сообщают и не дают сведений об истинных механистических путях, связанных с восприимчивостью к уровням ЭГ, которые развиваются. у любого конкретного человека, не говоря уже о том, что мы видели закономерности, которые могут указывать на определенный уровень устойчивости к ЭГ.
Этот же параметр является маркером устойчивости, поскольку его значения падают ниже базовых уровней. То же самое относится и к ИЛ-6 [12]. Кроме того, уровни IgA могут увеличиваться в фазе разрешения, но это зависит от анализа стимулированной или нестимулированной слюны. Неясно, насколько тесно количество зубного налета (микробная нагрузка) связано с секрецией IgA. Таким образом, мы можем заключить, что обычные провоспалительные маркеры могут увеличиваться во время фазы индукции ЭГ в качестве маркера резистентности, но об этом не всегда сообщают и не дают сведений об истинных механистических путях, связанных с восприимчивостью к уровням ЭГ, которые развиваются. у любого конкретного человека, не говоря уже о том, что мы видели закономерности, которые могут указывать на определенный уровень устойчивости к ЭГ. Ряд биохимических маркеров в слюне был изучен на уровне концентрации белка или активности ферментов во время курса ЭГ. Протеомный анализ выявил факторы, связанные с защитой клеток и тканей, как мишени регуляции во время ЭГ [27].
 Образцы для этого исследования стимулировали цельной слюной. Концентрации ингибиторов протеазы цистатин-SN и цистатин-S увеличились более чем в 2 раза на 21-й день по сравнению с исходным уровнем. Цистатины обладают антибактериальной активностью в отношении некоторых периопатогенов [33, 34]. Следовательно, повышенная активность цистатина является показателем устойчивости к возмущению. Несколько исследований показали, что общая активность цистатина повышена в слюне пациентов с пародонтитом по сравнению с контрольной группой [33, 35, 36]. Однако картина не совсем ясна, поскольку другие исследования показали снижение общей активности цистатина и специфическое снижение цистатина-SN и цистатина-S у пациентов с пародонтитом [37, 38]. Несмотря на то, что в нашем исследовании исключались конструкции с разделенным ртом, важно отметить, что цистатин-B и -S практически не изменились в GCF в течение 21 дня ЭГ в одном исследовании с разделенным ртом [39].]. Экспрессия цистатина может в некоторой степени зависеть от курения.
Образцы для этого исследования стимулировали цельной слюной. Концентрации ингибиторов протеазы цистатин-SN и цистатин-S увеличились более чем в 2 раза на 21-й день по сравнению с исходным уровнем. Цистатины обладают антибактериальной активностью в отношении некоторых периопатогенов [33, 34]. Следовательно, повышенная активность цистатина является показателем устойчивости к возмущению. Несколько исследований показали, что общая активность цистатина повышена в слюне пациентов с пародонтитом по сравнению с контрольной группой [33, 35, 36]. Однако картина не совсем ясна, поскольку другие исследования показали снижение общей активности цистатина и специфическое снижение цистатина-SN и цистатина-S у пациентов с пародонтитом [37, 38]. Несмотря на то, что в нашем исследовании исключались конструкции с разделенным ртом, важно отметить, что цистатин-B и -S практически не изменились в GCF в течение 21 дня ЭГ в одном исследовании с разделенным ртом [39].]. Экспрессия цистатина может в некоторой степени зависеть от курения. Уровни цистатина С были относительно постоянными во время ЭГ у некурящих, но значительно снижались за это время у курильщиков [24]. Исходя из этого вывода, курение является фактором, приводящим к низкой резистентности полости рта, возможно, также снижающей резильентность. Ясно, что требуется дополнительная работа, чтобы определить, может ли экспрессия цистатина быть полезным индикатором устойчивости, и опять же, биохимическое подтверждение курения/некурения было бы лучше.
Уровни цистатина С были относительно постоянными во время ЭГ у некурящих, но значительно снижались за это время у курильщиков [24]. Исходя из этого вывода, курение является фактором, приводящим к низкой резистентности полости рта, возможно, также снижающей резильентность. Ясно, что требуется дополнительная работа, чтобы определить, может ли экспрессия цистатина быть полезным индикатором устойчивости, и опять же, биохимическое подтверждение курения/некурения было бы лучше. Секвестрация ионов металлов считается важной антимикробной функцией жидкостей организма. Уровни лактоферрина в GCF и во всей слюне увеличивались во время ЭГ [25, 26]. Возможно, локальная концентрация железосвязывающих хелаторов в ротовой полости важна для предотвращения избыточного роста требующих железа пародонтальных патогенов, таких как P. gingivalis . Если это так, то концентрация этих белков или общая способность связывания железа слюной или GCF может коррелировать с резистентностью к индукции гингивита.
 Однако важно отметить, что в этих исследованиях не измерялась общая доступность железа в слюне или GCF, и возможно, что утечка железа гема через GCF из крови в эти жидкости могла привести к увеличению содержания ионов металлов, несмотря на повышенные уровни энтеросорбенты. Кальпротектин — еще один хелатор ионов металлов, однако его пероральный и слюнный уровни не были такими четкими, как у лактоферрина. Одно исследование показало, что уровни кальпротектина кратковременно подскакивали в конце фазы индукции или сразу после профессиональной чистки [12, 21]. Можно предположить, что в ротовой полости есть сенсоры для изменения выделения важных антибактериальных пептидов слюной во время ЭГ.
Однако важно отметить, что в этих исследованиях не измерялась общая доступность железа в слюне или GCF, и возможно, что утечка железа гема через GCF из крови в эти жидкости могла привести к увеличению содержания ионов металлов, несмотря на повышенные уровни энтеросорбенты. Кальпротектин — еще один хелатор ионов металлов, однако его пероральный и слюнный уровни не были такими четкими, как у лактоферрина. Одно исследование показало, что уровни кальпротектина кратковременно подскакивали в конце фазы индукции или сразу после профессиональной чистки [12, 21]. Можно предположить, что в ротовой полости есть сенсоры для изменения выделения важных антибактериальных пептидов слюной во время ЭГ. Было идентифицировано несколько других биохимических маркеров с потенциалом устойчивости и устойчивости к гингивиту, и некоторые из них были отмечены более чем в одном исследовании. К сожалению, ни в одном из исследований, посвященных биохимическим маркерам, не сообщалось о подробностях индивидуальных ответов на протокол ЭГ или скорости восстановления маркеров во время фазы разрешения.
 Таким образом, предстоит еще большая работа по выявлению потенциальных биохимических маркеров реактивности и устойчивости к ЭГ.
Таким образом, предстоит еще большая работа по выявлению потенциальных биохимических маркеров реактивности и устойчивости к ЭГ. Таким образом, неоднородность методов включенных исследований затруднила сравнение результатов или получение твердых выводов на основе последовательных результатов. Ограничения для сравнения исследований между собой заключались главным образом в различиях в месте отбора проб, продолжительности исследования, организации исследования (до, во время и после). Например, не все исследования включали предварительную фазу, включающую профессиональную профилактику для достижения состояния отсутствия воспаления перед фазой индукции. Это могло повлиять на результаты и различия между результатами при сравнении. Кроме того, ни в одном из исследований не проводились расчеты мощности, что, скорее всего, приводило к заниженным результатам. Таким образом, высокий уровень отсутствия значимых изменений, обнаруженный во многих исследованиях, которые имели фазу разрешения, мог быть связан с низкой мощностью.
 Кроме того, ни в одном из исследований не использовались термины «сопротивление» или «устойчивость» и не рассматривались конкретно оральные сопротивления и устойчивость. Устойчивость — это относительно новый подход к гигиене полости рта. Таким образом, интерпретация сопротивления и устойчивости проводится авторами на основе полученных данных и предположений.
Кроме того, ни в одном из исследований не использовались термины «сопротивление» или «устойчивость» и не рассматривались конкретно оральные сопротивления и устойчивость. Устойчивость — это относительно новый подход к гигиене полости рта. Таким образом, интерпретация сопротивления и устойчивости проводится авторами на основе полученных данных и предположений. В свете растущего количества данных о том, что разные группы населения по-разному реагируют на ЭГ, к результатам текущего систематического обзора следует относиться с осторожностью, пока дополнительные данные не дадут четкой картины того, какие из обсуждаемых исходов характерны для конкретных групп населения. В большинстве исследований ЭГ принимали участие здоровые молодые люди; весьма сомнительно, можно ли обобщить результаты этих субъектов на другие возрастные группы, можно ожидать различий в устойчивости и устойчивости к ЭГ у пожилых и молодых участников. Действительно, в одном исследовании уровни TNF-α в GCF указывали на более низкую резистентность к ЭГ у пожилых участников, в то время как в другом исследовании того же биомаркера молодые люди показали устойчивость в фазе разрешения [17, 28].
 Еще одним отличием между исследуемыми группами было курение. Хорошо охарактеризованным отличием является реакция кровотечения в исследовании ЭГ у курильщиков и некурящих [23, 26]. Мы выяснили из исследований, что курильщики имеют более низкий уровень как активности цистатина С, так и выделения цистатина С в слюне, чем некурящие, без соответствующих различий по другим параметрам, таким как индекс налета, околоушная слюна, скорость слюноотделения и общий слюнный белок [40]. .
Еще одним отличием между исследуемыми группами было курение. Хорошо охарактеризованным отличием является реакция кровотечения в исследовании ЭГ у курильщиков и некурящих [23, 26]. Мы выяснили из исследований, что курильщики имеют более низкий уровень как активности цистатина С, так и выделения цистатина С в слюне, чем некурящие, без соответствующих различий по другим параметрам, таким как индекс налета, околоушная слюна, скорость слюноотделения и общий слюнный белок [40]. . В общем, из текущего обзорного обзора мы отметили, что в подавляющем большинстве исследований ЭГ участвовало небольшое или очень небольшое количество участников, и практически все они были недостаточно мощными. Очень важно сделать надежные выводы о сопротивлении и устойчивости экосистемы полости рта и тканей десны, чтобы будущие исследования ЭГ следовали исходной ЭГ-модели, включая фазу разрешения, применяя расчеты мощности для определения соответствующего размера популяции. . Кроме того, для будущих исследований статус курения следует оценивать биохимически, чтобы исключить неправильную классификацию.

Из нашего предварительного обзора становится ясно, что в настоящее время мы упускаем из виду реальную информацию о резистентности и устойчивости тканей десны и многих других компонентов полости рта к воздействию ЭГ. Полученные нами результаты на самом деле являются «моментальными снимками» не полностью сопоставимых ситуаций ЭГ. Это привело к нашей самой большой задаче разработать теорию сопротивления и устойчивости к ЭГ. Другими словами, включенные исследования не позволяют нам определить четкую картину экологической устойчивости и устойчивости полости рта, поскольку некоторые биомаркеры показывают разные результаты в большинстве исследований, а также часто имеют разный дизайн.
Выводы
В этом исследовании был выделен ряд потенциальных микробиологических, иммунологических и биохимических маркеров, которые могут быть полезны для характеристики степени резистентности или резильентности к заражению ЭГ. В настоящее время необходимы дальнейшие исследования, чтобы определить уровни индивидуальных вариаций этих параметров в течение курса ЭГ и через разрешение после восстановления гигиены полости рта.
 В конечном счете, важно понимать индивидуальную реакцию на накопление зубного налета, чтобы лучше управлять стоматологической помощью и как мы можем вмешиваться в создание устойчивых и устойчивых экосистем полости рта.
В конечном счете, важно понимать индивидуальную реакцию на накопление зубного налета, чтобы лучше управлять стоматологической помощью и как мы можем вмешиваться в создание устойчивых и устойчивых экосистем полости рта. Наличие данных и материалов
Неприменимо.
Сокращения
- ALB:
-
Альбумин
- КОЕ:
-
Блок формирования колоний
- CSF:
-
Колониестимулирующий фактор
- НАПРИМЕР:
-
Экспериментальный гингивит
- ЗКФ:
-
Жидкость десневой борозды
- ИКАМ:
-
Молекула внутриклеточной адгезии
- Иг:
-
Иммуноглобулины
- Ил:
-
Интерлейкин
- ГЦН-1:
-
Хемоаттрактантный белок-1 моноцитов
- ПГЭ-2:
-
Простагландин-Е2
- Телефон:
-
Полиморфно-ядерный нейтрофил
- TbX2:
-
Тромбоксан 2
- ФНО-α:
-
Фактор некроза опухоли альфа
- VEGF:
-
Фактор роста эндотелия сосудов
Ссылки
- «>
Ло Х., Тейлад Э., Дженсен С.Б. Экспериментальный гингивит у человека. J Пародонтол. 1965; 36: 177–87.
Артикул Google ученый
-
van der Veen MH, Volgenant CM, Keijser B, Ten Cate JB, Crielaard W. Динамика красного флуоресцентного зубного налета во время экспериментального гингивита — когортное исследование. Джей Дент. 2016;48:71–6.
Артикул Google ученый
-
Марш П.Д., Заура Э. Стоматологическая биопленка: экологические взаимодействия в норме и болезни. Дж. Клин Пародонтол. 2017; 44 (Приложение 18): S12–22.
Артикул Google ученый
-
Лоос Б.Г., Папантонопулос Г., Джепсен С., Лайне М.Л. Каков вклад генетики в пародонтальный риск? Дент Клин N Am. 2015;59(4):761–80.
Артикул Google ученый
«>
Furuichi Y, Ramberg P, Lindhe J, Nabi N, Gaffar A. Некоторые эффекты ополаскивателей для полости рта, содержащих слюноотделение, на образование зубного налета de novo и развитие гингивита. Дж. Клин Пародонтол. 1996;23(8):795–802.
Артикул Google ученый
- Максименко А.В., Шешукова О.В., Ткаченко И.В.
Цель: Нашей научной работы явилось изучение уровня провоспалительного интерлейкина-18 (ИЛ-18) в ротовой жидкости детей с сахарным диабетом (СД) I типа, определение их пародонтального статуса и уровня гигиены полости рта.
ПАЦИЕНТЫ И МЕТОДЫ
Материалы и методы: обследовано 82 ребенка, которые были разделены на группы по наличию гингивита и сахарного диабета. Уровень интерлейкина-18 в ротовой жидкости определяли иммуноферментным методом.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
Результаты: у пациентов…
-
Мохер Д., Либерати А., Тецлафф Дж., Альтман Д.Г., Группа П. Предпочтительные элементы отчетности для систематических обзоров и метаанализов: отчет PRISMA. ПЛОС Мед. 2009;6(7):e1000097.
Артикул Google ученый
-
Институт Джоанны Бриггс. Руководство для рецензентов Института Джоанны Бриггс, 2015 г., методология обзорных обзоров JBI. 2015.
Google ученый
-
Ouzzani M, Hammady H, Fedorowicz Z, Elmagarmid A. Rayyan — веб-приложение и мобильное приложение для систематических обзоров. Системная редакция 2016; 5(1):210.

Артикул Google ученый
-
Вахаиди В.Ю., Коволик М.Дж., Эккерт Г.Дж., Галли Д.М. Эндотоксемия и системный ответ хозяина при экспериментальном гингивите. Дж. Клин Пародонтол. 2011;38(5):412–7.
Артикул Google ученый
-
Siegel B, Weihe E, Bette M, Nüsing RM, Flores-de-Jacoby L, Mengel R. Влияние возраста на ферменты, синтезирующие простагландины, на развитие гингивита. J Периодонтальная Рез. 2007;42(3):259–66.
Артикул Google ученый
-
Seemann R, Hägewald SJ, Sztankay V, Drews J, Bizhang M, Kage A. Уровни околоушного и поднижнечелюстного/подъязычного слюнного иммуноглобулина a в ответ на экспериментальный гингивит у людей. Clin Oral Investig. 2004;8(4):233–7.
Артикул Google ученый
«> -
Чжоу М., Мэн Х.С., Чжао Ю.Б., Чен З.Б. Изменения четырех провоспалительных белков в цельной слюне при экспериментальном гингивите. Чин Дж. Дент Рез. 2012;15(2):121–7.
ПабМед Google ученый
-
Brecx MC, Schlegel K, Gehr P, Lang NP. Сравнение гистологических и клинических параметров при экспериментальном гингивите человека. J Периодонтальная Рез. 1987; 22(1):50–7.
Артикул Google ученый
-
Heasman PA, Collins JG, Offenbacher S. Изменения в щелевой жидкости уровней интерлейкина-1 бета, лейкотриена B4, простагландина E2, тромбоксана B2 и фактора некроза опухоли альфа при экспериментальном гингивите у людей.
 J Периодонтальная Рез. 1993;28(4):241–7.
J Периодонтальная Рез. 1993;28(4):241–7. Артикул Google ученый
-
Кинане Д.Ф., Уинстенли Ф.П., Адоногианаки Э., Могал Н.А. Биоанализ интерлейкина 1 (IL-1) в жидкости десневой борозды человека при экспериментальном гингивите. Arch Oral Biol. 1992;37(2):153–6.
Артикул Google ученый
-
Лейшман С.Дж., Сеймур Г.Дж., Форд П.Дж. Местные и системные воспалительные реакции на экспериментально индуцированный гингивит. Дис маркеры. 2013;35(5):543–9..
Артикул Google ученый
-
Лоос Б.Г., Шенк К., Тиммерман М.Ф., ван дер Вейден Г.А., ван дер Вельден У., Ли М.А. и др. Антитела к S-IgA околоушной слюны при экспериментальном гингивите у курильщиков и некурящих. J Периодонтальная Рез. 2002;37(2):86–92.
Артикул Google ученый
«> -
Ройланд-Босма В., Лием Р.С., Янсен Х.В., ван Дейк Л.Дж., ван дер Виле Л.Т. Клеточные аспекты и влияние на десну у детей с синдромом Дауна при экспериментальном гингивите. Дж. Клин Пародонтол. 1988;15(5):303–11.
Артикул Google ученый
-
Que ML, Andersen E, Mombelli A. Миелоидно-родственный белок (MRP) 8/14 (кальпротектин) и его субъединицы MRP8 и MRP14 при раннем воспалении десен, вызванном зубным налетом. Дж. Клин Пародонтол. 2004;31(11):978–84.
Артикул Google ученый
«> -
Салви Г.Э., Рамсейер К.А., Кандылаки М., Сигрист Л., Аведова Э., Ланг Н.П. Экспериментальный гингивит у курильщиков сигарет: клиническое и микробиологическое исследование. Дж. Клин Пародонтол. 2005;32(5):441–7.
Артикул Google ученый
-
Ли М.А., ван дер Вейден Г.А., Тиммерман М.Ф., Лоос Б.Г., ван Стенберген Т.Дж., ван дер Вельден У. Возникновение Prevotella intermedia и Prevotella nigrescens в связи с гингивитом и здоровьем десен. Дж. Клин Пародонтол. 2001;28(2):189–93.
Артикул Google ученый
«> -
Оздемир Б., Озджан Г., Карадуман Б., Теоман А.И., Айхан Э., Озер Н. и др. Лактоферрин в десневой борозде и периферической крови при экспериментальном гингивите. Евр Джей Дент. 2009;3(1):16–23.
ПабМед ПабМед Центральный Google ученый
-
Aboodi GM, Sima C, Moffa EB, Crosara KTB, Xiao Y, Siqueira WL, et al. Цитопротекторные белки слюны при воспалении и разрешении экспериментального гингивита — экспериментальное исследование. Front Cell Infect Microbiol. 2015;5:92.
ПабМед Google ученый
-
Цаликис Л., Парапанисиу Э.
 , Бата-Кирку А., Полименидес З., Константинидис А. Уровни интерлейкина-1альфа и интерлейкина-1бета в щелевой жидкости при экспериментальном гингивите у молодых и пожилых людей. J Int Acad Periodontol. 2002;4(1):5–11.
, Бата-Кирку А., Полименидес З., Константинидис А. Уровни интерлейкина-1альфа и интерлейкина-1бета в щелевой жидкости при экспериментальном гингивите у молодых и пожилых людей. J Int Acad Periodontol. 2002;4(1):5–11. ПабМед Google ученый
-
Giannopoulou C, Cappuyns I, Mombelli A. Влияние курения на цитокиновый профиль жидкости десневой борозды при экспериментальном гингивите. Дж. Клин Пародонтол. 2003;30(11):996–1002.
Артикул Google ученый
-
Белстром Д., Гранде М.А., Семблер-Моллер М.Л., Киркби Н., Коттон С.Л., Пастер Б.Дж. и др. Влияние пародонтологического лечения на поддесневую и слюнную микробиоту. J Пародонтол. 2018; 89: 531–9.
Артикул Google ученый
-
Сокрански С.С., Хаффаджи А.Д., Куджини М.А., Смит С., Кент Р.Л. Младший. Микробные комплексы в поддесневом налете.
 Дж. Клин Пародонтол. 1998;25(2):134–44.
Дж. Клин Пародонтол. 1998;25(2):134–44. Артикул Google ученый
-
Цаликис Л. Влияние возраста на состав жидкости десневой борозды при экспериментальном гингивите. Пилотное исследование. Open Dent J. 2010; 4:13–26.
Артикул Google ученый
-
Хенскенс Ю.М., Веерман Э.К., Мантел М.С., ван дер Вельден У., Ньюв Амеронген А.В. Цистатины S и C в цельной слюне человека и в железистой слюне при здоровье и заболеваниях пародонта. Джей Дент Рез. 1994;73(10):1606–14.
Артикул Google ученый
-
Jasir A, Kasprzykowski F, Kasprzykowska R, Lindstrom V, Schalen C, Grubb A. Новый противомикробный пептид на основе цистатина C, активный против грамположительных бактериальных патогенов, включая метициллин-резистентный Staphylococcus aureus и полирезистентный коагулазонегативный стафилококк.
 АПМИС. 2003;111(11):1004–10.
АПМИС. 2003;111(11):1004–10. Артикул Google ученый
-
Хенскенс Ю.М., Ван дер Фельден У., Веерман Э.С., Нью-Амеронген А.В. Концентрация белка, альбумина и цистатина в слюне здоровых людей и пациентов с гингивитом или пародонтитом. J Периодонтальная Рез. 1993;28(1):43–8.
Артикул Google ученый
-
Henskens YM, van den Keijbus PA, Veerman EC, Van der Weijden GA, Timmerman MF, Snoek CM, et al. Белковый состав цельной и околоушной слюны здоровых и больных пародонтитом. Определение цистатина, альбумина, амилазы и IgA. J Периодонтальная Рез. 1996;31(1):57–65.
Артикул Google ученый
-
Goncalves Lda R, Soares MR, Nogueira FC, Garcia C, Camisasca DR, Domont G, et al. Сравнительный протеомный анализ цельной слюны больных хроническим пародонтитом.
 J Протеом. 2010;73(7):1334–41.
J Протеом. 2010;73(7):1334–41. Артикул Google ученый
-
Барон А.С., Гански С.А., Райдер М.И., Фезерстоун Д.Д. Ингибирующая активность цистеиновой протеазы и уровни цистатина слюны в цельной слюне пациентов с заболеваниями пародонта. J Периодонтальная Рез. 1999;34(8):437–44.
Артикул Google ученый
-
Grant MM, Creese AJ, Barr G, Ling MR, Scott AE, Matthews JB, et al. Протеомный анализ неинвазивной модели острого воспаления у человека и его разрешения: модель гингивита в течение двадцати одного дня Z1. J Протеом Res. 2010;9(9):4732–44.
Артикул Google ученый
-
Ли М.А., Лоос Б.Г., Хенскенс Ю.М., Тиммерман М.Ф., Веерман Э.К., Ван дер Вельден У. и др. Цистатиновая активность слюны и цистатин С при естественном и экспериментальном гингивите у курильщиков и некурящих.
 Дж. Клин Пародонтол. 2001;28(10):979–84.
Дж. Клин Пародонтол. 2001;28(10):979–84. Артикул Google ученый
-
Кафедра профилактической стоматологии, Академический центр стоматологии Амстердама (ACTA), Университет Амстердама и Свободный университет Амстердама, Амстердам, Нидерланды
Чарифа Земури, Вим Криелаард и 9000 Заура
-
Центр исследований здоровья полости рта, Школа стоматологических наук, Ньюкаслский университет, Фрамлингтон-плейс, Ньюкасл-апон-Тайн, Великобритания
Николас С. Якубович
-
Mars-Wrigley Confectionery, Chicago, IL, USA
Michael Dodds
-
ILSI Europe a.i.s.b.l, Avenue E. Mounier 83 (box 6), Brussels, Belgium
Bettina Schelkle
-
Department of Periodontology , Академический центр стоматологии Амстердама (ACTA), Университет Амстердама и Свободный университет Амстердама, Амстердам, Нидерланды
Бруно Г. Лоос
- Чарифа Земури
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Nicholas S.
 Jakubovics
Jakubovics Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Wim Crielaard
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Egija Zaura
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Michael Dodds
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Bettina Schelkle
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Bruno G. Loos
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
Uitto VJ, Nieminen A, Coil J, Hurttia H, Larjava H. Эластаза ротовой жидкости как показатель здоровья пародонта. Дж. Клин Пародонтол. 1996;23(1):30–7.
Артикул Google ученый
Норман М.Э., Бэни П.С., Цай К.С., Столлер Н., Макартур В.П., Тайчман Н.С. Изучение реакций хозяина при экспериментальном гингивите у людей. II. Изменения реактантов острой фазы, сывороточных иммуноглобулинов и комплемента при развитии воспаления десен. J Периодонтальная Рез. 1979;14(5):361–9.
Артикул Google ученый
Ли М.А., ван дер Вейден Г.А., Тиммерман М.Ф., Лоос Б.Г., ван Стенберген Т.Дж., ван дер Вельден У. Микробиота полости рта у курильщиков и некурящих при естественном и экспериментально индуцированном гингивите. Дж. Клин Пародонтол. 1998;25(8):677–86.
Артикул Google ученый
Адоногианаки Э., Могал Н.А., Муни Дж., Стремя Д.Р., Кинане Д.Ф. Белки острой фазы в жидкости десневой борозды при экспериментально индуцированном гингивите. J Периодонтальная Рез. 1994;29(3):196–202.
Артикул Google ученый
Ссылки на скачивание
Благодарности
Авторы хотели бы поблагодарить д-ра Мануэлу Сайлер и д-ра Лизу Риззетто за их подробные отзывы к предыдущим черновым версиям обзора, а также профессора Брайана Хэнли за поддержку английского языка. правки. Авторы хотели бы поблагодарить Департамент профилактической стоматологии ACTA за их идеи и отзывы о данных и их интерпретации. ILSI Europe содействовала проведению научных встреч и координировала общее управление проектом и административные задачи, связанные с завершением этой работы.
Экспертная группа Целевой группы по функциональным пищевым продуктам выполняла работу, то есть сбор/анализ данных/информации и написание научной статьи отдельно от других видов деятельности Целевой группы. Опубликованное исследование является результатом научной оценки в соответствии со структурой ILSI Europe для обеспечения предконкурентных условий для государственно-частного партнерства (ГЧП). Для получения дополнительной информации об ILSI Europe пишите по адресу [email protected] или звоните по телефону + 32 2 771 00 14. Мнения, выраженные в настоящем документе, и выводы, сделанные в этой публикации, принадлежат авторам и не отражают точку зрения ILSI Europe или компании-участники.
Для получения дополнительной информации об ILSI Europe пишите по адресу [email protected] или звоните по телефону + 32 2 771 00 14. Мнения, выраженные в настоящем документе, и выводы, сделанные в этой публикации, принадлежат авторам и не отражают точку зрения ILSI Europe или компании-участники.
Финансирование
Эта работа была проведена группой экспертов из Целевой группы по функциональным продуктам питания Европейского отделения Международного института наук о жизни (ILSI Europe). Отраслевые члены этой целевой группы перечислены на веб-сайте ILSI Europe по адресу http://ilsi.eu/task-forces/nutrition/functional-foods/. Затраченное на эту работу время экспертам не оплачивается; тем не менее, неотраслевые члены группы экспертов получили небольшую компенсационную сумму (гонорар) и оплату проезда от Целевой группы по функциональным продуктам питания для участия в совещаниях по обсуждению обзора. ILSI Europe не участвовала в разработке исследования, сборе, анализе и интерпретации данных, а также в написании рукописи.
Информация об авторе
Авторы и организации
Авторы
Вклады
WC, NSJ, BGL внесли свой вклад в концепцию или дизайн работы; CZ, NSJ, BGL участвовали в сборе, анализе и интерпретации данных для работы; CZ, NSJ, BS, BGL подготовили документ; М. Д., Э.З., В.К. критически отредактировали статью на предмет интеллектуального содержания; все авторы одобрили окончательную версию рукописи для публикации.
Д., Э.З., В.К. критически отредактировали статью на предмет интеллектуального содержания; все авторы одобрили окончательную версию рукописи для публикации.
Автор, ответственный за переписку
Беттина Шелкле.
Декларации этики
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
Не применимо.
Конкурирующие интересы
Майкл Доддс работает полный рабочий день в компании MARS-Wrigley Confectionary, США. Все остальные авторы заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Дополнительные файлы
Дополнительный файл 1:
Список исключенных исследований и причины исключения (DOCX 53 кб)
Дополнительный файл 2:
Таблица параметров, включенных в окончательный анализ, и их основные функции (DOCX 45 кб)
Дополнительный файл 3:
Резюме дизайна исследования EG включенных исследований, стратифицированных на основе здоровых добровольцев и курящих и некурящих (DOCX 41 kb)
Дополнительный файл 4:
Методологическое качество и потенциальный риск оценка смещения для включенных исследований.
