НМИЦ онкологии им. Н.Н. Блохина
В марте 2021 года 61-летний жительнице подмосковного Ступино Наталье Гуськовой поставили диагноз «рак слизистой оболочки щеки». – Жевала на одну сторону, потому что с другой стороны зубы расшатались, всё некогда было ими заняться – рассказывает женщина, – и эту щёку я постоянно прикусывала. Образовалась ранка. По совету стоматолога полоскала ромашкой, мазала облепиховым маслом. А уж потом сделали биопсию и сказали про рак. Из районного онкодиспансера отправили в Блохина.
– На приёме доктор описал ход операции – нужно будет удалять фрагменты челюсти, я тут же в слёзы, – вспоминает пациентка. – В июне у внучки свадьба, я так хотела увидеть её в фате! Вообще, у меня четверо внуков, но эта старшая и самая любимая. А вдруг я вообще не выживу после операции? И не побываю на свадьбе. А если выживу, что будет с лицом? Как я буду выглядеть на свадьбе? И вообще – может быть, всё ещё само собой рассосётся?
На свадьбе внучки Наталья Алексеевна погуляла от души – была, по её словам, абсолютно счастлива и обо всём плохом просто забыла.
– Пациентка обратилась с уже довольно распространённым процессом, с 3-й стадией рака слизистой оболочки щеки, – говорит заведующий хирургическим отделением опухолей головы и шеи Онкоцентра, д.м.н. Михаил Кропотов. – Процесс локализован в переднем отделе щеки. Была поражена часть губы, опухоль переходила на альвеолярный отросток нижней челюсти, верхняя не пострадала, сустав на месте. На первом этапе больным с этим диагнозом мы всегда выполняем хирургическое лечение и в последующем лучевую или химиолучевую терапию
– Возраст пациентки и её сопутствующие патологии могли повлиять на выбор нашего метода реконструкции, – комментирует реконструктивный хирург отделения опухолей головы и шеи, к.м.н. Оксана Саприна. – Ведь можно восстанавливать челюсть, а можно не восстанавливать.
На подготовительном этапе к реконструктивной операции хирурги отделения опухолей головы и шеи совместно с биоинженерами выполняют компьютерное моделирование по снимкам челюсти пациента. В полном соответствии с формой и размерами челюсти изготавливаются компьютерные модели для резекционных, позиционных шаблонов, при помощи которых хирурги миллиметр в миллиметр сделают разрезы в нужных местах под нужным углом.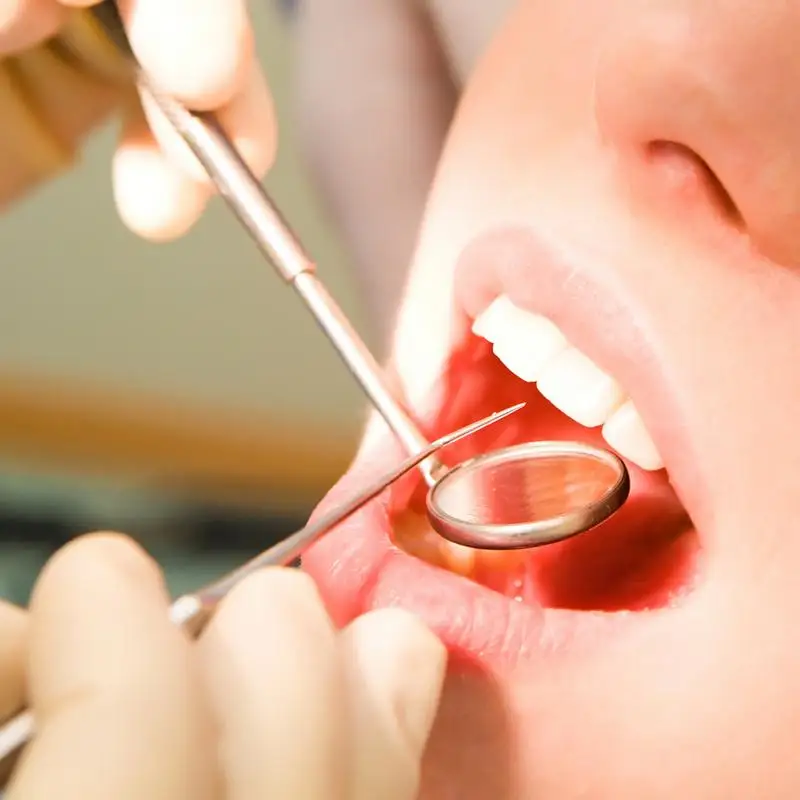
Надрезы на удалённой из ноги малоберцовой кости, сделанные по заранее смоделированным шаблонам, позволят в точности, безошибочно воспроизвести челюсть пациентки. После удаления опухоли и близлежащих тканей кость с кожей и мышцей переносится в зону дефекта, где фиксируется на пластину по индивидуальной форме челюстной дуги и крепится при помощи специальных крошечных винтиков. На шее под микроскопом сшиваются артерии и вены, которые будут питать лоскут и надкостницу, чтобы трансплантированный костный фрагмент был «живым». Крайне сложная процедура забора мягких и костных тканей, моделирования трансплантата, возобновления кровотока в трансплантируемых тканях требует слаженной, отточенной в каждом движении работы всей бригады.
Губа Натальи Алексеевны имела опухолевые поражения внутри, хирурги смогли удалить их так, чтобы эстетически лицо женщины не пострадало. Части зубов на удалённом фрагменте челюсти пришлось лишиться, но со временем зубной ряд можно восстановить при помощи имплантов.
– Несмотря на сложность, сейчас эти операции поставлены на поток, – говорит Оксана Саприна, мы выполняем их еженедельно две с костными трансплантатами, с мягкотканными – три. Пациенты через десять дней реабилитируются – мы удаляем носо-пищеводный зонд, они могут питаться через рот, без зонда, дыхание через естественные пути. Течение послеоперационного периода определяется качеством выполненного хирургического вмешательства. Если лоскут прижился и хорошо подшит к окружающим здоровым тканям, соответственно, вероятность осложнений минимальна. Наша пациентка преодолела этот этап благополучно, патоморфологи дали гистологическое заключение удалённого материала – операция прошла радикально, в краях резекций опухолевых клеток не обнаружено.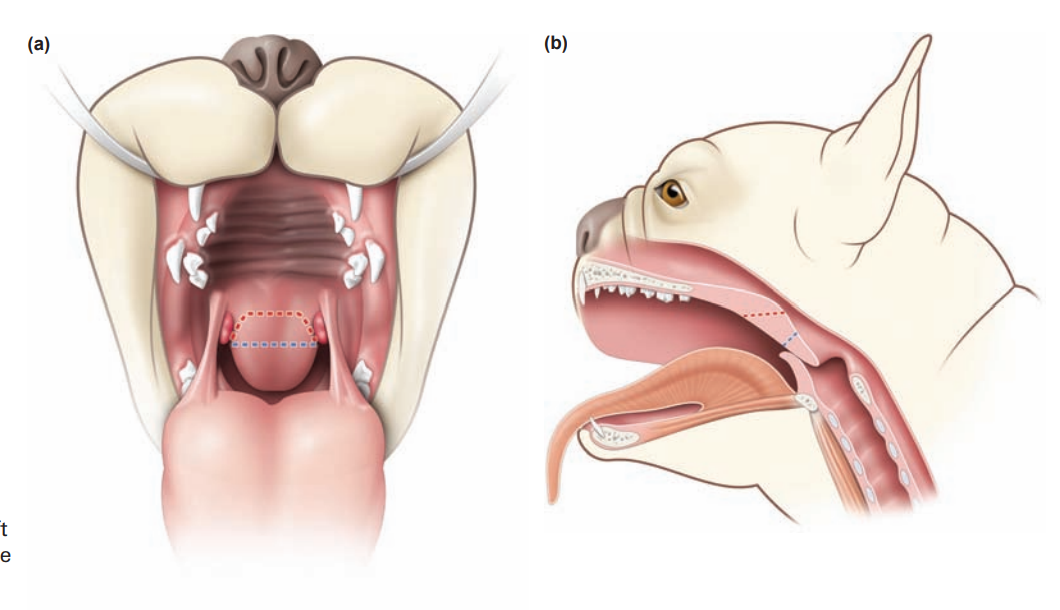
Наталья Алексеевна прихорашивается перед зеркалом. Через две недели после операции ещё сохраняется отёк правой части лица. Но она уже припудрилась, подкрасила ресницы и привела в порядок причёску – благо, в Онкоцентре есть парикмахерская. – Хочу прийти домой красивая, – не может сдержать улыбки женщина. – Муж ждёт. Мы прожили вместе целую жизнь, но любим друг друга так, будто вчера поженились. Плачет всё время, скучает по мне: «Когда же я смогу тебя обнять, моя Наталка!».
– Я вдруг поняла, что значит – просто иметь возможность разговаривать, – признаётся Наталья Гуськова, – какое это счастье! Когда в первые дни после операции дочка за мной ухаживала, я целую тетрадку исписала, говорить-то не могла. Вот думаю – сохранить на память? А зачем она мне, такая память, выброшу я её. Впереди ещё много хороших дней, весна скоро, переедем с мужем на дачу – он пчёлами занимается, я – цветами.
Рак слизистой оболочки органов полости рта (рак языка, дна рта, нижней челюсти, щеки)/губы: современные терапевтические технологии
Ключевые слова
рак полости рта/губы
конформная дистанционная лучевая терапия (КДЛТ)
комбинированное лечение (хирургия, КДЛТ)
брахитерапия (БТ)
сочетанная лучевая терапия (КДЛТ, БТ)
КДЛТ с ФДТ и лазерная гипертермия
Аннотация
Цель — оценка эффективности трех вариантов лечения рака слизистой оболочки органов полости рта (язык, дно рта, щека, нижняя челюсть) и губы (ПР/губы). Материалы и методы. Лечили 100 больных рака ПР/губы: комбинированное лечение с операцией на первом этапе и послеоперационной конформной дистанционной лучевой терапии (КДЛТ) 50 Гр — 40 больных; сочетанная лучевая терапия (ЛТ) — КДЛТ и брахитерапия (БТ) — 40 пациентов; КДЛТ и фотодинамическая терапия (ФДТ) с лазерной гипертермией — 20 больных. Возраст пациентов варьировал от 26 до 90 лет; среди них было 55 мужчин и 45 женщин. Результаты. 5-летняя общая выживаемость (OB) и безрецидивная выживаемость (БВ) у пациентов с опухолями ПР /губы составила 88 и 73,3% соответственно с хорошим качеством жизни. 5-летняя OB составила для комбинированного метода лечения — 82,8%; сочетанной ЛТ — 94,4% и КДЛТ в сочетании с ФДТ и лазерной гипертермией — 83,3% (р=0,561). При опухолях ПР/губы I–II стадии 5-летняя ОВ достигала 94,4%; при III–IV стадии — снижалась до 73,1% с высоким уровнем статистической значимости χ²=6,042; р=0,014.
Выводы. Рак органов ПР/губы наиболее эффективно излечивается в I–II стадии заболевания при реализации хирургического этапа, предшествующего КДЛТ. КДЛТ с ФДТ и лазерной гипертермией эффективны при противопоказаниях для БТ. Определение предиктивных маркеров (ПМ) является перспективным направлением в оптимизации противоопухолевого лечения злокачественных новообразований ПР/губы.
Результаты. 5-летняя общая выживаемость (OB) и безрецидивная выживаемость (БВ) у пациентов с опухолями ПР /губы составила 88 и 73,3% соответственно с хорошим качеством жизни. 5-летняя OB составила для комбинированного метода лечения — 82,8%; сочетанной ЛТ — 94,4% и КДЛТ в сочетании с ФДТ и лазерной гипертермией — 83,3% (р=0,561). При опухолях ПР/губы I–II стадии 5-летняя ОВ достигала 94,4%; при III–IV стадии — снижалась до 73,1% с высоким уровнем статистической значимости χ²=6,042; р=0,014.
Выводы. Рак органов ПР/губы наиболее эффективно излечивается в I–II стадии заболевания при реализации хирургического этапа, предшествующего КДЛТ. КДЛТ с ФДТ и лазерной гипертермией эффективны при противопоказаниях для БТ. Определение предиктивных маркеров (ПМ) является перспективным направлением в оптимизации противоопухолевого лечения злокачественных новообразований ПР/губы.https://doi.org/10.37469/0507-3758-2022-68-1-66-74
Библиографические ссылки
Furniss CS. Human papillomavirus 6 seropositivity is associated with risk of head and neck squamous cell carcinoma, independent of tobacco and alcohol use // Annals of Oncology. 2009;20(3):534–541. doi:10.1093/annonc/mdn643
2009;20(3):534–541. doi:10.1093/annonc/mdn643
Na Im II, Kang HJ, Cho SY et al. EGFR mutations and human papillomavirus in squamous cell carcinoma of tongue and tonsil // Eur. Journ. Cancer. 2007;43(3):520–526. doi:10.1016/ j.ejca.2006.09.025
Tитова В.А. Рак орофарингеальной области — требуется ли смена приоритетов в условиях интенсивной системной бактериально-вирусного воздействия // Голова и шея. 2020;8(3):76–79 [Titova V.A. Cancer of the oropharyngeal region — is a change of priorities required in conditions of intensive systemic bacterial-viral exposure // Head and neck. Russian Journal. 2020;8(3):76–79 (In Russ.)]. doi:10.25792/HN.2020.8.3.76-79
Lindholm P, Valavaara R. Preoperative hyperfractionated accelerated radiotherapy and radical surgery in advanced head and neck cancer: prospective phase II study // Radiother.Onco1. 2006;78(2):146–151. doi:10.1016/j.radonc.2005.11.002
Корытова Л.И., Сокуренко В.П., Масленникова А.В. Современные тенденции в терапии местно-распространенного рака ротоглотки и полости рта. СПб.:Фолиант, 2011 [Korytova LI, Sokurenko VP, Maslennikova AV. Modern trends in the treatment of locally advanced cancer of the oropharynx and oral cavity. Spb.: Foliant, 2011 (In Russ.)].
СПб.:Фолиант, 2011 [Korytova LI, Sokurenko VP, Maslennikova AV. Modern trends in the treatment of locally advanced cancer of the oropharynx and oral cavity. Spb.: Foliant, 2011 (In Russ.)].
Кропотов М.А., Епихина А.В. Хирургические аспекты лечения рака ротоглотки // Опухоли головы и шеи. 2011(2):5–14 [Kropotov MA, Epikhina AV. Surgical aspects of the treatment of oropharyngeal cancer // Head and Neck tumors. 2011(2):5–13 (In Russ.)]. eLIBRARY ID:16542634
 )]. doi:org/10.17 650/2222-1468-2016-6-3-12-21
)]. doi:org/10.17 650/2222-1468-2016-6-3-12-21Решетов И.В., Каприн А.Д, Ратушный М.В и др. Микрохирургическая реконструкция тканей головы и шеи висцеральными аутотрансплантатами, сформированными из мини-доступа // Опухоли головы и шеи. 2015(2):14–19 [Reshetov IV, Kaprin AD, Ratushnyi MV et al. Microsurgical reconstruction of head and neck tissues with visceral autografts formed from mini-access // Head and Neck tumors. 2015(2):14–19 (In Russ.)]. doi:10.17650/2222-1468-2015-5-2-14-19
Setton J, Caria N, Romanyshyn J et al. Intensity-modulated radiotherapy in the treatment of oropharyngeal cancer: an update of the Memorial Sloan-Kettering Cancer Center experience // Int. J. Radiat. Oncol. Biol. Phys. 2012;82(1):291–298. doi:10.1001/ jamaoto. 2013.5892
Романов И.С., Гельфанд И.М., Удинцов Д.Б. Тактика лечения локализованных форм рака слизистой оболочки полости рта // Опухоли головы и шеи. 2016;6(1):43–45 [Romanov IS, Gel’fand IM, Udintsov DB. Tactics of treatment of localized forms of cancer of the oral mucosa // Head and Neck tumors. 2016;6(1):43–45 (In Russ.)]. doi:10.17 650/2222-1468-2016-6-1-43-45
2016;6(1):43–45 (In Russ.)]. doi:10.17 650/2222-1468-2016-6-1-43-45
Чойнзонов Е.Л., Старцева Ж.А., Мухамедов М.Р. и др. Комбинированное лечение местно-распространенного рака гортани и гортаноглотки с применением локальной гипертермии // Сибирский онкологический журнал. 2015(6):13–18 [Choinzonov EL, Startseva ZhA, Mukhamedov MR et al. Combined treatment of locally advanced cancer of the larynx and hypolarynx with the use of local hyperthermia // Siberian Journal of Oncology. 2015(6):13–18 (In Russ.)]. eLIBRARY ID:25055718
Worden FP et al. Efficacy of induction selection chemotherapy vs primary surgery for patients with advanced oral cavity carcinoma // JAMA Otolaryngol Head Neck Surg. 2014;140(2):134–142. doi:10.1001/ jamaoto.2013.5892
Титова В.А., Снигирева Г.П., Петровский В.Ю., Телышева Е.Н. Современные подходы к лучевому лечению опухолей полости рта // Сибирский онкологический журнал. 2016;15(5):47–54 [Titova VA, Snigireva GP, Petrovskiy VYu, Telysheva EN. Modern approaches to radiation treatment of oral tumors // Siberian Journal of Oncology. 2016;15(5):47–54 (In Russ.)]. doi:10.21294/1814-4861-2016-15-5-47-54
2016;15(5):47–54 (In Russ.)]. doi:10.21294/1814-4861-2016-15-5-47-54
Reshetov IV, Sukortseva NS et al. The robotically-assisted oropharyngeal resection // Vestn Otorinolaringol. 2018;83(5):36–39. doi:10.17116/otorino 20188305136
Бойко А.В., Болотина Л.В., Черниченко А.В. и др. Первый опыт лучевой терапии рака орофарингеальной зоны с радиомодификацией цетуксимабом и цисплатином // Современная онкология. 2010;12(2):26–31 [Boiko AV, Bolotina LV, Chernichenko AV et al. The first experience of radiation therapy of cancer of the oropharyngeal zone with radiomodification with cetuximab and cisplatin // Journal of Modern Oncology. 2010;12(2):26–31 (In Russ.)]. doi: modernonco. orscience. ru/1815-1434/article/view/26811
Johnson K. Brachytherapy Boost an Opinion for Base of Tongue Cancer. www/medscape medical news/com. 2013/803037
Замятин О.А., Петровский В.Ю., Вахрамова М.П. и др. Сочетанная лучевая терапия рака языка II–IV стадии в условиях локальной радиомодификации 5-фторурацилом. Российский онкологический журнал. 2004(1):17–21 [Zamyatin. OA, Petrovskiy VYu, Vakhramova MP. et al. Combined radiation therapy of tongue cancer stage II-IV in conditions of local radiomodification with 5-fluorouracil. Russian Oncology Journal. 2004(1):17–21 (In Russ.)]. eLIBRARY ID:17089502
Российский онкологический журнал. 2004(1):17–21 [Zamyatin. OA, Petrovskiy VYu, Vakhramova MP. et al. Combined radiation therapy of tongue cancer stage II-IV in conditions of local radiomodification with 5-fluorouracil. Russian Oncology Journal. 2004(1):17–21 (In Russ.)]. eLIBRARY ID:17089502
Chen WC. Comparison between conventional and intensity-modulated post-operative radiotherapy for stage III and IV oral cavity cancer in terms of treatment results and toxicity // Journ. Oral Oncology. 2009;45: 505–510. PMID:1880547 doi:10.1016/ j.oraloncology.2008.07.002
Titova VA, Charchenko NV, Petrovskiy VY et al. Photodynamic therapy and local interstitial thermotherapy in organ-preserve multimodal treatment of primary and recurrent oral cancer // lntern. J. Brachytherapy. 2008;7(2):158. doi:10.1016/j.brachy. 2008.02.432
Bahassiel M, Ya-Qin Li, Wise-Draper TM et al. A patient-derived somatic mutation in the ephidermal growth factor receptor ligand-binding domain confers increased sensitivity to cetuximab in head and neck cancer // Eur. J Cancer. 2013;49(10):2345–55 doi:10.1016/j.ejca.2013.03.005
J Cancer. 2013;49(10):2345–55 doi:10.1016/j.ejca.2013.03.005
Смирнов В.П., Полихов С.А., Крылова Т.А. и др. Отечественные инновационные медико-технологические возможности дистанционной лучевой терапии и брахитерапии злокачественных опухолей // Медицинская физика. 2021;89(1):94–98 [Smirnov VP, Polikhov SA, Krylova TA et al. Domestic innovative medical and technological possibilities of remote radiation therapy and brachytherapy of malignant tumors // Medical Physics. 2021;89(1):94–98 (In Russ.)].
Титова В.А., Аванесов А.М., Петровский В.Ю. и др. Возможности оптимизации контактной лучевой терапии злокачественных опухолей с использованием индивидуальных фиксирующих систем из современных стоматологических масс. Труды HK РУДН МО РФ, апрель 2014 г [Titova VA, Avanesov AM, Petrovskiy VYu et al. Possibilities of optimization of contact radiation therapy of malignant tumors using individual fixing systems from modern dental masses. Trudy HK RUDN MO RF. aprel’ 2014 g (In Russ.)].
Бржезовский В. Ж., Любаев В.Л., Хасанов Р.А. Выбор тактики лечения при плоскоклеточном раке слизистой оболочки полости рта и ротоглотки // Сибирский онкологический журнал. 2010(3):58–59 [Brzhezovskii VZh, Lyubaev VL, Khasanov RA. The choice of treatment tactics for squamous cell carcinoma of the oral mucosa and oropharynx // Siberian Journal of Oncology. 2010(3):58–59 (In Russ.)]. eLIBRARY ID:15138780
Ж., Любаев В.Л., Хасанов Р.А. Выбор тактики лечения при плоскоклеточном раке слизистой оболочки полости рта и ротоглотки // Сибирский онкологический журнал. 2010(3):58–59 [Brzhezovskii VZh, Lyubaev VL, Khasanov RA. The choice of treatment tactics for squamous cell carcinoma of the oral mucosa and oropharynx // Siberian Journal of Oncology. 2010(3):58–59 (In Russ.)]. eLIBRARY ID:15138780
Это произведение доступно по лицензии Creative Commons «Attribution-NonCommercial-NoDerivatives» («Атрибуция — Некоммерческое использование — Без производных произведений») 4.0 Всемирная.
Copyright (c) 2021 Владимир Солодкий, Георгий Паньшин, Владимир Петровский, Тимур Измайлов, Вера Титова
Плоскоклеточный рак слизистой оболочки щек с вовлечением жевательного пространства: клинический случай
J Korean Assoc Oral Maxillofac Surg. 2017 июнь; 43(3): 191–196.
Опубликовано онлайн 2017 июня 28. doi: 10.5125/jkaom.2017.43.3.191
1 и 1, 2
Информация о авторе. Примечания к сообщению об информации о сообщении о авторском правом и лицензии
Примечания к сообщению об информации о сообщении о авторском правом и лицензии
Squamous Carcinom слизистая оболочка щеки имеет агрессивный характер, так как быстро разрастается и хорошо проникает с высокой частотой рецидивов. Если рак, происходящий из слизистой оболочки щеки, проникает в соседние анатомические структуры, хирургическая резекция опухоли становится более сложной задачей, что вызывает особые соображения относительно реконструкции в зависимости от степени резекции. В данном случае описывается хирургическое лечение 58-летнего мужчины с персистирующим изъязвлением слизистой оболочки и ограничением открывания рта на 11 мм. Диагностическая визуализация выявила опухоль слизистой оболочки щеки, проросшую в ретроантральное пространство вверх с вовлечением переднего края жевательной мышцы в латеральную часть опухоли. В этом отчете мы представляем хирургический доступ, который мы использовали для доступа к жевательному пространству за верхнечелюстной пазухой, и обсуждаем, как справиться с возможным повреждением протока Стенсена во время резекции опухолей слизистой оболочки щеки.
Ключевые слова: Плоскоклеточный рак, Рак полости рта, слизистая оболочка щеки, проток Стенсена
Рак слизистой оболочки щеки преимущественно возникает в окклюзионной плоскости и характеризуется болью и изъязвлением, которые обычно сопровождаются буккальным образованием. Плоскоклеточный рак (SCC) слизистой оболочки щеки встречается редко и составляет примерно 10% всех случаев рака ротовой полости1,2. При исследовании мест развития плоскоклеточного рака полости рта у корейцев слизистая оболочка щек оказалась четвертой по частоте локализацией после нижней челюсти, языка и верхней челюсти3.
SCC слизистой оболочки щеки, как известно, растет быстрее и хорошо проникает с более высокой частотой рецидивов, чем плоскоклеточный рак ротовой полости в других местах. Поэтому плоскоклеточный рак слизистой оболочки щек требует тщательного лечения даже на ранних стадиях4. Слизистая оболочка щек анатомически связана с преддверием верхней и нижней челюсти, ретромолярным треугольником и жевательной мышцей. Таким образом, рак слизистой оболочки щеки может поражать соседние структуры, такие как верхняя и нижняя челюсти, жевательные мышцы и щеки, что часто затрудняет хирургическую резекцию и реконструкцию, особенно когда рак проникает в жевательное пространство; кроме того, еще сложнее, когда открывание рта ограничено. После хирургической резекции опухоли необходима соответствующая реконструкция, чтобы свести к минимуму функциональные и эстетические проблемы.
Таким образом, рак слизистой оболочки щеки может поражать соседние структуры, такие как верхняя и нижняя челюсти, жевательные мышцы и щеки, что часто затрудняет хирургическую резекцию и реконструкцию, особенно когда рак проникает в жевательное пространство; кроме того, еще сложнее, когда открывание рта ограничено. После хирургической резекции опухоли необходима соответствующая реконструкция, чтобы свести к минимуму функциональные и эстетические проблемы.
Здесь мы представляем отчет о клиническом случае, чтобы поделиться нашим опытом лечения пациента с плоскоклеточным раком слизистой оболочки щеки, инфильтрирующим в жевательное пространство. От пациента было получено письменное информированное согласие.
В поликлинику поступил мужчина 58 лет с жалобами на постепенно усиливающийся тризм и болезненную язвенную рану на слизистой оболочке правой щеки, которая не заживает в течение последнего года. Пациент принимал лекарства от гипертонии и тромбоза коронарных артерий и не имел других специфических системных заболеваний. Клинически максимальное открывание рта составляло 11 мм, на слизистой оболочке левой щеки наблюдалось изъязвление, на коже левой щеки пальпировалось плотное образование. Пальпируемой шейной лимфаденопатии не наблюдалось. Пациенту было проведено обследование по поводу подозрения на злокачественное новообразование слизистой оболочки щеки. После визуализирующих тестов была выполнена инцизионная биопсия слизистой оболочки левой щеки, которая подтвердила диагноз SCC. Компьютерная томография (КТ) показала опухоль слизистой оболочки щеки, которая распространялась вверх в ретроантральное пространство и разрушала латеральную стенку верхнечелюстной пазухи, внизу ретромолярный треугольник и латерально на щечную мышцу и передний край жевательной мышцы, без каких-либо признаков. метастазов в шейные лимфатические узлы. () Никаких признаков регионарных или отдаленных метастазов не было обнаружено на основании результатов позитронно-эмиссионной томографии-КТ и других тестов.
Клинически максимальное открывание рта составляло 11 мм, на слизистой оболочке левой щеки наблюдалось изъязвление, на коже левой щеки пальпировалось плотное образование. Пальпируемой шейной лимфаденопатии не наблюдалось. Пациенту было проведено обследование по поводу подозрения на злокачественное новообразование слизистой оболочки щеки. После визуализирующих тестов была выполнена инцизионная биопсия слизистой оболочки левой щеки, которая подтвердила диагноз SCC. Компьютерная томография (КТ) показала опухоль слизистой оболочки щеки, которая распространялась вверх в ретроантральное пространство и разрушала латеральную стенку верхнечелюстной пазухи, внизу ретромолярный треугольник и латерально на щечную мышцу и передний край жевательной мышцы, без каких-либо признаков. метастазов в шейные лимфатические узлы. () Никаких признаков регионарных или отдаленных метастазов не было обнаружено на основании результатов позитронно-эмиссионной томографии-КТ и других тестов.
Открыть в отдельном окне
A. Вид спереди до операции. Обратите внимание на ямочку на левой щеке, которая вызвала подозрение на инвазию подкожного слоя. Б. На контрастной компьютерной томографии выявлена опухоль, распространяющаяся в жевательное пространство и разрушающая стенку левой верхнечелюстной пазухи. C. Наряду с опухолью слизистой оболочки щеки при магнитно-резонансной томографии выявлена латерально распространяющаяся опухоль в области (стрелка) подкожного слоя.
Вид спереди до операции. Обратите внимание на ямочку на левой щеке, которая вызвала подозрение на инвазию подкожного слоя. Б. На контрастной компьютерной томографии выявлена опухоль, распространяющаяся в жевательное пространство и разрушающая стенку левой верхнечелюстной пазухи. C. Наряду с опухолью слизистой оболочки щеки при магнитно-резонансной томографии выявлена латерально распространяющаяся опухоль в области (стрелка) подкожного слоя.
Хирургическая тактика была следующей: поскольку опухоль распространилась на жевательное пространство за верхнечелюстной пазухой и присутствовал тризм, хирургический доступ к этой ограниченной опухоли стал более сложным; таким образом, мы использовали технику поворота нижней челюсти в сочетании с модифицированным разрезом Вебера-Фергюсона для доступа к опухоли. Соответственно, мандибулотомия была выполнена в области между № 33 и № 34 после расщепления нижней губы, и разрез был продлен до левой поднижнечелюстной области. Разрез над верхней губой продлевали до наружной ринотомии до уровня на 1 см ниже медиального угла глазной щели слева. Разрез кожи был продолжен во внутриротовой вестибулярный разрез, а верхний и нижний щечные лоскуты были подняты после выполнения поднадкостничной диссекции на верхней и нижней челюсти. С помощью этого доступа было получено широкое обнажение подвисочного пространства, необходимого для хирургической резекции.
Разрез кожи был продолжен во внутриротовой вестибулярный разрез, а верхний и нижний щечные лоскуты были подняты после выполнения поднадкостничной диссекции на верхней и нижней челюсти. С помощью этого доступа было получено широкое обнажение подвисочного пространства, необходимого для хирургической резекции.
Резекция единым блоком была выполнена с запасом прочности 1 см, поскольку опухоль слизистой оболочки щеки распространилась на ретроантральное пространство, ретромолярный треугольник и жевательную мышцу за пределы щечной мышцы с подозрительной инвазией в подкожный слой щеки. В единую массу были включены прилегающие к опухоли участки верхнечелюстной пазухи от венечного отростка нижней челюсти до нижней области ретромолярного треугольника и кожи щеки. На предоперационной визуализации были отмечены признаки метастазирования шейных лимфатических узлов. Для оценки края опухоли и регионарных метастазов шеи во время операции был изучен диагноз замороженных срезов, который был отрицательным на злокачественность.
Открыть в отдельном окне
Хирургический доступ и объемная резекция. Был выполнен модифицированный разрез Вебера-Фергюсона без латерального удлинения на верхней челюсти в сочетании с рассечением нижней губы с мандибулотомией, а затем щечный лоскут был отогнут латерально, чтобы обеспечить достаточную экспозицию латеро-задней части верхнечелюстной пазухи.
После хирургической резекции сквозной дефект орофациальной области восполнен свободным лоскутом с двойной лопастью широчайшей мышцы спины. Накладывали анастомоз конец в конец между верхней щитовидной артерией и торакодорсальной артерией, анастомоз конец в бок накладывали между ветвью внутренней яремной вены и торакодорсальной веной.
Послеоперационный период у пациента был хорошим, без каких-либо отклонений от нормы клинических и лабораторных показателей. Однако желтоватые выделения через дренаж области шеи наблюдались с 5-х суток после операции и продолжались в течение нескольких дней. Пациент жаловался на тупую боль в левой преаурикулярной области, но при ежедневном допплеровском исследовании лоскут казался хорошо перфузируемым без признаков подозрительного послеоперационного воспаления. Мы считали боль задержкой слюны и перевариванием тканей вытекшей слюной, просачивающейся из поврежденного протока Стенсена. Поэтому мы выполнили релокацию протока Стенсена на 12-е сутки после операции. Был идентифицирован разорванный проток, и после установления проходимости просвета в проток была вставлена обрезанная трубка, и трубка была закреплена на слизистой оболочке верхней губы таким образом, чтобы слюна могла попасть в полость рта. После дутопластики на левую лицевую область накладывали давящую повязку. Слюноотделение через трубку возобновилось, боли у больного прекратились, желтоватые выделения прекратились ()). После завершения послеоперационной лучевой терапии урезанная трубка удалена.
Пациент жаловался на тупую боль в левой преаурикулярной области, но при ежедневном допплеровском исследовании лоскут казался хорошо перфузируемым без признаков подозрительного послеоперационного воспаления. Мы считали боль задержкой слюны и перевариванием тканей вытекшей слюной, просачивающейся из поврежденного протока Стенсена. Поэтому мы выполнили релокацию протока Стенсена на 12-е сутки после операции. Был идентифицирован разорванный проток, и после установления проходимости просвета в проток была вставлена обрезанная трубка, и трубка была закреплена на слизистой оболочке верхней губы таким образом, чтобы слюна могла попасть в полость рта. После дутопластики на левую лицевую область накладывали давящую повязку. Слюноотделение через трубку возобновилось, боли у больного прекратились, желтоватые выделения прекратились ()). После завершения послеоперационной лучевой терапии урезанная трубка удалена.
Открыть в отдельном окне
A. В проксимальную культю разорванного стенсенова протока введена вырезанная трубка. B. Возобновление слюноотделения через трубку, закрепленную в полости рта, и клиническая симптоматика улучшилась.
B. Возобновление слюноотделения через трубку, закрепленную в полости рта, и клиническая симптоматика улучшилась.
До выписки не сообщалось о послеоперационных осложнениях, таких как инфицирование области хирургического вмешательства или некроз лоскута. Никаких проблем, связанных с произношением или жеванием, не было отмечено, и пациент мог перейти на обычную диету. Тризм разрешился с максимальным открытием рта 34 мм. Кроме того, на донорском участке не наблюдалось специфического функционального дефицита плеча. () На основании заключительного отчета о патологии край резекции закрылся в медиальной и задней областях массы без метастазов в регионарные лимфатические узлы; впоследствии плановая послеоперационная лучевая терапия проводилась без дальнейшей резекции.
Открыть в отдельном окне
Вид спереди через 1 месяц после операции. Наблюдалась асимметрия лица за счет двухлопастной реконструкции со свободным лоскутом широчайшей мышцы спины, но ожидается постепенная атрофия лоскута. B. Максимальное открывание рта через 1 месяц после операции. Тризм разрешился. C. Пациент мог свободно двигать левым плечом и не жаловался на дискомфорт в донорской зоне.
B. Максимальное открывание рта через 1 месяц после операции. Тризм разрешился. C. Пациент мог свободно двигать левым плечом и не жаловался на дискомфорт в донорской зоне.
Слизистая оболочка щеки Известно, что ПКР агрессивен по своей природе по сравнению с раком ротовой полости других локализаций. Сообщалось, что он имеет плохой местный контроль и 5-летнюю выживаемость по конкретным причинам при карциномах на ранней стадии по сравнению с карциномами полости рта, языка и дна рта4. Зарегистрированная частота рецидивов плоскоклеточного рака слизистой оболочки щеки составляет от 30% до 80%5,6,7,8,9, 10. Таким образом, достижение адекватного хирургического края резекции имеет решающее значение во время хирургической резекции. На ранних стадиях, когда рак ограничен слизистой оболочкой щеки и подслизистой областью, в край резекции рекомендуется включать щечную мышцу. Если поражение распространяется за пределы подслизистой области на щечную мышцу, следует рассмотреть возможность резекции, включая щечное пространство. Когда в подкожной клетчатке отмечаются положительные края, следует выполнить широкую резекцию, включая кожу. Профилактическая диссекция шеи рекомендуется даже при опухолях размером от 2 до 4 см, потому что при распространенном раке слизистой более вероятно развитие латентных метастазов даже при отсутствии клинических метастазов в регионарных лимфатических узлах11. Сообщалось, что местный контроль улучшается при послеоперационной лучевой терапии на ранней стадии рака слизистой оболочки щеки12.
Когда в подкожной клетчатке отмечаются положительные края, следует выполнить широкую резекцию, включая кожу. Профилактическая диссекция шеи рекомендуется даже при опухолях размером от 2 до 4 см, потому что при распространенном раке слизистой более вероятно развитие латентных метастазов даже при отсутствии клинических метастазов в регионарных лимфатических узлах11. Сообщалось, что местный контроль улучшается при послеоперационной лучевой терапии на ранней стадии рака слизистой оболочки щеки12.
Жевательное пространство содержит медиальную и латеральную крыловидную мышцу, жевательную мышцу, височную мышцу, вертикальную ветвь и височно-нижнечелюстной сустав. Через это пространство проходит третья ветвь тройничного нерва и его ветви, а внутренняя верхнечелюстная артерия с ее ветвями проходит через это пространство и входит в крылонебную ямку13. Несколько пространств контактируют с жевательным пространством, например, щечное и ретроантральное пространства спереди, парафарингеальное пространство медиально и околоушное пространство латерально.
Для резекции опухолей в этом пространстве было введено несколько хирургических подходов. Разрез Weber-Ferguson и его модификации были введены в качестве переднего доступа к верхней челюсти, но эти методы имеют недостатки, так как разделение верхней челюсти выполняется вслепую, а доступ к задней части верхней челюсти ограничен. Лицевой разрез и костный дефект не эстетичны и имеют тот недостаток, что приходится жертвовать несколькими более глубокими структурами. Был предложен латеральный подход Conley с продолжением преаурикулярного разреза до шеи вторым поднижнечелюстным разрезом, но он имеет недостатки лицевого разреза и костного дефекта, а также жертвует внутренними глубокими структурами14. Позже Castro et al.13 пересмотрели этот метод и опубликовали подход к лечению злокачественных опухолей жевательного пространства через преаурикулярный разрез и трансцервикальный разрез; однако этот метод также требует обхода стволов лицевого нерва для доступа к внутренним новообразованиям. Dingman и Conley15 представили нижний доступ через поднижнечелюстной разрез, который включал расщепление губы по средней линии и расширение кзади к сосцевидному отростку. После горизонтальной остеотомии восходящей ветви нижней челюсти, ретракции верхней части наружу и ретракции нижней части вниз возможен прямой доступ к крыловидно-верхнечелюстной области14. Spiro et al.16 сообщили, что нижнечелюстной «качающийся» доступ, включающий разрез с расщеплением губы, расширенный до ментально-сосцевидной части, и срединную мандибулотомию с паралингвальным расширением, обеспечивает адекватный доступ для резекции опухолей ротоглотки.
Dingman и Conley15 представили нижний доступ через поднижнечелюстной разрез, который включал расщепление губы по средней линии и расширение кзади к сосцевидному отростку. После горизонтальной остеотомии восходящей ветви нижней челюсти, ретракции верхней части наружу и ретракции нижней части вниз возможен прямой доступ к крыловидно-верхнечелюстной области14. Spiro et al.16 сообщили, что нижнечелюстной «качающийся» доступ, включающий разрез с расщеплением губы, расширенный до ментально-сосцевидной части, и срединную мандибулотомию с паралингвальным расширением, обеспечивает адекватный доступ для резекции опухолей ротоглотки.
В нашем случае злокачественное новообразование, развившееся на слизистой оболочке щеки, прорастало в жевательное пространство, что сопровождалось тризмом, что затрудняло оперативный доступ. Поэтому мы переняли предыдущие хирургические подходы и модифицировали их, сделав упор на получение адекватного поля зрения жевательного пространства. Был выполнен модифицированный разрез Вебера-Фергюсона без латерального удлинения века на верхней челюсти с расщеплением нижней губы до поднижнечелюстной области с использованием продолжающегося внутриротового вестибулярного разреза. В последующем, после выполнения мандибулотомии, верхний щечный лоскут верхней челюсти и нижний щечный лоскут нижней челюсти отодвигали кнаружи. С помощью этого доступа можно получить прямой обзор боковых и задних аспектов верхней челюсти и анатомических структур, расположенных медиальнее ветви нижней челюсти. Это позволило выполнить полную хирургическую резекцию с адекватным запасом прочности, сократить время операции и лучше контролировать кровотечение из внутренней верхнечелюстной артерии и ее ветвей или крыловидного сплетения. С эстетической точки зрения этот подход может минимизировать рубцы на средней части лица, не удлиняя латеральный разрез века; кроме того, рубцы в поднижнечелюстной области практически не видны при естественном положении головы. Более того, поскольку разрез был сделан по линии складки пациента, большая часть рубцов была скрыта в морщинах.
В последующем, после выполнения мандибулотомии, верхний щечный лоскут верхней челюсти и нижний щечный лоскут нижней челюсти отодвигали кнаружи. С помощью этого доступа можно получить прямой обзор боковых и задних аспектов верхней челюсти и анатомических структур, расположенных медиальнее ветви нижней челюсти. Это позволило выполнить полную хирургическую резекцию с адекватным запасом прочности, сократить время операции и лучше контролировать кровотечение из внутренней верхнечелюстной артерии и ее ветвей или крыловидного сплетения. С эстетической точки зрения этот подход может минимизировать рубцы на средней части лица, не удлиняя латеральный разрез века; кроме того, рубцы в поднижнечелюстной области практически не видны при естественном положении головы. Более того, поскольку разрез был сделан по линии складки пациента, большая часть рубцов была скрыта в морщинах.
Предложены различные лоскуты, которые могут быть использованы для закрытия сквозного дефекта полости рта после хирургической резекции, в том числе свободный лучевой отдел предплечья, дельтопектальный, большой грудной, свободный широчайшей мышцы спины, мышечно-кожный поперечный прямой мышцы живота и мышечно-кожный трапециевидный закрылки 17,18,19,20. Свободный лоскут широчайшей мышцы спины представляет собой богато васкуляризированную мышцу с наибольшей потенциальной площадью поверхности, обеспечивающую достаточный объем и покрытие любого дефекта ротовой и челюстно-лицевой области. Более того, этот лоскут имеет то преимущество, что позволяет первично закрыть донорский участок, что может предотвратить дополнительные осложнения19.. Если складчатый лоскут прикрыт орофациальным дефектом, он может выглядеть менее эстетично из-за большого объема, но по мере уменьшения объема лоскута со временем результаты становятся более эстетичными17,18. В предыдущем исследовании сообщалось об уменьшении объема примерно на 20% в случаях реконструкции с помощью лоскута широчайшей мышцы спины после удаления опухоли, а также о дополнительной жировой и мышечной атрофии у пациентов, получавших послеоперационную лучевую терапию19. Следовательно, необходимо учитывать послеоперационную атрофию лоскута, например, преднамеренную гиперкоррекцию во время реконструкции лоскута.
Свободный лоскут широчайшей мышцы спины представляет собой богато васкуляризированную мышцу с наибольшей потенциальной площадью поверхности, обеспечивающую достаточный объем и покрытие любого дефекта ротовой и челюстно-лицевой области. Более того, этот лоскут имеет то преимущество, что позволяет первично закрыть донорский участок, что может предотвратить дополнительные осложнения19.. Если складчатый лоскут прикрыт орофациальным дефектом, он может выглядеть менее эстетично из-за большого объема, но по мере уменьшения объема лоскута со временем результаты становятся более эстетичными17,18. В предыдущем исследовании сообщалось об уменьшении объема примерно на 20% в случаях реконструкции с помощью лоскута широчайшей мышцы спины после удаления опухоли, а также о дополнительной жировой и мышечной атрофии у пациентов, получавших послеоперационную лучевую терапию19. Следовательно, необходимо учитывать послеоперационную атрофию лоскута, например, преднамеренную гиперкоррекцию во время реконструкции лоскута.
Проток Стенсена начинается от передней части околоушной железы и проходит впереди через передний край жевательной мышцы. На уровне жевательной мышцы проток направляется внутрь, проникая через щечную жировую ткань и щечную мышцу, образуя отверстие сосочка в слизистой оболочке щеки на уровне второго моляра верхней челюсти. Длина протока составляет примерно 7,0 см, и его расположение можно оценить, проведя линию, соединяющую козелок с средней частью верхней губы21.
Повреждения околоушной железы и протока обычно лечат путем восстановления травмы, установки стента в проток и наложения давящей повязки. Если стент вводят после повреждения околоушного протока, его обычно удаляют через 1 неделю. При тяжелом повреждении железы и ее протока рекомендуется перевязка проксимального отдела протока, при этом железа постепенно атрофируется22. Известно, что стриктуры, отек щек, свищи и обструктивный сиалоаденит могут возникать, если проток перерезан без пластики23.
Вышеупомянутые принципы лечения повреждений протока околоушной железы можно аналогичным образом применять после резекции доброкачественных или злокачественных новообразований слизистой оболочки щеки. Deygles и соавт.24 сообщили об успешных результатах введения внутривенного катетера в околоушный проток и активации слюнооттока на 1 неделю после хирургической резекции фиброэпителиальной гиперплазии слизистой оболочки правой щеки. Longo et al.25 сообщили, что после резекции плоскоклеточного рака слизистой оболочки щеки был установлен и удален ангиокатетер через 10 дней, что позволило сохранить функцию околоушной железы без каких-либо осложнений. Кроме того, Mehta et al.23 сообщили, что частота возникновения сиалоцеле и паротита в раннем послеоперационном периоде была значительно снижена за счет канюляции внутривенного катетера и изменения маршрута околоушного протока после хирургической резекции рака слизистой оболочки щеки.
Deygles и соавт.24 сообщили об успешных результатах введения внутривенного катетера в околоушный проток и активации слюнооттока на 1 неделю после хирургической резекции фиброэпителиальной гиперплазии слизистой оболочки правой щеки. Longo et al.25 сообщили, что после резекции плоскоклеточного рака слизистой оболочки щеки был установлен и удален ангиокатетер через 10 дней, что позволило сохранить функцию околоушной железы без каких-либо осложнений. Кроме того, Mehta et al.23 сообщили, что частота возникновения сиалоцеле и паротита в раннем послеоперационном периоде была значительно снижена за счет канюляции внутривенного катетера и изменения маршрута околоушного протока после хирургической резекции рака слизистой оболочки щеки.
Мы также подтвердили, что выделения желтоватого цвета прекратились, а клинические симптомы значительно улучшились после введения обрезанной трубки в проток Стенсена и реактивации околоушного слюноотделения с последующим наложением давящей повязки. Поэтому мы рекомендуем включать процесс сохранения функции околоушной железы на этапе планирования хирургического вмешательства, если край резекции слизистой оболочки щеки включает определенные отделы околоушного протока.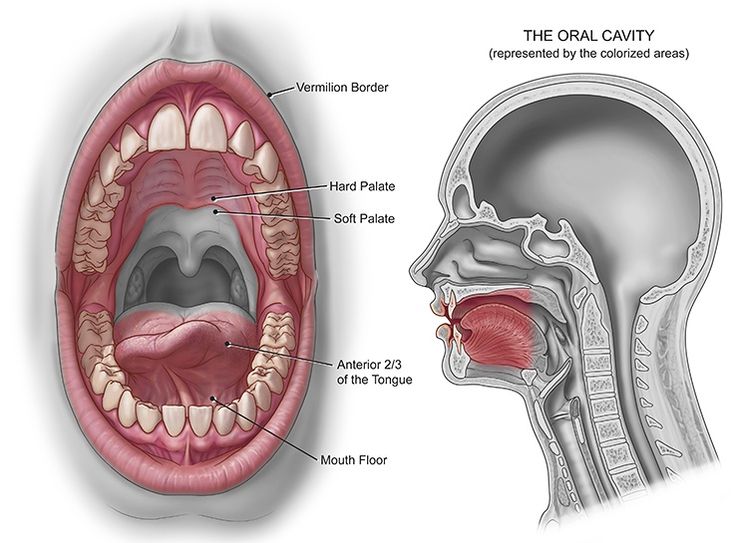
Таким образом, плоскоклеточный рак слизистой оболочки щек агрессивен, быстро растет и имеет высокую частоту рецидивов; поэтому требуется тщательное лечение, даже если рак находится на ранней стадии. Если выявлена опухоль ≥T2, рекомендуется профилактическая диссекция шеи, а послеоперационная лучевая терапия может быть полезна для местного контроля. В данном случае модифицированный разрез Верхней челюсти по Веберу-Фергюсону в сочетании с нижнечелюстным поворотным доступом способствовал адекватному обнажению поражения в жевательном пространстве, был процедурой, позволяющей сэкономить время, и обеспечил приемлемые эстетические результаты после операции. Тем не менее, также необходимо учитывать сохранение функции околоушных желез из-за повреждения протока Стенсена во время операции по поводу рака слизистой оболочки щеки путем выполнения простой процедуры стенсеновской дуктопластики.
Конфликт интересов: О потенциальном конфликте интересов, имеющем отношение к этой статье, не сообщалось.
1. Шах Дж.П., Сендон Р.А., Фарр Х.В., Стронг Э.В. Карцинома полости рта. факторы, влияющие на неэффективность лечения в первичной локализации и на шее. Am J Surg. 1976; 132: 504–507. [PubMed] [Google Scholar]
2. Vegers JW, Snow GB, van der Waal I. Плоскоклеточный рак слизистой оболочки щеки. Обзор 85 дел. Арка Отоларингол. 1979; 105: 192–195. [PubMed] [Академия Google]
3. Кук С.К., Ким Б.К., Юн Х.Дж., Хонг С.Д., Хун С.П., Ли Джи. Исследование возраста и локализации плоскоклеточного рака полости рта в Корее. Корейский J Oral Maxillofac Pathol. 2015; 39: 393–402. [Google Scholar]
4. Lin CS, Jen YM, Cheng MF, Lin YS, Su WF, Hwang JM, et al. Плоскоклеточный рак слизистой оболочки щеки: агрессивный рак, требующий комплексного лечения. Шея головы. 2006; 28: 150–157. [PubMed] [Google Scholar]
5. Блум Н.Д., Спиро Р.Х. Карцинома слизистой щеки. Ретроспективный анализ. Am J Surg. 1980;140:556–559. [PubMed] [Google Scholar]
6. Конли Дж., Садояма Дж. А. Плоскоклеточный рак слизистой оболочки щек. Обзор 90 дел. Арка Отоларингол. 1973; 97: 330–333. [PubMed] [Google Scholar]
А. Плоскоклеточный рак слизистой оболочки щек. Обзор 90 дел. Арка Отоларингол. 1973; 97: 330–333. [PubMed] [Google Scholar]
7. Lapeyre M, Peiffert D, Malissard L, Hoffstetter S, Pernot M. Оригинальный метод брахитерапии в лечении эпидермоидных карцином слизистой оболочки щеки. Int J Radiat Oncol Biol Phys. 1995; 33: 447–454. [PubMed] [Google Scholar]
8. Pop LA, Eijkenboom WM, de Boer MF, de Jong PC, Knegt P, Levendag PC, et al. Оценка результатов лечения плоскоклеточного рака слизистой оболочки щеки. Int J Radiat Oncol Biol Phys. 1989;16:483–487. [PubMed] [Google Scholar]
9. Strome SE, To W, Strawderman M, Gersten K, Devaney KO, Bradford CR, et al. Плоскоклеточный рак слизистой оболочки щеки. Отоларингол Head Neck Surg. 1999; 120:375–379. [PubMed] [Google Scholar]
10. Urist MM, O’Brien CJ, Soong SJ, Visscher DW, Maddox WA. Плоскоклеточный рак слизистой оболочки щек: анализ прогностических факторов. Am J Surg. 1987; 154: 411–414. [PubMed] [Google Scholar]
11. Хаким А.Х., Прадхан С.А., Тубачи Дж., Каннан Р. Результат перорального широкого иссечения локализованного плоскоклеточного рака T1-2 N0 слизистой оболочки щеки — анализ 156 случаев. Ларингоскоп. 2013; 123:177–180. [PubMed] [Академия Google]
Хаким А.Х., Прадхан С.А., Тубачи Дж., Каннан Р. Результат перорального широкого иссечения локализованного плоскоклеточного рака T1-2 N0 слизистой оболочки щеки — анализ 156 случаев. Ларингоскоп. 2013; 123:177–180. [PubMed] [Академия Google]
12. Sieczka E, Datta R, Singh A, Loree T, Rigual N, Orner J, et al. Рак слизистой оболочки щек: являются ли края и Т-стадия точными предикторами локального контроля? Am J Отоларингол. 2001; 22: 395–399. [PubMed] [Google Scholar]
13. Castro J, Likhterov I, Mehra S, Bassiri-Tehrani M, Scherl S, Clain J, et al. Подход к резекции единым блоком и реконструкции первичных злокачественных новообразований жевательного пространства. Ларингоскоп. 2016; 126:372–377. [PubMed] [Google Scholar]
14. Погрел М.А., Каплан М.Дж. Хирургический доступ к крыловидно-верхнечелюстной области. J Oral Maxillofac Surg. 1986;44:183–187. [PubMed] [Google Scholar]
15. Дингман Д.Л., Конли Дж. Боковой доступ к крыловидно-верхнечелюстной области. Энн Отол Ринол Ларингол. 1970; 79: 967–969. [PubMed] [Google Scholar]
1970; 79: 967–969. [PubMed] [Google Scholar]
16. Spiro RH, Gerold FP, Strong EW. Нижнечелюстной «качающийся» доступ при опухолях полости рта и ротоглотки. Хирургия головы и шеи. 1981; 3: 371–378. [PubMed] [Google Scholar]
17. Welvaart K, Caspers RJ, Verkes RJ, Hermans J. Выбор между хирургической резекцией и лучевой терапией для пациентов с раком пищевода и кардии: ретроспективное сравнение двух методов лечения. Дж. Хирург Онкол. 1991;47:225–229. [PubMed] [Google Scholar]
18. Хираки А., Ямамото Т., Йошида Р., Нагата М., Кавахара К., Накагава Ю. и др. Факторы, влияющие на изменение объема кожно-мышечных лоскутов при раке ротовой полости. Int J Oral Maxillofac Surg. 2016;45:1395–1399. [PubMed] [Google Scholar]
19. Li BH, Jung HJ, Choi SW, Kim SM, Kim MJ, Lee JH. Свободный лоскут широчайшей мышцы спины (LD) и реконструктивная пластина, используемые для обширной челюстно-нижнечелюстной реконструкции после удаления опухоли. J Краниомаксиллофак Хирург. 2012;40:e293–е300. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
20. Yang ZH, Zhang DM, Chen WL, Wang YY, Fan S. Реконструкция сквозных дефектов полости рта с помощью складчатого удлиненного вертикального мышечно-кожного лоскута нижнего трапециевидного острова. Br J Oral Maxillofac Surg. 2013;51:731–735. [PubMed] [Google Scholar]
21. Haggerty CJ, Laughlin RM. Атлас оперативной челюстно-лицевой хирургии. Эймс: Издательство Wiley-Blackwell; 2015. [Google Scholar]
22. Van Sickels JE. Лечение травм околоушной железы и протоков. Oral Maxillofac Surg Clin North Am. 2009 г.;21:243–246. [PubMed] [Google Scholar]
23. Мехта С., Агравал Дж., Деван А.К., Прадхан Т. Перемещение околоушного протока при резекции рака слизистой оболочки щеки. J Craniofac Surg. 2014; 25:1746–1747. [PubMed] [Google Scholar]
24. Deygles C, Jr, Medeiros R, Carvalho EJ, Carvalho AA. Катетеризация Стенонова протока для хирургического удаления оральной фиброэпителиальной гиперплазии. Браз Дж. Оториноларингол. 2012;78:141. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Longo B, Germano S, Laporta R, Belli E, Santanelli F. Перемещение протока Стенсена после резекции опухоли слизистой оболочки щеки. J Craniofac Surg. 2012; 23:e250–e251. [PubMed] [Академия Google]
Карцинома и слизистая оболочка полости рта
Рак и слизистая оболочка полости рта | Причины, симптомы и лечение
Что такое карцинома слизистой оболочки щеки?
Слизистая оболочка щек – это слизистая оболочка щек и задней части губ, внутри, где они соприкасаются с зубами. Развитие раковых клеток или опухоли в этой области приводит к карциноме слизистой оболочки щеки, которая …
- Симптомы
- Причины
- Риски
- Профилактика
Симптомы
Симптомы и признаки карциномы слизистой оболочки щек:
- Красная или белая опухоль или пятна во рту или на слизистой щек.
- Рана или поражение во рту, склонное к кровотечению.

- Припухлость или любое плотное образование во рту.
- Боль во время еды и питья.
- Постоянная боль в горле и охриплость.
- Дискомфорт или трудности при глотании или жевании.
- Боль в ухе.
- Затрудненное движение языка или челюсти.
- Онемение языка.
- Опухшие челюсти.
Показать больше Показать меньше
Причины
Некоторые распространенные причины рака слизистой оболочки щеки:
- Употребление табака.
- Чрезмерное употребление алкоголя.
- Слабая иммунная система.
- Вирус папилломы человека (ВПЧ).
Показать больше Показать меньше
Риски
Некоторые распространенные риски карциномы слизистой оболочки рта:
- Ксеростомия.
- Кожная реакция.
- Мукозит.
- Разрушение раны.
- Дисгевзия.
- Гипотиреоз.
- Миелит спинного мозга.
Показать больше Показать меньше
Профилактика
Ниже приведены некоторые методы, которые можно использовать для предотвращения болезни:
- Борьба с алкоголем.

- Сексуальная гигиена.
- Не курить и не употреблять табак.
- Хорошая гигиена полости рта.
- Здоровое питание.
Показать больше Скрыть
Как это диагностируется?
Первым этапом диагностики является общий медицинский осмотр пораженных и близлежащих участков. Диагностика также включает в себя понимание перенесенных заболеваний пациента, общий осмотр…
Первым этапом диагностики является общий физикальный осмотр пораженных и близлежащих участков. Диагностика также включает в себя понимание прошлых болезней пациента, общее обследование здоровья, использование лекарств и другие подобные аспекты, которые помогают практикующему врачу получить представление об общем состоянии здоровья.
-
Blood tests
-
X-rays
-
CT scan
-
MRI scan
-
Fine needle aspiration biopsy
-
PET scan
-
Хирургия
-
Лучевая терапия
Консультации с опытными врачами
Д-р Теджиндер Катариа
Председатель
Радиационная онкология
Просмотр профиля
Доктор Ашок Кумар Вайд
Председатель
Медицинский и хемато онкология
Профиль
Доктор Jyoti Wadhwa
Старший директор — Медицинская Oncology & Haemato-oncologol
. Просмотреть профиль0003
Просмотреть профиль0003
Номер мобильного телефона:
Код проверки:
Пользователь соглашается и признает, что Пользователь прочитал, понял и принимает положения и условия, содержащиеся в брошюре, прилагаемой к Устройству («Устройство ») в отношении его использования. , эксплуатация, возврат/замена и гарантийная политика.
Настоящим Пользователь соглашается и признает, что Устройство (аппаратное и программное обеспечение), используемое при предоставлении
услуг Medanta предоставляется на условиях «как есть» и «по мере доступности» через Alivecor India Private.
Ограничено. Меданта никоим образом не поддерживает и не продвигает Устройство, а также не несет ответственности.
за любые претензии, заверения или гарантии, явные или подразумеваемые, в отношении безопасности, надежности,
долговечность и производительность устройства.
Когда-то использованные услуги не могут быть отменены, за исключением случаев, когда Пользователь просит отменить
услугу в день покупки, в этом случае полная сумма платы за услугу возвращается Пользователю. при условии, что Устройство не распаковывалось.
при условии, что Устройство не распаковывалось.
До истечения срока действия услуги Пользователь может продлить услуги, воспользовавшись различными программами
опции. Для указанных целей Пользователь может позвонить по номеру нашей горячей линии +91 124 4141414 или посетить сайт www.medanta.org. Расширенная программа, которой воспользовался Пользователь, активируется автоматически по истечении срока действия существующей программы услуг.
В случаях, когда Пользователь решил воспользоваться Услугами через арендованное Устройство, возвращаемый депозит
Сумма в размере 5000 ₹ (« Сумма депозита ») применяется и оплачивается Пользователем. Возврат депозита
Сумма подлежит возврату Устройства в рабочем и неповрежденном состоянии. Возврат депозита
Сумма должна быть внесена тем же способом оплаты, что и при покупке, в случаях, когда Пользователь
лично посещает Меданту для возврата Устройства. Если Пользователь решит вернуть Устройство по почте,
Сумма депозита будет возвращена в электронном виде через НЕФТЬ или банковским переводом через Medanta в течение
семь (7) рабочих дней с момента получения Устройства и получения отсканированного изображения/копии Аннулированного
Чек банковского счета Пользователя.
