лечение опущения, причины и диагностика — ROOTT
Классификация Причины рецессии Диагностика и последствия рецессии Методы лечения Профилактика
Рецессия десны — процесс убыли тканей десны, при котором обнажается шейка корня зуба. Визуально это выглядит так: за счёт оголения прикорневой части, зубы кажутся длиннее, а на краю десны образуется небольшая бороздка. Повышается чувствительность зубов к кислому, сладкому, соленому и перепадам температуры. Рецессия десны может наблюдаться как в зоне одного зуба, так и нескольких. Однако для установления точного диагноза нужно обратиться в стоматологию.
Классификация
В зависимости от сохранения ткани десны существует 4 стадии рецессии дёсен:
- На первой стадии уменьшается только прикрепленная часть десны. Уменьшение объёма ткани незначительно.
- Разрушается область прикреплённой десны, но костная и десневая ткани сохраняются, повышается чувствительность зубов.

- На третьем этапе обнажается внешняя поверхность зуба, чувствительность зубов становится болезненной.
- Зуб оголяется по периметру, в том числе в месте межзубных промежутков.
Опущение десны — это постепенный процесс. В большинстве случаев он вызван определённым стоматологическим заболеванием. Десна истончается и уменьшается, в результате чего появляется подвижность зубов, расшатывание, что может привести к их потере.
Причины опущения десен
Причинами рецессии десны могут являться различные факторы. Самодиагностика — первый шаг к выявлению проблемы, чтобы не расплачиваться за невнимательность слишком высокой ценой. Ниже приведены самые распространённые причины рецессии:
- неправильная гигиена полости рта. Например, слишком агрессивная чистка зубов: использование жесткой зубной щетки, механические повреждения во время ухода за зубами;
-
отсутствие ухода за полостью рта.
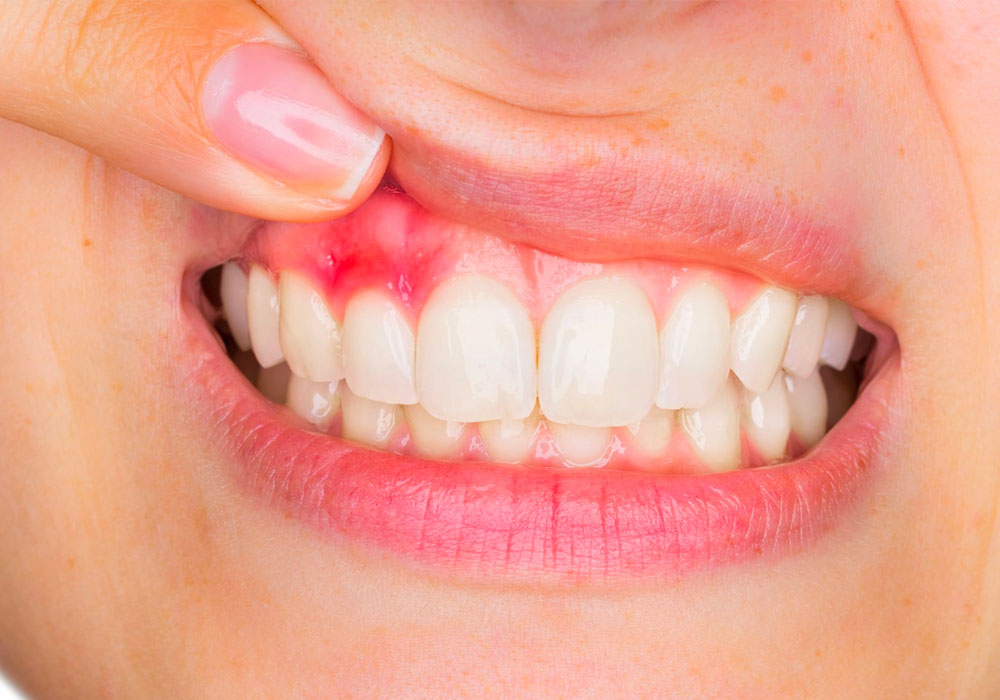 Если не счищать зубной налёт, это приведёт к образованию зубного камня, а он в свою очередь является причиной заболевания дёсен и их рецессии;
Если не счищать зубной налёт, это приведёт к образованию зубного камня, а он в свою очередь является причиной заболевания дёсен и их рецессии; - пародонтоз. Это заболевание десён часто сопровождается их рецессией. Если вовремя не заняться лечением — это приведёт к потере зубов;
- естественное старение организма;
- вредные привычки: кусание губ и ногтей, прикусывание ручки, карандашей, курение;
- травматичное, неаккуратное лечение зубов, в том числе процедура отбеливания.
Помимо этого, предрасполагающими факторами могут быть особенности строения ротовой полости, челюсти (патология прикуса, расположение отдельных зубов, укороченные уздечки губ и так далее) и соматические заболевания (метаболический синдром, сахарный диабет, прочее).
Диагностика и последствия рецессии дёсен
Своевременная диагностика рецессии десны способствует скорейшему устранению проблемы и предотвращению развития неприятных последствий.
- десна покраснела и воспалилась;
- некоторые зубы выглядят длиннее остальных;
- между корнями зубов появились щели, которые продолжают увеличиваться;
- появилась высокая чувствительность зубов;
- присутствует неприятный запах изо рта.
При обнаружении одного или нескольких признаков необходимо срочно обратиться к врачу-стоматологу, чтобы незамедлительно начать лечение опущения десны. В противном случае, помимо физического дискомфорта, увеличивается риск развития кариеса и пульпита. Происходит это из-за активного размножения бактерий в прикорневой части зуба, где эмаль имеет наименьшую толщину. В конечном счете, если пустить процесс на самотек, это приведет к расшатыванию зубов и даже их потере.
Чем больше запущено заболевание, тем сложнее лечение и сильнее возрастает стоимость такой операции.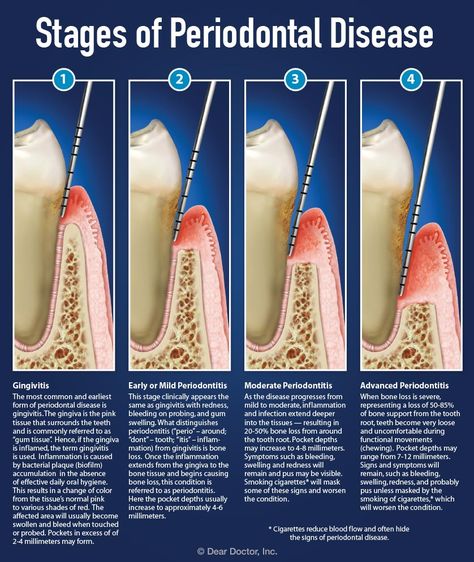 Поэтому тянуть с визитом в клинику не стоит.
Поэтому тянуть с визитом в клинику не стоит.
Лечение рецессии десны
В зависимости от степени опущения десны существует несколько способов лечения:
- Медикаментозное. Данный способ лечения применим при первой и второй стадиях. Лечащим врачом назначается курс антибиотиков или препараты для укрепления иммунитета, снятия воспаления, улучшения кровообращения. Сюда же можно отнести полоскание рта различными лекарственными настойками, втирание в десны медикаментов (гели, мази).
- Физиотерапия. В основном это процедуры, направленные на улучшение кровообращения десен и их питания. А именно: массаж десен, токотерапия, лазерная терапия, ультрафиолетовое излучение.
- Плазмолифтинг. В данном случае в десну вводится состав, полученный из крови пациента. Плазма содержит уникальные компоненты, которые помогают скорейшему восстановлению тканей.
-
Хирургическое вмешательство. К такому способу относится лоскутная операция, при которой производится закрытие рецессии десны с помощью среза ткани десны и очищения корневых дентальных каналов.
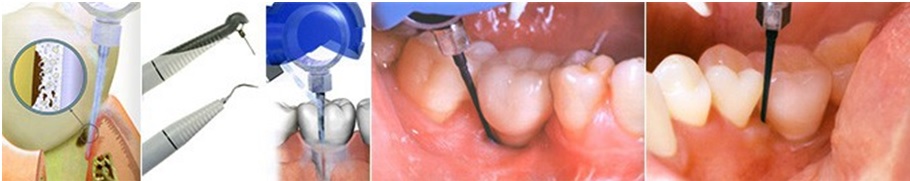 В некоторых случаях снимается слой здорового нёба, чтобы восстановить недостающую часть биоматериала. По завершении лоскутной операции часто возникает необходимость провести дополнительную процедуру, которая называется — пластика при рецессии десны. Она нужна для того, чтобы восстановить естественный внешний вид десны. Это довольно простые и быстрые манипуляции, которые полностью восстанавливают эстетику улыбки.
В некоторых случаях снимается слой здорового нёба, чтобы восстановить недостающую часть биоматериала. По завершении лоскутной операции часто возникает необходимость провести дополнительную процедуру, которая называется — пластика при рецессии десны. Она нужна для того, чтобы восстановить естественный внешний вид десны. Это довольно простые и быстрые манипуляции, которые полностью восстанавливают эстетику улыбки. - Регенерация. Хирургическая процедура, позволяющая наращивать поврежденные мягкие ткани. Сначала проводится очищение оголенного участка над линией десен, затем накладывается материал, который стимулирует восстановление тканей. Например, мембрана или трансплантат. Это способствует росту десневой кости и ткани на поврежденном участке. Далее десну фиксируют к корню зуба.
Сочетание вышеперечисленных методов обеспечат быстрое восстановление ткани десен при рецессии и исключат повторное развитие.
Профилактика развития рецессии десны
Как и любое заболевание, опущение или рецессию десен проще и дешевле предотвратить, чем думать, как остановить уже начавшийся процесс. Все вышеописанные методы устранения рецессии десны не понадобятся, если своевременно осуществлять профилактику данного заболевания. А именно:
Все вышеописанные методы устранения рецессии десны не понадобятся, если своевременно осуществлять профилактику данного заболевания. А именно:
- ежегодно делать профессиональную чистку зубов от зубного камня;
- совершать ортодонтическое лечение в случае наличия неправильного прикуса;
- проводить тщательную ежедневную гигиену полости рта;
- избегать травмирования и кровотечения десен.
Очень важно не допускать развития воспалений и присоединения инфекции в ротовой полости. Для этого необходимо использовать препараты с противовоспалительным действием в качестве средств для полоскания или чистки зубов.
При должном уходе ваши зубы и десны прослужат вам долгие десятилетия и не доставят хлопот.
причины возникновения, симптомы, методы лечения
Рецессия десны является сопутствующей патологией при заболеваниях тканей пародонта. Может возникнуть в любом возрасте: у детей, взрослых, пожилых людей. Патология обусловлена уменьшением объема слизистой рта, при которой обнажается шейка зуба.
Область, где коронковая часть переходит в корень зуба, не имеет верхнего слоя эмали. Поэтому при оголении шейки зуба участок становится чувствительным к любому механическому и химическому воздействию. И, как следствие, больше подвержен влиянию патогенной микрофлоры.
Заболевание создает больше не физический, а психологический дискомфорт. Нарушение эстетики зубного ряда, особенно в зоне улыбке, доставляет массу неудобств. Человек теряет уверенность в себе, находится в постоянном стрессе. Это только ускоряет развитие патологии.
О причинах заболевания и способах лечения поговорим в данной статье.
Предпосылки
Практически все патологии слизистой связаны со здоровьем организма в целом. Рецессия десны – не исключение. На развитие заболевания может повлиять множество факторов. Основными причинами являются:
- Снижение иммунитета, ухудшение обмена веществ и кровообращения.
- Дефекты зубного ряда и аномалии прикуса. Патология характерна для глубокого и открытого прикуса, а также при сильной скрученности зубов.
- Возрастная атрофия мягких тканей ротовой полости. Рецессия чаще появляется у пожилых людей.
- Плохая гигиена полости рта. Это основная причина заболеваний десен и зубов. Мягкий и твердый налет провоцируют воспалительные процессы в тканях пародонта. Это приводит к опущению десны, атрофии костной ткани, расшатыванию и выпадению зубов.
Рецессия может возникнуть при травмировании слизистой оболочки. А также при непрофессиональном ортодонтическом лечении. Если брекет-систему установили неправильно, десны сдавливаются постоянной чрезмерной нагрузкой, что вызывает постепенное истончение мягких тканей и некорректное смещение зубов.
Аналогичная ситуация при некачественной установке искусственной коронки. Край протеза будет «нависать» над десной и повреждать ее.
Симптоматика
Визуально рецессию десны можно обнаружить только в запущенной форме, когда обнажается шейка зуба. Более ранние симптомы схожи с другими заболеваниями десен – гингивитом и пародонтитом. Диагностироваться рецессию может только стоматолог на профосмотре.
Первыми признаками, при обнаружении которых следует обратиться к врачу, является воспаление, отек и кровоточивость десен, повышенная чувствительность зубов, оголение корня зуба.
Виды рецессии десны
Рецессию десны разделяют по нескольким параметрам: локализация, степень опущения слизистой, видимость, причины развития.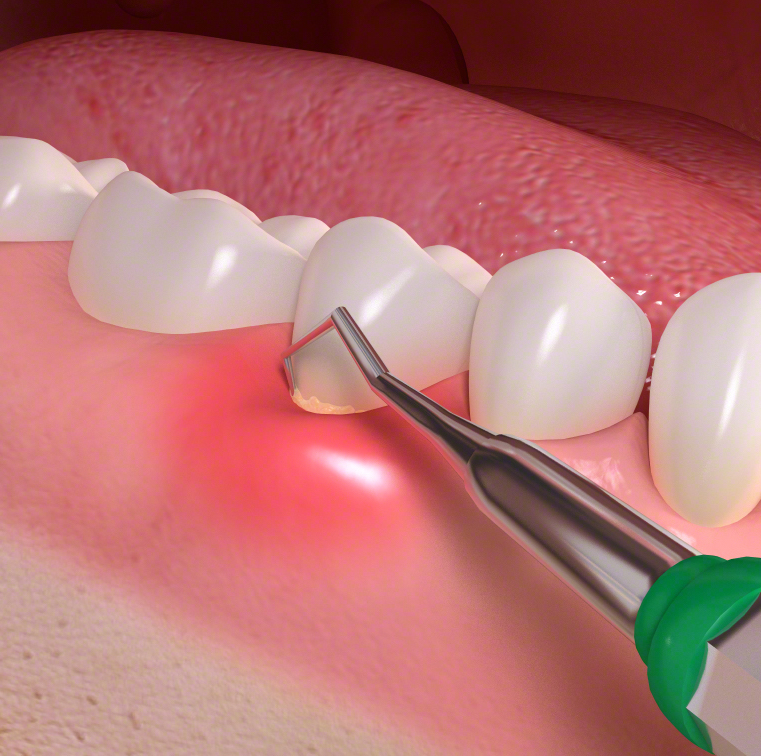 В первом случае заболевание может развиваться локально, вокруг 1-2 зубных единиц. Или распространиться на весь зубной ряд.
В первом случае заболевание может развиваться локально, вокруг 1-2 зубных единиц. Или распространиться на весь зубной ряд.
По степени убывания десны различают легкую, среднюю и тяжелую форму рецессии. В легкой форме корень зуба обнажается до 3 мм, в средней – 3-5 мм, в тяжелой – более 5 мм.
Развитие заболевания может быть визуально заметно. Или иметь скрытую форму и диагностироваться только при помощи процедуры зонирования.
Причина появления рецессии также классифицирует заболевание по трем видам:
- Симптоматическая. Возникает локально, на одном зубе. Или в мягких тканях в межзубных промежутках. Отличие этого вида рецессии десны от других – острые воспалительные процессы и большое скопление зубных отложений. В процессе развития болезни десна меняет цвет, появляется отек и кровоточивость. Постепенно возникают десневые карманы, что приводит к подвижности зубов. Этот вид рецессии развивается на фоне основных заболеваний десен: гингивита, пародонтита, пародонтоза.

- Физиологическая. Обусловлена возрастными изменениями организма. Как правило, появляется после 60 лет. Характерные признаки: поражение всей поверхности десны, значительное оголение шейки зуба, клиновидное форма зубных единиц. В данном случае воспалительные процессы в слизистой рта отсутствуют, поэтому верхушки корней плотно держатся в лунках зубов.
- Травматическая. Возникает вследствие получения челюстно-лицевой травмы. В месте поражения мягкая ткань уплотняется, и вызывает смещение десны до 3 мм. Может задействовать резцы, верхние клыки и премоляры. У пациента наблюдается повышенная чувствительность зубов. Воспалений и отечности десен нет. Зубных отложений также не наблюдается (при соответствующей гигиене полости рта).
Важно: вредные привычки, такие как курение и употребление алкоголя, увеличивают риск развития патологических процессов в деснах. Связано это с нарушением кровотока в мягких тканях ротовой полости, спазму и разрушению сосудов. А также с чрезмерным скоплением бактериального налета и общим снижением иммунитета.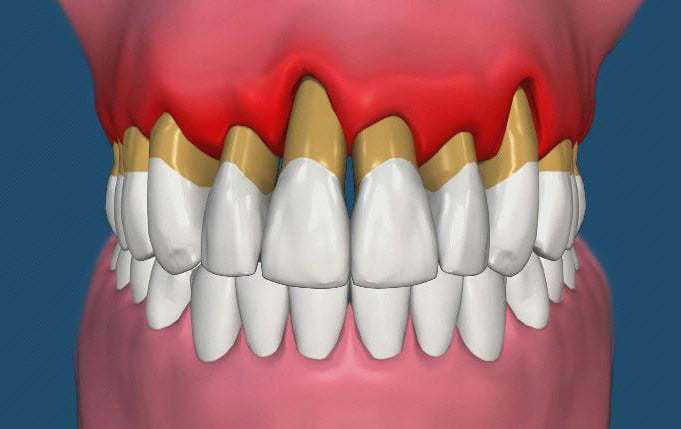
Специализированная классификация
Более ранним описанием рецессии десны считается классификация Миллера, предложенная доктором в 1985 году. Определяющими параметрами патологии является высота и ширина десны в динамике. Высота измеряется от эмали на стыке с корнем зуба, до края десны. Ширина – между убывающими тканями слизистой.
Также учитывается состояние мягких тканей и положение межзубных сосочков. Для понимания вопроса нужно знать, что десна бывает свободной и прикрепленной. В первом случае это светло-розовая внешняя оболочка вокруг зубов. Прикрепленная десна находится за свободной и плотно прилегает к поверхности зуба. Итак, классификация по Миллеру:
- Первая стадия. Опущение свободной десны. Межзубная ткань без изменений.
- Вторая стадия. Рецессия прикрепленной десны. Межзубные сосочки по-прежнему не затронуты.
- Третья стадия. Незначительное опущение десны. Костная ткань практически не повреждена.

- Четвертая стадия. Сильное опущение десны, в том числе в межзубном пространстве, атрофия костной ткани.
Важно понять, что вылечить рецессию десны на ранних стадиях гораздо проще и быстрее. В запущенных формах период восстановления будет долгим и дорогим. Помимо эстетического дискомфорта при отсутствии терапии может добавиться риск возникновения подвижности и потери зубов. К последствиям болезни без лечения относится клиновидный эффект, нарушение прикуса, развитие кариеса на нижней границы эмали, хрупкость зубов.
Профессиональная гигиена полости рта
Профессиональная чистка зубов является важным этапом при лечении любого заболевания ротовой полости. Качественное удаление зубных отложений помогает устранить воспалительные процессы в слизистой. А при лечении гингивита и пародонтита профгигиена является неотъемлемой частью терапии. Без этой процедуры устранить данные заболевания просто невозможно.
Аппаратная чистка зубов предотвращает появление пародонтальных карманов, выравнивает край десны, снижает отечность и кровоточивость десен.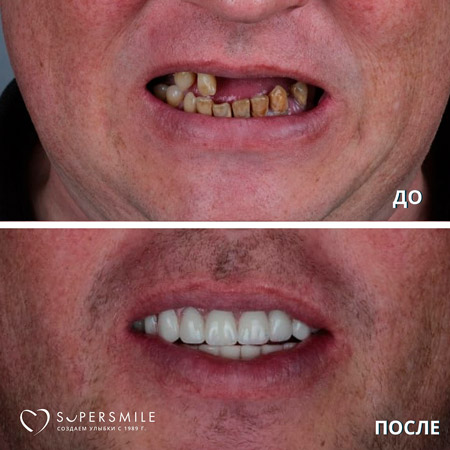
При лечении рецессии профгигиена является подготовительным этапом для основной терапии.
Терапия
Устранить рецессию в большинстве случаев можно только при помощи хирургического вмешательства. Терапевтические и неинвазивные методики обычно не эффективны. Лечебные препараты могут использоваться в ходе терапии, но как вспомогательные средства. Например, в качестве восстановительной терапии.
Главная задача стоматолога во время операции – выравнивание края десны и закрытие оголенной шейки зуба. Бояться не нужно – операция не сложная, проводится под местной анестезией и не требует длительной реабилитации.
Среди методик хирургического устранения рецессии десны выделяют следующие:
- Однослойные. Лоскутные операции, с трансплантацией здоровых тканей слизистой.
- Двухслойные. Приживление донорского лоскута мягкой ткани с наложением на соединительную здоровую ткань, которую врач берет с других участков ротовой полости.

- Регенерация. Приживление специальной мембраны, которая способствует активному восстановлению десны.
До проведения пластики важно устранить сопутствующие патологии: клиновидный эффект зубов, наличие кариозных полостей. Если рецессия развилась из-за нарушения прикуса, то сначала ортодонт устраняет первопричину патологии, и затем приступает к лечению.
Трансплантация тканей
Наиболее востребованной при лечении рецессии десны является лоскутная методика. Операция имеет самый короткий и безболезненный реабилитационный период.
Суть процедуры в следующем. Здоровую мягкую ткань для пересадки врач берет с участка в ротовой полости, где ее достаточно. Как правило, используется та же десна, где есть рецессия. В этом случае разница в оттенке десны практически не заметна.
Отсоединенный лоскут стоматолог накладывает на пораженную область слизистой. Если мягкой ткани не хватает, врач может взять часть биоматериала с твердого нёба.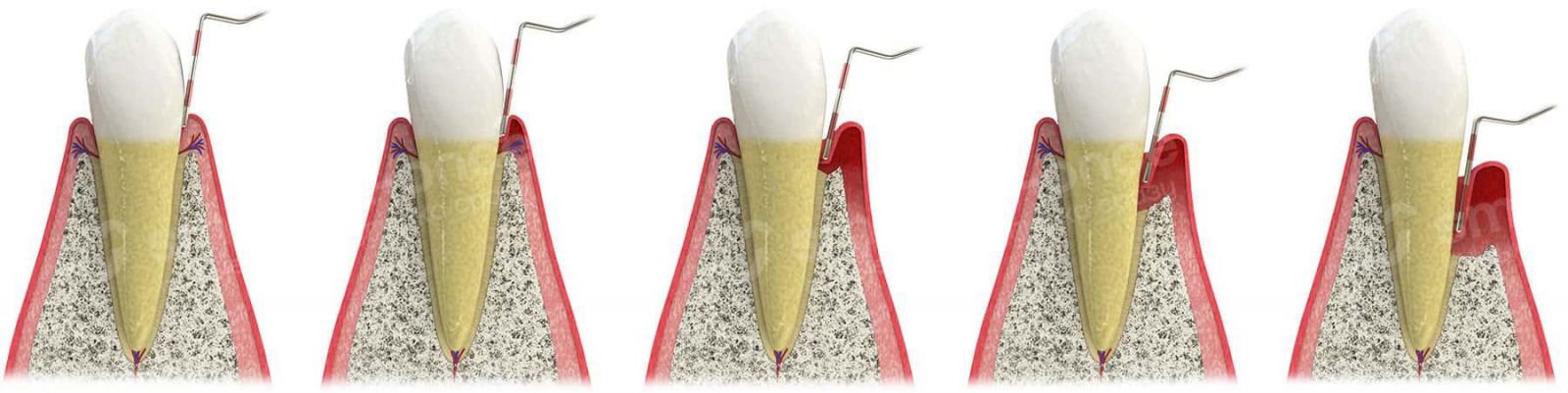
Вся процедура состоит из трех этапов:
- Устранение воспалений в слизистой рта.
- Профессиональная чистка зубов.
- Трансплантация мягких тканей на пораженный участок.
К недостаткам этой методики можно отнести разницу в цвете десны, если лоскут брали с нёба. А также небольшой дискомфорт на участке слизистой, где брали мягкую ткань для трансплантации. Для коррекции цвета десны используется композиционный материал, который полностью выравнивает оттенок.
Установка мембраны
Другая методика устранения рецессии десны – регенерация мягкой ткани. Суть процесса – фиксация мембраны, которая способствует активному росту клеток. Мембраны бывают резорбируемые и нерезорбируемые. Во втором случае после закрытия рецессии десны мембрану необходимо извлечь. То есть провести еще одну операцию. В первом случае мембрана остается в слизистой. Однако эффективность данного способа чуть ниже.
Преимущества процедуры регенерации:
- Отсутствие рецидивов.
 Заболевание больше не будет беспокоить пациента (при надлежащей гигиене полости рта).
Заболевание больше не будет беспокоить пациента (при надлежащей гигиене полости рта). - Короткий период реабилитации.
- Нет дискомфорта и повышенной чувствительности слизистой к внешнему воздействию после операции.
Хирургического вмешательства при лечении рецессии можно избежать только на ранних стадиях патологии. Благодаря длительной терапии ткани пародонта полностью восстанавливаются. В качестве стимулирующего фактора используется методика купирования, с применением коллагена. Также для регенерации мягких тканей применяются белковые препараты, которые дополнительно укрепляют эмаль зубов. После лечения восстанавливается кровоток и обменные процессы в слизистой рта.
Профилактические меры
Никому не хочется заниматься затяжным и не самым приятным лечением. Развитие рецессии десны можно избежать, если соблюдать несложные рекомендации.
Главное правило – своевременное посещение стоматолога для осмотра и проведения профессиональной гигиены.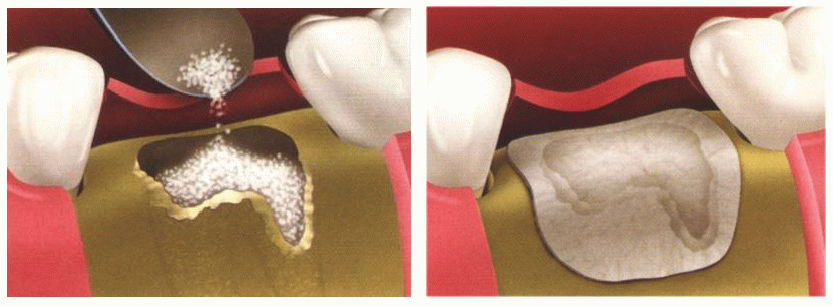 Это поможет выявить заболевание на ранних стадиях, а также исключить возникновение других патологий полости рта. Оптимальная периодичность – раз в полгода.
Это поможет выявить заболевание на ранних стадиях, а также исключить возникновение других патологий полости рта. Оптимальная периодичность – раз в полгода.
Второй важный момент – качественная ежедневная гигиена ротовой полости. Использовать зубную щетку нужной жесткости и пасту по рекомендации врача. Полоскать рот водой после каждого приема пищи. Не забывать использовать зубную нить, флосс и ирригатор для очищения межзубного пространства и массажа десен. Пройти обучение у стоматолога, как правильно чистить зубы, чтобы не травмировать слизистую.
Также нужно позаботиться о своем рационе, включить больше свежей, натуральной пищи. Убывания десны и оголения шейки зуба можно избежать, если отказаться от вредных привычек: курения, алкоголя, чрезмерного употребления сахара, кофе и черного чая. Важно заботиться о своем здоровье, принимать витамины в межсезонье, вовремя лечить возникающие заболевания. При первых признаках патологии зубов или десен обратиться к врачу.
Домашние варианты лечения
Использование народных методов не способно устранить рецессию десны.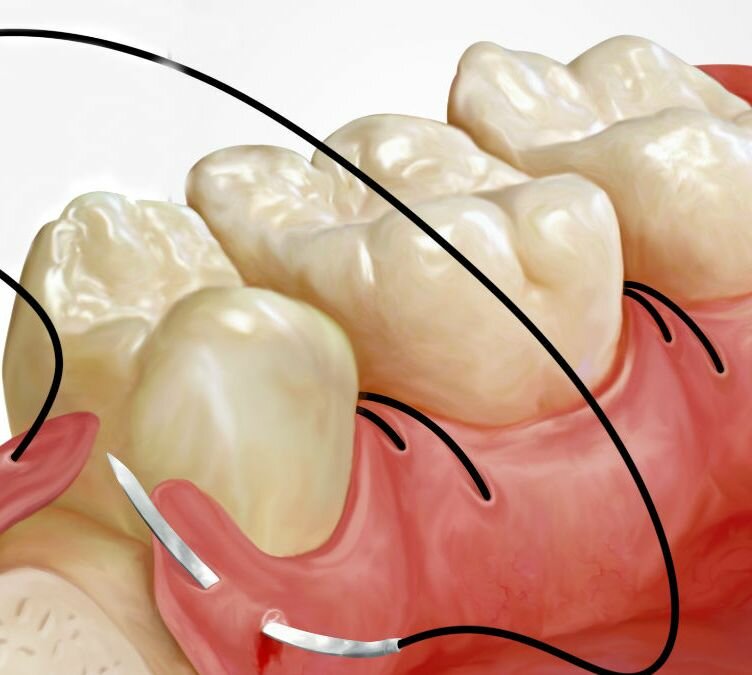 Однако это является хорошей профилактикой заболеваний тканей пародонта. К наиболее эффективным профилактическим мерам в домашних условиях относятся:
Однако это является хорошей профилактикой заболеваний тканей пародонта. К наиболее эффективным профилактическим мерам в домашних условиях относятся:
- Полоскание рта настоем прополиса. Для полоскания применяется спиртовой раствор не более 10%, в разбавленном виде, согласно инструкции. Также для массажа десен эффективно использовать мед.
- Для полоскания рта можно сделать простой раствор с добавлением чайной ложки соды и щепотки соли на стакан воды. Процедуру проводить минимум 2 раза в день, после чистки зубов.
- Массаж десен также можно проводить с применением морской соли.
Снять отечность, воспаление и кровоточивость десен помогают отвары трав: ромашки, коры дуба, календулы и шалфея.
Важно помнить, что домашняя терапия является частью комплексного лечения под наблюдение квалифицированного врача-стоматолога. Если у вас появились симптомы заболевания десен, необходимо в кратчайшие сроки обратиться за стоматологической помощью. И не заниматься самолечением.
И не заниматься самолечением.
В клиниках ЭспаДент первичный осмотр и аппаратная диагностика осуществляется бесплатно. К вашим услугам врачи высшей категории, а также современное профессиональное оборудование, которое позволяет выявить даже скрытые патологии челюсти.
Стоимость лечения пациент узнает сразу после окончания осмотра и постановки диагноза, без скрытых платежей и доплат. На дорогостоящие услуги в наших клиниках действует беспроцентная рассрочка.
Также для пациентов доступны приятные спецпредложения на различные виды стоматологического лечения. Например, «замороженная» цена на профессиональную чистку зубов.
В связи со сложной эпидемиологической ситуацией, специалисты клиник ЭспаДент принимают все необходимые меры для безопасного приема пациентов. Наши врачи работают в средствах индивидуальной защиты (маска, очки, медицинская одежда). Помещения клиник регулярно проветриваются и дезинфицируются, проводится влажная уборка.
Наши врачи проходят регулярный осмотр, 2 раза в день, на наличие симптомов вируса. Пациенты принимаются строго по записи, без очередей и ожидания на ресепшене. Мы делаем все, чтобы профессиональное стоматологическое лечение было доступным и комфортным для наших пациентов.
Пациенты принимаются строго по записи, без очередей и ожидания на ресепшене. Мы делаем все, чтобы профессиональное стоматологическое лечение было доступным и комфортным для наших пациентов.
Статья была проверена: Галюк (Кирсанова) Наталия Михайловна
Если вам понравился этот пост — поделитесь им со своими друзьями и подписчиками.
Закрытие рецессии десны
Что такое рецессия десны?
Рецессия – это уменьшение объема, фактически – убыль десны, которая приводит к оголению шейки и корней зуба. Рецессии в области фронтальных зубов портит вид улыбки, формирует у пациента привычку не улыбаться, т. к. негативно сказывается на психологическом состоянии, а при неправильном лечении может остаться у человека до конца жизни.
Рецессия десны может проявляться в области одного, нескольких зубов и даже всей челюсти.
Почему возникает рецессия десны?
Десна может начать убывать в результате нескольких причин:
- Воспаление пародонта.
- Постоянные травмы при зубной гигиене вследствие нарушение техники чистки зубов, использования жесткой зубной щетки.
- Аномалии уздечек и слизистых тяжей.
- Неправильный прикус.
Как происходит лечение (закрытие) рецессии десны?
Закрытие рецессии десны проводят в несколько этапов.
I Подготовительный этап лечения.
На этом этапе нужно убрать факторы, которые рецессию десны вызывают:
- Необходимо пройти профессиональную гигиену полости рта, чтобы убрать зубной налет и камень.
- Подобрать подходящие средства гигиены и научиться правильно чистить зубы, чтобы их не травмировать.
- При необходимости сделать пластику уздечек и слизистых тяжей.
- Пройти ортодонтическое лечение при необходимости.
- Вылечить клиновидный дефект зубов, если он имеется. Важно, чтобы при этом пломбы не были установлены на корни зубов – они не дадут, впоследствии, прижиться тканям, трансплантированным в ходе хирургического этапа лечения.
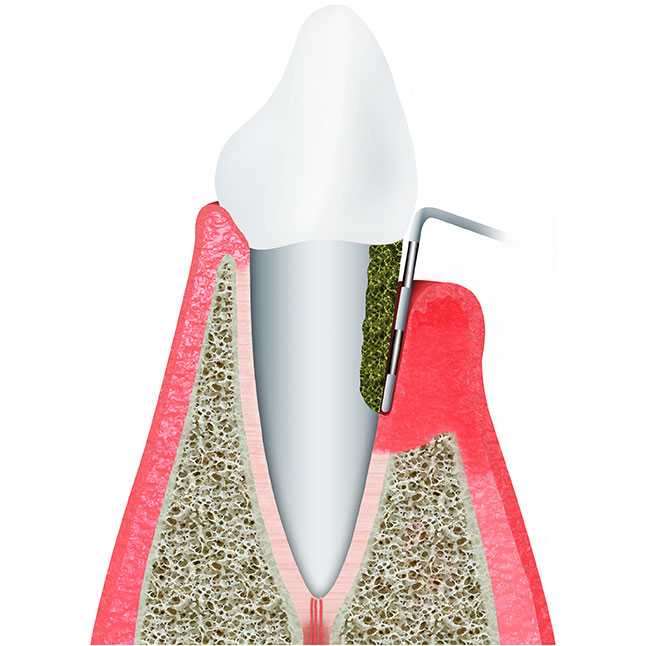
II Хирургический этап лечения
Закрытие рецессии десны — это хирургическая операция по трансплантации тканей, взятых у пациента, в область дефекта с целью воссоздания естественного контура здоровых десен. Эта операция несложная, проводится в основном амбулаторно, в условиях хирургического кабинета под местной проводниковой анестезией.
Операция закрытия рецессии десны может проводиться по различным методикам:
- Закрытие рецессии латеральным лоскутом. Проводится в случае, если в зоне убыли десны имеется достаточно окружающих тканей, которые могут быть перемещены.
- Закрытие рецессии десневым лоскутом.
- Трансплантация лоскута из твердого неба.
- Комбинированный метод, при котором совмещают перемещение тканей десны и тканей твердого неба.
- Методика направленной регенерации тканей. Это пластика рецессии десны, которая предполагает вживление специальных мембран, способствующих восстановлению собственных тканей десны.
 Такие мембраны бывают, как нерезорбируемые – они требуют последующего удаления, так и резорбируемые, которые сами рассасываются через некоторое время, но их эффективность уступает первым.
Такие мембраны бывают, как нерезорбируемые – они требуют последующего удаления, так и резорбируемые, которые сами рассасываются через некоторое время, но их эффективность уступает первым.
Какую из методик выберет врач – зависит от результатов оценки состояния пародонта и диагностики у хирурга — перед лечением их должен пройти каждый пациент.
III Послеоперационный период – рекомендации.
В этот период назначают антибиотики и антибактериальные полоскания и гели для ускорения заживления тканей, пища рекомендуется щадящая, не травмирующая, зубная гигиена – согласно рекомендациям вашего лечащего врача.
Альтернативный консервативный метод лечения рецессии десны.
В некоторых случаях, если не упущено время и пациент обратился за помощью в самом начале развития рецессии десны, лечение может быть проведено коллагеном – это консервативный метод лечения, который хорошо зарекомендовал себя в случаях незапущенной рецессии воспалительного происхождения.
Как предупредить рецессию десны?
- Чистить зубы правильно, использовать подходящие средства гигиены.

- Механически не травмировать десна, не допускать кровотечений.
- Раз в полгода проходить профгигиену, чтобы не допускать отложения зубного налета и камней.
- Регулярно с профилактической целью посещать стоматолога, своевременно лечить кариес и заболевания десен.
- Как можно раньше исправить неправильный прикус.
Примеры закрытия рецессии у наших пациентов формате ДО и ПОСЛЕ лечения:
РАЗВЕЯТЬ ВСЕ СТРАХИ И МИФЫ О РЕЦЕССИИ ДЕСНЫ
ТЕПЕРЬ ПРОСТО КАК 1-2-3
Рецессия десны — это болезнь людей пожилого возраста.
К сожалению, рецессия десны может начаться у пациента практически в любом, в том числе — активном возрасте. Заболевание имеет выраженный косметический недостаток, поэтому очень часто негативно влияет на личную и профессиональную жизнь таких пациентов, ухудшая ее качество. К счастью, сегодня стоматологи в силе помочь таким людям, главное начать лечение как можно раньше – от этого зависит дальнейший прогноз.
От чистки зубов десна не «счищается».
Десна может и не «счищается», но постоянно травмируется, воспаляется и постепенно «убегает» с шеек зубов. Особенно вредно для дёсен, если вы чистите зубы с нажимом, жесткой щеткой, движениями «туда-сюда». Заметили, что десна кровоточит? Первое, что нужно сделать – поменять вашу зубную щетку на мягкую. Начинайте чистить зубы подметающими движениями от десны к режущему краю, не давите сильно на щетку. Желательно все же и стоматолога посетить, т.к. кровотечение – первый «звоночек», что с зубами и деснами не все в порядке.
Если оголились корни зубов нужно делать регулярные полоскания – помогает.
Рецессия десны — это деструктивный процесс в тканях десен и кости челюсти, и, к сожалению, без серьезного лечения обратного развития у него нет. Кроме того, этот процесс часто имеет серьезные физиологические причины – неправильный прикус или короткую уздечку, на которые полоскание повлиять никак не может. Народные средства и травы помогут вам оздоровить полость рта. Часто такие полоскания назначают в процессе восстановления после операции, как вспомогательное средство, они точно полезны, но не являются радикальной лечебной мерой. Ожидая излечения народными методами и не обращаясь к врачу, можно упустить время и запустить болезнь.
Часто такие полоскания назначают в процессе восстановления после операции, как вспомогательное средство, они точно полезны, но не являются радикальной лечебной мерой. Ожидая излечения народными методами и не обращаясь к врачу, можно упустить время и запустить болезнь.
причины и лечение опущения десен
Рецессия десны (или опущение десны) — это патология в ротовой полости, для которой характерно уменьшение объёма слизистой оболочки с последующим оголением корня зуба. Она может затронуть верхнюю и нижнюю челюсть, один или несколько зубов. Наносит вред не только эстетике (портится улыбка), но и здоровью (например, корни зубов остаются без защиты и будут подвержены кариесу).
Опущение десен: причины развития
- Возраст. Согласно ряду авторитетных исследований, у 38% молодых людей есть, по крайней мере, 1 зуб с рецессией десны до 1 мм. У людей в возрасте 30-55 лет патология затрагивает несколько зубных единиц (опущение на ≥ 3 мм). Больше всего проблем испытывают пожилые.
 По статистике, убыль слизистой наблюдалась у 88% респондентов.
По статистике, убыль слизистой наблюдалась у 88% респондентов. - Неправильный уход за полостью рта. Плохая гигиена приводит к появлению зубного камня, развитию гингивита и пародонтита. Чрезмерная чистка зубов (слишком частая, долгая, с использованием твёрдой щётки) также опасна для здоровья и провоцирует травму мягких тканей, которая может привести к рецессии.
- Пародонтит. Воспаление слизистой, которое способствует разрушению и дистрофии альвеолярного отростка.
- Пародонтоз или запущенная стадия пародонтита, для которого характерно глубокое поражение околозубной ткани и значительная убыль дёсен/костной ткани.
- Проблемы с прикусом, из-за которых травмируются мягкие ткани (например, когда нарушается работа механизма по распределению жевательной нагрузки).
- Последствия неправильного ортодонтического лечения. Были проведены исследования, показывающие, что в течение 5 лет после лечения у 11% пациентов может развиться рецессия слизистой.

- Механические повреждения, вызванные привычкой грызть орехи, карандаши и другие твёрдые предметы.
- Пирсинг. При пирсинге на нижней и верхней губе, рецессия десны обнаруживается почти у 80% пациентов. Доказано, что пирсинг в ротвой полости в 11 раз увеличивает этот риск.
Также заболевание провоцируют вредные привычки (курение, алкоголь), недостаток витаминов и неверно подобранные ортопедические конструкции.
Симптомы и классификация патологии
Симптомы:
- Самый очевидный – это визуальное удлинение зуба из-за убыли десневого края. Сначала заболевание может проявиться возле одной зубной единицы, но впоследствии может охватить большую часть зубного ряда.
- Необычный цвет зуба возле десневого края (открылась часть, не защищённая эмалью).
- Повышенная чувствительность к сладкому, кислому, солёному или горячему.
- Щели в прикорневой зоне, в которые постоянно попадает еда.

Классификация рецессии десны по Миллеру:
- Опущение свободной, неприкреплённой десны с минимальным уменьшением её объёма.
- Разрушение слизистой в области прикреплённой десны, при которой её объём не уменьшается.
- Оголение прикорневой, боковой части между зубами.
- Визуально заметное оголение зубного корня по окружности.
Классификация по другим признакам:
- Травматическая. Появилась в результате пореза, удара, ушиба.
- Физиологическая (естественная). Развивается с возрастом, не связана с патологиями.
- Симптоматическая. Результат запущенного заболевания (например, пародонтоза, пародонтита).
- Локальная (рецессия на 1-2 зубах) и генерализованная.
Методы лечения
В зависимости от клинической ситуации лечение рецессии десны осуществляется терапевтическим или хирургическим методом.
В этом случае воспаление возникает в результате того, что врач не до верхушки запломбировал корневые каналы.
- Профессиональная гигиена полости рта (удаление наддеснового и поддесневого зубного камня, жёлтого налёта).
- Лазерная терапия.
- Индивидуальный курс антибиотиков и противовоспалительных лекарств (обязательный этап при всех видах лечения).
- Курс поливитаминных препаратов если одна из причин развития патологии – гиповитаминоз.
Для восстановления эстетики при значительной убыли слизистой, используются хирургические способы лечения.
- Операции с использованием белковых ферментов или других биоэлементов, способствующих быстрой регенерации десны (её росту).
- Лоскутная хирургия. На опущенную десну пришивается ткань, взятая со здорового участка нёба/десны пациента.
- Лечение коллагеном. Вещество вводится в поражённый участок слизистой.
 Убирает воспаления, восстанавливает поражённые области.
Убирает воспаления, восстанавливает поражённые области.
Эффективность различных хирургических вмешательств.
Согласно исследованию, опубликованному Dent Clin North Am, коронковая репозиция лоскута с субэпителиальным трансплантатом соединительной ткани (CAF + SCTG) считается золотым стандартом для покрытия поражённых областей (закрывает> 80% поверхности). Кроме того, в некоторых случаях, применение биопрепаратов (например, EMD или PDGF) способствовало быстрой регенерации ткани и её полному охвату вокруг корня. Также, многообещающие результаты были зафиксированы у второго поколения аллотрансплантатов /ксенотрансплантатов и процедур, связанных с тканевой инженерией 3 поколения. Они устраняют необходимость сбора аутогенных тканей (требуются дополнительные исследования в этой области).
Современная стоматология не стоит на месте. Существуют эффективные методики, позволяющие полностью восстановить утраченный объём ткани. В клиниках «Менделеев» вам предложат современные и безболезненные процедуры для решения этой проблемы. Запишитесь к нам на приём, и наш пародонтолог составит индивидуальный план лечения в зависимости от клинической картины.
Запишитесь к нам на приём, и наш пародонтолог составит индивидуальный план лечения в зависимости от клинической картины.
Профилактика опущения десны
Как предотвратить появление этого заболевания? Врачи нашей клиники делятся следующими рекомендациями:
- Ответственно относитесь к ежедневной чистке зубов.
- Подберите правильную зубную щётку (средней жёсткости).
- Сведите к минимуму зависимость от курения и употребления алкоголя.
- Раз в полгода посещайте кабинет стоматолога для планового осмотра и прохождения профгигиены.
Спасибо за внимание и будьте здоровы!
Пародонтология | Услуги | Стоматологическая клиника «Оптима», шинирование, тканевая регенерация
Пародонтология
Красивую улыбку невозможно представить без здоровых зубов и десен.
Пародонтология — раздел стоматологии, занимающийся диагностикой, лечением и профилактикой заболеваний околозубных тканей — пародонта.
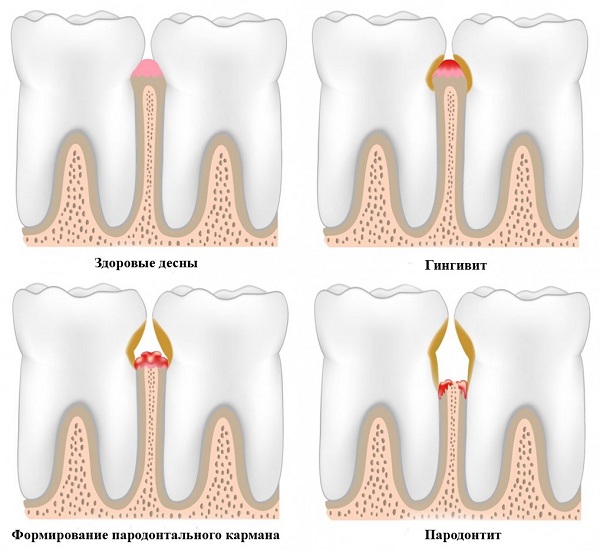
Основная функция пародонта — удержание зубов и их защита. Нарушение его целостности приводит к различным заболеваниям, самые распространенные из них — гингивит, пародонтит и пародонтоз.
Опытные стоматологи-пародонтологи, современное оборудование и новые технологии клиники «Оптима» позволяют провести эффективное лечение даже в сложных случаях. Специалисты проведут диагностику, предложат оптимальный план лечения, дадут необходимые рекомендации по уходу за полостью рта.
Выбор метода лечения тканей пародонта определяется врачом на основании тщательной диагностики.
Записаться на консультацию:
+7 (4812) 33-99-33
Шинирование зубов
Некоторые запущенные заболевания пародонта могут приводить к расшатыванию и выпадению зубов. Шинирование — метод объединения подвижных зубов с неподвижными в единый блок, или «шину». При этом на внутреннюю поверхность зубного ряда фиксируется специальное стекловолокно или ортодонтический ретейнер.
В результате уменьшается подвижность зубов, что значительно снижает риск их выпадения, а также существенно улучшается качество процесса пережевывания пищи.
Пластика рецессии десны
Рецессия — это состояние, при котором обнажается корневая система зуба. Наиболее продуктивный метод лечения — проведение пластики десны. Это процедура перераспределения десны для закрытия корня. В зависимости от клинической ситуации проведение пластики возможно в нескольких вариантах:
1. Накладывание на зону рецессии латерального лоскута, который берут в прилегающих донорских областях. Метод эффективен для лечения локализованного недуга, если в мягких тканях вокруг пораженного зуба найдется достаточное количество материала. Способ дает превосходный эстетический результат за счет совпадения тканей по цвету.
2. Перемещение десневого лоскута на место рецессии. Метод подходит для лечения локализованных и генерализованных рецессий при условии достаточного объема десны.
3. Трансплантация ткани из области твердого неба. Лоскут ткани извлекают из слизистой оболочки неба помещают на место дефекта.
4. Сочетание перемещения лоскута десны с добавлением лоскута с твердого неба.
5. Направленная регенерация тканей. Мембраны, вживляемые в пораженный участок, способствуют росту собственных тканей десны. Нерассасывающиеся мембраны обеспечивают лучшую регенерацию тканей, а рассасывающиеся не требуют удаления путем повторной операции.
Операция тканевой регенерации
Направленная тканевая регенерация — стимуляция костной ткани при помощи специальных мембран для ее разрастания. Операция направлена на восстановление недостающих тканей.
Процедура выполняется одномоментно на 1-8 зубах. Под местной анестезией врач обнажает пораженный участок корня зуба, очищает его от поддесневых отложений. Далее в подготовленные лунки закладывают искусственный костный материал и устанавливают рассасывающуюся мембрану для его закрепления.
Любой метод костной пластики имеет свои показания и некоторые ограничения. Вопрос о необходимости проведения той или иной процедуры решается специалистом на основании диагностики.
Вопрос о необходимости проведения той или иной процедуры решается специалистом на основании диагностики.
Аутостимуляция регенерации тканей пародонта с помощью тромбоцитарной аутоплазмы
В стоматологической клинике «Оптима» проводится аутостимуляция регенерации тканей пародонта с помощью трамбоцитарной аутоплазмы — уникальная методика эффективного лечения воспалительных процессов тканей десны.
Новая безболезненная технология ускоряет регенерацию костной ткани, препятствуя ее дальнейшему разрушению; не вызывает отторжений и аллергических реакций; не дает осложнений и побочных эффектов.
Процедура заключается в заборе крови пациента, выделения плазмы с помощью специального оборудования. Далее врач делает инъекции в проблемную область.
Полученная плазма является естественным стимулятором роста тканей, благодаря высокой концентрации гормонов и питательных веществ.
Через определенное количество процедур заметно улучшается состояние костной ткани, нормализуются обменные процессы, наблюдается рост кровеносных капилляров. Кроме этого, значительно укрепляется иммунитет.
Кроме этого, значительно укрепляется иммунитет.
Данная методика способствует восстановлению структуры десны, устранению кровоточивости, неприятного запаха изо рта, исчезновению покраснений и появлению естественной окраски мягких тканей.
Записаться онлайн
Мы предлагаем широкий диапазон процедур, которые помогут вам получить идеальную улыбку.
Заказать звонок
Наши услуги
Диагностика
Лечение и эстетика
Протезирование
Имплантация
Все услуги
Методы лечение рецессии десны
Что такое рецессия десны? Эта патология распространена среди людей пожилого возраста и некоторого процента взрослых. Заболевание заключается в том, что десна изменяет свое положение, оголяя зубы. Иногда это является патологией, которая проявляется уже в детстве, однако чаще всего рецессия происходит в силу возраста и ослабления функций тканей. Следствием процесса оголения зубов часто становятся всевозможные неприятные процессы, такие как повышение чувствительности.
Эстетически рецессия также не представляет собой ничего привлекательного и часто становится психологическим барьером для общения с окружающими. В клинике Mira вы можете записаться на лечение рецессии десны и исправить любой дефект, восстановить нормальные функции зубов, а также красоту своей улыбки!
Причины рецессии десны включают в себя ряд анатомических особенностей и механических воздействий. Таким образом, рецессия может произойти внезапно или стать закономерным результатом тех или иных процессов в полости рта. К причинам, наиболее часто встречающимся, относятся следующие:
- Отсутствие правильной гигиены полости рта. Активное и неосторожное использование зубной щетки с жесткой щетиной может оказать чрезмерное влияние на десну и стать причиной рецессии. Недостаточный же уход за зубами в целом очень опасен. Так, если говорить о риске рецессии, то зубной камень и налет в некоторых случаях могут стать причиной постепенного опущения десны.
- Пародонтит или другие воспаления десен могут вызвать рецессию.

- Внешние механические воздействия, травмы могут привести к изменению положения зубов и десны. Иногда некорректно установленные ортодонтические аппараты или конструкции для исправления неправильного прикуса влияют на положение десны. Кроме того, при слабых характеристиках костной ткани есть риск последствий для десен даже при правильно установленных брекетах. Также большое значение имеет профессиональная гигиена зубов во время ношения конструкций.
- Анатомические особенности альвеолярного отростка, уздечки губ, корней и кортикальной кости, глубокий прикус. В подобных случаях назначается индивидуальное решение проблемы рецессии.
Симптомы рецессии десны будут разными в зависимости от причины. Общим симптомом, который можно наблюдать практически в каждом случае, является повышенная чувствительность зубов.
Опущение десны происходит на расстояние от 3 мм в легкой форме до 5 и более мм в тяжелой. Стоит отметить, что рецессия может распространяться на все десны одновременно или иметь строго ограниченный характер.
В процессе диагностики и выбора метода лечения врач определяет рецессию как травматическую, симптоматическую или физиологическую. К каждому типу заболевания необходим особый подход:
- Травматический характер имеет рецессия, которая чаще всего проявляется на фронтальной поверхности зубов. Десна опускается на 1–2 мм, при этом воспалений в большинстве случаев не наблюдается, но чувствительность тканей заметно возрастает.
- Симптоматическая рецессия может протекать на внешней и внутренней поверхности зубов, в том числе на межзубных участках десны. Причиной становится, как правило, недостаточная гигиена полости рта. Поэтому к симптомам этого типа относят всевозможные воспаления, отеки, подвижность зубов.
- Физиологическая рецессия — это следствие возраста и снижения тонуса пародонта, при котором оголяются корни зубов. Протекает этот тип без воспалений и других последствий.
Лечение рецессии десны необходимо в рамках подготовительного процесса к ортопедическому лечению. Также при сильной чувствительности зубов и склонности к кариесу врач назначит лечение. Эстетический дискомфорт пациента также будет достаточной причиной для устранения рецессии.
Также при сильной чувствительности зубов и склонности к кариесу врач назначит лечение. Эстетический дискомфорт пациента также будет достаточной причиной для устранения рецессии.
Лечение рецессии десны по стоимости, указанной в нашем прайсе, доступно каждому пациенту. В зависимости от метода терапии, которая бывает оперативной хирургической или безоперационной, цена несколько отличается. Чаще всего, и особенно при сильной степени развития заболевания, врач проводит хирургическую операцию по восстановлению нормального уровня десны относительно корней зубов. Чем серьезнее рецессия, тем меньше шансов восстановить десну даже хирургически. В наиболее тяжелых случаях операцию проводить не имеет смысла.
Поэтому при первых симптомах оголения зубов лучше сразу обратиться в клинику Mira.
Среди хирургических методов терапии рецессии можно выделить метод латерального лоскута (когда часть ткани берется с близлежащего участка десны или неба пациента и пришивается к опущенной десне), метод использования биологически активных элементов (белковый фермент или другие биоэлементы провоцируют быструю регенерацию и восстанавливают десну, укрепляя при этом корни зубов), метод использования эмалевого матрикса, лечение коллагеном (вещество вводится в ткань десен и эффективно восстанавливает пораженные воспалениями области) и другие.
Кроме того, врачи рекомендуют уделять внимание профилактике рецессии при высоком риске развития заболевания. К подобным мерам относятся наблюдение за здоровьем зубов и полости рта, лечение кариеса и проблем с деснами, профилактическое укрепление эмали, качественная гигиена и использование не слишком жесткой зубной щетки, периодические консультации и осмотр у стоматолога.
Сохранить зубы здоровыми поможет регулярное посещение стоматолога клиники Mira! Запись на прием и консультацию по телефону +7 (391) 277-44-72.
Источник фото: © depositphotos.com/ luckybusiness
Лечение рецессии десны – Зубные имплантаты и пародонтология Большого Питтсбурга
Стоматология Большого Питтсбурга
Имплантаты и пародонтология
Результаты, которые вам понравятся… результаты, которые останутся надолго.
4290 Шоссе Уильяма Флинна,
Suite 104
Allison Park, PA 15101
Результаты, которые вам понравятся… результаты, которые останутся надолго.
412-201-0633
Запись на прием
Greater Pittsburgh Dental
Имплантаты и пародонтология
Результаты, которые вам понравятся… результаты, которые останутся надолго.
4290 Шоссе Уильяма Флинна,
Suite 104
Allison Park, PA 15101
Результаты, которые вам понравятся… результаты, которые останутся надолго.
412-201-0633
Запись на прием
Наше средство для рецессии десен устраняет чувствительность и оживляет вашу улыбку.
Чрезмерно обнаженные корни зубов не только ухудшают эстетику улыбки, но и часто чувствительны к горячим и холодным температурам. Теперь это состояние можно исправить с помощью пересадки десны.
Д-р Бакури и д-р Азарноуш используют микрохирургические методы, чтобы аккуратно покрыть корни ваших открытых корней, чтобы улучшить эстетику вашей улыбки и положить конец чувствительности корней.
Что вызывает рецессию десен?
Рецессия десны – это обнажение корней зубов, вызванное ретракцией ткани десны. Чаще всего это вызвано одним или несколькими из следующих факторов:
- Генетика
- Неправильные зубы
- Шлифование зубов
- Травма зубов
- Чрезмерно агрессивная чистка щеткой или зубной нитью
- Тяжелое заболевание десен
Опасность рецессии десны
Поскольку поверхности корней намного мягче зубной эмали, они более подвержены эрозии и более чувствительны к теплу, холоду и даже сладкому. Корни могут настолько изнашиваться, что зубы расшатываются или ломаются.
Лечение тонких десен
Тонкие десны не могут должным образом поддерживать зуб и в конечном итоге приводят к рецессии десны и потере костной массы. Пересадка десны также может быть использована для лечения слишком тонкой десны.
$149 Осмотр рецессии десны, рентген и консультация
- Комплексное обследование полости рта
- Диагностические фотографии
- Обследование на заболевание десен
- Скрининг рака полости рта
- Консультация врача
- Письменный план лечения
Позвоните по телефону 412-201-0633 или нажмите здесь, чтобы записаться на прием.
Цена 289 долларов!
Обеспечение вашего комфорта в любое время
Ваш комфорт всегда является главным приоритетом для всей нашей команды. Мы используем местную анестезию при пересадке десны, а также предлагаем пероральную или внутривенную седацию для пациентов, которые просят об этом.
Пересадка десны вызывает очень небольшой дискомфорт, поэтому обычно рекомендуются безрецептурные обезболивающие. В течение нескольких недель требуется диета из более мягких продуктов, и большинство пациентов возвращаются к своей обычной деятельности на следующий день.
Наши процедуры пересадки десны
Наши врачи выбирают наилучший вариант для ваших конкретных потребностей
Наши врачи используют несколько типов процедур при лечении пересадки десны и определяют, какая процедура или комбинация процедур лучше всего соответствует вашим конкретным потребностям. Вы можете быть уверены, что любой вариант будет предоставлен с умением, состраданием и с учетом вашего комфорта.
Аутогенный метод позволяет получить ткань из нёба для пересадки. Наши врачи используют специальные методы, чтобы сделать эту хирургическую процедуру практически безболезненной и требующей минимального наложения повязки на область удаления ткани.
AlloDerm® — это ткань из банка доноров, прошедшая строгие испытания Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США. AlloDerm используется для большинства процедур пластики десен. Это самый сложный метод прививки десны, который дает множество преимуществ.
Так как натуральная ткань AlloDerm может быть получена в больших количествах, можно обрабатывать сразу несколько участков десен. Для пациентов, у которых недостаточно ткани или они просто не хотят брать ткань с нёба, AlloDerm является лучшим вариантом.
Протеины, тромбоцитарные факторы роста и направленная регенерация тканей – это методы, включенные в процедуру трансплантации, когда рецессия десны довольно серьезная.
Эмдогейн® гель — это революционный продукт, в котором используется белок для стимуляции восстановления ткани десны, утраченной из-за тяжелого периодонтита.
Тромбоцитарные факторы роста представляют собой белки, которые могут стимулировать восстановление и заживление десен. Они особенно полезны для реформирования кровеносных сосудов.
Направленная регенерация тканей включает введение коллагена, который действует как барьер между тканями, которые заживают быстрее (десны и связки), и костью. Эта процедура дает время для регенерации кости без вторжения в более быстро заживающие ткани.
Позвоните по телефону 412-201-0633 или нажмите здесь, чтобы записаться на прием.
Pinhole Gum Регенерация Beachwood | Repair Gum Recession
Восстановление десен в Бичвуде, штат Огайо, может быть именно тем, что вам нужно для улучшения здоровья и внешнего вида ваших десен.
Описание кого-либо как «длинный в зубах» относится к старению, и это выражение происходит от того, что десны могут отходить от зубов и вызывать слишком длинный вид.
Наряду с эстетической проблемой рецессии десны, открытые корни чувствительны и с гораздо большей вероятностью могут привести к развитию трудноизлечимого кариеса и чувствительности зубов к горячему и холодному.
Рецессия десны является частым симптомом заболеваний пародонта. Это серьезная проблема со здоровьем, которая выходит за рамки вашей улыбки! Но это только одна причина из многих.
Если вы заметили, что зубы выглядят «длинными в зубах», или если вы хотите записаться на профилактический стоматологический осмотр для оценки состояния и внешнего вида ваших десен, свяжитесь с Beachwood Smiles.
- Что вызывает рецессию десны?
- Что такое пинхол-хирургическая техника при рецессии десны?
- Каковы преимущества пинхол-хирургической техники по сравнению с тканевыми трансплантатами?
- Если я нервничаю, вы можете мне помочь?
- Как избежать рецессии десны в будущем?
Что вызывает рецессию десны?
Рецессии десны могут способствовать несколько различных факторов. Тем не менее, ваш лучший стоматолог в Бичвуде, штат Огайо, может помочь с комфортом восстановить здоровье или внешний вид ваших десен благодаря новейшим технологиям и навыкам доктора Йови Тауба и его преданной команды стоматологов.
Тем не менее, ваш лучший стоматолог в Бичвуде, штат Огайо, может помочь с комфортом восстановить здоровье или внешний вид ваших десен благодаря новейшим технологиям и навыкам доктора Йови Тауба и его преданной команды стоматологов.
Распространенные причины рецессии десны — или «длинного зуба» — включают:
Заболевания пародонта. Инфекция в ткани десны приводит к тому, что десна отслаивается от зуба. Глубокие карманы приводят к некрозу тканей и раздражению, что требует профессионального лечения, а также улучшенного домашнего ухода. Лечение заболеваний пародонта имеет решающее значение для здоровья вашей улыбки и общего самочувствия.
Чрезмерная чистка зубов. Когда пациенты слишком сильно чистят зубы или используют зубную щетку с жесткой щетиной, происходит рецессия десны. Используйте только зубную щетку с мягкой щетиной и аккуратно чистите кончики щетинок под углом к линии десен. Если вы не уверены, спросите нашего стоматолога-гигиениста о лучших методах чистки зубов, чтобы защитить вашу улыбку и здоровье десен.
Неправильный прикус (неправильный прикус). Неравномерное давление вызывает травму зубов и десен. Неправильный прикус вызывает неравномерное усилие, напрягая связки, которые прикрепляют зубы к ткани десны. При отсутствии лечения могут возникнуть трещины зубов и болезненная рецессия. Без лечения эта проблема может привести к потере зубов.
Бруксизм. Скрежетание зубами, как и неправильный прикус, травмирует ткань десны, вызывая рецессию десны, износ, переломы зубов и повышенную чувствительность. В случаях бруксизма часто рекомендуется использование оральных приспособлений после лечения. Оральный прибор или каппа защищает ваши зубы во время сна, предотвращая скрежетание и сжимание зубов, которые могут стоить вам улыбки и способствовать рецессии десен.
В Beachwood Smiles мы предлагаем уход за деснами, который поможет восстановить их здоровье!
Что такое регенерация десен?
До недавнего времени единственным способом устранения рецессии десны было удаление здоровой ткани с нёба и прикрепление ее под тканью десны в области рецессии. Это был инвазивный процесс.
Это был инвазивный процесс.
Точечная регенерация десны устраняет необходимость использования донорской ткани для лечения рецессии. Небольшое отверстие в десне дает доктору Йови Таубу доступ для отделения ткани десны от зубов и кости и перемещения ее на рецессивные области.
Размещение небольших коллагеновых волокон под перемещенной тканью добавляет вещества и объема для защиты корней зубов со здоровой тканью, удерживая новое положение ткани на месте.
Ваш дантист в Бичвуде успешно лечил многих пациентов с помощью этого менее инвазивного метода, и мы думаем, что вы будете очень довольны результатами.
Преимущества регенерации десен в Бичвуде, Огайо
Когда д-р Йоав Тауб DDS сталкивается с новой техникой или технологией, которая делает лечение зубов более комфортным и менее инвазивным, он работает над тем, чтобы представить ее в нашем стоматологическом кабинете в Бичвуде, Огайо.
Он обнаружил, что точечная хирургия десны имеет много преимуществ по сравнению с трансплантацией тканей, позволяя улучшить восстановление десны.
Некоторые из преимуществ точечной хирургии десны по сравнению с трансплантацией тканей включают:
Уменьшение боли. Традиционная пересадка десны вызывает болезненные разрезы и швы как на нёбе, так и вокруг тканей. Регенерация десны точечным отверстием устраняет необходимость удаления ткани из области нежного неба, что означает меньше боли для вас.
Более быстрое заживление. Часто называемая «подтяжкой десен во время обеда», регенерация точечных отверстий быстро заживает с минимальным временем простоя. Для заживления традиционной пластики десны может потребоваться шесть или более месяцев, а для достижения идеальных результатов может потребоваться несколько операций. Более быстрое заживление важно для вас, и оно важно для вашего стоматолога в Юниверсити-Хайтс, штат Огайо.
Минимально инвазивный. Избегайте традиционного разрезания и сшивания с помощью регенерации десны с точечным отверстием, которая работает за счет растяжения существующей ткани поверх обнаженных корней. Менее инвазивные всегда идеально!
Менее инвазивные всегда идеально!
Без швов. Поскольку регенерация точечной десны перемещает ткань десны на рецессивные области, наложение швов не требуется. Коллагеновые полоски стимулируют рост тканей и фиксируют их на месте до тех пор, пока не произойдет повторное прикрепление и заживление. Отсутствие швов означает более комфортное восстановление и меньше ограничений.
Избавьтесь от беспокойства о зубах в Beachwood Smiles
Если вы чувствуете тревогу или страх перед посещением стоматолога или восстановлением десен, вы не одиноки. У нашей первоклассной профессиональной и сострадательной команды есть дар успокаивать наших пациентов.
Мы предлагаем несколько удобств для релаксации, чтобы сделать ваш визит в Beachwood Smiles более расслабляющим и приятным, в том числе:
- Подушки для шеи
- Уютные одеяла
- Netflix в наших палатах
Если вам нужна дополнительная помощь, чтобы расслабиться, у нас есть несколько вариантов седации в стоматологии на выбор.
Закись азота. Наше самое мягкое успокаивающее средство, закись азота, попадает в организм через маленькую маску для носа. Мы контролируем уровень седации на протяжении всей процедуры, чтобы вы чувствовали себя комфортно и расслабленно.
Одним из наиболее значительных преимуществ закиси азота является то, что эффекты быстро исчезают, что позволяет вам вернуться домой и вернуться к обычному графику работы без сонливости или снижения времени реакции.
Оральная седация в стоматологии. Пациентам с сильным беспокойством или сильным рвотным рефлексом мы предлагаем пероральную седацию с помощью отпускаемого по рецепту лекарства под названием Halcion. Пероральная седация будет иметь более продолжительный эффект и потребует поездки на прием и обратно, и вам следует планировать отдых на оставшуюся часть дня.
Полный медицинский анамнез определит, безопасна ли для вас пероральная седация.
Как избежать рецессии десны в будущем?
Существует несколько способов снизить риск рецессии десен, но очень важно соблюдать дома надлежащую гигиену полости рта и разрешать стоматологические осмотры и чистку зубов не реже двух раз в год.
Если вы не знаете, как аккуратно, но эффективно чистить зубы, спросите нашего гигиениста о советах по уходу за полостью рта, которые вы можете использовать дома.
Если вы страдаете от бруксизма, спросите у нашего стоматолога о специальной каппе, которая помогает держать верхние и нижние зубы отдельно друг от друга во время сна.
Запишитесь на осмотр, чтобы ваш стоматолог рядом с Юниверсити-Хайтс мог оценить ваш прикус или назначить лечение для исправления перекрестного, неправильный или нижнего прикуса.
Свяжитесь с нашим стоматологическим кабинетом в Бичвуде сегодня!
В качестве альтернативы традиционной хирургии десен свяжитесь с Beachwood Smiles, чтобы записаться на консультацию к доктору Таубу, или позвоните по телефону (216) 292-9920, чтобы узнать о точечной регенерации десен и о том, принесет ли она вам пользу. Наш комплексный подход к уходу за пациентами помогает пациентам в нашем сообществе восстановить свои улыбки и здоровье полости рта.
Избранные сообщения в блоге — Регенерация точечной десны
20 декабря 2019 г.
Точечная хирургия десны в Бичвуде, Огайо: что это такое и стоит ли оно того?
Точечная хирургия десен — отличный способ лечения рецессии и заболеваний десен, восстановления здоровья десен без повреждения или удаления здоровых тканей.
Этот инновационный метод того стоит, поскольку обеспечивает более комфортное лечение десен и более быстрое восстановление.
Поможет ли операция на деснах при повышенной чувствительности зубов?
Рецессия десны придает зубам удлиненный вид, часто обнажая корни, что может привести к повышенной чувствительности зубов.
С помощью точечной хирургии десны стоматолог меняет положение десны и помещает внутрь коллагеновые волокна, создавая более объемную и здоровую ткань для защиты корней зубов и снижения чувствительности.
Как…
Подробнее
Читайте наш блог
Регенерация периодонтальной кости, связок и цемента с помощью каркасов и стволовых клеток
1. Эрнандес-Монхараз Б., Сантьяго-Осорио Э., Монрой-Гарсия А., Ледесма-Мартинес Э., Мендоса-Нуньес В.М. Мезенхимальные стволовые клетки стоматологического происхождения для индукции регенерации тканей при пародонтите: мини-обзор. Междунар. Дж. Мол. науч. 2018;19:944. doi: 10.3390/ijms1
Эрнандес-Монхараз Б., Сантьяго-Осорио Э., Монрой-Гарсия А., Ледесма-Мартинес Э., Мендоса-Нуньес В.М. Мезенхимальные стволовые клетки стоматологического происхождения для индукции регенерации тканей при пародонтите: мини-обзор. Междунар. Дж. Мол. науч. 2018;19:944. doi: 10.3390/ijms1
2. Карасол М., Ллодра Х.К., Фернандес-Месегер А., Браво М., Гарсия-Маргалло М.Т., Кальво-Боначо Э., Санс М. , Herrera D. Заболевания пародонта среди работающих взрослых в Испании. Дж. Клин. Пародонтол. 2016; 43: 548–556. doi: 10.1111/jcpe.12558. [PubMed] [CrossRef] [Академия Google]
3. Шаудинн С., Горур А., Келлер Д., Седгизаде П.П., Костертон Дж.В. Пародонтит: архетипическое биопленочное заболевание. Варенье. Вмятина. доц. 2009; 140:978–986. doi: 10.14219/jada.archive.2009.0307. [PubMed] [CrossRef] [Google Scholar]
4. Хан М.А. Состояние здоровья полости рта и поведение выживших после рака в Корее на основе общенационального опроса. Междунар. Дж. Окружающая среда. Рез. Здравоохранение. 2018;15:14. doi: 10.3390/ijerph25010014. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Междунар. Дж. Окружающая среда. Рез. Здравоохранение. 2018;15:14. doi: 10.3390/ijerph25010014. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Бёкерс Н.Г., Гж В.Д.Х., ван Вейк А.Дж., Лоос Б.Г. Пародонтит является независимым индикатором риска атеросклеротических сердечно-сосудистых заболеваний среди 60 174 участников крупной стоматологической школы в Нидерландах. Дж. Эпидемиол. Здоровье общества. 2017;71:37–42. doi: 10.1136/jech-2015-206745. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Тонетти М.С., Ван Дайк Т.Е., Бек Дж., Бушар П., Катлер К.В., Д’Айуто Ф., Дитрих Т., Эке П. , Грациани Ф., Гансолли Дж. Пародонтит и атеросклеротические сердечно-сосудистые заболевания. Дж. Пародонтол. 2013;84:С24–С29. doi: 10.1902/jop.2013.1340019. [PubMed] [CrossRef] [Google Scholar]
7. Meurman J.H., Sanz M., Janket S.-J. Здоровье полости рта, атеросклероз и сердечно-сосудистые заболевания. крит. Преподобный Орал Биол. Мед. 2004; 15:403–413. doi: 10. 1177/154411130401500606. [PubMed] [CrossRef] [Google Scholar]
1177/154411130401500606. [PubMed] [CrossRef] [Google Scholar]
8. Isola G., Cicciù M., Fiorillo L., Matarese G. Связь между одонтомой и ретенированными зубами. Дж. Краниофак. Surg. 2017; 28: 755–758. doi: 10.1097/SCS.0000000000003433. [PubMed] [CrossRef] [Академия Google]
9. Ferlazzo N., Currò M., Zinellu A., Caccamo D., Isola G., Ventura V., Carru C., Matarese G., Ientile R. Влияние генетического фона mthfr на p16 и метилирование mgmt в плоскоклеточный рак ротовой полости. Междунар. Дж. Мол. науч. 2017;18:724. doi: 10.3390/ijms18040724. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Sculean A., Chapple I.L., Giannobile W.V. Модели ран для периодонтальной и костной регенерации: роль биологических исследований. Пародонтология. 2015;68:7–20. doi: 10.1111/prd.12091. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Совмя С., Мони У., Джаячандран П., Решма С., Кумар Р.А., Арзате Х., Наир С.В., Джаякумар Р. Трехслойный нанокомпозитный гидрогелевый каркас для одновременной регенерации цемента, периодонтальной связки и альвеолярной кости. Доп. Здоровьеc. Матер. 2017;6:1601252. doi: 10.1002/adhm.201601251. [PubMed] [CrossRef] [Google Scholar]
Доп. Здоровьеc. Матер. 2017;6:1601252. doi: 10.1002/adhm.201601251. [PubMed] [CrossRef] [Google Scholar]
12. Маске Б.С., Ратод С., Ваникар И. Критические вопросы регенерации пародонта. SRM Дж. Рез. Вмятина. науч. 2018;9: 119–124. [Google Scholar]
13. Xu X.-Y., Li X., Wang J., He X.-T., Sun H.-H., Chen F.-M. Краткий обзор: Регенерация тканей пародонта с использованием стволовых клеток: стратегии и аспекты применения. Стволовые клетки Пер. Мед. 2018; 8: 392–403. doi: 10.1002/sctm.18-0181. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
14. Chaudhari A., Borse H., Mali A., Agrawal P., Landge N., Khadtare Y. Направляйте ткани для регенерации пародонта (gtr ): Обзор. Междунар. Дж. Карр. Рез. 2017;9: 59269–59278. [Google Scholar]
15. Шейх З., Хамдан Н., Икеда Ю., Гринпас М., Гансс Б., Глогауэр М. Натуральные трансплантационные ткани и синтетические биоматериалы для реконструктивных применений пародонта и альвеолярной кости: обзор. Биоматер. Рез. 2017;21:9. doi: 10.1186/s40824-017-0095-5. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1186/s40824-017-0095-5. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Pihlstrom B.L., Michalowicz B.S., Johnson N.W. Заболевания пародонта. Ланцет. 2005; 366: 1809–1820. doi: 10.1016/S0140-6736(05)67728-8. [PubMed] [CrossRef] [Академия Google]
17. Ануши М., Суреш К. Регенерация периодонтальной кости при внутрикостных дефектах с использованием остеокондуктивного костного трансплантата по сравнению с комбинацией остеокондуктивного и остеостимулирующего костного трансплантата: сравнительное исследование. Вмятина. Рез. Дж. 2015; 12:25–30. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Zhou M., Geng Y.-M., Li S.-Y., Yang X.-B., Che Y.-J., Pathak J.L. , Wu G. Каркас на основе нанокристаллического гидроксиапатита адсорбирует и обеспечивает замедленное высвобождение остеоиндуктивного фактора роста и способствует регенерации кости в эктопической модели мышей. Дж. Наноматер. 2019;2019:10. дои: 10.1155/2019/1202159. [CrossRef] [Google Scholar]
19. Chen M., Xu Y., Zhang T., Ma Y., Liu J., Yuan B., Chen X., Zhou P., Zhao X., Pang F. Листы мезенхимальных стволовых клеток: новая клеточная стратегия восстановления и регенерации кости. Биотехнолог. лат. 2019;41:305–318. doi: 10.1007/s10529-019-02649-7. [PubMed] [CrossRef] [Google Scholar]
Chen M., Xu Y., Zhang T., Ma Y., Liu J., Yuan B., Chen X., Zhou P., Zhao X., Pang F. Листы мезенхимальных стволовых клеток: новая клеточная стратегия восстановления и регенерации кости. Биотехнолог. лат. 2019;41:305–318. doi: 10.1007/s10529-019-02649-7. [PubMed] [CrossRef] [Google Scholar]
20. Ivanovski S., Vaquette C., Gronthos S., Hutmacher D., Bartold P. Многофазные каркасы для инженерии тканей пародонта. Дж. Дент. Рез. 2014;93:1212–1221. doi: 10.1177/0022034514544301. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Park CH, Kim KH, Lee YM, Seol YJ Передовые инженерные стратегии для регенерации периодонтального комплекса. Материалы. 2016;9:57. дои: 10.3390/ma
57. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Саккас А., Уайлд Ф., Хойфельдер М., Винтер К., Шрамм А. Аутогенные костные трансплантаты в оральной имплантологии. Золотой стандарт»? Последовательный обзор 279пациентам с 456 клиническими процедурами. Междунар. J. Имплантат Дент. 2017;3:23. doi: 10.1186/s40729-017-0084-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Имплантат Дент. 2017;3:23. doi: 10.1186/s40729-017-0084-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Рейнольдс М.А., Айхельманн-Рейди М.Е., Бранч-Майс Г.Л. Регенерация тканей пародонта: костные трансплантаты. Вмятина. клин. 2010;54:55–71. doi: 10.1016/j.cden.2009.09.003. [PubMed] [CrossRef] [Google Scholar]
24. Кит Дж.Д., младший, Петрунгаро П., Леонетти Дж.А., Элвелл К.В., младший, Зерен К.Дж., Капуто К., Никитакис Н.Г., Шёпф К., Уорнер М.М. Клиническая и гистологическая оценка минерализованного блочного аллотрансплантата: результаты периода развития (2001–2004 гг.) Int. Дж. Пародонт. Восстановить. Вмятина. 2006; 26: 320–327. [PubMed] [Академия Google]
25. Piattelli A., Scarano A., Fau-Corigliano M., Corigliano M., Fau-Piattelli M., Piattelli M. Сравнение регенерации кости с использованием минерализованных и деминерализованных лиофилизированных костных аллотрансплантатов: гистологический и гистохимическое исследование у человека. Биоматериалы. 1996; 17:1127–1131. doi: 10.1016/0142-9612(96)85915-1. [PubMed] [CrossRef] [Google Scholar]
1996; 17:1127–1131. doi: 10.1016/0142-9612(96)85915-1. [PubMed] [CrossRef] [Google Scholar]
26. Liu X., Li Q., Wang F., Wang Z. Увеличение дна верхнечелюстной пазухи и установка зубного имплантата с использованием стромальных клеток костного мозга, модифицированных геном дентинного матриксного белка-1. смешанный с депротеинизированной говяжьей костью: сравнительное исследование биглей. Арка Оральный биол. 2016;64:102–108. doi: 10.1016/j.archoralbio.2016.01.004. [PubMed] [CrossRef] [Академия Google]
27. Чжан Ю., Сюй Х.Х., Такаги С., Чоу Л.К. Каркас на основе гидроксиапатита, твердеющий in situ, для восстановления кости. Дж. Матер. науч. Матер. Мед. 2006; 17: 437–445. doi: 10.1007/s10856-006-8471-z. [PubMed] [CrossRef] [Google Scholar]
28. Белал М., Аль-Ноамани Ф., Эль-Тонси М., Эль-Гинди Х., Исикава И. Лечение дефектов фуркации II класса у человека с использованием соединительнотканных трансплантатов , биорассасывающаяся мембрана и рассасывающийся гидроксиапатит: сравнительное исследование. Дж. Междунар. акад. Пародонтол. 2005; 7: 114–128. [PubMed] [Академия Google]
Дж. Междунар. акад. Пародонтол. 2005; 7: 114–128. [PubMed] [Академия Google]
29. Чжан Ю., Сюй Х.Х.К. Влияние синергетического армирования и прочности рассасывающихся волокон на гидроксиапатитовый костный цемент. Дж. Биомед. Матер. Рез. Часть А. 2005; 75А: 832–840. doi: 10.1002/jbm.a.30461. [PubMed] [CrossRef] [Google Scholar]
30. Hayashi C., Kinoshita A., Oda S., Mizutani K., Shirakata Y., Ishikawa I. Инъекционный костный цемент на основе фосфата кальция обеспечивает благоприятное пространство и каркас для пародонта. регенерация у собак. Дж. Пародонтол. 2006; 77: 940–946. doi: 10.1902/jop.2006.050283. [PubMed] [CrossRef] [Академия Google]
31. Chu K., Oshida Y., Hancock E., Kowolik M., Barco T., Zunt S. Композиты гидроксиапатит/пмма в качестве костного цемента. биомед. Матер. англ. 2004; 14:87–105. [PubMed] [Google Scholar]
32. Fu Q., Saiz E., Rahaman M.N., Tomsia AP. Тканевая инженерия: к прочным и жестким стеклянным и керамическим каркасам для восстановления костей. Доп. Функц. Матер. 2013;23:5460. doi: 10.1002/adfm.201370227. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Доп. Функц. Матер. 2013;23:5460. doi: 10.1002/adfm.201370227. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Tsai H.-C., Li Y.-C., Young T.-H., Chen M.-H. Новый микроинъектор для введения костных заменителей для регенерации кости при заболеваниях пародонта. Дж. Формос. Мед. доц. 2016; 115:45–50. doi: 10.1016/j.jfma.2014.10.009. [PubMed] [CrossRef] [Google Scholar]
34. Simon C.G., Jr., Khatri C.A., Wight S.A., Wang F.W. Предварительный отчет о биосовместимости формовочного резорбируемого композитного костного трансплантата, состоящего из кальций-фосфатного цемента и поли( лактид-ко-гликолид) микросферы. J. Ортопед. Рез. 2002; 20: 473–482. doi: 10.1016/S0736-0266(01)00140-1. [PubMed] [CrossRef] [Google Scholar]
35. Brown W.E., Chow L.C. Комбинации труднорастворимых фосфатов кальция в суспензиях и пастах в качестве минерализаторов и цементов. 4 612 053. Патент США. 1986 сен 16;
36. Такаги С., Чоу Л.К., Хираяма С., Эйхмиллер Ф.К. Свойства эластомерных композитов на основе кальцийфосфатного цемента и хитозана. Вмятина. Матер. 2003; 19: 797–804. doi: 10.1016/S0109-5641(03)00028-9. [PubMed] [CrossRef] [Google Scholar]
Вмятина. Матер. 2003; 19: 797–804. doi: 10.1016/S0109-5641(03)00028-9. [PubMed] [CrossRef] [Google Scholar]
37. Xu H.H., Wang P., Wang L., Bao C., Chen Q., Weir MD, Chow LC, Zhao L., Zhou X., Reynolds M.A. Кальций Фосфатные цементы для костной инженерии и их биологические свойства. Кость рез. 2017;5:17056. doi: 10.1038/boneres.2017.56. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Виллалона Г.А., Удельсман Б., Дункан Д.Р., Макгилликадди Э., Сох-Мартинес Р.Ф., Хибино Н., Пейнтер С., Миренский Т., Эриксон Б., Шинока Т. Методы посева клеток в сосудистой тканевой инженерии . Ткань англ. Часть B Ред. 2010; 16:341–350. doi: 10.1089/ten.teb.2009.0527. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Wang P., Song Y., Weir MD, Sun J., Zhao L., Simon C.G., Xu H.H.K. Самотвердеющая паста ipsmsc-альгинат-кальций-фосфат для инженерии костной ткани. Вмятина. Матер. 2016; 32: 252–263. doi: 10.1016/j.dental.2015.11.019. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
40. Grosfeld E.-C., Hoekstra JWM, Herber R.-P., Ulrich D.J., Jansen J.A., van den Beucken J.J. Долгосрочные биологические характеристики инъецируемого и разлагаемого кальций-фосфатного цемента. Биомед. Матер. 2016;12:015009. doi: 10.1088/1748-605X/12/1/015009. [PubMed] [CrossRef] [Google Scholar]
Grosfeld E.-C., Hoekstra JWM, Herber R.-P., Ulrich D.J., Jansen J.A., van den Beucken J.J. Долгосрочные биологические характеристики инъецируемого и разлагаемого кальций-фосфатного цемента. Биомед. Матер. 2016;12:015009. doi: 10.1088/1748-605X/12/1/015009. [PubMed] [CrossRef] [Google Scholar]
41. Song Y., Zhang C., Wang P., Wang L., Bao C., Weir MD, Reynolds M.A., Ren K., Zhao L., Xu H.H. Инженерная регенерация кости с помощью нового гидрогелевого каркаса из микроволокна, наполненного клетками, для инъекций фосфата кальция. Матер. науч. англ. К. 2017; 75:895–905. doi: 10.1016/j.msec.2017.02.158. [PubMed] [CrossRef] [Google Scholar]
42. Zhao L., Weir MD, Xu HH Инъекционная паста из мезенхимальных стволовых клеток фосфата кальция и альгината гидрогеля пуповины для инженерии костной ткани. Биоматериалы. 2010;31:6502–6510. doi: 10.1016/j.biomaterials.2010.05.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Мициадис Т.А., Феки А., Папаччо Г., Катон Дж. Стволовые клетки пульпы зуба, ниши и сигнализация надреза при травме зуба. Доп. Вмятина. Рез. 2011; 23: 275–279. doi: 10.1177/0022034511405386. [PubMed] [CrossRef] [Google Scholar]
Стволовые клетки пульпы зуба, ниши и сигнализация надреза при травме зуба. Доп. Вмятина. Рез. 2011; 23: 275–279. doi: 10.1177/0022034511405386. [PubMed] [CrossRef] [Google Scholar]
44. Wang P., Liu X., Zhao L., Weir MD, Sun J., Chen W., Man Y., Xu H.H.K. Инженерия костной ткани с помощью индуцированных человеком плюрипотентных, пуповинных и мезенхимальных стволовых клеток костного мозга в черепе крысы. Акта Биоматер. 2015;18:236–248. doi: 10.1016/j.actbio.2015.02.011. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Ван Л., Чжан С., Ли С., Вейр М.Д., Ван П., Рейнольдс М.А., Чжао Л., Сюй Х.Х. Инъекционный фосфат кальция с гидрогелевыми волокнами, инкапсулирующими индуцированные плюрипотентные клетки зубной пульпы и стволовые клетки костного мозга для восстановления кости. Матер. науч. англ. С. 2016; 69: 1125–1136. doi: 10.1016/j.msec.2016.08.019. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Schweikle M.Z.T., Lund R., Tiainen H. Синтетический гидрогель для инъекций для регенерации кости: физико-химическая характеристика гелеобразующей системы с высоким и низким ph. Матер. науч. англ. К. 2018; 90: 67–76. doi: 10.1016/j.msec.2018.04.049. [PubMed] [CrossRef] [Google Scholar]
Синтетический гидрогель для инъекций для регенерации кости: физико-химическая характеристика гелеобразующей системы с высоким и низким ph. Матер. науч. англ. К. 2018; 90: 67–76. doi: 10.1016/j.msec.2018.04.049. [PubMed] [CrossRef] [Google Scholar]
47. Acar A.H., Alan H., Ozgur C., Vardi N., Asutay F., Guler C. Эффективна ли более кортикальная декортикация кости при направленной аугментации кости? Дж. Краниофак. Surg. 2016;27:1879–1883. doi: 10.1097/SCS.0000000000002932. [PubMed] [CrossRef] [Google Scholar]
48. Du B., Liu W., Deng Y., Li S., Liu X., Gao Y., Zhou L. Ангиогенез и костная регенерация пористого наногидроксиапатита /coralline блоки, покрытые rhvegf165, при дефектах альвеолярной кости критических размеров in vivo. Междунар. Дж. Наномед. 2015;10:2555–2565. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Zhang C., Hu K., Liu X., Reynolds M.A., Bao C., Wang P., Zhao L., Xu H.H. -культура для преваскуляризации каркаса из фосфата кальция для улучшения формирования костей и сосудов. Матер. науч. англ. С. 2017; 79: 296–304. doi: 10.1016/j.msec.2017.05.035. [PubMed] [CrossRef] [Google Scholar]
Матер. науч. англ. С. 2017; 79: 296–304. doi: 10.1016/j.msec.2017.05.035. [PubMed] [CrossRef] [Google Scholar]
50. Бесинис А., Де Перальта Т., Тредвин С.Дж., Хэнди Р.Д. Обзор наноматериалов в стоматологии: взаимодействие с микросредой полости рта, клиническое применение, опасности и преимущества. АКС Нано. 2015;9:2255–2289. doi: 10.1021/nn505015e. [PubMed] [CrossRef] [Google Scholar]
51. Batool F., Strub M., Petit C., Bugueno I., Bornert F., Clauss F., Huck O., Kuchler-Bopp S., Benkirane- Джессел Н. Ткани пародонта, кость верхней челюсти и подходы к регенерации зубов: от анализа моделей на животных до клинических применений. Наноматериалы. 2018;8:337. дои: 10.3390/нано8050337. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Мициадис Т.А., Волошик А., Хименес-Рохо Л. Наностоматология: сочетание наноструктурированных материалов и стволовых клеток для регенерации тканей зуба. Наномедицина. 2012;7:1743–1753. doi: 10.2217/nnm.12.146. [PubMed] [CrossRef] [Google Scholar]
53. Полини А., Бай Х., Томсия А.П. Применение наноструктурированного биоактивного стекла и его композитов в стоматологии. Уайли Междисциплинарный. Преподобный Наномед. Нанобиотехнология. 2013;5:399–410. doi: 10.1002/wnan.1224. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Полини А., Бай Х., Томсия А.П. Применение наноструктурированного биоактивного стекла и его композитов в стоматологии. Уайли Междисциплинарный. Преподобный Наномед. Нанобиотехнология. 2013;5:399–410. doi: 10.1002/wnan.1224. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
54. Xu H.H., Weir MD, Zhao L., Moreau J.L., Arola DD, Simon C.G. Новые нанотехнологии в стоматологии. Издательство Уильяма Эндрю; Парк-Ридж, Нью-Джерси, США: 2012. Нано-апатитовые композитные каркасы для доставки стволовых клеток и инженерии костной ткани; стр. 189–207. [Google Scholar]
55. Ли Г., Чжоу Т., Линь С., Ши С., Линь Ю. Наноматериалы для инженерии тканей черепа и зубов. Дж. Дент. Рез. 2017;96: 725–732. doi: 10.1177/0022034517706678. [PubMed] [CrossRef] [Google Scholar]
56. Li J., Li Y., Ma S., Gao Y., Zuo Y., Hu J. Усиление формирования кости трансдуцированными bmp-7 МСК на биомиметическом нано — гидроксиапатит/полиамидные композитные каркасы для восстановления дефектов нижней челюсти. Дж. Биомед. Матер. Рез. Часть А. 2010; 95:973–981. doi: 10.1002/jbm.a.32926. [PubMed] [CrossRef] [Google Scholar]
Дж. Биомед. Матер. Рез. Часть А. 2010; 95:973–981. doi: 10.1002/jbm.a.32926. [PubMed] [CrossRef] [Google Scholar]
57. Xia Y., Chen H., Zhang F., Bao C., Weir MD, Reynolds M.A., Ma J., Gu N., Xu H.H. Наночастицы золота в инъекциях Кальций-фосфатный цемент усиливает остеогенную дифференцировку стволовых клеток пульпы зуба человека. Наномед. нанотехнологии. биол. Мед. 2018;14:35–45. doi: 10.1016/j.nano.2017.08.014. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Zhu W., Zhang Q., Zhang Y., Cen L., Wang J. Регенерация Pdl посредством самонаведения клеток при отсроченной реплантации вырванных зубов. Дж. Пер. Мед. 2015;13:357. doi: 10.1186/s12967-015-0719-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Бартольд П.М., Ши С., Гронтос С. Стволовые клетки и регенерация периодонта. Пародонтология 2000. 2006;40:164–172. doi: 10.1111/j.1600-0757.2005.00139.x. [PubMed] [CrossRef] [Google Scholar]
60. Catón J., Bostanci N., Remboutsika E. , De Bari C., Mitsiadis T.A. Стоматология будущего: клеточная терапия сочетается с восстановлением и регенерацией зубов и периодонта. Дж. Селл. Мол. Мед. 2011;15:1054–1065. дои: 10.1111/j.1582-4934.2010.01251.х. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
, De Bari C., Mitsiadis T.A. Стоматология будущего: клеточная терапия сочетается с восстановлением и регенерацией зубов и периодонта. Дж. Селл. Мол. Мед. 2011;15:1054–1065. дои: 10.1111/j.1582-4934.2010.01251.х. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
61. Shi H., Zong W., Xu X., Chen J. Улучшенный двухфазный фосфат кальция в сочетании со стволовыми клетками периодонтальной связки может служить многообещающим методом. для регенерации пародонта. Являюсь. Дж. Пер. Рез. 2018;10:4030. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Du J., Shan Z., Ma P., Wang S., Fan Z. Аллогенная трансплантация мезенхимальных стволовых клеток костного мозга для регенерации периодонта. Дж. Дент. Рез. 2014;93: 183–188. doi: 10.1177/0022034513513026. [PubMed] [CrossRef] [Google Scholar]
63. Мохаммед Э., Халил Э., Сабри Д. Влияние стволовых клеток, полученных из жировой ткани, и их экзогенных стволовых клеток в качестве дополнительной терапии к нехирургическому лечению пародонта: гистологическое и гистоморфометрическое исследование на крысах . Биомолекулы. 2018;8:167. doi: 10.3390/biom8040167. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Биомолекулы. 2018;8:167. doi: 10.3390/biom8040167. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
64. Duan X., Tu Q., Zhang J., Ye J., Sommer C., Mostoslavsky G., Kaplan D., Yang P. , Chen J. Применение индуцированных плюрипотентных стволовых (ips) клеток в регенерации тканей пародонта. Дж. Селл. Физиол. 2011; 226:150–157. doi: 10.1002/jcp.22316. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
65. Bosshardt D.D., Sculean A. Действительно ли работает регенерация тканей пародонта? Пародонтол. 2000. 2009; 51: 208–219. doi: 10.1111/j.1600-0757.2009.00317.x. [PubMed] [CrossRef] [Google Scholar]
66. Siaili M., Chatzopoulou D., Gillam D.G. Обзор регенеративных процедур пародонта для стоматолога общей практики. Сауди Дент. Ж. 2018; 30:26–37. doi: 10.1016/j.sdentj.2017.11.001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Сингх А.К. Мембраны GTR: барьеры для периодонтальной регенерации. ДХР Интерн. Дж. Мед. науч. 2013; 4:31–38. [Академия Google]
[Академия Google]
68. Боттино М.С., Томас В., Шмидт Г., Вохра Ю.К., Чу Т.-М.Г., Коволик М.Ю., Яновский Г.М. Недавние достижения в разработке мембран gtr/gbr для пародонтальной регенерации — взгляд на материалы. Вмятина. Матер. 2012; 28:703–721. doi: 10.1016/j.dental.2012.04.022. [PubMed] [CrossRef] [Google Scholar]
69. Кэш А. 20 лет направленной костной регенерации в имплантологии. 2-е изд. Издательство Оксфордского университета; Oxford, UK: 2019. [Google Scholar]
70. Pretzl B., Kim T.-S., Holle R., Eickholz P. Отдаленные результаты направленной регенерации тканей с помощью нерезорбируемых и биодеградируемых барьеров. Ив. Случай серии внутрикостных дефектов через 10 лет. Дж. Пародонтол. 2008;79: 1491–1499. doi: 10.1902/jop.2008.070571. [PubMed] [CrossRef] [Google Scholar]
71. Corinaldesi G., Lizio G., Badiali G., Morselli-Labate A.M., Marchetti C. Лечение внутрикостных дефектов после удаления ретинированных третьих моляров нижней челюсти с помощью биорассасывающихся и нерассасывающихся материалов мембраны. Дж. Пародонтол. 2011;82:1404–1413. doi: 10.1902/jop.2011.100466. [PubMed] [CrossRef] [Google Scholar]
Дж. Пародонтол. 2011;82:1404–1413. doi: 10.1902/jop.2011.100466. [PubMed] [CrossRef] [Google Scholar]
72. Мошавериния А., Чен С., Сюй С., Акияма К., Ансари С., Заде Х.Х., Ши С. Потенциал костной регенерации стволовых клеток, полученных из периодонтальной связки или источники десневой ткани, инкапсулированные в rgd-модифицированный альгинатный каркас. Ткань англ. Часть А. 2013; 20:611–621. дои: 10.1089/тен.чай.2013.0229. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Боллати Д., Морра М., Кассинелли К., Каскардо Г. Имплантируемые устройства с антибактериальными свойствами и многофункциональными поверхностями. 9 999 706. Патент США. 2018 19 июня;
74. Нямсурен Э., Баярчимег Б., Урджинлхам Дж., Оюн-енх П., Х О., Бацуури М., Лу С.-л. Эффективность природной биополимерной хитозановой мембраны для направленной регенерации тканей. Инновации. 2018;12:16–20. [Google Scholar]
75. Cui J., Liang J., Wen Y., Sun X., Li T., Zhang G., Sun K., Xu X. In vitro и in vivo оценка хитозана/β- Композитная мембрана из глицеринфосфата для направленной костной регенерации. Дж. Биомед. Матер. Рез. Часть А. 2014;102:2911–2917. doi: 10.1002/jbm.a.34874. [PubMed] [CrossRef] [Google Scholar]
In vitro и in vivo оценка хитозана/β- Композитная мембрана из глицеринфосфата для направленной костной регенерации. Дж. Биомед. Матер. Рез. Часть А. 2014;102:2911–2917. doi: 10.1002/jbm.a.34874. [PubMed] [CrossRef] [Google Scholar]
76. Xue Y., Hong X., Gao J., Shen R., Ye Z. Получение и биологическая характеристика смеси поли(молочной-со-гликолевой кислоты) /хитозан/аг наночастицы для тканевой инженерии пародонта. Междунар. Дж. Наномед. 2019;14:483. doi: 10.2147/IJN.S184396. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
77. Lausch A.J., Chong L.C., Uludag H., Sone E.D. Многофазные коллагеновые каркасы для инженерных интерфейсов тканей. Доп. Функц. Матер. 2018;28:1804730. doi: 10.1002/adfm.201804730. [Перекрестная ссылка] [Академия Google]
78. Zhou T., Liu X., Sui B., Liu C., Mo X., Sun J. Разработка композитных нановолокон рыбий коллаген/биоактивное стекло/хитозан в качестве мембраны gtr/gbr для индукции регенерации тканей пародонта. Биомед. Матер. 2017;12:055004. doi: 10.1088/1748-605X/aa7b55. [PubMed] [CrossRef] [Google Scholar]
2017;12:055004. doi: 10.1088/1748-605X/aa7b55. [PubMed] [CrossRef] [Google Scholar]
79. Фостер Б.Л., Нагатомо К.Дж., Нокити Ф.Х., мл., Фонг Х., Данн Д., Тран А.Б., Ван В., Нарисава С., Миллан Дж.Л., Сомерман М.Дж. Центральная роль пирофосфата в формировании бесклеточного цемента. ПЛОС ОДИН. 2012;7:e38393. doi: 10.1371/journal.pone.0038393. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
80. Маталова Э., Лунгова В., Шарп П. Биология стволовых клеток и тканевая инженерия в стоматологии. Академическая пресса; Кембридж, Массачусетс, США: 2015. Развитие зубов и связанных с ними структур; стр. 335–346. [Google Scholar]
81. Фостер Б.Л., Попович Т.Е., Фонг Х.К., Сомерман М.Дж. Достижения в определении регуляторов развития цемента и регенерации периодонта. Курс. Верхний. Дев. биол. 2007; 78: 47–126. [PubMed] [Академия Google]
82. Arzate H., Zeichner-David M., Mercado-Celis G. Белки цемента: роль в цементогенезе, биоминерализации, формировании и регенерации периодонта. Пародонтология 2000. 2015;67:211–233. doi: 10.1111/prd.12062. [PubMed] [CrossRef] [Google Scholar]
Пародонтология 2000. 2015;67:211–233. doi: 10.1111/prd.12062. [PubMed] [CrossRef] [Google Scholar]
83. Hoz L., Romo E., Zeichner-David M., Sanz M., Nuñez J., Gaitán L., Mercado G., Arzate H. Цементный белок 1 (cemp1) индуцирует дифференцировку клеток периодонтальной связки человека в условиях трехмерного культивирования. Клеточная биол. Междунар. 2012;36:129–136. doi: 10.1042/CBI20110168. [PubMed] [CrossRef] [Google Scholar]
84. Bosshardt D.D., Schroeder H.E. Обзор цементогенеза: сравнение премоляров человека и коренных зубов грызунов. Анат. Рек. 1996; 245: 267–292. doi: 10.1002/(SICI)1097-0185(199606)245:2<267::AID-AR12>3.0.CO;2-N. [PubMed] [CrossRef] [Google Scholar]
85. Бар-Кана И., Савион Н., Нараянан А., Питару С. Проявление белка прикрепления цемента ограничено минерализованными тканями, образующими клетки периодонта. Евро. Дж. Устные науки. 1998;106:357–364. doi: 10.1111/j.1600-0722.1998.tb02198.x. [PubMed] [CrossRef] [Google Scholar]
86. Zhu W. , Liang M. Стволовые клетки периодонтальной связки: текущее состояние, проблемы и перспективы на будущее. Стволовые клетки 2015;2015:972313. doi: 10.1155/2015/972313. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Liang M. Стволовые клетки периодонтальной связки: текущее состояние, проблемы и перспективы на будущее. Стволовые клетки 2015;2015:972313. doi: 10.1155/2015/972313. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
87. Lemaitre M., Monsarrat P., Blasco-Baque V., Loubières P., Burcelin R., Casteilla L., Planat-Bénard V. , Kémoun P. Регенерация пародонтальной ткани с использованием сингенных стромальных клеток, полученных из жировой ткани, на мышиной модели. Стволовые клетки Пер. Мед. 2017; 6: 656–665. дои: 10,5966/ст.2016-0028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
88. Ян Б., Чен Г., Ли Дж., Цзоу К., Се Д., Чен Ю., Ван Х., Чжэн X. , Long J., Tang W. Регенерация корня зуба с использованием клеточных пластин зубных фолликулов в сочетании с каркасом на основе дентинной матрицы. Биоматериалы. 2012;33:2449–2461. doi: 10.1016/j.biomaterials.2011.11.074. [PubMed] [CrossRef] [Google Scholar]
89. Crossman J., Elyasi M., Elbialy T., Flores C. M. Регенерация цемента с использованием стволовых клеток на модели собаки: систематический обзор. Арка Оральный биол. 2018;91: 78–90. doi: 10.1016/j.archoralbio.2018.04.001. [PubMed] [CrossRef] [Google Scholar]
M. Регенерация цемента с использованием стволовых клеток на модели собаки: систематический обзор. Арка Оральный биол. 2018;91: 78–90. doi: 10.1016/j.archoralbio.2018.04.001. [PubMed] [CrossRef] [Google Scholar]
90. Yang Z.H., Zhang X.J., Dang NN, Ma Z.F., Xu L., Wu J.J., Sun Y.J., Duan Y.Z., Lin Z., Jin Y. Верхушечная зародышевая клетка зуба Кондиционированная среда усиливает дифференцировку стволовых клеток периодонтальной связки в ткани, подобные цементу/периодонтальной связке. Дж. Пародонт. Рез. 2009;44:199–210. doi: 10.1111/j.1600-0765.2008.01106.x. [PubMed] [CrossRef] [Google Scholar]
91. Оваки Т., Симидзу Т., Ямато М., Окано Т. Инженерия клеточных листов для регенеративной медицины: текущие проблемы и стратегии. Биотехнолог. Дж. 2014;9: 904–914. doi: 10.1002/biot.201300432. [PubMed] [CrossRef] [Google Scholar]
92. Pedroni A.C.F., Sarra G., de Oliveira N.K., Moreira M.S., Deboni M.C.Z., Marques M.M. Клеточные листы стволовых клеток пульпы зуба человека для будущего применения при замене кости. клин. Оральное расследование. 2018;23:2713–2721. doi: 10.1007/s00784-018-2630-8. [PubMed] [CrossRef] [Google Scholar]
клин. Оральное расследование. 2018;23:2713–2721. doi: 10.1007/s00784-018-2630-8. [PubMed] [CrossRef] [Google Scholar]
93. Йорукоглу А.С., Китер А., Аккая С., Сатироглу-Туфан Н.Л., Туфан А.С. Краткий обзор использования мезенхимальных стволовых клеток в тканевой инженерии на основе клеточных пластин с особое внимание уделяется регенерации костной ткани. Стволовые клетки 2017;2017:13. doi: 10.1155/2017/2374161. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
94. Ивата Т., Ямато М., Цучиока Х., Такаги Р., Мукобата С., Васио К., Окано Т., Исикава И. Регенерация пародонта с помощью многослойных клеточных пластин, полученных из периодонтальной связки, у собаки. модель. Биоматериалы. 2009;30:2716–2723. doi: 10.1016/j.biomaterials.2009.01.032. [PubMed] [CrossRef] [Google Scholar]
95. Ивата Т., Васио К., Йошида Т., Исикава И., Андо Т., Ямато М., Окано Т. Инженерия клеточных слоев и ее применение для регенерации пародонта . Дж. Тиссью Инж. Реген. Мед. 2015;9: 343–356. doi: 10.1002/term.1785. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1002/term.1785. [PubMed] [CrossRef] [Google Scholar]
96. Mao L., Liu J., Zhao J., Chang J., Xia L., Jiang L., Wang X., Lin K., Fang B. Effect микро-нано-гибридной структурированной гидроксиапатитовой биокерамики на остеогенную и цементогенную дифференцировку стволовых клеток периодонтальной связки человека через сигнальный путь wnt. Междунар. Дж. Наномед. 2015;10:7031. doi: 10.2147/IJN.S
. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]97. Yin Y., Li X., He X., Wu R., Sun H., Chen F. Использование стволовых клеток для терапевтической регенерации. Дж. Дент. Рез. 2017;96: 601–609. doi: 10.1177/0022034517706070. [PubMed] [CrossRef] [Google Scholar]
98. Lane S.W., Williams D.A., Watt F.M. Модулирование ниши стволовых клеток для регенерации тканей. Нац. Биотехнолог. 2014;32:795. doi: 10.1038/nbt.2978. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
99. Андреас К., Ситтингер М., Ринге Дж. На пути к тканевой инженерии in situ: рекрутирование стволовых клеток под контролем хемокинов. Тенденции биотехнологии. 2014; 32: 483–492. doi: 10.1016/j.tibtech.2014.06.008. [PubMed] [CrossRef] [Академия Google]
Тенденции биотехнологии. 2014; 32: 483–492. doi: 10.1016/j.tibtech.2014.06.008. [PubMed] [CrossRef] [Академия Google]
100. Чжао Д., Лей Л., Ван С., Ни Х. Понимание регенерации тканей на основе клеточного самонаведения с точки зрения материалов. Дж. Матер. хим. Б. 2015;3:7319–7333. doi: 10.1039/C5TB01188D. [CrossRef] [Google Scholar]
101. Liu H., Li M., Du L., Yang P., Ge S. Местное введение фактора-1, полученного из стромальных клеток, способствует рекрутированию стволовых клеток и регенерации костей у крыс. Модель костного дефекта периодонта. Матер. науч. англ. С. 2015; 53:83–94. doi: 10.1016/j.msec.2015.04.002. [PubMed] [CrossRef] [Академия Google]
102. Tian B.M., He X.T., Xu X.Y., Li X., Wu R.X., Chen F.M. Передовые биотехнологии для создания клеточного дома для размещения стволовых клеток. Доп. Матер. Технол. 2017;2:1700022. doi: 10.1002/admt.201700022. [CrossRef] [Google Scholar]
103. Wu R.-X., Xu X.-Y., Wang J., He X.-T., Sun H.-H., Chen F.-M. Биоматериалы для эндогенной регенеративной медицины: стимулирование возвращения стволовых клеток и не только. заявл. Матер. Сегодня. 2018;11:144–165. doi: 10.1016/j.apmt.2018.02.004. [Перекрестная ссылка] [Академия Google]
заявл. Матер. Сегодня. 2018;11:144–165. doi: 10.1016/j.apmt.2018.02.004. [Перекрестная ссылка] [Академия Google]
104. Carter S.-S.D., Costa P.F., Vaquette C., Ivanovski S., Hutmacher D.W., Malda J. Аддитивное биопроизводство: передовой подход к регенерации тканей пародонта. Анна. Биомед. англ. 2017;45:12–22. doi: 10.1007/s10439-016-1687-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
105. Obregon F., Vaquette C., Ivanovski S., Hutmacher D., Bertassoni L. Трехмерная биопечать для регенеративной стоматологии и черепно-лицевой инженерии тканей. Дж. Дент. Рез. 2015;94:143С–152С. doi: 10.1177/0022034515588885. [PubMed] [CrossRef] [Google Scholar]
106. Sun J., Lee Y. 3D-печать сополимеров с контролируемым составом. 15/702 779. Патент Гугла. 2018 29 марта;
107. Vaquette C., Fan W., Xiao Y., Hamlet S., Hutmacher D.W., Ivanovski S. Двухфазная конструкция каркаса в сочетании с технологией клеточного листа для одновременной регенерации комплекса альвеолярной кости/периодонтальной связки. Биоматериалы. 2012;33:5560–5573. doi: 10.1016/j.biomaterials.2012.04.038. [PubMed] [CrossRef] [Академия Google]
Биоматериалы. 2012;33:5560–5573. doi: 10.1016/j.biomaterials.2012.04.038. [PubMed] [CrossRef] [Академия Google]
108. Пак Ч.Х., Риос Х.Ф., Джин К., Блэнд М.Е., Фланаган К.Л., Холлистер С.Дж., Джаннобиле В.В. Биомиметические гибридные каркасы для создания интерфейсов человеческих зубов и связок. Биоматериалы. 2010;31:5945–5952. doi: 10.1016/j.biomaterials.2010.04.027. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
109. Park C.H., Rios H.F., Jin Q., Sugai J.V., Padial-Molina M., Taut A.D., Flanagan C.L., Hollister S.J., Giannobile W.V. Тканевая инженерия костно-связочных комплексов с использованием каркасов, направляющих волокна. Биоматериалы. 2012;33:137–145. doi: 10.1016/j.biomaterials.2011.090,057. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
110. Park C.H., Rios H.F., Taut A.D., Padial-Molina M., Flanagan C.L., Pilipchuk S.P., Hollister S.J., Giannobile W.V. Каркасы для направления волокон на основе изображений: платформа для регенерации поверхностей тканей. Ткань англ. Методы части С. 2013;20:533–542. doi: 10.1089/ten.tec.2013.0619. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ткань англ. Методы части С. 2013;20:533–542. doi: 10.1089/ten.tec.2013.0619. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
111. Мициадис Т.А., Смит М.М. Как гены делают зубы упорядоченными в процессе развития? Дж. Эксп. Зоол. Часть B Мол. Дев. Эвол. 2006; 306B: 177–182. doi: 10.1002/jez.b.21104. [PubMed] [CrossRef] [Академия Google]
112. Лаханн Дж. Полимерные покрытия на паровой основе для потенциальных биомедицинских применений. Полим. Междунар. 2006; 55: 1361–1370. doi: 10.1002/pi.2098. [CrossRef] [Google Scholar]
113. Rios H.F., Lin Z., Oh B., Park C.H., Giannobile W.V. Клеточные и генные терапевтические стратегии для регенеративной медицины пародонта. Дж. Пародонтол. 2011;82:1223–1237. doi: 10.1902/jop.2011.100710. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
114. Вхора И., Лалани Р., Бхатт П., Патил С., Патель Х., Патель В., Мисра А. Коллоидно стабильный небольшой однослойный липоплексы стеариламина для эффективных bmp-9доставка генов в стволовые клетки для остеогенной дифференцировки. AAPS PharmSciTech. 2018;19:3550–3560. doi: 10.1208/s12249-018-1161-6. [PubMed] [CrossRef] [Google Scholar]
AAPS PharmSciTech. 2018;19:3550–3560. doi: 10.1208/s12249-018-1161-6. [PubMed] [CrossRef] [Google Scholar]
115. Tsuchiya S., Chiba M., Kishimoto K., Nakamura H., Mitani H. Перенос генов в ткани пародонта с помощью электропорации in vivo. Дж. Дент. Рез. 2002;81:А452. [Google Scholar]
116. Jin Q., Anusaksathien O., Webb S.A., Printz M.A., Giannobile W.V. Разработка структур, поддерживающих зубы, путем доставки векторов генной терапии pdgf. Мол. тер. 2004;9: 519–526. doi: 10.1016/j.ymthe.2004.01.016. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
117. Mah T.F., Pitts B., Pellock B., Walker G.C., Stewart P.S., O’Toole G.A. Генетическая основа устойчивости биопленок синегнойной палочки к антибиотикам. Природа. 2003; 426:306–310. doi: 10.1038/nature02122. [PubMed] [CrossRef] [Google Scholar]
118. Sharma A., Honma K., Evans R.T., Hruby D.E., Genco R.J. Пероральная иммунизация рекомбинантным Streptococcus gordonii, экспрессирующим домены porphyromonas gingivalis fima. Заразить. Иммун. 2001;69: 2928–2934. doi: 10.1128/IAI.69.5.2928-2934.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Заразить. Иммун. 2001;69: 2928–2934. doi: 10.1128/IAI.69.5.2928-2934.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
119. Lee J.H., Lin J.D., Fong J.I., Ryder M.I., Ho S.P. крысиная модель периодонтита. Биомед Рез. Междунар. 2013;2013:876316. doi: 10.1155/2013/876316. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
120. Wu M., Wang J., Zhang Y., Liu H., Dong F. Индукция минерализации фибробластов десны и создание многослойной ткани. разработанный комплекс для устранения дефектов пародонта. Мед. науч. Монит. 2018;24:1112–1123. дои: 10.12659/МСМ.1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
121. Lee C.H., Hajibandeh J., Suzuki T., Fan A., Shang P., Mao J.J. Трехмерные печатные многофазные каркасы для регенерации пародонтального комплекса. Ткань англ. Часть А. 2014; 20:1342–1351. doi: 10.1089/ten.tea.2013.0386. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
122. Wu R.-X., Yin Y., He X. -T., Li X., Chen F.-M. Разработка клеточного дома для размещения и размещения стволовых клеток. Доп. Биосист. 2017;1:1700004. doi: 10.1002/adbi.201700004. [Перекрестная ссылка] [Академия Google]
-T., Li X., Chen F.-M. Разработка клеточного дома для размещения и размещения стволовых клеток. Доп. Биосист. 2017;1:1700004. doi: 10.1002/adbi.201700004. [Перекрестная ссылка] [Академия Google]
Доктор Рави, DDS, DABOI, DICOI | Регенерация костей и десен
Из-за травмы, инфекции или потери зубов пациент может фактически потерять часть десны и костной ткани, поддерживающей зубы, что делает его улыбку гораздо более уязвимой для будущих проблем. Однако с помощью методов регенерации десен и костей доктора Доктора он может помочь восстановить эту важную ткань, что приведет к более здоровой и сильной улыбке. Процедуры, описанные ниже, также часто необходимы, прежде чем пациент сможет установить зубные имплантаты для замены отсутствующих зубов.
Регенерация тканей и костей
По мере прогрессирования заболевания десен, оно начинает разрушать мягкие и твердые ткани полости рта, подвергая чувствительные корни зубов инфекции и резко увеличивая риск потери зубов. Доктор Доктор может исправить обе эти проблемы, используя передовые тканевые и костные трансплантаты. На десны можно наложить специальную мембрану, чтобы стимулировать рост новой здоровой ткани, а челюстную кость можно нарастить с помощью костного трансплантата (подробнее об этом ниже). Это может решить многие проблемы, когда речь идет о внешнем виде и функции зубов пациента, а также может сделать кого-то жизнеспособным кандидатом на установку зубных имплантатов.
На десны можно наложить специальную мембрану, чтобы стимулировать рост новой здоровой ткани, а челюстную кость можно нарастить с помощью костного трансплантата (подробнее об этом ниже). Это может решить многие проблемы, когда речь идет о внешнем виде и функции зубов пациента, а также может сделать кого-то жизнеспособным кандидатом на установку зубных имплантатов.
Направленная регенерация тканей и направленная костная регенерация
Целью этих процедур является восстановление утраченной ткани пародонта, кости, периодонтальных связок и соединительных тканей, поддерживающих зубы. Они достигают этого с помощью биосовместимых мембран, костных трансплантатов и/или специальных белков, которые стимулируют рост тканей. Хотя эти процедуры подходят в различных обстоятельствах, они особенно распространены до или во время установки зубных имплантатов. Управляемая костная регенерация позволяет естественной кости пациента максимизировать потенциал заживления после хирургических процедур.
Процедура
Лечение относительно простое. Доктор Доктор помещает биосовместимую мембрану между десной и костью. Он действует как барьер, который не позволяет росту десны ограничивать рост подлежащей кости по мере ее восстановления.
Мембраны, накладываемые на зубы, обычно рассасываются сами по себе через несколько недель после первоначальной процедуры. Однако некоторые мембраны, например те, которые используются для восстановления костных гребней в челюсти, не рассасываются и должны быть удалены.
Синус-лифтинг
Для пациентов, желающих заменить свои верхние задние зубы, можно использовать синус-лифтинг для утолщения челюстной кости в этой области, чтобы она могла обеспечить достаточную поддержку для зубных имплантатов. Эта процедура также помогает предотвратить случайное прокалывание корнями имплантата чувствительной мембраны пазухи, расположенной прямо над костью. Он получил свое название, потому что мембрана пазухи аккуратно приподнимается, чтобы создать место для размещения материала для костной пластики, что приводит к созданию новой, прочной кости, которая будет удерживать корни имплантата.
Многим пациентам, заинтересованным в установке зубных имплантатов для замены отсутствующих зубов на верхней челюсти, сначала необходимо пройти процедуру, известную как синус-лифтинг. Обычно это необходимо, когда задняя часть верхней челюсти слишком тонкая или хрупкая для поддержки штифтов имплантатов. К счастью для пациентов доктора Доктора, он может сам обеспечить все этапы ухода за имплантатами, поэтому, если окажется, что вам все-таки нужен синус-лифтинг в Арлингтоне, вам не придется обращаться к другому специалисту, и вы можете ему доверять. будет выполняться с использованием новейших методов и самых передовых технологий, как и остальная часть вашего ухода.
Что такое синус-лифтинг?
Синус-лифтинг — это особый тип костного трансплантата, который используется для укрепления и утолщения задней части верхней челюсти, чтобы подготовить ее к установке зубных имплантатов. После того, как зубы в этой области выпадают, кость естественным образом начинает сморщиваться и атрофироваться. Если кость слишком тонкая, она может быть не в состоянии адекватно поддерживать имплантаты, а имплантаты на самом деле рискуют пройти сквозь кость и проткнуть чувствительную мембрану пазухи прямо над ней, что неприятно! К счастью, синус-лифтинг может помочь пациенту избежать обеих этих потенциальных проблем, чтобы он мог получить новые крепкие, удобные и долговечные зубы.
Если кость слишком тонкая, она может быть не в состоянии адекватно поддерживать имплантаты, а имплантаты на самом деле рискуют пройти сквозь кость и проткнуть чувствительную мембрану пазухи прямо над ней, что неприятно! К счастью, синус-лифтинг может помочь пациенту избежать обеих этих потенциальных проблем, чтобы он мог получить новые крепкие, удобные и долговечные зубы.
Крестальный синус-лифтинг
Существует несколько способов, которыми доктор может выполнить синус-лифтинг, и метод, который он выберет, будет основан на ваших конкретных потребностях и плотности челюстной кости:
- Синус-лифтинг с установкой имплантата. Врач сделает синус-лифтинг и поставит имплантаты в одно и то же время. На боковой стороне челюстной кости создается небольшое окно, которое позволяет доктору аккуратно приподнять мембрану пазухи. Затем он помещает материал для костной пластики в новое пространство, а затем размещает корни имплантата в кости.
- Пьезо подтяжка пазухи: врач создает окно доступа в кости челюсти, чтобы он мог поднять мембрану пазухи, а затем помещает под нее материал для костной пластики.
 Это в конечном итоге превратится в новую, здоровую ткань, которая будет поддерживать имплантаты пациента.
Это в конечном итоге превратится в новую, здоровую ткань, которая будет поддерживать имплантаты пациента. - Гидравлический синус-лифтинг: дрель создает путь в пазуху через пустую зубную лунку, а затем постоянный поток воды используется для поднятия мембраны, чтобы можно было разместить материал для костной пластики.
- Синус-лифтинг с внутренней конденсацией выпуклости: этот метод создает пространство внутри челюстной кости для имплантатов без фактического удаления кости. Кость в основном уплотняется, что делает ее более плотной и прочной, поэтому она может обеспечить прочную основу для имплантатов.
Преимущества синус-лифтинга
Самое большое преимущество синус-лифтинга заключается в том, что он позволяет пациенту, который обычно не подходит для имплантации зубов, получить доступ к этому современному методу лечения. В прошлом пациентам с тонкими или хрупкими челюстными костями из-за длительной потери зубов приходилось довольствоваться традиционными мостовидными протезами или зубными протезами, но теперь, благодаря таким процедурам, как синус-лифтинг, они могут получить наиболее полную и долговечную замену, доступную на сегодняшний день.
Атрофия синус-лифтинга
При удалении верхнего моляра и поломке верхушки корня его можно удалить элеваторами с минимальной травмой окружающих тканей. Несмотря на то, что над корнем достаточно кости, после удаления зуба десна зарастает над отверстием, а кость зарастает в области лунки. Если имплантат не будет установлен, гребень будет атрофироваться из-за неиспользования. Медленное расширение пазухи может вызвать атрофию в верхней задней области, а в наиболее тяжелых случаях кость, разделяющая пазуху и ротовую полость, может стать тонкой, как бумага.
Сохранение альвеолярного отростка
Эта процедура позволяет сохранить кость и ткани десны, окружающие зуб после его удаления. Это может в значительной степени предотвратить потерю костной массы, которая обычно развивается после потери зуба, а также может позволить пациенту быстро заменить зуб зубным имплантатом без необходимости сначала получать костный трансплантат. Как правило, сохранение альвеолярного гребня проводится одновременно с удалением, чтобы пациент мог как можно быстрее восстановить свой зуб.
Костная пластика
После потери зуба челюстная кость естественным образом начинает сморщиваться и ослабевать. Это может привести к смещению оставшихся зубов, создать косметические дефекты улыбки и сделать невозможной замену зубов зубными имплантатами. К счастью, костный трансплантат может все исправить! Используя собственную кость пациента, донорскую кость или материал, изготовленный в лаборатории, доктор Доктор может наращивать и утолщать челюстную кость именно там, где это необходимо пациенту для достижения сильной и привлекательной улыбки. Часто это первый шаг перед тем, как пациент получит зубные имплантаты.
Цитопластовая мембрана
После выполнения костного трансплантата одной из потенциальных проблем является то, что окружающая ткань десны может прорасти в эту область и помешать заживлению. Чтобы этого не произошло, доктор Доктор может поместить цитопластическую мембрану во время выполнения костной пластики. Это сохраняет общую структуру области и помогает пациенту наслаждаться более быстрым и эффективным процессом восстановления.
Одноэтапная процедура наращивания прикрепленной десны
Пока доктор Доктор устанавливает зубные имплантаты пациента, он также может использовать трансплантат мягких тканей для исправления любой рецессии десны, которая развилась. И корни имплантата, и тканевой трансплантат располагаются во рту одновременно, поэтому такой подход известен как «одноэтапный». Эта процедура может значительно улучшить внешний вид улыбки, оказать ценную поддержку новым зубам и обеспечить долговечность зубных имплантатов пациента.
Пародонтальная регенерация с использованием аутологичных клеточных пластин, полученных из периодонтальной связки – исследование безопасности и эффективности на десяти пациентах
- Список журналов
- Реген Тер
- т.9; 2018 дек.
- PMC6222282
Реген Тер. 2018 декабрь; 9: 38–44.
2018 декабрь; 9: 38–44.
Published online 2018 Aug 24. doi: 10.1016/j.reth.2018.07.002
, a, b, ∗ , a , a , a , c , C , A, B, C , C , B , A, ∗∗ Copyright A
09 Автор.0006- Дополнительные материалы
История вопроса
Пародонтит приводит к разрушению тканей пародонта, поддерживающих зуб, и не имеет способности к самопроизвольному заживлению. Были внедрены различные подходы к регенерации тканей пародонта; однако эти подходы имеют ограниченную эффективность для лечения тяжелых дефектов. Цитотерапия объединяет биологию стволовых клеток и тканевую инженерию, формируя многообещающий подход для преодоления этих ограничений. В этом исследовании мы выделили клетки, полученные из периодонтальной связки (PDL), от пациентов и создали клеточные листы с помощью «Технологии клеточного листа», используя чашки для культивирования, чувствительные к температуре, в которых все культивированные клетки могут быть собраны в виде интактного клеточного листа для трансплантации путем снижение температуры чашки для культивирования. Впоследствии безопасность и эффективность аутологичных клеточных слоев, полученных из PDL, оценивали в клинических условиях.
Впоследствии безопасность и эффективность аутологичных клеточных слоев, полученных из PDL, оценивали в клинических условиях.
Методы
Клиническое исследование в одной группе и в одном институте было проведено для проверки безопасности и эффективности аутологичных клеточных слоев, полученных из PDL, у пациентов с пародонтитом. Зубы мудрости были удалены у пациентов с диагнозом хронический пародонтит в возрасте от 33 до 63 лет (среднее значение [±SD], 46 ± 12), а ткани периодонта были соскоблены для получения источников клеток. Трехслойные клеточные листы, полученные из PDL, были сконструированы с использованием чувствительных к температуре культуральных чашек и трансплантированы аутологичным образом после стандартных операций с лоскутами. Костные дефекты заполнены гранулами бета-трикальцийфосфата. Клинические переменные оценивались исходно, через 3 и 6 месяцев. Конусно-лучевая компьютерная томография выполнялась исходно и через 6 мес. Кроме того, по согласованию с пациентами было проведено среднесрочное последующее наблюдение.
Результаты
Наш метод признан безопасным, серьезных нежелательных явлений выявлено не было. Все результаты, в том числе уменьшение глубины пародонтального зондирования (среднее ± SD, 3,2 ± 1,9 мм), усиление клинического прикрепления (2,5 ± 2,6 мм) и увеличение рентгенологической высоты кости (2,3 ± 1,8 мм), были улучшены во всех 10 случаях. через 6 месяцев после трансплантации. Эти терапевтические эффекты сохранялись в течение среднего периода наблюдения 55 ± 19 месяцев, и серьезных побочных эффектов не было.
Выводы
Результаты этого исследования подтверждают безопасность и эффективность аутологичных клеточных слоев, полученных из PDL, при тяжелых дефектах пародонта, а также стабильность этой эффективности в течение средне-долгосрочного наблюдения. Этот цитотерапевтический подход, основанный на инженерии клеточных слоев, предлагает инновационную стратегию лечения признанной неудовлетворенной потребности в лечении тяжелых пародонтальных дефектов.
Ключевые слова: Пародонтальная регенерация, Цитотерапия, Клеточный лист, Клиническое исследование, Мультипотентные мезенхимальные стромальные клетки (МСК), Периодонтальная связка, Конусно-лучевая компьютерная томография (КЛКТ), Стволовые клетки
Пародонтит (заболевание десен) представляет собой вызванное бактериями воспалительное заболевание, поражающее опорные структуры зубов, включая челюстную кость, периодонтальную связку (PDL) и цемент. Пародонтит не только вызывает функциональные и эстетические проблемы в полости рта, но и связан с системными заболеваниями, такими как сахарный диабет, преждевременные роды, сердечно-сосудистые заболевания, инсульт и заболевания легких [1]. Обычные методы лечения могут лишь отсрочить прогрессирование заболевания, а терапевтический эффект от различных резекционных операций считается минимальным. Чтобы смягчить эти ограничения, регенеративная терапия исследуется уже почти 100 лет [2]. Костные трансплантаты, барьерные мембраны и другие биологические материалы одобрены в клиниках для лечения дефектов относительно небольших размеров; однако не существует подходящих методов лечения тяжелых дефектов, таких как одностеночные внутрикостные дефекты, дефекты фуркации класса III и горизонтальные дефекты. Большинство пародонтальных дефектов имеют такие тяжелые формы [3], поэтому цитотерапевтические подходы были исследованы в течение 21 века на основе развития тканевой инженерии и биологии стволовых клеток [4].
Пародонтит не только вызывает функциональные и эстетические проблемы в полости рта, но и связан с системными заболеваниями, такими как сахарный диабет, преждевременные роды, сердечно-сосудистые заболевания, инсульт и заболевания легких [1]. Обычные методы лечения могут лишь отсрочить прогрессирование заболевания, а терапевтический эффект от различных резекционных операций считается минимальным. Чтобы смягчить эти ограничения, регенеративная терапия исследуется уже почти 100 лет [2]. Костные трансплантаты, барьерные мембраны и другие биологические материалы одобрены в клиниках для лечения дефектов относительно небольших размеров; однако не существует подходящих методов лечения тяжелых дефектов, таких как одностеночные внутрикостные дефекты, дефекты фуркации класса III и горизонтальные дефекты. Большинство пародонтальных дефектов имеют такие тяжелые формы [3], поэтому цитотерапевтические подходы были исследованы в течение 21 века на основе развития тканевой инженерии и биологии стволовых клеток [4].
Стволовые клетки были идентифицированы из ткани PDL человека и предложены в качестве перспективного источника клеток для регенерации пародонта [5], [6]. В то же время наша лаборатория разработала «технологию разработки клеточного листа», используя термочувствительную поверхность клеточной культуры [7], в которой все культивируемые клетки могут быть собраны в виде интактного трансплантируемого клеточного листа путем снижения температуры чашки для культивирования. Сообщалось о нескольких клинических исследованиях с использованием «технологии инженерии клеточных листов», таких как реконструкция роговицы [8], лечение кардиомиопатии [9), эндоскопическое лечение изъязвления пищевода [10] и регенерацию слизистой оболочки среднего уха [11], а также безопасность и эффективность этих методов лечения аутологичными клеточными листками. Наша группа сосредоточилась на клетках, полученных из PDL, и объединила их с этой технологией для создания слоев клеток, полученных из PDL. Предыдущие эксперименты на животных показали эффективность клеточных слоев, полученных из PDL, в нескольких экспериментальных моделях пародонтальных дефектов [12], [13], [14], [15]. Кроме того, мы установили оптимальные методы экстракции и культивирования клеток, полученных из PDL человека [6], и подтвердили безопасность этих клеток [16], [17].
Кроме того, мы установили оптимальные методы экстракции и культивирования клеток, полученных из PDL человека [6], и подтвердили безопасность этих клеток [16], [17].
В этом исследовании мы изучили безопасность аутологичных клеточных слоев, полученных из PDL, в сочетании с бета-трикальцийфосфатом, а также регенеративный потенциал этого нового подхода в клинических условиях.
Это исследование было проведено в соответствии с принципами, изложенными в Хельсинкской декларации, и одобрено Институциональным наблюдательным советом Токийского женского медицинского университета (TWMU) по исследованиям на людях и министром здравоохранения, труда и социального обеспечения Японии в соответствии с « Руководство по клиническим исследованиям с использованием стволовых клеток человека». Все образцы были обработаны и культивированы в центре обработки клеток TWMU в соответствии с рекомендациями по надлежащей производственной практике (GMP). Это клиническое исследование было зарегистрировано в Реестре клинических испытаний UMIN под номером UMIN000005027 и контролировалось контрактной исследовательской организацией. Общий дизайн этого клинического исследования по регенерации тканей пародонта представлен на рис.
Общий дизайн этого клинического исследования по регенерации тканей пародонта представлен на рис.
Открыть в отдельном окне
Процедура регенерации пародонта с использованием аутологичных клеточных слоев, полученных из PDL, в сочетании с гранулами β-трикальцийфосфата. 1. Собственный лишний зуб пациента был удален, ткань PDL была соскоблена и ферментативно расщеплена до отдельных клеток. 2. После размножения клетки, полученные из PDL, распределяли на чувствительных к температуре чашках для культивирования, затем создавали трехслойные клеточные листы, полученные из PDL. 3. Трехслойные клеточные листы, полученные из PDL, с сеткой PGA обрезали до размера дефекта и трансплантировали на поверхность корня. 4. Заполнение костных дефектов гранулами β-трикальцийфосфата.
2.1. Пациенты
Десять пациентов в возрасте от 33 до 63 лет (среднее значение [±SD], 46 ± 12) получили аутологичные трансплантации клеточных слоев, полученных из PDL, с ноября 2011 г. по май 2014 г. (). Все пациенты давали устное и письменное информированное согласие на каждое инвазивное вмешательство, всего 4 раза. Пациенты, у которых был периодонтит с глубиной зондирования более 4 мм после начальной терапии, подходили для включения. Другие критерии включения включали возраст >20 лет и наличие лишнего зуба, в котором сохранилась здоровая ткань пародонта в качестве источника клеток. Критерии исключения включали соответствующие медицинские состояния, противопоказанные хирургическим вмешательствам (например, сахарный диабет, сердечно-сосудистые заболевания, заболевания почек, печени или легких или ослабленная иммунная система), беременность или лактация, тяжелое курение табака (более 11 сигарет в день) или положительные результаты. на гепатит В, гепатит С, ВИЧ, HTLV или сифилис при первичном исследовании крови. График перед трансплантацией написан на дополнительном рис. 1. 9.0006
(). Все пациенты давали устное и письменное информированное согласие на каждое инвазивное вмешательство, всего 4 раза. Пациенты, у которых был периодонтит с глубиной зондирования более 4 мм после начальной терапии, подходили для включения. Другие критерии включения включали возраст >20 лет и наличие лишнего зуба, в котором сохранилась здоровая ткань пародонта в качестве источника клеток. Критерии исключения включали соответствующие медицинские состояния, противопоказанные хирургическим вмешательствам (например, сахарный диабет, сердечно-сосудистые заболевания, заболевания почек, печени или легких или ослабленная иммунная система), беременность или лактация, тяжелое курение табака (более 11 сигарет в день) или положительные результаты. на гепатит В, гепатит С, ВИЧ, HTLV или сифилис при первичном исследовании крови. График перед трансплантацией написан на дополнительном рис. 1. 9.0006
Таблица 1
Список пациентов, формы их дефектов и количество трансплантированных клеток. Количество клеток одного клеточного листа (880 мм 2 ) измеряли за сутки до трансплантации. Количество трехслойных клеточных листов рассчитывали на основе размера обрезанных клеточных листов. В некоторых случаях 2 или 3 зуба получали клеточную трансплантацию. Номер зуба указывает на зуб с самым глубоким дефектом.
Количество трехслойных клеточных листов рассчитывали на основе размера обрезанных клеточных листов. В некоторых случаях 2 или 3 зуба получали клеточную трансплантацию. Номер зуба указывает на зуб с самым глубоким дефектом.
| № | лет/пол | Smoking | Defect shape | Tooth number | Defect position | Million cells/sheet | Estimated transplanted cells (Million) |
|---|---|---|---|---|---|---|---|
| 1 | 33/M | − | 1 | 47 | Distal–Lingual | 2.00 | 0. 64 64 |
| 2 | 39/F | + | horizontal | 33 | Mesial–Lingual | 1.20 | 0.19 |
| 3 | 52/F | − | horizontal | 42 (43) | Distal–Buccal | 0.82 | 0.31 |
| 4 | 63/F | − | horizontal | 47 (45, 46) | Distal–Buccal | 1. 20 20 | 1.23 |
| 5 | 35/M | former | 1 | 46 | Mesial–Buccal | 0.66 | 0.17 |
| 6 | 58/F | former | circumferential | 17 | Mesial–Buccal | 0.55 | 0.12 |
| 7 | 57/F | former | horizontal | 25 (26) | Center–Buccal | 0. 63 63 | 0.38 |
| 8 | 36/M | former | 3 | 36 | Mesial–Lingual | 1.10 | 0.12 |
| 9 | 35/M | − | 1 | 37 | Distal–Buccal | 1.60 | 0.24 |
| 10 | 54/M | former | 2 | 44 | Мезиально-щечный | 1,30 | 0,53 |
Открыть в отдельном окне
2.
 2. Приготовление аутологичных сывороток
2. Приготовление аутологичных сывороток Периферическая кровь каждого пациента была исследована для подтверждения отрицательных результатов на гепатит В, гепатит С, ВИЧ, HTLV и сифилис. Для получения аутологичной сыворотки перед удалением зуба собирали 100–125 мл периферической крови и транспортировали в центр обработки клеток (ЦПК) Токийского женского медицинского университета. Затем кровь переносили в центрифужные пробирки объемом 50 мл и инкубировали при 37 °C в течение 1 часа. Проводят центрифугирование и собирают супернатант. Супернатант снова центрифугировали, супернатант фильтровали и затем использовали в качестве аутологичной сыворотки в культурах клеток.
2.3. Обработка клеток и листы клеток
Листы клеток, полученные из PDL, были созданы в центре обработки клеток, как описано ранее [16]. Вкратце, ткань PDL, полученная из зуба мудрости пациента, расщепляли коллагеназой/диспазой, а суспензии отдельных клеток пропускали через 70-мкм клеточный фильтр (Falcon, Франклин Лейкс, Нью-Джерси, США) и инкубировали на культуральном планшете (Falcon T-25). колба, primaria; BD Biosciences) в полной среде (α-MEM, содержащей 10 % аутологичной человеческой сыворотки, 2 мМЛ-глютамина (Sigma-Aldrich), 82,1 мкг/мл-фосфат магниевой соли аскорбиновой кислоты, n-гидрат (Wako Junyaku, Токио) , 40 мкг/мл гентамицина (GENTCIN; Schering-Plough, Осака) и 0,25 мкг/м амфотерицина B (FUNGIZONE; Bristol-Myers Squibb, Tokyo)). После 3 пассажей размножения в колбах Т-75 клетки высевали на термочувствительные чашки для культивирования (диаметром 35 мм, UpCell®, Cell Seed, Токио, Япония) при плотности клеток 2–4 × 10 4 клеток/чашку и культивировали в полной среде с дополнительным 82,1 мкг/мл n-гидрата магниевой соли фосфата аскорбиновой кислоты, 10 нМ дексаметазона (DEXART; Fuji pharma, Toyama) и 10 мМ β-глицерофосфата (Sigma-Aldrich ). Через две недели после культивирования в этой остеоиндуктивной среде аутологичные клеточные листы, полученные из PDL, собирали путем снижения температуры чашки для культивирования. Перед трансплантацией были проведены тесты на безопасность и контроль качества обработанных клеток in vitro , как описано ранее [6], [18] (дополнительные таблицы 1 и 3).
колба, primaria; BD Biosciences) в полной среде (α-MEM, содержащей 10 % аутологичной человеческой сыворотки, 2 мМЛ-глютамина (Sigma-Aldrich), 82,1 мкг/мл-фосфат магниевой соли аскорбиновой кислоты, n-гидрат (Wako Junyaku, Токио) , 40 мкг/мл гентамицина (GENTCIN; Schering-Plough, Осака) и 0,25 мкг/м амфотерицина B (FUNGIZONE; Bristol-Myers Squibb, Tokyo)). После 3 пассажей размножения в колбах Т-75 клетки высевали на термочувствительные чашки для культивирования (диаметром 35 мм, UpCell®, Cell Seed, Токио, Япония) при плотности клеток 2–4 × 10 4 клеток/чашку и культивировали в полной среде с дополнительным 82,1 мкг/мл n-гидрата магниевой соли фосфата аскорбиновой кислоты, 10 нМ дексаметазона (DEXART; Fuji pharma, Toyama) и 10 мМ β-глицерофосфата (Sigma-Aldrich ). Через две недели после культивирования в этой остеоиндуктивной среде аутологичные клеточные листы, полученные из PDL, собирали путем снижения температуры чашки для культивирования. Перед трансплантацией были проведены тесты на безопасность и контроль качества обработанных клеток in vitro , как описано ранее [6], [18] (дополнительные таблицы 1 и 3).
2.4. Трансплантация клеточного слоя
Хирургическая процедура состояла из предоперационной очистки, введения местной анестезии и отгибания щечных и язычных лоскутов на всю толщину для обеспечения хирургического обзора. Процедуры обеззараживания проводились с помощью ручных, ультразвуковых и вращающихся инструментов, а открытые поверхности корней впоследствии обрабатывались ЭДТА (PrefGel ® , Straumann, Базель, Швейцария) в течение 2 мин. После достаточного промывания физиологическим раствором трехслойные аутологичные клеточные листы, полученные из PDL, обрезали до размера дефекта и помещали на оголенную поверхность корня с помощью биоразлагаемой сетки из полигликолевой кислоты (Neoveil, толщина 0,15 мм; Gunze, Токио) и костной ткани. дефект был заполнен гранулами бета-трикальцийфосфата (β-TCP) (Osferion®, G1, Olympus Terumo Biomaterials, Tokyo, Japan) (). Послеоперационный уход включал системное введение азитромицина (Zithromac®, Pfizer, Токио, Япония) по 500 мг/сут в течение 3 дней. Диклофенак натрия (Вольтарен®, Новартис Фарма, Токио, Япония) был предоставлен по мере необходимости для обезболивания. Послеоперационная наддесневая профессиональная чистка зубов, а также клинические и рентгенологические измерения были запланированы через 6 месяцев после операции ().
Диклофенак натрия (Вольтарен®, Новартис Фарма, Токио, Япония) был предоставлен по мере необходимости для обезболивания. Послеоперационная наддесневая профессиональная чистка зубов, а также клинические и рентгенологические измерения были запланированы через 6 месяцев после операции ().
Открыть в отдельном окне
Хирургическая процедура. После операции с открытым лоскутом в соответствии с модифицированной процедурой Видмана (рис. 2А) 3-слойный клеточный лист, полученный из PDL, сохраненный с помощью тканого PGA, был обрезан до размера дефекта и установлен на поверхности корня (черный треугольник). Тканый PGA был установлен снаружи клеточных листов, полученных из PDL (рис. 2B). Гранулы β-трикальцийфосфата заполнили костный дефект, чтобы покрыть клеточные листы (рис. 2C).
Таблица 2
График клинического исследования. Были проведены опросы пациентов о 4 видах боли (спонтанная боль, гиперпселафезия, боль во время еды и судорожная боль), и каждая боль оценивалась по 4° (0: отсутствие боли, 1: слабая боль, 2: умеренная боль, 3: сильная боль). Осмотр полости рта включал наблюдение и фотографирование. Осмотр тканей пародонта включал определение глубины кармана при зондировании (PPD), кровоточивости при зондировании (BOP), уровня клинического прикрепления (CAL), десневого индекса (GI) и индекса зубного налета (PI). В профилактических целях проводилась наддесневая профессиональная чистка зубов.
Осмотр полости рта включал наблюдение и фотографирование. Осмотр тканей пародонта включал определение глубины кармана при зондировании (PPD), кровоточивости при зондировании (BOP), уровня клинического прикрепления (CAL), десневого индекса (GI) и индекса зубного налета (PI). В профилактических целях проводилась наддесневая профессиональная чистка зубов.
| Item | Before registration | Before transplantation | Transplantation | After transplantation | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Week | Month | |||||||||||||||||
| 1 | 2 | 1 | 2 | 3 История болезни пациента3 | Patient agreement | ● | ● | |||||||||||
| Blood tests for infectious disease | ● | |||||||||||||||||
| Interview | ● | ● | ● | ● | ● | ● | ● | |||||||||||
| Oral cavity inspection | ● | ● | ● | ● | ● | ● | ● | |||||||||||
| Transplantation of cell sheet | ● | |||||||||||||||||
| CBCT | ● | ● | Реагирование на неблагоприятные события0715||||||||||||||||
| Preventive treatment | ● | ● | ● | ● | ● | ● | ● | ● | ||||||||||
Open in a separate окно
2.
 5. Конечные точки исследования
5. Конечные точки исследования Первичной конечной точкой была безопасность аутологичных клеточных слоев, полученных из PDL, у пациентов с тяжелым периодонтитом. Безопасность оценивали на основании клинических данных и оценки боли, которые были получены из интервью с помощью вербальной оценочной шкалы с 4 степенями через 1, 2, 4, 8, 12 и 24 недели после трансплантации.
Вторичные конечные точки оценивали эффективность данного лечения. Клинические параметры, включая десневой индекс (GI), индекс зубного налета (PI), глубину кармана для зондирования (PPD), кровоточивость при зондировании (BOP) и уровень клинического прикрепления (CAL), регистрировали для оценки терапевтического эффекта на исходном уровне, через 3 месяца. , и 6 мес. Рентгенографическую оценку проводили с помощью конусно-лучевой рентгеновской компьютерной томографии (КЛКТ) (3DX, J. Morita, Киото, Япония) и программного обеспечения производителя (I-View; Morita) в начале исследования и через 6 месяцев. В каждом случае выбирали самую глубокую точку дефекта и измеряли линейную высоту кости двумя исследователями вслепую. Анализировали среднее расстояние между цементно-эмалевой границей (ЦЭГ) и самой глубокой точкой дефекта. Среднесрочное последующее наблюдение проводилось с согласия пациентов, а КЛКТ выполнялась с интервалом не менее 6 месяцев.
Анализировали среднее расстояние между цементно-эмалевой границей (ЦЭГ) и самой глубокой точкой дефекта. Среднесрочное последующее наблюдение проводилось с согласия пациентов, а КЛКТ выполнялась с интервалом не менее 6 месяцев.
2.6. Статистический анализ
Статистически проанализированы изменения между исходным уровнем и периодами наблюдения с точки зрения первичных и вторичных конечных точек. Результаты выражены как среднее значение ± стандартное деление (SD), и был проведен критерий знакового ранга Уилкоксона. Двусторонняя вероятность (P) <0,05 считалась значимой.
В этом клиническом исследовании с ноября 2011 г. по май 2014 г. 10 пациентов (5 женщин) подверглись пародонтальной хирургии и трансплантации аутологичных клеточных слоев, полученных из PDL. информированное согласие. Хотя период наблюдения за каждым пациентом заканчивался через 6 месяцев после трансплантации в протоколе этого клинического исследования, пациенты с трансплантацией наблюдались в среднем в течение 55 месяцев (диапазон 15–79 месяцев). ).
).
Удаление зуба для сбора аутологичных клеток, полученных из PDL, не сопровождалось значительными осложнениями. Клетки, полученные из одного зуба, полученные из PDL, размножали в течение 2 недель и высевали на 6 температурно-чувствительных культуральных чашек с плотностью клеток 2–4 × 10 4 клеток/чашку. После 2 недель дополнительного культивирования с остеоиндуктивными добавками были созданы плотные и толстые 3-слойные клеточные листы, полученные из PDL (4,8 ± 2,1 × 10 5 клеток/см 2 ). Перед трансплантацией были проведены тесты контроля качества (дополнительная таблица 1), и все 10 продуктов прошли все тесты, установленные ранее [16], демонстрируя, что все продукты обладают характеристиками, подобными PDL. Мультипотентность всех продуктов, кроме № 6, также была показана после индукции остеогенеза или адипогенеза (дополнительная таблица 2), что позволяет предположить, что они также обладают свойствами, подобными мультипотентным мезенхимальным стромальным клеткам (МСК) [19]. ]. Для испытаний на безопасность кондиционированная среда для культивирования промежуточных продуктов была передана инспекционной компании (SRL Inc., Токио, Япония) для определения любого загрязнения перед отправкой. Конечные продукты также были проверены на микробное загрязнение, и все они прошли испытания (дополнительная таблица 3).
]. Для испытаний на безопасность кондиционированная среда для культивирования промежуточных продуктов была передана инспекционной компании (SRL Inc., Токио, Япония) для определения любого загрязнения перед отправкой. Конечные продукты также были проверены на микробное загрязнение, и все они прошли испытания (дополнительная таблица 3).
Хирургические вмешательства прошли без осложнений. После операции некоторые пациенты жаловались на боли; тем не менее, боль прошла без осложнений, как и ожидалось при обычных операциях на пародонте [20] (дополнительная таблица 4). В частности, пациент № 2 жаловался на сильную боль во время еды и схваткообразные боли через 1 неделю после операции. Ранее ей дважды делали пародонтальную операцию, и она упомянула, что боль после трансплантации была похожа на предыдущую пародонтальную операцию. О других осложнениях, связанных с трансплантацией клеточного листа, полученного из PDL, не сообщалось.
Изменения клинических и рентгенологических показателей представлены в . Клинические параметры, включая CAL, PPD и линейную высоту кости, значительно улучшились через 3 месяца и 6 месяцев по сравнению с исходными показателями. Среднее увеличение CAL составило 2,5 ± 1,8 мм через 3 месяца и 2,5 ± 2,6 мм через 6 месяцев. Среднее уменьшение PPD составило 2,8 ± 1,3 мм через 3 месяца и 3,2 ± 1,9 мм. Оценка визуализации с помощью КТ подтвердила увеличение линейной высоты кости на 2,3 ± 1,8 мм через 6 месяцев (), и не было никаких признаков анкилоза ни в одном из трансплантированных участков по данным анализа КЛКТ. Значимых изменений ГИ и ИП не было.
Клинические параметры, включая CAL, PPD и линейную высоту кости, значительно улучшились через 3 месяца и 6 месяцев по сравнению с исходными показателями. Среднее увеличение CAL составило 2,5 ± 1,8 мм через 3 месяца и 2,5 ± 2,6 мм через 6 месяцев. Среднее уменьшение PPD составило 2,8 ± 1,3 мм через 3 месяца и 3,2 ± 1,9 мм. Оценка визуализации с помощью КТ подтвердила увеличение линейной высоты кости на 2,3 ± 1,8 мм через 6 месяцев (), и не было никаких признаков анкилоза ни в одном из трансплантированных участков по данным анализа КЛКТ. Значимых изменений ГИ и ИП не было.
Таблица 3
Результаты обследования тканей пародонта и анализа КЛКТ. Осмотр тканей пародонта проводили через 3 и 6 месяцев после трансплантации. КЛКТ оценивали через 6 месяцев после трансплантации.
| Pt.# | 3M | 6M | |||
|---|---|---|---|---|---|
| Gain of CAL | Reduction of PPD | Gain of CAL | Reduction of PPD | Gain of linear bone | |
| 1 | 2 | 3 | 3 | 3 | 2. 31 31 |
| 2 | 1 | 1 | 3 | 2 | 0.50 |
| 3 | 1 | 3 | 1 | 3 | 1.07 |
| 4 | 5 | 5 | 7 | 7 | 5.89 |
| 5 | 3 | 4 | 1 | 4 | 3.59 |
| 6 | 3 | 2 | 2 | 2 | 1. 42 42 |
| 7 | 2 | 3 | 0 | 2 | 1.37 |
| 8 | 1 | 2 | 1 | 2 | 0.74 |
| 9 | 6 | 4 | 7 | 6 | 1.36 |
| 10 | 1 | 1 | 0 | 1 | 4.60 |
| Average | 2. 5 5 | 2.8 | 2.5 | 3.2 | 2.29 |
| SD | 1.8 | 1.3 | 2.6 | 1.9 | 1.81 |
Открыть в отдельном окне
Типичные случаи показаны в . A, B и C показывают изображения КЛКТ пациентов № 1, № 4 и № 10 соответственно. В частности, резкое заживление наблюдалось в случае B. Пациентка, 63-летняя женщина, потеряла альвеолярный отросток над верхушкой корня с вовлечением фуркаций в нижний правый второй моляр в результате периодонтита и окклюзионной травмы. После первоначальной пародонтальной терапии глубокие пародонтальные дефекты в нижних правых премолярах и молярах были обработаны тканевыми клеточными пластинами. Через 6 месяцев после операции у пациента восстановилась жевательная функция, регенерация пародонта была подтверждена КЛКТ (В, в центре). На момент написания этой статьи, через 35 месяцев после операции, у пациента не было проблем с трансплантацией, а уровень кости был стабильным (В, справа).
На момент написания этой статьи, через 35 месяцев после операции, у пациента не было проблем с трансплантацией, а уровень кости был стабильным (В, справа).
Открыть в отдельном окне
A: КТ исходного состояния (слева), через 6 месяцев (в центре) и через 75 месяцев (справа) после операции для пациента № 1. У больного 33-х лет выявлен межкостный дефект 1 стенки дистально нижнего второго моляра справа. Линейная высота кости увеличилась на 2,31 мм за 6 месяцев и постепенно увеличивалась в течение этого наблюдения. B: КТ-изображения исходного уровня (слева), 6 месяцев (в центре) и 35 месяцев (справа) после операции для пациента № 4. У больной 63-х лет выявлены внутрикостные дефекты нижних премоляров и моляров слева с вовлечением фуркаций. Костный дефект доходил до верхушки дистального корня второго моляра. Через 6 мес после операции фуркация закрылась, линейная высота кости увеличилась на 5,89.мм (рис. 3B, центр). Через 35 месяцев уровень кости был стабильным (рис. 3B справа). C: КТ исходного уровня (слева), 6 месяцев (в центре) и 12 месяцев (справа) после операции для пациента № 10. У мужчины 54-х лет выявлен двухстеночный внутрикостный дефект в вестибулярной области нижнего правого первого моляра. Линейная высота кости увеличилась на 4,6 мм через 6 месяцев (рис. 3C в центре) и постепенно увеличивалась через 12 месяцев после операции (рис. 3C справа). Стрелки указывают на наиболее апикальную часть костных дефектов.
C: КТ исходного уровня (слева), 6 месяцев (в центре) и 12 месяцев (справа) после операции для пациента № 10. У мужчины 54-х лет выявлен двухстеночный внутрикостный дефект в вестибулярной области нижнего правого первого моляра. Линейная высота кости увеличилась на 4,6 мм через 6 месяцев (рис. 3C в центре) и постепенно увеличивалась через 12 месяцев после операции (рис. 3C справа). Стрелки указывают на наиболее апикальную часть костных дефектов.
Перспективным источником клеток для регенерации пародонта являются стволовые клетки, полученные из тканей PDL [21], и механизм действия регенерации периодонта включает в себя то, как стволовые клетки, полученные из PDL, рекрутируются, пролиферируют и дифференцируются в пародонтальные компоненты с соответствующей пространственно-временной последовательностью. [22]. Для достижения этой регенерации были внедрены различные подходы тканевой инженерии [23]. Наша лаборатория разработала «Технологию создания клеточных листов» [24], [25], а безопасность и эффективность клеточных слоев, полученных из PDL, ранее тестировали на моделях собак [12], [13]. Кроме того, мы оптимизировали условия культивирования клеток, полученных из PDL человека [6], проверили качество клеток, полученных из PDL человека [16], [17], и в январе 2011 г. и благосостояние в Японии.
Кроме того, мы оптимизировали условия культивирования клеток, полученных из PDL человека [6], проверили качество клеток, полученных из PDL человека [16], [17], и в январе 2011 г. и благосостояние в Японии.
В данное клиническое исследование было включено 12 пациентов; однако 2 случая были исключены во время культивирования клеток. Эти случаи были исключены, поскольку в одном случае клетки плохо размножались, а в другом произошло заражение коагулазонегативными стафилококками (ЦНС). В первом случае возможно, что прикрепленная ткань PDL была слишком маленькой, потому что источником клеток были остаточные корни с кариесом (верхний правый первый моляр). В последнем случае возможно, что первоначальное промывание зуба было недостаточным, поскольку к удаленному зубу прикрепились более крупные, чем ожидалось, сгустки крови. Напротив, создание листов клеток, полученных из PDL, для других 10 случаев было успешно завершено и прошло все тесты на безопасность и контроль качества. Таким образом, протокол выделения и культивирования клеток, полученных из PDL человека, был оптимизирован и проверен в этом исследовании.
Качество клеток, полученных из PDL, проверяли во всех случаях. Судя по результатам тестирования контроля качества перед отправкой, их жизнеспособность и реакция на остеоиндуктивную среду были такими, как и ожидалось для клеток, полученных из PDL. Как активность щелочной фосфатазы (ЩФ), так и положительная частота ЩФ были выше, чем заданные критерии (дополнительная таблица 1). Кроме того, экспрессия гена периостина была достаточной во всех случаях, что свидетельствует о том, что трансплантированные клетки сохраняли PDL-подобный фенотип [6], [26] без фенотипов фибробластов десен. Мы также провели анализы CFU-F и анализы множественной дифференцировки с использованием оставшихся клеток с фетальной бычьей сывороткой, и все, кроме № 6, обладали МСК-подобным фенотипом (дополнительная таблица 2). Трудность индуцирования образования кальцифицированных узелков из всех образцов может быть связана с индивидуальными вариациями, хотя в этом исследовании все они обладали колониеобразующей активностью и адипогенным потенциалом.
Аутологичные клеточные пластины, полученные из PDL, в сочетании с костными наполнителями β-TCP улучшили клинические и рентгенологические результаты в этом клиническом исследовании. До сих пор серьезных осложнений, связанных с трансплантацией клеток, в среднесрочном периоде наблюдения (в среднем 55 ± 19 месяцев) не было. Два случая наблюдались в местной клинике после 15 и 35 месяцев наблюдения из-за большого расстояния.
β-TCP, использованный в этом исследовании, представлял собой биоразлагаемые гранулы небольшого размера, которые, как было показано, замещались новообразованной костью через 6 месяцев [27]. В этом исследовании гистологические данные не могли быть собраны из-за этических ограничений; однако частицы имплантированного β-ТКФ не наблюдались, а костеподобная непрозрачная масса появлялась во всех случаях через 6 мес после операции. Большая часть β-TCP оказалась биодеградированной, как и предсказывал производитель, поэтому в этом протоколе можно было определить изменения линейной высоты кости. Кроме того, уровень кости был стабильным, и в этом исследовании были выявлены структуры, подобные костным трабекулам (1). Предыдущее клиническое исследование показало, что прирост линейной кости только за счет β-TCP составил 0,9.± 0,1 мм через 6 месяцев [28]. Хорошо известно, что морфология дефекта является одним из факторов, влияющих на регенерацию пародонта [29]. Наше исследование включало более крупные и сложные случаи, и мы смогли наблюдать улучшение многих параметров в этом клиническом исследовании. Таким образом, клеточные пластины, полученные из PDL, являются широко применимой терапией для лечения тяжелых дефектов пародонта. Во время среднесрочного наблюдения за этим исследованием было сообщено о рандомизированном клиническом испытании аутологичных стволовых клеток PDL с минеральными материалами бычьей кости для регенерации пародонта [30], основанное на предварительных отчетах о клинических случаях [31]. Авторам не удалось обнаружить значимой терапевтической эффективности стволовых клеток PDL; однако это может быть связано с медленной биорезорбируемостью бычьих материалов или одним из выбранных критериев включения, когда были выбраны дефекты небольшого размера.
Кроме того, уровень кости был стабильным, и в этом исследовании были выявлены структуры, подобные костным трабекулам (1). Предыдущее клиническое исследование показало, что прирост линейной кости только за счет β-TCP составил 0,9.± 0,1 мм через 6 месяцев [28]. Хорошо известно, что морфология дефекта является одним из факторов, влияющих на регенерацию пародонта [29]. Наше исследование включало более крупные и сложные случаи, и мы смогли наблюдать улучшение многих параметров в этом клиническом исследовании. Таким образом, клеточные пластины, полученные из PDL, являются широко применимой терапией для лечения тяжелых дефектов пародонта. Во время среднесрочного наблюдения за этим исследованием было сообщено о рандомизированном клиническом испытании аутологичных стволовых клеток PDL с минеральными материалами бычьей кости для регенерации пародонта [30], основанное на предварительных отчетах о клинических случаях [31]. Авторам не удалось обнаружить значимой терапевтической эффективности стволовых клеток PDL; однако это может быть связано с медленной биорезорбируемостью бычьих материалов или одним из выбранных критериев включения, когда были выбраны дефекты небольшого размера. Необходимы дальнейшие исследования для выбора подходящих материалов и форм дефектов для цитотерапевтического подхода к регенерации пародонта.
Необходимы дальнейшие исследования для выбора подходящих материалов и форм дефектов для цитотерапевтического подхода к регенерации пародонта.
В этом исследовании КЛКТ использовали для оценки костной регенерации пародонта. Была продемонстрирована точность КЛКТ [32], а также сообщается, что КЛКТ полезна для измерения пародонтальных дефектов [33]. Кроме того, с помощью внутриротовых рентгенограмм можно оценить только интерпроксимальные дефекты, поэтому мы внедрили КЛКТ для рентгенографической оценки регенерации пародонта, а линейное расстояние кости между цементно-эмалевой границей и основанием дефекта измеряли двумя слепыми экспертами.
Основным ограничением этого исследования аутологичной трансплантации было небольшое количество пациентов, у которых был избыточный зуб со здоровой тканью пародонта для использования в качестве источника клеток. Эту проблему можно решить с помощью аллогенных МСК, поскольку МСК обладают иммуномодулирующей активностью, которая должна минимизировать иммунное отторжение [34]. В стоматологии молодые зубы обычно удаляют по ортодонтическим показаниям или из-за ретенции, а затем выбрасывают в клиниках как медицинские отходы, таким образом, можно регулярно получать клетки, полученные из аллогенных тканей зубов. Поскольку пациенты в группах без трансплантации не могут получить трансплантацию, несмотря на удаление зуба, этически сложно начать рандомизированное исследование с аутологичными клетками. Кроме того, аутологичные клетки нельзя использовать для трансплантации другим пациентам, кроме исходного донора, что приводит к дорогостоящим медицинским расходам. Поэтому в настоящее время мы планируем создать банк аллогенных клеток МСК, происходящих из PDL, и оптимальные процедуры для отбора, криоконсервации и накопления стволовых клеток, которые накапливаются для будущих аллогенных клинических испытаний.
В стоматологии молодые зубы обычно удаляют по ортодонтическим показаниям или из-за ретенции, а затем выбрасывают в клиниках как медицинские отходы, таким образом, можно регулярно получать клетки, полученные из аллогенных тканей зубов. Поскольку пациенты в группах без трансплантации не могут получить трансплантацию, несмотря на удаление зуба, этически сложно начать рандомизированное исследование с аутологичными клетками. Кроме того, аутологичные клетки нельзя использовать для трансплантации другим пациентам, кроме исходного донора, что приводит к дорогостоящим медицинским расходам. Поэтому в настоящее время мы планируем создать банк аллогенных клеток МСК, происходящих из PDL, и оптимальные процедуры для отбора, криоконсервации и накопления стволовых клеток, которые накапливаются для будущих аллогенных клинических испытаний.
Т.О. является основателем и директором совета директоров CellSeed, Inc. и владеет лицензиями на технологии и патентами Токийского женского медицинского университета. К. также является акционером CellSeed, Inc. Токийский женский медицинский университет получает средства на исследования от CellSeed, Inc. О других потенциальных конфликтах интересов, имеющих отношение к этой статье, не сообщалось.
К. также является акционером CellSeed, Inc. Токийский женский медицинский университет получает средства на исследования от CellSeed, Inc. О других потенциальных конфликтах интересов, имеющих отношение к этой статье, не сообщалось.
Авторы благодарят Хозуэ Курода из Института передовой биомедицинской инженерии и науки Токийского женского медицинского университета за превосходное культивирование клеток в центре обработки клеток и техническую поддержку; Йошиаки Хара из стоматологической клиники Belledame за набор пациента; а также Халли Торп и Себастьян Шёквист из Института передовой биомедицинской инженерии и науки Токийского женского медицинского университета за редактирование на английском языке и ценные советы.
Это исследование было поддержано Программой создания инновационных центров для перспективных междисциплинарных областей исследований Проекта по разработке инновационных систем «Центр инженерии клеточных листов ткани (CSTEC)» Министерства образования, культуры, спорта, науки и технологий (MEXT). ), Япония.
), Япония.
Экспертная оценка под ответственностью Японского общества регенеративной медицины.
Приложение A Дополнительные данные, относящиеся к этой статье, можно найти по адресу https://doi.org/10.1016/j.reth.2018.07.002.
Ниже приведены дополнительные данные, относящиеся к этой статье:
Дополнительный рисунок 1. График клинического потока, производственного потока и осмотра. Информированное согласие было получено 4 раза при каждом инвазивном событии. Каждое исследование проводилось в соответствии с этим графиком, и результаты показаны в дополнительных таблицах 1 и 3.
Дополнительная таблица 1. В таблице показаны результаты тестов контроля качества, проведенных за день до отправки, как описано ранее [16], [18]. Два листа клеток, полученных из PDL, использовались только для этих проверок. Экспрессию гена периостина исследовали с помощью зонда Taqman (Hs00170815_m1) и рассчитывали ΔCT внутреннего контроля (4326315E) в двух повторностях.
Дополнительная таблица 2. В этой таблице показаны результаты соотношений колониеобразующих единиц фибробластов (КОЕ-Ф) и потенциала остео- и адиподифференцировки каждой клетки, происходящей из PDL. Когда проводили 3-й пассаж для посева в температурно-чувствительные чашки, остальные клетки, полученные из PDL, выводили из CPC. Эти клетки, полученные из PDL, распределяли на чашках для культивирования диаметром 100 мм по 50 или 100 клеток на чашку, затем проводили исследования CFU-F и дифференцировки с эмбриональной бычьей сывороткой, как описано ранее [6]. Вкратце, 100 клеток распределяли на чашке для культивирования диаметром 100 мм в трех экземплярах и культивировали в течение 9 дней.или 10 дней, окрашивают кристаллическим фиолетовым и подсчитывают. Количество колоний, положительных по кристаллическому фиолетовому, >2 мм в диаметре рассматривали как КОЕ-F (%). Для остеогенной (Os) или адипогенной (Ad) дифференцировки клетки распределяли на культуральных чашках диаметром 100 мм по 50 или 100 клеток/чашку соответственно. Клетки росли в нормальной среде в течение 9 или 10 дней, затем культуральную среду переводили на остеоиндуктивную или адипоиндуктивную среду на 21 день. Подсчитывали количество положительных колоний на ализарин красный-S или масляный красный О, затем рассчитывали коэффициент дифференциации в трех повторностях в каждом образце соответственно. Среднее соотношение было показано в таблице.
Клетки росли в нормальной среде в течение 9 или 10 дней, затем культуральную среду переводили на остеоиндуктивную или адипоиндуктивную среду на 21 день. Подсчитывали количество положительных колоний на ализарин красный-S или масляный красный О, затем рассчитывали коэффициент дифференциации в трех повторностях в каждом образце соответственно. Среднее соотношение было показано в таблице.
Дополнительная таблица 3. В таблице показаны результаты внешних испытаний на загрязнение. Безопасность клеточных листов, полученных из PDL, была подтверждена этими тестами, запланированными на дополнительном рисунке 1.
Дополнительная таблица 4. Результаты интервью с 4-степенной вербальной оценочной шкалой на 1, 2, 4, 8, 12 и 24. недель после трансплантации. Четыре вида боли (спонтанная боль, гиперпселафезия, боль во время еды и схваткообразная боль) оценивались по четырем вариантам (0: нет, 1: легкая, 2: умеренная, 3: сильная).
Мультимедийный компонент 1:
Щелкните здесь для просмотра. (174K, pptx) Мультимедийный компонент 1
(174K, pptx) Мультимедийный компонент 1
1. Pihlstrom B.L., Michalowicz B.S., Johnson N.W. Заболевания пародонта. Ланцет. 2005; 366: 1809–1820. [PubMed] [Google Scholar]
2. Хегедус З. Восстановление альвеолярных отростков костной трансплантацией. Стоматологический Космос. 1923; 65: 736–742. [Google Scholar]
3. Джаякумар А., Рохини С., Навин А., Харита А., Редди К. Горизонтальная потеря альвеолярной кости: пародонтальная сирота. J Indian Soc Periodontol. 2010;14:181–185. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Ивата Т., Васио К., Йошида Т., Исикава И., Андо Т., Ямато М. Инженерия клеточных пластин и ее применение для регенерации периодонта. J Tissue Eng Regen Med. 2015;9:343–356. [PubMed] [Google Scholar]
5. Сео Б.М., Миура М., Гронтос С., Бартольд П.М., Батули С., Брахим Дж. Исследование мультипотентных постнатальных стволовых клеток периодонтальной связки человека. Ланцет. 2004; 364: 149–155. [PubMed] [Google Scholar]
6. Ивата Т., Ямато М., Чжан З., Мукобата С., Васио К., Андо Т. Валидация клеток, полученных из периодонтальной связки человека, как надежного источника для цитотерапевтического применения. Дж. Клин Пародонтол. 2010; 37: 1088–109.9. [PubMed] [Google Scholar]
Ивата Т., Ямато М., Чжан З., Мукобата С., Васио К., Андо Т. Валидация клеток, полученных из периодонтальной связки человека, как надежного источника для цитотерапевтического применения. Дж. Клин Пародонтол. 2010; 37: 1088–109.9. [PubMed] [Google Scholar]
7. Ямада Н., Окано Т., Сакаи Х., Карикуса Ф., Савасаки Ю., Сакураи Ю. Термочувствительные полимерные поверхности; контроль прикрепления и открепления культивируемых клеток. Makromol Chem Rapid Commun. 1990; 11: 571–576. [Google Scholar]
8. Нисида К., Ямато М., Хаяшида Ю., Ватанабэ К., Маэда Н., Ватанабэ Х. Функциональные биоинженерные трансплантаты эпителия роговицы из стволовых клеток роговицы, выращенных ex vivo на термочувствительных клетках. Поверхность культуры. Трансплантация. 2004;77:379–385. [PubMed] [Google Scholar]
9. Miyagawa S., Domae K., Yoshikawa Y., Fukushima S., Nakamura T., Saito A. Фаза I клинических испытаний аутологичной трансплантации стволовых клеток для лечения кардиомиопатии. J Am Heart Assoc. 2017;6 [PMC free article] [PubMed] [Google Scholar]
2017;6 [PMC free article] [PubMed] [Google Scholar]
10. Ohki T., Yamato M., Ota M., Takagi R., Murakami D., Kondo M. Предотвращение стриктур пищевода после эндоскопической подслизистой диссекции с использованием тканеинженерных клеточных пластин. Гастроэнтерология. 2012;143 582-8 e1–2. [PubMed] [Академия Google]
11. Ямамото К., Ямато М., Морино Т., Сугияма Х., Такаги Р., Ягучи Ю. Регенерация слизистой оболочки среднего уха с помощью трансплантации тканеинженерных клеточных слоев. NPJ Regen Med. 2017;2:6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Ивата Т., Ямато М., Цучиока Х., Такаги Р., Мукобата С., Васио К. Регенерация пародонта с помощью многослойных клеток, полученных из периодонтальной связки листы в собачьей модели. Биоматериалы. 2009;30:2716–2723. [PubMed] [Google Scholar]
13. Цуманума Ю., Ивата Т., Васио К., Йошида Т., Ямада А., Такаги Р. Сравнение различных слоев тканевых стволовых клеток для регенерации периодонта у собак 1 — модель дефекта стенки. Биоматериалы. 2011;32:5819–5825. [PubMed] [Google Scholar]
Биоматериалы. 2011;32:5819–5825. [PubMed] [Google Scholar]
14. Ивата Т., Ямато М., Исикава И., Андо Т., Окано Т. Тканевая инженерия тканей пародонта. Анат Рек. 2014; 297:16–25. [PubMed] [Google Scholar]
15. Цуманума Ю., Ивата Т., Киношита А., Васио К., Йошида Т., Ямада А. Аллогенная трансплантация слоев мультипотентных мезенхимальных стромальных клеток, полученных из периодонтальной связки, у собак в критическом состоянии. Модель супраальвеолярного пародонтального дефекта размеров. Биорес в открытом доступе. 2016;5:22–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Washio K., Iwata T., Mizutani M., Ando T., Yamato M., Okano T. Оценка клеточных слоев, полученных из клеток периодонтальной связки человека: доклиническое исследование. Сотовые Ткани Res. 2010; 341:397–404. [PubMed] [Google Scholar]
17. Йошида Т., Васио К., Ивата Т., Окано Т., Исикава И. Текущее состояние и будущее развитие клеточной трансплантационной терапии для регенерации тканей пародонта. Инт Дж. Дент. 2012; 2012:307024. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Инт Дж. Дент. 2012; 2012:307024. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Washio K., Kuroda H., Iwata T., Yoshida T., Yamato M., Okano T. Улучшенная ферментативная обработка для точного подсчета клеток внеклеточного матрикса. богатые клеточные листки периодонтальной связки. Оральные челюстно-лицевые имплантаты Int J. 2014;29: e117–e121. [PubMed] [Google Scholar]
19. Доминичи М., Ле Блан К., Мюллер И., Слапер-Кортенбах И., Марини Ф., Краузе Д. Минимальные критерии для определения мультипотентных мезенхимальных стромальных клеток. Заявление Международного общества клеточной терапии. Цитотерапия. 2006; 8: 315–317. [PubMed] [Google Scholar]
20. Curtis J.W., Jr., McLain J.B., Hutchinson R.A. Частота и тяжесть осложнений и боли после операций на пародонте. J Пародонтол. 1985; 56: 597–601. [PubMed] [Академия Google]
21. Бартольд П.М., Ши С., Гронтос С. Стволовые клетки и регенерация периодонта. Пародонтол. 2000; 2006(40):164–172. [PubMed] [Google Scholar]
22. Мирон Р.Дж., Чжан Ю.Ф. Остеоиндукция: обзор старых концепций с новыми стандартами. Дж. Дент Рез. 2012; 91: 736–744. [PubMed] [Google Scholar]
Мирон Р.Дж., Чжан Ю.Ф. Остеоиндукция: обзор старых концепций с новыми стандартами. Дж. Дент Рез. 2012; 91: 736–744. [PubMed] [Google Scholar]
23. Chen F.M., Sun HH, Lu H., Yu Q. Терапия доставки стволовых клеток для регенерации тканей пародонта. Биоматериалы. 2012;33:6320–6344. [PubMed] [Google Scholar]
24. Hasegawa M., Yamato M., Kikuchi A., Okano T., Ishikawa I. Листы клеток периодонтальной связки человека могут регенерировать ткань периодонтальной связки на бестимусной модели крысы. Ткань англ. 2005;11:469–478. [PubMed] [Google Scholar]
25. Akizuki T., Oda S., Komaki M., Tsuchioka H., Kawakatsu N., Kikuchi A. Применение клеточного слоя периодонтальной связки для регенерации периодонта: пилотное исследование на собаках породы бигль. . J пародонтальный рез. 2005; 40: 245–251. [PubMed] [Google Scholar]
26. Somerman M.J., Archer S.Y., Imm G.R., Foster R.A. Сравнительное исследование клеток периодонтальной связки человека и фибробластов десен in vitro. Дж. Дент Рез. 1988; 67: 66–70. [PubMed] [Академия Google]
Дж. Дент Рез. 1988; 67: 66–70. [PubMed] [Академия Google]
27. Катагири В., Осуги М., Каваи Т., Хиби Х. Первое исследование на людях и отчеты о клинических случаях регенерации альвеолярной кости с помощью секретома мезенхимальных стволовых клеток человека. Голова Лицо Мед. 2016;12:5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Невинс М., Джаннобиле В.В., Макгуайр М.К., Као Р.Т., Меллониг Дж.Т., Хинрихс Дж.Е. Тромбоцитарный фактор роста стимулирует наполнение кости и скорость увеличения уровня прикрепления: результаты крупного многоцентрового рандомизированного контролируемого исследования. J Пародонтол. 2005;76:2205–2215. [PubMed] [Академия Google]
29. Рейнольдс М.А., Као Р.Т., Камарго П.М., Катон Дж.Г., Клем Д.С., Фиореллини Дж.П. Регенерация пародонта — внутрикостные дефекты: согласованный отчет семинара по регенерации AAP. J Пародонтол. 2015;86:S105–S107. [PubMed] [Google Scholar]
30. Chen F.M., Gao L.N., Tian B.M., Zhang X.Y., Zhang Y.J. , Dong G.Y. Лечение пародонтальных внутрикостных дефектов с использованием аутологичных стволовых клеток периодонтальной связки: рандомизированное клиническое исследование. Стволовые клетки Res Ther. 2016;7:33. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Dong G.Y. Лечение пародонтальных внутрикостных дефектов с использованием аутологичных стволовых клеток периодонтальной связки: рандомизированное клиническое исследование. Стволовые клетки Res Ther. 2016;7:33. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Фэн Ф., Акияма К., Лю Ю., Ямаза Т., Ван Т.М., Чен Дж.Х. Полезность предшественников PDL для регенерации тканей in vivo: отчет о 3 случаях. Оральный Дис. 2010;16:20–28. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Lascala C.A., Panella J., Marques M.M. Анализ точности линейных измерений, полученных с помощью конусно-лучевой компьютерной томографии (CBCT-NewTom) Dentomaxillofac Radiol. 2004; 33: 291–294. [PubMed] [Google Scholar]
33. Миш К.А., Йи Э.С., Сармент Д.П. Точность конусно-лучевой компьютерной томографии для измерения дефектов пародонта. J Пародонтол. 2006; 77: 1261–1266. [PubMed] [Академия Google]
34. Каплан А.И., Корреа Д. МСК: травмпункт. Клеточная стволовая клетка. 2011; 9:11–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
Статьи по регенеративной терапии предоставлены здесь с разрешения Японского общества регенеративной медицины
Новый класс мембран, способных регенерировать ткани и кости, эффективное решение для пародонтита
Пародонтитом страдает почти половина американцев в возрасте 30 лет и старше, и на поздних стадиях он может привести к ранней потере зубов или к более серьезным последствиям. Недавние исследования показали, что пародонтит может также увеличить риск сердечно-сосудистых заболеваний и болезни Альцгеймера.
Группа исследователей Калифорнийского университета в Лос-Анджелесе разработала методы, которые могут привести к более эффективной и надежной терапии заболеваний пародонта, которые способствуют регенерации ткани десны и кости с биологическими и механическими свойствами, которые можно регулировать в зависимости от потребностей лечения. Исследование опубликовано онлайн в ACS Nano.
Пародонтит — это хроническое деструктивное заболевание, при котором воспаляются десны, окружающие зуб, и в конечном итоге разрушается структура, удерживающая зуб на месте, образуя инфицированные карманы, что приводит к потере кости и зубов. Текущие методы лечения включают методы борьбы с инфекциями; применение молекул, способствующих росту тканей, также известных как факторы роста; и направленная регенерация тканей, которая считается оптимальным стандартом лечения пародонтита.
Направленная регенерация тканей в случае пародонтита включает использование мембраны или тонкой пленки, которую хирургическим путем помещают между воспаленной десной и зубом. Мембраны, которые выпускаются в небиоразлагаемых и биоразлагаемых формах, предназначены не только как барьеры между инфекцией и деснами, но и как система доставки лекарств, антибиотиков и факторов роста в ткань десны.
К сожалению, результаты направленной регенерации тканей противоречивы. Существующие мембраны не способны напрямую регенерировать ткань десны и не способны сохранять свою структуру и стабильность при помещении в полость рта. Мембрана также не может поддерживать длительную доставку лекарств, что необходимо для заживления инфицированной ткани десны. Для небиоразлагаемых мембран требуется несколько операций по удалению мембраны после того, как были выпущены какие-либо лекарства, что ставит под угрозу процесс заживления.
Мембрана также не может поддерживать длительную доставку лекарств, что необходимо для заживления инфицированной ткани десны. Для небиоразлагаемых мембран требуется несколько операций по удалению мембраны после того, как были выпущены какие-либо лекарства, что ставит под угрозу процесс заживления.
«Учитывая текущие недостатки направленной регенерации тканей, мы увидели необходимость в разработке нового класса мембран, обладающих свойствами регенерации тканей и костей, а также гибким покрытием, которое может прилипать к ряду биологических поверхностей», — сказал д-р. Алиреза Мошавериния, соавтор исследования и доцент кафедры ортопедии в Школе стоматологии Калифорнийского университета в Лос-Анджелесе. «Мы также нашли способ продлить сроки доставки лекарств, что является ключом к эффективному заживлению ран».
Команда начала с одобренного FDA полимера — крупномасштабной синтетической молекулы, обычно используемой в биомедицинских целях. Поскольку поверхность полимера не подходит для адгезии клеток при пародонтологическом лечении, исследователи ввели полидофаминовое покрытие — полимер, обладающий превосходными адгезивными свойствами и способный прикрепляться к поверхностям во влажных условиях. Еще одно преимущество использования такого покрытия заключается в том, что оно ускоряет регенерацию кости, способствуя минерализации гидроксиапатита, минерала, входящего в состав зубной эмали и кости.
Еще одно преимущество использования такого покрытия заключается в том, что оно ускоряет регенерацию кости, способствуя минерализации гидроксиапатита, минерала, входящего в состав зубной эмали и кости.
Определив оптимальную комбинацию для своей новой мембраны, исследователи использовали электропрядение, чтобы соединить полимер с полидофаминовым покрытием. Электропрядение — это производственный метод, который одновременно вращает два вещества с высокой скоростью с положительными и отрицательными зарядами и сплавляет их вместе для создания одного вещества. Чтобы улучшить поверхность и структурные характеристики своей новой мембраны, исследователи использовали шаблоны из металлической сетки в сочетании с электроспиннингом для создания различных рисунков или микрорисунков, подобных поверхности марли или вафли.
«Создавая микроструктуру на поверхности мембраны, мы теперь можем локализовать клеточную адгезию и управлять структурой мембраны», — сказал соавтор Пол Вайс, президентский председатель Калифорнийского университета и выдающийся профессор химии и биохимии. биоинженерия, а также материаловедение и инженерия в Калифорнийском университете в Лос-Анджелесе. «Мы смогли имитировать сложную структуру ткани пародонта, и при размещении наша мембрана дополняет правильную биологическую функцию с каждой стороны».
биоинженерия, а также материаловедение и инженерия в Калифорнийском университете в Лос-Анджелесе. «Мы смогли имитировать сложную структуру ткани пародонта, и при размещении наша мембрана дополняет правильную биологическую функцию с каждой стороны».
Чтобы проверить безопасность и эффективность своей новой мембраны, исследователи вводили крысам человеческие стволовые клетки, полученные из десны, и человеческие стволовые клетки периодонтальной связки. После восьми недель оценки деградации мембран и реакции ткани они заметили, что узорчатая полимерная мембрана с покрытием из полидофамина обеспечивает более высокий уровень прироста костной массы по сравнению с моделями без мембраны или с мембраной без покрытия.
Чтобы удовлетворить широкий спектр медицинских и стоматологических применений, исследователи также придумали способ регулировать скорость, с которой их мембраны разрушаются при вставке в свои модели. Они сделали это, добавляя и удаляя различные окислители или используя более легкие полимерные основы, прежде чем пройти процесс электропрядения. Возможность увеличивать или уменьшать скорость деградации помогла исследователям контролировать время доставки лекарств в нужные области.
Возможность увеличивать или уменьшать скорость деградации помогла исследователям контролировать время доставки лекарств в нужные области.
«Мы определили, что наши мембраны способны замедлять пародонтальную инфекцию, способствовать регенерации костей и тканей и оставаться на месте достаточно долго, чтобы продлевать доставку полезных лекарств», — сказал Мошавериния. «Мы видим, что это приложение распространяется не только на лечение периодонтита, но и на другие области, требующие ускоренного заживления ран и пролонгированной терапии доставки лекарств».
Следующие шаги исследователей заключаются в том, чтобы оценить, могут ли их мембраны доставлять клетки с факторами роста в присутствии или в отсутствие стволовых клеток.
Первый автор исследования — Мохаммад Махди Хасани-Садрабади, ученый проекта Калифорнийского университета в Лос-Анджелесе в области химии; биохимия и биоинженерия. Другими авторами являются Патрисия Саррион, Нако Накацука, Томас Янг, Ника Тагдири, Сахар Ансари, Тара Агалу, Сонг Ли и Али Хадемхосейни, все из Калифорнийского университета в Лос-Анджелесе.
