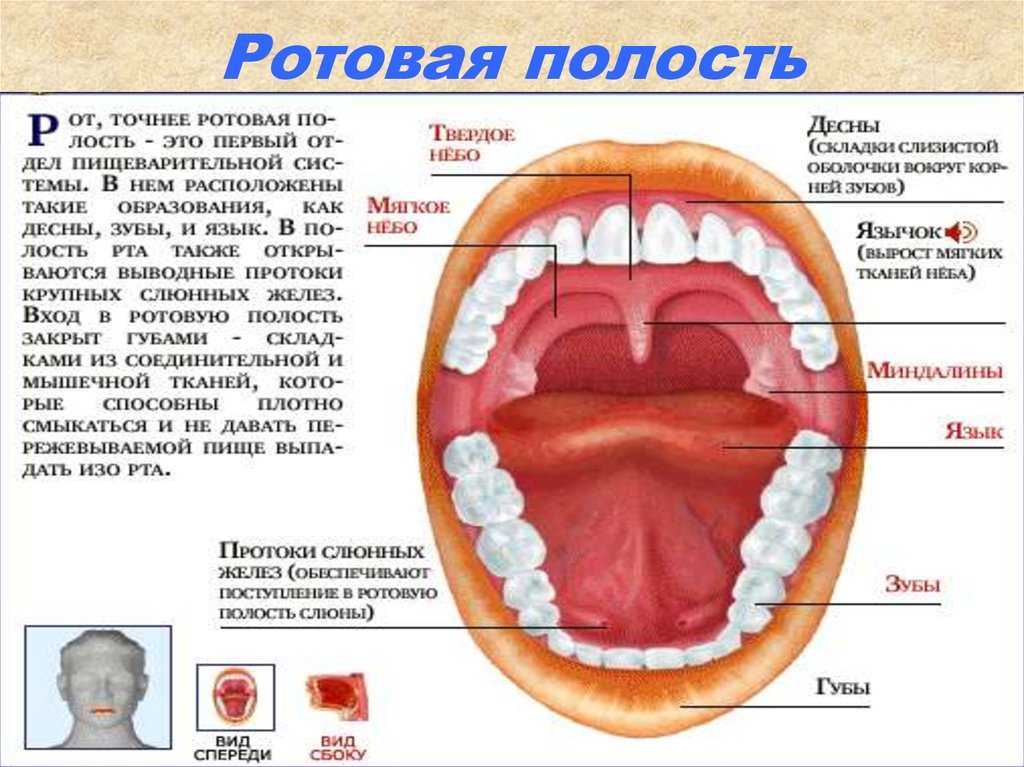
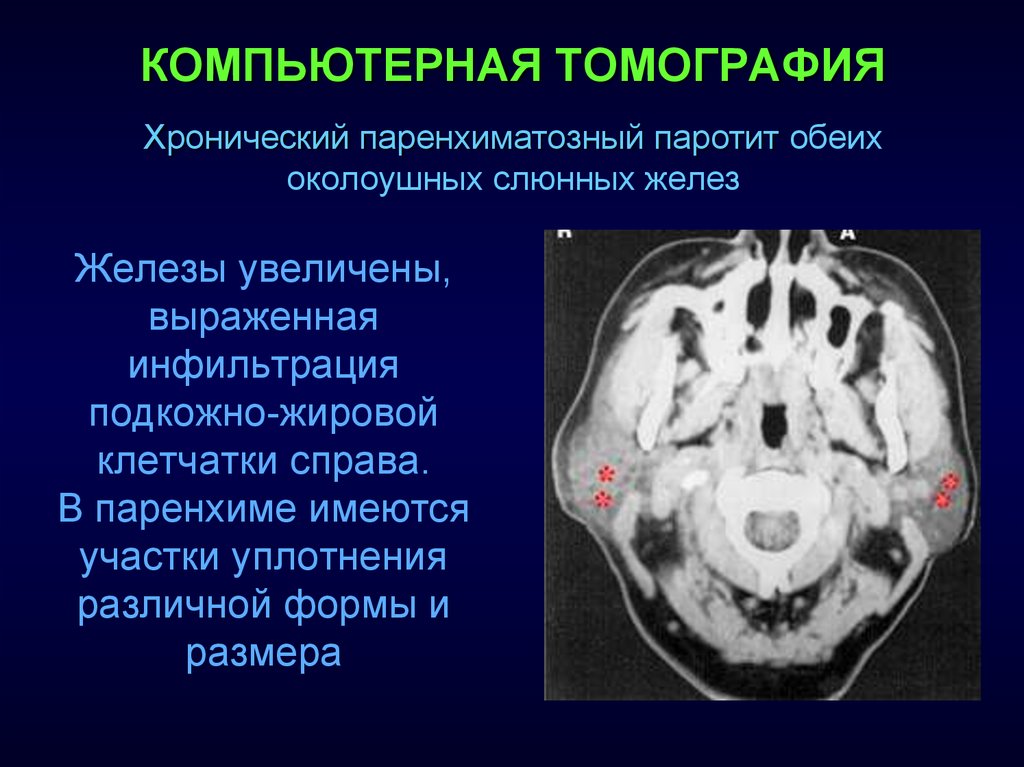
УЗИ слюнных желез в Новосибирске
Слюнные железы представляют собой парный орган, отвечающий за синтез слюны. Данная железа подвержена разнообразным патологическим процессам, а они существенно снижают качество жизни больного. Чтобы своевременно диагностировать заболевание, нужно выполнить ультразвуковую диагностику слюнных желез. Манипуляция абсолютно безопасна и безболезненна, а также обладает невероятно высокой информативностью, точностью.
Преимущества
Все виды УЗИ-диагностики
Опытные специалисты с большим стажем работы
Высокий сервис обслуживания
Показания к УЗИ слюнных желез.
При наличии следующих симптомов рекомендуют проходить ультразвуковое исследование слюнных желез:
- Высокая температура тела;
- Боли возле уха;
- Уплотнение, покраснение, отек за ухом;
- Дискомфортные ощущения, локализующиеся в области между челюстью и ухом;
-
Чрезмерная сухость в ротовой полости, не спровоцированная диабетом.

Сперва выполняется сбор всего анамнеза. УЗИ назначают при подозрении на такие патологии, как:
- Кисты – проявляются в результате сбоя гормонального фона, а также при повреждении желез;
- Воспаление в слюнных железах — является осложнением гриппа, отита и прочих патологий простудного типа;
- Слюннокаменная болезнь — формируются при неправильном обмене кальция, провоцируют закупорку желез;
- Абсцессы — на УЗИ проявляются в виде расплывчатых и неровных контуров, отличаются сложным строением внутри, болевыми ощущениями при прощупывании, протекают на фоне повышенной температуры тела;
- Увеличение лимфатических узлов, которые расположены поблизости;
- Болезни органа врожденного характера — лишние протоки и дополнительные дольки;
-
Новообразования злокачественного и доброкачественного характера.

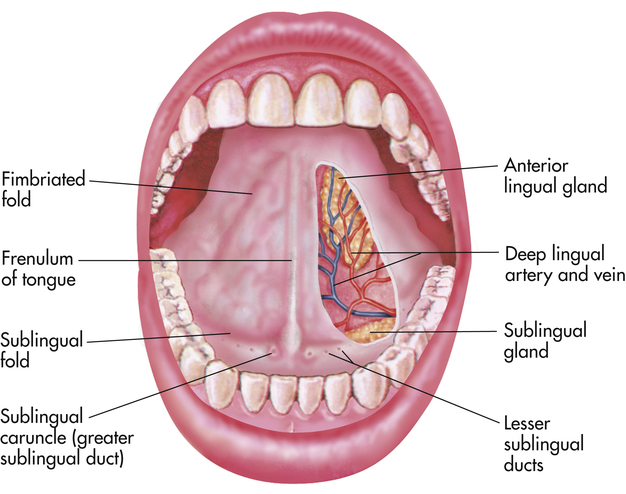
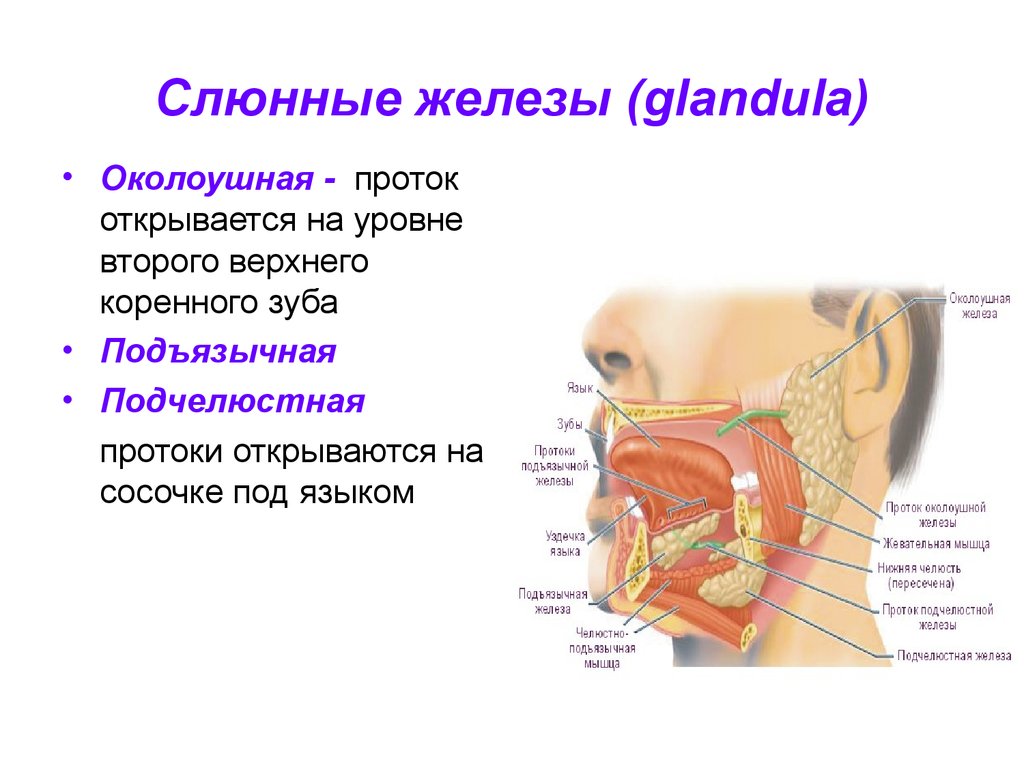
В ходе диагностики врачи способны оценить общее состояние больших слюнных желез: подъязычной, околоушной и подчелюстной.
Особенности подготовки и процесс диагностики.
УЗИ слюнных желез нужно выполнять натощак, это поможет избежать развитие рвотного рефлекса. Нежелательно пить какую-либо жидкость. Если волосы слишком длинные, то их необходимо собрать. Процесс исследования весьма простой. Пациент ложится на кушетку. Околоушная зона обрабатывается гелем с обеих сторон. Длительность манипуляции составляет около двадцати минут. После этого врач выдает результаты исследования с подробной расшифровкой.
УЗИ челюстно-лицевой зоны вызывает небывалый профессиональный интерес, так как патологии могут быть аутоиммунными, воспалительными, опухолевыми, а также дегенеративно-дистрофическими. Ультразвуковое исследование слюнных желез — наиболее точный, эффективный метод диагностики патологий этой области, включая опухоли, врожденные заболевания, сиалоадениты, травмы.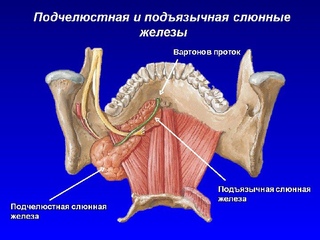 Способ диагностики может похвастаться отменной информативностью и безопасностью. Полноценное функционирование слюнной железы играет невероятно важное значение абсолютно для всего человеческого организма. Именно они отвечают за производство слюны, оказывают немаловажное воздействие на органы внутренней секреции, участвуют в процессе пищеварения.
Способ диагностики может похвастаться отменной информативностью и безопасностью. Полноценное функционирование слюнной железы играет невероятно важное значение абсолютно для всего человеческого организма. Именно они отвечают за производство слюны, оказывают немаловажное воздействие на органы внутренней секреции, участвуют в процессе пищеварения.
Специалисты по данному направлению
Бойко Галина Александровна
Врач ультразвуковой диагностики
Данченко Ольга АнатольевнаВрач ультразвуковой диагностики, рентгенолог
Иваницкая Ирина Викторовна
Руководитель службы ультразвуковой диагностики, врач ультразвуковой диагностики
Клешнина Татьяна Валерьевна
Врач ультразвуковой диагностики, рентгенолог
Котенко Наталья Николаевна
Врач ультразвуковой диагностики
Маус Мария Сергеевна
Врач ультразвуковой диагностики
Тузова Ольга Юрьевна
Врач ультразвуковой диагностики
Фадеева Татьяна Александровна
Врач ультразвуковой диагностики
Шалыгина Наталья Валерьевна
Врач ультразвуковой диагностики
Стоимость услуг
| Наименование | Цена | |
|---|---|---|
| УЗИ слюнных желез | 2300 руб | |
УЗИ слюнных желез.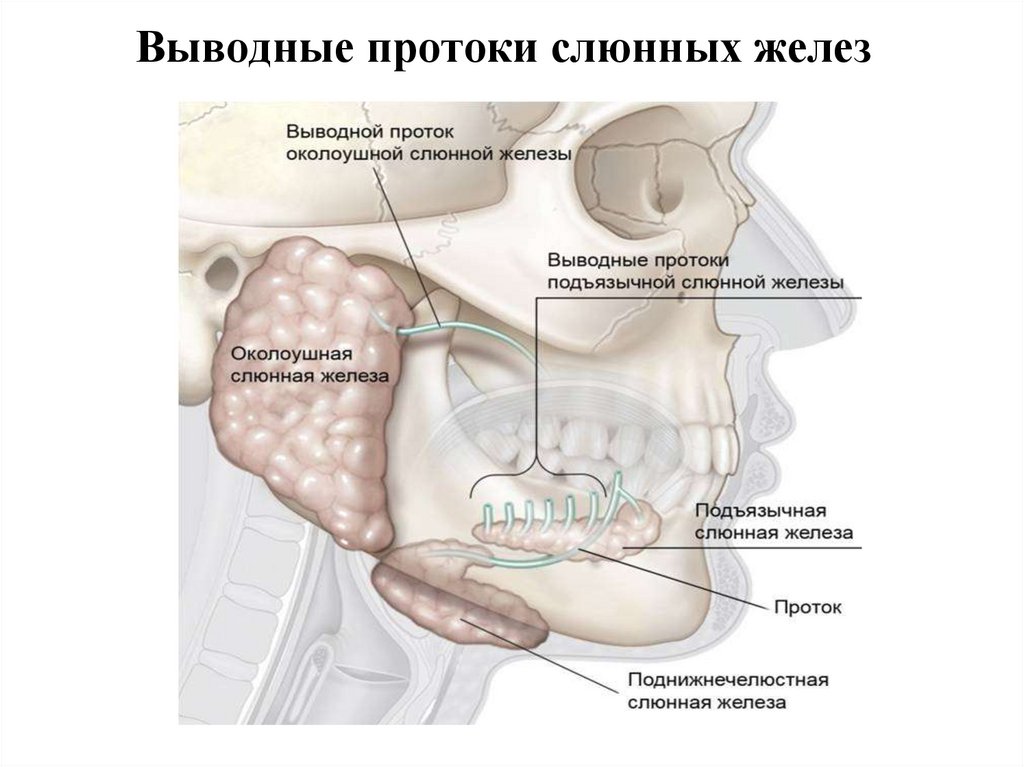 Врач категории А Врач категории А |
2420 руб |
Абсцесс слюнной железы — симптомы, причины развития, лечение, профилактика, прогноз
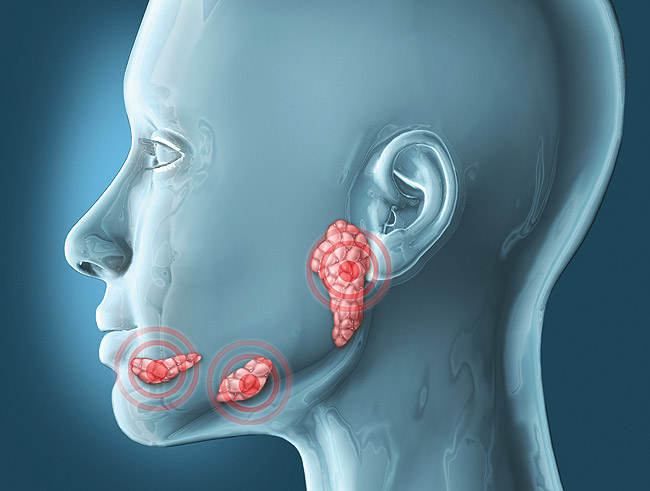
Абсцесс слюнной железы– гнойно-воспалительная патология желез, вырабатывающих слюну. Абсцесс представляет собой скопление гнойной массы, отделенное от окружающих мягких тканей пиогенной капсулой.Его наиболее частая локализация – околоушные слюнные железы, реже поражаются малые,подчелюстные и подъязычные. В патологический процесс может быть вовлечена слюнная железа как с одной,так и с обеих сторон.По мере прогрессирования болезни возможен разрыв капсулы абсцесса и выход гнойногосодержимого в окружающие мягкие ткани. Данное состояние опасно развитием тяжелых осложнений, угрожающих жизни. Поэтому при появлении первых симптомов болезни следует незамедлительно обратиться за помощью к хирургу-стоматологу.
Механизм и причины возникновения гнойного процесса
Абсцесс образуется в результате присоединения бактериальной инфекции, вызванной патогенной микрофлорой (стрептококки, стафилококки, анаэробные микроорганизмы).
Основанием для развитиягнойного воспалениямогут стать следующие заболевания и патологические состояния:
- Сиалоденит (воспаление слюнных желез) и слюннокаменная болезнь. В этом случае гнойный процесс возникает как осложнение при отсутствии своевременного лечения. В детском возрастеабсцесс слюнной железы может быть осложнением цитомегаловирусного сиалоденита.
- Закупорка выводного протока железы мелким инородным предметом (косточка, зернышко и др.).
- Снижение общей сопротивляемости организма на фоне бактериальных, вирусных инфекций, а также при тяжелых соматических заболеваниях.
- Эпидемический паротит (свинка) может спровоцировать развитие абсцесса слюнной железы. Мишенью тяжелого инфекционного заболевания являются железы внутренней и внешней секреции (слюнные, половые, поджелудочная железа).
- Истощение организма.
- Отсутствие должного ухода за слюнными железами после операции. Побочным эффектом препаратов для наркоза является снижение выработки слюны, которая препятствует проникновению патогенных микроорганизмов.
 Поэтому при неудовлетворительной гигиене полости рта в этот период возможно проникновение инфекции в слюнную железу.
Поэтому при неудовлетворительной гигиене полости рта в этот период возможно проникновение инфекции в слюнную железу.
Признаки развития абсцесса
Проявляется заболевание как общими, так и локальными изменениями в организме.
Общие симптомы: высокая температура до 40 °C, слабость и недомогание.
Местные проявления:
- Сухость слизистой ротовой полости.
- Неприятный вкус во рту.
- Болезненность при глотании, жевании и повороте головы.
- Чувство распирания и стреляющая боль в пораженной слюнной железе, отдающая в ухо, челюсть и шею.
- Отечность мягких тканей лица и шеи.
- При пальпации в области воспаленной железы обнаруживается болезненное уплотнение.
Гнойный процесс быстро прогрессирует и за 1-2 дня может привести к полному отмиранию слюнной железы. В половине случаев патологический процесс переходит на парную слюнную железу. При избыточном скоплении гноя происходит самопроизвольный разрыв абсцесса. Гной может истекать в ротовую полость с образованием свищевого хода или в окружающие мягкие ткани.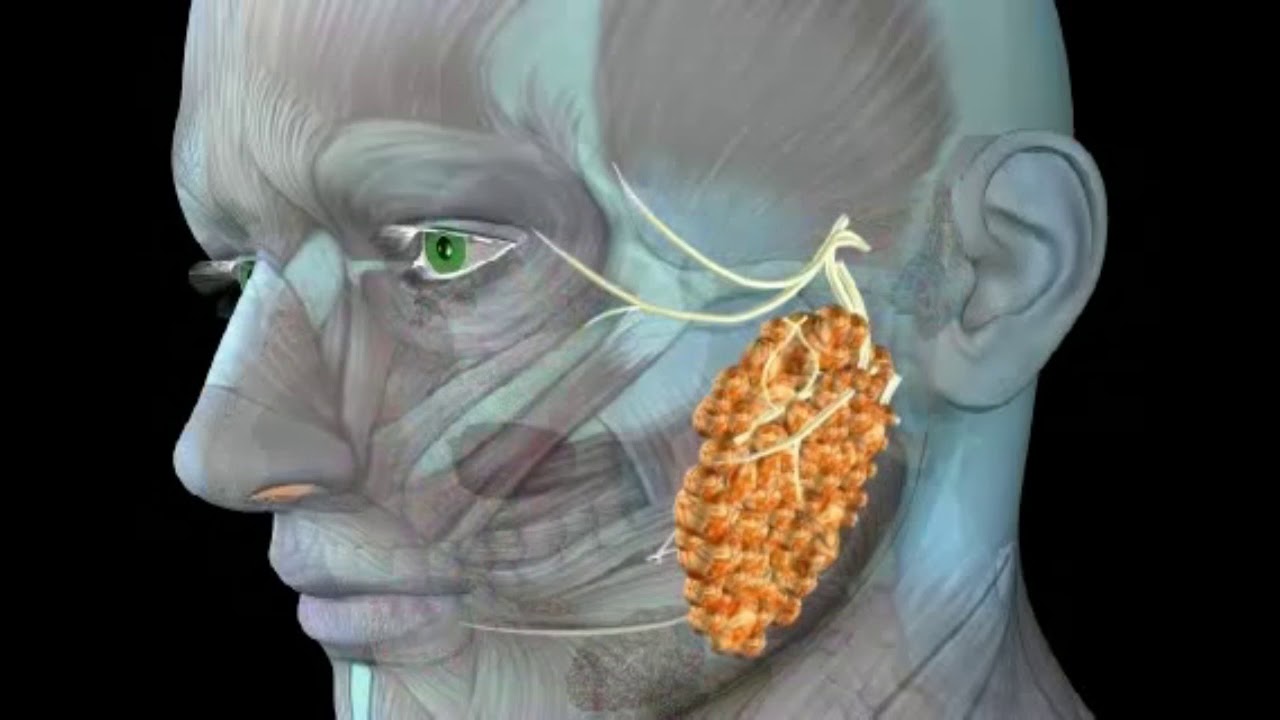
Диагностика
Стоматолог устанавливает диагноз на основании результатов опороса пациента и проведения дополнительных исследований.
Диагностика включает следующие этапы:
- Инструментальные обследования: сиалограмма и ультразвуковое исследование. Необходимы для уточнения локализации, стадии и степени поражения слюнной железы.
- Бактериологический анализвыделений из железы. Позволяет выявить возбудителя заболевания.
- Цитологическое исследование. Данный анализ проводят с целью исключения злокачественного новообразования.
Следует дифференцировать заболеваниеот других патологий слюнной железы:
- Сиалоденита.
- Калькулёзногосиалоденита.
- Лимфаденита.
- Опухолей и кист.
Методы лечения
Единственный эффективный метод лечения – хирургическая операция. Вмешательство проводится в условиях стационара под обезболиванием.
Хирург выполняет вскрытие абсцесса и удаляет гнойное содержимое. Затем производится визуальная оценка состояния слюнной железы и её выводных протоков. Если имеются участки, подвергшиеся некрозу, то производят частичное удаление ткани железы. В случае некроза выводного протока слюнной железы производят её полное удаление. Завершается операция установкой дренажа и наложением швов. Дренаж создает условия для выхода слюнных камней и оттока воспалительного экссудата. Для профилактики распространения инфекции на окружающие мягкие ткани в рану вводятся антибактериальные препараты.
Послеоперационный период включает комплексные лечебные мероприятия, направленные на восстановление организма. В период реабилитации необходимо придерживаться сбалансированной диеты, назначенной врачом.Для борьбы с бактериальной инфекцией назначают антибиотики. С целью повышения общей сопротивляемости в этот период показаны иммуномодулирующие препараты и витаминно-минеральные комплексы. Также проводятся физиотерапевтические процедуры: магнито- и лазеротерапия.
Прогноз
Абсцесс слюнной железы является серьёзным заболеванием, которое требует незамедлительного обращения к врачу.Чем раньше будет проведена операция, тем ниже риск возникновения осложнений. Полное восстановление организма после вмешательства происходит уже через 14 дней.
Несвоевременное обращение к врачу грозит развитием грозных осложнений, таких как сепсис, флегмона, остеомиелит. В более тяжелых случаях возможен летальный исход.
Появление первых признаков заболевания слюнной железы является поводом для обращения к врачу. Только специалист может правильно установить диагноз и назначить соответствующее лечение.
Профилактика
Предупредить развитие абсцесса и тяжелых осложнений помогут следующие мероприятия:
- Своевременная санация полости рта.
- Укрепление иммунитета и лечение соматических заболеваний.

- Соблюдать гигиену полости рта, в особенности после хирургических вмешательств.
- При появлении первых симптомов заболевания слюнной железы обращаться к врачу.
Список литературы
- Калитеевский П. Ф. Макроскопическая дифференциальная диагностика патологических процессов.— М., 1987.
- Кулаков А.А. Хирургическая стоматология и челюстно-лицевая хирургия. Национальное руководство / под ред. А.А. Кулакова, Т.Г. Робустовой, А.И. Неробеева. — М.: ГЭОТАР-Медиа, 2010.
- Barnes L., Eveson J. W., Reichart P., Sidransky D. (Eds.): World Health Organization Classification of Tumours. Pathology and Genetics of Head and Neck Tumours.— Lyon: IARC Press, 2005.
- Ellis G. L., Auclair P. L. Tumors of the Salivary Glands.— Washington: Armed Forces Inst. Pathol., 1996.
Воспаление, психосоциальный стресс и цитокины слюны – Salimetrics
Дата выпуска: ноябрь 2011 г.
В этой капле: биологические исследования слюны, воспаление и его влияние на здоровье человека Здоровье человека было главной темой интереса в последние десятилетия. Многочисленные исследования показали, что состояние низкого уровня системного воспаления является общей чертой метаболических заболеваний, таких как ожирение, резистентность к инсулину и диабет, а также ряда других состояний, включая сердечно-сосудистые заболевания, рак и аутоиммунные заболевания. (См. обзор Hotamisligil 2006). Это распространенное воспалительное состояние включает сдвиг в балансе про- и противовоспалительных полипептидных медиаторов, известных как цитокины, что, в свою очередь, приводит к изменениям уровней других воспалительных биомаркеров, включая белки острой фазы, такие как C- реактивный белок. (Гантер и др. 1989)
В дополнение к этим изменениям в физическом здоровье исследования также показали, что системное воспаление может быть связано с изменениями в здоровье мозга. Психонейроиммунологи теперь признают, что мозг и иммунная система взаимодействуют через группу общих сигнальных молекул, которые включают цитокины, нейропептиды и нейротрансмиттеры. (См. ретроспективные обзоры: Blalock 2005, Dantzer & Kelley 2007, Dinarello 2007 и Irwin 2008.) Детали того, как периферические цитокины взаимодействуют с мозгом, еще не совсем ясны, но ряд вероятных путей был предложен и находится в стадии изучения. . Как только эти цитокиновые сигналы достигают мозга, считается, что они влияют на уровни связанных с настроением нейротрансмиттеров, таких как серотонин, норадреналин и дофамин, которые затем влияют на поведение.
(См. ретроспективные обзоры: Blalock 2005, Dantzer & Kelley 2007, Dinarello 2007 и Irwin 2008.) Детали того, как периферические цитокины взаимодействуют с мозгом, еще не совсем ясны, но ряд вероятных путей был предложен и находится в стадии изучения. . Как только эти цитокиновые сигналы достигают мозга, считается, что они влияют на уровни связанных с настроением нейротрансмиттеров, таких как серотонин, норадреналин и дофамин, которые затем влияют на поведение.
Одним из основных достижений в этой области стало осознание того, что связь между мозгом и периферическим воспалением работает двунаправленно. Исследования показали, что психосоциальный стресс может активировать системный воспалительный цитокиновый ответ, и считается, что этот ответ, в свою очередь, может привести к изменениям в работе мозга и развитию психических заболеваний, таких как большое депрессивное расстройство. (См. обзоры: Debnath, et al., 2011; Leonard, 2010; Miller, et al., 2009.; и Данцер и др. 2008)
Однако вопросы, касающиеся взаимосвязи между воспалением и мозгом, еще предстоит решить. Например, неясно, ускоряет ли само по себе системное воспаление прогрессирование психических расстройств, или же периферическая и центральная воспалительные системы действуют параллельно, увеличивая риск расстройств. (Debnath, et al. 2011) Кроме того, было отмечено, что маркеры воспаления не всегда повышены у пациентов с клинической депрессией. (Данцер и др., 2008 г.)
Например, неясно, ускоряет ли само по себе системное воспаление прогрессирование психических расстройств, или же периферическая и центральная воспалительные системы действуют параллельно, увеличивая риск расстройств. (Debnath, et al. 2011) Кроме того, было отмечено, что маркеры воспаления не всегда повышены у пациентов с клинической депрессией. (Данцер и др., 2008 г.)
В обзоре Miller et al. описывает путь, по которому стресс, действующий через симпатическую нервную систему (СНС), может привести к повышению уровня периферических цитокинов. В этой схеме катехоламины, высвобождаемые из СНС, действуют через альфа- и бета-адренорецепторы на макрофаги и другие иммунные клетки, чтобы активировать сигнальные пути, включая воспалительный транскрипционный фактор NF-κB. Затем передача сигналов NF-κB побуждает иммунные клетки высвобождать провоспалительные цитокины в ответ на стресс.
Поскольку неконтролируемое воспаление оказывает негативное влияние на здоровье, мозг распознает повышенные системные уровни цитокинов и индуцирует ось HPA для увеличения секреции кортизола, который ослабляет воспалительную реакцию путем ингибирования передачи сигналов NF-κB. Ингибирующая активность парасимпатической нервной системы (ПНС) и, возможно, механизмы обратной связи в СНС также участвуют в контроле воспалительной реакции. (Rohleder 2011; Sternberg 2006)
Ингибирующая активность парасимпатической нервной системы (ПНС) и, возможно, механизмы обратной связи в СНС также участвуют в контроле воспалительной реакции. (Rohleder 2011; Sternberg 2006)
Цитокины слюны
За последнее десятилетие число исследований, связанных с цитокинами слюны, увеличилось, и эти исследования чаще всего были сосредоточены на заболеваниях пародонта или других заболеваниях полости рта, таких как синдром Шегрена, красный плоский лишай и грибковые инфекции. При изучении реакции воспалительных цитокинов на стресс в основном использовались измерения этих маркеров in vitro или в сыворотке, но в настоящее время начинают изучаться взаимосвязи между стрессом, функцией мозга и слюнными цитокинами.
Рисунок 2. Рост числа исследований, посвященных слюнному ИЛ-6, 2000–2011 гг.
Основная проблема, препятствующая более широкому использованию слюнных цитокинов в общих психобиологических исследованиях, заключается в том, что исследования, как правило, обнаруживают, что уровни этих маркеров в слюне лишь незначительно коррелируют с их значениями в сыворотке. (Minetto, et al., 2005; Sjögren, et al., 2006; Fernandez-Botran, et al., 2011). Очевидное отсутствие корреляции неудивительно из-за множества путей попадания этих биомаркеров в слюну. В дополнение к местному продуцированию в слюнных железах, цитокины продуцируются в различных тканях слизистой оболочки и иммунных клетках во рту, и они также могут проникать через микротравмы или транссудацию из крови. (Schapher, et al., 2011; Dongari-Bagtzoglou, et al., 2005) Проницаемость мембран в тканях полости рта изменяется в ответ на инфекцию и воспаление, уровни гормонов и, как предполагается в одном из исследований, представленных в этом выпуске, возможно, даже посредством вегетативного нервного контроля; поэтому вероятны как долгосрочные, так и краткосрочные изменения вклада крови.
(Minetto, et al., 2005; Sjögren, et al., 2006; Fernandez-Botran, et al., 2011). Очевидное отсутствие корреляции неудивительно из-за множества путей попадания этих биомаркеров в слюну. В дополнение к местному продуцированию в слюнных железах, цитокины продуцируются в различных тканях слизистой оболочки и иммунных клетках во рту, и они также могут проникать через микротравмы или транссудацию из крови. (Schapher, et al., 2011; Dongari-Bagtzoglou, et al., 2005) Проницаемость мембран в тканях полости рта изменяется в ответ на инфекцию и воспаление, уровни гормонов и, как предполагается в одном из исследований, представленных в этом выпуске, возможно, даже посредством вегетативного нервного контроля; поэтому вероятны как долгосрочные, так и краткосрочные изменения вклада крови.
Поскольку слюнные железы и другие ткани во рту также подвержены влиянию того же оттока вегетативных нервных сигналов, которые управляют системным повышением уровня цитокинов, кажется вероятным, что слюнные цитокины найдут применение в психобиологических исследованиях.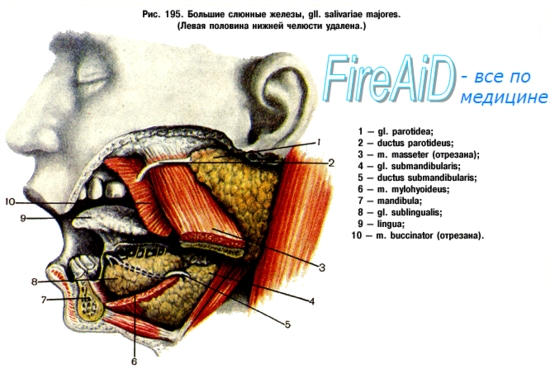 Следующее поколение исследований должно будет тщательно изучить эти маркеры, чтобы понять характер их связи со стрессом и различными болезненными состояниями.
Следующее поколение исследований должно будет тщательно изучить эти маркеры, чтобы понять характер их связи со стрессом и различными болезненными состояниями.
Чтобы проиллюстрировать потенциальную ценность слюнных цитокинов для биомедицинских исследований, в этом выпуске The Spit Report мы представляем несколько исследовательских работ, в которых изучалась взаимосвязь между психосоциальным стрессом, слюнными цитокинами и функцией мозга, связанной с психическим здоровьем. Кроме того, в последние годы появилось небольшое количество поисковых исследований, в которых сообщается о взаимосвязи между слюнными цитокинами и заболеваниями в тканях, удаленных от полости рта; их примеры приведены ниже в разделе «Дополнительная литература».
Ссылки >
Технический совет
Сбор и обработка образцов слюны для анализа цитокинов образцы слюны по-прежнему ограничены для этих аналитов.
*Salimetrics предоставляет эту информацию только для исследовательских целей (RUO). Информация не предоставляется для пропаганды использования медицинских устройств не по прямому назначению. Ознакомьтесь с полным текстом статьи.
Информация не предоставляется для пропаганды использования медицинских устройств не по прямому назначению. Ознакомьтесь с полным текстом статьи.
Избранные статьи
Связь между иммунитетом слизистых оболочек и психическим здоровьем детей: роль детского пола.
Келлер П.С., Эль-Шейх М., Во Б. и Грейнджер Д.А. (2010). Brain Physiol Behav, 101 (5), 705-12.
Секреторный IgA (SIgA) и интерлейкин-6 (IL-6) были измерены в образцах слюны, взятых у детей, с целью изучения взаимосвязи между иммунными параметрами слюны и психическим здоровьем детей. Было обнаружено, что более высокие уровни SIgA связаны с большей импульсивностью, делинквентностью и эмоциональным дистрессом у девочек. Было обнаружено, что более высокие уровни IL-6 в слюне связаны с самооценкой депрессии и тревоги, а также с импульсивностью и социальной замкнутостью, по сообщениям родителей, эмоциональным дистрессом и правонарушениями у девочек. Более высокий уровень SIgA был незначительно связан с более низкой импульсивностью и эмоциональным дистрессом у мальчиков. Результаты для IL-6 в слюне и психического здоровья соответствовали результатам исследований с участием IL-6 в сыворотке, в то время как результаты для SIgA показали результаты, отличные от результатов нескольких исследований с участием взрослых.
Результаты для IL-6 в слюне и психического здоровья соответствовали результатам исследований с участием IL-6 в сыворотке, в то время как результаты для SIgA показали результаты, отличные от результатов нескольких исследований с участием взрослых.
Область исследований: стресс, поведение и развитие; Здоровье и воспаление
Фокус: Поведенческие расстройства; Социальное поведение и эмоции; Воспаление и иммунная функция
Когда горе накаляется: провоспалительные цитокины предсказывают региональную активацию мозга.
О’Коннор М.-Ф., Ирвин М.Р. и Веллиш Д.К. (2009). Нейроимидж, 47 (3), 891-96.
Уровни в слюне двух провоспалительных цитокинов, интерлейкина-1β (IL-1β) и растворимого рецептора фактора некроза опухоли II (sTNFrII), измеряли у переживающих тяжелую утрату женщин, прошедших фМРТ-сканирование во время задачи по выявлению горя. Анализ показал, что уровни обоих маркеров в слюне были положительно связаны с региональной активацией мозга и обработкой эмоций. Результаты подтверждают идею о том, что периферическое воспаление (во рту) передается в мозг и что возникающие в результате изменения мотивационного состояния могут влиять на обработку эмоций.
Результаты подтверждают идею о том, что периферическое воспаление (во рту) передается в мозг и что возникающие в результате изменения мотивационного состояния могут влиять на обработку эмоций.
Область исследований: стресс, поведение и развитие; Здоровье и воспаление
Фокус: Социальное поведение и эмоции; Воспаление и иммунная функция
Влияние отвращения на оральную иммунную функцию.
Стивенсон Р.Дж., Ходжсон Д., Оатен М.Ф., Баруэи Дж. и Кейс Т.И. (2011). Психофизиология, 48 (7), 900-907.
Экспериментальная группа участников просматривала изображения, которые должны были вызвать отвращение, по сравнению с контрольными группами негативной и нейтральной индукции. Слюну собирали в трех временных точках для мониторинга изменений уровней секреторного IgA (SIgA) и фактора некроза опухоли-альфа (TNF-α) в качестве индикаторов иммунной функции и воспаления полости рта соответственно. У участников группы отвращения наблюдалось снижение SIgA и увеличение TNF-α по сравнению с группами отрицательного и нейтрального контроля. Повышение TNF-α сопровождалось повышением содержания альбумина в слюне, что свидетельствует о повышенной проницаемости мембран для компонентов сыворотки. Авторы предполагают, что увеличение TNF-α и сопровождающее его повышение уровня альбумина являются ответом на усиление активности вегетативной нервной системы, связанное с состоянием отвращения.
Повышение TNF-α сопровождалось повышением содержания альбумина в слюне, что свидетельствует о повышенной проницаемости мембран для компонентов сыворотки. Авторы предполагают, что увеличение TNF-α и сопровождающее его повышение уровня альбумина являются ответом на усиление активности вегетативной нервной системы, связанное с состоянием отвращения.
Области исследований: стресс, поведение и развитие; Здоровье и воспаление
Фокус: вегетативная нервная система; Воспаление и иммунная функция
Уровни интерлейкина-6 в связи с психосоциальными факторами: исследования сыворотки, слюны и продукции мононуклеаров крови in vitro.
Шегрен, Э., Леандерсон, П., Кристенсон, М., и Эрнеруд, Дж. (2006). Brain Behav Immun, 20 (3), 270-78.
Уровни ИЛ-6 анализировали в сыворотке, слюне и в супернатантах клеточных культур, стимулированных in vitro липополисахаридом. Было обнаружено, что уровни ИЛ-6 в сыворотке и слюне отрицательно связаны с психосоциальными ресурсами и положительно связаны с психосоциальными факторами риска, с противоположными результатами для супернатантов, стимулированных ЛПС. Корреляции между уровнями ИЛ-6 в сыворотке крови и слюне обнаружено не было. Результаты подтверждают мнение о том, что IL-6 участвует в опосредовании риска развития заболевания, связанного с психосоциальными факторами.
Корреляции между уровнями ИЛ-6 в сыворотке крови и слюне обнаружено не было. Результаты подтверждают мнение о том, что IL-6 участвует в опосредовании риска развития заболевания, связанного с психосоциальными факторами.
Области исследований: стресс, поведение и развитие; Здоровье и воспаление
Фокус: Социальное поведение и эмоции; Воспаление и иммунная функция
ССЫЛКИ И ДОПОЛНИТЕЛЬНЫЕ ИССЛЕДОВАНИЯ
- Аурер А., Аурер-Кожель Дж., Ставленич-Рукавина А., М., Иумвич, С. Каленич, Хабан, В. (1999). Медиаторы воспаления в слюне больных быстропрогрессирующим пародонтитом во время военного стресса увеличивают заболеваемость. Сб Антропол, 23 (1), 117-24.
- Бумба, Д., Скопули, Ф.Н., и Мутсопулос, Х.М. (1995). Экспрессия мРНК цитокинов в тканях губных слюнных желез у пациентов с первичным синдромом Шегрена. Br J Rheumatol, 34 (4), 326–33.
- Бреннан, М.Т., и Фокс, П.К. (2000). Экспрессия мРНК цитокинов в губных слюнных железах здоровых добровольцев.
 Oral Dis, 6
Oral Dis, 6 - Катов, Дж. М., Боднар, Л. М., Несс, Р. Б., Бэррон, С. Дж., и Робертс, Дж. М. (2007). Воспаление и дислипидемия связаны с риском спонтанных преждевременных родов. Am J Epidemiol, 166 (11), 1312-19.
- Чиаппелли, Ф., Ирибаррен, Ф.Дж., и Проло, П. (2006). Слюнные биомаркеры в психобиологической медицине.
- Биоинформация, 1 (8), 331‐34.
- Хрусос, Г.П. (2009). Стресс и нарушения стрессовой системы. Nat Rev Endocrinol, 5 (7), 374-81.
- Кокс, А.Дж., Пайн, Д.Б., Глесон, М., и Каллистер, Р. (2008). Концентрации ИЛ-6 в плазме покоя и слюне у бегунов на длинные дистанции не коррелируют. Eur J Appl Physiol, 103 (4), 477-79.
- Дикерсон, С.С., Кемени, М.Э., Азиз, Н., Ким, К.Х., и Фэйи, Дж.Л. (2004). Иммунологические эффекты индуцированного стыда и вины. Psychosom Med, 66 (1), 124-31.
- Dugué, B., Ilardo, C., Aimone-Gastine, I., Guéant, J.
 L., Mouzé-Amady, M., Cnockaert, J.C., Mur, J.M., et al. (1996). Цитокины в слюне: базальные концентрации и влияние высокой температуры окружающей среды (сауна). Stress Med, 12 (3), 193-97.
L., Mouzé-Amady, M., Cnockaert, J.C., Mur, J.M., et al. (1996). Цитокины в слюне: базальные концентрации и влияние высокой температуры окружающей среды (сауна). Stress Med, 12 (3), 193-97. - Эль-Шейх, М., Бакхальт, Дж. А., Грейнджер, Д. А., Эрат, С. А., и Ацебо, К. (2007). Связь между нарушением сна у детей и слюнным ИЛ-6. J Sleep Res, 16 (2), 188-97.
- Фернандес-Санчес, А., Мадригал-Сантильян, Э., Баутиста, М., Эскивель-Сото, Х., Морлаес-Гонсалес, А., Эскивель-Чирино, К., Дюранте-Монтьель, И., Санчес- Ривера Г., Валадес-Вега К. и Моралес-Гонсалес Дж.А. (2011). Воспаление, окислительный стресс и ожирение. Междунар. J Mol Sci, 12 (5), 3117-32.
- Фокс, П.С., Бреннан, М., и Ди Сан, П. (1999). Экспрессия цитокинов в эпителиальных клетках малой губной слюнной железы человека в норме и при патологии. Arch Oral Biol, 44 (Приложение 1), S49-S52.
- Фокс Р.И., Канг Х.И., Андо Д., Абрамс Дж. и Пиза Э. (1994).
 Экспрессия мРНК цитокинов в биоптатах слюнных желез при синдроме Шегрена. J Immunol, 152 (11), 5532-39.
Экспрессия мРНК цитокинов в биоптатах слюнных желез при синдроме Шегрена. J Immunol, 152 (11), 5532-39. - Джаннобиле, В. В., Бейклер, Т., Кинни, Дж. С., Рамсейер, К. А., Морелли, Т., и Вонг, Д. Т. (2009 г.). Слюна как диагностический инструмент пародонтита: текущее состояние и направления на будущее. Пародонтология 2000, 50, 52-64.
- Гилл, Дж., Витилингам, М., и Пейдж, Г.Г. (2008). Низкий уровень кортизола, высокий уровень ДГЭА и высокий уровень стимулированного ФНОα и ИЛ-6 у женщин с посттравматическим стрессовым расстройством. J Trauma Stress, 21 (6), 530-39.
- Голд, С. М., и Ирвин, М. Р. (2009). Депрессия и иммунитет: воспаление и симптомы депрессии при рассеянном склерозе. Immunol Allergy Clin North Am, 29 (2), 309-20.
- Groer, M., Murphy, R., Bunnell, W., Salomon, K., Van, Eepoel, J., Rankin, B., et al. (2010). Слюнные показатели стресса и иммунитета у полицейских, вовлеченных в смоделированные сценарии критических происшествий.
 J Occup Environ Med, 52 (6), 595-602.
J Occup Environ Med, 52 (6), 595-602. - Холмс К., Каннингем К., Зотова Э., Вулфорд Дж., Дин К., Керр С., Каллифорд Д. и Перри В. Х. (2009). Системное воспаление и прогрессирование болезни при болезни Альцгеймера. Неврология, 73 (10), 768-74.
- Лизманн, К., Клапп, Б., и Петерс, Э.М.Дж. (2011). Стресс, атопия и аллергия: переоценка с психонейроиммунологической точки зрения. Дерматоэндокринол, 3 (1), 37-40.
- Ламас Мойя, С., Бойл, Л., Линч, П.Б., и Аркинс, С. (2006). Реакция провоспалительных цитокинов и белков острой фазы на введение низких доз липополисахарида (ЛПС) у свиней. Animal Sci, 82, 527-34.
- Люменг, К.Н. и Салтиэль, А.Р. (2011). Воспалительные связи между ожирением и нарушением обмена веществ. J Clin Invest, 121 (6), 2111-17.
- Мастролонардо, М., Аличино, Д., Зефферино, Р., Пасквини, П., и Пикарди, А. (2007). Влияние психологического стресса на слюнный интерлейкин-1β при псориазе.
 Arch Med Res, 38 (2), 206-11.
Arch Med Res, 38 (2), 206-11. - Миллер, К.С., Фоли, Дж.Д., Бейли, А.Л., Кампелл, К.Л., Хамфрис, Р.Л., Христодулидес, Н., Флориано, П.Н., и соавт. (2010). Современные разработки в диагностике слюны. Biomark Med, 4 (1), 171-89.
- Минетто, М.А., Гаццони, М., Ланфранко, Ф., Бальди, М., Саба, Л., Педрола, Р., Коми, П.В., и др. (2007). Влияние метода сбора образцов на уровень интерлейкина-6 в слюне в состоянии покоя и после тренировки. Eur J Appl Physiol, 101 (2), 249-56.
- Moons, W.G., Eisenberger, N.I., & Taylor, S.E. (2009). Реакции гнева и страха на стресс имеют разные биологические профили. Brain Behav Immun, 24 (2), 215-19.
- Мутсопулос, Н.М. и Мадианос, П.Н. (2006). Вялотекущее воспаление при хронических инфекционных заболеваниях: Парадигма пародонтальных инфекций. Ann NY Acad Sci, 1088, 251-64.
- Нильсен, А.А., Нильсен, Дж.Н., Шмедес, А., Брандслунд, И., и Хей, Х. (2005). Интерлейкин-6 слюны у пациентов с воспалительными заболеваниями кишечника.
 Scand J Gastroenterol, 40 (12), 1444-48.
Scand J Gastroenterol, 40 (12), 1444-48. - Нишанян, П., Азиз, Н., Чанг, Дж., Детелс, Р., и Фэйи, Дж. Л. (1998). Пероральные жидкости как альтернатива сыворотке для измерения маркеров иммунной активации. Clin Diag Lab Immunol, 5 (4), 507-12.
- О’Коннор, М.-Ф., Бауэр, Дж.Э., Чо, Х.Дж., Кресуэлл, Дж.Д., Димитров, С., Хэмби, М.Е., Хойт, М.А., и соавт. (2009). Оценить, контролировать, исключить: влияние биоповеденческих факторов на циркулирующие воспалительные маркеры. Brain Behav Immun, 23 (7), 887-97.
- Пальмквист П., Лундберг П., Лундгрен И., Ханстрем и Лернер У.Х. (2008). IL-1β и TNF-α регулируют цитокины типа IL-6 в фибробластах десны. J Dent Res, 87 (6), 558‐63.
- Пекинер, Ф.Н., Бумру, Б., Демирель, Г.Ю., и Озбайрак, С. (2009). Синдром жжения во рту и слюна: Обнаружение микроэлементов и цитокинов в слюне. J Oral Pathol Med, 38 (3), 269-75.
- Перуццо, округ Колумбия, Бенатти, Б.
 Б., Амброзано, Г.М., Ногейра-Фильо, Г.Р., Саллум, Э.А., Касати, М.З., и Ночити, Ф.Х., младший (2008). Систематический обзор стресса и психологических факторов как возможных факторов риска заболеваний пародонта. J Пародонтология, 78 (8), 1491-504.
Б., Амброзано, Г.М., Ногейра-Фильо, Г.Р., Саллум, Э.А., Касати, М.З., и Ночити, Ф.Х., младший (2008). Систематический обзор стресса и психологических факторов как возможных факторов риска заболеваний пародонта. J Пародонтология, 78 (8), 1491-504. - Пайк, Дж.Л., Смит, Т.Л., Хаугер, Р.Л., Никассио, П.М., Паттерсон, Т.Л., МакКлинтик, Дж., Костлоу, К., и Ирвин,
- MR (1997). Хронический жизненный стресс изменяет симпатическую, нейроэндокринную и иммунную реакции человека на острый психологический стресс. Psychosom Med, 59 (4), 447-57.
- Прелиаско, В.Ф., Бенчуя, К., Паван, В., де ла Каль, К., Ганзинелли, С., и Стерин-Борда, Л. (2008). Уровни IL-1β и PGE2 повышены в слюне детей с лангергансоклеточным гистиоцитозом. J Oral Pathol Med, 37 (9), 522-27.
- Родус, Н.Л., Ченг, Б., Майерс, С., Боулз, В., Хо, В., и Ондри, Ф. (2005). Сравнение провоспалительных, NF-κB-зависимых цитокинов: TNF-альфа, IL-1-альфа, IL-6 и IL-8 в различных ротовых жидкостях пациентов с красным плоским лишаем полости рта.
 Clin Immunol, 114 (3), 278-83.
Clin Immunol, 114 (3), 278-83. - Рул С., Хамбергер С., Бетц Р., Суккар Т., Шмальц Г., Сеймур Р. А., Хиллер К.-А. и Томасон Дж. М. (2005). Белки слюны и цитокины при медикаментозном разрастании десен. J Dent Res, 83 (4), 322-26.
- Сато, Дж., Гото, Дж., Мурата, Т., Китамори, С., Ямадзаки, Ю. Сато, А., и Китагава, Ю. (2010). Изменения уровня интерлейкина-6 в слюне у пациентов с плоскоклеточным раком полости рта. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 110 (3), 330-6.
- Скопец, Р. (2011). Механизм связи агрессивного стресса через воспаление с раком. J Cancer Sci Ther, 3 (5), 134-39.
- Соуза П.П., Пальмквист П., Лундгрен И., Ли А., Коста-Нето С.М., Лундберг П. и Лернер У.Х. (2010). Стимуляция цитокинов ИЛ-6 в фибробластах толл-подобными рецепторами 2, J Dent Res, 89 (8), 802-7.
- Танда, Н., Ояма, Х., Ямакава, М., Эрикссон, М., Цудзи, Т., Макбрайд, Дж., Элович, А., Вонг, Д.Т., и Логин, Г.
 Р. (1998). IL-1β и IL-6 в ацинарных клетках околоушной железы мыши: характеристика синтеза, хранения и высвобождения. Am J Physiol, 274 (1 часть 1), G147-G156.
Р. (1998). IL-1β и IL-6 в ацинарных клетках околоушной железы мыши: характеристика синтеза, хранения и высвобождения. Am J Physiol, 274 (1 часть 1), G147-G156. - Тобон-Аррояве, С.И., Харамильо-Гонсалес, ЧП, Исаза-Гусман, Д.М. (2008). Корреляция между уровнями IL-1β в слюне и клиническим статусом пародонта. Арка Орал Биол, 53 (4), 346-52.
- Вейк, У., Херфорт, А., Кольб-Бахофен, В., и Дейнцер, Р. (2008). Острый стресс индуцирует провоспалительную передачу сигналов в местах хронического воспаления. Психосоматика Мед, 70 (8), 906-912.
- Wellen, KE, & Hotamisligil, GS (2005). Воспаление, стресс и диабет. J Clin Invest, 115 (5), 1111‐
- 1119.
- Яо, К., Ли, X., Мурдиастути, К., Косуги-Танака, К., Акамацу, Т., Канамори, Н., и Хосой, К., (2005). Липополисахарид-индуцированное повышение и секреция интерлейкина-1β в поднижнечелюстной железе самцов мышей. Иммунология, 116 (2), 213-22.
- Youinou, P., Taher, T.E., Pers, J.O., Mageed, R.A., & Renaudineau, Y. (2009). Цитокины В-лимфоцитов и ревматическое аутоиммунное заболевание. Артрит Реум, 60 (7), 1873-80.
- Зунт, Л.Л., Бертон, Л.В., Голдлатт, Л.И., Доббинс, Э.Э., и Шринивасан, М. (2009). Растворимые формы Toll-подобного рецептора 4 присутствуют в слюне человека и модулируют секрецию фактора некроза опухоли-α макрофагоподобными клетками. Clin Exp Immunol, 156 (2), 285-93.
Параллели с воспалением десен Новый «Цитокиновый показатель»
Исследователи Стоматологического колледжа Нью-Йоркского университета разработали единый показатель для описания уровня цитокинов в слюне, и этот показатель связан с тяжестью клинического воспаления десен, согласно опубликованному исследованию. в журнале PLOS ONE .
Хотя необходимы дополнительные исследования для проверки «цитокинового показателя», он может быть многообещающим для измерения того, насколько хорошо пациент реагирует на лечение заболеваний десен, прогнозирования рецидивов заболеваний десен или выявления продолжающегося воспаления, связанного с системными заболеваниями.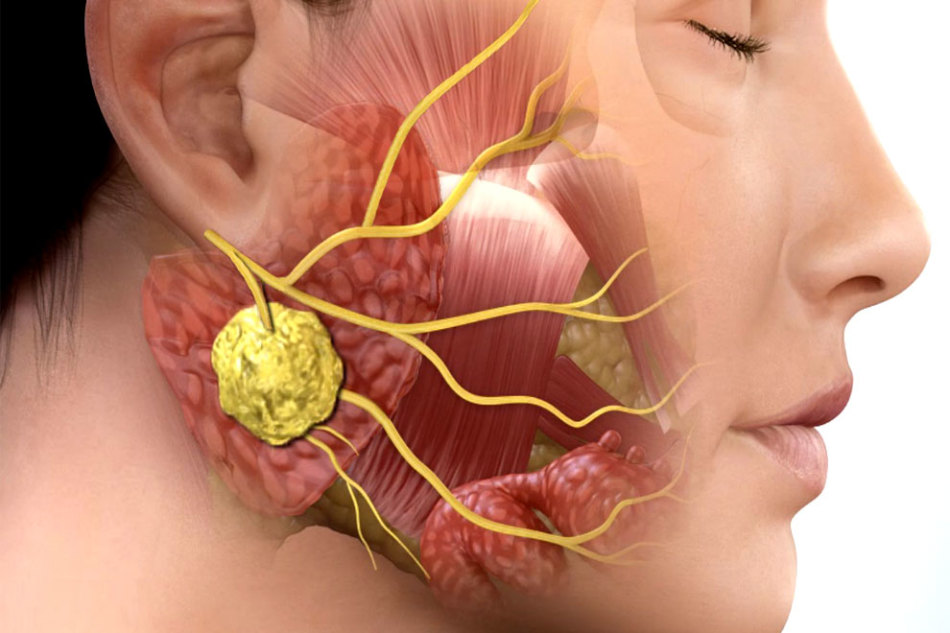
«Воспаление пародонта не только видно при осмотре, но и отражается в слюне пациента», — сказала Анджела Камер, доктор медицинских наук, доктор медицинских наук, доцент кафедры пародонтологии и имплантологии Эшмана в стоматологии Нью-Йоркского университета и старший автор исследования. .
Заболевание пародонта (или десен) — это хроническое воспалительное заболевание, которым страдает примерно половина взрослых. Заболевание пародонта, отмеченное воспаленными деснами, которые могут кровоточить и отслаиваться от зуба, возникает в результате сложного взаимодействия между дисбалансом здоровых и нездоровых бактерий под десной и реакцией иммунной системы. Этот ответ вызывает высокие уровни цитокинов — небольших белков, которые сигнализируют иммунной системе — в воспаленных деснах, особенно провоспалительных цитокинов, таких как IL-8, IL-1β, IL-6 и TNFα.
Пародонтоз также связан с системными заболеваниями, включая сердечно-сосудистые заболевания, диабет и болезнь Альцгеймера. Ученые считают, что воспаление десен способствует возникновению этих состояний как косвенным путем (цитокины усиливают системное воспаление), так и прямым путем (цитокины попадают в определенный орган, например, сердце или мозг), но изучение этого затруднено из-за сложности измерения цитокинов в организме. жидкость, обнаруженная глубоко в карманах в деснах.
Ученые считают, что воспаление десен способствует возникновению этих состояний как косвенным путем (цитокины усиливают системное воспаление), так и прямым путем (цитокины попадают в определенный орган, например, сердце или мозг), но изучение этого затруднено из-за сложности измерения цитокинов в организме. жидкость, обнаруженная глубоко в карманах в деснах.
К счастью, цитокины также обнаруживаются в слюне, которую легче собрать. В исследовании PLOS ONE исследователи хотели узнать, может ли клинически выявленное воспаление десен предсказать уровень цитокинов, обнаруженных в слюне.
«Цитокины слюны — это окно в молекулярный состав среды полости рта», — сказала Вера Танг, доктор медицинских наук, магистр медицины, клинический доцент кафедры пародонтологии и имплантологии Эшмана в стоматологии Нью-Йоркского университета и первый автор исследования.
Исследователи изучили десны и слюну 67 взрослых в возрасте 45 лет и старше, у которых была определенная степень заболевания пародонта, но в остальном они были здоровы.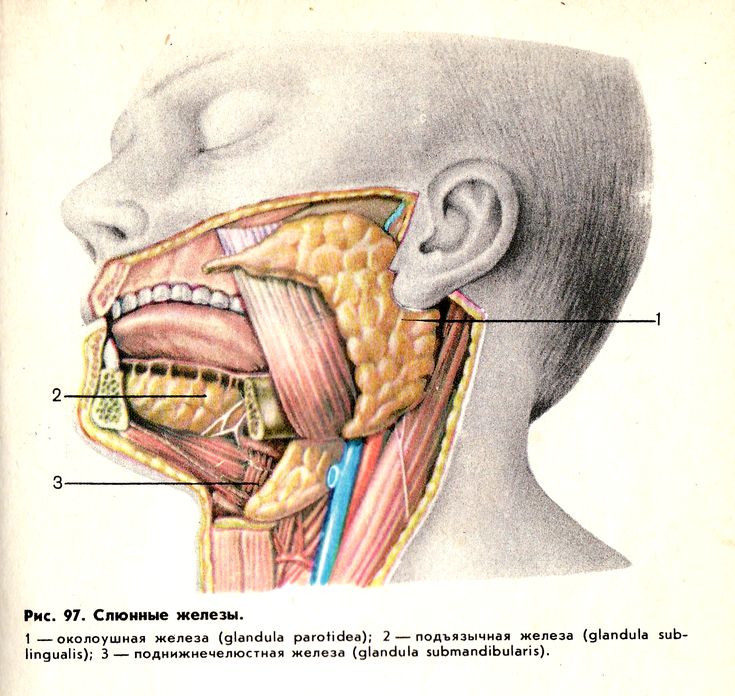 Чтобы измерить клиническое воспаление пародонта, исследователи использовали формулу, называемую площадью воспаленной поверхности пародонта (PISA), которая рассчитывается с использованием измерений глубины карманов в деснах и кровоточивости при зондировании. PISA обеспечивает единую меру воспаления пародонта; более высокий балл PISA указывает на усиление воспаления.
Чтобы измерить клиническое воспаление пародонта, исследователи использовали формулу, называемую площадью воспаленной поверхности пародонта (PISA), которая рассчитывается с использованием измерений глубины карманов в деснах и кровоточивости при зондировании. PISA обеспечивает единую меру воспаления пародонта; более высокий балл PISA указывает на усиление воспаления.
Участников также просили плевать в стерильные пробирки для сбора образцов слюны, которые затем анализировали для измерения ряда как про-, так и противовоспалительных цитокинов: IL-1β, IL-6, IL-8, IL-13, TNF-α и IL-10. Под руководством статистика Малвина Джанала, доктора философии, исследователи использовали два разных способа (индекс цитокинового компонента и составной воспалительный индекс), чтобы объединить эти цитокины в единую оценку.
Они обнаружили, что баллы PISA были значительно связаны с новыми баллами цитокинов, независимо от других факторов, включая возраст, пол, курение и индекс массы тела (ИМТ). Чем выше цитокиновый балл, тем сильнее воспаление пародонта.
Чем выше цитокиновый балл, тем сильнее воспаление пародонта.
«Это демонстрирует, что одна оценка, охватывающая несколько цитокинов слюны, коррелирует с тяжестью воспаления пародонта», — сказала Лина Паломо, доктор медицинских наук, профессор и заведующая кафедрой пародонтологии и имплантологии Эшмана в стоматологии Нью-Йоркского университета и соавтор исследования. .
Исследователи предупреждают, что необходимы дополнительные исследования для подтверждения оценки цитокинов у пациентов с различными состояниями здоровья, а также у пациентов со всеми уровнями заболеваний пародонта, включая здоровые десны и заболевание десен на ранней стадии. Однако, если оценка цитокинов будет проверена на более крупных и разнообразных популяциях пациентов, ее можно будет использовать для лучшего понимания прогрессирования и рецидивов заболеваний пародонта, а также потенциальной связи с другими системными состояниями.
«Мы знаем, что при лечении заболеваний десен, таком как удаление зубного камня и строгание, оценка PISA снижается. Было бы интересно посмотреть, упадет ли также показатель цитокинов — или, если он сохранится, посмотреть, что это значит», — добавил Камер. «Выявляет ли это первопричину, например, продолжающееся воспаление от системного заболевания? Или, если у кого-то есть гипервоспалительная реакция, о которой мы узнали бы по высокому показателю цитокинов, можно ли предсказать, будет ли пародонтит рецидивировать или прогрессировать в будущем? Мы надеемся изучить эти вопросы в будущих исследованиях».
Было бы интересно посмотреть, упадет ли также показатель цитокинов — или, если он сохранится, посмотреть, что это значит», — добавил Камер. «Выявляет ли это первопричину, например, продолжающееся воспаление от системного заболевания? Или, если у кого-то есть гипервоспалительная реакция, о которой мы узнали бы по высокому показателю цитокинов, можно ли предсказать, будет ли пародонтит рецидивировать или прогрессировать в будущем? Мы надеемся изучить эти вопросы в будущих исследованиях».
Дополнительные авторы исследования включают Бабака Хамиди, DDS, MPH, Шерил Барбер, MS, MPH, и Бенджамина Годдера, DMD, NYU Dentistry. Это исследование финансировалось Национальным институтом здравоохранения (R03-DE023139).
О Стоматологическом колледже Нью-Йоркского университета
Стоматологический колледж Нью-Йоркского университета (NYU Dentistry), основанный в 1865 году, является третьим старейшим и крупнейшим стоматологическим учебным заведением в США, в котором обучается почти 10 процентов стоматологов страны.