Сварочные флюсы классификация и особенности
Содержание
1. Для чего нужен флюс при сварке
2. Условия использования сварочных флюсов
3. Недостатки
4. Как работают флюсы
5. Сварочные флюсы — классификация
6. Химический состав флюсов для сварки
7. Виды флюсов для сварки по назначению
8. Назначение сварочного флюса — примеры
9. Флюсы для газовой сварки
10. Флюсы для автоматической сварки
При электродуговой или газовой сварке в условиях высоких температур значительно увеличивается химическая активность обрабатываемой зоны. Металл усиленно окисляется под воздействием атмосферного воздуха, в результате шлаки и окислы попадают в него, снижая интенсивность металлургических процессов и в итоге ухудшая качество сварного шва. Для предотвращения этих процессов необходима защитная газовая или жидкая среда, которая изолирует зону сварки. Ее и создают флюсы — неметаллические композитные порошковые компоненты.
Таким образом, назначение флюсов при сварке — изоляция сварочной ванны от атмосферного воздуха, защита наплавляемого металла от интенсивных окислительных процессов, стабильное горение сварочной дуги и получение сварного шва необходимого качества.
Для чего нужен флюс при сварке
Использование флюсов обеспечивает следующие преимущества при сварке.
- Как при электродуговой, так и при газовой сварке флюс сварочный обеспечивает более интенсивное расплавление металла — (соответственно при больших токах или высокой концентрации кислорода). Благодаря этому нет необходимости заблаговременно разделывать кромки будущего сварного шва.
- В зоне шва и на прилегающих к нему поверхностях удается избежать угара металла — его потерь на окисление и испарение.
- Горение дуги имеет более высокую стабильность, что особенно важно при сложных конфигурациях шва
- Снижаются потери энергии источника тока на нагрев металла, соответственно увеличивается его КПД.
- Оптимизируется расход присадочного материала.
- Более удобное выполнение работ для сварщика, потому что флюс экранирует некоторую часть пламени дуги.

Условия использования сварочных флюсов
Задача флюса — стабилизация металлургических процессов при сохранении необходимой производительности электродов. Для этого в процессе сварки следует соблюдать определенные условия.
- Флюс не должен вступать в химическую реакцию с металлом стержня и основным металлом.
- Зона сварной ванны должна оставаться изолированной на протяжении всего сварочного процесса.
Остатки флюса, связанные со шлаковой коркой в результате сварки, по завершении работ должны легко удаляться. При этом до 80% материла после очистки можно использовать заново.
Недостатки
Условных минусов в использовании сварочных флюсов немного.
- Высокая стоимость, которая примерно сопоставима с ценой на сварочную проволоку.
- Yевозможность сразу осмотреть сварной шов. В силу этого, особенно в конструкциях сложной формы, место сварки предварительно тщательно подготавливается.

Как работают флюсы
- Перед сваркой на места соединений наносится толстый (40-60 мм) слой флюса.
- Электрод вводится в зону сварки, происходит поджиг дуги.
- Под воздействием высоких температур (до 6000 °C) флюс с его низкой плотностью быстро плавится в газовом пузыре, изолируя сверху сварную ванну, перекрывая к ней доступ газовых, водяных паров и других химических веществ.
- Имея высокое поверхностное натяжение, таким же образом расплав флюса предотвращает интенсивное разбрызгивание металла.
- Это позволяет значительно увеличить ток дуги (до 1000-2000 Ампер) без серьезных потер материала электрода и с сохранением хорошего качества шва.
- Под воздействием флюса в зоне дуги происходит концентрация тепловой мощности — в результате плавление металла происходит быстрее.
- При этом металлом заполняются все стыки, независимо от состояния кромок.
- Изменяется материальный баланс сварного шва — 60-65% процентов в нем составляет металл свариваемых деталей, и только остальное — это металл сварочного электрода.
Сварочные флюсы — классификация
Классификация флюсов чрезвычайно широка. Их различают по внешнему виду и физическому состоянию, химическому составу, способу получения, назначению. Так, например, для наплавки или дуговой сварки, как правило, используются гранулированные или порошковые флюсы с определенными показателями электропроводности, а для газовой — газы, порошки, пасты.
По способу получения композитов
Различают флюсы плавленые и неплавленые.
Флюс сварочный плавленый широко используют не только при сварке, но при наплавке. Он демонстрирует высокую эффективность в случаях, когда поверхность металла сварного шва путем добавления дополнительных химических элементов должна получить более высокие технические характеристики — например, повышенную стойкость к коррозии или очень ровный и гладкий шов.
Наплавка под флюсом
Получают плавленые флюсы следующим способом: компоненты размалывают, смешивают, затем расплавляют в пламенных или электропечах при полном отсутствии кислорода. Далее нагретые частицы пропускаются через непрерывный поток воды, затвердевая и превращаясь таким образом в гранулят. Размер частиц различен — чем тоньше сварочный пруток, тем меньше должны быть и гранулы.
Далее нагретые частицы пропускаются через непрерывный поток воды, затвердевая и превращаясь таким образом в гранулят. Размер частиц различен — чем тоньше сварочный пруток, тем меньше должны быть и гранулы.
Неплавленые флюсы (керамические) для сварки изготавливаются путем перемешивания измельченных частиц шихты из ферросплавов, минералов, шлакообразующих без последующего плавления. Частицы смешиваются со стеклом и далее спекаются.
В ряду их преимуществ:
- низкий расход,
- возможность многократного использования,
- высокое качество получаемого шва.
Пример — керамический сварочный флюс марки UF (UF-01, UF-02, UF-03) который используется в энергетике и гражданском строительстве для сварки металлоконструкций из низколегированных сталей повышенной прочности.
Химический состав флюсов для сварки
Химический состав — важная составляющая в характеристике флюсов. Материал должен быть химически инертен в условиях очень высоких температур.Помимо этого, он должен обеспечивать эффективную диффузию отдельных элементов (например, легирующих) в металл шва.
Наибольшую массовую долю (от 35…80% от общего объема) в сварочном флюсе обычно (но не во всех) составляет диоксид кремния (кремнезём) — кислотный оксид, бесцветный прозрачный кристаллический минерал. Кремний препятствует процессу образования углерода, тем самым снижая риски появления трещин и пор в металле шва.
Значительную часть составляет марганец. Как активный раскислитель, этот компонент флюсов для сварки снижает образование окислов в зоне сварочной ванны, вступая в реакцию вначале с кислородом в окислах железа, затем и с оксидом кремния. Результат сложной реакции — оксид марганца, нерастворяемый в стали и впоследствии легко удаляемый. Кроме того, марганец реагирует с вредной для металла шва серой — он связывается с ней в сульфид, который затем также удаляется с поверхности шва.
Также в ряду химических элементов флюсов — легирующие добавки — помимо кремния и марганца это молибден, хром, титан, вольфрам, ванадий и другие. Из задача — восстановить первичный химический состав металла, а в ряде случаев — путем легирования восполнить собой выгоревшие основные примеси стали и обеспечить металлу шва дополнительные специальные свойства. Обычно во флюсе они представлены соединениями с железом — ферросплавами (феррохром и т. д.).
Виды флюсов для сварки по назначению
От назначения сварочных флюсов напрямую зависит их выбор по химическому составу.
- Для сварки низкоуглеродистых сталей применяются флюсы с большим содержанием кремния и марганца в сочетании с проволокой из низкоуглеродистой стали без легирующих добавок. Второй вариант — малая доля марганца (или вообще его отсутствие) во флюсе, но легирующие добавки присутствуют в стали сварочного прутка.
- Для сварки низколегированных сталей используются флюсы с высокой химической инертностью, — выше, чем для низкоуглеродистых сталей.
 Благодаря этому получают более пластичный сварной шов. Пример — флюс для сварки стали АН-46.
Благодаря этому получают более пластичный сварной шов. Пример — флюс для сварки стали АН-46. - Для сварки высоколегированных металлов применяются флюсы с минимальной химической активностью. Кремний, как и марганец, практически не используется — его заменяет флюорит (плавиковый шпат), благодаря которому образуются легко отделяемые легкоплавкие шлаки. Также в таких флюсах обычно содержатся оксид алюминия, негашеная известь.
- Для сварки активных металлов (таких, как титан) используют солевые флюсы — как правило, это хлоридные и фторидные соли щелочных металлов. Примесь кислорода в них полностью отсутствует, поскольку она снижает пластичность шва.
Назначение сварочного флюса — примеры
| Плавленые флюсы | Неплавленые флюсы | ||
| АН-348-А, АН-348-АМ, АН-348-В, АН-348-ВМ, ОСЦ-45, ОСЦ-45М, АН-60, ФЦ-9 | Механическая сварка и наплавка низколегированных и углеродистых сталей низколегированной и углеродистой сварочной проволокой | АНК-35 | Сварка низкоуглеродистых сталей низкоуглеродистой проволокой Св-08 и Св-08А |
| АН-8 | Электрошлаковая сварка углеродистых и низколегированных сталей; сварка низколегированных сталей углеродистой и низколегированной сварочной проволокой. |
АНК-46 | Сварка низкоуглеродистых и низколегированных сталей |
| АН-15М, АН-18, АН-20С, АН-20П, АН-20СМ | Дуговая автоматическая сварка и наплавка высоко- и среднелегированных сталей | АНК-30, АНК-47 | Сварка швов высокой хладостойкости |
| АН-22 | Электрошлаковая сварка и дуговая автоматическая наплавка и сварка низко- и среднелегированных сталей | АНК-45 | Сварка высоколегированных сталей |
| АН-26С, АН-26П, АН-26СП | Автоматическая и полуавтоматическая сварка нержавеющих, коррозионностойких и жаропрочных сталей | АНК-40, АНК-18, АНК-19 | Наплавка низкоуглеродистой сварочной проволокой Св-08 и Св-08А; |
| АН-17М, АН-43 и АН-47 | Дуговая сварка и наплавка углеродистых, низко- и среднелегированных сталей высокой и повышенной прочности | АНК-3 | В качестве добавки к флюсам марок АН-348А, ОСЦ-45, АН-60 для повышения стойкости швов к образованию пор |
Флюсы для газовой сварки
Для сварки алюминия и других цветных металлов, чугуна, инструментальных сталей, отдельных марок тонколистовой стали используется защитная газовая атмосфера. Ее обеспечивают газообразные, пастообразные, а также порошковые флюсы. Они могут наносится:
Ее обеспечивают газообразные, пастообразные, а также порошковые флюсы. Они могут наносится:
- на кромки соединяемых деталей;
- напрямую в сварную ванну;
- на присадочный пруток.
В зависимости от физического состояния материала флюсы для сварки подают в рабочую зону по-разному. Некоторую сложность вызывают порошкообразные композиты — их необходимо равномерно и точно вносить в расплав, не позволяя потоку газа раздувать порошок. Составы в виде паст подают на участок соединения. Для подачи газообразных флюсов используют расходомеры — с их помощью газ дозированно подается в рабочую зону.
Электромагнитный расходомер
Важный момент: для газовой сварки флюс по составу подбирают в зависимости от образующихся в ходе сварки оксидов. Если они кислые, флюсы должны быть щелочными (основными), напротив, если щелочные оксиды — выбирают кислые флюсы.
Флюсы, применяемые при газовой сварке наиболее широко:
- медь, латунь, бронза — для их сварки используют кислые флюсы с включением борсодержащих соединений (борная кислота и т.
 д.) — например, такие марки, как МБ-2 или БМ-1;
д.) — например, такие марки, как МБ-2 или БМ-1; - чугун — для его сварки обычно используются флюсы с включением различных соединений щелочных металлов — натрия и калия;
- алюминий — здесь используются составы с содержанием фторидов калия, лития и натрия, а также хлориды. В этом случае наиболее широко применяется сварочный флюс марки АФ-4А.
Флюсы для газовой сварки не используются для соединения деталей из низкоуглеродистых сталей, поскольку на поверхности расплавленного металла интенсивно скапливаются легкоплавкие оксиды железа.
Флюсы для автоматической сварки
Автоматическая и полуавтоматическая сварка наиболее широко применяется при работе с большими конструкциями. Благодаря высоким токам и флюсу возможно сваривание деталей значительной толщины, при этом — без предварительной разделки кромки. Области использования — сваривание труб, изготовление резервуаров, судостроение.
Для такого способа сварки характерно автоматическое поддержание стабильно горящей электродуги, необходимого количества флюса (с отсосом нерасплавившегося), а также непрерывное обновление расплавленного электрода. Чтобы поддерживать в сварочной зоне защитное газовое облако нужного состава, толщина слоя флюса должна быть 40-80 мм, ширина 50-100 мм. Марка флюса для автоматической сварки, как и для классической дуговой, также зависит от характеристик свариваемого металла. Сварка осуществляется в нижнем пространственном положении.
Чтобы поддерживать в сварочной зоне защитное газовое облако нужного состава, толщина слоя флюса должна быть 40-80 мм, ширина 50-100 мм. Марка флюса для автоматической сварки, как и для классической дуговой, также зависит от характеристик свариваемого металла. Сварка осуществляется в нижнем пространственном положении.
Выгодно купить флюс для сварки различных типов и марок вы можете в компании «Центр Метиз».
Как лечить флюс народными средствами
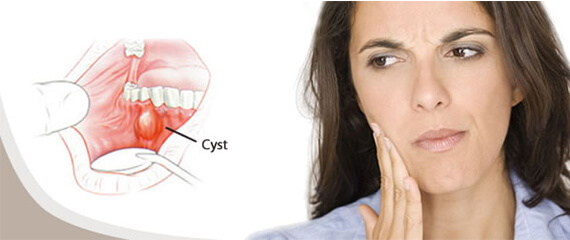
Что такое флюс, знают почти все. Заболевание является достаточно распространенным. С ним сталкиваются как дети, так и взрослые. Зуб начинает болеть, так как у его основания появляется выпуклая шишка. Тогда человеку приходится искать способы, чем вылечить недуг.
Существует множество народных способов удаления флюса. Однако использовать их неразумно. Как избавиться от проблемы, необходимо узнать у квалифицированного врача. В противном случае можно не убрать заболевание, а перевести его в хроническую вялотекущую форму, что очень опасно.
Содержание
- Флюс десны — что это такое
- От чего появляется флюс на десне
- Признаки зубного флюса
- Как долго проходит
- Что делать при флюсе
- Нужно ли удалять зуб при периостите
- Опасность нарушения
- Профилактика
Флюс десны — что это такое
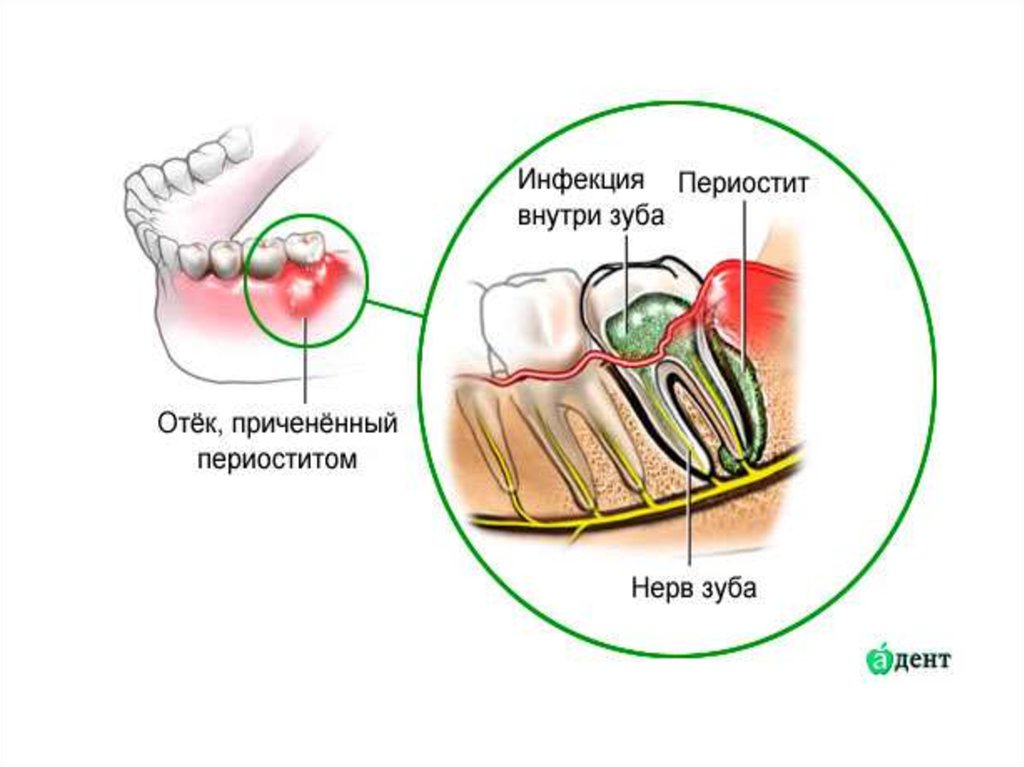
Прежде чем рассказать, что помогает при флюсе и что делать, если он появился, опишем этот недуг. В сфере медицины болезнь называется периоститом. Ее возникновению способствует воспаление тканей надкостницы.
Визуально патологический очаг напоминает упругий мешочек, заполненный гнойным содержимым. Его границы красные, болезненные. Если вовремя не обеспечить отток некротических масс, содержащиеся в них болезнетворные микроорганизмы могут попасть в системный кровоток и разнестись по всему организму.
От чего появляется флюс на десне
Чаще всего зубной флюс развивается из-за неправильного/несвоевременного лечения:
- кариеса;
- пульпита;
- периодонтита;
- воспалительного процесса в костных тканях челюсти;
- альвеолита;
- ретинированных «восьмерок»;
- пародонтита;
- нагноившейся кисты надкостницы.

Бывает, что толчком для возникновения болезни становится острая респираторная инфекция , грипп, корь, скарлатина, ангина, тонзиллит. Лечение флюса, возникшего после травмы, — тоже не редкость. Предпосылки к болезни возникают при переломе челюсти, инфицировании мягких тканей лица.
У многих больных наблюдается прямая связь между переохлаждением или, наоборот, перегревом и периоститом. Негативно влияют на здоровье полости рта и длительные стрессы.
Признаки зубного флюса
Взрослые сталкиваются с болезнью намного чаще детей. Периостит никогда не протекает незаметно. Он вызывает выраженные дискомфортные ощущения, ухудшает качество жизни, заставляет принимать обезболивающие.
В большинстве случаев пациенты жалуются на:
- неприятную пульсацию в десне;
- боль;
- отек тканей;
- воспаление десны;
- опухание щеки;
- увеличение размеров подчелюстных лимфатических узлов;
- усиление болезненной симптоматики при разговоре, употреблении твердой пищи;
- онемение губы/подбородка.

Как долго проходит
Нет смысла ждать, пока периостит пройдет. Некоторые думают, что если шишка лопнула и из нее вытек гной, то больше можно ничего не делать. Это не совсем так. Чтобы рана очистилась полностью, необходимо установить стоматологический дренаж. Это может сделать только врач.
Если терапия проводится грамотно, выздоровление наступает через одну-две недели. При этом очень важно, чтобы больной выполнял все врачебные назначения . В запущенных случаях реабилитационный период может растянуться на целый месяц.
Что делать при флюсе
Подходящий способ лечения заболевания должен подобрать врач. Клиническая ситуация при периостите у пациентов примерно одинаковая, но все-таки могут быть некоторые особенности, поэтому пропускать диагностический этап нельзя. По рентген-снимку можно понять, поражены ли глубокие ткани, в каком состоянии находятся зубные корни.
Стандартное лечение включает в себя
- Хирургические манипуляции.
 Нужны, чтобы удалить скопления гнойных масс из десны. Доктор вводит анестетик местного действия. Затем выполняет небольшой надрез. Устанавливает тонкую дренажную трубочку в сформированное отверстие. Благодаря ей рана очистится полностью.
Нужны, чтобы удалить скопления гнойных масс из десны. Доктор вводит анестетик местного действия. Затем выполняет небольшой надрез. Устанавливает тонкую дренажную трубочку в сформированное отверстие. Благодаря ей рана очистится полностью. - Лечебные полоскания.Помогают снять воспаление. Раствор нужно использовать тот, который назначил стоматолог. Обычно врачи рекомендуют применять содовый состав, сделанный в домашних условиях, или «Мирамистин». Для обработки воспаленной зоны подходят отвары трав — ромашки, календулы.
- Местную противовоспалительную терапию. На пораженные ткани можно наносить заживляющие гели и мази. Хорошо зарекомендовали себя такие составы, как «Холисал», «Метрогил Дета» и пр.
- Антибиотикотерапию. Антибактериальные средства — важный этап лечения флюса. Они не позволяют присоединиться вторичной инфекции, быстро убирают воспаление. При периостите подходят препараты на основе амоксициллина, но по решению доктора могут использоваться лекарства и с другим активным веществом.

- Физиопроцедуры.Проводятся в амбулаторных условиях. Больного просят каждый день приходить в процедурный кабинет для их прохождения. Обеспечивают быстрое снятие воспаления, стимулируют регенеративные процессы. При флюсе эффективен ультразвук, лазер, электрофорез.
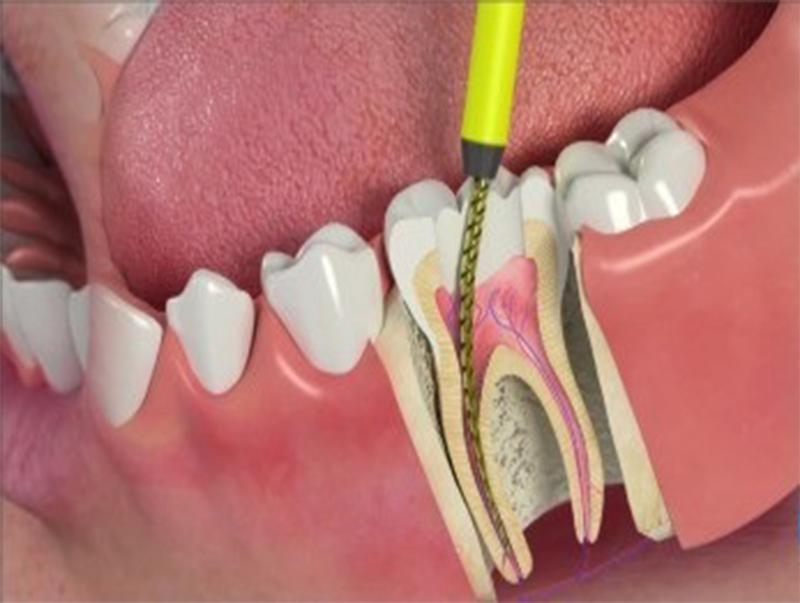
- Терапевтическое лечение.Проводится с целью сохранения зуба, у основания которого появилась шишка. Заключается в проведении эндодонтических манипуляций. Врач вскрывает зубную коронку, закладывает в каналы лекарство. Через некоторое время осуществляет их чистку и пломбирование. После устанавливает постоянную пломбу. В результате таких манипуляций воспалительный процесс полностью блокируется, обеспечивается надежная профилактика повторного образования флюса.
Нужно ли удалять зуб при периостите
Раньше при запущенной форме заболевания единицу, корни которой повреждены, вырывали. Сегодня доктора отдают предпочтение консервативным технологиям. Удаление осуществляет только при полном разрушении коронки и неудовлетворительном качестве корней.
Если снимок подтверждает, что корневые каналы не воспалены, проводится протезирование. Внутрь корня установляется вкладка. Она надежно удерживается благодаря стоматологическому цементу. Сверху фиксируется коронка из металла, металлокерамики, оксида циркония или иного материала.
Опасность нарушения
Воспаление в полости рта имеет свойство прогрессировать. Тогда болезнетворные организмы попадают в глубокие ткани зуба. Небольшая шишка на десне преобразуется в запущенную флегмону — воспалительный очаг, не имеющий четких границ.
Создаются условия для развития сепсиса. Это состояние, способное привести к летальному исходу.
Профилактика
Чтобы снизить вероятность возникновения периостита, необходимо:
- Ежегодно проходить профилактический осмотр в кабинете стоматолога. Врач проверит, нет ли заболеваний, и проведет профессиональную гигиену ротовой полости.
- Чистить зубы два-три раза в день. Для этого нужно использовать качественную пасту и щетку, подобранную специалистом.

- Своевременно лечить любые стоматологические заболевания. Ведь очень часто флюс является логическим продолжением глубокого кариеса.
- Отказаться от курения и правильно питаться. Рацион должен быть богат свежими овощами и фруктами. Они обеспечат организм полезными элементами и положительно скажутся на состоянии десен.
Подведем итог. Если вы хотите узнать, как быстро избавиться от периостита, обязательно посетите врача-стоматолога. Не «изобретайте велосипед» и не ищите народные рецепты. Терапия должна быть комплексной, поэтапной. За ее проведение должен отвечать доктор. Только тогда удастся быстро избавиться от болезни и вопрос, как вылечить флюс, будет окончательно закрыт.
Флюс для пайки: кислоты, твердые вещества и растворители
Флюс состоит из двух основных ингредиентов: кислоты для удаления оксидов и вещества или веществ («твердых веществ») для покрытия поверхности и предотвращения доступа кислорода к поверхности после удаления оксидов. Жидкий флюс — это те же ингредиенты в растворителе.
Жидкий флюс — это те же ингредиенты в растворителе.
Выбор флюса может быть самым важным решением, которое когда-либо будет приниматься на предприятии, занимающемся сборкой электроники. Правильный флюс может сэкономить огромные расходы, включая, помимо прочего, дефекты припоя, очистку и отказы продукта. Тем не менее, флюсы сложны, и правильный выбор включает в себя навигацию по химическому минному полю, осложненному иногда причудливой терминологией и, слишком часто, сомнительной маркетинговой практикой некоторых известных производителей флюсов.
Это вторая из трех частей объяснения флюсов: что они делают, как они это делают и какой из них лучше всего подходит для различных приложений. Если вы читали часть 1, значит, вы знакомы с основами флюса и готовы к особенностям выбора флюса, который значительно облегчит вашу жизнь при пайке. Если вы не читали часть 1 о флюсе для пайки, это действительно лучшее место для начала.
Течение припоя известно как смачивание и происходит только в том случае, если припой наносится на поверхность из чистого элементарного металла. Элементарный металл нестабилен и обладает энергией для притяжения припоя (межатомное притяжение). Однако окисленному металлу не хватает этой энергии, и он не допускает смачивания. За исключением золота, все поверхности компонентов окисляются, и этот оксид должен быть полностью удален, а раскисленная поверхность защищена от повторного окисления перед нанесением припоя. Удаление оксидов и предотвращение повторного окисления является ролью флюса.
Элементарный металл нестабилен и обладает энергией для притяжения припоя (межатомное притяжение). Однако окисленному металлу не хватает этой энергии, и он не допускает смачивания. За исключением золота, все поверхности компонентов окисляются, и этот оксид должен быть полностью удален, а раскисленная поверхность защищена от повторного окисления перед нанесением припоя. Удаление оксидов и предотвращение повторного окисления является ролью флюса.
Флюс состоит из двух основных ингредиентов: кислоты для удаления оксидов и вещества или веществ («твердых веществ») для покрытия поверхности и предотвращения доступа кислорода к поверхности после удаления оксидов. Жидкий флюс — это те же ингредиенты в растворителе.
B журнал написан: Часть флюса, удаляющая оксиды, которую промышленность по причинам, утерянным в древности, настаивает на том, чтобы называть их «активаторами», почти всегда представляет собой кислоту либо непосредственно, либо в соединении, выделяющем кислоту при нагревании. Сила кислоты определяется содержанием в ней ионов водорода; больше ионов водорода соответствует большей кислотности. При раскислении (взаимодействии кислоты с оксидом металла, основанием) водород из кислоты соединяется с отщепленным от оксида кислородом с образованием воды, а другие элементы кислоты соединяются с металлом с образованием солей металлов. Давайте сделаем паузу, чтобы извиниться перед химиками за использование слов «сильный» и «слабый» применительно к кислотности. Для наших целей мы можем думать, что «сильные» кислоты просто более мощные, чем «слабые». Но химики не думают о силе действия, когда классифицируют кислоты как сильные или слабые. Для них сильными кислотами являются те, которые распадаются на составные части («ионизируются») при добавлении в воду. Слабые кислоты не ионизируются полностью, в отличие от сильных кислот. Эта специальная терминология вызывает значительную путаницу у нехимиков, когда лаборатории, проверяющие чистоту схемных узлов, сообщают, что отказы происходят из-за чрезмерного количества слабых кислотных остатков. Водные растворы содержат водород в двух формах: ионы водорода [H + ][1] и ионы гидроксония [H 3 O + ]. Атом водорода (Н) состоит из одного протона и одного электрона. Ион водорода (H + ) — это просто протон (и его часто называют протоном, а не ионом водорода). Ионы водорода обладают высокой реакционной способностью и могут быть донорами протонов или реципиентами электронов в химических реакциях. Растворы, содержащие больше H + , чем H 3 O + , являются кислотами, а растворы с меньшим количеством относительных ионов водорода являются основными. Концентрация H + выражается как pH, отрицательный логарифм ионов водорода на литр – pH = −log 10 [H + ], где [H + ] представляет собой концентрацию ионов водорода в молях (M ).[2] Шкала pH варьируется от 0 до 14, где 7,0 означает нейтральное значение. Это очень упрощенный взгляд на кислоты. На самом деле существует три разных определения кислоты, два из которых относятся исключительно к водороду, а третье определяет кислоту таким образом, что водород не требуется. Для наших целей туда идти не обязательно. Люди, не являющиеся химиками, часто думают о силе кислоты с точки зрения рН, но по большей части рН не имеет значения, когда речь идет о потоке. По причинам, о которых мы поговорим позже, растворителем большинства жидких флюсов является спирт, а не вода, в то время как pH относится только к растворам на водной основе. Для растворов, не основанных на воде, соответствующей мерой прочности является «кислотное число», количество миллиграммов гидроксида калия (основания), необходимое для нейтрализации грамма кислого вещества. Для целей, которые здесь имеют значение, кислоты работают одинаково в водных и неводных растворах; отличается только система измерения кислоты. «Сила» кислоты зависит от концентрации ионов водорода. Более низкая концентрация (содержание по общему объему) кислоты будет иметь более низкий pH или кислотное число, чем более высокая концентрация той же кислоты. Это важно в отношении использования очень реакционноспособных галогенидов в потоках электроники, обсуждаемых ниже. Доступны флюсы с маркировкой «нейтральный pH», в том числе флюсы некоторых известных марок. И они чрезвычайно эффективны для удаления оксидов, способных раскислять некоторые из наименее поддающихся пайке металлов.[5] Как что-то «нейтральное» (что, в конце концов, означает нереактивное) может удалять оксиды? Ответ, конечно же, заключается в том, что они не являются «нейтральными» при всех температурах. Нейтральные потоки бывают двух видов. Первый остается нейтральным соединением, но при нагревании образует кислоты. Кислоты очень сильные и поэтому отлично подходят для раскисления. Но образуются высокопроводящие и вызывающие коррозию ионные остатки, которые необходимо удалять после пайки. Второй тип начинается с высокой кислотности, но нейтрализуется реакцией с кислородом при высоких температурах. Проблема в том, что бывают ситуации, когда не весь флюс достигает температуры нейтрализации и любой флюс в полостях или под компонентами вытесняет воздух (и кислород), необходимый для нейтрализации. Оба типа нейтрального флюса требуют смывания после пайки. Остатки водорастворимы и могут быть удалены водой , если вода может достичь остатков . Это не точно. Флюс имеет низкое поверхностное натяжение, что позволяет ему проникать в труднодоступные места. На самом деле очень важна способность флюса попадать в те пространства, которые требуют раскисления. Но вода имеет очень высокое поверхностное натяжение и не может достичь потока в полостях. Кроме того, водопроводная вода, как и флюс, содержит проводящие и потенциально вызывающие коррозию ионы, которые снижают надежность. Для очистки должна использоваться вода, из которой удалены ионы («деионизированная» вода). Раскисление является эндотермической химической реакцией и происходит быстрее при более высоких температурах. Хотя некоторые сильные кислоты могут удалять некоторые оксиды при комнатной температуре, все кислоты работают быстрее при нагревании, а кислоты во флюсе электроники обычно не начинают работать, пока не нагреются. Минимальная температура, при которой кислота начинает работать, называется «температурой активации». Температура активации часто находится в диапазоне 150°F/65°C, но это только начальная точка. Во многих случаях флюсовые кислоты изначально представляют собой инертные соединения при комнатной температуре. Они должны быть нагреты, чтобы разрушиться и сформировать кислоты. Хотя флюсы в основном основаны на кислотах для удаления оксидов, некоторые также содержат небольшие количества галогенидов металлов для усиления действия кислоты. Известно, что небольшое количество галогена (от разложения галоида) усиливает работу флюсовых кислот. Также известно, что галогены несут сильный электрический заряд, который в больших количествах разрушает электронные схемы. В идеальном мире не было бы негативных последствий использования сильных кислот и галогенидов. Однако наш мир не идеален, и как кислота, так и галогениды создают серьезные проблемы с надежностью. Кислотные и галогенидные остатки являются ионными, и их остатки после пайки называются «ионными загрязнениями». Ионные означает, что они являются электрическими проводниками и потенциально коррозионными. В целом, хотя и не абсолютно, проводимость и коррозионная активность увеличиваются с увеличением силы кислоты или основания. Проводящие остатки могут позволить электрическому току течь между не общими проводниками («утечка тока»), а не через схему. Большинство сборок электроники могут допустить некоторую утечку тока, но все сборки имеют пределы, легко превышающие ионные или анионные остатки относительно мягких флюсов. Более высокие уровни ионов (больший ионный заряд и/или большее количество ионного материала) могут способствовать образованию дендритов. И даже более высокие уровни ионов могут вызвать коррозию. Электронные флюсы классифицируются как низко-, средне- или высокоактивные (обозначаются L, M и H) на основе проводимости и коррозионной активности их остатков после пайки. Правила изложены в отраслевом документе J-STD-004B, выпущенном торговой ассоциацией IPC. Коррозионную активность определяют, нанося флюс на тонкий слой меди на стеклянной пластине и наблюдая, проникает ли флюс через медь и в какой степени, оставляя только стекло. Процедура определения проводимости довольно сложна, но, по сути, и очень Флюсы, образцы которых проходят испытание на электропроводность без очистки и не пробивают какую-либо зону покрытия при испытании медным зеркалом, классифицируются как низкоактивные (L). Тест на электропроводность имеет несколько критических недостатков. Самое главное, нагревание флюса в печи для оплавления или в системе для пайки волной припоя может нейтрализовать органические кислоты. При достаточной температуре (150°C и выше) в присутствии кислорода (воздух, который нас окружает) органические кислоты окисляются и становятся нейтральными. Другими словами, флюсовые кислоты могут быть нейтрализованы перед проведением испытаний проводимости и дендритов. При выборе флюса рекомендуется начать с рейтинга J-STD-004B; это экономит много времени, которое в противном случае могло бы быть потрачено на оценку совершенно неподходящих флюсов. Проводимость остатков флюса имеет огромное значение. Отказы происходят, когда слишком много электричества предпочитает протекать через остатки кислоты между не общими проводниками, а не по схеме. Степень утечки тока «слишком велика» зависит от требуемой точности используемого продукта и среды, в которой продукт должен работать. (Проблемы с ионным загрязнением возрастают по мере увеличения влажности. Сборка, находящаяся в пустыне, будет гораздо меньше подвержена ионному загрязнению, чем такая же сборка в болоте.) Галогениды имеют особое значение в классификации флюсов. Необходимо удалить оксиды, иначе припой не будет смачиваться. Однако удаление оксидов само по себе недостаточно. У производителей флюсов есть свой жаргон, например, «активаторы» вместо кислот. Традиционный, но все более редкий жаргон для твердых тел — «носитель», предположительно потому, что кислоты переносятся твердыми телами. «Твердые вещества» более точно отражают роль материала в обеспечении барьера против кислорода. Твердые вещества существуют только для предотвращения доступа кислорода к раскисленному металлу во время нанесения припоя. Вот и все. Они не удаляют оксиды. Они не токопроводящие. Они не вызывают коррозии. Они составляют гораздо больший процент объема флюса, чем кислоты. Исторически во всех флюсах для электроники использовалась канифоль[4] для твердых частиц. Канифоль получают из сока некоторых сосен после испарения большинства летучих компонентов (среди прочих производных образуется скипидар). Канифоль обладает двумя свойствами, которые делают ее идеальной для использования в электронных флюсах. Во-первых, он выдерживает температуры пайки без разрушения, гарантируя, что раскисленная поверхность остается защищенной от кислорода. Во-вторых, что еще более важно, он гидрофобный (отталкивает влагу). Канифоль инкапсулирует кислоты в среде без влаги, что сводит к минимуму проводимость и коррозию. (Все неприятные последствия ионного загрязнения требуют некоторой влажности. Сопротивление утечке тока снижается по мере увеличения влажности.) Канифоль в естественном состоянии содержит очень мягкую органическую кислоту, абиетиновую. Канифоль неполярна и не растворяется в воде, которая является полярной.[5] Попытка смешать канифоль с водой приводит к липкой массе (не технический термин, а точное описание). Мощные растворители, такие как трихлорэтан, которые в прошлом были очень эффективны для удаления остатков канифоли, теперь запрещены из-за проблем с окружающей средой и здоровьем. Ни один доступный в настоящее время растворитель не может сравниться с трихлорэтаном по способности удалять канифоль, а доступные растворители дороги. Он предназначен для того, чтобы оставить его на схеме после пайки. Основная проблема канифоли — ее видимость. После пайки выделяется коричневый осадок. Количество остатка, остающегося после пайки, определяется концентрацией твердых частиц во флюсе. Чтобы избежать неприятного количества остатков канифоли, нужно избегать флюсов с высокой концентрацией канифоли. Поскольку они были разработаны для ранних версий пайки волной припоя, где избыток припоя, например мостов, можно было предотвратить за счет высокой концентрации канифоли (в некоторых случаях 40% и более), многие канифольные флюсы, которые до сих пор широко используются, содержат во много раз больше твердых веществ, чем необходимо. Припой с порошковой проволокой оставляет остатки. Содержание флюса по умолчанию в проволочном припое составляет около 3% по весу, что соответствует очень большому количеству по объему. Использование припоя с содержанием флюса около 1% устраняет основной источник видимого остатка канифоли. Флюс внутри припоя в любом случае не дает большой пользы.[6] Недостатком канифоли для производителей флюса является получение прибыли. Канифоль есть канифоль, независимо от этикетки производителя флюса. Одним из материалов, используемых вместо канифоли, являются смолы. И это становится сложно. Кембриджский словарь определяет смолу как «густое, липкое вещество, производимое некоторыми деревьями и становящееся желтым и твердым после сбора, или любое из различных подобных веществ, получаемых в результате химического процесса для использования в промышленности». Мы уже обсуждали материал в первой части этого определения: канифоль. А некоторые смолы, очищенные от канифоли, имеют свойства, очень похожие на канифоль. Но другие смолы не имеют отношения к канифоли; они являются результатом химического синтеза. Канифоль есть канифоль, но смолы имеют много форм, и, поскольку ни один производитель не раскрывает свои запатентованные ингредиенты, невозможно узнать, какая смола используется в каком-либо конкретном флюсе на основе смолы. Заказчики контрактных производителей (или внутренние заказчики интегрированных компаний с собственным производством) часто отказываются от сборок с видимыми остатками флюса. Видимые остатки представляют собой безвредные остатки твердых веществ и не являются проблемой надежности, в отличие от невидимого ионного загрязнения, оставленного кислотами, но большинство аудиторов поставщиков ничего не знают о процессе. Самый простой способ успокоить неосведомленных клиентов — заменить видимые твердые вещества (канифоль или некоторые смолы) бесцветными твердыми веществами. Гликоли являются одними из самых популярных заменителей. Гликоли бесцветны и растворимы в воде. Они оставляют очень мало видимых следов после пайки и, в отличие от канифоли, при необходимости могут быть удалены промывкой водой. Отсутствие видимости и возможность удаления водой (в отличие от дорогостоящих химикатов, необходимых для удаления канифоли) делает эти флюсы очень популярными среди контрактных производителей, а также компаний, производящих для собственного использования, но не обладающих достаточными знаниями, чтобы понять, почему остатки канифоли сами по себе не означают плохой надежности (или что отсутствие видимых остатков в случае твердых веществ, таких как гликоли, не обязательно свидетельствует о высокой надежности). Доступны флюсы внутри проволочного припоя, смешанные с частицами припоя в паяльной пасте, в виде гелей или паст, а также в виде жидкостей. Особенностью, которая отличает жидкий флюс от других форм, является растворитель. Наиболее распространенным растворителем является спирт. На самом деле не имеет значения, какой алкоголь используется; все они ведут себя одинаково. Две характеристики делают спирт идеальным растворителем флюса: Спирты представляют собой летучие органические соединения (ЛОС), которые могут быть канцерогенными, способствуют образованию смога и действуют как парниковые газы. На водной основе не то же самое, что на водорастворимой. Водорастворимый означает, что остатки флюса после испарения растворителя растворяются в воде. Электронная книга по флюсам для пайки поясняет категории флюсов в соответствии с J-STD-004B. В заключение будут даны рекомендации по выбору флюса, наиболее подходящего для нужд продукта. [1] Ионы водорода H+ фактически связаны с кислородом в форме OH – , известной как гидроксид, но водород ведет себя как отдельный ион, и химики называют гидроксид ионами водорода. [2] M представляет количество молей на литр воды, где 1 моль = 602 214 076 000 000 000 000 000 [3] Литр чистой воды при 25°C содержит 1 × 10 -7 M ионов водорода и такое же количество ионов гидроксония. (1 × 10 -7 M)x(−log 10 ) = 7. [4] «Нейтральный» на самом деле является движущейся целью, которая зависит от температуры. Нейтральная вода при 25°C имеет pH 7,0. [5] В части 1 я определил «пригодность к пайке» как сложность удаления оксида с поверхности. Другими словами, прочность флюса, необходимая для раскисления детали. [6] У всех производителей флюсов есть свои собственные запатентованные рецепты, которые они охраняют так же, как кока-кола скрывает свою формулу. Помимо нескольких общих ингредиентов, таких как канифоль или изопропиловый спирт, большинство ключевых добавок держатся в секрете. В паспорте безопасности одного производителя флюса указано: «Освобождение от коммерческой тайны находится на рассмотрении [Комиссии по рассмотрению информации об опасных материалах] для одного или нескольких ингредиентов в этом продукте».
к:
PCBWay
03 марта 2023 г.
Флюс для припоя
Что такое флюс для припоя и как он работает? Флюс для припоя является полезным инструментом для улучшения связи между припоем и металлическими поверхностями компонентов в процессе пайки. В то время как паяльная паста представляет собой смесь частиц припоя и флюса, флюс служит химическим очищающим средством для удаления окисления и других загрязнений с металлических поверхностей перед пайкой. Без флюса окисление может создать барьер между металлом и припоем, что приведет к слабым и ненадежным паяным соединениям. Типы флюсов для припоя Канифольный флюс, флюс без очистки и водорастворимый флюс — это три основных типа флюсов. Среди них канифольный флюс является наиболее часто используемым из-за его неагрессивных свойств, эффективности в рекомендуемом диапазоне температур пайки для большинства приложений электроники и меньшей вероятности остатка флюса. Никакой чистый флюс не предназначен для применений, где очистка остатков флюса не требуется или невозможна. Флюс без очистки обычно оставляет минимальное количество остатков, которые не вредны для печатной платы или компонентов. Что касается водорастворимого флюса, то это раствор на основе гликоля, который обычно используется в автоматизированных процессах сборки печатных плат, где необходимо быстро обрабатывать большие объемы плат. Водорастворимый характер флюса позволяет легко смыть платы после пайки с помощью простой промывки водой. Существуют различные методы очистки остатков флюса, включая использование растворителей, изопропилового спирта или специальных чистящих растворов. Рекомендации по эффективной пайке с использованием флюса для припоя При использовании флюса для пайки необходимо учитывать два важных фактора. Во-первых, это совместимость с припаиваемыми материалами для предотвращения любого потенциального повреждения или коррозии. Например, если флюс несовместим с медью, это может привести к коррозии и выходу из строя паяного соединения. Другой уровень активности потока. Флюс должен быть достаточно активным, чтобы удалить любое окисление или загрязнения с припаиваемых поверхностей, но не должен быть слишком активным, чтобы повредить компоненты или паяные соединения. Нахождение правильного баланса между совместимостью и уровнем активности необходимо для получения прочных и надежных паяных соединений. В каких случаях возможна пайка без флюса? Несмотря на то, что флюс для пайки обычно рекомендуется для получения качественного паяного соединения, бывают случаи, когда он может не понадобиться.
Джеймс А. (Джим) Смит, доктор философии ABD, президент Electronics Manufacturing Sciences, Inc.0028 Кислоты  Для описания кислотности потока используется термин «активность». Чаще всего кислоты являются органическими (то есть содержат углерод). Неорганические кислоты (соединения водорода с неметаллами), такие как соляная или бромистоводородная, обладают исключительными свойствами удаления оксидов, но несовместимы с надежностью электроники; они оставляют высокопроводящие и вызывающие коррозию остатки, которые могут вызвать сбои в работе электрооборудования. Неорганические кислоты в форме галогенидов (обсуждаемые ниже) встречаются в некоторых флюсах для электроники, но в очень низких концентрациях и только в дополнение к большим количествам органических кислот.
Для описания кислотности потока используется термин «активность». Чаще всего кислоты являются органическими (то есть содержат углерод). Неорганические кислоты (соединения водорода с неметаллами), такие как соляная или бромистоводородная, обладают исключительными свойствами удаления оксидов, но несовместимы с надежностью электроники; они оставляют высокопроводящие и вызывающие коррозию остатки, которые могут вызвать сбои в работе электрооборудования. Неорганические кислоты в форме галогенидов (обсуждаемые ниже) встречаются в некоторых флюсах для электроники, но в очень низких концентрациях и только в дополнение к большим количествам органических кислот.  Более сильные кислоты обычно притягивают кислород с большей силой, чем более слабые кислоты. Большее притяжение означает, что более сильные кислоты обладают большей раскисляющей способностью (способны удалять большее количество оксидов быстрее, чем более слабые кислоты, и способны удалять оксиды из большего числа металлов, чем более слабые кислоты).
Более сильные кислоты обычно притягивают кислород с большей силой, чем более слабые кислоты. Большее притяжение означает, что более сильные кислоты обладают большей раскисляющей способностью (способны удалять большее количество оксидов быстрее, чем более слабые кислоты, и способны удалять оксиды из большего числа металлов, чем более слабые кислоты).
Сильные и слабые кислоты 
В основном речь идет о водороде  [3][4] Числа меньше 7,0 (более высокие концентрации H + ) являются кислыми, а более 7,0 — основными.
[3][4] Числа меньше 7,0 (более высокие концентрации H + ) являются кислыми, а более 7,0 — основными.
рН по сравнению с кислотным числом 
Флюс с нейтральным pH 
 Но поверхностное натяжение деионизированной воды больше, чем поверхностное натяжение водопроводной воды, что увеличивает вероятность того, что промывочная вода не достигнет всех остатков флюса.
Но поверхностное натяжение деионизированной воды больше, чем поверхностное натяжение водопроводной воды, что увеличивает вероятность того, что промывочная вода не достигнет всех остатков флюса.
Активация
Несколько слов о галогенидах  Хлорид натрия (поваренная соль) является обычным галогенидом, хотя и не обнаруженным во флюсе. Во флюсе используются только соединения хлора и брома, но есть несколько возможностей, и нет никакого способа узнать, какой галогенид находится во флюсе. Когда галогенид сталкивается с водой (один из побочных продуктов раскисления, когда водород кислоты соединяется с кислородом из оксида), он разделяется на ион металла и анион галогена, обычно либо хлорид, либо бромид. Интересно, что галоген является основанием, подобным оксиду металла, а не кислотой, но он энергично атакует оксид. Почему и как? Ответ не ясен. Ученые до сих пор спорят о причине, по которой галогены атакуют оксид металла (возможно, потому, что галоген является более сильным основанием, чем оксид, но это не доказано).
Хлорид натрия (поваренная соль) является обычным галогенидом, хотя и не обнаруженным во флюсе. Во флюсе используются только соединения хлора и брома, но есть несколько возможностей, и нет никакого способа узнать, какой галогенид находится во флюсе. Когда галогенид сталкивается с водой (один из побочных продуктов раскисления, когда водород кислоты соединяется с кислородом из оксида), он разделяется на ион металла и анион галогена, обычно либо хлорид, либо бромид. Интересно, что галоген является основанием, подобным оксиду металла, а не кислотой, но он энергично атакует оксид. Почему и как? Ответ не ясен. Ученые до сих пор спорят о причине, по которой галогены атакуют оксид металла (возможно, потому, что галоген является более сильным основанием, чем оксид, но это не доказано).  Чтобы флюс считался безгалогенидным в соответствии с J-STD-004B, действующей системой классификации, флюс должен содержать менее 0,05 % галогенида по объему (то есть для жидкого флюса объем без учета растворителя). Это очень сложный уровень, и большинство флюсов, подходящих для использования в производстве надежных продуктов, не соответствуют статусу безгалогенных. Однако флюсы высокой надежности содержат менее 0,5% галогенидов по объему.
Чтобы флюс считался безгалогенидным в соответствии с J-STD-004B, действующей системой классификации, флюс должен содержать менее 0,05 % галогенида по объему (то есть для жидкого флюса объем без учета растворителя). Это очень сложный уровень, и большинство флюсов, подходящих для использования в производстве надежных продуктов, не соответствуют статусу безгалогенных. Однако флюсы высокой надежности содержат менее 0,5% галогенидов по объему.
Проблема ионного загрязнения 
Классификация прочности флюса  (Там, где медь удалена, можно увидеть сквозь стеклянную подложку.) С проводимостью сложнее.
(Там, где медь удалена, можно увидеть сквозь стеклянную подложку.) С проводимостью сложнее.
 Некоторые флюсы средней активности (M) пробивают до 50% площади покрытия медного зеркала, но могут пройти испытание на проводимость без очистки, но большинство из них требуют очистки для прохождения испытания на проводимость. Потоки H пробивают более 50% площади покрытия медного зеркала и требуют очистки для прохождения теста на проводимость. Флюсы, которые не могут пройти тест на электропроводность, сильнее H и не подходят для использования в электронных узлах.
Некоторые флюсы средней активности (M) пробивают до 50% площади покрытия медного зеркала, но могут пройти испытание на проводимость без очистки, но большинство из них требуют очистки для прохождения испытания на проводимость. Потоки H пробивают более 50% площади покрытия медного зеркала и требуют очистки для прохождения теста на проводимость. Флюсы, которые не могут пройти тест на электропроводность, сильнее H и не подходят для использования в электронных узлах.
Недостаток в J-STD-004B 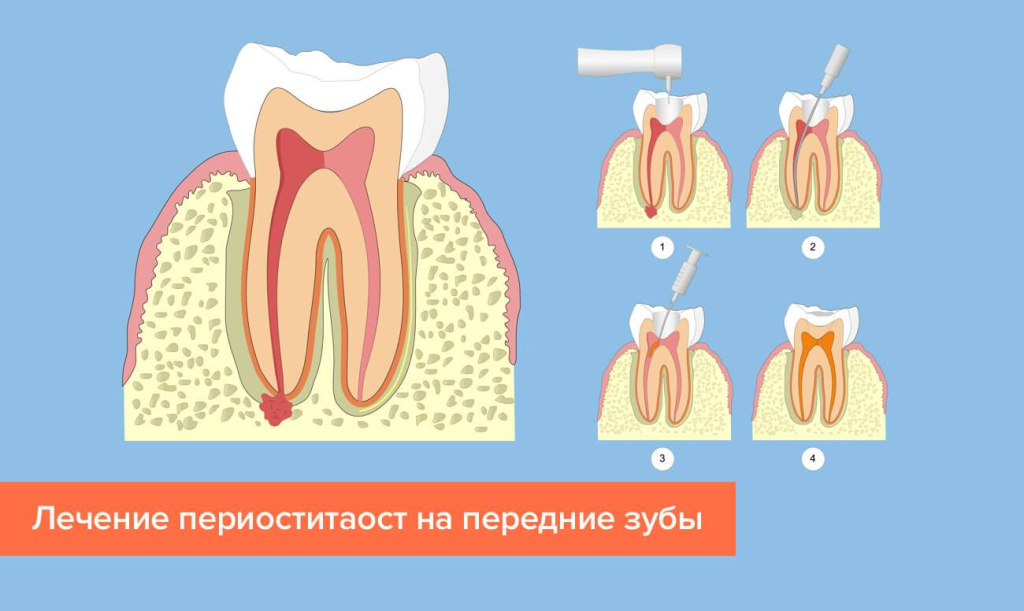 Сторонники процедуры классификации утверждают, что флюс превысит температуру нейтрализации во время нанесения припоя. Критики (включая меня) отмечают, что это никоим образом не гарантируется. Например, флюс, который не находится в контакте с паяльником, может никогда не нагреться выше комнатной температуры. Флюс, попавший в полости или под компоненты для поверхностного монтажа, вытесняет кислородсодержащий воздух и не окисляется независимо от температуры, в которой они находятся. Существуют и другие сценарии, при которых флюс не достигает температуры нейтрализации. Еще больше замутняя воду, группа флюсов использует соединения, изначально нейтральные, но образующие очень сильные кислоты при достижении достаточно высокой температуры, которая может быть больше пиковой температуры при обработке исследуемых образцов.
Сторонники процедуры классификации утверждают, что флюс превысит температуру нейтрализации во время нанесения припоя. Критики (включая меня) отмечают, что это никоим образом не гарантируется. Например, флюс, который не находится в контакте с паяльником, может никогда не нагреться выше комнатной температуры. Флюс, попавший в полости или под компоненты для поверхностного монтажа, вытесняет кислородсодержащий воздух и не окисляется независимо от температуры, в которой они находятся. Существуют и другие сценарии, при которых флюс не достигает температуры нейтрализации. Еще больше замутняя воду, группа флюсов использует соединения, изначально нейтральные, но образующие очень сильные кислоты при достижении достаточно высокой температуры, которая может быть больше пиковой температуры при обработке исследуемых образцов.  Однако сохранность флюса в чистом виде (не нагретом) тоже должна учитываться . Многие флюсы, классифицируемые как низкоактивные в соответствии с J-STD-004B, имеют подозрительно высокие кислотные числа, и не весь этот флюс в каждой области сборки схемы будет подвергаться значительному нагреву во время пайки. К сожалению, информация о проводимости потока перед нагревом обычно отсутствует.
Однако сохранность флюса в чистом виде (не нагретом) тоже должна учитываться . Многие флюсы, классифицируемые как низкоактивные в соответствии с J-STD-004B, имеют подозрительно высокие кислотные числа, и не весь этот флюс в каждой области сборки схемы будет подвергаться значительному нагреву во время пайки. К сожалению, информация о проводимости потока перед нагревом обычно отсутствует.
Еще немного о галогенидах  Поскольку остатки галогенидов обладают высокой электропроводностью и вызывают коррозию, флюсы, содержащие галогениды, классифицируются отдельно от флюсов, не содержащих галогенидов («не содержащие галогенидов»). Флюсы, содержащие галогениды, также классифицируются по процентному содержанию галогенидов. Только флюсы, содержащие менее 0,05 % галогенидов по объему (исходя из содержания флюса без растворителя), могут быть классифицированы как не содержащие галогенидов. Галогенные флюсы с низкой активностью содержат менее 0,5% галогенидов по объему. Предельное содержание галогенидов для галогенидных флюсов средней активности составляет менее 2,0%. Высокоактивные галогенидные флюсы содержат 2% или более галогенидов. Это приводит к шести уровням активности: L0, L1, M0, M1, H0 и h2, где 0 означает отсутствие галогенов и 1 — содержание галогенидов в указанных пределах.
Поскольку остатки галогенидов обладают высокой электропроводностью и вызывают коррозию, флюсы, содержащие галогениды, классифицируются отдельно от флюсов, не содержащих галогенидов («не содержащие галогенидов»). Флюсы, содержащие галогениды, также классифицируются по процентному содержанию галогенидов. Только флюсы, содержащие менее 0,05 % галогенидов по объему (исходя из содержания флюса без растворителя), могут быть классифицированы как не содержащие галогенидов. Галогенные флюсы с низкой активностью содержат менее 0,5% галогенидов по объему. Предельное содержание галогенидов для галогенидных флюсов средней активности составляет менее 2,0%. Высокоактивные галогенидные флюсы содержат 2% или более галогенидов. Это приводит к шести уровням активности: L0, L1, M0, M1, H0 и h2, где 0 означает отсутствие галогенов и 1 — содержание галогенидов в указанных пределах.
Твердые вещества  Если кислород может достичь раскисленной поверхности, новые оксиды будут мгновенно образовываться, а поверхностная энергия будет потеряна. В дополнение к удалению оксидов флюс должен создавать барьер, предотвращающий доступ кислорода к вновь раскисленному металлу до тех пор, пока не будет нанесен припой. Вот где на помощь приходят твердые вещества.
Если кислород может достичь раскисленной поверхности, новые оксиды будут мгновенно образовываться, а поверхностная энергия будет потеряна. В дополнение к удалению оксидов флюс должен создавать барьер, предотвращающий доступ кислорода к вновь раскисленному металлу до тех пор, пока не будет нанесен припой. Вот где на помощь приходят твердые вещества.
Роль твердых веществ  Любые видимые остатки флюса после пайки являются остатками твердых частиц; кислоты не видно. Однако, как известно контрактным производителям, их клиенты не разбираются в науке о пайке и хотят отказаться от сборок с видимыми остатками. (В зависимости от природы твердых частиц они могут вызвать такие проблемы, как загрязнение штифтов испытательного приспособления или нарушение надлежащей адгезии конформного покрытия, но сами по себе они не влияют на целостность продукта. В случае конформного покрытия замена материалов покрытия часто может устранить проблема адгезии.) Из-за давления со стороны неосведомленных клиентов многие контрактные производители приняли рецептуры флюсов, которые не оставляют видимых остатков, и, конечно же, производители флюсов создали новые рецептуры для удовлетворения спроса на невидимые твердые частицы.
Любые видимые остатки флюса после пайки являются остатками твердых частиц; кислоты не видно. Однако, как известно контрактным производителям, их клиенты не разбираются в науке о пайке и хотят отказаться от сборок с видимыми остатками. (В зависимости от природы твердых частиц они могут вызвать такие проблемы, как загрязнение штифтов испытательного приспособления или нарушение надлежащей адгезии конформного покрытия, но сами по себе они не влияют на целостность продукта. В случае конформного покрытия замена материалов покрытия часто может устранить проблема адгезии.) Из-за давления со стороны неосведомленных клиентов многие контрактные производители приняли рецептуры флюсов, которые не оставляют видимых остатков, и, конечно же, производители флюсов создали новые рецептуры для удовлетворения спроса на невидимые твердые частицы.
Канифоль  Любой, кто имел дело с рождественской елкой, хорошо знаком с одним свойством канифоли — она очень липкая (до тех пор, пока все оставшиеся летучие вещества не испарятся, после чего канифоль на ощупь и действует очень похоже на полиуретан, хотя эти два материала очень разные химически).
Любой, кто имел дело с рождественской елкой, хорошо знаком с одним свойством канифоли — она очень липкая (до тех пор, пока все оставшиеся летучие вещества не испарятся, после чего канифоль на ощупь и действует очень похоже на полиуретан, хотя эти два материала очень разные химически).
Музыканты используют его со струнными инструментами.  Кислота недостаточно сильна, чтобы удалить многие оксиды, кроме оксида олова. Во флюсы, пригодные для производства, добавляют более сильные кислоты, но канифоль в спирте без дополнительных кислот по-прежнему продается для использования с лужеными деталями. (Согласно устаревшему стандарту MIL для флюса канифоль в спирте обозначается как «Тип R».)
Кислота недостаточно сильна, чтобы удалить многие оксиды, кроме оксида олова. Во флюсы, пригодные для производства, добавляют более сильные кислоты, но канифоль в спирте без дополнительных кислот по-прежнему продается для использования с лужеными деталями. (Согласно устаревшему стандарту MIL для флюса канифоль в спирте обозначается как «Тип R».)  Остаток безвреден (хотя кислота, содержащаяся в канифоли, может быть проблемой, но только в том случае, если используется неправильная сила флюса), но слишком часто неосведомленные люди интерпретируют его как признак плохой надежности. Операторы пайки часто тратят много времени и усилий на удаление видимой канифоли после пайки, что является пустой тратой ресурсов. «Очистка» щеткой или тряпкой и растворителем после ручной пайки мало что дала, за исключением того, что остатки флюса распределились по большей площади, что сделало их менее заметными.
Остаток безвреден (хотя кислота, содержащаяся в канифоли, может быть проблемой, но только в том случае, если используется неправильная сила флюса), но слишком часто неосведомленные люди интерпретируют его как признак плохой надежности. Операторы пайки часто тратят много времени и усилий на удаление видимой канифоли после пайки, что является пустой тратой ресурсов. «Очистка» щеткой или тряпкой и растворителем после ручной пайки мало что дала, за исключением того, что остатки флюса распределились по большей площади, что сделало их менее заметными.  для сегодняшней пайки. Темно-коричневый жидкий флюс не дает преимуществ, компенсирующих время и деньги, необходимые для удаления остатков после пайки. Сегодня большинство производителей флюсов предлагают жидкие канифольные флюсы с низким содержанием твердых частиц (менее 5% по объему), которые не оставляют значимого остатка.
для сегодняшней пайки. Темно-коричневый жидкий флюс не дает преимуществ, компенсирующих время и деньги, необходимые для удаления остатков после пайки. Сегодня большинство производителей флюсов предлагают жидкие канифольные флюсы с низким содержанием твердых частиц (менее 5% по объему), которые не оставляют значимого остатка.
Смола  На фундаментальном уровне нет существенной разницы между одним брендом и другим. Но замена твердых веществ материалом, отличным от канифоли, позволяет дифференцировать продукт и дает возможность несколько повысить цену и прибыль.
На фундаментальном уровне нет существенной разницы между одним брендом и другим. Но замена твердых веществ материалом, отличным от канифоли, позволяет дифференцировать продукт и дает возможность несколько повысить цену и прибыль. 
Водорастворимые твердые вещества (органический флюс) 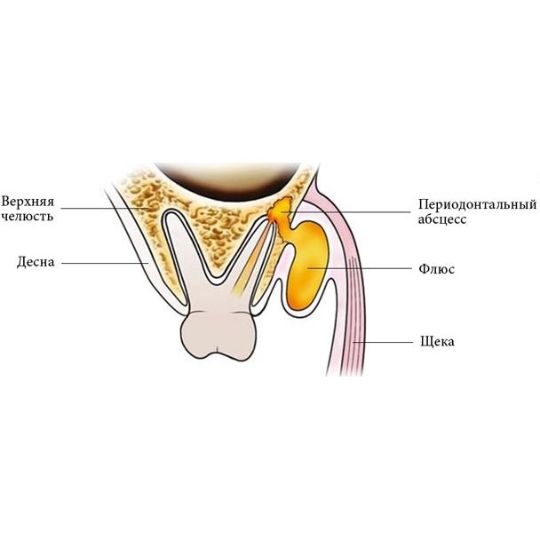
Растворители
 Ограничения по летучим органическим соединениям в некоторых регионах, особенно в некоторых частях Калифорнии, не позволяют использовать флюсы на спиртовой основе. Альтернативой спирту является вода, которая уступает спирту по четырем основным параметрам:
Ограничения по летучим органическим соединениям в некоторых регионах, особенно в некоторых частях Калифорнии, не позволяют использовать флюсы на спиртовой основе. Альтернативой спирту является вода, которая уступает спирту по четырем основным параметрам:
 Остатки многих флюсов на спиртовой основе (за исключением флюсов, содержащих канифоль и некоторые смолы) растворимы в воде.
Остатки многих флюсов на спиртовой основе (за исключением флюсов, содержащих канифоль и некоторые смолы) растворимы в воде.
Скоро  При 0°C нейтральный pH равен 7,4, тогда как нейтральный pH при 50°C равен 6,63.
При 0°C нейтральный pH равен 7,4, тогда как нейтральный pH при 50°C равен 6,63. Что такое флюс для припоя? | Основы пайки — основная информация о печатных платах
 358 просмотров
0 Комментарии
Опубликовано в
Основная информация о печатной плате
358 просмотров
0 Комментарии
Опубликовано в
Основная информация о печатной плате

 Конкретный используемый метод будет зависеть от типа флюса и имеющегося оборудования для очистки.
Конкретный используемый метод будет зависеть от типа флюса и имеющегося оборудования для очистки. 

