История болезни. Хронический гранулирующий периодонтит | Рефераты Терапевтическая стоматология
Скачай История болезни. Хронический гранулирующий периодонтит и больше Рефераты в PDF из Терапевтическая стоматология только в Docsity! 1 ЗАТВЕРДЖЕНО Наказ Міністерства охорони здоров’я України 14 лютого 2012 року № 110 Найменування міністерства, іншого органу виконавчої влади, підприємства, установи, організації, до сфери управління якого належить заклад охорони здоров’ Міністерство охорони здоров’я України МЕДИЧНА ДОКУМЕНТАЦІЯ Форма первинної облікової документації № 043/о Найменування та місцезнаходження (повна поштова адреса) закладу охорони здоров’я, де заповнюється форма Університетська клініка ЗДМУ ЗАТВЕРДЖЕНО Наказ МОЗ України Код за ЄДРПОУ 4 6 9 9 2 0 7 1 5 0 7 2 2 7 6 № 3 4 7 9 Медична карта стоматологічного хворого № 2134 2022 рік 1. Прізвище, ім’я, по батькові Клименко Юрій Олексійович 2. Стать: чоловіча – 1; жіноча – 2 1 3. Дата народження 2 8 0 3 9 6 (число, місяць, рік) 4. Місце проживання хворого, телефон м. Запоріжжя вул Перемоги 47 +380506856258 5. Діагноз Хронічний гранулюючий періодонтит 24 6. Скарги На затерплість зуба, скаржиться на тривалий біль, постійного характеру в ділянці зуба, який посилюється при пережовуванні їжі; неприємний запах з ротової порожнини при розмові. У ділянці кореня відчуває тяжкість і деяке розпирання, неодноразові загострення процесу із сильним болем, набряком, утворенням абсцесів і появою нориці з виділенням гною. 7. Перенесені та супутні захворювання На час звернення не має супутніх вірусних, бактеріальних та венеричних захворювань. Алергічний статус: алергічних реакцій хворий у себе не відмічає. 2 8. Розвиток теперішнього захворювання Перші скарги з’явилися місяць тому, по допомогу не звертався. Зуб 24 раніше лікований з приводу хронічного фіброзного пульпіту, девіталізований та запломбований 2 роки тому. За цей час ні разу не турбував, пацієнт відмічає що почав відчувати дискомфорт у зубі після тяжко перенесеної ангіни.
Місце проживання хворого, телефон м. Запоріжжя вул Перемоги 47 +380506856258 5. Діагноз Хронічний гранулюючий періодонтит 24 6. Скарги На затерплість зуба, скаржиться на тривалий біль, постійного характеру в ділянці зуба, який посилюється при пережовуванні їжі; неприємний запах з ротової порожнини при розмові. У ділянці кореня відчуває тяжкість і деяке розпирання, неодноразові загострення процесу із сильним болем, набряком, утворенням абсцесів і появою нориці з виділенням гною. 7. Перенесені та супутні захворювання На час звернення не має супутніх вірусних, бактеріальних та венеричних захворювань. Алергічний статус: алергічних реакцій хворий у себе не відмічає. 2 8. Розвиток теперішнього захворювання Перші скарги з’явилися місяць тому, по допомогу не звертався. Зуб 24 раніше лікований з приводу хронічного фіброзного пульпіту, девіталізований та запломбований 2 роки тому. За цей час ні разу не турбував, пацієнт відмічає що почав відчувати дискомфорт у зубі після тяжко перенесеної ангіни. В період ремісій зуб майже не непокоїв, лише при відкушуванні надто твердої їжі чи сильному натисканні. Продовження форми № 043/о 9. Дані об’єктивного дослідження, зовнішній огляд, стан зубів: Обличчя симетричне , пропорційне; носогубні складки згладжені; спостерігається носове дихання. Збільшені підщелепові лімфатичні вузли зліва , м’яко-еластичної консистенції, болючі при пальпації, шкірні покриви без елементів ураження та за кольором відповідають расовій приналежності. Пальпація СНЩС без патологічних змін. Locus morbi: Зуб 24 запломбовай, без візуальних дефектів пломбування,колір зубу змінений, тьмяний, без природнього блиску. Перехідна складка в області 24 зубу гіперемована із синюшним відтінком, виявляється симптом вазопарезу. В ділянці верхівки кореня виявляється постійна ясенна або шкірна нориця (фістула), з якої під час натискування виливається крапля гною. Зондування — безболісне. Перкусія вертикальна — дає больову реакцію; горизонтальна — безболісна, відчувається постукування, яке передається безпосередньо з коронки зуба на його корінь.
В період ремісій зуб майже не непокоїв, лише при відкушуванні надто твердої їжі чи сильному натисканні. Продовження форми № 043/о 9. Дані об’єктивного дослідження, зовнішній огляд, стан зубів: Обличчя симетричне , пропорційне; носогубні складки згладжені; спостерігається носове дихання. Збільшені підщелепові лімфатичні вузли зліва , м’яко-еластичної консистенції, болючі при пальпації, шкірні покриви без елементів ураження та за кольором відповідають расовій приналежності. Пальпація СНЩС без патологічних змін. Locus morbi: Зуб 24 запломбовай, без візуальних дефектів пломбування,колір зубу змінений, тьмяний, без природнього блиску. Перехідна складка в області 24 зубу гіперемована із синюшним відтінком, виявляється симптом вазопарезу. В ділянці верхівки кореня виявляється постійна ясенна або шкірна нориця (фістула), з якої під час натискування виливається крапля гною. Зондування — безболісне. Перкусія вертикальна — дає больову реакцію; горизонтальна — безболісна, відчувається постукування, яке передається безпосередньо з коронки зуба на його корінь. (феномен відведеного удару) Пальпація — виявляється набряк перехідної складки в області 24 зубу, проявляється симптом вазопарезу, пальпація в ділянці верхівки кореня 36 супроводжується больовими відчуттями. 5 4. Препарування та видалення пломби з порожнини зуба. Розкриття порожнини зуба та устя каналу 24. 5.Видалення пломбувальних матеріалів та путридних мас із кореневого каналу. 6. Інструментальне проходження та розширення кореневого каналу. Медикаментозне оброблення кореневого каналу розчином хлоргексидину 1%. 7.Розкриття верхівкового отвору. Проведення рентгенівського знімку для оцінки якості препарування к/к. 8.Введення протизапальних та регенеративних препаратів трансканально за апікальний отвір за допомогою кореневої голки. 9. Обтурація кореневого каналу гутаперчевим штифтом та силером на основі кальцію гідроксиду. Проведення контрольного рентгенівського знімку для оцінки якості пломбування к/к. 10.Накладання ізолюючої прокладки з світлотвердіючого СІЦ. 11. Відновлення та реставрація зуба 24 композитними пломбувальними матеріалами.
(феномен відведеного удару) Пальпація — виявляється набряк перехідної складки в області 24 зубу, проявляється симптом вазопарезу, пальпація в ділянці верхівки кореня 36 супроводжується больовими відчуттями. 5 4. Препарування та видалення пломби з порожнини зуба. Розкриття порожнини зуба та устя каналу 24. 5.Видалення пломбувальних матеріалів та путридних мас із кореневого каналу. 6. Інструментальне проходження та розширення кореневого каналу. Медикаментозне оброблення кореневого каналу розчином хлоргексидину 1%. 7.Розкриття верхівкового отвору. Проведення рентгенівського знімку для оцінки якості препарування к/к. 8.Введення протизапальних та регенеративних препаратів трансканально за апікальний отвір за допомогою кореневої голки. 9. Обтурація кореневого каналу гутаперчевим штифтом та силером на основі кальцію гідроксиду. Проведення контрольного рентгенівського знімку для оцінки якості пломбування к/к. 10.Накладання ізолюючої прокладки з світлотвердіючого СІЦ. 11. Відновлення та реставрація зуба 24 композитними пломбувальними матеріалами.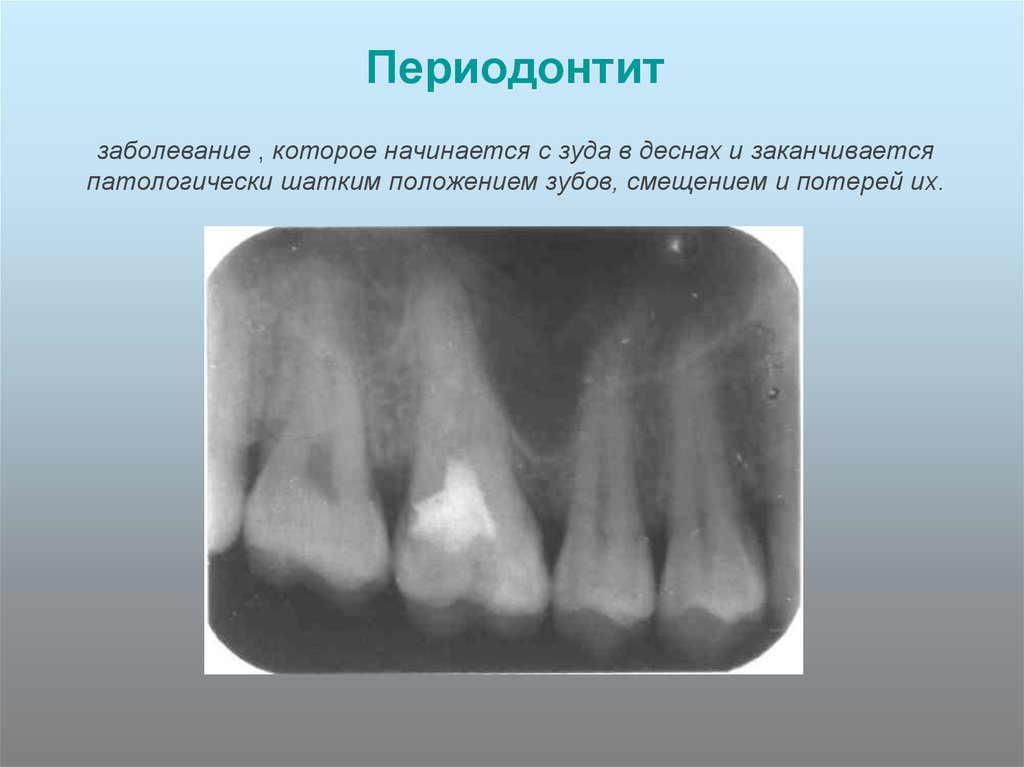 30.03.22р. У разі відсутності болю чи дискомфорту у зубі 36, для контролю якості лікування необхідно через 6 місяців відвідати стоматолога для проведення рентгенівського дослідження. Рекомендації — 2 рази на рік візит до стоматолога для планової гігієни порожнини рота. Прогноз лікування — сприятливий. Лікар Дранніков А.С. Дата заповнення “30” березня 2022р. 6 ДИФЕРЕНЦІЙНА ДІАГНОСТИКА 1. Хронічний гранулематозний періодонтит — у більшості випадків характеризується безсимптомним перебігом. 2. Гострий верхівковий періодонтит — характеризується бурно протікаючим і прогресуючим запаленням з наростаючою зміною одних симптомів іншими. Біль інтенсивного характеру, пульсуюча, із іррадіацією вздовж гілок трійничного нерва. 3. Гострий дифузний пульпіт — характеризується надто інтенсивним болем, не постійного характеру із «світлими» проміжками; тривалий біль після усунення дії подразника із іррадіацією вздовж гілок трійничного нерва; перкусія слабо позитивна; болюче зондування по дну каріозної порожнини.
30.03.22р. У разі відсутності болю чи дискомфорту у зубі 36, для контролю якості лікування необхідно через 6 місяців відвідати стоматолога для проведення рентгенівського дослідження. Рекомендації — 2 рази на рік візит до стоматолога для планової гігієни порожнини рота. Прогноз лікування — сприятливий. Лікар Дранніков А.С. Дата заповнення “30” березня 2022р. 6 ДИФЕРЕНЦІЙНА ДІАГНОСТИКА 1. Хронічний гранулематозний періодонтит — у більшості випадків характеризується безсимптомним перебігом. 2. Гострий верхівковий періодонтит — характеризується бурно протікаючим і прогресуючим запаленням з наростаючою зміною одних симптомів іншими. Біль інтенсивного характеру, пульсуюча, із іррадіацією вздовж гілок трійничного нерва. 3. Гострий дифузний пульпіт — характеризується надто інтенсивним болем, не постійного характеру із «світлими» проміжками; тривалий біль після усунення дії подразника із іррадіацією вздовж гілок трійничного нерва; перкусія слабо позитивна; болюче зондування по дну каріозної порожнини. 4. Хронічний гангренозний пульпіт — біль виникає від всіх видів подразників,особливо від гарячого, не перестає після їх усунення.Хворий вказує на інтенсивні болі в минулому, які з часом стихли.Перкусія негативна; ЕОД = 50-70 мкА.
4. Хронічний гангренозний пульпіт — біль виникає від всіх видів подразників,особливо від гарячого, не перестає після їх усунення.Хворий вказує на інтенсивні болі в минулому, які з часом стихли.Перкусія негативна; ЕОД = 50-70 мкА.
Гранулирующий периодонтит (хронический, острый): симптомы, лечение
Сохраняем прежние цены! Забронировать цену
Москва, ул. Большая Спасская, 10к1
Комсомольская Сухаревская Проспект Мира
+7 (495) 125-25-20
Время работы: понедельник — суббота с 10:00 до 21:00
- Клиника
-
- Услуги
- Имплантация
- Ортодонт
- Цены
- Врачи
- % АКЦИЯ %
- Наши работы
- Видео
- Контакты
- org/» typeof=»BreadcrumbList»>
- •
- FAQ (Часто задаваемые вопросы)
- •
- Болезни зубов
Технологии лечения зубов, предлагаемые стоматологией в Москве, быстро совершенствуются. Специалисты научились эффективно и безболезненно избавлять пациентов даже от таких сложных хронических заболеваний, как гранулирующий периодонтит.
ПРИЧИНЫ И ОПИСАНИЕ ПАТОЛОГИИ
Заболевание вызывают болезнетворные бактерии, поражающие периодонт — волокнистую ткань с плотной сетью капилляров и нервных окончаний, расположенную между цементом корня и альвеолой. Заражение происходит как осложнение глубокого кариеса, когда патологические микроорганизмы достигают сначала пульпы, а затем периодонта. В очагах разрушения костной ткани и постоянного воспаления начинает формироваться и быстро разрастаться патологическая грануляционная ткань.
Еще одной причиной может быть неквалифицированное пломбирование корневых каналов, попадание в ткань периодонта агрессивных материалов и паст, стимулирующих рост колоний анаэробных бактерий.
СИМПТОМЫ ЗАБОЛЕВАНИЯ
Проявляет себя гранулирующий периодонтит периодическими тупыми болями в области десен: больно надкусывать твердые продукты, жевать. При простукивании также появляется характерная боль. Пораженный зуб становится подвижным. В отличие от пульпита, нет выраженных реакций на горячее/холодное, спонтанных ночных болей.
Характерные признаки заболевания в стадии обострения — гиперемия слизистой, отечность, свищи с гнойными выделениями, неприятный запах, симптомы общей интоксикации (головная боль, слабость, увеличение лимфоузлов).
Если не начать лечение, количество грануляций увеличивается, они быстро растут, выходят на поверхность и превращаются в свищи, через открытые каналы которых происходит повторное заражение микроорганизмами, болезнь принимает затяжную форму.
ДИАГНОСТИКА ГРАНУЛИРУЮЩЕГО ПЕРИОДОНТИТА
Основной признак гранулирующего периодонтита — подкожные гранулемы или свищи, однако заболевание может протекать и без видимых изменений. Инструментально патологию можно обнаружить с помощью зонда и оценки электрочувствительности. Наблюдается изменение порога возбудимости, незначительные болезненные ощущения в районе вертикальной перкуссии.
В ответ на нажатие зондом слизистая десны сначала бледнеет, затем интенсивно краснеет. Отличить заболевание от пульпита можно по оттенку коронки — она становится сероватой, а при пульпите сохраняет нормальный цвет. Чтобы дифференцировать заболевание от гранулематозной формы периодонтита, назначают рентгеновское исследование.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА И РЕНТГЕНОГРАММА
Рентгенография помогает уточнить диагноз, установить причины патологии и разработать тактику терапии. На снимке четко визуализируется деформация щели между цементом корня и альвеолой. В зоне апекса корня видны области разрушения или разрежения костных тканей, края пластины теряют ясность контуров, область поражения характеризуется неправильной «изъеденной» формой без четких границ.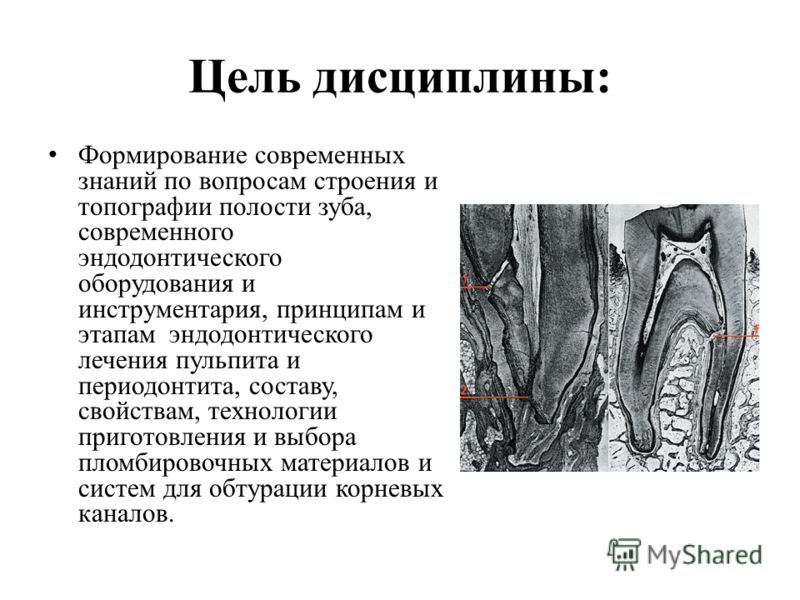 При гранулематозной форме заболевания на снимке просматривается правильная округлая форма очага разрушения кости с четкими линиями границ.
При гранулематозной форме заболевания на снимке просматривается правильная округлая форма очага разрушения кости с четкими линиями границ.
ЛЕЧЕНИЕ ГРАНУЛИРУЮЩЕГО ПЕРИОДОНТИТА
Основной метод восстановления очагов деструкции — заапикальная терапия, когда в периапикальные ткани вводят препараты, ускоряющие регенерацию. Делают это после глубокой санации канала, чтобы исключить вымывание болезненных организмов вместе с лечебным раствором.
Активные вещества в препаратах — лизоцим, витамины А и Е, гепарин, метилурацил, фуразолидон. Также в комплексную терапию входят пасты с иммуномодулирующими свойствами, например, на основе тимогена и гидрокортизона. Их задача — повысить иммунный статус тканей, исключить повторные воспаления. Длительность и стоимость лечения в стоматологии Москвы зависят от степени поражения периодонта, давности и формы заболевания, состояния иммунитета.
ПРОФИЛАКТИКА
Главное в профилактике гранулирующего периодонтита — гигиена и регулярные посещения стоматолога. Необходима тщательная чистка зубов и межзубных промежутков, важно правильно подбирать щетку и нить, чтобы не травмировать десны. Обязательны гигиенические процедуры в клинике хотя бы раз в год, удаление камней и налета. Для стоматологического лечения выбирайте клинику с хорошей репутацией и современным оснащением.
Необходима тщательная чистка зубов и межзубных промежутков, важно правильно подбирать щетку и нить, чтобы не травмировать десны. Обязательны гигиенические процедуры в клинике хотя бы раз в год, удаление камней и налета. Для стоматологического лечения выбирайте клинику с хорошей репутацией и современным оснащением.
Услуги стоматологии
О нашей клинике на других площадках
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Читать отзывыНаписать отзыв
Введите ваше имя*
Дата посещения клинники ЯнварьФевральМартАпрельМайИюньИюльАвгустСентябрьОктябрьНоябрьДекабрь20192018201720162015
Ваша оценка ОтличноХорошоНормальноПлохоОчень плохо
Введите ваш отзыв*
Написать в WhatsAppЛечение периодонтита, симптомы — Статьи
Автор:
Marbery Gedrean
| Проверил: Штеба Виктория Петровна
| Последняя редакция: 01 декабря 2020.
Периодонтит – одно из самых частых заболеваний в стоматологии. Он представляет собой воспаление корня и тканей, которые его окружают (периодонта). Болезнь имеет такие яркие симптомы, как неприятный запах изо рта и кровоточащие десна. Ни в коем случае нельзя недооценивать это заболевание, разрушая корень, периодонтит неизменно ведет к потере зуба. Как и многие болезни периодонта, он возникает на фоне недолеченного или невылеченного пульпита. После отмирания пульпы инфекция перемещается по каналам и попадает в ткани.
Формы периодонтита
Существует несколько признаков, по которым разделяют заболевание на виды:
• причина возникновения
• симптомы периодонтита
• степень сложности
Учитывая происхождение и причину появления в ротовой полости, выделяют такие виды периодонтита:
1. инфекционный: появляется вследствие плохого лечения зубов, после лечения воспаления нерва;
2. травматический: возникает после получения разного рода травмы и повреждения зуба, также причиной может быть травма, нанесенная стоматологом во время процедуры установки протезов;
3. медикаментозный: начинается как аллергическая реакция на материал, который использовался при пломбировании каналов, а также из-за применения сильнодействующих антисептических средств.
медикаментозный: начинается как аллергическая реакция на материал, который использовался при пломбировании каналов, а также из-за применения сильнодействующих антисептических средств.
Наблюдая за тем, как протекает заболевание, анализируя симптомы периодонтита зубов и характер протекания болезни, выделяют:
1. острый периодонтит: возникает резко, без предпосылок, протекает очень болезненно, особенно боли сильны при надавливании на пораженную часть ротовой полости, иногда наблюдается появление свищей;
2. хроническая форма: может возникнуть как следствие острого состояния, если не проводить никакого лечения, симптомами хронического состояния считают увеличенную подвижность зубов, возникновение щели между зубами, воспаление десен. Такая болезнь протекает медленно, с возможными рецидивами. Часто невозможно заметить явные симптомы и точно определяется такой периодонтит на рентгене. В свою очередь хронический периодонтит имеет три вида: фиброзную, гранулематозную и гранулирующую.
В зависимости от степени нанесенного болезнью урона, выделяют:
1. легкую форму: ткань, расположенная вокруг зуба поражена на 4 миллиметра, никаких изменений костного характера нет, наблюдается небольшая кровоточивость и дискомфорт при жевании;
2. среднюю: болезнь проникла глубже, а именно достигла 6 миллиметров, немного оголились корни, наблюдается подвижность зубов, десны воспаляются;
3. тяжелую: глубина проникновения болезни – 9 миллиметров, наблюдаются симптомы в комплексе, добавляются гнойные выделения.
Симптомы периодонтита
Сразу надо отметить, что диагностика периодонтита проводится, прежде всего, стоматологом. Не нужно заниматься самолечением. Обнаружив один из симптомов, которые перечислены ниже, обратитесь к врачу. Только так у вас будет гарантия правильного лечения заболевания периодонта.
Симптомы и лечение периодонтита отличаются в зависимости от того, с каким видом заболевания мы имеем дело:
• если заболевание протекает в острой форме, то обязательно будет наличие болевых ощущений при давлении на зуб; болеть может и пораженный зуб, и те, которые растут рядом и напротив; боли усиливаются при употреблении холодных и горячих продуктов. Вследствие воспалительного процесса наблюдается увеличение ткани десны, а также ощущается дискомфорт при смыкании зубов. Если не предпринимать никаких действий, то в дальнейшем боли усиливаются, приобретают пульсирующий характер, отекают губы и щека, повышается температура тела. Не обратившись за помощью к врачу, вы рискуете перенести болезнь в хроническую стадию.
Вследствие воспалительного процесса наблюдается увеличение ткани десны, а также ощущается дискомфорт при смыкании зубов. Если не предпринимать никаких действий, то в дальнейшем боли усиливаются, приобретают пульсирующий характер, отекают губы и щека, повышается температура тела. Не обратившись за помощью к врачу, вы рискуете перенести болезнь в хроническую стадию.
• хронический периодонтит может находиться в стадии покоя или ремиссии и в стадии обострения. В спокойной стадии болезнь не имеет ярко выраженных симптомов, присутствуют ноющие боли, которые усиливаются при надавливании на зуб, иногда можно наблюдать появление свища с гнойными накоплениями. В острой стадии симптомы усиливаются, зубы сильно шатаются, и чем дальше, тем сильней. Увеличиваются промежутки между зубами, появляются покраснения и отеки, повышается температура тела. Часто это приводит к образованию кисты, которую удаляют только вместе с зубом.
Острые формы: лечение
Болезненные ощущения при остром периодонтите направляют пациента в стоматологию. Чтобы правильно проводить лечение болезни нужно определить степень заболевания. Для начала делается рентген. Увидеть периодонтит на снимке сможет любой стоматолог, изучивший строение периодонта в университете. Присутствие темного пятна на корне указывает на присутствие болезни, а осмотр ротовой полости покажет степень прогресса.
Чтобы правильно проводить лечение болезни нужно определить степень заболевания. Для начала делается рентген. Увидеть периодонтит на снимке сможет любой стоматолог, изучивший строение периодонта в университете. Присутствие темного пятна на корне указывает на присутствие болезни, а осмотр ротовой полости покажет степень прогресса.
Все виды периодонтитов лечатся двумя способами:
• терапевтическим
• хирургическим
Проводя терапию, врач:
1. вскрывает каналы зуба
2. удаляет нерв
3. тщательно чистит каналы
4. обрабатывает каналы антисептиком
5. не закрывая каналы, проводит лечение тканей вокруг пораженного корня (возможно, придется посетить врача несколько раз)
6. после окончания лечения тканей, зуб хорошо очищается, в него помещается лекарство, которое снимает воспаление
7. ставится временная пломба на неделю
8. если боль продолжает беспокоить, то процедуру проводят еще раз
9. если боли прекратились, то при очередном посещении врач ставит постоянную пломбу, предварительно закрыв корневые каналы.
Хирургический метод сводится к тому, что на десне делается разрез, через который удаляется часть корня вместе с гнойным образованием, а затем место воспаления обрабатывают специальным лекарством.
Метод лечения требует применение антибиотиков. Применение такого препарата, как Бисептол при периодонтите – довольно частое явление. Но есть и другие лекарства. Также добавляют комплекс витаминов для укрепления иммунитета.
Хронические формы периодонтита
Хронические виды болезни имеют свои особенности:
• гранулирующий периодонтит – воспалительный процесс тканей, который сопровождается появлением свищей. Это болезненное состояние и может сопровождаться отеком. Необходимо увидеть гранулематозный периодонтит на рентгене, чтобы правильно проводить лечение.
• гранулематозный периодонтит – процесс, когда в ткани десны наблюдается образование новой структуры. В отличие от гранулирующего периодонтита, этот протекает спокойней. Возможно образование таких структур, как гранулема, киста и кистогранулема. Они снижают всасываемость и проникание микробов в ткани зуба путем блокировки их.
Они снижают всасываемость и проникание микробов в ткани зуба путем блокировки их.
• фиброзный периодонтит – такой вид болезни часто появляется как последствия лечения гранулирующего или гранулематозного. Некоторые стоматологи не считают этот вид формой болезни, ведь при нем нет изменений корня. Но если воспаленная ткань приобретает фиброзную структуру, есть риск, что в будущем это приведет к образованию гранулем. Симптомов у этой болезни практически не существует. Но профессиональный врач увидит цветовое изменение зуба, мягкую структуру дентина, увеличение межзубных щелей, и назначит своевременное и правильное лечение.
Периодонтит: качественное лечение в Харькове
Периодонтит: симптомы, опасность, лечение в Харькове
В этой статье квалифицированные специалисты ведущей стоматологии Харькова Leo Dent расскажут про периодонтит и лечение, предстоящее пациентам с таким диагнозом.
Почему нужно своевременно обследоваться у стоматолога и сразу решать возникшие проблемы с зубами либо деснами — об этом и много другом вы узнаете, прочитав данную статью.
Также здесь читатели смогут ознакомиться с дифференциальной диагностикой периодонтита по таблице.
Характеристика периодонтита
Прежде чем раскрыть нюансы лечения периодонтита зубов, хотелось бы остановиться на заболевании как таковом. Периодонтит — это воспаление соединительной ткани (периодонта), находящейся непосредственно между зубным корнем и альвеолой.
С одной стороны по некоторым качествам периодонтит схож с пародонтитом и пародонтозом, в том числе и по созвучному названию, поэтому их часто путают. С другой — заболевание не имеет отношения к тканям десны, а посему и сравнивать его с пародонтозом нелогично. Поставить единственно верный диагноз способен врач, как и назначить правильное лечение.
Заниматься самолечением при периодонтите нежелательно. Лучше всего — согласовывать каждый свой шаг, направленный на снятие воспаления внутри зуба, с лечащим стоматологом. В ином случае риск потерять зуб повышается в разы.
Действия зубного врача для постановки диагноза «периодонтит»:
- Первым делом стоматолог выслушивает жалобы пациента и потом приступает к первичному осмотру.

- После обнаружения больного зуба доктор назначает рентгенографию, которая позволит распознать причину появившихся неприятных симптомов.
- Последний этап — изучение и анализ рентгенологического снимка и назначение курса лечения.
К слову, когда начинается обострение хронического периодонтита, история болезни нередко завершается удалением зуба. Особенно, если сегмент уже довольно подвижен. О том, что зуб невозможно спасти, врач оповестит пациента сразу, потому как в дальнейшем лечение хронического периодонтита в стадии обострения не принесет желаемого результата.
Кто в группе риска
По статистике, от воспалительных заболеваний зубов и десен страдают чаще мужчины, нежели женщины. Исключения бывают, но мы рекомендуем полноценно ухаживать за зубами, чтобы не попасть на прием к стоматологу с острой невыносимой болью.
Что тут говорить, лечение периодонтитов молочных зубов у детей — довольно обычная и распространенная процедура. Дети до конца не осознают, насколько важно тщательно чистить зубы, а это приводит к развитию кариеса. Как следствие, развивается воспаление внутри одного или сразу в нескольких зубах, именуемое периодонтитом.
Как следствие, развивается воспаление внутри одного или сразу в нескольких зубах, именуемое периодонтитом.
Каким может быть периодонтит
Классифицируется периодонтит по острой и хронической форме. Соответственно, острый периодонтит возникает спонтанно и такую боль способен выдержать далеко не каждый.
Хроническая форма болезни может существовать долгие годы либо, наоборот, привести к подвижности и скоропостижной потере зубов. Допустим, гнойный периодонтит считается острым, а фиброзный периодонтит — хроническим.
Из-за множества причин возникновения делят периодонтит на виды:
- Медикаментозный — когда в ткани зуба попадает лекарство, например мышьяк либо фенол.
- Травматический — результат механического повреждения коронки и корня зуба.
- Инфекционный — выступает в роли осложнения после не вылеченного кариеса.
- Ятрогенный — возникает по причине некачественной пломбировки корневых каналов.
Чаще всего современные стоматологи сталкиваются с острым апикальным периодонтитом, который характеризуется невыносимой пульсирующей болью. И, чем отчетливее становятся болевые эффекты, тем больше риск того, что начался гнойный процесс.
И, чем отчетливее становятся болевые эффекты, тем больше риск того, что начался гнойный процесс.
Признаки периодонтита, которые нельзя игнорировать
Острая форма периодонтита, как правило, проявляется таким образом:
- сильный болевой эффект в области пострадавшего зуба;
- если надавить на зуб, то он начинает болеть еще больше;
- запах изо рта приобретает гнилостный оттенок;
- со временем боль может стать пульсирующей, на время утихать и потом снова возобновляться;
- большинству пациентов с периодонтитом кажется, что больной зуб выдвинулся вперед, хотя на самом деле это не так.
Обострение хронического периодонтита у детей и взрослых не так выражено, как в ситуации с острой формой. Но все-таки умеренные болезненные ощущения имеют место. К болям присоединяется повышенная чувствительность перед горячими продуктами и напитками.
Перечисленные симптомы должны стать первой причиной того, что человек пойдет к стоматологу в ближайшее время. Не стоит полагаться на эффективность обезболивающих препаратов, ведь во многих случаях она предельно низкая.
Не стоит полагаться на эффективность обезболивающих препаратов, ведь во многих случаях она предельно низкая.
Провоцирующие факторы для развития периодонтита
Наиболее частыми причинами воспаления периодонта являются:
- кариес и отсутствие его лечения;
- курение;
- не до конца вылеченный пульпит;
- сердечно-сосудистые заболевания;
- попадание в мягкие ткани зуба патогенных микроорганизмов;
- установка некачественной пломбы, которая все время оказывает давление на зуб и может его травмировать;
- некоторые лекарственные препараты, попадая внутрь зуба, приводят к медикаментозному периодонтиту;
- гайморит и остеомиелит могут спровоцировать проникновение инфекции в полость зуба;
- ослабленный иммунитет.
Традиционные и народные способы лечения периодонтита
В том случае, когда воспаление в тканях зуба спровоцировано бактериями, лечат периодонтит антибиотиками. Обострение хронического периодонтита предусматривает лечение подобно тому, что и в острой форме, правда, отличительные нюансы тоже имеются.
Включает в себя лечение хронического периодонтита следующие этапы:
- Механическое расширение каналов и их очистка.
- Ультразвуковая чистка зубов и снятие зубного камня.
- Пломбирование корневых каналов, если имеется такая необходимость.
Лечение хронического верхушечного, фиброзного, гранулирующего либо гранулематозного периодонтитов выполняется практически по одному и тому же протоколу. Тоже самое касается и маргинального периодонтита и лечения. Главное — довериться профессионалам и четко соблюдать их рекомендации.
Сколько болит зуб после лечения периодонтита? Дать точный ответ на этот вопрос не в состоянии даже стоматолог со стажем. Все зависит от возраста пациента, чувствительности и порога болевых ощущений. Обычно, болезненность может присутствовать еще 7-14 дней после вмешательства со стороны доктора. И эти боли имеют ноющий и ослабленный характер.
Из нетрадиционных способов лечения периодонтита выделим следующие:
- полоскания ротовой полости солевым раствором с содой;
- прием витаминов и употребление продуктов, обогащенных кальцием и железом;
- шалфеевый настой прекрасно справляется с задачей «снять воспаление» в деснах и зубах;
- аппликация из кусочка прополиса утихомирит разбушевавшийся нерв и избавит вас от боли.

Возможно ли предупредить периодонтит
На периодонтит цена лечения не так уж и низка, чтобы можно было махнуть рукой. К тому же, при этом недуге зуб постоянно болит, расшатывается и может в любой момент выпасть.
Дабы избежать подобной болезни и сохранить целостность зубного ряда, старайтесь:
- регулярно чистить зубы пастами с фтором;
- не допускать развития кариеса, а если это произошло уже, тогда следует немедленно приступить к его лечению;
- не реже двух раз в год делать профессиональную чистку зубов, избавляющую их поверхности от твердых каменистых отложений;
- употреблять больше растительных продуктов, нежели содержащих углеводы и сахарозу, так как они способствуют накоплению налета на зубах и образованию камней.
Также присутствовать в арсенале средств по уходу за зубами должны флосс и ирригатор.
Обязательно обращаться к стоматологу не только тогда, когда невыносимо разболелся зуб, но и просто так в целях профилактики различных заболеваний.
В какой стоматологии Харькова можно быстро вылечить периодонтит
Предлагаем обратиться к профессиональным специалистам, работающим порядка пятнадцати лет в стоматологии «Leo Dent». Клиника расположена в здании универмага «Харьков», который построен вблизи со станцией метро «Защитников Украины».
Наши врачи изо дня в день подтверждают высокий уровень квалификации. В клинике предоставляется широкий спектр услуг по доступным ценам. На все процедуры мы даем гарантии, а качество материалов подтверждаем сертификатами.
Записаться на прием к профильному специалисту или бесплатно проконсультироваться можно по телефонам, указанным ниже:
095-5-101-101 Viber
098-5-101-101
073-5-101-101
Дополнительные преимущества обслуживания в «Leo Dent»:
- Стоматология оснащена высокотехнологичным оборудованием.
- Имеется собственная техническая лаборатория, где производятся по индивидуальным заказам ортопедические протезы.
- Как при одноразовом посещении, так и в процессе лечения хронического периодонтита, история болезни каждого пациента заполняется строго по протоколу.

- Мы создали комфортную обстановку во всех кабинетах, поэтому наши клиенты, в том числе и самые маленькие, чувствуют себя в безопасности.
- Тех, кто безоговорочно доверяет нам уход за ротовой полостью, ждут скидки.
- Новым клиентам мы предлагаем акции на некоторые процедуры, за счет чего их стоимость существенно снижается.
- Наши стоматологи постоянно совершенствуют свои знания и навыки, а потому даже в самой запущенной ситуации в плане здоровья зубов и десен находят оптимальный выход.
Приходите в «Leo Dent» и вы не пожалеете! Мы докажем, что белоснежная улыбка — это не заоблачная роскошь, а реальность!
подкрался незаметно, оставил без зуба
- Главная
-
Пациентам
-
Статьи
-
Коварный периодонтит: подкрался незаметно, оставил без зуба
Периодонтит – следующий этап воспаления после пульпита. Инфекция локализуется на верхушке корня зуба и окружающих ее тканях. Болезнь часто протекает бессимптомно, но без своевременной помощи приводит к потере зуба.
Болезнь часто протекает бессимптомно, но без своевременной помощи приводит к потере зуба.
Причины:
- Вовремя не вылеченный пульпит. Если зуб болел, а потом перестал, значит, воспаление перешло в хроническую стадию. Хронический пульпит будет медленно распространяться по зубу и превратится в периоднонтит.
- Пульпит, леченый по устаревшим методикам. До появления апекс-локатора измерить длину корневого канала было нечем, и врач действовал вслепую. Если канал пролечен не полностью, и в нем остались частички инфицированной пульпы, возникают осложнения. Чтобы этого избежать, врач мог перестараться и вывести стоматологический материал за пределы верхушки корня. Вокруг комочка пасты иногда с годами развивается очаг инфекции.
-
Травма зуба. Частая проблема у активных детей. Вследствие травмы (часто страдают резцы), пульпа гибнет, и вслед за этим развивается периодонтит. По сути, причина — тот же не замеченный и не вылеченный вовремя пульпит.

Виды периодонтита
| Форма | Вид | Как болит |
|---|---|---|
| Острый | Серозный | Легкие ноющие боли в области зуба. |
| Гнойный | Пульсирующая боль. Может усилиться подвижность зуба. Возможна припухлость щеки, слабость, температура, флюс. | |
| Хронический | Фиброзный | Без симптомов или небольшое потемнение, тусклый цвет коронковой части зуба. |
| Гранулирующий | Легкая болезненность при накусывании со временем переходит в боль от горячего, при жевании, при давлении. Десна краснеет и опухает. | |
| Гранулематозный | Отсутствие симптомов. Появляется свищ для оттока отделяемого, но пациент не всегда может его увидеть. |
Самым агрессивным считается гранулирующий периодонтит, который очень быстро распространяется на соседние ткани. При таком диагнозе чаще всего зуб не удается сохранить.
При гранулематозной разновидности болезни у очага воспаления есть твердая оболочка, а внутри она заполнена гноем. В зависимости от размера эти новообразования называют гранулемой (до 5 мм), кистогранулемой или радикулярной кистой (более 1 см).
Таким образом, гранулема и киста корня зуба – это проявления хронического периодонтита.
Диагностика
Не путайте свищ со стоматитом. Свищ похож на прыщик, расположен на десне около корней зуба, не болит при надавливании. При появлении свища скорее обратитесь к стоматологу.
Заподозрить проблему до образования свища или флюса врач может по жалобам. Очень важно, чтобы пациент описывал все симптомы, не стеснялся жаловаться на слабую, невыраженную, изредка появляющуюся боль и дискомфорт.
Точно установить диагноз помогает рентген. Периодонтит виден даже на маленьком прицельном снимке. Далее для планирования лечения стоматолог предложит сделать панорамный снимок (все зубы на одном кадре) или компьютерную томограмму (трехмерное изображение зубочелюстной системы).
КТ — компьютерная 3D томограмма
позволяет увидеть вид периодонтита, локализацию и размер кистогранулемы, дать прогноз лечения.
Положительная динамика
видна на повтороной томограмме спустя 2 года
Со всех сторон
преимущество КТ — возможность рассмотреть зуб и ткани вокруг него с разных ракурсов
Лечение
В зависимости от стадии и формы болезни доктор подберет оптимальный метод.
1. Терапевтическое лечение. Как правило, требуется три посещения стоматологического кабинета.
- Неотложная помощь. Стоматолог удалит очаг воспаления: проведет очистку и дезинфекцию каналов с помощью лекарств и стерилизации лазером. При необходимости врач установит дренаж для оттока гноя.

- Лечение каналов зуба и установка временной пломбы. Если есть сомнения, что иммунитет справится с оставшимися микроорганизмами, стоматолог может назначить прием антибиотиков, физиотерапию, полоскания и лечебные ванночки.
- Реставрация зуба. На последнем визите стоматолог сделает рентгеновский снимок, чтобы убедиться, что очаг воспаления удален. После этого можно приступать к пломбированию и восстановлению эстетики и жевательной функции зуба.
- Наблюдение. О положительной динамике тканей, окружающих зуб, можно говорить через 1-2 года по результатам рентгенологического исследования.
2. Зубосохраняющие операции. Иногда консервативных методов недостаточно. Стоматолог-хирург может провести цистэктомию (удаление кисты) или резекцию верхушки корня (отсечение части зуба вместе с кистой).
3. Удаление зуба. В запущенных стадиях полностью победить очаги инфекции не получится. Попытки спасти зуб приведут к большим финансовым тратам и поставят под угрозу соседние зубы. Наилучшим решением будет установить на месте пораженного зуба имплантат.
Наилучшим решением будет установить на месте пораженного зуба имплантат.
Если оставить зуб без лечения, его ждет преждевременное удаление. Воспаление будет разрастаться и перейдет в острую стадию, причем в самый неудачный момент.
Хронический периодонтит врачи называют бомбой замедленного действия. Обострение провоцируется стрессами, нагрузками, переохлаждением или сменой климата. То есть, оно случится в долгожданной поездке на море, во время работы над важным проектом, перед экзаменом или при инфекционной болезни.
Периодонтит у детей
У ребенка воспаление периодонта может развиться как на молочных, так и на постоянных зубах. Особенности детского периодонтита:
- высокая скорость протекания,
- выраженная симптоматика (температура, боль, отек, возможны нагноения),
- повышенный риск осложнений. Если не принять срочные меры, пострадают зачатки постоянных зубов.
Лечение проходит по той же схеме, что и у взрослых. Если до выпадения молочного зуба осталось меньше года или корни уже рассосались, детский стоматолог предложит удалить зуб.
Если до выпадения молочного зуба осталось меньше года или корни уже рассосались, детский стоматолог предложит удалить зуб.
Профилактика
Простые и не затратные меры позволят снизить риски появления периодонтита и потери зуба.
- Соблюдайте гигиену полости рта.
- Правильно питайтесь. Избыток углеводной пищи провоцирует развитие патогенных микроорганизмов.
- Своевременно обращайтесь к специалисту для лечения зубов. Приходите на плановый осмотр раз в полгода, даже если ничего не болит. Озвучивайте все жалобы.
- С пониманием относитесь к предложению доктора пройти панорамную рентгенографию или компьютерную томографию. Полная информация позволит заметить и вылечить болезнь.
За экспертную помощь в написании статьи и предоставленные примеры работ благодарим стоматолога-терапевта Юрьеву Ольгу Юрьевну.
Роль фокальных очагов инфекции в возникновении и поддержании воспалительных заболеваний глаз
История вопроса
С древних времен считалось, что заболевания зубов и полости рта могут оказывать пагубное влияние на различные системы тела человека. Так, в Ниневии, столице Древней Ассирии, при раскопках была найдена табличка, автор текста которой, врач при дворе царя Ашурбанипала, писал: «Причина болей в его голове, руках и ногах — его зубы, которые следует удалить». В одном из вавилонских талмудов имеется запись, описывающая взаимосвязь между заболеваниями ротовой полости и глаз и предостерегающая от удаления «глазного зуба», так как может пострадать глаз. В иудейской книге «Sefer ha-Olamot o Ma’aseh Toviya» (Книга о Мирах) тело человека представлено как дом, а полость рта — как входная дверь, которая должна содержаться в чистоте для предотвращения попадания инфекции в человеческий организм.
Так, в Ниневии, столице Древней Ассирии, при раскопках была найдена табличка, автор текста которой, врач при дворе царя Ашурбанипала, писал: «Причина болей в его голове, руках и ногах — его зубы, которые следует удалить». В одном из вавилонских талмудов имеется запись, описывающая взаимосвязь между заболеваниями ротовой полости и глаз и предостерегающая от удаления «глазного зуба», так как может пострадать глаз. В иудейской книге «Sefer ha-Olamot o Ma’aseh Toviya» (Книга о Мирах) тело человека представлено как дом, а полость рта — как входная дверь, которая должна содержаться в чистоте для предотвращения попадания инфекции в человеческий организм.
В XVI в. W. Ryff написал медицинский трактат, посвященный стоматологическим заболеваниям «Полезные инструкции о том, как сохранить здоровье, силу и ясность глаз», где сказано, что глаза и зубы обладают «необычайно тесной взаимосвязью, по причине которой с легкостью способны передавать друг другу различные заболевания и нарушения, так что пока один из этих органов не является полностью здоровым, второй будет также поражен».
T. Berdmore в 1768 г. описывал влияние пораженных зубов на организм в целом как «опасный воспалительный процесс, охватывающий соседние структуры и поражающий организм симпатическим путем или проникновением инфекции в кровеносное русло». В разные времена врачи разных народов и государств отмечали важность гигиены полости рта и считали, что болезни зубов являются источниками многих патологий [1]. L. Cahn сообщил о записях F. Hildanus (XVI в.), в которых был зарегистрирован случай потери зрения вследствие абсцесса зуба, а V. Richter (XVIII в.) привел описание пациентки, страдавшей рецидивирующим кератитом в течение нескольких лет, зрение которой восстановилось после экстракции пораженного зуба [2].
C. Jones описал клинический случай пациента 16 лет, у которого развилось паренхиматозное воспаление роговиц обоих глаз. Несмотря на шесть месяцев активного антисифилитического и другого противовоспалительного лечения, кератит прогрессировал до состояния, когда обе роговицы стали полностью непрозрачными. При этом васкуляризации роговиц не отмечалось. Лишь спустя 9 мес после начала болезни у него были выявлены и удалены 9 зубов с апикальными абсцессами, а также была произведена тонзиллэктомия инфицированных миндалин. Посевы гнойного содержимого из миндалин и апикальных абсцессов выявили рост одного и того же микроорганизма — гемолитического стрептококка. Впервые за все время болезни, уже спустя 48 ч после санации очагов фокальной инфекции, состояние обоих глаз улучшилось — уменьшились мучительная фотофобия, гиперемия и резорбция инфильтрации обеих роговиц. Острота зрения стала уверенно расти и в итоге повысилась в правильной светопроекции до 1,0 в течение последующих 8 мес. При этом прозрачность обеих роговиц полностью восстановилась, за исключением помутнения верхненаружного квадранта роговицы правого глаза [3].
При этом васкуляризации роговиц не отмечалось. Лишь спустя 9 мес после начала болезни у него были выявлены и удалены 9 зубов с апикальными абсцессами, а также была произведена тонзиллэктомия инфицированных миндалин. Посевы гнойного содержимого из миндалин и апикальных абсцессов выявили рост одного и того же микроорганизма — гемолитического стрептококка. Впервые за все время болезни, уже спустя 48 ч после санации очагов фокальной инфекции, состояние обоих глаз улучшилось — уменьшились мучительная фотофобия, гиперемия и резорбция инфильтрации обеих роговиц. Острота зрения стала уверенно расти и в итоге повысилась в правильной светопроекции до 1,0 в течение последующих 8 мес. При этом прозрачность обеих роговиц полностью восстановилась, за исключением помутнения верхненаружного квадранта роговицы правого глаза [3].
«Фокальный сепсис»
Теория о том, что полость рта является одним из основных источников распространения инфекции, была широко принята в 1826 г. , но наиболее важный вклад в ее развитие внес английский врач W. Hunter (1861—1937), который обозначил «фокальный сепсис» как самую распространенную и преобладающую причину большинства заболеваний. В 1900 г. W. Hunter в журнале «British Medical Journal» писал: «…золотые пломбы, коронки и мосты, несъемные зубные протезы, построенные на зараженных корнях зубов погребают воспаленную массу под надежным мавзолеем, для которого во всем царстве медицины и хирургии не найдется сравнения. Это совершенная золотая ловушка сепсиса, которой пациент гордо владеет, и никакие уговоры не побудят его расстаться с нею, потому что она закрывает его черные разрушенные зубы и дорого ему обошлась». Основная идея его теории сводилась к тому, что фокальный сепсис является пусковым механизмом для распространения инфекции в различные системы и органы. К развитию фокального сепсиса полости рта, по его мнению, чаще предрасполагали гингивит, периодонтит, гранулемы и гнойные кисты на верхушках корней зубов. Причинами подверженности зубов септической инфекции являются особенности их строения и функций, а также сообщение с костными тканями челюстно-лицевой области [4].
, но наиболее важный вклад в ее развитие внес английский врач W. Hunter (1861—1937), который обозначил «фокальный сепсис» как самую распространенную и преобладающую причину большинства заболеваний. В 1900 г. W. Hunter в журнале «British Medical Journal» писал: «…золотые пломбы, коронки и мосты, несъемные зубные протезы, построенные на зараженных корнях зубов погребают воспаленную массу под надежным мавзолеем, для которого во всем царстве медицины и хирургии не найдется сравнения. Это совершенная золотая ловушка сепсиса, которой пациент гордо владеет, и никакие уговоры не побудят его расстаться с нею, потому что она закрывает его черные разрушенные зубы и дорого ему обошлась». Основная идея его теории сводилась к тому, что фокальный сепсис является пусковым механизмом для распространения инфекции в различные системы и органы. К развитию фокального сепсиса полости рта, по его мнению, чаще предрасполагали гингивит, периодонтит, гранулемы и гнойные кисты на верхушках корней зубов. Причинами подверженности зубов септической инфекции являются особенности их строения и функций, а также сообщение с костными тканями челюстно-лицевой области [4]. Исследования T. Berdmore показали, что степень выраженности и характер проявлений фокального сепсиса зависят как от характера и вирулентности микроорганизма, вызвавшего сепсис, так и от общего состояния человека [5].
Исследования T. Berdmore показали, что степень выраженности и характер проявлений фокального сепсиса зависят как от характера и вирулентности микроорганизма, вызвавшего сепсис, так и от общего состояния человека [5].
Согласно теории F. Billings, фокус инфекции может оставаться неактивным в течение продолжительного времени, так как защитные функции организма препятствуют развитию инфекции. Однако при негативных воздействиях на организм, например при травме, переохлаждении, стрессе, острой вирусной инфекции, высокой температуре и др., фокус латентной инфекции способен активироваться и привести к развитию септических осложнений [6].
R. Haden в своих исследованиях выделил бактериальные культуры из околоверхушечных тканей 1500 удаленных зубов. Из 400 не депульпированных удаленных зубов лишь в 15% результатов были выявлены стрептококки. Но из 500 ранее депульпированных удаленных зубов с выявленными рентгенологически гранулемами и кистами стрептококки выявлялись в 72,4% случаев, а из 600 ранее депульпированных удаленных зубов, где рентгенологически очаги инфекции выявлены не были, — в 55,7% случаев. Самой распространенной культурой являлись негемолитические стрептококки [7].
Самой распространенной культурой являлись негемолитические стрептококки [7].
Депульпирование зубов потенциально создает риск развития хронического инфекционно-воспалительного процесса полости рта из-за неправильной или неполной очистки зубных каналов, неполного удаления пораженных нервов или недостаточного пломбирования открытых каналов. Эти факторы способствуют распространению микробов и образованию фокальных очагов одонтогенной инфекции [8].
В работе А.С. Рабинович (1960) было установлено, что при исследовании корневых каналов в 800 зубах в 70% случаев имеется ряд боковых каналов и канальцев, оканчивающихся слепо — эти канальцы являются потенциальными зонами возникновения очагов фокальной инфекции, и их диагностика затруднена. Наиболее примечательны скрытые очаги инфекции в «вылеченных» депульпированных зубах, запломбированных или покрытых металлическими коронками. В случае возникновения инфекции в корневых канальцах в таких зубах доступ к ним будет закрыт пломбировочным материалом, и требуется удаление всего зуба [9].
P. Chojnocki внутривенно вводил подопытным кроликам инфекционный материал, выделенный из депульпированных зубов 10 пациентов с иридоциклитом и 4 пациентов с ретробульбарным невритом. В большинстве случаев у кроликов проявлялась та же глазная патология, что и у пациентов. Также ученый отметил, что экстракция больного зуба пациента благоприятно влияла на состояние его глаза [10].
C. Henry описал 50 случаев циклитов, иридоциклитов и конъюнктивитов, развившихся вследствие инфицирования непрорезавшегося зуба мудрости и быстро купированных после его удаления. Автор считал, что поиск зубного сепсиса никогда не должен рассматриваться как полноценный, если он не включает в себя прицельную рентгенограмму зубов мудрости. Зуб мудрости, как и любой другой зуб, может быть местом развития инфекции, однако автор приводит примеры, где совершенно здоровый, но непрорезавшийся дистопированный или ретинированный зуб мудрости вызывал воспаление глаза вследствие давления на верхние или нижние зубные нервные сплетения и рефлекторного раздражения тройничного нерва [11].
Дентальные источники инфекции расценивались J. Doggart и соавторами как пусковые факторы таких заболеваний глаза, как конъюнктивиты, склериты, эписклериты, различные формы кератитов с изъязвлениями или без, катаракты, хориоретиниты, тромбозы вен сетчатки, ретробульбарные невриты, орбитальные целлюлиты, блефариты, дакриоциститы [12].
A. McCallan также соотносил развитие кератитов с наличием фокального сепсиса. Так, при исследовании полости рта у подавляющего большинства больных с язвами роговицы были обнаружены активные формы «дентального сепсиса». Именно из этих очагов, по мнению автора, происходил постоянный отток гнойных бактерий к глазу. A. McCallan отводил важную роль абсорбции токсичных веществ лимфатической системой полости рта и последующее их распространение. По его мнению, это приводило к угнетению местного иммунитета и активному размножению микроорганизмов на поверхности конъюнктивы, оказывая эрозивное действие на роговицу. Автор считал, что для эффективного лечения пациенты, у которых была обнаружена язва роговицы, должны были непременно пройти стоматологический осмотр в первые 24 ч после постановки диагноза. В своей практике он имел богатый опыт лечения язв роговицы, связанных с дентальным сепсисом, и не сомневался во взаимосвязи этих заболеваний [13].
В своей практике он имел богатый опыт лечения язв роговицы, связанных с дентальным сепсисом, и не сомневался во взаимосвязи этих заболеваний [13].
P. Klieve и J. Reh описали более 50 случаев иридоциклитов и кератитов, успешно вылеченных лишь после удаления пораженных зубов. F. Krusin сообщил о нескольких случаях язв роговицы, полностью излеченных после устранения дентальных очагов инфекции [14].
S. Mujevic после тщательного обследования 127 пациентов с иридоциклитами определил, что одонтогенная инфекция явилась непосредственной причиной развития заболевания у 49 пациентов (38,5%). Причем автор заметил, что санация очагов инфекции приводила к короткому обострению симптомов с последующим немедленным выздоровлением, естественно на фоне адекватной консервативной терапии. W. Lang в ходе работы отмечал, что очаги одонтогенной инфекции были обнаружены примерно у 1/3 его пациентов, страдающих иридоциклитом. У ряда пациентов им же была выявлена ЛОР-патология, в частности тонзиллит. Однако одонтогенная инфекция вызывала иридоциклиты в 40 раз чаще, чем очаги инфекции в миндалинах [15, 16].
Однако одонтогенная инфекция вызывала иридоциклиты в 40 раз чаще, чем очаги инфекции в миндалинах [15, 16].
По мнению E. Brown и E. Irons, количество клинических случаев, при которых воспалительные заболевания глаз были связаны с патологией зубов, было почти таким же, как и при тонзиллите. Несколько лет спустя S. Gifford привел данные о том, что иридоциклит, возникший на фоне тонзиллита, встречался в его практике в 2 раза чаще, чем его «зубной» вариант [17, 18].
K. Langmann указывает на возможность рецидива герпетического кератита вследствие одонтогенной инфекции. У наблюдаемого им больного с тяжелым рецидивирующим герпетическим кератитом и вторичной глаукомой при рентгенологическом исследовании была обнаружена зубная гранулема в верхней челюсти на стороне пораженного глаза. После удаления зуба с гранулемой пациент быстро пошел на поправку, внутриглазное давление нормализовалось и рецидивы кератита не повторялись [19].
Наблюдения А.А. Каспарова, изложенные в монографии «Офтальмогерпес» (1994), полностью согласовались с идеей о провоцирующей роли одонтогенной инфекции: установленная при рентгенологическом исследовании зубная гранулема, как правило, верхней челюсти, стала, по предположению автора, причиной рецидива у 15 наблюдаемых им больных с герпетическим кератоиридоциклитом. У 1/3 из них отмечалась смешанная вирусно-бактериальная инфекция роговицы, обусловленная фокальным сепсисом и хроническим раздражением веточек тройничного нерва. Удаление зуба с гранулемой способствовало быстрому выздоровлению, и рецидивы кератита не повторялись. Впоследствии на основе богатейшего опыта А.А. Каспаров ввел в практику возглавляемого им отделения реконструктивной хирургии переднего отдела глаза ФГБНУ НИИ ГБ обязательное проведение диагностики очагов фокальной инфекции (обзорные рентгеновские снимки корней зубов и пазух носа с описанием специалистами) и их санацию у пациентов, обращающихся в отдел с рецидивирующими инфекционными (герпетическими, гнойными) кератитами и кератоиридоциклитами, что значительно сокращало сроки и тяжесть течения этих заболеваний (прим. Е.А. Каспаровой) [20].
У 1/3 из них отмечалась смешанная вирусно-бактериальная инфекция роговицы, обусловленная фокальным сепсисом и хроническим раздражением веточек тройничного нерва. Удаление зуба с гранулемой способствовало быстрому выздоровлению, и рецидивы кератита не повторялись. Впоследствии на основе богатейшего опыта А.А. Каспаров ввел в практику возглавляемого им отделения реконструктивной хирургии переднего отдела глаза ФГБНУ НИИ ГБ обязательное проведение диагностики очагов фокальной инфекции (обзорные рентгеновские снимки корней зубов и пазух носа с описанием специалистами) и их санацию у пациентов, обращающихся в отдел с рецидивирующими инфекционными (герпетическими, гнойными) кератитами и кератоиридоциклитами, что значительно сокращало сроки и тяжесть течения этих заболеваний (прим. Е.А. Каспаровой) [20].
W. Korytowski и E. Krzyzagorska, выявляя этиологическое значение местных очагов инфекции у 360 больных с различными заболеваниями глаз (кератиты, увеиты, невриты зрительного нерва, септический тромбоз центральной вены сетчатки) обнаружили у 151 (41,9%) пациента тонзиллит, а у 132 (36,7%) — очаги инфекции в зубах.
L. King и соавторы описали случай септического тромбоза центральной вены сетчатки, развившегося вследствие транзиторной бактериемии на фоне глубокого кариеса верхних моляров. После проведения системной антибиотикотерапии зрение пациента полностью воcстановилось.
Одонтогенная инфекция как причина кератита описана E. Streiff у 35% больных. По данным автора, чаще поражения глаз были на стороне больного зуба, редко — двусторонними и еще реже развивались на противоположной стороне. Позже, используя бактериологические методы, исследователи предположили, что бактерии и продукты их жизнедеятельности из инфицированных зубов могут распространяться в другие органы двумя путями: «открытым» и «закрытым»: I — «открытым» путем — по пищеварительному тракту и дыхательным путям; II — «закрытым» — из первичного очага инфекции через кровеносные и лимфатические сосуды [21, 22].
S. Blum и cоавторы полагали, что кератиты возникали под влиянием раздражения тригеминального ганглия, которое оказывал воспаленный зуб на тройничный нерв. S. Blum описал 7 случаев кератита, при которых устранение очага одонтогенной инфекции способствовало уменьшению выраженности симптомов кератита или излечению [14].
S. Blum описал 7 случаев кератита, при которых устранение очага одонтогенной инфекции способствовало уменьшению выраженности симптомов кератита или излечению [14].
S. Theobald также предположил рефлекторный ответ ветвей тройничного нерва на раздражители со стороны зубных очагов инфекции и, как следствие, развитие воспаления роговицы. Автор отметил, что значительно чаще подвергается воспалению тот глаз, на стороне которого находится пораженный зуб. Преимущественно такая связь наблюдалась при очагах, расположенных в верхней челюсти. В своих работах он призывал незамедлительно удалять пораженные зубы во избежание осложнений на глазах [23].
В 1954 г. Д.А. Энтин, опираясь на учение И.П. Павлова, доказал, что одонтогенный очаг является источником инфекции и интоксикации центральной нервной системы пациента. Исследования Д.А. Энтина, работавшего над нейротрофической концепцией патогенеза «ротового сепсиса», показали, что физические и химические раздражители (токсины, инфекция) могут нарушить физиологические взаимосвязи между центральной нервной и другими системами и органами, что приводит к различным нервно-дистрофическим процессам в виде болезней организма [24].
И.Г. Лукомский выдвинул нейротоксическую концепцию механизма действия инфекционных очагов полости рта на организм, суть которой заключается в следующем: при воспалительном процессе в тканях периодонта образуются промежуточные продукты распада белка типа биогенных или протеиногенных аминов, а также клеточные и тканевые яды. Эти вещества, всасываясь в кровь, раздражают нейротрофический аппарат и воздействуют на процессы обмена и функцию вегетативной нервной системы в отдельных органах. В то же время указанные вещества, будучи антигенами, изменяют чувствительность организма, что в свою очередь приводит к сенсибилизации и развитию общей интоксикации. И.Г. Лукомский считал, что наиболее частая причина ротового сепсиса — хронический гранулирующий апикальный периодонтит, который из всех других форм периодонтитов является наиболее активной формой нейротоксической связи между хроническими очагами в периодонте и другими системами организма [25].
Транзиторная бактериемия.
 Одонтогенные очаги инфекции
Одонтогенные очаги инфекции
Поскольку стоматологические манипуляции всегда сопровождаются кровотечением, риск развития транзиторной бактериемии очень высок. В 88% случаев микрофлора одонтогенных очагов инфекции попадает в кровяное русло и временно циркулирует там до 15 мин [26].
A. Heimdahl и соавторы выявили бактериемию после экстракции зуба у 100% пациентов, у 70% — после глубокой чистки зубов, у 55% — после хирургического вмешательства на 3-м моляре, у 20% — после эндодонтического лечения (механической и лекарственной обработки зубных каналов с последующей герметизацией) и у 55% — после тонзиллэктомии [27]. D. Kaye (1985) также установил, что в 90% случаев после удаления зубов возникала бактериемия. При этом в 74% удаленных зубов из корневых каналов были выделены Streptococcus viridans, а в 61% — Bacteroides melanogenicus. Также в корневых каналах выявлены стафилококки, энтерококки и другие микроорганизмы [28].
Чаще всего бактериемия протекает бессимптомно, однако пациенты со сниженным иммунитетом подвержены высокому риску развития тяжелых последствий — от случаев кератитов и эндофтальмитов, абсцессов орбиты, синдрома верхушки орбиты до абсцесса мозга, что требует срочного привлечения врачей других специальностей — офтальмологов, отоларингологов, нейрохирургов [3, 29—32]. G. Peyman и соавторы описали случай гематогенного распространения инфекции через 1 нед после стоматологического лечения, когда у пациента появились симптомы прогрессирующего увеита, перешедшего в эндофтальмит, что потребовало проведения эвисцерации [34]. Известно множество работ, описывающих развитие эндофтальмита после удаления больного зуба [34, 35].
В другом исследовании G. Debelian и соавторы использовали фенотипические и генетические методы исследования, чтобы проследить распространение микроорганизмов из полости рта на фоне эндодонтического лечения. Микробиологические образцы брали из корневых каналов 26 пациентов с бессимптомным апикальным периодонтитом однокорневых зубов. В материале были выявлены штаммы анаэробных бактерий: Propionibacterium acnes, Peptostreptococcus prevotii, Fusobacterium nucleatum, Prevotella intermedia, Saccharomyces cerevisiae, Actinomyces israelii, Streptococcus intermedius, Streptococcus sanguis. Те же штаммы были обнаружены в кровотоке пациентов через 10 мин по окончании пломбировки канала зуба [36].
В материале были выявлены штаммы анаэробных бактерий: Propionibacterium acnes, Peptostreptococcus prevotii, Fusobacterium nucleatum, Prevotella intermedia, Saccharomyces cerevisiae, Actinomyces israelii, Streptococcus intermedius, Streptococcus sanguis. Те же штаммы были обнаружены в кровотоке пациентов через 10 мин по окончании пломбировки канала зуба [36].
В подтверждение вышесказанного M. Kilian и соавторы приводят данные о том, что в подавляющем большинстве случаев микроорганизмы распространяются из полости рта в кровоток менее чем за 1 мин после стоматологических процедур, проникая из очагов инфекции в мозг, сердце и легкие [37].
Анализ статистических данных за последние 40 лет показывает, что число больных с острой одонтогенной инфекцией неуклонно растет. По данным стоматологических клиник, в 1978 г. этот показатель составил 51,1—56%, в 1992 г. — 56—59%, в 2000 г. — уже 63—70%, а в 2017 г. — 85,5—95,6%. Болезни периодонта занимают одно из важнейших мест среди проблем в современной стоматологии [38, 39].
Хронический гранулирующий и гранулематозный периодонтиты сопровождаются воспалительными и деструктивными изменениями кости альвеолярного отростка, а продукты распада тканевых белков (биогенные амины) представляют большую опасность для организма, вызывая хроническую интоксикацию и сенсибилизацию. В 85—98% случаев периодонтит зубов является этиологическим фактором острых воспалительных процессов челюстно-лицевой области (периостит, абсцесс, флегмона, лимфаденит, остеомиелит челюсти) [40].
Как правило, хронический апикальный периодонтит протекает в бессимптомной форме. Гранулемы и корневые кисты часто обнаруживают в области разрушенного зуба, а также зубов после травмы, и на фоне недостаточного или неправильного эндодонтического лечения кариеса и пульпита. Местом образования кисты может быть любой поврежденный зуб, однако в 2,5—3 раза чаще гнойные кисты локализуются на верхней челюсти. Киста образуется из околоверхушечной гранулемы, в которую пролиферируют активированные воспалением эпителиальные остатки периодонтальной связки, приводящие к образованию кистогранулемы, затем трансформирующейся в кисту. В неактивном состоянии гранулемы и кисты содержат незначительное количество гноя и не вызывают жалоб у пациентов, что затрудняет клиническую диагностику. В период обострения количество гноя увеличивается за счет гибели макрофагов. Гнойное воспаление повреждает костные структуры, нервные окончания и сосуды альвеолы и кости. Корневая киста всегда инфицирована — содержимое может варьировать от прозрачного серозного до гнойного, в нем обнаруживаются микроорганизмы, которые находятся в полости рта и в кариозных зубах. Прорыв гноя из полости кисты в околочелюстные мягкие ткани приводит к таким осложнениям, как абсцесс или флегмона, а также к образованию свищевого хода, который располагается в преддверии полости рта, небе или коже лица. Лечение корневых кист и гранулем подразделяют на хирургическое (удаление кисты вместе с корнем зуба, вылущивание кисты; цистэктомия с резекцией верхушек корней зуба; цистотомия с медикаментозным растворением остатков) и эндодонтическое (механическое удаление некротизированной ткани из каналов корней кисты или гранулемы, медикаментозная обработка гипохлоридом натрия, ферментативное растворение оболочки, тщательная санация внутриканальной системы для исключения оставления фрагментов кисты и повторного ее развития, установка пломбировочного материала под контролем рентгеновских снимков) [41, 42].
В неактивном состоянии гранулемы и кисты содержат незначительное количество гноя и не вызывают жалоб у пациентов, что затрудняет клиническую диагностику. В период обострения количество гноя увеличивается за счет гибели макрофагов. Гнойное воспаление повреждает костные структуры, нервные окончания и сосуды альвеолы и кости. Корневая киста всегда инфицирована — содержимое может варьировать от прозрачного серозного до гнойного, в нем обнаруживаются микроорганизмы, которые находятся в полости рта и в кариозных зубах. Прорыв гноя из полости кисты в околочелюстные мягкие ткани приводит к таким осложнениям, как абсцесс или флегмона, а также к образованию свищевого хода, который располагается в преддверии полости рта, небе или коже лица. Лечение корневых кист и гранулем подразделяют на хирургическое (удаление кисты вместе с корнем зуба, вылущивание кисты; цистэктомия с резекцией верхушек корней зуба; цистотомия с медикаментозным растворением остатков) и эндодонтическое (механическое удаление некротизированной ткани из каналов корней кисты или гранулемы, медикаментозная обработка гипохлоридом натрия, ферментативное растворение оболочки, тщательная санация внутриканальной системы для исключения оставления фрагментов кисты и повторного ее развития, установка пломбировочного материала под контролем рентгеновских снимков) [41, 42].
Синуситы. Помимо очагов одонтогенной инфекции, другим этиологическим фактором возникновения воспалительных заболеваний переднего отрезка глаза могут являться фокальные очаги инфекции околоносовых пазух. Несмотря на более близкое анатомическое расположение к глазу, синуситы значительно реже вызывают глазную патологию, чем стоматологические заболевания. По предположению R. Kern, фокальные очаги инфекции в пазухах развиваются реже, так как они, в отличие от зубов, не подвергаются постоянному механическому воздействию (сжимание, жевание) и анатомически лучше обособлены [43].
F. Weille и R. Vang описали 244 клинических случая у пациентов с кератитами, увеитами и ретробульбарными невритами: из 108 больных фокальными инфекциями у 56 были рентгенологически подтвержденные синуситы [44].
По мнению R. Castroviejo, терапевтическое или хирургическое лечение синуситов должно существенно снижать риск возникновения патологий роговицы. Он утверждал, что решение о лечении синусита в ряде случаев должно оставаться за врачом-офтальмологом, даже если рентгенологические данные не подтверждают наличие патологии [45].
Дакриоциститы. Автор книги «Очерки гнойной хирургии» В.Ф. Войно-Ясенецкий (1934) описывал периоститы верхней челюсти, абсцессы щеки, воспаления пазух черепа, гнойные дакриоциститы и дакриоадениты, карбункулы и фурункулы лица. Все эти патологии он относил к факторам, способствующим развитию гнойной инфекции роговицы и разработал различные хирургические методы по их устранению. На опыте большого числа пациентов с гнойными язвами роговицы он убедился, что в основе их заболевания лежит воспаление слезного мешка, и лечение следует начинать именно с него. Автор писал о том, что консервативное лечение или прижигание краев язвы не давало положительного результата, но только лишь после экстирпации слезного мешка язва роговицы заживала за несколько дней [46].
Трудность оказания помощи данным больным заключается в необходимости срочного лечения обоих заболеваний — дакриоцистита и гнойной язвы роговицы. Учитывая тот факт, что нарушение проходимости носослезного протока с явлениями воспаления требует, как правило, хирургического вмешательства, встает вопрос о выработке алгоритма лечебных и реабилитационных мероприятий этой категории больных. В.Г. Белоглазов и соавторы при наблюдении 37 больных с гнойными язвами роговицы обнаружили у 9 из них сопутствующие патологии слезоотводящих путей: у 2 больных был диагностирован дакриостеноз, у 2 — непроходимость устья слезных канальцев, у 5 пациентов был выявлен дакриоцистит. При активной медикаментозной терапии положительная динамика была незначительной, часто возникали рецидивы кератита. После хирургического лечения слезоотводящих путей и последующего медикаментозного или хирургического лечения гнойных язв роговицы положительные результаты и отсутствие рецидивов наблюдались у 8 человек. Исследование показало, что при наличии гнойных кератитов и гнойных язв роговицы диагностического промывания слезоотводящих путей недостаточно. Необходимо обязательно проводить рентгенографию слезоотводящих путей с контрастированием в двух проекциях. При сочетании инфекционного кератита и поражения слезоотводящего аппарата первоочередной и необходимой задачей является срочное радикальное хирургическое лечение слезоотводящих путей [47].
В.Г. Белоглазов и соавторы при наблюдении 37 больных с гнойными язвами роговицы обнаружили у 9 из них сопутствующие патологии слезоотводящих путей: у 2 больных был диагностирован дакриостеноз, у 2 — непроходимость устья слезных канальцев, у 5 пациентов был выявлен дакриоцистит. При активной медикаментозной терапии положительная динамика была незначительной, часто возникали рецидивы кератита. После хирургического лечения слезоотводящих путей и последующего медикаментозного или хирургического лечения гнойных язв роговицы положительные результаты и отсутствие рецидивов наблюдались у 8 человек. Исследование показало, что при наличии гнойных кератитов и гнойных язв роговицы диагностического промывания слезоотводящих путей недостаточно. Необходимо обязательно проводить рентгенографию слезоотводящих путей с контрастированием в двух проекциях. При сочетании инфекционного кератита и поражения слезоотводящего аппарата первоочередной и необходимой задачей является срочное радикальное хирургическое лечение слезоотводящих путей [47].
Пути распространения инфекции
Несмотря на то что пути распространения инфекции в организме еще мало изучены, экспериментальные данные позволяют считать возможным существование трех из них — неврального, гематогенного и лимфогенного.
Невральный путь. Экспериментальные исследования, проведенные А.К. Шубладзе и соавторами, И.Ф. Баринским и соавторами с помощью светового микроскопа в 1964 г. и 1986 г., подтвердили предположения S. Blum, S. Theobald, A. Nesburn и P. Absell: герпесвирусная инфекция распространяется в различные органы двумя путями — невральным (по чувствительным, двигательным и симпатическим нервным волокнам) и гематогенным (в результате выраженного эритротропизма вируса простого герпеса), вследствие чего происходит заражение новых клеток [20, 48, 49].
В ходе экспериментов на кроликах A. Nesburn и P. Absell (1976) доказали, что тригеминальный ганглий является основным резервуаром для латентного пребывания вируса простого герпеса (ВПГ) в течение многих лет [50, 51].
А.А. Каспаров и соавторы считают, что очаги инфекции в голове (кисты, гранулемы зубов, тонзиллиты, синуситы, дакриоциститы) воздействуют раздражающе на вторую верхнечелюстную и/или третью нижнечелюстную ветви тройничного нерва, что в свою очередь вызывает рефлекторное раздражение ганглия тройничного нерва и выход из него «легионов вирусов герпеса на тропу войны», которые, распространяясь по первой глазничной ветви тройничного нерва, далее по носоресничной ветви, ресничным ветвям через супрахориоидальное пространство и цилиарное тело достигают нервного сплетения в слоях роговицы, вызывая возникновение или обострение герпетического кератита (иридоциклита) [20].
При изучении механизма распространения герпетической инфекции K. Hayaski и Y. Uchida (1981) пришли к выводу, что раздражение ганглия приводит к реактивации ВПГ и обратному поступлению вируса из ганглия по первой ветви тройничного нерва к органу-мишени — глазу. Развивается острый герпетический кератит или его рецидивы. Миграция вируса по нервным путям происходит с помощью аксоплазматического транспорта в анте- и ретроградном направлениях, распространяется интрааксонально, периневрально, эндоневрально, по леммоцитам [52]. J. Szanto и J. Rajcani (1983) доказали, что вирионы вируса герпеса после прикрепления к нервным окончаниям поглощаются аксонами и транспортируются внутри них со скоростью 1,5 мм/ч. Авторы считают невральный путь распространения вируса простого герпеса преобладающим [53].
Миграция вируса по нервным путям происходит с помощью аксоплазматического транспорта в анте- и ретроградном направлениях, распространяется интрааксонально, периневрально, эндоневрально, по леммоцитам [52]. J. Szanto и J. Rajcani (1983) доказали, что вирионы вируса герпеса после прикрепления к нервным окончаниям поглощаются аксонами и транспортируются внутри них со скоростью 1,5 мм/ч. Авторы считают невральный путь распространения вируса простого герпеса преобладающим [53].
Гематогенный путь
По мнению J. Bullock и соавторов, предположительным путем гематогенного распространения инфекции является ретроградный занос через глазные вены. Верхняя и нижняя глазные вены анастомозируют с угловой и лицевой венами у медиального угла глаза. Нижняя глазная вена проходит через нижнюю глазную щель и соединяется с крыловидным венозным сплетением. Эти вены не имеют клапанов, и в них не происходит сопротивления распространению инфекции. Отсутствие клапанов при наличии анастомозов между венами глазницы и лица, пазух носа и крылонебной ямки формирует условия для оттока крови в трех направлениях: в пещеристую пазуху, крылонебную ямку и к венам лица. Это создает возможность распространения инфекции с кожи лица, из пазух носа в глазницу и пещеристую пазуху. С помощью этих вен орбита соединяется с полостью рта и пазухами, что обеспечивает быстрый заброс инфекции из этих зон в орбиту, далее — по глазным, вортикозным и эписклеральным венам, осуществляющим венозный отток от переднего отрезка глаза [29, 54, 55]. R. Brooks и D. Parke было описано множество случаев (38 и 32) гематогенного распространения Candida albicans, приводивших к возникновению эндофтальмитов [56, 57].
Отсутствие клапанов при наличии анастомозов между венами глазницы и лица, пазух носа и крылонебной ямки формирует условия для оттока крови в трех направлениях: в пещеристую пазуху, крылонебную ямку и к венам лица. Это создает возможность распространения инфекции с кожи лица, из пазух носа в глазницу и пещеристую пазуху. С помощью этих вен орбита соединяется с полостью рта и пазухами, что обеспечивает быстрый заброс инфекции из этих зон в орбиту, далее — по глазным, вортикозным и эписклеральным венам, осуществляющим венозный отток от переднего отрезка глаза [29, 54, 55]. R. Brooks и D. Parke было описано множество случаев (38 и 32) гематогенного распространения Candida albicans, приводивших к возникновению эндофтальмитов [56, 57].
Лимфогенный путь
Лимфатическая система находится в тесной связи с кровеносной, принимая активное участие в обменных процессах, а также обеспечивая защитную функцию организма от инфекционного и интоксикационного воздействий. От фокальных очагов инфекции бактерии, вирусы и грибки способны по афферентным лимфатическим сосудам достигать лимфатических узлов. Далее они распространяются от пораженного лимфатического узла к следующему лимфатическому узлу по эфферентным лимфатическим сосудам, достигая глубоких лимфатических узлов и попадая в кровеносное русло [58].
От фокальных очагов инфекции бактерии, вирусы и грибки способны по афферентным лимфатическим сосудам достигать лимфатических узлов. Далее они распространяются от пораженного лимфатического узла к следующему лимфатическому узлу по эфферентным лимфатическим сосудам, достигая глубоких лимфатических узлов и попадая в кровеносное русло [58].
По данным Y. Shinomura и соавторов, ВПГ обладает тропизмом не только к нервной ткани и эритроцитам, но и способностью к сохранению и размножению в лейкоцитах и лимфоцитах, что приводит к дальнейшей реактивации вируса при определенных условиях. Инфицированные ВПГ лейкоциты и лимфоциты обеспечивают последующее распространение по ходу лимфатических сосудов, поражая близлежащие структуры [59].
От перикорнеального лимфатического кольца лимфа оттекает в сторону экватора, в густую сеть широко анастомозирующих между собой извитых лимфатических сосудов. Первыми лимфоузлами для конъюнктивальных лимфатических сосудов являются околоушные, также установлены дренажные связи конъюнктивального лимфооттока с подчелюстными и шейными лимфоузлами. В подчелюстные узлы осуществляется отток от всех зубов, кроме нижних резцов и верхних зубов мудрости (для них отток лимфы идет в глубокие лимфатические узлы шеи). Таким образом, подчелюстные и шейные лимфоузлы могут являться связующим звеном лимфооттока зубов и глаз [60, 61].
В подчелюстные узлы осуществляется отток от всех зубов, кроме нижних резцов и верхних зубов мудрости (для них отток лимфы идет в глубокие лимфатические узлы шеи). Таким образом, подчелюстные и шейные лимфоузлы могут являться связующим звеном лимфооттока зубов и глаз [60, 61].
Многочисленные наблюдения врачей разных специальностей (офтальмологов, стоматологов и отоларингологов), изложенные в настоящем обзоре, подтверждают существование несомненной взаимосвязи между очагами инфекции в области головы и воспалительными заболеваниями глаз.
Своевременно не диагностированный либо неизлеченный «фокальный сепсис» (кисты и гранулемы зубов, тонзиллит, синусит, дакриоцистит) является потенциальной опасностью распространения инфекции и развития воспаления глаз. Данные литературы и собственный опыт позволяют сделать вывод о том, что очаги инфекции утяжеляют течение воспалительных заболеваний глаз (кератиты, кератоиридоциклиты, иридоциклиты) и провоцируют рецидивы болезни.
По данным литературы, фокальные очаги инфекции оказывают раздражающее или токсическое воздействие на вторую и третью ветви тройничного нерва, вызывая рефлекторное раздражение тригеминального ганглия, являющегося резервуаром для ВПГ. ВПГ, имеющий тропность к нервной ткани и эритроцитам, распространяется из ганглия тройничного нерва по глазничной ветви тройничного нерва нейрогенным, а также гематогенным путем. Таким образом, инфекция через сосуды и нервы в супрахориоидальном пространстве достигает переднего отрезка глаза. Гематогенный путь распространения микробной инфекции возможен благодаря анастомозу верхней и нижней глазных вен с угловой и лицевой венами. Лимфатический путь распространения предположительно осуществляется через подчелюстные и шейные узлы, которые становятся общим звеном в системе оттока лимфы зубов и глаз.
ВПГ, имеющий тропность к нервной ткани и эритроцитам, распространяется из ганглия тройничного нерва по глазничной ветви тройничного нерва нейрогенным, а также гематогенным путем. Таким образом, инфекция через сосуды и нервы в супрахориоидальном пространстве достигает переднего отрезка глаза. Гематогенный путь распространения микробной инфекции возможен благодаря анастомозу верхней и нижней глазных вен с угловой и лицевой венами. Лимфатический путь распространения предположительно осуществляется через подчелюстные и шейные узлы, которые становятся общим звеном в системе оттока лимфы зубов и глаз.
Знание о взаимосвязи локальных очагов инфекции и воспалительно-инфекционных поражений глаз позволяет не только своевременно исключить причины развития заболевания, но и дает больше возможностей для более эффективного его лечения и предупреждения рецидивов.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Каспарова Евгения Аркадьевна — канд. мед. наук, старший научный сотрудник, врач-офтальмолог; https://orcid.org/0000-0001-8594-2395; e-mail: [email protected]
Левицкий Юрий Владимирович — аспирант, врач-офтальмолог; https://orcid.org/0000-0002-8053-4808; e-mail: [email protected]
Ципурская Ольга Ильинична — врач-стоматолог, Научно-исследовательский институт глазных болезней; https://orcid.org/0000-0001-5813-0658; e-mail: [email protected]
Автор, ответственный за переписку: Каспарова Евгения Аркадьевна — e-mail: [email protected]
Разрешение локализованного хронического периодонтита, связанного с длительными отложениями зубного камня
1. Тиммерман М.Ф., ван дер Вейден Г.А. Факторы риска пародонтита. Международный журнал стоматологической гигиены . 2006;4(1):2–7. [PubMed] [Google Scholar]
2. Anerud A, Löe H, Boysen H. Естественная история и клиническое течение образования камней у человека. Журнал клинической пародонтологии . 1991;18(3):160–170. [PubMed] [Google Scholar]
Журнал клинической пародонтологии . 1991;18(3):160–170. [PubMed] [Google Scholar]
3. Friskopp J. Ультраструктура недекальцинированного наддесневого и поддесневого зубного камня. Журнал пародонтологии . 1983;54(9):542–550. [PubMed] [Google Scholar]
4. Roberts-Harry EA, Clerehugh V. Поддесневой зубной камень: где мы сейчас? Сравнительный обзор. Стоматологический журнал . 2000;28(2):93–102. [PubMed] [Google Scholar]
5. Белый ди-джей. Зубной камень: последние данные о возникновении, формировании, предотвращении, удалении и влиянии на здоровье полости рта наддесневых и поддесневых отложений. Европейский журнал устных наук . 1997;105(5, часть 2):508–522. [PubMed] [Google Scholar]
6. Джепсен С., Дешнер Дж., Браун А., Шварц Ф., Эберхард Дж. Удаление зубного камня и предотвращение его образования. Пародонтология 2000 . 2011;55(1):167–188. [PubMed] [Google Scholar]
7. Калабрезе Н., Галгут П., Мордан Н. Идентификация Actinobacillus actinomycetemcomitans, Treponema denticola и Porphyromonas gingivalis в зубном камне человека: экспериментальное исследование. Журнал Международной академии пародонтологии . 2007;9(4):118–128. [PubMed] [Google Scholar]
Идентификация Actinobacillus actinomycetemcomitans, Treponema denticola и Porphyromonas gingivalis в зубном камне человека: экспериментальное исследование. Журнал Международной академии пародонтологии . 2007;9(4):118–128. [PubMed] [Google Scholar]
8. Tan BTK, Mordan NJ, Embleton J, Pratten J, Galgut PN. Изучение жизнеспособности бактерий в наддесневом зубном камне человека. Журнал пародонтологии . 2004;75(1):23–29. [PubMed] [Google Scholar]
9. Муля Н.Н., Тхакур С., Равиндра С., Сетти С.Б., Кулкарни Р., Халликери К. Жизнеспособность бактерий в зубном камне — микробиологическое исследование. Журнал Индийского общества пародонтологии . 2010;14(4):222–226. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Zhang S-M, Tian F, Jiang X-Q, et al. Доказательства обызвествления наночастиц в жидкости десневой борозды и зубного камня при пародонтите. Журнал пародонтологии . 2009;80(9):1462–1470. [PubMed] [Google Scholar]
11. Tugnait A, Clerehugh V, Hirschmann PN. Полезность рентгенограмм в диагностике и лечении заболеваний пародонта: обзор. Стоматологический журнал . 2000;28(4):219–226. [PubMed] [Google Scholar]
Tugnait A, Clerehugh V, Hirschmann PN. Полезность рентгенограмм в диагностике и лечении заболеваний пародонта: обзор. Стоматологический журнал . 2000;28(4):219–226. [PubMed] [Google Scholar]
12. Buchanan SA, Jenderseck RS, Granet MA, Kircos LT, Chambers DW, Robertson PB. Рентгенологическое обнаружение зубного камня. Журнал пародонтологии . 1987; 58 (11): 747–751. [PubMed] [Google Scholar]
13. Wilson TG, Jr., Harrel SK, Nunn ME, Francis B, Webb K. Взаимосвязь между наличием зубных поддесневых отложений и воспалением, обнаруженным с помощью стоматологического эндоскопа. Журнал пародонтологии . 2008;79(11):2029–2035. [PubMed] [Google Scholar]
14. Kasaj A, Moschos I, Röhrig B, Willershausen B. Эффективность нового оптического зонда при обнаружении поддесневого зубного камня. Международный журнал стоматологической гигиены . 2008;6(2):143–147. [PubMed] [Google Scholar]
15. Курихара Э., Косэки Т., Гохара К., Нишихара Т. , Ансай Т., Такехара Т. Обнаружение поддесневого зубного камня и кариеса дентина с помощью лазерной флуоресценции. Журнал пародонтологических исследований . 2004;39(1):59–65. [PubMed] [Google Scholar]
, Ансай Т., Такехара Т. Обнаружение поддесневого зубного камня и кариеса дентина с помощью лазерной флуоресценции. Журнал пародонтологических исследований . 2004;39(1):59–65. [PubMed] [Google Scholar]
16. Badran Z, Demoersman J, Struillou X, Boutigny H, Weiss P, Soueidan A. Лазерно-индуцированная флуоресценция для обнаружения поддесневого зубного камня: научное рациональное и клиническое применение в пародонтологии. Фотомедицина и лазерная хирургия . 2011;29(9):593–596. [PubMed] [Google Scholar]
17. Rabbani GM, Ash MM, Jr., Caffesse RG. Эффективность поддесневого скейлинга и полировки корней при удалении зубного камня. Журнал пародонтологии . 1981;52(3):119–123. [PubMed] [Google Scholar]
18. Кепик Т.Дж., О’Лири Т.Дж., Кафрави А.Х. Полное удаление зубного камня: достижимая цель? Журнал пародонтологии . 1990;61(1):16–20. [PubMed] [Академия Google]
19. Бломлёф Л., Фрископп Дж., Аппельгрен Р., Линдског С., Хаммарстрём Л. Влияние грануляционной ткани, зубного камня и загрязненного корневого цемента на заживление пародонтальных ран. Экспериментальное исследование на обезьянах. Журнал клинической пародонтологии . 1989;16(1):27–32. [PubMed] [Google Scholar]
Влияние грануляционной ткани, зубного камня и загрязненного корневого цемента на заживление пародонтальных ран. Экспериментальное исследование на обезьянах. Журнал клинической пародонтологии . 1989;16(1):27–32. [PubMed] [Google Scholar]
20. Cugini MA, Haffajee AD, Smith C, Kent RL, Jr., Socransky SS. Влияние скейлинга и полировки корней на клинические и микробиологические параметры заболеваний пародонта: результаты 12 месяцев. Журнал клинической пародонтологии . 2000;27(1):30–36. [PubMed] [Google Scholar]
21. Кобб С.М., Джеффкоат Дж. Клиническое значение нехирургического пародонтологического лечения: доказательная точка зрения на масштабирование и полировку корней. Журнал клинической пародонтологии . 2002; 29 (приложение 2): 6–16. [PubMed] [Google Scholar]
22. Hellstein JW, Adler RA, Edwards B, et al. Управление уходом за пациентами, получающими антирезорбтивную терапию для профилактики и лечения остеопороза: краткое изложение рекомендаций Совета по научным вопросам Американской стоматологической ассоциации. Журнал Американской стоматологической ассоциации . 2011;142(11):1243–1251. [PubMed] [Google Scholar]
Журнал Американской стоматологической ассоциации . 2011;142(11):1243–1251. [PubMed] [Google Scholar]
23. Lindhe J, Westfelt E, Nyman S, Socransky SS, Haffajee AD. Отдаленный эффект хирургического/нехирургического лечения заболеваний пародонта. Журнал клинической пародонтологии . 1984;11(7):448–458. [PubMed] [Google Scholar]
24. Heitz-Mayfield LJA, Trombelli L, Heitz F, Needleman I, Moles D. Систематический обзор эффективности хирургической обработки по сравнению с нехирургической обработкой при лечении хронического периодонтита. Журнал клинической пародонтологии . 2002; 29 (приложение 3): 92–102. [PubMed] [Google Scholar]
25. Торнтон С., Гарник Дж. Сравнение ультразвуковых и ручных инструментов при удалении поддесневого налета. Журнал пародонтологии . 1982;53(1):35–37. [PubMed] [Google Scholar]
26. Джонс В.А., О’Лири Т.Дж. Эффективность планирования корней in vivo при удалении бактериального эндотоксина из корней пародонтальных зубов. Журнал пародонтологии . 1978;49(7):337–342. [PubMed] [Google Scholar]
Журнал пародонтологии . 1978;49(7):337–342. [PubMed] [Google Scholar]
27. Исидор Ф., Карринг Т. Долгосрочный эффект хирургического и нехирургического лечения пародонта. 5-летнее клиническое исследование. Журнал пародонтологических исследований . 1986;21(5):462–472. [PubMed] [Google Scholar]
28. Caton JG, Zander HA. Соединение между зубом и тканями десны после периодического шлифования корней и кюретажа мягких тканей. Журнал пародонтологии . 1979; 50 (9): 462–466. [PubMed] [Академия Google]
29. Hwang Y-J, Fien MJ, Lee S-S, et al. Влияние скейлинга и сглаживания корней на альвеолярную кость, измеренное с помощью субтракционной рентгенографии. Журнал пародонтологии . 2008;79(9):1663–1669. [PubMed] [Google Scholar]
30. Нибали Л., Пометти Д., Ту Ю.К., Донос Н. Клинические и рентгенологические результаты после нехирургического лечения межкостных дефектов периодонта: ретроспективное исследование. Журнал клинической пародонтологии . 2011;38(1):50–57. [PubMed] [Академия Google]
2011;38(1):50–57. [PubMed] [Академия Google]
31. Шерман П.Р., Хатченс Л.Х., младший, Джюсон Л.Г., Мориарти Дж.М., Греко Г.В., Макфолл В.Т., младший. Эффективность поддесневого скейлинга и планирования корня. I. Клиническое обнаружение остаточного конкремента. Журнал пародонтологии . 1990;61(1):3–8. [PubMed] [Google Scholar]
32. Waerhaug J. Заживление денто-эпителиального соединения после удаления поддесневого налета. I. Как наблюдается в материале биопсии человека. Журнал пародонтологии . 1978;49(1):1–8. [PubMed] [Академия Google]
33. Shen E-C, Maddalozzo D, Robinson PJ, Geivelis M. Строгание корней после кратковременного вздутия кармана. Журнал пародонтологии . 1997;68(7):632–635. [PubMed] [Google Scholar]
34. Buchanan SA, Robertson PB. Удаление зубного камня путем скейлинга/шлифовки корней с хирургическим доступом и без него. Журнал пародонтологии . 1987; 58 (3): 159–163. [PubMed] [Google Scholar]
35. Линде Дж., Сокрански С.С., Найман С., Хаффаджи А., Вестфельт Э. «Критическая глубина зондирования» в периодонтальной терапии. Журнал клинической пародонтологии . 1982;9(4):323–336. [PubMed] [Google Scholar]
Линде Дж., Сокрански С.С., Найман С., Хаффаджи А., Вестфельт Э. «Критическая глубина зондирования» в периодонтальной терапии. Журнал клинической пародонтологии . 1982;9(4):323–336. [PubMed] [Google Scholar]
36. Herrera D, Sanz M, Jepsen S, Needleman I, Roldán S. Систематический обзор влияния системных противомикробных препаратов в качестве дополнения к скейлингу и выравниванию корней у пациентов с пародонтитом. Журнал клинической пародонтологии . 2002; 29 (приложение 3): 136–159. [PubMed] [Google Scholar]
37. Smith SR, Foyle DM, Daniels J, et al. Двойное слепое плацебо-контролируемое исследование азитромицина в качестве дополнения к нехирургическому лечению пародонтита у взрослых: клинические результаты. Журнал клинической пародонтологии . 2002;29(1):54–61. [PubMed] [Google Scholar]
38. Haffajee AD, Torresyap G, Socransky SS. Клинические изменения после четырех различных пародонтологических терапий для лечения хронического пародонтита: результаты за 1 год. Журнал клинической пародонтологии . 2007;34(3):243–253. [PubMed] [Google Scholar]
Журнал клинической пародонтологии . 2007;34(3):243–253. [PubMed] [Google Scholar]
39. Mascarenhas P, Gapski R, Al-Shammari K, et al. Клинический ответ на азитромицин в качестве дополнения к нехирургической пародонтальной терапии у курильщиков. Журнал пародонтологии . 2005;76(3):426–436. [PubMed] [Google Scholar]
40. Kitzis MD, Goldstein FW, Miegi M, Acar JF. Активность азитромицина in vitro в отношении различных грамотрицательных бацилл и анаэробных бактерий. Журнал антимикробной химиотерапии . 1990; 25 (приложение А): 15–18. [PubMed] [Google Scholar]
41. Lai PC, Ho W, Jain N, Walters JD. Концентрации азитромицина в крови и жидкости десневой борозды после системного введения. Журнал пародонтологии . 2011;82(11):1582–1586. [Бесплатная статья PMC] [PubMed] [Google Scholar]
42. Jain R, Danziger LH. Макролидные антибиотики: фармакокинетический и фармакодинамический обзор. Текущий фармацевтический дизайн . 2004;10(25):3045–3053. [PubMed] [Google Scholar]
2004;10(25):3045–3053. [PubMed] [Google Scholar]
43. Jain N, Lai PC, Walters JD. Влияние гингивита на концентрацию азитромицина в жидкости десневой борозды. Журнал пародонтологии . 2012;83(9):1122–1128. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Gladue RP, Bright GM, Isaacson RE, Newborg MF. Поглощение азитромицина (CP-62,993) фагоцитарными клетками in vitro и in vivo: возможный механизм доставки и высвобождения в очагах инфекции. Противомикробные препараты и химиотерапия . 1989;33(3):277–282. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Gladue RP, Snider ME. Внутриклеточное накопление азитромицина культивируемыми фибробластами человека. Противомикробные препараты и химиотерапия . 1990;34(6):1056–1060. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Альтенбург Дж., Де Грааф К.С., Ван Дер Верф Т.С., Бурсма В.Г. Иммуномодулирующие эффекты макролидных антибиотиков — часть 1: биологические механизмы. Дыхание . 2010;81(1):67–74. [PubMed] [Google Scholar]
Дыхание . 2010;81(1):67–74. [PubMed] [Google Scholar]
47. Ho W, Eubank T, Leblebicioglu B, Marsh C, Walters J. Азитромицин уменьшает объем щелевой жидкости и содержание медиатора. Журнал стоматологических исследований . 2010;89(8):831–835. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Хирш Р., Дэн Х., Лаохачай М.Н. Азитромицин в пародонтологическом лечении: больше, чем антибиотик. Журнал пародонтологических исследований . 2012;47(2):137–148. [PubMed] [Google Scholar]
49. Хирш Р. Заживление периодонта и регенерация кости в ответ на азитромицин. Австралийский стоматологический журнал . 2010;55(2):193–199. [PubMed] [Google Scholar]
50. Шеннон Дж., Шеннон Дж., Моделевский С., Гриппо А.А. Бисфосфонаты и остеонекроз челюсти. Журнал Американского гериатрического общества . 2011;59(12):2350–2355. [PubMed] [Академия Google]
Лечение хронического пародонтита: текущее состояние, проблемы и будущие направления
1. Берт Б. Позиция: Эпидемиология заболеваний пародонта. J Пародонтол. 2005; 76: 1406–1409. [PubMed] [Google Scholar]
Берт Б. Позиция: Эпидемиология заболеваний пародонта. J Пародонтол. 2005; 76: 1406–1409. [PubMed] [Google Scholar]
2. Страница RC, Eke PI. Определения случаев для использования в популяционном эпиднадзоре за пародонтитом. J Пародонтол. 2007; 78: 1387–1399. [PubMed] [Google Scholar]
3. Hill RW, Ramfjord SP, Morrison EC, et al. Сравнение четырех видов пародонтологического лечения за два года. J Пародонтол. 1981;52:655–662. [PubMed] [Google Scholar]
4. Исидор Ф., Карринг Т. Долгосрочный эффект хирургического и нехирургического лечения пародонта. 5-летнее клиническое исследование. J Периодонтальная Рез. 1986; 21: 462–472. [PubMed] [Google Scholar]
5. Kaldahl WB, Kalkwarf KL, Patil KD, Molvar MP, Dyer JK. Долгосрочная оценка периодонтальной терапии: I. Ответ на 4 терапевтических метода. J Пародонтол. 1996; 67: 93–102. [PubMed] [Google Scholar]
6. Kaldahl WB, Kalkwarf KL, Patil KD, Molvar MP, Dyer JK. Долгосрочная оценка периодонтальной терапии: II. Частота поломок сайтов. J Пародонтол. 1996;67:103–108. [PubMed] [Google Scholar]
Частота поломок сайтов. J Пародонтол. 1996;67:103–108. [PubMed] [Google Scholar]
7. Брунсволд М.А., Наир П., Оутс Т.В., мл. Основные жалобы пациентов, обращающихся за лечением пародонтита. J Am Dent Assoc. 1999; 130:359–364. [PubMed] [Google Scholar]
8. Khocht A, Zohn H, Deasy M, Chang KM. Оценка пародонтального статуса с помощью ПСР и традиционного клинического пародонтологического исследования. J Am Dent Assoc. 1995; 126: 1658–1665. [PubMed] [Google Scholar]
9. Гринштейн Г. Современная интерпретация оценок глубины зондирования: диагностические и терапевтические последствия. Обзор литературы. J Пародонтол. 1997;68:1194–1205. [PubMed] [Google Scholar]
10. Jeffcoat MK, Reddy MS. Сравнение зондирующих и рентгенологических методов выявления прогрессирования заболеваний пародонта. Карр Опин Дент. 1991; 1: 45–51. [PubMed] [Google Scholar]
11. Stambaugh RV, Dragoo M, Smith DM, Carasali L. Пределы поддесневого масштабирования. Int J Пародонтология Restorative Dent. 1981; 1:30–41. [PubMed] [Google Scholar]
1981; 1:30–41. [PubMed] [Google Scholar]
12. Линде Дж., Найман С. Долгосрочное ведение пациентов, лечившихся от прогрессирующего заболевания пародонта. Дж. Клин Пародонтол. 1984;11:504–514. [PubMed] [Google Scholar]
13. Lindhe J, Westfelt E, Nyman S, Socransky SS, Haffajee AD. Отдаленный эффект хирургического/нехирургического лечения заболеваний пародонта. Дж. Клин Пародонтол. 1984; 11: 448–458. [PubMed] [Google Scholar]
14. Ramfjord SP, Caffesse RG, Morrison EC, et al. Сравнение четырех методов пародонтологического лечения за пять лет. J Периодонтальная Рез. 1987; 22: 222–223. [PubMed] [Google Scholar]
15. Cobb CM. Нехирургическая карманная терапия: механическая. Энн Пародонтолог. 1996;1:443–490. [PubMed] [Google Scholar]
16. Бадерстен А., Нильвеус Р., Эгельберг Дж. Эффект нехирургической пародонтальной терапии. III. Одиночная и повторная инструментальная обработка. Дж. Клин Пародонтол. 1984; 11: 114–124. [PubMed] [Google Scholar]
17. Бадерстен А., Нильвеус Р., Эгельберг Дж. Эффект нехирургической пародонтальной терапии. II. Тяжело прогрессирующий пародонтит. Дж. Клин Пародонтол. 1984; 11: 63–76. [PubMed] [Google Scholar]
Бадерстен А., Нильвеус Р., Эгельберг Дж. Эффект нехирургической пародонтальной терапии. II. Тяжело прогрессирующий пародонтит. Дж. Клин Пародонтол. 1984; 11: 63–76. [PubMed] [Google Scholar]
18. Cugini MA, Haffajee AD, Smith C, Kent RL., Jr Socransky SS. Влияние скейлинга и полировки корней на клинические и микробиологические параметры заболеваний пародонта: результаты 12 месяцев. Дж. Клин Пародонтол. 2000; 27:30–36. [PubMed] [Академия Google]
19. Kaldahl WB, Kalkwarf KL, Patil KD, Dyer JK, Bates RE., Jr Оценка четырех методов пародонтальной терапии. Средняя глубина зондирования, уровень прикрепления зондирования и изменения рецессии. J Пародонтол. 1988; 59: 783–793. [PubMed] [Google Scholar]
20. Morrison EC, Ramfjord SP, Hill RW. Краткосрочные эффекты начального нехирургического пародонтологического лечения (гигиеническая фаза) J Clin Periodontol. 1980; 7: 199–211. [PubMed] [Google Scholar]
21. Preshaw PM, Lauffart B, Zak E, et al. Прогрессирование и лечение хронического пародонтита взрослых. J Пародонтол. 1999;70:1209–1220. [PubMed] [Google Scholar]
J Пародонтол. 1999;70:1209–1220. [PubMed] [Google Scholar]
22. Ланг Н.П., Джосс А., Орсаник Т., Гусберти Ф.А., Зигрист Б.Е. Кровотечение при зондировании. Предиктор прогрессирования пародонтита? Дж. Клин Пародонтол. 1986; 13: 590–596. [PubMed] [Google Scholar]
23. Checchi L, Pelliccioni GA. Ручной и ультразвуковой инструментарий при удалении эндотоксинов с поверхности корня in vitro. J Пародонтол. 1988; 59: 398–402. [PubMed] [Google Scholar]
24. Dragoo MR. Клиническая оценка ручных и ультразвуковых инструментов при санации поддесневой ткани. 1. С немодифицированными и модифицированными ультразвуковыми вставками. Int J Пародонтология Restorative Dent. 1992;12:310–323. [PubMed] [Google Scholar]
25. Eberhard J, Jepsen S, Jervoe-Storm PM, Needleman I, Worthington HV. Полная дезинфекция полости рта при лечении хронического пародонтита у взрослых. Кокрановская система базы данных, ред. 2008: CD004622. [PubMed] [Google Scholar]
26. Serino G, Rosling B, Ramberg P, Socransky SS, Lindhe J. Первоначальный результат и долгосрочный эффект хирургического и нехирургического лечения поздних стадий пародонтоза. Дж. Клин Пародонтол. 2001; 28: 910–916. [PubMed] [Академия Google]
Первоначальный результат и долгосрочный эффект хирургического и нехирургического лечения поздних стадий пародонтоза. Дж. Клин Пародонтол. 2001; 28: 910–916. [PubMed] [Академия Google]
27. Heitz-Mayfield LJ, Trombelli L, Heitz F, Needleman I, Moles D. Систематический обзор эффективности хирургической обработки по сравнению с нехирургической обработкой при лечении хронического периодонтита. Дж. Клин Пародонтол. 2002; 29 (Приложение 3): 92–102. обсуждение 160–162. [PubMed] [Google Scholar]
28. Хиршфельд Л., Вассерман Б. Долгосрочное исследование потери зубов у 600 пациентов, прошедших курс лечения пародонта. J Пародонтол. 1978; 49: 225–237. [PubMed] [Google Scholar]
29. McFall WT. Jr. Потеря зубов у 100 пролеченных пациентов с заболеваниями пародонта. Долгосрочное исследование. J Пародонтол. 1982;53:539–549. [PubMed] [Google Scholar]
30. Mokdad AH, Bowman BA, Ford ES, et al. Продолжающиеся эпидемии ожирения и диабета в США. ДЖАМА. 2001; 286:1195–1200. [PubMed] [Google Scholar]
31. Albrecht M, Banoczy J, Tamas G. Jr Стоматологические и оральные симптомы сахарного диабета. Сообщество Dent Oral Epidemiol. 1988; 16: 378–380. [PubMed] [Google Scholar]
Albrecht M, Banoczy J, Tamas G. Jr Стоматологические и оральные симптомы сахарного диабета. Сообщество Dent Oral Epidemiol. 1988; 16: 378–380. [PubMed] [Google Scholar]
32. Берник С.М., Коэн Д.В., Бейкер Л., Ластер Л. Заболевания зубов у детей с сахарным диабетом. J Пародонтол. 1975;46:241–245. [PubMed] [Google Scholar]
33. Cianciola LJ, Park BH, Bruck E, Mosovich L, Genco RJ. Распространенность заболеваний пародонта при инсулинозависимом сахарном диабете (ювенильный диабет) J Am Dent Assoc. 1982; 104: 653–660. [PubMed] [Google Scholar]
34. Cohen DW, Friedman LA, Shapiro J, Kyle GC, Franklin S. Сахарный диабет и заболевания пародонта: двухлетние продольные наблюдения. I.J. Пародонтол. 1970; 41: 709–712. [PubMed] [Google Scholar]
35. de Pommereau V, Dargent-Pare C, Robert JJ, Brion M. Состояние пародонта у подростков с инсулинозависимым диабетом. Дж. Клин Пародонтол. 1992;19:628–632. [PubMed] [Google Scholar]
36. Ervasti T, Knuuttila M, Pohjamo L, Haukipuro K. Связь между контролем диабета и кровоточивостью десен. J Пародонтол. 1985; 56: 154–157. [PubMed] [Google Scholar]
Связь между контролем диабета и кровоточивостью десен. J Пародонтол. 1985; 56: 154–157. [PubMed] [Google Scholar]
37. Галеа Х., Аганович И., Аганович М. Опыт кариеса зубов и заболеваний пародонта у пациентов с ранним началом инсулинозависимого диабета. Инт Дент Дж. 1986; 36: 219–224. [PubMed] [Google Scholar]
38. Gusberti FA, Syed SA, Bacon G, Grossman N, Loesche WJ. Половозрелый гингивит у детей с инсулинозависимым диабетом. I. Поперечные наблюдения. J Пародонтол. 1983;54:714–720. [PubMed] [Google Scholar]
39. Hugoson A, Thorstensson H, Falk H, Kuylenstierna J. Заболевания пародонта у инсулинозависимых диабетиков. Дж. Клин Пародонтол. 1989; 16: 215–223. [PubMed] [Google Scholar]
40. Novaes Junior AB, Pereira AL, de Moraes N, Novaes AB. Проявления инсулинозависимого сахарного диабета в пародонте молодых бразильских пациентов. J Пародонтол. 1991; 62: 116–122. [PubMed] [Google Scholar]
41. Rylander H, Ramberg P, Blohme G, Lindhe J. Распространенность заболеваний пародонта у молодых диабетиков. Дж. Клин Пародонтол. 1987;14:38–43. [PubMed] [Google Scholar]
Дж. Клин Пародонтол. 1987;14:38–43. [PubMed] [Google Scholar]
42. Сеппала Б., Сеппала М., Айнамо Дж. Продольное исследование инсулинозависимого сахарного диабета и заболеваний пародонта. Дж. Клин Пародонтол. 1993; 20: 161–165. [PubMed] [Google Scholar]
43. Папапану ПН. Заболевания пародонта: Эпидемиология. Энн Пародонтолог. 1996; 1:1–36. [PubMed] [Google Scholar]
44. Emrich LJ, Shlossman M, Genco RJ. Заболевания пародонта при инсулиннезависимом сахарном диабете. J Пародонтол. 1991; 62: 123–131. [PubMed] [Академия Google]
45. Taylor GW, Burt BA, Becker MP, et al. Инсулиннезависимый сахарный диабет и прогрессирование потери альвеолярной кости в течение 2 лет. J Пародонтол. 1998; 69: 76–83. [PubMed] [Google Scholar]
46. Мили Б.Л., Оутс Т.В. Сахарный диабет и заболевания пародонта. J Пародонтол. 2006; 77: 1289–1303. [PubMed] [Google Scholar]
47. Loe H. Пародонтоз. Шестое осложнение сахарного диабета. Уход за диабетом. 1993; 16: 329–334. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
48. Нагиб Г., Аль-Машат Х., Деста Т., Грейвс Д.Т. Диабет продлевает воспалительную реакцию на бактериальный стимул из-за дисрегуляции цитокинов. Джей Инвест Дерматол. 2004; 123:87–92. [PubMed] [Google Scholar]
49. Salvi GE, Collins JG, Yalda B, et al. Характер моноцитарной секреции ФНО-альфа у пациентов с ИЗСД с заболеваниями пародонта. Дж. Клин Пародонтол. 1997; 24:8–16. [PubMed] [Google Scholar]
50. Salvi GE, Yalda B, Collins JG, et al. Медиаторный воспалительный ответ как потенциальный маркер риска заболеваний пародонта у больных инсулинозависимым сахарным диабетом. J Пародонтол. 1997; 68: 127–135. [PubMed] [Google Scholar]
51. Sorsa T, Ingman T, Suomalainen K, et al. Клеточный источник и ингибирование тетрациклином коллагеназы жидкости десневой борозды у пациентов с лабильным сахарным диабетом. Дж. Клин Пародонтол. 1992;19:146–149. [PubMed] [Google Scholar]
52. Monnier VM, Glomb M, Elgawish A, Sell DR. Механизм перекрестного связывания коллагена при диабете: загадка приближается к разрешению. Диабет. 1996; 45 (Приложение 3): S67–S72. [PubMed] [Google Scholar]
Диабет. 1996; 45 (Приложение 3): S67–S72. [PubMed] [Google Scholar]
53. Schmidt AM, Hori O, Cao R, et al. RAGE: новый клеточный рецептор для конечных продуктов гликирования. Диабет. 1996; 45 (Приложение 3): S77–S80. [PubMed] [Google Scholar]
54. Шмидт А.М., Ян С.Д., Вотье Дж.Л., Стерн Д. Активация рецептора конечных продуктов гликирования: механизм хронической сосудистой дисфункции при диабетической васкулопатии и атеросклерозе. Цирк рез. 1999;84:489–497. [PubMed] [Google Scholar]
55. Christgau M, Palitzsch KD, Schmalz G, Kreiner U, Frenzel S. Реакция заживления на нехирургическую пародонтальную терапию у пациентов с сахарным диабетом: клинические, микробиологические и иммунологические результаты. Дж. Клин Пародонтол. 1998; 25:112–124. [PubMed] [Google Scholar]
56. Seppala B, Ainamo J. Поэтапное последующее исследование влияния контролируемого и плохо контролируемого инсулинозависимого сахарного диабета. Дж. Клин Пародонтол. 1994;21:161–165. [PubMed] [Google Scholar]
57. Smith GT, Greenbaum CJ, Johnson BD, Persson GR. Краткосрочные ответы на пародонтальную терапию у пациентов с инсулинозависимым диабетом. J Пародонтол. 1996; 67: 794–802. [PubMed] [Google Scholar]
Smith GT, Greenbaum CJ, Johnson BD, Persson GR. Краткосрочные ответы на пародонтальную терапию у пациентов с инсулинозависимым диабетом. J Пародонтол. 1996; 67: 794–802. [PubMed] [Google Scholar]
58. Фариа-Алмейда Р., Наварро А., Басконес А. Клинические и метаболические изменения после традиционного лечения больных диабетом 2 типа с хроническим пародонтитом. J Пародонтол. 2006; 77: 591–598. [PubMed] [Google Scholar]
59. Киран М., Арпак Н., Унсал Э., Эрдоган М.Ф. Влияние улучшения состояния пародонта на метаболический контроль при сахарном диабете 2 типа. Дж. Клин Пародонтол. 2005; 32: 266–272. [PubMed] [Академия Google]
60. Stewart JE, Wager KA, Friedlander AH, Zadeh HH. Влияние пародонтологического лечения на гликемический контроль у пациентов с сахарным диабетом 2 типа. Дж. Клин Пародонтол. 2001; 28: 306–310. [PubMed] [Google Scholar]
61. Grossi SG, Skrepcinski FB, DeCaro T, et al. Лечение пародонтоза у диабетиков снижает гликированный гемоглобин. J Пародонтол. 1997; 68: 713–719. [PubMed] [Google Scholar]
1997; 68: 713–719. [PubMed] [Google Scholar]
62. Llambes F, Silvestre FJ, Hernandez-Mijares A, Guiha R, Caffesse R. Влияние нехирургического лечения пародонта с доксициклином или без него на пародонт пациентов с диабетом 1 типа. Дж. Клин Пародонтол. 2005;32:915–920. [PubMed] [Google Scholar]
63. Родригес Д.К., Таба М.Дж., Новаес А.Б., Соуза С.Л., Гризи М.Ф. Влияние нехирургической пародонтальной терапии на гликемический контроль у пациентов с сахарным диабетом 2 типа. J Пародонтол. 2003; 74: 136–137. [PubMed] [Google Scholar]
64. Berk BC, Weintraub WS, Alexander RW. Повышение С-реактивного белка при «активной» ИБС. Ам Джей Кардиол. 1990; 65: 168–172. [PubMed] [Google Scholar]
65. de Beer FC, Hind CR, Fox KM, et al. Измерение концентрации С-реактивного белка в сыворотке крови при ишемии и инфаркте миокарда. Бр Харт Дж. 1982;47:23–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Ridker PM, Cushman M, Stampfer MJ, Tracy RP, Hennekens CH. Воспаление, аспирин и риск сердечно-сосудистых заболеваний у практически здоровых мужчин. N Engl J Med. 1997; 336: 973–979. [PubMed] [Google Scholar]
Воспаление, аспирин и риск сердечно-сосудистых заболеваний у практически здоровых мужчин. N Engl J Med. 1997; 336: 973–979. [PubMed] [Google Scholar]
67. Ridker PM, Glynn RJ, Hennekens CH. С-реактивный белок увеличивает прогностическую ценность общего холестерина и холестерина ЛПВП при определении риска первого инфаркта миокарда. Тираж. 1998;97:2007–2011. [PubMed] [Академия Google]
68. Sesso HD, Buring JE, Rifai N, et al. С-реактивный белок и риск развития артериальной гипертензии. ДЖАМА. 2003; 290:2945–2951. [PubMed] [Google Scholar]
69. Армстронг Э.Дж., Морроу Д.А., Сабатин М.С. Воспалительные биомаркеры при острых коронарных синдромах: Часть IV: Матриксные металлопротеиназы и биомаркеры активации тромбоцитов. Тираж. 2006; 113:e382–e385. [PubMed] [Google Scholar]
70. Inoue T, Komoda H, Nonaka M, et al. Интерлейкин-8 как независимый предиктор отдаленных клинических исходов у пациентов с ишемической болезнью сердца. Int J Кардиол. 2008;124:319–325. [PubMed] [Google Scholar]
71. Хамфри Л.Л., Фу Р., Бакли Д.И., Фриман М., Хелфанд М. Заболеваемость периодонтом и ишемической болезнью сердца: систематический обзор и метаанализ. J Gen Intern Med. 2008;23:2079–2086. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Хамфри Л.Л., Фу Р., Бакли Д.И., Фриман М., Хелфанд М. Заболеваемость периодонтом и ишемической болезнью сердца: систематический обзор и метаанализ. J Gen Intern Med. 2008;23:2079–2086. [Бесплатная статья PMC] [PubMed] [Google Scholar]
72. D’Aiuto F, Parkar M, Nibali L, et al. Инфекции пародонта вызывают изменения в традиционных и новых сердечно-сосудистых факторах риска: результаты рандомизированного контролируемого клинического исследования. Am Heart J. 2006; 151: 977–984. [PubMed] [Google Scholar]
73. Paraskevas S, Huizinga JD, Loos BG. Систематический обзор и метаанализ С-реактивного белка в отношении периодонтита. Дж. Клин Пародонтол. 2008; 35: 277–290. [PubMed] [Google Scholar]
74. Tonetti MS, D’Aiuto F, Nibali L, et al. Лечение пародонтита и эндотелиальной функции. N Engl J Med. 2007; 356: 911–920. [PubMed] [Google Scholar]
75. Haraszthy VI, Zambon JJ, Trevisan M, Zeid M, Genco RJ. Выявление пародонтопатогенов в атероматозных бляшках. J Пародонтол. 2000;71:1554–1560. [PubMed] [Академия Google]
2000;71:1554–1560. [PubMed] [Академия Google]
76. Offenbacher S, Beck JD, Moss K, et al. Результаты исследования пародонтита и сосудистых заболеваний (PAVE): Пилотное многоцентровое рандомизированное контролируемое исследование по изучению эффектов периодонтальной терапии в модели вторичной профилактики сердечно-сосудистых заболеваний. J Пародонтол. 2009; 80: 190–201. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Peruzzo D, Benatti B, Ambrosano G, et al. Систематический обзор стресса и психологических факторов как возможных факторов риска заболеваний пародонта. J Пародонтол. 2007;78:1491–1504. [PubMed] [Google Scholar]
78. Genco RJ, Ho AW, Kopman J, et al. Модели для оценки роли стресса в заболеваниях пародонта. Энн Пародонтолог. 1998; 3: 288–302. [PubMed] [Google Scholar]
79. Kloostra P, Eber R, Inglehart M. Беспокойство, стресс, депрессия и реакция пациентов на пародонтологическое лечение: знания пародонтологов и профессиональное поведение. J Пародонтол. 2007; 78: 64–71. [PubMed] [Google Scholar]
J Пародонтол. 2007; 78: 64–71. [PubMed] [Google Scholar]
80. Монтейро да Силва А.М., Окли Д.А., Ньюман Х.Н., Нохл Ф.С., Ллойд Х.М. Психосоциальные факторы и быстро прогрессирующий пародонтит у взрослых. Дж. Клин Пародонтол. 1996;23:789–794. [PubMed] [Google Scholar]
81. Ng SK, Keung Leung W. Общественное исследование взаимосвязи между стрессом, преодолением трудностей, аффективными предрасположенностями и потерей пародонтального прикрепления. Сообщество Dent Oral Epidemiol. 2006; 34: 252–266. [PubMed] [Google Scholar]
82. Розания А.Е., Лоу К.Г., Маккормик К.М., Розания Д.А. Стресс, депрессия, кортизол и пародонтоз. J Пародонтол. 2009; 80: 260–266. [PubMed] [Google Scholar]
83. Elter JR, White BA, Gaynes BN, Bader JD. Связь клинической депрессии с результатами пародонтологического лечения. J Пародонтол. 2002; 73: 441–449.. [PubMed] [Google Scholar]
84. Коул-Кинг А., Хардинг К.Г. Психологические факторы и замедленное заживление хронических ран. Психозом Мед. 2001; 63: 216–220. [PubMed] [Google Scholar]
Психозом Мед. 2001; 63: 216–220. [PubMed] [Google Scholar]
85. Фини С. Связь между болью и негативным аффектом у пожилых людей: тревога как предиктор боли. J Тревожное расстройство. 2004; 18: 733–744. [PubMed] [Google Scholar]
86. Ah MK, Johnson GK, Kaldahl WB, Patil KD, Kalkwarf KL. Влияние курения на ответ на пародонтальную терапию. Дж. Клин Пародонтол. 1994;21:91–97. [PubMed] [Google Scholar]
87. Grossi SG, Genco RJ, Machtei EE, et al. Оценка риска заболеваний пародонта. II. Индикаторы риска потери альвеолярной кости. J Пародонтол. 1995; 66: 23–29. [PubMed] [Google Scholar]
88. Kaldahl WB, Johnson GK, Patil KD, Kalkwarf KL. Уровни потребления сигарет и реакция на пародонтальную терапию. J Пародонтол. 1996; 67: 675–681. [PubMed] [Google Scholar]
89. Kinane DF, Radvar M. Влияние курения на механическую и противомикробную пародонтальную терапию. J Пародонтол. 1997;68:467–472. [PubMed] [Google Scholar]
90. Ryder MI, Pons B, Adams D, et al. Влияние курения на местную доставку доксициклина с контролируемым высвобождением по сравнению с скейлингом и выравниванием корней. Дж. Клин Пародонтол. 1999; 26: 683–691. [PubMed] [Google Scholar]
Влияние курения на местную доставку доксициклина с контролируемым высвобождением по сравнению с скейлингом и выравниванием корней. Дж. Клин Пародонтол. 1999; 26: 683–691. [PubMed] [Google Scholar]
91. Томар С.Л., Асма С. Пародонтит, связанный с курением, в США: результаты исследования NHANES III. Национальное обследование здоровья и питания. J Пародонтол. 2000; 71: 743–751. [PubMed] [Академия Google]
92. Arbes SJ., Jr Agustsdottir H, Slade GD. Табачный дым в окружающей среде и пародонтоз в США. Am J Общественное здравоохранение. 2001; 91: 253–257. [Бесплатная статья PMC] [PubMed] [Google Scholar]
93. Yamamoto Y, Nishida N, Tanaka M, et al. Взаимосвязь между пассивным и активным курением оценивали по котинину слюны и пародонтиту. Дж. Клин Пародонтол. 2005; 32:1041–1046. [PubMed] [Google Scholar]
94. Бергстром Дж., Пребер Х. Употребление табака как фактор риска. J Пародонтол. 1994;65:545–550. [PubMed] [Google Scholar]
95. Grossi SG, Zambon JJ, Ho AW, et al. Оценка риска заболеваний пародонта. I. Индикаторы риска потери привязанности. J Пародонтол. 1994; 65: 260–267. [PubMed] [Google Scholar]
Оценка риска заболеваний пародонта. I. Индикаторы риска потери привязанности. J Пародонтол. 1994; 65: 260–267. [PubMed] [Google Scholar]
96. Trombelli L, Cho KS, Kim CK, Scapoli C, Scabbia A. Нарушение реакции заживления дефектов фуркации периодонта после хирургического удаления лоскута у курильщиков. Контролируемое клиническое исследование. Дж. Клин Пародонтол. 2003; 30:81–87. [PubMed] [Академия Google]
97. Содер Б., Недлич У., Джин Л.Дж. Продольный эффект нехирургического лечения и системного метронидазола в течение 1 недели у курильщиков и некурящих с рефрактерным пародонтитом: 5-летнее исследование. J Пародонтол. 1999; 70: 761–771. [PubMed] [Google Scholar]
98. Matarazzo F, Figueiredo LC, Cruz SE, Faveri M, Feres M. Клинические и микробиологические преимущества системного метронидазола и амоксициллина при лечении курильщиков с хроническим периодонтитом: рандомизированное плацебо-контролируемое исследование . Дж. Клин Пародонтол. 2008; 35: 885–89.6. [PubMed] [Google Scholar]
99. Machion L, Andia DC, Lecio G, et al. Местно доставляемый доксициклин в качестве дополнительной терапии к скейлингу и выравниванию корней при лечении курильщиков: 2-летнее наблюдение. J Пародонтол. 2006; 77: 606–613. [PubMed] [Google Scholar]
Machion L, Andia DC, Lecio G, et al. Местно доставляемый доксициклин в качестве дополнительной терапии к скейлингу и выравниванию корней при лечении курильщиков: 2-летнее наблюдение. J Пародонтол. 2006; 77: 606–613. [PubMed] [Google Scholar]
100. Пакетт Д., Орингер Р., Лессем Дж. и соавт. Местно поставляемые микросферы миноциклина для лечения пародонтита у курильщиков. Дж. Клин Пародонтол. 2003; 30: 787–794. [PubMed] [Google Scholar]
101. Tomasi C, Wennstrom JL. Местно доставляемый доксициклин улучшает заживление после нехирургической пародонтальной терапии у курильщиков. Дж. Клин Пародонтол. 2004;31:589–595. [PubMed] [Google Scholar]
102. Centers for Disease Control Cigarette Smoking Among Adults – United States, 2000 Morb Mortal Wkly Rep Surveill Summ 20025129642–645. Доступно по адресу: http://www.cdc.gov/mmwr/preview /mmwrhtml/mm5129a3.htmПроверено 17 мая 2010 г. [PubMed] [Google Scholar]
103. Bain CA. Курение и отторжение имплантата – преимущества протокола отказа от курения. Оральные челюстно-лицевые имплантаты Int J. 1996; 11: 756–759. [PubMed] [Google Scholar]
Оральные челюстно-лицевые имплантаты Int J. 1996; 11: 756–759. [PubMed] [Google Scholar]
104. Томар С.Л., Хустен С.Г., Мэнли М.В. Советуют ли стоматологи и врачи курильщикам бросить курить? J Am Dent Assoc. 1996;127:259–265. [PubMed] [Google Scholar]
105. Nordland P, Garrett S, Kiger R, et al. Эффект контроля зубного налета и санации корней моляров. Дж. Клин Пародонтол. 1987; 14: 231–236. [PubMed] [Google Scholar]
106. Клаффи Н., Эгельберг Дж. Клинические характеристики участков пародонта с потерей прикрепления зонда после первоначального лечения пародонта. Дж. Клин Пародонтол. 1994; 21: 670–679. [PubMed] [Google Scholar]
107. Waerhaug J. Заживление денто-эпителиального соединения после удаления поддесневого налета. II: Как видно на удаленных зубах. J Пародонтол. 1978;49:119–134. [PubMed] [Google Scholar]
108. Waerhaug J. Заживление денто-эпителиального соединения после удаления поддесневого зубного налета. I. Как наблюдается в материале биопсии человека. J Пародонтол. 1978; 49:1–8. [PubMed] [Google Scholar]
J Пародонтол. 1978; 49:1–8. [PubMed] [Google Scholar]
109. Fleischer HC, Mellonig JT, Brayer WK, Gray JL, Barnett JD. Эффективность удаления зубного камня и полировки корней в многокорневых зубах. J Пародонтол. 1989; 60: 402–409. [PubMed] [Google Scholar]
110. Брайер В.К., Меллониг Дж.Т., Данлэп Р.М., Маринак К.В., Карсон Р.Е. Эффективность масштабирования и выравнивания корня: влияние доступа к поверхности корня и опыта оператора. J Пародонтол. 1989;60:67–72. [PubMed] [Google Scholar]
111. Magnusson I, Lindhe J, Yoneyama T, Liljenberg B. Реколонизация поддесневой микробиоты после удаления зубного камня в глубоких карманах. Дж. Клин Пародонтол. 1984; 11: 193–207. [PubMed] [Google Scholar]
112. Mousques T, Listgarten MA, Phillips RW. Влияние скейлинга и полировки корней на состав поддесневой микробной флоры человека. J Периодонтальная Рез. 1980; 15: 144–151. [PubMed] [Google Scholar]
113. Sbordone L, Ramaglia L, Gulletta E, Iacono V. Реколонизация поддесневой микрофлоры после удаления зубного камня и полировки корней при пародонтите человека. J Пародонтол. 1990;61:579–584. [PubMed] [Google Scholar]
J Пародонтол. 1990;61:579–584. [PubMed] [Google Scholar]
114. Гарджуло А.В. Размеры и соотношения зубодесневого соединения у человека. J Пародонтол. 1961; 32: 261–267. [Google Scholar]
115. Вацек Дж. С., Гер М. Е., Асад Д. А., Ричардсон А. С., Джамбарреси Л. И. Размеры зубодесневого соединения человека. Int J Пародонтология Restorative Dent. 1994; 14: 154–165. [PubMed] [Google Scholar]
116. Newcomb GM. Взаимосвязь между расположением поддесневых краев коронки и воспалением десны. J Пародонтол. 1974;45:151–154. [PubMed] [Google Scholar]
117. Valderhaug J, Birkeland JM. Состояние пародонта у пациентов через 5 лет после установки несъемных протезов. Глубина кармана и потеря прикрепления. J Оральная реабилитация. 1976; 3: 237–243. [PubMed] [Google Scholar]
118. Valderhaug J, Ellingsen JE, Jokstad A. Гигиена полости рта, заболевания пародонта и кариозные поражения у пациентов, лечившихся мостовидными протезами. 15-летнее клинико-рентгенологическое наблюдение. Дж. Клин Пародонтол. 1993; 20: 482–489.. [PubMed] [Google Scholar]
Дж. Клин Пародонтол. 1993; 20: 482–489.. [PubMed] [Google Scholar]
119. Gunay H, Seeger A, Tschernitschek H, Geurtsen W. Размещение линии препарирования и здоровье пародонта – проспективное двухлетнее клиническое исследование. Int J Пародонтология Restorative Dent. 2000; 20: 171–181. [PubMed] [Google Scholar]
120. Davies SJ, Gray RJ, Linden GJ, James JA. Окклюзионные аспекты пародонтологии. Бр Дент Дж. 2001; 191: 597–604. [PubMed] [Google Scholar]
121. Показатель окклюзионного травматизма у больных хроническим пародонтитом. Американская академия пародонтологии. J Пародонтол. 2000; 71 (5 Дополнение): 873–875. [PubMed] [Академия Google]
122. Fleszar TJ, Knowles JW, Morrison EC, et al. Подвижность зубов и пародонтотерапия. Дж. Клин Пародонтол. 1980; 7: 495–505. [PubMed] [Google Scholar]
123. Vollmer WH, Rateitschak KH. Влияние окклюзионной коррекции обтачиванием на гингивит и подвижность травмированных зубов. Дж. Клин Пародонтол. 1975; 2: 113–125. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
124. Burgett FG, Ramfjord SP, Nissle RR, et al. Рандомизированное исследование коррекции прикуса при лечении пациентов с пародонтитом. Дж. Клин Пародонтол. 1992;19:381–387. [PubMed] [Google Scholar]
125. Slots J. Системные антибиотики в пародонтологии. J Пародонтол. 2004;7(5):1553–1565. [PubMed] [Google Scholar]
126. Уокер CB. Приобретение антибиотикорезистентности у пародонтальной микрофлоры. Пародонтология 2000. 1996;10:79–88. [PubMed] [Google Scholar]
127. Paster BJ, Boches SK, Galvin JL, et al. Бактериальное разнообразие поддесневого налета человека. J Бактериол. 2001; 183:3370–3383. [Бесплатная статья PMC] [PubMed] [Google Scholar]
128. Sedlacek MJ, Walker C. Устойчивость к антибиотикам в модели поддесневой биопленки in vitro. Оральный микробиол иммунол. 2007; 22: 333–339. [Бесплатная статья PMC] [PubMed] [Google Scholar]
129. Shaddox LM, Walker C. Микробиологическое тестирование в пародонтологии: ценность, ограничения и будущие направления. Пародонтология 2000. 2009;50:25–38. [PubMed] [Google Scholar]
Пародонтология 2000. 2009;50:25–38. [PubMed] [Google Scholar]
130. Руни Дж., Уэйд В.Г., Спраг С.В., Ньюкомб Р.Г., Эдди М. Дополнительные эффекты нехирургической периодонтальной терапии системным метронидазолом и амойциллином по отдельности и в комбинации. Плацебо-контролируемое исследование. Дж. Клин Пародонтол. 2002;29: 342–350. [PubMed] [Google Scholar]
131. Winkel EG, van Winkelhoff AJ, Barendregt DS, et al. Клинические и микробные эффекты начальной пародонтальной терапии в сочетании с амоксициллином и клавулановой кислотой у пациентов с пародонтитом взрослых. Рандомизированное двойное слепое плацебо-контролируемое исследование. Дж. Клин Пародонтол. 1999; 26: 461–468. [PubMed] [Google Scholar]
132. Винкель Э.Г., ван Винкельхофф А.Дж., Тиммерман М.Ф., ван дер Вельден У., ван дер Вейден К.А. Амоксициллин плюс метронидазол в лечении взрослых пациентов с пародонтитом. Двойное слепое плацебо-контролируемое исследование. Дж. Клин Пародонтол. 2001;28:296–305. [PubMed] [Google Scholar]
133. Winkel EG, van Winkelhoff AJ, van der Velden U. Дополнительные клинические и микробиологические эффекты амоксициллина и метронидазола после начальной периодонтальной терапии. Дж. Клин Пародонтол. 1998; 25: 857–865. [PubMed] [Google Scholar]
Winkel EG, van Winkelhoff AJ, van der Velden U. Дополнительные клинические и микробиологические эффекты амоксициллина и метронидазола после начальной периодонтальной терапии. Дж. Клин Пародонтол. 1998; 25: 857–865. [PubMed] [Google Scholar]
134. Уокер С., Карпиния К. Рациональное использование антибиотиков в пародонтологии. J Пародонтол. 2002; 73: 1189–1197. [Google Scholar]
135. Уокер С., Карпиния К., Бэни П. Химиотерапия: антибиотики и противомикробные препараты. Пародонтология 2000. 2004;36:146–165. [PubMed] [Академия Google]
136. Слоты Дж, Фейк Д, Рамс ТЭ. Распространенность и антимикробная чувствительность Enterobacteriaceae, Pseudomonadaceae и Acinobacter при пародонтите человека. Оральный микробиол иммунол. 1990; 5: 149–154. [PubMed] [Google Scholar]
137. Lowenguth R, Morad V, Gandini L, et al. Влияние местного введения тетрациклина на прогрессирование ювенильного пародонтита. Джей Дент Рез. Абстр. 1993451 (72): 160. [Google Scholar]
138. Vandekerckhove BN, Quirynen M, van Steenberghe D. Использование тетрациклинсодержащих волокон с контролируемым высвобождением при лечении рефрактерного периодонтита. J Пародонтол. 1997;68:353–361. [PubMed] [Google Scholar]
Vandekerckhove BN, Quirynen M, van Steenberghe D. Использование тетрациклинсодержащих волокон с контролируемым высвобождением при лечении рефрактерного периодонтита. J Пародонтол. 1997;68:353–361. [PubMed] [Google Scholar]
139. Rams TE, Slots J. Локальная доставка противомикробных препаратов в пародонтальный карман. В: Slots J, Rams T, редакторы. Пародонтология 2000. Копенгаген: Munksgaard; 1996. С. 139–159. [PubMed] [Google Scholar]
140. Machion L, Andia DC, Saito D, et al. Микробиологические изменения при применении местно доставляемого доксициклина при пародонтологическом лечении курильщиков. J Пародонтол. 2004; 75: 1600–1604. [PubMed] [Google Scholar]
141. Shaddox LM, Andia DC, Casati MZ, et al. Микробиологические изменения после местного применения доксициклина у курильщиков: 15-месячное наблюдение. J Пародонтол. 2007; 78: 2143–2149. [PubMed] [Google Scholar]
142. Machion L, Andia DC, Benatti BB, et al. Местно доставляемый доксициклин в качестве дополнительной терапии к скейлингу и выравниванию корней при лечении курильщиков: клиническое исследование. J Пародонтол. 2004; 75: 464–469. [PubMed] [Google Scholar]
J Пародонтол. 2004; 75: 464–469. [PubMed] [Google Scholar]
143. Wennstrom JL, Newman HN, MacNeill SR, et al. Применение местного доксициклина в нехирургическом лечении хронического пародонтита. Сравнительное многоцентровое исследование двух подходов к лечению. Дж. Клин Пародонтол. 2001; 28: 753–761. [PubMed] [Академия Google]
144. Голуб Л.М., Чансио С., Рамамамурти Н.С., Леунг М., Макнамара Т.Ф. Терапия низкими дозами доксициклина: влияние на активность коллагеназы десневой и десневой жидкости у человека. J Периодонтальная Рез. 1990; 25: 321–330. [PubMed] [Google Scholar]
145. Preshaw PM, Hefti AF, Jepsen S, et al. Субантимикробная доза доксициклина в качестве дополнительного лечения пародонтита. Обзор. Дж. Клин Пародонтол. 2004; 31: 697–707. [PubMed] [Google Scholar]
146. Cobb CM. Лазеры в пародонтологии: обзор литературы. J Пародонтол. 2006; 77: 545–564. [PubMed] [Академия Google]
147. Беккер В., Беккер Б.Е., Берг Л.Е. Лечение пародонта без поддерживающей терапии. Ретроспективное исследование у 44 пациентов. J Пародонтол. 1984; 55: 505–509. [PubMed] [Google Scholar]
Ретроспективное исследование у 44 пациентов. J Пародонтол. 1984; 55: 505–509. [PubMed] [Google Scholar]
148. Wilson TG., Jr Glover ME, Malik AK, Schoen JA, Dorsett D. Потеря зубов у поддерживающих пациентов в частной пародонтологической практике. J Пародонтол. 1987; 58: 231–235. [PubMed] [Google Scholar]
149. Axelsson P, Lindhe J. Значение поддерживающей терапии при лечении заболеваний пародонта. Дж. Клин Пародонтол. 1981;8:281–294. [PubMed] [Google Scholar]
150. Мендоза А.Р., Ньюкомб Г.М., Никсон К.С. Соблюдение поддерживающей пародонтологической терапии. J Пародонтол. 1991; 62: 731–736. [PubMed] [Google Scholar]
151. Wilson TG, Jr, Glover ME, Schoen J, Baus C, Jacobs T. Соблюдение поддерживающей терапии в частной пародонтологической практике. J Пародонтол. 1984; 55: 468–473. [PubMed] [Google Scholar]
Пародонтит, связанный с дефицитом плазминогена: клинический случай | BMC Здоровье полости рта
- История болезни
- Открытый доступ
- Опубликовано:
- Sarah H Neering 1 ,
- Sabine Adyani-Fard 1 ,
- Astrid Klocke 1 ,
- Stefan Rüttermann 2 ,
- Thomas F Flemmig 3 &
- …
- Томас Бейклер 1,4
BMC Здоровье полости рта том 15 , номер статьи: 59 (2015) Процитировать эту статью
-
4900 доступов
-
8 цитирований
-
4 Альтметрика
-
Сведения о показателях
Abstract
История вопроса
Дефицит плазминогена является редким аутосомно-рецессивным заболеванием, которое связано с агрессивным пародонтитом и увеличением десен. Описанные ранее методы лечения периодонтита, связанного с дефицитом плазминогена, показали ограниченный успех. Это первый клинический случай, указывающий на успешный терапевтический подход, состоящий из нехирургической над- и поддесневой обработки в сочетании с дополнительной системной антибиотикотерапией и строгим поддерживающим пародонтологическим режимом в течение периода наблюдения 4 года.
Описанные ранее методы лечения периодонтита, связанного с дефицитом плазминогена, показали ограниченный успех. Это первый клинический случай, указывающий на успешный терапевтический подход, состоящий из нехирургической над- и поддесневой обработки в сочетании с дополнительной системной антибиотикотерапией и строгим поддерживающим пародонтологическим режимом в течение периода наблюдения 4 года.
Представление клинического случая
При внутриротовом осмотре 17-летней турчанки с тяжелым дефицитом плазминогена было выявлено генерализованное увеличение глубины кармана при зондировании от 6 до 9 мм, кровоточивость при зондировании более 30%, генерализованная подвижность зубов и гиперплазия десен. Потеря альвеолярной кости колеблется от 30% до 50%. Клиническая потеря прикрепления соответствовала глубине зондирования кармана. Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis, Treponema denticola, Prevotella intermedia, Prevotella nigrescens и Eikenella corrodens были обнаружены с помощью полимеразной цепной реакции в реальном времени. Лечение пародонта состояло из полной дезинфекции полости рта и дополнительного системного введения амоксициллина (500 мг три раза в день) и метронидазола (400 мг три раза в день). Проводился строгий режим поддерживающей пародонтальной терапии каждые три месяца в виде над- и поддесневой санации. Сообщаемая терапия значительно улучшила здоровье пародонта и остановила прогрессирование заболевания. Внутриротовое обследование в конце периода наблюдения через 3,5 года после нехирургического пародонтологического лечения показало генерализованное уменьшение глубины зондирования кармана в пределах от 1 до 6 мм, кровоточивость при зондировании менее 30 % и класс подвижности зубов I и II. Кроме того, микробиологический анализ показывает отсутствие Porphyromonas gingivalis , Prevotella intermedia и Treponema denticola после лечения .
Лечение пародонта состояло из полной дезинфекции полости рта и дополнительного системного введения амоксициллина (500 мг три раза в день) и метронидазола (400 мг три раза в день). Проводился строгий режим поддерживающей пародонтальной терапии каждые три месяца в виде над- и поддесневой санации. Сообщаемая терапия значительно улучшила здоровье пародонта и остановила прогрессирование заболевания. Внутриротовое обследование в конце периода наблюдения через 3,5 года после нехирургического пародонтологического лечения показало генерализованное уменьшение глубины зондирования кармана в пределах от 1 до 6 мм, кровоточивость при зондировании менее 30 % и класс подвижности зубов I и II. Кроме того, микробиологический анализ показывает отсутствие Porphyromonas gingivalis , Prevotella intermedia и Treponema denticola после лечения .
Заключение
Дополнительное лечение антибиотиками может изменить микробиом полости рта и, таким образом, воспалительную реакцию заболеваний пародонта, связанную с дефицитом плазминогена, и снизить риск образования псевдомембран и прогрессирующей потери прикрепления.
Этот клинический случай показывает, что пациентам с дефицитом плазминогена может помочь нехирургическое пародонтологическое лечение в сочетании с дополнительной терапией антибиотиками и строгой поддерживающей пародонтальной терапией.
Отчеты экспертной оценки
Исходная информация
Плазминоген (PLG) является проферментом плазмина и преимущественно синтезируется в печени. Хотя роль плазмина во внутри- и внесосудистом фибринолизе хорошо определена, он также действует как протеолитический фактор широкого спектра действия, либо непосредственно разрушая белки внеклеточного матрикса, т.е. ламинина, фибронектина и протеогликанов, а также опосредованно за счет активации латентных металлопротеиназ [1,2]. Таким образом, он выполняет важные функции в тканевом гомеостазе, т.е. ремоделирование, ангиогенез и заживление ран [3-5]. Кроме того, было обнаружено, что плазмин играет важную роль в защите хозяина от инфекций [1].
Дефицит плазминогена является редким (1,6 на 1 миллион человек) аутосомно-рецессивным заболеванием, вызываемым гомозиготными или сложными гетерозиготными мутациями гена плазминогена PLG 6q26. Различают два типа дефицита плазминогена: гипоплазминогенемию (дефицит ПЛГ I типа), при которой снижены уровень и активность ПЛГ, и дисплазминогенемию (дефицит ПЛГ II типа), при которой уровень иммунореактивного ПЛГ находится в пределах нормы, но специфическая активность PLG снижается [6-9].
Клинические симптомы дефицита PLG типа I включают рецидивирующие, древесноподобные (деревянистые) псевдомембраны на слизистых оболочках глаз (87% случаев), верхних и нижних дыхательных путях (33%), влагалище (19%) и желудочно-кишечном тракте. 3%) [9]. Кроме того, примерно одна треть пораженных лиц страдает псевдомембранами ротовой полости [7,10,11].
Деревянистый периодонтит характеризуется увеличением десны и выраженной потерей прикрепления, что связано с накоплением амилоидоподобного материала в собственной пластинке [2]. Подходы к лечению пародонтита, связанного с дефицитом PLG, включали хирургическую и нехирургическую пародонтальную терапию. Пародонтальная хирургия без предшествующей над- и поддесневой обработки первоначально казалась многообещающей, но в конечном итоге привела к отрастанию псевдомембраны. Описано пародонтальное нехирургическое лечение отдельно, то есть без пародонтальной хирургии или в сочетании с полосканием рта хлоргексидином, местным введением плазминогена или гепарина или введением системных антибиотиков. Однако эти методы лечения не смогли остановить прогрессирование заболеваний пародонта у пациентов с дефицитом PLG I типа [8,12,2].
Подходы к лечению пародонтита, связанного с дефицитом PLG, включали хирургическую и нехирургическую пародонтальную терапию. Пародонтальная хирургия без предшествующей над- и поддесневой обработки первоначально казалась многообещающей, но в конечном итоге привела к отрастанию псевдомембраны. Описано пародонтальное нехирургическое лечение отдельно, то есть без пародонтальной хирургии или в сочетании с полосканием рта хлоргексидином, местным введением плазминогена или гепарина или введением системных антибиотиков. Однако эти методы лечения не смогли остановить прогрессирование заболеваний пародонта у пациентов с дефицитом PLG I типа [8,12,2].
В данном клиническом случае представлено лечение пациентки с тяжелым генерализованным пародонтитом, модифицированным системными факторами (дефицит PLG I типа), с использованием метода полной дезинфекции полости рта в сочетании со специфической дополнительной системной антибактериальной терапией, направленной на изменение микробиома полости рта. .
.
Описание случая
Представленный пациент — женщина из Турции с диагнозом дефицита PLG I типа (активность плазминогена 2%). У обоих ее братьев и сестер также был диагностирован дефицит PLG I типа. В возрасте 9 летлет, пациент поступил с лигнозным конъюнктивитом на кафедру педиатрии Дюссельдорфского университета, где были обнаружены дополнительные деревянистые поражения на слизистой оболочке среднего уха, дыхательных путей, влагалища и гиперплазия десен.
Внутриротовое обследование в отделении пародонтологии Дюссельдорфского университета выявило эритематозную и гиперплазированную десну на верхней и нижней челюсти и подвижность 3 класса всех молочных зубов [13]. Панорамная рентгенограмма показала тяжелую генерализованную потерю альвеолярной кости (рис. 1). Гистологическая оценка биоптата десны, взятого буккально со второго молочного моляра на правой нижней челюсти, показала гиперплазию реактивного плоского эпителия с локализованным отложением фибрина и массивными изъязвлениями. Поскольку пациент не явился на повторные приемы, пародонтологическое лечение в то время не проводилось.
Поскольку пациент не явился на повторные приемы, пародонтологическое лечение в то время не проводилось.
Панорамная рентгенограмма в возрасте 9 лет: признаки нелеченного пародонтоза.
Изображение в полный размер
Когда ей было 13 лет, пациентка снова обратилась за пародонтологической оценкой. В то время пациент получал системную иммуносупрессивную терапию микофенолат-мофетилом для лечения тяжелой пневмонии и гематокольпоса. Кроме того, она получала длительную антибактериальную терапию ципрофлоксацином и пиразиномидом по поводу легочной инфекции полирезистентными бактериями туберкулеза. При осмотре пародонта выявлены признаки тяжелого генерализованного пародонтита с гиперплазией десен, изъязвлением и фибринозными псевдомембранами. Панорамная рентгенограмма показала генерализованную горизонтальную потерю кости от 10% до 30% на верхних и нижних передних зубах и вертикальную потерю альвеолярной кости на всех первых молярах (Рисунок 2). Выполнена четырехквадрантная над- и поддесневая санация. Пациент не вернулся для поддерживающей пародонтальной терапии.
Выполнена четырехквадрантная над- и поддесневая санация. Пациент не вернулся для поддерживающей пародонтальной терапии.
Панорамная рентгенограмма в возрасте 13 лет: пародонтологическое лечение не проводилось с 9 лет.
Изображение в натуральную величину
В возрасте 16 лет пациент вернулся. Клиническое обследование выявило генерализованную повышенную подвижность зубов и гиперплазию десен (рис. 3). Пациентка предъявляла жалобы на выраженный неприятный запах изо рта и нарушение эстетики из-за гиперплазии десны. По сравнению с клинической и рентгенологической оценкой в возрасте 13 лет было отмечено прогрессирование прикрепления и потеря костной массы (рис. 4 и 5). Микробиологический анализ над- и поддесневого налета [14] выявил внутриротовое присутствие Porphyromonas gingivalis, Eikenella corrodens, Prevotella intermedia, Prevotella nigrescens, Tannerella forsythensis, и Treponema denticola. Aggregatibacter actinomycetemcomitans не обнаружен. Комбинированный образец над- и поддесневого зубного налета перед нехирургической пародонтальной терапией был взят из самого глубокого пародонтального кармана в каждом секстанте, и микробные виды были обнаружены с помощью полимеразной цепной реакции (ПЦР).
Комбинированный образец над- и поддесневого зубного налета перед нехирургической пародонтальной терапией был взят из самого глубокого пародонтального кармана в каждом секстанте, и микробные виды были обнаружены с помощью полимеразной цепной реакции (ПЦР).
Florida Probe Пародонтальная карта на исходном уровне: пародонтальное измерение перед полной над- и поддесневой санацией полости рта в сочетании с дополнительной терапией антибиотиками.
Изображение в натуральную величину
Фото 4Панорамная рентгенограмма в возрасте 16 лет: через три года после обычной квадрантной над- и поддесневой санации без какой-либо поддерживающей пародонтальной терапии.
Изображение в натуральную величину
Фото 5 Внутриротовые фотографии в возрасте 16 лет: через три года после обычной квадрантной над- и поддесневой санации без какой-либо поддерживающей пародонтальной терапии.
Полноразмерное изображение
Над- и поддесневая санация всех зубов была выполнена под местной анестезией в течение 24 часов, и были удалены верхние правые и оба нижних первых моляра. Пациенту были даны инструкции по гигиене полости рта. Дополнительная антимикробная терапия включала системное введение амоксициллина (500 мг 3 раза в день) и метронидазола (400 мг 3 раза в день) и полоскание дважды в день 0,2% раствором хлоргексидина диглюконата в течение двух недель [15-17]. Через восемь недель после лечения гиперплазия десны, глубина зондирования кармана и кровоточивость при зондировании заметно уменьшились (рис. 6). Пациент получал поддерживающую пародонтальную терапию каждые три месяца (рис. 7). При контрольном осмотре в возрасте 18 лет были выявлены лишь минимальные признаки остаточной гиперплазии десны (область 32–42) и признаки остановленного периодонтита (рис. 8 и 9).). Микробиологический анализ показал отсутствие в ротовой полости Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis, Prevotella intermedia и Treponema denticola . Интересно, что клинические признаки дефицита PLG типа I в ухе, урогенитальном тракте и верхних дыхательных путях, а также в глазах показали положительные изменения одновременно после пародонтальной терапии. С тех пор ситуация оказалась стабильной (Рисунок 10), и в возрасте 19 лет было принято решение улучшить эстетику в области верхних передних зубов путем прямой реставрации композитом (Filtek Supreme XTE, 3 M Espe, Зеефельд, Германия). В нижнепереднем отделе использовались прямые композитные реставрации (Filtek Supreme XTE, 3 M Espe, Зеефельд, Германия) в сочетании с армированными стекловолокном (Ribbond THM, Ribbond, Сиэтл, США) композитными промежуточными звеньями (рис. 11, 12 и 13).
Интересно, что клинические признаки дефицита PLG типа I в ухе, урогенитальном тракте и верхних дыхательных путях, а также в глазах показали положительные изменения одновременно после пародонтальной терапии. С тех пор ситуация оказалась стабильной (Рисунок 10), и в возрасте 19 лет было принято решение улучшить эстетику в области верхних передних зубов путем прямой реставрации композитом (Filtek Supreme XTE, 3 M Espe, Зеефельд, Германия). В нижнепереднем отделе использовались прямые композитные реставрации (Filtek Supreme XTE, 3 M Espe, Зеефельд, Германия) в сочетании с армированными стекловолокном (Ribbond THM, Ribbond, Сиэтл, США) композитными промежуточными звеньями (рис. 11, 12 и 13).
Периодонтальная карта Florida Probe на момент повторного осмотра: через шесть недель после полной над- и поддесневой обработки полости рта в сочетании с дополнительной терапией антибиотиками.
Изображение в натуральную величину
Рис. 7
7 Пародонтальная карта Florida Probe Поддерживающая пародонтологическая терапия: 12 месяцев после нехирургической пародонтальной терапии.
Изображение в полный размер
Рис. 8Внутриротовые фотографии в возрасте 18 лет: через два года после полной над- и поддесневой обработки полости рта в сочетании с дополнительной терапией антибиотиками и поддерживающей терапией пародонта каждые 3 месяца.
Изображение в натуральную величину
Рисунок 9Пародонтальная карта Florida Probe в возрасте 18 лет: Пародонтальная поддерживающая терапия через два года после полной над- и поддесневой обработки полости рта в сочетании с дополнительной терапией антибиотиками и поддерживающей пародонтальной терапией каждые 3 месяца.
Изображение в натуральную величину
Рис. 10 Florida Probe Пародонтальная карта в конце периода наблюдения: 3,5 года после полной над- и поддесневой обработки полости рта в сочетании с дополнительной антибактериальной терапией и поддерживающей пародонтальной терапией каждые 3 месяца.
Изображение в натуральную величину
Рисунок 11Внутриротовые фотографии в возрасте 19 лет: через три года после полной обработки над- и поддесневой полости рта в сочетании с дополнительной терапией антибиотиками и поддерживающей терапией пародонта каждые 3 месяца.
Изображение в натуральную величину
Рисунок 12Интраоральные фотографии в возрасте 19 лет: 3.5. лет после полной над- и поддесневой обработки полости рта в сочетании с дополнительной антибактериальной терапией и поддерживающей пародонтальной терапией каждые 3 месяца. Ситуация после прямой реставрации композитом в верхней и нижней передних отделах. Примечание: фотографии сделаны сразу после поддерживающей пародонтальной терапии.
Изображение в натуральную величину
Рисунок 13 Панорамная рентгенограмма в возрасте 19 лет: через 3,5 года после полной над- и поддесневой обработки полости рта в сочетании с дополнительной терапией антибиотиками и поддерживающей терапией пародонта каждые 3 месяца.
Увеличить
Обсуждение
Клинические признаки деревянистого периодонтита характеризуются агрессивной деструкцией тканей пародонта и потерей альвеолярной кости и зубов. Однако точная патофизиология деревянистого периодонтита остается неясной [18,1]. Данные in vitro и исследования на животных показали, что изменения в механизмах восстановления тканей и защитных механизмах хозяина ответственны за начало и прогрессирование деструкции периодонта [1,19]. Локальный внеклеточный фибринолиз плазмином необходим для начального удаления богатого фибрином матрикса, а также для ремоделирования грануляционной ткани и завершения заживления ран [9,20,5]. Нарушение пути из-за гипоплазминогенемии приводит к накоплению фибрина и усилению воспалительной реакции. Следовательно, процесс заживления раны останавливается на стадии образования грануляционной ткани и клеточного протеолиза, что в дальнейшем может способствовать инвазии возбудителей. Этот процесс особенно выражен в слизистых оболочках, таких как ткани пародонта [12,20]. Тот факт, что только у 32% пациентов с дефицитом PLG I типа развивается деревянистый периодонтит, убедительно подтверждает мнение о том, что внешние триггеры, т. е. травма или инфекция, могут играть дополнительную важную роль в патогенезе этого заболевания [21,10,9].,22,11,2]. Таким образом, снижение бактериальной нагрузки путем дополнительной системной антибактериальной терапии представляется разумной стратегией терапии для дальнейшего уменьшения воспаления и, следовательно, прогрессирования заболевания. Хорошо известно, что биопленочные бактерии проявляют гораздо большую устойчивость к антибиотикам, чем их свободноживущие собратья. Одной из возможных причин такой повышенной устойчивости является барьер проникновения, который биопленки представляют противомикробным препаратам. Таким образом, полное разрушение внутриротовой биопленки в течение короткого периода времени является необходимым условием максимально возможной эффективности антибиотиков. По этой причине подход к применяемой терапии соответствовал концепции полной дезинфекции полости рта, то есть полной над- и поддесневой санации в течение 24 часов с последующей дополнительной системной антибактериальной терапией.
Тот факт, что только у 32% пациентов с дефицитом PLG I типа развивается деревянистый периодонтит, убедительно подтверждает мнение о том, что внешние триггеры, т. е. травма или инфекция, могут играть дополнительную важную роль в патогенезе этого заболевания [21,10,9].,22,11,2]. Таким образом, снижение бактериальной нагрузки путем дополнительной системной антибактериальной терапии представляется разумной стратегией терапии для дальнейшего уменьшения воспаления и, следовательно, прогрессирования заболевания. Хорошо известно, что биопленочные бактерии проявляют гораздо большую устойчивость к антибиотикам, чем их свободноживущие собратья. Одной из возможных причин такой повышенной устойчивости является барьер проникновения, который биопленки представляют противомикробным препаратам. Таким образом, полное разрушение внутриротовой биопленки в течение короткого периода времени является необходимым условием максимально возможной эффективности антибиотиков. По этой причине подход к применяемой терапии соответствовал концепции полной дезинфекции полости рта, то есть полной над- и поддесневой санации в течение 24 часов с последующей дополнительной системной антибактериальной терапией. В дополнение к этому было показано, что полная дезинфекция полости рта резко снижает количество патогенов пародонта у пациентов с генерализованным агрессивным пародонтитом [23], что потенциально еще больше снижает риск прогрессирования заболевания. Представленная стратегия лечения также поддерживается рекомендациями Американской академии пародонтологии, а также Немецкого общества пародонтологии, которые рекомендуют использование системной дополнительной антибиотикотерапии у пациентов с агрессивным пародонтитом [16,24].
В дополнение к этому было показано, что полная дезинфекция полости рта резко снижает количество патогенов пародонта у пациентов с генерализованным агрессивным пародонтитом [23], что потенциально еще больше снижает риск прогрессирования заболевания. Представленная стратегия лечения также поддерживается рекомендациями Американской академии пародонтологии, а также Немецкого общества пародонтологии, которые рекомендуют использование системной дополнительной антибиотикотерапии у пациентов с агрессивным пародонтитом [16,24].
В литературе описано лишь ограниченное число случаев дефицита плазминогена и поражений полости рта [2]. Описано несколько терапевтических подходов [25-27,10,8,28], включая удаление зубного камня и планирование корня, полоскание хлоргексидином, введение антибиотиков [8,12] и пародонтальную хирургию. Однако в этих отчетах о случаях отсутствует подробная информация о проведенной стоматологической терапии и интраоральной колонизации пародонтальными патогенами. В этих очень немногих сообщениях о дополнительном применении антибиотиков не упоминается ни тип антибиотика, ни продолжительность его приема, ни его связь с каким-либо дополнительным пародонтологическим лечением [29]. ,26], что исключает валидацию дополнительной системной антибактериальной терапии. Большинство из вышеупомянутых сообщений были описаны как неудачи из-за быстрого отрастания десны и прогрессирующей потери костной массы [2]. Только Сильва и др. сообщают о полной ремиссии разрастания тканей полости рта при системном применении преднизолона без гингивэктомии [27]. Однако представленный пациент страдал не деревянистым периодонтитом, а только увеличением десны. В другом отчете о клиническом случае показано, что лечение варфарином обеспечивает защиту от рецидивирующей гиперплазии десен в течение 3-летнего периода наблюдения у 54-летнего пациента. Авторы сообщили о комбинации гингивэктомии, ежедневного приема 20 мг доксициклина и ополаскивателя для полости рта, содержащего 0,12% хлоргексидина диглюконата. Через неделю после операции пациент начал принимать 5 мг варфарина ежедневно в течение неопределенного времени. Поддерживающая пародонтальная терапия не упоминается [18]. Таким образом, неясно, какое из проведенных лечений или их комбинация способствовали наблюдаемому клиническому улучшению.
,26], что исключает валидацию дополнительной системной антибактериальной терапии. Большинство из вышеупомянутых сообщений были описаны как неудачи из-за быстрого отрастания десны и прогрессирующей потери костной массы [2]. Только Сильва и др. сообщают о полной ремиссии разрастания тканей полости рта при системном применении преднизолона без гингивэктомии [27]. Однако представленный пациент страдал не деревянистым периодонтитом, а только увеличением десны. В другом отчете о клиническом случае показано, что лечение варфарином обеспечивает защиту от рецидивирующей гиперплазии десен в течение 3-летнего периода наблюдения у 54-летнего пациента. Авторы сообщили о комбинации гингивэктомии, ежедневного приема 20 мг доксициклина и ополаскивателя для полости рта, содержащего 0,12% хлоргексидина диглюконата. Через неделю после операции пациент начал принимать 5 мг варфарина ежедневно в течение неопределенного времени. Поддерживающая пародонтальная терапия не упоминается [18]. Таким образом, неясно, какое из проведенных лечений или их комбинация способствовали наблюдаемому клиническому улучшению. Кроме того, описанный пациент, по-видимому, страдал клинически довольно легкой формой деревянистого периодонтита, потерял лишь несколько зубов и был значительно старше (54 года), чем другие пациенты с деревянистым периодонтитом, о которых сообщалось в литературе (средний возраст 12–18 лет). . Эти различия могут отражать изменчивость активности PLG из-за различных мутаций гена плазминогена. Сильва и др. [27] сообщили о полной регрессии поражений слизистой оболочки полости рта после системного и местного применения кортикостероидов. Данные о пародонтальном статусе и пародонтальной терапии не публиковались, что затрудняет оценку терапевтического воздействия на пародонтальные поражения.
Кроме того, описанный пациент, по-видимому, страдал клинически довольно легкой формой деревянистого периодонтита, потерял лишь несколько зубов и был значительно старше (54 года), чем другие пациенты с деревянистым периодонтитом, о которых сообщалось в литературе (средний возраст 12–18 лет). . Эти различия могут отражать изменчивость активности PLG из-за различных мутаций гена плазминогена. Сильва и др. [27] сообщили о полной регрессии поражений слизистой оболочки полости рта после системного и местного применения кортикостероидов. Данные о пародонтальном статусе и пародонтальной терапии не публиковались, что затрудняет оценку терапевтического воздействия на пародонтальные поражения.
Недавнее исследование на мышах с дефицитом плазминогена продемонстрировало массивное разрушение пародонта, параллельное накоплению фибрина и нейтрофилов в пораженных тканях пародонта [1]. Интересно, что количество колониеобразующих единиц в экстрактах, приготовленных из гомогенизированных нижних челюстей мышей с дефицитом PLG, было примерно в 100 раз выше по сравнению с мышами дикого типа. Результаты показывают, что бактериальная инвазия в ткани пародонта увеличивается у мышей с дефицитом PLG. Это открытие убедительно свидетельствует о том, что пациентам с дефицитом PLG I типа может быть полезна дополнительная системная антибактериальная терапия. Лишь в очень немногих случаях описано системное лечение антибиотиками при дефиците PLG I типа. Однако в этих описаниях случаев не упоминается ни тип используемого антибиотика, ни продолжительность и время его приема [29].,26], таким образом, не представляя объективной причины для сообщений о неэффективности антибактериальной терапии у пациентов с дефицитом PLG.
Результаты показывают, что бактериальная инвазия в ткани пародонта увеличивается у мышей с дефицитом PLG. Это открытие убедительно свидетельствует о том, что пациентам с дефицитом PLG I типа может быть полезна дополнительная системная антибактериальная терапия. Лишь в очень немногих случаях описано системное лечение антибиотиками при дефиците PLG I типа. Однако в этих описаниях случаев не упоминается ни тип используемого антибиотика, ни продолжительность и время его приема [29].,26], таким образом, не представляя объективной причины для сообщений о неэффективности антибактериальной терапии у пациентов с дефицитом PLG.
Выводы
В заключение мы сообщаем о первом успешном долгосрочном клиническом лечении пациента с дефицитом PLG I типа. включая полную дезинфекцию полости рта в сочетании с дополнительной антибактериальной терапией и строгим режимом поддерживающей терапии пародонта каждые три месяца.
Согласие
От пациента было получено письменное информированное согласие на публикацию данного отчета о болезни и любых сопровождающих изображений. Копия письменного согласия доступна для ознакомления редактору этого журнала.
Копия письменного согласия доступна для ознакомления редактору этого журнала.
Сокращения
- PLG:
-
Плазминоген
- тд:
-
тер в штампе (три раза в день)
- ПКР:
-
Полимеразная цепная реакция
Ссылки
-
Sulniute R, Lindh T, Wilczynska M, Li J, Ny T. Плазмин необходим для профилактики пародонтита у мышей. Ам Джей Патол. 2011;179(2):819–28. doi: 10.1016/j.ajpath.2011.05.003.
Артикул пабмед ПабМед Центральный Google ученый
-
Sivolella S, De Biagi M, Sartori MT, Berengo M, Bressan E. Деструктивное мембранозное заболевание пародонта (деревянистый гингивит): обзор литературы.
 J Пародонтол. 2012;83(4):465–76. Дои: 10.1902/jop.2011.110261.
J Пародонтол. 2012;83(4):465–76. Дои: 10.1902/jop.2011.110261. Артикул пабмед Google ученый
-
Dano K, Andreasen PA, Grondahl-Hansen J, Kristensen P, Nielsen LS, Skriver L. Активаторы плазминогена, деградация тканей и рак. Adv Рак Res. 1985; 44: 139–266.
Артикул пабмед Google ученый
-
Кармели П., Коллен Д. Развитие и заболевание у мышей с дефицитом протеиназы: роль плазминогена, матриксной металлопротеиназы и системы свертывания крови. Рез. Тромб. 1998;91(6):255–85.
Артикул пабмед Google ученый
-
Шаллер Дж., Гербер С.С. Система плазмин-антиплазмин: структурно-функциональные аспекты. Cell Mol Life Sci. 2011;68(5):785–801. doi: 10.1007/s00018-010-0566-5.
Артикул пабмед Google ученый
«> -
Шустер В., Серегард С. Деревянистый конъюнктивит. Сурв Офтальмол. 2003;48(4):369–88.
Артикул пабмед Google ученый
-
Куртулус И., Гокбугет А., Эфеоглу А., Синтан С., Тефс К., Шустер В. и др. Гипоплазминогенемия с деревянистым периодонтитом: неудачный местный терапевтический подход. J Пародонтол. 2007;78(6):1164–75. Дои: 10.1902/jop.2007.060422.
Артикул пабмед Google ученый
-
Шустер В., Хьюгл Б., Тефс К. Дефицит плазминогена. Джей Тромб Хемост. 2007;5(12):2315–22. doi:10.1111/j.1538-7836.
 2007.02776.x.
2007.02776.x. Артикул пабмед Google ученый
-
Тефс К., Георгиева М., Кламмт Дж., Аллен К.М., Актас Д., Анлар Ф.Ю. и др. Молекулярный и клинический спектр дефицита плазминогена I типа: серия из 50 пациентов. Кровь. 2006;108(9): 3021–6. doi: 10.1182 / кровь-2006-04-017350.
Артикул пабмед Google ученый
-
Klammt J, Kobelt L, Aktas D, Durak I, Gokbuget A, Hughes Q, et al. Идентификация трех новых мутаций гена плазминогена (PLG) в серии из 23 пациентов с низкой активностью PLG. Тромб Хемост. 2011;105(3):454–60. дои: 10.1160/Th20-04-0216.
Артикул пабмед Google ученый
-
Мехта Р., Шапиро АД. Дефицит плазминогена. гемофилия. 2008;14(6):1261–8. doi:10.1111/j.1365-2516.2008.01825.x.
Артикул пабмед Google ученый
«> -
Бейклер Т., Шнитцер С., Абдин Г., Эмке Б., Эйзенахер М., Флеммиг Т.Ф. Стратегия отбора проб для внутриротового обнаружения пародонтальных патогенов до и после пародонтальной терапии. J Пародонтол. 2006;77(8):1323–32. doi: 10.1902/jop.2006.050204.
Артикул пабмед Google ученый
-
Quirynen M, Bollen CM, Vandekerckhove BN, Dekeyser C, Papaioannou W, Eyssen H. Полная и частичная дезинфекция полости рта при лечении инфекций пародонта: краткосрочные клинические и микробиологические наблюдения. Джей Дент Рез. 1995;74(8):1459–67.
Артикул пабмед Google ученый
«> -
Бейклер Т., Прайор К., Эмке Б., Флеммиг Т.Ф. Специфические антибиотики в лечении пародонтита – предлагаемая стратегия. J Пародонтол. 2004;75(1):169–75. doi: 10.1902 / jop.2004.75.1.169.
Артикул пабмед Google ученый
-
Файн Г., Бауэр К., Аль-Мохая М., Ву С.Б. Успешное лечение деревянистого гингивита варфарином. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2009;107(1):77–80. doi:10.1016/j.tripleo.2008.08.007.
Артикул пабмед Google ученый
-
Gunhan O, Avci A, Dereci O, Akgun S, Celasun B. Обширное накопление фибрина и сопутствующие эпителиальные изменения в патогенезе деревянистого заболевания слизистой оболочки (деревянистого периодонтита).
 Am J Дерматопатол. 2012;34(1):35–40. Дои: 10.1097/DAD.0b013e3182169507.
Am J Дерматопатол. 2012;34(1):35–40. Дои: 10.1097/DAD.0b013e3182169507. Артикул пабмед Google ученый
-
Zorio E, Gilabert-Estelles J, Espana F, Ramon LA, Cosin R, Estelles A. Фибринолиз: ключ к новым патогенетическим механизмам. Курр Мед Хим. 2008;15(9):923–9.
Артикул пабмед Google ученый
-
Рао С.К., Бисвас Дж., Раджагопал Р., Ситалакшми Г., Падманабхан П. Деревянистый конъюнктивит: клинико-патологическое исследование 3 случаев. Инт офтальмол. 1998;22(4):201–6.
Артикул пабмед Google ученый
-
Чи А.С., Причард Э., Ричардсон М.С., Расенбергер К.П., Уэзерс Д.Р., Невилл Б.В. Псевдомембранозная болезнь (деревянистое воспаление) женских половых путей, брюшины, десен и околоносовых пазух, связанная с дефицитом плазминогена.
 Энн Диагн Патол. 2009;13(2):132–9. doi: 10.1016/j.anndiagpath.2008.02.005.
Энн Диагн Патол. 2009;13(2):132–9. doi: 10.1016/j.anndiagpath.2008.02.005. Артикул пабмед Google ученый
-
Айметти М., Романо Ф., Гуцци Н., Карневале Г. Одноэтапная полная дезинфекция полости рта как метод лечения генерализованного агрессивного пародонтита. J Пародонтол. 2011;82(6):845–53. doi: 10.1902/jop.2010.100468.
Артикул пабмед Google ученый
-
Greenwell H. Документ с изложением позиции: Рекомендации по пародонтологической терапии. J Пародонтол. 2001;72(11):1624–8. doi: 10.1902 / jop.2001.72.11.1624.
Артикул пабмед Google ученый
-
Суреш Л., Агирре А., Кумар В., Соломон Л.В., Сильски Э.А., Нейдерс М.Э. Рецидивирующая рекальцитрантная гиперплазия десен и дефицит плазминогена: клинический случай. J Пародонтол. 2003;74(10):1508–13.
 doi: 10.1902 / jop.2003.74.10.1508.
doi: 10.1902 / jop.2003.74.10.1508. Артикул пабмед Google ученый
-
Байкул Т., Бозкурт Ю. Деструктивное мембранозное заболевание пародонта (деревянистый периодонтит): отчет о болезни и 3-летнее наблюдение. Бр Дент Дж. 2004; 197(8):467–8. дои: 10.1038/sj.bdj.4811739.
Артикул пабмед Google ученый
-
Сильва Г.Б., Бариани С., Мендонка Э.Ф., Батиста А.С. Клинические проявления из-за тяжелой недостаточности плазминогена: история болезни. Джей Дент Чайлд. 2006;73(3):179–82.
Google ученый
-
Токер Х., Токер М.И., Гозе Ф., Тургут М., Йылмаз А. Древеснистый периодонтит и поражения конъюнктивы у пациента с дефицитом плазминогена. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2007;103(6):e35–8. doi:10.1016/j.tripleo.2007.01.002.
Артикул пабмед Google ученый
«>
Шустер В., Зайденспиннер С., Цейтлер П., Эшер С., Плейер У., Бернауэр В. и другие. Компаунд-гетерозиготные мутации в гене плазминогена предрасполагают к развитию деревянистого конъюнктивита. Кровь. 1999;93(10):3457–66.
ПабМед Google ученый
Линд Дж., Найман С. Роль окклюзии в заболеваниях пародонта и биологическое обоснование шинирования при лечении пародонтита. Oral Sci Rev. 1977; 10:11–43.
ПабМед Google ученый
Бейклер Т., Карч Х., Флеммиг Т.Ф. Вспомогательные антибиотики в терапии пародонтита. Wissenschaftliche Stellungnahme DGZMK и DGP. 2003.
Google ученый
Гунхан О., Гунхан М., Беркер Э., Гурган К.А., Йилдирим Х. Деструктивное мембранозное заболевание пародонта (деревянистый пародонтит). J Пародонтол. 1999;70(8):919–25. doi: 10.1902 / jop.1999.70.8.919.
Артикул пабмед Google ученый
Скачать ссылки
Благодарности
Мы благодарим пациентку и ее семью. Мы также благодарим весь коллектив отделения пародонтологии Университета имени Генриха Гейне в Дюссельдорфе.
Author information
Authors and Affiliations
-
Section of Periodontics, Heinrich-Heine University, Moorenstrasse 5, 40225, Düsseldorf, Germany
Sarah H Neering, Sabine Adyani-Fard, Astrid Klocke & Thomas Beikler
-
Отделение оперативной стоматологии Центр стоматологии и оральной медицины (Каролинум), Университет им. Гёте, Франкфурт, Теодор-Штерн-Кай 7, D-60598, Франкфурт, Германия
Штефан Рюттерманн
-
Декан стоматологического факультета, Стоматологическая больница принца Филиппа, 34 Hospital Road, Sai Ying Pun, Hong Kong
Thomas F Flemmig
-
Кафедра пародонтологии, Вашингтонский университет, 1959 NE Pacific St B307, Seattle, WA, 98195, USA
Thomas Beikler
Авторы
- Sarah H Neering
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Сабина Адьяни-Фард
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Astrid Klocke
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Stefan Rüttermann
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Thomas F Flemmig
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Thomas Beikler
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
Автор, ответственный за корреспонденцию
Сара Х Ниринг.
Дополнительная информация
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Отчет о клиническом случае был представлен в виде постера на Europerio 2012.
Вклад авторов
SN и SA провели лечение пациента и подготовили рукопись. ТБ помог составить рукопись. AK, SR, TB и TF критически пересмотрели рукопись на наличие важного интеллектуального содержания. Все авторы прочитали и одобрили окончательный вариант рукописи.
Права и разрешения
Эта статья опубликована по лицензии BioMed Central Ltd. Это статья с открытым доступом, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (http://creativecommons.org/licenses/by/4.0), которая разрешает неограниченное использование, распространение , а также воспроизведение на любом носителе при условии надлежащего указания оригинальной работы. Отказ от права Creative Commons на общественное достояние (http://creativecommons. org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
Перепечатки и разрешения
Об этой статье
Статус тканей пародонта и особенности клинического курса апикального периодонтита постоянных зубов с расстройствами формирования корней в результате травмы
VOL 16 (2020), клиническая медицина
Том 16 № 1 (2020)
КЛИНИЧЕСКАЯ МЕДИЦИНА
https://doi.org/10.32345/2664-4738.1.2020.08
Опубликовано 28 февраля 2020 г.
- +
- О. Плыска 9 −
- Э. Чехертма + −
- О. Лехенчук + −
О. Плыска
Национальный медицинский университет имени Богомольца, г. Киев
https://orcid.org/0000-0002-3843-5582
Е. Чехертма
Национальный медицинский университет имени Богомольца, г. Киев
https://orcid.org/0000-0002-4224-5300
О. Легенчук
Национальный медицинский университет имени Богомольца, г. Киев
Киев
https://orcid.org/0000-0001-6901-3932
Ключевые слова
травма, пародонтит, постоянные зубы с незавершенным формированием корней, клиника
Абстрактные просмотры: 141 Скачиваний в формате PDF: 116
Как цитировать
Плыска О., Чехертма Э. и Легенчук О. (2020). СОСТОЯНИЕ ТКАНЕЙ ПАРОДОНТА И ОСОБЕННОСТИ КЛИНИЧЕСКОГО ТЕЧЕНИЯ ВЕРХУШЕЧНОГО ПАРОДОНТИТА ПОСТОЯННЫХ ЗУБОВ С НАРУШЕНИЕМ ФОРМИРОВАНИЯ КОРНЯ В РЕЗУЛЬТАТЕ ТРАВМЫ. Медицинская наука Украины (МГУ) , 16 (1), 52-56. https://doi.org/10.32345/2664-4738.1.2020.08
Abstract
Актуальность. В детском возрасте часто встречаются травматические повреждения зубов. Некроз пульпы возникает у 34,2 % травмированных зубов, что вызывает повреждение периапикальных тканей. Посттравматические осложнения (одонтогенные кисты, периодонтит) в зубах с незавершенным формированием корня часто приводят к остановке развития корня. Хронический очаг инфекции может быть причиной развития соматической патологии. Это делает важной раннюю клинико-рентгенологическую диагностику посттравматических осложнений.
Хронический очаг инфекции может быть причиной развития соматической патологии. Это делает важной раннюю клинико-рентгенологическую диагностику посттравматических осложнений.
Цель работы — изучить клинические особенности посттравматического периодонтита постоянных зубов с незавершенным формированием корня зуба и оценить состояние тканей пародонта в постоянных зубах с нарушением формирования корня в результате травмы на основании данных клинических и рентгенологических исследований.
Материалы и методы . Под наблюдением находилось 17 детей 9-15 лет с посттравматическим периодонтитом постоянных зубов с незавершенным формированием корня зуба. При постановке диагноза мы опирались на данные клинических и рентгенологических исследований.
Результаты. Большинство детей жаловались на эстетический дефект. 9 детей (52,9%) после острой травмы зуба не обращались за помощью к стоматологу, после лечения 8 детей динамическое наблюдение не велось. В 76 % (13 зубов) пародонтит диагностируют в зубах с переломом коронки в пределах эмали, эмали и дентина.
В 76 % (13 зубов) пародонтит диагностируют в зубах с переломом коронки в пределах эмали, эмали и дентина.
Установлено, что среди деструктивных форм пародонтита наиболее часто встречается хронический гранулирующий периодонтит (12 зубов – 70,6%). Обострение хронического гранулирующего периодонтита диагностировано в 5 зубах. Хронический гранулематозный периодонтит в зубах с незавершенным формированием корней нами не констатирован. Преобладание гранулирующей формы хронического пародонтита у детей обусловлено гистоморфологическими особенностями пародонтита в детском возрасте.
8 детей, среди обследованных имелась патология прикуса – протрузия зубов передней части челюсти (5 детей) и дистальный глубокий прикус (3 ребенка). В 71% поражений деструктивные формы пародонтита чаще всего диагностировались в области резцов верхней челюсти.
Заключение. Несвоевременное обращение за помощью и отсутствие динамического наблюдения за травмированными зубами являются основными причинами развития посттравматического пародонтита. Клиническое течение пародонтита своеобразно – преобладает хронический гранулирующий периодонтит, воспалительный процесс в тканях пародонта в детском возрасте характеризуется быстропрогрессирующей деструкцией костной ткани. Неправильный прикус может быть фактором риска для травм зубов.
Клиническое течение пародонтита своеобразно – преобладает хронический гранулирующий периодонтит, воспалительный процесс в тканях пародонта в детском возрасте характеризуется быстропрогрессирующей деструкцией костной ткани. Неправильный прикус может быть фактором риска для травм зубов.
https://doi.org/10.32345/2664-4738.1.2020.08
Статья PDF (Українська)
использованная литература
1. Хегде Р., Агравал Г. Распространенность травматических повреждений постоянных передних зубов среди школьников в возрасте от 9 до 14 лет в Нави Мумбаи (регион Харгар-Белапур) // IndiaInt J Clin Pediatr Dent. 2017; 10(2): 177-82. DOI: 10.5005/jp-journals-10005-1430
2. Петти С., Глендор У., Андерссон Л. Мировая распространенность и заболеваемость травматическими повреждениями зубов, метаанализ. Травматические повреждения зубов у одного миллиарда живущих людей // Дент-травматол. 2018; 34(2): 71-86. DOI: 10.1111/изд.12389.
3. Кумар К.Н., Венкатасубраманян Р., Тогару Х. Частота травматических повреждений зубов у детей в возрасте 3-18 лет в Тирупати // Int J Pedod Rehabil. 2017; 2: 73-6. DOI: 10.4103/ijpr.ijpr_19_17
Частота травматических повреждений зубов у детей в возрасте 3-18 лет в Тирупати // Int J Pedod Rehabil. 2017; 2: 73-6. DOI: 10.4103/ijpr.ijpr_19_17
4. Лин С., Пилософ Н., Каравани М., Виглер Р. и соавт. Возникновение и сроки осложнений после травматических повреждений зубов: ретроспективное исследование в стоматологическом травматологическом отделении // J Clin Exp Dent. 2016; 8(4): 429-36. DOI: 10.4317/jced.53022.
5. Наумова В.Н., Туркина С.В., Маслак Е.Е. Взаимосвязь стоматологических и соматических заболеваний: обзор литературы // Волгоградский научно-медицинский журнал. 2016; 2(50): 25-7.
6. Фуртадо М.В., Хонг Б.И., Фава П.Л. Терминальная стадия почечной недостаточности как модификатор микробиома пародонта // BMC Nephrol. 2013; 16: 80-8. DOI: 10.1186/s12882-015-0081-x
Эта работа находится под лицензией Creative Commons Attribution 4.0 International License.
Удаяна Сеть | Universitas Udayana
ЛЕЧЕНИЕ ХРОНИЧЕСКОГО ПАРОДОНТИТА СЛУЧАЙ
Отчет о болезни
Стоматология Программа бакалавриата и профессия стоматолога
Факультет медицины
Удаяна Университет
РЕФЕРАТ
Проблема гигиены полости рта в
Индонезия требует внимания, она характеризуется высокой распространенностью
повреждения зубов и полости рта, такие как кариес и заболевания пародонта. пародонтальный
Заболевание начинается, когда на поверхности зуба скапливается зубной налет или камень.
Исчисление само по себе является фактором, который способствовал этиологическому фактору для
парадантоз. Пародонтоз часто отмечается карманом.
Начальное лечение пародонтита заключается в устранении этиологического
факторы, а именно снятие зубного камня, планирование корней и кюретаж, однако пародонтальные
карманы не являются диагнозом болезни. Определение пародонтальных карманов
представляет собой процесс увеличения десневой борозды и является одним из клинических
особенности пародонтоза. В этом отчете о клиническом случае будет обсуждаться управление лечением.
удаления зубного камня, планирования корня и выскабливания в случаях хронического пародонтита
пережила 56-летняя женщина в зубах 12 и 13.
пародонтальный
Заболевание начинается, когда на поверхности зуба скапливается зубной налет или камень.
Исчисление само по себе является фактором, который способствовал этиологическому фактору для
парадантоз. Пародонтоз часто отмечается карманом.
Начальное лечение пародонтита заключается в устранении этиологического
факторы, а именно снятие зубного камня, планирование корней и кюретаж, однако пародонтальные
карманы не являются диагнозом болезни. Определение пародонтальных карманов
представляет собой процесс увеличения десневой борозды и является одним из клинических
особенности пародонтоза. В этом отчете о клиническом случае будет обсуждаться управление лечением.
удаления зубного камня, планирования корня и выскабливания в случаях хронического пародонтита
пережила 56-летняя женщина в зубах 12 и 13.
Ключевые слова : Хронический пародонтит, шелушение,
планировка корня, кюретаж
ПРЕДВАРИТЕЛЬНАЯ
Проблема полости рта
здравоохранение в Индонезии требует внимания. На это указывает
распространенность повреждений зубов и полости рта, таких как кариес и заболевания пародонта
что довольно высоко. Болезнь возникает из-за отсутствия внимания и знаний о
здоровье ротовой полости. Заболевание пародонта используется для описания состояния, которое может вызвать
воспаление в опорных тканях зубов, а именно в деснах,
периодонтальная связка, цемент корня зуба и альвеолярная кость.
На это указывает
распространенность повреждений зубов и полости рта, таких как кариес и заболевания пародонта
что довольно высоко. Болезнь возникает из-за отсутствия внимания и знаний о
здоровье ротовой полости. Заболевание пародонта используется для описания состояния, которое может вызвать
воспаление в опорных тканях зубов, а именно в деснах,
периодонтальная связка, цемент корня зуба и альвеолярная кость.
Болезни пародонта
проблема со здоровьем зубов и полости рта, которая имеет довольно высокую распространенность в
сообщество. Распространенность заболеваний пародонта во всех возрастных группах в Индонезии
составляет 96,58%.1 Существуют две формы заболеваний пародонта, а именно гингивит и
периодонтит. Гингивит – это воспаление десны, которое является реакцией
ткани десен к накоплению бактериального налета. При этом перидонтит
воспаление тканей, покрывающих зубы и корни зубов. пародонтит
делится на два типа, а именно маргинальный периодонтит, который
продолжение развития нелеченного гингивита, тогда как апикальный
пародонтит – это воспаление, которое возникает в тканях вокруг верхушки
зубов, что является продолжением инфекции или воспаления пульпы. Пародонтит – это воспаление опорной ткани зуба, вызванное специфическим
микроорганизмы, вызывающие повреждение периодонтальной связки и альвеолярного
кость.2,4
Пародонтит – это воспаление опорной ткани зуба, вызванное специфическим
микроорганизмы, вызывающие повреждение периодонтальной связки и альвеолярного
кость.2,4
Хронический пародонтит определяется как медленно прогрессирующий пародонтит, который обычно является начальным терапия, состоящая из скейлинга и полировки корней, гигиены полости рта и, возможно, даже требуют корректировки прикуса или небольшого смещения зубов. Пародонтоз это часто можно увидеть с карманом. Однако пародонтальные карманы не являются диагнозом болезнь. Определение пародонтальных карманов – это процесс увеличения десневого борозды и является одним из клинических признаков пародонтоза
Процедуры удаления
этиогенных факторов в пародонтальных карманах можно провести с помощью выскабливания.
удалить поражения. Пародонтальные карманы часто сопровождают несколько пародонтальных
заболеваний, например при гингивите или хроническом пародонтите. пародонтальный
карманы, содержащие патогенную ткань и мусор, должны быть немедленно удалены, поэтому
что они не расширяются, чтобы стать более серьезными. Альтернативные методы лечения
пародонтальные карманы включают кюретаж. Кюретаж проводится по показаниям
пациенты. Выскабливание может быть выполнено как часть новой процедуры прикрепления в
внутрикостной карман средней глубины, который находится на доступной стороне. Кроме того,
выскабливание часто проводят при регулярных посещениях в связи с
поддерживающая фаза, как метод поддержания в зонах с рецидивами/
рецидив воспаления и углубление кармана. 2 В этом случае отчет будет
обсудили лечение кюретажем при хроническом пародонтите
пережила женщина 56 лет на зубах 12 и 13,3
Альтернативные методы лечения
пародонтальные карманы включают кюретаж. Кюретаж проводится по показаниям
пациенты. Выскабливание может быть выполнено как часть новой процедуры прикрепления в
внутрикостной карман средней глубины, который находится на доступной стороне. Кроме того,
выскабливание часто проводят при регулярных посещениях в связи с
поддерживающая фаза, как метод поддержания в зонах с рецидивами/
рецидив воспаления и углубление кармана. 2 В этом случае отчет будет
обсудили лечение кюретажем при хроническом пародонтите
пережила женщина 56 лет на зубах 12 и 13,3
Клинический случай
Женщина, 56 лет. пациент обратился в клинику RSGM Университета Удаяна с жалобами на наличие зубного камня. мешал ее внешний вид и неприятный запах изо рта. Из истории известно что пациент никогда раньше не чистил зубной камень, пациент сказал, что его десны часто кровоточил при чистке зубов и часто опухал, но никогда не было обследован или пролечен.
Для экстраорального применения
обследования, отклонений от нормы не обнаружено. Исследование правой и левой лимфы
узлы мягкие, безболезненные. При осмотре ротовой полости конкременты обнаружены во всех
передние и задние зубы верхней и нижней челюсти, а также припухлость
в деснах 12 и 13 коренных зубов. Оценка гигиены полости рта пациентки была
4,16 (плохо).
Исследование правой и левой лимфы
узлы мягкие, безболезненные. При осмотре ротовой полости конкременты обнаружены во всех
передние и задние зубы верхней и нижней челюсти, а также припухлость
в деснах 12 и 13 коренных зубов. Оценка гигиены полости рта пациентки была
4,16 (плохо).
Диагноз жалоба больного — хронический периодонтит, который осложняется миграцией. План лечения, который будет выполняться, включает масштабирование, корневое планирование и кюретаж с послеоперационным контролем.
Ведение дела
1. Первый визит (26.09.2019)
• История
• Экстраоральный, внутриротовые осмотры
• Удаление зубного камня и корня обшивка
• DHE
Рисунок 1. Внутриротовой условия перед масштабированием и корневым планированием
Результаты
при осмотре кармана при первом посещении были пародонтальные карманы на 12 мм
мезиолабиальные зубы на 4 мм, лабиальные 4 мм, дистолабиальные 4 мм и мезиолабиальные 13 мм
Зубы 4 мм, губные 4 мм, дистолабиальные 4 мм 4 мм. Во время этого визита масштабирование и
было проведено корневое планирование. Кровотечение при зондировании / BOP (+).
Во время этого визита масштабирование и
было проведено корневое планирование. Кровотечение при зондировании / BOP (+).
планирование. Кровотечение При зондировании /БОП(+).
Рисунок 2. После масштабирования и корневое планирование.
2. Второй визит (3 Октябрь 2019 г.)
• Пациенты приходят за контроль налета и планирование корня
• Пародонтальный карман обследование
• Показания к кюретаж
• Показания к панорамный рентген
Результаты Карманный чек на масштабирование первого контрольного поста и корневое планирование пародонтальные карманы на 12 зубах, мезиолабиальный отдел уменьшен с 4 мм до 3 мм, лабиальная часть осталась на 4 мм, дистолабиальная часть уменьшилась с 4 мм до 3 мм, а 13 зубов уменьшились на мезиолабиальные с 4 мм до 2 мм, лабиально 4 мм, дисто-лабиально 4 мм, дисто-палатально 4 мм
3. Третий визит (октябрь 16, 2019)
• Пациенты приходят за кюретаж
• Подготовка инструментов и материалы
• Обеззараживание работы участок с повидон-йодом
• Выполнить инфильтрацию анестезия
• Скейлинг и корень планирование восстановления зубов 42 и 43
• Изящный кюретаж
кюретка нет. 1-4
1-4
• Орошение с физиологический раствор
• Остановите кровотечение с помощью стерильная марля на 10-15 минут
• Манипуляции с Материал пародонтального пакета
• Пародонтальный пакет установка
• Амоксициллин и назначение мефенамовой кислоты, пациенты с ИЭК
·
Гамбар 4 . Инфильтрационная анестезия
Гамбар 5 . Проседур куретасе
Гамбар 6 . Иригаси денган ларутан солевой раствор дан повидон йод
Гамбар 7 . Setelah kontrol perdarahan
Gambar 8 . Пародонтальный пакет Pemasangan
Gambar 9 . Kontrol 1 minggu setelah куретасе
Рисунок 10. Исследование кармана во время второго кюретажа контрольного поста.
4. Четвертый визит (23 октябрь 2019 г.)
• Присутствие пациентов на кюретаж первый контрольный пост
• Пародонтальные тампоны интактны, а состояние мягких тканей вокруг зубов 12 и 13 не указывают на воспаление
• Откройте пародонтальный упаковка, повторное орошение послеоперационной зоны
5. Пятое посещение (30
Октябрь 2019 г.)
Пятое посещение (30
Октябрь 2019 г.)
• Pasen приходите на второй контрольный пост кюретаж
• Пародонтальный карман были проведены исследования 12 зубов, где мезиолабиальный срез был уменьшился с 4 мм до 1 мм, лабиальная часть уменьшилась с 4 мм до 2 мм, дистально-губная часть уменьшилась с 4 мм до 2 мм, а 13 зуб мезиолабиальная часть уменьшилась с 4 мм до 2 мм, вестибулярная часть уменьшилась с 4 мм до 1 мм, дистально-губная часть уменьшилась с 4 мм до 1 мм, дистально-небная часть уменьшилась с 4 мм до 3 мм. ПБ (-)
• Лечение зубов 12 и 13 объявлены полными, пациенты ИЭК для поддержания гигиены полости рта и зубов и контроль каждые 6 месяцев
• Лечение других лечение зубов с хроническим периодонтитом было продолжено другими операторами.
ОБСУЖДЕНИЕ
Согласно Newman et
др. пародонтит – воспаление опорной ткани зуба, вызванное
определенные микроорганизмы или определенные группы микроорганизмов, что приводит к
повреждение периодонтальной связки и альвеолярной кости с увеличением глубины
пародонтальный карман. 2 Клинические признаки формирования пародонтального кармана, такие как
покраснение, утолщение десневого края, кровоточивость и нагноение десен,
колебание зубов и образование промежутков между зубами, локальная боль или болезненность
в кости
2 Клинические признаки формирования пародонтального кармана, такие как
покраснение, утолщение десневого края, кровоточивость и нагноение десен,
колебание зубов и образование промежутков между зубами, локальная боль или болезненность
в кости
По словам Каррансы
и Takei надлежащий и надлежащий уход за пародонтом — это действие, предпринятое для
устранить имеющееся заболевание и предотвратить возвращение болезни. Масштабирование
и полировка корней, кюретаж и хорошая гигиена полости рта устранят воспаление
и уменьшить глубину кармана, даже во многих случаях можно устранить все
симптомы имеющихся заболеваний. Кюретаж – процедура при лечении
периодонтит. Действие выскабливания заключается в очищении грануляционной ткани
при хроническом воспалении, формирующемся на латеральной стенке
пародонтального кармана.4 Грануляционная ткань пародонтального кармана содержит
ткань с хроническим воспалением, частицы конкрементов и бактериальные
колонии. Камни и бактериальные колонии, которые все еще остаются в
пародонтальный карман усугубит заболевание пародонта и замедлит заживление
несмотря на масштабирование и корневое планирование.
Пародонтит воспаление опорной ткани зуба, вызванное микроорганизмами и может вызывают прогрессирующее повреждение периодонтальной связки, альвеолярной кости и сопровождается образованием карманов. Пародонтит вызывает постоянные ткани деструкция, характеризующаяся хроническим воспалением, срастанием эпителия с апикальной миграция, потеря соединительной ткани и потеря альвеолярной кости.3
Клиническая картина периодонтит – изменение цвета десен на ярко-красный, сопровождающееся края вздутия. Кровотечение при зондировании и глубине зондирования ≥ 4 мм вызывается за счет слившегося эпителия к апикальной миграции. Потеря альвеолярной кости и покачивание зубов происходить. Пародонтит подразделяют на два вида: хронический пародонтит и агрессивный пародонтит.
Хронический пародонтит
связано с накоплением зубного налета и камня и обычно развивается
медленно, но наступает период быстрого разрушения. Увеличение развития
пародонтит может быть вызван воздействием местных, системных и экологических
факторы, которые могут повлиять на накопление зубного налета. Системные заболевания, такие как диабет
mellitus и ВИЧ
Системные заболевания, такие как диабет
mellitus и ВИЧ
могут поражать хозяина защита; факторы окружающей среды, такие как курение и стресс, также могут влиять на реакция хозяина на накопление зубного налета. Следующие характеристики обнаруживаются у больных хроническим пародонтитом, а именно:
Более распространен в у взрослых, но может встречаться и у детей
Размер повреждения согласуется / в соответствии с местными факторами
Относится к картина микробных переменных
Поддесневой зубной камень было обнаружено
Уровень заболеваемости прогрессирование от медленного до умеренного с возможностью периода быстрого разработка
Можно модифицировать или связанные с: системными заболеваниями, такими как сахарный диабет и ВИЧ-инфекция факторы окружающей среды, такие как курение и эмоциональный стресс.
Хронический перидонтит можно разделить на локализованную и генерализованную формы. В то время как на основе тяжесть и внешний вид делятся на легкие, средние или тяжелые категории, следующим образом:
— Локализовано: <30% площадь вовлечена
— Обобщенный:> 30% пораженной области
Легкая: клиническая потеря прикрепления (CAL) 1-2 мм
Умеренная: клиническая потеря прикрепления (CAL) 3-4 мм
Вес: клинический потеря прикрепления (CAL) ≥ 5 мм
Основная причина
Пародонтоз – это наличие колонизирующих микроорганизмов в зубах. бляшка. Зубной налет представляет собой структурированное вещество, мягкое, желтого цвета, которое
прикрепляется к поверхности зуба. Состав зубного налета различен.
виды микроорганизмов, особенно остальные бактерии – это грибы, простейшие
и вирусы. Налет, содержащий эти патогенные микроорганизмы, играет важную роль.
важную роль в обострении пародонтальных инфекций. Увеличение количества
Грамотрицательные организмы в поддесневых бляшках, такие как бактерии
Porphiromonas gingivalis, Actinobacillus actinomycetemcomitans, Tannerela
forsythia и Treponema denticola могут вызывать инфекции тканей пародонта.
бляшка. Зубной налет представляет собой структурированное вещество, мягкое, желтого цвета, которое
прикрепляется к поверхности зуба. Состав зубного налета различен.
виды микроорганизмов, особенно остальные бактерии – это грибы, простейшие
и вирусы. Налет, содержащий эти патогенные микроорганизмы, играет важную роль.
важную роль в обострении пародонтальных инфекций. Увеличение количества
Грамотрицательные организмы в поддесневых бляшках, такие как бактерии
Porphiromonas gingivalis, Actinobacillus actinomycetemcomitans, Tannerela
forsythia и Treponema denticola могут вызывать инфекции тканей пародонта.
При лечении
кюретаж и планирование корней выполняются, чтобы гарантировать, что зубной камень не
частицы остаются. Произведено удаление эпителия кармана.
методом ручного кюретажа и с помощью инструмента Грейси Кюрет №. 1-
Кюретка вставлялась в карман до дна кармана, острая
сторона была обнажена к мягким тканям, наружная поверхность десны была слегка
проводится пальцами, которые не держали инструмент. Кюретаж зубов 12
а 13 выполняется с горизонтальным гребком по боковой стенке
карман. Повторите несколько раз, пока грануляционная ткань не поднимется, отмеченная
свежая кровь. Затем участок орошают после его высыхания, после чего
применение пародонтальных пакетов. После выскабливания область вокруг раны
часто болезненные из-за повреждения тканей. Острая боль часто вызывает неблагоприятные
условия для больных, такие как тревога, гемодинамические изменения, респираторные
проблемы, задержка мочи и др.5. Поэтому данное Dental Health
Обучение (DHE) относительно осложнений, которые могут возникнуть после действия
выскабливание, препараты, которые необходимо принимать, количество и время приема лекарств.
Затем больному был назначен обезболивающий препарат в виде мефенамовой кислоты.
Таблетки 500 мг и амоксициллин Таблетки 500 мг антибиотики в течение 5 дней, и оба
препараты принимали 3 раза в день после еды.
Кюретаж зубов 12
а 13 выполняется с горизонтальным гребком по боковой стенке
карман. Повторите несколько раз, пока грануляционная ткань не поднимется, отмеченная
свежая кровь. Затем участок орошают после его высыхания, после чего
применение пародонтальных пакетов. После выскабливания область вокруг раны
часто болезненные из-за повреждения тканей. Острая боль часто вызывает неблагоприятные
условия для больных, такие как тревога, гемодинамические изменения, респираторные
проблемы, задержка мочи и др.5. Поэтому данное Dental Health
Обучение (DHE) относительно осложнений, которые могут возникнуть после действия
выскабливание, препараты, которые необходимо принимать, количество и время приема лекарств.
Затем больному был назначен обезболивающий препарат в виде мефенамовой кислоты.
Таблетки 500 мг и амоксициллин Таблетки 500 мг антибиотики в течение 5 дней, и оба
препараты принимали 3 раза в день после еды.
Контроль после выскабливания
лечения, при субъективном осмотре не наблюдалось. Жалоб и жалоб не было.
при объективном осмотре: пародонтальных карманов и воспалений десны нет.
десна вокруг зуба 12 и зуба 13 в мезиолабиальном разрезе уменьшена с 4 мм до 1
мм, лабиальная часть уменьшилась с 4 мм до 2 мм, дистолабиальная часть уменьшилась.
редуцирован с 4 мм до 2 мм, а мезиолабиальная часть зуба 13 редуцирована с
4 мм до 2 мм, лабиальная часть уменьшилась с 4 мм до 1 мм, дистолабиальная
часть уменьшилась с 4 мм до 1 мм, дистально-небная часть уменьшилась
от 4 мм до 3 мм. и не указывает на кровотечение при зондировании. Это показывает
Прогноз кюретажа в этом случае благоприятный. Исцеление, полученное после
выскабливание – образование тромбов, заполняющих область кармана. Корневое планирование
может уменьшить глубину кармана, усилить клиническое прикрепление к тканям и ингибировать
прогрессирование болезни. Повышенное клиническое прилегание к тканям приводит к
образование новых соединительнотканных прикреплений, т. е. новых пародонтальных волокон, которые
находятся в цементе.
Жалоб и жалоб не было.
при объективном осмотре: пародонтальных карманов и воспалений десны нет.
десна вокруг зуба 12 и зуба 13 в мезиолабиальном разрезе уменьшена с 4 мм до 1
мм, лабиальная часть уменьшилась с 4 мм до 2 мм, дистолабиальная часть уменьшилась.
редуцирован с 4 мм до 2 мм, а мезиолабиальная часть зуба 13 редуцирована с
4 мм до 2 мм, лабиальная часть уменьшилась с 4 мм до 1 мм, дистолабиальная
часть уменьшилась с 4 мм до 1 мм, дистально-небная часть уменьшилась
от 4 мм до 3 мм. и не указывает на кровотечение при зондировании. Это показывает
Прогноз кюретажа в этом случае благоприятный. Исцеление, полученное после
выскабливание – образование тромбов, заполняющих область кармана. Корневое планирование
может уменьшить глубину кармана, усилить клиническое прикрепление к тканям и ингибировать
прогрессирование болезни. Повышенное клиническое прилегание к тканям приводит к
образование новых соединительнотканных прикреплений, т. е. новых пародонтальных волокон, которые
находятся в цементе.
ЗАКЛЮЧЕНИЕ
Хронический пародонтит определяется как медленно прогрессирующий пародонтит, который обычно является начальным Терапия, состоящая из скейлинга и полировки корней, кюретажа. Парадантоз часто характеризуется карманом. Однако пародонтальные карманы не являются диагнозом. болезни. Определение пародонтального кармана – это процесс увеличение десневой борозды и является одним из клинических признаков пародонтита. болезнь.
Кюретаж – это
процедура по избавлению от воспалительной грануляционной ткани, находящейся в пародонте
Карманная стенка является одним из пародонтологических хирургических методов, который очень ограничен в своем применении.
показания. Кюретаж необходим, особенно если новые соединения между
цемента и альвеолярного отростка ожидают в кармане путем очистки поврежденного
ткани пародонта, некротический цемент и ткани, которые могут раздражать десны
это стенка зубного кармана. Выскабливание может быть сделано только в том случае, если
после масштабирования и лечения корней все еще обнаруживаются признаки
воспаления в виде отека, покраснения и кармана глубиной 4-5 мм в
десна.
ССЫЛКИ
1. Астоэти, T.E., Boesro, S., Pengaruh Tingkat P ЛЕЧЕНИЕ ХРОНИЧЕСКОГО ПАРОДОНТИТА, СЛУЧАЙ
История болезни
Стоматология Программа бакалавриата и профессия стоматолога
Факультет медицины
Удаяна Университет
РЕФЕРАТ
Проблема гигиены полости рта в
Индонезия требует внимания, она характеризуется высокой распространенностью
повреждения зубов и полости рта, такие как кариес и заболевания пародонта. пародонтальный
Заболевание начинается, когда на поверхности зуба скапливается зубной налет или камень.
Исчисление само по себе является фактором, который способствовал этиологическому фактору для
парадантоз. Пародонтоз часто отмечается карманом.
Начальное лечение пародонтита заключается в устранении этиологического
факторы, а именно снятие зубного камня, планирование корней и кюретаж, однако пародонтальные
карманы не являются диагнозом болезни. Определение пародонтальных карманов
представляет собой процесс увеличения десневой борозды и является одним из клинических
особенности пародонтоза. В этом отчете о клиническом случае будет обсуждаться управление лечением.
удаления зубного камня, планирования корня и выскабливания в случаях хронического пародонтита
пережила 56-летняя женщина в зубах 12 и 13.
Определение пародонтальных карманов
представляет собой процесс увеличения десневой борозды и является одним из клинических
особенности пародонтоза. В этом отчете о клиническом случае будет обсуждаться управление лечением.
удаления зубного камня, планирования корня и выскабливания в случаях хронического пародонтита
пережила 56-летняя женщина в зубах 12 и 13.
Ключевые слова : Хронический пародонтит, шелушение,
планировка корня, кюретаж
ПРЕДВАРИТЕЛЬНАЯ
Проблема полости рта здравоохранение в Индонезии требует внимания. На это указывает распространенность повреждений зубов и полости рта, таких как кариес и заболевания пародонта что довольно высоко. Болезнь возникает из-за отсутствия внимания и знаний о здоровье ротовой полости. Заболевание пародонта используется для описания состояния, которое может вызвать воспаление в опорных тканях зубов, а именно в деснах, периодонтальная связка, цемент корня зуба и альвеолярная кость.
Болезни пародонта
проблема со здоровьем зубов и полости рта, которая имеет довольно высокую распространенность в
сообщество. Распространенность заболеваний пародонта во всех возрастных группах в Индонезии
составляет 96,58%.1 Существуют две формы заболеваний пародонта, а именно гингивит и
периодонтит. Гингивит – это воспаление десны, которое является реакцией
ткани десен к накоплению бактериального налета. При этом перидонтит
воспаление тканей, покрывающих зубы и корни зубов. пародонтит
делится на два типа, а именно маргинальный периодонтит, который
продолжение развития нелеченного гингивита, тогда как апикальный
пародонтит – это воспаление, которое возникает в тканях вокруг верхушки
зубов, что является продолжением инфекции или воспаления пульпы.
Пародонтит – это воспаление опорной ткани зуба, вызванное специфическим
микроорганизмы, вызывающие повреждение периодонтальной связки и альвеолярного
кость.2,4
Распространенность заболеваний пародонта во всех возрастных группах в Индонезии
составляет 96,58%.1 Существуют две формы заболеваний пародонта, а именно гингивит и
периодонтит. Гингивит – это воспаление десны, которое является реакцией
ткани десен к накоплению бактериального налета. При этом перидонтит
воспаление тканей, покрывающих зубы и корни зубов. пародонтит
делится на два типа, а именно маргинальный периодонтит, который
продолжение развития нелеченного гингивита, тогда как апикальный
пародонтит – это воспаление, которое возникает в тканях вокруг верхушки
зубов, что является продолжением инфекции или воспаления пульпы.
Пародонтит – это воспаление опорной ткани зуба, вызванное специфическим
микроорганизмы, вызывающие повреждение периодонтальной связки и альвеолярного
кость.2,4
Хронический пародонтит
определяется как медленно прогрессирующий пародонтит, который обычно является начальным
терапия, состоящая из скейлинга и полировки корней, гигиены полости рта и, возможно, даже
требуют корректировки прикуса или небольшого смещения зубов. Пародонтоз это
часто можно увидеть с карманом. Однако пародонтальные карманы не являются диагнозом
болезнь. Определение пародонтальных карманов – это процесс увеличения десневого
борозды и является одним из клинических признаков пародонтоза
Пародонтоз это
часто можно увидеть с карманом. Однако пародонтальные карманы не являются диагнозом
болезнь. Определение пародонтальных карманов – это процесс увеличения десневого
борозды и является одним из клинических признаков пародонтоза
Процедуры удаления
этиогенных факторов в пародонтальных карманах можно провести с помощью выскабливания.
удалить поражения. Пародонтальные карманы часто сопровождают несколько пародонтальных
заболеваний, например при гингивите или хроническом пародонтите. пародонтальный
карманы, содержащие патогенную ткань и мусор, должны быть немедленно удалены, поэтому
что они не расширяются, чтобы стать более серьезными. Альтернативные методы лечения
пародонтальные карманы включают кюретаж. Кюретаж проводится по показаниям
пациенты. Выскабливание может быть выполнено как часть новой процедуры прикрепления в
внутрикостной карман средней глубины, который находится на доступной стороне. Кроме того,
выскабливание часто проводят при регулярных посещениях в связи с
поддерживающая фаза, как метод поддержания в зонах с рецидивами/
рецидив воспаления и углубление кармана. 2 В этом случае отчет будет
обсудили лечение кюретажем при хроническом пародонтите
пережила женщина 56 лет на зубах 12 и 13,3
2 В этом случае отчет будет
обсудили лечение кюретажем при хроническом пародонтите
пережила женщина 56 лет на зубах 12 и 13,3
Клинический случай
Женщина, 56 лет. пациент обратился в клинику RSGM Университета Удаяна с жалобами на наличие зубного камня. мешал ее внешний вид и неприятный запах изо рта. Из истории известно что пациент никогда раньше не чистил зубной камень, пациент сказал, что его десны часто кровоточил при чистке зубов и часто опухал, но никогда не было обследован или пролечен.
Для экстраорального применения обследования, отклонений от нормы не обнаружено. Исследование правой и левой лимфы узлы мягкие, безболезненные. При осмотре ротовой полости конкременты обнаружены во всех передние и задние зубы верхней и нижней челюсти, а также припухлость в деснах 12 и 13 коренных зубов. Оценка гигиены полости рта пациентки была 4,16 (плохо).
Диагноз
жалоба больного — хронический периодонтит, который осложняется миграцией.
План лечения, который будет выполняться, включает масштабирование, корневое планирование и
кюретаж с послеоперационным контролем.
Ведение дела
1. Первый визит (26.09.2019)
• История
• Экстраоральный, внутриротовые осмотры
• Удаление зубного камня и корня обшивка
• DHE
Рисунок 1. Внутриротовой условия перед масштабированием и корневым планированием
Результаты при осмотре кармана при первом посещении были пародонтальные карманы на 12 мм мезиолабиальные зубы на 4 мм, лабиальные 4 мм, дистолабиальные 4 мм и мезиолабиальные 13 мм Зубы 4 мм, губные 4 мм, дистолабиальные 4 мм 4 мм. Во время этого визита масштабирование и было проведено корневое планирование. Кровотечение при зондировании / BOP (+).
планирование. Кровотечение При зондировании /БОП(+).
Рисунок 2. После масштабирования и корневое планирование.
2. Второй визит (3 Октябрь 2019 г.)
• Пациенты приходят за контроль налета и планирование корня
• Пародонтальный карман обследование
• Показания к кюретаж
• Показания к панорамный рентген
Результаты Карманный чек на масштабирование первого контрольного поста и корневое планирование пародонтальные карманы на 12 зубах, мезиолабиальный отдел уменьшен с 4 мм до 3 мм, лабиальная часть осталась на 4 мм, дистолабиальная часть уменьшилась с 4 мм до 3 мм, а 13 зубов уменьшились на мезиолабиальные с 4 мм до 2 мм, лабиально 4 мм, дисто-лабиально 4 мм, дисто-палатально 4 мм
3. Третий визит (октябрь
16, 2019)
Третий визит (октябрь
16, 2019)
• Пациенты приходят за кюретаж
• Подготовка инструментов и материалы
• Обеззараживание работы участок с повидон-йодом
• Выполнить инфильтрацию анестезия
• Скейлинг и корень планирование восстановления зубов 42 и 43
• Изящный кюретаж кюретка нет. 1-4
• Орошение с физиологический раствор
• Остановите кровотечение с помощью стерильная марля на 10-15 минут
• Манипуляции с Материал пародонтального пакета
• Пародонтальный пакет установка
• Амоксициллин и назначение мефенамовой кислоты, пациенты с ИЭК
·
Гамбар 4 . Инфильтрационная анестезия
Гамбар 5 . Проседур куретасе
Гамбар 6 . Иригаси денган ларутан солевой раствор дан повидон йод
Гамбар 7 . Setelah kontrol perdarahan
Хронический пародонтит ~ д-р У. Ракеш, д-р Киртана Рао
Резюме
Пародонтит — это воспалительное заболевание, поражающее десну и опорные структуры зубов. Это может повлиять на любую возрастную группу и вызвано различными факторами.
от плохой гигиены полости рта до генетической предрасположенности. Клинические признаки варьируют от легкого гингивита до тяжелого некротизирующего периодонтита. К сожалению, большинство пациентов
не имеют острых симптомов и, следовательно, обращаются к своим стоматологам только на поздних стадиях, требующих обширного стоматологического лечения. В этой статье мы представляем историю болезни
пациента с диагнозом генерализованный хронический пародонтит многофакторной этиологии. Для этого пациента был разработан конкретный план лечения, основанный на его клинической картине.
презентация и исследования, но из-за определенных проблем потребовалось отклонение от первоначального плана. Пациент лечился с мультидисциплинарным подходом,
уделение первоочередного внимания реабилитации, чтобы он мог использовать свои зубы, что, в свою очередь, улучшило его пищевой статус и общее состояние здоровья.
Это может повлиять на любую возрастную группу и вызвано различными факторами.
от плохой гигиены полости рта до генетической предрасположенности. Клинические признаки варьируют от легкого гингивита до тяжелого некротизирующего периодонтита. К сожалению, большинство пациентов
не имеют острых симптомов и, следовательно, обращаются к своим стоматологам только на поздних стадиях, требующих обширного стоматологического лечения. В этой статье мы представляем историю болезни
пациента с диагнозом генерализованный хронический пародонтит многофакторной этиологии. Для этого пациента был разработан конкретный план лечения, основанный на его клинической картине.
презентация и исследования, но из-за определенных проблем потребовалось отклонение от первоначального плана. Пациент лечился с мультидисциплинарным подходом,
уделение первоочередного внимания реабилитации, чтобы он мог использовать свои зубы, что, в свою очередь, улучшило его пищевой статус и общее состояние здоровья.
Ключевые слова: Гингивит, Пародонтит, Воспалительные заболевания, Борьба с зубным налетом, Профилактика полости рта
История вопроса
Гингивит – это воспалительное заболевание, поражающее десну вокруг зубов. Пародонтит определяется как воспалительное заболевание опорных тканей зубов.
вызываемые специфическими микроорганизмами. Это приводит к прогрессирующему разрушению периодонтальной связки и альвеолярной кости с увеличением глубины зондирования, образованию рецессии
или и то, и другое, что в конечном итоге приводит к преждевременной потере зубов. Приблизительно 10% взрослого населения мира очень уязвимы к тяжелому пародонтиту, 10-15%, как представляется,
полностью устойчивы к нему, в то время как остальные колеблются между этими двумя ситуациями [1]. Этиология пародонтита чаще всего связана с скоплением камней вокруг
зуб из-за плохой гигиены полости рта [2]. Другими предрасполагающими факторами могут быть сахарный диабет, половое созревание, менструация, беременность, менопауза, гиперпаратиреоз,
гематологические заболевания, иммунодефицитные состояния, генетические нарушения, стрессовые и психосоматические расстройства, влияние питания, лекарств, сердечные заболевания, курение, жевание
табак и др.
Пародонтит определяется как воспалительное заболевание опорных тканей зубов.
вызываемые специфическими микроорганизмами. Это приводит к прогрессирующему разрушению периодонтальной связки и альвеолярной кости с увеличением глубины зондирования, образованию рецессии
или и то, и другое, что в конечном итоге приводит к преждевременной потере зубов. Приблизительно 10% взрослого населения мира очень уязвимы к тяжелому пародонтиту, 10-15%, как представляется,
полностью устойчивы к нему, в то время как остальные колеблются между этими двумя ситуациями [1]. Этиология пародонтита чаще всего связана с скоплением камней вокруг
зуб из-за плохой гигиены полости рта [2]. Другими предрасполагающими факторами могут быть сахарный диабет, половое созревание, менструация, беременность, менопауза, гиперпаратиреоз,
гематологические заболевания, иммунодефицитные состояния, генетические нарушения, стрессовые и психосоматические расстройства, влияние питания, лекарств, сердечные заболевания, курение, жевание
табак и др. Пародонтит рассматривается как прямое следствие инвазии десны и окружающих структур преимущественно грамотрицательными анаэробными бактериями, такими как A.
Actinomycetemcomitans , P. Gingivalis , P. Intermedia , B. Forsythus , C. Retcure , E. Nodatum , P. Micros , E. Nodatum , P. Micros , S. , с. , S. , P. Micros , S. .
и Treponema sp. Хотя этиология понятна как
бактериальный, по патогенезу считается воспалительным. Появляющиеся данные свидетельствуют о том, что воспалительная реакция хозяина может диктовать состав биопленки и
появление возбудителей, вызывающих возникновение пародонтита у восприимчивого хозяина [3]. Пародонтит классифицируется как «генерализованный», когда поражено более 30% зубных рядов.
является вовлеченным и «локализованным», когда менее 30% зубного ряда поражено пародонтальным повреждением, а остальная часть зубного ряда поражена гингивитом.
Пародонтит рассматривается как прямое следствие инвазии десны и окружающих структур преимущественно грамотрицательными анаэробными бактериями, такими как A.
Actinomycetemcomitans , P. Gingivalis , P. Intermedia , B. Forsythus , C. Retcure , E. Nodatum , P. Micros , E. Nodatum , P. Micros , S. , с. , S. , P. Micros , S. .
и Treponema sp. Хотя этиология понятна как
бактериальный, по патогенезу считается воспалительным. Появляющиеся данные свидетельствуют о том, что воспалительная реакция хозяина может диктовать состав биопленки и
появление возбудителей, вызывающих возникновение пародонтита у восприимчивого хозяина [3]. Пародонтит классифицируется как «генерализованный», когда поражено более 30% зубных рядов.
является вовлеченным и «локализованным», когда менее 30% зубного ряда поражено пародонтальным повреждением, а остальная часть зубного ряда поражена гингивитом.
Клиническая картина представляет собой воспаление десны с видимой потерей прикрепления десны, кровоточивостью при зондировании, образованием пародонтального кармана с сопутствующим или не связанным
подвижность зубов. Видимая клиническая картина разрастания десен обусловлена различными этиологическими факторами и усугубляется локальной бактериальной биопленкой.
накопление. Продукты пародонтопатогена воздействуют на ткани десны, активируя клеточные процессы, вызывающие изменение гомеостаза соединительной ткани и
разрушение альвеолярного отростка. Полиморфноядерные лейкоциты и моноциты проходят из субэпителиальной соединительной ткани через соединительный эпителий и
в десневую борозду. Мононуклеарные клетки вместе с секретируемыми ими молекулами и другими молекулами, происходящими из соединительных эпителиальных клеток, крови и тканевой жидкости.
представляют собой первую линию обороны в борьбе с постоянной микробной проблемой. Это приводит к активации нескольких ключевых молекулярных путей, которые в конечном итоге
активируют протеиназы хозяина, которые способствуют потере волокон маргинальной периодонтальной связки, апикальной миграции соединительного эпителия и позволяют апикальному распространению
бактериальная биопленка вдоль поверхности корня, приводящая к образованию пародонтального кармана и потере костной массы [4].
Видимая клиническая картина разрастания десен обусловлена различными этиологическими факторами и усугубляется локальной бактериальной биопленкой.
накопление. Продукты пародонтопатогена воздействуют на ткани десны, активируя клеточные процессы, вызывающие изменение гомеостаза соединительной ткани и
разрушение альвеолярного отростка. Полиморфноядерные лейкоциты и моноциты проходят из субэпителиальной соединительной ткани через соединительный эпителий и
в десневую борозду. Мононуклеарные клетки вместе с секретируемыми ими молекулами и другими молекулами, происходящими из соединительных эпителиальных клеток, крови и тканевой жидкости.
представляют собой первую линию обороны в борьбе с постоянной микробной проблемой. Это приводит к активации нескольких ключевых молекулярных путей, которые в конечном итоге
активируют протеиназы хозяина, которые способствуют потере волокон маргинальной периодонтальной связки, апикальной миграции соединительного эпителия и позволяют апикальному распространению
бактериальная биопленка вдоль поверхности корня, приводящая к образованию пародонтального кармана и потере костной массы [4].
Представление клинического случая
60-летний пациент обратился в нашу стоматологическую поликлинику Kauvery с главной жалобой на чувствительность и подвижность зубов в области правого верхнего заднего зуба в течение двух недель.
с сопутствующим затруднением жевания. У него были периодические боли, которые стихали после приема лекарств. Он был аквалангистом и тренером по плаванию, работал в Саудовской Аравии.
Роялс. Пациент рассказал о курении 20 сигарет в день в течение последних 30 лет, которое он бросил год назад. Он был диабетиком и перенес коронарную артерию.
операция по шунтированию год назад. Его лекарства включали Aztor 20 мг, Cardivas 6,25, Clopilet A 150, Cilacar 10 мг, Ondero и Cipla. При внутриротовом осмотре выявлено
сильное скопление зубного налета, зубного камня и пятен на зубах с сопутствующим дурным запахом изо рта. При осмотре десна показалась гиперемированной, опухшей и сырой, с отступлениями.
края, охватывающие весь зубной ряд (рис. 1). При пальпации определяется болезненность, кровоточивость при зондировании, увеличение глубины пародонтального кармана. Подвижность 3 степени была
наблюдается в правых верхних и нижних молярах и премолярах, нескольких верхних и нижних резцах, а также в левых верхних премолярах и молярах. Генерализованная подвижность 1 степени была
наблюдается с вовлечением других зубов. Промежутки были видны в передних зубах верхней и нижней челюсти. Рентгенологические исследования включали ортопантамографию, которая выявила
горизонтальная потеря костной массы с вовлечением нескольких зубов и патологическая миграция передних зубов верхней и нижней челюсти (рис. 2). Время кровотечения 2 мин, время свертывания
было 5 мин. Окончательный диагноз: генерализованный хронический пародонтит, связанный с потерей костной массы.
1). При пальпации определяется болезненность, кровоточивость при зондировании, увеличение глубины пародонтального кармана. Подвижность 3 степени была
наблюдается в правых верхних и нижних молярах и премолярах, нескольких верхних и нижних резцах, а также в левых верхних премолярах и молярах. Генерализованная подвижность 1 степени была
наблюдается с вовлечением других зубов. Промежутки были видны в передних зубах верхней и нижней челюсти. Рентгенологические исследования включали ортопантамографию, которая выявила
горизонтальная потеря костной массы с вовлечением нескольких зубов и патологическая миграция передних зубов верхней и нижней челюсти (рис. 2). Время кровотечения 2 мин, время свертывания
было 5 мин. Окончательный диагноз: генерализованный хронический пародонтит, связанный с потерей костной массы.
Рис. 1. Внутриротовые фотографии до лечения, показывающие скопление зубного налета, зубного камня и связанные с ними опухшие десны.
Рис. 2. Ортопантамограмма, показывающая горизонтальную потерю костной массы с вовлечением нескольких зубов
План лечения
Лечение, запланированное для этого пациента, заключалось в проведении общего удаления зубного камня и удалении зубов с плохим прогнозом, выраженной подвижностью и потерей костной массы после проверки
общий анализ крови и заключение кардиолога. Экстракцию следует проводить после изменения дозы антикоагулянта в условиях антибиотикопрофилактики. Замена
должно было быть запланировано для беззубых областей после адекватного заживления.
Экстракцию следует проводить после изменения дозы антикоагулянта в условиях антибиотикопрофилактики. Замена
должно было быть запланировано для беззубых областей после адекватного заживления.
Проведенное лечение и результат
По рекомендации кардиолога прием антикоагулянтов был отменен за пять дней до процедуры. Было проверено МНО, которое было в пределах нормы и антибиотикопрофилактика
вводили в качестве предварительной подготовки. Было выполнено грубое скейлинг и введен 2% лигнокаин для блокирования нижнего альвеолярного нерва и длинного щечного нерва.
после чего было проведено внутриальвеолярное удаление правых нижних жевательных зубов. Лунки экстракции были хорошо высушены, чтобы удалить всю грануляционную ткань и физиологический раствор.
был сделан полив. После удаления зуба № 1 обильное кровотечение с гнойным отделяемым. 46 регион был просмотрен. Пальцевое давление марлей было помещено над экстракцией
лунки в обычном состоянии, но при постоянном обильном кровотечении из лунок возникла необходимость в кровоостанавливающем хирургическом впадине. Была попытка наложения швов, но
хрупкая слизистая оболочка начала кровоточить, что привело к заполнению операционного поля кровью, и удалось успешно наложить только один простой узловой шов. Цифровое давление с помощью марли
пропитанный адреналином, давали на 15-20 минут. После того, как кровотечение было в некоторой степени остановлено, накладывали от 5 до 6 простых узловых швов для сближения тканей.
и установить закрытие раны и гемостаз. Для обеспечения послеоперационного гемостаза пациенту была назначена таблетка Трапик 500 мг. Послеоперационные инструкции и экстренный контакт
номера поделились. На следующий день был проведен полный кюретаж десны вокруг других существующих зубов, чтобы гарантировать устранение грануляционной ткани и удаление зубного камня.
поддесневой камень. Пациент был осмотрен через одну неделю, а другие удаления были запланированы через четыре недели. Значительное уменьшение припухлости десен
были замечены. Десна имела кораллово-розовый цвет с точками, указывающими на нормальный цвет, контур и консистенцию.
Была попытка наложения швов, но
хрупкая слизистая оболочка начала кровоточить, что привело к заполнению операционного поля кровью, и удалось успешно наложить только один простой узловой шов. Цифровое давление с помощью марли
пропитанный адреналином, давали на 15-20 минут. После того, как кровотечение было в некоторой степени остановлено, накладывали от 5 до 6 простых узловых швов для сближения тканей.
и установить закрытие раны и гемостаз. Для обеспечения послеоперационного гемостаза пациенту была назначена таблетка Трапик 500 мг. Послеоперационные инструкции и экстренный контакт
номера поделились. На следующий день был проведен полный кюретаж десны вокруг других существующих зубов, чтобы гарантировать устранение грануляционной ткани и удаление зубного камня.
поддесневой камень. Пациент был осмотрен через одну неделю, а другие удаления были запланированы через четыре недели. Значительное уменьшение припухлости десен
были замечены. Десна имела кораллово-розовый цвет с точками, указывающими на нормальный цвет, контур и консистенцию. Повторно получено заключение и согласие кардиолога.
Введение антикоагулянтов снова было прекращено на пять дней, и другие экстракции были завершены. На этот раз значительное уменьшение кровотечения наблюдалось при использовании пальцевого
давление только с помощью марли делает свое дело. Впоследствии пациент был осмотрен, и заживление раны было удовлетворительным с адекватным закрытием экстракции.
розетки (рис. 3). Пациента попросили соблюдать тщательный режим борьбы с зубным налетом, который включал регулярную чистку зубов, использование антисептического ополаскивателя для рта, содержащего
хлоргексидином и массаж десен местным кровоостанавливающим раствором, содержащим цетримид, дубильную кислоту и хлорид цинка. После двухмесячного периода заживления
участки без зубов были заменены акриловыми съемными частичными протезами в качестве временной замены утраченных зубов, и он ожидает установки несъемных частичных протезов (рис. 4).
Повторно получено заключение и согласие кардиолога.
Введение антикоагулянтов снова было прекращено на пять дней, и другие экстракции были завершены. На этот раз значительное уменьшение кровотечения наблюдалось при использовании пальцевого
давление только с помощью марли делает свое дело. Впоследствии пациент был осмотрен, и заживление раны было удовлетворительным с адекватным закрытием экстракции.
розетки (рис. 3). Пациента попросили соблюдать тщательный режим борьбы с зубным налетом, который включал регулярную чистку зубов, использование антисептического ополаскивателя для рта, содержащего
хлоргексидином и массаж десен местным кровоостанавливающим раствором, содержащим цетримид, дубильную кислоту и хлорид цинка. После двухмесячного периода заживления
участки без зубов были заменены акриловыми съемными частичными протезами в качестве временной замены утраченных зубов, и он ожидает установки несъемных частичных протезов (рис. 4).
Рис. 3. Фотографии после экстракции, показывающие зажившую ткань десны.
Рис. 4. Фотографии после лечения, показывающие замену отсутствующих зубов временными частичными протезами.
Обсуждение
Первая проблема в лечении пародонтита – своевременная и правильная диагностика. Поскольку это заболевание протекает относительно бессимптомно, больной сообщает об этом только при умеренном или
продвинутая стадия. Вторая задача заключается в надлежащем контроле всех факторов, способствующих заболеванию, что жизненно важно для достижения хорошего результата лечения. Третий вызов
предполагает длительное сохранение пародонта. Основу пародонтологического лечения составляет механическое удаление бактериальных отложений и зубного камня из поддесневой области.
среды с использованием ручных инструментов или ультразвуковых устройств, выполняемых хирургическим или нехирургическим путем, наряду со строгим режимом борьбы с зубным налетом [5].
Лечение всегда направлено на сохранение большей части зубов и удаление только зубов с неблагоприятным прогнозом и тяжелой потерей костной ткани или потерей костной массы, связанной с фуркацией. это
также важно обеспечить самоочищающуюся среду для пациента, чтобы поддерживать отсутствие зубного налета в периодонте.
это
также важно обеспечить самоочищающуюся среду для пациента, чтобы поддерживать отсутствие зубного налета в периодонте.
В данном конкретном случае потребовалось поэтапное интервенционное стоматологическое лечение. Хотя почти каждое стоматологическое лечение должно начинаться с профилактики полости рта, такой как удаление зубного камня,
мы склонны упускать из виду это для исправления основной жалобы или по экономическим причинам. Распространено мнение, что трата времени и денег на профилактику неоправданна, т.к.
зуб будет удален, но подготовка воспаленных тканей очень важна перед любой инвазивной стоматологической процедурой. Мы также должны быть чрезвычайно бдительны в отношении
поведение тканей при наличии у пациента множественных сопутствующих заболеваний и парафункциональных привычек в течение длительного времени. Как говорится: «Не подготовиться — значит подготовиться к провалу».
чтобы получить хороший результат для любого метода лечения, необходимо получить все исходные данные как на местном, так и на системном уровне, проанализировать и обсудить различные варианты лечения и сформулировать
окончательный план. В этом случае пациент, а также поддерживающие врачи были проинформированы о проблемах, связанных с выполнением стоматологического лечения в один присест и поэтапно.
хирургическое лечение было согласовано с отличным конечным результатом.
В этом случае пациент, а также поддерживающие врачи были проинформированы о проблемах, связанных с выполнением стоматологического лечения в один присест и поэтапно.
хирургическое лечение было согласовано с отличным конечным результатом.
Заключение
Эффективное лечение пародонтита заключается в своевременной и точной диагностике. Устранение предрасполагающих факторов с последующим тщательным контролем зубного налета. одинаково важны для сдерживания прогрессирования заболевания (рис. 5).
Рис. 5. Предварительная, промежуточная и последующая обработка.
Ссылки
- Muñoz-Carrillo JL, Hernández-Reyes VE, García-Huerta OE, Chávez-Ruvalcaba F, Chávez-Ruvalcaba MI, Chávez-Ruvalcaba KM, et al. Патогенез заболеваний пародонта.
2019.
https://www.intechopen.com/books/periodontal-disease-diagnostic-and-adjunctive-non-surgical-considerations/pathogenesis-of-pardontal-disease. - Муна С, Эльбурки.

