Систематика хронических периодонтитов и их место в МКБ-10 Текст научной статьи по специальности «Клиническая медицина»
© САБЛИНА Г.И., КОВТОНЮК П.А., СОБОЛЕВА Н.Н., ЗЕЛЕНИНА Т.Г., ТАТАРИНОВА Е.Н.
УДК 616.314.17-036.12
СИСТЕМАТИКА ХРОНИЧЕСКИХ ПЕРИОДОНТИТОВ И ИХ МЕСТО В МКБ-10
Галина Иннокентьевна Саблина, Петр Алексеевич Ковтонюк, Наталья Николаевна Соболева,
Тамара Григорьевна Зеленина, Елена Николаевна Татаринова (Иркутский государственный институт усовершенствования врачей, ректор д.м.н., проф. В.В. Шпрах, кафедра стоматологии детского возраста и ортодонтии, зав. — к.м.н., доц. Н.Н. Соболева)
Резюме. В сообщении обоснованы уточнения к терминологии клинических форм хронического периодонтита. Клиническая классификация периодонтитов соотнесена с МКБ-10.
Ключевые слова: МКБ-10, периодонтит.
CLASSIFICATION OF CHRONIC PERIODONTITIS AND ITS POSITION IN ICD-10
G.I. Sablina, P.A. Kovtonyuk, Ы.Ы.8оЬо1еуа, T.G. Zelenina, E. N. Tatarinova (Irkutsk State Institute for Postgraduate Medical Education)
Summary. The specification of the terminology of clinical forms of chronic periodontitis has been substantiated. The clinical classification of periodontitis is correlated with ICD-10.
Key words: chronic destructive periodontitis, the International Classification of Diseases (ICD-10).
В связи с появлением приказа Минздрава РФ № 170 от 27.05.1997 г. «О переходе органов и учреждений здравоохранения Российской Федерации на МКБ-10» обозначилась проблема ведения стоматологической документации, связанная с необходимостью использования двух классификаций: статистической и клинической.
Клиническая классификация позволяет регистрировать нозологическую форму патологии, дифференцировать ее от других форм, определять оптимальный метод лечения и прогнозировать его результат.
Международная классификация болезней (МКБ-10) — это система рубрик, в которую отдельные патологические состояния включены в соответствии с определенными установленными критериями [16]. МКБ-10 используется для преобразования словесной формулировки диагнозов болезней и других проблем, связанных со здоровьем, в буквенно-цифровые коды, которые обеспечивают удобство хранения, извлечения и анализа данных.
 Например, Т.Л. Рединова (2010) хронический гранулирующий периодонтит предлагает относить к коду 04.6 — периапикальному абсцессу со свищем, тогда как Е.В. Боровский (2004) считает, что данная нозологическая форма соответствует коду 04.5 — хроническому апикальному периодонтиту.
Например, Т.Л. Рединова (2010) хронический гранулирующий периодонтит предлагает относить к коду 04.6 — периапикальному абсцессу со свищем, тогда как Е.В. Боровский (2004) считает, что данная нозологическая форма соответствует коду 04.5 — хроническому апикальному периодонтиту.
Целью сообщения явилось обоснование внесения изменений в клиническую классификацию хронических периодонтитов и адаптации ее к МКБ —10.
С 1936 года по настоящее время в нашей стране основной классификацией поражений тканей периодонта является классификация И.Г. Лукомского [5, 7, 10, 13, 25].Острые формы:
— острый серозный верхушечный периодонтит,
— острый гнойный верхушечный периодонтит.
Хронические формы:
— хронический верхушечный фиброзный периодонтит,
— хронический верхушечный гранулирующий периодонтит,
— хронический верхушечный гранулематозный периодонтит.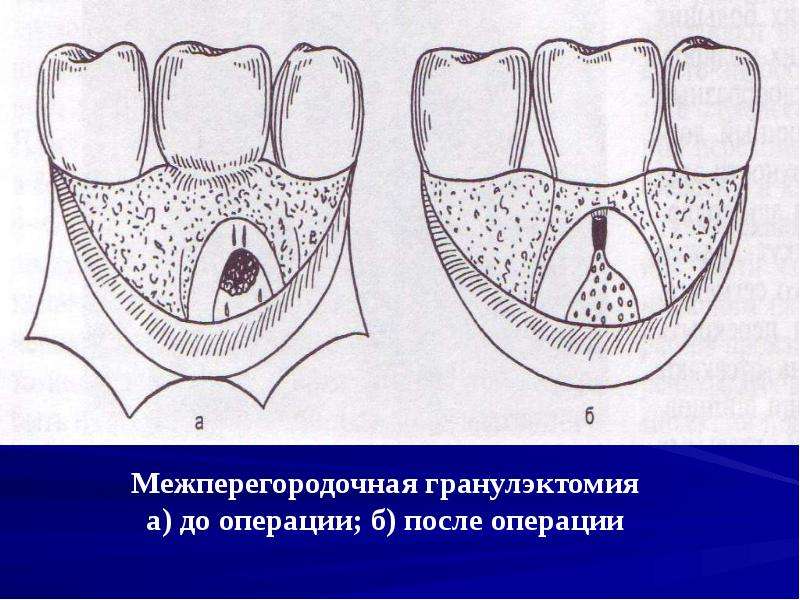
Обострившийся хронический верхушечный периодонтит.
Корневая киста.
Следует отметить, что изначально И.Г. Лукомский выделил всего две формы хронического периодонтита: фиброзный и грануломатозный. Позднее грануломатоз-ный периодонтит был дифференцирован на гранулома-тозный и гранулирующий в зависимости от степени активности процесса хронического воспаления и степени токсичности очагов [5].
Классификация И.Г. Лукомского основана на патологических морфологических изменениях в периодонте. В то же время, клинически часто сложно определить характер воспалительного процесса. Хронические периодонтиты нередко протекают со скудной симптоматикой [23]. Различия в клиническом течении гранулирующей и гранулематозной форм незначительны и недостаточны для дифференциальной диагностики этих форм, а фиброзный периодонтит не имеет собственных клинических признаков [23, 24].
В зависимости от клинической и патологоанатомической картины хронические периодонтиты допускают представлять в двух формах: стабилизированной и активной. К стабилизированной форме относят фиброзный периодонтит, к активной (деструктивной) — гранулирующую и гранулематозную формы. Активная форма хронических периодонтитов сопровождается образованием грануляций, свищевых ходов, гранулем, возникновением нагноений в околочелюстных тканях.
По этому поводу еще в 2003 году, заслуженный деятель науки РФ, профессор Е.В. Боровский утверждал, что нет необходимости деления хронического периодонтита на гранулирующий и гранулематозный [24]. Мы поддерживаем данную точку зрения в том, что эти формы хронического периодонтита целесообразно определять одним клиническим диагнозом «хронический деструктивный периодонтит», основываясь на том, что морфологическая картина характеризуется деструкцией костной ткани при той и другой формах патологии.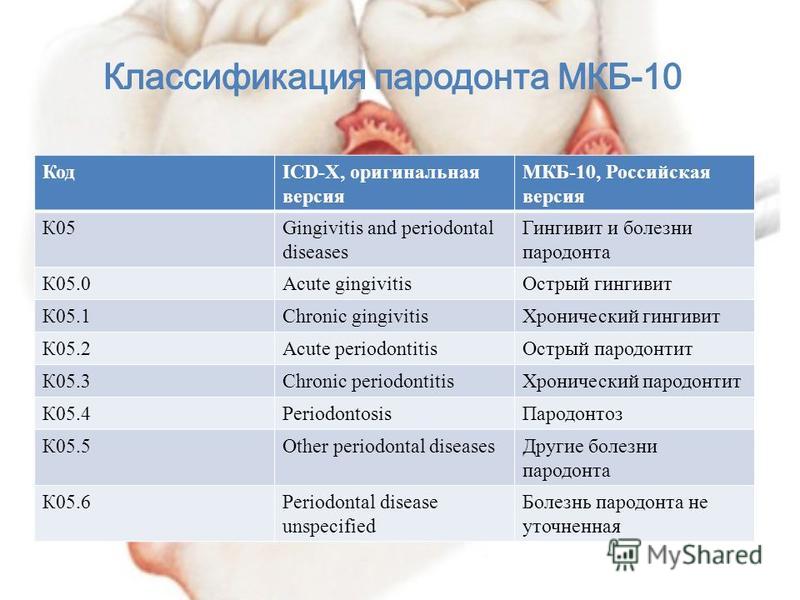
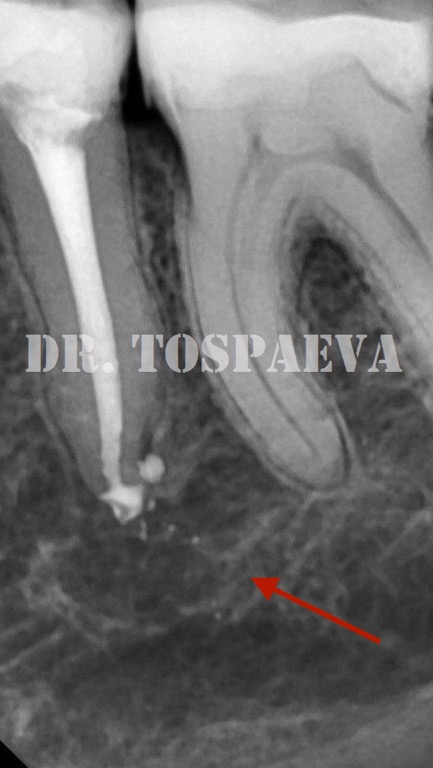
В руководствах и учебниках по стоматологии приводится традиционное описание рентгенологической характеристики хронического гранулирующего и гранулематозного периодонтитов [7,12, 13,14, 23, 24, 25].
Соответствие классификаций хронических периодонтитовНозологические формы периодонтитов по классификации И. Г. Лукомского Нозологическая форма по предлагаемой систематике Код по МКБ-10
Г. Лукомского Нозологическая форма по предлагаемой систематике Код по МКБ-10
Хронический гранулирующий периодонтит, хронический гранулематозный периодонтит Хронический деструктивный периодонтит К 04.5. Хронический апикальный периодонтит (апикальная гранулема)
Хронический фиброзный периодонтит Хронический фиброзный периодонтит К 04.9. Другие неуточненные болезни пульпы и периапикальных тканей
Обострившийся хронический периодонтит Обострившийся хронический периодонтит К 04.7. Периапикальный абсцесс без свища
Как отмечают Н.А. Рабухина, А.П. Аржанцев (1999) «Патоморфологические данные свидетельствуют, что более 90% рентгенологически выявляющихся периа-пикальных разрежений, не имеющих отчетливой клиники, являются гранулемами. Рентгенологическая характеристика гранулирующего и гранулематозного периодонтитов неспецифична, и поэтому не может служить основанием для выделения морфологических типов периодонтитов, как это нередко делают стоматологи на практике. На I Международном конгрессе челюстно-лицевых рентгенологов в 1969 году принято специальное решение об ошибочности использования рентгенологических данных для определения гистопа-тологической сущности зон периапикальной костной резорбции».
На I Международном конгрессе челюстно-лицевых рентгенологов в 1969 году принято специальное решение об ошибочности использования рентгенологических данных для определения гистопа-тологической сущности зон периапикальной костной резорбции».
Имеющиеся в литературе морфологические данные убедительно доказывают, что нет необходимости деления хронического периодонтита на гранулирующий и гранулематозный, т.к. это различные стадии одного и того же процесса. При снижении реактивности организма грануляционная ткань активно развивается с выходом в костную ткань альвеолы без четких границ, причем ее трансформация в зрелую соединительную ткань задерживается [2, 17]. При гранулематозной форме у верхушки корня пораженного зуба разрастание отграничивается макроорганизмом образованием зрелой волокнистой соединительной ткани в виде капсулы, не имеющей соединения с зубной альвеолой кости. Такое образование называется апикальной гранулемой.
Е. В. Боровский (2003) указывает на то, что размер и форма гранулемы может изменяться. В случае преобладания раздражителей корневого канала происходит активация процесса, что рентгенологически проявляется резорбцией костной ткани, отображающейся потерей четкости контуров очага разрежения и его увеличением. Если же побеждают защитные механизмы, то очаг разрежения костной ткани на рентгенограмме стабилизируется и имеет четкие контуры. Автор считает, что эти изменения являются различными стадиями одного и того же процесса.
В. Боровский (2003) указывает на то, что размер и форма гранулемы может изменяться. В случае преобладания раздражителей корневого канала происходит активация процесса, что рентгенологически проявляется резорбцией костной ткани, отображающейся потерей четкости контуров очага разрежения и его увеличением. Если же побеждают защитные механизмы, то очаг разрежения костной ткани на рентгенограмме стабилизируется и имеет четкие контуры. Автор считает, что эти изменения являются различными стадиями одного и того же процесса.
Таблица 1 Описанные изменения в очаге деструкции согласуются с его морфологической характеристикой, описанной Fisch (1968). Автор выделяет в периапикальном очаге четыре морфологические зоны:
— зону инфекции
— зону разрушения
— зону воспаления
— зону стимуляции.
Изложенные выше морфологические и
рентгенологические обоснования к объединению гранулирующего и гранулематозного периодонтитов в деструктивную нозологическую форму подтверждаются еще и тем, что выбор метода лечения и исход этих периодонтитов не зависит от формы деструкции патологического очага. И при гранулирующем и при гранулематозном периодонтите лечебные мероприятия должны быть направлены на устранение инфекционного очага, снижение инфекционно-токсического, аллергического и аутоиммунного воздействия на организм, предотвращение распространения инфекции [4, 6, 9, 11, 22, 24, 25].
Следует также отметить, что с точки зрения современной стоматологической терминологии в классификации периодонтитов не всегда употребляется слово «верхушечный» для уточнения локализации процесса. Многие специалисты, рассматривая патологию периодонта, понимают локализацию очага деструкции в околоверхушечной или фуркационной зоне зуба. Это объясняется тем, что деструкция, возникающая в маргинальном пародонте, характеризуемая ранее как «маргинальный периодонтит» [5], после принятия классификации заболеваний пародонта в 1986 году диагностируется как локализованный пародонтит [5, 18, 22, 26].
Это объясняется тем, что деструкция, возникающая в маргинальном пародонте, характеризуемая ранее как «маргинальный периодонтит» [5], после принятия классификации заболеваний пародонта в 1986 году диагностируется как локализованный пародонтит [5, 18, 22, 26].
Таким образом, мы считаем целесообразным различать следующие нозологические формы хронических периодонтитов:
— хронический фиброзный периодонтит
— хронический деструктивный периодонтит
— обострившийся хронический периодонтит.
Предложенная систематика была соотнесена нами с
кодами МКБ-10 (табл. 1).
Нами не принят код 04.6 — периапикальный абсцесс со свищем, рекомендуемый некоторыми авторами [21]. Мы считаем необоснованным использовать термин «свищ» для обозначения хронического гранулирующего периодонтита. Свищ наблюдается как при гранулирующем, так и при гранулематозном периодонтитах. Термин же «абсцесс» в Энциклопедическом словаре медицинских терминов (1982 год, том 1) трактуется как «отделяться, нарывать; син.: апостема, гнойник, нарыв», что не всегда соответствует клинической картине гранулирующего периодонтита.
Мы считаем необоснованным использовать термин «свищ» для обозначения хронического гранулирующего периодонтита. Свищ наблюдается как при гранулирующем, так и при гранулематозном периодонтитах. Термин же «абсцесс» в Энциклопедическом словаре медицинских терминов (1982 год, том 1) трактуется как «отделяться, нарывать; син.: апостема, гнойник, нарыв», что не всегда соответствует клинической картине гранулирующего периодонтита.
Известно, что хронический фиброзный периодонтит может являться исходом лечения пульпитов, периодонтитов, травм, функциональной перегрузки пародонта и др. Фиброзные изменения периодонта не имеют собственных клинических проявлений и поэтому по МКБ-10 он может быть отнесен к коду 04.9 — другие неуточ-ненные болезни пульпы и периапикальных тканей.
Гранулирующий и гранулематозный хронические периодонтиты, объединенные термином деструктивный периодонтит, соответствуют коду 04. 5 — хронический апикальный периодонтит (апикальная гранулема).
5 — хронический апикальный периодонтит (апикальная гранулема).
Код 04.7 — периапикальный абсцесс без свища соответствует обострению всех форм хронических периодонтитов.
Таким образом, обоснованная систематика хронических периодонтитов соответствует классификации ВОЗ 10-го пересмотра. Она упрощает клиническую диагностику, ведение документации, внутриведомственный контроль лечения и вневедомственную оценку страховыми компаниями уровня качества лечения (УКЛ).
ЛИTEPATУPA
1. Алимова М.Я., Боровский Е.В., Макеева И.М., Бондаренко И.В. Анализ классификационных систем раздела «Кариес и его осложнения» // Эндодонтия today. — 2008. — №2. — С. 49-54.
2. Бойкова С.П., Зайратьянц О.В. Клиникоморфологическая характеристика и классификация кариеса и его и его осложнений (пульпит, периодонтит, радикуляр-ная киста) в соответствии с требованиями Международной классификации стоматологических болезней // Эндодонтия today. — 2008. — №1. — С. 3-11.
— 2008. — №1. — С. 3-11.
3. Боровский Е.В. Терминология и классификация кариеса зубов и его осложнений // Клиническая стоматология. — 2004. — №1. — С. 6-9.
4. Галанова Т.А., Цепов Л.М., Николаев А.И. Алгоритм лечения хронического апикального периодонтита // Эндодонтия today. 2009. — № 3. — С. 74-78
5. Гофунг Е.М. Учебник терапевтической стоматологии. — М.: Медгиз, 1946. —510 с.
6. Гринин В.М., Буляков Р.Т., Матросов В.В. Пероральная антибактериальная терапия в лечении деструктивных форм верхушечного периодонтита на фоне системного остеопороза. // Эндодонтия today. — 2011. — №1. — С. 49-51
7. Детская терапевтическая стоматология: нац. рук./ Под ред. В.К. Леонтьева, Л.П. Кисельникова. — М.: ГЭОТАР-Медиа, 2010. — 896 с.
8. ЖурочкоЕ.И., Дегтярева Л.А. Комплексный метод оценки состояния околоверхушечных тканей зуба при хроническом верхушечном периодонтите // Эндодонтия today. — 2008. — № 2. — С. 27-31.
ЖурочкоЕ.И., Дегтярева Л.А. Комплексный метод оценки состояния околоверхушечных тканей зуба при хроническом верхушечном периодонтите // Эндодонтия today. — 2008. — № 2. — С. 27-31.
9. Звонникова Л.В., Георгиева О.А., Нисанова С.Е., Иванов Д.С. Использование современных антиоксидантов в комплексном лечении апикального периодонтита//Эндодонтия today. — 2008. — №1. — С. 85-87
10. Иванов В.С., Овруцкий Г.Д., Гемонов В.В. Практическая эндодонтия. — М.: Медицина, 1984. — 224 с.
11. Лавров И.К. Выбор метода лечения хронического апикального периодонтита у пациентов пожилого возраста в зависимости от сопутствующей патологии//Эндодонтия today. — 2010. — №2. — С. 68-72.
12. Лукиных Л.М., Лившиц Ю.Н. Верхушечный периодонтит. — Нижний Новгород, 1999. — с.
13. -lQ) // Эндодонтия today. — 2QQ9. — №3. — С. 17-2Q.
-lQ) // Эндодонтия today. — 2QQ9. — №3. — С. 17-2Q.
16. Mеждунapoднaя статистическая классификация болезней и проблем, связанных со здоровьем. Ш-й пересмотр. Т.1, Т.2, Т.З. — Женева: Всемирная организация здравоохранения, l995.
17. Мигунов Б.И. Патологическая анатомия заболеваний зубо-челюстной системы и полости рта. — M., 1963. — 136 с.
18. Mumpoнuн A.B., Bopoнuна К.Ю. Опыт эндодонтиче-ского лечения хронического периодонтита при наличии перфорации в области фуркации корней// Эндодонтия today. — 2Qm. — №4. — С. 3-5.
19. Pабуxuна H.A., Apжанuев A.n. Рентгенодиагностика в стоматологии. — M.: Mедицинскoе информационное агентство, 1999. — 452 с.
2Q. Pабуxuна H.A., Гpuгopьянu ЛЛ., Бадалян B.A. Роль рентгенологического исследования при эндодонтическом и хирургическом лечении зубов // Швое в стоматологии. злова. — СПб.: СпецЛит., 2QQ3. — C19Q-195.
злова. — СПб.: СпецЛит., 2QQ3. — C19Q-195.
24. Терапевтическая стоматология: Учебник для студентов медицинских вузов / Под ред. Е.В. Боровского. — M.: Mедицинскoе информационное агентство, 2QQ3. — 64Q с.
25. Терапевтическая стоматология: национальное руководство / Под ред. ЛА. Дмитриевой, ЮМ. Maксимoвскoгo. — M.: ГЭOTAP-Mедиa, 2QQ9. — 912 с.
26. Токмакова С.И., Жукова E.Q, Бондаренко O.B., Сысоева O.B. Оптимизация лечения деструктивных форм хронического периодонтита с применением препаратов гидроокиси кальция // Эндодонтия today. — 2Q1Q. — №4. — С. 61-64.
Информация об авторах: 664079, Иркутск, м-н Юбилейный, 100, ИГИУВ, e-mail: [email protected]
Галина Иннокентьевна Саблина — доцент, к.м.н.,
Петр Алексеевич Ковтонюк — доцент, к. м.н.,
м.н.,
Соболева Наталья Николаевна — заведующий кафедрой, к.м.н., доцент;
Тамара Григорьевна Зеленина — доцент, к.м.н.,
Елена Николаевна Татаринова — ассистент. тел. 89025695566, [email protected]
МКБ-10 код K04.5 | Хронический апикальный периодонтит
ICD-10
ICD-10 is the 10th revision of the International Statistical Classification of Diseases and Related Health Problems (ICD), a medical classification list by the World Health Organization (WHO).
It contains codes for diseases, signs and symptoms, abnormal findings, complaints, social circumstances, and external causes of injury or diseases.
ATC
The Anatomical Therapeutic Chemical (ATC) Classification System is used for the classification of active ingredients of drugs according to the organ or system on which they act and their therapeutic, pharmacological and chemical properties.
It is controlled by the World Health Organization Collaborating Centre for Drug Statistics Methodology (WHOCC).
DDD
The defined daily dose (DDD) is a statistical measure of drug consumption, defined by the World Health Organization (WHO).
It is used to standardize the comparison of drug usage between different drugs or between different health care environments.
| Назначение | Групповая принадлежность |
Название лекарственного препарата или средства/ МНН |
Дозировка, способ применения | Разовая доза, кратность и длительность применения |
|
Для обезболивания Выбрать из предложенного: |
Местные анестетики |
Аrticaine + epinephrine |
1:100 000, 1:200 000, 1,7 мл, инъекционное обезболивание |
1:100 000, 1:200 000 По 1,7 мл, однократно |
| Articaine + epinephrine | 4% 1,7 мл, инъекционное обезболивание | По 1,7 мл, однократно | ||
|
Лидокаин/ lidocainum |
2% раствор, 5,0 мл инъекционное обезболивание |
По 1,7 мл, однократно | ||
|
Для антисептической обработки Выбрать из предложенного: |
Хлорсодержащие препараты | Гипохлорит натрия | 3% раствор, обработка кариозной полости и корневых каналов |
Однократно 2-10мл |
|
Хлоргексидина биглюконат/ Хлоргексидин |
0,05% раствор 100 мл, обработка кариозной полости и корневых каналов |
Однократно 2-10мл |
||
| Йодсодержащие препараты |
Йодинол/ Iodinolum |
1% раствор 100 мл, внутриканально |
Однократно 2-3мл |
|
|
Для эндоповязок Выбрать из предложенного: |
Производные фенола | Крезофен | Раствор 13 мл, эндоповязка |
Однократно 1мл |
| Крезодент | Раствор 13 мл, эндоповязка |
Однократно 1мл |
||
| Для химической обработки корневых каналов Выбрать из предложенного: | Препараты на основе ЭДТА | Канал плюс |
Гель 5г внутриканально |
Однократно необходимое количество |
| МД-гель-крем |
Гель 5г , внутриканально |
Однократно необходимое количество | ||
| RC-PREP |
Гель 10г внутриканально |
Однократно необходимое количество | ||
| Для временной обтурации корневых каналов Выбрать из предложенного: | Временные пломбировочные материалы для корневых каналов | Абсцесс-ремеди |
Порошок 15 мг, жидкость 15 мл, внутриканально |
Однократно 2-3 капли жидкости смешать с порошком до пастообразной консистенции |
| Иодент | Паста 25 мг, внутриканально | Однократно необходимое количество | ||
| Демеклоциклин+Триамцинолон |
паста 5 г внутриканально |
Однократно необходимое количество | ||
| Водная суспензия гидроксида кальция |
Порошок 100г, дистиллированная вода 5мл внутриканально |
Однократно 0,05 мл дистиллированной воды смешать с порошком до пастообразной консистенции | ||
| Постоянные пломбировочные материалы для корневых каналов Выбрать из предложенного: | эвгенолсодержащие | Эндофил |
Порошок 15г, жидкость 15 мл внутриканально |
Однократно 2-3 капли жидкости смешать с порошком до пастообразной консистенции |
| Эндометазон |
Порошок 15г, жидкость 15мл внутриканально |
Однократно 2-3 капли жидкости смешать с порошком до пастообразной консистенции | ||
| на основе эпоксидных смол | АН плюс |
Паста А 4 мг Паста В 4 мг внутриканально |
Однократно 1:1 |
|
| АН-26 |
Порошок 8г, паста 7,5г внутриканально |
Однократно 1:1 | ||
| кальцийсодержащий | Сиалапекс |
Базовая паста 12г Катализатор 18г внутриканально |
Однократно 1:1 |
|
| на основе резорцин-формалина | Резодент |
Порошок 20г, жидкость лечебная 10мл, жидкость для отверждения 10 мл внутриканально |
Жидкости 1:1 и смешать с порошком до пастообразной консистенции |
|
| Для наложения изолирующей прокладки Выбрать из предложенного: |
Стеклоионо мерные цементы под пломбировочные материалы светового и химического отверждения |
Кетак моляр | Порошок А3 – 12,5г, жидкость 8,5мл. Изолирующая прокладка | Однократно 1 каплю жидкости смешать с 1 мерной ложкой порошка до пастообразной консистенции |
| Кавитан плюс |
Порошок 15г, жидкость 15мл Изолирующая прокладка |
Однократно 1 каплю жидкости смешать с 1 мерной ложкой порошка до пастообразной консистенции | ||
| Ионосил |
паста 4г, паста 2,5г Изолирующая прокладка |
Однократно необходимое количество | ||
| Цинк-фосфатные цементы под пломбировочные материалы химического отверждения | Адгезор |
Порошок 80г., жидкость 55г Изолирующая прокладка |
Однократно 2,30г порошка на 0,5 мл жидкости замешать |
|
| для наложения постоянной пломбы композитные пломбировочные материалы Выбрать из предложенного: |
Светового отверждения |
Филтек Z 550 |
4,0г пломба |
Однократно Средний кариес – 1,5г, Глубокий кариес – 2,5г, пульпит, периодонтит – 6,5г |
| Харизма |
4,0г пломба |
Однократно Средний кариес – 1,5г, Глубокий кариес – 2,5г, пульпит, периодонтит – 6,5г |
||
| Филтек Z 250 |
4,0г пломба |
Однократно Средний кариес – 1,5г, Глубокий кариес – 2,5г, пульпит, периодонтит – 6,5г |
||
| Филтек ультимат |
4,0г пломба |
Однократно Средний кариес – 1,5г, Глубокий кариес – 2,5г, пульпит, периодонтит – 6,5г |
||
| Химического отверждения | Харизма |
Базовая паста 12г катализатор 12г пломба |
Однократно 1:1 |
|
| Эвикрол |
Порошок 40г, 10г, 10г, 10г, жидкость 28г, пломба |
Однократно 1 каплю жидкости смешать с 1 мерной ложкой порошка до пастообразной консистенции | ||
| Адгезивная система для наложения пломбы из композита светового отверждения | Выбрать из предложенного: | Syngle Bond 2 |
жидкость 6г в кариозную полость |
Однократно 1 капля |
| Prime&Bond NT |
жидкость 4,5 мл в кариозную полость |
Однократно 1 капля |
||
| Для кондиционирования эмали и дентина | Эйч гель |
гель 5г в кариозную полость |
Однократно Необходимое количество |
|
| Для наложения временной пломбы Выбрать из предложенного: | Временные пломбировочные материалы | Искусственный дентин |
Порошок 80г, жидкость – дистиллированная вода в кариозную полость |
Однократно 3-4 капли жидкости смешать необходимым количеством порошка до пастообразной консистенции |
| Дентин-паста MD-TEMP |
Паста 40г в кариозную полость |
Однократно необходимое количество | ||
|
Для отделки пломбы Выбрать из предложенного: |
Абразивные пасты | Депурал нео |
Паста 75г для полирования пломбы |
Однократно необходимое количество |
| Супер полиш |
Паста 45г для полирования пломбы |
Однократно необходимое количество |
Классификация периодонтитов: код по мкб–10
Неоднозначные трактовки форм воспаления периодона и основных методов лечения породили множество классификаций, предложенных ведущими мировыми специалистами в этой области стоматологии.
Периодонтит — воспалительное заболевание периодонта, т.е. соединительных тканей, окружающих корень зуба.
Классифицировать периодонтиты по ряду признаков необходимо потому, что при разных формах течения данного заболевания лечебные тактики могут иметь значительные отличия.
Классификация по происхождению ↑
Инфекционный
Данная форма периодонтита является самой распространённой. Причиной его возникновения является микрофлора, чаще всего проникающая в периодонт из корневого канала через верхушечное отверстие.
Верхушечный ериодонтит
Другими путями инфицирования являются маргинальный (краевой) периодонт (при глубоких зубодесневых и костных карманах) и периодонт соседнего зуба (при образовании кисты значительного размера, разросшейся до вовлечения в процесс корней соседних зубов).
Маргинальный и боковой периодонтиты
Возможность попадания микрофлоры в область периодонта с током крови рядом врачей расценивается как маловероятная и обычно допускается при периодонтитах с невыясненной этиологией (причиной).
Травматический
Возникает при воздействии на периодонт нагрузки, превышающей его физиологические возможности.
Такая перегрузка может быть острой и кратковременной (удар, ушиб) или хронической (перегруженность зуба выступающей пломбой, несъёмным или съёмным протезом, при нарушении прикуса, при вредных привычках — удерживать курительную трубку передними зубами, и т.п.).
Травма периодонта зависит не только от интенсивности травмирующего фактора, но и от состояния самого периодонта. Если периодонт сильно повреждён или значительно утрачен, например, вследствие пародонтоза, то даже нормальная, физиологичная нагрузка может стать травмирующей.
Медикаментозный
Возникает при раздражающем воздействии на периодонт медицинских препаратов. Это может быть действие ошибочно применённых веществ, не предназначенных для использования в полости рта, или необходимых препаратов, но с нарушением требуемой технологии или рекомендуемой концентрации.
Медикаментозный (мышьяковистый) периодонтит
Вызвать медикаментозный периодонтит могут устаревшие методы лечения (при обработке каналов по Дубровину раствором «царской водки»), длительное наложение мышьяковистых паст при лечении пульпита.
При нарушении технологии внутриканального отбеливания также могут возникнуть нежелательные осложнения в виде периодонтита.
Травматический и медикаментозный периодонтиты первое время могут вести себя как асептические, но лёгкое присоединение инфекции быстро переводит эти формы воспаления в инфекционную.
Видео: периодонтит
Классификация периодонтитов по МКБ-10 (ВОЗ) ↑
Международная организация подошла к классификации периодонтитов всесторонне. Она предложила классификацию, которая учитывает не только острое или хроническое течение заболевания, но и наиболее часто встречающиеся виды осложнений.
Такой подход к обследованию и лечению различных форм периодонтитов помогает более полно воздействовать на все механизмы развития патологического процесса, а также объединять действия различных специалистов (например, стоматолог-терапевт, стоматолог-хирург и ЛОР).
В МКБ-10 периодонтиты обозначены в разделе К04 — болезни периапикальных тканей.
К04.4 Острый апикальный периодонтит пульпарного происхождения
Острый апикальный периодонтит — один из классических вариантов, с чётко обозначенными причиной и клиническими проявлениями. Первоочередная задача врача — снятие остроты процесса, а также источника инфицирования.
К04.5 Хронический апикальный периодонтит
Апикальная гранулёма — имеется давний очаг инфекции. При большом размере гранулёмы следует рассматривать и хирургические методы лечения, например резекцию, усечение корневой верхушки
Апикальная гранулема
К04.6 Периапикальный абсцесс со свищом:
- дентальный
- дентоальвеолярный,
- периодонтальный абсцесс пульпарного происхождения.
Свищи разделяются в зависимости от того, с чем имеется сообщение:
- К04.60 Имеющий сообщение [свищ] с верхнечелюстной пазухой.
- К04.61 Имеющий сообщение [свищ] с носовой полостью.
- К04.62 Имеющий сообщение [свищ] с полостью рта.
- К04.63 Имеющий сообщение [свищ] с кожей.
- К04.69 Периапикальный абсцесс со свищом неуточнённый.
Свищ, имеющий сообщение с полостью рта (слева) и с кожей (справа)
Эти диагнозы подразумевают возможность тесного сотрудничества со специалистами по лечению ЛОР-органов. Если есть свищевой ход в гайморову пазуху, без гайморита никак не обойдётся.
Если процесс давний, застарелый, то вполне возможно, что и свищ сформирован и после ликвидации причины сам уже не рассосётся. Следует подумать о хирургическом иссечении.
К04.7 Периапикальный абсцесс без свища
- Дентальный абсцесс,
- Дентоальвеолярный абсцесс,
- Периодонтальный абсцесс пульпарного происхождения,
- Периапикальный абсцесс без свища.
К04.8 Корневая киста
- К04.80 Апикальная и боковая.
Киста зуба
Корневая киста требует либо длительного воздействия, либо более решительного (хирургического).
При консервативном лечении следует дренировать кистозную полость, а также ликвидировать микрофлору, поддерживающую рост кисты. Кроме того, необходимо разрушит внутреннюю выстилку кисты, дав возможность восстановлению костной ткани.
По Лукомскому ↑
Классификация по Лукомскому на сегодняшний день является наиболее востребованной в практической стоматологии. При небольшом объёме она охватывает и характеризует все клинически значимые формы периодонтитов, при диагностике и лечении которых могут быть принципиальные различия.
Острый периодонтит
Острый периодонтит разделяется на:
- серозный. Жалобы на дискомфорт или болезненность, усиливающиеся при постукивании по зубу. Возможно чувство распирания. Интенсивность жалоб постепенно нарастают. При осмотре выявляется большая пломба или значительный дефект коронки зуба, зондирование и термопроба которого безболезненны.
- гнойный. Жалобы на сильную, рвущую, пульсирующую боль, значительно увеличивающуюся при малейшем прикосновении к зубу (при закрывании рта). Возможен отёк прилежащих мягких тканей, а также увеличение и болезненность ближайших лимфатических узлов. Нередко острый гнойный периодонтит сопровождается общими расстройствами организма: слабостью, повышением температуры, ознобом.
Хронический периодонтит
Хронические формы периодонтитов могут являться следствием острых, но могут возникать и как изначально хронические. Жалобы обычно не выражены или весьма незначительны, например, в виде лёгкой болезненности при постукивании по зубу.
Зуб может иметь большую пломбу или быть сильно разрушен, часто изменён в цвете.
Хронический периодонтит
Основным методом диагностики хронических периодонтитов является рентгенография, она же является и методом дифференциальной диагностики между отдельными формами хронических воспалений периодонта.
Гранулирующий
Гранулирующий периодонтит
Рентгенологически проявляется неравномерным расширением периодонтальной щели в области верхушечного отверстия. Расширение не имеет чётких контуров, размеры колеблются от 1–2 до 5–8 мм.
Гранулематозный
Гранулематозныей периодонтит
На снимке выглядит как округлый очаг разрушения костной структуры с чёткими, контрастными краями.
Может располагаться как в области верхушки корня, соприкасаясь с ней, так и окаймлять значительную часть нижней трети корня зуба. При дальнейшем прогрессировании процесса перерастает в околокорневую кисту.
Фиброзный
Проявляется в виде равномерного расширения периодонта либо только в области верхушки корня, либо на всём протяжении. При этом часто костная стенка лунки зуба не имеет признаков разрушения.
Если такой процесс наблюдается у зуба, ранее подвергнутому эндодонтическому лечению, если жалоб нет и состояние корневой пломбы не вызывает нареканий, то проведения лечения не требуется.
Хронический в стадии обострения
Клинически проявляется как острый периодонтит, но имеет рентгенологические признаки хронического. Часто сопровождается появлением припухлости (периоститом) и/или наличием свищевых ходов с активным гнойным отделяемым.
Хронический периодонтит — серьёзное осложнение не лечённого, или не вылеченного кариеса. Он является источником очень активной микрофлоры, способной дать как местные осложнения (периостит, остеомиелит, абсцессы и флегмоны челюстно-лицевой области), так и нанести общий вред организму (сепсис).
Особенно опасны периодонтальные очаги во время беременности. Поэтому задача каждого человека — не допускать появления любых форм периодонтитов и своевременно обращаться к стоматологу для оказания квалифицированной помощи.
Источник: http://zubzone.ru/lechenie-zubov/periodontit/klassifikacija-periodontitov.html
Как разобраться в формах периодонтита: классификация поможет в лечении болезни?
В соответствии с ней недуг относится к категории болезней периапикальных тканей (К04). Выделяются следующие основные формы периодонтита согласно этой классификации:
-
Острый апикальный периодонтит пульпарного происхождения — К04.4. Это наиболее типичная разновидность патологии с чётко выраженным проявлением.
Развивается она в 2 этапа. На первой стадии появляются продолжительный, ноющий болевой синдром. Вторая стадия характеризуется интенсивными, непрерывными болями, усиливающимися при любом прикосновении.
Появляется отёк тканей, зуб приобретает подвижность. Болезнь протекает с ухудшением общего состояния, головной болью, повышением температуры тела выше 37,5 ºС. В крови обнаруживается лейкоцитоз и увеличенная СОЭ.
-
Хронический апикальный периодонтит (код К04.5). Основным очагом поражения при это форме периодонтита становится апикальная гранулёма, но воспалительный процесс протекает медленно с чередованием стадий обострения и ремиссии.
Хроническая форма периодонтита чаще всего становится следствием невылеченного острого периодонтита, но может иметь и первичную этиологию. На стадии ремиссии симптоматика выражена нечётко: почернение зуба, небольшой болевой синдром при надавливании. А период обострения проявления аналогичен острой форме патологии.
Помимо 2 основных форм МКБ-10 выделяют характерные осложнения болезни. Отдельно классифицируется абсцесс периапикального типа с образованием свища (код К04.6) и без него (код К04.
7). Свищ может соединяться с носовой или ротовой полостью, достигать кожного покрова или верхнечелюстной пазухи. Кроме того, выделяется корневая киста (код К04.8) бокового или апикального типа.
Виды болезни по ММСИ
Наиболее часто обнаруживается верхушечная разновидность периодонтита, которая возникает в результате проникновения инфекции по корневым каналам через отверстия в их верхней части. В начальный период поражается корневая верхушка, но постепенно процесс переходит на периодонт.
Классификация по ММСИ предусматривает выделение разных видов периодонтита по клиническому течению:
-
Острый верхушечный — продолжительность может составлять от 2 до 10 суток, отмечается выраженное проявление всех симптомов: ноющая боль, отёк, покраснение, общая интоксикация.
В развитии острой формы прослеживаются 2 основные фазы: серозная и гнойная.
- Хронический верхушечный — этот вид периодонтита характеризуется вялотекущим воспалительным процессом с отсутствием ярко выраженных симптомов. В зависимости от локализации очага поражения и степени его выделяется несколько разновидностей этой формы патологии. В основном болезнь определяется по изменению цвета зуба и небольших болевых ощущениях при надавливании на него.
- Хронический на стадии обострения — данный вид хронического периодонтита возникает при появлении выраженных нарушениях ткани периодонта. Деструкция часто обнаруживается по глубоким полостям кариозного типа. Симптоматика во многом аналогична острой форме патологии, но боль при резком нажатии обычно менее интенсивна. Характерно также отсутствие реакции тканей на температурное воздействие.
Важно! Выявление формы заболевания помогает оптимизировать методику лечения.
При своевременном диагностировании проводится терапевтическое воздействие, направленное на прекращение воспаления, очистку, дезинфекцию и закрытие каналов. В запущенной стадии необходимо хирургическое вмешательство.
Вам также будет интересно:
Формы недуга в зависимости от патогенеза и этиологии
Патогенез и клиническая картина периодонтита во многом определяются его этиологией, т. е. причинами возникновения воспалительной реакции. По данному признаку проводится следующая классификация форм периодонтита.
Инфекционный
Это наиболее распространённая разновидность недуга, вызываемая проникновением патогенных микроорганизмов в периодонт. Процесс провоцируется токсинами, вырабатываемыми ими.
Источником поражения при данном виде периодонтита могут стать: продолжительный пульпит, гайморит, кариес и другие очаги инфекции, расположенные в ротовой полости.
Травматический
Механические воздействия, способные повредить ткани периодонта, могут стать причиной возникновения воспалительного процесса. Такой механизм характерен для ударов и ушибов при драках, падениях, ДТП. В группу повышенного риска попадают чрезмерно активные дети и спортсмены. Травмы могут наноситься и сопряжёнными зубами при неправильном протезировании или пломбировании.
Медикаментозный
Данный вид периодонтита развивается в результате химического воздействия некоторых медикаментозных средств и врачебных ошибок. Наиболее опасно влияние мышьяка, используемого при лечении зубов. Чрезмерная продолжительность или передозировка пасты могут привести к химическому поражению ткани периодонта.
- Похожее воздействие способны оказывать некоторые сильные антибиотики при их длительном приёме.
- Плохая очистка каналов при проведении лечения порой формирует очаги нагноения, которые провоцируют воспалительную реакцию.
- Этиология периодонтита может основываться и на аллергии к некоторым ингредиентам лекарственных препаратов.
Иногда причины возникновения заболевания не удаётся выявить, и тогда речь идёт о ятрогенной разновидности.
Следует также отметить, что вероятность развития любой из перечисленных форм болезни увеличивается у курящих людей.
При активном курении на зубной эмали образуется плёнка, содержащая патогенные составляющие, например, Staphylococcus aureus и Pseudomonas aeruginosa.
Классификация хронической формы болезни по МГМСУ
В РФ наиболее часто используется классификация по Лукомскому, предусматривающая разделение острой и хронической форм недуга на несколько разновидностей. Каждая из них имеет специфические признаки. Хроническая патология подразделяется на следующие подвиды:
- Фиброзный — данная форма периодонтита развивается без выраженных проявлений симптомов. Патология обусловлена расширением периодонта, как правило, в верхней зоне, что и выявляется при рентгенографии. Болевой синдром отсутствует, что осложняет диагностирование. Болезнь можно выявить по изменению цвета зуба и появления неприятного запаха изо рта.
- Гранулирующий — характеризуется определённой активностью процесса, что ведёт к разрушению костной ткани с формированием рыхлой грануляции. Появляется болевой синдром небольшой интенсивности с периодическим усилением при надкусывании. В тканях периодонта формируется свищ, что вызывает ощущение распирания. Прилегающий участок десны отекает и краснеет. Свищи имеют тенденцию исчезать, но затем появляться снова.
- Гранулёматозный — данный вид периодонтита выявляется по характерной, округлой полости в периодонте с грануляциями, имеющими чёткие границы. Размер её не превышает 5 мм. При больших размерах речь может идти о кисте, но, в отличие от неё, гранулёма не вызывает болевого синдрома, что затрудняет диагностирование.
Фото 1. Так выглядит гранулематозная стадия периодонтита: на десне верхней челюсти заметна небольшая гранулема.
Патология выявляется при проведении рентгенографии. Среди симптомов можно выделить изменение цвета зуба и небольшое болевое ощущение при постукивании по нему или резком надкусывании.
Важно! Из всех разновидностей хронического периодонтита самым активным признаётся гранулирующий тип, который способен вызывать заметный болевой синдром.
В целом хроническая форма опасна своими обострениями. Они характерны для гранулирующего и гранулёматозного течения, и крайне редко обнаруживаются при фиброзном типе заболевания.
Стадии острого периодонтита
В соответствии с классификацией Лукомского выделяются такие варианты течения острой формы недуга.
Серозный
Представляет собой начальную стадию воспалительной реакции. Симптоматическое проявление усиливается достаточно стремительно. Характерно нарастание болевых ощущений.
Периодические боли при надкусывании переходят в непрерывный болевой синдром ноющего характера. При надавливании он становится нестерпимым.
Постепенно разрушаются связки, фиксирующие зуб в альвеоле, что приводит к его расшатыванию. Начинают разрушаться и деградировать окружающие костные ткани.
Гнойный
При отсутствии лечения серозная стадия трансформируется в гнойную фазу. На этом этапе в периодонте начинает накапливаться гнойный экссудат, причём гной не находит путей для оттока. В результате такая масса попадает в кровяное русло и вызывает интоксикацию всего организма.
Ухудшается общее самочувствие: недомогание, головная боль, повышение температуры тела, озноб. Зуб становится крайне болезненным, а боли приобретают пульсирующий характер.
Появляется ощущение, будто он вылез наружу и уже не вписывается в зубной ряд. Усиливается подвижность зуба и отёчность мягких тканей.
Обнаруживается увеличение ближайших лимфатических узлов, что свидетельствует о попадании гноя в лимфу.
Через несколько дней проявление острой формы стихает, но это не означает, что болезнь прошла сама. Самый вероятный итог — переход острого периодонтита в хроническое течение.
Степени тяжести
Заболевание разных типов может протекать с различной стадией тяжести:
- Лёгкая — симптомы практически не ощущаются. Нет болевого синдрома, даже при надавливании. Можно обнаружить небольшие зубодесневые карманы и изменение цвета зуба. Возможна слабая, периодическая кровоточивость дёсен.
-
Средняя — возникают болезненные ощущения, усиливающиеся при надкусывании, надавливании и температурном воздействии.
Зубодесневой карман увеличивается до глубины 5—6 мм. Дёсны часто кровоточат, а сам зуб становится подвижным.
- Тяжёлая или запущенная — болевой синдром становится постоянным, возникает отёк мягких тканей. Зубы сильно шатаются и могут выйти из общего ряда. Глубина зубодесневого кармана превышает 7 мм. При надавливании может появляться гнойный экссудат.
Схема лечения существенно зависит от степени тяжести течения болезни. Если на первых двух стадиях обеспечивается терапевтическое лечение, то запущенная форма требует чаще всего хирургического вмешательства.
Чем чревата запущенная стадия
Отсутствие лечения, особенно при тяжёлой степени поражения, чревато серьёзными последствиями. Можно отметить такие опасные осложнения периодонтита: абсцессы, шейная флегмона, остеомиелит, гайморит, кистозные образования, сепсис.
Ознакомьтесь с видео, в котором рассказывается, как лечение периодонтита зависит от его стадии.
Общепринятые методики классификации периодонтита разрабатываются не ради статистики, а для практического использования. Они позволяют более полно понять происходящий процесс, его природу и возможные осложнения. Точная диагностика типа патологии с детализацией этиологии и клинической картины даёт возможность применить оптимальную схему лечения.
Источник: https://32zuba.guru/periodontit/klassifikatsiya/
Классификация периодонтитов
Последнее обновление: 14.10.2019
Разработка единой типологии воспалительных заболеваний периодонта на сегодняшний день остается одним из важных вопросов стоматологии. Врачи-клиницисты не перестают говорить о необходимости универсальной классификации периодонтита.
Тем не менее, до сих пор такая классификация не была выработана. Это связано, в том числе, с пробелами в используемых методах диагностики периодонтита. Применяемые сегодня методики не всегда позволяют выявлять клинические корреляции при обнаружении симптомов заболевания и прояснять природу морфологических изменений.
Мировые классификации периодонтитов
Сейчас в медицине применяется целый ряд различных типологий. Одной из наиболее распространенных является классификация периодонтита по МКБ-10, предложенная ВОЗ и обладающая рядом серьезных достоинств. Также в разных странах используются и другие системы, основанные на характерных признаках и разработанных методиках. Каждая из таких типологий имеет как свои преимущества, так и недостатки и противоречия с другими типологиями.
Например, российские стоматологи для диагностики и лечения применяют методику, согласно которой периодонтит классифицируется по характеру проявлений: острый, хронический или обострение хронического, а также по степени тяжести: серозный или гнойный. Также учитывается форма течения заболевания в случае его обострения, и такие разновидности патологии, как фиброзный, гранулирующий и гранулематозный периодонтит.
Данная классификация, именуемая классификацией по Лукомскому, является наиболее широко применяемой на территории России и СНГ, наряду с классификацией по МКБ-10. Еще одна распространенная типология — определение типа заболевания на основе его происхождения или этиологии. Для лучшего понимания используемых систем классификации следует познакомиться с каждой из них подробнее.
По происхождению (этиологии)
Периодонтит — это заболевание, проявляющееся в воспалении тканей, окружающих корень зуба, и разрушении околозубной костной ткани.
Источник: https://www.youtube.com/watch?v=-rh-u1xAdys
Существует три основных причины, вызывающее данную патологию:
- инфекция;
- травма;
- медикаментозное воздействие.
Инфекционный периодонтит развивается вследствие проникновения бактерий в костные ткани. Вредоносные микроорганизмы вырабатывают токсины, что приводит к развитию воспалительных процессов.
Чаще всего патологическая микрофлора проникает в периодонт через верхушечное отверстие корневого канала. При наличии глубоких зубодесневых карманов инфицирование происходит через краевой или маргинальный периодонт, а также причиной воспаления может стать периодонт соседнего зуба.
Причиной травматического периодонтита, как видно из названия, является травматическое воздействие на околозубную ткань. Патология может развиться вследствие сильной разовой травмы, например, удара или ушиба.
Но микротравмы с невысокой интенсивностью воздействия могут быть не менее опасными, если наносятся регулярно на протяжении длительного времени.
Источниками таких травм обычно становятся следующие факторы:
- выступающие пломбы;
- перегрузка зубного ряда;
- «прямой прикус»;
- вредные привычки, к которым относятся, например, привычка грызть карандаш или откусывать зубами нитки.
Еще одна возможная причина развития периодонтита — медикаментозная.
Этот тип заболевания связан с воздействием на периодонт сильных химических веществ, например, мышьяковистой пасты, применяемой стоматологами для девитализации пульпы.
Чаще всего медикаментозный периодонтит развивается вследствие применения препаратов, не предназначенных для использования в полости рта, либо применяемых с нарушением концентрации или установленной технологии.
Классификация периодонтита по Лукомскому
Эта типология получила широкое применение в практической стоматологии и является наиболее распространенной на постсоветском пространстве. Ее неоспоримым преимуществом является то, что, будучи достаточно лаконичной, классификация Лукомского содержит все клинически значимые формы периодонтитов, между которыми могут быть коренные различия при диагностике и лечении.
В рамках данной типологии периодонтит делится на две основных разновидности: острый и хронический. Острая форма в свою очередь может быть:
Хронический периодонтит подразделяется на:
- фиброзный;
- гранулирующий;
- гранулематозный.
Острый периодонтит
Источник: https://www.youtube.com/watch?v=ppWQTRJxnGI
Основной симптом острого периодонтита — непрекращающаяся резкая боль в зоне воспаления, повышенная чувствительность при соприкосновении больного зуба со здоровыми. Продолжительность этой стадии заболевания составляет до двух недель
Первая фаза периодонтита — серозная, она представляет собой начальный этап в развитии заболевания. Обычно в этот период патология выражается в появлении сильных болевых ощущений в зубе и воспалении слизистой оболочки вокруг него. В некоторых случаях возникает ощущение распирания, общая реакция организма отсутствует.
При серозном периодонтите не наблюдается иррадиации — распространения болезненности за пределы участка, пораженного заболеванием. Если боль иррадиирует, приобретает характер рвущей и пульсирующей, это говорит о переходе воспаления в гнойную стадию.
На этом этапе заболевания дискомфорт усиливается, начинает выделяться гнойный экссудат. Болезненные ощущения вызывает даже слабое прикосновение к пораженному зубу. Кроме того, воспаление периодонта приводит к ослаблению фиксации зуба, он начинает шататься. Рентгеновское обследование не выявляет изменений.
При гнойном периодонтите нередко наблюдается общее расстройство организма, характеризующееся следующими проявлениями:
- увеличение и болезненность лимфатических узлов;
- головные боли;
- повышение температуры до 39 градусов;
- общее ощущение слабости, озноб.
Если больной откладывает посещение врача, то через полторы-две недели после начала заболевания острая стадия переходит в хроническую.
Хронический периодонтит
Как уже было сказано выше, основная причина развития хронического периодонтита — пренебрежение лечением заболевания в острой стадии.
Тем не менее, в некоторых случаях данная патология может изначально развиваться как хроническая. Классификация этой формы заболевания выполняется в зависимости от характера и глубины повреждений костной ткани и периодонта.
При такой патологии нередко наблюдается сильное разрушение зуба и значительное изменение его цвета.
Первый тип заболевания — фиброзный периодонтит. Пациенты, страдающие этой патологией, как правило, не испытывают болевых ощущений. Это, а также тот факт, что фиброзная форма часто имеет те же клинические проявления, что и гангренозный пульпит, значительно затрудняет ее диагностику.
Основные отличительные особенности фиброзного периодонтита:
- изменение цвета зубов;
- наличие сильных кариозных полостей;
- обследование посредством зондирования, перкуссии, с применением температурных раздражителей не вызывает болезненности;
- часто наблюдается омертвение пульпы;
- на рентгеновских снимках отчетливо заметно расширение периодонтальной щели на верхней части корня либо на всем его протяжении, костная стенка зубной лунки не разрушена.
Часто фиброзный периодонтит возникает при перегрузке или вследствие утраты пациентом значительной части зубов. Также он может развиваться после эндодонтического лечения, но если пациент не испытывает дискомфорта и состояние пломбы не вызывает вопросов, лечение не требуется.
Гранулирующий периодонтит может выражаться в слабой болезненности, в том числе при соприкосновении больных и здоровых зубов. Часто это сопровождается образованием абсцессов и грануляционной ткани, которые со временем проходят.
Развитие данной формы заболевания может также вызывать гиперемию десны вокруг пораженного зуба, которая наблюдается при воздействии на десну концом инструмента.
Присутствует чувствительность и болезненная реакция при перкуссии зуба, увеличиваются регионарные лимфоузлы.
Рентгеновское обследование, как правило, показывает неравномерное разрежение костной ткани в зоне верхушечного отверстия. Расширение может составлять от одного-двух до пяти-восьми миллиметров, контур нечеткий.
Третья разновидность периодонтита — гранулематозный. Обычно он также протекает без выраженных симптомов. Часто в анамнезе пациентов с гранулематозным периодонтитом присутствуют перенесенные патологии периодонта и боли, связанные с развитием пульпита. Также данная форма периодонтита может иметь следующие признаки:
- отсутствие кариозной полости в пораженном зубе;
- изменение цвета зубной коронки;
- наличие кариозной полости и каналов с распавшейся пульпой;
- некачественно вставленная пломба.
На рентгене гранулематозный периодонтит проявляется в виде разрежений костной ткани округлой формы с четко очерченным контуром. Может быть виден как в зоне верхушки зуба, так и в зоне корня, часто сопровождается гиперцементозом боковых отделов. При надлежащем лечении возможен переход в фиброзную форму, в противном случае патология приводит к образованию корневой кисты.
И, наконец, существует еще одна, особая форма периодонтита — когда хроническое заболевание переходит в стадию обострения. От острой формы она отличается наличием признаков деструктивных изменений на рентгеновском снимке.
Классификация периодонтита по МКБ-10
Еще одна распространенная типология была предложена Всемирной организацией здравоохранения и сегодня признана стоматологами всего мира. Она учитывает форму протекания болезни и наиболее частые осложнения. Данная классификация включает следующие разновидности:
- острый верхушечный;
- хронический верхушечный;
- периапикальный абсцесс с образованием свища;
- периапикальный абсцесс без образования свища;
- радикулярная (прикорневая) киста;
- неуточненные заболевания пульпы зуба.
Лечение и профилактика периодонтита
Источник: https://www.youtube.com/watch?v=yNywXNvHnYs
Воспаление периодонта является источником активной микрофлоры, способной вызвать тяжелые осложнения как местного, так и общего характера. Наибольшую опасность очаги периодонтита представляют при беременности. Поэтому при появлении малейших симптомов, указывающих на наличие этого заболевания, необходимо обратиться к врачу.
Как известно, самый надежный и требующий наименьших затрат способ предотвращения заболевания — это его профилактика. Намного проще соблюдать несложные правила ухода за зубами и полостью рта, чем тратить время и деньги на дорогостоящее лечение запущенной патологии. Чтобы предотвратить образование периодонтита, необходимо следовать всего нескольким рекомендациям:
- не забывайте чистить зубы два раза в день. Для лучшей эффективности можно пользоваться электрической зубной щеткой. Также мы рекомендуем использовать лечебно-профилактические пасты «АСЕПТА», которые предохраняют зубы от кариеса, укрепляют эмаль, успокаивают и защищают десны;
- ешьте меньше сладкого. Чрезмерное употребление простых углеводов способствует не только набору веса, но и усиленному образованию зубного камня. Достаточное количество в рационе овощей, фруктов и белковых продуктов необходимо для поддержания зубов в хорошем состоянии;
- регулярно посещайте стоматолога, а именно – не реже двух раз в год. Даже если вам кажется, что поводов для беспокойства нет, необходимо, чтобы в этом убедился специалист. Кроме того, для качественной профилактики периодонтита необходимо регулярно удалять зубные отложения.
Если же у вас все-таки развилось воспаление околозубных тканей, воспользуйтесь бальзамом для десен и гелем для десен с прополисом «АСЕПТА». Данные средства не являются полноценной заменой лечения, назначенного стоматологом, но будут хорошей помощью в исцелении от заболевания.
Бальзам способствует устранению болезнетворных бактерий и запаха изо рта, а также снимает воспаление и кровоточивость. Гель оказывает выраженное противовоспалительное воздействие, успокаивает десны и снимает чувствительность. «АСЕПТА» — залог здоровых зубов и полноценной жизни без боли и дискомфорта!
Клинические исследования
Многократно проведенные клинические исследования доказали, что применение геля для дёсен с прополисом АСЕПТА в течение недели позволяет снизить воспаление дёсен на 31%.
Отзывы потребителей
lapkaa (otzovik.com)
«Пару дней назад почувствовала некоторой дискомфорт во рту. Десны ныли постоянно, немного жгло и пощиповало, усилилась чувствительность, сразу понятно что во рту что-то не то…
У меня раньше уже было такое то десна опушали то кровоточили, так что мучаюсь я так давно. Не так давно мне стаматолог посоветовала гель для десен с прополисом «Асепта».
Гель бело-желтоватого цвета, достаточно густой-вязкой консистенции. Вкус довольно приятный, чуть-чуть сладковатый. Рекомендуется наносить на дёсны 2—3 раза в день, в течение 7—14 дней. После применения геля стараюсь ничего не есть, примерно пол часа.
Гель для дёсен с прополисом «Асепта» —Это противовоспалительное, противомикробное на основе прополиса, применяется при инфекционно-воспалительных заболеваниях полости рта. Прополис же обладает противовоспалительным, противомикробным действием, а также противозудным и анальгезирующим эффектом, ускоряет процесс регенерации и заживления раневых поверхностей.
Результат не заставит себя ждать ! Рекомендую!»
- buba1 (otzovik.com)
- «Стоматолог в очередной раз назначил лечение десен препаратом «Асепта» в виде геля.
- Основной активный компонент геля — экстракт прополиса 10%, оказывающий быстрое противовоспалительное действие, а также благотворно влияющий на восстановление тканей и способствующий быстрому заживлению ран.
2-3 раза в день гель наносят тонким слоем на десну, можно сделать и небольшой массаж. Понятно, что процедура проводится после приема пищи и чистки зубов… .
…Подытожив, хочу заметить, если не назначено лечение именно гелем, то вполне можно купить в аптеке настойку прополиса, которая заметно дешевле, и делать полоскания».
Для точной диагностики обращайтесь к специалисту.
Источник: https://asepta.ru/spravochnik/desni/klassifikatsiya-periodontitov/
Этиология и патогенез периодонтитов. Пути проникновения инфекции в периодонт. Классификация периодонтитов (клиническая и МКБ -10)
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Воспалительный процесс в периодонте зуба является результатом его реакции на различные раздражители.
Наиболее часто причиной воспаления в перидонте являются микроорганизмы и их токсины, попадающие в периодонт вследствие гибели пульпы из кариозной полости через канал зуба и дентинные трубочки, из инфицированных пародонтальных карманов, или с крово- и лимфотоком при острых и хронических воспалительных заболеваниях, химические вещества (ингредиенты пломбировочных материалов, мышьяковистая паста), механические воздействия (острая или хроническая травма зуба, перемещение зубов при ортодонтическом лечении).
Основными возбудителями периодонтита являются стрептококки: гемолитические – 12% и негемолитические – 62% стрептококки. Обнаруживаются так же грамположительные палочки, фузоспирохеты и грибы.
Инфекционный периодонтит возникает при проникновении микроорганизмов (негемолитического, зеленящего и гемолитического стрептококков, золотистого и белого стафилококков, фузобактерий, спирохет, вейлонелл, лактобактерий, дрожжеподобных грибов), их токсинов и продуктов распада пульпы в периодонт из корневого канала или десневого кармана.
Травматический периодонтит может развиться в результате как острой травмы (ушиба зуба, накусывания твердого предмета), так и хронической травмы (завышения пломбы, регулярного воздействия мундштука курительной трубки или музыкального инструмента, вредных привычек). Кроме того, нередко наблюдается травма периодонта эндодонтическими инструментами в процессе обработки корневых каналов, а также вследствие выведения за верхушку корня зуба пломбировочного материала или внутриканального штифта.
Раздражение периодонта при острой травме в большинстве случаев быстро проходит самостоятельно, однако иногда повреждение сопровождается кровоизлиянием, нарушением кровообращения в пульпе и ее последующим некрозом. При хронической травме периодонт пытается приспособиться к возрастающей нагрузке. Если нарушены адаптационные механизмы, развивается хронический воспалительный процесс в периодонте.
Медикаментозный периодонтит возникает вследствие попадания в периодонт сильнодействующих химических веществ и лекарственных средств: мышьяковистой пасты, фенола, формалина и т.д.
К медикаментозному периодонтиту относят также воспаление периодонта, развившееся в результате аллергических реакций на различные препараты, использованные при эндодонтическом лечении (эвгенол, антибиотики, противовоспалительные средства и т.д.).
- КЛАССИФИКАЦИЯ ПЕРИОДОНТИТА(МКБ-10).
- К 04.4 — острый апикальный периодонтит
- К 04.5 — хронический апикальный периодонтит
- К 04.6 — периапикальный абсцесс со свищем
- К 04.7 — периапикальный абсцесс без свища
- К 04.8 — корневая киста апикальная и боковая
- К 04.8 — корневая киста периапикальная
- Острый апикальный периодонтит:
- — фаза интоксикации
- — фаза экссудации
- Хронический периодонтит
- — хронический фиброзный
- — хронический гранулирующий
— хронический гранулематозный, или гранулема
— хронический периодонтит в стадии обострения
Клиническая картина острого периодонтита. Диагностика, диф диагностика, лечение, осложнения и меры их профилактики.
Острый периодонтит — это острое воспаление периодонта. Этиология. Острые гнойные периодонтиты развиваются под действием смешанной флоры, где преобладают стрептококки, иногда стафилококки и пневмококки. Могут обнаруживаться палочковидные формы (грамположительные и грамотрицательные), анаэробная инфекция.
Клиническая картина.
При остром периодонтите больной отмечает боль в причинном зубе, усиливающуюся при надавливании на него, жевании, а также при постукивании (перкуссии) по жевательной или режущей его поверхности. Характерно ощущение как бы вырастания, удлинения зуба. При более длительном давлении на зуб боли несколько стихают.
В дальнейшем болевые ощущения усиливаются, становятся непрерывными или с короткими светлыми промежутками. Нередко они принимают пульсирующий характер. Тепловое воздействие, принятие горизонтального положения, прикосновение к зубу вызывают еще большие болевые ощущения. Наблюдается распространение болей (иррадиация) по ходу ветвей тройничного нерва.
Усиление болей при накусывании, прикосновении к зубу заставляет больных держать рот полуоткрытым.
При внешнем осмотре изменений, как правило, нет, наблюдаются увеличение и болезненность связанных с пораженным зубом лимфатического узла или узлов. У отдельных больных может быть нерезко выраженный коллатеральный отек соседних с этим зубом околочелюстных мягких тканей. Перкуссия его болезненна и в вертикальном, и горизонтальном направлении.
Слизистая оболочка десны, альвеолярного отростка, а иногда и переходной складки в проекции корня зуба гиперемирована и отечна. Пальпация альвеолярного отростка по ходу корня и особенно соответственно отверстию верхушки зуба болезненна.
Иногда при давлении инструментом на мягкие ткани преддверия рта по ходу корня и по переходной складке остается вдавление, свидетельствующее об их отеке.
Температурные раздражители, данные электроодонтометрии указывают на отсутствие реакции пульпы вследствие ее некроза. На рентгенограмме при остром процессе патологических изменений в периодонте может не выявляться или обнаруживается расширение периодонтальной щели.
При обострении хронического процесса возникают изменения, характерные для гранулирующего, гранулематозного, редко фиброзного периодонтитов.
В крови, как правило, изменений нет, но у некоторых больных наблюдается лейкоцитоз, умеренный нейтрофилез за счет палочкоядерных и сегментоядерных лейкоцитов, СОЭ чаще в пределах нормы.
Дифференциальный диагноз.
Острый периодонтит отличают от острого пульпита, периостита, остеомиелита челюсти, нагноения корневой кисты, острого одонтогенного гайморита. В отличие от пульпита при остром периодонтите боли бывают постоянными, при диффузном воспалении пульпы — приступообразными.
При остром периодонтите в отличие от острого пульпита наблюдаются воспалительные изменения в прилежащей к зубу десне, перкуссия более болезненна. Кроме того, помогают диагностике данные электроодонтометрии.
Дифференциальная диагностика острого периодонтита и острого гнойного периостита челюсти основывается на более выраженных жалобах, лихорадочной реакции, наличии коллатерального воспалительного отека околочелюстных мягких тканей и разлитой инфильтрации по переходной складке челюсти с образованием поднадкостничного гнойника. Перкуссия зуба при периостите челюсти малоболезненна или безболезненна в отличие от острого периодонтита.
По таким же, более выраженным общим и местным симптомам проводят дифференциальную диагностику острого периодонтита и острого остеомиелита челюсти. Для острого остеомиелита челюсти характерны воспалительные изменения прилежащих мягких тканей по обе стороны альвеолярного отростка и тела челюсти.
При остром периостите перкуссия резко болезненна в области одного зуба, при остеомиелите — несколько зубов, причем зуб, явившийся источником заболевания, реагирует на перкуссию меньше, чем соседние интактные зубы. Лабораторные данные — лейкоцитоз, СОЭ и др. — позволяют отличать эти заболевания.
Гнойный периодонтит следует дифференцировать от нагноения околокорневой кисты. Наличие ограниченного выбухания альвеолярного отростка, иногда отсутствие в центре костной ткани, смещение зубов в отличие от острого периодонтита характеризуют нагноившуюся околокорневую кисту. На рентгенограмме при кисте обнаруживается участок резорбции кости округлой или овальной формы.
Острый гнойный периодонтит следует дифференцировать от острого одонтогенного воспаления верхнечелюстной пазухи, при котором может развиваться боль в одном или нескольких прилежащих к ней зубах.
Однако заложенность соответствующей половины носа, гнойные выделения из носового хода, головные боли, общее недомогание характерны для острого воспаления верхнечелюстной пазухи.
Нарушение прозрачности верхнечелюстной пазухи, выявляемое на рентгенограмме, позволяет уточнить диагноз.
Лечение.
Терапия острого верхушечного периодонтита или обострения хронического периодонтита направлены на прекращение воспалительного процесса в периодонте и предотвращение распространения гнойного экссудата в окружающие ткани — надкостницу, околочелюстные мягкие ткани, кость. Лечение преимущественно консервативное и проводится по правилам, изложенным в соответствующем разделе учебника «Терапевтическая стоматология».
Более быстрому стиханию воспалительных явлений способствует блокада — введение по типу инфильтрационной анестезии 1,7 мл раствора ультрокаина или убистезина в область преддверия рта по ходу альвеолярного отростка соответственно пораженному и 2-3 соседним зубам. Это позволяет успешно провести консервативное лечение острого периодонтита.
Необходимо все же иметь в виду, что без оттока экссудата из периодонта (через канал зуба) блокады малоэффективны, часто безрезультатны. Можно сочетать блокаду с разрезом по переходной складке до кости. Это особенно показано при безуспешной консервативной терапии и нарастании воспалительных явлений, когда не представляется возможным удалить зуб в силу каких-то обстоятельств.
Консервативное лечение обеспечивает успех не во всех случаях острого и обострившегося хронического периодонтитов. При неэффективности лечебных мероприятий и нарастании воспалительных явлений зуб следует удалить.
Это можно сочетать с разрезом по переходной складке до кости в области корня зуба, пораженного острым периодонтитом. Кроме того, удаление зуба показано при значительном его разрушении, непроходимости канала или каналов, наличии инородных тел в канале.
Как правило, удаление зуба приводит к быстрому стиханию и последующему исчезновению воспалительных явлений.
После удаления зуба может наблюдаться усиление болей, повышение температуры тела, что часто обусловлено травматичностью вмешательства. Однако через 1-2 дня эти явления, особенно при проведении соответствующей противовоспалительной лекарственной терапии, ликвидируются.
Для профилактики осложнений после удаления в зубную альвеолу можно вводить антистафилококковую плазму, промывать ее стрептококковым или стафилококковым бактериофагом, ферментами.
Общее лечение острого или обострения хронического периодонтита заключается в назначении внутрь анальгина, амидопирина (по 0,25-0,5 г), фенацетина (по 0,25-0,5 г), ацетилсалициловой кислоты (по 0,25-0,5 г) 3-4 раза в сутки. Эти препараты обладают обезболивающим, противовоспалительным и десенсибилизирующим действием.
Чтобы приостановить развитие воспалительных явлений, целесообразно применять холод (пузырь со льдом на область мягких тканей соответственно зубу) в течение 1-2-3 ч после удаления зуба.
При стихании воспалительных явлений возможны назначения соллюкса (по 15 мин каждые 2-3 ч), других физических методов лечения: УВЧ, флюктуоризации, лекарственного электрофореза с димедролом, хлоридом кальция, протеолитическими ферментами.
Исход.
При правильном и своевременном консервативном лечении в большинстве случаев острого и обострения хронического периодонтитов наступает выздоровление. Возможно распространение воспалительного процесса на надкостницу, костную ткань, околочелюстные мягкие ткани, т. е. могут развиться острый периостит, остеомиелит челюсти, абсцесс, флегмона, лимфаденит, воспаление верхнечелюстной пазухи.
Профилактика основывается на санации полости рта, своевременном и правильном лечении
патологических одонтогенных очагов, функциональной разгрузке зубов при помощи ортопедических методов лечения, а также на проведении гигиенических и оздоровительных мероприятий.
Источник: https://studopedia.net/14_60369_etiologiya-i-patogenez-periodontitov-puti-proniknoveniya-infektsii-v-periodont-klassifikatsiya-periodontitov-klinicheskaya-i-mkb—.html
Клинический случай перелечивания зубов 1.1 и 2.1
Библиографическое описание:Беляева, Н. А. Клинический случай перелечивания зубов 1.1 и 2.1 / Н. А. Беляева, Е. Л. Лужкова. — Текст : непосредственный // Молодой ученый. — 2020. — № 48 (338). — С. 82-85. — URL: https://moluch.ru/archive/338/75679/ (дата обращения: 28.04.2021).
Хронический апикальный периодонтит занимает третье место по обращаемости к врачу-стоматологу. Главную роль в развитии данного заболевания отводят микробному фактору. Следовательно, при лечении апикального периодонтита главной задачей является удаление микробной микрофлоры с помощью механического и медикаментозного воздействия. Одним из методов более качественной обработки корневых каналов является применение системы САФ.
Ключевые слова: САФ, хронический апикальный периодонтит.
Пациент Б. 1953 года рождения обратился в клинику с целью эстетического протезирования центральных зубов. При проведении КЛКТ в области верхушек зубов 1.1, 2.1 обнаружен очаг разрежения ткани с четкими контурами. (рис. 1)
Анамнез: 1.1 и 2.1 ранее лечены эндодонтически, изменены в цвете, края пломб негерметичны, перкуссия безболезненная.
Объективно: Лицо симметрично. Кожные покровы бледно-розового цвета, умеренно влажные, слизистая оболочка полости рта бледно-розового цвета без патологических изменений. Свищей, отеков нет. Пальпация по переходной складке безболезненная. Состояние гигиены полости рта удовлетворительное. Вертикальная и горизонтальная перкуссия безболезненная.
Рентгенологическое обследование: На прицельном дентальном радиовизиографическом снимке зубов 1.1, 2.1 в областях верхушек корней определяется очаг деструкции костной ткани. Корневые каналы запломбированы по всем третям корня. (рис. 2)
Диагноз: Хронический апикальный периодонтит по МКБ-10 — К04.51
Лечение: С применением дентального микроскопа.
Под инфильтрационной анестезией (Sol. Ultracaini DS: 0,5 ml) после обработки зуба щеткой и пастой, наложения раббердама, удалены старые пломбы в 1.1 и 2.1 зубах. Создан доступ к корневым каналам. Устья обработали «Gates» № 2. Произвели распломбировку корневых каналов машинными роторными инструментами ProFiles 25/06, 20/06, 15/06 методом Crow Down, обработали САФ под обильным орошением 3 % NaCl. Рабочая длина корневых каналов определена с помощью апекслокатора и подтверждена рентгеновским снимком.
Далее каналы были расширены ручными инструментами K-Files (Mani) до 70 размера по iso.
После инструментальной обработки и тщательной ирригации корневых каналов они были заполнены «Calasept» и установлены временные пломбы из стеклоиномерного цемента «Fuji» (GC). (рис. 3)
Второй визит был назначен через три недели.
Объективно: Временная пломба сохранена.
Под инфильтрационной анестезией (Sol. Ultracaini DS: 0,5 ml) после наложения раббердама удалены временные пломбы, проведена обработка корневых каналов САФ и ирригация дистиллированной водой, MDCleanser и 2 % раствором хлоргексидина, обтурированы гуттаперчей с использованием силера «Adseal» комбинированным методом. (рис. 4) Установлена временная пломба из стеклоиномерного цемента «Fiji» (GC).
Пациенту рекомендовано установить стекловолоконный штифт и восстановить коронковую часть зуба с дальнейшей установкой цельнокерамических коронок.
Контрольная рентгенограмма: На прицельном дентальном снимке зубов 1.1, 2.1 в орторадиальной проекции отличается гомогенное заполнение корневых каналов на всем их протяжении. (рис. 5)
Рекомендован контрольный снимок через 6 месяцев.
На контрольной КЛКТ (через 6 месяцев) отмечается положительная динамика с уменьшением размера воспалительного очага. (рис. 6)
Рис. 1. КЛКТ до перелечивания
Рис. 2. Ортомантомограмма. Исходная ситуация до начала лечения
Рис. 3. После распломбировки каналов. Оставлен «Calasept»
Рис. 4. Каналы после пломбирования «Adseal» и гуттаперчей
Рис. 5. Восстановлены СВШ на u200 (3M) и пломбой для дальнейшего протезирования
Рис. 6. КЛКТ через 6 месяцев после перелечивания. Боковая проекция
Основные термины (генерируются автоматически): Хронический апикальный периодонтит, бледно-розовый цвет, временная пломба, инфильтрационная анестезия, канал.
Комплексное лечение хронического периодонтита с использованием самоадаптирующегося файла (SAF)
Актуальность. Успех лечения периодонтита во многом зависит от эффективности воздействия на микробный фактор. Основным критерием успешного лечения является тщательная механическая и медикаментозная обработка кариозной полости и корневого канала, предусматривающая максимально полное устранение бактерий и их токсинов. Используемые инструменты для механической обработки должны максимально бережно и эффективно очищать стенки корневого канала, а используемые для антисептической обработки растворы — обладать бактерицидными, противовоспалительными и противогипоксическими свойствами, не должны вызывать аллергические реакции и обладать раздражающим воздействием на ткани пародонта.
Цель исследования — повышение качества эндодонтического лечения пациентов с хроническим периодонтитом за счет применения самоадаптирующегося файла (SAF) и комплексной медикаментозной обработки корневых каналов.
Материал и методы. Под клиническим наблюдением находились 30 пациентов в возрасте от 20 до 45 лет с диагнозом «хронический периодонтит» (по международной классификации МКБ-10 К04.5). Все пациенты были разделены на три группы по 10 человек в каждой. Группы формировались исходя из применяемых технологий эндодонтического лечения. В 1-й группе обработку корневых каналов проводили по стандартной методике с применением NiTi-инструментов и 2 растворов — Parcan 3% и 17% ЭДТА. Растворы активировали с помощью ультразвука с частотой 20—40 кГц. Пломбирование каналов производили методом латеральной компакции. Во 2-й группе механическую обработку и формирование корневых каналов проводили с помощью SAF, затем медикаментозно обрабатывали раствором Parcan 3%, который активировали с помощью ультразвука с частотой 20—40 кГц. Корневые каналы пломбировали методом латеральной компакции. В 3-й группе применяли SAF и комплексную медикаментозную обработку корневых каналов, включающую последовательное применение антисептических растворов. Обработку корневого канала начинали раствором гипохлорита натрия (Parcan) в концентрации 3% 1—20 мл на один корневой канал при активации ультразвуком с частотой 20—40 кГц. Применяли как одномоментное активирование раствора ультразвуком в процессе обработки, так и чередование обработки раствором гипохлорида и активации звуком. Далее применяли озонированный физиологический раствор NaCl с концентрацией озона 30 млг/л, 1—20 мл на каждый корневой канал, также с одномоментной активацией ультразвуком и чередованием обработки. На конечном этапе медикаментозной обработки перед пломбированием использовали водный раствор хлоргексидина концентрацией 2% 1—20 мл на каждый корневой канал, при активации ультразвуком с частотой 20—40 кГц. Непосредственно перед пломбированием канала использовали дистиллированную воду в среднем 1—20 мл на каждый корневой канал. Получен Патент на изобретение № 2566066 РФ «Способ комплексной медикаментозной обработки корневого канала зуба» от 16.10.14. SAF представляет собой полый цилиндр из NiTi-сплава, стенки которого выполнены в виде сетки и имеют выраженный рисунок (как сетка рабица). При введении в корневой канал инструмент обладает способностью сжиматься и приспосабливаться к индивидуальной анатомии корневого канала зуба. Обработка проводится за счет обратно-поступательных движений, подаваемых от наконечника с одновременной подачей внутрь антисептического раствора. Наблюдение и контрольная рентгенография проводились через 3, 6 и 12 мес.
Результаты. После проведенного комплексного лечения хронического периодонтита в многокорневых зубах положительный результат получен в 90% случаев в 3-й группе пациентов. Больные отмечали отсутствие жалоб после проведенного эндодонтического лечения (отсутствие самопроизвольных болей и при накусывании на зуб). При анализе клинико-рентгенологических данных в ближайшие и отдаленные сроки наблюдения отмечалось сокращение сроков заживления периапикальных очагов деструкции на 1—1,5 мес (исчезновение расширения периапикальной щели, уменьшение радиолюцентных очагов).
Вывод. При использовании системы SAF и проведении комплексной медикаментозной обработки корневого канала достигаются устойчивые положительные результаты лечения хронического периодонтита.
Посетили семинар «Трехмерная радиодиагностика челюстно-лицевой области» — ЦНС
Семинар проводился 10-11 декабря в г. Тюмень.
Лектор: Рогацкин Дмитрий Васильевич.
Программа 1-го дня семинара:
Отличие секционного изображения зуба от суммационного. Трехмерная радиоанатомия зубов – стандартное строение и крайние варианты нормы. Соответствует ли написанному в учебнике то что, мы видим на трехмерном снимке? Пятикорневые моляры и С-образные премоляры – варианты нормы или уродство? Что представляют собой 15 % первых премоляров нижней челюсти. Какие зубы самые морфологически нестабильные? К каким врачебным ошибкам приводит лечение зубов с нестандартной анатомией? Мониторинг всех возможных вариантов строения зубов по компьютерной томограмме. Трехмерное исследование корневого канала и актуальность классификации Vertucci при оценке строения плоского корня.
Дентинодисплазия и микродонтия, несовершенный дентиногенез и посттравматическая облитерация – радиодиагностические признаки и способы распознавания Мальформации и аномалии строения зубов – статистика и казуистика. Существуют ли двухкорневые резцы? Геминация, фузион, Dens invaginatus, Dentes spinosi, talon cusp, эвагинация, диляцерации, сверхкомплектные корни, тауродонтия, макродонтия, микродонтия и т. д. Сверхкомплектный резец – резец ли это? Сверхкомплектные зубы – бикуспид и парамоляр. Определение и классификация сверхкомплектных зубов, визуализация патологических процессов, связанных с наличием лишних зубов. Олигодонтия и полидонтия. Как выглядят зубы пациентов с эктодермальной дисплазий и клейдо-краниальной дисплазией. Одонтомы – что это такое и как оно выглядит на КТ. Современная классификация одонтом. Dens invaginatus («зуб в зубе») – подробный диагностический отчет об этом состоянии – варианты проявления, диагностика, статистика, классификация. Коронко-корневая борозда, эмалевая прогрессия, энамелома как причины локального пародонтита, варианты развития и диагностика. Гигантоклеточный эпулис и эмалевые капли, связь мальформаций с другими патологиями, дифференциальная диагностика.
Норма на КТ. Крайние варианты нормального строения костной ткани, нераспознаваемые на двухмерных снимках. Состояние костной ткани в норме и при патологии по данным КТ. 3D диагностика осложнений кариеса. Начальные проявления периапикальной патологии, не распознаваемые на обычных снимках. Сравнение степени информативности различных методов лучевого обследования – внутриротовые снимки, панорамные и компьютерная томография при одинаковой патологии. Как выглядит воспалительный процесс на трехмерном снимке? Где кончается периодонтит и начинается внутрикостный абсцесс. Что из МКБ 10 можно увидеть на КТ, как оно выглядит «на вскрытии» и чего нельзя разглядеть на обычном снимке. Пошаговая визуализация – от острого и хронического периодонтита до остеомиелита. Структура костной ткани при различных патологических стояниях. Особенности визуализации отдельных структур и областей при различных патологических процессах. Киста, гранулема или периапикальный абсцесс – радиосемиотика и диагностические критерии для постановки правильного диагноза.
Программа 2-го дня семинара:
Диагностика патологических состояний и особенностей строения придаточных синусов носа на стоматологическом приеме (панорамная зонография синусов, «ортопантомография», внутриротовая рентгенография, рентгенография придаточных синусов носа, компьютерная томография).
Сопоставление рентгенологической картины при рентгенографии гайморовых пазух в носо-подбородочной укладке с панорамной томограммой зубных рядов (ортопантомограммой) и зонограммой параназальных синусов. Компьютерная томография как наиболее адекватный метод исследования придаточных синусов носа.
Что должен видеть стоматолог на снимке придаточных синусов носа. Чья она «пазуха» — стоматологов и ли ЛОРов? Зачем она нужна? Анатомия и физиология придаточных синусов носа. Распространенные заблуждения и мифы о Гайморовой Пазухе.
Варианты строения верхнечелюстных синусов. Гипогенезия синусов, silent sinus sindrom, конха булёза и другие аномалии – их влияние на формирование зубочелюстной системы.
Зависимость положения корней зубов верхней челюсти от строения гайморовых пазух. Как понять по снимку, где находится апекс относительно дна ВЧ синуса. Варианты положения корней моляров в/ч относительно нижней стенки в/ч синуса по данным КТ. Влияния положения корня на распространение периапикального патологического процесса.
Взаимосвязь и влияние стоматологических патологий и лечебных манипуляций в полости рта на состояние ЛОР органов. Характерная радиодиагностическая картина острого, хронического, одонтогенного и риногенного гайморита на панорамной томограмме зубных рядов, сравнение с данными КТ.
Патологические состояния гайморовой пазухи как результат неадекватного эндодонтического лечения. Эндо-антральный синдром – критерии диагностики. Положение инъецированного пломбировочного материала в просвете верхнечелюстного синуса в зависимости от ответной реакции со стороны слизистой. Аспергилиоз синусов или одонтогенный гайморит? Синдром одонтогенной блокады соустья.
Агрессивный пародонтит – случаи развития парадонтогенного гайморита при интактных зубных рядах. Гайморит не одонтогенный, а стоматогенный. Дифференциальная рентгенодиагностика одонтогенных кист субантральной области и риногенных кист верхнечелюстного синуса.
Ретенционные кисты и псевдокисты гайморовых пазух – патологии, актуальные для стоматолога. Своевременная и адекватная диагностика состояния ЛОР органов на стоматологическом приеме, как способ предотвращения осложнений, возникающих после лечения зубов верхней челюсти.
«Мероприятие соответствует требованиям для НЕПРЕРЫВНОГО МЕДИЦИНСКОГО ОБРАЗОВАНИЯ (НМО) и ДОПОЛНИТЕЛЬНОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (ДПО)
Транскриптомика и метиломика при хроническом пародонтите с употреблением табака: пилотное исследование | Клиническая эпигенетика
Отбор пациентов
В исследуемую популяцию вошли 20 практически здоровых пациентов без и с хроническим пародонтитом (таблица 1). В группу курильщиков ( n = 10) вошли люди, курящие не менее 5 лет; лица, которые никогда не курили, были включены в группу некурящих ( n = 10). Статистический анализ проводился с использованием SPSS 12.0 (SPSS Inc., Чикаго, Иллинойс, США). Для анализа возраста пациентов и состояния курения был проведен двусторонний критерий суммы рангов Вилкоксона. Для анализа пола использовался двусторонний точный критерий Фишера. Для диагностики пародонтита использовались визуальные признаки воспаления, зондирование глубины кармана (PPD), кровотечение при зондировании (BOP) и резорбция альвеолярной кости при рентгенографии. Десневая ткань пациентов без каких-либо клинических признаков воспаления, BOP и потери альвеолярной кости и с PPD ≤ 4 мм служила контролем (группа без пародонтита).Хронический пародонтит определяли по наличию хронических воспалительных признаков, PPD ≥ 6 мм, BOP и потери альвеолярной кости (группа хронического пародонтита). Критериями исключения были острый или агрессивный пародонтит, любое тяжелое системное заболевание, которое могло повлиять на состояние пародонта, текущую беременность или период лактации, а также использование системных антибиотиков или противовоспалительных препаратов в течение 6 месяцев до исходного уровня.
Таблица 1 Предыстория исследуемой популяцииСбор образцов тканей десны
Десневые ткани были резецированы из участков моляров верхней или нижней челюсти в процессе удлинения коронки для пациентов без пародонтита или санации открытым лоскутом для пациентов с хроническим периодонтитом.Все участки биопсии были впервые подвергнуты хирургическим вмешательствам, и образцы были получены одним и тем же опытным пародонтологом. После местной анестезии вокруг зубов вдали от свободного края десны делали щечный и небный / язычный зубчатый внутренний разрез. Размер взятого образца десны составлял приблизительно 0,5 × 1,0 см, включая эпителий и соединительную ткань. Ткани немедленно отправляли в лабораторию, где половина каждого образца использовалась для ДНК, а другая половина — для выделения РНК.
Выделение РНК, контроль качества и подготовка образцов для RNA-seq
Общую РНК выделяли из ткани десны с использованием набора RNeasy®-Mini (Qiagen, Валенсия, Калифорния, США). Качество РНК оценивали с помощью набора RNA 6000 NanoLabChip Kit для системы Bioanalyzer (Agilent Technologies, Санта-Клара, Калифорния, США). Все образцы имели значение целостности РНК> 8. Для каждого образца была создана библиотека кДНК, и ее качество оценивалось с помощью системы Bioanalyzer.
Выделение ДНК, контроль качества и подготовка образцов для бисульфитного секвенирования с уменьшенным представлением (RRBS)
Геномная ДНК (гДНК) была выделена из десневой ткани с использованием набора DNeasy® Blood & Tissue Kit (Qiagen), и ее качество оценивалось с помощью Спектрофотометр NanoDrop (NanoDrop Technologies, Уилмингтон, Делавэр, США).Отношение оптической плотности при 260 и 280 нм (OD260 / 280) использовалось в качестве индикатора чистоты образца: ДНК считалась чистой при OD260 / 280 1,8–2,0. Для дополнительной проверки качества был проведен электрофорез в агарозном геле, чтобы исключить такие эффекты, как интерференция РНК и разрыв или повреждение ДНК. Половину каждого образца гДНК подвергали бисульфитной конверсии с использованием набора EpiTect® Bisulfite (Qiagen).
Секвенирование РНК
Всего 10 образцов, не относящихся к периодонтиту, и 10 образцов хронического периодонтита дали достаточное количество РНК (300 нг) для последующего анализа.Библиотеки секвенирования РНК были подготовлены с использованием набора библиотек РНК Illumina TruSeq, а секвенирование парных концов с считыванием 100 п.н. было выполнено с использованием платформы Illumina Nextseq500, что дало в среднем 46,1 М считываний на образец. Для снятия переходников, обрезки и контроля качества мы использовали Trimmomatic [18]. PE-phred33 ILLUMINACLIP: TruSeq3-PE.fa: 2: 30: 10 MINLEN: 75 2. STAR15 [19] использовался для выравнивания файлов fastq с эталонным геномом человека GRCh47 / hg19 со следующими настройками: максимальный размер интрона, 500 kb; минимальный размер интрона — 20; допускается четыре несовпадения.HTSeq (версия HTSeq-0.6.1) [20] был выполнен для получения сырых подсчетов.
Сравнение профилей экспрессии генов между группами
Для оценки однородности профилей экспрессии генов между группами был рассчитан коэффициент ранговой корреляции Спирмена (SRCC) логарифмически трансформированной экспрессии гена для каждого образца с использованием функции корреляции в R (http: / /www.r-project.org). Были рассчитаны медиана и межквартильный диапазон SCC для всех сравнений между группами, и графики разброса худшего SRCC в каждой группе были получены в качестве репрезентативных графиков.Значения SRCC сравнивались с помощью критерия суммы рангов Вилкоксона, и P <0,05 считалось статистически значимым.
Анализ дифференциальной экспрессии с использованием DESeq2
DESeq2 в R-пакете использовался для идентификации дифференциально экспрессируемых (DE) генов в каждом состоянии [21]. В DESeq2 для идентификации дифференциально экспрессируемых генов использовался тест Вальда, специально разработанный для необработанных данных подсчета последовательностей РНК с отрицательной биномиальной моделью. Гены с P <0,05 использовали для дальнейшего анализа обогащения.
Анализ метилирования ДНК
Профили метилирования гДНК анализировали с использованием бисульфитного секвенирования с пониженным представлением. Вкратце, мы обрабатывали гДНК бисульфитом натрия с использованием набора EpiTech® Bisulfite (Qiagen), расщепляли рестриктазой Msp I и отбирали фрагменты со средним размером от 100 до 250 п.н. Мы мультиплексировали четыре образца на дорожку и секвенировали библиотеки, используя односторонние чтения 100 пар оснований и платформу Illumina Nextseq500; в итоге в среднем 25.Было получено 1 M считываний на образец. Мы выполнили первоначальный контроль качества файлов fastq с помощью FastaQC. Показания были выровнены с использованием режима сквозного выравнивания Bowtie2, допускающего четыре несовпадения; hg19 использовался в качестве эталонного генома [22]. BS-seeker2 [23] использовался для определения статуса метилирования отдельных сайтов CpG. Полученные текстовые файлы BS-seeker2 были очищены, чтобы получить процент метилирования отдельных сайтов CpG для каждого случая. В окне 1000 пар оснований (от + 500 до — 500 пар оснований), основанном на сайтах начала транскрипции всех генов, идентифицированных с помощью RNA-Seq, были получены проценты метилирования CpG для оценки влияния метилирования около сайтов начала транскрипции на экспрессию генов.Для групп некурящих / непародонтита (NN), некурящих / пародонтита (NP), курильщиков / непародонтита (SN) и курильщиков / пародонтита (SP) (таблица 1) статистическая значимость метилирования CpG для каждого гена рассчитывали для выявления статистически значимого метилирования вблизи локусов гена. Гены с P <0,05 использовали для дальнейшего анализа обогащения.
Корреляция между метилированием и экспрессией генов
Для анализа взаимосвязи между метилированием и экспрессией генов, которые показали статистически значимые различия по обоим параметрам, был проведен регрессионный анализ.Чтобы определить, происходит ли дифференциальное метилирование ДНК у субъектов с пародонтитом по сравнению с нормальными субъектами, была использована регрессионная модель с метилированием ( x i 1 ) и пародонтит ( x i 2 ) в качестве переменных-предикторов и экспрессии гена ( y и ), поскольку переменная ответа была подобрана функцией R aov:
$$ {y} _i = {\ beta} _0 + {\ beta} _1 {x} _ {i1} + {\ beta} _2 {x} _ { i2} + {\ beta} _3 {x} _ {i1} {x} _ {i2} + {\ epsilon} _i $$
, где i представляет каждый ген.Эта модель сравнивалась с нулевой линейной моделью, имеющей только метилирование ( x i 1 ) в качестве переменной-предиктора:
$$ {y} _i = {\ beta} _0 + {\ beta} _1 {x} _ {i1} + {\ epsilon} _i $$
Для выяснения влияния пародонтита на регрессионную модель был проведен дисперсионный анализ (ANOVA) двух моделей.
Анализ обогащения набора генов
Для анализа биологической значимости полученных данных метилирования мы выполнили анализ обогащения набора генов (GSEA) биологических процессов генной онтологии (GO-BP).Источник термина GO для расчета GSEA был получен с использованием библиотеки GO.db (версия 2.1) R. Тест GSEA для каждой группы выполнялся путем манипулирования библиотекой clusterProfiler в R [24]. Наборы генов с q <0,05 считались статистически значимыми.
Взаимодействие белок-белок
Исходя из предположения, что продукты метилированных генов могут прямо или косвенно взаимодействовать с другими белками, мы получили список генов, связанных с белок-белковым взаимодействием (PPI), выполнив анализ PPI для генов DE, проявляющих Метилирование ДНК у некурящих и курильщиков.Мы извлекли из базы данных гены, пораженные PPI, из iRefIndex 13.0 [25], манипулируя библиотекой iRefR, которая связывает базу данных iRefIndex со средой R. Список генов, полученный с помощью PPI, был проанализирован GSEA для выявления наборов генов, потенциально связанных как с генами DE, так и с метилированием ДНК.
Секвенирование транскриптома биопсии десны от пациентов с хроническим пародонтитом выявило новые паттерны экспрессии генов и сплайсинга | Геномика человека
Пильстрем Б.Л., Михалович Б.С., Джонсон Н.В.Заболевания пародонта. Ланцет. 2005; 366: 1809–20.
Артикул PubMed Google Scholar
Оффенбахер С., Баррос С.П., Бек Д.Д. Переосмысление воспаления пародонта. J Periodontol. 2008. 79: 1577–84.
CAS Статья PubMed Google Scholar
Гарлет GP. Деструктивная и защитная роль цитокинов при пародонтите: переоценка с точки зрения защиты хозяина и деструкции тканей.J Dent Res. 2010; 89: 1349–63.
CAS Статья PubMed Google Scholar
Буллон П., Морилло Дж. М., Рамирес-Тортоса М. К., Квилс Дж. Л., Ньюман Х. Н., Баттино М. Метаболический синдром и пародонтит: является ли оксидативный стресс общей связью? J Dent Res. 2009; 88: 503–18.
CAS Статья PubMed Google Scholar
Пишон Н., Хенг Н., Бернимулин Дж. П., Клебер Б. М., Виллих С. Н., Пишон Т.Ожирение, воспаление и пародонтоз. J Dent Res. 2007; 86: 400–9.
CAS Статья PubMed Google Scholar
Linden GJ, Lyons A, Scannapieco FA. Системные ассоциации пародонта: обзор доказательств. J Periodontol. 2013; 84: S8–19.
Артикул PubMed Google Scholar
Абэ Д., Кубота Т., Морозуми Т., Симидзу Т., Накасоне Н., Итагаки М., Йоши Х.Измененная экспрессия генов трансэндотелиальной миграции лейкоцитов и путей межклеточной коммуникации в тканях десен, пораженных пародонтитом. J Periodontal Res. 2011; 46: 345–53.
CAS Статья PubMed Google Scholar
Бейклер Т., Петерс Ю., Прайор К., Эйзенахер М., Флеммиг Т.Ф. Экспрессия генов в тканях пародонта после лечения. BMC Med Genomics. 2008; 1:30.
Артикул PubMed PubMed Central Google Scholar
Ким Д.М., Рамони М.Ф., Невинс М., Фиореллини Дж. П. Профиль экспрессии генов у пациентов с рефрактерным пародонтитом. J Periodontol. 2006; 77: 1043–50.
CAS Статья PubMed Google Scholar
Ван З., Герштейн М., Снайдер М. RNA-Seq: революционный инструмент для транскриптомики. Nat Rev Genet. 2009; 10: 57–63.
CAS Статья PubMed PubMed Central Google Scholar
Гарбер М., Грабхер М.Г., Гуттман М., Трапнелл С. Вычислительные методы аннотации транскриптомов и количественной оценки с использованием RNA-seq. Нат методы. 2011; 8: 469–77.
CAS Статья PubMed Google Scholar
Wu TD, Nacu S. Быстрое и устойчивое к SNP обнаружение сложных вариантов и сплайсинг при коротких чтениях. Биоинформатика. 2010; 26: 873–81.
CAS Статья PubMed PubMed Central Google Scholar
Андерс С., Хубер В. Анализ дифференциальной экспрессии для данных подсчета последовательностей. Genome Biol. 2010; 11: R106.
CAS Статья PubMed PubMed Central Google Scholar
Шен С., Парк Дж. У., Хуанг Дж., Диттмар К. А., Лу З. X, Чжоу К., Карстенс Р. П., Син Ю. MATS: байесовская структура для гибкого обнаружения дифференциального альтернативного сплайсинга из данных RNA-Seq. Nucleic Acids Res. 2012; 40: e61.
CAS Статья PubMed PubMed Central Google Scholar
Lee JH, Gao C, Peng G, Greer C, Ren S, Wang Y, Xiao X. Анализ сложности транскриптома посредством секвенирования РНК в нормальных и поврежденных сердцах мышей. Circ Res. 2011; 109: 1332–41.
CAS Статья PubMed PubMed Central Google Scholar
Ливак К.Дж., Шмитген Т.Д. Анализ данных относительной экспрессии генов с использованием количественной ПЦР в реальном времени и метода 2 (-ΔΔC (T)) . Методы. 2001; 25: 402–8.
CAS Статья PubMed Google Scholar
Tokheim C, Park JW, Xing Y. PrimerSeq: дизайн и визуализация праймеров RT-PCR для альтернативного сплайсинга с использованием данных RNA-seq. Геномика Протеомика Биоинформатика. 2014; 12: 105–9.
Артикул PubMed PubMed Central Google Scholar
Davanian H, Stranneheim H, Bage T., Lagervall M, Jansson L, Lundeberg J, Yucel-Lindberg T.Профили экспрессии генов в парных биоптатах десен из пораженных пародонтитом и здоровых тканей, выявленные путем массового параллельного секвенирования. PLoS One. 2012; 7: e46440.
CAS Статья PubMed PubMed Central Google Scholar
Фьюри В., Батливалла Ф., Грегерсен П.К., Ли В. Вероятности перекрытия списков генов высшего ранга, гипергеометрическое распределение и строгость критерия отбора генов. Conf Proc IEEE Eng Med Biol Soc.2006; 1: 5531–4.
PubMed Google Scholar
Ван Э.Т., Сандберг Р., Ло С., Хребтукова И., Чжан Л., Майр С., Кингсмор С.Ф., Шрот Г.П., Бердж CB. Альтернативная регуляция изоформ в транскриптомах тканей человека. Природа. 2008. 456: 470–6.
CAS Статья PubMed PubMed Central Google Scholar
Сяо Х, Ли Дж. Системный анализ альтернативной сварки и ее регулирования.Wiley Interdiscip Rev Syst Biol Med. 2010; 2: 550–65.
CAS Статья PubMed Google Scholar
Гейгер Б., Шпатц Ю.П., Бершадский А.Д. Восприятие окружающей среды через очаговые спайки. Nat Rev Mol Cell Biol. 2009; 10: 21–33.
CAS Статья PubMed Google Scholar
Белый ES, Muro AF. Варианты сплайсинга фибронектина: понимание их множественной роли в здоровье и болезнях с использованием инженерных моделей мышей.IUBMB Life. 2011; 63: 538–46.
CAS Статья PubMed Google Scholar
D’Aiuto F, Orlandi M, Gunsolley JC. Доказательства того, что лечение пародонта улучшает биомаркеры и исходы сердечно-сосудистых заболеваний. J Periodontol. 2013; 84: S85–105.
Артикул PubMed Google Scholar
Hang Y, Stein R. Активность MafA и MafB в бета-клетках поджелудочной железы. Trends Endocrinol Metab.2011; 22: 364–73.
CAS Статья PubMed PubMed Central Google Scholar
Круг С.М., Шульцке Дж. Д., Фромм М. Плотное соединение, избирательная проницаемость и родственные заболевания. Semin Cell Dev Biol. 2014; 36: 166–76.
CAS Статья PubMed Google Scholar
Пресланд РБ, Юревич RJ. Понимание эпителиального барьера: что молекулярная биология и генетика говорят нам о функциях слизистой оболочки полости рта и эпидермальных тканей.J Dent Educ. 2002; 66: 564–74.
PubMed Google Scholar
Сокранский С.С., Хаффаджи А.Д., Гудсон Дж. М., Линд Дж. Новые концепции деструктивного заболевания пародонта. J Clin Periodontol. 1984; 11: 21–32.
CAS Статья PubMed Google Scholar
Преза Д., Олсен И., Виллумсен Т., Гринде Б., Пастер Б.Дж. Разнообразие и сайт-специфичность микрофлоры полости рта у пожилых людей.Eur J Clin Microbiol Infect Dis. 2009; 28: 1033–40.
CAS Статья PubMed PubMed Central Google Scholar
Аас Дж. А., Пастер Б. Дж., Стокс Л. Н., Олсен И., Дьюхерст Ф. Э. Определение нормальной бактериальной флоры полости рта. J Clin Microbiol. 2005; 43: 5721–32.
Артикул PubMed PubMed Central Google Scholar
Lindhe J, Socransky S, Wennstrom J.Дизайн клинических испытаний традиционных методов лечения пародонтита. J Clin Periodontol. 1986; 13: 488–99.
CAS Статья PubMed Google Scholar
Okugawa T, Kaneko T, Yoshimura A, Silverman N, Hara Y. NOD1 и NOD2 опосредуют обнаружение пародонтальных патогенов. J Dent Res. 2010; 89: 186–91.
CAS Статья PubMed PubMed Central Google Scholar
Prates TP, Taira TM, Holanda MC, Bignardi LA, Salvador SL, Zamboni DS, Cunha FQ, Fukada SY. NOD2 способствует резорбции кости, вызванной Porphyromonas gingivalis. J Dent Res. 2014; 93: 1155–62.
CAS Статья PubMed PubMed Central Google Scholar
Belibasakis GN, Johansson A. Aggregatibacter actinomycetemcomitans нацелена на экспрессию инфламмасом NLRP3 и NLRP6 в мононуклеарных лейкоцитах человека. Цитокин.2012; 59: 124–30.
CAS Статья PubMed Google Scholar
Берглунд Т., Донати М. Аспекты адаптивного ответа хозяина при пародонтите. J Clin Periodontol. 2005. 32: 87–107.
CAS Статья PubMed Google Scholar
Берглунд Т., Донати М., Зицманн Н. В-клетки при пародонтите: друзья или враги? Периодонтол 2000. 2007; 45: 51–66.
Артикул PubMed Google Scholar
Gonzales JR. Подгруппы Т- и В-клеток при пародонтите. Периодонтол 2000. 2015; 69: 181–200.
Артикул PubMed Google Scholar
Abe T, AlSarhan M, Benakanakere MR, Maekawa T., Kinane DF, Cancro MP, Korostoff JM, Hajishengallis G. Стимулирующие B-клетки цитокины BLyS и APRIL повышены при пародонтите человека и необходимы для B-клеток. -зависимая потеря костной массы при экспериментальном периодонтите мышей.J Immunol. 2015; 195: 1427–35.
CAS Статья PubMed Google Scholar
Оливер-Белл Дж., Бутчер Дж. П., Малкольм Дж., Маклауд М.К., Адрадос Планелл А., Кэмпбелл Л., Ниббс Р.Дж., Гарсайд П., Макиннес И.Б., Калшоу С. Пародонтит в отсутствие В-клеток и специфических анти- бактериальные антитела. Mol Oral Microbiol. 2015; 30: 160–9.
CAS Статья PubMed Google Scholar
Gaffen SL, Hajishengallis G. Новый воспалительный цитокин на блоке: переосмысление пародонтоза и парадигмы Th2 / Th3 в контексте клеток Th27 и IL-17. J Dent Res. 2008. 87: 817–28.
CAS Статья PubMed PubMed Central Google Scholar
Cheng WC, Hughes FJ, Taams LS. Наличие, функция и регуляция клеток IL-17 и Th27 при пародонтите. J Clin Periodontol. 2014; 41: 541–9.
CAS Статья PubMed Google Scholar
Gamazon ER, Незнакомец BE. Геномика альтернативного сплайсинга: эволюция, развитие и патофизиология. Hum Genet. 2014; 133: 679–87.
CAS Статья PubMed Google Scholar
Биамонти Г., Катилло М., Пигнатаро Д., Монтекукко А., Гинья С. Альтернативная сплайсинговая сторона рака. Semin Cell Dev Biol. 2014; 32: 30–6.
CAS Статья PubMed Google Scholar
Тази Дж., Баккур Н., Стамм С. Альтернативное сращивание и болезнь. Biochim Biophys Acta. 2009; 1792: 14–26.
CAS Статья PubMed Google Scholar
Juan-Mateu J, Villate O, Eizirik DL. Механизмы в эндокринологии: альтернативный сплайсинг: новый рубеж в исследованиях диабета. Eur J Endocrinol. 2016; 174: R225.
CAS Статья PubMed Google Scholar
Радж Б., Бленкоу Б.Дж. Альтернативный сплайсинг в нервной системе млекопитающих: недавнее понимание механизмов и функциональных ролей. Нейрон. 2015; 87: 14–27.
CAS Статья PubMed Google Scholar
Fan X, Tang L. Аберрантный и альтернативный сращивание при заболеваниях скелетной системы. Ген. 2013; 528: 21–6.
CAS Статья PubMed Google Scholar
Фоглер М. BCL2A1: аутсайдер в семействе BCL2. Смерть клетки отличается. 2012; 19: 67–74.
CAS Статья PubMed Google Scholar
Lundmark A, Davanian H, Bage T, Johannsen G, Koro C, Lundeberg J, Yucel-Lindberg T. Анализ транскриптома показывает, что муцин 4 тесно связан с пародонтитом, а плекстрин является связующим звеном с системными заболеваниями. Научный доклад 2015; 5: 18475.
CAS Статья PubMed PubMed Central Google Scholar
Parkar MH, Bakalios P, Newman HN, Olsen I. Экспрессия и сплайсинг гена фибронектина в здоровой и больной ткани пародонта. Eur J Oral Sci. 1997; 105: 264–70.
CAS Статья PubMed Google Scholar
Белый ES, Baralle FE, Muro AF. Новое понимание формы и функции вариантов сплайсинга фибронектина. J Pathol. 2008; 216: 1–14.
CAS Статья PubMed PubMed Central Google Scholar
Микробиологический и метаболомный анализ десневой десневой жидкости у пациентов с общим хроническим пародонтитом: уроки для прогнозирующего, профилактического и персонализированного медицинского подхода
Использование секвенирования гена 16S рРНК и ГХ-МС технологий при пародонтите
Пародонтит — инфекционное заболевание со сложной этиологией и особенно актуален для целей PPPM из-за его огромного влияния на социальную жизнь людей [31].В течение многих лет продолжалось изучение бактериальной этиологии пародонтита, так как различные микроорганизмы рассматривались как наиболее важный фактор, вовлеченный в заболевание. Чтобы продвигать надежный метод эффективного клинического ведения, необходимо изучить сложную этиологию заболеваний пародонта [32]. Всестороннее понимание экологии поддесневой микробиоты и взаимосвязи между составом микробиома и метаболомным состоянием может позволить разработать новые стратегии профилактики и лечения пародонтита.
Используя секвенирование гена 16S рРНК и технологии ГХ-МС, мы показали значительные филогенетические различия в поддесневых микробных сообществах и сигнатурах метаболитов GCF хозяина между пациентами с пародонтитом и здоровыми людьми. В целом, анализ 16S рРНК показал, что филогенетический состав и структура микробиома полости рта отчетливо различались между пародонтозом и здоровыми людьми. Согласно анализу метаболомного профиля, дискриминация, полученная из образцов GCF, демонстрирует существование метабономической сигнатуры заболевания GCP в GCF.Более того, связь измененной микробиоты, метаболитов и клинических показателей была последовательной между двумя группами, что указывало на то, что бактерии и метаболизм в поддесневой среде были тесно связаны, и что эта корреляция и разница между пародонтитом и здоровьем микроэкологии также были показано в клинических данных. Таким образом, результат предоставил возможный подход к прогнозированию и различению пародонтита, поскольку метаболиты были индикатором воспалительного статуса.
Достижения в текущем исследовании: интерпретация результатов микробных сообществ
В текущем исследовании α-разнообразие не выявило четких различий между здоровыми индивидуальными образцами и индивидуальными образцами от пародонтита. Одно из возможных объяснений состоит в том, что общие типы в GCF относительно постоянны, потому что основные типы были похожи в предыдущих исследованиях. Кроме того, все люди в этом исследовании происходили из одной и той же жилой зоны, что привело к незначительным различиям в бактериальном α-разнообразии между двумя группами из-за высокого сходства диеты и жизненных привычек.Сравнение β-разнообразия выявило значительные различия в микробном сообществе между пародонтитом и здоровыми группами. По мере изменения состояния тканей пародонта состав сообщества поддесневых бляшек при пародонтите изменялся.
На уровне филума микробиота от пародонтита имела более высокие пропорции Bacteroidetes, Actinobacteria, Fusobacteria, Spirochetes и Synergistetes, в то время как доли Proteobacteria и Firmicutes были выше в микробиоте от здоровых людей, что показывает, что большинство таксонов совпадают с предыдущими. исследования, но не в той же пропорции [33,34,35] (дополнительный рис.S2b). Porphyromonas , Prevotella , Neisseria , Fusobacterium , Treponema и т. Д., Некоторые из них включали хорошо известные деструктивные патогены пародонта ( представлены Porphyromonas gingivalis 000, ola Treponema 000, ola Treponema при более высокой численности на уровне рода у людей с пародонтитом, тогда как Ralstonia , Streptococcus и Haemophilus показали более высокие пропорции у здоровых людей.Кроме того, анализ Metastats показал, что Porphyromonas , Prevotella , Filifactor , Fusobacterium и т. Д. Были значительно обогащены у пациентов с пародонтозом (дополнительная таблица S1). Наш результат согласуется с опубликованными исследованиями. Таксономическое обогащение этих таксонов может вносить вклад в различия в разнообразии образцов GCF и, в определенной степени, на функцию сообщества поддесневых микробов между пародонтитом и здоровыми людьми.Некоторые новые микроорганизмы, широко распространенные и тесно связанные с заболеванием, нуждаются в дальнейшем изучении, поскольку они могут играть значительную роль в развитии пародонтита. Например, исследователи доказали, что Filifactor alocis имеет общие характеристики с установленными патогенами пародонта и может вызывать разрушение тканей пародонта [36, 37].
При изучении микробной экологии нас больше всего интересует метаболическая функция микрофлоры. С развитием технологии анализа данных мы теперь можем прогнозировать метаболическую функцию бактерий на основе результатов секвенирования гена 16S рРНК, чтобы сопоставить «идентичность» видов с их «функцией».Согласно этому прогнозу, мы можем получить представление о микробной функции и возможном влиянии биохимической активности бактерий на хозяина. В нашем исследовании метаболическая активность, включая основной метаболизм (например, метаболизм энергии, кофактора и витаминов), семейства ферментов, биосинтез и метаболизм гликанов, а также биосинтез вторичных метаболитов, были активированы в микробиоте людей с пародонтозом по сравнению с таковыми у людей с пародонтозом. микробиота здорового контроля.Тем не менее в пародонтальных сообществах наблюдалось снижение углеводного обмена. Предыдущие исследования показали, что гены функционального метаболизма углеводов относительно схожи между пародонтитом и здоровыми людьми [38, 39]. Основываясь на наших результатах, было выдвинуто предположение, что сообщество пародонтальной группы может использовать сахара, всасываемые напрямую, вместо их биосинтеза, поэтому они демонстрируют относительно сниженный углеводный обмен. В заключение следует отметить, что результаты не только продемонстрировали композиционный дисбиоз, но и предсказали метаболические функциональные нарушения.
Достижения в текущем исследовании: интерпретация результатов метаболитов
Мы успешно проверили 17 дифференциальных метаболитов в образцах GCF с помощью GC-MS, возможно, отделив пациентов с GCP от здоровых людей. Многие метаболические изменения связаны с прогрессированием заболеваний пародонта.
Синтез, деградация и взаимопревращение ДНК, РНК, липидов и углеводов требуют участия метаболизма пиримидина. Нуклеиновая кислота клеток пародонта может высвобождаться, когда клетки повреждены непосредственно микробиотой пародонта или косвенно иммунной системой хозяина.Нуклеозиды и азотистые основания являются важным источником питательных веществ для бактерий и могут использоваться для биосинтеза нуклеиновых кислот или разложения на углерод и источники энергии. В результате MSEA и анализа топологии было обнаружено, что метаболизм пиримидина является наиболее значимым путем, участвующим в GCP (рис. 5). Повышенный уровень урацила и пониженный уровень тимидина и метилмалоновой кислоты указали на то, что метаболизм пиримидина у пациентов с GCP отличался от такового у здоровых людей. Кроме того, урацил имел положительную корреляцию с родами, обогащенными пародонтозом, и отрицательную корреляцию со здоровыми контрольными родами.Эта взаимосвязь между тимидином, метилмалоновой кислотой и родами была противоположной. Известно, что когда патогены вторгаются в клетки-хозяева, они могут влиять на метаболизм пиримидина в организме хозяина, создавая благоприятные условия для пролиферации [40]. Это открытие предполагает, что патогены, связанные с GCP, могут изменять метаболизм инфицированных хозяев по еще неизвестному механизму.
Ткани пародонта богаты белками. Как показано в MSEA и топологическом анализе, метаболизм d-глутамина и d-глутамата, метаболизм гистидина и метаболизм тирозина были связанными путями, участвующими в GCF у людей с пародонтитом, что подтверждает результаты предыдущей работы, в которой сообщалось об увеличенной деградации макромолекул, включая белки, у лиц с пародонтитом [41, 42].Периодонтальные микроорганизмы и воспалительные протеазы хозяина могут расщеплять протеины пародонта хозяина на пептиды и аминокислоты, которые будут служить обильным запасом энергии и источником питания для микробов [43, 44], в конечном итоге влияя на микроорганизмы и функциональную структуру. Ли и др. [39] указали, что поддесневые микробиомы могут непосредственно поглощать некоторое количество аммиака для физиологической активности вместо его биосинтеза, потому что гены микробиома полости рта, участвующие в синтезе аминокислот, показали пониженное относительное количество при пародонтите.Поскольку воспаление пародонта приводит к разрушению соединительной ткани, вероятно, что повышенный уровень глицина-d5 и β-глутаминовой кислоты в GCF был вызван разрушением ткани.
Активные формы кислорода участвуют в деструкции пародонта при воспалительных заболеваниях пародонта. Дисбаланс между окислительной и антиоксидантной активностью может быть ключевым фактором деструктивного действия активных форм кислорода [45]. Принимая во внимание результаты, повышенная антиоксидантная активность наблюдалась в GCF у пародонтов, что отражалось повышенной концентрацией N-карбамилглутамата.Предыдущие данные показали, что N-карбамилглутамат может уменьшать окислительный стресс за счет усиления активности антиоксидантных ферментов [46] и улучшения неферментативного содержания антиоксидантов [47] у млекопитающих. Кроме того, N-карбамилглутамат может облегчить воспалительный ответ путем подавления экспрессии мРНК IL-1b и TNF-a [46]. Однако наш результат не согласовывался с предыдущими исследованиями, которые подтвердили, что воспаление пародонта тесно связано с окислительным стрессом [48, 49].Объяснение заключается в том, что у пациентов, страдающих пародонтитом разной степени, только у пациентов с запущенным периодонтитом снижена общая антиоксидантная активность и повышен уровень активных форм кислорода [50, 51]. Наши образцы были взяты у пациентов с пародонтитом средней и тяжелой степени. По клиническим данным, средние PD и CAL не свидетельствовали о тяжелых показателях пародонтита.
Метаболизм GCF тесно связан с биохимией бактерий. Хорошо известно, что большинство бактерий, связанных с пародонтитом, используют сахар в качестве источника энергии и углерода.Результат, показывающий, что уровень фруктозы-1 был выше у пациентов с GCP, чем у здоровых людей, согласуется с предыдущим метаболомическим исследованием биопленок полости рта, показывающим повышенное содержание фруктозо-6-фосфата [52].
Как сообщается, 4-гидроксифенилуксусная кислота продуцируется Porphyromonas gingivalis , местной бактерией в полости рта человека, в качестве конечного продукта метаболизма во время метаболизма фенилаланина и тирозина [53]. В слюне здоровых людей концентрация 4-гидроксифенилуксусной кислоты была ниже 10 мкМ [54], тогда как концентрация 4-гидроксифенилуксусной кислоты выше 20 мкМ была обнаружена у лиц с пародонтитом [55].Увеличение популяции Porphyromonas gingivalis у пациентов с пародонтитом может способствовать такому увеличению 4-гидроксифенилуксусной кислоты.
Микробиота и метаболиты как инструменты для прогнозирования воспалительного статуса пародонта
Результаты показали явные различия в клинических данных, поддесневых микроорганизмах и метаболитах GCF между группой пародонтита и здоровой контрольной группой. Кроме того, анализ корреляционной тепловой карты микроорганизмов, метаболитов и клинических данных свидетельствует о наличии согласованной тенденции среди них (рис.6). В частности, клинические данные о тяжелых заболеваниях пародонта положительно коррелировали с типами, обогащенными пародонтитом, и метаболитами с повышенной регуляцией пародонтита, но отрицательно коррелировали с родами, обогащенными здоровыми, и с метаболитами с пониженной регуляцией пародонтита. Кроме того, большинство метаболитов с повышенной регуляцией пародонтита показали значительную положительную связь с некоторыми родами, обогащенными пародонтитом, и значительно отрицательную связь с родами, обогащенными здоровым пародонтитом. Точно так же метаболиты с пониженной регуляцией пародонтита имели противоположные отношения с родами.Эти результаты подтверждают, что микроорганизмы-хозяева и микроорганизмы полости рта тесно связаны и взаимодействуют при развитии пародонтита. Учитывая, что переход от здоровья пародонта к заболеванию связан с общим дисбалансом, в том числе с измененными метаболическими сигнатурами в организме хозяина и в сообществе пародонтальных микробов одновременно, эти результаты открывают возможность для помощи в изучении активности заболевания и модуляции сложных микробных взаимодействий в организме. формирование пародонтопатического сообщества. Кроме того, клинические данные пародонтита могут быть отражены в изменении микробного сообщества полости рта и изменении метаболитов в GCF.Этот результат предполагает, что микробиота и метаболиты могут быть инструментами для прогнозирования воспалительного статуса пародонта. В текущем исследовании ROC-кривая также использовалась для оценки того, как эти метаболиты в разном количестве указывают на периодонтит или в дальнейшем прогнозируют его. Комбинация цитрамалевой кислоты и N-карбамилглутамата дала удовлетворительную точность (AUC = 0,876) для прогнозной диагностики пародонтита в нашем исследовании, тогда как другое исследование обнаружило совершенно разные метаболиты для диагностики [56].Это несоответствие между различными исследованиями может быть вызвано разными образцами исследований и присущим им биологическим разнообразием между людьми. Эти показатели требуют дальнейшего изучения для подтверждения клинической значимости.
Ассоциация оральной микробиоты пародонтита и глобальное здоровье
Многочисленные отчеты продемонстрировали участие микробиоты полости рта в патогенезе системных заболеваний, таких как сердечно-сосудистые заболевания [57], ревматоидный артрит [58] и воспаление кишечника [59].В популяции с ослабленным иммунитетом попадание условно-патогенных или патогенных бактерий полости рта в кровоток через барьер слизистой оболочки полости рта может привести к аномальным местным или системным иммунным и метаболическим ответам и перевариванию питательных веществ [60, 61, 62]. И наоборот, системные многофакторные заболевания могут привести к прямой модификации микробиоты полости рта.
Что касается иммунитета, то система иммунной защиты, включая врожденные лимфоидные клетки и рецепторы распознавания образов, а также толерантность, очень сложна, и важно сохранить надлежащий микробиологический и функциональный гомеостаз полости рта.Несоответствующий ответ хозяина или недостаточный иммунный ответ либо вызовут повреждение ткани, либо допустят чрезмерный рост и инвазию микробов. Когда патогенные бактерии полости рта разрастаются из-за плохой гигиены полости рта, усиливаются реакции как врожденного, так и адаптивного иммунитета, что также может привести к более обширному повреждению коллатеральных тканей. В результате могут возникнуть заболевания пародонта [2]. В свою очередь, заболевания полости рта связаны со многими заболеваниями, связанными с иммунитетом (например, системным склерозом, синдромом Шегрена и ревматоидным артритом) [63, 64] через микробиом полости рта.
Системное метаболическое здоровье также тесно связано с заболеваниями пародонта. Зубные бактерии и бактерии полости рта часто являются ранними индикаторами и факторами риска ожирения [65]. Goodson et al. [66] предположили, что бактерии полости рта могут повышать метаболическую эффективность и энергетический метаболизм, способствуя инсулинорезистентности, влияя на увеличение веса и развитие ожирения. Ростислав и др. [67] обнаружили, что (1) ожирение, вызванное глутаматом натрия, вызывает изменения тканей пародонта; и (2) наноцерия вносит вклад в коррекцию патологических изменений в тканях пародонта за счет балансирования способности ингибировать белок и снижения деполимеризации фукозилированных белков и протеогликанов и антиоксидантной активности у крыс с ожирением, вызванным глутаматом.
Рот, как единственный естественный вход для пищи, контролирует потребление и начальное взаимодействие того, что может стать кишечной микробиотой. Соответственно, микробиом полости рта может иметь измененную структуру, состав и функцию из-за изменений микробиоты кишечника из-за взаимодействий микробиома хозяина. В некоторых исследованиях описаны вариации микробного разнообразия и состава ротовой полости у людей с воспалительными заболеваниями кишечника [68,69,70]. Xun et al. [71] исследовали стратификацию пациентов и биомаркеры, указывающие на воспалительные заболевания кишечника, в зависимости от микробного профиля полости рта.Кроме того, хорошо известно, что пробиотики и пребиотики могут манипулировать микробиотой и / или их метаболическим отпечатком в кишечнике, а затем действовать на удаленных участках, включая кожу, дыхательные пути, сердце, мозг и обмен веществ [72]. Благодаря такому системному поведению, правильное использование пробиотиков в полости рта или кишечнике может быть многообещающим применением при лечении пародонтита.
Потенциальное использование пробиотиков при пародонтите
Такие факторы, как диета, потребление лекарств, окружающая среда, генетика хозяина, способ доставки или фенотип, могут влиять на высокое микробное разнообразие [73].Наши результаты показали, что микробиота и метаболиты в полости рта меняются при пародонтите. В этом отношении могут быть предприняты усилия по изучению использования пробиотиков для изменения состава зубного налета в качестве монотерапии для профилактики хронического пародонтита и гингивита или в качестве дополнительной терапии с удалением зубного камня и выравниванием корня при лечении хронического пародонтита. Исследования показали, что пробиотики оказывают благотворное влияние на параметры пародонта, включая индекс зубного налета, индекс десен, кровотечение при зондировании, уровень клинического прикрепления, объем жидкости десневой щели и факторы реакции организма [74].Как два известных класса пробиотиков, молочнокислые бактерии (LAB) и бифидобактерии наиболее часто и успешно используются для лечения заболеваний, связанных с микробиотой кишечника и инфекциями ротоглотки [75]. Однако их роль в модуляции заболеваний пародонта до конца не изучена. Ростислав и др. [76] изучили специфические свойства шести штаммов LAB и двух штаммов бифидобактерий в отношении их устойчивости к антибиотикам, устойчивости к биологическим агентам (желудочный сок, желчь и ферменты поджелудочной железы) и адгезивных свойств, предоставив нам комплексный подход к оценке свойств и выбор «лучших» пробиотических штаммов для лечения пародонтита.
Концепция PPPM в текущем исследовании
Образцы GCP неинвазивно доступны и легко обрабатываются. Помимо патофизиологической роли, микрофлора полости рта и метаболиты в образцах ротовой полости являются ценными биомаркерами для стратификации пациентов, мониторинга заболеваний, прогнозной диагностики и целевой профилактики [77, 78]. Затем могут быть предоставлены услуги прогнозирования с учетом нескольких потенциальных относительных диагнозов: непосредственно для заболеваний пародонта и косвенно для расстройств пищеварительного тракта, ожирения, заболеваний иммунитета и рака.
Более того, мультиомиксы могут быть лучшим выбором для передовых диагностических инструментов, в частности, с использованием жидкой биопсии, поскольку эти подходы хорошо обоснованы несколькими недавними исследованиями [79]. Секвенирование генов РНК 16s и инструменты ГХ-МС помогают нам определить, сколько видов бактерий присутствует в образце, количество и соотношение каждого вида, а также предполагаемые функции и метаболические «отпечатки пальцев» обнаруженных экспрессий генов, что позволяет предположить, что у любого пациента индивидуальный микробиом и метаболическая информация могут быть идентифицированы [2].
Для отдельных людей с помощью мультиомного анализа GCF мы можем определить уникальные виды бактерий полости рта и информацию о метаболитах, а затем проанализировать соответствующий молекулярный путь в глобальном масштабе, что может предсказать, есть ли какие-либо нарушения в тканях пародонта или здоровье системы. В частности, с точки зрения результатов этого исследования, если самые прямые биомаркеры цитрамалевой кислоты и N-карбамилглутамата в GCF значительно увеличиваются по сравнению с предыдущим соотношением или находятся на высоком уровне, человек может быть подвержен риску пародонтита или уже болен пародонтитом. или другие родственные скрытые заболевания.Это прогнозирование затем запускает целевую профилактику в раннем возрасте, такую как повышенное внимание к гигиене полости рта, овладение правильным методом чистки зубов, поддержание здорового питания, переход на более здоровый образ жизни или более регулярные медицинские осмотры [80]. Если появляется какое-либо нарушение микробиоты полости рта или диагностируется заболевание, это также может помочь людям разработать индивидуальную стратегию лечения, такую как выбор подходящих индивидуализированных видов пробиотиков. В популяциях понимание активности микробиома и характеристика обычно используемых биомаркеров пародонтита имеет важное значение для разработки будущих стратегий общественного здравоохранения и потенциально предоставляет информацию для разработки пробиотиков.
Сильные стороны и ограничения
Биологические омики позволяют при исследовании и лечении заболеваний перейти от однопараметрической модели к многопараметрической модели [81]. В то же время стратегия PPPM в области гигиены полости рта требует комплексного анализа нескольких компонентов для систематического изучения молекулярных механизмов и выявления эффективных биомаркеров [82].
Однако ограничение этого исследования относится к сбору образцов из одного региона только за один раз. Дальнейшее когортное исследование с образцами от пациентов с разной степенью деструкции пародонта из обширной географической области может потребоваться для лучшего понимания динамических сдвигов в составе и функции микробиома, а также изменений в метаболизме во время развития заболевания.
Версия МКБ-10: 2016
Справка по расширенному поиску
Расширенный поиск позволяет выполнять поиск по выбранным свойствам классификации. Ты возможность поиска по всем свойствам или только по выбранному подмножеству
Во-первых, вам нужно введите ключевые слова в поле Search Text , затем проверьте свойства, которые вы хотите включить в поиск.
Система будет искать ключевые слова в свойствах, которые вы проверили и оценили результаты аналогично поисковой системе
Результаты будут отображены на панели результатов поиска.Если поисковый запрос дает более 200 результатов, то только 200 лучших будут отображается.
Если вы укажете более одного ключевого слова, система будет поиск предметов, в которых есть все ключевые слова.
Подстановочные знаки: Вы также можете использовать подстановочный знак *. см. примеры ниже.
Оператор ИЛИ : Возможны результаты, которые либо то, либо другое ключевое слово.См. Пример 4.
Примеры:
1. Поисковый текст: диабет {находит все слова «диабет» в поля поиска}
2. Поиск по тексту: diabet * {находит все слова, начинающиеся с «диабет»}
3. Поиск по тексту: diabet * mellitus {находит все слова, в которых есть начинается с «diabet» и также содержит слово «mellitus»}
4.Текст для поиска: tubercul * (легкое ИЛИ гортань) {находит все слова, в которых есть начинается с «туберкулеза» и затем включает в себя легкое ИЛИ гортань
Результаты поиска
После поиска результаты отображаются в правом нижнем углу экрана. Здесь в программе перечислены названия категорий МКБ, в которых выполняется поиск. ключевые слова найдены.
Нажав на любой результат, вы попадете в эту категорию
Вы можете закрыть окно расширенного поиска, щелкнув X в верхнем левом углу окна.
Размер панели результатов поиска можно изменить, перетащив горизонтальную линию над ней
границ | Комплемент-зависимые механизмы и вмешательства при заболеваниях пародонта
Введение
Комплементпредставляет собой интерактивную сеть растворимых, связанных с клеточной поверхностью и внутриклеточных молекул, которые активируют, усиливают и регулируют иммунитет и воспаление (1, 2). Помимо классических белков сыворотки (C1-9), сеть содержит в общей сложности около 50 белков, включая молекулы распознавания образов, конвертазы и другие протеазы, рецепторы и регуляторы.Активация комплемента инициируется различными путями: классическим, лектиновым или альтернативным (рис. 1). Классический и лектиновый пути активируются после связывания ассоциированных с комплементом молекул распознавания образов (например, C1q и маннозосвязывающий лектин, соответственно) с иммунными комплексами (классический путь) или с углеводными фрагментами, экспонируемыми на микробных или поврежденных / некротических клетках-хозяевах. (лектиновый путь). Альтернативный путь инициируется механизмом тикания и, кроме того, усиливает первоначальный ответ, вызванный двумя другими путями комплемента.
Рисунок 1 . Вовлечение комплемента и TLR в дисбактериоз и воспалительную потерю костной массы при пародонтите. Классический, лектиновый и альтернативный пути сходятся в центральном компоненте комплемента, C3, и активируют его, что приводит к образованию различных эффекторов, таких как опсонин C3b, воспалительные анафилатоксины C3a и C5a и комплекс атаки на мембрану C5b-9 ( MAC). Фрагменты активации C3a и C5a активируют соответственно C3aR и C5aR1, которые взаимодействуют с Toll-подобными рецепторами (TLR) и синергически активируют воспалительные лейкоциты.TLR также усиливают экспрессию C3aR и C5aR1. Воспаление, вызванное перекрестными взаимодействиями комплемента и TLR, не только вызывает разрушение десневой ткани и потерю костной массы при пародонтите, но также способствует ремоделированию симбиотической микробиоты в дисбиотическую, тем самым еще больше усиливая деструктивное воспаление.
Все три пути сходятся в центральном компоненте системы комплемента, C3, активация которого приводит к генерации эффекторов, которые способствуют способности антител и фагоцитов устранять микробные патогены (через опсонизацию C3b), индуцировать хемотаксис и воспаление (через анафилатоксины C3a и C5a) и лизировать чувствительные микробные мишени (через комплекс мембранной атаки C5b-9 [MAC]) (рис. 1).Кроме того, в сотрудничестве с другими иммунными и физиологическими системами комплемент способствует нормальному развитию тканей и органов, интегрирует и координирует врожденный и адаптивный иммунитет, опосредует клиренс апоптических клеток и способствует восстановлению тканей после повреждения (1, 3). В последние годы также стало все более очевидным, что комплемент продуцируется не только в печени, и его действие не ограничивается внутрисосудистым и внеклеточным компонентами. Действительно, было показано, что компоненты комплемента могут продуцироваться локально резидентными тканевыми клетками, а также рекрутированными лейкоцитами.Более того, была идентифицирована внутриклеточная система комплемента, и было показано, что она обладает новыми гомеостатическими и иммунными функциями, такими как регуляция активации Т-клеток CD4 + (2, 4).
Несмотря на свою важность для гомеостатического иммунитета, комплемент может нарушить регуляцию или чрезмерно активироваться (например, из-за генетических или микробных факторов вирулентности хозяина), тем самым превратившись из гомеостатического в патологический эффектор, который может вызывать или усугублять ряд заболеваний, таких как рак. или воспалительные заболевания, включая пародонтит (рис. 1), как подробно обсуждается в следующем разделе (5–8).Пародонтит — распространенное хроническое воспалительное заболевание, которое вызывает разрушение пародонта, то есть тканей, которые окружают и поддерживают зубы, а именно десны, периодонтальной связки и альвеолярной кости. Если не лечить, пародонтит может привести к потере зубов и, возможно, нарушению жевания (9). По оценкам, тяжелый периодонтит поражает около 10% взрослых (10, 11). В своей тяжелой форме заболевание пародонта связано с повышенным риском определенных системных состояний, таких как атеросклероз (12).
Недавние данные клинических исследований микробиома и механистических исследований на животных моделях показали, что пародонтит является дисбиотическим заболеванием, а не инфекцией, приписываемой нескольким избранным видам (13–15). Повреждение соединительной ткани и потеря альвеолярной кости опосредованы дисрегулируемой и чрезмерной воспалительной реакцией, которая включает компоненты как врожденного, так и адаптивного иммунитета, но не может контролировать вызвавшую ее дисбиотическую микробную нагрузку (16). Фактически, деструктивная воспалительная реакция пародонта используется дисбиотическими микробными сообществами для получения питательных веществ из продуктов распада тканей (17, 18).Тот факт, что заболевание преимущественно опосредуется воспалительной реакцией хозяина и что воспаление необходимо для поддержания дисбиотических микробных сообществ, оправдывает обоснование разработки стратегий модуляции хозяина для лечения периодонтита. Такие новые вмешательства могут использоваться в качестве дополнительных для улучшения существующих методов лечения (например, механического удаления патогенной биопленки), которые не всегда достаточны для лечения пародонтита (19–22), тем самым усиливая его значительное бремя для общественного здравоохранения и экономики (9, 11). , 23, 24).Здесь мы обсуждаем клинические и доклинические исследования, которые в совокупности связали чрезмерную активацию комплемента с пародонтитом и предоставили механистическое понимание этой взаимосвязи, открывая путь к терапии, направленной на комплемент, для лечения этого воспалительного заболевания полости рта с сильной связью с повышенным риском других системных состояний.
Клинические исследования
Возможное участие комплемента в пародонтите человека было впервые выявлено в 1970-х и 1980-х годах в результате гистологических и клинических исследований, посвященных анализу десневой трещинной жидкости (GCF) на здоровье и заболевания пародонта.GCF представляет собой воспалительный экссудат, который омывает десневую щель или карман, то есть пространство между свободной десной и поверхностью зубов (25). Было показано, что образцы GCF от пациентов с пародонтитом обладают комплемент-зависимой гемолитической активностью, что позволяет предположить, что в этом воспалительном экссудате присутствует функциональная система комплемента (26, 27). Было показано, что активированные фрагменты комплемента в большом количестве присутствуют в GCF от пациентов, но не обнаруживаются или присутствуют в более низких концентрациях в GCF от здоровых контрольных лиц (28–32).Точно так же компоненты комплемента и продукты расщепления также легко обнаруживались в хронически воспаленной десне, но не обнаруживались или были в меньшем количестве в образцах здоровых тканей; компоненты комплемента, обнаруженные в пораженной десне (а также в GCF), были репрезентативными для всего каскада (например, C1q, фактор B, Bb, C3, C3a, C3b, C3c, C3d, C4, C5, C5a, C5b, C9) ( 26–37).
Важно отметить, что пародонтальная терапия, которая привела к снижению клинических показателей воспаления пародонта и деструкции тканей, также привела к снижению активации C3 в GCF (38).И наоборот, прогрессирование воспаления десен во время экспериментального исследования гингивита у людей было связано с повышенным расщеплением C3 в GCF (32). В частности, это исследование изучало расщепление факторов B, C3 и C4 в GCF, собранных в течение экспериментального периода, и продемонстрировало, соответственно, их преобразование в Bb и C3c, но не в C4c, что подразумевает избирательную активацию альтернативного пути (32). Иммуногистохимическое исследование показало, что регулятор комплемента CD59 экспрессируется на более низких уровнях в деснах пациентов с пародонтитом по сравнению со здоровыми людьми, что может означать нарушение защиты тканей, пораженных пародонтитом, от MAC-опосредованного повреждения аутологичных тканей (35).
Более поздние исследования также подтверждают связь между комплементом и пародонтитом. Случай агрессивного пародонтита с тяжелым ангионевротическим отеком, локализованным в десне, был связан с нарушением регуляции функции комплемента, в частности с дефицитом ингибитора C1-эстеразы (C1INH) (39). Однонуклеотидный полиморфизм, влияющий на C5 (rs17611), который ранее был связан с повышенным содержанием C5 в сыворотке и восприимчивостью к фиброзу печени, ассоциированному с комплементом (40), был более распространен у пациентов с пародонтитом, чем у здоровых людей в контрольной группе (41). .Что касается его экспрессии, было показано, что C3 входит в 5% лучших генов, которые наиболее сильно подавляются после пародонтальной терапии (42). В другом исследовании использовалась интегративная приоритезация генов и базы данных из общегеномных ассоциативных исследований и экспериментов с микрочипами, и был идентифицирован C3 среди 21 наиболее многообещающих генов-кандидатов, участвующих в заболеваниях пародонта (43). Интересно, что частичная недостаточность гена C4 значительно чаще встречается у пациентов с пародонтитом, чем у здоровых людей (44).Это открытие может указывать на защитную функцию, связанную с C4, активация которой происходит через классический или лектиновый пути. Однако следует отметить, что недавно было показано, что C4a связывает и активирует рецепторы, активируемые протеазой (PAR) 1 и 4 (45), которые экспрессируются тромбоцитами и эндотелиальными клетками (46). Таким образом, эффекты, опосредованные C4, необязательно могут включать в себя запуск зависимых от C3 активностей ниже по течению. Может ли C4a опосредовать перекрестное взаимодействие комплемента с коагуляцией и / или системой эндотелиального барьера, в настоящее время неясно, как и влияние таких взаимодействий на периодонтит.
Вышеупомянутые клинические исследования в совокупности указывают на роль активации комплемента в патогенезе заболеваний пародонта. Однако коррелятивный характер этих исследований на людях не мог безопасно установить причинную связь между комплементом и пародонтитом и отличить ее от альтернативной возможности, что активация комплемента может быть просто маркером местного воспаления пародонта. Причинно-следственные доказательства были получены в результате механистических исследований на животных моделях, описанных ниже.
Механические исследования на моделях животных
Животные модели могут быть задействованы для определения причинных связей между потенциальными механизмами и патогенезом заболевания (47), тем самым не только продвигая знания о патогенезе, но также определяя терапевтические цели и прокладывая путь к клиническим испытаниям на людях. Поскольку запуск каскада комплемента переплетается с активацией TLR (3), эти две системы обсуждаются вместе в исследованиях, представленных здесь.
В ответ на микробную инфекцию или повреждение тканей комплемент и TLR быстро активируются, часто одними и теми же агонистами.В связи с этим бактериальный липополисахарид (LPS; агонист TLR4), грибной зимозан (агонист TLR2 / 6) и бактериальная ДНК CpG (агонист TLR9) не только индуцируют передачу сигналов TLR, но также могут активировать комплемент (48). Фактически, комплемент и TLR не только совместно активируются в ответ на микробную инфекцию и другие типы инсульта, такие как повреждение ткани, но они также участвуют во взаимодействиях перекрестных сигналов в нескольких типах миелоидных клеток (моноцитах, макрофагах, нейтрофилах и дендритных клетках). клетки) (49–54) (рис. 1).В новаторском исследовании различные агонисты TLR, систематически вводимые мышам, лишенным основного мембранного регулятора комплемента, фактора ускорения распада, индуцировали значительно более высокие уровни провоспалительных цитокинов в плазме, чем контроли дикого типа (55). Точно так же мыши, которым системно вводят совместно агонисты TLR (в частности, лиганды TLR2, TLR4 и TLR9) и мощный активатор комплемента (фактор яда кобры), демонстрируют чрезвычайно высокие уровни провоспалительных цитокинов в плазме (55). В перекрестном взаимодействии комплемента и TLR активированные сигнальные пути сходятся на митоген-активируемых протеинкиназах (регулируемые внеклеточными сигналами киназы-1 и-2 и N-концевые киназы c-Jun), которые, в свою очередь, активируют ключевые факторы транскрипции, а именно белок-активатор. -1 (AP-1) и ядерный фактор-κB (NF-κB) (55).Хотя эта синергия может укрепить врожденный иммунитет против инфекции, она также может способствовать деструктивным воспалительным реакциям.
В соответствии с этими данными, сопутствующая активация C5aR1 и TLR2 в десне мыши путем местного совместного введения специфических лигандов (C5a и Pam3Cys, соответственно) привела к индукции значительно более высоких уровней IL-1β, IL-6, IL-17 и TNF, чем стимуляция каждого рецептора по отдельности (56). Эти данные предполагают, что синергизм между комплементом и TLR может быть основным фактором индукции воспаления пародонта.В поддержку этого мнения, мыши, лишенные C5aR1, достаточно устойчивы к воспалительной потере костной массы независимо от присутствия TLR2 (57), и аналогичным образом мыши, лишенные TLR2, защищены от воспалительной потери костной массы независимо от присутствия C5aR1 (58). . Мыши с дефицитом TLR9 также защищены от экспериментального пародонтита (59), что, по крайней мере частично, можно отнести к синергии комплемента с TLR9 (55). В этих исследованиях использовалась модель пародонтита на мышах, в которой заболевание инициировалось дисбактериозом после перорального желудочного зондирования с ключевым патогеном Porphyromonas gingivalis (60, 61).В соответствии с важностью участия комплемента в патогенезе заболеваний пародонта, C3-дефицитные мыши были защищены от пародонтита в трех различных моделях: периодонтит, индуцированный лигатурой, периодонтит, индуцированный P. gingivalis , и пародонтит, связанный со старением (62). Модель лигатуры включает наложение шелковых лигатур вокруг коренных зубов, что приводит к массовому скоплению местных бактерий и индукции воспаления и потери альвеолярной кости у животных, свободных от специфических патогенов (но не свободных от микробов) (60, 63–65).В модели пародонтита, связанного со старением, воспаление пародонта и потеря костной массы развиваются естественным образом как функция старости, когда гомеостатические механизмы нарушаются (66–68). Интересно, что у мышей с дефицитом C3 также наблюдалось снижение бактериальной нагрузки на пародонт при пародонтите, вызванном P. gingivalis , по сравнению с контрольными однопометными животными дикого типа (62). Эти данные предполагают, что отсутствие активации комплемента не приводит к нарушению контроля над микробиотой пародонта и, более того, согласуются с концепцией, что деструктивное воспаление необходимо для поддержания количественно и композиционно измененной дисбиотической микробиоты (18).
Трансляционные доклинические исследования
Исследования, обсуждавшиеся ранее, показали, что комплемент может быть многообещающей мишенью для лечения пародонтита. Действительно, в модели пародонтита, индуцированного P. gingivalis через зонд, внутридесневая микроинъекция мышей дикого типа PMX-53, антагониста C5aR1 (69), подавляла индукцию воспалительных цитокинов (IL-1β, IL -6, IL-17 и TNF) в десневой ткани и ингибировал потерю альвеолярной кости (56). Этот защитный эффект проявляется, несмотря на присутствие интактного TLR2, иными словами, воспалительную потерю костной массы можно эффективно ингибировать, блокируя только один из двух перекрестных рецепторов (56).PMX-53 был также протестирован на модели пародонтита, вызванного лигатурой, где заболевание может быть инициировано независимо от P. gingivalis (63). Хотя значительная воспалительная потеря костной массы была индуцирована через 5 дней в лигированных областях мышей, получавших контрольную терапию, мыши, локально инъецированные (в лигированные участки) PMX-53, продемонстрировали значительную защиту от воспаления пародонта и потери костной массы (56). Крысы, получавшие PMX-205 [другой антагонист C5aR1 (70)] с питьевой водой, также были защищены от потери костной массы, вызванной лигатурой (71), хотя с меньшей эффективностью, возможно, из-за другого пути введения лекарства и / или использования разные виды животных.
Важно отметить, что одни и те же медиаторы воспаления (например, TNF, IL-1β, простагландин E2) участвуют в воспалительной потере пародонтальной костной массы у разных видов, таких как мыши, крысы, собаки, нечеловеческие приматы и люди. (72–77). Таким образом, мыши, по-видимому, являются полезной моделью пародонтита человека, особенно для механистических исследований, поскольку в настоящее время мыши представляют собой единственный доступный вид со спроектированными нокаутирующими или нокаутными мутациями для всей панели ключевых генов иммунного ответа.Однако многообещающие результаты, полученные на высших животных, таких как нечеловеческие приматы, увеличивают вероятность того, что лекарственные препараты-кандидаты могут иметь защитное действие и у людей. В этом отношении анатомия тканей пародонта и иммунная система приматов, отличных от человека, аналогичны таковым у людей, а пародонтит у обезьян проявляет клинические, микробиологические и иммуно-гистологические особенности, которые очень похожи на характеристики пародонтоза человека (78– 82). Фактически, использование приматов, не являющихся людьми, становится необходимым для тестирования лекарств, не обладающих специфичностью, для широко используемых моделей грызунов и других мелких животных.
В этом отношении компстатин и аналоги нового поколения представляют собой небольшие пептидные ингибиторы, обладающие исключительной специфичностью в отношении C3 человека и нечеловеческих приматов (83–85). Учитывая отсутствие доступных ингибиторов C3 у мышей, пригодность C3 в качестве терапевтической мишени при пародонтите можно было проверить только на приматах. В частности, аналог компстатина третьего поколения Cp40 был протестирован на яванских макаках ( Macaca fascicularis ) (62). Cp40 имеет субнаномолярное сродство к C3 (K D = 0.5 нМ; В 6000 раз больше, чем у исходного компстатина) и период полувыведения из плазмы человека (48 часов), который превосходит ожидания для большинства пептидных препаратов. Механически исходный компстатин и аналоги нового поколения связывают C3 и блокируют его взаимодействие с C3-конвертазой и расщепление ею на ее активные фрагменты, C3a и C3b (86) (рис. 2). Другими словами, семейство ингибиторов C3 компстатина защищает субстрат C3, а не мешает конвертазе C3. Как следствие, компстатины предотвращают распространение и усиление активации комплемента и генерацию эффекторных молекул независимо от механизма, инициировавшего активацию комплемента (83, 84).
Рисунок 2 . Модель активации С3 и его ингибирования компстатином. (вверху) Изображение ключевых белковых взаимодействий, приводящих к образованию конвертазы C3 на целевой поверхности (например, поверхности микробных клеток). Нативный C3 связывается с конвертазой (C3bBb) и расщепляется на ее активные фрагменты, C3a и C3b. (Внизу) Компстатин действует, блокируя межбелковое взаимодействие. В частности, компстатин связывает как нативный C3, так и C3b и стерически препятствует связыванию нативного C3 с помощью конвертаз C3, тем самым предотвращая расщепление C3 на его активные фрагменты.Из исх. 87. Используется с разрешения.
Пародонтит у взрослых обезьян cynomolgus индуцировали путем наложения шелковых лигатур вокруг задних зубов на обеих половинах нижней челюсти (нижняя челюсть) на период в 6 недель. Местное лечение (посредством внутридесневой инъекции) Cp40 началось через 3 дня после наложения лигатуры. Был применен экспериментальный план с разделенным ртом, при котором одну сторону обрабатывали Cp40, а другую — неактивным контрольным пептидом, таким образом, каждое животное служило отдельным контролем.Клиническое наблюдение за заболеванием осуществлялось путем анализа клинических показателей, оценивающих воспаление пародонта и деструкцию тканей (87). Лечение Cp40 привело к значительному снижению десневого индекса и потере клинического прикрепления, что коррелировало с более низкими уровнями провоспалительных и остеокластогенных цитокинов (например, TNF, IL-1β, IL-17 и RANKL) в GCF, а также со снижением количества остеокластов в биоптатах костей (62). В отличие от RANKL, содержание остеопротегерина (OPG), естественного ингибитора RANKL, в GCF поддерживалось на повышенных уровнях в Cp40-обработанных сайтах по сравнению с контрольными сайтами.Следовательно, Cp40, по-видимому, вызывает благоприятное изменение отношения RANKL / OPG, что является потенциальным индикатором периодонтита (88). В соответствии с этими данными рентгенологический анализ показал, что участки, обработанные Cp40, имели значительно меньшую потерю костной массы по сравнению с участками, обработанными контрольной группой (62).
Чтобы определить потенциальную полезность Cp40 в терапевтических условиях, препарат вводили взрослым макакам cynomolgus с уже существующим естественным хроническим периодонтитом (89). Животным локально вводили в десну Cp40 либо один раз в неделю (группа из 5 животных), либо три раза в неделю (группа из 10 животных) в течение 6-недельного периода лечения с последующим 6-недельным периодом наблюдения при отсутствии Лечение Cp40.Клинические исследования и сбор образцов GCF проводились на исходном уровне и на протяжении всего исследования. В обеих группах лечение Cp40 привело к значительному снижению клинических показателей, которые оценивают воспаление пародонта (индекс десен и кровотечение при зондировании), разрушение тканей (глубина кармана зондирования и потеря клинического прикрепления) или подвижность зубов, которая часто связана с потерей костной массы. Улучшение клинического состояния заболевания, что отражается в снижении клинических показателей, коррелировало со снижением уровней провоспалительных и остеокластогенных медиаторов (например,g., IL-17 и RANKL) в GCF и снижение количества остеокластов в костных биоптатах. Защитные эффекты, опосредованные Cp40, сохранялись, хотя и с меньшей эффективностью, в течение как минимум 6 недель после отмены препарата. Следовательно, Cp40 может обратить вспять ранее существовавшее хроническое воспаление пародонта без дополнительных методов лечения, таких как масштабирование и выравнивание корня (SRP) (89). Протеомный анализ образцов GCF, собранных в ходе этого исследования, показал участие как альтернативных, так и классических путей активации комплемента в естественном пародонтите приматов, кроме человека; однако альтернативный путь оказался наиболее богатым из всех биологических путей, выявленных с помощью анализа генной онтологии (90).Эти протеомные данные согласуются с ранними клиническими отчетами, показывающими, что альтернативный путь комплемента преимущественно активируется в образцах GCF от пациентов с пародонтитом человека, хотя классический путь также активирован (28, 29, 38). Исходя из этого соображения (и вероятности того, что углеводные или гликопротеиновые компоненты пародонтальных бактерий могут активировать лектиновый путь), сопутствующее ингибирование всех трех путей (как это может быть сделано с помощью Cp40), вероятно, обеспечит повышенную защиту от пародонтита по сравнению с ингибированием индивидуальные пути активации комплемента.Другой основной мишенью, выявленной с помощью протеомного фингерпринта образцов GCF из обработанных Cp40 NHP, была дегрануляция лейкоцитов. Нейтрофилы вызывают значительное повреждение тканей при пародонтите человека, в значительной степени за счет дегрануляции протеаз, разрушающих ткань, и цитотоксических молекул (76, 91–94). В этом отношении способность Cp40 подавлять экзоцитоз, вероятно, представляет собой еще один защитный механизм хозяина.
В последующем исследовании на яванских макаках с естественным хроническим периодонтитом было показано, что эффективная терапевтическая доза местного введенного Cp40 [100 мкг / участок; использованный в исследовании Maekawa et al.(89)] не вызывает местного раздражения и обладает долгосрочным защитным действием даже при нечастом приеме, например, один раз в 3 недели (95). Таким образом, взятые вместе, клинические наблюдения на людях и доклинические интервенционные исследования на приматах, кроме человека, предполагают, что комплемент чрезмерно активен при пародонтите и что ингибирование C3 с помощью Cp40 является многообещающей терапией модулирующей хозяина, которая требует исследования в качестве потенциального лечения пародонтита человека .
Учитывая потенциал синергизма между комплементом и TLR, ингибирование C3 при пародонтите также может ингибировать воспаление, которое активируется передачей сигналов TLR либо в ответ на микробные лиганды TLR (например,g., LPS, липопротеины и бактериальная ДНК) (96, 97) или в ответ на эндогенные лиганды TLR (например, бигликан, гиалуронан или фрагменты гепарансульфата), которые высвобождаются при повреждении ткани и действуют как связанные с опасностями молекулярные структуры ( DAMPs) (98, 99). Последнее предполагает, что ингибирование комплемента может также подавлять воспаление, вызванное поврежденной тканью, тем самым блокируя также прогрессирование периодонтита. Интересно, что несколько TLR (TLR2, TLR3, TLR4 и TLR9) при активации бактериальными молекулами или DAMP, высвобождаемыми из стрессированных / поврежденных тканей, индуцируют локальную экспрессию компонентов комплемента (например,g., продуцирование макрофагами факторов B и C3), тем самым дополнительно способствуя активности комплемента в воспалительной среде (100–103). Например, LPS индуцирует продукцию и высвобождение фактора B через путь TLR4-TRIF в макрофагах (100). Более того, передача сигналов TLR подавляет десенсибилизацию рецепторов, связанных с G-белком (GPCR), путем подавления экспрессии киназ, связанных с G-белком, рецепторов, необходимых для индукции фосфорилирования и интернализации GPCR (104). Это предполагает механизм, с помощью которого TLR могут потенциально продлевать активацию GPCR, таких как C3aR и C5aR1.Кроме того, индуцированные TLR цитокины, такие как IL-6, способствуют экспрессии C3aR и C5aR (105). Следовательно, TLR регулируют экспрессию факторов комплемента, а также экспрессию и активацию рецепторов комплемента, которые, как упоминалось ранее, в свою очередь, могут усиливать TLR-зависимые ответы. Эта провоспалительная и потенциально деструктивная петля прямой связи может быть нарушена ингибированием комплемента (рис. 3), идея, которая может лежать в основе успеха лечения Cp40 в доклинической модели приматов, не относящихся к человеку.Ингибирование комплемента на уровне C3 также может подавлять воспаление, зависимое от инфламмасомы, поскольку было показано, что пути комплемента (передача сигналов C3aR и комплекс сублитической мембранной атаки) способствуют активации инфламмасомы NLRP3 и высвобождению IL-1β (106, 107).
Рисунок 3 . Ингибирование, направленное на комплемент, блокирует порочный круг, связывающий деструктивное воспаление и дисбактериоз при пародонтите. Пародонтит вызван взаимно усиленным взаимодействием между дисбиотическими микробными сообществами и воспалением.В то время как дисбактериоз вызывает воспаление, благоприятная с точки зрения питания воспалительная среда является основным экологическим фактором, усугубляющим дисбактериоз. Исследования на различных доклинических моделях показали, что ингибирование комплемента устраняет перекрестную передачу сигналов комплемент-TLR и результирующее воспаление, тем самым разрывая порочный круг, провоцирующий заболевание, независимо от наличия интактной передачи сигналов TLR. Например, блокирование центрального компонента С3 комплемента с помощью пептидного соединения Cp40 / AMY-101 блокирует экспериментальный или естественный пародонтит у нечеловеческих приматов.
Безопасность и другие аспекты клинического использования
Учитывая участие дисбиотической микробиоты пародонта в патогенезе пародонтита, нацеливание на комплемент может не показаться интуитивно понятным терапевтическим вариантом для этого заболевания полости рта. В целом, потенциальное беспокойство относительно терапевтического использования ингибиторов комплемента заключается в том, может ли блокада комплемента подорвать эффективность противомикробной защиты хозяина и, таким образом, увеличить риск инфекции.Хотя эта возможность не может быть проблемой при острых состояниях, требующих временного ингибирования комплемента [например, при гемодиализе (108)], ее следует тщательно рассматривать в условиях, которые потребуют длительного применения ингибиторов комплемента. В этом отношении люди с первичной недостаточностью C3 имеют повышенный риск определенных инфекций (например, Neisseria meningitidis и Streptococcus pneumoniae ), хотя эта повышенная восприимчивость, по-видимому, снижается во взрослом возрасте, предположительно из-за развития компенсаторных защитных механизмов (109–109). 111).Текущий опыт применения одобренных FDA препаратов против комплемента, таких как экулизумаб, блокирующий активацию C5, показывает, что иммунизация против инкапсулированных бактерий (таких как менингококки) может в значительной степени снизить инфекционные риски. Следовательно, вакцинация, а также профилактическое использование антибиотиков могут быть включены, чтобы обеспечить безопасное использование ингибиторов комплемента в хронических условиях. Важно отметить, что в случаях ингибирования комплемента низкомолекулярными ингибиторами, такими как компстатин, при необходимости соединение может быть более легко выведено из употребления (чем, например, антитело), что обеспечивает быстрое восстановление комплемент-зависимых антимикробных функций.Важно отметить, что мониторинг приматов, не относящихся к человеку, при длительном (до 3 месяцев) системном лечении Cp40 не выявил значительных различий в биохимических, гематологических или иммунологических параметрах их крови или тканей по сравнению с таковыми у контрольных животных, получавших только носитель, несмотря на то, что полное ингибирование С3 в плазме. Интересно, что раны, нанесенные на коже животных, получавших Cp40, не проявляли никаких признаков инфекции, а скорее демонстрировали тенденцию к более быстрому заживлению ран по сравнению с контрольными животными, получавшими носитель (112).Этот результат согласуется с более ранними наблюдениями на мышах, у которых дефицит C3 приводил к более быстрому заживлению кожных ран по сравнению с контрольными мышами с достаточным уровнем C3 (113).
Несмотря на то, что пародонтит является хроническим заболеванием, он является местным воспалительным заболеванием, и поэтому его можно лечить с помощью местного ингибирования комплемента, что намного безопаснее, чем системное введение того же ингибитора. Системное воздействие ингибиторов комплемента после местной инъекции в ткани пародонта должно быть незначительным и, таким образом, не должно снижать активность комплемента в кровообращении или других тканях.Это представление можно проиллюстрировать на примере Cp40. Поскольку C3 является наиболее распространенным белком системы комплемента в крови (от 1,0 до 1,5 мг / мл), небольшие количества вводимого локально Cp40, который может «ускользнуть» из тканей пародонта, должны легко связываться избытком C3 в крови, следовательно, не достигать другие ткани в активных (ингибирующих) концентрациях. В схеме лечения, использованной в описанном выше исследовании NHP Maekawa et al. (89) всего вводили 1,5 мг Cp40 (15 сайтов по 100 мкг / сайт).Даже если бы полную местную дозу вводить системно, это привело бы только к количеству 0,2–0,3 мг / кг массы тела у нечеловеческих приматов (0,02–0,03 мг / кг массы тела у людей), тогда как системная доза Cp40 составила бы 1-2 мг / кг массы тела необходимо для надежного достижения целевых уровней лекарственного средства у нечеловеческих приматов (114).
Даже на местном уровне подавление комплемента вряд ли приведет к нарушению контроля микробиоты, связанной с пародонтитом. Как обсуждалось выше, у мышей с дефицитом C3 бактериальная нагрузка на пародонт снизилась по сравнению с контрольной группой с достаточным содержанием C3 во время экспериментального периодонтита (62).Эти данные согласуются с представлением о том, что воспаление является экологической причиной дисбактериоза при пародонтите (рис. 3). Действительно, деструктивное воспаление пародонта вызывает образование продуктов распада тканей (таких как деградированные пептиды коллагена или гемсодержащие соединения), которые используются в качестве источника питательных веществ подмножеством видов бактерий, связанных с дисбиозом; в основном это протеолитические / асахаролитические организмы с механизмами усвоения железа и / или они могут процветать за счет использования других побочных продуктов воспаления, таких как нитрат для анаэробного дыхания, тем самым превосходя бактерии, связанные со здоровьем, и усугубляя дисбактериоз (18, 115, 116).Следовательно, ингибирование комплемента с помощью Cp40 может не просто подавлять воспаление, но может дополнительно препятствовать росту дисбиотической микробиоты (рис. 3). Экспериментальная поддержка идеи о том, что противовоспалительные подходы могут иметь непрямой антимикробный эффект, была получена на моделях пародонтита на мышах и кроликах, где контроль воспаления не только защищал от болезни, но также снижал бактериальную нагрузку и обращал дисбактериоз (76, 77, 117–119). Напротив, и в соответствии с предыдущим утверждением, бактериальная биомасса биопленок, связанных с пародонтитом человека, увеличивается с увеличением клинического воспаления (120).
Выводы и перспективы
Исследования, обсужденные выше, предполагают клиническую ценность ингибирования всех трех основных путей активации комплемента при пародонтите, что может быть достигнуто путем воздействия на центральный компонент C3. Ингибирование C3 может напрямую подавлять воспаление и косвенно противодействовать дисбактериозу. Безопасность и эффективность Cp40 при пародонтите приматов, кроме человека (62, 89, 95), открывают путь к клиническим испытаниям для лечения пародонтита человека. С этой целью аспекты, которые необходимо учитывать, включают вопросы, касающиеся частоты введения, дозирования и выбора тех пациентов, которым такое лечение принесет наибольшую пользу.Несмотря на то, что Cp40 был успешно протестирован в качестве самостоятельного средства для лечения как индуцированного, так и естественного пародонтита у обезьян, препарат с большей вероятностью будет использоваться в качестве дополнительной терапии при лечении заболеваний пародонта человека. В будущих клинических испытаниях можно будет изучить комбинированный потенциал Cp40 и SRP для лечения воспаления пародонта и подавления потери костной массы по сравнению с одним SRP. В очень тяжелых случаях пародонтита комбинированную терапию Cp40 и SRP можно сравнить с хирургией пародонта, чтобы определить, может ли лечение Cp40 / SRP устранить необходимость хирургического вмешательства.Следует отметить, что лечение на основе Cp40 (и вмешательства по модуляции хозяина в целом) не обязательно может применяться в терапевтических условиях, но также и в профилактических целях (до начала пародонтита) к пациентам с высоким риском, таким как сигареты. курильщики и пациенты с диабетом (121–123).
Защитные эффекты Cp40 при пародонтите приматов, отличных от человека, сохраняются в течение многих недель после отмены препарата у обработанных обезьян (89, 95). Это обнадеживающее открытие, хотя оптимальную частоту введения Cp40 для длительного лечения пародонтита у человека, возможно, придется определять эмпирически.Уникальные фармакокинетические свойства Cp40, описанные ранее, согласуются с моделью «управляемой мишенью», где за начальным быстрым клиренсом избыточного свободного пептида (т.е. не связанного C3) следует медленный клиренс C3-связанного пептида. Таким образом, тесное связывание Cp40 с C3, по-видимому, замедляет его клиренс, и, действительно, определенные значения периода полужизни различных аналогов компстатина коррелируют с их аффинностью связывания C3 (85). Точно так же сильное связывание Cp40 с обильным C3 в воспаленной ткани пародонта может способствовать замедлению выведения лекарственного средства из ткани, тем самым способствуя устойчивой защите от воспаления пародонта.Более того, способность Cp40 останавливать воспаление и, предположительно, обращать вспять дисбиоз может сбрасывать баланс в сторону тканевого гомеостаза, который сам по себе (несмотря на отсутствие лекарства) может устойчиво подавлять или задерживать повторение патологических процессов.
Amyndas Pharmaceuticals разрабатывает Cp40, непегилированный аналог компстатина третьего поколения, в качестве клинического кандидата на лекарство AMY-101. AMY-101 разработан для терапевтических вмешательств при гломерулопатии C3 (C3G), осложнениях ABO-несовместимой трансплантации почки, пароксизмальной ночной гемоглобинурии (PNH) и заболеваниях пародонта (124, 125).Пегилированная версия более раннего аналога компстатина, POT-4/4 (1MeW) (APL-2, Apellis Pharmaceuticals), клинически разработана для использования при опосредованных комплементом расстройствах, включая возрастную дегенерацию желтого пятна и ПНГ. В исследовании фазы II было показано, что длительное лечение APL-2 безопасно и снижает скорость роста географической атрофии, связанной с возрастной дегенерацией желтого пятна. AMY-101 получил статус орфанного препарата для C3G и PNH от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и Европейского агентства по лекарственным средствам (EMA) в 2016 году, а недавно, в 2017 году, успешно завершил фазу I испытания безопасности (125, 126 ).Целенаправленные модификации N — и C -конца Cp40 / AMY-101 привели к серии компстатинов четвертого поколения с более высокой растворимостью, улучшенными PK-профилями, что расширило спектр путей введения и, вероятно, снизило частоту дозирования. этих пептидных препаратов в хронических режимах (127). В целом, более 20 лекарственных препаратов-кандидатов, нацеленных на комплемент, которые ингибируют отдельные точки каскада, в настоящее время проходят клинические испытания при различных воспалительных и дегенеративных заболеваниях (125).Документированная безопасность Cp40 / AMY-101 и его защитные эффекты в очень актуальных доклинических моделях пародонтита заслуживают изучения в будущих клинических испытаниях для лечения пародонтита у людей.
Взносы авторов
GH и JL: концептуализация; GH: первоначальный черновик. Все перечисленные авторы внесли значительный интеллектуальный вклад в рукопись, отредактировали и одобрили ее для публикации.
Заявление о конфликте интересов
JL является основателем Amyndas Pharmaceuticals, которая разрабатывает ингибиторы комплемента (включая аналоги компстатина третьего поколения, такие как AMY-101).JL и GH являются авторами патентов или патентных заявок, описывающих использование ингибиторов комплемента в терапевтических целях, некоторые из которых разработаны Amyndas Pharmaceuticals. JL также является изобретателем технологии компстатина, лицензированной для Apellis Pharmaceuticals [т.е. 4 (1MeW) 7W / POT-4 / APL-1 и ПЭГилированные производные].
Остальные авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Авторы поддерживаются грантами Национальных институтов здравоохранения США (AI068730 и AI030040 для JL; DE015254, DE021685 и DE024716 для GH) и Европейской комиссии (FP7-DIREKT 602699 для JL).
Список литературы
3. Hajishengallis G, Lambris JD. Больше, чем дополнительные потери: синергия рецепторов, подобных комплементу, и перекрестные помехи в врожденном иммунитете и воспалении. Immunol Rev. (2016) 274: 233–44. DOI: 10.1111 / imr.12467
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Рейс Е.С., Мастеллос, округ Колумбия, Риклин Д., Мантовани А., Ламбрис Дж. Д.. Комплемент при раке: распутывание запутанных отношений. Nat Rev Immunol. (2018) 18: 5–18. DOI: 10.1038 / н.в.2017.97
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Хаджишенгаллис Г., Абэ Т., Маэкава Т., Хаджишенгаллис Э., Ламбрис Дж. Д.. Роль комплемента в гомеостазе пародонта микробами-хозяевами. Semin Immunol. (2013) 25: 65–72. DOI: 10.1016 / j.smim.2013.04.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Eke PI, Dye BA, Wei L, Slade GD, Thornton-Evans GO, Borgnakke WS и др. Обновленная информация о распространенности пародонтита у взрослых в США: NHANES с 2009 по 2012 год. J Periodontol. (2015) 86: 611–22. DOI: 10.1902 / jop.2015.140520
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11. Кассебаум, штат Нью-Джерси, Бернабе Э., Дахия М., Бхандари Б., Мюррей С.Дж., Марсенс В.Глобальное бремя тяжелого пародонтита в 1990–2010 гг .: систематический обзор и мета-регресс. J Dent Res. (2014) 93: 1045–53. DOI: 10.1177 / 0022034514552491
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Диас П.И., Хоар А., Хонг Б.А. Изменения поддесневого микробиома и динамика сообществ при заболеваниях пародонта. J Calif Dent Assoc. (2016) 44: 421–35.
PubMed Аннотация | Google Scholar
16. Hajishengallis G, Korostoff JM.Возвращаясь к модели Пейджа и Шредера: положительное, отрицательное и неизвестное в реакции хозяина пародонта 40 лет спустя. Periodontol 2000. (2017) 75: 116–51. DOI: 10.1111 / prd.12181
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Коломбо А. П., Беннет С., Коттон С. Л., Гудсон Дж. М., Кент Р., Хаффаджи А. Д. и др. Влияние пародонтальной терапии на поддесневую микробиоту тяжелого пародонтита: сравнение пациентов с хорошим ответом и пациентов с рефрактерным пародонтитом с использованием микроматрицы для идентификации микробов полости рта человека. J Periodontol. (2012) 83: 1279–87. DOI: 10.1902 / jop.2012.110566
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Тонетти М.С., Чаппл, Иллинойс, Рабочая группа 3 седьмого Европейского семинара по П. Биологические подходы к разработке новых пародонтологических методов лечения — консенсус седьмого Европейского семинара по пародонтологии. J Clin Periodontol. (2011) 38Приложение 11: 114–8. DOI: 10.1111 / j.1600-051X.2010.01675.x
CrossRef Полный текст | Google Scholar
23.Бейклер Т., Флеммиг Т.Ф. Заболевания, связанные с биопленкой полости рта: тенденции и последствия для качества жизни, системного здоровья и расходов. Periodontol 2000. (2011) 55: 87–103. DOI: 10.1111 / j.1600-0757.2010.00360.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Петерсен П.Е., Огава Х. Глобальное бремя заболеваний пародонта: к интеграции с профилактикой и контролем хронических заболеваний. Periodontol 2000. (2012) 60: 15–39. DOI: 10.1111 / j.1600-0757.2011.00425.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Ламстер И.Б., Ало Дж. К.. Анализ десневой десневой жидкости применительно к диагностике заболеваний полости рта и системных заболеваний. Ann N Y Acad Sci. (2007) 1098: 216–29. DOI: 10.1196 / анналы.1384.027
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26. Суды FJ, Boackle RJ, Fudenberg HH, Silverman MS. Обнаружение функциональных компонентов комплемента в десневой щели у людей с заболеваниями пародонта. J Dent Res. (1977) 56: 327–31. DOI: 10.1177 / 00220345770560032001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27. Boackle RJ. Взаимодействие слюнных выделений с системой комплемента человека — модель для изучения систем защиты хозяина на воспаленных поверхностях слизистой оболочки. Crit Rev Oral Biol Med. (1991) 2: 355–67. DOI: 10.1177 / 104544110030401
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28.Attstrom R, Laurel AB, Lahsson U, Sjoholm A. Факторы дополнения в материале десневой щели из здоровой и воспаленной десны у людей. J Periodont Res. (1975) 10: 19–27. DOI: 10.1111 / j.1600-0765.1975.tb00003.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Schenkein HA, Genco RJ. Десневая жидкость и сыворотка при заболеваниях пародонта. II. доказательства расщепления компонентов комплемента C3, проактиватора C3 (фактор B) и C4 в десневой жидкости. J Periodontol. (1977) 48: 778–84. DOI: 10.1902 / jop.1977.48.12.778
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Schenkein HA, Genco RJ. Десневая жидкость и сыворотка при заболеваниях пародонта. я. количественное исследование иммуноглобулинов, компонентов комплемента и других белков плазмы. J Periodontol. (1977) 48: 772–7. DOI: 10.1902 / jop.1977.48.12.772
PubMed Аннотация | CrossRef Полный текст | Google Scholar
31. Challacombe SJ, Shirlaw PJ.Иммунология заболеваний полости рта. В: Mestecky J, Lamm ME, Strober W, Bienenstock J, McGhee JR, Mayer L, редакторы. Иммунология слизистой оболочки. Elsevier Academic Press (2005). п. 1517–46.
Google Scholar
32. Паттерс М.Р., Ниекраш CE, Lang NP. Оценка расщепления комплемента в десневой жидкости при экспериментальном гингивите у человека. J Clin Periodontol. (1989) 16: 33–7. DOI: 10.1111 / j.1600-051X.1989.tb01609.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
34.Николопулу-Папаконстантину А.А., Йоханнесен А.С., Кристофферсен Т. Отложения иммуноглобулинов, комплемента и иммунных комплексов в воспаленной десне человека. Acta Odontol Scand. (1987) 45: 187–93. DOI: 10.3109 / 0001635870
58
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35. Rautemaa R, Meri S. Защита эпителия десен от комплемент-опосредованного повреждения за счет сильной экспрессии протектина, ингибитора комплекса атаки на мембрану (CD59). J Dent Res. (1996) 75: 568–74. DOI: 10.1177 / 00220345960750010901
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36. Schenkein HA, Genco RJ. Продукты расщепления комплемента в воспалительных экссудатах пациентов с заболеваниями пародонта. J Immunol. (1978) 120: 1796.
Google Scholar
37. Лалли Е.Т., МакАртур В.П., Баэни ПК. Биосинтез компонентов комплемента в хронически воспаленной десне. J Periodontal Res. (1982) 17: 257–62.DOI: 10.1111 / j.1600-0765.1982.tb01152.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Ниекраш CE, Patters MR. Одновременная оценка компонентов комплемента C3, C4 и B и продуктов их расщепления в десневой жидкости человека. II. продольные изменения при пародонтологической терапии. J Periodontal Res. (1985) 20: 268–75. DOI: 10.1111 / j.1600-0765.1985.tb00434.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39.Робертс А., Шах М., Чаппл Иллинойс. Дисфункция ингибитора С-1 эстеразы, локализованная в тканях пародонта: ключ к разгадке роли стресса в патогенезе хронического пародонтита? J Clin Periodontol. (2003) 30: 271–7. DOI: 10.1034 / j.1600-051X.2003.01266.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
40. Хиллебрандт С., Васмут Х.Э., Вайскирхен Р., Хеллербранд С., Кеппелер Х., Верт А. и др. Фактор комплемента 5 — это ген количественного признака, который изменяет фиброгенез печени у мышей и людей. Nat Genet. (2005) 37: 835–43. DOI: 10,1038 / ng1599
PubMed Аннотация | CrossRef Полный текст | Google Scholar
41. Чай Л., Сон И-Кью, Зи К. И, Люн В.К. Однонуклеотидный полиморфизм компонента 5 комплемента и периодонтит. J Periodont Res. (2010) 45: 301–8. DOI: 10.1111 / j.1600-0765.2009.01234.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Zhan Y, Zhang R, Lv H, Song X, Xu X, Chai L, et al. Приоритезация генов-кандидатов на периодонтит с использованием нескольких вычислительных инструментов. J Periodontol. (2014) 85: 1059–69. DOI: 10.1902 / jop.2014.130523
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44. Сеппанен М., Локки М.Л., Ноткола И.Л., Маттила К., Валтонен В., Ниеминен А. и др. Аллели комплемента и нуль c4 при тяжелом хроническом пародонтите у взрослых. Scand J Immunol. (2007) 65: 176–81. DOI: 10.1111 / j.1365-3083.2006.01886.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
45. Ван Х, Риклин Д., Ламбрис Дж. Д..Фрагмент активации комплемента C4a опосредует эффекторные функции путем связывания в качестве свободного агониста с рецепторами 1 и 4, активируемыми протеазой. Proc Natl Acad Sci USA. (2017) 114: 10948–53. DOI: 10.1073 / pnas.1707364114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
46. Roumenina LT, Rayes J, Frimat M, Fremeaux-Bacchi V. Эндотелиальные клетки: источник, барьер и цель защитных медиаторов. Immunol Rev. (2016) 274: 307–29. DOI: 10.1111 / imr.12479
PubMed Аннотация | CrossRef Полный текст | Google Scholar
47.Hajishengallis G, Lamont RJ, Graves DT. Неизменная важность животных моделей в понимании заболеваний пародонта. Вирулентность. (2015) 6: 229–35. DOI: 10.4161 / 21505594.2014.9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Сеу В., Лим Дж., Айер А., Суен Дж. Й., Ариффин Дж. К., Хоэнхаус Д. М. и др. Воспалительные реакции, индуцированные липополисахаридом, усиливаются в первичных моноцитах человека, но подавляются в макрофагах белком комплемента C5a. J Immunol. (2013) 191: 4308–16. DOI: 10.4049 / jimmunol.1301355
PubMed Аннотация | CrossRef Полный текст | Google Scholar
50. Фанг Ц., Чжан Икс, Мива Т., Сун В. Комплемент способствует развитию воспалительных клеток Т-хелперов 17 за счет синергетического взаимодействия с передачей сигналов Toll-подобного рецептора и продукции интерлейкина-6. Кровь. (2009) 114: 1005–15. DOI: 10.1182 / кровь-2009-01-198283
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51.Маэкава Т., Краусс Дж. Л., Абэ Т., Джотвани Р., Триантафилу М., Триантафилу К. и др. Porphyromonas gingivalis манипулирует передачей сигналов комплемента и TLR, чтобы отделить бактериальный клиренс от воспаления и способствовать дисбактериозу. Клеточный микроб-хозяин. (2014) 15: 768–78. DOI: 10.1016 / j.chom.2014.05.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
52. Заал А., Лиссенберг-Тунниссен С.Н., ван Шейндел Г., Воутерс Д., Ван Хэм С.М., тен Бринке А. Перекрестные помехи между толл-подобными рецепторами и рецептором C5a в человеческих ДК, происходящих из моноцитов, подавляют продукцию воспалительных цитокинов. Иммунобиология. (2013) 218: 175–80. DOI: 10.1016 / j.imbio.2012.02.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
53. Босманн М., Сарма СП, Атефи Г., Зетун Ф.С., Уорд, Пенсильвания. Доказательства противовоспалительного действия C5a на врожденную ось IL-17A / IL-23. FASEB J. (2011) 26: 1640–51. DOI: 10.1096 / fj.11-199216
PubMed Аннотация | CrossRef Полный текст | Google Scholar
54. Ямада М., Оритани К., Кайсё Т., Исикава Дж., Йошида Х., Такахаши И. и др.Комплемент C1q регулирует LPS-индуцированную продукцию цитокинов в дендритных клетках костного мозга. евро J Immunol. (2004) 34: 221–30. DOI: 10.1002 / eji.200324026
PubMed Аннотация | CrossRef Полный текст | Google Scholar
55. Zhang X, Kimura Y, Fang C, Zhou L, Sfyroera G, Lambris JD, et al. Регуляция воспалительного ответа, опосредованного толл-подобными рецепторами, с помощью комплемента in vivo . Кровь. (2007) 110: 228–36 DOI: 10.1182 / blood-2006-12-063636
PubMed Аннотация | CrossRef Полный текст | Google Scholar
56.Абэ Т., Хосур К.Б., Хаджишенгаллис Э., Рейс Э.С., Риклин Д., Ламбрис Д.Д. и др. Вмешательство при пародонтите, направленное на местный комплемент: доказательство концепции с использованием антагониста рецептора C5a (CD88). J Immunol. (2012) 189: 5442–8. DOI: 10.4049 / jimmunol.1202339
PubMed Аннотация | CrossRef Полный текст | Google Scholar
57. Лян С., Краусс Дж.Л., Домон Х., Макинтош М.Л., Хосур К.Б., Ку Х. и др. Рецептор C5a нарушает зависимый от IL-12 клиренс Porphyromonas gingivalis и необходим для индукции потери костной ткани пародонта. J Immunol. (2011) 186: 869–77. DOI: 10.4049 / jimmunol.1003252
PubMed Аннотация | CrossRef Полный текст | Google Scholar
58. Burns E, Bachrach G, Shapira L, Nussbaum G. Передний край: TLR2 необходим для врожденного ответа на Porphyromonas gingivalis : активация приводит к персистенции бактерий, а дефицит TLR2 ослабляет индуцированную резорбцию альвеолярной кости. J Immunol. (2006) 177: 8296–300. DOI: 10.4049 / jimmunol.177.12.8296
PubMed Аннотация | CrossRef Полный текст | Google Scholar
59.Kim PD, Xia-Juan X, Crump KE, Abe T., Hajishengallis G, Sahingur SE. Воспаление, опосредованное Toll-подобным рецептором 9, вызывает потерю альвеолярной кости при экспериментальном периодонтите мышей. Infect Immun. (2015) 83: 2992–3002. DOI: 10.1128 / IAI.00424-15
PubMed Аннотация | CrossRef Полный текст | Google Scholar
60. Graves DT, Fine D, Teng YT, Van Dyke TE, Hajishengallis G. Использование моделей на грызунах для исследования взаимодействий бактерий-хозяев, связанных с заболеваниями пародонта. J Clin Periodontol. (2008) 35: 89–105. DOI: 10.1111 / j.1600-051X.2007.01172.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
61. Хаджишенгаллис Г., Лян С., Пейн М.А., Хашим А., Джотвани Р., Эскан М.А. и др. Малочисленные виды биопленок организуют воспалительные заболевания пародонта через комменсальную микробиоту и комплемент. Клеточный микроб-хозяин. (2011) 10: 497–506. DOI: 10.1016 / j.chom.2011.10.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
62.Маэкава Т., Абэ Т., Хаджишенгаллис Э., Хосур К.Б., ДеАнгелис Р.А., Риклин Д. и др. Генетические и интервенционные исследования показывают, что комплемент C3 является основной мишенью для лечения пародонтита. J Immunol. (2014) 192 6020–7. DOI: 10.4049 / jimmunol.1400569
PubMed Аннотация | CrossRef Полный текст | Google Scholar
64. Цзяо Ю., Дарзи Ю., Таварацумида К., Марчезан Дж. Т., Хасегава М., Мун Н. и др. Индукция потери костной массы с помощью патобионт-опосредованной передачи сигналов nod1 в полости рта. Клеточный микроб-хозяин. (2013) 13: 595–601. DOI: 10.1016 / j.chom.2013.04.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
65. Ровин С., Костич Е.Р., Гордон Х.А. Влияние бактерий и раздражения на возникновение заболеваний пародонта у стерильных и обычных крыс. J Periodontal Res. (1966) 1: 193–204. DOI: 10.1111 / j.1600-0765.1966.tb01860.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
67.Эскан М.А., Хаджишенгаллис Г., Кинан Д.Ф. Дифференциальная активация эпителиальных клеток и моноцитов десен человека фимбриями Porphyromonas gingivalis . Infect Immun. (2007) 75: 892–8. DOI: 10.1128 / IAI.01604-06
PubMed Аннотация | CrossRef Полный текст | Google Scholar
70. Delisle Milton RC, Milton SC, Chamberlin AR. Улучшение твердофазного синтеза fmoc антагониста C5a циклического гексапептида, PMX205. Int J Pept Res Ther. (2011) 17: 337–42.DOI: 10.1007 / s10989-011-9273-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
71. Брейвик Т., Гундерсен Ю., Гьермо П., Тейлор С.М., Вудрафф Т.М., Опстад П.К. Пероральное лечение антагонистами рецептора фактора комплемента C5a (CD88) подавляет экспериментальный пародонтит у крыс. J Periodontal Res. (2011) 46: 643–7. DOI: 10.1111 / j.1600-0765.2011.01383.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
72. Ассума Р., Оутс Т., Кокран Д., Амар С., Грейвс Д.Т.Антагонисты IL-1 и TNF подавляют воспалительную реакцию и потерю костной массы при экспериментальном пародонтите. J Immunol. (1998) 160: 403–9.
PubMed Аннотация | Google Scholar
75. Glowacki AJ, Yoshizawa S, Jhunjhunwala S, Vieira AE, Garlet GP, Sfeir C, et al. Профилактика опосредованной воспалением потери костной массы при пародонтозе мышей и собак путем привлечения регуляторных лимфоцитов. Proc Natl Acad Sci USA. (2013) 110: 18525–30. DOI: 10,1073 / PNAS.1302829110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
76. Эскан М.А., Джотвани Р., Абэ Т., Чмелар Дж., Лим Дж. Х., Лян С. и др. Антагонист интегрина лейкоцитов Del-1 ингибирует опосредованную IL-17 воспалительную потерю костной массы. Nat Immunol. (2012) 13: 465–73. DOI: 10.1038 / ni.2260
PubMed Аннотация | CrossRef Полный текст | Google Scholar
77. Мутсопулос Н.М., Конкель Дж., Сармади М., Эскан М.А., Уайлд Т., Дутзан Н. и др. Нарушение рекрутирования нейтрофилов при болезни типа I с дефицитом адгезии лейкоцитов вызывает локальную воспалительную потерю костной ткани, вызванную IL-17. Sci Transl Med. (2014) 6: 229ra40. DOI: 10.1126 / scitranslmed.3007696
PubMed Аннотация | CrossRef Полный текст | Google Scholar
78. Brecx MC, Налбандян Дж., Ооя К., Корнман К.С., Робертсон ПБ. Морфологические исследования заболеваний пародонта у яванских макак. II. Наблюдения под световым микроскопом пародонтита, вызванного лигатурой. J Periodontal Res. (1985) 20: 165–75. DOI: 10.1111 / j.1600-0765.1985.tb00423.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
79.Страница RC, Schroeder HE. Пародонтит у человека и других животных — сравнительный обзор. Базель: Каргер (1982).
Google Scholar
80. Корнман К.С., Холт С.К., Робертсон ПБ. Микробиология пародонтита, вызванного лигатурой, у яванского макака. J Periodontal Res. (1981) 16: 363–71. DOI: 10.1111 / j.1600-0765.1981.tb00987.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
81. Эберсол Дж. Л., Киракоду С., Новак М. Дж., Стромберг А. Дж., Шен С., Оррака Л. и др.Профили экспрессии генов цитокинов во время инициации, прогрессирования и разрешения пародонтита. J Clin Periodontol. (2014) 41: 853–61. DOI: 10.1111 / jcpe.12286
PubMed Аннотация | CrossRef Полный текст | Google Scholar
82. Эберсол Дж. Л., Капелли Д., Матис Э. К., Штеффен М. Дж., Зингер Р. Э., Монтгомери М. и др. Пародонтит у людей и приматов: орально-системная связь, индуцирующая белки острой фазы. Ann Periodontol. (2002) 7: 102–11. DOI: 10.1902 / annals.2002.7.1.102
PubMed Аннотация | CrossRef Полный текст | Google Scholar
84. Мастеллос, округ Колумбия, Янкопулу Д., Коккинос П., Хубер-Ланг М., Хаджишенгаллис Г., Бигларния АР и др. Компстатин: ингибитор комплемента, нацеленный на C3, наиболее эффективен для лечения у постели больного. евро J Clin Invest. (2015) 45: 423–40. DOI: 10.1111 / eci.12419
PubMed Аннотация | CrossRef Полный текст | Google Scholar
85. Ку Х., Риклин Д., Бай Х., Чен Х., Рейс Е.С., Мацеевски М. и др.Новые аналоги клинического ингибитора компстатина с субнаномолярным сродством и улучшенными фармакокинетическими свойствами. Иммунобиология. (2013) 218: 496–505. DOI: 10.1016 / j.imbio.2012.06.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
86. Janssen BJ, Halff EF, Lambris JD, Gros P. Структура компстатина в комплексе с компонентом комплемента C3c раскрывает новый механизм ингибирования комплемента. J Biol Chem. (2007) 282: 29241–7.DOI: 10.1074 / jbc.M704587200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
89. Маэкава Т., Брионес Р.А., Ресуэлло Р.Р., Туплано СП, Хаджишенгаллис Э., Кадзикава Т. и др. Ингибирование ранее существовавшего естественного пародонтита у нечеловеческих приматов с помощью местного введенного пептидного ингибитора комплемента С3. J Clin Periodontol. (2016) 43: 238–49. DOI: 10.1111 / jcpe.12507
PubMed Аннотация | CrossRef Полный текст | Google Scholar
90. Bostanci N, Bao K, Li X, Maekawa T., Grossmann J, Panse C, et al.Динамика десневого экссудатома предполагает ингибирование альтернативного пути комплемента в защитном действии ингибитора C3 Cp40 при пародонтите приматов, отличных от человека. J Prot Res. (2018) 17: 3153–75. DOI: 10.1021 / acs.jproteome.8b00263
CrossRef Полный текст | Google Scholar
91. Хаджишенгаллис Г., Мутсопулос Н.М., Хаджишенгаллис Э., Чавакис Т. Иммунные и регуляторные функции нейтрофилов при воспалительной потере костной массы. Semin Immunol. (2016) 28: 146–58.DOI: 10.1016 / j.smim.2016.02.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
92. Чаппл, Иллинойс, Мэтьюз Дж. Б.. Роль активных форм кислорода и антиоксидантов в разрушении тканей пародонта. Periodontol 2000. (2007) 43: 160–232. DOI: 10.1111 / j.1600-0757.2006.00178.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
93. Sima C, Glogauer M. Дисфункция нейтрофилов и восприимчивость хозяина к воспалению пародонта: текущее состояние знаний. Curr Oral Health Rep. (2014) 1: 95–103. DOI: 10.1007 / s40496-014-0015-x
CrossRef Полный текст | Google Scholar
94. Dutzan N, Kajikawa T., Abusleme L, Greewell-Wild T, Zuazo CE, Ikeuchi T, et al. Дисбиотический микробиом запускает клетки Th27, чтобы опосредовать иммунопатологию слизистой оболочки полости рта у мышей и людей. Sci Transl Med. (2018) 10: eaat0797. DOI: 10.1126 / scitranslmed.aat0797
PubMed Аннотация | CrossRef Полный текст | Google Scholar
95.Кадзикава Т., Брионес Р.А., Ресуэло РРГ, Туплано СП, Рейс Э.С., Хаджишенгаллис Э. и др. Безопасность и эффективность ингибитора комплемента AMY-101 на естественной модели пародонтита у нечеловеческих приматов. Mol Ther Methods Clin Dev. (2017) 6: 207–15. DOI: 10.1016 / j.omtm.2017.08.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
99. Шефер Л. Молекулы внеклеточного матрикса: сигналы эндогенной опасности как новые мишени для лекарств при заболеваниях почек. Curr Opin Pharmacol. (2010) 10: 185–90. DOI: 10.1016 / j.coph.2009.11.007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
100. Kaczorowski DJ, Afrazi A, Scott MJ, Kwak JH, Gill R, Edmonds RD, et al. Важнейший прогресс: лиганды рецептора распознавания образов липополисахарид и полиинозин-полицитидиловая кислота стимулируют синтез фактора B макрофагами посредством различных, но перекрывающихся механизмов. J Leukoc Biol. (2010) 88: 609–18. DOI: 10.1189 / jlb.0809588
PubMed Аннотация | CrossRef Полный текст | Google Scholar
101.Оствик А.Е., Гранлунд А., Густафссон Б.И., Торп С.Х., Эспевик Т., Моллнес Т.Э. и др. Толл-подобный рецептор 3 слизистой оболочки, зависимый от синтеза фактора B и системной активации комплемента при воспалительном заболевании кишечника. Воспаление кишечника. (2014) 20: 995–1003. DOI: 10.1097 / MIB.0000000000000035
PubMed Аннотация | CrossRef Полный текст | Google Scholar
102. Zou L, Feng Y, Li Y, Zhang M, Chen C, Cai J, et al. Фактор комплемента B является нижестоящим эффектором TLR и играет важную роль в мышиной модели тяжелого сепсиса. J Immunol. (2013) 191: 5625–35. DOI: 10.4049 / jimmunol.1301903
PubMed Аннотация | CrossRef Полный текст | Google Scholar
103. Папа М.Р., Хоффман С.М., Томлинсон С., Флеминг С.Д. Комплемент регулирует TLR4-опосредованные воспалительные реакции во время реперфузии кишечной ишемии. Mol Immunol. (2010) 48: 356–64. DOI: 10.1016 / j.molimm.2010.07.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
104. Фан Дж., Малик А.Б. Передача сигналов Toll-подобного рецептора-4 (TLR4) усиливает индуцированную хемокинами миграцию нейтрофилов, модулируя экспрессию хемокиновых рецепторов на клеточной поверхности. Nat Med. (2003) 9: 315–21. DOI: 10,1038 / нм832
PubMed Аннотация | CrossRef Полный текст | Google Scholar
106. Асгари Э., Ле Фрик Дж., Ямамото Х., Перуча Э, Сакс С.С., Кол Дж. И др. C3a модулирует секрецию IL-1β в моноцитах человека, регулируя отток АТФ и последующую активацию инфламмасомы NLRP3. Кровь. (2013) 122: 3473–81. DOI: 10.1182 / кровь-2013-05-502229
PubMed Аннотация | CrossRef Полный текст | Google Scholar
107.Триантафилу К., Хьюз Т.Р., Триантафилу М., Морган Б.П. Комплекс атаки мембраны комплемента запускает внутриклеточные потоки Ca2 +, ведущие к активации воспаления NLRP3. J Cell Sci. (2013) 126 (Pt 13): 2903–13. DOI: 10.1242 / jcs.124388
PubMed Аннотация | CrossRef Полный текст | Google Scholar
108. Рейс Е.С., ДеАнджелис Р.А., Чен Х., Ресуэло Р.Р., Риклин Д., Ламбрис Дж. Д.. Терапевтический ингибитор C3 Cp40 отменяет активацию комплемента, вызванную современными фильтрами для гемодиализа. Иммунобиология. (2015) 220: 476–82. DOI: 10.1016 / j.imbio.2014.10.026
PubMed Аннотация | CrossRef Полный текст | Google Scholar
109. S Reis E, Falcao DA, Isaac L. Клинические аспекты и молекулярные основы первичной недостаточности компонента C3 комплемента и его регуляторных белков, фактора I и фактора H. Scand J Immunol. (2006) 63: 155–68. DOI: 10.1111 / j.1365-3083.2006.01729.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
110.Audemard-Verger A, Descloux E, Ponard D, Deroux A, Fantin B, Fieschi C и др. Инфекции, выявляющие дефицит комплемента у взрослых: французское общенациональное исследование с участием 41 пациента. Медицина (Балтимор). (2016) 95: e3548. DOI: 10.1097 / MD.0000000000003548
PubMed Аннотация | CrossRef Полный текст
112. Reis ES. Профиль безопасности нечеловеческих приматов при длительном ингибировании C3. Clin Immunol. (2018) 197: 96–106. DOI: 10.1016 / j.clim.2018.09.004
CrossRef Полный текст
113.Rafail S, Kourtzelis I, Foukas PG, Markiewski MM, DeAngelis RA, Guariento M, et al. Дефицит комплемента способствует заживлению кожных ран у мышей. J Immunol. (2015) 194: 1285–91. DOI: 10.4049 / jimmunol.1402354
PubMed Аннотация | CrossRef Полный текст | Google Scholar
114. Risitano AM, Ricklin D, Huang Y, Reis ES, Chen H, Ricci P, et al. Пептидные ингибиторы активации C3 как новая стратегия ингибирования комплемента для лечения пароксизмальной ночной гемоглобинурии. Кровь. (2014) 123: 2094–101. DOI: 10.1182 / кровь-2013-11-536573
PubMed Аннотация | CrossRef Полный текст | Google Scholar
116. Нассар М., Табиб И., Капуча Т., Мизраджи Г., Нир Т., Певснер-Фишер М. и др. GAS6 является ключевым гомеостатическим иммунологическим регулятором взаимодействий хозяин-комменсал в слизистой оболочке полости рта. Proc Natl Acad Sci USA. (2017) 114: E337–46. DOI: 10.1073 / pnas.1614926114
PubMed Аннотация | CrossRef Полный текст | Google Scholar
117.Hasturk H, Kantarci A, Goguet-Surmenian E, Blackwood A, Andry C, Serhan CN и др. Резолвин Е1 регулирует воспаление на клеточном и тканевом уровне и восстанавливает тканевый гомеостаз in vivo . J Immunol. (2007) 179: 7021–9. DOI: 10.4049 / jimmunol.179.10.7021
PubMed Аннотация | CrossRef Полный текст | Google Scholar
118. Абэ Т., Шин Дж, Хосур К., Удей М.К., Чавакис Т., Хаджишенгаллис Г. Регулирование гомеостаза остеокластов и воспалительной потери костной массы с помощью MFG-E8. J Immunol. (2014) 193: 1383–91. DOI: 10.4049 / jimmunol.1400970
PubMed Аннотация | CrossRef Полный текст | Google Scholar
119. Ли С.-Т., Телес Р., Кантарси А., Чен Т., Маккафферти Дж., Старр Дж. Р. и др. Резолвин Е1 обращает вспять экспериментальный пародонтит и дисбактериоз. J Immunol. (2016) 197: 2796–806. DOI: 10.4049 / jimmunol.1600859
PubMed Аннотация | CrossRef Полный текст | Google Scholar
120. Abusleme L, Dupuy AK, Dutzan N, Silva N, Burleson JA, Strausbaugh LD, et al.Поддесневой микробиом в здоровье и пародонтите и его связь с биомассой сообщества и воспалением. ISME J. (2013) 7: 1016–25. DOI: 10.1038 / ismej.2012.174
PubMed Аннотация | CrossRef Полный текст | Google Scholar
121. Heitz-Mayfield LJ. Прогрессирование заболевания: определение групп и лиц высокого риска по пародонтиту. J Clin Periodontol. (2005) 6 (32 приложение): 196–209. DOI: 10.1111 / j.1600-051X.2005.00803.x
CrossRef Полный текст | Google Scholar
122.Genco RJ, Genco FD. Общие факторы риска в лечении заболеваний пародонта и связанных с ними системных заболеваний: стоматологическая установка и межпрофессиональное сотрудничество. J Evid Based Dent Pract. (2014) (14 приложение): 4–16. DOI: 10.1016 / j.jebdp.2014.03.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
123. Джоши В., Мэтьюз К., Аспирас М., де Ягер М., Уорд М., Кумар П. Курение снижает структурную и функциональную устойчивость поддесневой экосистемы. J Clin Periodontol. (2014) 41: 1037–47. DOI: 10.1111 / jcpe.12300
PubMed Аннотация | CrossRef Полный текст | Google Scholar
124. Мастеллос, округ Колумбия, Риклин Д., Хаджишенгаллис Е., Хаджишенгаллис Г., Ламбрис Дж. Д.. Дополнительные терапевтические средства при воспалительных заболеваниях: многообещающие лекарственные препараты-кандидаты для вмешательства, направленного на C3. Mol Oral Microbiol. (2016) 31: 3–17. DOI: 10.1111 / omi.12129
PubMed Аннотация | CrossRef Полный текст | Google Scholar
127. Бергер Н., Алайи Т.Д., Ресуэло Р.Р., Туплано СП, Рейс Е.С., Ламбрис Дж.Д.Новые аналоги ингибитора С3 компстатина с повышенной растворимостью и улучшенным фармакокинетическим профилем.
