Ортопантомограмма зубов (ОПТГ) в Петрозаводске, цены на панорамный рентгеновский снимок зубов
Качественная диагностика является одним из ключевых этапов при лечении стоматологических заболеваний. Ортопантомограмма — современный метод рентгенодиагностики для получения панорамного снимка зубов и мягких тканей двух челюстей.
Когда необходима ортопантомограмма
Ортопантомограмма (ОПТГ) или 3D-рентген — метод получения панорамного вида двух челюстей в развернутой плоскости. Благодаря изображению стоматолог может оценить состояния костей челюсти, зубов, корней и каналов, пародонта, синусов и гайморовых пазух. На рентген-снимке также отображаются пломбы и коронки.
Сделать ортопантомограмма рекомендуется при патологиях:
Так же диагностика необходима пациентам, планирующим протезирование зубов или сложное лечение, либо имеющим серьезные осложнения после проведенного ранее лечения.
Что врач может увидеть на снимке
Детальный снимок мягких и твердых тканей полости рта позволяет выявить патологии, протекающие внутри тканей и не имеющие выраженных симптомов:
-
скрытый кариес;
-
кисты;
-
воспалительные процессы;
-
абсцессы;
-
переломы;
-
ретинированные зубы;
-
атрофия костной ткани зуба;
-
«скрытые» зубы или их зачатки.

Ортопантомограмма считается лучшим методом диагностики при патологиях восьмерок, которые расположены в труднодоступной зоне зубного ряда. На панорамном снимке специалисту удается точно определить положение зуба и особенности его корневой системы.
Особенности получения изображения
Процедура ортопантомограммы челюсти проходит быстро и с комфортом. Пациент занимает положение сидя, а вокруг его головы вращается аппарат, выполняющий множество снимков, которые в последующим преобразуются в панорамное изображение. По завершению процедуры снимок пациенту выдается в течение 10–30 минут.
Готовый снимок может быть перенесен на рентген-пленку или цифровой носитель. Сохранение изображения в компьютерном формате позволяет в последующем стоматологу увеличить изображение и изучить его более детально, поэтому данный формат считается предпочтительным.
В стоматологии Дента Плюс ортопантомограмма проводится на современном оборудовании, позволяющем быстро получить четкий и качественный снимок. Продолжительность процедуры не более 20 секунд.
Продолжительность процедуры не более 20 секунд.
Стоимость ортопантомограммы
Сделать ортопантомограмму в клинике Дента Плюс могут пациенты стоматологии, а также пациенты других клиник. Наши специалисты всегда готовы оказать услуги консультации по готовым снимкам.
Узнать стоимость 3D рентгена челюсти можно на сайте клиники или по контактному телефону. В Петрозаводске стоматология Дента Плюс расположена по трем адресам, поэтому всегда можно связаться с ближайшей клиникой и записаться на диагностику. Готовый снимок может быть выдан в желаемом формате пациенту «на руки» или отправлен на электронную почту.
Для исключения осложнений, стоматолог должен иметь информацию о полной клинической картине поэтому, если у пациента имеются признаки скрытого патологического процесса или планируется ортодонтическое/ортопедическое лечение, квалифицированный и опытный стоматолог не начнет лечение.
Запишитесь на осмотр и консультацию
Заполните форму ниже или позвоните нам по телефону 8 (8142) 45-45-45
Ваше имя:
Введите телефон:
Даю согласие на
В ближайшее время с Вами свяжется администратор и проконсультирует Вас по условиям и стоимости лечения, подберёт врача и запишет Вас на приём.
Панорамный снимок зубов — «Стоматология на Марата 31»
Ортопантомограмма – это круговой снимок двух челюстей в одной плоскости. Сегодня такой снимок делают цифровым способом, поэтому степень облучения минимальна, а качество изображения отличное. Разница между обычным прицельным снимком и ортопантомограммой в том, что ОПТГ захватывает всю зубочелюстную систему и даже пазухи носа. Панорамный снимок назначают при различных патологиях зубов и десен.
Кому может понадобиться ортопантомограмма
- стоматологу-терапевту для выявления наличия заболеваний полости рта;
- стоматологу-ортодонту для того, чтобы рассмотреть состояние всей полости рта, увидеть наличие и расположение восьмых зубов;
- пародонтологу для выявления пародонтальных карманов и состояния альвеолярного отростка;
- хирургу-имплантологу в качестве контрольного снимка после проведенной операции по установке импланта;
- детскому стоматологу для определения прикуса юного пациента.

Что можно увидеть на ОПТГ
- состояние зубов, их корни и каналы;
- имеющиеся пломбы и коронки;
- пародонтальные ткани.
Что можно выявить при помощи панорамного снимка:
- кисты, гранулемы и другие подобные новообразования;
- кариес;
- воспалительные заболевания мягких тканей;
- состояние и расположение зубов мудрости;
- плотность челюстной кости;
- расстояние от верхней челюсти до гайморовых пазух.
Как проводится ОПТГ
Процедура продолжается около трех минут и состоит из нескольких этапов:
- Перед тем, как делать снимок, пациенту нужно снять имеющиеся металлические предметы: сережки, кольца, цепочки и т.д. Это нужно для того, чтобы снимок получился четким без каких-либо искажений.
- На пациента надевают защитный фартук.
- Между зубами пациенту закладывают специальный держатель, который нужно прикусывать.
 Изменять положение держателя, так же, как и зубов нельзя.
Изменять положение держателя, так же, как и зубов нельзя. - Сама процедура длится не более полминуты, после чего полученная картинка обрабатывается и выводится на экран компьютера.
Плюсы и минусы
Преимущества:
- Минимальная доза облучения.
- Снимок сразу двух челюстей.
- Четкое изображение.
- Картинку возможно увеличить на экране компьютера.
- Благодаря безопасности, такой снимок можно делать пожилым людям, детям и пациентам с ограниченными возможностями.
- Исследование дает выявить различные заболевания полости рта на ранних стадиях их развития.
- Процедура совершенно безболезненна и не занимает много времени.
- ОПТГ можно отправить по электронной почте или просто распечатать.
- Рентген можно хранить на диске или в памяти компьютера.
Минусы ортопантомограммы:
- Изображение плоское в 2D формате, поэтому точную информацию о наличии скрытых патологий такая картинка дать не может.

- Старые протезы, так называемого «советского» типа являются противопоказанием к проведению процедуры.
В таких случаях проводится более точное и современное 3D компьютерное исследование.
Оптика проливает свет на стоматологическую визуализацию
Новейшие стоматологические методы визуализации улучшают видимость трещин и полостей в зубах. Фото: Westend/Getty
Скоро человек сможет обнаружить кариес задолго до того, как он появится на рентгеновском снимке, и достаточно рано, чтобы можно было остановить кариес. Все, что для этого потребуется, — это инструмент, похожий на электрическую зубную щетку, оснащенный камерой и светодиодом вместо щетки. Вы полоскаете рот специальным ополаскивателем, проводите инструментом по зубам, а затем смотрите на свой смартфон, чтобы увидеть, какие области имеют признаки разъедания зубной эмали кислотой.
Поделитесь изображениями со своим стоматологом, и он или она могут прописать высококонцентрированный раствор фтора, который нужно осторожно нанести на опасные места. Затем через несколько недель вы снова проверите, реминерализована ли область, и при необходимости скорректируете лечение.
Затем через несколько недель вы снова проверите, реминерализована ли область, и при необходимости скорректируете лечение.
Таково видение Эрика Сейбела, директора Лаборатории фотоники человека Вашингтонского университета в Сиэтле. Он подал заявку на патент на эту технику и пытается найти компанию по производству медицинского оборудования, заинтересованную в создании такого инструмента.
Часть Nature Outlook: Здоровье полости рта
Сейбел — один из нескольких исследователей, разрабатывающих методы оптической визуализации для стоматологии, использующие свет вместо рентгеновских лучей для исследования зубов людей на наличие полостей и трещин. Свет в ближнем инфракрасном спектре может проникать через внешний слой эмали, нижележащий дентин, пульпу в центре и даже ткань десны.
Частично мотивация заключается в том, чтобы уменьшить воздействие ионизирующего излучения на пациентов, даже несмотря на то, что риск стоматологического рентгена чрезвычайно низок.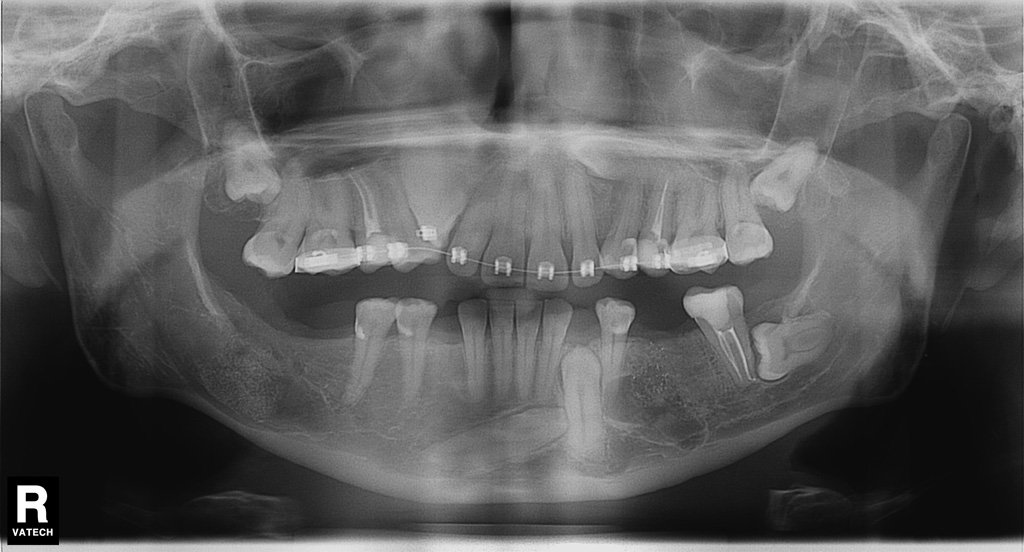 Национальная служба здравоохранения Великобритании сообщает, что увеличение риска смертельного рака в течение жизни от каждого стандартного стоматологического рентгеновского снимка составляет один случай на несколько миллионов. Тем не менее, для детей особенно желательны альтернативы рентгену, поскольку доза облучения больше по сравнению с размером их тела, а также потому, что детские зубы меняются достаточно быстро, и более частые снимки могут оказаться полезными. Стоматологи и ассистенты стоматолога, которые могут ежедневно находиться рядом с рентгеновскими лучами и, таким образом, подвергаться более высокому риску облучения, чем большинство людей, также могут получить пользу.
Национальная служба здравоохранения Великобритании сообщает, что увеличение риска смертельного рака в течение жизни от каждого стандартного стоматологического рентгеновского снимка составляет один случай на несколько миллионов. Тем не менее, для детей особенно желательны альтернативы рентгену, поскольку доза облучения больше по сравнению с размером их тела, а также потому, что детские зубы меняются достаточно быстро, и более частые снимки могут оказаться полезными. Стоматологи и ассистенты стоматолога, которые могут ежедневно находиться рядом с рентгеновскими лучами и, таким образом, подвергаться более высокому риску облучения, чем большинство людей, также могут получить пользу.
Но основная причина интереса к оптическим изображениям заключается в том, что они могут визуализировать проблемы, недоступные рентгеновским снимкам. «Проблема с рентгеном не только в том, что он использует ионизирующее излучение — он также не очень чувствителен к определенным типам поражений», — говорит Дэниел Фрид, научный сотрудник Школы стоматологии Калифорнийского университета в Сан-Франциско. Альтернативные методы могут позволить стоматологам обнаруживать трещины и зачатки полостей, которые слишком малы, чтобы их можно было обнаружить на рентгеновских снимках.
Альтернативные методы могут позволить стоматологам обнаруживать трещины и зачатки полостей, которые слишком малы, чтобы их можно было обнаружить на рентгеновских снимках.
Зубы хорошо подходят для оптической визуализации из-за их строения, говорит Джон Гиркин, физик, который руководит Институтом биофизических наук Даремского университета, Великобритания. «Эмаль — это, по сути, оптическое волокно, поэтому она направляет по нему свет», — говорит он. «Что происходит на ранней стадии заболевания, так это то, что это оптическое волокно повреждается, и вместо того, чтобы свет проходил через зуб, он рассеивается обратно. Так что в итоге вы получите эти белые пятна».
Эти белые поражения видны невооруженным глазом, но их часто трудно заметить на фоне белой эмали. Они являются ранними признаками кариеса до того, как разовьется большая полость. Когда они маленькие, их можно лечить фторидом, который вызывает реминерализацию слабого участка эмали.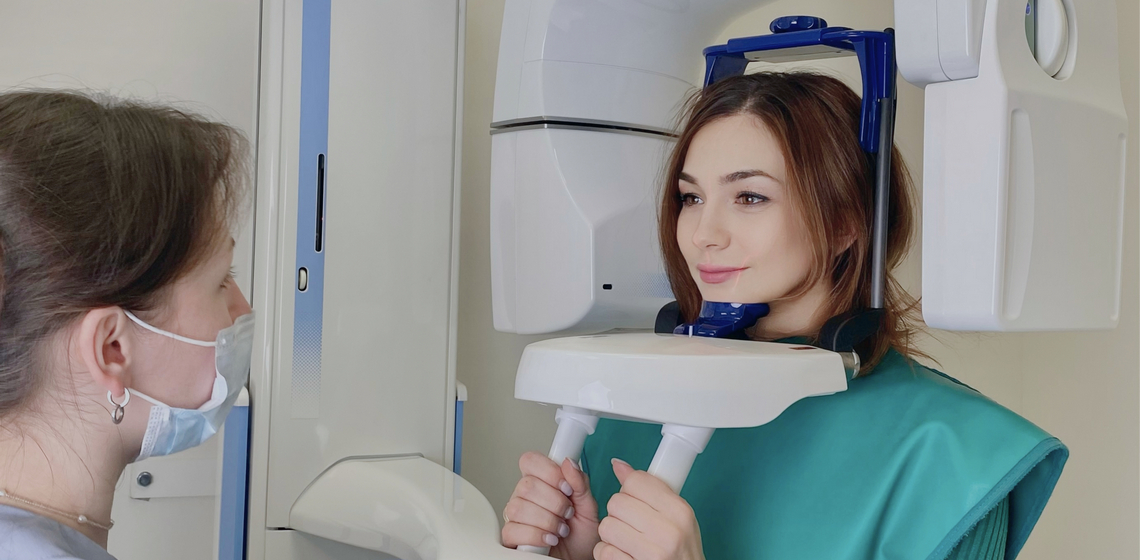 «Зуб, если вы сможете обнаружить проблему достаточно рано, способен излечиться сам», — говорит Гиркин. «Но проблема в том, что когда что-то появляется на рентгеновском снимке, оно выходит за пределы точки, в которой оно излечивает себя».
«Зуб, если вы сможете обнаружить проблему достаточно рано, способен излечиться сам», — говорит Гиркин. «Но проблема в том, что когда что-то появляется на рентгеновском снимке, оно выходит за пределы точки, в которой оно излечивает себя».
Гиркин имеет опыт работы в области оптики — его кандидатская диссертация была посвящена лазерной спектроскопии атомарного водорода — и он давно интересовался разработкой медицинских инструментов. Это заставило его задуматься о том, какие оптические технологии могли бы использовать светопропускающие характеристики зубной эмали. Сначала он попробовал многофотонную микроскопию, запуская короткие импульсы лазерного света в зуб, чтобы вызвать флуоресценцию, а затем искал области, где зуб не флуоресцировал так сильно, что указывало бы на наличие поврежденной ткани. По его словам, это хорошо работало на удаленных зубах в держателе на оптической скамье, но казалось слишком сложным для использования в клинических условиях.
Пытаясь избежать использования сложного оборудования и флуоресцентных измерений, Гиркин предложил использовать легко доступный источник инфракрасного света и коммерческую камеру, способную обнаруживать нужную длину волны. Он направил луч лазера от проигрывателя компакт-дисков через зуб в веб-камеру. «О чудо, вы можете получить изображение передачи через зуб с очень высоким качеством», — говорит он.
Он направил луч лазера от проигрывателя компакт-дисков через зуб в веб-камеру. «О чудо, вы можете получить изображение передачи через зуб с очень высоким качеством», — говорит он.
Следующим его шагом было превращение этого метода в трехмерное изображение зуба. Чтобы получить изображения с разной глубины зуба, он проецирует на структуру узор из линий и пространств. Ближний инфракрасный свет с длиной волны 850 нанометров проникает в зуб, но не все фотоны проходят сквозь него. Вместо этого они разбросаны, размывая рисунок. Степень размытия увеличивается по мере того, как фотоны проникают глубже в зуб, что позволяет измерить глубину. В местах, где присутствуют поражения, эффект нарушается, светопропускание падает, и поражение проявляется в виде темного пятна на изображении.
Гиркин перемещает образец и повторяет процесс до тех пор, пока он не отобразит весь зуб. Результат подобен компьютерной томографии (КТ), при которой трехмерное изображение строится слой за слоем. Изображение, которое можно раскрасить, чтобы сделать проблемы более заметными, показывает глубину и размер кариеса, что облегчает стоматологам выбор наилучшего лечения. Большинство оптических 3D-сканеров, которые уже используются стоматологами, отображают только поверхности зубов; если цель состоит в том, чтобы построить новый зуб, это дает достаточно информации.
Большинство оптических 3D-сканеров, которые уже используются стоматологами, отображают только поверхности зубов; если цель состоит в том, чтобы построить новый зуб, это дает достаточно информации.
Увидеть поражения, которые не видит рентген, — не единственное преимущество метода Гиркина. Поскольку в нем используется ближний инфракрасный свет, который безвреден для тканей, стоматологи могут выполнять этот тип визуализации так часто, как это необходимо. Они могут назначить лечение пораженного зуба фтором, а через несколько месяцев проверить, работает ли оно. Гиркин основал компанию NirVisio для превращения этой технологии в клинический инструмент и ищет финансирование для проведения клинических испытаний.
Еще более длинные волны Фрид, однако, заинтересован в еще более глубоком изучении инфракрасного спектра. «Когда вы проходите весь путь до 1300 нм, именно тогда эмаль становится наиболее прозрачной», — говорит он. «Это почти как стекло. Вы можете видеть сквозь него».
Использование света с большей длиной волны, по словам Фрида, дает более четкие изображения, чем длина волны, которую использует Гиркин (как также отмечает Гиркин), и гораздо лучше подходит для обнаружения распада, чем рентгеновские лучи. Пятна, которые могли бы скрыть кариес, становятся невидимыми при таком свете. Фрид также может направить свет на десну и увидеть, как свет выходит через верхнюю часть зуба (известную как окклюзионная поверхность). Это позволяет ему обнаруживать кариес, начинающий формироваться на верхней части зуба — полезный шаг вперед, потому что окклюзионная поверхность зуба обычно усеяна ямками, и с помощью рентгеновского снимка может быть трудно отличить раннюю кариозную полость от естественной впадины. .
В зубе видна трещина (слева; темная вертикальная линия слева), полученная с помощью флуоресцентного красителя и ближнего инфракрасного света, но ее невозможно обнаружить с помощью обычной компьютерной томографии (справа). Фото: Ref. 2
Несмотря на то, что прохождение света через зубы для выявления проблем оказалось полезным, Фрид говорит, что в некоторых случаях наблюдение за светом, отраженным от зуба, может работать даже лучше. Этот метод включает в себя освещение верхней части зуба светом и наблюдение за тем, что отскакивает. Деминерализованные поражения, более пористые, чем окружающая эмаль, рассеивают больше света, поэтому выглядят ярче. При правильных длинах волн разницу в рассеянии можно измерять на несколько порядков, обеспечивая высокий контраст между здоровой и больной тканью. Фрид изучает длины волн от 1450 нм до 1,950 нм для этого приложения; одно исследование, которое он и его коллеги опубликовали ранее в этом году, показало, что длина волны 1950 нм кажется наилучшей для четкой визуализации поражений 1 . Преимущество использования нескольких методов на разных длинах волн в одном и том же исследовании заключается в потенциальном исключении ложноположительных результатов, которые могут возникнуть в результате использования этого более чувствительного метода визуализации.
Этот метод включает в себя освещение верхней части зуба светом и наблюдение за тем, что отскакивает. Деминерализованные поражения, более пористые, чем окружающая эмаль, рассеивают больше света, поэтому выглядят ярче. При правильных длинах волн разницу в рассеянии можно измерять на несколько порядков, обеспечивая высокий контраст между здоровой и больной тканью. Фрид изучает длины волн от 1450 нм до 1,950 нм для этого приложения; одно исследование, которое он и его коллеги опубликовали ранее в этом году, показало, что длина волны 1950 нм кажется наилучшей для четкой визуализации поражений 1 . Преимущество использования нескольких методов на разных длинах волн в одном и том же исследовании заключается в потенциальном исключении ложноположительных результатов, которые могут возникнуть в результате использования этого более чувствительного метода визуализации.
Недостатком является то, что детекторы для этих длин волн сделаны из арсенида индия-галлия — редких и поэтому дорогих материалов. Свет с длиной волны 850 нм, который используют другие исследователи, можно обнаружить с помощью недорогих камер, обычно встроенных в смартфоны.
Свет с длиной волны 850 нм, который используют другие исследователи, можно обнаружить с помощью недорогих камер, обычно встроенных в смартфоны.
Один из методов, который часто упоминается в литературе по стоматологической визуализации, называется оптической когерентной томографией (ОКТ). За последние 30 лет ОКТ нашла применение в различных технологиях медицинской визуализации, от выявления рака до исследования сетчатки и коронарных артерий, но еще не применялась в стоматологии. ОКТ часто сравнивают с ультразвуком, потому что он также проникает в ткани для создания трехмерного изображения с высоким разрешением. Он использует лучи ближнего инфракрасного света для глубокого зондирования зуба и создает изображения с разрешением, измеряемым в микрометрах. Он может отображать серьезный кариес, который распространился с эмали на нижележащий дентин, даже если кариес не виден на рентгеновском снимке. Однако эта технология одновременно сканирует только небольшую область, и многие эксперты считают ее слишком медленной для использования в стоматологии, а также слишком дорогой.
Но Фрид говорит, что скорость сканирования значительно увеличилась, и считает, что затраты могут снизиться, если производитель медицинского оборудования посвятит усилия более эффективному созданию машин ОКТ. Он связывает отсутствие таких сканеров скорее с вопросами бизнеса, такими как, сочтут ли стоматологи, что машины стоят своих денег, чем с какой-либо технической проблемой, и ожидает, что они в конечном итоге войдут в область стоматологии: «Я вполне уверен, что они станут в наличии», — говорит он.
Идите со светом Одной стоматологической проблемой, которую почти невозможно обнаружить на ранней стадии — ни с помощью рентгена, ни при осмотре невооруженным глазом, — являются крошечные трещины в эмали, которые могут сделать зубы чувствительными и стать точкой доступа. для бактерий. К тому времени, когда такие трещины становятся видимыми с помощью существующих методов визуализации, они уже достаточно велики, чтобы потребовать лечения корневых каналов или удаления зуба. Чтобы выявить эти проблемы раньше, Цзянь Сюй, инженер-электрик, изучающий биомедицинскую визуализацию в Университете штата Луизиана в Батон-Руж, обратился к флуоресценции. С помощью флуоресцентного красителя Сюй и его коллеги продемонстрировали в 2019 г.исследование показало, что они могут находить трещины шириной всего 3 мкм 2 . По его словам, рентгеновские лучи не могут обнаружить эти трещины, пока они не вырастут как минимум до 15 мкм.
Чтобы выявить эти проблемы раньше, Цзянь Сюй, инженер-электрик, изучающий биомедицинскую визуализацию в Университете штата Луизиана в Батон-Руж, обратился к флуоресценции. С помощью флуоресцентного красителя Сюй и его коллеги продемонстрировали в 2019 г.исследование показало, что они могут находить трещины шириной всего 3 мкм 2 . По его словам, рентгеновские лучи не могут обнаружить эти трещины, пока они не вырастут как минимум до 15 мкм.
Этот метод основан на индоцианиновом зеленом, красителе, одобренном для различных видов медицинской визуализации с конца 1950-х годов. Хотя для этих диагностических методов его обычно вводят в виде инъекций, Сюй говорит, что для визуализации зубов краситель можно добавлять в жидкость для полоскания рта. Эмаль поглощает краситель и флуоресцирует при попадании на нее лазерного луча в ближнем инфракрасном диапазоне. Трещина выглядит как тень на изображении. Сюй провел свои исследования на удаленных зубах и разрабатывает протоколы клинических испытаний, которые, как он ожидает, начнутся в ближайшие два-три года.
Еще из Nature Outlooks
Метод измерения кислотности, разрабатываемый Сейбелом в Вашингтонском университете, также основан на флуоресценции. Кариес развивается, когда бактерии на зубах переваривают сахар и выделяют кислоту, которая разъедает эмаль. Поэтому Сейбел сосредоточился на поиске областей на зубах с повышенной кислотностью.
Как и Сюй, Сейбел использует флуоресцентный краситель под названием флуоресцеин, который уже одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США. Этот краситель можно возбудить фиолетовым светом с длиной волны 420 нм, и он имеет флуоресцентные пики на двух разных длинах волн, которые можно использовать для получения более точных показаний, а сила флуоресценции зависит от pH. Если рН кислый, что указывает на разрушение эмали, можно принять восстановительные меры. «У вас есть несколько месяцев, чтобы нанести местный фторид и восстановить его», — объясняет Сейбел. Тем не менее, местный фтор следует применять осторожно, чтобы избежать передозировки, которая может изменить цвет зубов и вызвать другие побочные эффекты.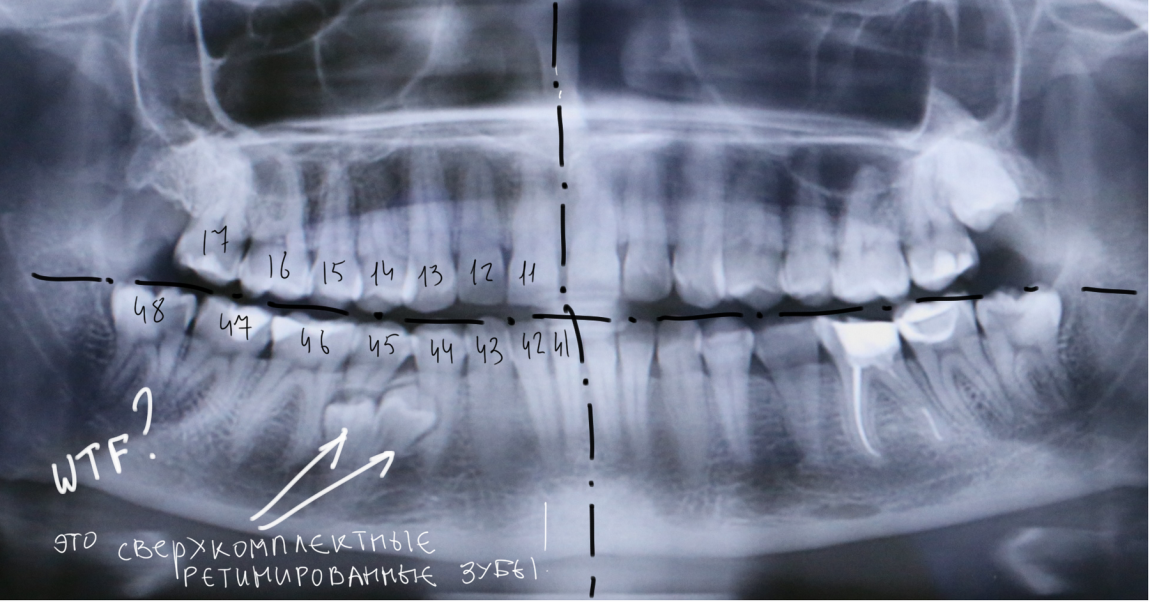
Исследователи говорят, что ни один из этих методов не заменит полностью рентгеновские лучи. «Рентгеновские лучи используются и для других целей, а не только для обнаружения полостей — например, для осмотра кости», — отмечает Фрид. «Однако я вижу потенциал для сокращения количества скринингов и, я думаю, самое главное, вы можете делать то, что вы не можете сделать с рентгенограммами».
Но методы оптической визуализации, позволяющие выявить проблемы на ранней стадии, могут сделать некоторые рентгеновские снимки ненужными. И если методы, использующие инфракрасные светодиоды или флуоресцентные жидкости для полоскания рта, войдут в повседневную стоматологическую практику, они могут осветить путь к улучшению здоровья полости рта.
Стоматологическая оптическая когерентная томография — PMC
1. Хуан Д., Суонсон Э.А., Лин С.П., Шуман Дж.С., Стинсон В.Г., Чанг В., Хи М.Р., Флотте Т., Грегори К., Пулиафито К.А., Фуджимото Дж.Г. Оптической когерентной томографии. Наука. 1991; 254:1178–1181. [Бесплатная статья PMC] [PubMed] [Google Scholar]
1991; 254:1178–1181. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Poneros J.M., Brand S., Bouma B.E., Tearney G.J., Compton C.C., Nishioka N.S. Диагностика специализированной кишечной метаплазии методом оптической когерентной томографии. Гастроэнтерология. 2001; 120:7–12. [PubMed] [Академия Google]
3. Эванс Дж.А., Понерос Дж.М., Боума Б.Е., Бресснер Дж., Халперн Э.Ф., Шишков М., Лауверс Г.Ю., Кенудсон М.М., Нишиока Н.С., Тирни Г.Дж. Оптическая когерентная томография для выявления внутрислизистой карциномы и дисплазии высокой степени в пищеводе Барретта. клин. Гастроэнтерол. Гепатол. 2006; 4:38–43. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Smith P.W., Lee K., Guo S., Zhang J., Osann K., Chen Z., Messadi D. In vivo диагностика дисплазии полости рта и злокачественные новообразования с использованием оптической когерентной томографии: предварительные исследования у 50 пациентов. Лазеры Surg. Мед. 2009 г.;41:353–357. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Ван Ю., Бауэр Б.А., Изатт Дж.А., Тан О., Хуанг Д. Измерение кровотока в сетчатке с помощью циркумпапиллярной допплеровской оптической когерентной томографии Фурье. Дж. Биомед. Опц. 2008; 13 doi: 10.1117/1.2998480. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ван Ю., Бауэр Б.А., Изатт Дж.А., Тан О., Хуанг Д. Измерение кровотока в сетчатке с помощью циркумпапиллярной допплеровской оптической когерентной томографии Фурье. Дж. Биомед. Опц. 2008; 13 doi: 10.1117/1.2998480. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Хангай М., Одзима Ю., Гото Н., Иноуэ Р., Ясуно Ю., Макита С., Яманари М., Ятагай Т. , Кита М., Йошимура Н. Трехмерное изображение макулярных отверстий с помощью высокоскоростной оптической когерентной томографии. Офтальмология. 2007; 114: 763–773. [PubMed] [Академия Google]
7. Yasuno Y., Hong Y., Makita S., Yamanari M., Akiba M., Miura M., Yatagai T. In vivo высококонтрастное изображение глубоких задних отделов глаза с помощью оптического источника со свипированием 1 мкм когерентная томография и рассеянная оптическая когерентная ангиография. Опц. Выражать. 2007; 15:6121–6139. [PubMed] [Google Scholar]
8. Pagnoni A., Knuettel A., Welker P., Rist M., Stoudemayer T., Kolbe L., Sadiq I. , Kligman A.M. Оптическая когерентная томография в дерматологии. Рез. кожи Технол. 1999; 5:83–87. [Академия Google]
, Kligman A.M. Оптическая когерентная томография в дерматологии. Рез. кожи Технол. 1999; 5:83–87. [Академия Google]
9. Pierce M.C., Strasswimmer J., Park B.H., Cense B., de Boer J.F. Измерения двойного лучепреломления в коже человека с использованием поляризационно-чувствительной оптической когерентной томографии. Дж. Биомед. Опц. 2004; 9: 287–291. [PubMed] [Google Scholar]
10. Colston B.W., Sathyam U.S., Jr., DaSilva L.B., Everett M.J., Stroeve P., Otis L.L. Dental OCT. Опц. Выражать. 1998; 3: 230–238. [PubMed] [Google Scholar]
11. Baumgartner A., Dichtl S., Hitzenberger C.K., Sattmann H., Robl B., Moritz A., Fercher A.F., Sperr W. Поляризационно-чувствительная оптическая когерентная томография зубных структур. Кариес рез. 2000;34:59–69. [PubMed] [Google Scholar]
12. Войтковски М., Шринивасан В., Фуджимото Дж.Г., Ко Т., Шуман Дж.С., Ковальчик А., Дукер Дж.С. Трехмерная визуализация сетчатки с помощью высокоскоростной оптической когерентной томографии сверхвысокого разрешения. Офтальмология. 2005; 112:1734–1746. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Офтальмология. 2005; 112:1734–1746. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Fujimoto J.G. Оптическая когерентная томография для визуализации сверхвысокого разрешения in vivo . Нац. Биотехнолог. 2003; 21:1361–1367. [PubMed] [Академия Google]
14. Брезински М.Е., Тирни Г.Дж., Вайсман Н.Дж., Боппарт С.А., Боума Б.Е., Хи М.Р., Вейман А.Е., Суонсон Э.А., Южный Дж.Ф., Фудзимото Дж.Г. Оценка морфологии атеросклеротических бляшек: сравнение оптической когерентной томографии и высокочастотного внутрисосудистого ультразвука. Сердце. 1997; 77: 397–403. [PMC free article] [PubMed] [Google Scholar]
15. Звягин А.В., Фицджеральд Дж.Б., Сильва К.К.М.Б.Д., Сэмпсон Д.Д. Метод обнаружения в реальном времени для доплеровской оптической когерентной томографии. Опц. лат. 2000; 25:1645–1647. [PubMed] [Академия Google]
16. Ян Х.Д.В., Мао Ю.Х., Мунс Н., Стэндиш Б., Кухарчик В., Маркон Н.Е., Уилсон Б.С., Виткин И.А. Интерстициальная допплеровская оптическая когерентная томография. Опц. лат. 2005; 30: 1791–1793. [PubMed] [Google Scholar]
Опц. лат. 2005; 30: 1791–1793. [PubMed] [Google Scholar]
17. Де Бур Дж.Ф., Милнер Т.Е., ван Гемерт М.Дж.С., Нельсон Дж.С. Двумерное двулучепреломление в биологических тканях с помощью поляризационно-чувствительной оптической когерентной томографии. Опц. лат. 1997; 22: 934–936. [PubMed] [Google Scholar]
18. Ясуно Ю., Макита С., Суто Ю., Ито М., Ятагай Т. Двулучепреломление кожи человека с помощью поляризационно-чувствительной спектральной интерферометрической оптической когерентной томографии. Опц. лат. 2002; 27: 1803–1805. [PubMed] [Академия Google]
19. Pircher M., Goetzinger E., Leitgeb R., Hitzenberger C. Трехмерная поляризационно-чувствительная ОКТ кожи человека in vivo . Опц. Выражать. 2004; 12:3236–3244. [PubMed] [Google Scholar]
20. Пан Ю.Т., Се Х.К., Феддер Г.К. Эндоскопическая оптическая когерентная томография на основе микроэлектромеханического зеркала. Опц. лат. 2010; 26:1966–1968. [PubMed] [Google Scholar]
21. Herz P., Chen Y. , Aguirre A., Fujimoto J., Mashimo H., Schmitt J., Koski A., Goodnow J., Petersen C. Оптическая биопсия сверхвысокого разрешения с помощью эндоскопической оптической когерентной томографии. Опц. Выражать. 2004; 12:3532–3542. [PubMed] [Академия Google]
, Aguirre A., Fujimoto J., Mashimo H., Schmitt J., Koski A., Goodnow J., Petersen C. Оптическая биопсия сверхвысокого разрешения с помощью эндоскопической оптической когерентной томографии. Опц. Выражать. 2004; 12:3532–3542. [PubMed] [Академия Google]
22. Lesaffre M., Farahi S., Gross M., Delaye P., Boccara C., Ramaz F. Акустооптическая когерентная томография с использованием случайных скачков фазы в ультразвуке и свете. Опц. Выражать. 2009;17:18211–18218. [PubMed] [Google Scholar]
23. Lesaffre M., Farahi S., Boccara A.C., Ramaz F., Gross M. Теоретическое исследование акустооптической когерентной томографии с использованием случайных скачков фазы в ультразвуке и свете. Дж. опт. соц. Являюсь. А. 2011; 28:1436–1444. [PubMed] [Google Scholar]
24. Iftimia N., Iyer A.K., Hammer D.X., Lue N., Mujat M., Pitman M., Ferguson R.D., Amiji M. Оптическая когерентная томография с флуоресцентным наведением для скрининга рака толстой кишки : предварительное исследование на мышах. Биомед. Опц. Выражать. 2012; 3: 178–19.1. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Биомед. Опц. Выражать. 2012; 3: 178–19.1. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Park J., Jo J.A., Shrestha S., Pande P., Wan Q.J., Applegate B.E. Двухрежимная система оптической когерентной томографии и флуоресцентной микроскопии для одновременной морфологической и биохимической характеристики тканей. Биомед. Опц. Выражать. 2010; 1:186–200. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Colston B.W., Everett MJ, Jr., da Silva L.B., Otis L.L., Stroeve P., Nathel H. Визуализация структуры твердых и мягких тканей в полость рта с помощью оптической когерентной томографии. заявл. Опц. 1998;37:3582–3585. [PubMed] [Google Scholar]
27. Drexler W., Fujimoto J.G. Оптическая когерентная томография: технология и приложения. Спрингер Берлин Гейдельберг; New York, NY, USA: 2008. [Google Scholar]
28. Hsieh Y.S., Ho Y.C., Lee S.Y., Lu C.E., Jiang C.P., Chuang C.C., Wang C.Y., Sun C.W. Визуализация поддесневого зубного камня на основе оптической когерентности с качающимся источником томография. Дж. Биомед. Опц. 2011; 16 doi: 10.1117/1.3602851. [PubMed] [CrossRef] [Google Scholar]
Дж. Биомед. Опц. 2011; 16 doi: 10.1117/1.3602851. [PubMed] [CrossRef] [Google Scholar]
29. Xiang X., Sowa M.G., Iacopino A.M., Maev R.G., Hewko M.D., Man A., Liu K.Z. Обновленная информация о новых неинвазивных подходах к диагностике пародонта. Дж. Пародонтол. 2009 г.;81:186–198. [PubMed] [Google Scholar]
30. Leitgeb R., Hitzenberger C.K., Fercher AF. Производительность области Фурье против . Оптическая когерентная томография во временной области. Опц. Выражать. 2003; 11: 889–894. [PubMed] [Google Scholar]
31. Шмитт Дж. М. Оптическая когерентная томография (ОКТ): обзор. Сел. Верхний. Квантовый электрон. IEEE J. 1999; 5:1205–1215. [Google Scholar]
32. Zhao Y., Chen Z.P., Saxer C., Xiang S.H., de Boer J.F., Nelson S, D.J. Оптическая когерентная томография с фазовым разрешением и оптическая допплеровская томография для визуализации кровотока в коже человека с быстрым скорость сканирования и высокая чувствительность скорости. Опц. Буквы. 2000;25:114–116. [PubMed] [Академия Google]
[PubMed] [Академия Google]
33. Сакаи С., Яманари М., Лим Ю., Накагава Н., Ясуно Ю. In vivo оценка анизотропии кожи человека с помощью поляризационно-чувствительной оптической когерентной томографии. Биомед. Опц. Выражать. 2011;2:2623–2631. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Де Бур Дж.Ф., Сринивас С.М., Парк Б.Х., Фам Т.Х., Чен З.П., Милнер Т.Е., Нельсон Дж.С. Поляризационные эффекты в оптической когерентной томографии различных биологических тканей. IEEE Дж. Сел. Верхний. Квантовый электрон. 1999;5:1200–1204. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Harry E.A.R., Clerehugh V. Поддесневой зубной камень: где мы сейчас? Сравнительный обзор. Дж. Дент. 2000; 28: 93–102. [PubMed] [Google Scholar]
36. Meissner G., Oehme B., Strackeljan J., Kocher T. Клиническое обнаружение поддесневого зубного камня с помощью интеллектуального ультразвукового устройства: экспериментальное исследование. Дж. Клин. Пародонтол. 2008; 35: 126–132. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
37. Meissner G., Oehme B., Strackeljan J., Kocher T. Новая система для обнаружения остаточного поддесневого зубного камня: In vitro пределы обнаружения. Дж. Клин. Пародонтол. 2006; 33: 195–199. [PubMed] [Google Scholar]
38. Krause F., Braun A., Jepsen S., Frentzen M. Обнаружение поддесневого зубного камня с помощью нового стоматологического оптического зонда на основе светодиодов. Дж. Пародонтол. 2005; 76: 1202–1206. [PubMed] [Google Scholar]
39. Krause F., Braun A., Frentzen M. Возможность обнаружения поддесневого зубного камня с помощью лазерной флуоресценции. в пробирке. Лазеры Surg. Мед. 2003; 18:32–35. [PubMed] [Google Scholar]
40. Томас С.С., Моханти С., Джаянти Дж.Л., Варугезе Дж.М., Балан А., Субхаш Н. Клинические испытания для обнаружения кариеса зубов с использованием эталонного стандарта коэффициента лазерно-индуцированной флуоресценции. Дж. Биомед. Опц. 2010; 15 doi: 10.1117/1.3365945. [PubMed] [CrossRef] [Google Scholar]
41. Цуда Х., Арендс Дж. Рамановская спектроскопия в зубном камне человека. Дж. Дент. Рез. 1993; 72: 1609–1613. [PubMed] [Google Scholar]
Цуда Х., Арендс Дж. Рамановская спектроскопия в зубном камне человека. Дж. Дент. Рез. 1993; 72: 1609–1613. [PubMed] [Google Scholar]
42. Кармона П., Белланато Дж., Эсколар Э. Инфракрасная и комбинационная спектроскопия мочевых камней: обзор. Биоспектроскопия. 1997; 3: 331–346. [Google Scholar]
43. Цуда Х., Арендс Дж. Рамановская спектроскопия в стоматологических исследованиях: краткий обзор недавних исследований. Дж. Дент. Рез. 1997; 11: 539–547. [PubMed] [Академия Google]
44. Курихара Э., Косеки Т., Гохара К., Нишихара Т., Ансаи Т., Такехара Т. Обнаружение поддесневого зубного камня и кариеса дентина с помощью лазерной флуоресценции. J. Периодонтальная рез. 2004; 39: 59–65. [PubMed] [Google Scholar]
45. Фельдштейн Ф., Геликонов В., Иксанов Р., Геликонов Г., Куранов Р., Сергеев А., Гладкова Н., Оурутина М., Рейтце Д., Уоррен Дж. In vivo ОКТ твердых и мягких тканей полости рта. Опц. Выражать. 1998; 3: 239–250. [PubMed] [Академия Google]
46. Ван С.Дж., Милнер Т.Е., де Бур Дж.Ф., Чжан Ю., Пэшли Д.Х., Нельсон Дж.С. Характеристика дентина и эмали с помощью оптической когерентной томографии. заявл. Опц. 1999;38:2092–2096. [PubMed] [Google Scholar]
Ван С.Дж., Милнер Т.Е., де Бур Дж.Ф., Чжан Ю., Пэшли Д.Х., Нельсон Дж.С. Характеристика дентина и эмали с помощью оптической когерентной томографии. заявл. Опц. 1999;38:2092–2096. [PubMed] [Google Scholar]
47. Отис Л.Л., Мэтью Дж.Э., Уджвал С.С., Колсон Б.В. мл. Оптическая когерентная томография: новая технология визуализации для стоматологии. Варенье. Вмятина. доц. 2000; 131: 511–514. [PubMed] [Google Scholar]
48. Уоррен Дж. А., Гейнсвилл Ф. Л., мл., Геликонов Г. В., Геликонов В. М., Фельдштейн Ф. Дж., Бич Н. М., Мурс М. Д., Рейце Д. Х. Визуализация и характеристика структуры зубов с помощью оптической когерентной томографии. Труды Lasers Electro-Optics, CLEO; Сан-Франциско, Калифорния, США. 3–8 мая 1998. [Google Scholar]
49. Imai K., Shimada Y., Sadr A., Sumi Y., Tagami J. Неинвазивная визуализация трещин эмали в поперечном сечении с помощью оптической когерентной томографии. в пробирке. Дж. Эндод. 2012;38:1269–1274. [PubMed] [Google Scholar]
50. Braz A.K.S., Aguiar C.M., Gomes A.S.L. Оценка распространения трещин в стоматологических композитах методом оптической когерентной томографии. Вмятина. Матер. 2009; 25:74–79. [PubMed] [Google Scholar]
Braz A.K.S., Aguiar C.M., Gomes A.S.L. Оценка распространения трещин в стоматологических композитах методом оптической когерентной томографии. Вмятина. Матер. 2009; 25:74–79. [PubMed] [Google Scholar]
51. Nakajima Y., Shimada Y., Miyashin M., Takagi Y., Tagami J., Sumi Y. Неинвазивная визуализация поперечного сечения неполных переломов коронки (трещин) с использованием скользящего источника оптической когерентной томографии. Междунар. Эндод. Дж. 2012; 45:933–941. [PubMed] [Google Scholar]
52. Садр Т.А.Б.А., Шимада Ю., Тагами Дж., Суми Ю. Неинвазивная количественная оценка межфазных зазоров между полимером и дентином с использованием оптической когерентной томографии: проверка по сравнению с конфокальной микроскопией. Вмятина. Матер. 2011;27:915–925. [PubMed] [Google Scholar]
53. Braz A.K.S., Aguiar C.M., Gomes A.S.L. Оценка целостности зубных герметиков методом оптической когерентной томографии. Вмятина. Матер. 2011;27:e60–e64. [PubMed] [Google Scholar]
54. Исибаси К., Озава Н., Тагами Дж., Суми Ю. Оптическая когерентная томография с переменным источником как новый инструмент для оценки дефектов композитных реставраций на основе смолы. Дж. Дент. 2011;39: 543–548. [PubMed] [Google Scholar]
Исибаси К., Озава Н., Тагами Дж., Суми Ю. Оптическая когерентная томография с переменным источником как новый инструмент для оценки дефектов композитных реставраций на основе смолы. Дж. Дент. 2011;39: 543–548. [PubMed] [Google Scholar]
55. Hsieh Y.S., Lu CW, Ho YC, Lee S.Y., Chuang C.C., Huang WC, Sun CW Обнаружение микропротечек на основе стоматологической оптической когерентной томографии. проц. ШПАЙ. 2013;8566:8566–8569. [Google Scholar]
56. Браз А.К., Киотоку Б.Б., Гомес А.С. Томографическое изображение комплекса пульпа-дентин человека in vitro : оптическая когерентная томография и гистология. Дж. Эндод. 2009;35:1218–1221. [PubMed] [Google Scholar]
57. Петерсен П.Е. Будущее использование материалов для реставрации зубов. Всемирная организация здравоохранения; Женева, Швейцария: 2009 г.. [Google Scholar]
58. Timonen1 P., Niskanen1 M., Taipale L.S., Jula A., Knuuttila1 M., Ylöstalo P. Метаболический синдром, пародонтальная инфекция и кариес зубов. Дж. Дент. Рез. 2010;89:1068–1073. [PubMed] [Google Scholar]
Дж. Дент. Рез. 2010;89:1068–1073. [PubMed] [Google Scholar]
59. Акар Х., Акар Г.К., Карреро Дж.Дж., Стенвинкель П., Линдхольм Б. Системные последствия плохого состояния полости рта у пациентов с хронической болезнью почек. клин. Варенье. соц. Нефрол. 2011;6:218–226. [PubMed] [Google Scholar]
60. Грант В.Б. Обзор роли солнечного ультрафиолетового излучения B и витамина D в снижении риска кариеса зубов. Дерматоэндокринология. 2011;3:193–198. [PMC free article] [PubMed] [Google Scholar]
61. de Cássia Negrini T., Duque C., Höfling J.F., Goncalves R.B. Фундаментальные механизмы иммунного ответа на бактерии полости рта и основные перспективы вакцины против кариеса зубов: Краткий обзор. Дж. Дент. науч. 2009; 124:198–204. [Google Scholar]
62. Хольцман Дж.С., Осанн К., Фарар Дж., Ли К., Ан Ю., Такер Т., Сабет С., Чен З., Гукасян Р., Смит П.В. Способность оптической когерентной томографии обнаруживать кариес под обычно используемыми стоматологическими герметиками. Лазеры Surg. Мед. 2010; 42: 752–759.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Лазеры Surg. Мед. 2010; 42: 752–759.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Амаечи Б.Т., Подолеану А., Хайэм С.М., Джексон Д.А. Корреляция количественной светоиндуцированной флуоресценции и оптической когерентной томографии, применяемых для выявления и количественной оценки раннего кариеса зубов. Дж. Биомед. Опц. 2003; 8: 642–647. [PubMed] [Google Scholar]
64. Амаечи Б.Т., Хайэм С.М., Подолеану А., Роджерс Дж.А., Джексон Д.А. Использование оптической когерентной томографии для оценки кариеса зубов: количественная процедура. J. Оральная реабилитация. 2001;28:1092–1093. [PubMed] [Google Scholar]
65. Шимада Ю., Садр А., Берроу М.Ф., Тагами Дж., Одзава Н., Суми Ю. Валидация оптической когерентной томографии с качающимся источником (SS-OCT) для диагностики окклюзионный кариес. Дж. Дент. 2010; 38: 655–665. [PubMed] [Google Scholar]
66. Баумгартнер А., Хитценбергер К.К., Дихт С., Саттманн Х., Мориц А., Сперр В., Ферчер А.Ф. Оптическая когерентная томография или стоматологические структуры. проц. ШПАЙ. 1998;3248:130–136. [Google Scholar]
проц. ШПАЙ. 1998;3248:130–136. [Google Scholar]
67. Baumgartner A., Dicht S., Hitzenberger C.K., Sattmann H., Robi B., Moritz A., Sperr W., Fercher A.F. Поляризационно-чувствительная оптическая когерентная томография зубных структур. проц. ШПАЙ. 1999;3593:169–176. [Google Scholar]
68. Jones R.S., Darling C.L., Featherstone J.D.B., Fried D. Реминерализация in vitro кариеса зубов, оцененная с помощью поляризационно-чувствительной оптической когерентной томографии. Дж. Биомед. Опц. 2006;11:014016. [PubMed] [Google Scholar]
69. Everett M.J., Colston B.W., Sathyam U.S., Silva L.B.D., Fried D., Featherstone J.D.B. Неинвазивная диагностика раннего кариеса с помощью поляризационно-чувствительной оптической когерентной томографии (PS-OCT) Proc. ШПАЙ. 1999;3593:177–183. [Google Scholar]
70. Fried D., Xie J., Shafi S., Featherstone J.D., Breunig TM, Le C. Визуализация кариеса и прогрессирования поражения с помощью поляризационно-чувствительной оптической когерентной томографии. Дж. Биомед. Опц. 2002; 7: 618–627. [PubMed] [Google Scholar]
Дж. Биомед. Опц. 2002; 7: 618–627. [PubMed] [Google Scholar]
71. Ле М.Х., Дарлинг С.Л., Фрид Д. Автоматический анализ глубины поражения и интегрированной отражательной способности при PS-OCT-сканировании деминерализации зубов. Лазеры Surg. Мед. 2010;42:62–68. [Бесплатная статья PMC] [PubMed] [Google Scholar]
72. Lee C, Darling C.L., Fried D. Поляризационно-чувствительная оптическая когерентная томография искусственной деминерализации на открытых поверхностях корней зубов. Вмятина. Матер. 2009; 25: 721–728. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Wu J., Fried D. Высококонтрастные поляризованные изображения деминерализации в ближнем инфракрасном диапазоне на щечной и окклюзионной поверхностях зубов при λ = 1310 нм. Лазеры Surg. Мед. 2009;41:208–213. [Бесплатная статья PMC] [PubMed] [Google Scholar]
74. Chen Y., Otis L., Piao D., Zhu Q. Характеристика дентина, эмали и кариозных поражений с помощью поляризационно-чувствительной системы оптической когерентной томографии. заявл. Опц. 2005;44:2041–2048. [PubMed] [Google Scholar]
заявл. Опц. 2005;44:2041–2048. [PubMed] [Google Scholar]
75. Louie T., Lee C, Hsu D., Hirasuna K., Manesh S., Staninec M., Darling C.L., Fried D. Клиническая оценка ранней деминерализации зубов с использованием поляризационно-чувствительного оптического когерентная томография. Лазеры Surg. Мед. 2010;42:738–745. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Фрид Д., Станинец М., Дарлинг С., Канг Х., Чан К. Мониторинг деминерализации зубов с помощью кросс-поляризационной оптической когерентной томографической системы со встроенным МЭМС-сканером. проц. ШПАЙ. 2012; 8208 doi: 10.1117/12.914599. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
77. Hugoson A., Sjödin B., Norderyd O. Тенденции за 30 лет, 1973–2003 гг., Распространенность и тяжесть заболеваний пародонта. Дж. Клин. Пародонтол. 2008; 35: 405–414. [PubMed] [Академия Google]
78. Браун Л.Дж., Лоэ Х. Распространенность, степень, тяжесть и прогрессирование заболеваний пародонта. Пародонтология 2000. 1993;2:57–71. [PubMed] [Google Scholar]
1993;2:57–71. [PubMed] [Google Scholar]
79. Петерсен П.Е. Всемирный отчет о состоянии полости рта. Всемирная организация здравоохранения; Женева, Швейцария: 2003. [Google Scholar]
80. Khader Y.S., Ta’ani Q. Заболевания пародонта и риск преждевременных родов и низкой массы тела при рождении: метаанализ. Дж. Пародонтол. 2005; 76: 161–165. [PubMed] [Google Scholar]
81. Бек Дж. Д., Оффенбах С. Системные эффекты пародонтита: эпидемиология заболеваний пародонта и сердечно-сосудистых заболеваний. Дж. Пародонтол. 2005;76(11-с):2089–2100. [PubMed] [Google Scholar]
82. Якопин А. М., Катлер К. В. Патофизиологические отношения между пародонтитом и системным заболеванием: современные концепции липидов в сыворотке. Дж. Пародонтол. 2000;71:1375–1384. [PubMed] [Google Scholar]
83. Колстон Б.В., Эверетт М.Дж., Сильва Л.Б.Д., Отис Л.Л., Нател Х. Оптическая когерентная томография для диагностики заболеваний пародонта. проц. ШПАЙ. 1997; 2973: 216–220. [Google Scholar]
84. Smith P.W., Holtzman J., Epstein J., Le A. Оптическая диагностика в полости рта: обзор. Оральный Дис. 2010; 16:717–728. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Smith P.W., Holtzman J., Epstein J., Le A. Оптическая диагностика в полости рта: обзор. Оральный Дис. 2010; 16:717–728. [Бесплатная статья PMC] [PubMed] [Google Scholar]
85. Пэк Дж.Х., На Дж., Ли Б.Х., Чхве Э., Сон В.С. Оптический доступ к периодонтальной связке при ортодонтическом перемещении зубов: предварительное исследование с помощью оптической когерентной томографии. Являюсь. Дж. Ортод. Дентофак. Ортоп. 2009; 135: 252–259. [PubMed] [Google Scholar]
86. Отчет о регистрации рака. Министерство здравоохранения: Тайвань; 2003. [Google Scholar]
87. Parkin D.M., Bray F., Ferlay J., Pisani P. Global Cancer Statistics, 2002. CA Cancer J. Clin. 2005; 55: 74–108. [PubMed] [Академия Google]
88. Джемал А., Мюррей Т., Уорд Э., Сэмюэлс А., Тивари Р.К., Гафур А., Фейер Э.Дж., Тун М.Дж. Статистика рака, 2005. CA Cancer J. Clin. 2005; 55:10–30. [PubMed] [Google Scholar]
89. Smith P.W., Jung W.G., Brenner M., Osann K., Beydoun H., Messadi D., Chen Z. Оптическая когерентная томография In vivo для диагностики злокачественных новообразований полости рта. Лазеры Surg. Мед. 2004; 35: 269–275. [PubMed] [Google Scholar]
Лазеры Surg. Мед. 2004; 35: 269–275. [PubMed] [Google Scholar]
90. Jung W., Zhang J., Chung J., Smith P.W., Brenner M., Nelson J.S., Chen Z. Достижения в обнаружении рака ротовой полости с помощью оптической когерентной томографии. Сел. Верхний. Квантовый электрон. IEEE J. 2005; 11:811–817. [Академия Google]
91. Цай М.Т., Ли Х.К., Лу К.В., Ван Ю.Н., Ли К.К., Ян К.К., Чанг К.П. Очерчивание очага рака ротовой полости с помощью оптической когерентной томографии с вращающимся источником. Дж. Биомед. Опц. 2008; 13 doi: 10.1117/1.2960632. [PubMed] [CrossRef] [Google Scholar]
92. Ян С.С., Цай М.Т., Ли Х.С., Ли С.К., Ю Ч.Х., Чен Х.М., Чан С.П., Чанг С.С., Ван Ю.М., Ян С.С. Эффективные показатели для диагностики рака полости рта с помощью оптической когерентной томографии. Опц. Выражать. 2008;16:15847–15862. [PubMed] [Академия Google]
93. Ценг Х.Ю., Ли К.К., Ву С.Ю., Чи Т.Т., Ян К.М., Ван Дж.Ю., Кианг Ю.В., Ян К.С., Цай М.Т., Ву Ю.К., Чжоу Х.Ю., Чан С.П. Нанокольца Au для усиления поглощения и обратного рассеяния, контролируемые с помощью оптической когерентной томографии. Нанотехнологии. 2010; 21 doi: 10.1088/0957-4484/21/29/295102. [PubMed] [CrossRef] [Google Scholar]
Нанотехнологии. 2010; 21 doi: 10.1088/0957-4484/21/29/295102. [PubMed] [CrossRef] [Google Scholar]
94. Kim C.S., Smith P.W., Ahn Y.C., Liaw L.H.L., Chen Z., Kwon Y.J. Расширенное выявление рака полости рта на ранней стадии in vivo с помощью оптической когерентной томографии с использованием мультимодальной доставка наночастиц золота. Дж. Биомед. Опц. 2009 г.;14 doi: 10.1117/1.3130323. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дифференциация поражений полости рта на разных стадиях канцерогенеза с помощью оптической когерентной томографии. Дж. Биомед. Опц. 2009; 14 doi: 10.1117/1.3200936. [PubMed] [CrossRef] [Google Scholar]
96. Lee C.K., Tsai M.T., Lee H.C., Chen H.M., Chiang C.P., Wang Y.M., Yang C.C. Диагностика подслизистого фиброза полости рта с помощью оптической когерентной томографии. Дж. Биомед. Опц. 2009 г.;14 doi: 10.1117/1.3233653. [PubMed] [CrossRef] [Google Scholar]
97. Klein T., Wieser W., Biedermann B.R., Eigenwillig C.


 Изменять положение держателя, так же, как и зубов нельзя.
Изменять положение держателя, так же, как и зубов нельзя.